Способ получения дабигатрана и его промежуточные соединения
Формула / Реферат
1. Способ получения дабигатрама, отличающийся тем, что осуществляют реакцию соединения формулы VII-2HCl
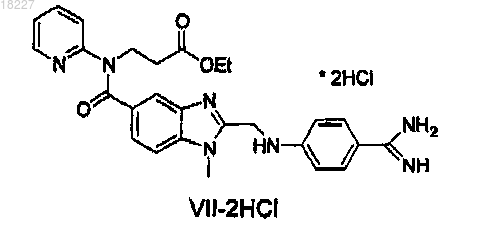
или формулы VII-HCl
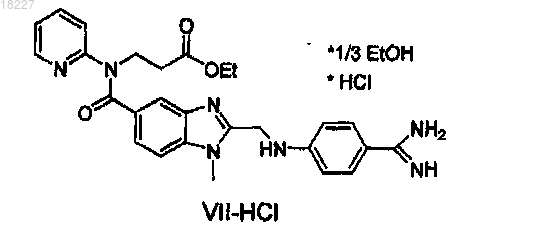
с гексилхлорформиатом в присутствии неорганического или органического основания в инертном растворителе, выбранном из простого эфира, кетона, хлорированного углеводорода или ацетонитрила, и полученный дабигатран необязательно превращают в фармацевтически приемлемую соль.
2. Способ по п.1, отличающийся тем, что реакцию осуществляют в хлорированном углеводороде в присутствии третичного амина в качестве основания.
3. Соединение формулы VII-2HCl
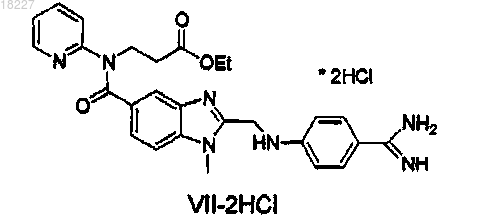
4. Соединение формулы VII-HCl
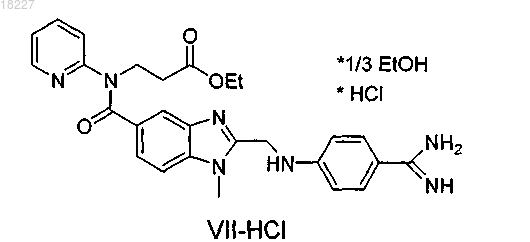
5. Способ получения соединения формулы VII-HCl, отличающийся тем, что осуществляют реакцию соединения формулы VI-оксалат
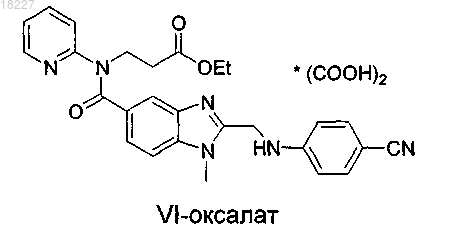
в две стадии: сначала в растворе хлорида водорода в этаноле, а затем в смеси карбоната аммония с этанолом, после фильтрования и выпаривания растворителей выделяют соединение, которое затем перекристаллизуют из этанола или из его смеси с другим органическим растворителем.
6. Способ по п.5, отличающийся тем, что выделенное вещество дополнительно перемешивают в смеси этанола и органического растворителя, выбранного из группы сложных эфиров C1-C6 органических кислот.
7. Способ по п.5 или 6, отличающийся тем, что выделенное соединение перемешивают в смеси этанола и этилацетата.
8. Способ по любому из пп.5-7, отличающийся тем, что перемешивание проводят при температуре от 0 до 60°C.
9. Способ получения соединения формулы VII-2HCl, которое служит промежуточным соединением для получения дабигатрана, отличающийся тем, что соединение формулы VII-HCl или формулы VII
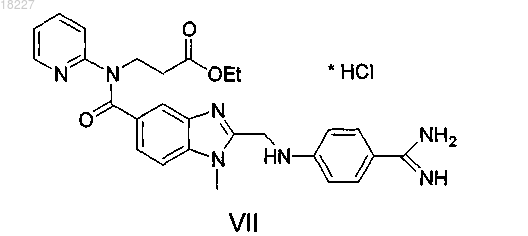
превращают в дигидрохлорид формулы VII-2HCl путем растворения хлорида водорода в инертном растворителе, выбранном из C3-C6 простых эфиров, кетонов, сложных эфиров или C1-C5 спиртов.
Текст
СПОСОБ ПОЛУЧЕНИЯ ДАБИГАТРАНА И ЕГО ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ Промежуточные соединения для получения дабигатрана формул VII-2HCl и VII-HCl, способы их получения и способ получения дабигатрана формулы VIII с применением этих промежуточных соединений Область техники Изобретение относится к новому способу получения 3-([2-(4-(N-н-гексилоксикарбонилкарбамидоил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил]пиридин-2-ил-амино)этилпропионата формулы VIII известного под непатентованным названием дабигатран. Дабигатран представляет собой антикоагулянт и используется для лечения тромбозов, сердечно-сосудистых заболеваний и т.п. Предшествующий уровень техники Получение дабигатрана было впервые описано в документе WO 98/37075, однако этот способ имеет много технологических проблем, например, очень сложные процедуры очистки, проблемы с низким уровнем чистоты промежуточных соединений и малым выходом и низким уровнем чистоты конечного продукта. Одно из улучшенных промежуточных соединений при получении дабигатрана представляет собой соединение формулы VI Соединение формулы VI получают с помощью реакции соединения IV с реагентом V, как показано на схеме 1. Схема 1 Способом, описанным в WO 9837075, получают соединение VI в форме его основания или ацетата. Оба этих продукта нуждаются в хроматографической очистке, что очень затруднительно осуществить в промышленных масштабах. Эта очистка значительно удорожает способ и имеет отрицательное влияние на выход. На следующей стадии проводят кислотный гидролиз нитрильной функции соединения VI и реакцию с карбонатом аммония для получения соединения формулы VII. Реакция показана на схеме 2. Схема 2 Способом по WO 9837075 получают соединение VII в форме моногидрохлорида. Воспроизводя способ по WO 9837075, авторы изобретения обнаружили в соответствии с WO 9837075, что соединение VII, полученное этим способом, требует дополнительной хроматографической очистки, и это была маслянистая субстанция с относительно высоким содержанием примесей. Мы не нашли растворитель, который бы обеспечил очистку этой субстанции кристаллизацией. Последнюю стадию составляет реакция промежуточного соединения VII с гексилхлорформиатом, в результате которой получают дабигатран, и его превращение в фармацевтически приемлемую соль (в случае вышеуказанной заявки на патент - метансульфонат). Однако способ по WO 9837075 не дает возможности получать дабигатран высокой чистоты, что требуется в случае фармацевтического вещества, и с выходом, приемлемым в промышленных масштабах. Основная причина состоит в низком уровне чистоты промежуточных соединений, которые, более того, получают в форме, требующей сложной очистки с применением хроматографических методов. Описание изобретения Данное изобретение описывает получение и применение новых, еще не описанных улучшенных промежуточных соединений дабигатрана: моногидрохлорида соединения VII в форме сольвата с этанолом формулы VII-HCl и новый способ получения дабигатрана, основанный на этих промежуточных соединениях. Выделение любого из двух промежуточных соединений существенно увеличит очищающую способность кристаллизации в сравнении с кристаллизацией описанного выше гидрохлорида. Способом по WO 98/37075 получают соединение VII с содержанием 85-90%. Превращение этого соединения в VII-HCl и его кристаллизация повышают его содержание до 93-95%. Получение соединения VII-2HCl приводит к дальнейшему повышению содержания, а именно, до 96-98%. Получение вышеупомянутых солей позволяет избежать хроматографической очистки соединенияVII, которое описано в WO 9837075 и необходимо для получения соединения VII высокого качества. Получение соединения формулы VII проводят путем кислотного гидролиза нитрильной функции соединения VI с последующей реакцией с карбонатом аммония (см. схему 2). С применением исходного соединения VI в форме оксалата данным способом получают моногидрохлорид соединения VII в форме сольвата с этанолом формулы VII-HCl Этот способ имеет значительный очищающий эффект, который ведет к получению промежуточного соединения формулы VII-HCl высокой чистоты (88-90%) и с более высоким выходом (85-90%). Соединение VII-HCl может быть дополнительно очищено кристаллизацией в отличие от VII, получаемого по WO 98/37075, которое может быть очищено только с применением хроматографических методов. Таким способом чистота соединения VII-HCl может быть увеличена до содержания 90-95%. Еще больший очищающий эффект был достигнут получением соединения VII формулы VII-2HCl. Раствор сухого хлорида водорода в растворителе, выбранном, например, из группы простых эфиров, сложных эфиров, кетонов или спиртов добавляется по каплям к раствору соединения VII-HCl при перемешивании. Оказывается, что спирты являются самыми подходящими растворителями. Это соединение также может быть очищено кристаллизацией. Таким способом получают продукт очень высокой чистоты (96-98%). Получение соединения VII в форме вышеупомянутых солей обеспечивает их очистку кристаллизацией в отличие от соединения VII, получаемого с применением способа по документу WO 98/37075, где необходимо очищать соединение VII с применением хроматографических методов. Следовательно, это означает очень значительное упрощение и увеличение эффективности всего процесса получения, поскольку хроматографическая очистка представляет серьезную технологическую и экономическую проблему при промышленном применении. Кроме того, способом по данному изобретению получают промежуточные соединения дабигатрана,а именно VII-HCl и VII-2HCl, очень высокой чистоты, необходимой для получения высококачественного фармацевтического соединения. Последней стадией является реакция промежуточного VII-HCl или VII-2HCl с гексилхлорформиатом с получением дабигатрана и его превращение в фармацевтически приемлемую соль. Реакцию проводят в инертном растворителе, выбранном из ароматических углеводородов, нитрилов и кетонов в присутствии подходящего основания, органического или неорганического (третичные амины, циклические третичные амины, гидроокиси, карбонаты). Предпочтительное осуществление всего способа по данному изобретению показано на схеме 3. Схема 3 Изобретение также раскрывает удобный способ получения новых промежуточных соединений. Очищающая способность описанного сольвата или дигидрохлорида может быть успешно объединена с таковой способностью солей их предшественников. Способ обеспечивает получение дабигатрана высокой чистоты и с приемлемым для промышленности выходом. Изменение методов очистки, обеспеченное использованием этих солей, например, замена хроматографической очистки кристаллизацией, приводит к значительному удешевлению способа в целом. Доказано, что соль щавелевой кислоты формулы VI особенно удобна для этих целей. Это исходное соединение может быть получено способом, который показан на схеме 4. Соединение Соединение VI получают способом по WO 98/37075 в форме ацетата. Оба эти соединения требуют хроматографической очистки, что очень трудно реализовать в промышленном масштабе. По способу, раскрытому по данному изобретению, соединение VI получают в форме соли щавелевой кислоты. Эта соль просто повторно очищается дальнейшей кристаллизацией, и по этому способу промежуточное соединение VI получают с высоким уровнем чистоты и с выходом, приемлемым для промышленного производства, приблизительно 60-80%. Эта кристаллизация может быть осуществлена из полярного протонсодержащего органического растворителя, предпочтительно из низших спиртов C1-C5, например из этилового спирта. Способ по данному изобретению обеспечивает получение высококачественного продукта с низким содержанием примесей (содержание продукта: 98%) и с высоким выходом (65-70%). Получение промежуточных соединений VI и VII в форме следующих солей VI-оксалат, VII-HCl иVII-2HCl значительно упростит процедуры очистки при получении дабигатрана. Хроматографическая очистка по WO 98/37075 не может быть применена в промышленных масштабах. Замена хроматографической очистки кристаллизацией обеспечивает значительное технологическое упрощение и удешевляет весь способ производства. Изобретение далее проиллюстрировано на следующих примерах. Пример 1. Получение VII-HCl. 40 г соединения VI-оксалат добавляют к этанолу с хлоридом водорода. Смесь перемешивают при комнатной температуре 14 ч. Затем этанол с хлоридом водорода выпаривают и осадок от выпаривания растворяют в 1000 мл этанола. 110 г карбоната аммония добавляют в этот раствор и всю смесь перемешивают при комнатной температуре 26 ч. По истечении этого периода нерастворенную фракцию удаляют отсасыванием жидкости и фильтрат концентрируют. Полученное соединение растворяют в 560 мл смеси 2:1 этилацетата и этанола при комнатной температуре. После 30 мин получают белый осадок, который охлаждают в холодильнике и отсасывают и сушат при 50C. Выход: 28,5 г (81%), содержание согласно ВЭЖХ: 89%. Согласно ЯМР соединение является сольватом с этанолом в пропорции 3:1 (VII-HCl).1 Н ЯМР (ДМСО-d6, 30C, 250 МГц) [м.д.]: 1,16 (t, 3H), 1,10 (t, 1H), 2,78 (t, 2H), 3,83 (s, 3H), 3,49 (q, 0.66H), 4,02 (q, 2 Н), 4,28 (t, 2H) 4,7 (d, 2H),6,9 (m,1H), 6,9 (d, 2H), 7,18(m, 1H), 7,19 (dd, 1H), 7,45 (d, 1 Н), 7,53 (d, 1 Н), 7,56 (m, 1 Н), 7,60 (m, 1H), 7,76(d, 2H), 8,43 (dd, 1H), 8,86 (bs, 2H), 9,02, (bs, 2H).13 С ЯМР: (ДМСО-d6, 30C, 62,90 МГц) [м.д.]: 14,02 (CH3), 30,07 (CH3), 33,11 (CH2), 39,93 (CH2), 44,42 (CH2), 60,07 (CH2), 109,58, 111,77, 119,55,121,33, 122,14, 122,87, 129,71, 137,96, 148,74 (все CH), 113,27, 129,45, 137,29, 140,83, 153,13, 153,48,156,04, 164,52, 170,39, 171,09 (все C-q). Пример 2. Получение VII-2HCl. 9,7 г соединения VII-HCl-EtOH растворяют в смеси этанола с этилацетатом. Раствор хлорида водорода в этаноле, содержащий эквимолярное количество кислоты, добавляется в этот раствор по каплям. После отделения осадка суспензию охлаждают, и продукт отсасывают и высушивают. Выход: 9,1 г (87,8%); содержание согласно ВЭЖХ: 96,2%.1 Н ЯМР (ДМСО-d6, 30C, 250 МГц) [м.д.]: 1,16 (t, 3H); 2,56 (t, 2H); 4,03 (m, 5H); 4,26 (t, 2H); 5,04 (bs, 2H); 6,99 (d, 2H); 7,13(d, 1 Н); 7,21 (dd,1 Н); 7,41 (dd, 1 Н); 7,68 (т, 1 Н), 7,71 (d, 1H), 7,82 (d, 2H), 7,84 (d, 1H), 8,41 (dd, 1H), 8,99 (bs, 2H), 9,17, (bs,2H).13 С ЯМР: (ДМСО-d6, 30C, 62,90 МГц) [м.д.]: 14,03 (CH3), 31,51 (CH3), 32,91 (CH2), 39,59 (CH2), 44,56 (CH2), 60,11 (CH2), 112,12, 112,25, 115,20,121,94, 122,12, 125,35, 129,80, 138,48, 148,87 (все CH), 114,59, 130,73, 133,43, 134,24, 152,42, 153,69,155,33, 164,50 , 168,96 , 171,00 (все C-q). Пример 3. Получение мезилата дабигатрана. К 9,1 г соединения VII-2HCl (0,016 моль) добавляют 270 мл хлороформа и 9 мл (0,064 моль) триэтиламина. Затем раствор 3,1 мл (0,018 моль) гексилхлорформиата в хлороформе добавляют по каплям при комнатной температуре. После 1 ч реакционную смесь встряхивают с солевым раствором и отделяют органический слой, который высушивают с сульфатом натрия и концентрируют. Полученный после выпаривания осадок кристаллизуют из этилацетата. Выход: 8,6 г (86%). Это соединение растворяют в ацетоне и добавляют по каплям эквимолярное количество метансульфоновой кислоты. Отделенный осадок отсасывают и высушивают при комнатной температуре. Выход: 75%; содержание согласно ВЭЖХ: 99,5%. Пример 4. Получение мезилата дабигатрана. 9 г соединения VII-HCl (0,017 моль) растворяют в 300 мл хлороформа. 6 мл триэтиламина добавляют к этому раствору и затем раствор 3,4 мл (0,02 моль) гексилхлороформиата в хлороформе добавляют по каплям. После 1 ч реакционную смесь встряхивают с солевым раствором, органический слой отделяют и его высушивают с сульфатом натрия и концентрируют. Полученный после выпаривания осадок кристаллизуют из этилацетата. Выход: 9,6 г (90%). Это соединение растворяют в ацетоне и добавляют по каплям метансульфоновую кислоту в эквимолярном количестве. Отделенный после выпаривания осадок отсасывают и высушивают при комнатной температуре. Выход: 73%; содержание согласно ВЭЖХ: 99,5%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения дабигатрама, отличающийся тем, что осуществляют реакцию соединения формулы VII-2HCl с гексилхлорформиатом в присутствии неорганического или органического основания в инертном растворителе, выбранном из простого эфира, кетона, хлорированного углеводорода или ацетонитрила, и полученный дабигатран необязательно превращают в фармацевтически приемлемую соль. 2. Способ по п.1, отличающийся тем, что реакцию осуществляют в хлорированном углеводороде в присутствии третичного амина в качестве основания. 3. Соединение формулы VII-2HCl 5. Способ получения соединения формулы VII-HCl, отличающийся тем, что осуществляют реакцию соединения формулы VI-оксалат в две стадии: сначала в растворе хлорида водорода в этаноле, а затем в смеси карбоната аммония с этанолом, после фильтрования и выпаривания растворителей выделяют соединение, которое затем перекристаллизуют из этанола или из его смеси с другим органическим растворителем. 6. Способ по п.5, отличающийся тем, что выделенное вещество дополнительно перемешивают в смеси этанола и органического растворителя, выбранного из группы сложных эфиров C1-C6 органических кислот. 7. Способ по п.5 или 6, отличающийся тем, что выделенное соединение перемешивают в смеси этанола и этилацетата. 8. Способ по любому из пп.5-7, отличающийся тем, что перемешивание проводят при температуре от 0 до 60C. 9. Способ получения соединения формулы VII-2HCl, которое служит промежуточным соединением для получения дабигатрана, отличающийся тем, что соединение формулы VII-HCl или формулы VII превращают в дигидрохлорид формулы VII-2HCl путем растворения хлорида водорода в инертном растворителе, выбранном из C3-C6 простых эфиров, кетонов, сложных эфиров или C1-C5 спиртов.
МПК / Метки
МПК: C07D 401/12
Метки: промежуточные, способ, дабигатрана, получения, соединения
Код ссылки
<a href="https://eas.patents.su/7-18227-sposob-polucheniya-dabigatrana-i-ego-promezhutochnye-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения дабигатрана и его промежуточные соединения</a>











