Новый способ синтеза 7,8-диметокси-1,3-дигидро-2h-3-бензазепин-2-она и его применение при синтезе ивабрадина и его солей присоединения с фармацевтически приемлемой кислотой
Номер патента: 17333
Опубликовано: 30.11.2012
Авторы: Бриго Даниель, Лекув Жан-Пьер, Лерестиф Жан-Мишель
Формула / Реферат
1. Способ синтеза соединения формулы (I)
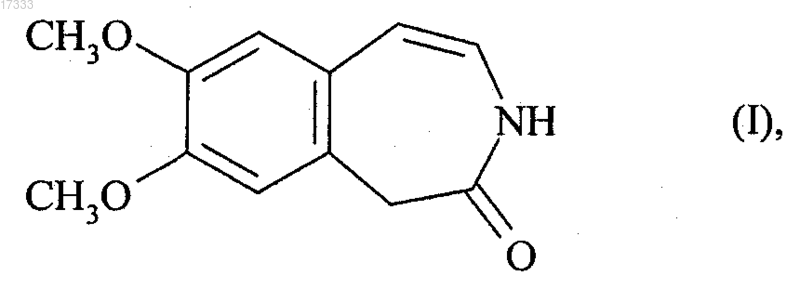
который характеризируется тем, что (3,4-диметоксифенил)уксусную кислоту формулы (IV)

превращают в соединение формулы (V)
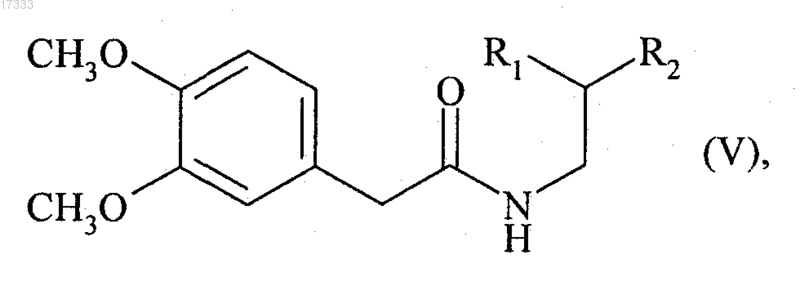
где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С1-С6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены, образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,
либо с помощью предварительного превращения соединения формулы (IV) в соединение формулы (VI)
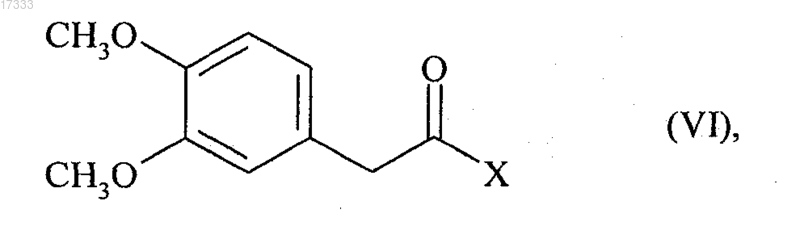
в которой X представляет собой атом галогена или группу OCOR3, где R3 представляет собой линейную или разветвленную (С1-С6)алкильную группу, фенильную группу, бензильную группу или имидазолильную группу,
в органическом растворителе, затем соединение формулы (VI) подвергают реакции конденсации с соединением формулы (VII)
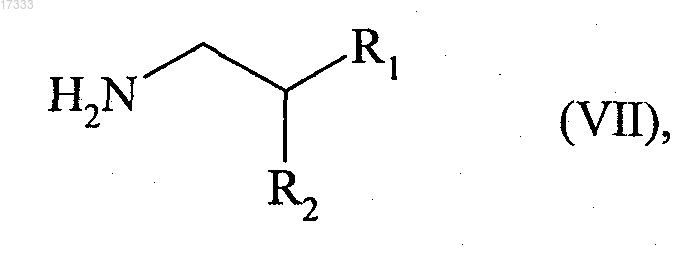
где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С1-С6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены, образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,
в присутствии основания в органическом растворителе с получением соединения формулы (V),
либо путем взаимодействия с соединением формулы (VII)
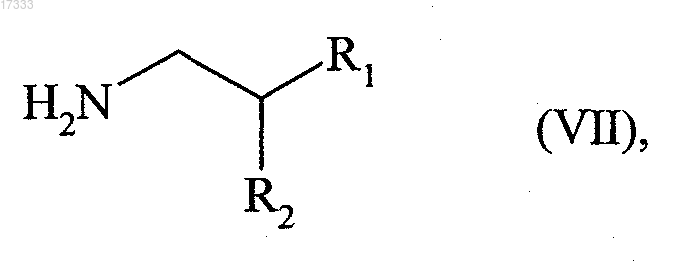
где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С1-С6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены, образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,
в присутствии связующего вещества в органическом растворителе с получением соединения формулы (V), указанное соединение формулы (V) не выделяют и непосредственно подвергают реакции циклизации в кислой среде, получая, после выделения, соединение формулы (I).
2. Способ синтеза по п.1, отличающийся тем, что соединение формулы (VI) не выделяют.
3. Способ синтеза по п.1 или 2, отличающийся тем, что в соединении формулы (VI) X представляет собой атом хлора.
4. Способ синтеза по любому из пп.1-3, отличающийся тем, что растворитель, используемый для превращения соединения формулы (IV) в соединение формулы (VI), представляет собой дихлорметан.
5. Способ синтеза по любому из пп.1-4, отличающийся тем, что температура реакции превращения соединения формулы (IV) в соединение формулы (VI) составляет от 20 до 40°С.
6. Способ синтеза по любому из пп.1-5, отличающийся тем, что реагент, используемый для превращения соединения формулы (IV) в соединение формулы (VI), представляет собой тионилхлорид.
7. Способ синтеза по п.6, отличающийся тем, что количество тионилхлорида, используемое в реакции для превращения соединения формулы (IV) в соединение формулы (VI), составляет от 1 до 1,3 моль на 1 моль соединения формулы (IV).
8. Способ синтеза по любому из пп.1-7, отличающийся тем, что растворитель, используемый для реакции между соединениями формул (VI) и (VII), представляет собой дихлорметан.
9. Способ синтеза по любому из пп.1-8, отличающийся тем, что температура реакции между соединениями формул (VI) и (VII) составляет от 0 до 40°С.
10. Способ синтеза по любому из пп.1-9, отличающийся тем, что количество соединения (VII), используемое в реакции с соединением формулы (VI), составляет от 1 до 1,2 моль на 1 моль соединения формулы (VI).
11. Способ синтеза по любому из пп.1-10, отличающийся тем, что количество основания, используемое в реакции между соединениями формул (VI) и (VII), составляет от 1 до 1,3 моль на 1 моль соединения (VI).
12. Способ синтеза по любому из пп.1-11, отличающийся тем, что основание, используемое в реакции между соединениями формул (VI) и (VII), представляет собой пиридин, DMAP или третичный амин.
13. Способ синтеза по п.12, отличающийся тем, что основание, используемое в реакции между соединениями формул (VI) и (VII), представляет собой триэтиламин.
14. Способ синтеза по любому из пп.1-13, отличающийся тем, что количество кислоты, используемое в реакции для циклизации соединения формулы (V), составляет от 5 до 15 моль на 1 моль соединения формулы (V).
15. Способ синтеза по любому из пп.1-14, отличающийся тем, что температура реакции для циклизации соединения формулы (V) в кислой среде составляет от 0 до 40°С.
16. Способ синтеза по любому из пп.1-15, отличающийся тем, что кислота, используемая для циклизации соединения формулы (V), представляет собой концентрированную серную кислоту.
17. Способ синтеза по п.16, отличающийся тем, что количество концентрированной серной кислоты, используемое в реакции для циклизации соединения формулы (V), составляет от 1,5 до 3 мл/г (3,4-диметоксифенил)уксусной кислоты формулы (IV).
18. Способ синтеза ивабрадина и его фармацевтически приемлемых солей, где соединение формулы (IV) превращают в соединение формулы (I) в соответствии со способом по п.1, затем соединение формулы (I) превращают в ивабрадин, который необязательно может быть превращен в его соли присоединения с фармацевтически приемлемой кислотой, выбранной из соляной, бромисто-водородной, серной, фосфорной, уксусной, трифторуксусной, молочной, пировиноградной, малоновой, янтарной, глутаровой, фумаровой, винной, малеиновой, лимонной, аскорбиновой, щавелевой, метансульфокислоты, бензолсульфокислоты и камфорной кислот, и в их гидраты.
Текст
НОВЫЙ СПОСОБ СИНТЕЗА 7,8-ДИМЕТОКСИ-1,3-ДИГИДРО-2H-3-БЕНЗАЗЕПИН-2 ОНА И ЕГО ПРИМЕНЕНИЕ ПРИ СИНТЕЗЕ ИВАБРАДИНА И ЕГО СОЛЕЙ ПРИСОЕДИНЕНИЯ С ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМОЙ КИСЛОТОЙ Изобретение относится к способу синтеза соединения формулы (I) и его применению для синтеза ивабрадина, его соли присоединения с фармацевтически приемлемой кислотой и их гидратов.(71)(73) Заявитель и патентовладелец: ЛЕ ЛАБОРАТУАР СЕРВЬЕ (FR) 017333 Настоящее изобретение относится к способу синтеза 7,8-диметокси-1,3-дигидро-2H-3-бензазепин-2 она формулы (I) и его применению для синтеза ивабрадина, его солей присоединения с фармацевтически приемлемой кислотой и их гидратов Соединение формулы (I), полученное согласно способу по изобретению, пригодно для синтеза ивабрадина формулы (II) или 3-3-(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил(метил)амино]-пропил-7,8 диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-она,его солей присоединения с фармацевтически приемлемой кислотой и их гидратов. Ивабрадин и его соли присоединения с фармацевтически приемлемой кислотой, более предпочтительно его гидрохлорид, обладают ценными фармакологическими и терапевтическими свойствами, в особенности брадикардическими свойствами, что делает эти соединения пригодными для лечения или профилактики различных клинических состояний ишемии миокарда, таких как стенокардия, инфаркт миокарда и ассоциированные нарушения ритма, а также различных патологий, связанных с нарушениями ритма, в особенности суправентрикулярных нарушений ритма, и при сердечной недостаточности. Получение и терапевтическое применение ивабрадина и его солей присоединения с фармацевтически приемлемой кислотой, и более предпочтительно его гидрохлорида, описаны в заявке на европейский патент ЕР 0534859. В этой патентной заявке описан синтез гидрохлорида ивабрадина, используя в качестве исходного вещества соединение формулы (III) и упоминается публикация J. Med. Chem., 1990, том 33 (5), 1496-1504 для приготовления этого соединения. В пути синтеза, описанном в этой публикации для соединения формулы (III), используется реакция алкилирования на соединении формулы (I) В вышеуказанной публикации описано приготовление соединения формулы (I) путем использования в качестве промежуточного продукта, N-(2,2-диметоксиэтил)-2-(3,4-диметоксифенил)ацетамида, полученного при использовании в качестве исходного соединения (3,4-диметоксифенил)уксусной кислоты. Кристаллизацию полученного фенилацетамида осуществляют в присутствии соляной кислоты в уксусной кислоте, получая соединение формулы (I) в суммарном выходе 58% относительно(3,4-диметоксифенил)уксусной кислоты. С учетом промышленной ценности ивабрадина и его солей является важным выявление эффективного способа, который в особенности позволяет получить 7,8-диметокси-1,3-дигидро-2H-3-бензазепин-2 он формулы (I) с очень хорошим выходом. Сейчас заявителем неожиданно было обнаружено, что при использовании специфических технологических условий предоставляется возможность получения соединения формулы (I) в промышленном масштабе с выходом больше 92% и с химической чистотой больше 99,5%.-1 017333 Более специфически, настоящее изобретение относится к способу синтеза соединения формулы (I) где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С 1-С 6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены,образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо, которое подвергают реакции циклизации в кислой среде, получая, после выделения, соединение формулы (I). В одном из предпочтительных вариантов осуществления изобретения превращение соединения формулы (IV) в соединение формулы (V) осуществляют с помощью предварительного превращения соединения формулы (IV) в соединение формулы (VI) в которой X представляет собой атом галогена или группу OCOR3, где R3 представляет собой линейную или разветвленную (С 1-С 6)алкильную группу, фенильную группу, бензильную группу или имидазольную группу,в органическом растворителе, затем соединение формулы (VI) подвергают реакции конденсации с соединением формулы (VII) где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С 1-С 6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены,образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,в присутствии основания в органическом растворителе, получая соединение формулы (V) В другом предпочтительном варианте осуществления изобретения превращение соединения формулы (IV) в соединение формулы (V) осуществляют путем взаимодействия с соединением формулы (VII) где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С 1-С 6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены,образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,в присутствии связующего вещества в органическом растворителе, получая соединение формулы (V) Из связующих веществ, которые можно использовать для реакции конденсации соединения формулы (VII) с соединением формулы (IV), могут быть упомянуты, но не ограничиваясь только ими, следующие реагенты или пары реагентов: EDCl, EDCl/HOBT, EDCl/HOAT, EDCl/NHS, DCC, DCC/HOBT,DCC/HOAT, DCC/NHS, HATU, HBTU, TBTU, ВОР, РуВОР, CDI, Т 3 Р.-2 017333 Из органических растворителей, которые могут использоваться для реакции конденсации соединения формулы (VII) с соединением формулы (IV) в присутствии связующего вещества, могут быть упомянуты, но не ограничиваясь только ими, толуол, дихлорметан, 2-метилтетрагидрофуран, хлорбензол,1,2-дихлорэтан, хлороформ и диоксан. В одном из предпочтительных вариантов осуществления изобретения соединение формулы (V) не выделяют. В одном из предпочтительных вариантов осуществления изобретения соединение формулы (VI) не выделяют. Группа X в соединении формулы (VI) предпочтительно представляет собой атом хлора. Из органических растворителей, которые могут использоваться для реакции превращения соединения формулы (IV) в соединение формулы (VI), могут быть упомянуты, но не ограничиваясь только ими,толуол, дихлорметан, 2-метилтетрагидрофуран, хлорбензол, 1,2-дихлорэтан, хлороформ и диоксан. Предпочтительным органическим растворителем для реакции превращения соединения формулы(IV) в соединение формулы (VI) является дихлорметан. Температура реакции превращения соединения формулы (IV) в соединение формулы (VI) предпочтительно составляет от 20 до 40 С. Реагент, который предпочтительно используют для осуществления превращения соединения формулы (IV) в соединение формулы (VI), где X представляет собой атом хлора, представляет собой тионилхлорид. Количество тионилхлорида, используемое при реакции превращения соединения формулы (IV) в соединение формулы (VI), предпочтительно составляет от 1 до 1,3 моль на 1 моль соединения формулы(IV). Из органических растворителей, которые могут использоваться для реакции между соединением формулы (VI) и соединением формулы (VII), могут быть упомянуты, но не ограничиваясь только ими,толуол, дихлорметан, 2-метилтетрагидрофуран, хлорбензол, 1,2-дихлорэтан, хлороформ и диоксан. Предпочтительным органическим растворителем для реакции между соединением формулы (VI) и соединением формулы (VII) является дихлорметан. Температура реакции между соединением формулы (VI) и соединением формулы (VII) предпочтительно составляет от 0 до 40 С. Количество соединения формулы (VII), используемое в реакции с соединением формулы (VI),предпочтительно составляет от 1 до 1,2 моль на 1 моль соединения формулы (VI). Количество основания, используемое в реакции между соединением формулы (VI) и соединением формулы (VII), предпочтительно составляет от 1 до 1,3 моль на 1 моль соединения формулы (VI). Из оснований, которые можно использовать для взаимодействия между соединением формулы (VI) и соединением формулы (VII), могут быть упомянуты, но не ограничиваясь только ими, пиридин, DMAP и третичные амины, например триэтиламин, DIEA, N-метилпиперидин, DBU, DABCO, DBN иN-метилморфолин. Основание, которое предпочтительно используется для реакции между соединением формулы (VI) и соединением формулы (VII), представляет собой триэтиламин. Из кислот, которые можно использовать для циклизации соединения формулы (V) с образованием соединения формулы (I), могут быть упомянуты, но не ограничиваясь только ими, концентрированная серная кислота, полифосфорная кислота, концентрированная соляная кислота в водном растворе, концентрированная соляная кислота в растворе в уксусной кислоте, концентрированная бромистоводородная кислота в растворе в уксусной кислоте и метансульфокислота. Количество кислоты, используемое для циклизации соединения формулы (V) с образованием соединения формулы (I), предпочтительно составляет от 5 до 15 моль на 1 моль соединения формулы (V). Температура реакции для циклизации соединения формулы (V) в кислой среде предпочтительно составляет от 0 до 40 С. Кислота, предпочтительно используемая для циклизации соединения формулы (V) с образованием соединения формулы (I), представляет собой концентрированную серную кислоту. Если промежуточные продукты реакции не выделяют при осуществлении процесса, то количество концентрированной серной кислоты, используемое в реакции для циклизации соединения формулы (V),предпочтительно составляет от 1,5 до 3 мл/г (3,4-диметоксифенил)уксусной кислоты формулы (IV). Соединение формулы (I), полученное в соответствии со способом по настоящему изобретению, в особенности пригодно в качестве промежуточного продукта синтеза для синтеза ивабрадина, его солей присоединения с фармацевтически приемлемой кислотой и их гидратов.-3 017333 В качестве примера, при алкилировании соединения формулы (I) с соединением формулы (VIII) где группы R4 и R5, которые могут быть одинаковыми или разными, каждая, представляют собой линейную или разветвленную (С 1-С 6)алкоксигруппу или вместе с атомом углерода, к которому они присоединены, образуют 1,3-диоксановое или 1,3-диоксолановое кольцо;Y представляет собой атом галогена, предпочтительно атом брома, или тозилатную, мезилатную или трифлатную группу,получают соединение формулы (IX) при каталитическом гидрировании которого получают соответствующее гидрированное соединение формулы (X) где R4 и R5 имеют значения, указанные для формулы (VIII),при снятии защиты с диацетальной части которого получают альдегид формулы (XI) который подвергают реакции с [(7S)-3,4-диметоксибицикло[4,2,0]окта-1,3,5-триен-7-ил]-Nметилметанамином в условиях восстановительного аминирования, получая ивабрадин, который необязательно может быть превращен в его соли присоединения с фармацевтически приемлемой кислотой, выбранной из соляной, бромисто-водородной, серной, фосфорной, уксусной, трифторуксусной, молочной,пировиноградной, малоновой, янтарной, глутаровой, фумаровой, винной, малеиновой, лимонной, аскорбиновой, щавелевой, метансульфокислоты, бензолсульфокислоты и камфорной кислот, и в их гидраты. Используемые сокращения ВОР - гексафторфосфат бензотриазол-1-илокси-трис-(диметиламино)фосфония;TBTU - тетрафторборат O-(бензотриазол-1-ил)-1,1,3,3-тетраметилурония; Т 3 Р - п-пропанфосфоновый ангидрид. Пример, представленный ниже, иллюстрирует изобретение. Получение 7,8-диметокси-1,3-дигидро-2H-3-бензазепин-2-она. Стадия А. Хлорид (3,4-диметоксифенил)уксусной кислоты. В реактор загружали 135 г (3,4-диметоксифенил)уксусной кислоты и 270 мл дихлорметана и затем температуру реакционной смеси доводили до флегмы и по каплям добавляли 90 г тионилхлорида. Смесь перемешивали в колбе с обратным холодильником в течение 3 ч. Полученный раствор использовали как таковой на следующей стадии.-4 017333 Стадия В. N-(2,2-Диметоксиэтил)-2-(3,4-диметоксифенил)ацетамид. В реактор загружали 225 мл дихлорметана, 44,15 г 2,2-диметоксиэтиламина и 44,35 г триэтиламина и затем смесь охлаждали до 10 С и по каплям добавляли 237,4 г раствора, полученного на предыдущей стадии (что соответствует 75 г (3,4-диметоксифенил)уксусной кислоты), тогда как масс-температуру поддерживали равной 10 С. Смесь перемешивали в течение 2 ч при 15 С. Полученный раствор использовали как таковой на следующей стадии. Стадия С. 7,8-Диметокси-1,3-дигидро-2 Н-3-бензазепин-2-он. В реактор, содержащий раствор, полученный на предыдущей стадии и охлажденный до 10 С, добавляли 150 мл 36 н. серной кислоты, при этом температуру поддерживали ниже 20 С. Смесь перемешивали при 15-20 С в течение 10 ч, затем позволяли реакционной смеси разделиться и собирали фазу, содержащую продукт-серную кислоту. Продукт получали путем осаждения из смеси вода/NMP (4/1), фильтрования и высушивания, с выходом 92,9% относительно (3,4-диметоксифенил)уксусной кислоты с химической чистотой больше 99,5%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ синтеза соединения формулы (I) где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С 1-С 6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены,образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,либо с помощью предварительного превращения соединения формулы (IV) в соединение формулы (VI) в которой X представляет собой атом галогена или группу OCOR3, где R3 представляет собой линейную или разветвленную (С 1-С 6)алкильную группу, фенильную группу, бензильную группу или имидазолильную группу,в органическом растворителе, затем соединение формулы (VI) подвергают реакции конденсации с соединением формулы (VII) где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С 1-С 6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены,образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,в присутствии основания в органическом растворителе с получением соединения формулы (V),либо путем взаимодействия с соединением формулы (VII) где группы R1 и R2, которые могут быть одинаковыми или разными, представляют собой линейные или разветвленные (С 1-С 6)алкоксигруппы или вместе с атомом углерода, к которому они присоединены,образуют 1,3-диоксановое, 1,3-диоксолановое или 1,3-диоксепановое кольцо,в присутствии связующего вещества в органическом растворителе с получением соединения формулы(V), указанное соединение формулы (V) не выделяют и непосредственно подвергают реакции циклизации в кислой среде, получая, после выделения, соединение формулы (I). 2. Способ синтеза по п.1, отличающийся тем, что соединение формулы (VI) не выделяют. 3. Способ синтеза по п.1 или 2, отличающийся тем, что в соединении формулы (VI) X представляет-5 017333 собой атом хлора. 4. Способ синтеза по любому из пп.1-3, отличающийся тем, что растворитель, используемый для превращения соединения формулы (IV) в соединение формулы (VI), представляет собой дихлорметан. 5. Способ синтеза по любому из пп.1-4, отличающийся тем, что температура реакции превращения соединения формулы (IV) в соединение формулы (VI) составляет от 20 до 40 С. 6. Способ синтеза по любому из пп.1-5, отличающийся тем, что реагент, используемый для превращения соединения формулы (IV) в соединение формулы (VI), представляет собой тионилхлорид. 7. Способ синтеза по п.6, отличающийся тем, что количество тионилхлорида, используемое в реакции для превращения соединения формулы (IV) в соединение формулы (VI), составляет от 1 до 1,3 моль на 1 моль соединения формулы (IV). 8. Способ синтеза по любому из пп.1-7, отличающийся тем, что растворитель, используемый для реакции между соединениями формул (VI) и (VII), представляет собой дихлорметан. 9. Способ синтеза по любому из пп.1-8, отличающийся тем, что температура реакции между соединениями формул (VI) и (VII) составляет от 0 до 40 С. 10. Способ синтеза по любому из пп.1-9, отличающийся тем, что количество соединения (VII), используемое в реакции с соединением формулы (VI), составляет от 1 до 1,2 моль на 1 моль соединения формулы (VI). 11. Способ синтеза по любому из пп.1-10, отличающийся тем, что количество основания, используемое в реакции между соединениями формул (VI) и (VII), составляет от 1 до 1,3 моль на 1 моль соединения (VI). 12. Способ синтеза по любому из пп.1-11, отличающийся тем, что основание, используемое в реакции между соединениями формул (VI) и (VII), представляет собой пиридин, DMAP или третичный амин. 13. Способ синтеза по п.12, отличающийся тем, что основание, используемое в реакции между соединениями формул (VI) и (VII), представляет собой триэтиламин. 14. Способ синтеза по любому из пп.1-13, отличающийся тем, что количество кислоты, используемое в реакции для циклизации соединения формулы (V), составляет от 5 до 15 моль на 1 моль соединения формулы (V). 15. Способ синтеза по любому из пп.1-14, отличающийся тем, что температура реакции для циклизации соединения формулы (V) в кислой среде составляет от 0 до 40 С. 16. Способ синтеза по любому из пп.1-15, отличающийся тем, что кислота, используемая для циклизации соединения формулы (V), представляет собой концентрированную серную кислоту. 17. Способ синтеза по п.16, отличающийся тем, что количество концентрированной серной кислоты, используемое в реакции для циклизации соединения формулы (V), составляет от 1,5 до 3 мл/г(3,4-диметоксифенил)уксусной кислоты формулы (IV). 18. Способ синтеза ивабрадина и его фармацевтически приемлемых солей, где соединение формулы(IV) превращают в соединение формулы (I) в соответствии со способом по п.1, затем соединение формулы (I) превращают в ивабрадин, который необязательно может быть превращен в его соли присоединения с фармацевтически приемлемой кислотой, выбранной из соляной, бромисто-водородной, серной,фосфорной, уксусной, трифторуксусной, молочной, пировиноградной, малоновой, янтарной, глутаровой,фумаровой, винной, малеиновой, лимонной, аскорбиновой, щавелевой, метансульфокислоты, бензолсульфокислоты и камфорной кислот, и в их гидраты.
МПК / Метки
МПК: C07D 223/16
Метки: приемлемой, способ, фармацевтически, ивабрадина, применение, синтеза, присоединения, синтезе, новый, кислотой, 7,8-диметокси-1,3-дигидро-2h-3-бензазепин-2-она, солей
Код ссылки
<a href="https://eas.patents.su/7-17333-novyjj-sposob-sinteza-78-dimetoksi-13-digidro-2h-3-benzazepin-2-ona-i-ego-primenenie-pri-sinteze-ivabradina-i-ego-solejj-prisoedineniya-s-farmacevticheski-priemlemojj-kislotojj.html" rel="bookmark" title="База патентов Евразийского Союза">Новый способ синтеза 7,8-диметокси-1,3-дигидро-2h-3-бензазепин-2-она и его применение при синтезе ивабрадина и его солей присоединения с фармацевтически приемлемой кислотой</a>











