Способ получения кристаллического моногидрата n-формимидоил-тиенамицина (моногидрата имипенема)
Номер патента: 6442
Опубликовано: 29.12.2005
Авторы: Рай Бишва Пракаш, Тевари Неера, Ариан Рэм Чандер, Ахуджа Сеема, Кумар Ятендра
Формула / Реферат
1. Способ получения кристаллического моногидрата N-формимидоилтиенамицина (имипенема) формулы I, включающий
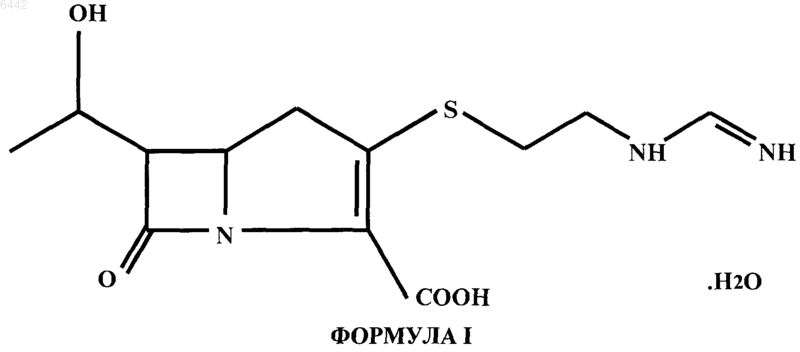
(a) активацию кетоэфирного соединения формулы I
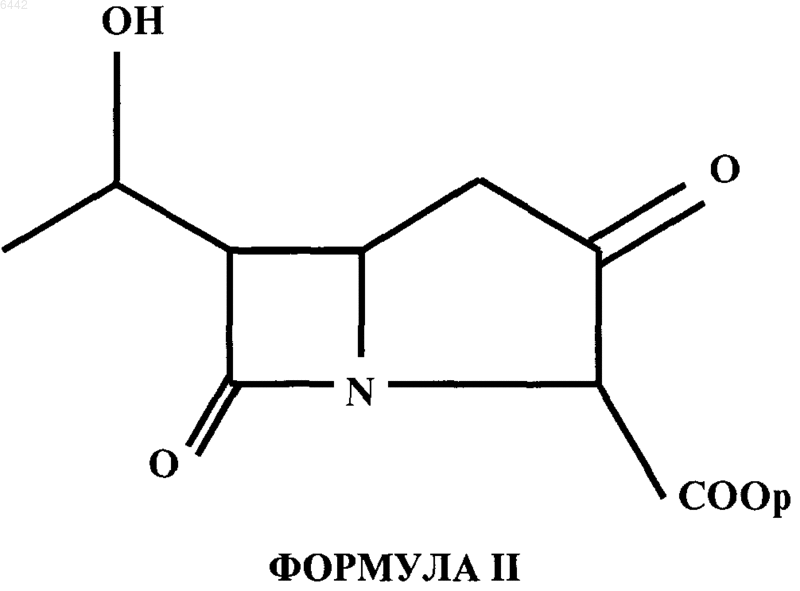
где p представляет собой водород или защитную группу, в присутствии подходящего вторичного амина, в подходящем N-замещенном лактаме или N,N-дизамещенном амиде в качестве растворителя, необязательно в сочетании с инертным органическим растворителем, с получением соединения формулы III
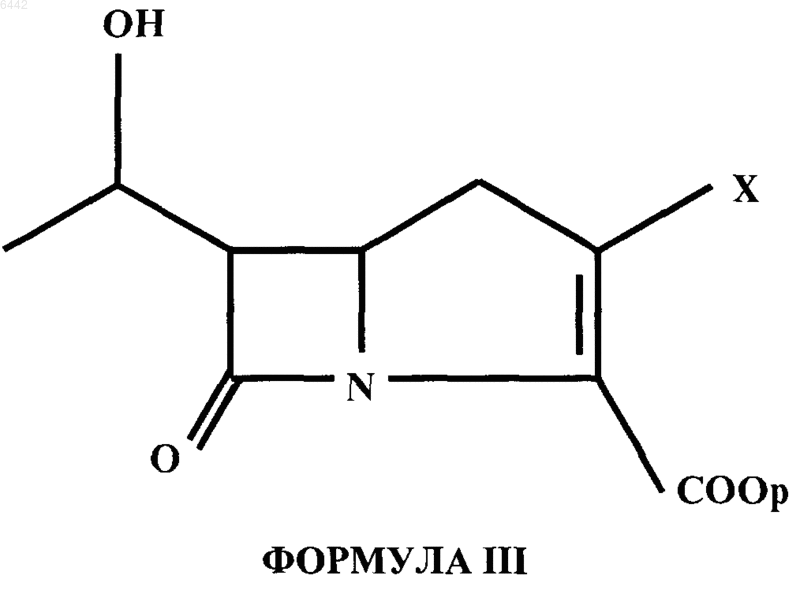
где X представлят собой OP(O)(OR)2 или OS(O)2R и R представляет собой C1-6-алкил, C1-6-алкарил, арил или перфтор-C1-6-алкил; термин алкил обозначает линейную или разветвленную цепь, которая при достижении достаточного размера может образовывать цикл; предпочтительные линейные или разветвленные алкильные группы включают метил, этил, пропил, изопропил, бутил и трет.-бутил;
предпочтительные циклоалкильные группы включают циклопропил, циклопентил, циклогексил и циклопропилметил; термин арил обозначает ароматическое кольцо, включая фенил, замещенный фенил и нафтил; арильные группы могут быть замещены одним-тремя заместителями, независимо выбранными из галогена, алкила и галогенированной низшей алкильной группы, где алкил такой, как указано выше,
(b) взаимодействие активированного кетоэфира формулы III in situ с 2-аминоэтантиолом (цистеамином) или его солью в присутствии вторичного амина в N-замещенном лактаме или N,N-дизамещенном амиде с получением эфира тиенамицина формулы IV
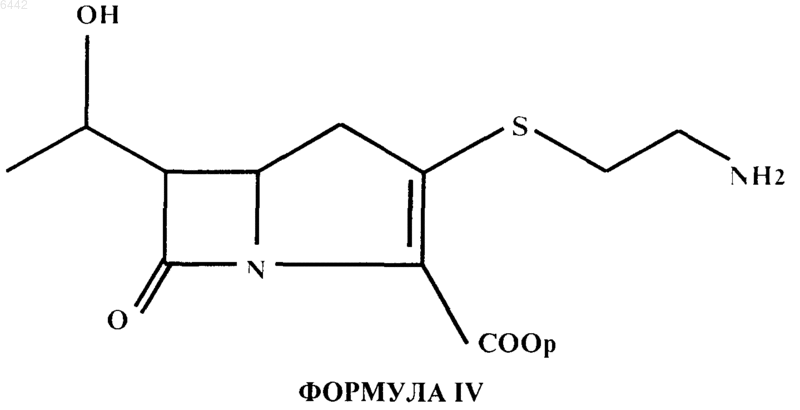
где p, N-замещенный лактам и N,N-дизамещенный амин такие, как указано выше,
(c) взаимодействие эфира тиенамицина формулы IV in situ с гидрохлоридом бензилформимидата (C6H5CH2OCH=NH2+Cl-) в присутствии вторичного амина в N-замещенном лактаме или N,N-дизамещенном амиде с получением амидина эфира карбоновой кислоты (защищенного N-формимидоилтиенамицина) формулы V

где p, N-замещенный лактам и N,N-дизамещенный амин такие, как указано выше,
(d) восстановление защищенного N-формимидоилтиенамицина формулы V с получением N-формимидоилтиенамицина (имипенема) в растворе и очистку раствора, содержащего реакционную смесь, при помощи дианионной хроматографии, с последующей кристаллизацией в присутствии подходящего спирта или кетона в качестве сорастворителя с получением кристаллического моногидрата N-формимидоилтиенамицина (моногидрата имипенема) формулы I высокой степени чистоты.
2. Способ по п.1, отличающийся тем, что защитную группу p выбирают из группы, состоящей из бензила, п-нитробензила и метоксиметила.
3. Способ по п.1, отличающийся тем, что подходящий вторичный амин выбирают из группы, состоящей из диизопропиламина, дициклогексиламина, 2,2,6,6-тетраметилэтилпиперидина (TMP) и 1,1,3,3-тетраметилгуанидина (TMG).
4. Способ по п.1, отличающийся тем, что N-замещенный лактам или N,N-дизамещенный амид используют отдельно или в сочетании с инертным растворителем.
5. Способ по п.4, отличающийся тем, что N-замещенный лактам выбирают из группы, состоящей из N-метилпирролидона (NMP), N-этилпирролидона (NEP), N-метилпиперидона и 1,3-диметил-3,4,5,6-тетрагидро(2H)-пиримидинона.
6. Способ по п.4, отличающийся тем, что подходящий N,N-дизамещенный амид выбирают из группы, состоящей из диметилформамида (DMF) и диметилацетамида (DMAc).
7. Способ по п.4, отличающийся тем, что инертный растворитель представляет собой теграгидрофуран.
8. Способ по п.4, отличающийся тем, что в качестве растворителя используют смесь 1,3-диметил-3,4,5,6-тетрагидро-2(H)пиримидинона и тетрагидрофурана.
9. Способ по п.1, отличающийся тем, что спирт выбирают из группы, состоящей из этанола и изопропилового спирта.
10. Способ по п.1, отличающийся тем, что кетон выбирают из группы, состоящей из ацетона и метилизобутилкетона.
11. Способ по п.1, отличающийся тем, что кристаллический моногидрат N-формимидоилтиенамицин выделяют путем фильтрации.
Текст
006442 Область техники Настоящее изобретение относится к экономически выгодному и подходящему для производства в промышленном масштабе способу получения кристаллического моногидрата N-формимидоилтиенамицина (моногидрата имипенема) формулы I Уровень техники Моногидрат имипенема, кристаллический моногидрат N-формимидоильного производного тиенамицина формулы I, первым из членов нового класса -лактамных антибиотиков, содержащих циклическую систему карбапенема, стал доступным для клинического применения. Имипенем обладает чрезвычайно широким спектром активности в отношении грамположительных и грамотрицательных аэробных и анаэробных микроорганизмов, что, в частности, является следствием его высокой устойчивости к действию -лактамаз. Имипенем был впервые получен методом лиофилизации, раскрытым в патенте US 4,194,047. Аналогичный процесс кристаллизации вымораживанием или лиофилизации был описан М. Connolly et. al в J.Pharm. Sci, 85, 174-175 (1996). Однако большая часть полученного таким образом продукта часто оказывается аморфной и поэтому термодинамически неустойчивой. Кристаллическая форма моногидрата имипенема, полученная путем кристаллизации лиофилизованного образца, описана в патенте US 4260543, и было неожиданно обнаружено, что она обладает большей устойчивостью по сравнению с лиофилизованной (аморфной) формой. При этом сообщалось о том, что путем изменения условий лиофилизации можно изменить степень кристалличности конечного продукта. Кристалличность представляет особый интерес при исследовании свойств лиофилизованного имипенема, поскольку кристаллический имипенем более термодинамически устойчив, чем аморфный или неупорядоченный имипенем. Способы получения кристаллического имипенема, известные из уровня техники, требуют использования специального оборудования, такого как сублимационная сушилка или лиофилизатор, и делают невыгодным производство в промышленном масштабе, а также не позволяют получить продукт с достаточной степенью кристалличности. Сущность изобретения Задачей настоящего изобретения является предложение экономически выгодного и подходящего для производства в промышленном масштабе способа получения термически устойчивого кристаллического моногидрата имипенема высокой степени чистоты из водного раствора, полученного из реакционной смеси, без применения лиофилизации на какой-либо стадии. Более конкретно, настоящее изобретение относится к способу получения кристаллического моногидрата N-формимидоилтиенамицина (моногидрата имипенема) формулы I, который включает(а) активацию кетоэфирного соединения формулы II где р представляет собой водород или защитную группу, в присутствии подходящего вторичного амина,в подходящем N-замещенном лактаме или N,N-дизамещенном амиде в качестве растворителя, необязательно в сочетании с инертным органическим растворителем, с получением активированного кетоэфира формулы III где Х представляет собой OP(O)(OR)2 или OS(O)2R и R представляет собой С 1-6-алкил, C1-6-алкарил, арил или перфтор-С 1-6-алкил. Термин алкил обозначает линейную или разветвленную цепь, которая при достижении достаточного размера может образовывать цикл. Предпочтительные линейные или разветвлен-1 006442 ные алкильные группы включают метил, этил, пропил, изопропил, бутил и трет.-бутил. Предпочтительные циклоалкильные группы включают циклопропил, циклопентил, циклогексил и циклопропилметил. Термин арил обозначает ароматическое кольцо, включая фенил, замещенный фенил и нафтил. Арильные группы могут быть замещены одним-тремя заместителями, независимо выбранными из галогена, алкила и галогенированной низшей алкильной группы, где алкил такой, как указано выше. Защитная группа р может представлять собой любую легко удаляемую защитную группу карбоксила. Предпочтительно, р может быть выбрано из группы, состоящей из бензила, п-нитробензила и метоксиметила. Подходящий вторичный амин выбирают из группы, состоящей из диизопропиламина, дициклогексиламина, 2,2,6,6-тетраметилэтилпиперидина (ТМР) и 1,1,3,3-тетраметилгуанидина (TMG). Подходящий N-замещенный лактам выбирают из группы, состоящей из N-метилпирролидона(NMP), N-этилпирролидона (NEP), N-метилпиперидинона и 1,3-диметил-3,4,5,6-тетрагидро 2(Н)пиримидинона (DMPH). Подходящий N,N-дизамещенный амид выбирают из группы, состоящей из диметилформамида (DMF), диметилацетамида (DMAc), a необязательный инертный органический растворитель предпочтительно представляет собой тетрагидрофуран. Реакцию проводят при температуре в интервале от -20 до -70 С. Соединение формулы II может быть получено при помощи методов, известных из уровня техники.(b) Взаимодействие активированного кетоэфира формулы III in situ с 2-аминоэтантиолом (цистеамином) или его солью в присутствии вторичного амина в N-замещенном лактаме или N,N-дизамещенном амиде при температуре в интервале от -80 до -40 С с получением эфира тиенамицина формулы IV(с) Взаимодействие эфира тиенамицина формулы IV in situ с гидрохлоридом бензилформимидата(C6H5CH2OCH=NH2+Cl-) в присутствии вторичного амина в N-замещенном лактаме или N,Nдизамещенном амиде с получением амидина эфира карбоновой кислоты (защищенного N-формимидоилтиенамицина) формулы V(d) Восстановление защищенного N-формимидоилтиенамицина формулы V с получением имипенема и очистка раствора, содержащего реакционную смесь при помощи дианионной хроматографии, с последующей кристаллизацией в присутствии подходящего спирта или кетона в качестве сорастворителя с получением кристаллического моногидрата N-формимидоилтиенамицина (моногидрата имипенема). Подходящий спирт и кетон могут быть выбраны из этанола, изопропанола, ацетона и метилизобутилкетона. Подробное описание изобретения В данном разделе приведен пример, иллюстрирующий осуществление способа по изобретению, с целью описания одного из предпочтительных вариантов осуществления изобретения. Однако это не означает, что объем настоящего изобретения должен быть ограничен этим примером. Пример 1. Получение кристаллического моногидрата имипенема Стадия I. Получение (5R,6S)п-Нитробензил-3-(дифенилфосфоно)-6-[(1R)-1-гидроксиэтил]-1 азабицикло[3.2.0]гепт-2-ен-7-он-2-карбоксилата К раствору п-нитробензил-(5R,6S)п-нитробензил-6[(1R)-1-гидроксиэтил]-1-азабицикло[3.2.0]гептан-3,7-дион-2-карбоксилата (20,0 г, 57 ммоль) в смеси тетрагидрофурана и 1,3-диметил-3,4,5,6 тетрагидро(2 Н) пиримидинона (160 мл; 1:1 об./об.) при температуре от -25 до -30 С добавили диизопропиламин (7,0 г, 69 ммоль), а затем дифенилхлорфосфат (17,0 г, 63 ммоль). Смесь перемешивали в течение 40-45 мин при температуре от -10 до -15 С и использовали на следующей стадии без выделения фосфоенольного промежуточного соединения. Стадия II. Получение (5R,6S)п-Нитробензил-3-[(2-аминоэтил)тио]-6-[(1R)-1-гидроксиэтил]-1 азабицикло[3.2.0]гепт-2-ен-7-он-2-карбоксилата-2 006442 Реакционную смесь со стадии I охладили до -75 С. При температуре от -75 до -50 С в течение 10 мин добавили раствор гидрохлорида цистеамина (2-аминоэтантиола) (7.2 г, 63 ммоль) в 1,3-диметил 3,4,5,6-тетрагидро-(2 Н)пиримидиноне (70 мл) и диизопропиламине (7,0 г, 69 ммоль). Полученную таким образом реакционную смесь затем перемешивали при температуре от -40 до -45 С в течение примерно 1 ч и использовали на следующей стадии без выделения продукта. Стадия III. Получение (5R,6S)п-Нитробензил-3-2-[(иминометил)-амино]этил]тио]-6-[(1R)-1 гидроксиэтил]-1-азабицикло[3.2.0]гепт-2-ен-7-он-2-карбоксилата Реакционную смесь со стадии II охладили до -45 С, и добавили сначала диизопропиламин (8,7 г, 86 ммоль), а затем гидрохлорид бензилформимидата (12.8 г, 74.6 ммоль). Полученную реакционную смесь перемешивали при температуре от -45 до -40 С в течение примерно 30 мин, а затем от -20 до -15 С в течение примерно 1 ч 30 мин. Добавили тетрагидрофуран (200 мл) при температуре от -20 до -15 С и отфильтровали из реакционной смеси соли диизопропиламина. Фильтрат содержал PNB эфир Nформамидоил-тиенамицина. Стадия IV. Получение [5R-[5,6(R)-6-(1-гидроксиэтил)-3-2-[(иминометил)амино]этил]тио]-7 оксо-1-азабицикло[3.2.0]гепт-2-ен-2-карбоновой кислоты Фильтрат со стадии III, содержащий PNB-N-формимидоилтиенамицин, вылили в смесь воды (400 мл), N-метилморфолина (18 г) и изопропилового спирта (200 мл) при 0-5 С и рН, примерно равном 7,0. Затем реакционную смесь гидрировали при давлении водорода 3-4 кг при температуре 5-10 С. Реакционную смесь отфильтровали, экстрагировали хлористым метиленом (2 х 300 мл) и отделили водный слой. Водный слой концентрировали до 200 мл путем отгонки при пониженном давлении. Концентрированный раствор очистили при помощи дианионной хроматографии с использованием воды в качестве элюента. Фракции, содержащие целевой продукт, объединили и концентрировали при пониженном давлении либо с использованием простой методики обратного осмоса через полупроницаемую мембрану до объема 50 мл. Затем концентрированный раствор охладили до 0-5 С и добавили к нему изопропиловый спирт (25 мл). После этого раствор перемешивали в течение 40-45 мин при той же самой температуре. Добавили еще одну порцию изопропилового спирта (25 мл) и продолжали перемешивание примерно в течение 1 ч при 0-5 С. Полученный кристаллический осадок отфильтровали, промыли изопропиловым спиртом и ацетоном (2 х 10 мл) и сушили с получением 4,0 г кристаллического N-формимидоилтиенамицина. На рентгенограмме (фиг. 1) показаны пики, характерные для кристаллической формы моногидрата имипенема, аналогичные описанным в патенте US 4,260,543; Чистота по ВЭЖХ = 99.23%. Хотя настоящее изобретение было описано с точки зрения его предпочтительного варианта осуществления, специалисту в данной области будет понятно, что в объем настоящего изобретения следует включить также некоторые его очевидные модификации и эквиваленты. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения кристаллического моногидрата N-формимидоилтиенамицина (имипенема) формулы I, включающий(а) активацию кетоэфирного соединения формулы I где р представляет собой водород или защитную группу, в присутствии подходящего вторичного амина,в подходящем N-замещенном лактаме или N,N-дизамещенном амиде в качестве растворителя, необязательно в сочетании с инертным органическим растворителем, с получением соединения формулы III где X представлят собой OP(O)(OR)2 или OS(O)2R и R представляет собой С 1-6-алкил, C1-6-алкарил, арил или перфтор-С 1-6-алкил; термин алкил обозначает линейную или разветвленную цепь, которая при достижении достаточного размера может образовывать цикл; предпочтительные линейные или разветвленные алкильные группы включают метил, этил, пропил, изопропил, бутил и трет.-бутил; предпочтительные циклоалкильные группы включают циклопропил, циклопентил, циклогексил и циклопропилметил; термин арил обозначает ароматическое кольцо, включая фенил, замещенный фенил и нафтил; арильные группы могут быть замещены одним-тремя заместителями, независимо выбранными из галогена, алкила и галогенированной низшей алкильной группы, где алкил такой, как указано выше,(b) взаимодействие активированного кетоэфира формулы III in situ с 2-аминоэтантиолом (цистеамином) или его солью в присутствии вторичного амина в N-замещенном лактаме или N,N-дизамещенном амиде с получением эфира тиенамицина формулы IV где р, N-замещенный лактам и N,N-дизамещенный амин такие, как указано выше,(с) взаимодействие эфира тиенамицина формулы IV in situ с гидрохлоридом бензилформимидата(С 6 Н 5 СH2 ОСH=NH2+Cl-) в присутствии вторичного амина в N-замещенном лактаме или N,Nдизамещенном амиде с получением амидина эфира карбоновой кислоты (защищенного N-формимидоилтиенамицина) формулы V где р, N-замещенный лактам и N,N-дизамещенный амин такие, как указано выше,(d) восстановление защищенного N-формимидоилтиенамицина формулы V с получением Nформимидоилтиенамицина (имипенема) в растворе и очистку раствора, содержащего реакционную смесь, при помощи дианионной хроматографии, с последующей кристаллизацией в присутствии подходящего спирта или кетона в качестве сорастворителя с получением кристаллического моногидрата Nформимидоилтиенамицина (моногидрата имипенема) формулы I высокой степени чистоты. 2. Способ по п.1, отличающийся тем, что защитную группу р выбирают из группы, состоящей из бензила, п-нитробензила и метоксиметила. 3. Способ по п.1, отличающийся тем, что подходящий вторичный амин выбирают из группы, состоящей из диизопропиламина, дициклогексиламина, 2,2,6,6-тетраметилэтилпиперидина (ТМР) и 1,1,3,3 тетраметилгуанидина (TMG). 4. Способ по п.1, отличающийся тем, что N-замещенный лактам или N,N-дизамещенный амид используют отдельно или в сочетании с инертным растворителем. 5. Способ по п.4, отличающийся тем, что N-замещенный лактам выбирают из группы, состоящей изN-метилпирролидона (NMP), N-этилпирролидона (NEP), N-метилпиперидона и 1,3-диметил-3,4,5,6 тетрагидро(2 Н)-пиримидинона. 6. Способ по п.4, отличающийся тем, что подходящий N,N-дизамещенный амид выбирают из группы, состоящей из диметилформамида (DMF) и диметилацетамида (DMAc). 7. Способ по п.4, отличающийся тем, что инертный растворитель представляет собой теграгидрофуран.-4 006442 8. Способ по п.4, отличающийся тем, что в качестве растворителя используют смесь 1,3-диметил 3,4,5,6-тетрагидро-2(Н)пиримидинона и тетрагидрофурана. 9. Способ по п.1, отличающийся тем, что спирт выбирают из группы, состоящей из этанола и изопропилового спирта. 10. Способ по п.1, отличающийся тем, что кетон выбирают из группы, состоящей из ацетона и метилизобутилкетона. 11. Способ по п.1, отличающийся тем, что кристаллический моногидрат N-формимидоилтиенамицин выделяют путем фильтрации.
МПК / Метки
МПК: C07D 477/20
Метки: моногидрата, кристаллического, имипенема, получения, способ, n-формимидоил-тиенамицина
Код ссылки
<a href="https://eas.patents.su/6-6442-sposob-polucheniya-kristallicheskogo-monogidrata-n-formimidoil-tienamicina-monogidrata-imipenema.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения кристаллического моногидрата n-формимидоил-тиенамицина (моногидрата имипенема)</a>
Предыдущий патент: Способ и композиция для уменьшения воспалительного процесса и/или аномальной активации неспецифической иммунной реакции
Следующий патент: Ингибиторы трипептидил пептидазы
Случайный патент: Фторпроизводные фенилзамещенных 4-азастероидов и их применение










