Замещенные конденсированные гетероциклические с-гликозиды
Формула / Реферат
1. Соединение формулы
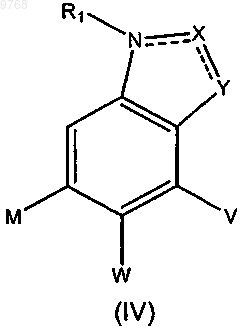
в которой одна из пунктирных линий находится между NR1 и X, или между X и Y, или обе отсутствуют;
два из V, M и W представляют Н и третий является
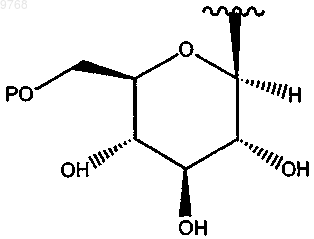
R1 представляет Н или C1-4алкил или R1 отсутствует, когда имеется пунктирная линия между NR1 и X;
X представляет N, C=O, CH или C-Q-Z;
Y представляет N-Q-Z или C-Q-Z, когда X является N, C=O или CH;
Y представляет CH, когда X является C-Q-Z;
Q = -(CH2)n-, где n=1 или 2;
Р = Н, C1-7ацил или (C1-6алкокси)карбонил;
Z является замещенным или незамещенным, и выбран из C3-7циклоалкила, фенила, 5- или
6-членного гетероарила, содержащего 1 или 2 гетероатома, независимо выбранных из N, О и S, биарила, 9- или 10-членного конденсированного бициклила и конденсированного гетеробициклила, где указанный конденсированный гетеробициклил содержит от 1 до 4 гетероатомов, независимо выбранных из N, О и S; или фармацевтически приемлемая соль.
2. Соединение по п.1, в котором R1 представляет Н или отсутствует.
3. Соединение по п.1, в котором Z независимо замещен 1-3 заместителями, независимо выбранными из C1-4алкокси, фенокси, C1-4алкила, C3-6циклоалкила, атома галогена, гидрокси, циано, амино,
C1-4алкилтио, C1-4алкилсульфонила, C1-4алкилсульфинила, C1-4аминоалкила, моно- и ди-C1-4алкиламино, фенила, C1-4алкиламиносульфонила (SO2NHR), амино (C1-4алкилсульфонила) (NHSO2R),
ди-C1-4алкиламиносульфинила (SONHRR), C1-4алкиламидо (NHCOR), C1-4алкилкарбамидо (CONHR),
5-6-членного гетероциклила, содержащего 1-3 гетероатомов, независимо выбранных из N, S и О; и где заместитель(и) в Z может быть дополнительно независимо замещен 1-3 заместителями, независимо выбранными из C1-4алкокси, C1-4алкила, атома галогена, гидрокси, циано, амино, моно- и ди-C1-4алкиламино и C1-4алкилтио.
4. Соединение по п.1, в котором Z представляет 4-замещенный фенил, 3,4-дизамещенный фенил, бензгидрил, замещенный или незамещенный тиофенил, биарил, бензофуранил, гидробензофуранил,
дигидробензофуранил, 4-замещенный пиридил, бензо[b]тиенил, хроманил, бензотиофенил, инданил, нафтил и 2,3-дигидробензо[1,4]диоксан.
5. Соединение по п.3, в котором Z является незамещенным или замещенным 1-2 заместителями, независимо выбранными из метокси, этокси, атома фтора, атома хлора, метила, этила, пропила, бутила и изопропила.
6. Соединение по п.1, в котором Z представляет бифенил, 4-(3-пиридил)фенил, 4-(2-тиенил)фенил, 4-(1Н-пиразол-1-ил)фенил, (4-этил)фенил, (4-пропил)фенил, (4-метокси)фенил, дигидробензофуран-5-ил или дигидробензофуран-6-ил.
7. Соединение по п.1, в котором R1 представляет Н.
8. Соединение по п.1, в котором n равно 1.
9. Соединение по п.8, в котором R1 представляет Н или отсутствует.
10. Соединение по п.1, в котором Z представляет бифенил, 4-(3-пиридил)фенил, 4-(2-тиенил)фенил, 4-(1Н-пиразол-1-ил)фенил, (4-этил)фенил, (4-пропил)фенил, (4-метокси)фенил, дигидробензофуран-5-ил или дигидробензофуран-6-ил и Z является незамещенным или замещенным 1-2 заместителями, независимо выбранными из метокси, этокси, атома фтора, атома хлора, метила, этила, пропила, бутила и изопропила.
11. Соединение по п.10, в котором n равно 1.
12. Соединение по п.10, в котором R представляет Н.
13. Соединение по п.1, в котором М и V представляют Н.
14. Соединение по п.1, в котором М и W представляют Н.
15. Соединение по п.1, в котором X представляет CH и Y является C-Q-Z.
16. Соединение по п.1, в котором X представляет C-Q-Z и Y является CH.
17. Соединение по п.15, в котором R1 представляет Н или отсутствует и n=1.
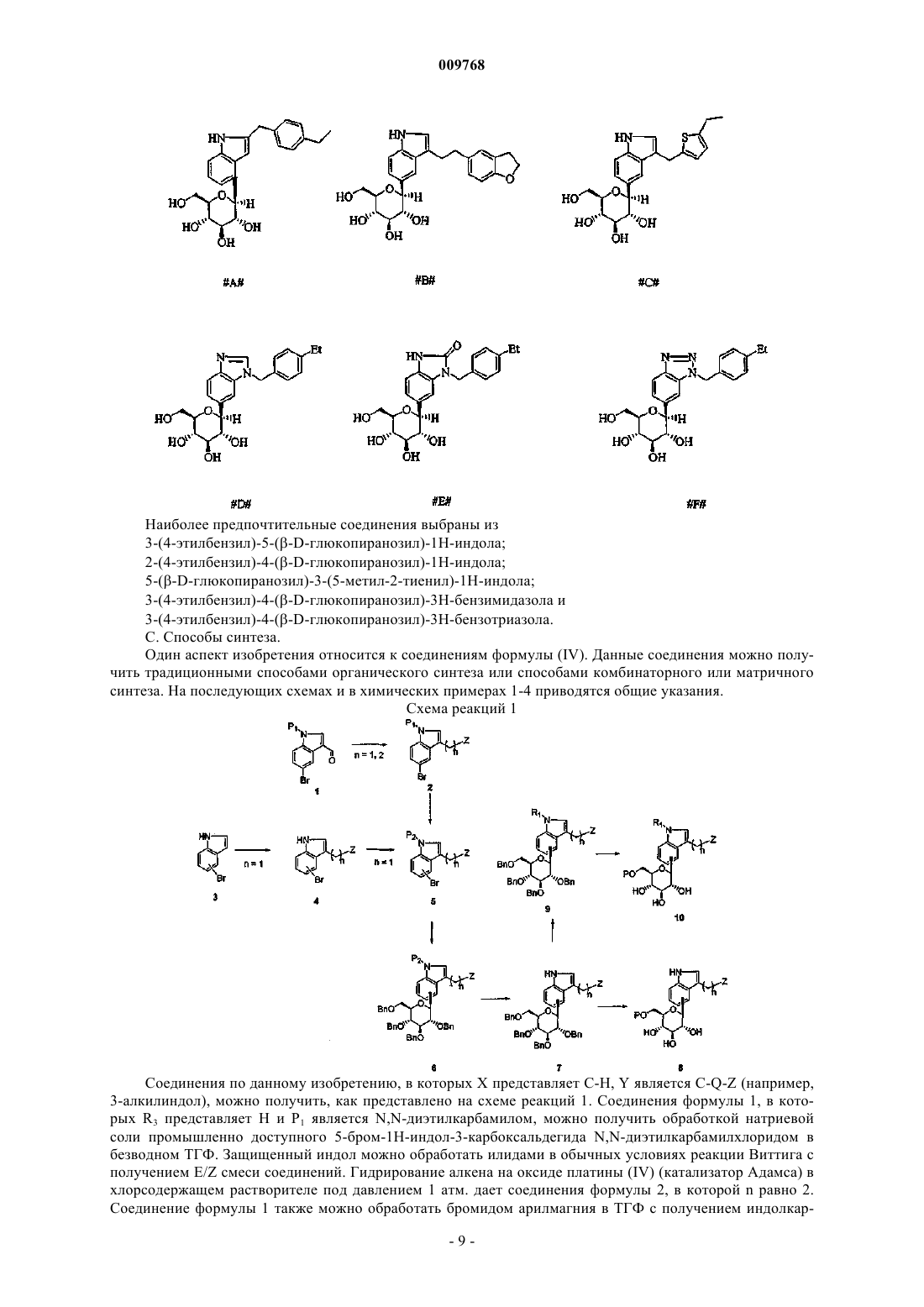
18. Соединение по п.1, выбранное из
3-(4-этилбензил)-5-(b-D-глюкопиранозил)-1Н-индола,
5-(b-D-глюкопиранозил)-3-(4-метоксибензил)-1Н-индола,
5-(b-D-глюкопиранозил)-3-[2-(4-метоксифенил)этил]-1Н-индола и
3-(4-этилбензил)-4-(b-D-глюкопиранозил)-1Н-индола.
19. Соединение по п.1, выбранное из
2-(4-этилбензил)-4-(b-D-глюкопиранозил)-1Н-индола,
3-[2-(2,3-дигидробензофуран-5-ил)этил]-5-(b-D-глюкопиранозил)-1Н-индола,
5-(b-D-глюкопиранозил)-3-(5-метил-2-тиенил)-1Н-индола,
3-(4-этилбензил)-4-(b-D-глюкопиранозил)-3Н-бензимидазола,
3-(4-этилбензил)-4-(b-D-глюкопиранозил)-1,3-дигидробензимидазол-2-она и
3-(4-этилбензил)-4-(b-D-глюкопиранозил)-3Н-бензотриазола.
20. Соединение по п.1, выбранное из
3-(4-этилбензил)-5-(b-D-глюкопиранозил)-1Н-индола,
2-(4-этилбензил)-4-(b-D-глюкопиранозил)-1Н-индола,
5-(b-D-глюкопиранозил)-3-(5-метил-2-тиенил)-1Н-индола,
3-(4-этилбензил)-4-(b-D-глюкопиранозил)-3Н-бензимидазола и
3-(4-этилбензил)-4-(b-D-глюкопиранозил)-3Н-бензотриазола.
21. Фармацевтическая композиция, содержащая соединение по пп.1, 5, 6, 11-19 или 20.
22. Фармацевтическая композиция по п.21, содержащая соединение по п.14 и фармацевтически приемлемый носитель.
23. Способ лечения диабета у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21.
24. Способ по п.23, в котором указанный диабет представляет диабет типа II.
25. Способ снижения концентрации глюкозы в сыворотке крови у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21.
26. Способ лечения пониженной толерантности к глюкозе у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21.
27. Способ лечения или ингибирования пониженной толерантности к глюкозе у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21.
28. Способ снижения индекса массы тела, массы тела или процента жировой ткани тела у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21.
29. Способ по п.28, где указанный способ снижения индекса массы тела представляет способ лечения ожирения или избыточной массы тела.
30. Способ ингибирования переносчика натрия-глюкозы в клетке воздействием на данную клетку соединением по п.1 или его метаболитом.
31. Способ лечения диабета или синдрома X, или связанных с ними симптомов или осложнений у субъекта, включающий:
а) введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы формулы (IV) и
b) введение указанному субъекту совместно эффективного количества второго противодиабетического средства,
где указанное совместное введение проводят в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый терапевтический эффект.
32. Способ по п.31, в котором второе противодиабетическое средство представляет агонист RXR.
33. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения выбррэы из IDDM, NIDDM, IGT, IFG, ожирения, нефропатии, нейропатии, ретинопатии, атеросклероза, синдрома поликистоза яичников, гипертензии, ишемии, инсульта, заболевания сердца, синдрома раздраженного кишечника, воспаления и катаракты.
34. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения представляют IDDM.
35. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения представляют NIDDM.
36. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения представляют IGT или IFG.
37. Способ по п.31, дополнительно включающий введение указанному субъекту совместно эффективного количества третьего противодиабетического средства.
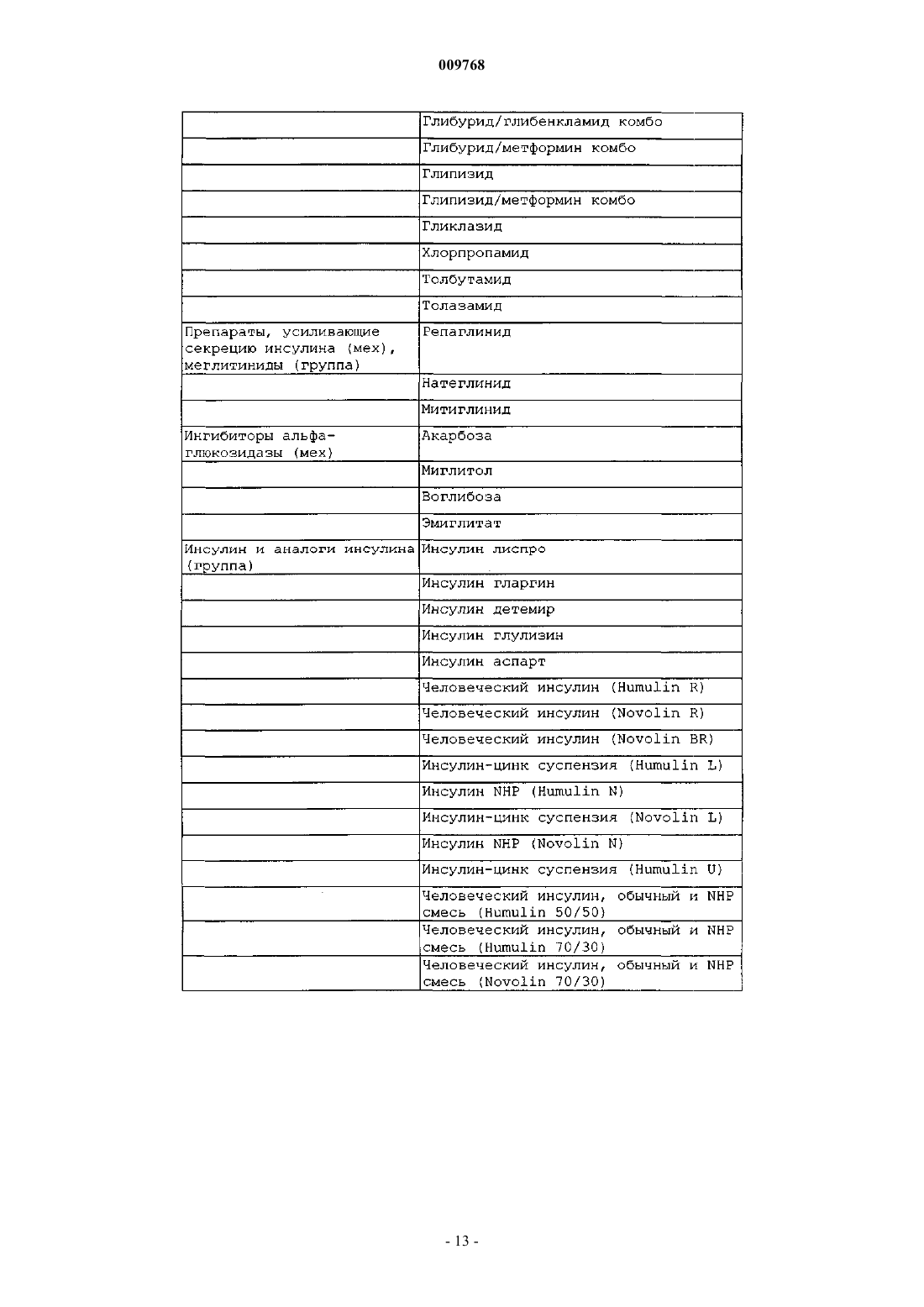
38. Способ по п.37, в котором третье противодиабетическое средство выбрано из:
а) инсулинов,
b) аналогов инсулина,
c) модуляторов секреции инсулина и
d) средств, стимулирующих секрецию инсулина.
39. Способ по п.31, в котором ингибитором реабсорбции глюкозы является ингибитор SGLT.
40. Способ по п.31, в котором ингибитором реабсорбции глюкозы является ингибитор SGLT1.
41. Способ по п.31, в котором ингибитором реабсорбции глюкозы является ингибитор SGLT2.
42. Способ по п.31, в котором ингибитором реабсороции глюкозы является соединение формулы (IV) или его оптический изомер, энантиомер, диастереомер, рацемат или рацемическая смесь, сложный эфир, пролекарство или его фармацевтически приемлемая соль.
43. Способ по п.31, в котором совместно эффективное количество ингибитора SGLT находится в пределах примерно от 10 до 1000 мг.
44. Способ по п.31, в котором совместно эффективное количество ингибитора SGLT представляет количество, достаточное для снижения изменения уровня глюкозы в плазме крови после приема пищи.
45. Способ подавления начала развития диабета или синдрома X или связанных с ними симптомов или осложнений у субъекта, где указанный способ включает:
a) введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы формулы (IV) и
b) введение указанному субъекту совместно эффективного количества второго противодиабетического средства,
где указанное совместное введение проводят в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый профилактический эффект.
46. Способ по п.45, в котором указанное начало развития представляет переход от состояния преддиабета до NIDDM.
47. Фармацевтическая композиция, содержащая ингибитор реабсорбции глюкозы формулы (IV), второе противодиабетическое средство и фармацевтически приемлемый носитель.
48. Фармацевтическая композиция по п.47, в которой ингибитором реабсорбции глюкозы является ингибитор SGLT .
49. Фармацевтическая композиция по п.47, в которой ингибитором реабсорбции глюкозы является ингибитор SGLT1.
50. Фармацевтическая композиция по п.47, в которой ингибитором реабсорбции глюкозы является ингибитор SGLT2.
51. Способ составления рецептуры фармацевтической композиции, предусматривающий включение в рецептуру ингибитора реабсорбции глюкозы, второго противодиабетического средства и фармацевтически приемлемого носителя.
52. Способ получения фармацевтической композиции, включающий смешение одного или более ингибиторов реабсорбции глюкозы в комбинации со вторым противодиабетическим средством для получения лекарственного препарата для лечения состояния, выбранного из IDDM, NIDDM, IGT, IFG, ожирения, нефропатии, нейропатии, ретинопатии, атеросклероза, синдрома поликистоза яичников, гипертензии, ишемии, инсульта, заболевания сердца, синдрома раздраженного кишечника, воспаления и катаракты.
53. Способ подавления прогрессирования состояния преддиабета до диабета у субъекта, включающий:
a) введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы формулы (IV) и
b) введение указанному субъекту совместно эффективного количества второго противодиабетического средства,
где указанное совместное введение проводят в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый подавляющий эффект.
54. Способ по п.53, в котором указанное состояние представляет IGT или IFG.
55. Способ по п.53, в котором указанное подавление прогрессирования состояния преддиабета представляет профилактику прогрессирования состояния преддиабета до диабета.
56. Способ по п.53, в котором ингибитором реабсорбции глюкозы является соединение формулы (IV), необязательно содержащее одну или более гидроксил- или диолзащищающих групп, или его оптический изомер, энантиомер, диастереомер, рацемат или рацемическая смесь, сложный эфир, пролекарство, или его фармацевтически приемлемая соль.
Текст
009768 Область техники, к которой относится изобретение Данное изобретение относится к замещенным конденсированным гетероциклическимC-гликозидам, композициям, содержащим их, способам их применения, например, для лечения или профилактики диабета и синдрома X. Уровень техники Диабет является хроническим заболеванием, оказывающим отрицательное влияние на углеводный,жировой и белковый обмен у животных. Сахарный диабет типа I, который составляет примерно 10% всех случаев диабета, ранее относили к инсулинзависимому сахарному диабету (IDDM) или ювенильному диабету. Данное заболевание характеризуется прогрессирующей потерей функции секреции инсулина у бета-клеток поджелудочной железы. Данную характеристику также разделяет неидиопатический или вторичный диабет, который развивается в результате заболевания поджелудочной железы. Для сахарного диабета типа I характерны следующие клинические признаки или симптомы: устойчиво повышенная концентрация глюкозы в плазме крови или гипергликемия; полиурия; полидипсия и/или гиперфагия; хронические микрососудистые осложнения, такие как ретинопатия, нефропатия и нейропатия; макрососудистые осложнения, такие как гиперлипидемия и гипертензия, которые могут привести к слепоте, заболеванию почек на конечной стадии, ампутации конечностей и инфаркту миокарда. Сахарный диабет типа II (неинсулинзависимый сахарный диабет или NIDDM) представляет собой обменное заболевание, заключающееся в нарушении регуляции метаболизма глюкозы и пониженной чувствительности к инсулину. Сахарный диабет типа II, как правило, развивается во взрослом возрасте и связан с неспособностью организма утилизировать или продуцировать в достаточном количестве инсулин. Помимо резистентности к инсулину, наблюдаемой в тканях-мишенях, у пациентов, страдающих сахарным диабетом типа II, имеется относительная недостаточность инсулина, т.е. у пациентов имеется более низкий, чем предполагаемый уровень инсулина для данной концентрации глюкозы в плазме крови. Сахарный диабет типа II характеризуется следующими клиническими признаками или симптомами: устойчиво повышенная концентрация глюкозы в плазме крови или гипергликемия; полиурия; полидипсия и/или гиперфагия; хронические микрососудистые осложнения, такие как ретинопатия, нефропатия и нейропатия; макрососудистые осложнения, такие как гиперлипидемия и гипертензия, которые могут привести к слепоте, заболеванию почек на конечной стадии, ампутации конечностей и инфаркту миокарда. Синдром X, также называемый синдромом резистентности к инсулину (IRS), обменным синдромом или обменным синдромом X, обнаруживается в 2% случаев диагностических катетеризаций коронарных сосудов. Часто оказывая отрицательное влияние, он индуцирует симптомы или факторы риска для развития сахарного диабета типа II или сердечно-сосудистого заболевания, включая пониженную толерантность к глюкозе (IGT), пониженный уровень глюкозы натощак (IFG), гиперинсулинемию, резистентность к инсулину, дислипидемию (например, высокая концентрация триглицеридов, низкая HDL), гипертензию и ожирение. Лечение пациентов с IDDM в течение длительного периода времени основывалось на введении экзогенного инсулина, полученного из различных источников (например, человеческого, бычьего, свиного инсулина). Применение вещества от гетерологичных видов приводит к продукции антител против инсулина, которые оказывают ограничивающее активность действие и приводят к прогрессирующей необходимости в использовании более высоких доз для достижения желаемого гипогликемического эффекта. Обычное лечение сахарного диабета типа II основано на поддержании уровня глюкозы в крови, как можно близкого к норме, при изменении образа жизни в отношении рациона и нагрузок, и когда это необходимо, на лечении противодиабетическими средствами, инсулином или их сочетанием. ЛечениеNIDDM, который невозможно контролировать рационом, основано на противодиабетических средствах для приема внутрь. Несмотря на то что резистентность к инсулину не всегда подвергается лечению у всех пациентов с синдромом X, у тех, у которых имеется состояние преддиабета (например, IGT, IFG), когда уровни глюкозы натощак могут быть выше по сравнению с нормой, но не на уровне диагностического критерия для диабета, его лечат в некоторых странах (например, в Германии) метформином для профилактики диабета. Противодиабетические средства можно комбинировать с фармакологическими средствами для лечения сопутствующих заболеваний (например, гипотензивными препаратами при гипертонии, гиполипидемическими средствами при липидемии). Лекарственные препараты первого ряда включают метформин и сульфонилмочевины, а также тиазолидиндионы. Монотерапия метформином представляет выбор первого ряда, особенно для лечения пациентов с диабетом типа II, у которых также имеется ожирение и/или дислипидемия. При отсутствии соответствующей ответной реакции на метформин часто лечение метформином продолжают в комбинации с сульфонилмочевинами, тиазолидиндионами или инсулином. Монотерапия сульфонилмочевиной(включая все поколения лекарственных препаратов) также является распространенным лечением первого ряда. Другим выбором терапии первого ряда могут быть тиазолидиндионы. Ингибиторы альфаглюкозидазы также применяют в качестве препаратов первого и второго ряда. Пациентам, которые не реагируют соответствующим образом на монотерапию противодиабетическими средствами для приема внутрь, назначают комбинации вышеуказанных средств. В тех случаях, когда гликемический контроль невозможно поддерживать только при применении противодиабетических препаратов для перорального введения, применяют лечение инсулином в качестве монотерапии или комбинации с противодиабетическими средствами для приема внутрь. Одно последнее достижение в лечении гипергликемии основано на выделении избыточного количества глюкозы непосредственно в мочу. Было показано, что избирательные ингибиторы SGLT повышают выделение глюкозы в мочу и снижают концентрацию глюкозы в крови на моделях IDDM и NIDDM на грызунах. Сущность изобретения Один аспект настоящего изобретения относится к способам и композициям для лечения и профилактики диабета, синдрома X или связанных с ними симптомов и осложнений. Конкретнее, данное изобретение относится к новому способу лечения диабета или синдрома X или связанных с ними симптомов и осложнений у субъекта, страдающего таким состояниям, где указанный способ включает введение одного или более ингибиторов реабсорбции глюкозы и введение одного или более противодиабетических средств для лечения диабета или синдрома X или связанных с ними симптомов и осложнений. Другой аспект изобретения относится к соединениям формулы в которой одна из пунктирных линий находится между NR1 и X или между X и Y или обе отсутствуют; два из V, М и W представляют Н и третий являетсяR1 представляет Н или C1-4 алкил или R1 отсутствует, когда имеется пунктирная линия между NR1 и X;Z является замещенным или незамещенным и выбран из C3-7 циклоалкила, фенила, 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, независимо выбранных из N, O и S, биарила,9- или 10-членного конденсированного бициклила (такого как нафтил) и конденсированного гетеробициклила, где указанный конденсированный гетеробициклил содержит от 1 до 4 гетероатомов (и предпочтительно 1-3 или 1-2 гетероатома), независимо выбранных из N, O и S;P=H, C1-7 ацил или (C1-6 алкокси)карбонил; или их фармацевтически приемлемой соли. Один аспект изобретения относится к фармацевтической композиции, содержащей ингибитор реабсорбции глюкозы, по меньшей мере одно дополнительное противодиабетическое средство и фармацевтически приемлемый носитель. Изобретение также относится к способу составления рецептуры фармацевтической композиции, включающему включение в рецептуру ингибитора реабсорбции глюкозы, одного или более противодиабетических средств и фармацевтически приемлемого носителя. Одним вариантом осуществления изобретения является способ лечения диабета или синдрома X либо связанных с ними симптомов и осложнений у субъекта, где указанный способ включает введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы и введение указанному субъекту совместно эффективного количества по меньшей мере одного противодиабетического средства, где указанное комбинированное введение обеспечивает желаемый терапевтический эффект.-2 009768 Другим вариантом осуществления изобретения является способ подавления начала развития диабета или синдрома X либо связанных с ними симптомов и осложнений у субъекта, где указанный способ включает введение указанному субъекту совместно эффективной дозы ингибитора реабсорбции глюкозы и введение указанному субъекту совместно эффективного количества одного или более противодиабетических средств, где указанное комбинированное введение обеспечивает желаемый профилактический эффект. В раскрытых способах диабет или синдром X либо связанные с ними симптомы и осложнения выбраны из IDDM, NIDDM, IGT, IFG, ожирения, нефропатии, нейропатии, ретинопатии, атеросклероза,синдрома поликистоза яичников, гипертензии, ишемии, инсульта, заболевания сердца, синдрома раздраженного кишечника, воспаления и катаракты. Также в изобретение включается применение одного или более ингибиторов реабсорбции глюкозы в комбинации с одним или более противодиабетическими средствами для получения лекарственного препарата для лечения состояния, выбранного из IDDM, NIDDM, IGT, IFG, ожирения, нефропатии, нейропатии, ретинопатии, атеросклероза, синдрома поликистоза яичников, гипертензии, ишемии, инсульта,заболевания сердца, синдрома раздраженного кишечника, воспаления и катаракты. Подробное описание изобретения Все типы диабета, независимо от их генетических и обусловленных окружающими условиями причин, имеют общее, заключающееся в явной недостаточности инсулина или неадекватной функции инсулина. Поскольку транспорт глюкозы из крови в мышечную и жировую ткань является зависимым от инсулина, то при диабете теряется способность адекватно утилизировать глюкозу, что приводит к нежелательному накоплению глюкозы в крови (гипергликемии). Хроническая гипергликемия приводит к снижению секреции инсулина и вносит свой вклад в развитие повышенной резистентности к инсулину, и в результате концентрация глюкозы в крови повышается таким образом, что диабет самообстряется (Diabetologia, 1985, Hyperglycaemia as an inducer as well as a consequence of impaired isle cell function and insulin resistance: implications for the management of diabetes. Vol. 28, p. 119); Diabetes Cares, 1990, vol. 13, 6, Glucose Toxicity, p. 610-630). Следовательно, при лечении гипергликемии вышеуказанный цикл самообострения прерывают таким образом, что становятся возможными профилактика или лечение диабета. В патенте США 6153632, R. Rieveley, раскрываются способ и композиция для лечения сахарного диабета (типа I, нарушенная толерантность к глюкозе [IGT] и типа II), которая включает терапевтически эффективное количество одного или более сенсибилизаторов инсулина наряду с одним или более инсулином для перорального введения, инъекционным инсулином, сульфонилмочевиной, бигуанидом или ингибитором альфа-глюкозидазы для лечения сахарного диабета. По одному аспекту изобретение относится к комбинации модулятора PPAR, предпочтительно-агониста PPAR, и ингибитора SGLT, предпочтительно ингибитора SGLT 2 или избирательного ингибитора SGLT 2. А. Термины. Ниже приводится определение некоторых терминов и их использование в данном раскрытии. Если не указано иначе, то термины алкил и алкокси, в том смысле, в котором они здесь применяются, используются они самостоятельно или как часть заместителя, включают прямой, циклический и разветвленный алкил, содержащий 1-8 атомов углерода или любое число в данных пределах. Например,алкильные радикалы включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, третбутил, 2-бутенил, 2-бутинил, н-пентил, 3-(2-метил)бутил, 2-пентил, 2-метилбутил, неопентил, н-гексил,2-гексил и 2-метилпентил. Алкоксильные радикалы представляют собой кислородсодержащие эфиры,образованные из описанных выше алкильных групп с прямой или разветвленной цепью. Алкильная и алкоксильная группы могут быть независимо замещены от одной до пяти, предпочтительно от одной до трех групп, выбранных из атома галогена (F, Cl, Br, I), оксо, ОН, амино, карбоксила и алкокси. Алкильная и алкоксильная группы могут быть также независимо связаны с одним или более ПЭГ-радикалами(полиэтиленгликоль). Термин ацил, в том смысле, в котором он здесь применяется, используется он самостоятельно или как часть заместителя, означает органический радикал, содержащий карбонильную группу, связанную с гидрокарбильной группой, содержащей 1-7 атомов углерода (с разветвленной или прямой цепью,или циклической), полученный из органической кислоты удалением гидроксильной группы. Например,C4 ацил может включать (CO)CH2CH2CH2CH3 и (CO)(CH2)(CH)(CH3)2, аналогично C6 ацил включает(CO)(C6H13) и (CO)(C6H5). Термин Ас, в том смысле, в котором он здесь применяется, используется самостоятельно или как часть заместителя, означает ацетил. Арил представляет карбоциклический ароматический радикал, включая, но не ограничиваясь этим, фенил, 1- или 2-нафтил и т.п. Карбоциклический ароматический радикал может быть замещен независимым замещением 1-3 атомов водорода в нем атомом галогена, ОН, CN, меркапто, нитро, амино,циано, необязательно замещенным C1-C8 алкилом, необязательно замещенным алкокси, алкилтио,алкилсульфинилом, алкилсульфонилом, алкиламино, ди(C1-C8 алкил)амино, формилом, карбоксилом,алкоксикарбонилом, алкоксикарбонилокси, алканоилокси, фенилом, карбамоилом, карбоксамидом,ди-низшим алкилкарбамоилокси, феноксикарбонилокси, низшим алкилендиокси, бензоилокси,-3 009768 алкил-CO-O-, алкил-O-CO-, -CONH2, алкил-O-CO-O- или алкил-CO-NH-. Показательные арильные радикалы включают, например, фенил, нафтил, бифенил, инден индан фторфенил, дифторфенил, бензил, бензоилоксифенил, карбоэтоксифенил, ацетилфенил, этоксифенил, феноксифенил, гидроксифенил, карбоксифенил, трифторметилфенил, метоксиэтилфенил, ацетамидофенил, толил, ксилил,диметилкарбамилфенил и т.п. Ph или РН означает фенил. Термин гетероарил, в том смысле, в котором он здесь используется, означает стабильную 5- или 6-членную моноциклическую или бициклическую ароматическую кольцевую систему, которая состоит из атомов углерода и от одного до трех гетероатомов, выбранных из N, О и S. Гетероарильная группа может быть соединена с любым гетероатомом или атомом углерода, что приводит к образованию стабильной структуры. Примеры гетероарильных групп включают, но не ограничиваются ими, бензофуранил, бензотиофенил, пиридинил, пиразинил, пиридазинил, пиримидинил, тиофенил, фуранил, имидазолил, изоксазолил, оксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, триазолил, бензимидазолил,бензофуранил, бензотиенил, бензизоксазолил, бензоксазолил, бензопиразолил, индолил, бензотиазолил,бензотиадиазолил, бензотриазолил или хинолинил. Предпочтительные гетероарильные группы включают пиридинил, тиофенил, фуранил и хинолинил. В том случае, когда гетероарильная группа является замещенной, то она может иметь от одного до трех заместителей, которые независимо выбраны из атома галогена, ОН, CN, меркапто, нитро, амино, циано,необязательно замещенного C1-C8 алкила, необязательно замещенного алкокси, алкилтио, алкилсульфинила, алкилсульфонила, алкиламино, ди(C1-C8 алкил)амино, формила, карбоксила, алкоксикарбонила,алкоксикарбонилокси, алканоилокси, фенила, карбамоила, карбоксамида, ди-низшего алкилкарбамоилокси, феноксикарбонилокси, низшего алкилендиокси, бензоилокси, алкил-CO-O-, алкил-O-CO-,-CONH2, алкил-O-CO-O- или алкил-CO-NH-. Термины гетероцикл, гетероциклический и гетероциклил относятся к необязательно замещенной, полностью или частично насыщенной, ароматической или неароматической циклической группе, которая, например, является 4-7-членной моноциклической, 7-11-членной (или 9-10-членной) бициклической (или гетеробициклил) или 10-15-членной трициклической кольцевой системой, которая содержит по меньшей мере один гетероатом по меньшей мере в одном содержащем атом углерода кольце. Каждый цикл гетероциклической группы, содержащей гетероатом, может иметь 1, 2 или 3 гетероатома,выбранных из атомов азота, атомов кислорода и атомов серы, где гетероатомы азота и серы также могут быть необязательно окислены. Атомы азота могут быть необязательно кватернизованы. Гетероциклическая группа может быть присоединена по любому гетероатому или атому углерода. Примеры моноциклических гетероциклических групп включают пирролидинил; оксетанил; пиразолинил; имидазолинил; имидазолидинил; оксазолил; оксазолидинил; изоксазолинил; тиазолидинил; изотиазолидинил; тетрагидрофурил; пиперидинил; пиперазинил; 2-оксопиперазинил; 2-оксопиперидинил; 2-оксопирролидинил; 4-пиперидонил; тетрагидропиранил; тетрагидротиопиранил; тетрагидротиопиранилсульфон; морфолинил; тиоморфолинил; тиоморфолинилсульфоксид; тиоморфолинилсульфон; 1,3-диоксолан; диоксанил; тиетанил; тииранил и т.п. Примеры бициклических гетероциклических групп (или гетеробициклилов) включают хинуклидинил; тетрагидроизохинолинил; дигидроизоиндолил; дигидрохиназолинил (такой как 3,4-дигидро-4 оксохиназолинил); дигидробензофурил; дигидробензотиенил; дигидробензотиопиранил; дигидробензотиопиранилсульфон; дигидробензопиранил; индолинил; изохроманил; изоиндолинил; бензимидазолил; бензтиазолил; пиперонил; тетрагидрохинолинил и т.п. В том случае, когда гетероарильная группа является замещенной, то гетероциклил может быть независимо замещен 1-5, предпочтительно 1-3 группами, выбранными из атома галогена, OH, CN,меркапто, нитро, амино, циано, необязательно замещенного C1-C8 алкила, необязательно замещенного алкокси, алкилтио, алкилсульфинила, алкилсульфонила, алкиламино, ди(C1-C8 алкил)амино, формила,карбоксила, алкоксикарбонила, алкоксикарбонилокси, алканоилокси, фенила, карбамоила, карбоксамида,ди-низшего алкилкарбамоилокси, феноксикарбонилокси, низшего алкилендиокси, бензоилокси, алкилCO-O-, алкил-O-CO-, -CONH2, алкил-O-CO-O- или алкил-CO-NH-. Термин биарил включает гетероарил, связанный с фенилом; фенил, связанный с гетероарилом Термин композиция предназначен для характеристики продукта, содержащего указанные ингредиенты в указанных количествах, а также любой продукт, который происходит, прямо или опосредованно, из комбинаций указанных ингредиентов в указанных количествах.-4 009768 Термин комбинированное введение включает совместное введение, когда 1) два или более средств вводят субъекту в основном в одно и то же время и 2) два или более средств вводят субъекту в различное время с независимыми интервалами, которые могут или не могут перекрываться или совпадать. Термин субъект, в том смысле, в котором он здесь используется, относится к животному, предпочтительно млекопитающему, наиболее предпочтительно человеку, который является объектом лечения, наблюдения или эксперимента. Термин модулятор RXR, в том смысле, в котором он здесь используется, относится к агонистам,неполным агонистам или антагонистам ретиноидных Х рецепторов. Предпочтительно модулятор повышает чувствительность к инсулину. По одному аспекту модулятор представляет агонист RXR. Диабет, синдром X и связанные симптомы и осложнения включают такие состояния, как IDDM,NIDDM, IGT, IFG, ожирение, нефропатия, нейропатия, ретинопатия, атеросклероз, синдром поликистоза яичников, гипертензия, ишемия, инсульт, заболевание сердца, синдром раздраженного кишечника, воспаление и катаракта. Примеры состояния преддиабета включают IGT и IFG. В данной области известны способы определения эффективных доз для терапевтических и профилактических целей для описанных фармацевтических композиций или описанных комбинаций лекарственных препаратов, независимо от того, включены они или нет в состав одной композиции. Для терапевтических целей совместно эффективное количество, в том смысле, в котором этот термин здесь используется, означает такое количество каждого активного соединения или фармацевтического средства,одного или в комбинации, которое вызывает биологическую или лечебную ответную реакцию в системе ткани, у животного или человека, которую добивается реализовать исследователь, ветеринарный врач,врач-медик или другой клиницист, которая включает ослабление симптомов заболевания или нарушения, которое подвергается лечению. Для профилактических целей (т.е. подавления начала развития или прогрессирования нарушения) термин совместно эффективное количество относится к такому количеству каждого активного соединения или фармацевтического средства, одного или в комбинации, которое подавляет у субъекта начало развития или прогрессирования нарушения, которое добивается реализовать исследователь, ветеринарный врач, врач-медик или другой клиницист, где подавление данного нарушения опосредуется модуляцией активности реабсорбции глюкозы или активности другого противодиабетического средства или обоих. Таким образом, настоящее изобретение обеспечивает комбинации двух или более лекарственных препаратов, когда, например, а) каждый препарат вводят в независимо терапевтически или профилактически эффективном количестве; b) по меньшей мере один лекарственный препарат в комбинации вводят в количестве, которое является субтерапевтическим или субпрофилактическим, если оно вводится одно,но становится терапевтическим или профилактическим, когда его вводят в комбинации со вторым или дополнительными препаратами по изобретению; или с) оба препарата вводят в количестве, которое является субтерапевтическим или субпрофилактическим, если вводится одно, но становится терапевтическим или профилактическим, когда вводят вместе. Термин защитные группы относится к таким группам, известным в данной области, которые используются для маскирования функциональных групп; защитные группы можно удалить во время последующих синтетических превращений или в результате метаболизма, или в других условиях in vivo при введении. Во время любого из способов получения соединений по настоящему изобретению может быть необходимым и/или желательным защитить лабильные или реакционноспособные группы в любой из имеющих отношение к изобретению молекул. Этого можно достичь с помощью обычных защитных групп, таких как описаны в Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973 и T.W. GreeneP.G.M. Wuts, Protective Groups in Organic Synthesis, Third Edition, John WileySons,1999. Защитные группы можно удалить на подходящей последующей стадии с использованием способов,известных в данной области. Ниже приводятся примеры гидроксил- и диолзащитных групп. Защитные группы для гидроксильных групп включают метиловые эфиры, замещенные метиловые эфиры, замещенные этиловые эфиры, замещенные бензиловые эфиры и силиловые эфиры. Замещенные метиловые эфиры Примеры замещенных метиловых эфиров включают метоксиметил, метилтиометил,трет-бутилтиометил, (фенилдиметилсилил)метоксиметил, бензилоксиметил, п-метоксибензилоксиметил,(4-метоксифенокси)метил,трет-бутоксиметил,4-пентенилоксиметил,силоксиметил,2-метоксиэтоксиметил,2,2,2-трихлорэтоксиметил,бис-(2-хлорэтокси)метил,2-(триметилсилил)этоксиметил, тетрагидропиранил, 3-бромтетрагидропиранил, тетрагидротиопиранил, 1-метоксициклогексил,4-метокситетрагидропиранил,4-метокситетрагидротиопиранил,4-метокситетрагидротиопиранил S,S-диоксидо, 1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-ил, 1,4-диоксан-2-ил,тетрагидрофуранил, тетрагидротиофуранил и 2,3,3 а,4,5,6,7,7 а-октагидро-7,8,8-триметил-4,7-метанобензофуран-2-ил. Замещенные этиловые эфиры Примеры замещенных этиловых эфиров включают 1-этоксиэтил, 1-(2-хлорэтокси)этил, 1-метил-1 метоксиэтил,1-метил-1-бензилоксиэтил,1-метил-1-бензилокси-2-фторэтил,2,2,2-трихлорэтил,2-триметилсилилэтил, 2-(фенилселенил)этил, трет-бутил, аллил, п-хлорфенил, п-метоксифенил,-5 009768 2,4-динитрофенил, бензил и полиэтиленгликолевые эфиры. Замещенные бензиловые эфиры Примеры замещенных бензиловых эфиров включают п-метоксибензил, 3,4-диметоксибензил,о-нитробензил, п-нитробензил, п-галогенбензил, 2,6-дихлорбензил, п-цианобензил, п-фенилбензил, 2- и 4-пиколил, 3-метил-2-пиколил N-оксидо, дифенилметил, п,п'-динитробензгидрил, 5-дибензосуберил,трифенилметил,-нафтилдифенилметил,п-метоксифенилдифенилметил,ди(п-метоксифенил)фенилметил, три(п-метоксифенил)метил, 4-(4'-бромфенацилокси)фенилдифенилметил, 4,4',4"-трис-(4,5 дихлорфталимидофенил)метил, 4,4',4"-трис-(левулиноилоксифенил)метил, 4,4',4"-трис-(бензоилоксифенил)метил, 3-(имидазол-1-илметил)-бис-(4,4"-диметоксифенил)метил, 1,1-бис-(4-метоксифенил)-1'пиренилметил, 9-антрил, 9-(9-фенил)ксантенил, 9-(9-фенил-10-оксо)антрил, 1,3-бензодитиолан-2-ил и бензизотиазолил S,S-диоксидо. Силиловые эфиры Примеры силиловых эфиров включают триметилсилил, триэтилсилил, триизопропилсилил,диметилизопропилсилил, диэтилизопропилсилил, диметилгексилсилил, трет-бутилдиметилсилил,трет-бутилдифенилсилил, трибензилсилил, три-п-ксилилсилил, трифенилсилил, дифенилметилсилил и трет-бутилметоксифенилсилил. Сложные эфиры Помимо простых эфиров гидроксильную группу можно защитить в виде сложного эфира. Примеры сложных эфиров включают формиат, бензоилформиат, ацетат, хлорацетат, дихлорацетат, трихлорацетат,трифторацетат, метоксиацетат, трифенилметоксиацетат, феноксиацетат, п-хлорфеноксиацетат,п-Р-фенилацетат, 3-фенилпропионат, 4-оксопентаноат(левулинат), 4,4-(этилендитио)пентаноат, пивалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, п-фенилбензоат, 2,4,6-триметилбензоат(мезитоат) и полиэтиленгликолевые эфиры. Карбонаты Примеры карбонатов включают метил, 9-флуоренилметил, этил, 2,2,2-трихлорэтил,2-(триметилсилил)этил, 2-(фенилсульфонил)этил, 2-(трифенилфосфонио)этил, изобутил, винил, аллил,п-нитрофенил, бензил, п-метоксибензил, 3,4-диметоксибензил, о-нитробензил, п-нитробензил,S-бензилтиокарбонат, 4-этокси-1-нафтил, метилдитиокарбонат и полиэтиленгликолькарбонаты. Вспомогательные вещества для отщепления Примеры веществ для вспомогательного отщепления включают 2-иодбензоат, 4-азидобутират,4-нитро-4-метилпентаноат, о-(дибромметил)бензоат, 2-формилбензолсульфонат, 2-(метилтиометокси)этилкарбонат, 4-(метилтиометокси)бутират и 2-(метилтиометоксиметил)бензоат. Различные сложные эфиры Примеры различных сложных эфиров включают 2,6-дихлор-4-метилфеноксиацетат, 2,6-дихлор-4(1,1,3,3-тетраметилбутил)феноксиацетат, 2,4-бис-(1,1-диметилпропил)феноксиацетат, хлордифенилацетат, изобутират, моносукциноат, (Е)-2-метил-2-бутеноат(тиглоат), о-(метоксикарбонил)бензоат,р-Р-бензоат, -нафтоат, нитрат, алкил N,N,N',N'-тетраметилфосфородиамидат, N-фенилкарбамат, борат,диметилфосфинотиоил и 2,4-динитрофенилсульфенат. Сульфонаты Примеры сульфонатов включают сульфат, метансульфонат(мезилат), бензилсульфонат и тозилат. Защита для 1,2- и 1,3-диолов Циклические ацетали и кетали Примеры циклических ацеталей и кеталей включают метилен, этилиден, 1-трет-бутилэтилиден,1-фенилэтилиден, (4-метоксифенил)этилиден, 2,2,2-трихлорэтилиден, ацетонид (изопропилиден),циклопентилиден,циклогексилиден,циклогептилиден,бензилиден,п-метоксибензилиден,2,4-диметоксибензилиден, 3,4-диметоксибензилиден и 2-нитробензилиден. Циклические ортоэфиры Примеры циклических ортоэфиров включают метоксиметилен, этоксиметилен, диметоксиметилен,1-метоксиэтилиден, 1-этоксиэтилиден, 1,2-диметоксиэтилиден, -метоксибензилиден, производное 1-(N,N-диметиламино)этилидена, производное -(N,N-диметиламино)бензилидена и 2-оксациклопентилиден. Силильные производные Примеры силильных производных включают ди-трет-бутилсилилен и производное 1,3-(1,1,3,3 тетраизопропилдисилоксанилидена). Ингибиторы реабсорбции глюкозы Одним способом лечения гипергликемии является выделение избыточного количества глюкозы непосредственно в мочу таким образом, чтобы в результате нормализовалась концентрация глюкозы в крови. Например, совместные переносчики натрия-глюкозы (SGLT), в основном обнаруженные в мембране щеточной каемки кишечника и почек, представляют семейство белков, принимающих активное участие в нормальном процессе всасывания глюкозы. Среди них SGLT1 находится в эпителиальных клетках кишечника и почек (Lee et al., 1994), в то время как SGLT2 обнаружен в эпителии почек (You et al., 1995,-6 009768MacKenzie et al., 1994). Всасывание глюкозы в кишечнике в основном опосредуется SGLT1, переносчиком с высокой аффинностью, низкой производительностью, с соотношением транспорта Na+:глюкоза,равным 2:1. SGLT2, также известный как SAAT1, переносит Na+ и глюкозу в соотношении 1:1 и функционирует как переносчик с низкой аффинностью и высокой производительностью. Характеристика данных SGLT представлена в табл. 1. Таблица 1 Ренальная (почечная) реабсорбция глюкозы опосредуется SGLT1 и SGLT2 (Silverman et al., 1992;Deetjen et al., 1995). Глюкоза плазмы крови фильтруется в почечных клубочках и реабсорбируется через эпителий в проксимальных канальцах. SGLT1 и SGLT2 располагаются в апикальных плазматических мембранах эпителия и получают энергию от внутреннего натриевого градиента, создаваемогоNa+/K+-АТФ-азными насосами, расположенными в базолатеральной мембране. После реабсорбции повышенные концентрации цитозольной глюкозы переносятся в интерстициальное пространство с помощью соответствующих переносчиков глюкозы (GLUT1 и GLUT2). Следовательно, ингибирование SGLT приводит к снижению уровня глюкозы в плазме крови посредством подавления реабсорбции глюкозы в почке. Терапевтически или профилактически эффективное количество ингибитора SGLT, которое является достаточным для увеличения выделения глюкозы с мочой или снижения уровня глюкозы в плазме крови у субъекта с помощью желаемого количества в сутки, можно легко определить с использованием общепринятых в данной области методов. Недавно было установлено, что флоризин, природный гликозид, находящийся в коре и стеблях Rosaceae (например, яблонь, груш и т.д.) ингибирует совместные переносчики Na+-глюкозы, расположенные в мембране щеточной каемки кишечника и почек. Ингибируя активность совместного переносчика Na+-глюкозы, флоризин подавляет реабсорбцию глюкозы в почечных канальцах и способствует выделению глюкозы так, что уровень глюкозы в плазме крови поддерживается на нормальном уровне в течение длительного периода времени при подкожном ежедневном введении (Journal of Clinical Investigation, 1987, vol. 79, p. 1510). Другие ингибиторы SGLT включают алкил- и фенилглюкозиды, 1-(5-изохинолинсульфонил)-2 метилпиперазин-HCl (непосредственно через протеинкиназу C), п-хлормеркурибензоат (PCMB),N,N'-дициклогексилкарбодиимид (DCCD), ионы меди и кадмия, и трехвалентные лантаниды. в которой одна из пунктирных линий находится между NR1 и X или между X и Y либо или обе отсутствуют; два из V, М и W представляют Н и третий являетсяR1 представляет Н или C1-4 алкил или R1 отсутствует, когда имеется пунктирная линия между NR1 и X;Z является замещенным или незамещенным и выбран из C3-7 циклоалкила, фенила, 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, независимо выбранных из N, О и S, биарила,9- или 10-членного конденсированного бициклила (такого как нафтил) и конденсированного гетеробициклила, где указанный конденсированный гетеробициклил содержит от 1 до 4 гетероатомов (и предпочтительно 1-3 или 1-2 гетероатома), независимо выбранных из N, О и S; Р=Н, C1-7 ацил или (C1-6 алкокси)карбонил; или их фармацевтически приемлемой соли. Примеры предпочтительных соединений формулы (VI) включают:(b) Z независимо замещен 1-3 заместителями, независимо выбранными из C1-4 алкокси, фенокси,C1-4 алкила, C3-6 циклоалкила, атома галогена, гидрокси, циано, амино, C1-4 алкилтио, C1-4 алкилсульфонила,C1-4 алкилсульфинила, C1-4 аминоалкила, моно- и диC1-4 алкиламино, фенила, C1-4 алкиламиносульфонила(SO2NHR), амино(C1-4 алкилсульфонила) (NHSO2R), диC1-4 алкиламиносульфинила (SONHRR),C1-4 алкиламидо (NHCOR), C1-4 алкилкарбамидо (CONHR), 5-6-членного гетероциклила, содержащего 1-3 гетероатома, независимо выбранных из N, S и О; и где заместитель(и) в Z могут быть дополнительно независимо замещены 1-3 заместителями, независимо выбранными из C1-4 алкокси, C1-4 алкила, атома галогена, гидрокси, циано, амино, моно- и диC1-4 алкиламино и C1-4 алкилтио;(с) Z представляет 4-замещенный фенил, 3,4-дизамещенный фенил, бензгидрил, замещенный или незамещенный тиенил, биарил, бензофуранил, дигидробензофуранил, 4-замещенный пиридил,бензо[b]тиенил, хроманил, бензотиофенил, инданил, нафтил и 2,3-дигидробензо[1,4]диоксан;(d) ограничения по п.(с), где Z является незамещенным или замещенным 1-2 заместителями, независимо выбранными из метокси, этокси, атома фтора, атома хлора, метила, этила, пропила, бутила и изопропила;(i) Z представляет бифенил, 4-(3-пиридил)фенил, 4-(2-тиенил)фенил, 4-(1 Н-имидазол-1-ил)фенил,4-(1 Н-пиразол-1-ил)фенил, (4-этил)фенил, (4-пропил)фенил, (4-метокси)фенил, дигидробензофуран-5-ил или дигидробензофуран-6-ил и Z является незамещенным или замещенным 1-2 заместителями, независимо выбранными из метокси, этокси, атома фтора, атома хлора, метила, этила, пропила, бутила и изопропила;(р) сочетания вышеуказанного. Предпочтительные примеры соединений по изобретению включают 3-(4-этилбензил)-5-(-D-глюкопиранозил)-1 Н-индол; 5-(-D-глюкопиранозил)-3-(4-метоксибензил)-1 Н-индол; 5-(-D-глюкопиранозил)-3-[2-(4-метоксифенил)этил]-1 Н-индол и 3-(4-этилбензил)-4-(-D-глюкопиранозил)-1H-индол. Дополнительные предпочтительные соединения включают соединения, выбранные из 2-(4-этилбензил)-4-(-D-глюкопиранозил)-1 Н-индола; 3-[2-(2,3-дигидробензофуран-5-ил)этил]-5-(-D-глюкопиранозил)-1 Н-индола; 5-(-D-глюкопиранозил)-3-(5-этил-2-тиенил)-1 Н-индола; 3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензимидазола; 3-(4-этилбензил)-4-(-D-глюкопиранозил)-1,3-дигидробензимидазол-2-она и 3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензотриазола. Наиболее предпочтительные соединения выбраны из 3-(4-этилбензил)-5-(-D-глюкопиранозил)-1 Н-индола; 2-(4-этилбензил)-4-(-D-глюкопиранозил)-1 Н-индола; 5-(-D-глюкопиранозил)-3-(5-метил-2-тиенил)-1 Н-индола; 3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензимидазола и 3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензотриазола.C. Способы синтеза. Один аспект изобретения относится к соединениям формулы (IV). Данные соединения можно получить традиционными способами органического синтеза или способами комбинаторного или матричного синтеза. На последующих схемах и в химических примерах 1-4 приводятся общие указания. Схема реакций 1 Соединения по данному изобретению, в которых X представляет C-H, Y является C-Q-Z (например,3-алкилиндол), можно получить, как представлено на схеме реакций 1. Соединения формулы 1, в которых R3 представляет Н и P1 является N,N-диэтилкарбамилом, можно получить обработкой натриевой соли промышленно доступного 5-бром-1 Н-индол-3-карбоксальдегида N,N-диэтилкарбамилхлоридом в безводном ТГФ. Защищенный индол можно обработать илидами в обычных условиях реакции Виттига с получением E/Z смеси соединений. Гидрирование алкена на оксиде платины (IV) (катализатор Адамса) в хлорсодержащем растворителе под давлением 1 атм. дает соединения формулы 2, в которой n равно 2. Соединение формулы 1 также можно обработать бромидом арилмагния в ТГФ с получением индолкар-9 009768 бинола. Сырой индолкарбинол можно восстановить триэтилсиланом и хлоридом олова в дихлорметане при температуре -78C с получением соединений формулы 2, в которой n равно 1. С азота индола соединений формулы 2, в которой n равно 1 или 2, можно снять защиту обработкой водным раствором основания, такого как гидроксид натрия, в кипящем этаноле для удаления N,N-диэтилкарбамильной группы с последующей повторной защитой с помощью трет-бутилдиметилсилильной (TBDMS) группы (Р 2) обработкой трет-бутилдиметилсилилхлоридом с использованием известных методик с получением производного формулы 5 5-броминдола. Альтернативно соединение формулы 5, в которой n равно 1 (производные 4-броминдола, или производные 5-броминдола, или 6-броминдола), можно получить в три стадии из промышленно доступных соединений формулы 3. Ацилирование Фриделя-Крафтса соединений формулы 3 замещенными бензоилхлоридами с использованием кислоты Льюиса, такой как трихлорид алюминия, в хлорсодержащем растворителе, таком как дихлорметан, с последующим восстановлением карбонильной группы боргидридом натрия дает соединения формулы 4. Азот индола соединения формулы 4 можно защитить группойTBDMS, как описано выше, с получением соединений формулы 5, в которой n равно 1. Соединения формулы 5 активируют для проведения сочетания обработкой t-BuLi при температуре-78C в растворителе, таком как ТГФ, перед добавлением 2,3,4,6-тетра-O-бензилD-глюколактона, как описано Czernecki and Ville [J. Org. Chem. 1989, 53, 610-612]. Полученный лактол можно обработать силанами, такими как триэтилсилан, в растворителе, таком как дихлорметан, при температуре -30C с получением соединений формулы 6. Группу TBDMS можно удалить водным раствором основания, такого как гидроксид натрия, в кипящем ТГФ с получением соединений формулы 7. Гидрогенолиз глюкопиранозы 7 на гидроокиси палладия (катализатор Перлмана) под давлением 1 атм. может обеспечить соединения формулы 8, в которой P представляет H. Натриевую соль соединения 7 можно обработать алкилгалогенидом с получениемN-алкилированного (R1) продукта 9, который подвергают гидрогенолизу, как описано выше, с получением соединения формулы 10, в которой Р представляет Н. Дальнейшая обработка соединений формулы 8 или 10, в которых P представляет H, одним эквивалентом алкилхлорформиата или алканоилхлорида в коллидине для селективного ацилирования 6-OH-группы глюкопиранозы может обеспечить соединения формулы 8 или 10, в которых P представляет ацил или алкоксикарбонил. Схема реакций 2- 10009768 Соединения по данному изобретению, в которых Y представляет N-Q-Z, X представляет N, C=O или C-H и R1 имеет значения, определенные выше, можно получить, как представлено на схеме реакций 2, с использованием методик, известных в данной области для описанных синтетических превращений. Промышленно доступный N-(2-бром-6-нитрофенил)ацетамид можно нагреть в кислых условиях для удаления ацетильной группы, затем алкилировать с использованием замещенных бензил-, арил- или гетероарилалкилгалогенидов, ацилировать бензоил- или фенилацетилхлоридами с последующим восстановлением LAH или бораном или подвергнуть восстановительному аминированию с помощью замещенных бензальдегидов в присутствии цианоборогидрида натрия с получением соединений формулы 9. Затем нитрогруппу можно восстановить с использованием реагентов, таких как хлорид олова (II) или железо в уксусной кислоте с получением соединений формулы 11, в которых бром находится в положении V по п.1. Альтернативно можно начинать с промышленно доступного 4-бром-2-нитроанилина, ввести содержащую Z боковую цепь, как описано выше, с получением соединений формулы 10, в которой R' представляет -(CH2)nZ, затем восстановить нитрогруппу с получением соединений 11, в которых бром находится в положении М по п.1. С другой стороны, азот анилина в промышленно доступном 4-бром-2-нитроанилине можно ацетилировать или альтернативно защитить соответствующей защитной группой, такой как толуолсульфонил или бензолсульфонил, с получением соединений формулы 10, в которой R' представляет защитную группу. Затем нитрогруппу можно восстановить до первичного амина с помощью хлорида олова (II) и затем алкилировать обработкой замещенными бензил-, арил- или гетероарилалкилгалогенидами в щелочных условиях или подвергнуть восстановительному аминированию замещенными бензальдегидами в присутствии цианоборогидрида натрия. Альтернативно первичный амин можно ацилировать бензоилили фенилацетилхлоридами с последующим восстановлением LAH или бораном. Конечное удаление азотзащитной группы с использованием методик, известных в данной области, может обеспечить соединения формулы 11, в которой бром находится в положении W по п.1. Соединения формулы 11 можно подвергнуть дальнейшему взаимодействию с получением соединений формулы 12, 13 и 14. Данные превращения можно провести обработкой диамина 1,1'-тиокарбонилдиимидазолом или сероуглеродом с получением соединения формулы 12 или трифосгеном, мочевиной или карбонилдиимидазолом с получением соединений формулы 13. Альтернативно диамин 11 можно обработать нитратом натрия в кислых условиях при охлаждении с получением соединений формулы 14. Метилирование соединений 12 йодметаном в присутствии основания может дать соединения формулы 16. Соединения формулы 13 можно обработать основанием, таким как гидрид натрия, и алкилировать алкилгалогенидами с получением соединений формулы 17, в которой R1 представляет алкил. Незамещенный азот в соединении формулы 13 можно также защитить алкоксикарбонильной группой, как описано Meanwell et al. [J. Org. Chem. 1995, 60, 1565-1582], с получением соединений формулы 17, в которой R1 представляет этоксикарбонил или трет-бутоксикарбонил. Получение C-гликозидов можно провести обработкой соединений формулы 14, 16 или 17 (соединение 15 пропускается) бутиллитием при температуре -78C перед добавлением 2,3,4,6-тетра-O-бензил-D-глюколактона с последующим восстановлением полученного полуацеталя в присутствии избытка триэтилсилана и диэтилэферата трифторида бора в подходящем растворителе, таком как дихлорметан, как описано Czernecki and Ville (J. Org. Chem. 1989, 54, 610-612). Соединения формулы 18, в которой R1 представляет Н, можно получить удалением защитных групп в щелочных условиях (для этоксикарбонильной группы) или в кислых условиях (для трет-бутоксикарбонильной группы) с последующим дебензилированием гидроксильных групп с использованием палладиевых катализаторов в условиях гидрирования. Соединения формулы 18, в которой R1 представляет алкильную группу, или формулы 19 можно получить дебензилированием гидроксильных групп с использованием палладиевых катализаторов в условиях гидрирования. Соединения формулы 20, в которой R3 представляет H, можно получить опосредуемым никелем Ренея отщеплением 2-метилтиогруппы, как описано Townsend et al. (J. Med. Chem. 1994, 37, 2942-2949) с последующим дебензилированием гидроксильных групп с использованием палладиевых катализаторов в условиях гидрирования. Дальнейшая обработка одним эквивалентом алкилхлорформиата или алканоилхлорида в коллидине для селективного ацилирования 6-ОН группы глюкопиранозы может обеспечить соединения формулы 21, в которой Р представляет ацил или алкоксикарбонил. Соединения по данному изобретению, в которых X представляет C-Q-Z, и Y является CH (например, 2-алкилиндол), как определено выше, можно получить, как представлено на схеме реакций 3. Соединения формулы 22 можно получить обработкой натриевой соли промышленно доступных броминдолов (4-броминдола, или 5-броминдола, или 6-броминдола) алкилгалогенидами в безводном ТГФ. Полученный N-алкилиндол можно подвергнуть перегруппировке в 2-алкилиндол при температуре 180C в полифосфорной кислоте под действием микроволн с последующей защитой индольного азота TBDMSгруппой (Р 2) с получением соединений формулы 23. Получение C-гликозидов можно провести обработкой соединений формулы 23 бутиллитием при температуре -78C перед добавлением 2,3,4,6-тетра-O-бензилD-глюколактона, как представлено на схеме реакций 1. Полученный лактол можно обработать силанами, такими как триэтилсилан, в растворителе, таком как дихлорметан, при температуре -30C с последующим снятием защиты TBDMS-группой водным раствором основания, таким как гидроксид натрия, в кипящем ТГФ с получением соединений 24. Гидрогенолиз глюкопиранозы 24 на гидроокиси палладия (катализатор Перлмана) под давлением 1 атм. может дать соединения формулы 25, в которой Р представляет Н. Натриевую соль соединения 24 можно обработать алкилгалогенидом с получением N-алкилированного (R1) продукта 26 с последующим проведением гидрогенолиза, как описано ранее, с получением соединения формулы 27, в которой Р представляет Н.D. Дополнительные противодиабетические средства. Противодиабетические средства, которые можно использовать по изобретению, в качестве второго,третьего или последующего противодиабетического средства, в композиции, формуляции или комбинированном способе лечения (схеме введения) включают, но не ограничиваются группами и соединениями,представленными в качестве примеров, в табл. 2. Таблица 2 Препараты для комбинированной терапии с ингибиторами SGLT Е. Комбинации. Изобретение относится к комбинированной терапии, включающей введение ингибитора реабсорбции глюкозы, такого как ингибитор SGLT, и одного или более противодиабетических средств для лечения диабета или синдрома X, или связанных с ними симптомов или осложнений. Продемонстрированная эффективность ингибиторов SGLT на многочисленных моделях NIDDM подтверждает применимость одного данного лекарственного препарата для лечения NIDDM у людей. Поскольку ингибиторы реабсорбции глюкозы имеют механизм действия, отличный от такового у других противодиабетических средств, таких как модуляторы RXR, то описанная здесь комбинация может обладать преимуществом снижать количество каждого препарата, необходимое для достижения комбинированного терапевтического или фармацевтического действия, по сравнению с применением одного препарата, тем самым снижая один или более побочных эффектов, которые часто включают увеличение массы тела, отеки, гипертрофию сердца, гипертрофию печени, гипогликемию или гепатотоксичность либо сочетания указанного. Изобретение обеспечивает способ лечения диабета или синдрома X, или их осложнений у субъекта,где указанный способ включает введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы в комбинации с совместно эффективным количеством противодиабетического средства, такого как модулятор RXR. В одном аспекте изобретения противодиабетическое средство представляет агонист RXR или антагонист RXR, который повышает чувствительность к инсулину у субъекта. Например, сенсибилизатор инсулина может повысить толерантность к глюкозе у субъекта в- 17009768 пероральном тесте определения толерантности к глюкозе. Предпочтительно диабет или синдром X либо связанные с ними симптомы или осложнения выбраны из IDDM, NIDDM, IGT и IFG. Данное изобретение также обеспечивает фармацевтическую композицию, содержащую один или более ингибиторов реабсорбции глюкозы (один или в комбинации с одним или более противодиабетическими средствами) и фармацевтически приемлемый носитель. В одном аспекте изобретения противодиабетическое средство представляет агонист RXR или антагонист RXR, который повышает чувствительность к инсулину у субъекта. В частности, ингибитор реабсорбции глюкозы представляет ингибитор SGLT1 и/или SGLT2. Для применения в медицине соль или соли соединений формулы (IV) относятся к нетоксичной,фармацевтически приемлемой соли или солям. Однако другие соли могут быть пригодными в получении соединений по данному изобретению или их фармацевтически приемлемых солей. Репрезентативные органические или неорганические кислоты включают, но не ограничиваются этим, хлористоводородную, бромисто-водородную, йодисто-водородную, перхлорную, серную, азотную, фосфорную,уксусную, пропионовую, гликолевую, молочную, янтарную, малеиновую, фумаровую, яблочную, винную, лимонную, бензойную, миндальную, метансульфоновую, гидроксиэтансульфоновую, бензолсульфоновую, щавелевую, памовую, 2-нафталинсульфоновую, п-толуолсульфоновую, циклогексансульфаминовую, салициловую, сахариновую или трифторуксусную кислоту. Показательные основные/катионные соли включают, но не ограничиваются этим, бензатин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумин, прокаин, алюминий, кальций, литий, магний, калий, натрий или цинк. Соединения формулы (IV) или их фармацевтически приемлемые соли могут включать их внутримолекулярную соль, или их сольват, или гидрат.F. Введение, формуляция и дозировки. Возможность использования описанных соединений, композиций и комбинаций для лечения нарушений в обмене глюкозы и липидов можно определить методиками, хорошо известными в данной области (см. источники, представленные ниже), а также методами, описанными в патентах США 5424406, 5731292, 5767094, 5830873, 6048842, WO 01/16122 и WO 01/16123, которые включены в данное описание для сведения. Соединение можно вводить пациенту любым обычным путем введения,включая, но не ограничиваясь, внутривенное, пероральное, подкожное, внутримышечное, внутрикожное и парентеральное введение. Предпочтительно композиции предназначены для перорального введения. Настоящее изобретение также относится к фармацевтическим композициям, содержащим один или более ингибиторов реабсорбции глюкозы и один или более модуляторов RXR в комбинации с фармацевтически приемлемым носителем. Суточная доза продуктов может варьировать в широком пределе от 1 до 1000 мг для взрослого человека в сутки. Для перорального введения композиции предпочтительно обеспечены в виде таблеток,содержащих 0,01, 0,05, 0,1, 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100, 150, 200, 250 или 500 мг активного ингредиента для симптоматической корректировки дозы для пациента, который подвергается лечению. Соединения можно вводить 1 или 2 раза в сутки. Однако дозы могут варьировать в зависимости от потребностей пациентов, тяжести состояния, которое подвергается лечению, и используемого соединения. Можно использовать ежедневное введение или периодическое введение. Предпочтительно данные композиции находятся в разовых лекарственных формах, таких как таблетки, пилюли, капсулы, порошки,гранулы, стерильные парентеральные растворы или суспензии, дозированные аэрозольные или жидкие спреи, капли, ампулы, аутоинъекторы или суппозитории; для перорального, парентерального, интраназального, сублингвального или ректального введения, или для введения ингаляцией или инсуффляцией. Альтернативно композиция может находиться в форме, подходящей для введения один раз в неделю или один раз в месяц; например, нерастворимую соль активного соединения, такую как деканоат, можно адаптировать для получения препарата-депо для внутримышечной инъекции. Для получения твердых композиций, таких как таблетки, основной активный ингредиент или ингредиенты смешивают с фармацевтическим носителем, например обычными ингредиентами, используемыми для таблетирования, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния,дикальций фосфат или камеди, и другими фармацевтическими разбавителями, например водой, для получения предшествующей твердой композиции, содержащей гомогенную смесь одного или более ингибиторов реабсорбции глюкозы и одно или более противодиабетических средств, или их фармацевтически приемлемую соль. При ссылке на предшествующие композиции в качестве гомогенных понимается, что активный ингредиент или ингредиенты равномерно распределены в композиции так, что композицию можно легко разделить на равноценно эффективные лекарственные формы, такие как таблетки, пилюли и капсулы. Затем данную предшествующую твердую композицию разделяют на разовые лекарственные формы типа, описанного выше, содержащие от 0,1 до примерно 500 мг активного ингредиента или ингредиентов по настоящему изобретению. Таблетки или пилюли новой композиции можно покрыть оболочкой или формулировать иначе для получения лекарственной формы, предоставляющей преимущество пролонгированного действия. Например, таблетка или пилюля может включать компонент внутренней дозы и внешней дозы, где последний находится в виде оболочки над первым. Два компонента можно- 18009768 разделить кишечным слоем, который служит для предупреждения распада в желудке и позволяет внутреннему компоненту пройти интактным в двенадцатиперстную кишку или замедленно высвобождаться. Можно использовать различные вещества для кишечных слоев или оболочек, такие вещества включают ряд полимерных кислот с такими веществами, как шеллак, цетиловый спирт и ацетат целлюлозы. Жидкие формы, в которые можно включать новые композиции по настоящему изобретению для перорального или инъекционного введения, включают водные растворы, сиропы, которым придан вкус и запах, водные или масляные суспензии и эмульсии, которым придан вкус и запах, с пищевыми маслами,такими как масло из семян хлопчатника, кунжутное масло, кокосовое масло или арахисовое масло, а также эликсиры и подобные фармацевтические носители. Подходящие диспергирующие или суспендирующие вещества для водных суспензий включают синтетические и природные камеди, такие как трагакант, аравийская камедь, альгинат, декстран, натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза,поливинилпирролидон или желатин. Жидкие формы помимо соответствующих ароматизирующих суспендирующих или диспергирующих веществ также могут включать синтетические и природные камеди,например трагакант, аравийскую камедь, метилцеллюлозу и т.п. Для парентерального введения желательными являются стерильные суспензии и растворы. Изотонические препараты, которые обычно содержат подходящие консерванты, применяются, когда желательным является внутривенное введение. Преимущественно комбинации одного или более ингибиторов реабсорбции глюкозы по настоящему изобретению, одни или в сочетании с одним или более дополнительными противодиабетическими средствами, можно вводить в разовой суточной дозе, или общую суточную дозу можно вводить дозами,разделенными на два, три или четыре раза в день. Кроме того, один или более ингибиторов реабсорбции глюкозы и/или одно или более противодиабетических средств по настоящему изобретению можно вводить в интраназальной форме посредством местного применения подходящих интраназальных носителей или с помощью трансдермальных накожных пластырей, хорошо известных специалистам в данной области. При введении в форме системы для трансдермального введения введение дозы, конечно, будет в большей степени непрерывным, а не прерывающимся во время схемы введения. Например, для перорального введения в форме таблетки или капсулы активный лекарственный компонент можно объединить с нетоксичным, фармацевтически приемлемым инертным носителем для перорального введения, таким как этанол, глицерин, вода и т.п. Кроме того, когда это желательно или необходимо, то в смесь можно также включить подходящие связующие вещества, смазывающие вещества, разрыхлители и красители. Подходящие связующие вещества включают, без ограничения, крахмал,желатин, природные сахара, такие как глюкоза или бета-лактоза, кукурузные подсластители, природные и синтетические камеди, такие как аравийская камедь, трагакант или олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п. Разрыхлители включают, без ограничения, крахмал, метилцеллюлозу, агар, бентонит, ксантановую камедь и т.п. Когда настоящее изобретение относится к введению комбинации, то соединения можно вводить одновременно, последовательно или в одной фармацевтической композиции. В тех случаях, когда соединения вводят раздельно, то количество доз каждого соединения, вводимого в сутки, необязательно может быть одинаковым, например, когда одно соединение может обладать большей продолжительностью действия, то, следовательно, его нужно вводить менее часто. Оптимальные дозы для введения могут легко определить специалисты в данной области, и они будут варьировать в зависимости от используемого конкретного соединения, активности препарата, способа введения и тяжести болезненного состояния. Кроме того, факторы, связанные с конкретным пациентом, который подвергается лечению, включая возраст, массу, рацион и время введения, будут приводить к необходимости в корректировке дозы. Новые композиции по настоящему изобретению можно также вводить в форме липосомальных систем для доставки, таких как небольшие униламеллярные везикулы, крупные униламеллярные везикулы и мультиламеллярные везикулы. Липосомы можно получить из различных липидов, включая, но не ограничиваясь этим, амфифильные липиды, такие как фосфатидилхолины, сфингомиелины, фосфатидилэтаноламины, кардиолипины, фосфатидилсерины, фосфатидилглицерины, фосфатидные кислоты, фосфатидилинозиты, диацилтриметиламмоний пропаны, диацилдиметиламмоний пропаны и стеариламин,нейтральные липиды, такие как триглицериды и их комбинации. Они могут содержать холестерин или холестерин может отсутствовать. Из формулы (IV) и других раскрытых формул становится очевидным, что некоторые соединения в композициях по изобретению могут содержать один или более асимметричных атомов углерода в их структуре. Предполагается, что настоящее изобретение включает в своем объеме стереохимически чистые изомерные формы соединений, а также их рацематы. Стереохимически чистые изомерные формы могут быть получены применением известных в данной области принципов. Диастереоизомеры можно разделить методами физического разделения, такими как фракционированная кристаллизация и хроматографические методы, и энантиомеры можно отделить друг от друга селективной кристаллизацией диастереоизомерных солей с оптически активными кислотами или основаниями или хиральной хроматографией. Чистые стереоизомеры можно также получить синтетически из соответствующих стереохимически чистых исходных веществ или с использованием стереоспецифиче- 19009768 ских реакций. Некоторые соединения в композициях по настоящему изобретению могут иметь различные индивидуальные изомеры, такие как транс- и цис-, и различные альфа- и бета-присоединения (ниже и выше плоскости рисунка). Кроме того, когда способы получения соединений по изобретению дают смесь стереоизомеров, то данные изомеры можно разделить обычными методами, такими как препаративная хроматография. Соединения можно получить в виде одного стереоизомера или в рацемической форме в виде смеси некоторых возможных стереоизомеров. Нерацемические формы можно получить синтезом или разделением. Например, соединения можно разделить на их энантиомеры-компоненты стандартными методами, такими как получение диастереоизомерных пар образованием солей. Соединения можно также разделить ковалентным связыванием с хиральным вспомогательным веществом с последующим хроматографическим разделением, и/или кристаллографическим разделением, и удалением хирального вспомогательного вещества. Альтернативно соединения можно разделить с использованием хиральной хроматографии. Если не указано иначе, то предполагается, что в объем настоящего изобретения входят все такие изомеры или стереоизомеры сами по себе, а также смеси цис- и транс-изомеров, смеси диастереоизомеров и рацемические смеси энантиомеров (оптических изомеров). Терапевтическое действие ингибитора реабсорбции глюкозы, вводимого в комбинации с одним или более противодиабетическими средствами в лечении диабета, синдрома X или связанных с ними симптомов или осложнений, можно продемонстрировать методами, известными в данной области. Последующие примеры комбинированного лечения ингибиторами SGLT и другими противодиабетическими средствами, такими как модуляторы RXR, предназначены для иллюстрации изобретения, но без его ограничения.G. Синтетические химические примеры. Один аспект изобретения относится к соединениям формулы (IV), как описано выше в разделе Сущность изобретения, описании и прилагаемой формуле изобретения. Данные раскрытые соединения можно получить традиционными методами органического синтеза или методами матричного или комбинаторного синтеза. На схемах и в примерах 1-9 ниже приводятся общие указания, и в детальных примерах, как можно получить раскрытые соединения. 1 Н ЯМР-спектры записывали на спектрометре Brucker AC-300 (300 МГц) с использованием тетраметилсилана (TMS) в качестве внутреннего стандарта. Пример 1. 3-(4-Этилбензил)-5-(-D-глюкопиранозил)-1 Н-индолA. Диэтиламид 5-бром-3-формилиндол-1-карбоновой кислоты. К суспензии гидрида натрия (0,93 г, 37 ммоль) в безводном ТГФ (75 мл) добавляли по каплям раствор 5-бром-1 Н-индол-3-карбальдегида (7,5 г, 34 ммоль) в безводном ТГФ (60 мл) при 0C. После перемешивания при 0C в течение 15 мин к реакционной смеси добавляли по каплямN,N-диэтилкарбамилхлорид (5,0 г, 37 ммоль). Смесь подогревали до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь гасили водой и экстрагировали этилацетатом. Органические фракции промывали насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток кристаллизовали из смеси диэтиловый эфир/гексан с получением указанного в заголовке соединения (8,75 г, 80%) в виде белого твердого вещества.B. Диэтиламид 5-бром-3-(4-этилбензил)индол-1-карбоновой кислоты. К раствору соединения со стадии А (3,3 г, 10 ммоль) в 20 мл безводного ТГФ добавляли по каплям 0,5 М раствор 4-этилфенилмагния бромида в безводном ТГФ (22 мл, 11 ммоль) при 0C. Продолжали перемешивание реакционной смеси при 0C в течение 30 мин, гасили насыщенным раствором хлорида аммония и экстрагировали этилацетатом. Органические экстракты высушивали над сульфатом натрия и концентрировали в вакууме. Сырой продукт непосредственно использовали на следующей стадии. К раствору сырого индолкарбинола в 20 мл дихлорметана добавляли триэтилсилан (1,16 г,10,0 ммоль) при -78C с последующим добавлением 1,0 М раствора хлорида олова в дихлорметане (20 мл,20 ммоль). Перемешивание реакционной смеси продолжали при температуре -78C в течение 20 мин,гасили водой и подогревали до комнатной температуры. После экстракции дихлорметаном органические экстракты высушивали над сульфатом натрия, концентрировали в вакууме и хроматографировали на силикагеле, элюируя смесью этилацетат/гексан (10:100), с получением указанного в заголовке соединения(3,4 г, выход: 82%) в виде белого твердого вещества.C. 5-Бром-3-(4-этилбензил)-1 Н-индол. Соединение, полученное на стадии В (3,4 г, 8,2 ммоль), растворяли в этаноле (60 мл) и 25% водном растворе гидроксида натрия (20 мл) и полученный раствор доводили до кипения в течение 3 ч. После охлаждения до комнатной температуры смесь разбавляли водой (60 мл), концентрировали в вакууме для удаления большей части этанола и экстрагировали этилацетатом. Органические экстракты промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан(1:4), с получением указанного в заголовке соединения (2,0 г, 79%) в виде белых игольчатых кристаллов.D. 5-Бром-1-(трет-бутилдиметилсиланил)-3-(4-этилбензил)-1 Н-индол. К суспензии гидрида натрия (0,12 г, 4,8 ммоль) в безводном ТГФ (2 мл) добавляли по каплям раствор соединения, полученного на стадии C (1,28 г, 4,0 ммоль), в безводном ТГФ (6 мл) при 0C. После перемешивания при 0C в течение 30 мин в реакционную смесь добавляли по каплям 1,0 М раствор третбутилхлордиметилсилана в безводном ТГФ (4,5 мл, 4,5 ммоль). Смесь подогревали до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь гасили водой и экстрагировали этилацетатом. Органические фракции промывали насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (0,5:100), с получением указанного в заголовке соединения(1,75 г, 100%) в виде светло-желтого масла. Е. 3-(4-Этилбензил)-5-(2,3,4,6-тетра-O-бензилD-глюкопиранозил)-1-(трет-бутилдиметилсиланил)-1 Н-индол. К перемешиваемому раствору соединения, полученного на стадии D (1,75 г, 4,0 ммоль), в сухом ТГФ (2 мл) при температуре -78C добавляли 1,7 М раствор трет-бутиллития в гептане (4,7 мл, 8,0 ммоль) в течение 15 мин. После перемешивания в течение 30 мин добавляли раствор 2,3,4,6-тетра-O-бензилDглюколактона (4,3 г, 8,0 ммоль; полученного как описано Benhaddou, R.; Carbohydrate Research 1994, 260,243-250) в сухом ТГФ (10 мл) при температуре -78C в течение 15 мин. Реакционную смесь перемешивали при температуре -78C в течение 1 ч (протекание реакции прослеживали ТСХ). По окончании реакционную смесь гасили насыщенным водным раствором NH4Cl (5 мл), подогревали до комнатной температуры и реакционную смесь разбавляли этилацетатом. Органические экстракты промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (1:4), с получением смеси желаемого лактола и непрореагировавшего 2,3,4,6-тетра-O-бензилD-глюколактона(2,8 г, 50% желаемого лактола) в виде светло-коричневого масла. Данную смесь непосредственно использовали на следующей стадии без дополнительной очистки. К раствору вышеуказанной смеси (2,8 г) в дихлорметане (20 мл) добавляли триэтилсилан (0,5 мл,3,2 ммоль) при температуре -30C с последующим добавлением трифторборана-диэтилового эфира(0,2 мл, 1,6 ммоль). После перемешивания при температуре в пределах от -30 до -20C в течение 1 ч, когда анализ ТСХ указывал, что реакция завершена, реакционную смесь гасили добавлением насыщенного водного раствора NaHCO3 (3 мл). Смесь подогревали до комнатной температуры и перемешивали в течение 1 ч. Реакционную смесь экстрагировали этилацетатом. Органические экстракты промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (1:4),с получением указанного в заголовке соединения (0,68 г, 19% с двух стадий) в виде светло-желтого масла.F. 3-(4-Этилбензил)-5-(2,3,4,6-тетра-O-бензилD-глюкопиранозил)-1H-индол. Соединение со стадии Е (0,68 г, 0,78 ммоль) растворяли в ТГФ (15 мл) и 25% водном растворе гидроксида натрия (5 мл) и полученный раствор доводили до кипения в течение 3 ч. После охлаждения до комнатной температуры смесь разбавляли водой (30 мл) и экстрагировали этилацетатом. Органические экстракты промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (1:3), с получением указанного в заголовке соединения (0,5 г, 85%) в виде белого твердого вещества.G. 3-(4-Этилбензил)-5-(-D-глюкопиранозил)-1 Н-индол. Раствор соединения со стадии F (0,30 г, 0,4 ммоль) в этаноле (10 мл) и этилацетате (20 мл) гидрировали на 10% катализаторе Перлманса (0,30 г) под давлением H2 14 фунт/кв.дюйм в течение 40 ч. Катализатор удаляли фильтрованием и фильтрат концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью метанол/хлороформ (10:100), с получением указанного в заголовке соединения (0,04 г, 25%) в виде белого твердого вещества. 1 Н ЯМР (300 МГц, CD3OD)7,51 (с, 1 Н), 7,32 (д, J=8,52 Гц, 1 Н), 7,19-7,15 (м, 3 Н), 7,06 (д,J=7,87 Гц, 2 Н), 6,95 (с, 1 Н), 4,18-4,15 (м, 1 Н), 4,04 (с, 2 Н), 3,87 (д, J=12,2 Гц, 1 Н), 3,71-3,65 (м, 1 Н), 3,533,48 (м, 2 Н), 3,45-3,41 (м, 2 Н), 2,58 (кв, J=7,58 Гц, 2 Н), 1,19 (т, J=7,65 Гц, 3 Н). МС: m/z (M+Na) 420. Указанное в заголовке соединение получали в виде белого твердого вещества из диэтиламида 5-бром-3-формилиндол-1-карбоновой кислоты (пример 1, стадия А) и 4-метоксифенилмагния бромида,следуя той же методике, описанной в примере 1, стадии от В до G. 1 Н ЯМР (300 МГц, CD3OD)7,49 (с, 1 Н), 7,32 (д, J=8,20 Гц, 1 Н), 7,19-7,15 (м, 3 Н), 6,95 (с, 1 Н), 6,79 А. Диэтиламид 5-бром-3-[2-(4-метоксифенил)этил]индол-1-карбоновой кислоты. К раствору 4-метоксибензилтрифенилфосфония хлорида (7,5 г, 18 ммоль) в безводном ТГФ (75 мл) при температуре -78C добавляли LDA (9,0 мл, 18 ммоль) и полученную реакционную смесь перемешивали при -78C в течение 1 ч. Затем добавляли диэтиламид 5-бром-3-формилиндол-1-карбоновой кислоты (1,9 г, 6 ммоль, пример 1, стадия А) и полученную реакционную смесь перемешивали при -78C в течение 1 ч и затем подогревали до комнатной температуры для перемешивания в течение ночи. Реакционную смесь выливали в 1 н. раствор HCl и экстрагировали этилацетатом. Объединенные этилацетатные экстракты промывали насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле,элюируя смесью этилацетат/гексан (1:4), с получением смеси алкенов (2,3 г, 90%, E:Z1:1) в виде коричневого масла. Раствор вышеуказанных алкенов (2,3 г, 5,4 ммоль) в дихлорметане (100 мл) гидрировали на катализаторе Адамса (300 мг) в атмосфере Н 2 (15 фунт/кв.дюйм) в течение 2 ч. Катализатор удаляли фильтрованием и фильтрат концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (1:4), с получением указанного в заголовке соединенияB. 5-Бром-3-[2-(4-метоксифенил)этил]-1 Н-индол. Соединение со стадии В (1,43 г, 3,3 ммоль) растворяли в этаноле (30 мл) и 25% водном растворе гидроксида натрия (10 мл) и полученный раствор доводили до кипения в течение 3 ч. После охлаждения до комнатной температуры смесь разбавляли водой (30 мл), концентрировали в вакууме для удаления большей части этанола и экстрагировали этилацетатом. Органические экстракты промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (1:4), с получением указанного в заголовке соединения (1,0 г, 91%) в виде светло-коричневого масла.C. 5-Бром-1-(трет-бутилдиметилсиланил)-3-[2-(4-метоксифенил)этил]-1H-индол. К суспензии гидрида натрия (0,081 г, 4,0 ммоль) в безводном ТГФ (2 мл) добавляли по каплям раствор соединения со стадии C (0,85 г, 2,7 ммоль) в безводном ТГФ (3 мл) при 0C. После перемешивания в течение 30 мин в реакционную смесь добавляли по каплям 1,0 М раствор трет-бутилхлордиметилсилана в безводном ТГФ (3,2 мл, 3,2 ммоль). Смесь подогревали до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь гасили водой и экстрагировали этилацетатом. Органические экстракты промывали насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексан (0,5:100), с получением указанного в заголовке соединения (0,92 г, 79%) в виде светложелтого масла.D. 5-(-D-Глюкопиранозил)-3-[2-(4-метоксифенил)этил]-1 Н-индол. Указанное в заголовке соединение получали в виде белого твердого вещества из соединения со стадии C, следуя той же методике, описанной в примере 1, стадии E, F и G. 1 Н ЯМР (300 МГц, CD3OD)7,58 (с, 1 Н), 7,31 (д, J=8,06 Гц, 1 Н), 7,18 (дд, J=8,39, 1,59 Гц, 1 Н), 7,10(2,21 г, 11,3 ммоль) в дихлорметане (25 мл) при комнатной температуре в течение 20 мин с последующим добавлением раствора 4-этилбензоилхлорида (2,5 мл, 17 ммоль) в дихлорметане (25 мл) в течение 20 мин. Полученный раствор перемешивали при комнатной температуре в течение ночи и добавляли насыщенный раствор бикарбоната натрия на ледяной бане для гашения реакции. Водный слой экстрагировали дихлорметаном. Органические экстракты промывали насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт растирали с диэтиловым эфиром с получением указанного в заголовке соединения (1,8 г, 48%) в виде белых твердых частиц.B. (1-Бензолсульфонил-4-бром-1 Н-индол-3-ил)-(4-этилфенил)метанон. Смесь соединения, полученного на стадии А (1,6 г, 5 ммоль), тетрабутиламмония бромида (0,16 г,0,5 ммоль) и бензолсульфонилхлорида (1,3 г, 7,5 ммоль) в 25% водном растворе гидроксида натрия(10 мл) и бензоле (50 мл) перемешивали при комнатной температуре в течение ночи. Реакционную смесь гасили добавлением воды и экстрагировали этилацетатом. Органический слой промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия, концентрировали в вакууме и хроматографировали на силикагеле, элюируя смесью этилацетат/гексан (30:100), с получением указанного в заголовке соединения (1,80 г, 76%).C. 1-Бензолсульфонил-4-бром-3-(4-этилбензил)-1 Н-индол. К суспендированному AlCl3 (0,8 г, 6 ммоль) в дихлорметане (10 мл) добавляли комплекс борантрет-бутиламин (0,52 г, 6 ммоль) при 0C. Полученную смесь перемешивали при 0C в течение 10 мин с последующим добавлением раствора соединения со стадии В (0,94 г, 2 ммоль) в дихлорметане (15 мл). Реакционную смесь перемешивали при комнатной температуре в течение ночи и добавляли NaOH (3M раствор, 20 мл) с размолотым льдом для гашения реакции. Основной водный слой экстрагировали дихлорметаном. Органические экстракты промывали насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт (0,90 г, 99%) был достаточно чистым для его использования на следующей стадии без дополнительной очистки.D. 4-Бром-3-(4-этилбензил)-1H-индол. Соединение со стадии C (0,90 г, 2 ммоль) растворяли в смеси этанол-ТГФ 1:1 (20 мл) с 50% водным раствором гидроксида натрия (2 мл). Полученный раствор доводили до кипения в течение 3 ч. После охлаждения до комнатной температуры смесь разбавляли водой (20 мл), концентрировали в вакууме для удаления большей части этанола и экстрагировали этилацетатом. Органические экстракты промывали водой и насыщенным раствором соли, высушивали над безводным сульфатом натрия и концентрировали в вакууме. Сырой продукт очищали хроматографией на силикагеле, элюируя смесью этилацетат/гексанE. 3-(4-Этилбензил)-4-(-D-глюкопиранозил)-1 Н-индол. Указанное в заголовке соединение получали в виде белого твердого вещества из соединения со стадии D, следуя той же методике, описанной в примере 1, стадии D, F и G. 1 Н ЯМР (300 МГц, CD3OD)7,33 (дд, J=7,42, 1,64 Гц, 1 Н), 7,18 (д, J=1,79 Гц, 1 Н), 7,16-7,07 (м, 5 Н),6,90 (с, 1 Н), 4,72 (д, J=9,64 Гц, 1 Н), 4,35 (д, J=16,5 Гц, 1 Н), 4,26 (д, J=16,4 Гц, 1H), 3,69-3,52 (м, 3 Н), 3,443,39 (м, 2 Н), 2,95 (с, 1 Н), 2,58 (кв, J=7,58 Гц, 2 Н), 1,19 (т, J=7,65 Гц, 3 Н). МС: m/z (M+Na) 420.H. Биологические примеры. Пример 1. Материалы и методы. Клонирование кДНК человеческого SGLT1 и человеческого SGLT2 и конструирование экспрессирующего вектора млекопитающих: кДНК человеческого SGLT1 (Genbank M24847) клонировали из тонкого кишечника человека. кДНК человеческого SGLT2 (Genbank М 95549) клонировали из почки человека. Обе полноразмерные кДНК субклонировали в ркДНК и секвенировали для подтверждения целостности конструкции. Получение клеток CHO-K1, стабильно экспрессирующих человеческий SGLT1 или человеческийgies, Gaithersburg, MD). Затем отбирали трансфектанты в присутствии антибиотика G418 (Gibco-BRL,Grand Island, NY) в концентрации 400 мкг/мл. Затем охарактеризовывали отдельные клоны использованием функционального теста, описанного ниже. Клеточный тест для оценки натрийзависимого транспорта глюкозы: затем клеточные линии, стабильно экспрессирующие человеческий SGLT1 или человеческий SGLT2, использовали для проведения функционального анализа Na+-зависимого поглощения глюкозы. Кратко, клетки высевали с титром 65000 клеток на лунку в 96-луночном планшете и культивировали в течение 48 ч. Затем клетки промывали один раз буфером для анализа (50 мМ HEPES, рН 7,4, 20 мМ Трис, 5 мМ KCl, 1 мМ MgCl2, 1 мМCaCl2 и 137 мМ NaCl) и обрабатывали соединением в отсутствие или присутствии NaCl в течение 15 мин. Затем клетки метили 14Cметилглюкопиранозидом (AMG, Sigma, St. Louis, МО), неметаболизируемым аналогом глюкозы, специфичным для натрийзависимых переносчиков глюкозы, как описано ранее (Peng, H. and Lever J.E. Post-transcriptional regulation of Na+/glucose cotransporter (SGLT1) gene expression in LLC-PK1 cells. J. Biol. Chem., 1995; 270: 20536-20542). Через 2 ч меченые клетки промывали три раза охлажденным на льду PBS. После аспирации клетки солюбилизировали с использованиемMicroscint 20 (Packard, Meriden, CT) и количественно оценивали Na-зависимое поглощение 14C-AMG по определению радиактивности. Радиоактивность планшетов определяли на счетчике TopCount (Packard, Meriden, CT). Результаты выражали в % ингибирования или значении IC50 по данным репрезентативного опыта. Вариабельность функционального теста, как правило, составляла 20%. Таблица 3 Пример 2. Тест для оценки эффективности в условиях in vivo. Крыс-самцов с сахарным диабетом и ожирением (ZDF) (7-8 недель) получали из Charles River. Животных содержали с 12 ч циклом свет/темнота в помещении с контролируемой температурой. Корм(стандартный рацион для грызунов Purina 5008) и воду животные получали вволю. Перед началом опыта животных выдерживали голодными в течение 12 ч. Утром в день опыта животным вводили растворитель(0,5% метилцеллюлозу) или соединение перорально (1 мл/кг). Через 1 ч животным давали глюкозную нагрузку перорально (4 мл/кг 50% раствора) и их немедленно помещали в метаболитные камеры. Животным вволю давали воду и в течение 4 ч собирали мочу. Концентрацию глюкозы в моче определяли с использованием Reagent Trinder (Sigma). Пример 3. Влияние на концентрацию глюкозы в плазме крови, уровень инсулина в плазме крови,концентрацию триглицеридов в плазме крови, уровень свободных жирных кислот в плазме крови, массу печени и массу тела. Для исследования влияния ингибитора SGLT в комбинации с агонистом RXR мышей-самок db/db (в возрасте 6-7 недель/Jackson Labs, ME) обрабатывали ежедневно в течение 11 суток растворителем (0,5% метилцеллюлозой), агонистом RXR (0,1-10 мпк (мг/кг, ингибитором SGLT (100 мпк) или агонистомRXR плюс ингибитор SGLT. Мыши (n=8 животных/группу) получали тестируемые соединения или растворитель перорально в объеме 10 мл/кг массы тела. Массу тела регистрировали на 1 сутки, перед введением, и на 4, 8 и 11 сутки. Через 18 ч после последнего введения мышей взвешивали и анестезировали введением CO2/O2 (70:30). Затем у мышей отбирали пробы крови пункцией ретробульбарного глазного синуса в полипропиленовые пробирки емкостью 2 мл с гепарином, находящиеся на льду. Затем пробы крови анализировали на содержание глюкозы, инсулина, триглицеридов и свободных жирных кислот. Извлекали печени, взвешивали и замораживали. Ингибиторы SGLT и агонисты RXR имеют различные механизмы действия. Улучшенный гликемический контроль, определенный по снижению уровня глюкозы в плазме крови, инсулина в плазме крови,свободных жирных кислот в плазме крови или триглицеридов в плазме крови или их сочетаний, можно наблюдать при более низких концентрациях агониста RXR при введении в комбинации с ингибиторомSGLT. Следовательно, становится очевидным сдвиг влево на кривой зависимости доза-эффект для действия агониста RXR в отношении вышеуказанных параметров. Кроме того, увеличение массы тела, наблюдаемое после лечения агонистами RXR, менее выражено при введении с ингибитором SGLT, поскольку показано стимулирующее действие ингибиторов SGLT на выделение глюкозы с мочой и потерю калорий из организма по снижению массы тела и привесов. Также, поскольку ингибиторы SGLT обладают мягким диуретическим действием, то отеки (и привесы в результате отеков), обычно наблюдаемые после лечения агонистами RXR, могут быть менее выраженными или отсутствовать. Уменьшение количества агониста RXR, такого как МХ-6054, необходимого для достижения эффективности, в свою оче- 24009768 редь, улучшает профиль проявления побочных эффектов. Сниженные побочные эффекты могут включать такие состояния, как ожирение печени, повышенная масса печени, увеличение массы тела, увеличение массы сердца, отеки, гипертрофия сердца, гипертрофия печени, гипогликемия и гепатотоксичность,или их любые сочетания. Пример 4. Влияние на концентрацию глюкозы в плазме крови, HbA1c, гематокрит, на уровень инсулина в плазме крови, концентрацию триглицеридов в плазме крови, уровень свободных жирных кислот в плазме крови, общий холестерин, HDL, концентрацию препарата в плазме крови, массу печени, массу сердца, содержание жира и массу тела. Для исследования влияния ингибитора SGLT в комбинации с агонистом RXR крыс-самцов ZDF (в возрасте 6 недель/GMI) обрабатывали ежедневно в течение 28 суток растворителем (0,5% метилцеллюлозой), агонистом RXR (0,1-10 мпк), ингибитором SGLT (3-100 мпк) или агонистом RXR плюс ингибитор SGLT. Крысы (n=8 животных/группу) получали тестируемые соединения или растворитель перорально в объеме 2 мл/кг массы тела. Массу тела регистрировали на 1 сутки, перед введением, и дважды в неделю в течение опыта. За одни сутки перед последним введением животных выдерживали голодными в течение ночи. Через 1 ч после последнего введения крыс взвешивали и анестезировали CO2/O2 (70:30). Затем у крыс отбирали пробы крови пункцией ретробульбарного глазного синуса в полипропиленовые пробирки емкостью 2 мл с гепарином, находящиеся на льду. Затем крысам давали глюкозную нагрузку(2 г/кг перорально) и помещали в метаболитные камеры для сбора мочи (4 ч). Затем животных умерщвляли и извлекали эпидидимальный жир, печень и сердце, взвешивали и замораживали для проведения гистологических исследований. Затем пробы крови анализировали на содержание глюкозы, HbA1c, инсулина, гематокрита, определяли концентрацию препарата в плазме крови, общего холестерина, HDL,свободных жирных кислот и триглицеридов. Определяли объем мочи и содержание в моче глюкозы,белка, осмомолярность, уровень электролитов (Na, K, Cl), BUN и креатинина. Ингибиторы SGLT и агонисты RXR имеют различные механизмы действия. Улучшенный гликемический контроль, определенный по снижению уровня глюкозы в плазме крови, HbA1c, инсулина в плазме крови или триглицеридов в плазме крови или их сочетаний, можно наблюдать при более низких концентрациях агонистов RXR при введении в комбинации с ингибитором SGLT. Следовательно, становится очевидным сдвиг влево на кривой зависимости доза-эффект для действия агониста RXR в отношении вышеуказанных параметров. Кроме того, увеличение массы тела, наблюдаемое после лечения агонистами RXR, менее выражено при введении с ингибитором SGLT, поскольку показано стимулирующее действие ингибиторов SGLT на выделение глюкозы с мочой и потерю калорий из организма по снижению массы тела и привесов. Также, поскольку ингибиторы SGLT обладают мягким диуретическим действием,то отеки (и привесы в результате отеков), обычно наблюдаемые после лечения агонистами RXR, могут быть менее выраженными или отсутствовать. Это можно продемонстрировать по снижению индуцируемого агонистом RXR увеличения массы сердца. Уменьшение количества агонистов RXR, необходимого для достижения эффективности, в свою очередь, улучшает профиль проявления побочных эффектов. Сниженные побочные эффекты могут включать такие состояния, как ожирение печени, повышенная масса печени, увеличение массы тела, увеличение массы сердца, отеки, гипертрофия сердца, гипертрофия печени, гипогликемия и гепатотоксичность, или их любые сочетания. Приведенные выше примеры также могут показать, что пероральное введение ингибитора SGLT в комбинации с противодиабетическими средствами, такими как модулятор RXR, улучшают состояние других маркеров сахарного диабета, включая уровень гликозилированного гемоглобина (HgbA1c). В частности, пероральное введение ингибитора SGLT в комбинации с одним или более модуляторами RXR может привести к снижению массы тела или привесов, а также массы печени или увеличения массы печени по сравнению с введением только одного или более модуляторов RXR. Таким образом, для лечения диабета, особенно сахарного диабета типа II или синдрома X, можно использовать соединение формулы (IV) в комбинации с одним или более противодиабетическими средствами, такими как агонист RXR, который повышает чувствительность к инсулину, включая пероральное введение многократных доз соединения формулы (IV) в пределах примерно от 25 до 1000 мг один или два раза в сутки или многократных доз противодиабетического средства или средств в совместно эффективных дозах. Совместно эффективную дозу для противодиабетических средств, раскрытых здесь, могут легко определить специалисты в данной области, основываясь на обычных рекомендациях для доз. В частности, такое комбинированное введение может быть эффективным для снижения массы тела, привесов, массы печени или увеличения массы печени у субъекта. Кроме того, способ, включающий (а) введение субъекту совместно эффективного количества ингибитора реабсорбции глюкозы и (b) введение субъекту совместно эффективного количества противодиабетического средства, такого как модулятор RXR, можно использовать для снижения массы тела, привесов или массы печени субъекта, нуждающегося в этом, в котором комбинированное введение можно проводить в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый терапевтический эффект. Кроме того, способ, включающий (а) введение субъекту совместно эффективного количества ингибитора реабсорбции глюкозы и (b) введение субъекту совместно эффективного количества противодиа- 25009768 бетического средства, можно использовать для контроля массы тела, увеличения массы тела, массы печени или увеличения массы печени у субъекта, страдающего диабетом, синдромом X или связанными с ними симптомами или осложнениями, в котором комбинированное введение можно проводить в любом порядке, и объединенные совместно эффективные количества обеспечивают желаемый терапевтический эффект. Оптимальные дозы для введения могут легко определить специалисты в данной области, и они будут варьировать в зависимости от конкретного используемого соединения, способа введения, эффективности препарата и тяжести болезненного состояния. Кроме того, факторы, связанные с конкретным пациентом, который подвергается лечению, включающие пол, возраст, массу, рацион пациента, время введения и сопутствующие заболевания, будут приводить к необходимости в корректировке доз. Несмотря на то что в приведенном выше описании представлены принципы настоящего изобретения с примерами, представленными в целях иллюстрации, очевидно, понятно, что практика изобретения включает все обычные вариации, адаптации и/или модификации, которые находятся в объеме последующей формулы изобретения и ее эквивалентных вариантов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы в которой одна из пунктирных линий находится между NR1 и X, или между X и Y, или обе отсутствуют; два из V, M и W представляют Н и третий являетсяR1 представляет Н или C1-4 алкил или R1 отсутствует, когда имеется пунктирная линия между NR1 иZ является замещенным или незамещенным, и выбран из C3-7 циклоалкила, фенила, 5- или 6-членного гетероарила, содержащего 1 или 2 гетероатома, независимо выбранных из N, О и S, биарила,9- или 10-членного конденсированного бициклила и конденсированного гетеробициклила, где указанный конденсированный гетеробициклил содержит от 1 до 4 гетероатомов, независимо выбранных из N, О и S; или фармацевтически приемлемая соль. 2. Соединение по п.1, в котором R1 представляет Н или отсутствует. 3. Соединение по п.1, в котором Z независимо замещен 1-3 заместителями, независимо выбранными из C1-4 алкокси, фенокси, C1-4 алкила, C3-6 циклоалкила, атома галогена, гидрокси, циано, амино,C1-4 алкилтио, C1-4 алкилсульфонила, C1-4 алкилсульфинила, C1-4 аминоалкила, моно- и ди-C1-4 алкиламино,фенила,C1-4 алкиламиносульфонила(NHSO2R),ди-C1-4 алкиламиносульфинила (SONHRR), C1-4 алкиламидо (NHCOR), C1-4 алкилкарбамидо (CONHR),5-6-членного гетероциклила, содержащего 1-3 гетероатомов, независимо выбранных из N, S и О; и где заместитель(и) в Z может быть дополнительно независимо замещен 1-3 заместителями, независимо выбранными из C1-4 алкокси, C1-4 алкила, атома галогена, гидрокси, циано, амино, моно- и ди-C1-4 алкиламино и C1-4 алкилтио. 4. Соединение по п.1, в котором Z представляет 4-замещенный фенил, 3,4-дизамещенный фенил,бензгидрил, замещенный или незамещенный тиофенил, биарил, бензофуранил, гидробензофуранил,дигидробензофуранил, 4-замещенный пиридил, бензо[b]тиенил, хроманил, бензотиофенил, инданил,нафтил и 2,3-дигидробензо[1,4]диоксан.- 26009768 5. Соединение по п.3, в котором Z является незамещенным или замещенным 1-2 заместителями, независимо выбранными из метокси, этокси, атома фтора, атома хлора, метила, этила, пропила, бутила и изопропила. 6. Соединение по п.1, в котором Z представляет бифенил, 4-(3-пиридил)фенил, 4-(2-тиенил)фенил,4-(1 Н-пиразол-1-ил)фенил, (4-этил)фенил, (4-пропил)фенил, (4-метокси)фенил, дигидробензофуран-5-ил или дигидробензофуран-6-ил. 7. Соединение по п.1, в котором R1 представляет Н. 8. Соединение по п.1, в котором n равно 1. 9. Соединение по п.8, в котором R1 представляет Н или отсутствует. 10. Соединение по п.1, в котором Z представляет бифенил, 4-(3-пиридил)фенил, 4-(2-тиенил)фенил,4-(1 Н-пиразол-1-ил)фенил, (4-этил)фенил, (4-пропил)фенил, (4-метокси)фенил, дигидробензофуран-5-ил или дигидробензофуран-6-ил и Z является незамещенным или замещенным 1-2 заместителями, независимо выбранными из метокси, этокси, атома фтора, атома хлора, метила, этила, пропила, бутила и изопропила. 11. Соединение по п.10, в котором n равно 1. 12. Соединение по п.10, в котором R представляет Н. 13. Соединение по п.1, в котором М и V представляют Н. 14. Соединение по п.1, в котором М и W представляют Н. 15. Соединение по п.1, в котором X представляет CH и Y является C-Q-Z. 16. Соединение по п.1, в котором X представляет C-Q-Z и Y является CH. 17. Соединение по п.15, в котором R1 представляет Н или отсутствует и n=1. 18. Соединение по п.1, выбранное из 3-(4-этилбензил)-5-(-D-глюкопиранозил)-1 Н-индола,5-(-D-глюкопиранозил)-3-(4-метоксибензил)-1 Н-индола,5-(-D-глюкопиранозил)-3-[2-(4-метоксифенил)этил]-1 Н-индола и 3-(4-этилбензил)-4-(-D-глюкопиранозил)-1 Н-индола. 19. Соединение по п.1, выбранное из 2-(4-этилбензил)-4-(-D-глюкопиранозил)-1 Н-индола,3-[2-(2,3-дигидробензофуран-5-ил)этил]-5-(-D-глюкопиранозил)-1 Н-индола,5-(-D-глюкопиранозил)-3-(5-метил-2-тиенил)-1 Н-индола,3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензимидазола,3-(4-этилбензил)-4-(-D-глюкопиранозил)-1,3-дигидробензимидазол-2-она и 3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензотриазола. 20. Соединение по п.1, выбранное из 3-(4-этилбензил)-5-(-D-глюкопиранозил)-1 Н-индола,2-(4-этилбензил)-4-(-D-глюкопиранозил)-1 Н-индола,5-(-D-глюкопиранозил)-3-(5-метил-2-тиенил)-1 Н-индола,3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензимидазола и 3-(4-этилбензил)-4-(-D-глюкопиранозил)-3 Н-бензотриазола. 21. Фармацевтическая композиция, содержащая соединение по пп.1, 5, 6, 11-19 или 20. 22. Фармацевтическая композиция по п.21, содержащая соединение по п.14 и фармацевтически приемлемый носитель. 23. Способ лечения диабета у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21. 24. Способ по п.23, в котором указанный диабет представляет диабет типа II. 25. Способ снижения концентрации глюкозы в сыворотке крови у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21. 26. Способ лечения пониженной толерантности к глюкозе у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21. 27. Способ лечения или ингибирования пониженной толерантности к глюкозе у млекопитающего,где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21. 28. Способ снижения индекса массы тела, массы тела или процента жировой ткани тела у млекопитающего, где указанный способ включает введение млекопитающему, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.21. 29. Способ по п.28, где указанный способ снижения индекса массы тела представляет способ лечения ожирения или избыточной массы тела. 30. Способ ингибирования переносчика натрия-глюкозы в клетке воздействием на данную клетку соединением по п.1 или его метаболитом.- 27009768 31. Способ лечения диабета или синдрома X, или связанных с ними симптомов или осложнений у субъекта, включающий: а) введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы формулы (IV) иb) введение указанному субъекту совместно эффективного количества второго противодиабетического средства,где указанное совместное введение проводят в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый терапевтический эффект. 32. Способ по п.31, в котором второе противодиабетическое средство представляет агонист RXR. 33. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения выбраны из IDDM, NIDDM, IGT, IFG, ожирения, нефропатии, нейропатии, ретинопатии, атеросклероза, синдрома поликистоза яичников, гипертензии, ишемии, инсульта, заболевания сердца, синдрома раздраженного кишечника, воспаления и катаракты. 34. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения представляют IDDM. 35. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения представляют NIDDM. 36. Способ по п.31, в котором диабет или синдром X или связанные с ними симптомы или осложнения представляют IGT или IFG. 37. Способ по п.31, дополнительно включающий введение указанному субъекту совместно эффективного количества третьего противодиабетического средства. 38. Способ по п.37, в котором третье противодиабетическое средство выбрано из: а) инсулинов,b) аналогов инсулина,c) модуляторов секреции инсулина иd) средств, стимулирующих секрецию инсулина. 39. Способ по п.31, в котором ингибитором реабсорбции глюкозы является ингибитор SGLT. 40. Способ по п.31, в котором ингибитором реабсорбции глюкозы является ингибитор SGLT1. 41. Способ по п.31, в котором ингибитором реабсорбции глюкозы является ингибитор SGLT2. 42. Способ по п.31, в котором ингибитором реабсороции глюкозы является соединение формулы(IV) или его оптический изомер, энантиомер, диастереомер, рацемат или рацемическая смесь, сложный эфир, пролекарство или его фармацевтически приемлемая соль. 43. Способ по п.31, в котором совместно эффективное количество ингибитора SGLT находится в пределах примерно от 10 до 1000 мг. 44. Способ по п.31, в котором совместно эффективное количество ингибитора SGLT представляет количество, достаточное для снижения изменения уровня глюкозы в плазме крови после приема пищи. 45. Способ подавления начала развития диабета или синдрома X или связанных с ними симптомов или осложнений у субъекта, где указанный способ включает:a) введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы формулы (IV) иb) введение указанному субъекту совместно эффективного количества второго противодиабетического средства,где указанное совместное введение проводят в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый профилактический эффект. 46. Способ по п.45, в котором указанное начало развития представляет переход от состояния преддиабета до NIDDM. 47. Фармацевтическая композиция, содержащая ингибитор реабсорбции глюкозы формулы (IV),второе противодиабетическое средство и фармацевтически приемлемый носитель. 48. Фармацевтическая композиция по п.47, в которой ингибитором реабсорбции глюкозы является ингибитор SGLT . 49. Фармацевтическая композиция по п.47, в которой ингибитором реабсорбции глюкозы является ингибитор SGLT1. 50. Фармацевтическая композиция по п.47, в которой ингибитором реабсорбции глюкозы является ингибитор SGLT2. 51. Способ составления рецептуры фармацевтической композиции, предусматривающий включение в рецептуру ингибитора реабсорбции глюкозы, второго противодиабетического средства и фармацевтически приемлемого носителя. 52. Способ получения фармацевтической композиции, включающий смешение одного или более ингибиторов реабсорбции глюкозы в комбинации со вторым противодиабетическим средством для получения лекарственного препарата для лечения состояния, выбранного из IDDM, NIDDM, IGT, IFG, ожирения, нефропатии, нейропатии, ретинопатии, атеросклероза, синдрома поликистоза яичников, гипертензии, ишемии, инсульта, заболевания сердца, синдрома раздраженного кишечника, воспаления и катаракты.- 28009768 53. Способ подавления прогрессирования состояния преддиабета до диабета у субъекта, включающий:a) введение указанному субъекту совместно эффективного количества ингибитора реабсорбции глюкозы формулы (IV) иb) введение указанному субъекту совместно эффективного количества второго противодиабетического средства,где указанное совместное введение проводят в любом порядке и объединенные совместно эффективные количества обеспечивают желаемый подавляющий эффект. 54. Способ по п.53, в котором указанное состояние представляет IGT или IFG. 55. Способ по п.53, в котором указанное подавление прогрессирования состояния преддиабета представляет профилактику прогрессирования состояния преддиабета до диабета. 56. Способ по п.53, в котором ингибитором реабсорбции глюкозы является соединение формулы(IV), необязательно содержащее одну или более гидроксил- или диолзащищающих групп, или его оптический изомер, энантиомер, диастереомер, рацемат или рацемическая смесь, сложный эфир, пролекарство, или его фармацевтически приемлемая соль.
МПК / Метки
МПК: A01N 43/04, C07H 1/00, A61K 31/70
Метки: с-гликозиды, гетероциклические, замещенные, конденсированные
Код ссылки
<a href="https://eas.patents.su/30-9768-zameshhennye-kondensirovannye-geterociklicheskie-s-glikozidy.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные конденсированные гетероциклические с-гликозиды</a>
Предыдущий патент: Производные пролина, обладающие сродством к альфа-2-дельта субъединице кальциевого канала
Следующий патент: Производные хинолилпропилпиперидина и их применение в качестве антимикробных средств
Случайный патент: Защитная проволочная сетка, защитная конструкция, сооружаемая из сетки, и применение защитной проволочной сетки для сооружения защитной конструкции