Замещенные бензопираны в качестве селективных агонистов бета-рецептора эстрогена
Номер патента: 7382
Опубликовано: 27.10.2006
Авторы: Пфайфер Ланс Аллен, Кришнан Венкатеш Гари, Лугар Чарльз Уиллис III, Додж Джеффри Алан, Норман Брайан Херст, Нойбауэр Блейк Ли, Ричардсон Тимоти Айво
Формула / Реферат
1. Соединение формулы (I)
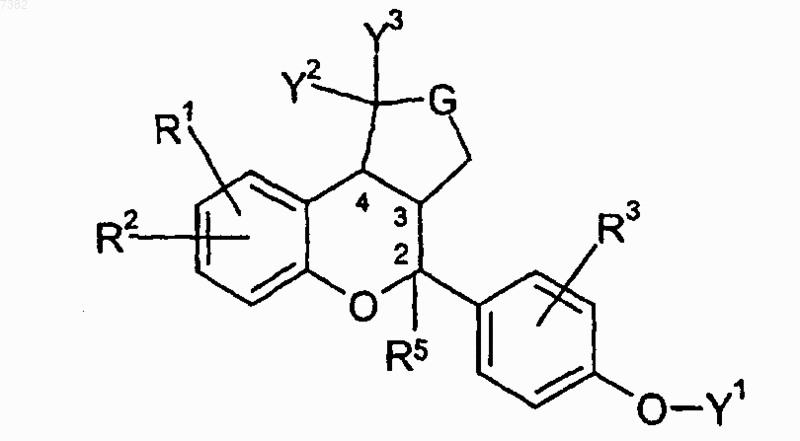
где R1, R2 и R3, каждый независимо, является -Н, C1-С6 алкилом, -ОН, C1-С6 алкокси, галогеном или -СFз;
R5 является водородом или C1-С6 алкилом;
Y1, Y2 и Y3, каждый независимо, является -Н или C1-С6 алкилом и
G является -СН2-, -СН2-СН2- или -СН2-СН2-СН2-;
или его фармацевтически приемлемые соли.
2. Соединение по п.1, в котором G является -СН2-.
3. Соединение по любому из пп.1 или 2, в котором Y2 и Y3 оба являются -Н.
4. Соединение по любому из пп.1-3, в котором по крайней мере один из R1 и R2 является -ОН.
5. Соединение по любому из пп.1-4, в котором R3 является Н.
6. Соединение по любому из пп.1-5, в котором Y1 является -Н.
7. Соединение по п.2, в котором один из R1 и R2 является -ОН и другой является -Н.
8. Соединение формулы (II)

где Rla является -Н, -ОН или F;
R2a является -Н, -СН3 или -ОСН3;
R3a является -Н или -СН3;
G является -СН2-, -СН2-СН2- или -СН2-СН2-СН2-;
или его фармацевтически приемлемые соли.
9. Соединение по любому из пп.1-8, в котором соединение имеет формулу IB или IС

или его фармацевтически приемлемые соли.
10. Соединение по любому из пп.1-8, в котором соединение имеет формулу ID или IE

или его фармацевтически приемлемые соли.
11. Соединение по п.1, в котором соединение имеет формулу
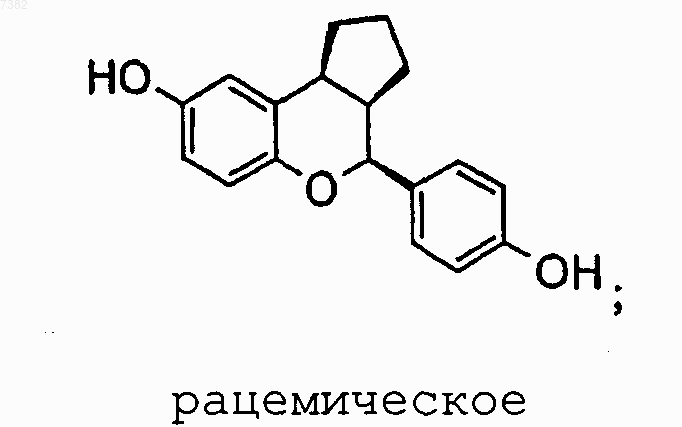
или его фармацевтически приемлемая соль или энантиомер.
12. Соединение по п.11, в котором соединение является (2S,3R,4S) энантиомером формулы
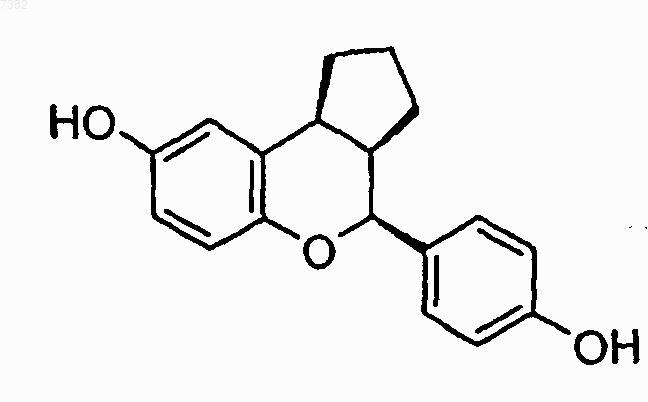
или его фармацевтически приемлемая соль.
13. Соединение по п.11, в котором соединение является (2R,3S,4R) энантиомером формулы
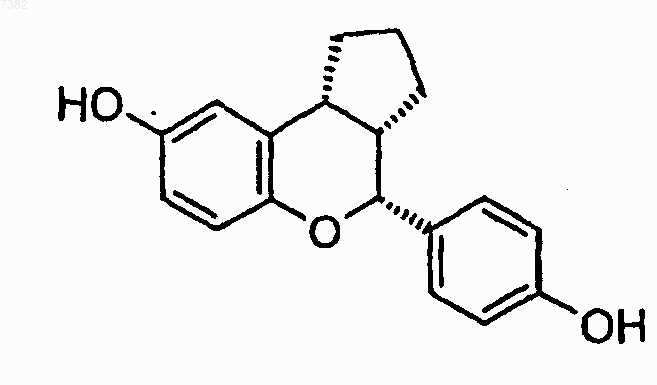
или его фармацевтически приемлемая соль.
14. Соединение по п.1, выбранное из группы, включающей
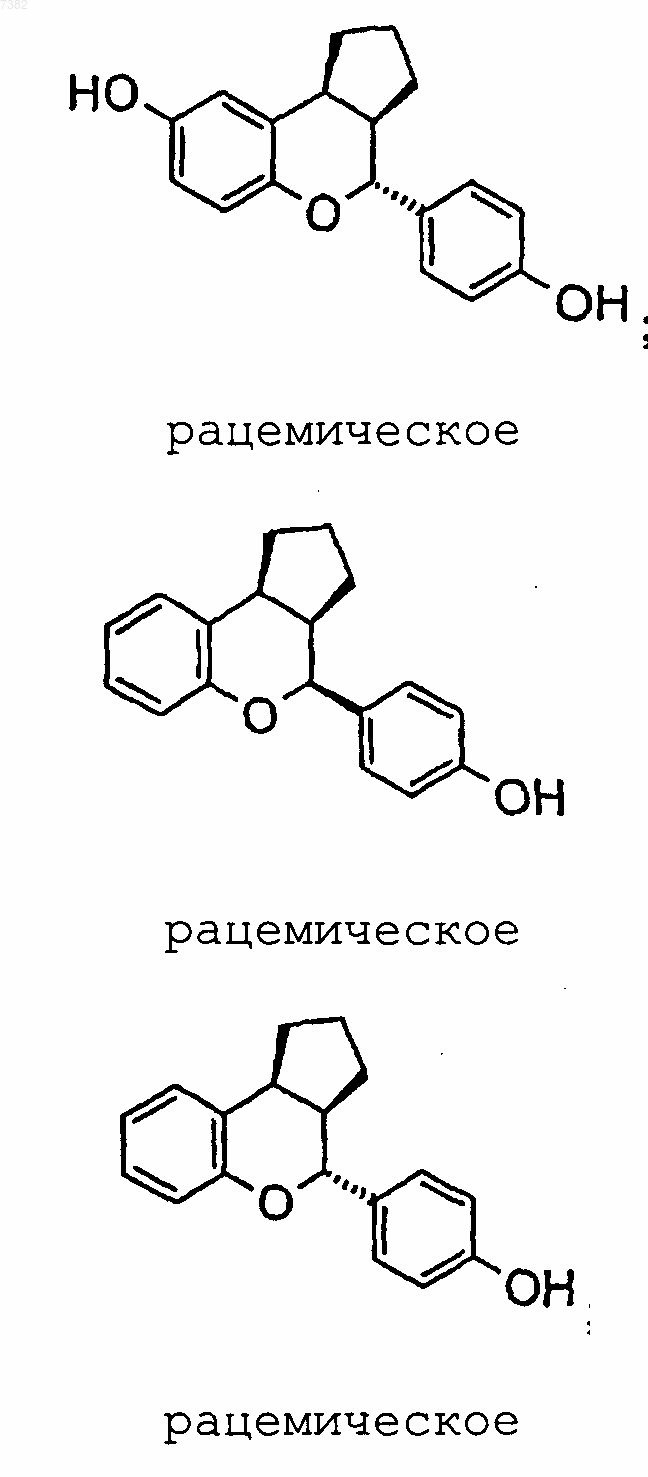
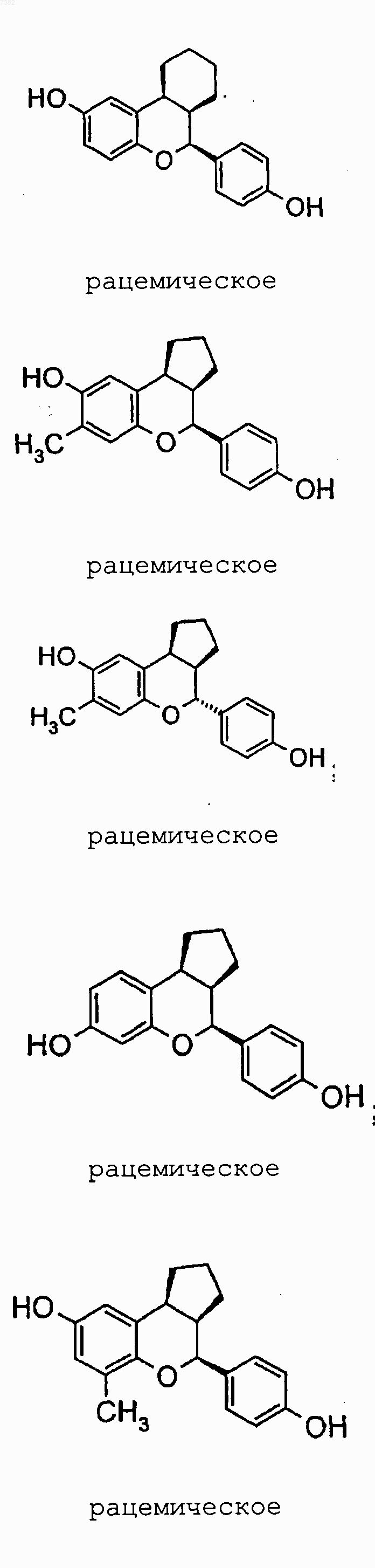
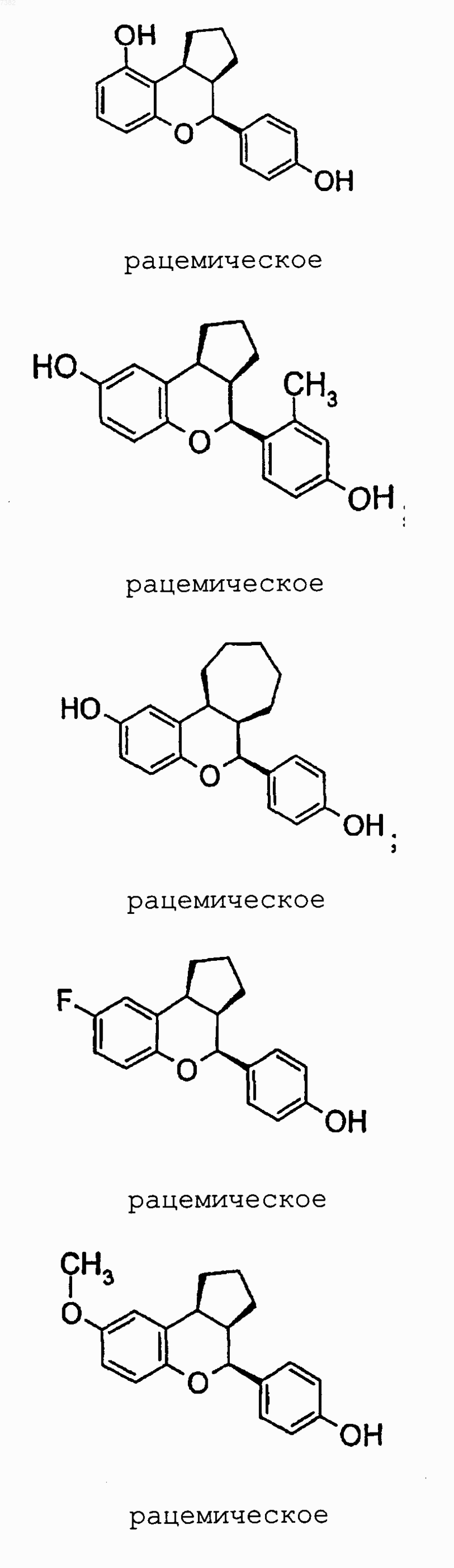
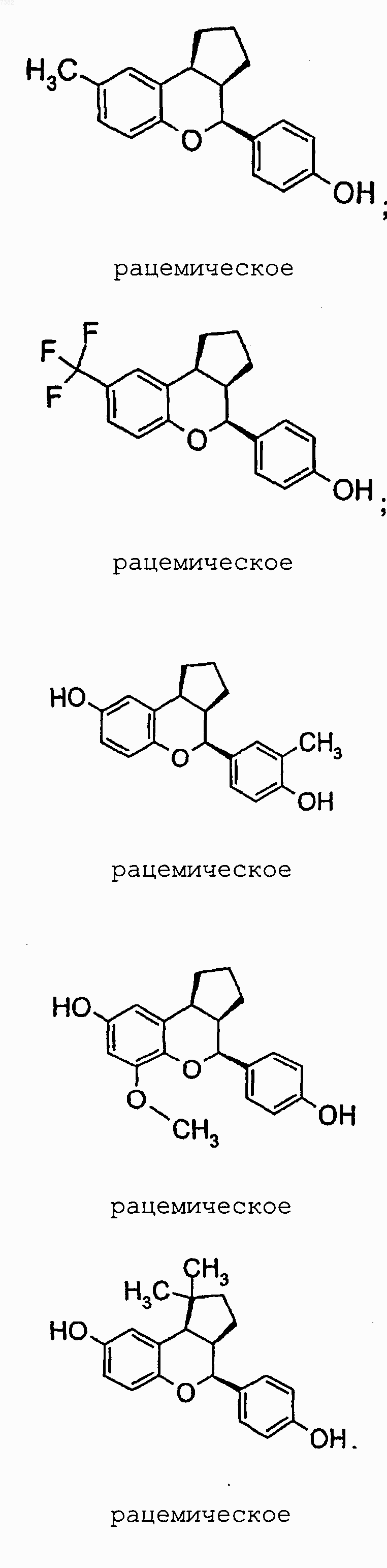
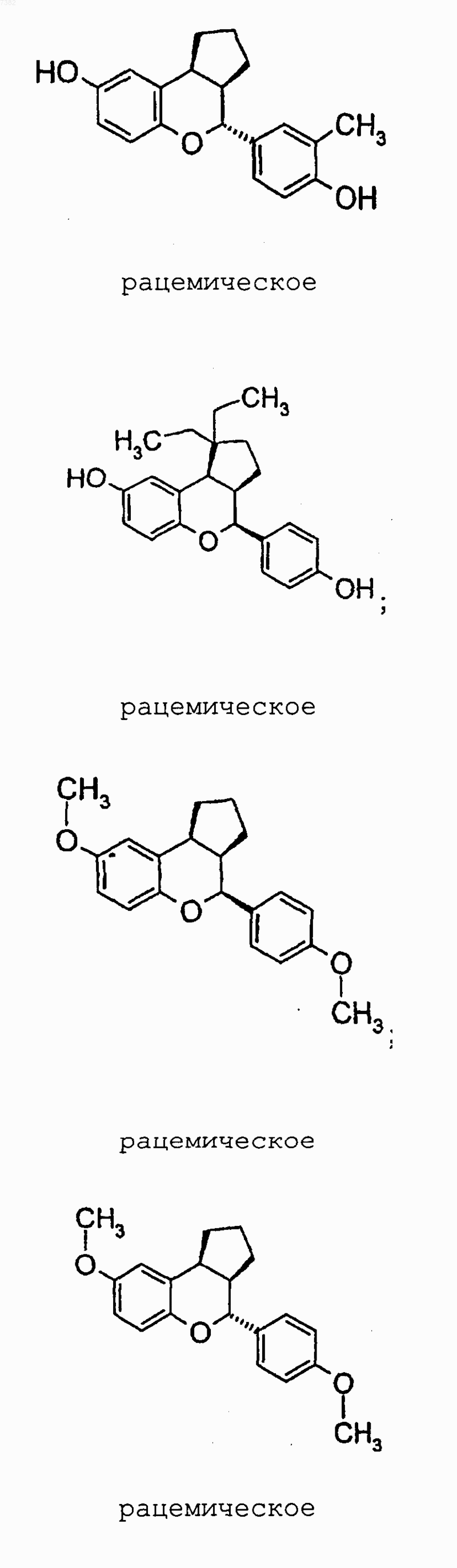
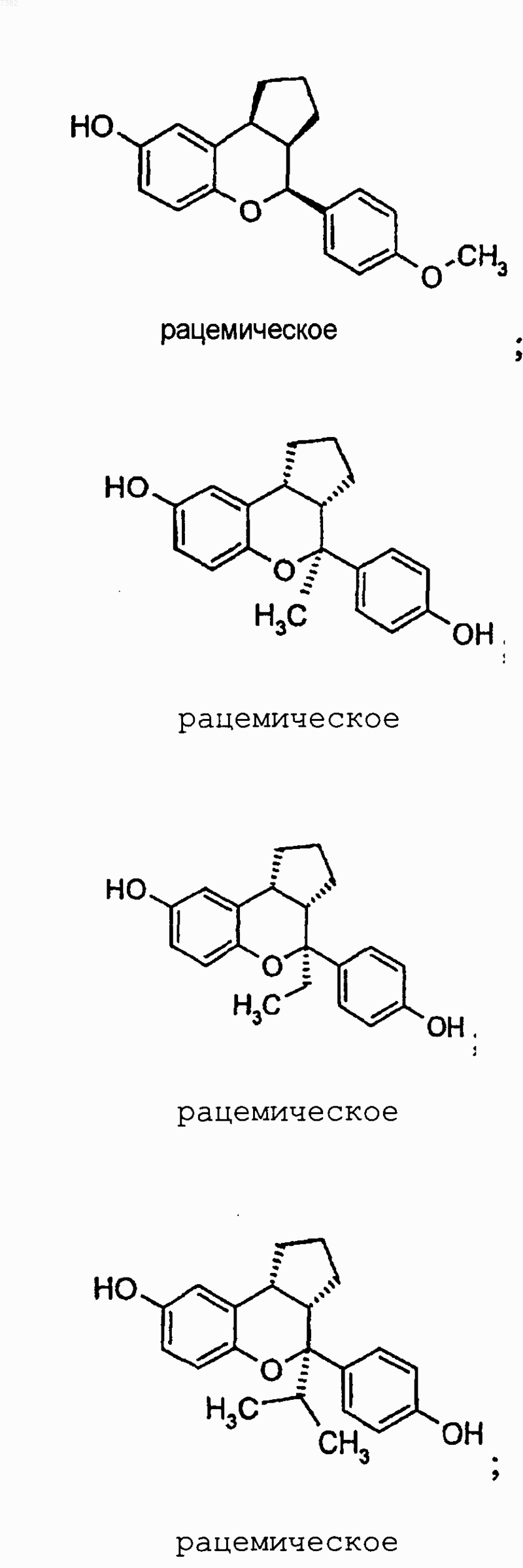
или их фармацевтически приемлемая соль или энантиомер.
15. Соединение формулы III
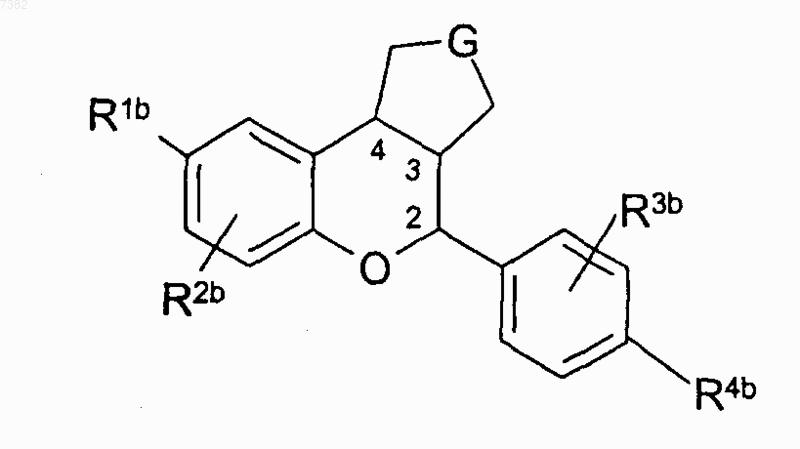
где Rlb является амидо или гидрокси;
R2b является -Н или C1-С6 алкилом;
R3b является -Н или C1-С6 алкилом;
R4b является амидо или гидрокси и
G является -СН2-, -СН2-СН2- или -СН2-СН2-СН2-;
или его фармацевтически приемлемые соли.
16. Соединение по п.15, в котором соединение имеет формулу
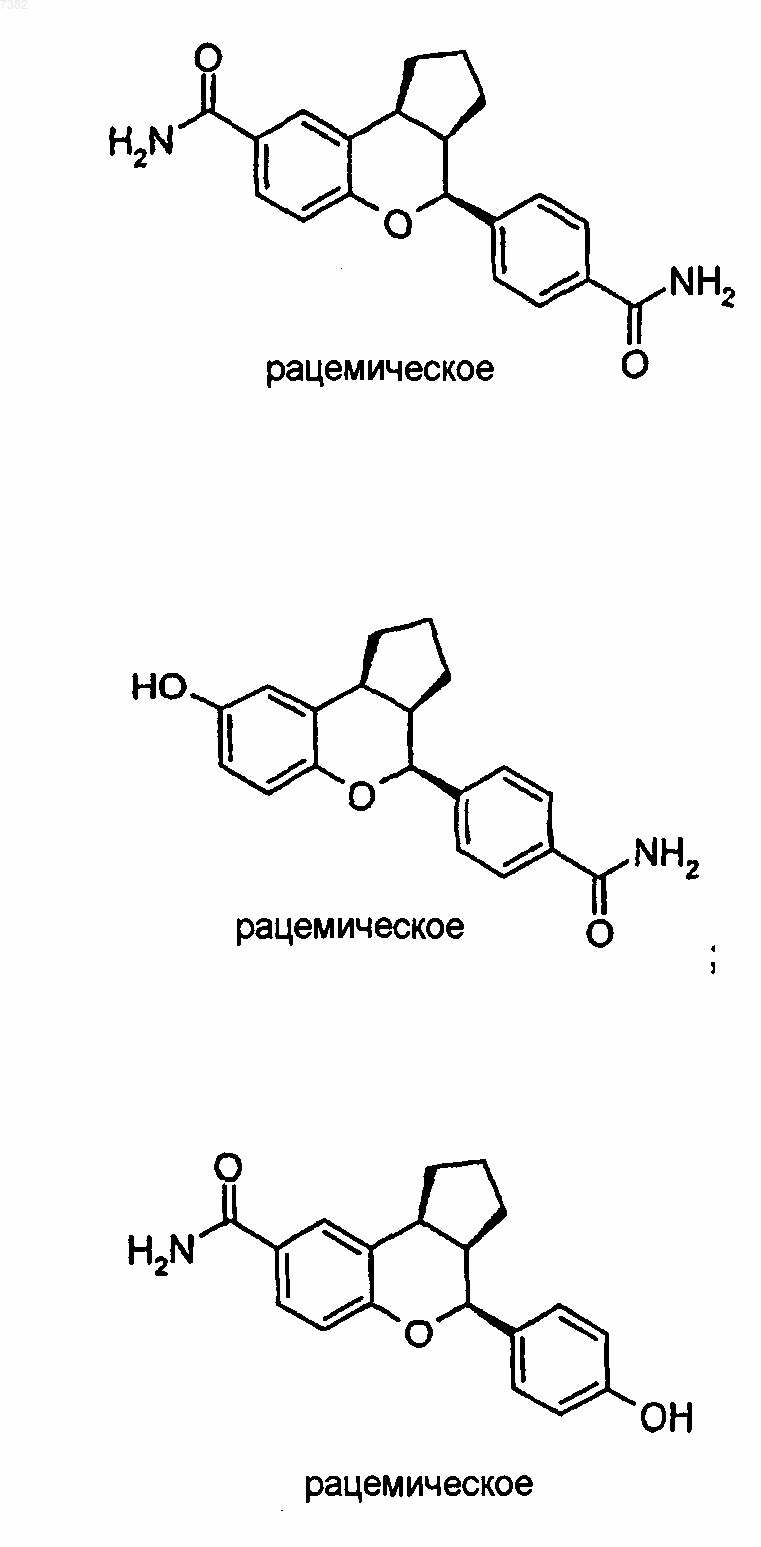
или его фармацевтически приемлемая соль или энантиомер.
17. Соединения, выбранные из группы, включающей
a) (+)-2-(4-гидроксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
b) (+)-2-(4-гидроксифенил)-6-трифторметилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
c) (+)-2-(4-гидроксифенил)-6-метилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
d) (+)-2-(4-гидроксифенил)-6-фторциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
e) (+)-2-(4-гидроксифенил)-5-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
f) (+)-2-(4-гидроксифенил)-7-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
g) (+)-2-(4-гидроксифенил)-6-гидрокси-8-метилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
h) (+)-2-(4-гидроксифенил)-6-гидроксициклогептил[с]3,4-дигидро-2Н-1-бензопиран,
i) (+)-2-(4-гидроксифенил)-6-гидрокси-8-метоксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
j) (+)-2-(4-гидроксифенил)-6-гидрокси-11,11-диметилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
k) (+)-2-(4-гидроксифенил)-6-гидрокси-11,11-диэтилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
l) (+)-2-(4-гидроксифенил)-6-метоксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
m) (+)-2-(4-гидрокси-3-метилфенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
n) (+)-2-(2-метил-4-гидроксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
o) (+)-2-(4-гидроксифенил)циклопентил[с]3,4-дигидро-2Н-1-бензопиран,
р) (+)-2-(4-гидроксифенил)-6-гидрокси-7-метилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
q) (+)-2-(4-гидроксифенил)-6-гидроксициклогексил[с]3,4-дигидро-2Н-1-бензопиран,
r) (+)-2-(4-метоксифенил)-6-метоксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
s) (+)-2-(4-аминокарбонилфенил)-6-аминокарбонилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
t) (+) -2-(4-аминокарбонилфенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
u) (+)-2-(4-гидроксифенил)-6-аминокарбонилциклопентил[с]3,4-дигидро-2Н-1-бензопиран,
v) (+)-2-(4-метоксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
w) (+)-2-метил-2-(4-гидроксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
х) (+)-2-этил-2-(4-гидроксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
у) (+)-2-(1-метилэтил)-2-(4-гидроксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2Н-1-бензопиран,
и их фармацевтически приемлемые соли или энантиомеры.
18. Фармацевтическая композиция, содержащая соединение по любому из пп.1-17 и фармацевтически приемлемый носитель.
19. Способ селективного связывания с бета-рецептором эстрогена у пациента, нуждающегося в этом, включающий введение указанному пациенту терапевтически эффективного количества соединения по любому из пп.1-17.
Текст
007382 Уровень техники Данное изобретение относится к новым циклоалкилбензопиранам и их производным, композициям,содержащим указанные соединения, их применению в качестве селективных агонистов бета-рецептора эстрогена и их применению при лечении медиированных бета-рецептором эстрогена заболеваний, таких как рак простаты, доброкачественная гиперплазия простаты, рак яичек, рак яичников, рак легких, сердечно-сосудистые заболевания, нейродегенеративные заболевания, недержание мочи, расстройства центральной нервной системы (ЦНС), расстройства желудочно-кишечного тракта (ЖКТ) и остеопороз. Эстрогены играют важную роль в развитии и гомеостазе репродуктивной, центральной нервной,скелетной и сердечно-сосудистой систем, как мужчин, так и женщин. Рецептор эстрогена (РЭ) в настоящее время является единственным членом стероидного подсемейства рецепторов ядра, который имеет различные подтипы. Недавно новая изоформа РЭ, РЭ-бета (также известная как РЭ-бета 1) была клонирована из библиотеки кДНК простаты крысы, она также присутствует в простате мышей и человека. Следовательно, предыдущий РЭ в настоящее время обозначен как РЭ-альфа. РЭ-альфа и РЭ-бета имеют высокий уровень гомологии по аминокислотам, имеют схожие афинности связывания с 17- Эстрадиолом(Е 2) и могут гетеро- или гомодимеризоваться с получением сигнального комплекса; Kuiper GG, et al.,Endocrinol. 138:863-70 (1997); Kuiper GG, et al., Proc. Natl. Acad. Sci. USA 93: 5925-30 (1996). Хотя Е 2 активирует как РЭ-альфа, так и РЭ-бета, РЭ-альфа стимулирует транскрипцию и пролиферацию клеток, а РЭ-бета подавляет активацию РЭ-альфа. Интересно, что 3-бета, 17-бета-андростандиол и 5-альфаандростан были предложены в качестве эндогенных лигандов для РЭ-бета; Weihua Z. et al., PNAS 98: 6330-5 (2001). 3-бета, 17-бета-андростандиол является основным метаболитом дигидротестостерона(ДГТ), 5-альфа-восстановленного активного внутриклеточного андрогена в мужских второстепенных половых органах. Активация РЭ-бета также стимулирует повышенную экспрессию глутатион Sтрансферазы и хинонредуктазы. Было продемонстрировано, что эти два фермента обладают хемозащитными детоксифицирующими свойствами; Chang WY et al., Prostate 40: 115-24 (1999); Montano MM et al.,J. Biol. Chem. 273: 25443-9 (1998). С учетом недавней идентификации РЭ-бета и признанием того, что РЭ-альфа и РЭ-бета играют различную биологическую роль, РЭ-селективные модуляторы будут также иметь значительное клиническое применение. Так как РЭ-бета в значительной степени экспрессируется в нескольких тканях, включая простату, мочевой пузырь, яичники, яички, легкие, тонкий кишечник, сосудистый эндотелий и различные части мозга, соединения, которые селективно модулируют РЭ-бета, будут иметь значительную клиническую важность при лечении различных болезненных состояний, таких как рак простаты, рак яичек,рак яичников, рак легких, сердечно-сосудистые заболевания, нейродегенеративные расстройства, недержание мочи, расстройства ЦНС, расстройства ЖК тракта и остеопороз. Такие соединения будут оказывать минимальное влияние на ткани, которые содержат РЭ-альфа, и, таким образом, иметь различные профили побочного действия. Таким образом, агонисты РЭ-бета будут демонстрировать терапевтические профили, отличные от терапевтических профилей антагонистов или агонистов РЭ-альфа, и будут особенно предпочтительны в тканях, реагирующих на передачу сигналов РЭ-бета. Железа простаты производит компоненты, которые были найдены в семени и крови. Некоторые из них являются регуляторными пептидами. Железа простаты включает клетки стромы и эпителия, где последние состоят из столбчатых секреторных клеток и базальных несекреторных клеток. Пролиферация таких базальных клеток, а также клеток стромы увеличивает доброкачественную гиперплазию простаты(ДГП), которая является одним из наиболее распространенных заболеваний простаты. ДГП является прогрессирующим состоянием, которое характеризуется узелковым увеличением ткани простаты, что приводит к закупорке уретры. Это, в свою очередь, приводит к увеличению частоты мочеиспускания, нонкурии, плохому току мочи и приостановке или задержке мочеиспускания. Последствия ДГП могут включать гипертрофию гладкой мышцы мочевого пузыря, декомпенсацию мочевого пузыря и увеличению случаев инфицирования мочевых путей. Развитие ДГП считается неизбежным явлением для пожилого мужского населения. ДГП наблюдается у приблизительно 70% мужчин в возрасте старше 70 лет. Лекарственное лечение ДГП в настоящее время включает альфа адренергические антагонисты для облегчения симптомов или стероидные ингибиторы 5-альфа редуктазы для снижения объема гиперплазической ткани. Такие подходы дают ограниченный терапевтический эффект. Смертность вследствие рака простаты при применении стратегии ожидания под наблюдением достаточно мала (9-15%) у мужчин, которые имеют локализованные опухоли. Однако эти показатели относятся к пациентам, которые имеют локализованное заболевание; они не обязательно применимы к более молодым мужчинам с повышенным риском. Более молодые мужчины с опухолями на стадии Т 1 а имеют более длительный предполагаемый период риска по сравнению с более старшими мужчинами с той же стадией заболевания, и поэтому являются более вероятными кандидатами для потенциального полезного лечения. При изучении ожидания под наблюдением высокие показатели развития заболевания (34-80%) показали, что некоторые клинически очевидные раковые опухоли простаты являются дремлющими. Краткое описание изобретения Данное изобретение относится к новым производным бензопирана формулы (I) или производным формулы II где R1, R2, R3 и R4, каждый независимо является -Н, C1-С 6 алкилом, -ОН, C1-С 6 алкокси, галогеном,амидо или -CF3;R5 является водородом или C1-С 6 алкилом;G является -СН 2-, -СН 2-СН 2- или -СН 2-СН 2-СН 2-; или их фармацевтически приемлемые соли. Соединения в соответствии с данным изобретением включают следующие, которые не должны считаться ограничивающими каким-либо образом, соединения, включенные в объем данного изобретения:-2-(1-метилэтил)-2-(4-гидроксифенил)-6-гидроксициклопентил[с]3,4-дигидро-2 Н-1-бензопиран и их фармацевтически приемлемые соли или энантиомеры. Во втором варианте воплощения данное изобретение представляет фармацевтическую композицию,содержащую терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель. В другом варианте воплощения данное изобретение представляет медицинские способы применения соединений формулы (I) в качестве агонистов бета-рецептора эстрогена (РЭ), кроме того применяемым для лечения медиированных РЭ-бета заболеваний, таких как рак простаты, доброкачественная гиперплазия простаты, рак яичек, сердечно-сосудистые заболевания, нейродегенеративные заболевания,недержание мочи, расстройства центральной нервной системы (ЦНС), расстройства желудочнокишечного (ЖК) тракта и остеопороза.-2 007382 Подробное описание изобретения В данной заявке:a) термин амидо относится к аминокарбонильной (-C(O)NH2) группе;b) термин галоген относится к атому фтора, атому хлора, атому брома или атому йода;b) термин C1-С 6 алкил относится к алкильному радикалу с прямой или разветвленной цепью, содержащему от 1 до 6 атомов углерода, такому как метил, этил, н-пропил, изопропил, н-бутил, изобутил,втор-бутил, трет-бутил, пентил, гексил и т.д.;c) термин C1-С 6 алкокси относится к алкоксильной группе с прямой или разветвленной цепью,содержащей от 1 до 6 атомов углерода, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси,изобутокси, втор-бутокси, трет-бутокси, пентокси, гексокси и т.д.; относится к связи, для которой стереохимия не обозначена;d) обозначение относится к связи, которая выдается вперед от плоскости страницы; е) обозначениеf) обозначениеобозначает связь, которая выдается назад от плоскости страницы;g) в примерах приготовления и примерах следующие термины имеют указанные значения: нг обозначает нанограммы; мкг обозначает микрограммы; мг обозначает миллиграммы; г обозначает граммы; кг обозначает килограммы; нмоль обозначает наномоли; ммоль обозначает миллимоли; моль обозначает моли; мкл обозначает микролитры; мл обозначает миллилитры; л обозначает литры; Rf обозначает коэффициент удерживания; С обозначает градусы Цельсия; т.к. обозначает температуру кипения; мм рт.ст. обозначает миллиметры ртутного столба; т.п. обозначает температуру плавления; разл. обозначает разложение; []2D0 обозначает удельное вращение D линии натрия при 20 С, полученное в 1 дециметровой ячейке; к обозначает концентрацию в г/мл; нМ обозначает наномолярную концентрацию; мкМ обозначает микромолярную концентрацию; мМ обозначает миллимолярную концентрацию; М обозначает молярную концентрацию; Ki обозначает константу ингибирования; Kd обозначает константу диссоциации; ф/д 2 обозначает фунты на квадратный дюйм; об/мин обозначает обороты в минуту; ВЭЖХ обозначает высокоэффективную жидкостную хроматографию; МСВР обозначает масс-спектр с высоким разрешением; ТГФ обозначает тетрагидрофуран; солевой раствор обозначает насыщенный водный раствор хлорида натрия; ППС обозначает потеря при сушке; мкКи обозначает микрокюри; в.б. обозначает внутрибрюшинно; в.в. обозначает внутривенно и разл./мин обозначает разложение в минуту; понимают то, что метил присоединен в положении 1 и заместитель или заместители, представленные R, могут быть присоединены в любом из положений 2, 3, 4 или 6; относится к фенилу или замещенному фенилу и понятно, что любой из двух заместителей может быть присоединен в любом положении 1, 2, 3, 4, 5 или 6. Также понятно, что если один из заместителей присоединен в положении 1, другой заместитель, представленный R, может быть присоединен в любом положении 2, 3, 4, 5 или 6, что если один из заместителей присоединен в положении 2, другой заместитель, представленный R, может быть присоединен в любом положении 1, 3, 4, 5 или 6, что если один из заместителей присоединен в положении 3, другой заместитель, представленный R, может быть присоединен в любом положении 1, 2, 4, 5 или 6, что если один из заместителей присоединен в положении 4,другой заместитель, представленный R, может быть присоединен в любом положении 1, 2, 3, 5 или 6, что если один из заместителей присоединен в положении 5, другой заместитель, представленный R, может быть присоединен в любом положении 1, 2, 3, 4 или 6, и что если один из заместителей присоединен в положении 6, другой заместитель, представленный R, может быть присоединен в любом положении 1, 2,3, 4 или 5;j) система нумерации и название трициклической кольцевой системы формулы (I) и формулы (II) таковы если G является -СН 2 циклопентил[с]3,4-дигидро-2 Н-1-бензопиран,-3 007382 если G является -СН 2-СН 2 циклогексил[с]3,4-дигидро-2 Н-1-бензопиран,если G является -СН 2-СН 2-СН 2 циклогептил[с]3,4-дигидро-2 Н-1-бензопиран,k) термин энантиомерный избыток или эи обозначает процент, в котором один энантиомер, Е 1,находится в избытке в смеси двух энантиомеров, Е 1 и Е 2, таков, что (Е 1-Е 2)(Е 1+Е 2)х 100=эи. Соединения, применяемые в способе в соответствии с данным изобретением, могут иметь один или более асимметрических центров. В результате существования таких хиральных центров соединения данного изобретения могут существовать в виде рацематов и в виде отдельных энантиомеров, а также в виде диастереомеров и смесей диастереомеров. Все асимметрические формы, отдельные изомеры и их сочетания входят в объем данного изобретения. Три основных хиральных центра, обозначенных как 2, 3 и 4,показаны в формуле (I). Предпочтительной относительной стереохимией соединений формулы (I) является такая, при которой все хиральные центры 2, 3 и 4 находятся в цис-конфигурации, как показано формулами IB и IС ниже В целях данного изобретения соединение, обозначенное IB рацемическое или IС рацемическое или их формулы, обозначают рацемическую структуру соединения IB и IС. Также для целей данного изобретения соединение, обозначенное ID рацемическое или IE рацемическое или их формулы, показанные ниже, обозначают рацемическую структуру соединения ID или IE. Для предпочтительного получения одного оптического изомера по отношению к его энантиомеру можно применять множество методов. В качестве примера, может быть получена смесь энантиомеров, и затем два энантиомера могут быть разделены. Широко применяемым методом разделения рацемической смеси является применение хиральной жидкостной хроматографии высокого давления. Более подробно разделение энантиомерных смесей описано в J. Jacques, et al., Enantiomers, Racemates, and Resolutions,(1991). Термин их фармацевтически приемлемые соли относится либо к кислотно-аддитивным солям,либо к основно-аддитивным солям. Выражение фармацевтически приемлемые кислотно-аддитивные соли применяется к любым нетоксичным органическим или неорганическим кислотно-аддитивным солям основных соединений, представленных формулой (I). Иллюстративными примеры неорганических кислот, которые образуют подходящие соли, включают хлористо-водородную, бромисто-водородную, серную и фосфорную кислоты и кислые соли металлов, такие как моногидроортофосфат натрия и гидросульфат калия. Иллюстративные примеры органических кислот, которые образуют подходящие соли, включают моно-, ди- и трикарбоновые кислоты. Иллюстративными примерами таких кислот являются, например, уксусная, гликолевая,молочная, пировиноградная, малоновая, янтарная, глутаровая, фумаровая, яблочная, винная, лимонная,аскорбиновая, малеиновая, гидроксималеиновая, бензойная, гидроксибензойная, фенилуксусная, коричная, салициловая, 2-феноксибензойная, п-толуолсульфоновая кислоты и сульфоновые кислоты, такие как бензолсульфокислота, метансульфокислота и 2-гидроксиэтансульфокислота. Такие соли могут сущест-4 007382 вовать либо в гидратированной, либо в практически безводной форме. В общем, кислотно-аддитивные соли соединений в соответствии с данным изобретением растворимы в воде и различных гидрофильных органических растворителях и, в отличие от их свободных оснований, обычно имеют более высокие температуры плавления. Выражение фармацевтически приемлемые основно-аддитивные соли применяется к любым нетоксичным органическим или неорганическим основно-аддитивным солям соединений, представленных формулой (I). Иллюстративные примеры оснований, которые образуют подходящие соли, включают гидроксиды щелочных металлов или щелочно-земельных металлов, такие как гидроксиды натрия, калия,кальция, магния или бария; аммиак и алифатические, алициклические или ароматические органические амины, такие как метиламин, диметиламин, триметиламин и пиколин. С этими соединениями могут быть получены либо моно-, либо двухосновные соли. Ниже представлены предпочтительные варианты соединений формулы (I):(4) предпочтительны соединения, в которых один из R1 и R2 является -ОН;(7) предпочтительны соединения, в которых один из R1 и R2 является -ОН и другой является -Н. Понятно, что более предпочтительные варианты соединений формулы (I) могут быть выбраны в соответствии с перечисленными выше вариантами. Например, ограничения (1) могут быть объединены с ограничениями (2); ограничения (3) могут быть объединены с ограничениями (4); ограничения (1), (2),(3), (5), (6) и (7) могут быть объединены и т.д. В другом варианте данное изобретение относится к соединениям формулы IIIG является -СН 2-, -СН 2-СН 2- или -СН 2-СН 2-СН 2-,и или их фармацевтически приемлемым солям. В другом варианте данное изобретение относится к соединениям формулы IV где Rlb является амидо или гидрокси;R4b является амидо или гидрокси иG является -СН 2-, -СН 2-СН 2- или -СН 2-СН 2-СН 2-; или их фармацевтически приемлемым солям. Иллюстративные примеры соединений, входящих в объем данного изобретения, включают рацемические смеси и конкретные энантиомеры следующих соединений: Схемы реакций Соединения формулы (I) и их промежуточные соединения могут быть получены как показано на схемах реакций A-D ниже. Все заместители, если не указано иначе, такие как определены выше. Реагенты и исходные материалы легко доступны специалисту в данной области техники. В данной схеме R1', R2', R3' и Y1' соответствуют заместителям R1, R2, R3 и Y1, соответственно, за исключением того случая, когда R1, R2 и R3 заместители являются гидрокси и Y1 заместитель является -Н(что делает -O-Y1 группу гидрокси). В этих случаях соответствующую гидроксигруппу защищают алкоксиметиловым простым эфиром, таким как метоксиметил (MOM) или метоксиэтоксиметил (МЭМ). В реакционной схеме А, стадия 1 а, гидроксигруппы фенола формулы (2) защищают подходящей защитной группой с получением защищенного фенола формулы (4), применяя методы и методики, хорошо известные специалисту в данной области техники. Например, фенол формулы (2) объединяют с суспензией, содержащей подходящий безводный растворитель, такой как безводный диметилформамид(ДМФ) и подходящее сильное основание, такое как гидрид металла, наиболее предпочтительно, гидрид натрия. К этой суспензии добавляют некоторое количество хлорида простого алкоксиметилового эфира,предпочтительно, МOМ-Сl, которое соответствует приблизительно эквимолярному количеству в зависимости от количества гидроксигрупп, которые должны быть защищены в феноле формулы (2). Реакцию проводят при комнатной температуре в течение от около 30 мин до около 2 дней. Затем реакцию гасят водой и подходящим простым эфиром, таким как диэтиловый эфир или EtOAc, и органический слой промывают подходящим основанием, таким как гидроксид натрия или NaНСО 3 и солевым раствором. Защищенный фенол формулы (4) может быть выделен и очищен методами, хорошо известными в данной области техники, такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. На схеме А, стадия 1b, 2-оксоциклоалканкарбоксилат формулы (3) активируют через трифлат с получением активированного карбоксилата циклоалкана формулы (5), применяя методы и методики, хорошо известные в данной области техники; G.T. Crisp et al., J. Org. Chem. 57, 6972-6975 (1992). Например,метил-2-оксоциклоалканкарбоксилат формулы (3) растворяют в безводных условиях в подходящем растворителе, таком как тетрагидрофуран, дихлорметан, ацетон, этилацетат, толуол или диэтиловый эфир, и-8 007382 подвергают взаимодействию с подходящим активирующим агентом, таким как ангидрид трифлата. Реакцию проводят в присутствии основания, такого как N-метилморфолин, карбонат натрия, триэтиламин,N,N-диизопропилэтиламин, карбонат калия, бикарбонат натрия, пиридин и 2,6-ди-трет-бутил-4-метилпиридин. Реакцию обычно проводят при температурах от -78 С до температуры окружающей среды. Обычно реакция занимает от 1 до 24 ч. Затем реакция может быть погашена. Продукт формулы (5) может быть выделен и очищен методами, хорошо известными в данной области техники, такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. На схеме А, стадия 2, защищенный фенол формулы (4) сочетают с активированным карбоксилатом циклоалкана формулы (5) с получением продукта сочетания формулы (6). Например, реакцию сочетания проводят в присутствии бутиллития, хлорида цинка и соединений Pd. Предпочтительно, реакцию проводят в подходящем растворителе, таком как тетрагидрофуран (ТГФ), и она может начинаться в безводных условиях. Предпочтительно, защищенный фенол формулы (4) растворяют в подходящем растворителе,таком как ТГФ, обрабатывают бутиллитием при пониженной температуре, затем добавляют хлорид цинка в растворителе и температуру повышают до температуры окружающей среды. Соединения палладия,такие как тетракис(трифенилфосфин)Pd(0), добавляют вместе с активированным карбоксилатом циклоалкана формулы (5) и температуру предпочтительно повышают до температуры кипения с обратным холодильником растворителя в течение от 6 до 24 ч. Продукт сочетания формулы (6) может быть выделен и очищен методами, хорошо известными в данной области техники, такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. На схеме А, стадия 3, продукт сочетания формулы (6) восстанавливают подходящим восстанавливающим агентом с получением восстановленного продукта формулы (7) с применением методов и методик, хорошо известных в данной области техники. Например, продукт сочетания формулы (6) подвергают взаимодействию с подходящим восстанавливающим агентом, таким как соединения палладия, предпочтительно 5 или 10% палладием на угле, в подходящем растворителе или смеси растворителей, таком как метанол. Реакцию предпочтительно проводят в присутствии подходящего основания, такого как триалкиламин, более предпочтительно триэтиламин. Затем реакционной смеси дают нагреться до температуры от около 30 С до температуры кипения с обратным холодильником в течение от около 2 до 24 ч. Восстановленный продукт формулы (7) может быть выделен и очищен методами, хорошо известными в данной области техники, такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. На схеме А, стадия 4, восстановленный продукт формулы (7) может быть превращен в амид Вейнреба формулы (8). Эта реакция может быть проведена с применением реагента такого типа, как описан уJ.M. Williams, et al., Tetrahedron Letters 36, 5641-5464 (1995). Например, восстановленный продукт формулы (7) объединяют с гидрохлоридом N,О-диметилгидроксиламина в подходящем апротонном растворителе, таком как тетрагидрофуран, предпочтительно в безводных условиях и охлаждают до температуры от около 0 до около -30 С, более предпочтительно до около -10 С. Затем добавляют подходящий реактив Гриньяра, предпочтительно изопропилхлорид магния, в молярном соотношении около 1,5, и реакционную смесь перемешивают в течение от около 15 мин до 2 ч. Затем реакцию гасят источником протонов, таким как, например, насыщенный хлорид аммония. Амид Вейнреба формулы (8) может быть выделен и очищен методами, хорошо известными в данной области техники, такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. На схеме А, стадия 5, амид Вейнреба формулы (8) объединяют с ариллитием формулы (9) с получением кетона формулы (10). Например, ариллитий формулы (9) добавляют к раствору амида Вейнреба формулы (8) в подходящем апротонном растворителе, таком как безводный ТГФ, охлаждают до температуры от около -20 до около 5 С, предпочтительно 0 С, и перемешивают в течение от около 15 мин до 3 ч. Затем реакцию гасят источником протонов, таким как, например, насыщенный бикарбонат натрия. Кетон формулы (10) может быть выделен и очищен методами, хорошо известными в данной области техники,такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. На схеме А, стадия 6 а или 6b, кетон формулы (10) подвергают катализируемой кислотой циклизации с последующим восстановлением полученного полукеталя с получением соединения формулы (IA или IA'), которое представляет собой рацемическую смесь соединения формулы (I). Например, на стадии 6 а п-толуолсульфокислоту добавляют в приблизительно эквимолярной пропорции к кетону формулы(10) в подходящем спиртовом растворителе, таком как безводный метанол. Затем смесь нагревают до температуры от около 40 до 60 С, предпочтительно до 50 С, в течение от 12 до 24 ч, предпочтительно 18 ч. Затем реакцию охлаждают до температуры окружающей среды и добавляют подходящий восстанавливающий агент, такой как цианоборгидрид натрия, вместе с подходящим индикатором, таким как зеленый бромкреозол, по методике, описанной у А. Srikrishna, et al., Tetrahedron, том 51,11, стр. 3339-3344, 19 95. Затем медленно добавляют метанол, насыщенный хлористо-водородной кислотой, пока сохраняется желтый цвет. Реакцию перемешивают в течение от около 1 до 2 ч после окончательного изменения цвета. Затем реакцию гасят подходящим акцептором протонов, таким как насыщенный бикарбонат натрия. Такие условия для стадии 6 а дают цис-конфигурацию хиральных центров (например, соединения IB илиIС). Условия R3SiH/TFA для стадии 6b дадут транс-конфигурацию хиральных центров (например, соединения ID или IE). Продукт формулы (IA) или (IA') затем может быть выделен и очищен методами,хорошо известными в данной области техники, такими как экстракция, выпаривание, растирание, хроматография и перекристаллизация. Альтернативно, продукт сочетания формулы (6) может быть синтезирован, как описано на схеме реакции В. Все заместители, если не указано иначе, такие как определены выше. Реагенты и исходные материалы легко доступны специалисту в данной области техники. Схема В На схеме В, стадия 1, гидроксигруппы бромфенола формулы (11) защищают подходящей защитной группой с получением защищенного бромфенола формулы (12), применяя методы и методики, описанные для схемы А, стадия 1 а. На схеме В, стадия 2, защищенный бромфенол формулы (12) сочетают с активированным карбоксилатом циклоалкана формулы (5) с получением продукта сочетания формулы (6) методами и методиками, описанными для схемы А, стадия 2. Альтернативный метод получения конкретных бром-замещенных соединений описан на схеме С. Схема С Кроме того, определенные соединения формулы (I), в которых Y1 является метилом, могут быть получены по схеме D. Схема D Кроме того, амидосоединения формулы (II), такие, как показаны формулами (16) и (17), могут быть синтезированы как описано на схеме Е. Все заместители, если не указано иначе, такие как определены выше. Реагенты и исходные материалы легко доступны специалисту в данной области техники. На схеме Е, стадия 1, дигидрокси соединение формулы (13) может быть превращено в смесь монотрифлата формулы (14) и дитрифлата формулы (15). Полученная смесь может быть выделена с помощью обычной хроматографии. На схеме Е, стадия 2, монотрифлат формулы (14) и дитрифлат формулы (15) подвергают перекрестному сочетанию в катализируемых палладием условиях карбонилирования с 1,1,1,3,3,3 гексаметилдисилилазаном с получением карбоксамидов формул (16) и (17). Кроме того, амидосоединение формулы (19) может быть синтезировано, как описано на схеме F. Все заместители, если не указано иначе, такие как определены выше. Схема F Реагенты и исходные материалы легко доступны специалисту в данной области техники. На схемеF, стадия 1, дигидрокси формулы (13) может быть селективно превращен в простой бензиловый эфир формулы (18). На схеме F, стадия 2, оставшийся фенол превращают в трифлат, затем немедленно подвергают перекрестному сочетанию в условиях, таких же, как и для схемы Е, стадии 2. Наконец, бензильную группу удаляют с получением карбоксамида формулы (19) после ВЭЖХ очистки. Кроме того, соединения, в которых R5 является C1-С 6 алкилом, могут быть получены, как описано на схеме G. Схема G На схеме G кетон формулы (10) подвергают взаимодействию с алкилметаллорганическим соединением, таким как метиллитий или этилбромид магния, с получением третичных спиртов формулы (20). В кислых условиях, описанных для схемы А, стадия 6 а, третичные спирты образуют бензопираны формулы (21). Пример получения 1- 11007382 Суспензию гидрида натрия (60% в минеральном масле, 3,81 г, 95,45 ммоль) в безводном ДМФ (50 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор гидрохинона(5,0 г, 4 5,45 ммоль) в безводном ДМФ (50 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (7,2 мл, 95,45 ммоль) с отмеченным дополнительным газовыделением. Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэшхроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 1 (5,64 г,63%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,97 (с, 4 Н), 5,11 (с, 4 Н), 3,47 (c, 6 Н). Пример получения 2 Суспензию гидрида натрия (60% в минеральном масле, 0,67 г, 16,67 ммоль) в безводном ДМФ (25 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор трифторметил-п-крезола (2,50 г, 15,15 ммоль) в безводном ДМФ (25 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (1,3 мл, 16,67 ммоль). Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 2 (2,50 г, 80%) в виде прозрачного масла. 1 Суспензию гидрида натрия (60% в минеральном масле, 0,89 г, 22,17 ммоль) в безводном ДМФ (25 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор гваякола (2,50 г, 20,16 ммоль) в безводном ДМФ (25 мл). К этой суспензии по каплям добавляют метоксиметилхлорид(1,7 мл, 22,17 ммоль). Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 3 (2,22 г, 66%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,97-6,89 (м, 4 Н), 5,01 (с, 2 Н), 3,89 (с, 3 Н), 3,22 (с, 3 Н). Пример получения 4 Суспензию гидрида натрия (60% в минеральном масле, 0,41 г, 10,30 ммоль) в безводном ДМФ (25 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор 2-бром-4 метилфенола (2,50 г, 14,71 ммоль) в безводном ДМФ (25 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (0,78 мл, 10,30 ммоль). Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 4 (2,45 г, 72%) в виде прозрачного масла. Пример получения 5 Суспензию гидрида натрия (60% в минеральном масле, 0,58 г, 14,40 ммоль) в безводном ДМФ (25 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор 2-бром-4 фторфенол (2,50 г, 13,09 ммоль) в безводном ДМФ (25 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (1,1 мл, 14,40 ммоль). Реакционной смеси дают нагреться до температуры окружаю- 12007382 щей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 5 (2,71 г, 88%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,40-7,35 (м, 1 Н), 7,01-6,89 (м, 1 Н), 6,85-6,79 (м, 1 Н), 4,99 (с, 2 Н), 3,87 (с, 3 Н). Пример получения 6 Суспензию гидрида натрия (60% в минеральном масле, 1,90 г, 47,68 ммоль) в безводном ДМФ (25 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор резорцинола(2,50 г, 22,70 ммоль) в безводном ДМФ (25 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (3,6 мл, 47,68 ммоль) с отмеченным дополнительным газоотделением. Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэшхроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 6 (2,49 г,55%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,20 (т, J=8,2, 1H), 6,74-6,68 (м, 3 Н), 5,16 (с, 4 Н), 3,48 (с, 6 Н). МС рассчитанный 198,2; МС (М+1) 199,0. Пример получения 7 Суспензию гидрида натрия (60% в минеральном масле, 1,11 г, 27,78 ммоль) в безводном ДМФ (25 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор 4 бромрезорцина (2,50 г, 13,22 ммоль) в безводном ДМФ (25 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (2,1 мл, 27,78 ммоль) с отмеченным дополнительным газоотделением. Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэшхроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 7 (2,46 г,67%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,40 (д, J=7,8, 1H), 6,87 (д, J=2,7, 1H), 6,63 (дд, J=2,7, 7,8,1 Н), 5,22 (с, 2 Н), 5,14 (с,2 Н), 3,51 (с, 3 Н), 3,46 (с, 3 Н). МС рассчитанный 277,12; МС (М+1) 277,2, 279,2. Пример получения 8 Суспензию гидрида натрия (60% в минеральном масле, 1,58 г, 39,21 ммоль) в безводном ДМФ (50 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор 2,6 дибромгидрохинона (5,00 г, 18,67 ммоль) в безводном ДМФ (50 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (3,0 мл, 39,21 ммоль) с отмеченным дополнительным газоотделением. Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 8 (3,49 г, 53%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,23 (с, 2 Н), 5,10 (с, 4 Н), 3,46 (с, 6 Н). Суспензию гидрида натрия (60% в минеральном масле, 3,00 г, 74,92 ммоль) в безводном ДМФ (50 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор метоксигидрохинона (5,00 г, 35,67 ммоль) в безводном ДМФ (50 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (5,2 мл, 74,92 ммоль) с отмеченным дополнительным газоотделением. Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэшхроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 9 (5,84 г,72%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,05 (д, J=8,6, 1H), 6,63 (д, J=2,7, 1H), 6,55 (дд, J=9,0, 2,7, 1 Н), 5,14 (с, 2 Н), 5,12 (с,2 Н), 3,86 (с, 3 Н), 3,51 (с, 3 Н), 3,47 (с, 3 Н). Пример получения 10 Суспензию гидрида натрия (60% в минеральном масле, 3,54 г, 88,61 ммоль) в безводном ДМФ (100 мл) перемешивают в атмосфере азота при температуре 0 С и по каплям добавляют раствор 4-метоксифенол (10,00 г, 80,55 ммоль) в безводном ДМФ (50 мл). К этой суспензии по каплям добавляют метоксиметилхлорид (6,7 мл, 88,61 ммоль). Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 10 (11,55 г, 85%) в виде прозрачного масла. Пример получения 11 К суспензии промытого гексаном гидрида натрия (60% в минеральном масле, 1,64 г, 68,2 ммоль) в безводном ТГФ (70 мл) в атмосфере азота при комнатной температуре по каплям добавляют раствор 4 бром-2-крезола (10,6 г, 56,8 ммоль) и метоксиметилбромид (5,6 мл, 68,2 ммоль) в безводном ТГФ (30 мл). После перемешивания в течение 18 ч смесь разделяют между разбавленным водным бикарбонатом натрия и диэтиловым эфиром. Органический слой промывают водой и солевым раствором, сушат над безводным сульфатом натрия, концентрируют в вакууме с получением соединения примера получения 11 (12,74 г, 97%) в виде прозрачного масла. Пример получения 12 Охлаждают раствор соединения примера получения 8 (1,00 г, 2,81 ммоль) до температуры -78 С и по каплям добавляют втор-BuLi (1,3M в циклогексане, 2,10 мл, 2,81 ммоль). Раствор перемешивают в течение 15 мин, затем добавляют метилйодид (0,18 мл, 2,81 ммоль) и перемешивают в течение ночи, давая нагреться до температуры окружающей среды. Гасят насыщенным бикарбонатом натрия и добавляют этилацетат. Промывают солевым раствором, сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 10% этилацетатом/гексаном с получением соединения примера получения 12 (0,66 г, 81%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,12 (д, J=2,9, 1H), 6,83 (д, J=2,9, 1H), 5,10 (с, 2 Н), 5,04 (с, 2 Н), 3,63 (с, 3 Н), 3,48 (с,3 Н), 2,30 (с, 3 Н). МС рассчитанный 291,1; МС (М+1) 291,2, 293,2. Этот пример получения проводят по методике, описанной в J. Org. Chem. 57, 1992, 6972-6975. Перемешивают раствор метил-2-оксоциклопентанкарбоксилата (10,0 г, 70,42 ммоль) в безводном дихлорметане (300 мл), охлажденный до температуры -78 С, и добавляют диизопропилэтиламин (61,5 мл, 352,1 ммоль) и ангидрид трифлата (14,2 мл, 84,51 ммоль). Реакционную смесь перемешивают в течение 16 ч,давая нагреться до температуры окружающей среды. Реакцию гасят водой и промывают 10% лимонной кислотой, затем солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 13 (12,0 г, 63%) в виде темного масла, которое применяют без дальнейшей очистки. 1 Применяют методику примера получения 13 за исключением того, что используют метил 2-оксо-1 циклогептанкарбоксилат (5,00 г, 29,37 ммоль) с получением соединения примера получения 14 (4,34 г, 4 9%) в виде темного масла. Пример получения 15 Перемешивают раствор метил-2-оксо-5,5-диметилциклопентанкарбоксилата (J. Chem. Soc., 1996,1539-1540) (0,85 г, 5,00 ммоль) в безводном дихлорметане (15 мл), охлажденный до температуры -78 С, и добавляют диизопропилэтиламин (4,4 мл, 25,00 ммоль) и ангидрид трифлата (1,0 мл, 6,00 ммоль). Реакционную смесь перемешивают в течение 16 ч, давая нагреться до температуры окружающей среды. Реакцию гасят водой и промывают 10% лимонной кислотой, затем солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 15 (1,16 г, 77%) в виде темного масла,которое применяют без дальнейшей очистки. 1 Н ЯМР (CDCl3): 3,78 (с, 3 Н), 2,64 (т, J=7,l, 2H), 1,83 (т, J=7,l, 2 Н), 1,18 (с, 6 Н). Пример получения 16 Перемешивают раствор метил 2-оксо-5,5-диэтилциклопентанкарбоксилата (J. Chem. Soc., 1996,1539-1540) (2,94 г, 14,85 ммоль) в безводном дихлорметане (100 мл), охлажденный до температуры-78 С, и добавляют диизопропилэтиламин (13,0 мл, 74,25 ммоль) и ангидрид трифлата (3,0 мл, 17,82 ммоль). Реакционную смесь перемешивают в течение 16 ч, давая нагреться до температуры окружающей среды. Реакцию гасят водой и промывают 10% лимонной кислотой, затем солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 16 (3,96 г, 82%) в виде темного масла, которое применяют без дальнейшей очистки. 1 Н ЯМР (CDCl3): 3,78 (с, 3 Н), 2,60 (т, J=7,4, 7,8, 2 Н), 1,83 (т, J=7,8, 7,l, 2H), 1,46 (кв., J=7,4, 7,4, 7,4,4 Н), 0,91 (т, J=7,4, 7,4, 6 Н). Охлаждают раствор соединения примера получения 1 (0,95 г, 4,81 ммоль) в безводном ТГФ (25 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 2,8 мл, 4,81 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка(1,0 М в диэтиловом эфире, 4,8 мл, 4,81 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13(0,88 г, 3,21 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,37 г, 0,32 ммоль) в безводном ТГФ (25 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 17 (0,56 г, 55%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,04 (д, J=9,0, 1H), 6,90 (дд, J=3,l, 9,0, 1 Н), 6,81 (д, J=3,l, 1 Н), 5,10 (с, 2 Н), 5,02 (с,2 Н), 3,56 (с, 3 Н), 3,46 (с, 3 Н), 3,42 (с, 3 Н), 2,80 (т, J=8,6, 8,2, 4 Н), 2,05-1,95 (м, 2 Н). МС рассчитанный 322,2; МС (М+1) 323,1. Пример получения 18 Охлаждают раствор соединения примера получения 2 (2,50 г, 12,14 ммоль) в безводном ТГФ (40 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 7,9 мл, 13,35 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 12,1 мл, 12,14 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (3,32 г, 12,14 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,70 г, 0,61 ммоль) в безводном ТГФ (40 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 18 (2,87 г, 72%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,49 (дд, J=l,9, 8,2, 1 Н), 7,37 (д, J=2,3, 1 Н), 7,20 (д, 8,6, 1 Н), 5,16 (с, 2 Н), 3,55 (с,3 Н), 3,43 (с, 3 Н), 2,80 (т, J=7,4, 7,8, 4 Н), 2,06-1,98 (м, 2 Н). МС рассчитанный 330,1; МС (М+1) 331,1. Пример получения 19 Охлаждают раствор соединения примера получения 6 (2,49 г, 12,57 ммоль) в безводном ТГФ (25 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 7,4 мл, 12,57 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 12,6 мл, 12,57 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (2,30 г, 8,38 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,48 г, 0,41 ммоль) в безводном ТГФ (25 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 19 (1,70 г, 41%) в виде бес- 16007382 цветного масла. 1 Н ЯМР (CDCl3): 7,15 (т, J=8,2, 8,6, 1 Н), 6,78 (д, J=8,2, 2 Н), 5,09 (ушир.с, 4 Н), 3,52 (с, 3 Н), 3,42 (с,6 Н), 2,83-2,77 (м, 4 Н), 2,04-1,99 (м, 2 Н). МС рассчитанный 322,1; МС (М+1) 323,1. Пример получения 20 Охлаждают раствор соединения примера получения 1 (2,00 г, 10,13 ммоль) в безводном ТГФ (25 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 5,9 мл, 10,13 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 10,1 мл, 10,13 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 14 (2,04 г, 6,75 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,40 г, 0,34 ммоль) в безводном ТГФ (25 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 20 (2,13 г, 90%) в виде бесцветного масла. 1 Н ЯМР (CDCl3): 6,98 (д, J=9,0, 1H, 6,85 (дд, J=3,l, 9,0, 1 Н), 6,65 (д, J=3,l, 1 Н), 5,10 (с, 4 Н), 3,45 (с,3 Н), 3,44 (с, 3 Н), 3,38 (с, 3 Н), 2,56-2,50 (м, 4 Н), 1,84-1,80 (м, 2 Н), 1,65-1,60 (м, 4 Н). МС рассчитанный 350,1; MS(M+1) 351,1. Пример получения 21 Охлаждают раствор соединения примера получения 9 (2,18 г, 9,56 ммоль) в безводном ТГФ (40 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 6,2 мл, 10,52 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 9,6 мл, 9,56 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (2,62 г, 9,56 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,55 г, 0,48 ммоль) в безводном ТГФ (40 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 21 (0,62 г, 18%) в виде бесцветного масла. 1 Н ЯМР (CDCl3): 6,57 (д, J=2,7, 1H), 6,40 (д, J=2,7, 1H), 5,11 (с, 2 Н), 4,89 (с, 2 Н), 3,81 (с, 3 Н), 3,58 (с,3 Н), 3,47, (с, 3 Н), 3,44 (с, 3 Н), 2,83-2,77 (м, 4 Н), 2,03-1,96 (м, 2 Н). МС рассчитанный 352,1; МС (М+1) 353,1. Пример получения 22 Охлаждают раствор соединения примера получения 1 (1,13 г, 5,71 ммоль) в безводном ТГФ (40 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 3,4 мл, 5,71 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка(1,0 М в диэтиловом эфире, 5,7 мл, 5,71 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 15(1,15 г, 3,80 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,55 г, 0,48 ммоль) в безводном ТГФ (40 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаж- 17007382 дают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 22 (0,42 г, 32%) в виде бесцветного масла. 1 Н ЯМР (CDCl3): 7,05 (д, J=9,0, 1H), 6,92 (дд, J=3,l, 9,0, 1 Н), 6,62 (д, J=3,l, 1 Н), 5,11 (с, 2 Н), 5,01 (с,2 Н), 3,49 (с, 3 Н), 3,46 (с, 3 Н), 3,40 (с, 3 Н), 2,70 (т, J=7,0, 7,4, 2 Н), 1,86 (т, J=7,4, 7,0, 2 Н), 1,59 (ушир.с, 6 Н). МС рассчитанный 350,1; МС (М+1) 351,1. Пример получения 23 Охлаждают раствор соединения примера получения 1 (3,64 г, 18,38 ммоль) в безводном ТГФ (50 мл) до температуры -78 С и добавляют трет-BuLi (1,7 М в пентане, 3,4 мл, 5,71 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 10,8 мл, 18,38 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 16 (3,96 г, 12,25 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,71 г, 0,61 ммоль) в безводном ТГФ(50 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 23 (3,30 г, 84%) в виде бесцветного масла. 1 Н ЯМР (CDCl3): 7,05 (д, J=9,0, 1H), 6,89 (дд, J=3,l, 9,0, 1 Н), 6,62 (д, J=2,7, 1 Н), 5,11 (с, 2 Н), 5,00 (с,2 Н), 3,49 (с, 3 Н), 3,46 (с, 3 Н), 3,40 (с, 3 Н), 2,65 (ушир.т, J=7,8, 7,0, 2 Н), 1,87 (т, J=7,8, 7,4, 2 Н), 1,45-1,38 Охлаждают раствор соединения примера получения 4 (2,43 г, 10,51 ммоль) в безводном ТГФ (25 мл) до температуры -78 С и добавляют втор-BuLi (1,3 М в циклогексане, 8,9 мл, 11,56 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 10,51 мл, 10,51 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (2,88 г, 10,51 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,60 г, 0,52 ммоль) в ТГФ(25 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 24 (1,07 г, 26%) в виде бледножелтого масла. 1 Охлаждают раствор соединения примера получения 5 (2,60 г, 11,06 ммоль) в безводном ТГФ (25 мл) до температуры -78 С и добавляют втор-BuLi (1,3 М в циклогексане, 9,3 мл, 12,16 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 11,0 мл, 11,06 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения при- 18007382 мера получения 13 (3,03 г, 11,06 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,63 г, 0,50 ммоль) в ТГФ (25 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 25 (1,49 г, 48%) в виде бледножелтого масла. 1 Н ЯМР (CDCl3): 7,07-7,04 (м, 1 Н), 6,93-6,90 (м, 1 Н), 6,82 (дд, J=3,l, 9,0, 1 Н), 5,05 (с, 2 Н), 3,56 (с,3 Н), 3,42 (с, 3 Н), 2,82-2,78 (м, 4 Н), 2,03-1,96 (м, 2 Н). МС рассчитанный 280,1; МС (М+1) 281,1. Пример получения 26 Охлаждают раствор соединения примера получения 7 (2,46 г, 8,88 ммоль) в безводном ТГФ (25 мл) до температуры -78 С и добавляют втор-BuLi (1,3 М в циклогексане, 6,8 мл, 8,88 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 8,9 мл, 8,88 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (1,60 г, 5,86 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,51 г, 0,44 ммоль) в ТГФ (25 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 26 (1,20 г, 42%) в виде бесцветного масла. 1 Н ЯМР (CDCl3): 7,05 (д, J=8,6, 1H), 6,81 (д, J=2,0, 1H), 6,69 (дд, J=2,3, 8,6, 1 Н), 5,15 (с, 2 Н), 5,09 (с,2 Н), 3,58 (с, 3 Н), 3,48 (с, 3 Н), 3,43 (с, 3 Н), 2,79 (т, J=7,0, 7,4, 4 Н), 2,04-1,95 (м, 2 Н). МС рассчитанный 322,2; МС (М+1) 323,1. Пример получения 27 Охлаждают раствор соединения примера получения 12 (1,24 г, 4,26 ммоль) в безводном ТГФ (20 мл) до температуры -78 С и добавляют втор-BuLi (1,3 М в циклогексане, 3,3 мл, 4,26 ммоль). Раствор перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 4,3 мл, 4,26 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (1,17 г, 4,26 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,24 г, 0,21 ммоль) в ТГФ (20 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 27 (0,54 г, 38%) в виде бесцветного масла. 1 Н ЯМР (CDCl3): 6,80 (д, J=2,4, 1H), 6, 61 (д, J=2,3, 1H), 5,09 (с, 2 Н), 4,79 (с, 2 Н), 3,57 (с, 3 Н), 3,48 (с,3 Н), 3,46 (с, 3 Н), 2,83-2,76 (м, 4 Н), 2,29 (с, 3 Н), 2,02-1,96 (м, 2 Н). МС рассчитанный 336,2; МС (М+1) 337,2. Пример получения 28 Охлаждают раствор соединения примера получения 10 (2,00 г, 11,90 ммоль) в безводном ТГФ (20 мл) до температуры -78 С и добавляют втор-BuLi (1,3 М в циклогексане, 7,7 мл, 13,09 ммоль). Раствор- 19007382 перемешивают в течение 15 мин, затем нагревают до температуры 0 С. По каплям добавляют раствор хлорида цинка (1,0 М в диэтиловом эфире, 11,9 мл, 11,90 ммоль) и дают нагреться полученному раствору до температуры окружающей среды. Этот раствор добавляют через канюлю в раствор соединения примера получения 13 (3,26 г, 11,90 ммоль) и тетракис(трифенилфосфин)Pd(0) (0,69 г, 0,58 ммоль) в ТГФ (20 мл) и дают нагреться полученному раствору до температуры 50 С в течение 16 ч. Реакционную смесь охлаждают до температуры окружающей среды и гасят водой. Добавляют этилацетат и полученный органический слой промывают насыщенным бикарбонатом натрия и солевым раствором. Сушат органический слой над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением указанного в заголовке соединения (1,28 г, 38%) в виде бесцветного масла, которое представляет собой смесь региоизомеров согласно 1 Н ЯМР. МС рассчитанный 292,1; МС (М+1) 293,1. Пример получения 29 К суспензии 5% палладия на угле (0,27 г) в метаноле (15 мл) добавляют раствор соединения примера получения 17 (0,27 г, 0,8 4 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 29 (0,20 г, 75%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,98 (д, J=8,6, 1H), 6,86 (д, J=3,l, 1H), 6,81 (дд, J=3,l, 9,0, 1 Н), 5,1 (с, 2 Н), 5,08 (с,2 Н), 3,64-3,59 (м, 1 Н), 3,50 (с, 3 Н), 3,45 (с, 3 Н), 3,39-3,30 (м, 1 Н), 3,19 (с, 3 Н), 2,12-1,98 (м, 4 Н), 1,93-1,82 К суспензии 5% палладия на угле (0,19 г) в метаноле (50 мл)/триэтиламине (1,0 мл) добавляют раствор соединения примера получения 18 (1,51 г, 4,58 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 30 (0,95 г, 63%) в виде прозрачного масла. 1 К суспензии 5% палладия на угле (0,13 г) в метаноле (50 мл)/тризтиламине (1,0 мл) добавляют раствор соединения примера получения 24 (1,07 г, 3,88 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 31 (0,72 г, 67%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,96-6,93 (м, 3 Н), 5,17 (с, 2 Н), 3,67-3,60 (м, 1 Н), 3,50 (с, 3 Н), 3,34-3,28 (м, 1 Н), 3,15 К суспензии 5% палладия на угле (0,24 г) в метаноле (50 мл)/триэтиламине (1,0 мл) добавляют раствор соединения примера получения 25 (1,31 г, 4,68 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 32 (1,01 г, 77%) в виде прозрачного масла. МС рассчитанный 282,1; МС (М+1) 283,1. Пример получения 33 К суспензии 5% палладия на угле (0,34 г) в метаноле (50 мл) добавляют раствор соединения примера получения 19 (1,70 г, 5,28 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 33 (0,99 г, 58%) в виде прозрачного масла. 1 К суспензии 5% палладия на угле (0,60 г) в метаноле (25 мл) добавляют раствор соединения примера получения 26 (1,20 г, 3,7 3 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 34 (0,82 г, 68%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,06 (д, J=8,6, 1H), 6,77 (д, J=2,3, 1H), 6,60 (дд, J=2,4, 8,6, 1 Н), 5,20 (с, 2 Н), 5,14 (дд,J=6,6, 9,7, 2 Н), 3,61-3,54 (м, 1 Н), 3,50 (с, 6 Н), 3,45 (с, 3 Н), 3,31-3,26 (м, 1 Н), 2,16-1,94 (м, 4 Н), 1,86-1,80 (м,1 Н), 1,71-1,60 (м, 1 Н). МС рассчитанный 324,2; МС (М+1) 325,2. Пример получения 35 К суспензии 5% палладия на угле (0,25 г) в метаноле (25 мл) добавляют раствор соединения приме- 21007382 ра получения 27 (0,54 г, 1,61 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 35 (0,49 г, 8 9%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,69 (д, J=2,8, 1H), 6,65 (д, J=3,l, 1H), 5,04 (м, 2 Н), 4,93 (дд, J=5,9, 16,0, 2 Н), 3,733,67 (м, 1 Н), 3,57 (с, 3 Н), 3,42 (с, 3 Н), 3,25-3,19 (м, 4 Н), 2,25 (с, 3 Н), 2,17-2,12 (м, 1 Н), 2,05-1,85 (м, 4 Н),1,70-1,60 (м, 1 Н). МС рассчитанный 338,2; МС (М+1) 339,2. Пример получения 36 К суспензии 5% палладия на угле (0,38 г) в метаноле (35 мл) добавляют раствор соединения примера получения 20 (0,75 г, 2,14 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 36 (0,63 г, 84%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,95 (д, J=9,0, 1H), 6,85 (д, J=3,l, 1H), 6,79 (дд, J=3,l, 9,0, 1 Н), 5,15 (с, 2 Н), 5,13-5,05 К суспензии 5% палладия на угле (0,08 г) в метаноле (50 мл)/триэтиламине (1,0 мл) добавляют раствор соединения примера получения 21 (0,62 г, 1,76 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 37 (0,50 г, 81%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 6,50 (д, J=2,7, 1H), 6,44 (д, J=2,7,1H), 5,14-5,05 (м, 4 Н), 3,80 (м, 4 Н), 3,58 (с, 3 Н),3,46 (с, 3 Н), 3,25 (м, 4 Н), 2,15-2,09 (м, 1 Н), 2,07-1,90 (м, 4 Н), 1,72-1,64 (м, 1 Н). МС рассчитанный 354,1; МС (М+1) 355,1. Пример получения 38 К суспензии 5% палладия на угле (0,05 г) в метаноле (50 мл)/триэтиламине (1,0 мл) добавляют раствор соединения примера получения 22 (0,42 г, 1,19 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 38 (0,16 г, 38%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,00 (д, J=8,2, 0,5H), 6,94 (д, J=7,8, 0,5 Н), 6,84-6,75 (м, 1,5 Н), 6,67 (д, J=3,l, 0,5H),5,12-5,01 (м, 4 Н), 3,77 (д, J=9,0, 0,5H), 3,64 (д, J=11,3, 0,5H), 3,52 (с, 1,5 Н), 3,49 (с, 1,5 Н), 3,48-3,43 (с,4,5 Н), 3,35 (с, 1,5 Н), 2,55-2,42 (м, 0,5 Н), 2,17-2,02 (м, 1 Н), 1,95-1,88 (м, 0,5 Н), 1,81-1,75 (м, 1 Н), 1,69-1,60 К суспензии 5% палладия на угле (0,58 г) в метаноле (50 мл)/триэтиламине (1,0 мл) добавляют раствор соединения примера получения 23 (1,25 г, 3,89 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 39 (0,89 г, 72%) в виде прозрачного масла. МС рассчитанный 380,2; МС (М+1) 381,2. Пример получения 40 К суспензии 5% палладия на угле (0,15 г) в метаноле (50 мл)/триэтиламине (1,0 мл) добавляют раствор соединения примера получения 28 (0,58 г, 1,80 ммоль) в метаноле (10 мл). Помещают смесь в аппарат Парра в атмосфере водорода (60 ф/д 2) при температуре 40 С на 12 ч. Реакционную смесь продувают азотом и фильтруют через целит. Фильтрат концентрируют в вакууме и очищают флэш-хроматографией с 15% этилацетатом/гексаном с получением соединения примера получения 40 (0,25 г, 43%) в виде прозрачного масла. МС рассчитанный 294,1; МС (М+1) 295,1. Пример получения 41 В этом примере получения применяют методику, описанную в Tet. Letters 36, 31, 1995, 5461-5464. Охлаждают суспензию примера получения 29 (0,50 г, 1,54 ммоль) и гидрохлорида N,О-диметилгидроксиламина (0,23 г, 2,31 ммоль) в безводном ТГФ (25 мл) до температуры -10 С на бане лед/ацетон,добавляют изопропилхлорид магния (2,0 М, 2,3 мл, 4,62 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 41 (0,49 г, 90%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 42 Охлаждают суспензию примера получения 30 (0,95 г, 2,86 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,43 г, 4,29 ммоль) в безводном ТГФ (40 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 4,3 мл, 8,58 ммоль) и перемешивают реакцион- 23007382 ную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 42 (0,86 г, 83%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 43 Охлаждают суспензию соединения примера получения 31 (0,71 г, 2,55 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,37 г, 3,83 ммоль) в безводном ТГФ (40 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 2,5 мл, 5,10 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 43 (0,36 г, 46%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 44 Охлаждают суспензию соединения примера получения 32 (0,98 г, 3,4 8 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,51 г, 5,22 ммоль) в безводном ТГФ (40 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 5,2 мл, 10,42 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 44 (0,61 г, 56%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 45 Охлаждают суспензию соединения примера получения 33 (0,97 г, 2,99 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,44 г, 4,49 ммоль) в безводном ТГФ (40 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 4,5 мл, 9,00 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэшхроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 45 (0,71 г,67%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Охлаждают суспензию соединения примера получения 34 (0,82 г, 2,53 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,37 г, 3,80 ммоль) в безводном ТГФ (30 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 3,8 мл, 7,60 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 46 (0,80 г, 90%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 47 Охлаждают суспензию соединения примера получения 35 (0,48 г, 1,42 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,21 г, 2,13 ммоль) в безводном ТГФ (20 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 2,1 мл, 4,20 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 47 (0,46 г, 88%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 48 Охлаждают суспензию соединения примера получения 36 (0,63 г, 2,53 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,26 г, 2,68 ммоль) в безводном ТГФ (30 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 2,7 мл, 5,40 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 48 (0,54 г, 7 6%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 49- 25007382 Охлаждают суспензию соединения примера получения 37 (0,50 г, 1,41 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,24 г, 2,12 ммоль) в безводном ТГФ (30 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 2,1 мл, 4,20 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 49 (0,31 г, 57%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 50 Охлаждают суспензию соединения примера получения 38 (0,16 г, 0,45 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,07 г, 0,68 ммоль) в безводном ТГФ (10 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 0,7 мл, 1,40 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 50 (0,15 г, 87%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 51 Охлаждают суспензию соединения примера получения 39 (0,25 г, 0,7 7 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,11 г, 1,16 ммоль) в безводном ТГФ (20 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 1,2 мл, 2,40 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 51 (0,20 г, 74%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 52 Охлаждают суспензию соединения примера получения 40 (0,91 г, 3,07 ммоль) и гидрохлорида N,Одиметилгидроксиламина (0,45 г, 4,64 ммоль) в безводном ТГФ (20 мл) до температуры -10 С на бане лед/ацетон, добавляют изопропилхлорид магния (2,0 М, 3,1 мл, 6,20 ммоль) и перемешивают реакционную смесь в течение 30 мин. Реакцию гасят насыщенным хлоридом аммония. Добавляют этилацетат и органический слой промывают солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 52 (0,36 г, 36%) в виде бесцветного масла, которое применяют без дальнейшего исследования. Пример получения 53 Охлаждают суспензию гидрида натрия (60% в минеральном масле, 2,54 г, 63,58 ммоль) в безводном- 26007382 ДМФ (50 мл) в атмосфере азота до температуры 0 С и по каплям добавляют раствор 4-бромфенола (10,00 г, 57,80 ммоль) в безводном ДМФ (50 мл). К этой суспензии по каплям добавляют метоксиметилхлорид(4,8 мл, 63,58 ммоль). Реакционной смеси дают нагреться до температуры окружающей среды и перемешивают в течение 1 ч. Реакцию гасят водой и добавляют диэтиловый эфир. Органический слой промывают 1 н гидроксидом натрия и солевым раствором. Органический слой сушат над сульфатом натрия,концентрируют в вакууме и очищают флэш-хроматографией с 10% этилацетатом/гексаном с получением соединения примера получения 53 (10,42 г, 83%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,38 (д, J=8,8, 2 Н), 6,93 (д, J=8,7, 2H), 5,14 (с, 2 Н), 3,43 (с, 3 Н). Пример получения 54 Охлаждают раствор соединения примера получения 53 (3,03 г, 14,00 ммоль) в безводном ТГФ (40 мл) до температуры -78 С в атмосфере азота и по каплям добавляют втор.-бутиллитий (1,3 М в циклогексане, 10,7 мл, 14,00 ммоль). Раствор перемешивают при температуре -78 С в течение 30 мин с получением 0,40 М раствора. Применяют немедленно, сохраняя температуру -78 С. Пример получения 55 Добавляют соединение примера получения 54 (0,40 М, 42,5 мл, 17,00 ммоль) в раствор соединения примера получения 41 (6,00 г, 17,00 ммоль) в безводном ТГФ (50 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 55 (7,11 г, 97%) в виде бесцветной пены. 1 Н ЯМР (CDCl3): 7,61 (д, J=8,6, 2 Н), 6,83 (д, J=8,6, 2H), 6,76 (д, J=2,7, 1H), 6,71 (д, J=8,7, 1H), 6,60 Добавляют соединение примера получения 54 (0,40 М, 8,9 мл, 3,57 ммоль) в раствор соединения примера получения 42 (0,86 г, 2,38 ммоль) в безводном ТГФ (50 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 20% этилацетатом/гексаном с получением соединения примера получения 56 (1,03 г, 99%) в виде прозрачного масла. Пример получения 57- 27007382 Добавляют соединение примера получения 54 (0,40 М, 6,1 мл, 2,34 ммоль) в раствор соединения примера получения 43 (0,36 г, 1,17 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% тилацетатом/гексаном с получением соединения примера получения 57 (0,41 г, 92%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,61 (д, J=7,4, 2H), 6,92-6,81 (м, 3 Н), 6,76-6,65 (м, 2 Н), 5,15 (с, 2 Н), 4,93 (м, 2 Н),4,29-4,23 (м, 1 Н), 3,82-3,76 (м, 1 Н), 3,45 (с, 3 Н), 3,40 (с, 3 Н), 2,23-1,92 (м, 8 Н), 1,80-1,69 (м, 1 Н). Пример получения 58 Добавляют соединение примера получения 54 (0,40 М, 9,8 мл, 3,92 ммоль) в раствор соединения примера получения 44 (0,61 г, 1,96 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 58 (0,59 г, 92%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,61 (д, J=7,4, 2H), 6,92-6,80 (м, 3 Н), 678-,672 (м, 1 Н), 6,63-6,59 (м, 1 Н), 5,17 (дд,J=6,6, 9,4, 2 Н), 4,90 (дд, J=4,5, 6,6, 2 Н), 4,30-4,26 (м, 1 Н), 3,80-3,75 (м, 1 Н), 3,43 (с, 3 Н), 3,39 (с, 3 Н), 2,201,91 (м, 5 Н), 1,80-1,70 (м, 1 Н). Пример получения 59 Добавляют соединение примера получения 54 (0,40 М, 7,5 мл, 3,03 ммоль) в раствор соединения примера получения 45 (0,71 г, 2,01 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 59 (0,80 г, 93%) в виде прозрачного масла. 1- 28007382 Добавляют соединение примера получения 54 (0,40 М, 8,5 мл, 3,40 ммоль) в раствор соединения примера получения 46 (0,80 г, 2,26 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 60 (0,87 г, 90%) в виде прозрачного масла. 1 Добавляют соединение примера получения 54 (0,40 М, 4,7 мл, 1,88 ммоль) в раствор соединения примера получения 47 (0,46 г, 1,25 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 61 (0,43 г, 77%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,61 (д, J=8,6, 2H), 6,80 (д, J=9,0, 2H), 6,51 (д, J=2,7, 1 Н), 6,41 (д, J=2,7, 1 Н), 5,13 (с,2 Н), 4,97-4,85 (м, 4 Н), 4,26-4,21 (м, 1 Н), 3,85-3,80 (м, 1 Н), 3,61 (с, 3 Н), 3,42 (с, 3 Н), 3,37 (с, 3 Н), 2,33-2,22 Добавляют соединение примера получения 54 (0,40 М, 6,8 мл, 2,74 ммоль) в раствор соединения примера получения 48 (0,54 г, 1,37 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 62 (0,25 г, 40%) в виде прозрачного масла. 1- 29007382 Добавляют соединение примера получения 54 (0,40 м, 4,0 мл, 1,62 ммоль) в раствор соединения примера получения 49 (0,31 г, 0,81 ммоль) в безводном ТГФ (10 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 63 (0,12 г, 32%) в виде прозрачного масла. 1 Н ЯМР (CDCl3): 7,65 (д, J=8,0, 2 Н), 6,99-6,96 (м, 1 Н), 6,80 (д, J=8,0, 2H), 6,29 (д, J=2,7, 1H), 6,23 (д,J=2,7, 1H), 5,13 (с, 2 Н), 5,02-4,89 (м, 4 Н), 4,24-4,19 (м, 1 Н), 3,94-3,89 (м, 1 Н), 3,67 (с, 3 Н), 3,60 (с, 3 Н), 3,44 Добавляют соединение примера получения 54 (0,40 М, 1,5 мл, 0,59 ммоль) в раствор соединения примера получения 50 (0,15 г, 0,39 ммоль) в безводном ТГФ (10 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слои сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 64 (50 мг, 28%) в виде прозрачного масла. Пример получения 65 Добавляют соединение примера получения 54 (0,40 М, 2,1 мл, 0,85 ммоль) в раствор соединения примера получения 51 (0,20 г, 0,57 ммоль) в безводном ТГФ (10 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 30% этилацетатом/гексаном с получением соединения примера получения 65 (0,21 г, 86%) в виде прозрачного масла. Пример получения 66 Добавляют соединение примера получения 52 (0,40 М, 5,5 мл, 2,22 ммоль) в раствор соединения примера получения 50 (0,36 г, 1,11 ммоль) в безводном ТГФ (20 мл) при температуре 0 С и перемешивают полученный раствор в течение 30 мин при температуре 0 С. Реакцию гасят насыщенным бикарбонатом натрия. Добавляют этилацетат и промывают солевым раствором. Органический слой сушат над сульфатом натрия, концентрируют в вакууме и очищают флэш-хроматографией с 50% этилацетатом/гексаном с получением соединения примера получения 66 (0,41 г, 92%) в виде прозрачного масла.
МПК / Метки
МПК: C07D 311/60, A61P 35/00
Метки: селективных, эстрогена, бензопираны, агонистов, качестве, бета-рецептора, замещенные
Код ссылки
<a href="https://eas.patents.su/30-7382-zameshhennye-benzopirany-v-kachestve-selektivnyh-agonistov-beta-receptora-estrogena.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные бензопираны в качестве селективных агонистов бета-рецептора эстрогена</a>