Ингибиторы фосфолипазных ферментов
Номер патента: 3876
Опубликовано: 30.10.2003
Авторы: Лаверинг Фрэнк, Нопф Джон Л., Чен Лихрен, Сихра Джасбир С., Ксианг Йибин, Бемис Джин Э., Маккью Джон К.
Формула / Реферат
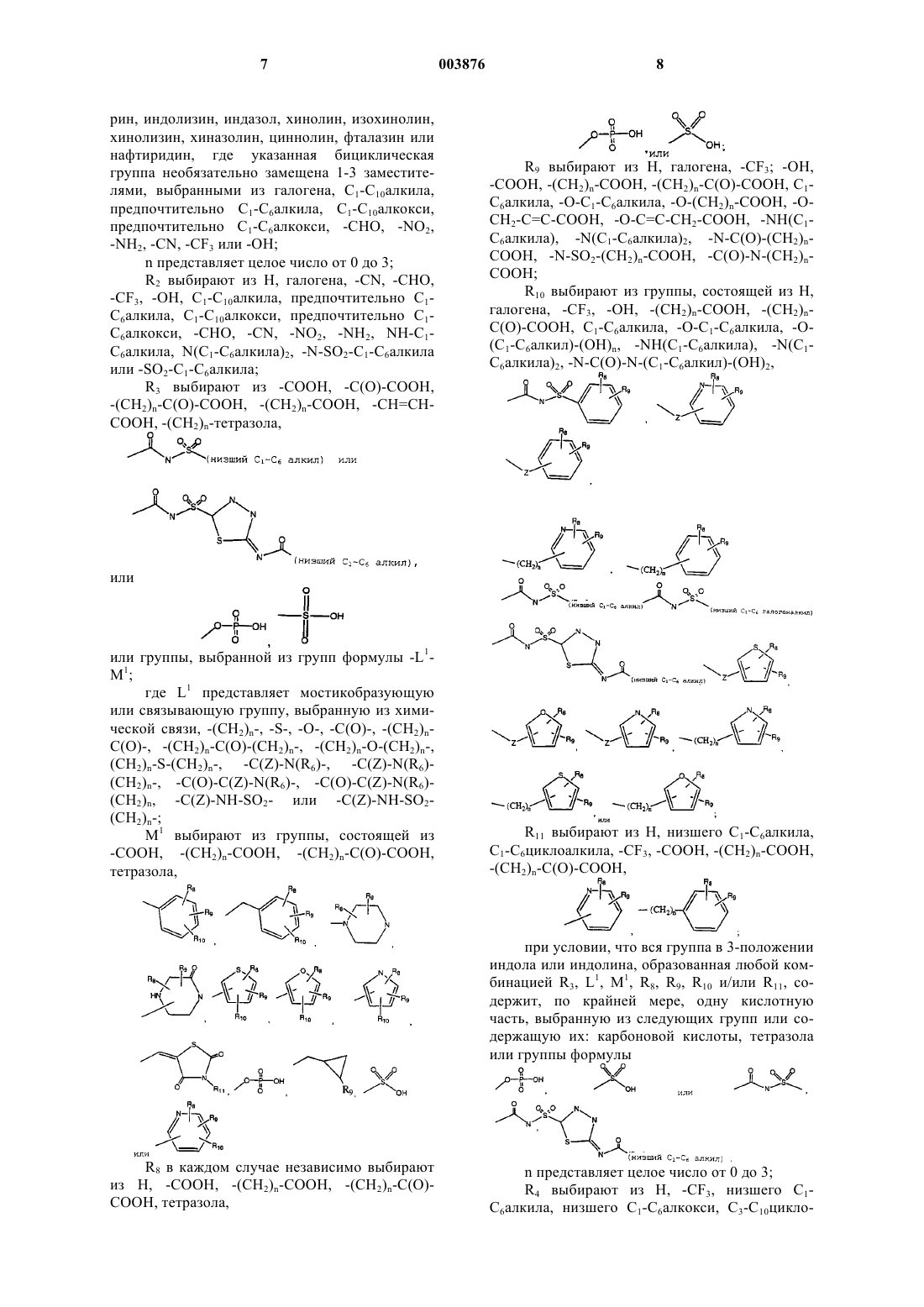
1. Соединение формулы
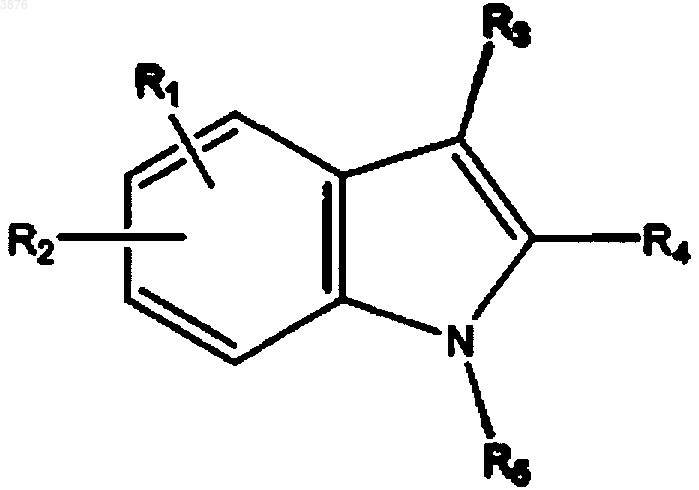
где R1 выбирают из H, галогена, C1-C6алкила, -S-C1-C6алкила, C1-C6алкокси, -CN, -NO2, -NH2, фенила, -O-фенила, -S-фенила, бензила, -O-бензила, -S-бензила, тиенила, бензофуранила, где ароматические или гетероароматические циклы необязательно замещены трифторметилом, или группы формулы
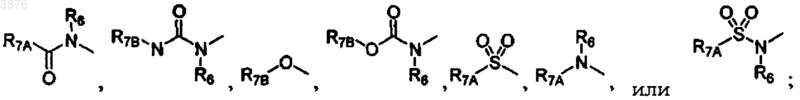
R6 представляет собой H;
R7A выбирают из -CF3, C1-C6алкила, C1-C6алкокси, -NH-(C1-C6алкила), N(C1-C6алкил)2, пиридинила, тиенила, фурила, пирролила, фенила, бензила, -O-бензила, пиразолила, тиазолила, тиенила и изоксазолила, причем кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-C6алкила, -NO2, ацетамидо;
R7B выбирают из -CF3, C1-C6алкила, пиридинила, тиенила, фурила, пирролила, фенила, бензила, пиразолила, тиазолила, тиенила и изоксазолила, причем кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-C6алкила, -NO2, ацетамидо;
R2 выбирают из H и галогена;
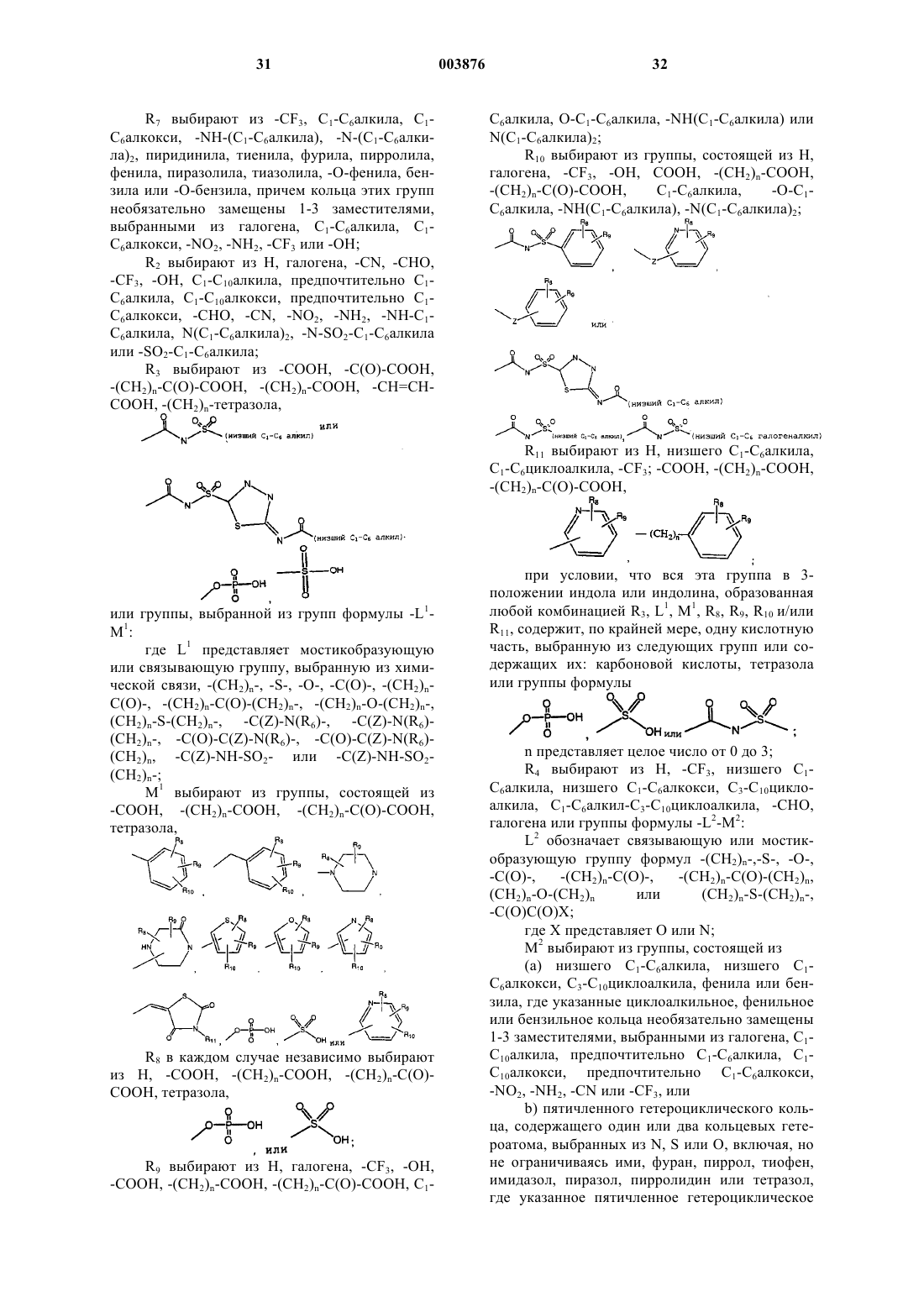
R3 выбирают из -CH=CH-COOH,
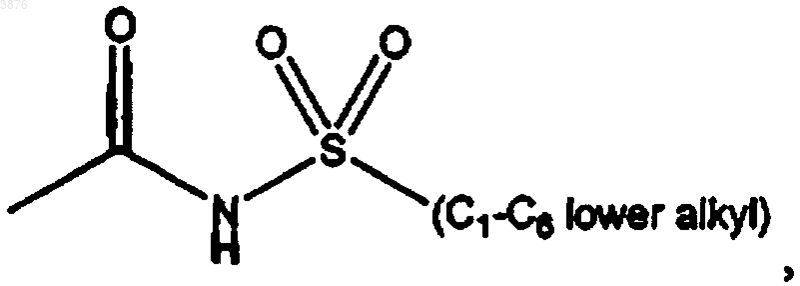
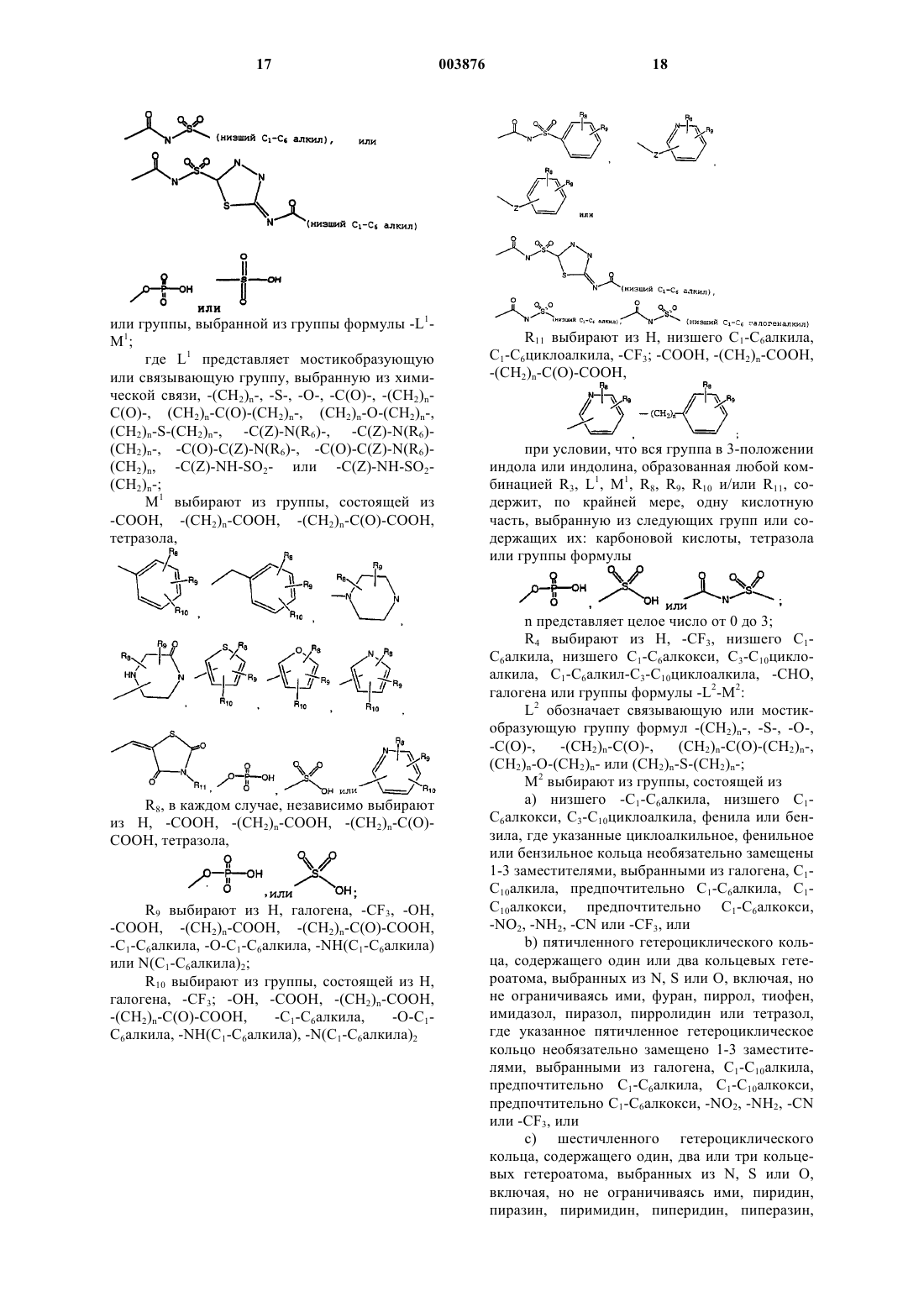
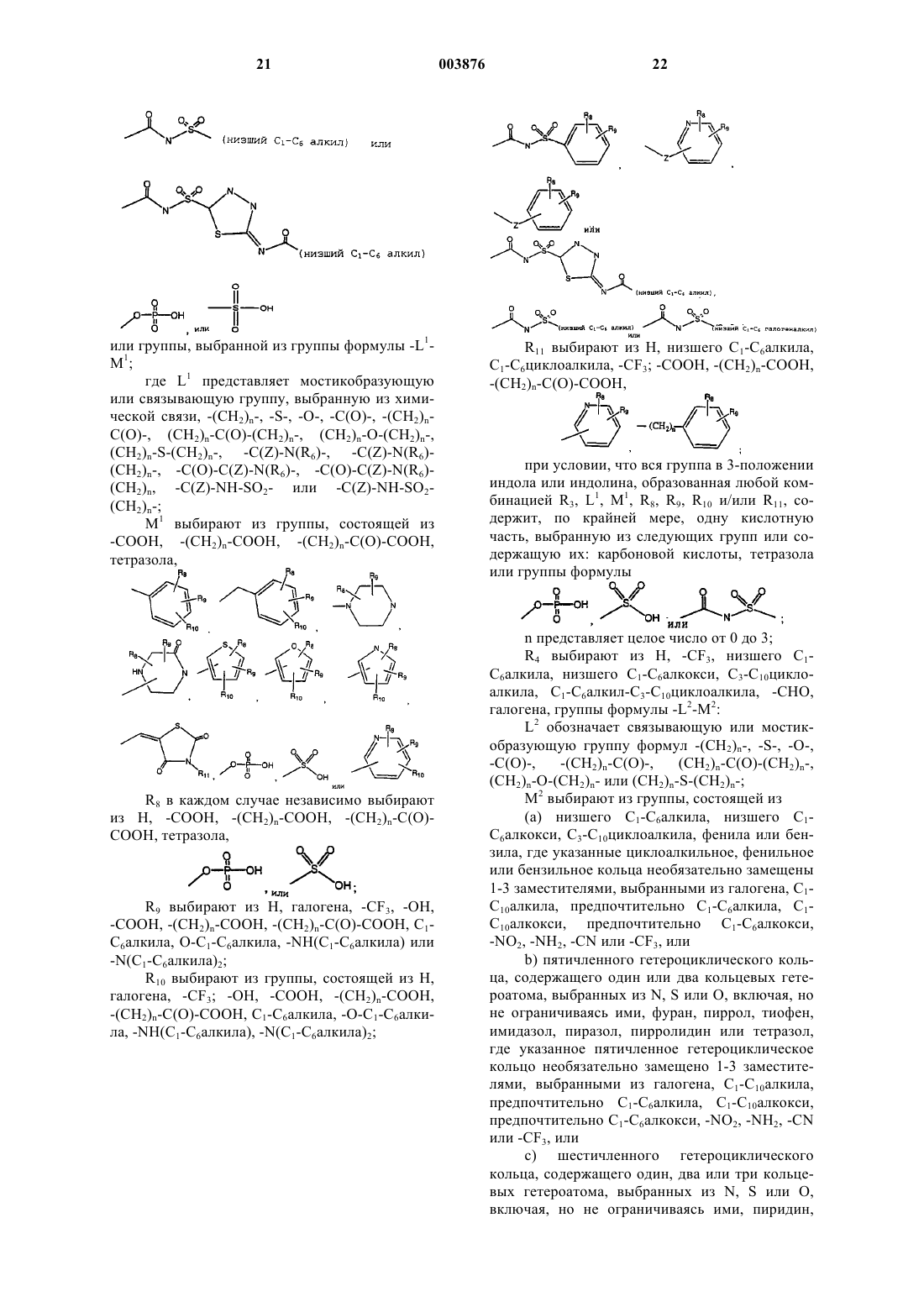
или остатка, выбранного из групп формулы -L1-M1;
где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(CH2)n-, -C(O)-, -(CH2)n-C(O)-, -(CH2)n-NH-, -C(Z)-N(R6)-, -C(Z)-N(R6)-(CH2)n-, -C(O)-C(Z)-N(R6)-, -C(O)-C(Z)-N(R6)-(CH2)n, -C(Z)-NH-SO2- или -C(Z)-NH-SO2-(CH2)n-;
где Z представляет собой O или N;
M1 выбирают из группы, состоящей из -COOH, -(CH2)n-COOH, -(CH2)n-C(O)-COOH, тетразола,
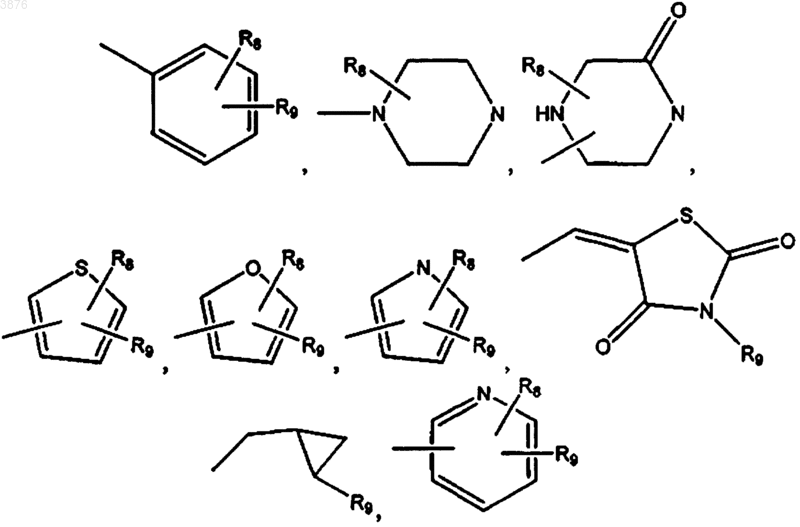
R8 в каждом случае его присутствия независимо выбирают из H, -COOH, -(CH2)n-COOH, -(CH2)n-C(O)-COOH,
R9 выбирают из H, галогена, -CF3, -OH, -COOH, -(CH2)n-COOH, -(CH2)n-C(O)-COOH, -C1-C6алкила, -O-C1-C6алкила, -O-(CH2)n-COOH, -O-CH2-C=C-COOH, -O-C=C-CH2-COOH и -C(O)-N-(CH2)n-COOH;
при условии, что вся группа, образованная любой комбинацией, L1 и M1, содержит, по крайней мере, одну кислотную часть, которая включает группу -COOH или группу
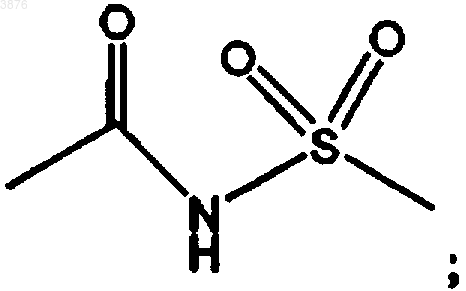
n представляет целое число от 0 до 3;
R4 выбирают из H, низшего C1-C6алкила, C3-C10циклоалкила, хинолилсульфанилметила;
R5 выбирают из групп формулы -(CH2)n-A, где A представляет остаток
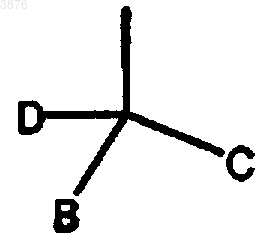
где n представляет целое число от 0 до 3;
D представляет H;
B и C независимо являются фенильными группами, каждая из которых необязательно замещена 1-3 заместителями, выбранными из H, галогена, -CN, -CHO, -CF3, -OH, C1-C6алкила, C1-C6алкокси, -NH2, -N(C1-C6)2, -NH(C1-C6), -N-C(O)-(C1-C6) и -NO2;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R4 представляет водород или метил, или его фармацевтически приемлемая соль.
3. Соединение по п.2, где R1 находится в 5 положении индола, или его фармацевтически приемлемая соль.
4. Соединение по п.3, где R1 представляет бензилоксигруппу, или его фармацевтически приемлемая соль.
5. Соединение по п.1, где R3 представляет -L1-M1, где M1 является группой
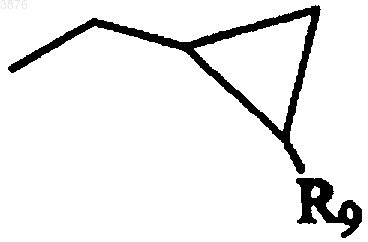
а L1 и R9 определены, как указано в п.1.
6. Соединение, имеющее формулу
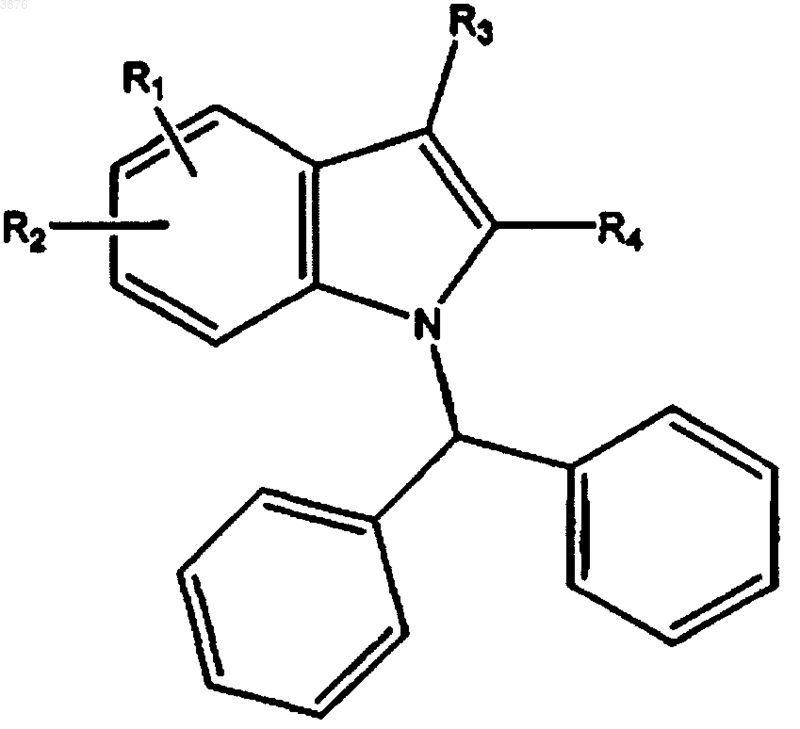
где R1, R2, R3, R4, R6, R7, R8, R9, L1, M1 определены, как указано в п.1.
7. Соединение по п.6, где заместители R1 и R2 расположены в 5 либо в 6 положении индольного кольца и определяются следующим образом:
R1 выбирают из H, галогена, C1-C6алкила, -S-C1-C6алкила, C1-C6алкокси, фенила, -O-фенила, -S-фенила, бензила, -O-бензила;
R2 выбирают из H и галогена;
R3 выбирают из остатка, выбранного из групп формулы -L1-M1;
где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(CH2)n-, -(CH2)n-C(O)- или -(CH2)n-NH-;
M1 выбирают из группы, состоящей из
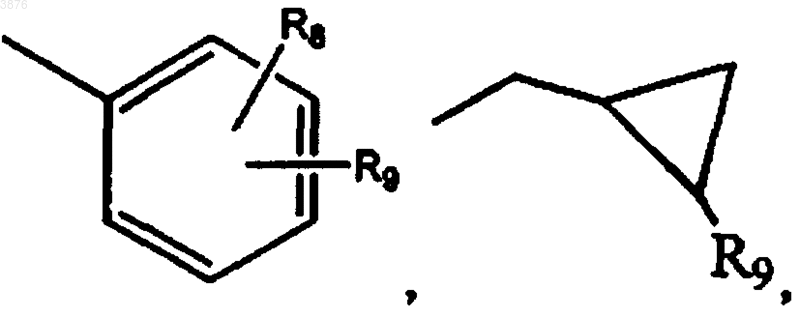
R8 в каждом случае его присутствия независимо выбирают из H, -COOH, -(CH2)n-COOH, -(CH2)n-C(O)-COOH,
R9 выбирают из H, галогена, -CF3, -OH, -COOH, -(CH2)n-COOH, -C1-C6алкила, -O-C1-C6алкила, -O-(CH2)n-COOH;
при условии, что вся замещающая группа при индоле, образованная любой комбинацией R3, L1, M1, R8, R9, содержит, по крайней мере, одну кислотную часть, выбранную из группы карбоновой кислоты или содержащую группу карбоновой кислоты;
n представляет целое число от 0 до 3 и
R4 представляет H или метил.
8. Соединение, имеющее формулу
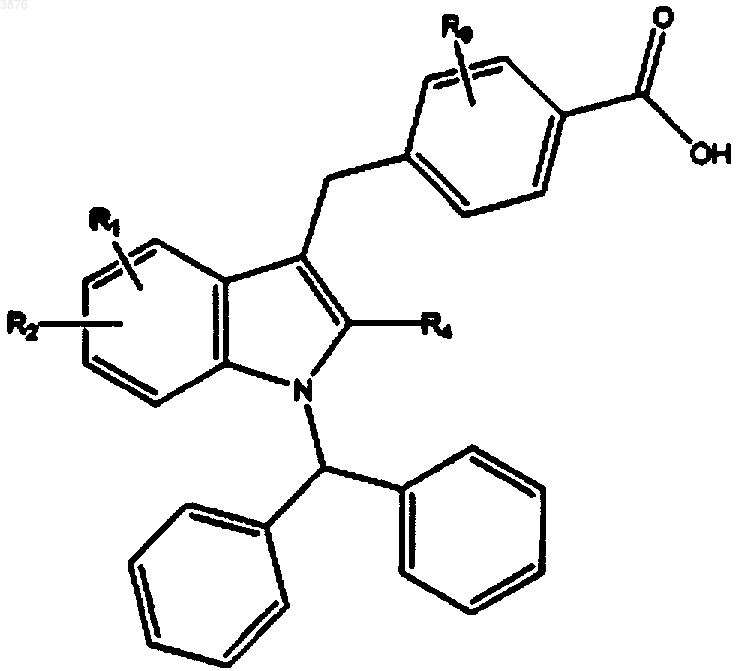
где заместители R1 и R2 находятся в 5 и 6 положениях индольного кольца и определены, как указано в п.7, а R4 и R9 определены, как указано в п.7.
9. Соединение по п.1, которое выбирают из
a) 4-[(5-{[(циклопентилокси)карбонил]амино}-1-пропил-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
b) циклопентил-N-{3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1-пропил-1H-индол-5-ил}карбамата;
c) 4-[(1-бензгидрил-5-{[(циклопентилокси)карбонил]амино}-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
d) 4-{[5-{[(циклопентилокси)карбонил]амино}-1-(2-нафтилметил)-1H-индол-3-ил] метил} -3-метоксибензойной кислоты;
e) 4-{[5-{[(циклопентилокси)карбонил]амино}-1-(циклопропилметил)-1H-индол-3-ил] метил} -3-метоксибензойной кислоты;
f) 4-{[5-{[(циклопентилокси)карбонил]амино}-1-(циклопропилметил)-1H-индол-3-ил] метил} -3-метоксибензойной кислоты;
g) 4-{[5-{[(циклопентилокси)карбонил]амино}-1-(4-пиридинилметил)-1H-индол-3-ил] метил} -3-метоксибензойной кислоты;
h) 4-{[5-{[(циклопентилокси)карбонил]амино}-1-изопропил-1H-индол-3-ил] метил} -3-метоксибензойной кислоты;
i) 4-[(1-циклопентил-5-{[(циклопентилокси)карбонил]амино}-1H-индол-3-ил)метил]-3-метоксибензойной кислоты или
j) 4-[(1-бензгидрил-5-{[(бутиламино)карбонил]амино}-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
или его фармацевтически приемлемая соль.
10. Соединение по п.1, которое выбирают из
a) 4-({1-бензгидрил-5-[(метилсульфонил)амино]-1H-индол-3-ил}метил)-3-метоксибензойной кислоты;
b) 4-({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}метил)-3-метоксибензойной кислоты;
c) 4-[(1-бензгидрил-5-нитро-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
d) 4-[(1-бензгидрил-5-фтор-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
e) 4-[(1-бензгидрил-5-метил-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
f) 4-[(5-бензгидрил-5H-[1,3]диоксоло[4,5-f]-индол-7-ил)метил]-3-метоксибензойной кислоты;
g) 4-[(1-бензгидрил-5-циано-1H-индол-3-ил)метил]-3-метоксибензойной кислоты;
h) 4-{[1-бензгидрил-5-(метилсульфонил)-1H-индол-3-ил]метил}-3-метоксибензойной кислоты или
j) циклопентил-N-{1-бензгидрил-3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
или его фармацевтически приемлемая соль.
11. Соединение по п.1, которое выбирают из
a) циклопентил-N-{3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1-пропил-1H-индол-5-ил}карбамата;
b) N-{1-(циклопропилметил)-3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
c) циклопентил-N-{3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1-(4-пиридинилметил)-1H-индол-5-ил}карбамата;
d) циклопентил-N-{3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1-(2-нафтилметил)-1H-индол-5-ил}карбамата;
e) циклопентил-N-{1-(изопропил)-3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
f) циклопентил-N-{1-(циклопентил)-3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
g) циклопентил-N-{1-бензгидрил-3-[2-метокси-4-({[(трифторметил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
h) циклопентил-N-{1-бензгидрил-3-[2-метокси-4-{[(метилсульфонил)амино]карбонил}бензил]-1H-индол-5-ил}карбамата;
i) N-{1-бензгидрил-3-[4-({[(2-хлорфенил)сульфонил]амино}карбонил)-2-метоксибензил]-1H-индол-5-ил}карбамата или
j) циклопентил-N-(3-{4-[({[5-(ацетилимино)-4-метил-4,5-дигидро-1,3,4-тиадиазол-2-ил]сульфонил}амино)карбонил]-2-метоксибензил}-1-бензгидрил-1H-индол-5-ил)карбамата;
или его фармацевтически приемлемая соль.
12. Соединение по п.1, которое выбирают из
a) циклопентил-N-{1-бензгидрил-3-[4-[({[5-(диметиламино)-1-нафтил]сульфонил}амино)карбонил]-2-метоксибензил] -1H-индол-5-ил}карбамата;
b) циклопентил-N-{1-бензгидрил-3-[4-{[ (бензилсульфонил)амино]карбонил}-2-метоксибензил] -1H-индол-5-ил}карбамата;
c) циклопентил-N-{1-бензгидрил-3-[4-[{[ (2,4-диметил-1,3-тиазол-5-ил)сульфонил]амино}карбонил] -2-метоксибензил]-1H-индол-5-ил}карбамата;
d) циклопентил-N-{1-бензгидрил-3-[4-({[(3,5-диметил-4-изоксазолил)сульфонил] амино}карбонил)-2-метоксибензил]-1H-индол-5-ил}карбамата;
e) циклопентил-N-(3-{4-[({[5-(ацетиламино)-1,3,4-тиадиазол-2-ил]сульфонил}амино)карбонил]-2-метоксибензил}-1-бензгидрил-1H-индол-5-ил)карбамата;
f) циклопентил-N-{1-бензгидрил-3-[2-метокси-4-[({[4-(3-метил-5-оксо-4,5-дигидро-1H-пиразол-1-ил)фенил]сульфонил}амино)карбонил]бензил] -1H-индол-5-ил}карбамата;
g) N-{4-[(1-бензгидрил-5-нитро-1H-индол-3-ил)метил]-3-метоксибензоил}-2-метилбензолсульфонамида;
h) N-{4-[(1-бензгидрил-5-нитро-1H-индол-3-ил)метил]-3-метоксибензоил}(трифтор)метансульфонамида;
i) N-{4-[(1-бензгидрил-5-бром-1H-индол-3-ил)метил]-3-метоксибензоил}-2-метилбензолсульфонамида;
j) N-{4-[(1-бензгидрил-5-бром-1H-индол-3-ил)метил]-3-метоксибензоил}(трифтор)метансульфонамида;
или его фармацевтически приемлемая соль.
13. Соединение по п.1, которое выбирают из
a) N-{1-бензгидрил-3-[2-метокси-4-({[(трифторметил)сульфонил]амино}карбонил)бензил] -1H-индол-5-ил}циклопентанкарбоксамида;
b) N-{4-[(1-бензгидрил-5-[(метилсульфонил)амино]-1H-индол-3-ил)метил]-3-метоксибензоил} (трифтор)метансульфонамида;
c) N-{4-[(1-бензгидрил-5-{[(бутиламино)карбонил]амино}-1H-индол-3-ил)метил]-3-метоксибензоил}(трифтор)метансульфонамида;
d) N-{1-бензгидрил-3-[2-метокси-4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил] -1H-индол-5-ил}циклопентанкарбоксамида;
e) 4-[5-{[(циклопентилкарбонил)амино]-1-[фенил(2-пиридинил)метил]-1H-индол-3-ил}метил] -3-метоксибензойной кислоты;
f) N-[4-({ 1-бензгидрил-5-[(бензилсульфонил)амино]-1H-индол-3-ил}метил)-3-метоксибензоил](трифтор)метансульфонамида;
g) N-{1-бензгидрил-3-{ 2-метокси-4-[ {[(трифторметил)сульфонил]амино}карбонил]бензил}-1H-индол-5-ил}-3-тиофенкарбоксамида;
h) бензил-N-{1-бензгидрил-3-[2-метокси-4-({[(трифторметил)сульфонил]амино}карбонил)бензил] -1H-индол-5-ил}карбамата;
i) 4-[(1-бензгидрил-5-нитро-1H-индол-3-ил)метил]бензойной кислоты;
j) 4-[(1-бензгидрил-5-бром-1H-индол-3-ил)метил]бензойной кислоты;
k) 4-[(1-бензгидрил-5-{[(циклопентилокси)карбонил]амино}-1H-индол-3-ил)метил]бензойной кислоты или
l) циклопентил-N-{1-бензгидрил-3-[4-({[(2-метилфенил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
или его фармацевтически приемлемая соль.
14. Соединение по п.1, которое выбирают из
a) циклопентил-N-{1-бензгидрил-3-[4-({[(трифторметил)сульфонил]амино}карбонил)бензил]-1H-индол-5-ил}карбамата;
b) N-{4-[(1-бензгидрил-5-нитро-1H-индол-3-ил)метил]бензоил}(трифтор)метансульфонамида;
c) N-{4-[(1-бензгидрил-5-нитро-1H-индол-3-ил)метил]бензоил}-2-метилбензолсульфонамида;
d) N-{4-[(1-бензгидрил-5-бром-1H-индол-3-ил)метил]бензоил}-2-метилбензолсульфонамида;
e) N-{4-[(1-бензгидрил-5-бром-1H-индол-3-ил)метил]бензоил}(трифтор)метансульфонамида;
f) 3-({2-[1-(4-бензилбензил)-1H-индол-3-ил] -2-оксоацетил}амино)бензойной кислоты;
g) 3-({2-[1-(4-{[3,5-бис(трифторметил)фенокси]метил}бензил)-1H-индол-3-ил] -2-оксоацетил}амино)бензойной кислоты;
h) 3-({2-(1-бензгидрил-1H-индол-3-ил)-2-оксоацетил}амино)бензойной кислоты;
i) 3-({2-[1-[3-(4-бензилфенокси)пропил]-1H-индол-3-ил] -2-оксоацетил}амино)бензойной кислоты или
j) 3-({2-[1-[3,4-бис(бензилокси)бензил] -1H-индол-3-ил] -2-оксоацетил}амино)бензойной кислоты;
или его фармацевтически приемлемая соль.
15. Соединение по п.1, которое выбирают из
a) 3-({2-[1-[2-(бензилсульфонил)бензил] -1H-индол-3-ил] -2-оксоацетил}амино)бензойной кислоты;
b) 3-[({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}метил)амино]бензойной кислоты;
c) 2-[4-({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}метил)пиперазино]уксусной кислоты;
d) 2-[1-({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}метил)-3-оксо-2-пиперазинил]уксусной кислоты;
e) 2-[({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}метил)амино]-3-гидроксипропановой кислоты;
f) 2-[1-(4-бензилбензил)-5-(бензилокси)-1H-индол-3-ил]-2-оксоуксусной кислоты;
g) 2-{5-(бензилокси)-1-[2,4-бис(трифторметил)бензил]-1H-индол-3-ил} -2-оксоуксусной кислоты;
h) 3-({2-[1-(4-бензилбензил)-5-(бензилокси)-1H-индол-3-ил]-2-оксоацетил}амино)бензойной кислоты;
i) 5-[(2-{5-(бензилокси)-1-[2,4-бис(трифторметил)бензил]-1H-индол-3-ил} -2-оксоацетил)амино]изофталевой кислоты или
j) 3-[(2-{5-(бензилокси)-1-[2,4-бис(трифторметил)бензил]-1H-индол-3-ил} -2-оксоацетил)амино]бензойной кислоты;
или его фармацевтически приемлемая соль.
16. Соединение по п.1, которое выбирают из
a) 5-({2-[1-(4-бензилбензил)-5-(бензилокси)-1H-индол-3-ил]-2-оксоацетил} амино)-2-[(5-хлор-3-пиридинил)окси]бензойной кислоты;
b) 5-[(2-{5-(бензилокси)-1-[2,4-бис(трифторметил)бензил]-1H-индол-3-ил}-2-оксоацетил)амино]-2-[(5-хлор-3-пиридинил)окси]бензойной кислоты;
c) 2-[1-(4-бензилбензил)-5-(бензилокси)-1H-индол-3-ил]-N-({[(4-метилфенил)сульфонил]амино}карбонил)фенил-2-оксоацетамида;
d) 2-[5-бром-1-(циклопропилметил)-1H-индол-3-ил] уксусной кислоты;
e) 2-[1-(циклопропилметил)-5-(2-тиенил)-1H-индол-3-ил] уксусной кислоты;
f) 2-[1-(циклопропилметил)-5-[3-(трифторметил)фенил]-1H-индол-3-ил] уксусной кислоты;
g) 2-[5-(1-бензофуран-2-ил)-1-бензил-1H-индол-3-ил] уксусной кислоты;
h) 2-(1-бензил-5-фенил-1H-индол-3-ил)уксусной кислоты;
i) 4-{[5-((E)-{1-[3-(3-бензилфенокси)пропил]-1H-индол-3-ил}метилиден)-2,4-диоксо-1,3-тиазолан-3-ил]метил}бензойной кислоты или
j) 2-[5-((E)-{1-[3-(3-бензилфенокси)пропил]-1H-индол-3-ил}метилиден)-2,4-диоксо-1,3-тиазолан-3-ил]уксусной кислоты;
или его фармацевтически приемлемая соль.
17. Соединение по п.1, которое выбирают из
a) 3-{1-[3-(3-бензилфенокси)пропил]-1H-индол-3-ил}пропановой кислоты;
b) 3-{1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}пропановой кислоты;
c) N-(1-бензгидрил-3-{3-[(метилсульфонил)]-3-оксопропил}-1H-индол-5-ил)циклопентанкарбоксамида;
d) (E)-3-{1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}-2-пропеновой кислоты;
e) N-(1-бензгидрил-3-{(E)-3-[(метилсульфонил)амино]-3-оксо-1-пропенил}-1H-индол-5-ил)циклопентанкарбоксамида;
f) (E)-3-{1-бензгидрил-5-нитро-1H-индол-3-ил}-2-пропеновой кислоты;
g) N-((E)-3-{1-бензгидрил-5-нитро-1H-индол-3-ил}-2-пропеноил)метансульфонамида;
h) 4-{[1-бензгидрил-5-({[4-(трифторметил)фенил]сульфонил}амино)-1H-индол-3-ил]метил}-3-метоксибензойной кислоты;
i) 4-{[5-({[2-(ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил} амино)-1-бензгидрил-1H-индол-3-ил]метил}-3-метоксибензойной кислоты;
j) 4-[(1-бензгидрил-5-({(4-хлор-3-нитрофенил)сульфонил} амино)-1H-индол-3-ил)метил] -3-метоксибензойной кислоты;
или его фармацевтически приемлемая соль.
18. Соединение по п.1, которое выбирают из
a) 4-[(1-бензгидрил-5-{[(диметиламино)сульфонил]амино}-1-1H-индол-3-ил)метил] -3-метоксибензойной кислоты;
b) 4-[(1-бензгидрил-5-({[4-(трифторметокси)фенил]сульфонил}амино)-1H-индол-3-ил)метил] -3-метоксибензойной кислоты;
c) 4-[(1-бензгидрил-5-{[(2-метилфенил)сульфонил]амино}-1-1H-индол-3-ил)метил] -3-метоксибензойной кислоты;
d) 4-[(1-бензгидрил-5-{[(5-хлор-1,3-диметил-1H-пиразол-4-ил)сульфонил]амино}-1H-индол-3-ил)метил] -3-метоксибензойной кислоты;
e) 4-[(1-бензгидрил-5-{[(3,5-диметил-4-изоксазолил)сульфонил]амино}-1H-индол-3-ил)метил] -3-метоксибензойной кислоты;
f) циклопентил-N-{3-[4-(аминокарбонил)-2-метоксибензил]-1-бензгидрил-1H-индол-5-ил}карбамата;
g) циклопентил-N-{1-бензгидрил-3-[2-метокси-4-(1H-1,2,3,4-тетразол-5-ил)бензил]-1H-индол-5-ил}карбамата;
h) 4-[({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}карбонил)амино]-3-тиофенкарбоновой кислоты;
i) 3-[({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}карбонил)амино]бензойной кислоты;
j) 3-[({1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}карбонил)амино]пропановой кислоты;
или его фармацевтически приемлемая соль.
19. Соединение по п.1, которое выбирают из
a) N-[1-бензгидрил-3-({[(2-метилфенил)сульфонил]амино}карбонил)-1H-индол-5-ил]циклопентанкарбоксамида;
b) 3-[(2-{1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}-2-оксоацетил)амино]пропановой кислоты;
c) 3-[(2-{1-бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-ил}-2-оксоацетил)амино]бензойной кислоты или
d) 3-({2-[1-(4-бензилбензил)-5-(бензилокси)-1H-индол-3-ил]ацетил}амино)бензойной кислоты;
или его фармацевтически приемлемая соль.
20. Соединение по п.1, которое выбирают из
c) 2-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-2,6-диметилфенокси}уксусной кислоты;
d) 2-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-3-метоксифенокси}уксусной кислоты;
e) 2-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]фенокси}уксусной кислоты;
f) 2-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-3-хлорфенокси}уксусной кислоты;
g) 2-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-2-метоксифенокси}уксусной кислоты;
h) (E)-4-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]фенокси}-2-бутеновой кислоты;
i) 4-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]анилино}-4-оксобутановой кислоты или
j) натриевой соли 3-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]анилино}-3-оксопропановой кислоты;
или его фармацевтически приемлемая соль.
21. Соединение по п.1, которое выбирают из
a) 2-{4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]анилино}-2-оксоуксусной кислоты;
b) 2-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]циклопропанкарбоновой кислоты;
c) 2-[(1-бензгидрил-6-хлор-5-фтор-1H-индол-3-ил)метил]циклопропанкарбоновой кислоты;
d) 2-[(1-бензгидрил-5,6-дихлор-1H-индол-3-ил)метил]циклопропанкарбоновой кислоты;
e) 2-({1-бис(4-гидроксифенил)метил-6-хлор-1H-индол-3-ил}метил)циклопропанкарбоновой кислоты;
f) '4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-3-гидроксибензойной кислоты;
g) '4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-3-(3-гидроксипропокси)бензойной кислоты;
h) '4-({1-[(4-аминофенил)(фенил)метил]-6-хлор-1H-индол-3-ил}метил)-3-метоксибензойной кислоты;
i) '4-({6-хлор-1-[(4-метоксифенил)(фенил)метил]-1H-индол-3-ил}метил)-3-метоксибензойной кислоты;
j) '4-({1-бис[(4-метоксифенил)метил]-6-хлор-1H-индол-3-ил}метил)-3-метоксибензойной кислоты;
m) '4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-3-метоксибензойной кислоты или
n) 2-({4-[(1-бензгидрил-6-хлор-1H-индол-3-ил)метил]-3-метоксибензоил}амино)уксусной кислоты;
или его фармацевтически приемлемая соль.
22. Фармацевтическая композиция, содержащая соединение по п.1 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
23. Фармацевтическая композиция, содержащая соединение по п.5 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
24. Фармацевтическая композиция, содержащая соединение по п.6 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
25. Фармацевтическая композиция, содержащая соединение по п.7 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
26. Фармацевтическая композиция, содержащая соединение по п.8 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
27. Фармацевтическая композиция, содержащая соединение по п.9 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
28. Фармацевтическая композиция, содержащая соединение по п.10 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или наполнитель.
29. Способ лечения воспалений у млекопитающих, предусматривающий введение млекопитающему, нуждающемуся в таком лечении, фармацевтически эффективного количества соединения по п.1 или его фармацевтически приемлемой соли.
Текст
1 Настоящее изобретение относится к химическим ингибиторам активности различных фосфолипазных ферментов, а в частности ферментов типа фосфолипазы А 2. Предшествующий уровень техники Лейкотриены и простагландины являются важными медиаторами воспаления, и каждый из медиаторов этих классов участвует в развитии воспалительной реакции различным образом. Лейкотриены участвуют в рекрутинге участвующих в воспалении клеток, таких как нейтрофилы, в зону воспаления, стимулируют экстравазацию этих клеток и индуцируют высвобождение супероксида и протеаз, которые разрушают ткань. Лейкотриенты также играют определенную патофизиологическую роль в гиперчувствительности, обычно наблюдаемой у астматиков [см., В. Samuelson et al., Science, 237: 1171-76 (1987)]. Простагландины усиливают воспалительный процесс путем увеличения кровотока, и, тем самым, инфильтрации лейкоцитов на участках воспаления. Простагландины также потенциируют болевую реакцию, индуцируемую стимулятором. Простагландины и лейкотриены являются нестабильными и не сохраняются в клетках, но вместо этого они синтезируются [W.L. Smith,Biochem. J. 259:315-324 (1989)] из арахидоновой кислоты под действием стимулятора. Простагландины продуцируются из арахидоновой кислоты под действием ферментов СОХ-1 и СОХ 2. Арахидоновая кислота также является субстратом для ферментов, участвующих в различных каскадах ферментативных реакций, ведущих к продуцированию лейкотриенов. Арахидоновая кислота, которая обеспечивает эти два различных пути воспалительных реакций, высвобождается из sn-2-положения мембранных фосфолипидов под действием фосфолипазных ферментов А 2 (обозначаемых далее PLA2). Полагают, что реакция, катализируемая PLA2, представляет собой лимитирующую стадию в процессе опосредованного липидом биосинтеза и в продуцировании простагландинов и лейкотриентов, участвующих в воспалении. Если фосфолипидным субстратомPLA2 является субстрат класса фосфотидилхолинов с простой эфирной связью в положенииsn-1, то продуцируемым лизофосфолипидом является непосредственный предшественник фактора активации тромбоцитов (далее обозначаемого ФАТ) - другого сильного медиатора воспаления [S.I. Wasserman, Hospital Practice,15:49-58 (1988)]. Большинство схем противовоспалительной терапии направлено на предупреждение продуцирования либо простагландинов, либо лейкотриенов в этих различных каскадах реакций, но не того и другого вместе. Так, например, ибупрофен, аспирин и индометацин являются нестероидными противовоспалительными средствами (НСПВС), которые ингибируют продуци 003876 2 рование простагландинов под действием СОХ 1/СОХ-2, но не оказывают никакого влияния на продуцирование участвующих в воспалении лейкотиренов из арахидоновой кислоты, происходящее в других каскадах реакций. Напротив,зилейтон ингибирует лишь каскад реакций превращения арахидоновой кислоты в лейкотриен и не оказывает какого-либо влияния на продуцирование простагландинов. Ни один из этих широко используемых противовоспалительных агентов не влияет на продуцирование ФАТ. Поэтому предполагается, что прямое ингибирование активности PLA2 является эффективным механизмом для терапевтического агента,т.е. оно предотвращает продуцирование воспалительной реакции [см. J. Chang et al., Biochem.Pharmacol., 36:2429-2436 (1987)]. Семейство ферментов PLA2, которые характеризуются присутствием в них секвенированного сигнала секреции и которые в конечном счете секретируются из клетки, было секвенировано и структурно определено. Эти секретированные PLA2 имеют молекулярную массу 14 кДа и содержат семь дисульфидных связей, которые необходимы для их активности. Эти ферменты PLA2 были обнаружены в больших количествах в поджелудочной железе млекопитающих, в пчелином яде и в различных змеиных ядах [см., например, ссылки 13-15 в работе J.Chang et al., см. выше; и Е.А. Dennis, Drug Devel. Res., 10:205-220 (1987)]. Однако панкреатический фермент, как полагают, обеспечивает пищеварительную функцию, и как таковой он не должен играть важной роли в продуцировании медиаторов воспаления, которое (продуцирование) должно жестко регулироваться. Была определена первичная структура первой, не имеющей панкреатического происхождения PLA2 человека. Эта непанкреатическая PLA2 обнаружена в тромбоцитах, синовиальной жидкости и в селезенке и также является секретируемым ферментом. Этот фермент является членом вышеупомянутого семейства. [См.Biophys. Res. Comm., 163:42-48 (1989)]. Однако есть сомнения относительно того, что этот фермент играет важную роль в синтезе простагландинов, лейкотриенов и ФАТ, поскольку непанкреатическая PLA2 представляет собой внеклеточный белок, который трудно поддается регуляции, тогда как другие ферменты, участвующие в каскадах реакций биосинтеза этих соединений, представляют собой внутриклеточные белки. Более того, известно, что PLA2 регулируется белками протеинкиназы С и G [R. BurchJ. Axelrod, Proc. Natl. Acad. Sci. USA, 84:63746378 (1989)], представляющими собой цитозольные белки, которые должны воздействовать на внутриклеточные белки. Эта непанкреатическая PLA2 не может функциониро 3 вать в цитозоле, поскольку ее высокий восстановительный потенциал должен приводить к восстановлению дисульфидных связей и инактивированию фермента. Мышиная PLA2 была идентифицирована в линии макрофаговых клеток мышей, обозначенной RAW 264.7. Сообщалось, что удельная активность в 2 моль/мин/мг, резистентная к восстановительным условиям, ассоциирована с молекулой размером приблизительно 60 кДа. Однако этот белок не был очищен до гомогенности. [См. С.С. Leslie et al., Biochem. Biophys.Acta., 963:476-492 (1988)]. Работы, цитируемые выше и упомянутые в настоящем описании для сведения, приводятся для сообщения сведений относительно функций фосфолипазных ферментов, в частности PLA2. Была также идентифицирована и клонирована цитозольная фосфолипаза A2 (обозначаемая далее "cPLA2"). См. патенты США 5322776 и 5354677, которые во всей своей полноте упомянуты в настоящем описании для сведения. Фермент, описанный в этих патентах,является внутриклеточным ферментом PLA2,который был выделен из его природного источника или продуцирован каким-либо другим способом в очищенной форме, и который функционирует внутри клетки, продуцируя арахидоновую кислоту в ответ на стимулятор воспалительной реакции. В настоящее время желательно идентифицировать фармацевтически ценные соединения,ингибирующие действие этих фосфолипазных ферментов, в целях их использования для лечения или предупреждения воспалительных состояний, в частности, таких состояний, где ингибирование продуцирования простагландинов,лейкотриенов и ФАТ дает хорошие результаты. Идентификация таких противовоспалительных агентов, которые могут быть использованы для лечения ряда патологических состояний, все еще остается актуальной. Существует множество фактов, подтверждающих главную роль cPLA2 в биосинтезе липидных медиаторов, а именно, cPLA2 является единственным ферментом, который обладает высокой селективностью по отношению к фосфолипидам, содержащим арахидоновую кислоту в положении sn-2 (Clark et al., 1991, 1995; HanelGelb, 1993); активация cPLA2 или ее повышенная экспрессия оказалась связана с повышенным синтезом лейкотриенов и простагландинов (Lin et al., 1992 а, 1992b, 1993); и после активации cPLA2 происходит ее транслокация в ядерную мембрану, где она локализуется вместе с циклооксигеназой и липоксигеназой, что приводит к метаболизму арахидоната с образованием простагландинов и лейкотриенов (Schievellaet al., 1995; Glover et al., 1995). Хотя эти данные представляют большой интерес, однако, наиболее точное свидетельство о центральной роли 4 было получено в экпериментах на мышах, дефицитных по cPLA2 вследствие гомологичной рекомбинации (Uozumi et al., 1997; Bonventre etal., 1997). Перитонеальные макрофаги, полученные от этих животных, были неспособны продуцировать лейкотриены, простагландины или ФАТ. сРLА 2-дефицитные мыши также дали информацию о роли cPLA2 в развитии заболевания, поскольку эти мыши обнаруживают резистентность к бронхиальной гиперреактивности в модели анафилактического шока, использованной для имитации астмы (Uozumi et al., 1997). Таким образом, несмотря на обширность суперсемейства фосфолипазы A2, cPLA2 играет главную роль в продуцировании простагландинов,лейкотриенов и ФАТ.phospholipase A2. Nature 390, 622-625. Краткое описание изобретения Соединения настоящего изобретения имеют следующую формулу: где R1 и R1' независимо выбирают из Н, галогена, -СF3, -ОН, -C1-С 10 алкила, предпочтительноC1-С 6 алкокси, -CN, -NO2, -NH2, фенила, -Oфенила, -S-фенила, бензила, -O-бензила, -Sбензила; или кольцевых остатков в виде нижеуказанных групп а), b) или с), непосредственно связанных с индольным кольцом, либо связанных с индольным кольцом посредством мостикаa) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, изотиазол, изоксазол, пирролидин, пирролин, имидазолидин, пиразолидин, пиразол, пиразолин, имидазол, тетразол,оксатиазол, где указанное пятичленное гетероциклическое кольцо необязательно замещено 13 заместителями, выбранными из галогена, -C1 С 10 алкила, предпочтительно -C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN, -СF3 илиb) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиран, пиридин, пиразин, пиримидин, пиридазин, пиперидин, пиперазин, тетразин, тиазин, тиадиазин,оксазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, -C1-С 10 алкила, предпочтительно -C1-С 6aлкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; илиc) бициклической кольцевой группы, необязательно содержащей 1-3 кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваяся ими, бензофуран, хромен, индол, изоиндол, индолин, изоиндолин, нафталин,пурин, индолизин, индазол, хинолин, изохинолин, хинолизин, хиназолин, циннолин, фталазин или нафтиридин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, -C1 С 10 алкила, предпочтительно -C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-СНО, -NO2, -NH2, -CN, -СF3 или -ОН; илиR6 выбирают из членов группы, состоящей из Н, -СF3, -C1-С 10 алкила, предпочтительно -C1 С 6 алкила, C1-С 10 алкокси, предпочтительно C1 С 6 алкокси, фенила, -O-фенила, -S-фенила, бензила, -O-бензила или -S-бензила; где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1 С 6 алкила, C1-С 10 алкокси, предпочтительно C1 С 6 алкокси, -СНО, -NO2, -NH2, -CN, -СF3 илиR7 выбирают из членов группы, включающей -ОН, -СF3, C1-С 10 алкил, предпочтительноa) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничивась ими, фуран, пиррол, тиофен,имидазол, пиразол, изотиазол, изоксазол, пирролидин, пирролин, имидазолидин, пиразолидин, пиразол, пиразолин, имидазол, тетразол,оксатиазол, где указанное пятичленное гетероциклическое кольцо необязательно замещено 13 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиb) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиран, пиридин, пиразин, пиримидин, пиридазин, пиперидин, пиперазин, тетразин, тиазин, тиадиазин,оксазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; или с) бициклической кольцевой группы, содержащей 8-10 кольцевых атомов и необязательно содержащей 1-3 кольцевых гетероатома,выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол,изоиндол, индолин, изоиндолин, нафталин, пу 7 рин, индолизин, индазол, хинолин, изохинолин,хинолизин, хиназолин, циннолин, фталазин или нафтиридин, где указанная бициклическая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -СНО, -NO2,-NH2, -CN, -СF3 или -ОН;n представляет целое число от 0 до 3; или группы, выбранной из групп формулы -L1M1; где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(СН 2)n-, -S-, -О-, -С(О)-, -(СН 2)nС(O)-, -(СН 2)n-С(O)-(СН 2)n-, -(СН 2)n-O-(СН 2)n-,(СН 2)n-S-(CH2)n-, -C(Z)-N(R6)-, -C(Z)-N(R6)(CH2)n-, -С(О)-С(Z)-N(R6)-, -C(O)-C(Z)-N(R6)(CH2)n, -C(Z)-NH-SO2- или -С(Z)-NH-SO2(CH2)n-; М 1 выбирают из группы, состоящей изR11 выбирают из Н, низшего C1-С 6 алкила,C1-С 6 циклоалкила, -СF3, -СООН, -(СН 2)n-СООН,-(СН 2)n-С(O)-СООН, при условии, что вся группа в 3-положении индола или индолина, образованная любой комбинацией R3, L1, M1, R8, R9, R10 и/или R11, содержит, по крайней мере, одну кислотную часть, выбранную из следующих групп или содержащую их: карбоновой кислоты, тетразола или группы формулыR8 в каждом случае независимо выбирают из Н, -СООН, -(СН 2)n-СООН, -(СН 2)n-С(O)СООН, тетразола,n представляет целое число от 0 до 3;L2 обозначает связывающую или мостикобразующую группу формулы -(CH2)n-,-S-,-O-,-С(О)-, -(CH2)n-C(O)-, -(CH2)n-C(O)-(CH2)n-,-(СН 2)n-O-(СН 2)nилиM2 выбирают из а) группы, состоящей из низшего C1 С 6 алкила, низшего C1-С 6 алкокси, C3-С 10 циклоалкила, фенила или бензила, причем указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -NO2, -NH2, -CN или -СF3, илиb) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, изотиазол, изоксазол, пирролидин, пирролин, имидазолидин, пиразолидин, пиразол, пиразолин, имидазол, тетразол,оксатиазол, где указанное пятичленное гетероциклическое кольцо необязательно замещено 13 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиc) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиран, пиридин, пиразин, пиримидин, пиридазин, пиперидин, пиперазин, тетразин, тиазин, тиадиазин,оксазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещенно 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; илиd) бициклической кольцевой группы, содержащей от 8 до 10 атомов в кольце и необязательно содержащей 1-3 кольцевых гетероатома,выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол,изоиндол, индолин, изоиндолин, нафталин, пурин, индолизин, индазол, хинолин, изохинолин,хинолизин, хиназолин, циннолин, фталазин или нафтиридин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-СНО, -NO2, -NH2, -CN, -СF3 или -ОН;R5 выбирают из низшего C1-С 6 алкила,низшего C1-С 6 алкокси, (CH2)n-C3-С 10 циклоалкила,-(CH2)n-S-(CH2)n-C3-С 10 циклоалкила,(CH2)n-O-(СН 2)n-C3-С 10 циклоалкила или групп где n представляет целое число от 0 до 3,предпочтительно от 1 до 3, а более предпочтительно от 1 до 2,Y представляет С 3-С 6 циклоалкил, фенил,бифенил, каждый из которых необязательно замещен 1-3 группами, выбранными из галогена, С 1-С 10 алкила, предпочтительно С 1-С 6 алкила,С 1-С 10 алкокси, предпочтительно С 1-С 6 алкокси,-NO2, -NH2, -CN или -СF3; илиa) пятичленное гетероциклическое кольцо,содержащее один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, изотиазол, изоксазол, пирролидин, пирролин, имидазолидин, пиразолидин, пиразол, пиразолин, имидазол, тетразол,оксатиазол, где указанное пятичленное гетероциклическое кольцо необязательно замещено 13 заместителями, выбранными из галогена, С 1 С 10 алкила, предпочтительно С 1-С 6 алкила, С 1 С 10 алкокси, предпочтительно С 1-С 6 алкокси,-NO2, -NH2, -CN, -СF3, или одним фенильным кольцом, необязательно замещенным 1-3 заместителями, выбранными из галогена, С 1 С 10 алкила, предпочтительно С 1-С 6 алкила, С 1 С 10 алкокси, предпочтительно С 1-С 6 алкокси,-NO2, -NH2, -CN, -СF3, илиb) шестичленное гетероциклическое кольцо, содержащее один, два или три кольцевых гетероатома, выбранных из N, S или О, включая,но не ограничиваясь ими, пиран, пиридин, пиразин, пиримидин, пиридазин, пиперидин, пиперазин, тетразин, тиазин, тиадиазин, оксазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 13 заместителями, выбранными из галогена, С 1 С 10 алкила, предпочтительно С 1-С 6 алкила, С 1 С 10 алкокси, предпочтительно С 1-С 6 алкокси,-СНО, -NO2, -NH2, -CN, -СF3 или -ОН; илиc) бициклическую кольцевую группу, содержащую от 8 до 10 атомов в кольце и необязательно содержащую 1-3 кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол, изоиндол, индолин, изоиндолин, нафталин,пурин, индолизин, индазол, хинолин, изохино 11 лин, хинолизин, хиназолин, циннолин, фталазин или нафтиридин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, С 1 С 10 алкила, предпочтительно С 1-С 6 алкила, С 1 С 10 алкокси, предпочтительно С 1-С 6 алкокси,-СНО, -NO2, -NH2, -CN, -СF3 или -ОН; где D представляет Н, низший С 1-С 6 алкил, низший С 1-С 6 алкокси, -СF3 или -(СН 2)n-СF3; В и С независимо выбирают из фенильной,пиридинильной, пиримидинильной, фурильной,тиенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, а предпочтительно 1-2 заместителями, выбранными из Н, галогена, -CN,-СНО,-СF3,-ОН, -С 1 С 6 алкила, С 1-С 6 алкокси, -NH2, N(С 1-С 6)2, NH(С 1-С 6), -N-C(O)-(С 1-С 6), -NO2-, или 5- или 6 членным гетероциклическим или гетероароматическим кольцом, содержащим 1 или 2 гетероатома, выбранных из О, N или S, таким как, например, морфолино; или фармацевтически приемлемые соли указанных соединений. Одна группа соединений настоящего изобретения включает те соединения, в которых индол или индолин в 2-положении (R4) замещен только водородом, а заместители в других положениях индола или индолина являются такими, как описано выше. Другой R3 представляет -L1-M1, где L1 определен выше, а более предпочтительно L1 представляет химическую связь, а М 1 представляет группу где R9 определен как указано выше. Другая группа соединений настоящего изобретения включает соединения, в которых R2 и R4 представляют водород, а группы R1, R1', R3 и R5 являются такими, как определено выше. В эту группу входят две дополнительные предпочтительные группы. В первой группе, R1 находится в 5-положении индола или индолина, а во второй группе, R1 находится в 6-положении индола или индолина. В еще одной предпочтительной группе соединений, описанной в настоящей заявке, R1 находится в 5-положении индола или индолина и представляет бензилокси, R2 и R4 представляют водород, а R3 и R5 являются такими, как определено выше. Более предпочтительными соединениями настоящего изобретения являются соединения следующей формулы:R6 выбирают из Н, -С 1-С 6 алкила, С 1 С 6 алкокси, фенила, -O-фенила, бензила, -Oбензила; где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, С 1 С 6 алкила, С 1-С 6 алкокси, -NO2, -NH2, -CN, -СF3 или -ОН;R7 выбирают из -ОН, -СF3, С 1-С 6 алкила,С 1-С 6 алкокси,-NH-(С 1-С 6 алкила),-N-(С 1 С 6 алкила)2, пиридинила, тиенила, фурила, пирролила, фенила, -O-фенила, бензила, -Oбензила, пиразолила и тиазолила, где кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, -CN, С 1 С 6 алкила, С 1-С 6 алкокси, -NO2, -NH2, -СF3 или или группы, выбранной из групп формулы -L1M1; где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(CH2)n-, -S-, -О-, -С(О)-, -(CH2)nC(O)-, (CH2)n-C(O)-(CH2)n-, (СН 2)n-O-(СН 2)n-,(СН 2)n-S-(СН 2)n-, -C(Z)-N(R6)-, -C(Z)-N(R6) 13R8 в каждом случае независимо выбирают из H, -СООН, -(СН 2)n-COOH, -(СН 2)n-С(O)СООН, тетразола,R11 выбирают из Н, низшего C1-С 6 алкила,C1-С 6 циклоалкила, -СF3, -СООН, -(СН 2)n-СООН,-(СН 2)n-С(O)-СООН, при условии, что вся группа в 3-положении индола или индолина, образованная любой ком 003876 14 бинацией R3, L1, M1, R8, R9, R10 и/или R11, содержит, по крайней мере, одну кислотную часть, выбранную из следующих групп или содержащих их: карбоновой кислоты, тетразола или группы формулыn представляет целое число от 0 до 3;R4 выбирают из Н, -СF3, низшего C1 С 6 алкила, низшего C1-С 6 алкокси, C3-С 10 циклоалкила, C1-С 6 алкил-C3-С 10 циклоалкила, -СНО,галогена или группы формулы -L2-M2:L2 обозначает связывающую или мостикобразующую группу формул -(СН 2)n-, -S-, -О-,-С(O)-,-(СН 2)n-С(O)-,(СН 2)n-С(O)-(СН 2)n-,(СН 2)n-O-(СН 2)n- или (СН 2)n-S-(СН 2)n-; М 2 выбирают из группы, состоящей из низшего -C1-С 6 алкила, низшего C1-С 6 алкокси,C3-С 10 циклоалкила, фенила или бензила, причем указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиa) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, пирролидин или тетразол,где указанное пятичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -NO2, -NH2, -CN или -СF3, илиb) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиридин,пиримидин, пиперидин, пиперазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-СНО, -NO2, -NH2, -CN, -СF3 или -ОН; илиc) бициклической кольцевой группы, содержащей от 8 до 10 кольцевых атомов и необязательно содержащей 1-3 кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, индол, индолин, нафталин, пурин или хинолин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительноR5 выбирают из низшего C1-С 6 алкила,низшего C1-С 6 алкокси, (СН 2)n-С 3-С 10 циклоалки 15 ла, (СН 2)n-S-(СН 2)n-С 3-С 10 циклоалкила, (СН 2)nO-(СН 2)n-С 3-С 10 циклоалкила или групп, выбранных из а) -(СН 2)n-фенил-O-фенила, -(СН 2)n-фенилСН 2-фенила,-(СН 2)n-O-фенил-СН 2-фенила,-(СН 2)n-фенил-(O-СН 2-фенила)2,-СН 2-фенилС(О)-бензотиазола или группы формулы где n представляет целое число от 0 до 3,предпочтительно от 1 до 3, а более предпочтительно от 1 до 2; Y представляет С 3 С 5 циклоалкил, фенил, бензил, нафтил, пиридинил, хинолил, фурил, тиенил, пирролил, бензотиазол и пиримидинил, причем кольца этих групп необязательно замещены 1-3 заместителями, выбранными из Н, галогена, -СF3, -ОН,C1-С 6 алкила, C1-C6 алкокси, -CN, -NH2, -NО 2 или пятичленного гетероциклического кольца, содержащего один гетероатом, выбранный из N, S или О, а предпочтительно S или О; или где D представляет Н, низший C1-С 6 алкил, низший C1-С 6 алкокси, -СF3 или -(СН 2)n-СF3; В и С независимо выбирают из фенильной,пиридинильной, пиримидинильной, фурильной,тиенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, а предпочтительно 1-2 заместителями, выбранными из Н, галогена, -СF3, -ОН, C1-С 6 алкила, C1 С 6 алкокси, -NH2 или -NO2; или их фармацевтически приемлемая соль. Одна группа соединений настоящего изобретения включает те соединения, в которых индол или индолин в 2-положении (R4) замещен только водородом, а заместители в других положениях индола или индолина являются такими, как определено выше. В другой предпочтительной группе соединений настоящего изобретения, R1 находится в 5-или 6-положении индола или индолина и представляет циклопентилкарбоксамид или циклопентилоксикарбониламино, R2 и R4 представляют водород, а R3 и R5 являются такими,как определено выше. Следующая предпочтительная группа соединений настоящего изобретения включает R1 и R2 в 5- или 6-положении индола или индолина, и каждый из них выбирают из группы, состоящей из C1-С 6 алкокси, циано, сульфонила или галогена, R2 и R4 представляют водород, а 16 Другая группа соединений настоящего изобретения включает соединения, в которых R2 и R4 представляют водород, a R1, R3 и R5 являются такими, как определено выше. В эту группу входят две другие предпочтительные группы. В первой группе R1 находится в 5-положении индола или индолина, а во второй группе R1 находится в 6-положении индола или индолина. Еще в одной предпочтительной группе соединений, описанной в настоящей заявке, R1 находится в 5-положении индола или индолина и представляет бензилокси, R2 и R4 представляют водород, а R3 и R5 являются такими, как определено выше. Предпочтительной группой соединений настоящего изобретения являются соединения следующих формул:R6 выбирают из Н, C1-С 6 алкила, C1 С 6 алкокси, фенила, -O-фенила, бензила, -Oбензила, где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 6 алкила, C1-С 6 алкокси, -NH2, -NO2, -СF3 илиR7 выбирают из -СF3, C1-С 6 алкила, C1 С 6 алкокси, -NH-(C1-С 6 алкила), -N-(C1-С 6 алкила)2, пиридинила, тиенила, фурила, пирролила,фенила, -O-фенила, бензила, -O-бензила, пиразолила и тиазолила, где кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С 6 алкила, C1 С 6 алкокси, -NH2, -NO2, -СF3 или -ОН; или группы, выбранной из группы формулы -L1M1; где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(СН 2)n-, -S-, -О-, -С(О)-, -(СН 2)nС(О)-, (СН 2)n-С(O)-(СН 2)n-, (СН 2)n-O-(СН 2)n-,(СН 2)n-S-(СН 2)n-, -C(Z)-N(R6)-, -C(Z)-N(R6)(СН 2)n-, -С(О)-С(Z)-N(R6)-, -C(O)-C(Z)-N(R6)(СН 2)n, -C(Z)-NH-SO2- или -С(Z)-NH-SO2(СН 2)n-;R8, в каждом случае, независимо выбирают из Н, -СООН, -(СН 2)n-СООН, -(СН 2)n-С(O)СООН, тетразола,R11 выбирают из Н, низшего C1-С 6 алкила,C1-С 6 циклоалкила, -СF3; -СООН, -(СН 2)n-СООН,-(СН 2)n-С(O)-СООН, при условии, что вся группа в 3-положении индола или индолина, образованная любой комбинацией R3, L1, M1, R8, R9, R10 и/или R11, содержит, по крайней мере, одну кислотную часть, выбранную из следующих групп или содержащих их: карбоновой кислоты, тетразола или группы формулыn представляет целое число от 0 до 3;R4 выбирают из Н, -СF3, низшего C1 С 6 алкила, низшего C1-С 6 алкокси, C3-С 10 циклоалкила, C1-С 6 алкил-C3-С 10 циклоалкила, -СНО,галогена или группы формулы -L2-M2:L2 обозначает связывающую или мостикобразующую группу формул -(CH2)n-, -S-, -О-,-С(O)-,-(CH2)n-C(O)-,(CH2)n-C(O)-(CH2)n-,(CH2)n-O-(CH2)n- или (CH2)n-S-(CH2)n-; М 2 выбирают из группы, состоящей изa) низшего -C1-С 6 алкила, низшего C1 С 6 алкокси, C3-С 10 циклоалкила, фенила или бензила, где указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиb) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, пирролидин или тетразол,где указанное пятичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -NO2, -NH2, -CN или -СF3, илиc) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиридин,пиразин, пиримидин, пиперидин, пиперазин, 19 тиазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -CHO, -NO2, -NH2, -CN,-СF3 или -ОН; илиd) бициклической кольцевой группы, содержащей от 8 до 10 кольцевых атомов и необязательно содержащей 1-3 кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол,изоиндол, индолин, изоиндолин, нафталин, пурин, хинолин или изохинолин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1 С 6 алкила, C1-С 10 алкокси, предпочтительно C1 С 6 алкокси, -CHO, -NO2, -NH2, -CN, -СF3 илиR5 выбирают из низшего C1-С 6 алкила,низшего C1-С 6 алкокси, (СН 2)n-C3-С 5 циклоалкила, (CH2)n-S-(СН 2)n-C3-С 5 циклоалкила, (СН 2)n-O(СН 2)n-С 3-С 5 циклоалкила или групп, выбранных из а) -(СН 2)n-фенил-O-фенила, -(СН 2)n-фенилСН 2-фенила,-(СН 2)n-O-фенил-СН 2-фенила,-(СН 2)n-фенил-(O-СН 2-фенила)2,-СН 2-фенилС(О)бензотиазола или группы формул где n представляет целое число от 0 до 3, предпочтительно от 1 до 3, а более предпочтительно от 1 до 2, Y представляет С 3-С 5 циклоалкил, фенил, бензил, нафтил, пиридинил, хинолил, фурил, тиенил, пирролил, бензотиазол или пиримидинил, причем кольца этих групп необязательно замещены 1-3 заместителями, выбранными из Н, галогена, -СF3, -ОН, C1-С 6 алкила,C1-С 6 алкокси, -NH2, -NO2 или пятичленного гетероциклического кольца, содержащего один гетероатом, выбранный из N, S или О, а предпочтительно S или О; или где D представляет Н, низший C1-С 6 алкил, низший C1-С 6 алкокси, -(СН 2)n-СF3 или -СF3; В и С независимо выбирают из фенильной,пиридинильной, пиримидинильной, фурильной,тиенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, а предпочтительно, 1-2 заместителями, выбранными 20 из Н, галогена, -СF3, -ОН, -C1-С 6 алкила, C1 С 6 алкокси, -NH2 или -NO2-; или их фармацевтически приемлемая соль. Из группы соединений, описанных выше,предпочтительными являются соединения, в которых заместитель R1 находится в 5 положении индольного или индолинового кольца, а другие заместители определены, как указано выше. Другой предпочтительной группой соединений настоящего изобретения являются соединения следующих формул:R6 выбирают из Н, C1-С 6 алкила, C1 С 6 алкокси, фенила, -O-фенила, бензила, -Oбензила, где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 6 алкила, C1-С 6 алкокси, -NO2, -СF3 или -ОН;R7 выбирают из -СF3, C1-С 6 алкила, C1 С 6 алкокси, -NH-(C1-С 6 алкила), -N-(C1-С 6 алкила)2, пиридинила, тиенила, фурила, пирролила,фенила, -O-фенила, бензила, -O-бензила, пиразолила и тиазолила, где кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С 6 алкила, C1 С 6 алкокси, -NH2, -NO2, -СF3 или -ОН; или группы, выбранной из группы формулы -L1M1; где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(СН 2)n-, -S-, -О-, -С(О)-, -(СН 2)nС(O)-, (СН 2)n-С(O)-(СН 2)n-, (СН 2)n-O-(СН 2)n-,(СН 2)n-S-(СН 2)n-, -C(Z)-N(R6)-, -C(Z)-N(R6)(СН 2)n-, -С(О)-С(Z)-N(R6)-, -C(O)-C(Z)-N(R6)(СН 2)n, -C(Z)-NH-SO2- или -C(Z)-NH-SO2(СН 2)n-;R8 в каждом случае независимо выбирают из Н, -СООН, -(СН 2)n-СООН, -(СН 2)n-С(O)СООН, тетразола,R11 выбирают из Н, низшего C1-С 6 алкила,C1-С 6 циклоалкила, -СF3; -СООН, -(СН 2)n-СООН,-(СН 2)n-С(O)-СООН, при условии, что вся группа в 3-положении индола или индолина, образованная любой комбинацией R3, L1, M1, R8, R9, R10 и/или R11, содержит, по крайней мере, одну кислотную часть, выбранную из следующих групп или содержащую их: карбоновой кислоты, тетразола или группы формулыn представляет целое число от 0 до 3;L2 обозначает связывающую или мостикобразующую группу формул -(CH2)n-, -S-, -О-,-С(O)-,-(CH2)n-C(O)-,(CH2)n-C(O)-(CH2)n-,(CH2)n-O-(CH2)n- или (CH2)n-S-(CH2)n-; М 2 выбирают из группы, состоящей из(а) низшего C1-С 6 алкила, низшего C1 С 6 алкокси, C3-С 10 циклоалкила, фенила или бензила, где указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиb) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, пирролидин или тетразол,где указанное пятичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -NO2, -NH2, -CN или -СF3, илиc) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиридин, 23 пиразин, пиримидин, пиперидин, пиперазин,тиазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; илиd) бициклической кольцевой группы, содержащей от 8 до 10 кольцевых атомов, и необязательно содержащей 1-3 кольцевых гетероатома, выбранных из N, S или О, включая но не ограничиваясь ими, бензофуран, хромен, индол, изоиндол, индолин, изоиндолин, нафталин,пурин, хинолин или изохинолин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1 С 6 алкила, C1-С 10 алкокси, предпочтительно C1 С 6 алкокси, -СНО, -NO2, -NH2, -CN, -СF3, илиR5 выбирают из низшего C1-С 6 алкила,низшего C1-С 6 алкокси, -(СН 2)n-С 3-С 5 циклоалкила или -(CH2)n-A, -(CH2)n-S-A или (СН 2)n-O-А,где А выбирают изR12 представляет Н, низший C1-С 6 алкил,низший C1-С 6 алкокси или -СF3; или их фармацевтически приемлемая соль. Другие соединения настоящего изобретения имеют следующую формулу:R6 выбирают из Н, C1-С 6 алкила, C1 С 6 алкокси, фенила, -O-фенила, бензила, -Oбензила, где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 6 алкила, C1-С 6 алкокси, -NH2, -NO2, -СF3 илиR7 выбирают из -СF3, C1-С 6 алкила, C1 С 6 алкокси, -NH-(C1-С 6 алкила), -N-(C1-С 6 алкила)2, пиридинила, тиенила, фурила, пирролила,фенила, пиразолила, тиазолила, -O-фенила, бензила или -O-бензила, где кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С 6 алкила, C1 С 6 алкокси, NO2, -NH2, -СF3 или -ОН;R3 выбирают из -СООН, -С(O)-СООН,-(СН 2)n-С(О)-СООН, -(СН 2)n-СООН, -СН=СНСООН, -(СН 2)n-тетразола, или группы, выбранной из групп формулы -L1 М 1 или L2-M2:L1 обозначает мостикобразующую или связывающую группу, выбранную из химической связи, -(CH2)n-, -S-, -О-, -С(О)-, -(СН 2)nС(O)-, (СН 2)n-С(O)-(СН 2)n-, (СН 2)n-O-(СН 2)n-,(СН 2)n-S-(СН 2)n-, -C(Z)-N(R6)-, -C(Z)-N(R6)(СН 2)n-, -С(О)-С(Z)-N(R6)-, -C(O)-C(Z)-N(R6)(СН 2)n, -C(Z)-NH-SO2- или -С(Z)-NH-SO2(СН 2)n-;L2 представляет мостикобразующую или связывающую группy, выбранную из химической связи, -S-, -О-, -С(О)-, -(СН 2)n-С(О)-,(СН 2)n-С(О)-(СН 2)n-, (СН 2)n-O-(СН 2)n-, (СН 2)n-S(СН 2)n-,-С(Z)-N(R6)-,-C(Z)-N(R6)-(СН 2)n-,-C(O)-C(Z)-N(R6)-,-С(О)-С(Z)-N(R6)-(СН 2)n,-C(Z)-NH-SO2- или -C(Z)-NH-SO2-(СН 2)n-; М 2 представляет группуR8 в каждом случае независимо выбирают из Н, -СООН, -(СН 2)n-COOH, -(СН 2)n-С(O)СООН, тетразола,R11 выбирают из Н, низшего C1-С 6 алкила,C1-С 6 циклоалкила, -СF3; -СООН, -(СН 2)n-СООН,-(СН 2)n-С(O)-СООН, при условии, что вся группа в 3-положении индола или индолина, образованная любой комбинацией R3, L1, M1, L2, M2, R8, R9, R10 и/или R11,содержит, по крайней мере, одну кислотную часть, выбранную из следующих групп или со 003876 26 держащую их: карбоновой кислоты, тетразола или группы формулыn представляет целое число от 0 до 3;R4 выбирают из Н, -СF3, низшего C1 С 6 алкила, низшего C1-С 6 алкокси, C3-С 10 циклоалкила, C1-С 6 алкил-C3-С 10 циклоалкила, -СНО,галогена или группы формулы -L3-М 3:L3 обозначает связывающую или мостикобразующую группу формул -(CH2)n-, -S-, -О-,-С(O)-,-(CH2)n-С(O)-,(CH2)n-С(O)-(CH2)n-,(CH2)n-O-(CH2)n- или (CH2)n-S-(CH2)n-; М 3 выбирают из группы, состоящей из(а) низшего C1-С 6 алкила, низшего C1 С 6 алкокси, C3-С 10 циклоалкила, фенила или бензила, где указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиb) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, пирролидин или тетразол,где указанное пятичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -NO2, -NH2,-CN, или -СF3, илиc) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиридин,пиразин, пиримидин, пиперидин, пиперазин,тиазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; илиd) бициклической кольцевой группы, содержащей от 8 до 10 кольцевых атомов и необязательно содержащей 1-3 кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол,изоиндол, индолин, изоиндолин, нафталин, пурин, хинолин или изохинолин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1 С 6 алкила, C1-С 10 алкокси, предпочтительно C1 С 6 алкокси, -СНО, -NO2, -NH2, -CN, -СF3, илиR5 выбирают из низшего C1-С 6 алкила,низшего C1-С 6 алкокси, -(CH2)n-С 3-С 5 циклоалки 27 ла, -(CH2)n-S-(CH2)n-С 3-С 5 циклоалкила, -(CH2)nO-(CH2)n-С 3-С 5 циклоалкила или групп а) -(CH2)n-фенил-О-фенила, -(CH2)n-фенилСН 2-фенила,-(CH2)n-O-фенил-СН 2-фенила,-(CH2)n-фенил-(O-СН 2-фенила)2,-СН 2-фенилС(О)бензотиазола или группы формулы где n представляет целое число от 0 до 3,предпочтительно от 1 до 3, более предпочтительно от 1 до 2; Y представляет С 3C5 циклоалкил, фенил, бензил, нафтил, пиридинил, хинолил, фурил, тиенил, пирролил, бензотиазол или пиримидинил, причем кольца этих групп необязательно замещены 1-3 заместителями, выбранными из Н, галогена, -СF3, -ОН,C1-С 6 алкила, C1-С 6 алкокси, -NH2, -NO2 или пятичленного гетероциклического кольца, содержащего один гетероатом, выбранный из N, S или О, предпочтительно, S или О; или где D представляет Н, низший C1-С 6 алкил, низший C1-С 6 алкокси, -СF3 или -(CH2)n-СF3; В и С независимо выбирают из фенильной,пиридинильной, пиримидинильной, фурильной,тиенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, предпочтительно 1-2 заместителями, выбранными из Н,галогена, -СF3, -ОН, C1-С 6 алкила, C1-С 6 алкокси,-NH2 или -NO2-; или фармацевтически приемлемая соль вышеописанных соединений. Другой предпочтительной группой соединений настоящего изобретения являются соединения следующей формулы: 28 бензила, где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 6 алкила, C1-С 6 алкокси, NH2-, -NO2, -СF3 илиR7 выбирают из -СF3, C1-С 6 алкила, C1 С 6 алкокси, -NH-(C1-С 6 алкила), -N-(C1-С 6 алкила)2, пиридинила, тиенила, фурила, пирролила,фенила, -O-фенила, бензила, -O-бензила, пиразолила и тиазолила, где кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1-С 6 алкила, C1 С 6 алкокси, -NO2, -NH2, -СF3 или -ОН;n представляет целое число от 0 до 3;R4 выбирают из Н, -СF3, низшего C1 С 6 алкила, низшего C1-С 6aлкокси, C3-С 10 циклоалкила, C1-С 6 алкил-C3-С 10 циклоалкила, -СНО,галогена или группы формулы -L2-M2;L2 обозначает связывающую или мостикобразующую группу формул -(CH2)n-, -S-, -О-,-С(O)-,-(CH2)n-C(O)-,(CH2)n-C(O)-(CH2)n-,(CH2)n-O-(CH2)n- или (CH2)n-S-(CH2)n-; М 2 выбирают из группы, состоящей из(а) низшего С 1-С 6 алкила, низшего С 1 С 6 алкокси, С 3-С 10 циклоалкила, фенила или бензила, где указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, С 1 С 10 алкила, предпочтительно С 1-С 6 алкила, С 1 С 10 алкокси, предпочтительно С 1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиb) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, пирролидин или тетразол,где указанное пятичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, С 1-С 10 алкила,предпочтительно С 1-С 6 алкила, С 1-С 10 алкокси,предпочтительно С 1-С 6 алкокси, -NO2, -NH2, -CN или -СF3, илиc) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиридин,пиразин, пиримидин, пиперидин, пиперазин,тиазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещение 1-3 заместителями, выбранными из галогена, С 1-С 10 алкила, предпочтительно С 1-С 6 алкила, С 1-С 10 алкокси, предпочтительно С 1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; илиd) бициклической кольцевой группы, содержащей от 8 до 10 кольцевых атомов и необязательно содержащей 1-3 кольцевых гетероатомов, выбранных из N, S или О, включая,но не ограничиваясь ими, бензофуран, хромен,индол, изоиндол, индолин, изоиндолин, нафталин, пурин, хинолин или изохинолин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, С 1-С 10 алкила, предпочтительно С 1-С 6 алкила, С 1-С 10 алкокси, предпочтительно С 1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3, или -ОН;R5 выбирают из низшего С 1-С 6 алкила,низшего С 1-С 6 алкокси, -(СН 2)n-С 3-С 5 циклоалкила или -(CH2)n-A, -(СН 2)n-S-А или (СН 2)n-O-А,где А выбирают изR12 представляет Н, низший С 1-С 6 алкил,низший С 1-С 6 алкокси или -СF3; или их фармацевтически приемлемая соль. Соединения настоящего изобретения имеют следующую формулу:R6 выбирают из Н, С 1-С 6 алкила, С 1 С 6 алкокси, фенила, -O-фенила, бензила, -Oбензила, где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, С 1 С 6 алкила, С 1-С 6 алкокси, -NO2, -NH2, -СF3 илиR7 выбирают из -СF3, С 1-С 6 алкила, С 1 С 6 алкокси, -NH-(С 1-С 6 алкила), -N-(С 1-С 6 алкила)2, пиридинила, тиенила, фурила, пирролила,фенила, пиразолила, тиазолила, -O-фенила, бензила или -O-бензила, причем кольца этих групп необязательно замещены 1-3 заместителями,выбранными из галогена, С 1-С 6 алкила, С 1 С 6 алкокси, -NO2, -NH2, -СF3 или -ОН;R11 выбирают из Н, низшего C1-С 6 алкила,С 1-С 6 циклоалкила, -СF3; -СООН, -(CH2)n-СООН,-(CH2)n-С(O)-СООН, или группы, выбранной из групп формулы -L1M1: где L1 представляет мостикобразующую или связывающую группу, выбранную из химической связи, -(CH2)n-, -S-, -О-, -С(О)-, -(CH2)nС(O)-, -(CH2)n-C(O)-(CH2)n-, -(CH2)n-O-(CH2)n-,(CH2)n-S-(CH2)n-, -C(Z)-N(R6)-, -C(Z)-N(R6)(CH2)n-, -С(О)-С(Z)-N(R6)-, -C(O)-C(Z)-N(R6)(CH2)n, -C(Z)-NH-SO2- или -С(Z)-NH-SO2(CH2)n-;R8 в каждом случае независимо выбирают из Н, -СООН, -(CH2)n-СООН, -(CH2)n-С(O)СООН, тетразола,R9 выбирают из Н, галогена, -СF3, -ОН,-СООН, -(CH2)n-СООН, -(CH2)n-С(О)-СООН, C1 при условии, что вся эта группа в 3 положении индола или индолина, образованная любой комбинацией R3, L1, M1, R8, R9, R10 и/илиR11, содержит, по крайней мере, одну кислотную часть, выбранную из следующих групп или содержащих их: карбоновой кислоты, тетразола или группы формулыn представляет целое число от 0 до 3;R4 выбирают из Н, -СF3, низшего C1 С 6 алкила, низшего C1-С 6 алкокси, C3-С 10 циклоалкила, C1-С 6 алкил-C3-С 10 циклоалкила, -СНО,галогена или группы формулы -L2-M2:L2 обозначает связывающую или мостикобразующую группу формул -(CH2)n-,-S-, -O-,-C(O)-,-(CH2)n-C(O)-,-(CH2)n-C(O)-(CH2)n,(CH2)n-O-(CH2)n или(а) низшего C1-С 6 алкила, низшего C1 С 6 алкокси, C3-С 10 циклоалкила, фенила или бензила, где указанные циклоалкильное, фенильное или бензильное кольца необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 10 алкила, предпочтительно C1-С 6 алкила, C1 С 10 алкокси, предпочтительно C1-С 6 алкокси,-NO2, -NH2, -CN или -СF3, илиb) пятичленного гетероциклического кольца, содержащего один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, пирролидин или тетразол,где указанное пятичленное гетероциклическое 33 кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила,предпочтительно C1-С 6 алкила, C1-С 10 алкокси,предпочтительно C1-С 6 алкокси, -NO2, -NH2, -CN или -СF3, илиc) шестичленного гетероциклического кольца, содержащего один, два или три кольцевых гетероатома, выбранных из N, S или О,включая, но не ограничиваясь ими, пиридин,пиразин, пиримидин, пиперидин, пиперазин,тиазин или морфолин, где указанное шестичленное гетероциклическое кольцо необязательно замещено 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -NO2, -NH2, -CN,-СF3 или -ОН; илиd) бициклической кольцевой группы, содержащей от 8 до 10 кольцевых атомов и необязательно содержащей 1-3 кольцевых гетероатомов, выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол,изоиндол, индолин, изоиндолин, нафталин, пурин, хинолин или изохинолин, где указанная бициклическая кольцевая группа необязательно замещена 1-3 заместителями, выбранными из галогена, C1-С 10 алкила, предпочтительно C1 С 6 алкила, C1-С 10 алкокси, предпочтительно C1 С 6 алкокси, -СНО, -NO2, -NH2, -CN, СF3 илиR5 выбирают из -(CH2)n-S-(CH2)n-С 3 С 5 циклоалкила, -(CH2)n-O-(CH2)n-С 3-С 5 циклоалкила или групп а) -(CH2)n-фенил-O-фенила, -(CH2)n-фенилСН 2-фенила,-(CH2)n-O-фенил-СН 2-фенила,-(CH2)n-фенил-(O-СН 2-фенила)2,-СН 2-фенилС(О)бензотиазола или группы формулы 34 от 1 до 2; Y представляет нафтил, пиридинил,хинолил, фурил, тиенил, пирролил, бензотиазол или пиримидинил, причем кольца этих групп необязательно замещены 1-3 заместителями,выбранными из Н, галогена, -СF3, -ОН, C1 С 6 алкила, C1-С 6 алкокси, -NH2, -NO2 или пятичленного гетероциклического кольца, содержащего один гетероатом, выбранный из N, S или О, а предпочтительно S или О; или с) группы формулы -(CH2)n-A, -(CH2)n-S-A или -(CH2)n-O-А, где А представляет группу где D представляет Н, низший C1-С 6 алкил, низший C1-С 6 алкокси, -(CH2)n-СF3 или СF3; В и С независимо выбирают из фенильной,пиридинильной, пиримидинильной, фурильной,тиенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, а предпочтительно 1-2 заместителями, выбранными из Н, галогена, -СF3, -ОН, C1-С 6 алкила, C1 С 6 алкокси, -NН 2 или -NO2-; или фармацевтически приемлемая соль вышеописанных соединений. Еще в одной предпочтительной группе соединений в рамках подкласса, описанного выше, R1 представляет бензилокси, a R4, R3 и R5 являются такими, как определено выше. Другой предпочтительной группой соединений настоящего изобретения являются соединения формулы где n представляет целое число от 0 до 3,предпочтительно от 1 до 3, более предпочтительно от 1 до 2; Y представляет С 3-С 5 циклоалкил, фенил, бензил, нафтил, пиридинил, хинолил, фурил, тиенил, пирролил, бензотиазол или пиримидинил, причем кольца этих групп необязательно замещены 1-3 заместителями,выбранными из Н, галогена, -СF3, -ОН, C1 С 6 алкила, C1-С 6 алкокси, -NO2, -NH2 или пятичленного гетероциклического кольца, содержащего один гетероатом, выбранный из N, S или О, а предпочтительно S или О; илиb) группы формулы где n представляет целое число от 0 до 3, предпочтительно от 1 до 3, более предпочтительноR6 выбирают из Н, C1-С 6 алкила, C1 С 6 алкокси, фенила, -O-фенила, бензила, -Oбензила, где фенильное и бензильное кольца этих групп необязательно замещены 1-3 заместителями, выбранными из галогена, C1 С 6 алкила, C1-С 6 алкокси, -NH2, -NO2, -СF3 илиR7 выбирают из -СF3, C1-С 6 алкила, C1 С 6 алкокси, -NH-(C1-С 6 алкила), -N-(C1-С 6 алкила)2, пиридинила, тиенила, фурила, пирролила,фенила, -O-фенила, бензила, -O-бензила, пиразолила или тиазолила, где кольца этих групп необязательно замещены 1-3 заместителями,выбранными из галогена, C1-С 6 алкила, C1 С 6 алкокси, -NH2, -NO2, -СF3 или -ОН;R8 и R9 независимо выбирают из Н, галогена, -СF3, -ОН, -СООН, -(CH2)n-СООН, -(CH2)nC(O)-COOH, -C1-С 6 алкила, -О-С 1-С 6 алкила,-NH(C1-С 6 алкила) или N(C1-С 6 алкила)2;n представляет целое число от 0 до 3;R5 выбирают из низшего C1-С 6 алкила,низшего C1-С 6 алкокси, -(CH2)n-С 3-С 5 циклоалкила или групп-С(О)-О-(CH2)n-С 3-С 5 циклоалкила,(CH2)n-фенила, (CH2)n-S-фенила, -(CH2)n-фенилO-фенила, -(CH2)n-фенил-СН 2-фенила, -(CH2)nO-фенил-СН 2-фенила,-(CH2)n-фенил-(O-СН 2 фенила)2,С(О)-O-фенила,С(О)-O-бензила,С(О)-O-пиридинила, С(О)-O-нафтила, (CH2)n-Sнафтила, (CH2)n-S-пиридинила, (CH2)n-пиридинила или (CH2)n-нафтила, где фенильные, пиридинильное и нафтильные кольца этих групп необязательно замещены 1-3 заместителями,выбранными из Н, галогена, -СF3, -ОН, C1 С 6 алкила, C1-С 6 алкокси, -NH2 или -NO2-; или где D представляет Н, низший C1-С 6 алкил, низший C1-С 6aлкокси или -СF3; В и С независимо выбирают из фенильной,пиридинильной, фурильной, тиенильной или пирролильной групп, каждая из которых необязательно замещена 1-3, а предпочтительно 1-2 заместителями, выбранными из Н, галогена,-СF3, -ОН, C1-С 6 алкила, C1-С 6 алкокси, -NH2 или-NO2-; или их фармацевтически приемлемая соль. Подробное описание изобретения Используемые здесь термины "арил" и"замещенный арил" означают моноциклические,в частности, пяти- и шестичленные моноциклические, ароматические и гетероароматические кольцевые группы и бициклические ароматические и гетероароматические кольцевые группы,в частности, группы, имеющие от 9 до 10 атомов в кольце. Подразумевается, что такими арильными группами являются фенильные кольца, включая кольца, находящиеся в фенокси-, бензильной, бензилокси-, бифенильной группах и в других таких группах. Арильной и гетероарильной группами настоящего изобретения также являются следующие группы:a) пятичленное гетероциклическое кольцо,содержащее один или два кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, фуран, пиррол, тиофен,имидазол, пиразол, изотиазол, изоксазол, пирролидин, пирролин, имидазолидин, пиразолидин, пиразол, пиразолин, имидазол, тетразол или оксатиазол; илиb) шестичленное гетероциклическое кольцо, содержащее один, два или три кольцевых гетероатома, выбранных из N, S или О, включая,но не ограничиваясь ими, пиран, пиридин, пиразин, пиримидин, пиридазин, пиперидин, пиперазин, тетразин, тиазин, тиадиазин, оксазин или морфолин; илиc) бициклическая кольцевая группа, необязательно содержащая 1-3 кольцевых гетероатома, выбранных из N, S или О, включая, но не ограничиваясь ими, бензофуран, хромен, индол, 37 изоиндол, индолин, изоиндолин, нафталин, пурин, индолизин, индазол, хинолин, изохинолин,хинолизин, хиназолин, циннолин, фталазин или нафтиридин. Термин "замещенные арильные" группы настоящего изобретения означает группы, необязательно замещенные 1-3 заместителями,выбранными из галогена, C1-С 10 алкила, предпочтительно C1-С 6 алкила, C1-С 10 алкокси, предпочтительно C1-С 6 алкокси, -СНО, -СООН или их сложных эфиров, -NO2, -NH2, -CN, -СF3 или-ОН или их комбинаций, таких как, -СН 2 СF3,-NН(СН 3) и т.п. Предпочтительный более узкий набор этих необязательно замещенных групп, как только что описано, составляют группы, образованные из бензольного, пиридинового, нафтиленового или хинолинового колец. Другими предпочтительными группами являются группы, образованные из фуранового, пирролового, тиофенового, пиримидинового и морфолинового колец. Из бициклических ароматических колец, предпочтительными являются бензофурановое, индоловое, нафталиновое и хинолиновое кольца. Алкильные, алкенильные и алкинильные группы, упоминаемые в настоящем описании,означают группы, которые имеют от 1 до 10, а предпочтительно от 1 до 6 атомов углерода и которые могут быть прямыми, разветвленными или циклическими группами. Если это не оговорено особо, то предпочтительными группами являются прямые или разветвленные группы. Галогенами, упоминаемыми в настоящем описании, являются F, Cl, Вr и I. Используемый в настоящем описании термин "фосфолипазная ферментативная активность" означает положительную активность в испытании на метаболизм фосфолипидов (предпочтительно, в одном из испытаний, описанных ниже в примере 116). Говорят, что соединение"имеет фосфолипазную ферментативную ингибирующую активность", если оно ингибирует активность фосфолипазы (предпочтительно,cPLA2) в любом доступном испытании (предпочтительно, в испытании, описанном ниже в примере 116 или примере 117) на ферментативную активность. В предпочтительных вариантах осуществления изобретения, соединение имеет(1) величину IC50 менее чем около 25 мкМ,предпочтительно менее чем около 6 мкМ, в анализе LysoPC; (2) величину IC50 менее чем около 50 мкМ в везикулярном анализе; (3) величинуIC50 менее чем около 1 мкМ, в анализе на PMN;(4) величину IC50 менее чем около 15 мкМ, в анализе с использованием кумарина; и/или (5) измеряемую активность (предпочтительно, по крайней мере, примерно 5% уменьшение отека,более предпочтительно, по крайней мере, примерно 10% снижение, еще более предпочтительно, по крайней мере, примерно 15% снижение, а наиболее предпочтительно 20-30% сни 003876 38 жение отека) в тесте на крысах с отеком подушечки лапы, индуцированным каррагенаном. Соединения настоящего изобретения могут быть использованы для ингибирования активности фосфолипазного фермента (предпочтительно cPLA2), а следовательно, они могут быть использованы для "лечения" (т.е. лечения,предупреждения или ослабления) воспалительных или ассоциированных с воспалением реакций или состояний (например, ревматоидного артрита, псориаза, астмы, воспалительных заболеваний кишечника и других заболеваний, опосредованных простагландинами, лейкотриенами или ФАТ), а также других состояний, таких как остеопороз, колит, миелогенный лейкоз, диабет,истощение и атеросклероз. Настоящее изобретение относится как к фармацевтическим композициям, так и к терапевтическим методам лечения или применения этих композиций, предусматривающим использование соединений настоящего изобретения. Соединения настоящего изобретения могут быть использованы в фармацевтической композиции в комбинации с фармацевтически приемлемым носителем. Такая композиция может также содержать (помимо соединения или соединений настоящего изобретения и носителя) разбавители, наполнители, соли, буферы,стабилизаторы, солюбилизаторы и другие соединения, хорошо известные специалистам. Термин "фармацевтически приемлемый" относится к нетоксическому веществу, которое не влияет на эффективность биологически активного действия активного ингредиента(ов). Свойства указанного носителя зависят от способа введения. Данная фармацевтическая композиция может, кроме того, содержать другие противовоспалительные агенты. Такие другие факторы и/или агенты могут быть включены в фармацевтическую композицию для достижения синергического эффекта с использованием соединений настоящего изобретения, или для минимизации побочных эффектов, вызываемых соединениями настоящего изобретения. Фармацевтическая композиция настоящего изобретения может быть изготовлена в форме липосомы, в которых соединения настоящего изобретения, помимо других фармацевтически приемлемых носителей, объединены с амфипатическими агентами, такими как, липиды, которые находятся в агрегированной форме, такой как, мицеллы, нерастворимые монослои, жидкие кристаллы или ламеллярные слои в водном растворе. Подходящими липидами для липосомной композиции являются, без ограничения ими,моноглицериды, диглицериды, сульфатиды,лизолецитин, фосфолипиды, сапонин, желчные кислоты и т.п. Получение таких липосомных препаратов доступно любому специалисту и описано, например, в патенте США 4235871,в патенте США 4501728, в патенте США 39 4837028 и в патенте США 4737323, все из которых упомянуты здесь для сведения. Используемый здесь термин "терапевтически эффективное количество" означает полное количество каждого активного компонента, которое используется в фармацевтической композиции или в методе, и которое является достаточным для достижения благоприятного воздействия на пациента, т.е. для лечения, заживления, профилактики или ослабления воспалительной реакции или воспалительного состояния, либо для ускорения достижения результатов лечения, заживления, профилактики или облегчения указанных состояний. При использовании определенного активного ингредиента,вводимого отдельно, этот термин означает лишь один ингредиент. При использовании комбинации активных ингредиентов, этот термин означает объединенное количество активных ингредиентов, которые благоприятствуют терапевтическому эффекту, независимо от того, вводятся ли они в комбинации, последовательно или одновременно. При осуществлении способа лечения или применения согласно настоящему изобретению,терапевтически эффективное количество соединения настоящего изобретения вводят млекопитающему в состоянии, требующем такого лечения. Соединения настоящего изобретения могут быть введены в соответствии со способом настоящего изобретения либо отдельно, либо в комбинации с другими способами терапии, такими как, лечение с применением других противовоспалительных агентов, цитокинов, лимфокинов или других гемопоэтических факторов. При совместном введении с одним или несколькими другими противовоспалительным(и) агентом(ами), цитокином(ами), лимфокином(ами) или другим(и) гемопоэтическим(и) фактором(ами), соединения настоящего изобретения могут быть введены либо одновременно с другим противовоспалительным(и) агентом(ами),цитокином(ами), лимфокином(ами) или другим(и) гемопоэтическим(и) фактором(ами),тромболитическими или антитромботическими факторами, либо последовательно. Если введение осуществляют последовательно, то лечащий врач сам назначает соответствующий порядок введения соединений настоящего изобретения в комбинации с другим противовоспалительным агентом(ами),цитокином(ами),лимфокином(ами) или другим(и) гемопоэтическим(и) фактором(ами), тромболитическими или антитромботическими факторами. Введение соединений настоящего изобретения, используемых в фармацевтической композиции или в способе настоящего изобретения,может быть осуществлено рядом стандартных способов, таких как пероральное введение, ингаляция или чрескожные, подкожные или внутривенные инъекции. 40 При пероральном введении терапевтически эффективного количества соединений настоящего изобретения, эти соединения могут быть изготовлены в виде таблеток, капсул, порошка, раствора или эликсира. При введении фармацевтической композиции настоящего изобретения в форме таблетки, эта фармацевтическая композиция может, кроме того, содержать твердый носитель, такой как, желатин, или адъювант. Таблетка, капсула и порошок содержат от около 5 до 95% соединения настоящего изобретения, а предпочтительно от около 25 до 90% соединения настоящего изобретения. При введении фармацевтической композиции настоящего изобретения в жидкой форме может быть добавлен жидкий носитель, такой как вода,вазелиновое масло, масло животного или растительного происхождения, такое как арахисовое масло, минеральное масло, соевое масло, кунжутное масло, или синтетические масла. Жидкая форма фармацевтической композиции может, кроме того, содержать физиологический раствор, раствор декстрозы или раствор другого сахарида, либо гликоли, такие как этиленгликоль, пропиленгликоль или полиэтиленгликль. При введении фармацевтической композиции настоящего изобретения в жидкой форме, эта фармацевтическая композиция содержит от около 0,5 до 90 мас.% соединения настоящего изобретения, а предпочтительно от около 1 до 50% соединения настоящего изобретения. При введении терапевтически эффективного количества соединений настоящего изобретения путем внутривенной, чрескожной или подкожной инъекции, эти соединения могут быть изготовлены в форме апирогенного парентерально приемлемого водного раствора. Получение таких парентерально приемлемых белковых растворов, имеющих соответствующие рН,изотоничность, стабильность и т.п., может быть осуществлено квалифицированным специалистом. Предпочтительные фармацевтические композиции для внутривенных, чрескожных или подкожных инъекций должны, помимо соединений настоящего изобретения, содержать изотонический носитель, такой как раствор хлорида натрия для инъекций, раствор Рингера, декстрозный раствор для инъекций, раствор для инъекций, содержащий декстрозу и хлорид натрия, лактатсодержащий раствор Рингера или другой носитель, известный специалистам. Фармацевтическая композиция настоящего изобретения может также содержать стабилизаторы, консерванты, буферы, антиоксиданты или другие добавки, известные специалистам. Количество соединения(й) настоящего изобретения в фармацевтической композиции настоящего изобретения зависит от природы и тяжести состояния, подвергаемого лечению, и от конкретных заболеваний пациента, которыми он страдал ранее. И, наконец, лечащий врач может самостоятельно установить дозу соедине 41 ния настоящего изобретения, необходимую для лечения каждого отдельного пациента. Сначала лечащий врач может назначить низкие дозы соединения настоящего изобретения, а затем понаблюдать за реакцией организма пациента. После этого могут быть назначены большие дозы соединения настоящего изобретения и так далее, вплоть до достижения терапевтического эффекта, оптимального для данного пациента,после чего эту дозу больше не увеличивают. Предполагается, что для осуществления способа настоящего изобретения, различные фармацевтические композиции должны содержать от около 0,1 мкг до около 100 мг (предпочтительно, от около 0,1 до около 50 мг, а более предпочтительно от около 1 до около 2 мг) соединения настоящего изобретения на один кг веса тела пациента. Продолжительность внутривенной терапии с использованием фармацевтической композиции настоящего изобретения может варьироваться в зависимости от тяжести заболевания,подвергаемого лечению, и от состояния и потенциального идиосинкразического ответа каждого отдельного пациента. Предполагается, что продолжительность каждого введения соединений настоящего изобретения должно варьироваться в пределах от 12 до 24 ч непрерывного внутривенного введения. И, наконец, лечащий врач может самостоятельно установить соответствующую продолжительность внутривенной терапии с использованием фармацевтической композиции настоящего изобретения. Соединения настоящего изобретения могут быть получены в соответствии со способами и примерами, описанными ниже. В нижеследующих примерах описан синтез предпочтительных соединений настоящего изобретения. Способ А. Индол может быть алкилирован в положении С 3 соответствующим алкилбромидом при обработке льюисовой кислотой, такой как окись серебра (I) или тетрафторборат серебра в растворителе, таком как диоксан или ТГФ при повышенных температурах 50-100 С. Альтернативно, он может быть алкилирован двухстадийным способом путем обработки индола нбутиллитием (n-BuLi) в растворителе, таком как ТГФ или эфир, а затем ZnCl2, с последующим концентрированием и обработкой соответствующим алкилирующим агентом в различных растворителях, таких как ТГФ, эфир, толуол или бензол. Азот индола может быть затем алкилирован путем обработки сильным основанием,таким как бис(триметилсилил)амид натрия, нBuLi, гидрид натрия или гидрид калия в растворителе, таком как ДМФА, ДМСО или ТГФ с последующей обработкой алкилгалогенидом. Сложный эфир может быть гидролизован в щелочных условиях гидроксидом натрия в воде и метаноле и ТГФ. Альтернативно, он может быть расщеплен путем обработки тиометилатом на 003876 42 трия в растворителе, таком как ТГФ или ДМФА,при повышенных температурах (50-100 С). Полученную кислоту подвергают реакции сочетания с сульфонамидом с помощью различных связующих реагентов, таких как DCC, EDCI или карбонилдиимидазол в растворителе, таком как ТГФ, дихлорметан, дихлорэтан или ДМФА в присутствии основания, такого как триэтиламин и/или N,N-диметилпиридин. В случае, еслиR1=нитро, эта нитрогруппа может быть восстановлена путем обработки Pt/C в присутствии водорода в растворителе, таком как метанол,этилацетат или ТГФ. Полученный амин может быть ацилирован или сульфирован под действием соответствующего агента в присутствии основания, такого как триэтиламин, бикарбонат натрия или пиридин в двухфазной системе растворителей, такой как метиленхлорид:вода (1:1) или ТГФ:вода (1:1), или в однофазном органическом растворителе, таком как метиленхлорид,ТГФ или ДМФА с триэтиламином. Затем полученная кислота может быть гидролизована и модифицирована, как описано выше. В случаеR1=Br, он может быть замещен с помощью медной соли нужного нуклеофила, такой как тиометилат, метилат или сульфиновая кислота. Способ А 43 Способ В. Индолглиоксалилхлорид может быть подвергнут реакции с нужным сложным аминоэфиром в двухфазной системе с метиленхлоридом и насыщенным бикарбонатом натрия или в однофазной системе с растворителем, таким как метиленхлорид, этилацетат или ТГФ, и основанием, таким как триэтиламин, основание Хьюнигса или пиридин. Индол у атома азота затем может быть алкилирован с использованием ряда алкилирующих реагентов в растворителе, таком как ДМФА, ДМСО или ТГФ, и основания, такого как гидрид натрия,н-BuLi или бис(триметилсилил)амид калия. Затем этот сложный эфир может быть гидролизован гидроксидом натрия или гидроксидом лития в системе растворителей, такой как смесь вода: метанол:ТГФ. Способ В Способ С. 3-Карбоксииндол получают восстановительным аминированием путем конденсации альдегида со сложным аминоэфиром в растворителе, таком как метиленхлорид или дихлорэтан, с уксусной кислотой или без нее. Полученный имин восстанавливают in situ с использованием восстановителя, такого как борогидрид натрия, цианоборогидрид натрия или триацетоксиборогидрид натрия. Затем получают кислоту путем гидролиза полученного сложного эфира гидроксидом натрия или гидроксидом лития в системе растворителей, такой как смесь вода:метанол:ТГФ. Способ С 44 Способ D. 5-Бензилоксииндол может быть обработан основанием, таким как метиловый или этиловый реактив Гриньяра, и ацилирован в 3-положении этилоксалилхлоридом в подходящем растворителе, таком как эфир или ТГФ. Азот индола затем может быть алкилирован бензилбромидом под действием основания, такого как гидрид натрия или н-бутиллитий в растворителе, таком как ТГФ или ДМФА. Затем этот сложный эфир гидролизуют в основных условиях гидроксидом натрия или гидроксидом тетрабутиламмония в подходящей системе растворителей, такой как смесь вода:МеОН:ТГФ. Затем может быть проведена реакция сочетания соответствующего сложного аминоэфира с использованием связывающего агента, такого как DCC или EDCI, в растворителе, таком как метиленхлорид, ТГФ или ДМФА. Целевая кислота может быть выделена путем гидролиза сложного эфира в условиях, описанных выше. Способ D Способ Е. Индол-3-уксусную кислоту алкилируют соответствующим алкилбромидом, а затем подвергают реакции сочетания Сузуки с использованием Рd(РРh3)4 в качестве катализатора в смешанном растворителе (смесь этанол-бензолвода) при повышенной температуре с получением 1-алкил-5-замещенного индола. Способ Е Способ F. В результате алкилирования атома азота соединения I с использованием соответствующего основания, такого как гидрид натрия или карбонат калия, и алкилгалогенида получают альдегид II. Этот альдегид может быть превращен в тиазолидиндион III с использованием основания, такого как пиперидин, и выделен с помощью кислоты, такой как уксусная кислота. В результате депротонирования с использованием соответствующего основания, такого как 45 гидрид натрия, и алкилирования атома азота тиазолидиндиона с использованием выбранных электрофилов, таких как алкил- или бензилгалогенидов получают такие соединения, как соединение IV. Способ F Способ G. Нитроиндол I превращают в ненасыщенный сложный эфир посредством реакции Хорнера-Виттига с триметоксифосфоноацетатом в подходящем растворителе, таком как тетрагидрофуран. Восстановление нитрогруппы II может быть осуществлено путем гидрирования в присутствии палладия-на-угле в атмосфере водорода и ацилирования полученного амина в условиях реакции Шоттена-Баумана с получением амидов, таких как соединение III. В результате омыления сложноэфирной функциональной группы получают кислоту-индол IV. Способ G Способ Н. 5-Хлор-2-метилиндол может быть подвергнут восстановительному алкилированию в 3-положении с использованием соответствующего альдегида в присутствии кислоты, такой как трифторуксусная кислота, и восстановителя,такого как триэтилсилан, в подходящем растворителе, таком как метиленхлорид, с получением сложного эфира II. Атом азота может быть алкилирован путем обработки подходящим основанием, таким как гидрид натрия и дифенилбромметан, и полученное соединение III может быть подвергнуто омылению с получением соединения IV. Способ I. В исходный индол вводят функциональную группу в положение С 3 путем либо реакции с ДМФА/РОСl3, либо реакции магниевой соли индола с метилоксалилхлоридом. Затем полученные сложные эфиры и альдегиды подвергают N-алкилированию путем обработки различными алкилгалогенидами соли индола,образованной посредством обработки индола сильным основанием. В случае альдегидов, гдеr представляет нитрогруппу, эту нитрогруппу восстанавливают до амина с использованиемPt/C и Н 2 или смеси ацетата меди/борогидрида натрия, а затем ацилируют с использованием различных хлорангидридов, изоцианатов, хлорформиатов или подвергают восстановительному алкилированию с использованием альдегидов и триацетоксиборогидрида натрия. Затем эти альдегиды могут быть окислены до нужной кислоты, которая может быть подвергнута реакции сочетания с аминоалкиловыми или ариловыми сложными эфирами методом сочетания с использованием EDCI или посредством вначале превращения этой кислоты в хлорангидрид под действием оксалилхлорида, а затем реакции этого хлорангидрида с аминоалкиловым или ариловым сложным эфиром. После этого их гидролизуют с получением конечного продукта. Сложные эфиры, полученные как описано выше, могут быть обработаны аналогичным способом. Сложный эфир может быть гидролизован, а затем подвергнут реакции сочетания с аминоалкиловыми или ариловыми сложными эфирами методом сочетания с применениемEDCI или путем вначале превращения кислоты в хлорангидрид под действием оксалилхлорида,а затем реакции этого хлорангидрида с аминоалкиловым или ариловым сложным эфиром. После этого проводят гидролиз с получением конечного продукта. Способ I(а) Способ J. Исходный амин обрабатывают различными сульфонилхлоридами в присутствии пиридина, а затем избыток сульфонилхлорида удаляют путем добавления связанного с полимером амина. Затем нужные продукты гидролизуют с использованием гидроксида натрия в смеси ТГФ/МеОН, и реакционную смесь подкисляют с использованием смолы IR-120 с получением нужных продуктов. Способ J Способ К. Исходный индол подвергают бисалкилированию путем добавления сильного основания,такого как гидрид натрия, а затем алкилирующего агента, такого как алкил- или арилгалогенид, после чего полученный сложный эфир подвергают гидролизу с использованием гидроксида натрия в смеси ТГФ/МеОН. После этого кислоту подвергают реакции сочетания со сложным алкиловым или ариловым аминоэфиром, а затем гидролизуют с получением нужной кислоты. Пример 1. 4-[(5-[(Циклопентилокси)карбонил]амино-1-пропил-1H-индол-3-ил)метил]3-метоксибензойная кислота. Стадия 1. К раствору 5-нитроиндола (21,24 г, 131 ммоль) в диоксане (128 мл) в реакционном сосуде, обернутом алюминиевой фольгой, добавляли окись серебра (I) (30,34 г, 131 ммоль, 1,5 экв.) и метил-4-(бромметил)-3-метоксибензоат(34 г, 131 ммоль) и эту смесь доводили до 60 С и перемешивали в течение 20 ч. Реакционную смесь охлаждали, фильтровали через целит, растворяли в этилацетате (500 мл), промывали солевым раствором (2 х 50 мл), сушили (MgSO4) и фильтровали. Неочищенный продукт очищали с помощью хроматографии на двуокиси кремния(15% этилацетат/гексаны) с получением нужного продукта (5,8 г, 55%). Стадия 2. С 3-алкилированный индол (1,5 г, 4,4 ммоль) растворяли в 15 мл ТГФ. В отдельной колбе суспендировали NaH (185 г, 4,61 ммоль) в 25 мл ТГФ при 0 С. Раствор исходного продукта вводили через канюлю в суспензию NaH с получением темно-красного раствора. Затем этот раствор оставляли на 10 мин при комнатной температуре при перемешивании. После этого добавляли 1-иодпропан (0,47 мл, 1,1 ммоль) и реакционную смесь оставляли на ночь при комнатной температуре для прохождения реакции. Так как реакция не была завершена(ТСХ), то добавляли еще 0,5 мл 1-иодпропана, и реакция продолжалась еще 3 ч. ТСХ не показывала никаких изменений, и реакционную смесь выливали в холодную 1 н. НСl и экстрагировали СН 2 Сl2 (3 х 75 мл). Объединенные органические слои сушили над MgSO4, фильтровали и выпаривали с получением неочищенного N-алкилированного нитроиндола. Неочищенный продукт абсорбировали на двуокись кремния и загружали в колонку с силикагелем. Эту колонку элюировали 100% CH2Cl2 с получением чистого желтого N-алкилированного нитроиндола (0,96 г,57%). Стадия 3.N-алкилированный нитроиндол (0,95 г) растворяли в 40 мл безводного ТГФ. Эту систему продували аргоном. К прозрачному желтому раствору добавляли Pt/C (0,462 г). Затем аргон удаляли путем откачивания и в эту систему вводили водород. Реакционную смесь перемешивали в течение 6,5 ч. После этого водород откачивали и через систему продували аргон. Реакци 49 онную смесь фильтровали через целит с ТГФ. Растворитель удаляли на роторном испарителе с получением неочищенного амина в виде темного масла. После хроматографии (5% этилацетат/СН 2 Сl2) получали нужный продукт (0,7 г,80%). Стадия 4. Амин, полученный в вышеуказанной стадии (0,7 г), растворяли в 40 мл СН 2 Сl2. Затем добавляли 4-метилморфолин (0,3 мл, 3,0 ммоль) и циклопентилхлорформиат (383 мг, 2,57 ммоль) и получали желто-оранжевый раствор. Реакционную смесь оставляли на 3 ч при комнатной температуре для прохождения реакции. Затем реакционную смесь подкисляли 1 н. НСl и смесь экстрагировали 50 мл СН 2 Сl2. Объединенные органические фазы промывали солевым раствором, сушили над MgSO4, фильтровали и концентрировали с получением неочищенного карбамата. Неочищенный продукт абсорбировали на силикагеле и загружали в колонку с силикагелем. Колонку элюировали 100% СН 2 Сl2 с получением нужного продукта (0,87 г, 39%) в виде желтой пены. Стадия 5. Карбамат (0,831 г) растворяли раствором для гидролиза (ТГФ:МеОН:2 н. NaOH=2:1:1), и реакционную смесь оставляли на 5,25 ч для прохождения реакции. Реакционную смесь подкисляли до рН 2 путем добавления 2 н. НСl и экстрагировали CH2Cl2. Органический слой промывали водой и солевым раствором. Затем объединенные органические слои сушили над МgSО 4, фильтровали и выпаривали с получением неочищенной кислоты, которую перекристаллизовывали из CH2Cl2, в результате чего получали целевое соединение (0,575 г, 71%) в виде розовых кристаллов. МС: m/z (M-1) 449. Пример 2. Циклопентил-N-3-[2-метокси 4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1-пропил-1 Н-индол-5-илкарбамат. Стадия 1. Промежуточный 5-нитроиндол получали как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. 50 Пример 3. 4-[(1-Бензгидрил-5-[(циклопентилокси)карбонил]амино-1 Н-индол-3-ил) метил]-3-метоксибензойная кислота. Стадия 1. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. Пример 4. 4-[5-[(Циклопентилокси)карбонил]амино-1-(2-нафтилметил)-1H-индол-3 ил]метил-3-метоксибензойная кислота. Стадия 1. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. МС: m/z (M-1) 547. Пример 5. 4-[5-[(Циклопентилокси)карбонил]амино-1-(циклопропилметил)-1H-индол 3-ил]метил-3-метоксибензойная кислота. Стадия 1. Промежуточный 5-нитроиндол получали,как описано в примере 1, стация 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. 51 Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. МС: m/z (M-1) 461. Пример 6. 4-[5-[(Циклопентилокси)карбонил]амино-1-(4-пиридинилметил)-1H-индол 3-ил]метил-3-метоксибензойная кислота. Стадия 1. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. Пример 7. 4-[5-[(Циклопентилокси)карбонил]амино-1-изопропил-1 Н-индол-3-ил] метил-3-метоксибензойная кислота. Стадия 1. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. МС: m/z (M-1) 449. Пример 8. 4-[(1-Циклопентил-5-[(циклопентилокси)карбонил]амино-1 Н-индол-3-ил) метил]-3-метоксибензойная кислота. Стадия 1. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3, с использованием вышеуказанного промежуточного соединения. 52 Стадия 3. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 4. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. МС: m/z (M-1) 475. Пример 9. 4-[(1-Бензгидрил-5-[(бутиламино)карбонил]амино-1 Н-индол-3-ил)метил]3-метоксибензойная кислота. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента, а промежуточный 5-аминоиндол получали, как описано в примере 1, стадия 3, с использованием промежуточного 5-нитроиндола. Промежуточное производное мочевины получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием промежуточного производного мочевины. МС: m/z (M-1) 560. Пример 10. 4-(1-Бензгидрил-5-[(метилсульфонил)амино]-1H-индол-3-илметил)-3 метоксибензойная кислота. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента, а затем получали промежуточный 5 аминоиндол как описано в примере 1, стадия 3,с использованием 5-нитроиндола. Затем получали промежуточный сульфонамид как описано в примере 1, стадия 4 с использованием соответствующего ацилирующего агента. После этого получали целевое соединение, как описано в примере 1, стадии 5, с использованием промежуточного сульфонамида. МС: m/z (M-1) 539. Пример 11. 4-(1-Бензгидрил-5-[(циклопентилкарбонил)амино]-1H-индол-3-илметил)3-метоксибензойная кислота. Промежуточный 5-нитроиндол получали,как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента, а промежуточный 5-аминоиндол получали, как описано в примере 1, стадия 3, с использованием промежуточного 5-нитроиндола. После этого получали соответствующий промежуточный амид, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Целевое соединение получали, как описано в примере 1, стадия 5, с использованием этого промежуточного амида. МС: m/z (M-1) 557. Пример 12. 4-[(1-Бензгидрил-5-нитро-1 Ниндол-3-ил)метил]-3-метоксибензойная кислота. Промежуточный 5-нитроиндол получали как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего 53 агента, а целевое соединение получали с использованием этого промежуточного соединения, как описано в примере 1, стадия 5. МС: m/z (M-1) 657. Пример 13. 4-[(1-Бензгидрил-5-бром-1 Ниндол-3-ил)метил]-3-метоксибензойная кислота. Промежуточный 5-броминдол получали,как описано в примере 1, стадия 1, с использованием соответствующего индола, и как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. Затем с использованием вышеуказанного промежуточного соединения получали целевое соединение,как описано в примере 1, стадия 5. МС: m/z (M-1) 526. Пример 14. 4-[(1-Бензгидрил-5-фтор-1 Ниндол-3-ил)метил]-3-метоксибензойная кислота. Промежуточный 5-фториндол получали,как описано в примере 1, стадии 1, с использованием соответствующего индола, и как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. А затем с использованием вышеуказанного промежуточного соединения получали целевое соединение, как описано в примере 1, стадия 5. МС: m/z (M-1) 464. Пример 15. 4-[(1-Бензгидрил-5-метил-1 Ниндол-3-ил)метил]-3-метоксибензойная кислота. Промежуточный 5-метилиндол получали,как описано в примере 1, стадия 1, с использованием соответствующего индола и как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. А затем с использованием вышеуказанного промежуточного соединения получали целевое соединение,как описано в примере 1, стадия 5. МС: m/z (M-1) 460. Пример 16. 4-[(5-Бензгидрил-5 Н-[1,3]диоксоло[4,5-f]-индол-7-ил)метил]-3-метоксибензойная кислота. Промежуточный 5,6-метилендиоксииндол получали, как описано в примере 1, стадия 1, с использованием соответствующего индола, и как описано в примере 1, стадия 2, с использованием соответствующего алкилирующего агента. А затем с использованием вышеуказанного промежуточного соединения получали целевое соединение, как описано в примере 1, стадия 5. МС: m/z (M-1) 490. Пример 17. 4-[(1-Бензгидрил-5-циано-1 Ниндол-3-ил)метил]-3-метоксибензойная кислота. Стадия 1. К промежуточному соединению, полученному как описано в примере 13, стадия 2 (0,25 г,0,46 ммоль), в ДМФА (1 мл) добавляли CuCN(0,05 г, 1,2 экв.), и реакционную смесь перемешивали при 145 С в течение ночи, а затем охлаждали. К этой охлажденной реакционной смеси добавляли FеСl3 (0,09 г, 1,2 экв.). Реакционную смесь перемешивали в течение 5 мин, растворяли в этилацетате (30 мл), промывали соле 003876 54 вым раствором (3 х 10 мл), сушили (МgSO4),фильтровали и концентрировали. Продукт очищали с помощью хроматографии на двуокиси кремния (20% этилацетат/гексаны) с получением промежуточного сложного эфира (0,2 г, 89%) в виде бесцветного масла. Стадия 2. К промежуточному сложному эфиру (0,2 г,0,41 ммоль) в ДМФА (2 мл) добавляли тиометилат натрия (0,1 г, 3,4 экв.) и реакционную смесь перемешивали при 90 С в течение 10 мин. Реакционную смесь охлаждали, выливали в этилацетат (5 мл), промывали бифосфатом натрия (1 х 2 мл), солевым раствором (2 х 2 мл), сушили(MgSO4), фильтровали и концентрировали. После очистки с помощью хроматографии на двуокиси кремния (1% уксусная кислота, 25% этилацетат/гексан) получали целевое соединение(0,114 г, 59%) в виде бесцветного аморфного порошка. МС: m/z (M-1) 471. Пример 18. 4-[1-Бензгидрил-5-(метилсульфонил)-1H-индол-3-ил]метил-3-метоксибензойная кислота. Стадия 1. К промежуточному соединению, полученному, как описано в примере 13, стадия 3 (1 г,1,9 ммоль), в растворе ТГФ (2 мл) и метанола (2 мл) добавляли гидроксид натрия (0,41 мл,4,63 М, 1 экв.). Смесь перемешивали в течение 20 мин, а затем концентрировали. Оставшуюся воду удаляли путем добавления толуола и после этого удаления (3X) получали белый порошок (1 г, 100%). Стадия 2. К натриевой соли, полученной, как описано выше (0,88 г, 1,6 ммоль), в ДМФА (3 мл) добавляли натриевую соль метансульфиновой кислоты (0,72 г, 4,4 экв.) и CuI (0,74 г, 2,4 экв.). Реакционную смесь перемешивали в течение ночи при 130 С, охлаждали, растворяли в этилацетате (50 мл) и уксусной кислоте (10 мл),фильтровали (через целит), промывали солевым раствором (4 х 10 мл), сушили над MgSO4,фильтровали и концентрировали. После хроматографии на двуокиси кремния (1% уксусная кислота, 25% этилацетат/гексаны - 1% уксусная кислота, 50% этилацетат/гексаны) получали целевое соединение (0,2 г, 24%) в виде бесцветного аморфного твердого вещества. МС: m/z (M-1): 524. Пример 19. Циклопентил-N-1-бензгидрил-3-[2-метокси-4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5 илкарбамат. К продукту, полученному, как описано в примере 3, стадия 4 (0,5 г, 0,87 ммоль), в СН 2 Сl2(4 мл) добавляли EDCI (0,2 г, 1,0 ммоль, 1,2 экв.), DMAP (0,011 г, 0,087 ммоль, 0,1 экв.) и ортотолуолсульфонамид. Реакционную смесь перемешивали в течение ночи при комнатной температуре, растворяли в этилацетате (50 мл), 55 промывали бифосфатом натрия (1 х 10 мл), солевым раствором (2 х 10 мл), сушили (MgSO4),фильтровали и концентрировали. После хроматографии на двуокиси кремния (1% уксусная кислота, 25% этилацетат/гексаны) получали целевое соединение (0,4 г, 63%) в виде бесцветного твердого вещества. Пример 20. Циклопентил-N-3-[2-метокси 4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1-пропил-1 Н-индол-5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 1, стадия 5 и соответствующего сульфонамида. Пример 21. Циклопентил-N-1-(циклопентилметил)-3-[2-метокси-4-([(2-метилфенил) сульфонил]аминокарбонил)бензил]-1 Н-индол 5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 5, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 614. Пример 22. Циклопентил-N-3-[2-метокси 4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1-(4-пиридинилметил)-1 Н-индол-5 илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 6, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 651. Пример 23. Циклопентил-N-3-[2-метокси 4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1-(2-нафтилметил)-1 Н-индол-5 илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 4, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 700. Пример 24. Циклопентил-N-1-(изопропил)-3-[2-метокси-4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5-ил карбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 7, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 602. Пример 25. Циклопентил-N-1-(циклопентил)-3-[2-метокси-4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5 илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 8, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 628. Пример 26. Циклопентил-N-1-бензгидрил-3-[2-метокси-4-([(трифторметил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5 илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 704. 56 Пример 27. Циклопентил-N-1-бензгидрил-3-[2-метокси-4-([(метилсульфонил) амино]карбонилбензил)-1H-индол-5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 650. Пример 28. Циклопентил-N-1-бензгидрил-3-[4-([(2-хлорфенил)сульфонил] аминокарбонил)-2-метоксибензил]-1 Н-индол 5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. Пример 29. Циклопентил-N-(3-4-[([5(ацетилимино)-4-метил-4,5-дигидро-1,3,4 тиадиазол-2-ил]сульфониламино)карбонил]-2 метоксибензил-1-бензгидрил-1 Н-индол-5-ил) карбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. Пример 30. Циклопентил-N-1-бензгидрил-3-[4-[([5-(диметиламино)-1-нафтил] сульфониламино)карбонил]-2-метоксибензил 1 Н-индол-5-ил)карбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. Пример 31. Циклопентил-N-1-бензгидрил-3-[4-[(бензилсульфонил)амино]карбонил 2-метоксибензил)-1 Н-индол-5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 726. Пример 32. Циклопентил-N-1-бензгидрил-3-[4-[([2,4-диметил-1,3-тиазол-5-ил)сульфонил]аминокарбонил)-2-метоксибензил]-1 Ниндол-5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 747. Пример 33. Циклопентил-N-1-бензгидрил-3-[4-[(3,5-диметил-4-изоксазолил)сульфонил]аминокарбонил]-2-метоксибензил-1 Ниндол-5-илкарбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 731. Пример 34. Циклопентил-N-(3-4-[([5(ацетиламино)-1,3,4-тиадиазол-2-ил]сульфониламино)карбонил]-2-метоксибензил-1-бензгидрил-1 Н-индол-5-ил)карбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. Пример 35. Циклопентил-N-1-бензгидрил-3-[2-метокси-4-[([4-(3-метил-5-оксо-4,5 57 дигидро-1 Н-пиразол-1-ил)фенил]сульфонил амино)карбонил]бензил]-1 Н-индол-5-ил карбамат. Целевое соединение получали, как описано в примере 19, из продукта примера 3, стадия 4 и соответствующего сульфонамида. Пример 36. N-4-[(1-бензгидрил-5-нитро 1 Н-индол-3-ил)метил]-3-метоксибензоил-2 метилбензолсульфонамид. Целевое соединение получали, как описано в примере 19, из продукта примера 12, стадия 2 и соответствующего сульфонамида. МС: m/z (M-1) 644. Пример 37. N-4-[(1-бензгидрил-5-нитро 1 Н-индол-3-ил)метил]-3-метоксибензоил(трифтор)метансульфонамид. Целевое соединение получали, как описано в примере 19, из продукта примера 12, стадия 2 и соответствующего сульфонамида. МС: m/z (M-1) 622. Пример 38. N-4-[(1-бензгидрил-5-бром 1 Н-индол-3-ил)метил]-3-метоксибензоил-2 метилбензолсульфонамид. Целевое соединение получали, как описано в примере 19, из продукта примера 13, стадия 2 и соответствующего сульфонамида. МС: m/z (M-1) 679. Пример 39. N-4-[(1-бензгидрил-5-бром 1 Н-индол-3-ил)метил]-3-метоксибензоил(трифтор)метансульфонамид. Целевое соединение получали, как описано в примере 19, из продукта примера 13, стадия 2 и соответствующего сульфонамида. МС: m/z (M-1) 657. Пример 40. N-1-бензгидрил-3-[2-метокси 4-([(трифторметил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5-илциклопентанкарбоксамид. Целевое соединение получали, как описано в примере 19, из продукта примера 11, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 688. Пример 41.N-4-(1-бензгидрил-5[(метилсульфонил)амино]-1H-индол-3-ил метил)-3-метоксибензоил(трифтор)метансульфонамид. Целевое соединение получали, как описано в примере 19, из продукта примера 10, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 670. Пример 42.N-4-[(1-бензгидрил-5[(бутиламино)карбонил]амино-1 Н-индол-3 ил)метил]-3-метоксибензоил(трифтор)метансульфонамид. Целевое соединение получали, как описано в примере 19, из продукта примера 9, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 691. Пример 43. N-1-бензгидрил-3-[2-метокси 4-([(2-метилфенил)сульфонил]аминокарбо 003876 58 нил)бензил]-1 Н-индол-5-илциклопентанкарбоксамид. Целевое соединение получали, как описано в примере 19, из продукта примера 11, стадия 4 и соответствующего сульфонамида. МС: m/z (M-1) 710. Пример 44. [1-Бензгидрил-3-(2-метокси-4 трифторметансульфониламинокарбонил)бензил]-1 Н-индол-5-иламид тиофен-2-сульфоновой кислоты Стадия 1. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3. Стадия 2. Промежуточный сульфонамид получали,как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 3. Промежуточную кислоту получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. Стадия 4. Целевое соединение получали, как описано в примере 19, из вышеуказанного промежуточного соединения и соответствующего сульфонамида. МС: m/z (M-1) 738. Пример 45. 4-[4-(1-Бензгидрил-5[(бензилсульфонил)амино]-1-1H-индол-3 метоксибензоил](трифтор)метансульфонамид. Стадия 1. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3. Стадия 2. Промежуточный сульфонамид получали,как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 3. Промежуточную кислоту получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. Стадия 4. Целевое соединение получали, как описано в примере 19, из вышеуказанного промежуточного соединения и соответствующего сульфонамида.MC: m/z (M-1) 746. Пример 46. N-1-бензгидрил-3-[2-метокси 4-([(трифторметил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5-ил-3-тиофенкарбоксамид. Стадия 1. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадии 3. Стадия 2. Промежуточный амид получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. 59 Стадия 3. Промежуточную кислоту получали как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. Стадия 4. Целевое соединение получали, как описано в примере 19, из вышеуказанного промежуточного соединения и соответствующего сульфонамида.MC: m/z (M-1) 702. Пример 49. Бензил-N-1-бензгидрил-3-[2 метокси-4-([(трифторметил)сульфонил] аминокарбонил)бензил]-1 Н-индол-5-илкарбамат. Стадия 1. Промежуточный 5-аминоиндол получали,как описано в примере 1, стадия 3. Стадия 2. Промежуточный карбамат получали, как описано в примере 1, стадия 4, с использованием соответствующего ацилирующего агента. Стадия 3. Промежуточную кислоту получали, как описано в примере 1, стадия 5, с использованием вышеуказанного промежуточного соединения. Стадия 4. Целевое соединение получали, как описано в примере 19, из вышеуказанного промежуточного соединения и соответствующего сульфонамида.MC: m/z (M-1) 726. Пример 50. 4-[(1-Бензгидрил-5-нитро-1 Ниндол-3-ил)метил]бензойная кислота. Стадия 1. Промежуточный 3-алкилированный 5 нитроиндол получали, как описано в примере 1,стадия 1, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 3-алкилированный 5 нитроиндол подвергали N-алкилированию, как описано в примере 3, стадия 1. Стадия 3. Целевое соединение получали, как описано в примере 1, стадия 5. МС: m/z (M-1) 461. Пример 51. 4-[(1-Бензгидрил-5-бром-1 Ниндол-3-ил)метил]бензойная кислота. Стадия 1. Промежуточный 3-алкилированный 5 броминдол получали, как описано в примере 13,стадия 1, с использованием соответствующего алкилирующего агента. Стадия 2. Промежуточный 3-алкилированный 5 нитроиндол подвергали N-алкилированию, как описано в примере 13, стадия 2. Стадия 3. Целевое соединение получали, как описано в примере 13, стадия 3. 60 МС: m/z (M-1) 494. Пример 52. 4-[(1-Бензгидрил-5-[(циклопентилокси)карбонил]амино-1 Н-индол-3-ил) метил]бензойная кислота. Стадия 1. Из соединения, полученного, как описано в примере 50, стадия 2, получали нужное промежуточное соединение, как описано в примере 3, стадии 2. Стадия 2. Из вышеуказанного промежуточного соединения получали промежуточный карбамат,как описано в примере 3, стадия 3. Стадия 3. Целевое соединение получали из вышеуказанного промежуточного соединения, как описано в примере 3, стадия 4. МС: m/z (M-1) 543. Пример 53. Циклопентил-N-1-бензгидрил-3-[4-([(2-метилфенил)сульфонил]аминокарбонил)бензил]-1 Н-индол-5-илкарбамат. Целевое соединение получали из продукта примера 52, стадия 3, как описано в примере 19. МС: m/z (M-1) 697. Пример 54. Циклопентил-N-1-бензгидрил-3-[4-([(трифторметил)сульфонил] аминокарбонил)бензил]-1 Н-индол-5-илкарбамат. Целевое соединение получали из продукта примера 52, стадия 3, как описано в примере 26. МС: m/z (M-1) 674. Пример 55. N-4-[(1-бензгидрил-5-нитро 1 Н-индол-3-ил)метил]бензоил(трифтор) метансульфонамид. Целевое соединение получали из продукта примера 55, стадия 3, как описано в примере 26. МС: m/z (M-1) 592. Пример 56. N-4-[(1-бензгидрил-5-нитро 1 Н-индол-3-ил)метил]бензоил-2-метилбензолсульфонамид. Целевое соединение получали из продукта примера 55, стадия 3, как описано в примере 19. МС: m/z (M-1) 614. Пример 57. N-4-[(1-бензгидрил-5-бром 1 Н-индол-3-ил)метил]бензоил-2-метилбензолсульфонамид. Целевое соединение получали из продукта примера 51, стадия 3, как описано в примере 38. МС: m/z (M-1) 649. Пример 58. N-4-[(1-бензгидрил-5-бром 1 Н-индол-3-ил)метил]бензоил(трифтор)метансульфонамид. Целевое соединение получали из продукта примера 51, стадия 3, как описано в примере 39.
МПК / Метки
МПК: A61P 29/00, C07D 209/12, A61K 31/404
Метки: ингибиторы, ферментов, фосфолипазных
Код ссылки
<a href="https://eas.patents.su/30-3876-ingibitory-fosfolipaznyh-fermentov.html" rel="bookmark" title="База патентов Евразийского Союза">Ингибиторы фосфолипазных ферментов</a>
Предыдущий патент: Способ получения эфиров глиоксиловой кислоты или их гидратов
Следующий патент: Ингибиторы фарнезилпротеинтрансферазы, обладающие in vivo радиосенсибилизирующими свойствами
Случайный патент: 8-замещенные пиридо[2,3-в]пиразины и их применение