Карбануклеозидные аналоги для противовирусного лечения
Формула / Реферат
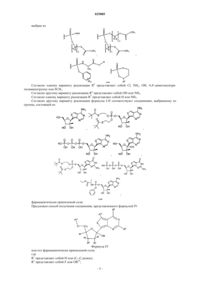
1. Соединение формулы I
или его фармацевтически приемлемая соль;
где R1 представляет собой Н или (С1-С6)алкил;
R2 представляет собой ORa или F;
R4 представляет собой ORa или Н; или
R2 и R4, взятые вместе, представляют собой -О(С=О)О-, -OC(CH3)2O- или -ОСН(фенил)О-;
R6 представляет собой Н, ORa, CN или (С1-С6)алкил;
каждый Ra независимо представляет собой Н, (С1-С6)алкил, (С2-С8)алкенил, (С2-С8)алкинил, (С6-С14)арил(С1-С6)алкил, насыщенный или частично ненасыщенный (С3-С12)карбоциклил(С1-С6)алкил, -C(=O)R11 или -C(=O)OR11;
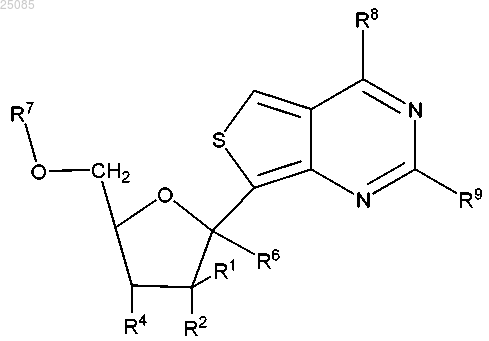
R7 представляет собой Н, -C(=O)R11, -Si(R43)3 или
каждый R43 независимо представляет собой (С1-С6)алкил, замещенный (C1-С6)алкил или (С6-С14)арил;
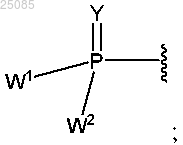
Y представляет собой О;
W1 и W2, взятые совместно, представляют собой -Y3(C(Ry)2)3Y3-; или один из W1 или W2 вместе с R3 или R4 представляет собой -Y3-, а другой из W1 или W2 соответствует формуле Ia; или каждый из W1 и W2 независимо представляет собой группу формулы Ia
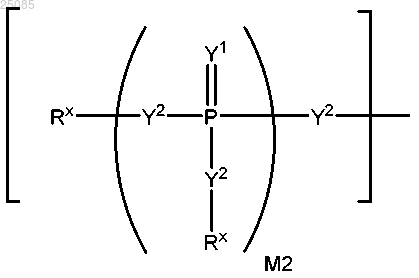
где каждый Y1 представляет собой О;
каждый Y2 независимо представляет собой связь, О, NR или S;
каждый Y3 представляет собой О;
М2 равен 0, 1 или 2;
каждый Rx независимо представляет собой Ry или соответствует формуле
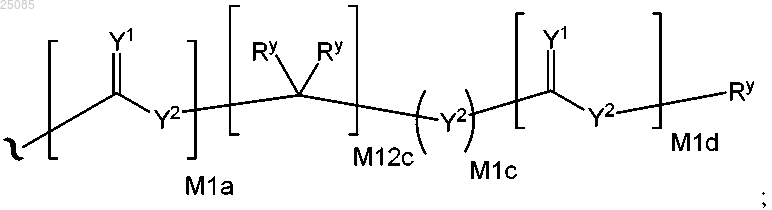
где каждый M1a, M1с и M1d независимо равен 0 или 1;
М12с равен 0, 1 или 2;
каждый Ry независимо представляет собой Н, ОН, R, -C(=Y1)R, -C(=Y1)OR, -SC(=Y1)R, -OR или W3;
каждый R независимо представляет собой Н, (C1-С6)алкил, замещенный (C1-С6)алкил, (С2-С8)алкенил, замещенный (С2-С8)алкенил, (C2-C8)алкинил, замещенный (С2-С8)алкинил, (С6-С14)арил, замещенный (С6-С14)арил;
W3 представляет собой W5;
W5 представляет собой пиридинил;
R8 представляет собой галоген, NH2, ОН, SCH3 или 4,4'-диметокситритиламиногруппу;
R9 представляет собой Н, NH2 или 4,4'-диметокситритиламиногруппу;
каждый R11 независимо представляет собой Н, (С1-С6)алкил, (С6-С14)арил, замещенный (С6-С14)арил или (С6-С14)арил(С1-С6)алкил; и
при условии, что когда R9 представляет собой Н и R8 представляет собой NH2, ОН, или SCH3, тогда по меньшей мере один из R1, R2, R4 и R6 представляет собой CN, F, (С1-С6)алкил, или R7 представляет собой
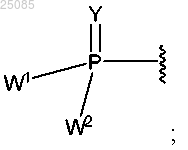
при этом замещение означает, что один или более атомов водорода независимо замещены заместителем, представляющим собой -Rb или =O, где каждый Rb независимо представляет собой (С1-С6)алкил или (С6-С14)арил.
2. Соединение по п.1 формулы II
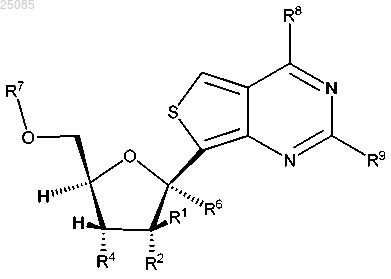
3. Соединение по п.2, отличающееся тем, что R8 представляет собой Cl, NH2, ОН, 4,4'-диметокситритиламиногруппу или SCH3.
4. Соединение по п.3, отличающееся тем, что R6 представляет собой Н, ORa, CN или метил.
5. Соединение по п.4, отличающееся тем, что R2 представляет собой ОН или O-Bn.
6. Соединение по п.5, отличающееся тем, что R4 представляет собой ORa.
7. Соединение по п.6, отличающееся тем, что R1 представляет собой СН3.
8. Соединение по п.7, отличающееся тем, что R6 представляет собой CN или ORa.
9. Соединение по п.6, отличающееся тем, что R6 представляет собой CN или ORa.
10. Соединение по п.7, отличающееся тем, что R6 представляет собой Н.
11. Соединение по п.6, отличающееся тем, что R6 представляет собой Н.
12. Соединение по п.6, отличающееся тем, что R8 представляет собой ОН или NH2.
13. Соединение по п.6, отличающееся тем, что R9 представляет собой Н или NH2.
14. Соединение по п.6, отличающееся тем, что R7 представляет собой Н или

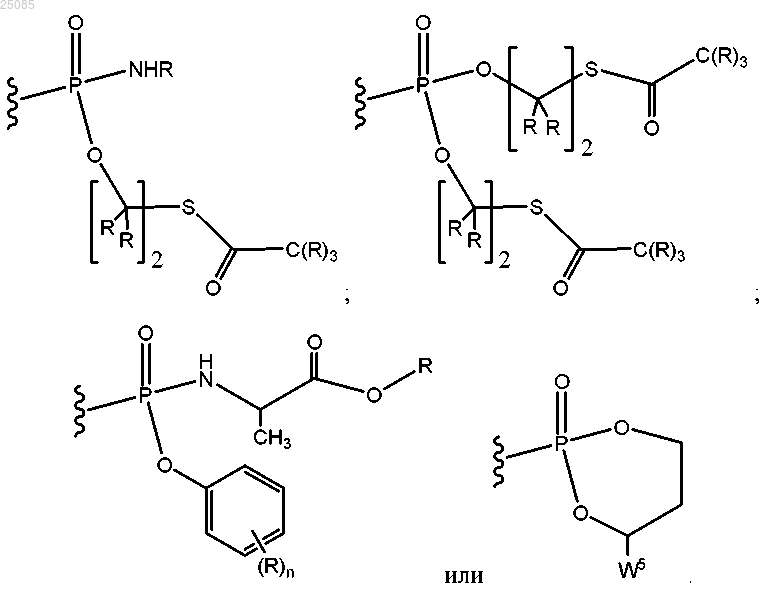
15. Соединение по п.14, отличающееся тем, что
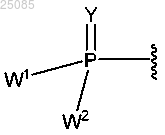
выбран из
16. Соединение, которое представляет собой
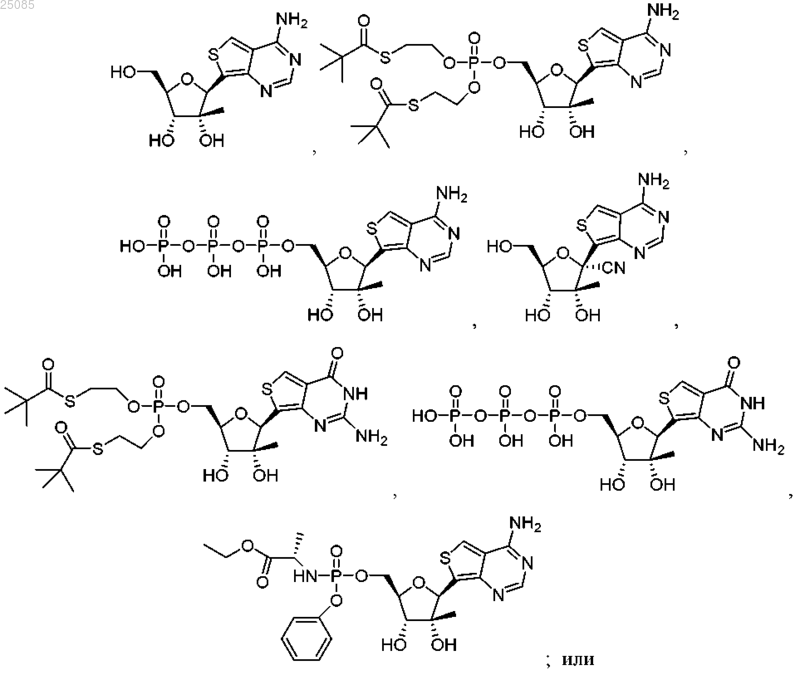
фармацевтически приемлемую соль указанных соединений.
17. Фармацевтическая композиция для лечения вирусной инфекции, вызванной вирусом семейства Flaviviridae, содержащая терапевтически эффективное количество соединения по п.1 и фармацевтически приемлемый носитель.
18. Фармацевтическая композиция по п.17, дополнительно содержащая по меньшей мере один дополнительный терапевтический агент, выбранный из группы, состоящей из интерферонов, рибавирина или его аналогов, ингибиторов NS3-протеазы ВГС, ингибиторов альфа-глюкозидазы 1, гепатопротекторов, нуклеозидных или нуклеотидных ингибиторов NS5B-полимеразы ВГС, ненуклеозидных ингибиторов NS5B-полимеразы ВГС, ингибиторов NS5A ВГС, агонистов TLR-7, ингибиторов циклофилина, ингибиторов IRES ВГС, усилителей фармакокинетики или других лекарственных средств для лечения ВГС или их смесей.
19. Способ лечения вирусной инфекции, вызванной вирусом семейства Flaviviridae, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества соединения по п.1.
20. Способ лечения вирусной инфекции, вызванной вирусом семейства Flaviviridae, включающий введение млекопитающему, нуждающемуся в этом, терапевтически эффективного количества фармацевтической композиции по пп.17-18.
21. Способ по п.19 или 20, отличающийся тем, что указанный вирус выбран из группы, состоящей из вируса денге, вируса желтой лихорадки, вируса Западного Нила, вируса японского энцефалита, вируса клещевого энцефалита, вируса Кунджин, вируса энцефалита долины Мюррей, вируса энцефалита Сент-Луис, вируса омской геморрагической лихорадки, вируса вирусной диареи крупного рогатого скота, вируса Зика и вируса гепатита С.
22. Способ по п.21, отличающийся тем, что вирусная инфекция вызвана вирусом гепатита С.
23. Способ по п.21, дополнительно включающий введение по меньшей мере одного дополнительного терапевтического агента, выбранного из группы, состоящей из интерферонов, рибавирина или его аналогов, ингибиторов NS3-протеазы ВГС, ингибиторов альфа-глюкозидазы 1, гепатопротекторов, нуклеозидных или нуклеотидных ингибиторов NS5B-полимеразы ВГС, ненуклеозидных ингибиторов NS5B-полимеразы ВГС, ингибиторов NS5A ВГС, агонистов TLR-7, ингибиторов циклофилина, ингибиторов IRES ВГС, усилителей фармакокинетики и других лекарственных средств для лечения ВГС или их смесей.
24. Промежуточное соединение формулы IX для синтеза противовирусного соединения формулы I
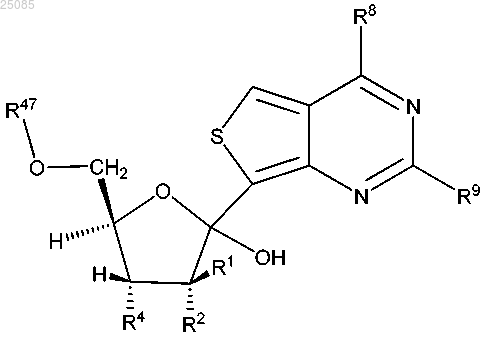
или его фармацевтически приемлемая соль;
где R1 представляет собой Н или (С1-С6)алкил;
R2 независимо представляет собой F или OR44;
R4 независимо представляет собой Н или OR44;
R43 представляет собой (C1-С6)алкил, замещенный (C1-С6)алкил или (С6-С14)арил;
R44 представляет собой -C(R45)2R46, -C(O)R45 или -C(O)OR45;
R47 представляет собой -C(R45)2R46, -Si(R43)3, -C(O)R45, -C(O)OR45 или
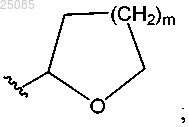
или любые два R44, взятые совместно, представляют собой -C(R59)2;
каждый R45 представляет собой Н, (C1-С6)алкил, (С6-С14)арил или (С6-С14)арил(С1-С6)алкил;
каждый R59 независимо представляет собой Н, (C1-С6)алкил или (С6-С14)арил;
R46 представляет собой (С6-С14)арил;
каждый m равен 1 или 2;
R8 представляет собой галоген, NH2, ОН или SCH3;
R9 представляет собой Н или NH2;
при этом замещение означает, что один или более атомов водорода независимо замещены заместителем, представляющим собой -Rb или =O, где каждый Rb независимо представляет собой (С1-С6)алкил или (С6-С14)арил.
25. Соединение по п.24, выбранное из группы, состоящей из
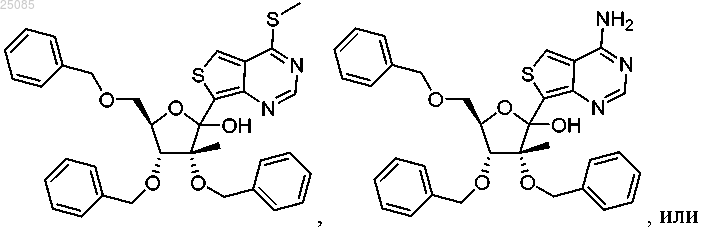
фармацевтически приемлемая соль указанного соединения.
Текст
КАРБАНУКЛЕОЗИДНЫЕ АНАЛОГИ ДЛЯ ПРОТИВОВИРУСНОГО ЛЕЧЕНИЯ Формула I а также промежуточные соединения и способы их получения. Предложенные соединения формулы(I) и композиции на их основе подходят для лечения вирусных инфекций Flaviviridae. Область техники Настоящее изобретение, в целом, относится к соединениям, обладающим противовирусной активностью, более конкретно, к нуклеозидам, обладающим активностью против вирусных инфекций Flaviviridae. Уровень техники Вирусы, образующие семейство Flaviviridae, включают по меньшей мере три различных рода,включая пестивирусы, флавивирусы и гепацивирусы (Кэлишер с соавторами, Calisher, et al.), J. Gen.Virol., 1993, 70, 37-43). Несмотря на то, что пестивирусы вызывают множество заболеваний у животных,которые оказывают существенное влияние на экономику, в частности, такие как вирус вирусной диареи крупного рогатого скота (BVDV), вирус классической свиной чумы (ВКСЧ, чума свиней) и пограничная болезнь овец (ПБО), роль этих вирусов в заболеваниях у людей охарактеризована в меньшей степени(Мэнниг с соавторами, (Moennig, V.), et al., Adv. Vir. Res. 1992, 48, 53-98). Флавивирусы ответственны за серьезные заболевания у людей, такие как лихорадка денге и желтая лихорадка, в то время как гепацивирусы вызывают у человека вирусные инфекции гепатита С. Другие серьезные вирусные инфекции, вызываемые вирусами семейства Flaviviridae, включают вирус Западного Нила (WNV), вирус японского энцефалита (JEV), вирус клещевого энцефалита, вирус Кунджин, энцефалит долины Мюррей, энцефалит Сент-Луи, вирус омской геморрагической лихорадки и вирус Зика. В целом, инфекции, вызываемые вирусами семейства Flaviviridae, являются причиной значительной смертности, заболеваемости и экономических потерь по всему миру. Следовательно, существует необходимость разработки эффективных способов лечения вирусных инфекций Flaviviridae. Вирус гепатита С (ВГС) является главной причиной хронических заболеваний печени во всем мире(Н. Бойер с соавторами, (Boyer, N. et al.) J Hepatol. 32:98-112, 2000), поэтому настоящее противовирусное исследование в значительной степени сфокусировано на разработке усовершенствованных способов лечения хронических инфекций ВГС у людей (A.M. Ди Беселье и Б.Р. Бэкон (Di Besceglie, A.M. and Bacon,В.R., Scientific American, Oct.: 80-85, (1999); К.П. Гордон с соавторами (Gordon, С.Р., et al.), J. Med.Chem. 2005, 48, 1-20; Д. Марадпур с соавторами (Maradpour, D.; et al.), Nat. Rev. Micro. 2007, 5(6), 453463). Ряд способов лечения ВГС представлен в обзоре Бимока с соавторами (Bymock et al.) в AntiviralChemistryChemotherapy, 11:2; 79-95 (2000). РНК-зависимая РНК полимераза (RdRp) является одной из наиболее изученных мишеней для разработки новых терапевтических агентов против ВГС. NS5 В-полимераза является мишенью для ингибиторов в ранних клинических исследованиях на людях (Дж. Сомадосси (Sommadossi, J.), WO 01/90121 А 2,US 2004/0006002 Al). Указанные ферменты подробно охарактеризованы на биохимическом и структурном уровне путем скрининговых исследований для определения селективных ингибиторов (Э. Де Клер(De Clercq, Е.) (2001) J. Pharmacol. Exp.Ther. 297:1-10; Э. Де Клер (De Clercq, Е.) (2001) J. Clin. Virol. 22:73-89). Биохимические мишени, такие как NS5B, важны для разработки терапии ВГС, так как ВГС не реплицируется в лабораторных условиях, и существуют трудности в разработке клеточных исследований и доклинических систем на животных. В настоящее время существует, главным образом, два противовирусных соединения - рибавирин,являющийся аналогом нуклеозида, и интерферон-альфа(ИФН), которые применяют для лечения хронических инфекций ВГС у человека. Рибавирин в отдельности не эффективен для снижения содержания вирусной РНК, имеет значительную токсичность и, как известно, вызывает анемию. Сообщалось, что комбинация ИФН и рибавирина является эффективной для контроля хронического гепатита С (Л.Дж. Скотт с соавторами, (Scott, L.J., et al.) Drugs 2002, 62, 507-556), но менее чем у половины пациентов, которым проводили указанное лечение, наблюдалось постоянное улучшение. Другие заявки на патенты, в которых описано применение аналогов нуклеозидов для лечения вируса гепатита С, включают WO 01/32153, WO 01/60315, WO 02/057425, WO 02/057287, WO 02/032920, WO 02/18404, WO 04/046331, WO 2008/089105 и WO 2008/141079, но дополнительные способы лечения инфекций ВГС до настоящего времени не были доступны пациентам. Проведение вирусологического лечения пациентов с хроническими инфекциями ВГС затруднено вследствие очень большого количества вирусов, продуцируемых ежедневно у пациентов с хронической инфекцией, и высокой спонтанной мутабильности вируса ВГС (Нойманн с соавторами (Neumann, et al.),Science 1998, 282, 103-7; Фукимото с соавторами (Fukimoto, et al.), Hepatology, 1996, 24, 1351-4; Доминго с соавторами (Domingo, et al.), Gene, 1985, 40, 1-8; Мартелл с соавторами (Martell, et al.), J. Virol. 1992, 66,3225-9). Было показано, что экспериментальные противовирусные нуклеозидные аналоги вызывают появление устойчивых мутаций вируса ВГС как in vivo, так и in vitro (Мильяччо с соавторами (Migliaccio,et al.), J. Biol. Chem. 2003, 926; Кэрролл с соавторами (Carroll, et al.), Antimicrobial Agents Chemotherapy 2009, 926; А.Б. Браун (Brown, А. В.), Expert Opin. Investig. Drugs 2009, 18, 709-725). Следовательно, срочно требуются лекарственные средства, обладающие улучшенными противовирусными свойствами, в частности, повышенной активностью против резистентных штаммов вируса; улучшенной пероральной биодоступностью; пониженными нежелательными побочными эффектами и более продолжительным эффективным периодом полувыведения in vivo (Р. Де Франческо с соавторами (De Francesco, R. et al.) Были описаны некоторые 7-рибозилтиено[3,4-d]пиримидины (Москоу с соавторами (Moscow, et al.);International Journal of Cancer 1997, 72, p 184-190; Оттер с соавторами (Otter, et al.), NucleosidesNucleotides 1996, p 793-807; Патил с соавторами (Patil, et al.), J. Heterocyclic Chemistry 1993, p 509-515; Патил с соавторами (Patil, et al.), NucleosidesNucleotides 1990, p 937-956; Pao с соавторами (Rao, et al.); Tetrahedron Letters 1988, p 3537-3540; Хаманн с соавторами (Hamann, et al.), Collection Symposium Series 2008,10, p 347-349; Хаманн с соавторами (Hamann, et al.), Bioorg. Med. Chem. 2009, 17, p 2321-2326), однако отсутствуют сведения о том, что указанные соединения подходят для лечения вирусных инфекций Flaviviridae. Краткое описание изобретения В настоящем изобретении предложены соединения, подавляющие вирусы семейства Flaviviridae. Настоящее изобретение также включает соединения, которые ингибируют полимеразы вирусных нуклеиновых кислот, в частности РНК-зависимые РНК полимеразы ВГС (RdRp), но не полимеразы нуклеиновых кислот клетки. Следовательно, соединения согласно настоящему изобретению подходят для лечения инфекций Flaviviridae у людей и других животных. Согласно одному из аспектов в настоящем изобретении предложено соединение формулы I Формула I или его фармацевтически приемлемая соль; гдеR2 и R4, взятые вместе, представляют собой -O(С=O)O-, -ОС(СН 3)2 О- или -ОСН(фенил)О-; или R6 представляет собой Н, ORa, CN или (С 1-С 6)алкил; каждый Ra независимо представляет собой Н, (С 1-С 6)алкил, (С 2-С 8)алкенил, (С 2-С 8)алкинил, (С 6 С 14)арил(С 1-С 6)алкил, насыщенный или частично ненасыщенный (С 3-С 12)карбоциклил(С 1-С 6)алкил,-C(=O)R11 или -C(=O)OR11; каждый R43 независимо представляет собой (С 1-С 6)алкил, замещенный (C1-С 6)алкил или (С 6 С 14)арил;W1 и W2, взятые совместно, представляют собой -Y3(C(Ry)2)3Y3-; или один из W1 или W2 вместе с R3 или R4 представляет собой -Y3-, а другой из W1 или W2 соответствует формуле Ia; или каждый из W1 иW2 независимо представляет собой группу формулы Ia Формула Ia где каждый Y1 представляет собой О; или каждый Y2 независимо представляет собой связь, О, NR или S; каждый Y3 представляет собой О; М 2 равен 0, 1 или 2; каждый Rx независимо представляет собой Ry или соответствует формуле где каждый M1a, M1 с и M1d независимо равен 0 или 1; М 12 с равен 0, 1 или 2; каждый Ry независимо представляет собой Н, ОН, R, -C(=Y1)R, -C(=Y1)OR, -SC(=Y1)R, -OR или W3; каждый R независимо представляет собой Н, (C1-С 6)алкил, (C1-С 6)замещенный алкил, (С 2-С 8)алкенил, (C2-C8)замещенный алкенил, (C2-C8)алкинил, (C2-C8) замещенный алкинил, (С 6-С 14)арил, (С 6 С 14)замещенный арил;R9 представляет собой Н, NH2 или 4,4'-диметокситритиламиногруппу; каждый R11 независимо представляет собой Н, (С 1-С 6)алкил, (С 6-С 14)арил, замещенный (С 6 С 14)арил, (С 6-С 14)арил(С 1-С 6)алкил; и при этом замещение означает, что один или более атомов водорода независимо замещены заместителем, представляющим собой -Rb или =O, где каждый Rb независимо представляет собой (С 1-С 6)алкил или (С 6-С 14)арил,при условии, что когда R9 представляет собой Н и R8 представляет собой NH2, ОН, или SCH3, тогда по меньшей мере один из R1, R2, R4 и R6 представляет собой CN, F, (С 1-С 6)алкил, или R7 представляет собой Согласно другому аспекту настоящее изобретение включает соединения формулы I и их фармацевтически приемлемые соли, а также все рацематы, энантиомеры, диастереомеры, таутомеры, полиморфы,псевдополиморфы и аморфные формы указанных соединений. Согласно другому аспекту в настоящем изобретении предложены новые соединения формулы I, обладающие активностью против инфекционных вирусов Flaviviridae. He желая быть связанными теорией,соединения согласно настоящему изобретению могут ингибировать вирусную РНК-зависимую РНК полимеразу и, таким образом, ингибировать репликацию вируса. Соединения согласно настоящему изобретению подходят для лечения людей, инфицированных вирусом человека, таким как гепатит С. Согласно другому аспекту в изобретении предложена фармацевтическая композиция, содержащая эффективное количество соединения Формулы I или его фармацевтически приемлемой соли, в комбинации с фармацевтически приемлемым разбавителем или носителем. Согласно другому варианту реализации в настоящей заявке предложена комбинация фармацевтического агента, содержащая:a) первую фармацевтическую композицию, содержащую соединение формулы I или его фармацевтически приемлемую соль; иb) вторую фармацевтическую композицию, содержащую по меньшей мере один дополнительный терапевтический агент, выбранный из группы, состоящей из интерферонов, аналогов рибавирина, ингибиторов NS3 протеазы, ингибиторов NS5a, ингибиторов альфа-глюкозидазы 1, гепатопротекторов, ненуклеозидных ингибиторов ВГС и других лекарственных средств для лечения ВГС. Согласно другому варианту реализации в настоящей заявке предложен способ ингибирования полимеразы ВГС, включающий взаимодействие клетки, инфицированной ВГС, и эффективного количества соединения формулы I или его фармацевтически приемлемых солей, сольватов и/или сложных эфиров. Согласно другому варианту реализации в настоящей заявке предложен способ ингибирования полимеразы ВГС, включающий взаимодействие клетки, инфицированной ВГС, и эффективного количества соединения формулы I или его фармацевтически приемлемых солей, сольватов и/или сложных эфиров; и по меньшей мере одного дополнительного терапевтического агента. Согласно другому варианту реализации в настоящей заявке предложен способ лечения и/или профилактики заболевания, вызванного вирусной инфекцией, причем вирусная инфекция вызвана вирусом,выбранным из группы, состоящей из вируса денге, вируса желтой лихорадки, вируса Западного Нила,вируса японского энцефалита, вируса клещевого энцефалита, вируса Кунджин, вируса энцефалита доли-3 025085 ны Мюррей, вируса энцефалита Сент-Луис, вируса омской геморрагической лихорадки, вируса вирусной диареи крупного рогатого скота, вируса Зика и вируса гепатита С; путем введения терапевтически эффективного количества соединения формулы I или его фармацевтически приемлемой соли нуждающемуся в этом субъекту. Согласно другому варианту реализации в настоящей заявке предложен способ лечения ВГС у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I или его фармацевтически приемлемой соли, сольвата и/или сложного эфира. Согласно другому варианту реализации в настоящей заявке предложен способ лечения ВГС у пациента, включающий введение указанному пациенту терапевтически эффективного количества соединения формулы I; или его фармацевтически приемлемой соли, сольвата и/или сложного эфира; и по меньшей мере одного дополнительного терапевтического агента. Согласно другому аспекту в изобретении предложен способ лечения или профилактики симптомов или проявлений инфекции ВГС у инфицированного животного, который включает введение, т.е. лечение, указанному животному фармацевтической комбинированной композиции, или состава, содержащей эффективное количество соединения формулы I и второго соединения, обладающего свойствами, направленными против ВГС. Согласно другому аспекту в изобретении также предложен способ ингибирования ВГС, включающий введение млекопитающему, инфицированному ВГС, соединения формулы I в количестве, эффективном для подавления роста указанных клеток, инфицированных ВГС. Согласно другому аспекту в изобретении также предложены способы и новые промежуточные соединения, описанные в заявке, которые подходят для получения соединений формулы I согласно настоящему изобретению. Согласно другим аспектам предложены новые способы синтеза, анализа, разделения, выделения,очистки, характеристики и исследования соединений согласно настоящему изобретению. Подробное описание типовых вариантов реализации В данном разделе приведено подробное описание конкретных вариантов реализации настоящего изобретения, примеры которых проиллюстрированы в представленном описании, структурах и формулах. Несмотря на то, что изобретение описано в связи с перечисленными вариантами реализации, следует понимать, что указанные варианты реализации не предназначены для ограничения изобретения данными вариантами реализации. Напротив, изобретение охватывает все альтернативы, модификации и эквиваленты, которые могут быть включены в рамки настоящего изобретения. Согласно другому аспекту соединения формулы I представлены формулой II Формула II или фармацевтически приемлемой солью; где все переменные определены в формуле I. Согласно одному из вариантов реализации формулы II R1 представляет собой СН 3. Согласно одному из вариантов реализации формулы II R2 представляет собой ОН или O-Bn. Согласно одному из вариантов реализации формулы II R4 представляет собой ORa. Согласно одному из вариантов реализации формулы II R6 представляет собой Н, ORa, CN или метил. Согласно одному из вариантов реализации формулы II R6 представляет собой CN или ORa. Согласно одному из вариантов реализации формулы II R6 представляет собой Н. Согласно одному из вариантов реализации формулы II R6 представляет собой Согласно одному из вариантов реализации формулы II R7 представляет собой Н или Согласно другому предпочтительному аспекту указанного варианта реализации Согласно одному варианту реализации R8 представляет собой Cl, NH2, ОН, 4,4'-диметокситритиламиногруппу или SCH3. Согласно другому варианту реализации R8 представляет собой ОН или NH2. Согласно одному варианту реализации R9 представляет собой Н или NH2. Согласно другому варианту реализации формулы I-II соответствуют соединению, выбранному из группы, состоящей из фармацевтически приемлемой соли. Предложен способ получения соединения, представленного формулой IV Формула IV или его фармацевтически приемлемой соли; где или любые два R44, взятые совместно, представляют собой -C(R59)2-; каждый R45 независимо представляет собой Н, (C1-С 6)алкил, (С 6-С 14)арил или (С 6-С 14)арил(С 1-С 6)алкил; каждый R59 независимо представляет собой Н, (C1-С 6)алкил или (С 6-С 14)арил;R9 представляет собой NH2 или Н; при этом замещение означает, что один или более атомов водорода независимо замещены заместителем, представляющим собой -Rb или =O, где каждый Rb независимо представляет собой (С 1-С 6)алкил или (С 6-С 14)арил, причем указанный способ включает:(а) обеспечение соединения формулы V(b) обработку соединения формулы V цианидным реагентом и кислотой Льюиса; с получением соединения формулы IV. Соединения формулы IV подходят для получения противовирусных соединений формулы I. Согласно одному из вариантов реализации соединение формулы IV соответствует формуле IVb Как правило, способ получения соединений формулы IVb из соединений формулы Vb осуществляют в подходящем апротонном растворителе при примерно -78-80 С в течение примерно от 10 мин до 24 ч. Неограничивающие примеры подходящих апротонных растворителей включают CH2Cl2, ацетонитрил,CH2ClCH2Cl или другие галогенуглеродные растворители. Более конкретно, способ проводят при примерно -10-65 С в течение примерно от 10 мин до 4 ч. Мольное отношение соединения формулы Vb к цианидному реагенту составляет примерно от 1:1 до 1:10, более конкретно, примерно от 1:2 до 1:6. Мольное отношение соединения формулы Vb к кислоте Льюиса составляет примерно от 1:0,1 до примерно 1:10, более конкретно, примерно от 1:0,7 до примерно 1:6. Стандартные, но неограничивающие, цианидные реагенты включают (R43)3SiCN, R45C(O)CN и 43R C(O)CN, где R43 и R45 определены выше. Предпочтительным цианидным реагентом является(CH3)3SiCN. Другим предпочтительным цианидным реагентом является R43C(O)CN, где R43 представляет собой (C1-C8)алкокси или (C1-C8)замещенный алкокси. Превращение соединений формулы Vb в соединение формулы IVb ускоряют кислотами Льюиса. Многие кислоты Льюиса могут ускорять указанное превращение и включают многие кислоты Льюиса,которые являются коммерчески доступными. Неограничивающие примеры кислот Льюиса, содержащих бор, подходящих для ускорения указанного превращения, представляют собой эфираты трифторида бора и метилового, этилового, пропилового и бутилового эфиров; трифторид-трет-бутилметилэфират бора; комплекс трифторида бора и трифторидметилсульфида бора. Неограничивающие примеры кислот Льюиса, содержащих триалкилсилильные группы, подходящих для ускорения указанного превращения, представляют собой триметилсилилтрифторметансульфонат, другие триметилсилилполифтор-алкилсульфонаты, трет-бутилдиметилсилилтрифторметансульфонат и триэтилсилилтрифторметансульфонат. Дополнительные неограничивающие примеры кислот Льюиса, подходящих для ускорения указанного превращения, представляют собой TiCl4, AlCl3, ZnCl2, ZnI2, SnCl4, InCl3, Sc(трифторметансульфонат)3, трифторметансульфонат серебра, трифторметансульфонат цинка, трифторметансульфонат магния, трифлат таллия, трифторметансульфонат лантана, трифторметансульфонат индия (III), трифторметансульфонат церия (IV), трифторметансульфонат эрбия (III), трифторметансульфонат гадолиния (III), трифторметансульфонат лютеция (III), трифторметансульфонат неодима (III), трифторметансульфонат празеодима(III), трифторметансульфонат самария (III), трифторметансульфонат тербия (III), трифторметансульфонат диспрозия (III), трифторметансульфонат европия, трифторметансульфонат гольмия (III), трифторметансульфонат тулия (III), трифторметансульфонат иттрия (III), никелевая соль трифторметансульфокислоты, трифторметансульфонат гафния, трифторметансульфонат висмута (III), трифторметансульфонат галлия (III), трифторметансульфонат церия (III), трифторметансульфонат иттербия (III), трифторметансульфонат теллура (IV), трифторметансульфонат циркония (IV), трифторметансульфонат висмута, трифторметансульфонат железа (II), Sn(трифторметансульфонат)2, InBr3, AuCl3, монтмориллонитые глины,Cu(трифторметансульфонат)2, трифторметансульфонат ванадила и солевые комплексы Ti и Vn (Белоконь с соавторами (Belokon, et al.), Tetrahedron 2001, 771). Согласно предпочтительному варианту реализации кислота Льюиса представляет собой триметилсилилтрифторметансульфонат. Согласно другому предпочтительному варианту реализации кислота Льюиса представляет собой триметилсилилтрифторметансульфонат, а выход соединения формулы IVb составляет 50% или более. Согласно другому предпочтительному варианту реализации кислота Льюиса представляет собой триметилсилилтрифтор-метансульфонат,а выход соединения формулы IVb составляет 70% или более. Согласно другому предпочтительному варианту реализации кислота Льюиса представляет собой триметилсилилтрифторметансульфонат, а выход соединения формулы IVb составляет 90% или более. Согласно другому варианту реализации способа получения соединения формулы IVb R56 в соединении формулы Vb представляет собой ОН. Дополнительные независимые аспекты указанного варианта реализации представляют собой: Кислота Льюиса содержит бор. Кислота Льюиса содержит BF3 или BCl3. Кислота Льюиса представляет собой BF3-O(R53)2, BF3-S(R53)2, BCl3-O(R53)2 или BCl3-S(R53)2, причем каждый R53 независимо представляет собой (C1-C8)алкил, (C1-C8)замещенный алкил, (С 2-С 8)алкенил, (C2-C8) замещенный алкенил,(C2-C8)алкинил, (C2-C8)замещенный алкинил, С 6-С 20 арил, С 6-С 20 замещенный арил, С 2-С 20 гетероциклил,С 2-С 20 замещенный гетероциклил, С 7-С 20 арилалкил или С 7-С 20 замещенный арилалкил; причем каждый(С 1-С 8)алкил, (С 2-С 8)алкенил, (С 2-С 8)алкинил или арил(С 1-С 8)алкил в каждом из R53 независимо возможно замещен одним или более галогенами, и при этом один или более нетерминальных атомов углерода в каждом из указанных (С 1-С 8)алкилов возможно заменены на -О- или -S(O)n-; или два R53 вместе с атомом кислорода, к которому они оба присоединены, образуют 3-7-членное гетероциклическое кольцо, причем один атом углерода указанного гетероциклического кольца может быть заменен на -О- или -S(O)n-. Кислота Льюиса представляет собой BF3-O(R53)2, a R53 представляет собой (C1-C8) алкил. Кислота Льюиса содержит R57S(O)2OSi(R43)3, причем R57 замещен двумя или более галогенами и представляет собой (С 1 С 8)алкил или замещенный (С 1-С 8)алкил. Кислота Льюиса представляет собой R57S(O)2OSi(CH3)3, a R57 представляет собой (С 1-С 8)алкил, замещенный тремя или более атомами фтора. Кислота Льюиса представляет собой триметилсилилтрифлат. Кислота Льюиса содержит переходный металл или его соль. Кислота Льюиса содержит титан или его соль. Кислота Льюиса содержит TiCl4. Кислота Льюиса содержит лантанид или его соль. Кислота Льюиса содержит скандий или его соль. Кислота Льюиса содержит ванадий или его соль. Кислота Льюиса содержит олово или его соль. Кислота Льюиса содержит SnCl4. Кислота Льюиса содержит цинк или его соль. Кислота Льюиса содержит ZnCl2. Кислота содержит самарий или его соль. Кислота Льюиса содержит никель или его соль. Кислота Льюиса содержит медь или ее соль. Кислота Льюиса содержит алюминий или его соль. Кислота Льюиса содержит золото или его соль. Кислота Льюиса содержит трифторметансульфонат цинка. Кислота Льюиса содержит трифторметансульфонат индия (III). Кислота Льюиса содержит трифторметансульфонат скандия (III). Кислота Льюиса содержит трифторметансульфонат иттрия (III). Дополнительные независимые аспекты указанного варианта реализации представляют собой: Кислота Льюиса содержит бор. Кислота Льюиса содержит BF3 или BCl3. Кислота Льюиса представляет собой BF3-O(R53)2, BF3-S(R53)2, BCl3-O(R53)2 или BCl3-S(R53)2, причем каждый R53 независимо представляет собой (C1-C8)алкил, (C1-C8)замещенный алкил, (С 2-С 8)алкенил, (C2-C8)замещенный алкенил, (C2C8)алкинил, (C2-C8)замещенный алкинил, С 6-С 20 арил, С 6-С 20 замещенный арил, С 2-С 20 гетероциклил, С 2 С 20 замещенный гетероциклил, С 7-С 20 арилалкил или С 7-С 20 замещенный арилалкил; причем каждый (С 1 С 8)алкил, (С 2-С 8)алкенил, (С 2-С 8)алкинил или арил(С 1-С 8)алкил в каждом R53 независимо возможно замещен одним или более галогенами и при этом один или более нетерминальных атомов углерода в каждом из указанных (С 1-С 8)алкилов возможно заменены на -О- или -S(O)n-; или два R53 вместе с атомом кислорода, к которому они оба присоединены, образуют 3-7-членное гетероциклическое кольцо, причем один атом углерода указанного гетероциклического кольца может быть заменен на -О- или -S(O)n-. Кислота Льюиса представляет собой BF3-O(R53)2, a R53 представляет собой (C1-C8)алкил. Кислота Льюиса содержит R57S(O)2OSi(R43)3, причем R57 замещен двумя или более галогенами и представляет собой (С 1 С 8)алкил или замещенный (С 1-С 8)алкил. Кислота Льюиса представляет собой R57S(O)2OSi(CH3)3, a R57 представляет собой (С 1-С 8)алкил, замещенный тремя или более атомами фтора. Кислота Льюиса представляет собой триметилсилилтрифлат. Кислота Льюиса содержит переходный металл или его соль. Кислота Льюиса содержит титан или его соль. Кислота Льюиса содержит TiCl4. Кислота Льюиса содержит лантанид или его соль. Кислота Льюиса содержит скандий или его соль. Кислота Льюиса содержит ванадий или его соль. Кислота Льюиса содержит олово или его соль. Кислота Льюиса содержит SnCl4. Кислота Льюиса содержит цинк или его соль. Кислота Льюиса содержит ZnCl2. Кислота Льюиса содержит самарий или его соль. Кислота Льюиса содержит никель или его соль. Кислота Льюиса содержит медь или ее соль. Кислота Льюиса содержит алюминий или его соль. Кислота Льюиса содержит золото или его соль. Кислота Льюиса содержит трифторметансульфонат цинка. Кислота Льюиса содержит трифторметансульфонат индия (III). Кислота Льюиса содержит трифторметансульфонат скандия (III). Кислота Льюиса содержит трифторметансульфонат иттрия (III). Согласно одному из вариантов реализации способа получения соединения формулы Vb, в которомR56 представляет собой -OC(O)R58 или OC(O)OR58, мольное отношение соединения формулы Vb, в котором R56 представляет собой ОН, к YC(O)R58 или YC(O)OR58 составляет примерно от 1:1 до 1:10, предпочтительно примерно от 1:1 до 1:6,5. Как правило, соединение формулы Vb, в котором R56 представляет собой ОН, обрабатывают YC(O)R58 или YC(O)OR58 в апротонном растворителе, не ограничивающимся только ими, таком как пиридин, ТГФ или диэтиловый эфир, при примерно -30-125 С в течение примерно от 30 мин до 24 ч. Согласно одному из аспектов указанного варианта реализации Y представляет собой галоген. Согласно другому аспекту указанного варианта реализации Y представляет собой Cl. Согласно другому аспекту указанного варианта реализации Y представляет собой циано. Согласно другому аспекту указанного варианта реализации Y представляет собой имидазол-1-ил. Согласно другому аспекту указанного варианта реализации Y представляет собой пиразол-1-ил. Согласно другому аспекту указанного варианта реализации Y представляет собой -O-C(O)R58. Согласно другому аспекту указанного варианта реализации Y представляет собой -O-C(O)OR58. Согласно другому аспекту указанного варианта реализации R58 представляет собой C1-С 6 алкил. Согласно другому аспекту указанного варианта реализации R58 представляет собой СН 3. Согласно другому аспекту указанного варианта реализации R58 представляет собой C1-С 6 алкил, a Y представляет собой -O-C(O)R58. Согласно другому аспекту указанного варианта реализации R58 представляет собой СН 3, a Y представляет собой -O-C(O)R58. Взаимодействие соединения формулы Vb, в котором R56 представляет собой ОН и YC(O)R58 илиYC(O)OR58 можно катализировать или ускорить в присутствии подходящего основания. Неограничивающие примеры подходящих оснований включают триэтиламин, диизопропилэтиламин, пиридин, 4 диметиламинопиридин, DBU, NaH и KH. Мольное отношение YC(O)R58 или YC(O)OR58 к основанию,как правило, составляет примерно от 1:1 до 1:4. Предложен способ получения соединения формулы V, в котором R56 представляет собой ОН, причем указанный способ включает:(е) обеспечение соединения формулы VI(f) обработку соединения формулы VI металлорганическим соединением формулы VII Формула VII где М представляет собой MgX3 или Li, a X3 представляет собой галоген; с получением, таким образом, соединения формулы V, в котором R56 представляет собой ОН. Согласно другому варианту реализации способа получения соединения формулы V, в котором R56 представляет собой ОН, соединение формулы V соответствует формуле Vb, в котором R56 представляет собой ОН, а соединение формулы VI представляет собой соединение формулы VIb Формула VIb Дополнительные независимые аспекты указанного варианта реализации представляют собой М представляет собой MgX3. M представляет собой Li. Как правило, способ получения соединения формулы Vb, в котором R56 представляет собой ОН,проводят в подходящем апротонном растворителе при примерно -100-50 С в течение примерно 5 мин-24 ч. Неограничивающие примеры подходящих апротонных растворителей включают ТГФ, диоксан и диэтиловый эфир. Более конкретно, подходящий растворитель представляет собой ТГФ, а предпочтительная температура составляет примерно -78-0 С. Мольное отношение соединения формулы VII к соединению формулы VIb составляет примерно от 1:2 до 2:1, предпочтительно примерно 1:1. Предложен способ получения соединения формулы VII, в котором М представляет собой MgX3 илиLi, a X3 представляет собой галоген, причем указанный способ включает(g) обеспечение соединения формулы VIII(h) обработку соединения формулы VIII металлорганическим реагентом, включающим магнийорганическое или литийорганическое соединение; с получением, таким образом, соединения формулы VII. Согласно другому варианту реализации способ получения соединения формулы VII из соединения формулы VIII включает следующие независимые аспекты.(c) Каждый R11 или R12 независимо представляет собой (С 1-С 8)алкил, -С(=О)(С 1-С 8)алкил, -S(О)n(С 1 С 8)алкил, арил(С 1-С 8)алкил или Si(R43)3; или R11 и R вместе с атомом азота, к которому они присоединены, образуют 3-7-членное гетероциклическое кольцо; или R11 и R12, взятые совместно, представляют собой -Si(R43)2(X42)mSi(R43)2-. Каждый R11 или R12 независимо представляет собой (C1-С 8)алкил. Каждый R11 или R12 независимо представляет собой Si(R43)3. Каждый R11 или R12 независимо представляет собойSi(R43)3, причем по меньшей мере два из R43 представляют собой СН 3 или фенил. Каждый R11 или R12 независимо представляет собой Si(СН 3)3. Каждый R11 и R+ в NR11R12 независимо выбран из Si(R43)3, илиNR11R12 независимо выбран из Si(R43)3, или R11 и R12 в NR11R12, взятые совместно, представляют собой(d) X3 представляет собой Cl. X3 представляет собой Br. X3 представляет собой I. Согласно другому варианту реализации способ получения соединения формулы VII путем обработки соединения формулы VIII металлорганическим реагентом включает применение магнийорганического соединения. Как правило, реакцию трансметаллирования проводят в подходящем апротонном растворителе при примерно -78-50 С в течение примерно от 5 мин до 24 ч. Неограничивающие примеры под-9 025085 ходящих апротонных растворителей включают ТГФ, диоксан и диэтиловый эфир. Согласно одному из вариантов реализации мольное отношение соединения формулы VIII к магнийорганическому соединению составляет примерно от 1:1 до 1:3, предпочтительно 1:2. Согласно одному из вариантов реализации магнийорганическое соединение включает хлорид, бромид или йодид алкилмагния. Согласно другому варианту реализации магнийорганическое соединение включает хлорид 2-пропилмагния. Согласно одному из вариантов реализации магнийорганическое соединение включает хлорид, бромид или йодид алкилмагния и хлорид лития. Согласно другому варианту реализации магнийорганическое соединение включает хлорид 2-пропилмагния и хлорид лития. Согласно другому варианту реализации магнийорганическое соединение представляет собой хлорид 2-пропилмагния и хлорид лития в мольном отношении 1:1. Согласно предпочтительному варианту реализации магнийорганическое соединение включает хлорид 2-пропилмагния и хлорид лития в мольном отношении 1:1, и X в формуле VIII представляет собойBr или I. Согласно другому варианту реализации в способе получения соединения формулы VII путем обработки соединения формулы VIII металлорганическим реагентом, соединение формулы VIII можно обрабатывать более чем одним магнийорганическим соединением. Указанный способ является предпочтительным в случае, если соединение формулы VIII содержит заместитель с кислым атомом водорода. Неограничивающие примеры с кислыми атомами водорода представляют собой NH2, ОН, SH, NH(C1 С 6 алкил) и т.д. Специалисты в данной области техники понимают, что группа, содержащая кислый атом водорода, в заместителе соединения формулы VIII расходует один мольный эквивалент магнийорганического соединения. Расходуемое магнийорганическое соединение может отличаться от магнийорганического соединения, которое участвует в реакции трансметаллирования. В качестве примера, но не ограничения, обработка соединения формулы VIII примерно одним мольным эквивалентом хлорида метилмагния приводит к нейтрализации кислого атома водорода в NH(С 1-С 6 алкил), ОН или SH заместителе за счет образования магниевой соли, и группа X3 (группа Cl, Br или I) в соединении формулы VIII быть трансметаллирована другим магнийорганическим соединением, таким как хлорид 2-пропилмагния или хлорид 2-пропилмагния и хлорид лития. Аналогично, если присутствуют дополнительные кислые атомы водорода, для нейтрализации каждого дополнительного кислого атома водорода дополнительно потребуется примерно один эквивалент магнийорганического соединения, например, каждый дополнительный заместитель NH2 требует примерно два дополнительных эквивалента магнийорганического соединения. Как правило, реакции трансметаллирования, согласно указанному аспекту, проводят в подходящем апротонном растворителе при примерно -78-50 С в течение примерно от 5 мин до 24 ч. Неограничивающие примеры подходящих апротонных растворителей включают ТГФ, диоксан и диэтиловый эфир. Согласно одному из вариантов реализации соединение формулы VII получают путем обработки соединения формулы VIII примерно одним мольным эквивалентом, в расчете на каждый кислый атом водорода в заместителе, первого магнийорганического соединения с последующей обработкой вторым магнийорганическим соединением для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому аспекту указанного варианта реализации мольное отношение первого магнийорганического соединения к каждому кислому атому водорода в заместителе молекулы формулы VIII составляет примерно от 1:1 до 1:1,4, а мольное отношение второго магнийорганического соединения к соединению формулы VIII составляет примерно от 1:0,8 до 1:2. Согласно другому аспекту указанного варианта реализации первое магнийорганическое соединение включает хлорид, бромид или йодид алкилмагния. Согласно другому аспекту указанного варианта реализации первое магнийорганическое соединение включает хлорид метилмагния. Согласно другому аспекту указанного варианта реализации второе магнийорганическое соединение включает хлорид, бромид или йодид алкилмагния. Согласно другому аспекту указанного варианта реализации второе магнийорганическое соединение включает хлорид 2-пропилмагния. Согласно другому аспекту указанного варианта реализации второе магнийорганическое соединение включает хлорид, бромид или йодид алкилмагния и хлорид лития. Согласно другому аспекту указанного варианта реализации магнийорганическое соединение представляет собой хлорид 2-пропилмагния и хлорид лития в мольном отношении 1:1. Согласно предпочтительному аспекту указанного варианта реализации первое магнийорганическое соединение представляет собой хлорид метилмагния, а второе магнийорганическое соединение включает хлорид 2-пропилмагния. Согласно другому предпочтительному аспекту указанного варианта реализации первое магнийорганическое соединение представляет собой хлорид метилмагния, а второе магнийорганическое соединение представляет собой хлорид 2 пропилмагния и хлорид лития в мольном отношении 1:1. Согласно другому предпочтительному аспекту указанного варианта реализации первое магнийорганическое соединение представляет собой хлорид метилмагния, второе магнийорганическое соединение представляет собой хлорид 2-пропилмагния и хлорид лития в мольном отношении примерно 1:1, а X3 в соединении формулы VIII представляет собой Br или I. Согласно другому предпочтительному аспекту указанного варианта реализации первое магнийорганическое соединение представляет собой хлорид метилмагния, второе магнийорганическое соединение представляет собой хлорид 2-пропилмагния и хлорид лития в мольном отношении примерно 1:1, X3 в соединении формулы VIII представляет собой Br или I, a R8 представляет собой NH2. Магниевые соли заместителей в соединениях формулы VIII, обсуждаемые выше, можно превра- 10025085 щать в защищенную форму заместителя, в качестве примера, но не ограничения, в силилзащищенный заместитель. Следовательно, группа X3 (группа Cl, Br или I) в соединении формулы VIII может быть трансметаллирована одним или различными магнийорганическими соединениями, такими как хлорид 2 пропилмагния или хлорид 2-пропилмагния и хлорид лития. Аналогично, в случае если присутствуют дополнительные кислые атомы водорода, для нейтрализации каждого дополнительного кислого атома водорода дополнительно требуется примерно один эквивалент магнийорганического соединения, например, каждый дополнительный заместитель NH2 требует двух дополнительных эквивалентов магнийорганического соединения, и полученные магниевые соли можно превратить в защищенные группы, в качестве примера, но не ограничения, силилзащищенные группы. Неограничивающие примеры полученных защищенных заместителей представляют собой OSi(R43)3, SSi(R43)3, N[Si(R43)3][С 1-С 6 алкил],N[Si(R43)2(CH2)2Si(R43)2] и N[Si(R43)3]2. Все указанные промежуточные соединения включены в рамки настоящего изобретения. Неограничивающие примеры силилирующих реагентов, необходимых для превращения промежуточной магниевой соли заместителя в защищенный заместитель, включают X3Si(R43)3,X3Si(R43)2(CH2)2Si(R43)2X3 и R57S(O)2OSi(R43)3; более конкретно ClSi(R43)3, ClSi(R43)2(CH2)2Si(R43)2Cl иCF3S(O)2OSi(R43)3; наиболее конкретно ClSi(CH3)3, ClSi(CH3)2(CH2)2 Si(CH3)2Cl и CF3S(O)2OSi(CH3)3. Указанные силилирующие реагенты могут присутствовать перед добавлением начального металлорганического агента в случае, если температуру реакции в достаточной степени контролируют, или силилирующие агенты можно добавлять после превращения заместителя в магниевую соль. Как правило, конверсия заместителей соединений формулы VIII, содержащих кислые атомы водорода, в защищенные заместители, проводят в подходящем апротонном растворителе при примерно -78-50 С в течение примерно от 5 мин до 24 ч. Неограничивающие примеры подходящих апротонных растворителей включают ТГФ, диоксан и диэтиловый эфир. Согласно одному из вариантов реализации соединение формулы VII получают путем обработки соединения формулы VIII, содержащего заместители с кислыми атомами водорода, примерно одним мольным эквивалентом первого магнийорганического соединения на каждый кислый атом водорода в заместителе, обработки примерно 1-1,4 эквивалентами реагента, содержащего защитную группу, на каждый кислый атом водорода и обработку 1-2 эквивалентами аналогичного или отличающегося магнийорганического соединения для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому варианту реализации соединение формулы VII получают путем обработки смеси соединения формулы VIII и примерно 1-1,4 эквивалентов реагента, содержащего защитную группу, на каждый кислый атом водорода, содержащийся в соединении формулы VIII примерно 1-1,4 эквивалентами первого магнийорганического соединения на каждый кислый атом водорода в заместителе, с последующей обработкой 1-2 эквивалентами аналогичного или отличающегося магнийорганического соединения для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому варианту реализации соединение формулы VII получают путем обработки смеси соединения формулы VIII и примерно 1-1,4 эквивалентов защитного реагента на каждый кислый атом водорода в соединении формулы VIII 1-1,4 эквивалентами магнийорганического соединения на каждый кислый атом водорода в заместителе и дополнительно 1-2 эквивалентами магнийорганического соединения для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому аспекту указанного варианта реализации X3 в соединении формулы VIII представляет собой Br или I, a R8 в соединении формулы VIII представляет собой NH2. Согласно другому варианту реализации способ получения соединения формулы VII, в котором М представляет собой Li, включает обработку соединения формулы VIII литийорганическим соединением. Как правило, реакцию трансметаллирования проводят в подходящем апротонном растворителе при примерно -100-20 С в течение примерно от 5 мин до 24 ч. Неограничивающие примеры подходящих апротонных растворителей включают ТГФ и диэтиловый эфир. Согласно одному из аспектов указанного варианта реализации мольное отношение соединения формулы VIII к литийорганическому соединению составляет примерно от 1:1 до 1:3, предпочтительно примерно 1:1,4. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает алкиллитиевое соединение. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает н-бутиллитий. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает изобутиллитий. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает трет-бутиллитий. Согласно предпочтительному варианту реализации литийорганическое соединение включает алкиллитиевое соединение, а X3 в формуле VIII представляет собой Br или I. Согласно другому варианту реализации, в котором соединение формулы VII получают путем обработки соединения формулы VIII литийорганическим соединением, соединение формулы VIII может быть обработано более чем одним мольным эквивалентом литийорганического соединения. Указанный способ является предпочтительным в случае, если соединение формулы V содержит заместитель с кислым атомом водорода. Неограничивающие примеры заместителей с кислыми атомами водорода представляют собой NH2, ОН, SH, NH(C1-C6 алкил) и т.д. Специалисты в данной области техники понимают, что группа, содержащая кислый атом водорода, в заместителе соединения формулы VIII расходует один мольный эквивалент литийорганического соединения. В качестве примера, но не ограничения, обработка соединения формулы V примерно одним мольным эквивалентом литийорганического соединения приводит к нейтрализации кислого атома водорода в NH(С1-С 6 алкил), ОН или SH заместителе за счет образования литиевой соли, и группа X (группа Cl, Br или I) в соединение формулы VIII может быть трансметаллирована другим мольным эквивалентом литийорганического соединения. Аналогично, в случае если присутствуют дополнительные кислые атомы водорода, для нейтрализации каждого кислого атома водорода дополнительно требуется примерно эквивалентное количество литийорганического соединения, например, каждый дополнительный заместитель NH2 требует примерно два дополнительных эквивалента литийорганического соединения, как правило, реакции трансметаллирования, согласно указанному аспекту, проводят в подходящем апротонном растворителе при примерно -100-20 С в течение примерно от 5 мин до 24 ч. Неограничивающие примеры подходящих апротонных растворителей включают ТГФ, диоксан и диэтиловый эфир. Согласно одному из аспектов указанного варианта реализации мольное отношение литийорганического соединения к каждому кислому атому водорода в заместителях в молекуле формулы VIII составляет примерно от 1:1 до 1:1,4, а мольное отношение дополнительного количества литийорганического соединения к соединению формулы VIII составляет примерно от 1:0,8 до 1:1,4. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает алкиллитиевое соединение. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает н-бутиллитий. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает изобутиллитий. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает трет-бутиллитий. Согласно предпочтительному аспекту указанного варианта реализации литийорганическое соединение включает (С 1-С 6)алкиллитий, а X3 в формуле VIII представляет собой Br или I. Литиевые соли заместителей в соединениях формулы VIII, обсуждаемые выше, можно превращать в защищенные формы заместителей, в качестве примера, но не ограничения, в силилзащищенный заместитель. Следовательно, группа X (группа Cl, Br или I) в соединении формулы VIII может быть трансметаллирована одним или различными литийорганическим соединением. Аналогично, в случае если присутствуют дополнительные кислотные атомы водорода, для нейтрализации каждого дополнительного кислотного атома водорода дополнительно требуется примерно один эквивалент литийорганического соединения; например, каждый дополнительный заместитель NH2 требует примерно два дополнительных эквивалента литийорганического соединения, и получаемые литиевые соли можно превращать в защитные группы, в качестве примера, но не ограничиваясь ими, в силилзащитные группы. Неограничивающие примеры получаемых защищенных заместителей представляют собой OSi(R43)3, SSi(R43)3,N[Si(R43)3][С 1-С 6 алкил], N[Si(R43)2(CH2)2 Si(R43)2] и N[Si(R43)3]2. Все указанные промежуточные соединения, содержащие защищенные заместители, включены в рамки настоящего изобретения. Неограничивающие примеры силилирующих реагентов, необходимых для превращения промежуточной литиевой соли заместителей в защищенные заместители, включают X3Si(R43)3, X3Si(R43)2(CH2)2Si(R43)2X3 иR57S(O)2OSi(R43)3; более конкретно ClSi(R43)3, ClSi(R43)2(CH2)2Si(R43)2Cl и CF3S(O)2OSi(R43)3, наиболее конкретно ClSi(CH3)3, ClSi(CH3)2(CH2)2Si(CH3)2Cl и CF3S(O)2OSi(CH3)3. Указанные силилирующие агенты могут присутствовать перед добавлением начального металлорганического агента в случае если, температуру реакции в достаточной степени контролируют, или силилирующие агенты можно добавлять после превращения заместителя в литиевую соль. Как правило, конверсию заместителей соединения формулы VIII, содержащих кислые атомы водорода, в защищенные заместители проводят в подходящем апротонном растворителе при примерно -10020 С в течение примерно от 5 мин до 24 ч. Неограничивающие примеры подходящих апротонных растворителей включают ТГФ, диоксан и диэтиловый эфир. Согласно одному из вариантов реализации соединение формулы VII получают путем обработки соединения формулы VIII, содержащего заместители с кислыми атомами водорода, примерно 1-1,4 мольными эквивалентами литийорганического соединения на каждый кислый атом водорода в заместителе,обработки примерно 1-1,4 эквивалентами реагента, содержащего защитную группу, на каждый кислый атом водорода, и обработки 1-1,4 эквивалентами аналогичного или отличающегося литийорганического соединения для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому варианту реализации соединение формулы VII получают путем обработки смеси соединения формулы VIII и примерно 1-1,4 эквивалентов реагента, содержащего защитную группу, на каждый кислый атом водорода в соединении формулы VIII примерно 1-1,4 эквивалентами первого литийорганического соединения на каждый кислый атом водорода в заместителе, с последующей обработкой 1-1,4 эквивалентами аналогичного или отличающегося литийорганического соединения для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому варианту реализации соединение формулы VII получают путем обработки смеси соединения формулы VIII и примерно 1-1,4 эквивалентов защитного реагента на каждый кислый атом водорода в соединении формулы VIII примерно 1-1,4 эквивалентами литийорганического соединения на каждый кислый атом водорода в заместителе и дополнительно 1-1,4 эквивалентами литийорганического соединения для трансметаллирования группы X3 в соединении формулы VIII. Согласно другому аспекту- 12025085 указанного варианта реализации X3 в формуле VIII представляет собой Br или I, a R в формуле VIII представляет собой NH2. Согласно другому аспекту указанного варианта реализации литийорганическое соединение включает алкиллитиевое соединение. Согласно другому варианту реализации литийорганическое соединение включает н-бутиллитий. Согласно другому варианту реализации литийорганическое соединение включает изобутиллитий. Согласно другому варианту реализации литийорганическое соединение включает трет-бутиллитий. Согласно предпочтительному варианту реализации литийорганическое соединение включает (С 1-С 6)алкиллитиевое соединение, а X3 в формуле VIII представляет собой Br илиI. Согласно другому варианту реализации реагент, содержащий защитную группу, представляет собой силилирующий реагент. Согласно другому варианту реализации реагент, содержащий защитную группу,представляет собой X3Si(R43)3 или R57S(O)2OSi(R43)3. Согласно другому варианту реализации реагент,содержащий защитную группу, представляет собой ClSi(R43)3 или CF3S(O)2OSi(R43)3. Согласно другому варианту реализации реагент, содержащий защитную группу, представляет собой ClSi(CH3)3 илиCF3S(O)2OSi(CH3)3. Предложено соединение, подходящее для синтеза противовирусного соединения формулы Ib, представленного формулой IX Формула IX или его фармацевтически приемлемая соль; гдеR2 независимо представляет собой F или OR44;R4 независимо представляет собой Н или OR44; или любые два R44, взятые совместно, представляют собой -C(R59)2; каждый R45 представляет собой Н, (C1-С 6)алкил, (С 6-С 14)арил или (С 6-С 14)арил(С 1-С 6)алкил; каждый R59 независимо представляет собой Н, (C1-С 6)алкил или (С 6-С 14)арил;R9 представляет собой Н или NH2; при этом замещение означает, что один или более атомов водорода независимо замещены заместителем, представляющим собой -Rb или =O, где каждый Rb независимо представляет собой (С 1-С 6)алкил или (С 6-С 14)арил. Согласно другому варианту реализации соединение формулы IX выбрано из группы, состоящей из фармацевтически приемлемых солей. Предложен способ получения соединения формулы X Формула X или его фармацевтически приемлемой соли или сложного эфира; гдеR43 представляет собой (C1-С 6)алкил; каждый R44 или R47 независимо представляет собой -C(R45)2R46, -C(O)R45 или -C(O)OR45; каждый R45 независимо представляет собой Н, (C1-С 6)алкил, (С 6-С 14)арил или (С 6-С 14)арил(С 1-С 6)алкил;R9 представляет собой Н или NH2; при этом замещение означает, что один или более атомов водорода независимо замещены заместителем, представляющим собой -Rb или =O, где каждый Rb независимо представляет собой (С 1-С 6)алкил или (С 6-С 14)арил; причем указанный способ включает обработку соединения формулы V Формула V где R56 представляет собой ОН кислотой Льюиса и восстановителем, представляющим собойHSi(R43)3; с получением, таким образом, соединения формулы X. Соединения формулы X подходят для получения противовирусных соединений формулы I. Согласно одному из вариантов реализации способа соединение формулы X соответствует формуле Как правило, способ получения соединений формулы Xb из соединений формулы Vb осуществляют в подходящем апротонном растворителе при примерно -78-80 С в течение примерно от 10 мин до 7 дней. Неограничивающие примеры подходящих апротонных растворителей включают CH2Cl2, ацетонитрил,CH2ClCH2Cl или другие галогенуглеродные растворители. Более конкретно, способ проводят при примерно -78 -25 С в течение примерно от 3 ч до 7 дней. Мольное отношение соединения формулы Vb кHSi(R43)3 составляет примерно от 1:1 до 1:10, более конкретно примерно от 1:2 до 1:6. Мольное отношение соединения формулы Vb к кислоте Льюиса составляет примерно от 1:0,1 до примерно 1:10, более конкретно примерно от 1:1 до 1:6. Как правило, мольное отношение кислоты Льюиса к HSi(R43)3 составляет примерно от 0,1:1 до 1:10, предпочтительно примерно 1:1. Превращение соединения формулы Vb в соединение формулы Xb ускоряют кислотами Льюиса. Многие кислоты Льюиса, включая многие кислоты Льюиса, которые являются коммерчески доступными, могут ускорять указанное превращение. Неограничивающие примеры кислот Льюиса, содержащих бор, которые подходят для ускорения указанного превращения, представляют собой эфираты трифторида бора и метилового, этилового, пропилового и бутилового эфира; трифторид-трет-бутилметилэфират бора, комплекс трифторида бора и трифторидметилсульфида бора. Неограничивающие примеры кислот Льюиса, содержащих триалкилсилильные группы, которые подходят для ускорения указанного превращения, представляют собой триметилсилилтрифторметансульфонат, другие триметилсилилполифторалкилсульфонаты, трет-бутилдиметилсилилтрифтор-метансульфонат и триэтилсилилтрифторметансульфонат. Дополнительные неограничивающие примеры кислот Льюиса, подходящих для ускорения указанного превращения, представляют собой TiCl4, AlCl3, ZnCl2, ZnI2, SnCl4, InCl3, Sc(трифторметансульфонат)3,трифторметансульфонат серебра, трифторметансульфонат цинка, трифторметансульфонат магния, трифлат таллия, трифторметансульфонат лантана, трифторметансульфонат индия (III), трифторметансульфонат церия (IV), трифторметансульфонат эрбия (III), трифторметансульфонат гадолиния (III), трифторметансульфонат лютеция (III), трифторметансульфонат неодима (III), трифторметансульфонат празеодима(III), трифторметансульфонат самария (III), трифторметансульфонат тербия (III), трифторметансульфонат диспрозия (III), трифторметансульфонат европия, трифторметансульфонат гольмия (III), трифторметансульфонат тулия (III), трифторметансульфонат иттрия (III), никелевая соль трифторметансульфокислоты, трифторметансульфонат гафния, трифторметансульфонат висмута (III), трифторметансульфонат галлия (III), трифторметансульфонат церия (III), трифторметансульфонат иттербия (III), трифторметансульфонат теллура (IV), трифторметансульфонат циркония (IV), трифторметансульфонат висмута, трифторметансульфонат железа (II), Sn(трифторметансульфонат)2, InBr3, AuCl3, монтмориллонитные глины,Cu(трифторметансульфонат)2, трифторметансульфонат ванадила и солевые комплексы Ti и Vn (Белоконь с соавторами (Belokon, et al.), Tetrahedron 2001, 771). Согласно предпочтительному варианту реализации кислота Льюиса представляет собой трифторидэфират бора. Согласно другому предпочтительному варианту реализации кислота Льюиса представляет собой трифторидэфират бора, а выход соединения формулы Xb составляет 50% или более. Согласно другому предпочтительному варианту реализации кислота Льюиса представляет собой трифторидэфират бора, а выход соединения формулы Xb составляет 70% или более. Согласно другому предпочтительному варианту реализации кислота Льюиса представляет собой трифторидэфират бора, а выход соединения формулы Xb составляет 90% или более. Согласно другому варианту реализации способа получения соединения формулы Xb, R56 в формулеVb представляет собой ОН. Дополнительные независимые аспекты указанного варианта реализации представляют собой: Кислота Льюиса содержит бор. Кислота Льюиса содержит BF3 или BCl3. Кислота Льюиса представляет собой BF3-O(R53)2, BF3-S(R53)2, BCl3-O(R53)2 или BCl3-S(R53)2, причем каждый R53 независимо представляет собой (C1-C8)алкил, (C1-C8)замещенный алкил, (С 2-С 8)алкенил, (C2-C8)замещенный алкенил, (C2C8)алкинил, (C2-C8)замещенный алкинил, С 6-С 20 арил, С 6-С 20 замещенный арил, С 2-С 20 гетероциклил, С 2 С 20 замещенный гетероциклил, С 7-С 20 арилалкил или С 7-С 20 замещенный арилалкил; причем каждый (C1 С 8)алкил, (С 2-С 8)алкенил, (С 2-С 8)алкинил или арил(С 1-С 8)алкил в каждом из R53 независимо возможно замещен одним или более галогенами и при этом один или более нетерминальных атомов углерода в каждом из указанных (С 1-С 8)алкилов возможно заменены на -О- или -S(O)n-; или два R53 вместе с атомом кислорода, к которому они оба присоединены, образуют 3-7-членное гетероциклическое кольцо, причем один атом углерода указанного гетероциклического кольца может быть заменен на -О- или -S(O)n-. Кислота Льюиса представляет собой BF3-O(R53)2, a R53 представляет собой (C1-C8)алкил. Кислота Льюиса содержит R57S(O)2OSi(R43)3, причем R57 замещен двумя или более галогенами и представляет собой (С 1 С 8)алкил или замещенный (С 1-С 8)алкил. Кислота Льюиса представляет собой R57S(O)2OSi(CH3)3, a R57 представляет собой (С 1-С 8)алкил, замещенный тремя или более атомами фтора. Кислота Льюиса представляет собой триметилсилилтрифлта. Кислота Льюиса содержит титан или его соль. Кислота Льюиса содержит TiCl4 Кислота Льюиса содержит лантанид или его соль. Кислота Льюиса содержит скандий или его соль. Кислота Льюиса содержит ванадий или его соль. Кислота Льюиса содержит олово или его соль. Кислота Льюиса содержит SnCl4. Кислота Льюиса содержит цинк или его соль. Кислота Льюиса содержит ZnCl2. Кислота Льюиса содержит самарий или его соль. Кислота Льюиса содержит никель или его соль. Кислота Льюиса содержит медь или ее соль. Кислота Льюиса содержит алюминий или его соль. Кислота Льюиса содержит золото или его соль. Кислота Льюиса содержит трифторметансульфонат цин- 15025085 ка. Кислота Льюиса содержит трифторметансульфонат индия (III). Кислота Льюиса содержит трифторметансульфонат скандия (III). Кислота Льюиса содержит трифторметансульфонат иттрия (III). Определения Если не указано иное, следующие термины и фразы, используемые в настоящем описании, имеют следующие значения: В случае если в настоящем описании используют товарные знаки, заявитель независимо включает товарный знак продукта и активного(ых) ингредиента(ов) продукта. Используемое в настоящем описании "соединение согласно настоящему изобретению" или "соединение формулы I" означает соединение формулы I или его фармацевтически приемлемую соль. Аналогично, применительно к выделяемым промежуточным соединениям, фраза "соединение формулы (номер)" означает соединение указанной формулы и его фармацевтически приемлемые соли."Алкил" представляет собой углеводород, содержащий первичный, вторичный, третичный атомы углерода или атом углерода цикла. Например, алкильная группа может содержать от 1 до 20 атомов углерода (т.е. C1-С 20 алкил), от 1 до 8 атомов углерода (т.е. С 1-С 8 алкил) или от 1 до 6 атомов углерода (т.е.C1-С 6 алкил). Примеры подходящих алкильных групп включают, но не ограничиваются только ими, метил (Me, -СН 3), этил (Et, -СН 2 СН 3), 1-пропил (н-Pr, н-пропил, -СН 2 СН 2 СН 3), 2-пропил (и-Pr, изо-пропил,-СН(СН 3)2), 1-бутил (н-Bu, н-бутил, -СН 2 СН 2 СН 2 СН 3), 2-метил-1-пропил (и-Bu, и-бутил, -СН 2 СН(СН 3)2),2-бутил (втор-Bu, втор-бутил, -СН(СН 3)СН 2 СН 3), 2-метил-2-пропил (т-Bu, т-бутил, -С(СН 3)3), 1-пентил"Алкенил" представляет собой углеводород, содержащий первичный, вторичный, третичный атом углерода или атом углерода в цикле и по меньшей мере одно место ненасыщения, т.е. углерод-углеродную sp2 двойную связь. Например, алкенильная группа может содержать от 2 до 20 атомов углерода(т.е. С 2-С 20 алкенил), от 2 до 8 атомов углерода (т.е. С 2-С 8 алкенил) или от 2 до 6 атомов углерода (т.е. С 2 С 6 алкенил). Примеры подходящих алкенильных групп включают, но не ограничиваются только ими,этилен или винил (-СН=СН 2), аллил (-СН 2 СН=СН 2), циклопентенил (-С 5 Н 7) и 5-гексенил"Алкинил" представляет собой углеводород, содержащий первичный, вторичный, третичный атом углерода или атом углерода в цикле и по меньшей мере одно место ненасыщения, т.е., углеродуглеродную sp тройную связь. Например, алкинильная группа может содержать от 2 до 20 атомов углерода (т.е. С 2-С 20 алкинил), от 2 до 8 атомов углерода (т.е. С 2-С 8 алкинил) или от 2 до 6 атомов углерода(т.е. С 2-С 6 алкинил). Примеры подходящих алкинильных групп включают, но не ограничиваются только ими, ацетиленовую (-ССН), пропаргиловую (-СН 2 ССН) и т.д."Амино" относится в целом к азотному радикалу, который можно рассматривать как производное аммиака, имеющему формулу -N(X)2, в котором каждый "X" независимо представляет собой Н, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил и т.д. Гибридизация атома азота составляет примерно sp3. Неограничивающие типы аминогрупп включают -NH2, -N(алкил)2, -NH(алкил), -N(карбоциклил)2, -NH(карбоциклил),N(гетероциклил)2, -NH(гетероциклил), -N(арил)2, -NH(арил), -N(алкил)(арил), -N(алкил)(гетероциклил), N(карбоциклил)(гетероциклил), -N(арил)(гетероарил), -N(алкил)(гетероарил) и т.д. Термин "алкиламино" относится к аминогруппе, замещенный по меньшей мере одной алкильной группой. Неограничивающие примеры аминогрупп включают -NH2, -NH(CH3), -N(CH3)2, -NH(CH2CH3), -N(CH2CH3)2,-NH(фенил), -N(фенил)2, -NH(бензил), -N(бензил)2 и т.д. Замещенная алкиламиногруппа относится в целом к алкиламиногруппам, определенным выше, в которых по меньшей мере один замещенный алкил,определенный выше, соединен с атомом азота аминогруппы. Неограничивающие примеры алкиламиногрупп включают"Арил" означает ароматический углеводородный радикал, полученный в результате удаления одного атома водорода от одного атома углерода исходной ароматической кольцевой системы. Например,арильная группа может содержать от 6 до 20 атомов углерода, от 6 до 14 атомов углерода или от 6 до 10 атомов углерода. Типичные арильные группы включают, но не ограничиваются только ими, радикалы,полученные из бензола (например, фенил), замещенного бензола, нафталина, антрацена, бифенила и т.д."Арилалкил" относится к ациклическому алкильному радикалу, в котором один из атомов водорода,связанный с атомом углерода, как правило, терминальным или sp3 атомом углерода, заменен на арильный радикал. Типичные арилалкильные группы включают, но не ограничиваются только ими, бензил, 2- 16025085 фенилэтан-1-ил, нафтилметил, 2-нафтилэтан-1-ил, нафтобензил, 2-нафтофенилэтан-1-ил и т.д. Арилалкильная группа может содержать от 7 до 20 атомов углерода, например, алкильный фрагмент содержит от 1 до 6 атомов углерода, а арильный фрагмент содержит от 6 до 14 атомов углерода. Термин "замещенный" в отношении алкила, алкилена, арила, арилалкила, алкокси, гетероциклила,гетероарила, карбоциклила и т.д., например, "замещенный алкил", "замещенный алкилен", "замещенный арил", "замещенный арилалкил", "замещенный гетероциклил" и "замещенный карбоциклил" означают алкил, алкилен, арил, арилалкил, гетероциклил, карбоциклил, соответственно, в которых каждый из одного или более атомов водорода независимо заменен на отличный от водорода заместитель. Типичные заместители включают, но не ограничиваются только ими, -X, -Rb, -О-, =O, -ORb, -SRb, -S-, -NRb2, -N+Rb3,=NRb, -CX3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, =N2, -N3, -NHC(=O)Rb, -OC(=O)Rb,-NHC(=O)NRb2, -S(=O)2-, -S(=O)2OH, -S(=O)2Rb, -OS(=O)2ORb, -S(=O)2NRb2, -S(=O)Rb, -OP(=O)(ORb)2,-P(=O)(ORb)2, -P(=O)(O-)2, -P(=O)(OH)2, -P(O)(ORb)(O-), -C(=O)Rb, -C(=O)X, -C(S)Rb, -C(O)ORb, -C(O)O-,-C(S)ORb, -C(O)SRb, -C(S)SRb, -C(O)NRb2, -C(S)NRb2, -C(=NRb)NRb2, причем каждый Х независимо представляет собой галоген: F, Cl, Br или I; а каждый Rb независимо представляет собой Н, алкил, арил, арилалкил, гетероцикл или защитную группу или фрагмент пролекарства. Алкиленовые, алкениленовые и алкиниленовые группы могут быть замещены аналогично. Если не указано обратное, в случае если термин "замещенный" используют вместе с группами, такими как арилалкил, которые содержат два или более фрагмента, в которых возможно замещение, заместители могут быть соединены с арильным фрагментом, алкильным фрагментом или с обоими фрагментами. Специалисты в данной области техники понимают, что заместители и другие фрагменты соединений формулы I-III следует выбирать для получения соединения, которое является достаточно стабильным для получения фармацевтически подходящего соединения, которое может входить в достаточно стабильный фармацевтический состав. Соединения формулы I-III, которые обладают указанной стабильностью, входят в рамки настоящего изобретения."Карбоцикл" или "карбоциклил" относится к насыщенному (т.е. циклоалкилу), частично ненасыщенному (например, циклоалкенилу, циклоалкадиенилу) или ароматическому кольцу, содержащему от 3 до 7 атомов углерода в моноцикле, от 7 до 12 атомов углерода в бицикле и до 20 атомов углерода в полицикле. Моноциклические карбоциклы содержат от 3 до 7 атомов в кольце, более конкретно 5 или 6 атомов в кольце. Бициклические карбоциклы содержат от 7 до 12 атомов в кольце, например, распределенных в виде бицикло [4,5], [5,5], [5,6] или [6,6] систему или 9 или 10 атомов в кольце, распределенных в виде бицикло [5,6] или [6,6] системы или спироконденсированных колец. Неограничивающие примеры моноциклических карбоциклов включат циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1 циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил и фенил. Неограничивающие примеры бициклокарбоциклов включают нафтил, тетрагидронафталин и декалин."Карбоциклилалкил" относится к ациклическому алкильному радикалу, в котором один из атомов водорода, связанных с атомом углерода, заменен на карбоциклильный радикал, описанный в настоящей заявке. Типичные, но не ограничивающие, примеры карбоциклилалкильных групп включают циклопропилметил, циклопропилэтил, циклобутилметил, циклопентилметил и циклогексилметил. Термин "возможно замещенный", применительно к конкретному фрагменту соединения формулы IIII (например, возможно замещенная арильная группа) относится к группе, в которой все заместители представляют собой атомы водорода или в которой один или более атом водорода может быть заменен на заместитель, например, перечисленный в определении термина "замещенный". Термин "возможно замещенный на", применительно к конкретному фрагменту соединения формулы I-III (например, атомы углерода в указанном (С 1-С 8)алкиле могут быть возможно заменены на-О-, -Sили -NRa-) означает, что одна или более метиленовых групп в (C1-C8)алкиле могут быть замещены на 0,1, 2 или более указанных групп (например, -О-, -S- или -NRa-). Конкретные альтернативы Y и Y1 представляют собой оксиды азота, такие как +N(O)(R) илиN(O)(OR). Указанные оксиды азота, представленные в настоящем описании, соединенные с атомом углерода, также могут присутствовать в группах с разделенными зарядами, например, соответственно, и являются эквивалентами представленных выше определений, необходимых для описания настоящего изобретения. Если не указано обратное, атомы углерода согласно настоящему изобретению имеют валентность,равную четырем. В некоторых представленных химических структурах, в которых атомы углерода не содержат достаточное для достижения валентности, равной четырем, количество присоединенных переменных, понимают, что оставшиеся заместители углерода, необходимые для достижения валентности,равной четырем, представляют собой атомы водорода. Например,- 17025085 Необходимо отметить, что все энантиомеры, диастереомеры и рацемические смеси, таутомеры, полиморфы, псевдополиморфы соединений формулы I, формулы II или формулы III, и их фармацевтически приемлемых солей, охвачены настоящим изобретением. Все смеси указанных энантиомеров и диастереомеров также находятся в рамках настоящего изобретения. Соединение формулы I-III и его фармацевтически приемлемые соли, могут существовать в виде различных полиморфов или псевдополиморфов. Используемый в настоящем описании, кристаллический полиморфизм означает способность кристаллического соединения существовать в виде различных кристаллических структур. Кристаллический полиморфизм может быть вызван различиями в кристаллической упаковке (упаковочный полиморфизм) или различиями в упаковке различных конформеров одной и той же молекулы (конформационный полиморфизм). Используемый в настоящем описании, кристаллический псевдополиморфизм означает способность гидрата или сольвата соединения существовать в виде различных кристаллических структур. Псевдополиморфы согласно настоящему изобретению могут существовать в результате различий в кристаллической упаковке (упаковочный псевдополиморфизм) или в результате различий в упаковке между различными конформерами одной и той же молекулы (конформационный псевдополиморфизм). Настоящее изобретение охватывает все полиморфы и псевдополиморфы соединений формулы I-III и их фармацевтически приемлемых солей. Соединение формулы I-III и его фармацевтически приемлемые соли также могут существовать в виде аморфного твердого вещества. Используемое в настоящем описании, аморфное твердое вещество представляет собой твердое вещество, в котором отсутствует дальний порядок расположения атомов в твердом веществе. Данное определение применяют в случае, если размер кристалла составляет два нанометра или менее. Добавки, включая растворители, можно применять для получения аморфных форм согласно настоящему изобретению. Настоящее изобретение охватывает все аморфные формы соединений формулы I-III и их фармацевтически приемлемых солей. Рекурсивные заместители Выбранные заместители, входящие в состав соединений согласно настоящему изобретению, представлены в рекурсивной степени. В контексте настоящего описания, "рекурсивный заместитель" означает, что заместитель может описывать другое проявление самого себя. Вследствие рекурсивной природы указанных заместителей, в теории, любой данный вариант реализации может охватывать большое количество соединений. Например, Rx включает заместитель Ry. Ry может представлять собой R. R может представляет собой W3. W3 может представлять собой W4, a W4 может представлять собой R или включать заместители, составляющие Ry. Специалисты в области медицинской химии понимают, что общее количество указанных заместителей обоснованно ограничено требуемыми свойствами конкретного соединения. Указанные свойства включают, в качестве примера, но не ограничения, физические свойства,такие как молекулярная масса, растворимость или log P, свойства, относящиеся к применению, такие как активность против требуемой цели, и практические свойства, такие как простота синтеза. В качестве примера, но не ограничения, W3 и Ry представляют собой рекурсивные заместители в конкретных вариантах реализации. Как правило, каждый рекурсивный заместитель может независимо встречаться 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1 или 0 раз в данном варианте реализации. Чаще всего каждый рекурсивный заместитель может независимо встречаться 10 или менее раз в данном варианте реализации. Еще более часто, W3 встречается от 0 до 8 раз, Ry встречается от 0 до 6 раз в данном варианте реализации. Еще более конкретно, W3 встречается от 0 до 6 раз, a Ry встречается от 0 до 4 раз в данном варианте реализации. Рекурсивные заместители представляют собой необходимый аспект настоящего изобретения. Специалисты в области медицинской химии понимают разнообразие указанных заместителей. Когда рекурсивные заместители присутствуют в варианте реализации, их общее количество определяется, как показано выше. Соединения формулы I-III могут содержать в качестве R7 фосфатную группу, которая может представлять собой пролекарственный фрагментW1 и W2, взятые совместно, представляют собой -Y3(C(Ry)2)3Y3-; или один из W1 или W2 вместе с R3 или R4 представляет собой -Y3-, а другой из W1 или W2 соответствует формуле Ia; или каждый из W1 иW2 независимо представляет собой группу формулы Ia Формула Ia где каждый Y1 представляет собой О; каждый Y2 независимо представляет собой связь, О, NR или S; каждый Y3 представляет собой О; М 2 равен 0, 1 или 2; каждый Rx независимо представляет собой Ry или соответствует формуле где каждый M1a, M1c и М 1d независимо равен 0 или 1; М 12 с равен 0, 1 или 2; каждый Ry независимо представляет собой Н, ОН, R, -C(=Y1)R, -C(=Y1)OR, -SC(=Y1)R, -OR или W3; каждый R независимо представляет собой Н, (C1-С 6)алкил, замещенный (C1-С 6)алкил, (С 2-С 8)алкенил, замещенный (C2-C8)алкенил, (С 2-С 8)алкинил, замещенный (C2-C8)алкинил, (С 6-С 14)арил, замещенный (С 6-С 14)арил;W5 представляет собой пиридинил. Согласно предпочтительному варианту реализации Любые ссылки на соединения согласно настоящему изобретению, описанные в настоящей заявке,также включают ссылки на физиологически приемлемые соли указанных соединений. Примеры физиологически приемлемых солей соединений согласно настоящему изобретению включают соли, полученные из подходящего основания, например, щелочных металлов или щелочноземельных металлов (например, Na+, Li+, K+, Са+2 и Mg+2), аммония и NR4+ (где R определен в настоящем описании). Физиологически приемлемые соли, образованные по атому азота или с аминогруппой включают (а) соли, полученные в результате добавления неорганических кислот, например, хлороводородной кислоты, бромоводородной кислоты, серной кислоты, сульфаминовых кислот, фосфорной кислоты, азотной кислоты и т.д.;(b) соли, полученные из органических кислот, таких как, например, уксусная кислота, оксалиловая кислота, винная кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, глюконовая кислота,лимонная кислота, малевая кислота, аскорбиновая кислота, бензойная кислота, изетионовая кислота, лактобионовая кислота, таниновая кислота, пальмитиновая кислота, альгиновая кислота, полиглутаминовая кислота, нафталинсульфоновая кислота, метансульфоновая кислота, н-толуолсульфоновая кислота, бензолсульфоновая кислота, нафталиндисульфоновая кислота, полигалактуроновая кислота, малоновая кислота, сульфосалициловая кислота, гликолиевая кислота, 2-гидрокси-3-нафтоат, памоат, салициловая кислота, стеариновая кислота, фталевая кислота, миндальная кислота, молочная кислота, этансульфокислота, лизин, аргинин, глутаминовая кислота, глицин, серии, треонин, аланин, изолейцин, лейцин и т.д.; и(с) соли, образованные с элементными анионами, например, с хлором, бромом и йодом. Физиологически приемлемые соли соединений, содержащих гидроксигруппу, включают анион указанного соединения в комбинации с подходящим катионом, таким как Na+ и NR4+. Для терапевтического применения физиологически приемлемыми являются соли активных ингредиентов соединений согласно настоящему изобретению, т.е., соли, полученные из физиологически приемлемой кислоты или основания. Тем не менее, соли кислот и оснований, которые не являются физиологически приемлемыми, также могут находить применение, например, в получении или очистке физиологически приемлемого соединения. Все соли, полученные из физиологически приемлемых или не приемлемых кислот и оснований, включены в рамки настоящего изобретения. Наконец, следует понимать, что композиции согласно настоящему описанию содержат соединения согласно настоящему изобретению в неионизованной, а также цвиттерионной форме, и в комбинации со стехиометрическими количествами воды в виде гидратов. Соединения согласно настоящему изобретению, представленные формулами I-III могут иметь хиральные центры, например, хиральные атомы углерода или фосфора. Соединения согласно настоящему изобретению, таким образом, включают рацемические смеси всех стереоизомеров, включая энантиомеры, диастереомеры и атропоизомеры. Кроме того, соединения согласно настоящему изобретению включают смеси с преимущественным содержанием одного оптического изомера или разделенные изомеры любых или всех асимметрических хиральных атомов. Другими словами, хиральные центры, очевидные из изображений, представлены в качестве хиральных изомеров или рацемических смесей. Рацемические и диастереомерные смеси, а также выделенные или синтезированные индивидуальные оптические изомеры, по существу не содержащие своих энантиомерных или диастереомерных партнеров, включены в рамки настоящего изобретения. Рацемические смеси разделяют на индивидуальные, по существу оптически чистые изомеры при помощи хорошо известных способов, таких как, например, разделение диастереомерных солей, полученных из оптически активных добавок, например, кислот или оснований, с последующим превращением обратно в оптически активные вещества. В большинстве случаев целевой оптический изомер синтезируют с помощью стереоспецифических реакций, применяя в качестве исходного вещества подходящий стереоизомер требуемого исходного вещества. Термин "хиральный" относится к молекулам, которые обладают свойством несовместимости с партнером-зеркальным отражением, при этом термин "ахиральный" относится к молекулам, которые совместимы со своим партнером-зеркальным отражением. Термин "стереоизомеры" относится к соединениям, которые имеют одинаковый химический состав,но отличаются расположением атомов или групп в пространстве."Диастереомер" относится к стереомеру с двумя или более центрами хиральности, молекулы которого не являются зеркальными отражениями друг друга. Диастереомеры обладают различными физическими свойствами, например, температурой плавления, температурой кипения, спектральными свойствами и реакционной способностью. Смеси диастереомеров можно разделять при помощи аналитических способов с высоким разрешением, например, элекрофореза и хроматографии."Энантиомеры" относятся к двум стереоизомерам соединения, которые являются несовместимыми зеркальными отражениями друг друга. Стереохимические определения и условные обозначения, используемые в настоящем описании, как правило, соответствуют S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-HillWileySons, Inc., New York. Многие органические соединения существуют в оптически активных формах, т.е. обладают способностью вращать плоскость плоскополяризованного света. При описании оптически активного соединения приставки D и L или R и S используют для описания абсолютной конфигу- 20025085 рации молекулы относительно ее хирального(ых) центра(ов). Приставки d и l, D и L или (+) и (-) используют для обозначения знака вращения соединением плоскополяризованного света, при этом S, (-) или l означают, что соединение является левовращающим, а соединением с префиксами R, (+) или d является правовращающим. Для данной химической структуры указанные стереоизомеры являются идентичными за исключением того, что они являются зеркальными отражениями друг друга. Конкретный стереоизомер также можно назвать энантиомером, а смесь указанных энантиомеров часто называют энантиомерной смесью. 50:50 смесь энантиомеров называют рацемической смесью или рацематом, указанная смесь может быть получена в результате отсутствия стереоселективности или стереоспецифичности в химической реакции или процессе. Термины "рацемическая смесь" и "рацемат" относятся к эквимолярной смеси двух энантиомерных частиц, лишенной оптической активности. В случае если соединение, описанное в настоящей заявке, замещено более чем одной обозначенной группой, например, "R" или "R1", следует понимать, что группы могут быть одинаковыми или различными, т.е. каждую группу выбирают независимо. Волнистые линии обозначают место присоединения при помощи ковалентной связи с расположенными рядом подструктурами, группами, фрагментами или атомами. Соединения согласно настоящему изобретению в конкретных случаях также могут существовать в виде таутомерных изомеров. Несмотря на то, что может быть отображена только одна делокализованная резонансная структура, все указанные формы включены в рамки настоящего изобретения. Например,енаминовые таутомеры могут существовать в пуриновых, пиримидиновых, имидазольных, гуанидиновых, амидиновых и тетразольных системах, все возможные таутомерные формы включены в рамки настоящего изобретения. Специалисты в данной области техники понимают, что тиено[3,4-d]пиримидинильный и фуро[3,4d]пиримидинильный гетероциклы могут существовать в таутомерных формах. Например, не для ограничения, структуры (а) и (b) могут иметь одинаковые таутомерные формы, представленные далее Все возможные таутомерные формы гетероциклов во всех вариантах реализации, описанных в настоящей заявке, включены в рамки настоящего изобретения. Соединения согласно настоящему изобретению подходят для лечения или профилактики инфекций ВГС у животных или человека. Исследование ингибиторов полимеразы ВГС Композиции согласно настоящему изобретению исследуют в отношении ингибирующей активности против полимеразы ВГС, определяемой при помощи любых традиционных способов оценки ферментной активности. В рамках настоящего изобретения, как правило, композиции сначала исследуют на ингибирование полимеразы ВГС in vitro, а затем композиции, обладающие ингибирующей активностью,затем исследуют на активность in vivo. Композиции, имеющие in vitro Ki (константы ингибирования) менее чем примерно 510-6 М, как правило, менее чем примерно 110-7 М и предпочтительно менее чем примерно 510-8 М, являются предпочтительными для применения in vivo. Подходящие исследования in vitro подробно описаны в и не будут рассмотрены в подробностях в настоящем описании. Тем не менее, в примерах описаны подходящие исследования in vitro. Фармацевтические составы Соединения согласно настоящему изобретению входят в состав с традиционными носителями и наполнителями, которые выбирают согласно общепринятой практике. Таблетки содержат наполнители,глиданты, вещества-наполнители, связывающие вещества и т.д. Водные составы получают в стерильной форме, и если предназначены для доставки путем, отличным от перорального введения, как правило,составы являются изотоническими. Все составы возможно содержат наполнители, например, описанные в "Handbook of Pharmaceutical Excipients" (1986). Наполнители включают аскорбиновую кислоту и другие антиоксиданты, хелатообразующие агенты, такие как ЭДТА, углеводы, такие как декстран, гидроксиалкилцеллюлоза, гидроксиалкилметилцеллюлоза, стеариновая кислота и т.д. рН составов находится в диапазоне примерно от 3 до 11, но, как правило, составляет примерно от 7 до 10. Несмотря на то, что существует возможность введения индивидуальных активных ингредиентов,может быть предпочтительным нахождение указанных ингредиентов в виде фармацевтических составов. Составы, для ветеринарного применения и применения у человека, согласно настоящему изобретению содержат по меньшей мере один активный ингредиент, определенный выше, вместе с одним или более приемлемым носителем и возможно другими терапевтическими ингредиентами. Носитель(и) должен(ны) быть "приемлемым" с точки зрения совместимости с другими ингредиентами состава и физиологически безопасным для пациента. Составы включают составы, подходящие для представленных далее способов введения. Составы могут подходящим образом присутствовать в стандартной дозированной форме и могут быть получены при помощи любых способов, хорошо известных в области фармацевтики. Способы и составы, в целом,представлены в Remington's Pharmaceutical Sciences (Mack Publishing Co., Easton, PA). Указанные способы включают стадию смешения активного ингредиента и носителя, который содержит один или более вспомогательных ингредиентов. В целом, составы получают путем однородного и тщательного смешения активного ингредиента и жидкого носителя или мелкодисперсного твердого носителя или обоих указанных носителей, а затем, при необходимости, формования продукта. Составы согласно настоящему изобретению, подходящие для перорального введения, могут находиться в виде раздельных единиц, таких как капсулы, оболочки или таблетки, каждая из которых содержит заданное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной или неводной жидкости; или в виде жидкой эмульсии типа масло-в-воде или жидкой эмульсии типа вода-в-масле. Активный ингредиент также можно вводить в виде болюса, электуария или пасты. Таблетки получают путем прессования или формования, возможно с одним или более вспомогательным ингредиентом. Прессованные таблетки можно получать путем прессования в подходящем устройстве активного ингредиента в свободно-текучей форме, такой как порошок или гранулы, возможно смешанного со связывающим веществом, смазывающим веществом, инертным разбавителем, консервантом, поверхностно-активным веществом или диспергирующим агентом. Формованные таблетки можно получать путем формования в подходящем устройстве смеси порошкового активного ингредиента, увлажненного инертным жидким разбавителем. Таблетки могут содержать покрытие или насечку и входить в состав для обеспечения замедленного или контролируемого высвобождения активного ингредиента. В случае инфекций глаз или других внешних тканей, например, рта и кожи, составы предпочтительно применяют в виде топической мази или крема, содержащей активный(е) ингредиент(ы) в количестве, равном, например, от 0,075 до 20% (мас./мас.) (включая активный(е) ингредиент(ы) в диапазоне от 0,1% до 20% с шагом границы диапазона, равным 0,1% (мас./мас.), например, 0,6% (мас./мас.), 0,7%(мас./мас.) и т.д.), предпочтительно от 0,2 до 15% (мас./мас.) и наиболее предпочтительно от 0,5 до 10%(мас./мас.). При приготовлении состава в виде мази активные ингредиенты можно применять с парафиновой или смешиваемой с водой основой для мази. В качестве альтернативы активные ингредиенты могут входить в состав крема с кремовой основой типа вода-в-масле. При необходимости водная фаза крема может содержать, например, по меньшей мере 30%(мас./мас.) многоатомного спирта, т.е. спирта, содержащего две или более гидроксильные группы, такие как пропиленгликоль, бутан-1,3-диол, маннит, сорбит, глицерин и полиэтиленгликоль (включая ПЭГ 400) и их смеси. Топические составы могут предпочтительно включать соединение, которое улучшает абсорбцию или проницаемость активного ингредиента через кожу или другие пораженные участки. Примеры указанных ускорителей проникновения через кожу включают диметилсульфоксид и его аналоги. Масляная фаза эмульсий согласно настоящему изобретению может состоять из известных ингредиентов в известном порядке. Несмотря на то, что фаза может содержать исключительно эмульгатор (также известный как эмульгент), данная фаза предпочтительно содержит смесь по меньшей один эмульгатор и жир или масло, или и жир и масло. Предпочтительно гидрофильный эмульгатор содержится вместе с липофильным эмульгатором, выступающим в качестве стабилизатора. Также предпочтительно содержания масла и жира. Вместе, эмульгатор(ы) со стабилизатором(ами) или без него образуют так называемый эмульгиующий воск, а воск вместе с маслом и жиром образуют так называемую эмульгирующую основу мази, которая образуют масляную диспергированную фазу кремовых составов. Эмульгаторы и стабилизаторы эмульсий, подходящие для применения в составах согласно настоящему изобретению, включают Tween 60, Span 80, цетостеариловый спирт, бензиловый спирт, миристиловый спирт, глицерин моностеарат и лаурилсульфат натрия. Выбор подходящих масел или жиров для состава основан на достижении требуемых косметических свойств. Крем, предпочтительно должен быть нежирным, не оставляющим пятен и смываемым продуктом с подходящей консистенцией для предотвращения вытекания из туб или других контейнеров. Можно применять моно- или двухосновные алкильные сложные эфиры с линейной или разветвленной цепью,такие как диизоадипат, изоцетилстеарат, пропиленгликолевый сложный диэфир жирных кокосовых кислот, изопропилмиристат, децилолеат, изопропилпальмитат, бутилстеарат, 2-этилгексилпальмитат или смесь сложных эфиров с разветвленной цепью, известную как Crodamol CAP, причем три последних являются предпочтительными сложными эфирами, которые можно применять индивидуально или в комбинации в зависимости от требуемых свойств. В качестве альтернативы применяют липиды с высокой температурой плавления, такие как белый мягкий парафин и/или жидкий парафин или другие минеральные масла. Фармацевтические составы согласно настоящему изобретению содержат комбинацию согласно настоящему изобретению вместе с одним или более фармацевтически приемлемыми носителями или наполнителями и возможно другими терапевтическими агентами. Фармацевтические составы, содержащие активный ингредиент, могут находиться в любой форме, подходящей для назначенного способа введения. При применении для перорального введения можно получать, например, таблетки, формованные пастилки, пастилки, водные или масляные суспензии, диспергируемые порошки или гранулы, эмульсии,твердые или мягкие капсулы, сиропы или эликсиры. Композиции, предназначенные для перорального применения можно получать согласно любым способам, известным в данной области техники для производства фармацевтических композиций, и указанные композиции могут содержать один или более агентов, включая подсластители, ароматизаторы, красители и консерванты, для обеспечения привлекательного для потребителя препарата. Приемлемы таблетки, содержащие активный ингредиент в смеси с нетоксичным фармацевтически приемлемым наполнителем, который подходит для производства таблеток. Указанные наполнители могут представлять собой, например, инертные разбавители, такие как карбонаты натрия или кальция, лактоза, фосфаты натрия или кальция; гранулирующие или улучшающие распадаемость агенты, такие как кукурузный крахмал или альгиновая кислота; связывающие агенты, такие как крахмал, желатин или камедь; и смазки, такие как стеарат магния, стеариновая кислота или тальк. Таблетки могут быть без покрытия или с покрытием, нанесенным при помощи известных способов, включая микроинкапсулирование, для задержки разложения и поглощения в желудочно-кишечном тракте и обеспечения, таким образом, замедленного действия в течение длительного периода. Например, можно применять вещество с замедленным высвобождением, такое как глицерилмоностеарат, индивидуально или с воском. Составы для перорального применения также могут существовать в виде твердых желатиновых капсул, в которых активный ингредиент смешан с инертным твердым разбавителем, например, фосфатом кальция или каолином, или мягких желатиновых капсул, в которых активный ингредиент смешан с водной или масляной средой, такой как ореховое масло, жидкий парафин или оливковое масло. Водные суспензии согласно настоящему изобретению содержат активные вещества в смеси с наполнителями, подходящими для производства водных суспензий. Указанные наполнители включают суспендирующий агент, такой как карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксипропилметилцеллюлоза, алгинат натрия, поливинилпирролидон, трагакантовая камедь и аравийская камедь, и диспергирующий или увлажняющий агент, такой как природный фосфатид (например, лецитин), продукт конденсации алкиленоксида и жирной кислоты (например, полиоксиэтиленстеарат), продукт конденсации этиленоксида и длинноцепочечного алифатического спирта (например, гептадекаэтиленоксицетанол), продукт конденсации этиленоксида и неполного сложного эфира, полученного из жирной кислоты и ангидрида гексита (например, полиоксиэтиленсорбитана моноолеат). Водная суспензия также может содержать один или более консервант, такой как этил- или н-пропил-п-гидроксибензоат, один или более краситель, один или более ароматизатор и один или более подсластителей, таких как сахароза или сахарин. Масляные суспензии могут быть получены в результате суспендирования активного ингредиента в растительном масле, таком как арахисовое масло, оливковое масло, кунжутное масло или кокосовое масло, или в минеральном масле, таком как жидкий парафин. Пероральные суспензии могут содержать загуститель, такой как пчелиный воск, твердый парафин или цетиловый спирт. Для получения привлекательных для потребителя пероральных препаратов можно добавлять подсластители, например, представленные выше, и ароматизаторы. Указанные композиции можно консервировать путем добавления антиоксиданта, такого как аскорбиновая кислота. Диспергируемые порошки и гранулы согласно настоящему изобретению, подходящие для получения водной суспензии путем добавления воды, содержат активный ингредиент в смеси с диспергирующим или увлажняющим агентом и одним или более консервантом. Подходящие диспергирующие или увлажняющие агенты и суспендирующие агенты представлены агентами, описанными выше. Также могут содержаться дополнительные наполнители, например, подсластители, ароматизаторы и красители. Фармацевтические композиции согласно настоящему изобретению также могут находиться в виде эмульсий типа масло-в-воде. Масляная фаза может представлять собой растительное масло, такое как оливковое масло или арахисовое масло, минеральное масло, такое как жидкий парафин, или их смесь. Подходящие эмульгаторы включают природную камедь, такую как аравийская камедь и трагакантовая камедь, природные фосфатиды, такие как соевый лецитин, сложные эфиры или неполные сложные эфиры, полученные из жирных кислот и ангидридов гексита, такие как сорбитана моноолеат, и продукты конденсации указанных неполных эфиров и этиленоксида, такие как полиоксиэтиленсорбитана моноолеат. Эмульсия также может содержать подсластители и ароматизаторы. Сиропы и эликсиры можно получать с подсластителями, такими как глицерин, сорбит или сахароза. Указанные составы также могут содержать успокоительное средство (demulcent), консервант, ароматизатор или краситель. Фармацевтические композиции согласно настоящему изобретению могут находиться в виде стерильного инъецируемого препарата, такого как стерильная инъецируемая водная или масляная суспензия. Указанная суспензия может быть получена согласно уровню техники с применением диспергирующих или увлажняющих агентов и суспендирующих агентов, указанных выше. Стерильный инъецируемый препарат также может представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3 бутандиоле или лиофилизированного порошка. В число приемлемых носителей и растворителей, которые можно применять, входят вода, раствор Рингера и изотонический раствор хлорида натрия. В дополнение, в качестве растворителя или суспендирующей среды можно применять стерильные нелетучие масла. Для указанных целей также можно применять любые нераздражающие нелетучие масла, включая синтетические моно- или диглицериды. В дополнение для получения инъецируемых препаратов также можно применять жирные кислоты, такие как олеиновая кислота. Количество активного ингредиента, которое можно смешивать с носителем с получением дозированной формы для однократного введения зависит от подвергаемого лечению субъекта и конкретного пути введения. Например, состав с длительным высвобождением, предназначенный для перорального введения людям, может содержать примерно от 1 до 1000 мг активного вещества, смешанного с подходящим и соответствующим количеством носителя, которое может изменяться примерно от 5 до 95% композиции (масса:масса). Фармацевтический состав можно получать для обеспечения легко измеряемых количеств, необходимых для введения. Например, водный раствор, предназначенный для внутривенной инфузии, может содержать примерно от 3 до 500 мкг активного ингредиента на миллилитр раствора, чтобы могла проходить инфузия подходящего объема со скоростью, равной примерно 30 мл/ч. Составы, подходящие для топического введения в глаза, также включают глазные капли, в которых активный ингредиент растворен или суспендирован в подходящем носителе, конкретно в водном растворителе активного ингредиента. Активный ингредиент предпочтительно содержится в указанных составах в концентрации, равной от 0,5 до 20%, преимущественно от 0,5 до 10%, в частности, примерно 1,5%(мас./мас.). Составы, подходящие для топического введения в рот, включают пастилки, содержащие активный ингредиент в ароматизированной основе, как правило, сахарозе и камеди или трагакантовой камеди; пастилы, содержащие активный ингредиент в инертной основе, такой как желатин и глицерин, или сахароза и камедь; и растворы для полоскания рта, содержащие активный ингредиент в подходящем жидком носителе. Составы для ректального введения могут существовать в виде суппозиториев в подходящей основе,содержащих, например, масло какао или салицилат. Составы, подходящие для внутрилегочного или назального введения, имеют размер частиц, например, в диапазоне от 0,1 до 500 микрон, например, 0,5, 1, 30, 35 и т.д., которые вводят путем быстрой ингаляции через носовой канал или путем ингаляции через рот для обеспечения доставки в альвеолярные мешочки. Подходящие составы включают водные или масляные растворы активного ингредиента. Составы, подходящие для введения в виде аэрозоля или сухого порошка, можно получить согласно традиционным способам и доставить с другими терапевтическими агентами, такими как соединения, которые в настоящее время применяют для лечения или профилактики инфекций ВГС, описанных далее. Составы, подходящие для вагинального введения, могут существовать в виде пессариев, тампонов,кремов, гелей, паст, пен или спреев, содержащих, в дополнение к активному ингредиенту, подходящие носители, известные в данной области техники. Составы, подходящие для парентерального введения, включают водные или неводные стерильные инъецируемые растворы, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые превращают раствор в изотонический с кровью пациента; и водные и неводные стерильные суспензии, которые могут содержать суспендирующие агенты и загустители. Составы находятся в контейнерах с единичной дозой или контейнерах, содержащих несколько доз,например, в герметичных ампулах и пробирках, и могут храниться в полученном в результате сублимационной сушки (лиофилизированном) состоянии, которое требует только добавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед применением. Приготовленные для немедленного применения инъецируемые растворы и суспензии получают из стерильных порошков, гранул и таблеток, описанных ранее. Предпочтительные стандартные дозированные составы представляют собой составы, содержащие дневную дозу или единичную дневную часть дозы активного ингредиента,- 24025085 как показано ранее в настоящем описании, или подходящую часть указанной дозы. Следует понимать, что в дополнение к ингредиентам, конкретно представленным выше, составы согласно настоящему изобретению могут содержать другие агенты, общепринятые в данной области техники, имеющие отношение к данному типу состава, например, составы, подходящие для перорального введения могут содержать ароматизаторы. В изобретении дополнительно предложены ветеринарные композиции, содержащие по меньшей мере один активный ингредиент, определенный выше, вместе с применяемым в ветеринарии носителем для активного ингредиента. Применяемые в ветеринарии носители представляют собой вещества, подходящие для введения композиции, и могут представлять собой твердые, жидкие или газообразные вещества, которые являются инертными или приемлемыми в области ветеринарии и являются совместимыми с активным ингредиентом. Указанные композиции для применения в ветеринарии можно вводить перорально, парентерально или при помощи любых требуемых способов. Соединения согласно настоящему изобретению применяют для получения фармацевтических составов с контролируемым высвобождением, содержащих в качестве активного ингредиента одно или более соединений согласно настоящему изобретению (составы с контролируемым высвобождением), в которых высвобождение активного ингредиента контролируется и регулируется для достижения меньшей частоты дозирования или для улучшения фармакокинетических или токсичных свойств данного активного ингредиента. Эффективная доза активного ингредиента зависит по меньшей мере от природы состояния, требующего лечения, токсичности, профилактического применения соединения (требует меньших доз) или применения против активной вирусной инфекции, способа доставки и фармацевтического состава, и определяется лечащим врачом с применением традиционных исследований с увеличением дозы. Эффективная доза, как можно предположить, составляет примерно от 0,0001 до 100 мг/кг массы тела в день; как правило, примерно от 0,01 до 10 мг/кг массы тела в день; более конкретно, примерно от 0,01 до 5 мг/кг массы тела в день; наиболее конкретно, примерно от 0,05 до 0,5 мг/кг массы тела в день. Например,возможная дневная доза для взрослого человека с массой тела, равной примерно 70 кг, находится в диапазоне от 1 до 1000 мг, предпочтительно от 5 до 500 мг и может приниматься в виде единственной или нескольких доз. Способы введения Одно или более соединений согласно настоящему изобретению (далее - активный ингредиент) вводят любыми способами, подходящими для состояния, требующего лечения. Подходящие способы включают пероральный, ректальный, назальный, топический (включая трансбуккальный и подъязычный),вагинальный и парентеральный (включая подкожный, внутримышечный, внутривенный, внутрикожный,интратекальный и эпидуральный) и т.д. Следует понимать, что предпочтительный способ может изменяться, например, в зависимости от состояния пациента. Преимуществом соединений согласно настоящему изобретению является то, что указанные соединения являются перорально биодоступными и могут быть дозированы перорально. Комбинированная терапия Композиции согласно настоящему изобретению также применяют в комбинации с другими активными ингредиентами. Предпочтительно, другие активные ингредиенты или агенты представляют собой интерфероны, рибавирин или его аналоги, ингибиторы NS3 протеазы ВГС, ингибиторы альфа-глюкозидазы 1, гепатопротекторы, нуклеозидные или нуклеотидные ингибиторы NS5B полимеразы ВГС, ненуклеозидные ингибиторы NS5B полимеразы ВГС, ингибиторы NS5A ВГС, агонисты TLR-7, ингибиторы циклофилина, ингибиторы IRES ВГС, усилители фармакокинетики и другие лекарственные средства для лечения ВГС или их смеси. Комбинации соединений формулы I-III, как правило, выбирают с учетом состояния, требующего лечения, перекрестной реакционной способности и фармакологических свойств комбинации. Например, при лечении инфекции (например, ВГС) композиции согласно настоящему изобретению объединяют с другими активными терапевтическими агентами (например, описанными в настоящей заявке). Подходящие активные терапевтические агенты или ингредиенты, которые можно объединять с соединениями формулы I-III, могут включать интерфероны, например, пегилированный рИФН-альфа 2b,пегилированный рИФН-альфа 2 а, рИФН-альфа 2b, ИФН альфа-2b XL, рИФН-альфа 2 а, консенсус ИФН альфа, инферген, ребиф, локтерон, AVI-005, ПЭГ-инферген, пегилированный ИФН-бета, пероральный интерферон альфа, ферон, реаферон, интермакс альфа, р-ИФН-бета, инферген + актиммун, ИФН-омега и производные бензо-1,2,4-тиадиазина и производные фенилаланина; и другие лекарственные средства для лечения ВГС, например, задаксин, нитазоксанид (alinea), BIVN-401 (виростат), DEBIO-025, VGX-410C,EMZ-702, AVI 4065, бавитуксимаб, оглуфанид, PYN-17, KPE02003002, актилон (CPG-10101), KRN-7000,цивацир, GI-5005, ANA-975, XTL-6865, ANA 971, NOV-205, тарвацин, ЕНС-18 и NIM811. Согласно другому варианту реализации в настоящей заявке описаны фармацевтические композиции, содержащие соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, и/или сложный эфир, в комбинации по меньшей мере с одним дополнительным терапевтическим агентом и фармацевтически приемлемым носителем или наполнителем. Согласно настоящему изобретению терапевтический агент, применяемый в комбинации с соединением согласно настоящему изобретению, может представлять собой любой агент, обладающий терапевтическим действием в случае применения в комбинации с соединением согласно настоящему изобретению. Например, терапевтический агент, применяемый в комбинации с соединением согласно настоящему изобретению, может представлять собой интерфероны, рибавирин или его аналоги, ингибиторы NS3 протеазы ВГС, ингибиторы альфа-глюкозидазы 1, гепатопротекторы, нуклеозидные или нуклеотидные ингибиторы NS5B полимеразы ВГС, ненуклеозидные ингибиторы NS5B полимеразы ВГС, ингибиторыNS5A ВГС, агонисты TLR-7, ингибиторы циклофилина, ингибиторы IRES ВГС, усилители фармакокинетики и другие лекарственные средства для лечения ВГС или их смеси. Согласно другому варианту реализации в настоящей заявке предложены фармацевтические композиции, содержащие соединение согласно настоящему изобретению или его фармацевтически приемлемую соль, сольват и/или сложный эфир, в комбинации с по меньшей мере одним дополнительным терапевтическим агентом, выбранным из группы, состоящей из пегилированного рИФН-альфа 2b, пегилированного рИФН-альфа 2 а, рИФН-альфа 2b, ИФН альфа-2b XL, рИФН-альфа 2 а, консенсус ИФН альфа,инфергена, ребифа, локтерона, AVI-005, ПЭГ-инфергена, пегилированного ИФН-бета, перорального интерферона альфа, ферона, реаферона, интермакса альфа, р-ИФН-бета, инфергена + актиммуна, ИФНомега с DUROS, альбуферона, ребетола, копегуса, VX-497, вирамидина (тарибавирина), А-831, А-689,NM-283, валопицитабина, R1626, PSI-6130 (R1656), PSI-7851, PSI-7977, HCV-796, BILB 1941, МК-0608,NM-107, R7128, VCH-759, PF-868554, GSK625433, XTL-2125, SCH-503034 (SCH-7), VX-950 (Telaprevir),ITMN-191 и BILN-2065, MX-3253 (целгосивира), UT-231B, IDN-6556, ME 3738, MitoQ и LB-84451, производных бензимидазола, производных бензо-1,2,4-тиадиазина и производных фенилаланина, задаксина,нитазоксанида (alinea), BIVN-401 (виростата), DEBIO-025, VGX-410C, EMZ-702, AVI 4065, бавитуксимаба, оглуфанида, PYN-17, КРЕ 02003002, актилона (CPG-10101), KRN-7000, цивацира, GI-5005, ANA975, XTL-6865, ANA 971, NOV-205, тарвацина, ЕНС-18 и NIM811 и фармацевтически приемлемым носителем или наполнителем. Комбинации соединений формулы I-III и дополнительных терапевтических агентов можно выбирать для лечения пациентов, инфицированных ВГС, и для пациентов с другими состояниями, такими как ВИЧ. Соответственно, соединения формулы I-III можно объединять с одним или более соединением,подходящим для лечения ВИЧ, например, с соединениями, ингибирующими протеазу ВИЧ, ненуклеозидными ингибиторами обратной транскриптазы ВИЧ, нуклеозидными ингибиторами обратной транскриптазы ВИЧ, нуклеотидными ингибиторами обратной транскриптазы ВИЧ, ингибиторами интегразы ВИЧ, ингибиторами gp41, ингибиторами CXCR4, ингибиторами gp120, ингибиторами CCR5, интерферонами, аналогами рибавирина, ингибиторами NS3 протеазы, ингибиторами NS5a, ингибиторами альфаглюкозидазы 1, гепатопротекторами, ненуклеозидными ингибиторами ВГС и другими лекарственными средствами для лечения ВГС. Более конкретно, одно или более соединений согласно настоящему изобретению, можно объединять с одним или более соединениями, выбранными из группы, состоящей из 1) ингибиторов протеазы ВИЧ, например, ампренавира, атазанавира, фосампренавира, индинавира, лопинавира, ритонавира, лопинавира + ритонавир, нелфавира, саквинавира, типранавира, бреканавина, дарунавира, ТМС-126, ТМС 114, мозенавира (DMP-450), JE-2147 (AG1776), AG1859, DG35, L-756423, RO0334649, KNI-272, DPC681, DPC-684 и GW640385X, DG17, PPL-100, 2) ненуклеозидных ингибиторов обратной транскриптазы ВИЧ, например, каправирина, эмивирина, делавиридина, эфавиренца, невирапина, (+) каланолида А,этравирина, GW5634, DPC-083, DPC-961, DPC-963, MIV-150 и ТМС-120, ТМС-278 (рилпивирина), эфавиренца, BILR 355 BS, VRX 840773, UK-453,061, RDEA806, 3) нуклеозидных ингибиторов обратной транскриптазы ВИЧ, например, зидовудина, эмтрицитабина, диданозина, ставудина, залцитабина, ламивудина, абакавира, амдоксовира, элвуцитабина, аловудина, MIV-210, рацивира (-FTC), D-d4FC, эмтрицитабина, фосфазида, фозивудина тидоксила, фосалвудина тидоксила, априцитибина (AVX754), амдоксовира, KP-1461, абакавира + ламивудин, абакавира + ламивудин + зидовудин, зидовудина + ламивудин,4) нуклеотидных ингибиторов обратной транскриптазы ВИЧ, например, тенофовира, тенофовира дизопроксилфумарата + эмтрицитабин, тенофовира дизопроксил фумарата + эмтрицитабин + эфавиренц и адефовира, 5) ингибиторов интегразы ВИЧ, например, куркумина, производных куркумина, цикориевой кислоты, производных цикориевой кислоты, 3,5-дикофеилхиновой кислоты, ауринтрикарбоновой кислоты, производных ауринтрикарбоновой кислоты, фенэтилового эфира кофейной кислоты, производных фенэтилового эфира кофейной кислоты, тирфостина, производных тирфостина, кверцетина, производ- 26025085NS5b полимеразы, например, NM-283, валопицитабина, R1626, PSI-6130 (R1656), PSI-7851, PSI-7977,HCV-796, BILB 1941, MK-0608, NM-107, R7128, VCH-759, PF-868554, GSK625433 и XTL-2125, 15) ингибиторов NS3 протеазы, например, SCH-503034 (SCH-7), VX-950 (Telaprevir), ITMN-191 и BILN-2065, 16) ингибиторов альфа-глюкозидазы 1, например, МХ-3253 (целгосивир) и UT-231B, 17) гепатопротекторов,например, IDN-6556, ME 3738, MitoQ и LB-84451, 18) ненуклеозидных ингибиторов ВГС, например,производных бензимидазола, производных бензо-1,2,4-тиадиазина и производных фенилаланина, 19) других лекарственных средств для лечения ВГС, например, задаксина, нитазоксанида, (alinea), BIVN-401(виростата), DEBIO-025, VGX-410C, EMZ-702, AVI 4065, бавитуксимаба, оглуфанида, PYN-17,KPE02003002, актилона (CPG-10101), KRN-7000, цивацира, GI-5005, ANA-975, XTL-6865, ANA 971,NOV-205, тарвацина, ЕНС-18 и NIM811, 20) усилителей фармакокинетики, например, BAS-100 и SPI452,21) ингибиторов РНКазы Н, например, ODN-93 и ODN-112, 21) других анти-ВИЧ средств, например,VGV-1, РА-457 (бевиримата), амплигена, HRG214, цитолина, полимуна, VGX-410, KD247, AMZ 0026,CYT 99007, А-221 HIV, BAY 50-4798, MDX010 (иплимумаба), PBS119, ALG889 и РА-1050040. Также возможно объединять любые соединения согласно настоящему изобретению с одним или более другим активным терапевтическим агентом в стандартной дозированной форме для одновременного или последовательного введения пациенту. Комбинированную терапию можно проводить в одновременном или последовательном режиме. При последовательном введении комбинацию можно вводить за два или более введения. Совместное введение соединения согласно настоящему изобретению и одного или более другого терапевтического агента, как правило, относится к одновременному или последовательному введению соединения согласно настоящему изобретению и одного или более другого терапевтического агента, таким образом, что в организме пациента присутствуют терапевтически эффективные количества соединения согласно настоящему изобретению и одного или более других активных терапевтических агентов. Совместное введение включает введение единичных дозировок соединений согласно настоящему изобретению до или после введения единичных дозировок одного или более других активных терапевтических агентов, например, введение соединений согласно настоящему изобретению проводят в секундном, минутном или часовом интервале относительно введения одного или более других активных терапевтических агентов. Например, единичную дозу соединения согласно настоящему изобретению можно вводить первой, а затем через секундный или минутный интервал можно вводить единичную дозу одного или более других активных терапевтических агентов. В качестве альтернативы, единичную дозу одного или более других активных терапевтических агентов можно вводить первой, а затем вводить единичную дозу соединения согласно настоящему изобретению через секундный или минутный интервал. В некоторых случаях может быть необходимо первой вводить стандартную дозу соединения согласно настоящему изобретению, а затем через часовой интервал (например, через 1-12 ч) вводить единичную дозу одного или более других активных терапевтических агентов. В других случаях может быть необходимо первой вводить стандартную дозу одного или более других активных терапевтических агентов, а затем через часовой интервал (например, через 1-12 ч) вводить единичную дозу соединения согласно настоящему изобретению. Комбинированная терапия может обеспечивать "синергизм" и "синергический" эффект, т.е. эффект,достигаемый в случае, если действие от применяемых вместе активных ингредиентов выше относительно суммы действий, которые оказывают соединения по отдельности. Синергический эффект может быть достигнут, когда активные ингредиенты: (1) входят в один состав и вводятся или доставляются одновременно в объединенном составе; (2) доставляются по очереди или параллельно в раздельных составах; или (3) некоторыми другими способами. В случае доставки при помощи последовательной терапии синергический эффект может быть достигнут, когда соединения вводят или доставляются последовательно,например, в виде отдельных таблеток, пилюль или капсул, или различных инъекций различными шприцами. В целом, в течение последовательной терапии эффективные дозировки каждого из активных ингредиентов вводят последовательно, т.е. сериями, тогда как в комбинированной терапии эффективные дозировки двух или более активных ингредиентов вводят вместе. Синергическое противовирусное действие означает противовирусное действие, которое превышает предполагаемое суммарное действие ин- 27025085 дивидуальных соединений в комбинации. Согласно другому варианту реализации в настоящей заявке предложены способы лечения ВГС у пациента, включающие: введение пациенту терапевтически эффективного количества соединения формулы I-III или его фармацевтически приемлемой соли, сольвата и/или сложного эфира. Согласно другому варианту реализации в настоящей заявке предложены способы лечения ВГС у пациента, включающие: введение пациенту терапевтически эффективного количества соединения формулы I-III или его фармацевтически приемлемой соли, сольвата и/или сложного эфира и по меньшей мере одного дополнительного активного терапевтического агента, в результате которого происходит ингибирование полимеразы ВГС. Согласно другому варианту реализации в настоящей заявке предложены способы лечения ВГС у пациента, включающие: введение пациенту терапевтически эффективного количества соединения формулы I-III или его фармацевтически приемлемой соли, сольвата и/или сложного эфира и по меньшей мере одного дополнительного активного терапевтического агента, выбранного из группы, состоящей из интерферонов, рибавирина или его аналогов, ингибиторов NS3 протеазы ВГС, ингибиторов альфаглюкозидазы 1, гепатопротекторов, нуклеозидных или нуклеотидных ингибиторов NS5B полимеразы ВГС, ненуклеозидных ингибиторов NS5B полимеразы ВГС, ингибиторов NS5A ВГС, агонистов TLR-7,ингибиторов циклофилина, ингибиторов IRES ВГС, усилителей фармакокинетики и других лекарственных средств для лечения ВГС или их смесей. Примеры При подробном описании экспериментов использованы некоторые аббревиатуры и сокращения. Несмотря на то, что многие из них очевидны специалистам в данной области техники, в табл. 1 представлен перечень многих указанных аббревиатур и сокращений. Таблица 1. Список аббревиатур и акронимов Получение соединений Соединение 1 К раствору соединения 1 а (22,0 г, 54,9 ммоль, получено согласно способу, описанному в J.O.C.,2004, 6257) в метаноле (300 мл) по каплям при 0 С с применением капельной воронки в течение 30 мин добавляли ацетилхлорид (22 мл), затем перемешивали при комнатной температуре в течение 16 ч. Смесь концентрировали, перерастворяли в этилацетате (400 мл), промывали ледяным 2 Н раствором NaOH и концентрировали насухо с получением неочищенного сложного метилового эфира 1b в виде маслянистой жидкости. МС = 437,2 (M+Na+). К раствору соединения 1b (полученного на предыдущей стадии) в метаноле (300 мл) добавляли 0,5 М раствор метоксида натрия в метаноле (20 мл, 10 ммоль) и перемешивали в течение 16 ч при комнатной температуре. Реакцию гасили 4,0 Н раствором HCl в диоксане (2,5 мл, 10 ммоль). Затем смесь концентрировали с получением неочищенного соединения 1 с. МС = 201,0 (M+Na+).KOH (в воде, 85 г) в толуоле (500 мл) кипятили с обратным холодильником с применением ловушки Дина-Старка. Через 1 ч собиралось 25 мл воды, и добавляли бензилхлорид (33 г, 260 ммоль) и продолжали кипячение при перемешивании в течение 16 ч. Затем смесь охлаждали и разделяли в этилацетате (400 мл) и воде (300 мл). Органический слой промывали водой (300 мл) и концентрировали. Остаток очищали посредством колоночной хроматографии на силикагеле (20% EtOAc/гексан) с получением простого метилового эфира 1d в виде маслянистой жидкости (22,0 г, выход 89% за три стадии). 1H ЯМР (300 МГц,CDCl3):7,3 (m, 15H), 4,5-4,9 (m, 7 Н), 4,37 (m, 1H), 3,87 (d, 1H), 3,56 (m, 2H), 3,52 (s, 3 Н), 1,40 (s, 3 Н). К раствору соединения 1d (22,0 г, 49,0 ммоль) в уксусной кислоте (110 мл) добавляли 3 М раствор серной кислоты (получен в результате смешения 4,8 г концентрированной серной кислоты и 24 мл воды) и перемешивали при 70 С в течение 8 ч. Смесь концентрировали до объема 20 мл и разделяли в этилацетате и ледяном 2 Н растворе NaOH. Слой в этилацетате концентрировали и очищали посредством колоночной хроматографии на силикагеле (35% EtOAc/гексан) с получением соединения 1 е в виде маслянистой жидкости (17,0 г, 80%). МС = 457,2 (М + Na+).
МПК / Метки
МПК: A61P 31/14, A61K 31/7064, C07H 19/24
Метки: аналоги, противовирусного, лечения, карбануклеозидные
Код ссылки
<a href="https://eas.patents.su/30-25085-karbanukleozidnye-analogi-dlya-protivovirusnogo-lecheniya.html" rel="bookmark" title="База патентов Евразийского Союза">Карбануклеозидные аналоги для противовирусного лечения</a>
Предыдущий патент: Многоуровневая автомобильная парковка с вертикальным развитием
Следующий патент: Производные индоламида и родственные соединения для использования при лечении нейродегенеративных заболеваний
Случайный патент: Способ лечения ревматоидного артрита