Производные хиназолиндиона, их получение и их различные терапевтические применения
Номер патента: 21765
Опубликовано: 31.08.2015
Авторы: Марсиньяк Жильбер, Гласс Кристоф, Клосс Анни, Виве Бертран, Нав Жан-Франсуа
Формула / Реферат
1. Соединение следующей общей формулы (I):
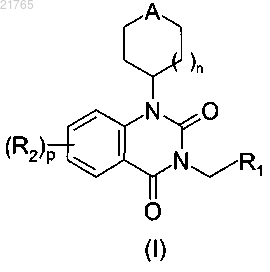
в которой А обозначает либо атом кислорода или серы, либо сульфоксидную группу (группа SO) или сульфоновую группу (группа SO2);
n имеет значение 1;
p имеет значение 1 или 2;
R2 обозначает нитро, амино, гидрокси, Br, F, I, -OCH2CN, пропаннитрил (изомер 1, изомер 2), пиридин-4-ил, -OCH2CCH, -OC(CH3)2CN, 2-гидроксиэтокси, циклопропилметокси, карбонитрил, 2-метилпропанамид, -OCH(CH3)CCH, 3-гидроксиазетидин-1-ил, NHCH2CCH, -CH2NHCCOCH3, -CH2NHCCONH2, -NHCH(CH3)CCH, -OCH2C2H5, -OCH2C(CH3)2, -OC(CH3)2, 1-гидроксиэтил, ацетил, 2,3-дигидроксипропокси, 2-гидроксипропокси, 1-гидрокси-1-метилэтил, этенил, гидроксиметил, 1-гидрокси-1-метилбут-3-ин-1-ил, 2-гидроксиэтил, (1R,1S)-2-гидрокси-1-метилэтокси, 2-фторэтокси, 2,2,2-трифторэтокси, 2,2-дифторэтокси, 3,3,3-трифторпропокси, [(1R),(1S)-1-метилпропокси]окси, 2-фтор-1-(фторметил)этокси, 2,2-дифторэтенил, (1S)-2-фтор-1-метилэтокси, бензилокси;
R1 обозначает 3,4-диметоксибензил, 6-метоксипиридин-3-ил, 4-(бензилокси)-3-метоксибензил, 4-[(3,4-дихлорбензил)окси]-3-метоксибензил, 4-гидрокси-3-метоксибензил;
в форме основания или кислотно-аддитивной соли.
2. Соединение по п.1, отличающееся тем, что когда p равно 2, тогда возможными комбинациями являются либо (i) два атома R2, одинаковых или разных, либо (ii) один атом R2 и одна группа R2, либо (iii) две группы R2, одинаковые или разные; в форме основания или кислотно-аддитивной соли.
3. Соединение по любому из пп.1, 2, отличающееся тем, что R2 означает атом или группу, выбираемую из Br, F, I, нитро, гидрокси, -OCH2CN, пропаннитрила (изомер 1, изомер 2), пиридин-4-ила, -OCH2CCH, -OC(CH3)2CN, 2-гидроксиэтокси, циклопропилметокси, карбонитрила, 2-метилпропанамида, -OCH(CH3)CCH, 3-гидроксиазетидин-1-ила, NHCH2CCH, -CH2NHCCOCH3, -CH2NHCCONH2, -NHCH(CH3)CCH, -OCH2C2H5, -OCH2C(CH3)2, -OC(CH3)2, 1-гидроксиэтила, ацетила, 2,3-дигидроксипропокси, 2-гидроксипропокси, 1-гидрокси-1-метилэтила, этенила, гидроксиметила, 1-гидрокси-1-метилбут-3-ин-1-ила, 2-гидроксиэтила, (1R,1S)-2-гидрокси-1-метилэтокси, 2-фторэтокси, 2,2,2-трифторэтокси, 2,2-дифторэтокси, 3,3,3-трифторпропокси, [(1R),(1S)-1-метилпропокси]окси, 2-фтор-1-(фторметил)этокси, 2,2-дифторэтенила, (1S)-2-фтор-1-метилэтокси, бензилокси; в форме основания или кислотно-аддитивной соли.
4. Соединение по любому из пп.1-3, отличающееся тем, что p равно 2 и две группы и/или два атома R2 выбирают из Br, F, I, гидрокси, -OCH2C2H5, -OCH2C(CH3)2, -OC(CH3)2; в форме основания или кислотно-аддитивной соли.
5. Соединение по любому из пп.1-4, отличающееся тем, что p равно 2 и две группы и/или атома R2 выбирают из атома фтора и гидрокси, -OCH2C2H5, -OCH2C(CH3)2, -OC(CH3)2; в форме основания или кислотно-аддитивной соли.
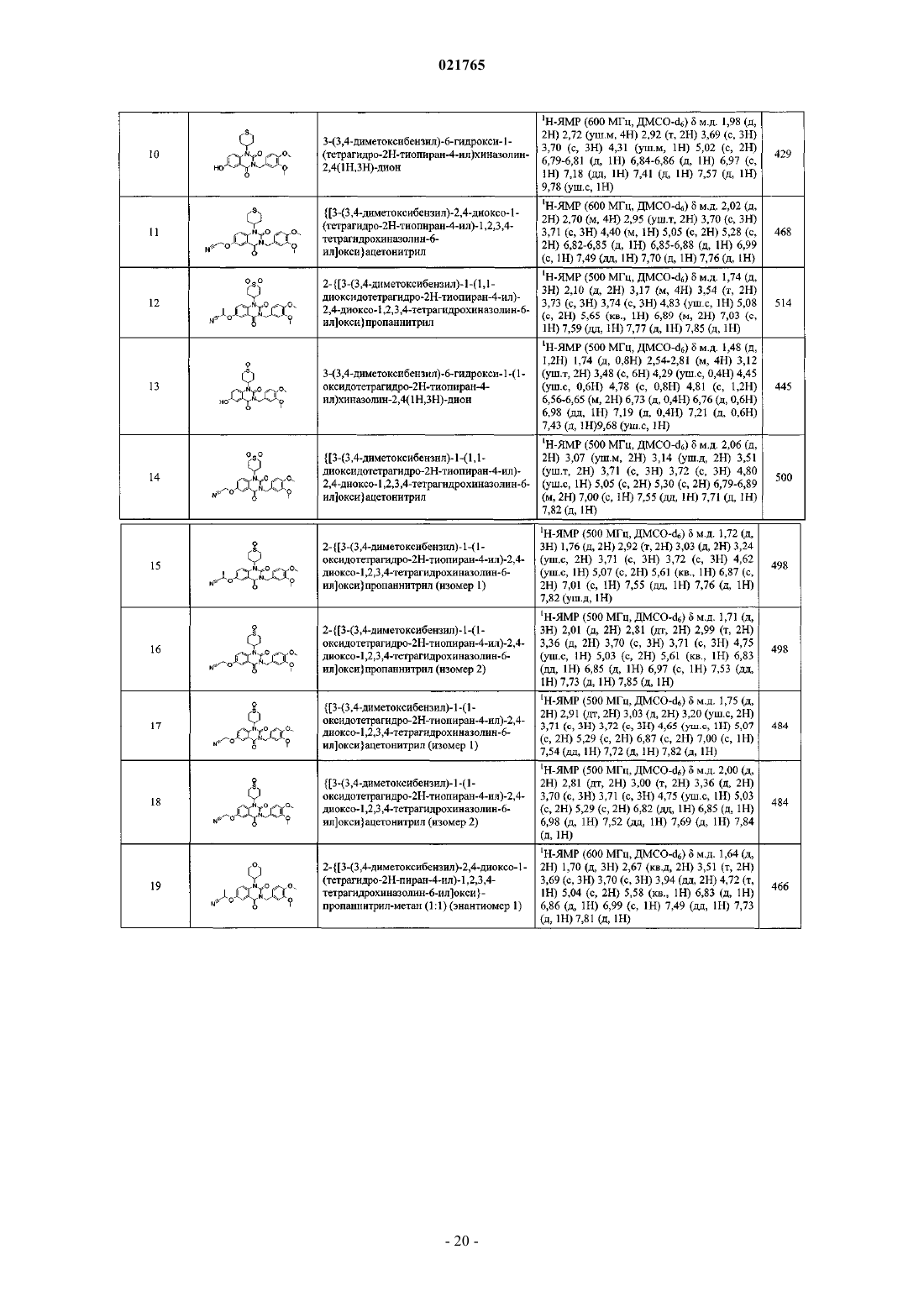
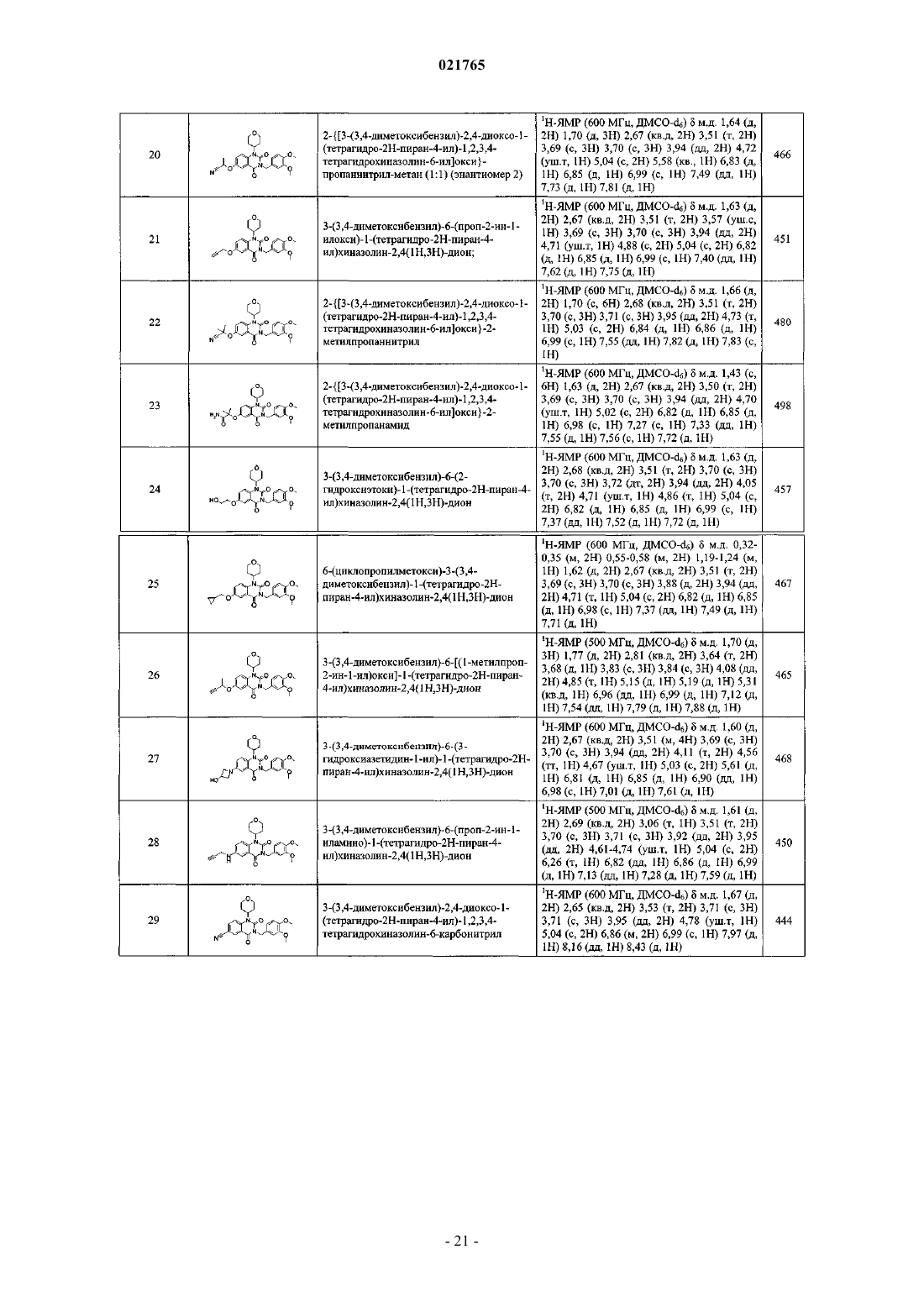
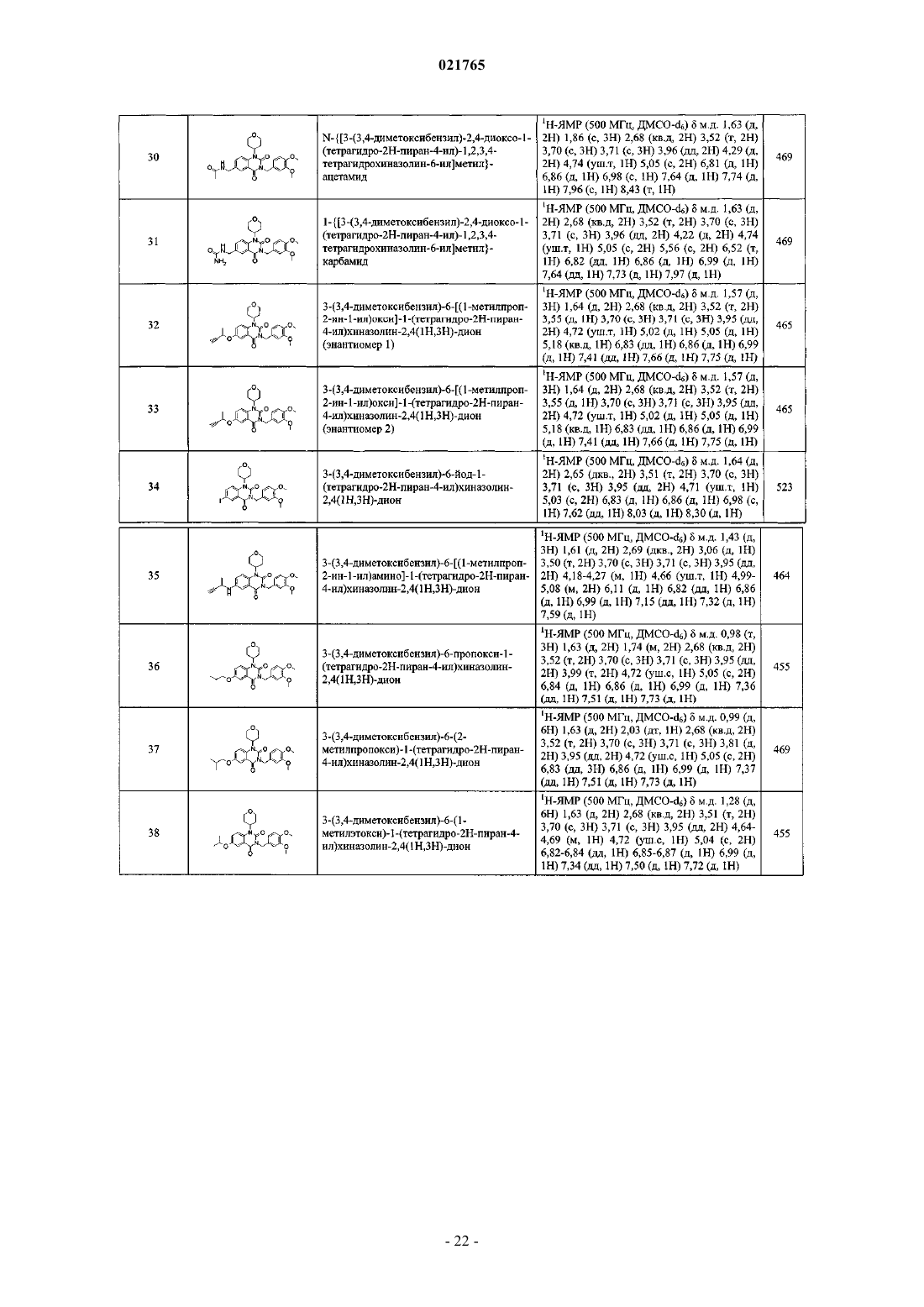
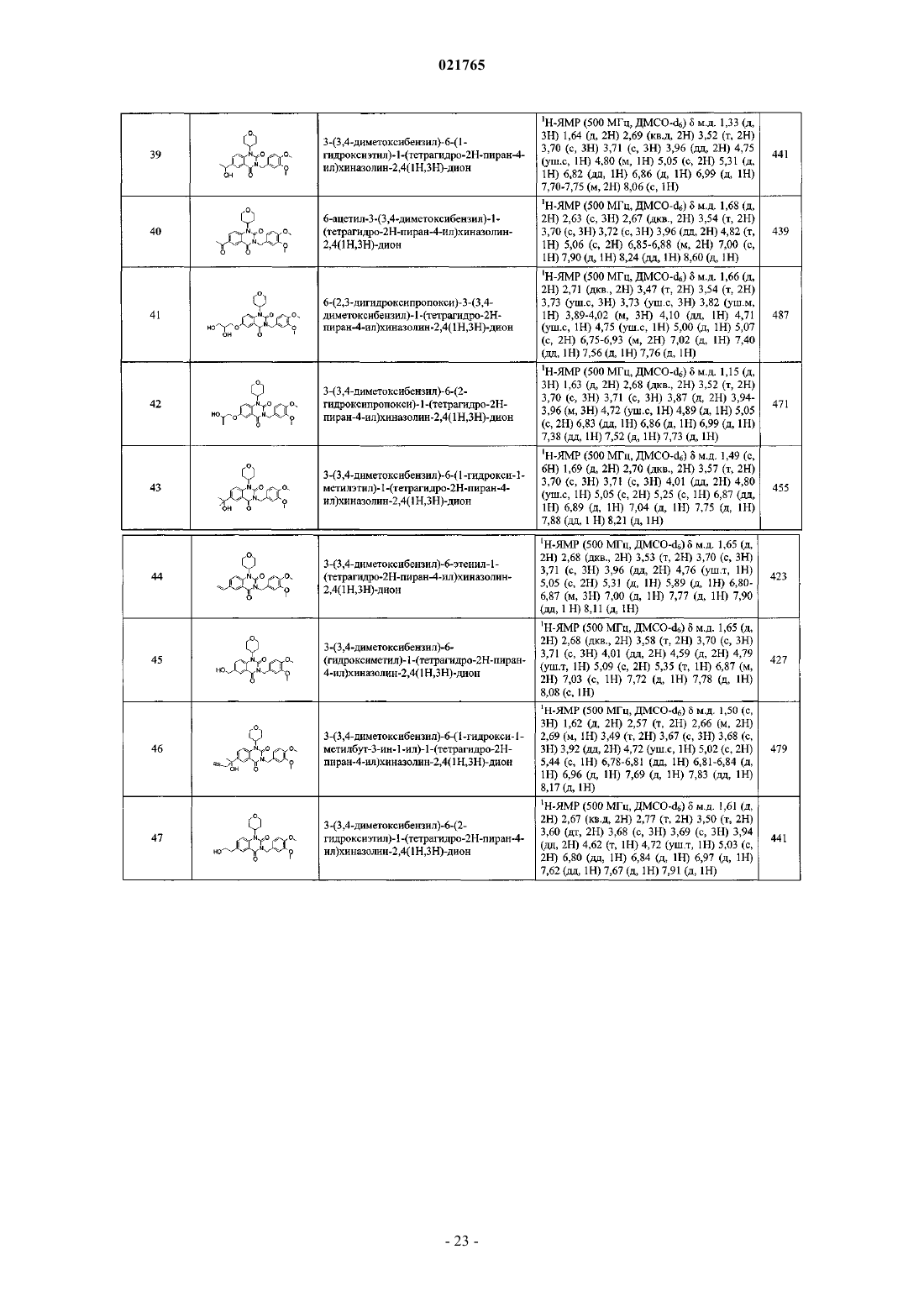
6. Соединение по любому из пп.1-5, отличающееся тем, что оно представляет собой одно из следующих соединений:
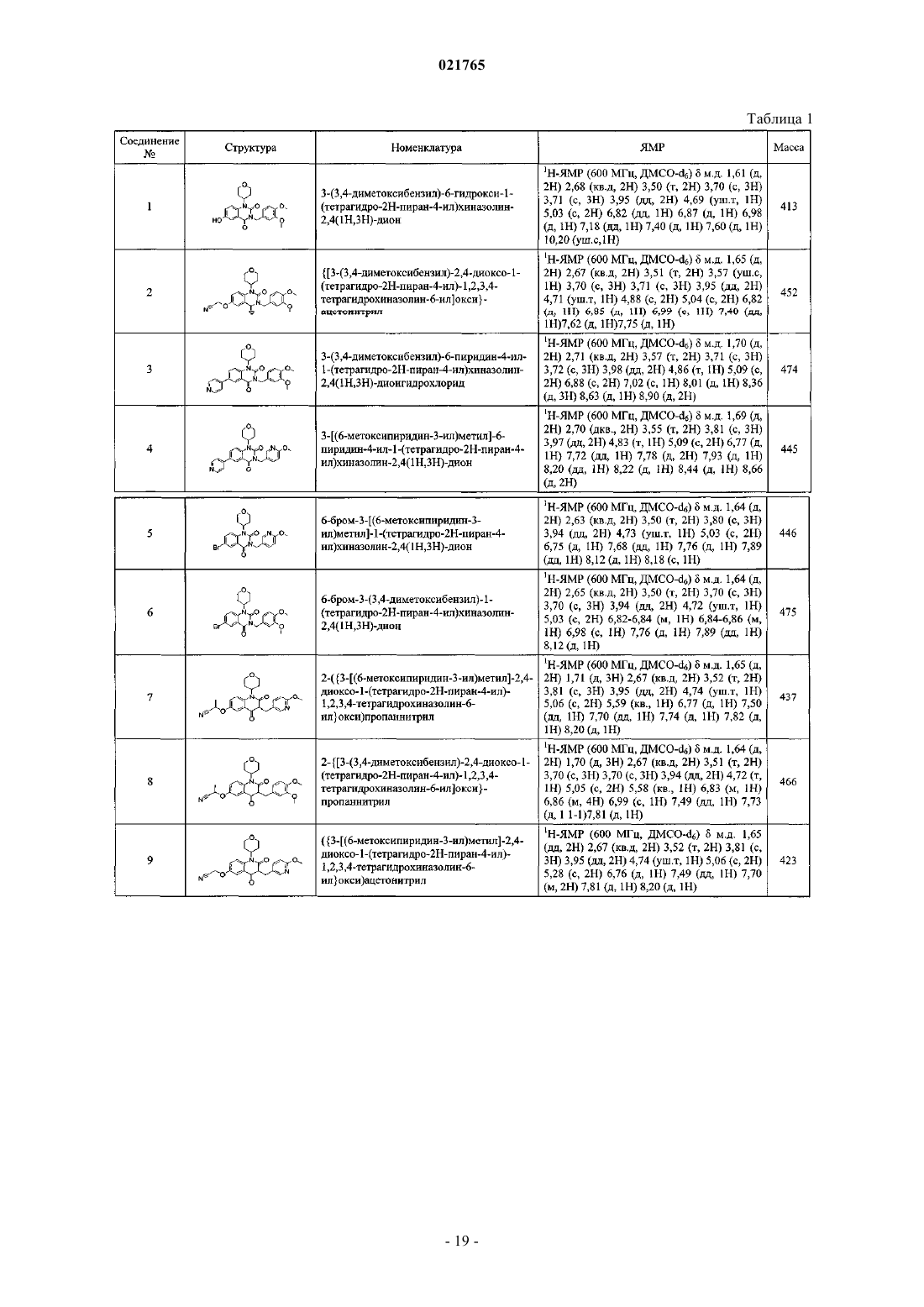
соединение №1: 3-(3,4-диметоксибензил)-6-гидрокси-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3H)-дион;
соединение №2: {[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}ацетонитрил;
соединение №3: 3-(3,4-диметоксибензил)-6-пиридин-4-ил-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дионгидрохлорид;
соединение №4: 3-[(6-метоксипиридин-3-ил)метил]-6-пиридин-4-ил-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №5: 6-бром-3-[(6-метоксипиридин-3-ил)метил]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №6: 6-бром-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №7: 2-({3-[(6-метоксипиридин-3-ил)метил]-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил}окси)пропаннитрил;
соединение №8: 2-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}пропаннитрил;
соединение №9: ({3-[(6-метоксипиридин-3-ил)метил]-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил}окси)ацетонитрил;
соединение №10: 3-(3,4-диметоксибензил)-6-гидрокси-1-(тетрагидро-2Н-тиопиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №11: {[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-тиопиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}ацетонитрил;
соединение №12: 2-{[3-(3,4-диметоксибензил)-1-(1,1-диоксидотетрагидро-2Н-тиопиран-4-ил)-2,4-диоксо-1,2,3,4-тетрагидрохиназолин-6-ил]окси}пропаннитрил;
соединение №13: 3-(3,4-диметоксибензил)-6-гидрокси-1-(1-оксидотетрагидро-2Н-тиопиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №14: {[3-(3,4-диметоксибензил)-1-(1,1-диоксидотетрагидро-2Н-тиопиран-4-ил)-2,4-диоксо-1,2,3,4-тетрагидрохиназолин-6-ил]окси}ацетонитрил;
соединение №15: 2-{[3-(3,4-диметоксибензил)-1-(1-оксидотетрагидро-2Н-тиопиран-4-ил)-2,4-диоксо-1,2,3,4-тетрагидрохиназолин-6-ил]окси}пропаннитрил (изомер 1);
соединение №16: 2-{[3-(3,4-диметоксибензил)-1-(1-оксидотетрагидро-2Н-тиопиран-4-ил)-2,4-диоксо-1,2,3,4-тетрагидрохиназолин-6-ил]окси}пропаннитрил (изомер 2);
соединение №17: {[3-(3,4-диметоксибензил)-1-(1-оксидотетрагидро-2Н-тиопиран-4-ил)-2,4-диоксо-1,2,3,4-тетрагидрохиназолин-6-ил]окси}ацетонитрил (изомер 1);
соединение №18: {[3-(3,4-диметоксибензил)-1-(1-оксидотетрагидро-2Н-тиопиран-4-ил)-2,4-диоксо-1,2,3,4-тетрагидрохиназолин-6-ил]окси}ацетонитрил (изомер 2);
соединение №19: 2-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}пропаннитрил-метан (1:1) (энантиомер 1);
соединение №20: 2-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}пропаннитрил-метан (1:1) (энантиомер 2);
соединение №21: 3-(3,4-диметоксибензил)-6-(проп-2-ин-1-илокси)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №22: 2-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}-2-метилпропаннитрил;
соединение №23: 2-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]окси}-2-метилпропанамид;
соединение №24: 3-(3,4-диметоксибензил)-6-(2-гидроксиэтоки)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №25: 6-(циклопропилметокси)-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №26: 3-(3,4-диметоксибензил)-6-[(1-метилпроп-2-ин-1-ил)окси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №27: 3-(3,4-диметоксибензил)-6-(3-гидроксиазетидин-1-ил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №28: 3-(3,4-диметоксибензил)-6-(проп-2-ин-1-иламино)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №29: 3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-карбонитрил;
соединение №30: N-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]метил}ацетамид;
соединение №31: 1-{[3-(3,4-диметоксибензил)-2,4-диоксо-1-(тетрагидро-2Н-пиран-4-ил)-1,2,3,4-тетрагидрохиназолин-6-ил]метил}карбамид;
соединение №32: 3-(3,4-диметоксибензил)-6-[(1-метилпроп-2-ин-1-ил)окси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион (энантиомер 1);
соединение №33: 3-(3,4-диметоксибензил)-6-[(1-метилпроп-2-ин-1-ил)окси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион (энантиомер 2);
соединение №34: 3-(3,4-диметоксибензил)-6-йод-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №35: 3-(3,4-диметоксибензил)-6-[(1-метилпроп-2-ин-1-ил)амино]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №36: 3-(3,4-диметоксибензил)-6-пропокси-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №37: 3-(3,4-диметоксибензил)-6-(2-метилпропокси)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №38: 3-(3,4-диметоксибензил)-6-(1-метилэтокси)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №39: 3-(3,4-диметоксибензил)-6-(1-гидроксиэтил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №40: 6-ацетил-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №41: 6-(2,3-дигидроксипропокси)-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №42: 3-(3,4-диметоксибензил)-6-(2-гидроксипропокси)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №43: 3-(3,4-диметоксибензил)-6-(1-гидрокси-1-метилэтил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №44: 3-(3,4-диметоксибензил)-6-этенил-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №45: 3-(3,4-диметоксибензил)-6-(гидроксиметил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №46: 3-(3,4-диметоксибензил)-6-(1-гидрокси-1-метилбут-3-ин-1-ил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №47: 3-(3,4-диметоксибензил)-6-(2-гидроксиэтил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №48: 3-(3,4-диметоксибензил)-6-[(1R)-2-гидрокси-1-метилэтокси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №49: 3-(3,4-диметоксибензил)-6-этокси-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №50: 3-(3,4-диметоксибензил)-6-(2-фторэтокси)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №51: 3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)-6-(2,2,2-трифторэтокси)хиназолин-2,4(1H,3Н)-дион;
соединение №52: 3-(3,4-диметоксибензил)-6-[(1S)-2-гидрокси-1-метилэтокси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №53: 6-(2,2-дифторэтокси)-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №54: 3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)-6-(3,3,3-трифторпропокси)хиназолин-2,4(1H,3Н)-дион;
соединение №55: 3-(3,4-диметоксибензил)-6-{[(1R)-1-метилпропил]окси}-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №56: 3-(3,4-диметоксибензил)-6-{[(1S)-1-метилпропил]окси}-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №57: 3-(3,4-диметоксибензил)-6-[2-фтор-1-(фторметил)этокси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №58: 3-(3,4-диметоксибензил)-6-[(1S)-2-фтор-1-метилэтокси]-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №59: 6-(2,2-дифторэтенил)-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №60: 3-(3,4-диметоксибензил)-6-(фторметил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №61: 3-(3,4-диметоксибензил)-7-фтор-6-гидрокси-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №62: 6-(бензилокси)-3-(3,4-диметоксибензил)-7-фтор-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1Н,3Н)-дион;
соединение №63: 6-(2,2-дифторэтокси)-3-(3,4-диметоксибензил)-7-фтор-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №64: 3-[4-(бензилокси)-3-метоксибензил]-6-[(1,3-дифторпропан-2-ил)окси]-7-фтор-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №65: 3-{4-[(3,4-дихлорбензил)окси]-3-метоксибензил}-6-[(1,3-дифторпропан-2-ил)окси]-7-фтор-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №66: 3-(3,4-диметоксибензил)-6-нитро-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №67: 6-амино-3-(3,4-диметоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион;
соединение №68: 6-[(1,3-дифторпропан-2-ил)окси]-7-фтор-3-(4-гидрокси-3-метоксибензил)-1-(тетрагидро-2Н-пиран-4-ил)хиназолин-2,4(1H,3Н)-дион,
в форме основания или кислотно-аддитивной соли.
7. Лекарственное средство для ингибирования фосфодиэстеразы 8 (PDE8) и/или фосфодиэстеразы (PDE7), отличающееся тем, что включает по меньшей мере одно соединение по любому из пп.1-6 или аддитивную соль этого соединения фармацевтически приемлемой кислоты.
8. Фармацевтическая композиция для ингибирования фосфодиэстеразы 8 (PDE8) и/или фосфодиэстеразы (PDE7), отличающаяся тем, что включает по меньшей мере одно соединение по любому из пп.1-6 или аддитивную соль этого соединения фармацевтически приемлемой кислоты, а также по меньшей мере один фармацевтически приемлемый эксципиент.
9. Применение по меньшей мере одного соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства.
10. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики по меньшей мере одного воспалительного или иммуновоспалительного заболевания.
11. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики астмы, обструктивной хронической бронхопневмонии (COPD), аллергического ринита, аллергий, болезни Крона, язвенного колита, тяжелой миастении, атопического дерматита, псориаза, обыкновенной красной волчанки, ревматоидного полиартрита, диабета и рассеянного склероза.
12. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики явлений отторжений во время трансплантации и/или иммуновоспалительных реакций после трансплантации, для лечения и/или профилактики некоторых типов раковых заболеваний, таких как остеосаркома и аденосаркома, для лечения и/или профилактики костных заболеваний, таких как остеопения и остеопороз, для лечения и/или профилактики острой почечной недостаточности, для лечения и/или профилактики боли, невропатической боли и висцеральной боли.
13. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики по меньшей мере одного сердечно-сосудистого заболевания и/или для профилактики развития по меньшей мере одного сердечно-сосудистого заболевания.
14. Применение по п.13, отличающееся тем, что сердечно-сосудистое заболевание выбирают из (i) коронарных заболеваний, (ii) заболеваний сердечной мышцы, (iii) связанных с сердечными клапанами заболеваний, (iv) заболеваний перикарда, (v) связанных с сердечным ритмом заболеваний и заболеваний проводящей системы сердца и (vi) сосудистых заболеваний.
15. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики возникновения инфаркта миокарда, сократительных сердечных дисфункций, являющихся следствием инфаркта миокарда, заболеваний, ассоциированных с повреждениями реперфузии сердечной и/или скелетной мышцы, пульмонарной гипертензии, гепатического фиброза, артериального рестеноза после ангиопластики с или без введения стента, атеросклероза и его осложнений, разрыва бляшки, аневризмы и коронарных заболеваний, сердечной недостаточности, расширенных кардиопатий и миокардитов вирусного и/или бактериального происхождения.
16. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики нарушения(ий), связанного(ных) с центральной нервной системой и/или связанного(ных) с периферической нервной системой.
17. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики психиатрического(их) нарушения(ий) и/или неврологического(их) нарушения(ий).
18. Применение по п.17, отличающееся тем, что (i) психиатрическое нарушение выбирают из тревоги, депрессии, нарушений настроения, инсомнии, связанных с бредом нарушений, связанных с навязчивой идеей нарушений, психозов, связанных с шизофренией нарушений, нарушений, связанных с дефицитом внимания и гиперактивностью (TDAH) у детей с гиперкинезом, нарушений, связанных с использованием психотропных веществ, в случае злоупотребления веществом и/или зависимости от вещества, включая туда алкогольную зависимость и/или никотиновую зависимость, мигрени, стресса, нарушений, связанных с заболеваниями психосоматического происхождения, приступов паники, эпилепсии, мнезических нарушений, когнитивных нарушений, старческого слабоумия, связанных с болезнью Альцгеймера нарушений, а также нарушений внимания или бдительности, ишемии, связанных с черепно-мозговыми травмами нарушений, связанных с острыми или хроническими нейродегенеративными заболеваниями нарушений, включая хорею и хорею Гентингтона, и тем, что (ii) неврологическое нарушение, которое может выражаться в аномалиях движения или моторных нарушениях, ассоциировано с патологией, выбираемой среди дискинезий, болезни Паркинсона, синдрома постэнцефалитического паркинсонизма, допа-чувствительных дистоний, синдрома Shy-Drager, синдрома нарушения периодических движений конечностей (PLMD), синдрома периодических движений конечностей во сне (PLMS), синдрома Туретта, синдрома беспокойных ног (RLS).
19. Применение соединения по любому из пп.1-6 в качестве лекарственного средства или для получения лекарственного средства, предназначенного для лечения и/или профилактики неврологических нарушений, выражающихся в аномалиях движения или моторных нарушениях, ассоциированных с повреждениями спинного мозга.
20. Соединение формулы
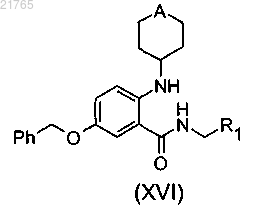
отличающееся тем, что R1 и А имеют указанные в п.1 значения.
Текст
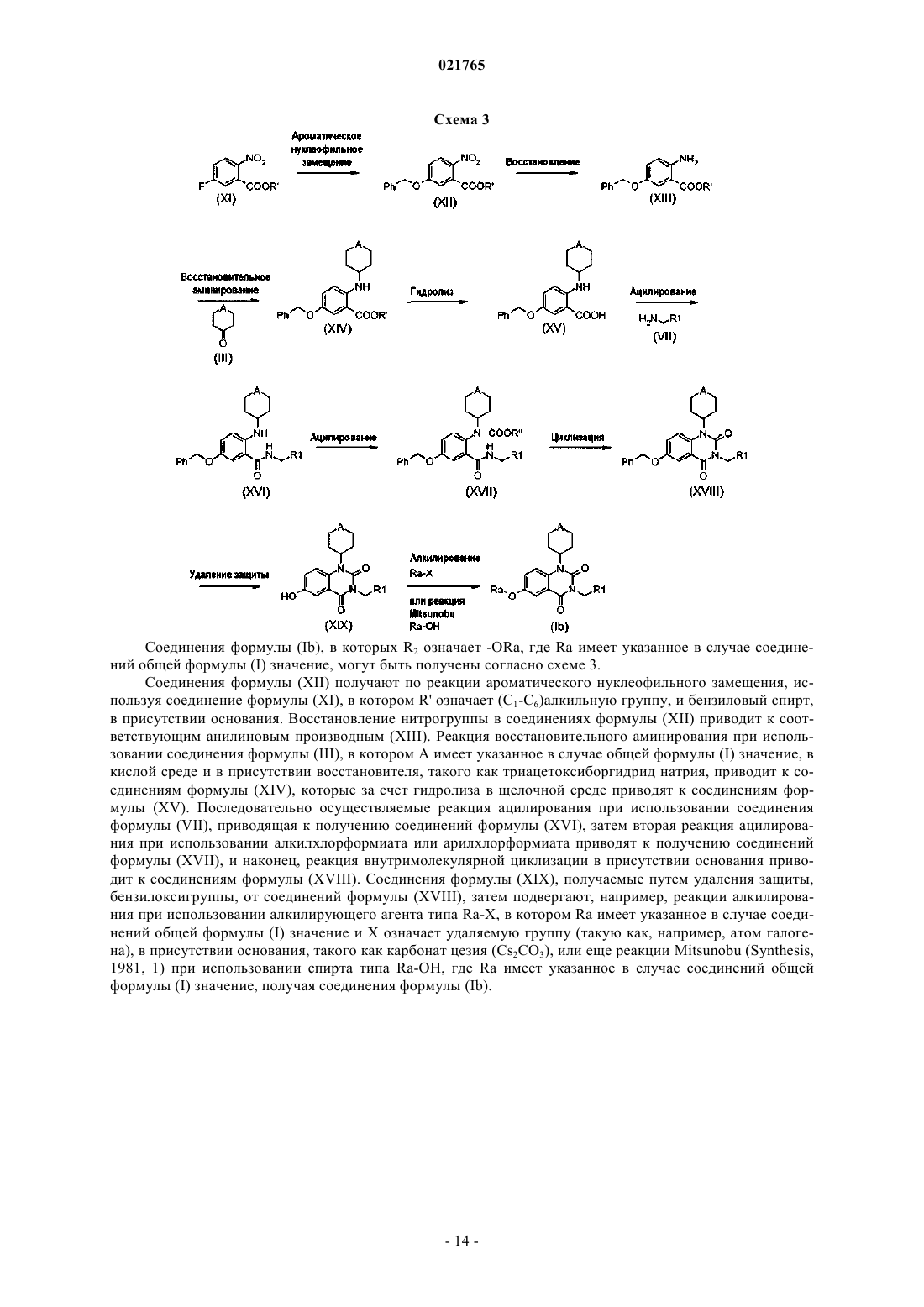
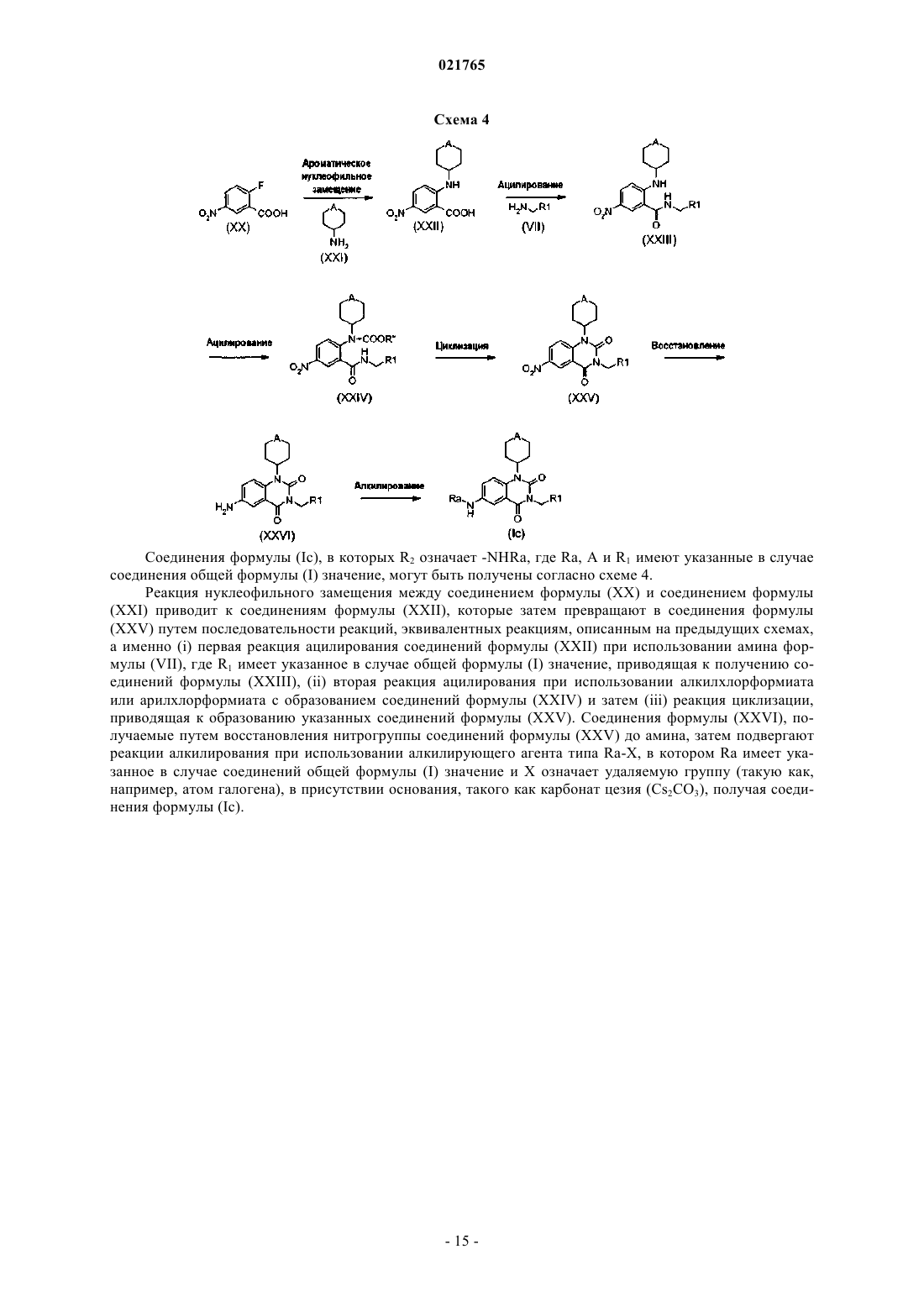
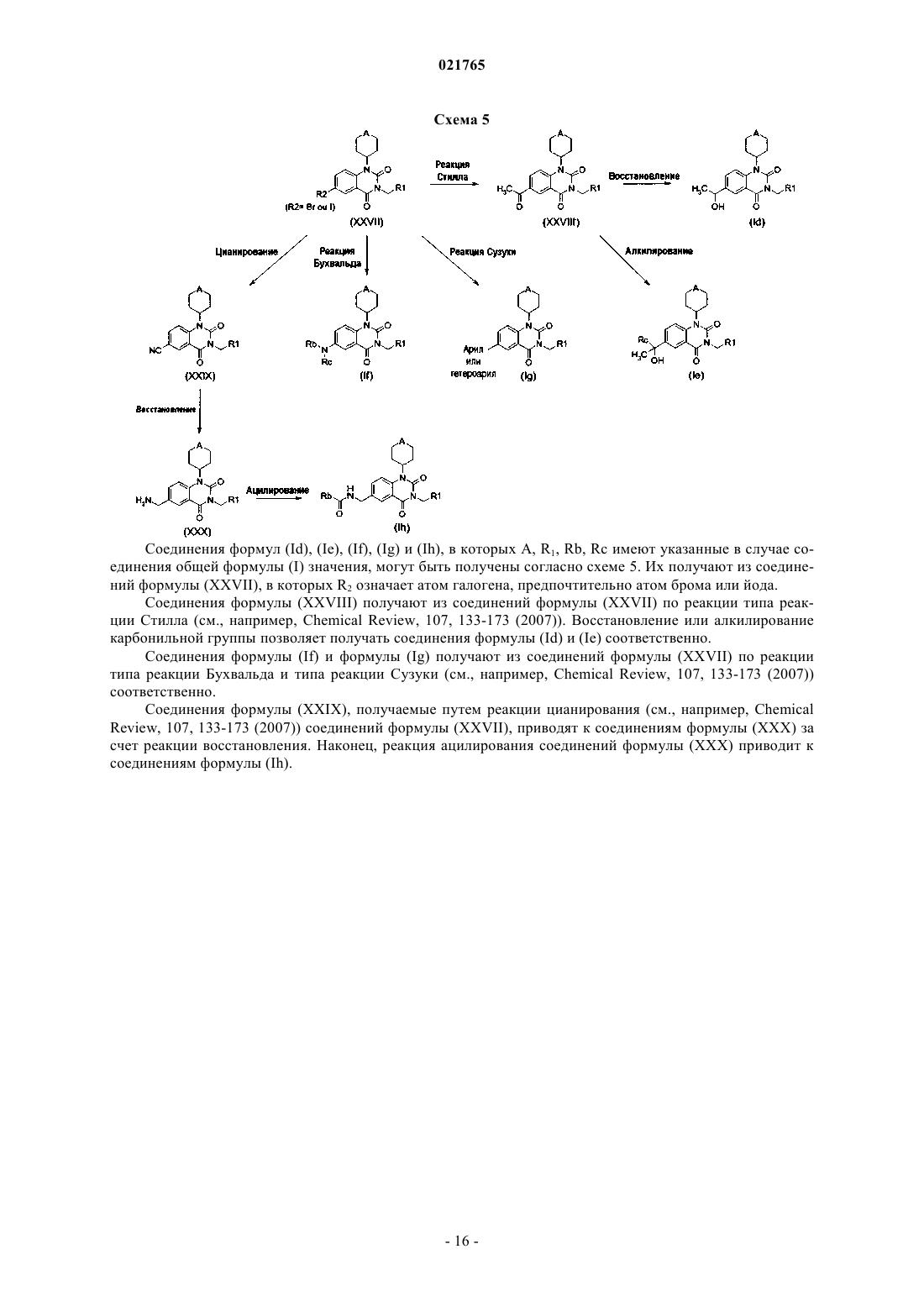
ПРОИЗВОДНЫЕ ХИНАЗОЛИНДИОНА, ИХ ПОЛУЧЕНИЕ И ИХ РАЗЛИЧНЫЕ ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ Объектом настоящего изобретения являются производные хиназолиндиона формулы (I), где А означает атом серы или кислорода или сульфоксидную или сульфоновую группу, способы их получения и их терапевтические применения, такие как, среди прочего, в случае рака, диабета,мышечных, костных, сердечно-сосудистых заболеваний, заболеваний центральной нервной системы, заболеваний периферической нервной системы Объектом настоящего изобретения являются производные хиназолиндиона, способы их получения,их промежуточные продукты синтеза и их терапевтические применения. Настоящее изобретение относится к производным хиназолиндиона, которые могут быть ингибиторами фосфодиэстеразы 7 (сокращенно PDE7). Некоторые из этих производных также могут ингибировать фосфодиэстеразу 8 (сокращенно PDE8). Настоящее изобретение также относится к применению таких прозводных хиназолиндиона, способных действовать в качестве ингибиторов фосфодиэстеразы 7 (PDE7), даже, в случае некоторых из этих производных, способных действовать также в качестве ингибиторов фосфодиэстеразы 8 (PDE8),причем не исключено, что эти же самые производные хиназолиндиона также способны действовать через другие биологические/биохимические пути. Фосфодиэстеразы (PDE) представляют собой внутриклеточные ферменты, ответственные за гидролиз вторичных матричных цАМФ (циклический аденозин-3',5'-монофосфат) и цГМФ (циклический гуанозин-3',5'-монофосфат) до неактивных нуклеотид-5'-монофосфатов. цАМФ и цГМФ играют существенную роль в случае путей клеточной сигнализации и принимают участие в многочисленных физиологических процессах. Ингибирование фосфодиэстераз выражается в увеличении внутриклеточных концентраций цАМФ и цГМФ, что вызывает специфическую активацию путей фосфорилирования, принимающих активное участие в разнообразных функциональных ответных реакциях. Увеличение внутриклеточных концентраций цАМФ или цГМФ за счет селективных ингибиторов фосфодиэстераз кажется подающим надежды подходом для лечения различных заболеваний (Bender и Beavo, Pharmacol. Rev., 58, 488-520 (2006. Ингибиторы фосфодиэстераз, следовательно, представляют интерес в качестве терапевтических агентов и в качестве фармакологических инструментов. На сегодняшний день идентифицировано одиннадцать семейств фосфодиэстераз. Они различаются по их первичной структуре, их специфичности к субстрату и их чувствительности по отношению к различным эффекторам и специфическим ингибиторам PDE. Каждое семейство образовано одним или несколькими генами, которые экспрессируются в различных тканях в форме гибридных вариантов (Bender и Beavo, Pharmacol. Rev., 58, 488-520 (2006); Lugnier, Pharmacol. Therapeut., 109, 366-398 (2006.PDE4, PDE7 и PDE8 специфически гидролизуют цАМФ, a PDE5, PDE6 и PDE9 специфически гидролизуют цГМФ. Семейство PDE7 представлено изоформами PDE7A и PDE7B, происходящими от двух различных генов. Человеческая PDE7A (Michaeli и др., J. biol. Chem., 268, 12925-12932 (1993); Han и др., J. Biol.Chem., 272, 16152-16157 (1997); Wang и др., Biochem. Biophys. Res. Commun., 276, 1271-1277 (2000 и человеческая PDE7B (Sasaki и др., Biochem. Biophys. Res. Commun., 271, 575-583 (2000); Gardner и др.,Biochem. Biophys. Res. Commun., 272, 186-192 (2000 селективно гидролизуют цАМФ с константами Михаэлиса (Km) 0,1-0,2 и 0,13-0,2 мкМ соответственно. Каталитическая часть PDE7B имеет около 67% гомологии с каталитической частью PDE7A. Для PDE7A известны три гибридных варианта. PDE7A1 и PDE7A3 экспрессируются главным образом в клетках иммунной системы и легких, тогда как PDE7A2 экспрессируется в особенности в мышцах скелета, сердце и почках. В случае PDE7B также недавно были индентифицированы три варианта (Giembycz и Smith, Drugs Future, 32, 207-229 (2006. Профили тканевого распределения PDE7A и PDE7B являются очень различными, что наводит на мысль, что эти две изоформы имеют различные функции с физиологической точки зрения. Тогда какPDE7A в изобилии экспрессируется в гематопоэтических клетках, легких, плаценте, клетках Leydig, селезенке, коллекторных каналах почек и надпочечниках, сильная экспрессия PDE7B обнаружена в поджелудочной железе, сердце, щитовидной железе и скелетных мышцах (Giembycz и Smith, Drugs Future, 32,207-229 (2006. Локализация PDE7 на уровне указанных органов наводит на мысль, что селективные ингибиторыPDE7 могут иметь применения в области мышечных, почечных, сердечных и панкреатических заболеваний, как и в случае лечения и/или профилактики диабета. Коэкспрессия матричных РНК (мРНК) PDE7A и PDE7B, однако, наблюдалась в некоторых тканях. Это имеет место в случае остеобластов (Ahistrom и др., Cell. Mol. Biol. Lett., 10, 305-319 (2005 и некоторых областях головного мозга: некоторые зоны коры головного мозга, зубчатая извилина, большинство компонентов обонятельной системы, стриатум, многочисленные ядра таламуса и пирамидальные клетки гиппокампа (Miro и др., Synapse, 40, 201-214 (2001); Reyes-Irisarri и др., Neuroscience, 132, 1173-1185(2005. Напротив, в некоторых зонах головного мозга экспрессируется только одна из двух изоформ. Так, одни мРНК PDE7A присутствуют в многочисленных ядрах ствола мозга. Так же мРНК PDE7B присутствуют в высоких концентрациях в аккумбенсовом ядре и заднем ядре блуждающего нерва, тогда как мРНК PDE7A не детектированы (Miro и др., Synapse, 40, 201-214 (2001); Reyes-Irisarri и др., Neuroscience,132, 1173-1185 (2005.PDE7 А 1-белок хорошо экспрессируется в T-лимфоцитах крови, линиях эпителиальных клеток бронхов, фибробластах легкого и эозинофилах (Smith и др., Am. J. Physiol. Lung Cell. Mol. Physiol., 284:L279-L289 (2003. Некоторые сообщения наводят на мысль, что PDE7A может играть роль в активацииT-лимфоцитов (Li и др., Science, 283, 848-851 (1999); Glavas и др., PNAS, 98, 6319-6324 (2001); Nakata и др., Clin. Exp. Immunol., 128, 460-466 (2002); Smith и др., Mol. Pharmacol., 66, 1679-1689 (2004. PDE7 А 1 белок также экспрессируется в клетках, которые играют центральную роль в патогенезе астмы и хронической обструктивной бронхопневмонии (COPD), таких как T-лимфоциты (CD4+ и CD8+), моноциты,нейтрофилы, альвеолярные макрофаги, гладкомышечные клетки дыхательных путей и легочных сосудов(Smith и др., Am. J. Physiol. Lung Cell. Mol. Physiol., 284: L279-L289 (2003. Локализация PDE7A в провоспалительных клетках и клетках иммунной системы и ее потенциальная роль в активации Tлимфоцитов наводят на мысль, что селективные ингибиторы PDE7 могут иметь применения в области заболеваний, связанных с T-лимфоцитами, и в области заболеваний легочных путей.PDE7 А-белок также присутствует в В-лимфоцитах и в клеточной линии В-лимфоцитов WSU-CLL,происходящей от пациента, пораженного хроническим лейкоцитарным лейкозом. Обработка клетокWSU-CLL с помощью IC242, специфического ингибитора PDE7, повышает экспрессию PDE7A (Lee и др., Cell Signal, 14, 277-284 (2002. Кроме того, показано, что экспрессия PDE7 В-белка примерно в 5-90 раз является более высокой в мононуклеарных клетках периферической крови (РВМС) пациентов, пораженных хроническим лимфоцитарным лейкозом (CLL-PBMC), чем в случае РВМС, выделенных из крови здоровых индивидов (WO 2007/067946). BRL-50481, селективный ингибитор PDE7, индуцирует зависимым от дозы образом апоптоз CLL-PBMC, однако он не оказывает воздействия на РВМС здоровых индивидов. Эти наблюдения наводят на мысль, что селективные ингибиторы PDE7 могут быть эффективными в случае лечения этого типа лейкоза. Селективные ингибиторы PDE4 повышают минеральную костную плотность у крысы и мыши, и их воздействия представляются связанными с уменьшением активности остеокластов и с увеличением активности остеобластов (Miyamoto и др., Biochem. Pharmacol., 54, 613-617 (1997); Waki и др., Jpn J. Pharmacol., 79, 477-483 (1999); Kinoshita и др., Bone, 27, 811-817 (2000. Активность PDE7 детектирована в случае остеобластов (Ahlstrm и др., Cell. Mol. Biol. Lett., 10, 305-319 (2005. Повышая внутриклеточную концентрацию цАМФ, ингибиторы PDE7, как и ингибиторы PDE4, могут оказываться эффективными при лечении остеопении и остеопороза. Кроме того, в случае недавно проведенных исследований (WO 2006/092691, WO 2006/092692) сообщается о фармакологических активностях различных ингибиторов PDE7 при использовании моделей невропатической боли у крысы, что наводит на мысль о применениях при лечении различных типов болей и, более конкретно, при лечении невропатической боли. Кроме того, в документе WO 2008/119057 описывается способ лечения аномалий движения, ассоциированных с патологией неврологического нарушения движения, такой как болезнь Паркинсона, способ лечения, включающий введение пациенту количества ингибитора PDE7, эффективного для ингибирования ферментативной активности PDE7. Объектом настоящего изобретения является соединение следующей общей формулы (I): в которой А означает либо атом кислорода или серы, либо сульфоксидную группу (группа SO) или сульфоновую группу (группа SO2);R2 означает атом или группу, выбираемую из: атома водорода,атома галогена,цианогруппы,нитрогруппы,арильной, арилалкильной или гетероарильной группы,(C1-C6)алкильной группы, необязательно замещенной -NH2, одним или несколькими атомами галогена, одной или несколькими гидроксигруппами, алкинильной группой, алкенильной группой, группой-NHC(O)Rb и/или группой -NHC(O)-NRbRc, где Rb и Rc имеют указанные ниже значения,группы -ORa, где Ra имеет указанное ниже значение,группы NRbRc, где Rb и Rc имеют указанные ниже значения,C(O)(C1-C6)алкильной группы,алкенильной группы или алкинильной группы, где указанные группы необязательно замещены по меньшей мере одним гидрокси или по меньшей мере одним атомом галогена,-2 021765p имеет значение 1, 2 или 3, при условии, что, когда p равно 2 или 3, тогда атомы R2 или группы R2 могут быть соответственно одинаковыми или различными;R1 означает арильную, арилалкильную или гетероарильную группы, где указанные группы необязательно замещены (i) атомом R3 или группой R3 или (ii) 2 или 3 атомами и/или группами R3, причем указанные атомы или группы R3 являются соответственно одинаковыми или различными; при условии, что R3 означает: атом водорода,атом галогена,гидроксигруппу,цианогруппу,группу -SCF3,нитрогруппу,-S(O)0-2-алкильную группу, -S(O)0-2-гетероциклоалкильную группу, -O-SO2-арильную группу или-O-SO2-арилалкильную группу, необязательно замещенную одним или несколькими атомами галогена,алкиламиноалкильную группу или циклоалкиламиноалкильную группу, где указанные группы необязательно замещены по концевому алкилу,сульфонамидную группу, необязательно замещенную,арильную, арилалкильную или гетероарильную группу, где указанная группа является моноциклической или полициклической и, кроме того, необязательно замещена (C1-C6)алкильной группой, одной или несколькими гидроксигруппами, одним или несколькими атомами галогена, одной или несколькими цианогруппами и/или одной или несколькими (C1-C6)алкоксилгруппами,гетероциклоалкильную группу, необязательно замещенную (C1-C6)алкильной группой,(C1-C6)алкильную группу, необязательно замещенную: одним или несколькими атомами галогена,арильной или арилалкильной группой, которая может быть замещена одним или несколькими атомами галогена, одной или несколькими (C1-C6)алкоксигруппами, одной или несколькими (C1C6)алкильными группами, одной или несколькими цианогруппами и/или одной или несколькими гидроксигруппами,гетероарильной группой,одной или несколькими гидроксигруппами, которые могут быть замещены арильной или арилалкильной группой, которая необязательно замещена одним или несколькими атомами галогена, или гетероциклоалкильной группой, необязательно замещенной группой CO(O)Ra или (C1C6)алкильной группой, где Ra имеет указанное ниже значение,группу -C(O)NRbRc, где Rb и Rc имеют указанные ниже значения,группу -C(O)ORc или группу -O-C(O)ORc, где Rc имеет указанное ниже значение,(C1-C6)алкоксигруппу, необязательно замещенную: аминоалкильной группой, аминоциклоалкильной группой,циклоалкильной группой,гетероциклоалкильной группой, моноциклической или полициклической гетероарильной группой,одной или несколькими гидроксигруппами,одним или несколькими атомами галогена,(C1-C6)алкоксигруппой,группой -C(O)ORc, где Rc имеет указанное ниже значение,группой -C(O)NRbRc, где Rb и Rc имеют указанные ниже значения, и/или арильной или арилалкильной группой, которая необязательно замещена по меньшей мере одним атомом и/или по меньшей мере одной группой, причем указанные атом(атомы) и группу(группы) выбирают из атомов галогена, цианогруппы, (C1-C6)алкокси, -O-галогеналкильных групп и галогеналкильных групп;-O-циклоалкильную группу, -O-арильную группу, -O-арилалкильную группу или -Oгетероциклоалкильную группу, где указанные группы необязательно замещены: арильной или арилалкильной группой, которая необязательно замещена одним или несколькими атомами галогена или (C1-C6)алкильной группой,одним или несколькими атомами галогена и/или(C1-C6)алкильной группой, которая может быть замещена арильной или арилалкильной группой;-NH-CO-NH-арильную группу, -NH-CO-NH-арилалкильную группу, -NH-CO-NH-гетероарильную группу или -NH-CO-NH-(C1-C6)алкильную группу, где указанные арил, арилалкил, гетероарил и алкил необязательно замещены по меньшей мере одним атомом и/или по меньшей мере одной группой, причем указанные атом(атомы) и группу(группы) выбирают из атомов галогена, цианогруппы, нитрогруппы,гидроксигруппы и (C1-C6)алкоксигрупп,-3 021765-N-(C1-C6)алкильную группу, где (С 1-C6)алкильная группа может быть замещена по меньшей мере одной арильной или арилалкильной группой, необязательно замещенной по меньшей мере одним атомом галогена и/или по меньшей мере одной группой SO2, или-NH-C(O)-арильную группу, -NH-C(O)-аралкильную группу или -NH-C(O)-гетероарильную группу,где указанные группы необязательно замещены по меньшей мере одним атомом галогена;Ra означает: атом водорода,(C1-C6)алкильную группу или (C1-C6)циклоалкильную группу, где указанные группы необязательно замещены одним или несколькими атомами галогена, одной или несколькими гидроксигруппами, арильной или арилалкильной группой, одной или несколькими цианогруппами и/или группой -C(O)NRbRc,где Rb и Rc имеют указанные ниже значения,(C2-C6)алкинильную группу,арильную или арилалкильную группу;Rb означает: атом водорода,(C1-C6)алкильную группу, необязательно замещенную одним или несколькими атомами галогена,одной или несколькими группами гидрокси, циано, амино, гетероциклоалкильными, (C1-C6)алкокси, или арильной или арилалкильной группой, необязательно замещенной одним или несколькими атомами галогена,(C3-C6)циклоалкильную группу,(C2-C6)алкенильную или алкинильную группу,(C1-C6)алкоксигруппу,арильную или арилалкильную группу, необязательно замещенную одним или несколькими атомами галогена;Rc означает атом водорода или (C1-C6)алкильную группу, необязательно замещенную одним или несколькими атомами галогена; при условии, что в группах -NRbRc, Rb и Rc вместе с атомом азота могут образовывать гетероарил или гетероциклоалкил, причем эти последние необязательно замещены; в форме основания или кислотно-аддитивной соли. Согласно одному варианту осуществления соединение согласно изобретению отличается тем, что n равно 1; в форме основания или кислотно-аддитивной соли. Согласно одному варианту осуществления соединение согласно изобретению отличается тем, что p имеет значение 1 или 2, при условии, что, когда p равно 2, тогда возможными комбинациями являются либо (i) два атома R2, одинаковых или различных, либо (ii) один атом R2 и одна группа R2, либо (iii) две группы R2, одинаковые или различные; в форме основания или кислотно-аддитивной соли. Согласно одному варианту осуществления соединение согласно изобретению отличается тем, чтоR2 означает атом или группу, выбираемую из: атома галогена,атома водорода,нитрогруппы,цианогруппы,арильной, арилалкильной или гетероарильной группы,(C1-C6)алкильной группы, необязательно замещенной -NH2, одной или несколькими гидроксигруппами, алкинильной группой, одним или несколькими атомами галогена, группой -NHC(O)Rb, где Rb означает необязательно замещенную (C1-C6)алкильную группу, группой -NHC(O)-NRbRc, где Rb и Rc означают атомы водорода, и/или алкенильной группой,группы -ORa, где Ra выбирают из: атома водорода,(C1-C6)алкильной группы, необязательно замещенной одним или несколькими атомами галогена,одной или несколькими гидроксигруппами, арильной или арилалкильной группой, одной или несколькими цианогруппами и/или группой -C(O)NRbRc,(C1-C6)циклоалкильной группы,(C2-C6)алкинильной группы,арильной группы,арилалкильной группы; группы NRbRc, где Rb выбирают из атома водорода и (C1-C6)алкильной группы, необязательно замещенной (С 2-C6)алкинильной группой, и Rc означает атом водорода, или Rb и Rc вместе с атомом азота образуют гетероциклоалкил, необязательно замещенный гидроксигруппой;C(O)(C1-C6)алкильной группы и алкенильной группы, необязательно замещенной по меньшей мере одним атомом галогена; в форме основания или кислотно-аддитивной соли. Согласно другому варианту осуществления соединение согласно изобретению отличается тем, чтоR2 означает атом или группу, выбираемую из: атома галогена, выбираемого из брома, фтора и йода,атома водорода,нитрогруппы,цианогруппы,арильной или гетероарильной группы, выбираемой из фенила и пиридинила,(C1-C6)алкильной группы, необязательно замещенной -NH2, одной или несколькими гидроксигруппами, алкинильной группой, одним или несколькими атомами фтора, группой -NHC(O)Rb, где Rb означает необязательно замещенную (C1-C6)алкильную группу, группой -NHC(O)-NRbRc, где Rb и Rc означают атомы водорода, и/или алкенильной группой,группы -ORa, где Ra выбирают из: атома водорода,(C1-C6)алкильной группы, необязательно замещенной одним или несколькими атомами галогена,одним или несколькими атомами фтора, одной или несколькими гидроксигруппами, бензильной или фенильной группой, одной или несколькими цианогруппами и/или группой -C(O)NRbRc, где Rb и Rc означают атомы водорода,(C1-C6)циклоалкила,(С 2-C6)алкинила,бензила; группы NRbRc, где Rb выбирают из атома водорода и (C1-C6)алкильной группы, необязательно замещенной (С 2-C6)алкинильной группой, и Rc означает атом водорода, или Rb и Rc вместе с атомом азота образуют гетероциклоалкил, необязательно замещенный гидроксигруппой; С(O)(C1-C6)алкильной группы и алкенильной группы, необязательно замещенной по меньшей мере одним атомом фтора; в форме основания или кислотно-аддитивной соли. Согласно другому варианту осуществления соединение по любому из предыдущих притязаний отличается тем, что p равно 2 и две группы и/или два атома R2 выбирают из: атома галогена и группы -ORa, где Ra выбирают из: атома водорода и(C1-C6)алкильной группы, необязательно замещенной одним или несколькими атомами галогена или арильной группой; в форме основания или кислотно-аддитивной соли. Согласно другому варианту осуществления соединение согласно изобретению отличается тем, что(C1-C6)алкильной группы, необязательно замещенной одним или несколькими атомами фтора или фенильной группой; в форме основания или кислотно-аддитивной соли. Согласно другому варианту осуществления соединение согласно изобретению отличается тем, чтоR1 означает фенил или пиридинил, необязательно замещенные (i) атомом R3 или группой R3 или (ii) двумя атомами и/или группами R3, причем тогда возможными комбинациями являются: либо два, одинаковых или различных, атома R3,либо один атом R3 и одна группа R3,либо две, одинаковые или различные, группы R3,где R3 выбирают из гидрокси и (C1-C6)алкоксигрупп, причем указанные (C1-C6)алкоксигруппы необязательно замещены арильной или арилалкильной группой, где указанная арильная или арилалкильная группа необязательно замещена по меньшей мере одним атомом галогена; в форме основания или кислотно-аддитивной соли. Согласно другому варианту осуществления соединение согласно изобретению отличается тем, чтоR1 означает фенил или пиридинил, необязательно замещенные (i) атомом R3 или группой R3 или (ii) двумя атомами и/или группами R3, причем тогда возможными комбинациями являются: либо два, одинаковых или различных, атома R3,либо один атом R3 и одна группа R3,либо две, одинаковые или различные, группы R3,где R3 выбирают из гидрокси и (C1-C6)алкоксигрупп, причем указанные (C1-C6)алкоксигруппы необязательно замещены бензильной группой, где указанная бензильная группа необязательно замещена по меньшей мере одним атомом хлора; в форме основания или кислотно-аддитивной соли. Из соединений формулы (I), являющихся объектами настоящего изобретения, можно назвать, в ча-5 021765 в форме основания или кислотно-аддитивной соли. Производные хиназолиндиона, являющиеся объектами настоящего изобретения, которые могут оказываться сильными ингибиторами PDE7 или PDE7 и PDE8, в зависимости от производных, или могут воздействовать на другие биологические пути, могут быть использованы в качестве лекарственных средств или для получения лекарственных средств. Соединения общей формулы (I) могут включать один или несколько асимметрических центров. Следовательно, они могут существовать в форме энантиомеров или диастереоизомеров. Эти энантиоме- 10021765 ры, диастереоизомеры, а также их смеси, включая рацемические смеси, составляют часть изобретения. Чистые энантиомеры соединений согласно изобретению могут быть получены из энантиомерно чистых предшественников или же путем хроматографии на хиральных фазах, или же, когда соединения включают кислотные группы или аминогруппы, путем селективных кристаллизации диастереоизомерных солей, получаемых за счет реакции соединений (I) соответственно с хиральными аминами или кислотами. По своей структуре соединения общей формулы (I) могут также существовать в форме изомеров ротамерного типа или типа атропоизомера. Соединения формулы (I) также могут существовать в виде оснований или кислотно-аддитивных солей. Такие аддитивные соли составляют часть изобретения. Эти соли преимущественно получают при использовании фармацевтически приемлемых кислот,однако соли других кислот, пригодные, например, для очистки или выделения соединений общей формулы (I), также составляют часть изобретения. Соединения общей формулы (I) также могут находиться в кристаллической, аморфной или маслянистой форме, причем эти формы составляют часть изобретения. Соединения общей формулы (I), кроме того, могут находиться в форме гидратов или сольватов, а именно в форме ассоциаций или комбинаций с одной или несколькими молекулами воды или с растворителем. Такие гидраты и сольваты также составляют часть изобретения. Согласно настоящему изобретению N-оксиды соединений, включающих амин, также составляют часть изобретения. Соединения формулы (I) согласно настоящему изобретению включают также соединения, в случае которых один или несколько атомов водорода, углерода или галогена, а именно хлора или фтора, заменены их радиоактивными изотопами, как, например, тритий, дейтерий для замены водорода или углерод 14 для замены углерода-12. Такие меченые соединения могут быть пригодны в случае научноисследовательских работ, работ в отношении метаболизма или фармакокинетики, при биологических и фармакологических испытаниях в качестве инструментов, в качестве лекарственного средства, в частности, в случае соединений, включающих дейтерий. В рамках настоящего изобретения приводятся нижеследующие определения: в случае (C1-C6) цифровые индексы определяют возможное число атомов углерода, присутствующих в группе, которую определяют. Так, в качестве примера, (C1-C6)алкил означает группу, такую как определенная выше, которая может иметь от 1 до 6 атомов углерода; термин "алкил" означает насыщенную, линейную или разветвленную алифатическую группу; например линейная или разветвленная углеродная цепь с 1-6 атомами углерода, в частности метил, этил,пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил; когда алкильная группа замещена одним или несколькими атомами галогена или одной или несколькими группами, такими как указанные в определениях, эти заместители могут находиться у одного и того же атома углерода и/или у разных атомов углерода; термин "алкинильная группа" означает линейную или разветвленную, моно- или полиненасыщенную алифатическую группу, включающую, например, одну или две ацетиленовые связи. Например, (С 2C6)алкинильная группа может представлять собой этинил, пропинил и т.д.; термин "алкенильная группа" означает линейную или разветвленную, моно- или полиненасыщенную алифатическую группу, включающую, например, одну или две этиленовые связи. Например, (C2C6)алкенильная группа может представлять собой этенил, пропенил, бутенил и т.д.; термин "алкокси" и "алкилокси" означает -O-алкил с линейной или разветвленной насыщенной алифатической цепью. Так, в качестве примера, (C1-C6)алкокси представляет собой -O-(С 1-C6)алкильную группу, причем (C1-C6)алкильная группа имеет указанное выше значение; атом галогена означает фтор, хлор, бром или йод; термин "гетероциклоалкил" означает насыщенный, необязательно замещенный, цикл, включающий от 3 до 8 атомов и содержащий по меньшей мере один гетероатом, такой как азот, сера или кислород, или несколько, одинаковых или отличающихся друг от друга, атомов. Например, гетероциклоалкил может представлять собой моноциклический гетероциклоалкил, такой как азетидин, пирролидин, пиперидин,тетрагидропиран, морфолин, пиперазин, азепин и т.д.; термин "циклоалкил" означает углеродный цикл, включающий предпочтительно от 3 до 8 атомов углерода, причем указанный цикл является насыщенным, необязательно замещенным. В качестве примера можно назвать циклопропил, метилциклопропил, циклобутил, циклопентил, циклогексил; термин "арил" означает циклическую ароматическую группу, включающую от 6 до 10 атомов углерода. В качестве примеров арильных групп можно назвать фенил или нафтил; термин "арилалкильная группа": арильная группа, такая как определенный выше, замещенная по меньшей мере одной алкильной группой, такой как определенная выше. Преимущественно речь идет о алкиленарильных радикалах. Можно назвать, например, бензил, т.е. радикал -CH2-Ph; термин "гетероарил" означает ароматическую систему, включающую от одного до нескольких гетероатомов, таких как атомы азота, кислорода или серы, и которая может быть моноциклической или по- 11021765 лициклической, т.е. включающей от 2 до 5 циклов. Когда система является полициклической, по меньшей мере один из циклов представляет собой ароматический цикл. Атомы азота могут быть в форме Nоксидов. В качестве примеров моноциклических гетероарильных групп можно назвать моноциклические гетероарилы, такие как тиазол, тиадиазол, тиофен, имидазол, триазол, тетразол, пиридин, фуран, оксазол,изоксазол, оксадиазол, пиррол, пиразол, пиримидин, пиридазин. В качестве примеров полициклических гетероарильных групп можно назвать бициклические гетероарилы, такие как индол, бензофуран, бензимидазол, бензотиофен, бензотриазол, бензотиазол, бензоксазол, хинолин, изохинолин, индазол, хиназолин, фталазин, хиноксалин, нафтиридин, 2,3-дигидро-1 Ниндол, 2,3-дигидробензофуран, 2,3-дигидроинден, тетрагидрохинолин, тетрагидроизохинолин, тетрагидроизохиназолин; термин "сульфонамидная группа" означает группу, отвечающую формуле SO2-N-алкил или SO2-Nциклоалкил, где алкил и циклоалкил имеют указанные выше значения; трифторметилтиогруппа определяется формулой -S-CF3; термины "феноксигруппа" и "бензилоксигруппа" означают соответственно группу C6H5-O- и C6H5CH2-O-, где группа С 6 Н 5 также обозначается аббревиатурой Ph. Среди соединений, являющихся объектами настоящего изобретения, можно назвать группу соединений формулы (I), в которой R1 означает арильную группу, в особенности фенил, или гетероарильную группу, в особенности пиридильную группу, причем все другие заместители и индексы являются такими,как определенные в случае приведенной выше общей формулы (I). В следующем ниже контексте под термином "удаляемая группа" понимают группу, которая может быть легко замещена, с удалением электронной пары, за счет разрыва гетеролитической связи. Эта группа также может быть легко заменена другой группой, например, во время реакции замещения. Такими удаляемыми группами являются, например, галогены, или активированная гидроксильная группа, такая как мезилат, тозилат, трифлат и т.д. Примеры удаляемых групп, а также ссылки на их получение, приводятся в руководстве J. March "Advanced Organic Chemistry", третье издание, Wiley Interscience, с. 310-316. Под термином "защитная группа", PG, понимают группу, позволяющую препятствовать реакционной способности группы или положения во время химической реакции, которая может его затрагивать, и которая регенерирует функцию после расщепления согласно способам, известным специалисту в данной области. Под временной защитной группой аминов или спиртов понимают защитные группы, такие как группы, описанные в руководстве T.W. Greene и P.G.M. Wuts "Protective Groups in Organic Synthesis",изд. Willey Intersciences, 1999, и в руководстве P.J. Kocienski "Protecting Groups", изд. Georg Thieme, 1994. Можно назвать, например, временные защитные группы аминов: бензильные, карбаматные (такие как трет-бутилоксикарбонил, расщепляющийся в кислой среде, бензилоксикарбонил, расщепляющийся путем гидрогенолиза); временные защитные группы карбоновых кислот: сложные алкиловые эфиры (такие как метиловый или этиловый, трет-бутиловый, гидролизующиеся в основной или кислой среде) и подвергающиеся гидрогенолизу бензиловые эфиры; временные защитные группы спиртов или фенолов,такие как тетрагидропираниловый, метилоксиметиловый или метилэтоксиметиловый, трет-бутиловый и бензиловый простые эфиры; временные защитные группы карбонилированных производных, такие как линейные или циклические ацетали, как, например, 1,3-диоксан-2-ил или 1,3-диоксолан-2-ил; и ссылаться на хорошо известные общие способы, описанные в вышеприведенном руководстве "Protective Groups". В зависимости от случаев, специалист в данной области в состоянии выбирать соответствующие защитные группы. На нижеследующих общих схемах синтеза, исходные соединения и реагенты, когда способ их получения не описывается, являются коммерчески доступными или описанными в литературе, или же они могут быть получены в соответствии с описанными или известными специалисту в данной области способами. Соединения формулы (I) могут включать группы-предшественники других функций, которые генерируются в дальнейшем за одну или несколько других стадий. Соединения согласно настоящему изобретению могут быть получены в соответствии с нижеследующими схемами 1-7. Эти пути синтеза служат только в качестве пояснения и ни в коем случае не являются ограничивающими объема охраны изобретения. Специалист в данной области может без затруднений адаптироваться к нижеприводимой инструкции в отношении получения соединений формулы (I), в случае которых A, R1, R2, n, p и необязательно R3, Ra, Rb и Rc определены в общей формуле (I). Он в состоянии выбирать, на основании его знаний и литературы, соответствующие защитные группы, позволяющие осуществлять введение всех групп или функций, описанных в настоящем изобретении. Для наглядности, выбирают n и p=1 и положение R2 такое, как указанное на схемах. Соединения, отвечающие формуле (Ia), в которых A, R1 и R2 имеют указанные в случае общей формулы (I) значения, могут быть получены согласно схеме 1. Соединения формулы (IV) получают по реакции восстановительного аминирования путем введения во взаимодействие соединения формулы (II), в которой R2 имеет указанное в случае формулы (I) значение и R' означает (C1-C6)алкильную группу, с соединением формулы (III), в котором А имеет указанное в случае формулы (I) значение, в кислой среде и в присутствии восстановителя, такого как триацетоксиборгидрид натрия. Таким образом полученные соединения формулы (IV) затем ацилируют, в соответствии с хорошо известными специалисту в данной области способами, при использовании алкилхлорформиата или арилхлорформиата, получая соединение формулы (V), в котором R" означает (C1C6)алкильную группу или замещенный арил. Реакция гидролиза в щелочной среде позволяет получать соединения формулы (VI), которые за счет реакции связывания с соединением формулы (VII), в которомR1 имеет указанное в случае соединений общей формулы (I) значение, приводят к соединениям формулы(VIII). Реакция внутримолекулярной циклизации в щелочной среде позволяет получать производные хиназолиндиона формулы (Ia). Схема 2 Альтернативно, соединения, отвечающие формуле (Ia), в которых A, R1 и R2 имеют указанные в случае общей формулы (I) значения, могут быть получены согласно схеме 2. Реакция восстановительного аминирования между соединением формулы (IX), в котором R1, R2 имеют указанные в случае общей формулы (I) значения, и соединением формулы (III), в котором А имеет указанное в случае общей формулы (I) значение, в кислой среде и в присутствии восстановителя, такого как триацетоксиборгидрид натрия, приводит к соединениям формулы (X). Соединения формулы (X) затем ацилируют при использовании алкилхлорформиата или арилхлорформиата, получая соединения формулы (VIII), где R" означает(C1-C6)алкильную группу или замещенную арильную группу, которые за счет реакции внутримолекулярной циклизации в щелочной среде приводят, как указано выше, к производным хиназолиндиона формулы (Ia). Соединения формулы (Ib), в которых R2 означает -ORa, где Ra имеет указанное в случае соединений общей формулы (I) значение, могут быть получены согласно схеме 3. Соединения формулы (XII) получают по реакции ароматического нуклеофильного замещения, используя соединение формулы (XI), в котором R' означает (C1-C6)алкильную группу, и бензиловый спирт,в присутствии основания. Восстановление нитрогруппы в соединениях формулы (XII) приводит к соответствующим анилиновым производным (XIII). Реакция восстановительного аминирования при использовании соединения формулы (III), в котором А имеет указанное в случае общей формулы (I) значение, в кислой среде и в присутствии восстановителя, такого как триацетоксиборгидрид натрия, приводит к соединениям формулы (XIV), которые за счет гидролиза в щелочной среде приводят к соединениям формулы (XV). Последовательно осуществляемые реакция ацилирования при использовании соединения формулы (VII), приводящая к получению соединений формулы (XVI), затем вторая реакция ацилирования при использовании алкилхлорформиата или арилхлорформиата приводят к получению соединений формулы (XVII), и наконец, реакция внутримолекулярной циклизации в присутствии основания приводит к соединениям формулы (XVIII). Соединения формулы (XIX), получаемые путем удаления защиты,бензилоксигруппы, от соединений формулы (XVIII), затем подвергают, например, реакции алкилирования при использовании алкилирующего агента типа Ra-X, в котором Ra имеет указанное в случае соединений общей формулы (I) значение и X означает удаляемую группу (такую как, например, атом галогена), в присутствии основания, такого как карбонат цезия (Cs2CO3), или еще реакции Mitsunobu (Synthesis,1981, 1) при использовании спирта типа Ra-OH, где Ra имеет указанное в случае соединений общей формулы (I) значение, получая соединения формулы (Ib). Соединения формулы (Ic), в которых R2 означает -NHRa, где Ra, А и R1 имеют указанные в случае соединения общей формулы (I) значение, могут быть получены согласно схеме 4. Реакция нуклеофильного замещения между соединением формулы (XX) и соединением формулы(XXI) приводит к соединениям формулы (XXII), которые затем превращают в соединения формулы(XXV) путем последовательности реакций, эквивалентных реакциям, описанным на предыдущих схемах,а именно (i) первая реакция ацилирования соединений формулы (XXII) при использовании амина формулы (VII), где R1 имеет указанное в случае общей формулы (I) значение, приводящая к получению соединений формулы (XXIII), (ii) вторая реакция ацилирования при использовании алкилхлорформиата или арилхлорформиата с образованием соединений формулы (XXIV) и затем (iii) реакция циклизации,приводящая к образованию указанных соединений формулы (XXV). Соединения формулы (XXVI), получаемые путем восстановления нитрогруппы соединений формулы (XXV) до амина, затем подвергают реакции алкилирования при использовании алкилирующего агента типа Ra-X, в котором Ra имеет указанное в случае соединений общей формулы (I) значение и X означает удаляемую группу (такую как,например, атом галогена), в присутствии основания, такого как карбонат цезия (Cs2CO3), получая соединения формулы (Ic). Соединения формул (Id), (Ie), (If), (Ig) и (Ih), в которых A, R1, Rb, Rc имеют указанные в случае соединения общей формулы (I) значения, могут быть получены согласно схеме 5. Их получают из соединений формулы (XXVII), в которых R2 означает атом галогена, предпочтительно атом брома или йода. Соединения формулы (XXVIII) получают из соединений формулы (XXVII) по реакции типа реакции Стилла (см., например, Chemical Review, 107, 133-173 (2007. Восстановление или алкилирование карбонильной группы позволяет получать соединения формулы (Id) и (Ie) соответственно. Соединения формулы (If) и формулы (Ig) получают из соединений формулы (XXVII) по реакции типа реакции Бухвальда и типа реакции Сузуки (см., например, Chemical Review, 107, 133-173 (2007 соответственно. Соединения формулы (XXIX), получаемые путем реакции цианирования (см., например, ChemicalReview, 107, 133-173 (2007 соединений формулы (XXVII), приводят к соединениям формулы (XXX) за счет реакции восстановления. Наконец, реакция ацилирования соединений формулы (XXX) приводит к соединениям формулы (Ih). Соединения формулы (Ii), формулы (Ij), в которых А и R1 имеют указанные в случае общей формулы (I) значения и R2 являются такими, как указанные на схеме 6, могут быть получены согласно схеме 6. Соединения формулы (XXXI), получаемые из соединений формулы (XXVII) по реакции Стилла,приводят к альдегидам формулы (XXXII) за счет реакции озонолиза. Соединения формулы (XXXIII) получают по реакции восстановления указанных альдегидов формулы (XXXIII), используя, например, гидриды бора в качестве восстановителя. Соединения формулы (Ii) получают из соединений формулы(XXXIII) путем реакции фторирования, используя, например, DAST в качестве фторирующего агента. Соединения формулы (XXXIV) получают из соединений формулы (XXXII) по реакции типа реакции Виттига. Наконец, соединения формулы (XXXV), получаемые из соединений формулы (XXXI) по реакции гидроборирования/окисления, превращают в соединения формулы (Ij) путем реакции фторирования. Соединения формул (Ik) и (Im), в которых А означает группу SO или SO2, соответственно, могут быть получены согласно схеме 7. Для наглядности, выбирают группу R2 общей формулы (I), как указано на схеме 7. Окисление соединений формулы (XXXVI) в присутствии перйодата калия приводит к сульфоксидным производным формулы (XXXVII). Бензилоксигруппу удаляют, например, путем реакции гидрогенолиза, получая соединения формулы (XXXVIII), которые за счет реакции алкилирования при использовании алкилирующего агента типа Ra-X, в котором Ra имеет указанное в случае соединения общей формулы (I) значение и X означает удаляемую группу (такую как, например, атом галогена), в присутствии основания, такого как карбонат цезия (Cs2CO3), приводят к соединениям формулы (Ik). Аналогичным образом, сульфоновые производные формулы (Im) могут быть получены согласно той же самой схеме синтеза за исключением стадии окисления, которая может быть осуществлена при использовании Oxone-, получая соединения формулы (XXXIX). Номера приводимых в качестве примеров соединений относятся к указанным в нижеприводимой табл. 1, в которой поясняются химические структуры и физические свойства некоторых соединений согласно изобретению. Программным обеспечением, используемым для номенклатуры соединений, указанных согласно настоящему изобретению, является ACD/Name (www.acdlabs.com). Примеры Согласно следующим методикам и примерам описывается получение некоторых соединений согласно изобретению. Эти методики и примеры не являются ограничивающими объема охраны изобретения и предназначены только для пояснения настоящего изобретения. Специалист в данной области может адаптироваться без затруднений к нижеприводимой технической инструкции в отношении соединений общей формулы (I). Он также в состоянии выбирать, на основании его знаний и литературы, соответствующие защитные группы, позволяющие осуществлять введение всех групп или функций, описываемых в настоящем изобретении. В приводимых ниже методиках и примерах: масс-спектры снимают на квадрупольном спектрометре типа Platform LCZ (WATERS) или типа ZQ 4000 (WATERS) с использованием метода ионизации электронным распылением с образованием положительных ионов; спектры ЯМР (ядерный магнитный резонанс) снимают на спектрометре с преобразованием Фурьеs = синглет (с),d = дублет (д),m = мультиплет (м),br = уширенный сигнал (уш.),t = триплет (т),q = квадруплет (кв.),DMSO-d6 = дейтерированный диметилсульфоксид (ДМСО-d6),CDCl3 = дейтерированный хлороформ; смеси растворителей определяют количественно в объемных соотношениях; ЯМР-спектры и масс-спектры подтверждают структуры соединений, получаемых согласно приводимым ниже примерам. В следующих примерах используют следующие аббревиатуры: В течение ночи при комнатной температуре перемешивают смесь 5 г 2-амино-5-бромбензойной кислоты, 9,27 г тетрагидро-4H-пиран-4-она, 32 г Na2SO4 в 50 мл уксусной кислоты. Реакционную смесь фильтруют. Добавляют 9,27 г тетрагидро-4 Н-пиран-4-она и 32 г Na2SO4 и перемешивают в течение ночи при комнатной температуре. Фильтруют и добавляют 9,81 г NaBH(OAc)3. Оставляют взаимодействовать в течение 2 ч 00 мин при комнатной температуре. Реакционную среду выпаривают при пониженном давлении и остаток обрабатывают этилацетатом. Промывают 1 н. водным раствором HCl. Органическую фазу сушат над Na2SO4, фильтруют, выпаривают при пониженном давлении, получая 3,35 г ожидаемого продукта. Стадия 1.2. 5-Бром-N-(3,4-диметоксибензил)-2-(тетрагидро-2H-пиран-4-иламино)бензамид. В течение 2 суток при комнатной температуре перемешивают смесь 1 г полученного на стадии 1.1 соединения, 0,646 г вератриламина, 1,152 г DIEA и 1,69 г HBTU в 50 мл ДМФА. Реакционную среду выпаривают при пониженном давлении. Путем хроматографирования остатка на силикагеле, элюируя смесью дихлорметан/этилацетат от (100/0, об./об.) вплоть до (80/20, об./об.), получают 1,2 г твердого вещества, которое используют без очистки на следующей стадии. Стадия 1.3. 6-Бром-3-(3,4-диметоксибензил)-1-(тетрагидро-2H-пиран-4-ил)хиназолин-2,4(1H,3H)-дион. В течение ночи перемешивают смесь 1,67 г IBCF, 1,1 г полученного на стадии 1.2 соединения, 3,23 г NaOH и 0,83 г тетрабутиламмонийгемисульфата в 150 мл 1,2-дихлорэтана. Реакционную смесь фильтруют и выпаривают при пониженном давлении. Путем хроматографирования остатка на силикагеле,элюируя смесью дихлорметан/этилацетат от (100/0, об./об.) вплоть до (80/20, об./об.), получают 0,649 г ожидаемого продукта. Пример 2: соединение 34. Синтез 3-(3,4-диметоксибензил)-6-йод-1-(тетрагидро-2H-пиран-4-ил)хиназолин-2,4(1H,3H)-диона. В течение ночи при комнатной температуре перемешивают смесь 14,22 г 5-йод-2-(тетрагидро-2Hпиран-4-иламино)бензойной кислоты, 18,4 г HBTU, 21,28 г DIEA и 9,18 г вератриламина в 200 мл ДМФА. Реакционную среду выпаривают при пониженном давлении. Остаток обрабатывают с помощью 3000 мл этилацетата. Промывают 0,5 н. водным раствором HCl, водным насыщенным раствором NaHCO3,затем водным насыщенным раствором NaCl. Органическую фазу сушат над MgSO4, фильтруют, выпаривают при пониженном давлении, получая 18 г ожидаемого продукта. Стадия 2.2. 3-(3,4-Диметоксибензил)-6-йод-1-(тетрагидро-2H-пиран-4-ил)хиназолин-2,4(1H,3H)-дион. 2,9 г NaOH добавляют к раствору 18 г полученного на стадии 2.1 соединения в 200 мл 1,2 дихлорэтана и оставляют взаимодействовать в течение 30 мин при комнатной температуре. Добавляют 1,5 г NaH и оставляют взаимодействовать в течение 30 мин при комнатной температуре. Добавляют 51,1 г IBCF и реакционную смесь нагревают в течение 4 ч 00 мин при температуре 80C. Выпаривают при пониженном давлении и остаток обрабатывают с помощью 200 мл ДМФА. Добавляют 8,7 г NaOH и 12,3 г тетрабутиламмонийгемисульфата. Нагревают в течение 4 ч 00 мин при температуре 80C, затем выдерживают в течение ночи при комнатной температуре. Путем хроматографирования остатка на силикагеле,элюируя смесью дихлорметан/этилацетат от (100/0, об./об.) вплоть до (80/20, об./об.), получают 9 г ожидаемого продукта. Пример 3: соединение 11. Синтез В течение 5 мин при температуре 130C под действием микроволнового излучения облучают смесь 0,235 г 2-амино-5-(бензилокси)-N-(3,4-диметоксибензил)бензамида, 0,090 г тетрагидро-4 Н-тиопиран-4 она, 0,78 г триацетоксиборгидрида натрия в 0,5 мл уксусной кислоты. Добавляют 1 н. HCl и экстрагируют этилацетатом. Органическую фазу сушат над MgSO4, фильтруют, фильтрат выпаривают при пониженном давлении. Путем хроматографирования остатка на силикагеле, элюируя смесью гептан/этилацетат от В течение 30 мин при комнатной температуре перемешивают смесь 2,5 г полученного на стадии 3.1 соединения, 6,7 г NaOH в 100 мл 1,2-дихлорэтана. Затем добавляют 2,77 г IBCF и перемешивают в течение 2 ч 00 мин при комнатной температуре. Добавляют такие же количества NaOH и IBCF и перемешивают в течение ночи при комнатной температуре. Не завершая реакцию, добавляют 6,7 г NaOH, 1,39 гIBCF и 0,05 г тетрабутиламмонийсульфата, затем перемешивают в течение 3 суток при комнатной температуре. Фильтруют, фильтрат выпаривают при пониженном давлении. Путем хроматографирования остатка на силикагеле, элюируя смесью дихлорметан/этилацетат от (100/0, об./об.) вплоть до (80/20,об./об.), получают 2,07 г ожидаемого продукта. Стадия 3.3. 3-(3,4-Диметоксибензил)-6-гидрокси-1-(тетрагидро-2H-тиопиран-4-ил)хиназолин-2,4(1H,3H)-дион. В течение 2 мин при температуре 180C под действием микроволнового излучения облучают смесь 0,200 г полученного на стадии 3.2 соединения, 1,22 г муравьиной кислоты. Реакционную смесь обрабатывают этилацетатом, затем выпаривают при пониженном давлении. Путем хроматографирования остатка на силикагеле, элюируя смесью CH2Cl2/MeOH от (100/0, об./об.) вплоть до (97/3, об./об.), получают ожидаемый продукт. Стадия 3.4. В течение 15 мин при температуре 100C под действием микроволнового излучения облучают смесь 0,16 г полученного на стадии 3.3 соединения, 0,054 г бромацетонитрила и 0,243 г Cs2CO3 в 1 мл ДМФА. Реакционную смесь выпаривают при пониженном давлении. Обрабатывают с помощью дихлорметана, промывают водой, сушат над Na2SO4, фильтруют, фильтрат выпаривают при пониженном давлении. Путем хроматографирования остатка на силикагеле, элюируя смесью этилацетат/дихлорметан от
МПК / Метки
МПК: A61P 29/00, A61P 11/00, A61P 9/00, C07D 409/04, C07D 335/02, A61P 25/00, C07D 405/04, C07D 309/14, C07D 239/96, C07D 405/14, C07D 407/04, A61P 37/00, A61K 31/517
Метки: производные, хиназолиндиона, терапевтические, получение, применения, различные
Код ссылки
<a href="https://eas.patents.su/30-21765-proizvodnye-hinazolindiona-ih-poluchenie-i-ih-razlichnye-terapevticheskie-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Производные хиназолиндиона, их получение и их различные терапевтические применения</a>
Предыдущий патент: Формовочная машина
Следующий патент: Способ и устройство для нанесения покрытия на стеклянную подложку