Соединения в качестве ингибиторов микросомной простагландин-е2-синтазы-1 (mpges-1)
Номер патента: 21433
Опубликовано: 30.06.2015
Авторы: Пелькман Беньямин, Штенкамп Дирк, Кюльцер Раймунд, Припке Хеннинг, Рённ Роберт, Пфау Роланд, Додс Хенри
Формула / Реферат
1. Соединение формулы I
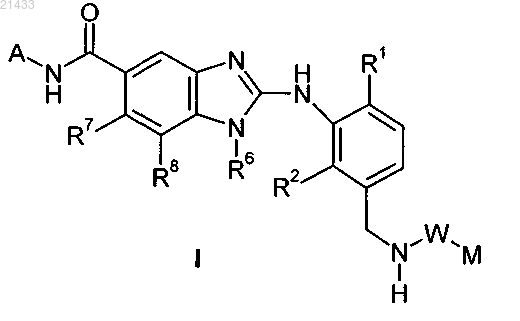
в которой R1 и R2 независимо обозначают галоген, -C1-C3-алкил, где алкильная группа необязательно замещена одним или более атомами фтора;
W обозначает -C(O)-, -C(O)O-, где эти группы присоединены к атому азота фрагмента -NH- через атом углерода;
М обозначает
-C1-C6-алкил, -C3-C7-циклоалкил, -CH2-циклопропил, эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -NH(C1-C2-алкил), -N(C1-C2-алкил)2, -O-C1-C3-алкила, -C1-C5-алкила, -C3-C4-циклоалкила, где в последних трех группах алкильные или циклоалкильные группы необязательно замещены одним или более атомами фтора; или
оксетанил-, тетрагидрофуранил-, тетрагидропиранил-, азетидинил-, пирролидинил-, пиперидинил-, все эти группы необязательно содержат один или более заместителей, выбранных из фтора, -CN, -C1-C3-алкила, где алкильная группа необязательно замещена одним или более атомами фтора; или
фенил-, пиридил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил-, оксазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из галогена, -CN или -C1-C3-алкила, где алкильная группа необязательно дополнительно замещена одним или более атомами фтора;
R8 обозначает -H, галоген, -C1-C3-алкил, где алкильная группа необязательно замещена одним или более атомами фтора;
R6 обозначает -H, -C1-C5-алкил, -C3-C5-циклоалкил-C0-C2-алкил, где алкильные или циклоалкильные фрагменты необязательно замещены одним или более атомами фтора;
R7 обозначает галоген, C1-C5-алкил-O-, C3-C7-циклоалкил-C0-C2-алкил-O-, 4-7-членный гетероциклоалкил-C0-C2-алкил-O-, где в указанном гетероциклоалкиле по меньшей мере один кольцевой атом выбран из группы, включающей N, О или S, и где алкильные, циклоалкильные или гетероциклоалкильные фрагменты необязательно содержат один или более заместителей, выбранных из -F и -O-C1-C3-алкила, где алкильная группа необязательно дополнительно замещена одним или более атомами фтора;
А обозначает C1-C8-алкил-, фенил-, инданил-, нафтил-, 1,2,3,4-тетрагидронафтил-, пиридил-, тиенил-, бензотиенил-, пирролил-, индолил-пиразолил-, индазолил-, тиазолил-, бензотиазолил-, оксазолил-, бензооксазолил-, изоксазолил-, бензизоксазолил-, фенил-C1-C3-алкил-, тиенил-C1-C3-алкил-, пиридил-C1-C3-алкил-, C3-C7-циклоалкил-C0-C3-алкил-, оксетанил-C0-C3-алкил-, тетрагидрофуранил-C0-C3-алкил, тетрагидропиранил-C0-C3-алкил, где в этих группах алкильные, циклоалкильные и гетероциклоалкильные фрагменты необязательно содержат один или более заместителей, выбранных из R9a, и арильные и гетероарильные фрагменты необязательно содержат один или более заместителей, выбранных из R9b;
каждый R9a независимо обозначает -F, -Cl, -C1-C3-алкил, который необязательно содержит один или более заместителей, выбранных из -F, -O-C1-C3-алкила;
каждый R9b независимо обозначает -галоген, -CN; -C1-C3-алкил, который необязательно замещен одним или более атомами фтора;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, в котором R8 обозначает -H или фтор.
3. Соединение по п.1 или 2, в котором R6 обозначает -H, -CH3, циклопропил.
4. Соединение по любому из предыдущих пунктов, в котором R1 и R2 независимо обозначают хлор, фтор, -CH3, -CH2F, -CHF2, -CF3.
5. Соединение по любому из предыдущих пунктов, в котором R7 обозначает фтор, -OCHF2, -OCF3, -OCH2CH2F, -OCH2CHF2, -OCH2CF3, -O-тетрагидрофуран-3-ил, -O-CH2-циклопропил.
6. Соединение по любому из предыдущих пунктов, в котором А обозначает C1-C4-алкил-, C3-C7-циклоалкил-C0-C2-алкил-, тетрагидрофуранилметил-, фенил-C1-C2-алкил-, пиридилметил-, фенил-, инданил-, пиридил-, тиенил-, тиазолил-, бензотиазолил-, где в этих группах алкильные, циклоалкильные или гетероциклоалкильные фрагменты необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CH2F, -CHF2, -CF3, и арильные и гетероарильные фрагменты необязательно замещены -F, -Cl, -Br, -CN, -CH3, -CH2F, -CHF2, -CF3.
7. Соединение по любому из предыдущих пунктов, в котором М обозначает
-C1-C4-алкил, -C3-C5-циклоалкил, обе эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CH2F, -CHF2, -CF3, циклопропила; или
оксетанил-, тетрагидрофуранил-, азетидинил- или пирролидинил-, все эти группы необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CH2F, -CHF2, -CF3; или
фенил-, инданил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3, -CH2F, -CHF2, -CF3.
8. Соединение по любому из предыдущих пунктов формулы Ia
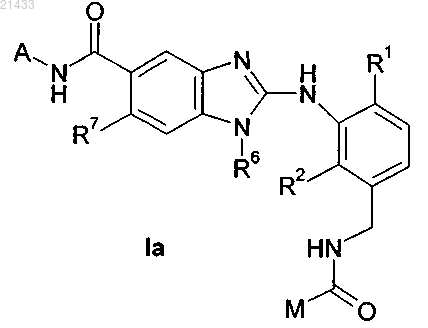
в которой
М обозначает метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, циклопропил, -CH2-циклопропил, циклобутил, циклопентил, все эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CF3; или
выбран из следующих групп:
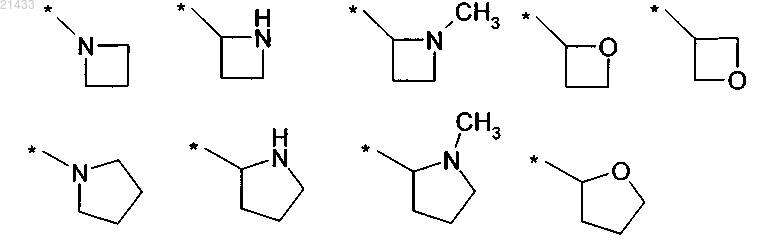
где последние девять групп необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CF3; или
выбран из следующих групп:
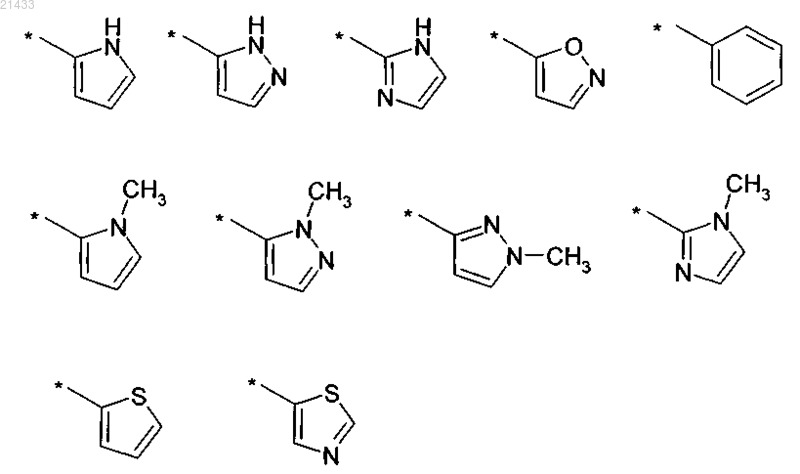
где последние одиннадцать групп необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3, -CF3;
A, R1, R2, R6, R7 имеют значения, определенные в любом из предыдущих пунктов.
9. Соединение по п.8, в котором
А обозначает
метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, где последние семь групп необязательно замещены одним или более атомами фтора; или
циклопропил, циклобутил, циклопентил, циклогексил, где последние четыре группы необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CHF2, -CF3; или
выбран из следующих групп:
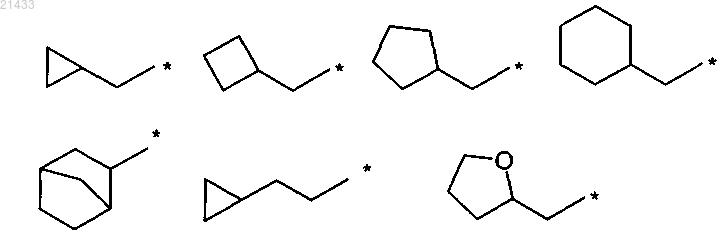
где последние семь групп необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CHF2, -CF3; или
выбран из следующих групп:
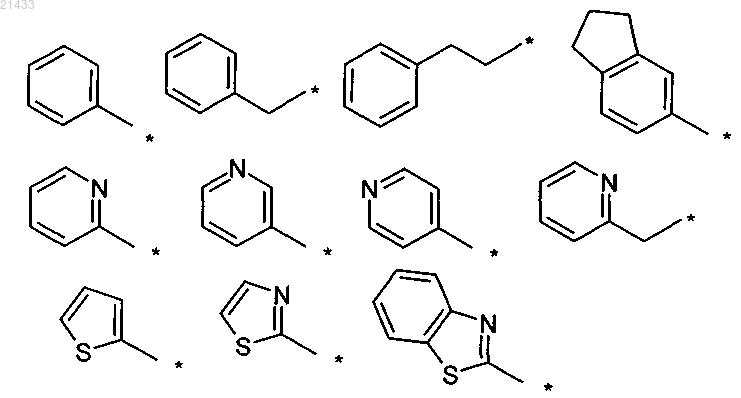
где в последних одиннадцати группах арильные и гетероарильные фрагменты необязательно содержат один или более заместителей, выбранных из -F, -Cl, -Br, -CN, -CH3, -CF3.
10. Соединение по любому из предыдущих пунктов формулы Ia или Ib'
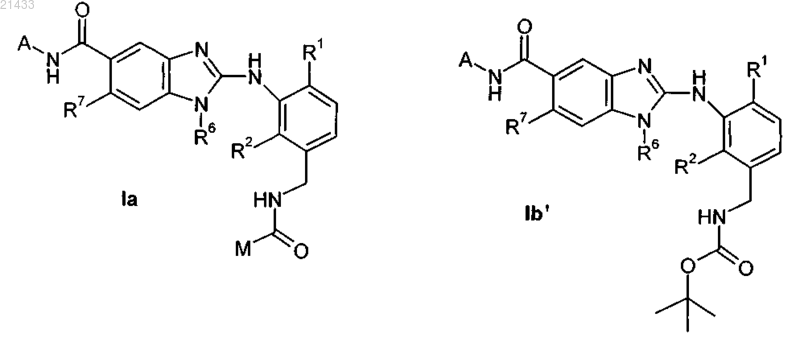
в которой R1 и R2 независимо обозначают -хлор, фтор, -CH3, -CH2F, -CHF2, -CF3;
R6 обозначает -H, -CH3, циклопропил;
R7 обозначает фтор, -OCHF2, -OCF3, -OCH2CH2F, -OCH2CHF2, -OCH2CF3, тетрагидрофуран-3-ил-O-, -O-CH2-циклопропил;
А обозначает
метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, где последние семь групп необязательно замещены одним или более атомами фтора; или
циклопропил, циклобутил, циклопентил, циклогексил, где последние четыре группы необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CHF2, -CF3; или
выбран из следующих групп:

где последние семь групп необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CHF2, -CF3; или
выбран из следующих групп:
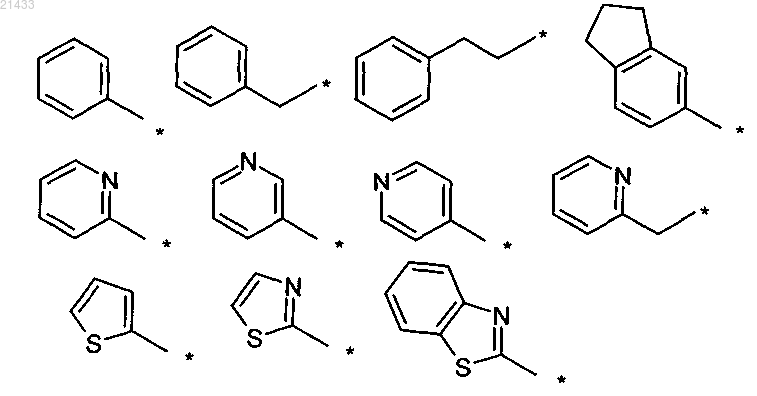
где в последних одиннадцати группах арильные и гетероарильные фрагменты необязательно содержат один или более заместителей, выбранных из -F, -Cl, -Br, -CN, -CH3, -CF3;
М обозначает
метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, циклопропил, -CH2-циклопропил, циклобутил, циклопентил, все эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CF3;
или выбран из следующих групп:
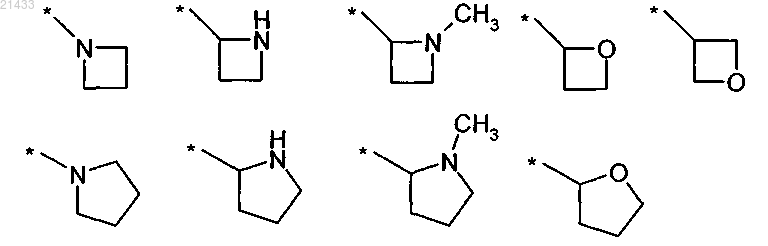
где последние девять групп необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CF3; или
выбран из следующих групп:
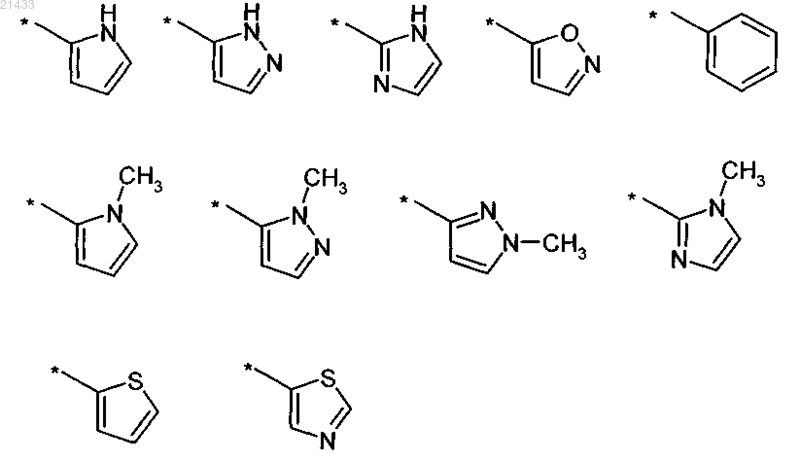
где последние одиннадцать групп необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3, -CF3,
или его фармацевтически приемлемая соль.
11. Соединение по любому из предыдущих пунктов, выбранное из группы, включающей:
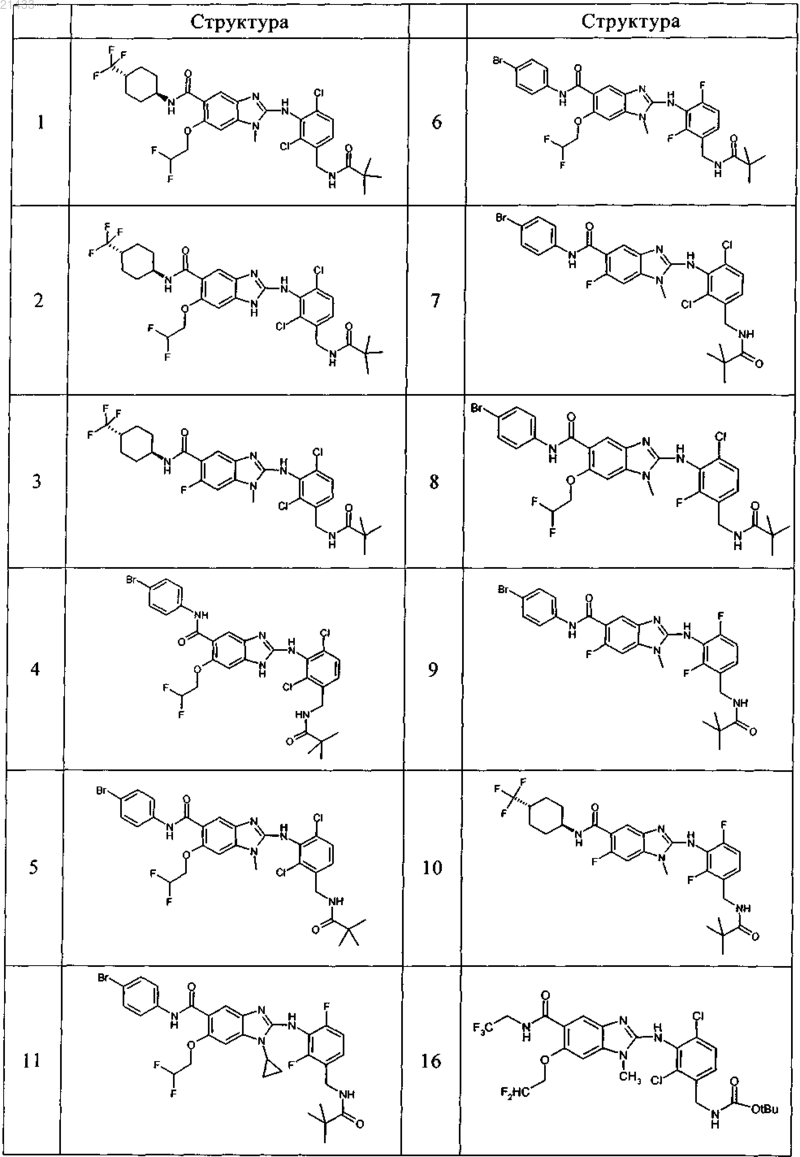
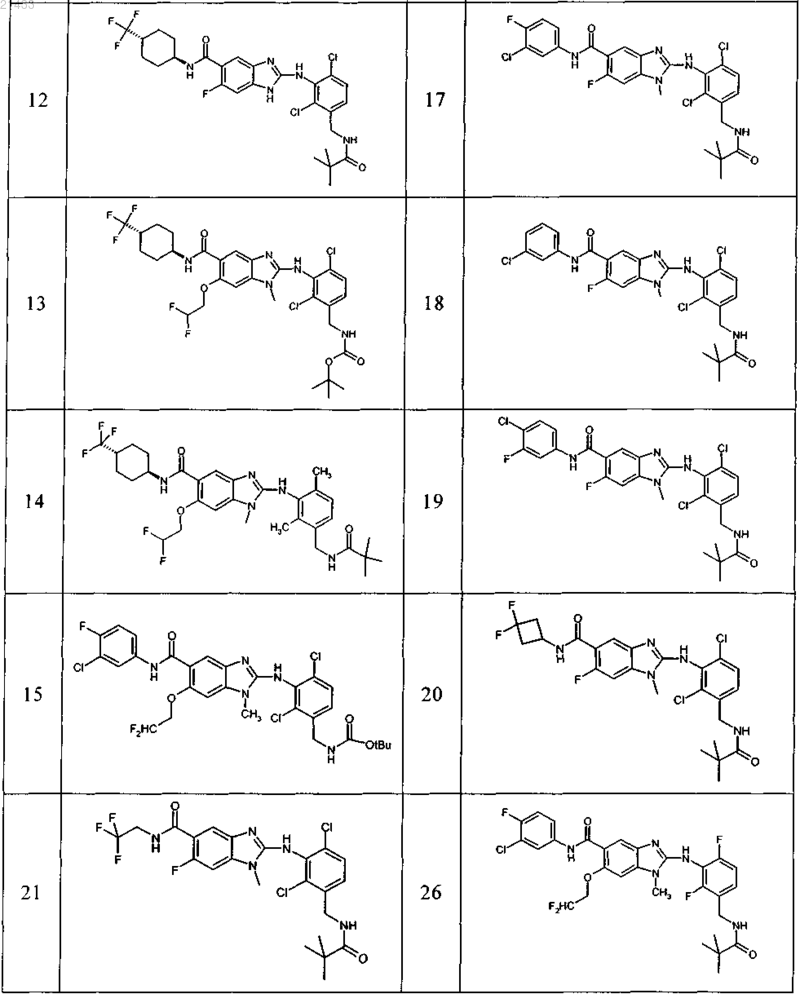
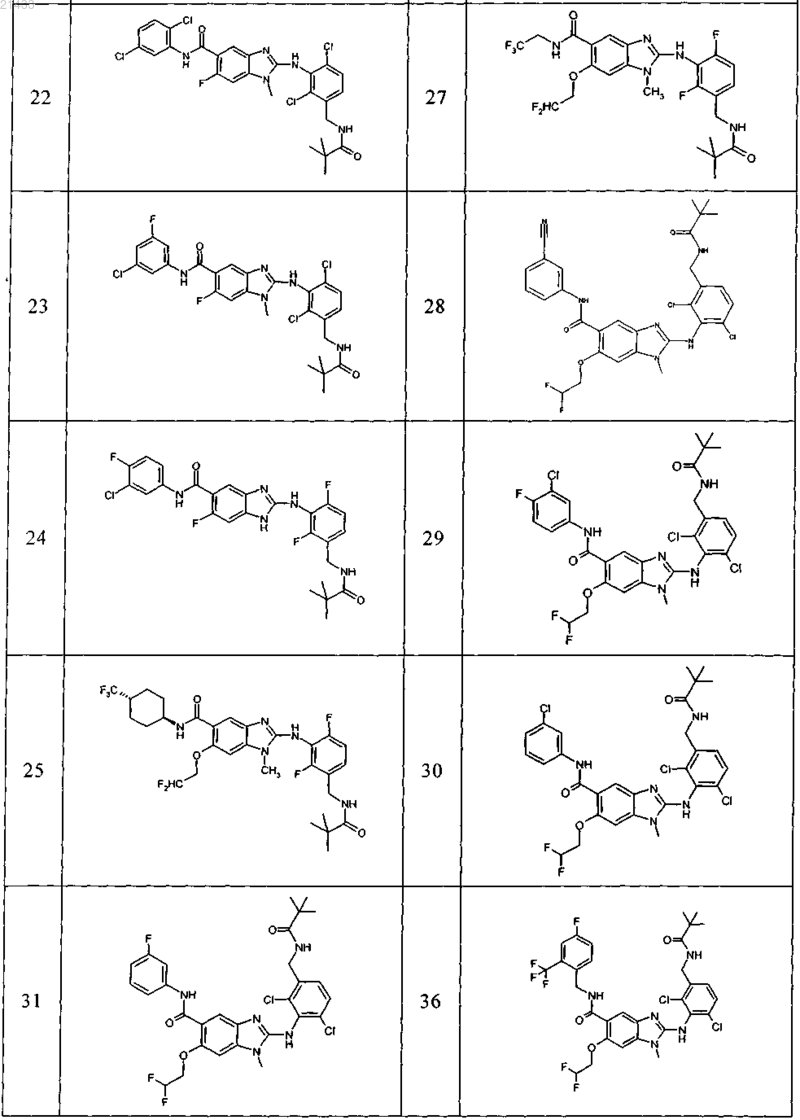
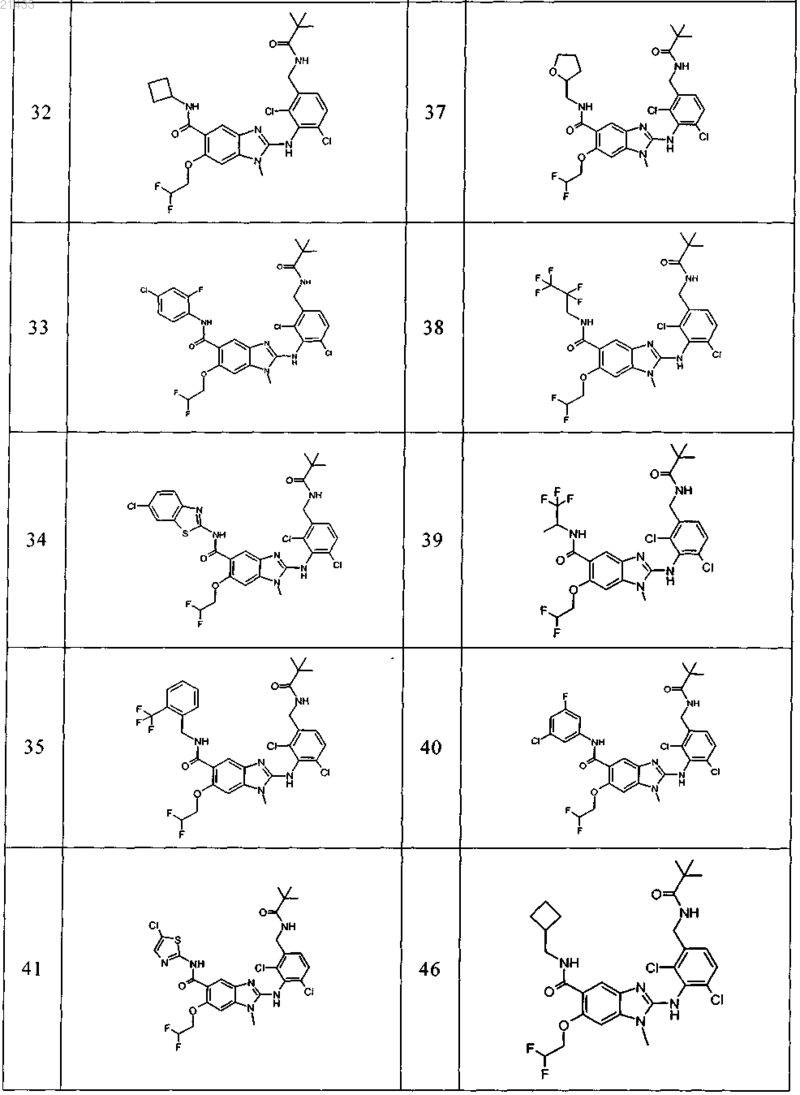
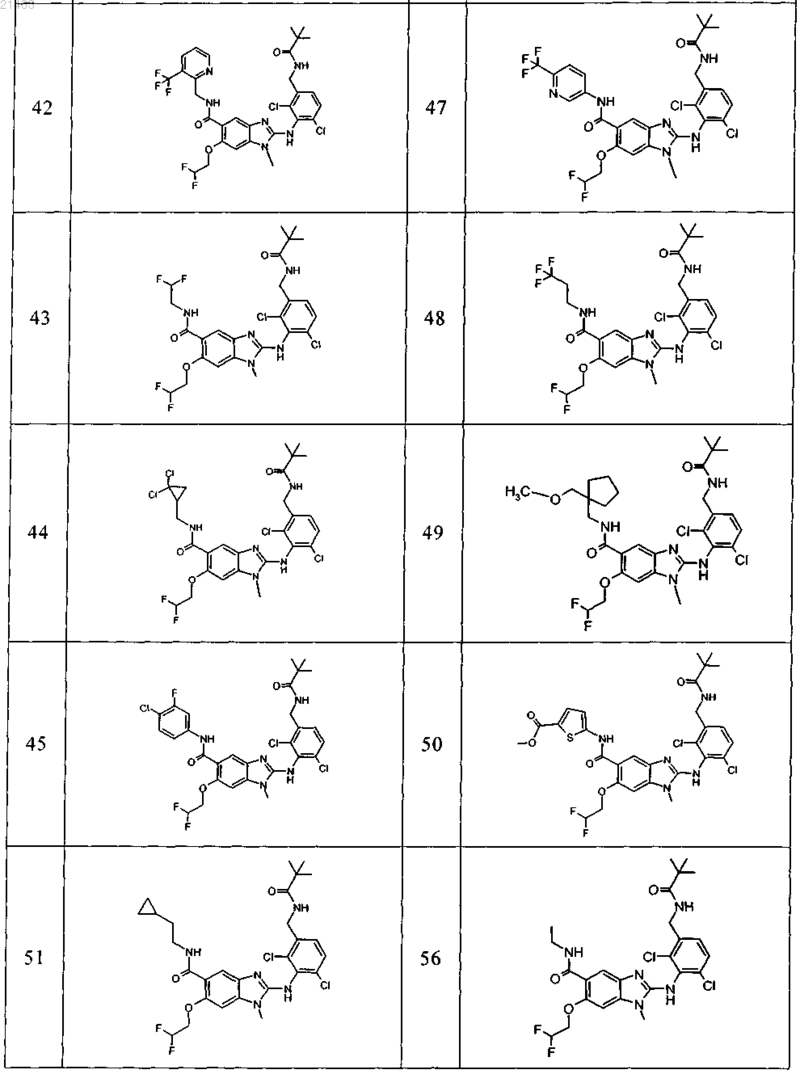
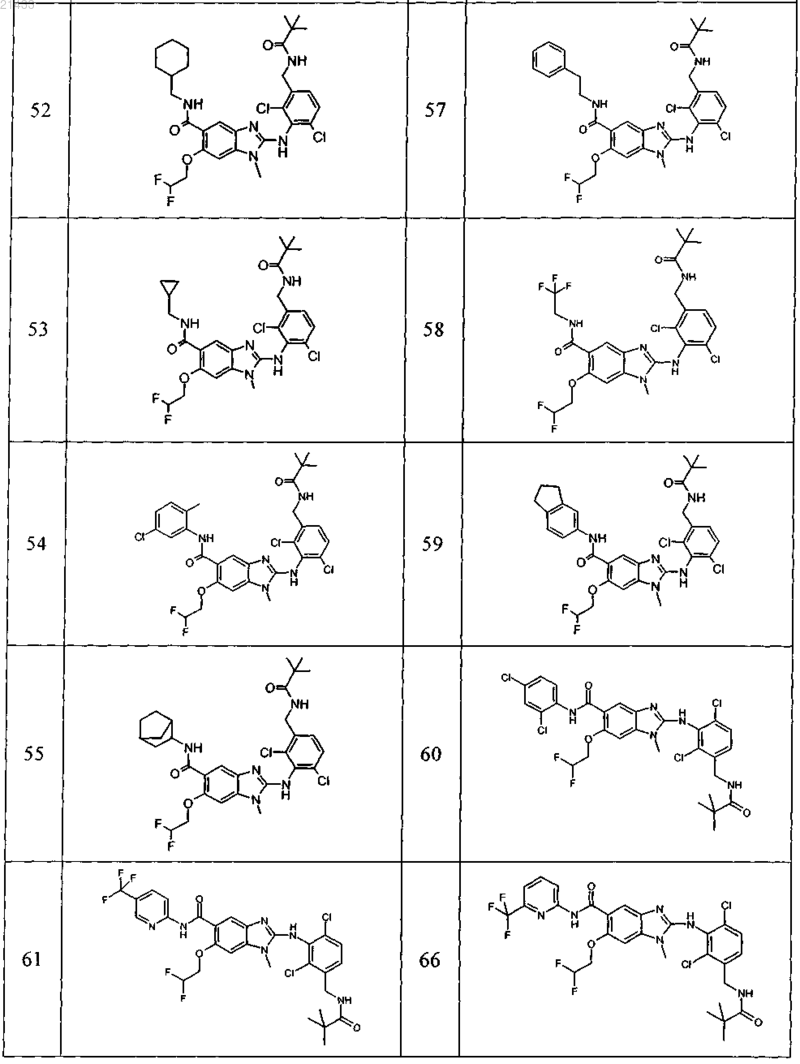
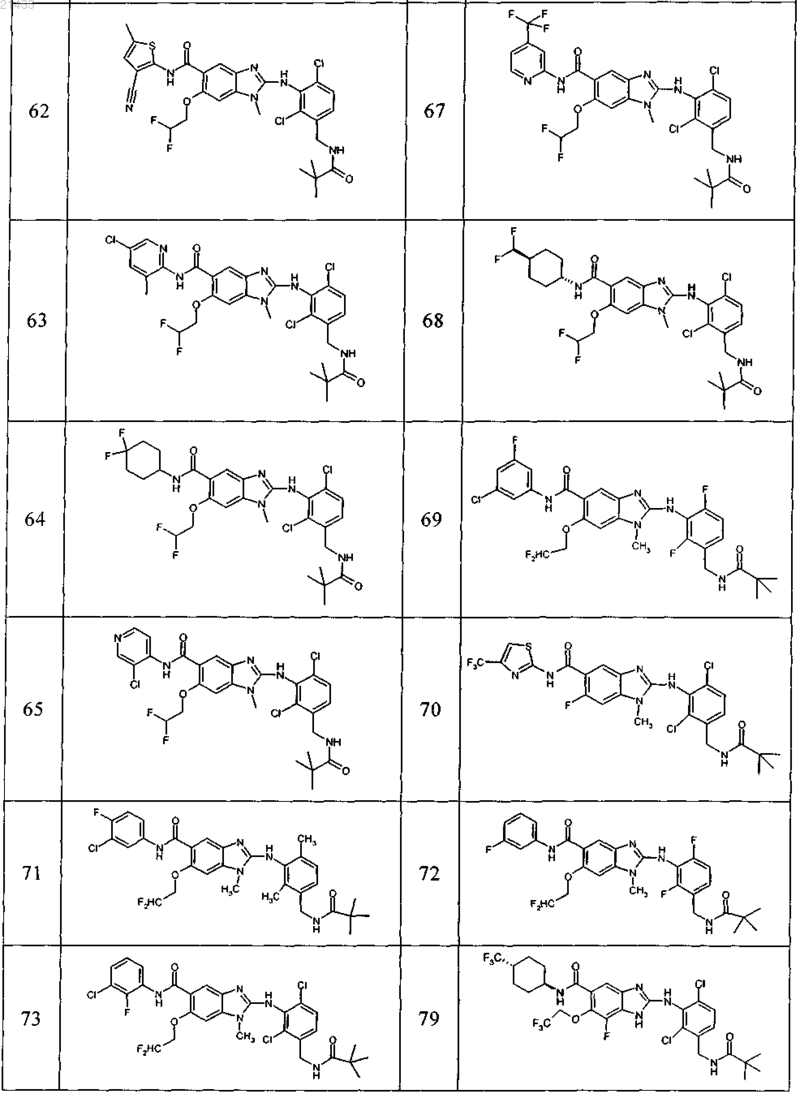
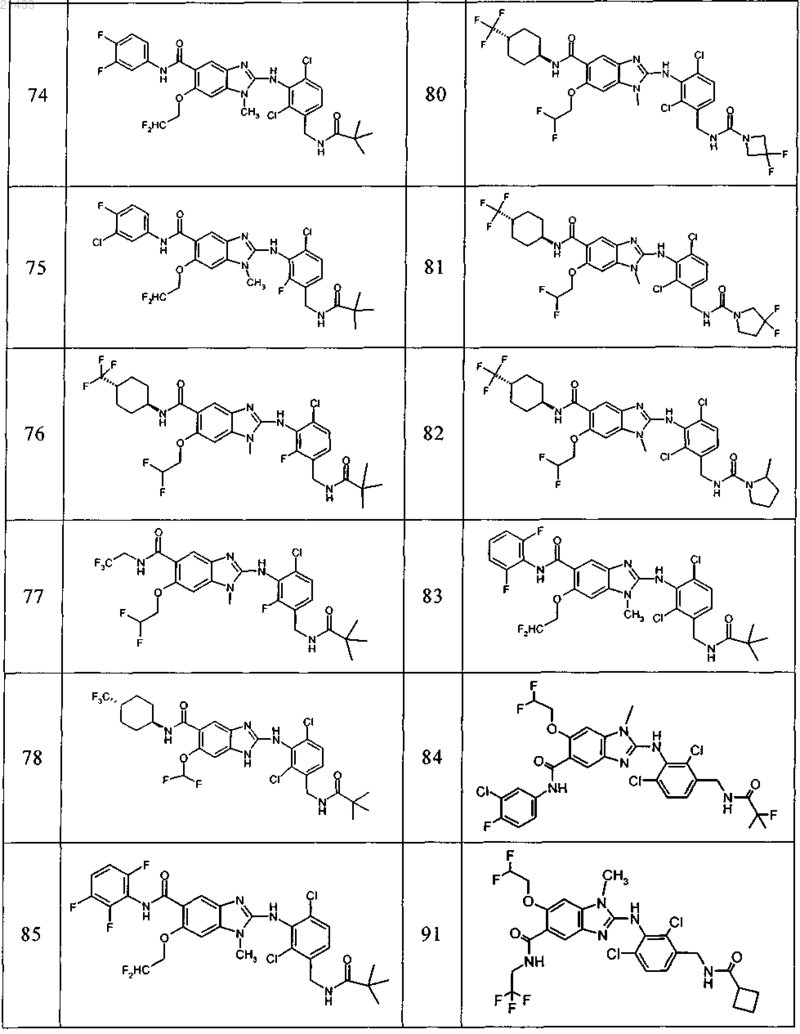
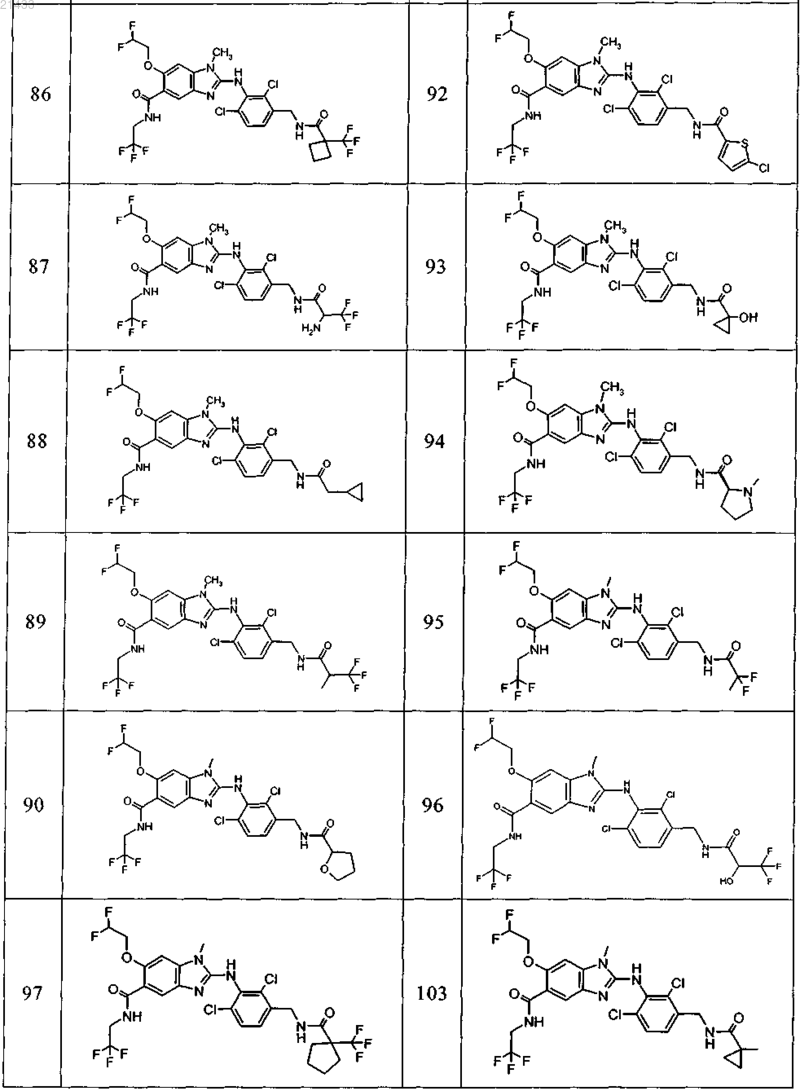
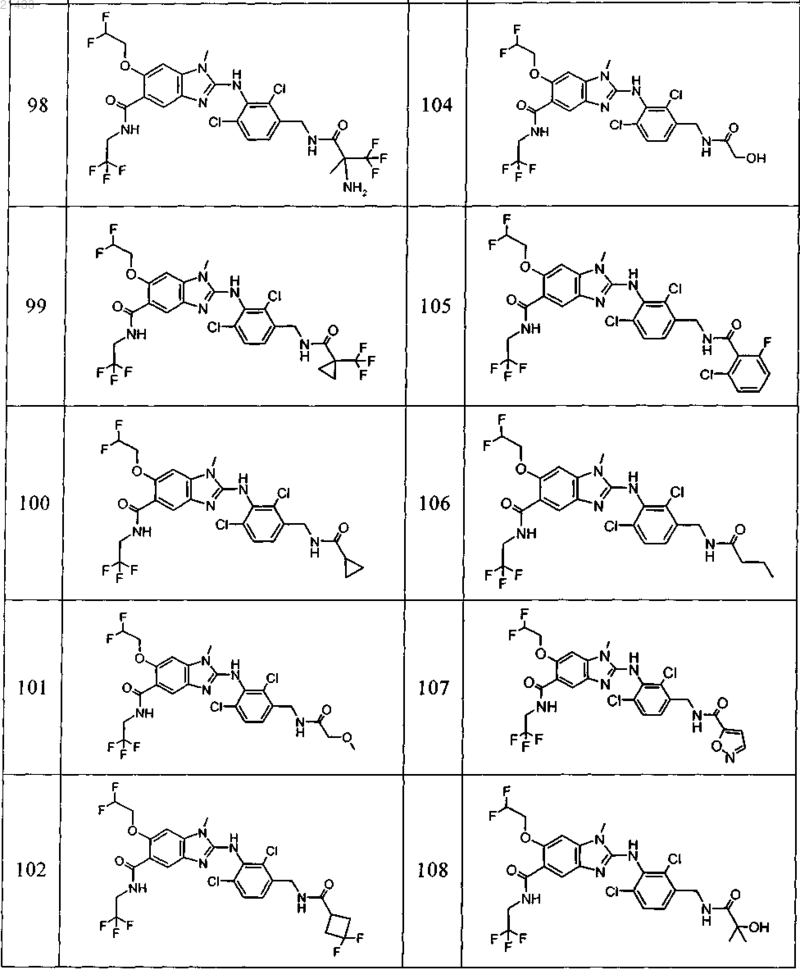
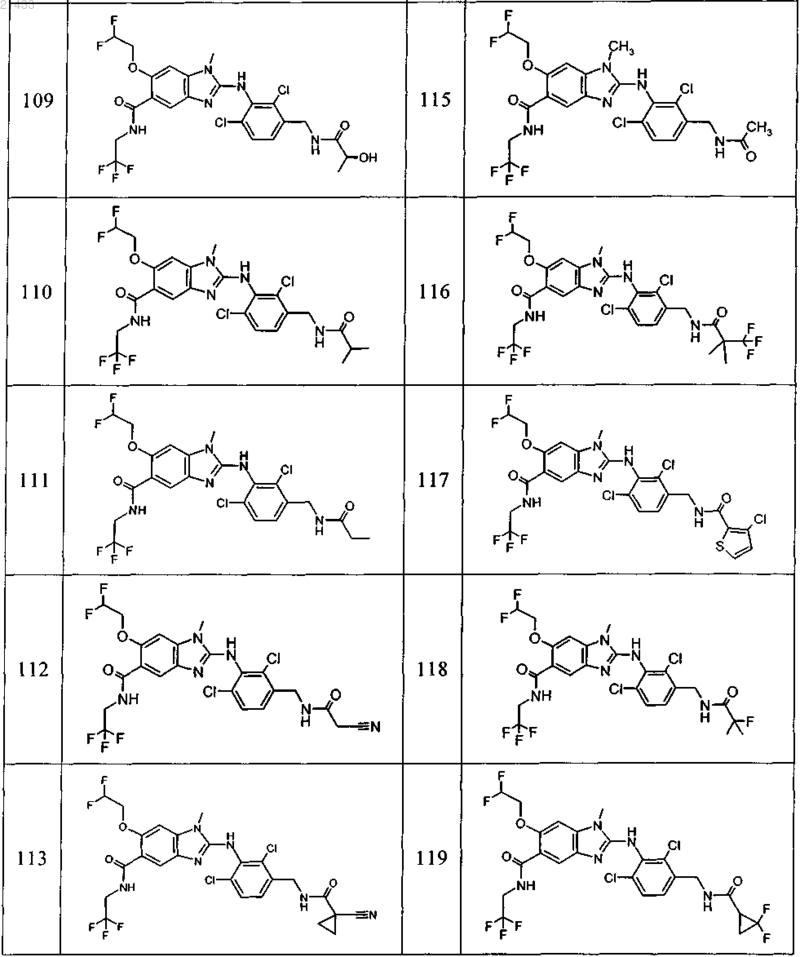
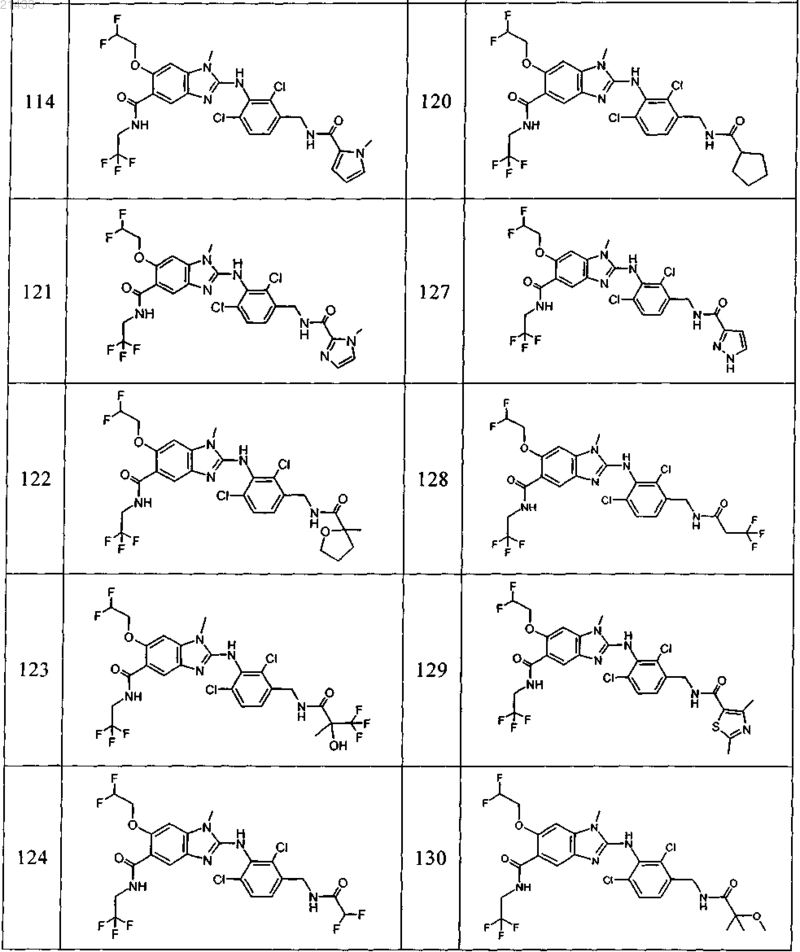
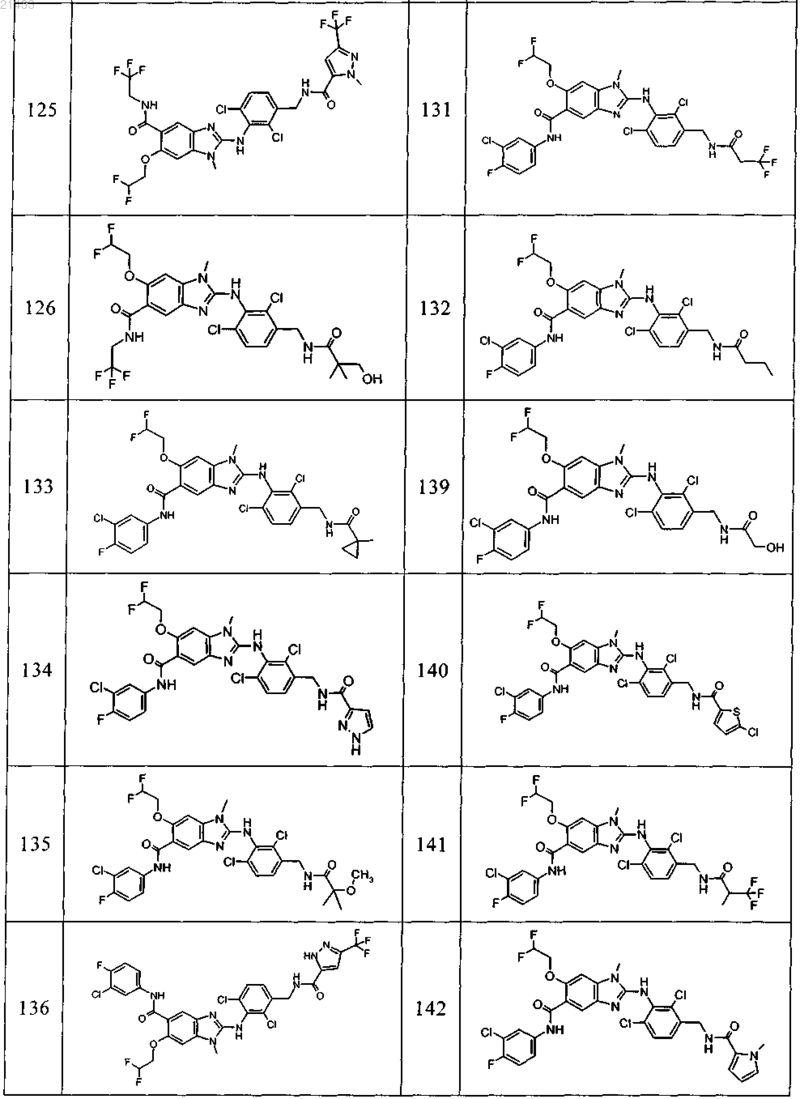
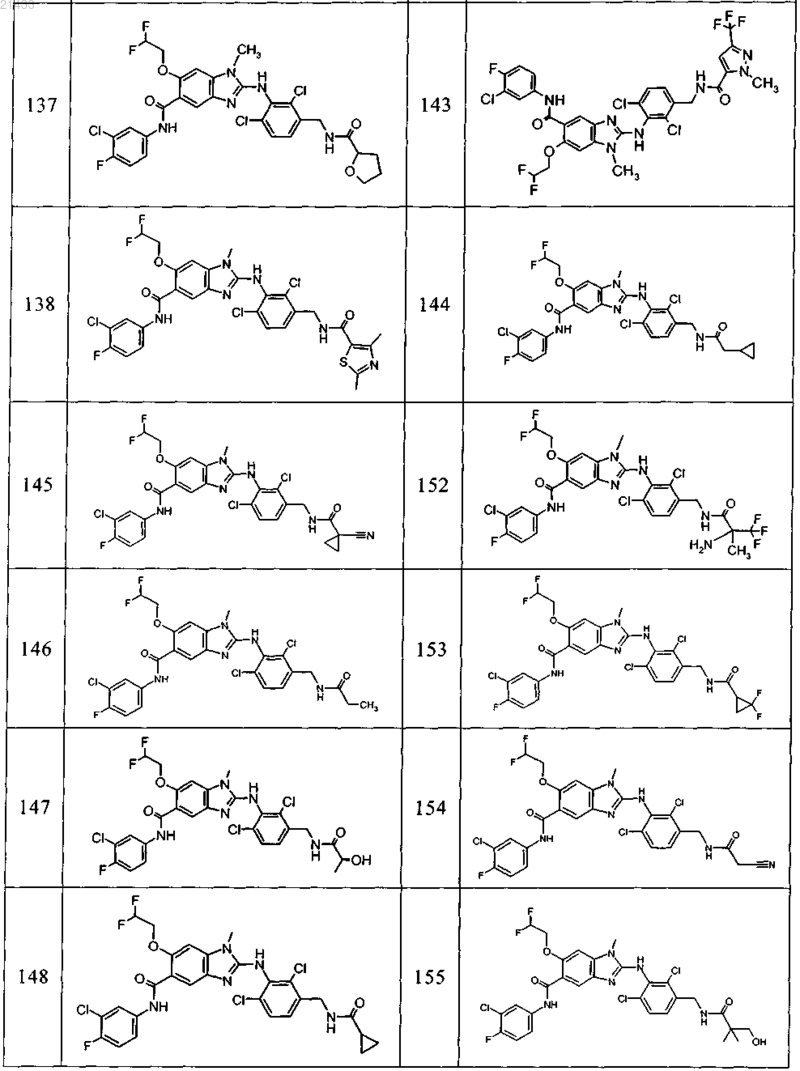
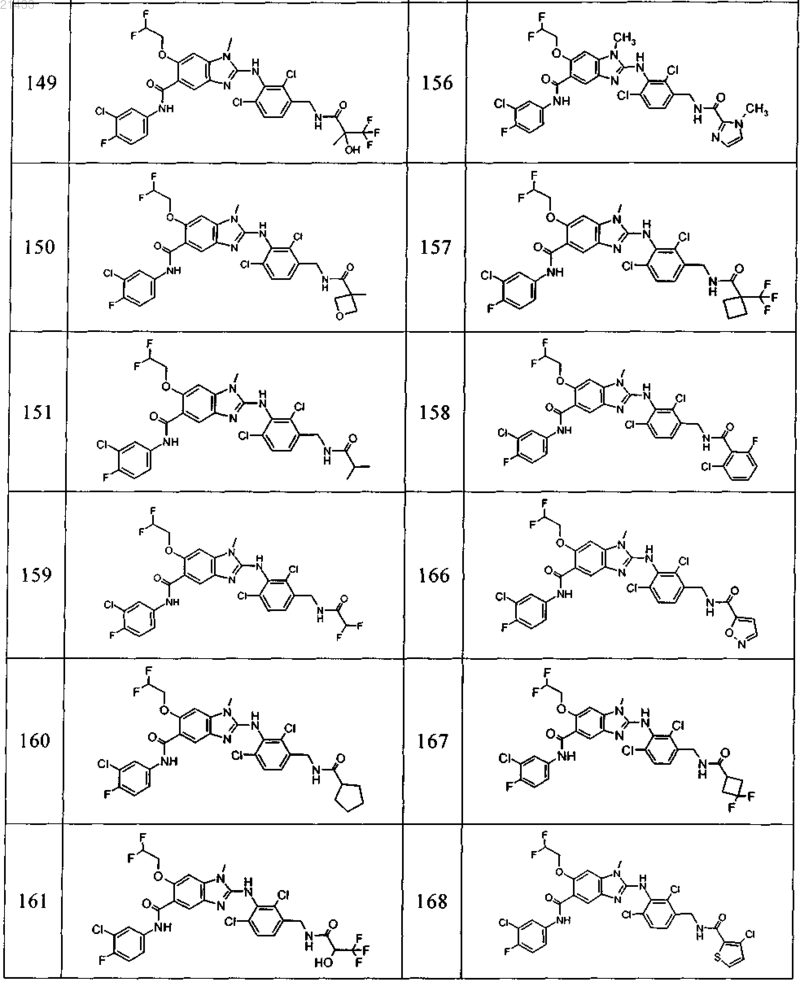
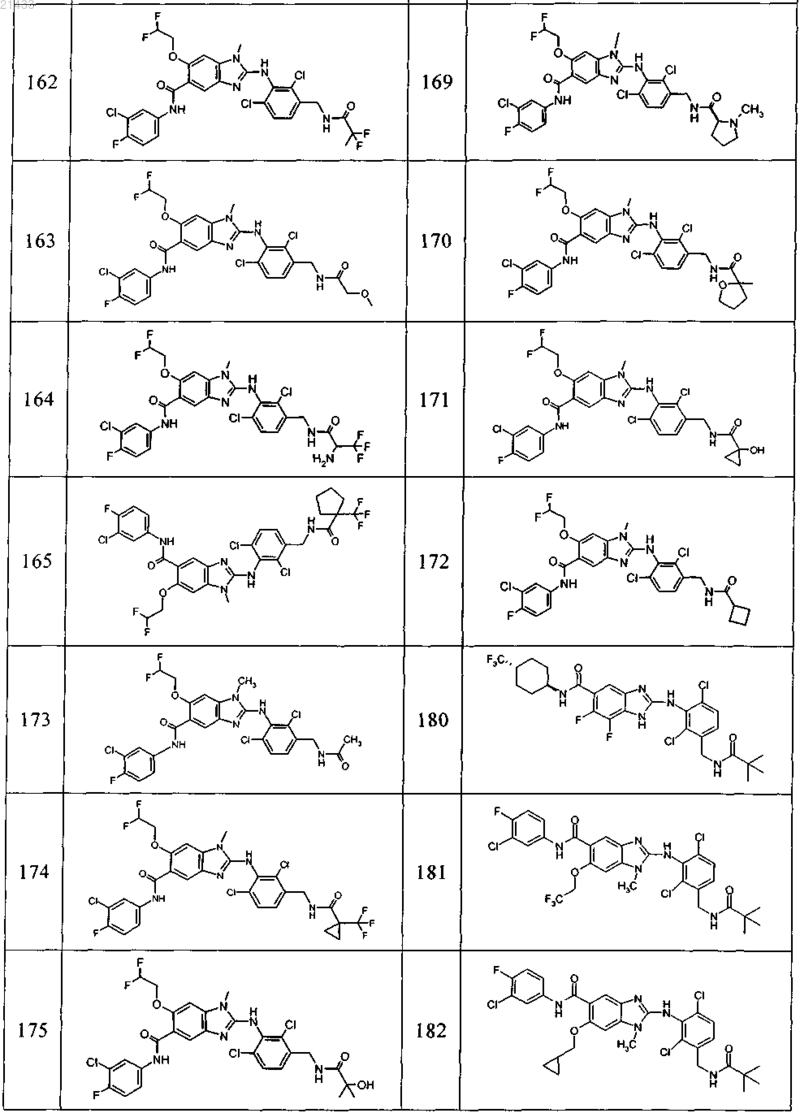
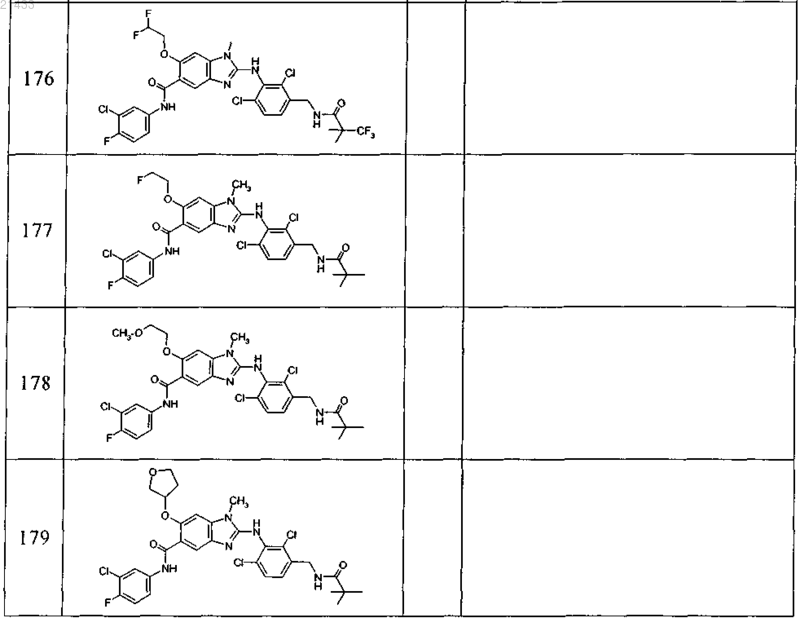
12. Фармацевтическая композиция, обладающая активностью в отношении ингибиторов микросомной простагландин-Е2-синтазы-1 (mPGES-1), содержащая по меньшей мере одно соединение по любому из пп.1-11 в эффективном количестве или его фармацевтически приемлемую соль в смеси с фармацевтически приемлемым вспомогательным веществом, разбавителем и/или носителем.
Текст
СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ МИКРОСОМНОЙ ПРОСТАГЛАНДИНЕ 2-СИНТАЗЫ-1 (mPGES-1) Изобретение относится к соединениям формулы I, к их применению в качестве ингибиторов микросомной простагландин-Е 2-синтазы-1 (mPGES-1), к фармацевтическим композициям,содержащим эти соединения, и к применению таких соединений в качестве лекарственных средств,предназначенных для лечения и/или предупреждения воспалительных заболеваний и связанных патологических состояний. Значения А, М, W, R1, R2, R6, R7, R8 определены в описании.(71)(73) Заявитель и патентовладелец: БРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНАЦИОНАЛЬ ГМБХ (DE) Область техники, к которой относится изобретение Настоящее изобретение относится к новым соединениям, которые являются ингибиторами микросомной простагландин-Е 2-синтазы-1 (mPGES-1), к фармацевтическим композициям, содержащим эти соединения, и к применению таких соединений в качестве лекарственных средств, предназначенных для лечения и/или предупреждения воспалительных заболеваний и связанных патологических состояний,таких как воспалительная/ноцицептивная боль. Уровень техники Существует много острых и хронических заболеваний/нарушений, которые являются воспалительными по своей природе, включая, но не ограничиваясь только ими, ревматоидные заболевания, например ревматоидный артрит, остеоартрит, заболевания внутренних органов, например воспалительная болезнь кишечника, аутоиммунные заболевания, например красная волчанка, заболевания легких, такие как астма и ХОЗЛ (хроническое обструктивное заболевание легких). Существующие способы лечения нестероидными противовоспалительными лекарственными средствами (НСПВС) и ингибиторами циклооксигеназы (СОХ-2) являются эффективными, но при этом часто проявляются побочные эффекты со стороны желудочно-кишечного тракта и сердечно-сосудистой системы. Настоятельно необходимы новые средства лечения, которые обладают такой же эффективностью и улучшенным профилем побочных эффектов. Ингибиторы mPGES могут обладать таким улучшенным профилем побочных эффектов, поскольку они блокируют образование PGE2 более специфическим образом, как это описано ниже. НСПВС и ингибиторы СОХ-2 уменьшают воспаление и боль посредством ингибирования обеих изоформ ферментов СОХ. Фермент циклооксигеназа (СОХ) существует в двух формах, одна из которых конститутивно экспрессируется во многих клетках и тканях (СОХ-1) и другая индуцируется в большинстве клеток и тканей провоспалительными факторами, такими как цитокины, во время воспалительного ответа (СОХ-2). В ходе метаболизма СОХ превращают арахидоновую кислоту в нестабильный промежуточный продукт, простагландин-H2 (PGH2). Затем PGH2 подвергается метаболизму с образованием других простагландинов, включая PGE2, PGF2, PGD2, простациклин и тромбоксан A2. Известно, что эти метаболиты арахидоновой кислоты обладают выраженной физиологической и патофизиологической активностью, включая провоспалительные эффекты. В частности, известно, что PGE2 является сильным провоспалительным медиатором и также известно, что он может являться причиной лихорадки, воспаления и боли. Поэтому было разработано много лекарственных средств, действие которых направлено на ингибирование образования PGE2, включая "НСПВС" (нестероидные противовоспалительные лекарственные средства) и "коксибы" (селективные ингибиторы СОХ-2). Действие таких лекарственных средств преимущественно основано на ингибировании СОХ-1 и/или СОХ-2, вследствие которого уменьшается образование PGE2. Однако ингибирование СОХ обладает тем недостатком, что оно приводит к уменьшению образования всех метаболитов PGH2 в прямом направлении, а для некоторых из них известно, что они обладают полезными характеристиками. Ввиду этого известно/предполагается, что лекарственные средства, действие которых основано на ингибировании СОХ, являются причиной неблагоприятных биологических эффектов. Например, неселективное ингибирование СОХ с помощью НСПВС может являться причиной побочных эффектов со стороны желудочно-кишечного тракта и влиять на тромбоциты и работу почек. Полагают, что, хотя при селективном ингибировании СОХ-2 коксибами ослабляются такие побочные эффекты со стороны желудочно-кишечного тракта, все же происходят нарушения сердечно-сосудистой системы. Таким образом, несомненно, полезным для клинической практики было бы альтернативное средство лечения воспалительных заболеваний, которое не приводит к указанным выше побочным эффектам. В частности, можно ожидать, что лекарственное средство, которое предпочтительно селективно ингибирует превращение PGH2 в провоспалительный медиатор PGE2, будет уменьшать воспалительный ответ при отсутствии соответствующего уменьшения образования других полезных метаболитов арахидоновой кислоты. Соответственно, можно ожидать, что такое ингибирование будет облегчать указанные выше нежелательные побочные эффекты.PGH2 можно превратить в PGE2 с помощью простагландин-Е-синтазы (PGES). Описаны две микросомные простагландин-Е-синтазы (mPGES-1 и mPGES-2) и одна цитозольная простагландин-Е-синтаза(cPGES). Предполагают, что mPGES-1 тесно связан с СОХ-2 и оба фермента подвергаются повышающей регуляции в ходе, например, воспаления. Таким образом, средства, способные ингибировать воздействиеmPGES-1 и, следовательно, уменьшать образование PGE2, вероятно, являются полезными для лечения воспаления и в более общем случае - острой и хронической боли. Производные бензимидазола и имидазопиридина, обладающие ингибирующей активностью по отношению к mPGES-1, раскрыты в WO 2010/034796, WO 2010/034797, WO 2010/034798, WO 2010/034799. В РСТ/ЕР 2010/052799 описан широкий класс различных 2-ариламинобензимидазолов, в которых арильная группа содержит особую боковую цепь. Подробное описание изобретения Настоящее изобретение относится к некоторым соединениям, описывающимся общей формулой,приведенной в РСТ/ЕР 2010/052799, и относится к соединениям, для которых по данным фармакологического исследования с использованием клеток неожиданно оказалось, что они обладают улучшенной активностью. Соединения, обладающие сходным сродством к ферменту mPGES-1, определенным в исследовании с использованием фермента, могут обладать другой активностью по данным исследования с использованием клеток. Предполагается, что сравнение результатов, полученных в фармакологическом исследовании с использованием клеток, с результатами, полученными в исследовании с использованием фермента, позволяет лучше предсказать и рассчитать терапевтически активные концентрации/дозы. Соединения, предлагаемые в настоящем изобретении, обладают высокой активностью по данным обоих исследований. Следовательно, вероятно, что они являются более подходящими для применения in vivo. Настоящее изобретение относится к соединению формулы I в которой R1 и R2 независимо обозначают галоген, -C1-C3-алкил, где последняя алкильная группа необязательно замещена одним или более атомами фтора;W обозначает -C(O)-, -C(O)O-, где эти группы присоединены к атому азота фрагмента -NH- через атом углерода; М обозначает-C1-C6-алкил, -C3-C7-циклоалкил, обе эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -NH(C1-C2-алкил), -N(C1-C2-алкил)2, -O-C1-C3-алкила,-C1-C5-алкила, -C3-C4-циклоалкила, где в последних трех группах алкильные или циклоалкильные группы необязательно замещены одним или более атомами фтора; или оксетанил-, тетрагидрофуранил-, тетрагидропиранил-, азетидинил-, пирролидинил-, пиперидинил-,все эти группы необязательно содержат один или более заместителей, выбранных из фтора,-CN, -C1-C3-алкила, где последняя алкильная группа необязательно замещена одним или более атомами фтора; или фенил-, пиридил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил-, оксазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из галогена,-CN или -C1-C3-алкила, где последняя алкильная группа необязательно дополнительно замещена одним или более атомами фтора;R8 обозначает -H, галоген, -C1-C3-алкил, где последняя алкильная группа необязательно замещена одним или более атомами фтора;R6 обозначает -H, -C1-C5-алкил, -C3-C5-циклоалкил-C0-C2-алкил, где в последних трех группах алкильные или циклоалкильные фрагменты необязательно замещены одним или более атомами фтора;R7 обозначает галоген, C1-C5-алкил-O-, C3-C7-циклоалкил-C0-C2-алкил-O-, 4-7-членный гетероциклоалкил-C0-C2-алкил-O-, где в последних трех группах алкильные, циклоалкильные или гетероциклоалкильные фрагменты необязательно содержат один или более заместителей, выбранных из -F и-O-C1-C3-алкила, где последняя алкильная группа необязательно дополнительно замещена одним или более атомами фтора; А обозначаетC1-C8-алкил-,фенил-,инданил-,нафтил-,1,2,3,4-тетрагидронафтил-,пиридил-, тиенил-, бензотиенил-, пирролил-, индолил-пиразолил-, индазолил-, тиазолил-,бензотиазолил-, оксазолил-, бензоксазолил-, изоксазолил-, бензизоксазолил-, фенил-C1-C3-алкил-,тиенил-C1-C3-алкил-, пиридил-C1-C3-алкил-, C3-C7-циклоалкил-C0-C3-алкил-, оксетанил-C0-C3-алкил-,тетрагидрофуранил-C0-C3-алкил, тетрагидропиранил-C0-C3-алкил, где в этих группах алкильные, циклоалкильные и гетероциклоалкильные фрагменты необязательно содержат один или более заместителей,выбранных из R9a, и арильные и гетероарильные фрагменты необязательно содержат один или более заместителей, выбранных из R9b; каждый R9a независимо обозначает -F, -Cl, -C1-C3-алкил, который необязательно содержит один или более заместителей, выбранных из -F, -O-C1-C3-алкила; каждый R9b независимо обозначает -галоген, -CN; -C1-C3-алкил, который необязательно замещен одним или более атомами фтора,или к его соли, предпочтительно к его физиологически приемлемой соли.-2 021433 Во втором варианте осуществления в общей формуле I группы А, М, W, R1, R2, R6, R7 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления, и R8 обозначает -H или фтор. В другом варианте осуществления в общей формуле I группы А, М, W, R1, R2, R7, R8 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления, и R6 обозначает -H, -CH3, циклопропил. В другом варианте осуществления в общей формуле I группы A, М, W, R6, R7, R8 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления, и R1 и R2 независимо обозначают хлор, фтор, -CH3, -CH2F, -CHF2, -CF3. В другом варианте осуществления в общей формуле I группы A, М, W, R1, R2, R6, R8 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления, и R7 обозначает фтор, -OCHF2, -OCF3, -OCH2CH2F, -OCH2CHF2, -OCH2CF3, -O-тетрагидрофуран-3-ил,-O-CH2-циклопропил. В другом варианте осуществления в общей формуле I группы М, W, R1, R2, R6, R7, R8 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления, и А обозначает C1-C4-алкил-, C3-C7-циклоалкил-C0-C2-алкил-, тетрагидрофуранилметил-, фенил-C1-C2-алкил-, пиридилметил-, фенил-, инданил-, пиридил-, тиенил-, тиазолил-, бензотиазолил-, где в этих группах алкильные, циклоалкильные или гетероциклоалкильные фрагменты необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CH2F, -CHF2, -CF3, и арильные и гетероарильные фрагменты необязательно замещены -F, -Cl, -Br, -CN, -CH3, -CH2F, -CHF2, -CF3. В другом варианте осуществления в общей формуле I группы A, W, R1, R2, R6, R7, R8 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления, и М обозначает -C1-C4-алкил, -C3-C5-циклоалкил, обе эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CH2F, -CHF2, -CF3, циклопропила; или оксетанил-,тетрагидрофуранил-, азетидинил- или пирролидинил-, все эти группы необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CH2F, -CHF2, -CF3; или фенил-, инданил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3, -CH2F, -CHF2, -CF3. Другой вариант осуществления настоящего изобретения относится к соединениям формулы Ia в которой А, М, R1, R2, R6, R7 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления. В другом варианте осуществления настоящее изобретение относится к соединениям формулы Ia в которой М обозначает метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, -CH2-циклопропил,циклопропил, циклобутил, циклопентил, все эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CF3; или выбран из следующих групп: где последние девять групп необязательно содержат один или более заместителей, выбранных из-F, -CH3, -CF3; или выбран из следующих групп: где последние одиннадцать групп необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3, -CF3;A, R1, R2, R6, R7 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления. В другом варианте осуществления настоящее изобретение относится к соединениям формулы Ia, в которой А обозначает метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, где последние семь групп необязательно замещены одним или более атомами фтора, или циклопропил, циклобутил, циклопентил, циклогексил, где последние четыре группы необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CHF2, -CF3; или выбран из следующих групп: где последние семь групп необязательно содержат один или более заместителей, выбранных из -F,-CH3, -CHF2, -CF3; или выбран из следующих групп: где в последних одиннадцати группах арильные и гетероарильные фрагменты необязательно содержат один или более заместителей, выбранных из -F, -Cl, -Br, -CN, -CH3, -CF3; М, R1, R2, R6, R7 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления. В другом варианте осуществления настоящее изобретение относится к соединениям формулы IbA, R1, R2, R6, R7 обладают такими же значениями, как определенные в любом из предыдущих вариантах осуществления. В другом варианте осуществления настоящее изобретение относится к соединениям формулы Ia или Ib':R7 обозначает фтор, -OCHF2, -OCF3, -OCH2CH2F, -OCH2CHF2, -OCH2CF3, тетрагидрофуран-3-ил-O-,-O-CH2-циклопропил; А обозначает метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, где последние семь групп необязательно замещены одним или более атомами фтора, или циклопропил, циклобутил, циклопентил, циклогексил, где последние четыре группы необязательно содержат один или более заместителей, выбранных из -F, -CH3, -CHF2, -CF3; или выбран из следующих групп: где последние семь групп необязательно содержат один или более заместителей, выбранных из -F,-CH3, -CHF2, -CF3; или выбран из следующих групп: где в последних одиннадцати группах арильные и гетероарильные фрагменты необязательно содержат один или более заместителей, выбранных из -F, -Cl, -Br, -CN, -CH3, -CF3; М обозначает метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, циклопропил,-CH2-циклопропил, циклобутил, циклопентил, все эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CF3; или выбран из следующих групп: где последние девять групп необязательно содержат один или более заместителей, выбранных из F, -CH3, -CF3; или выбран из следующих групп: где последние одиннадцать групп необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3, -CF3; или к их солям, предпочтительно к их физиологически приемлемым солям. Использующиеся термины и определения Общие определения. Терминам, специально не определенным в настоящем изобретении, следует придавать значения,которые им должен придавать специалист в данной области техники в соответствии с раскрытием и контекстом. Однако если не указано иное, то при использовании в описании приведенные ниже термины обладают указанными значениями и используются указанные ниже обозначения. В группах, радикалах или фрагментах, определенных ниже, количество атомов углерода часто указывается перед группой, например C1-C6-алкил означает алкильную группу или радикал, содержащий от 1 до 6 атомов углерода. Обычно в группах, содержащих две или более подгруппы, последняя названная подгруппа является местом присоединения радикала, например заместитель "арил-C1-C3-алкил-" означает арильную группу, которая присоединена к C1-C3-алкильной группе, последняя присоединена к ядру или к группе, к которой присоединен заместитель. В случае если соединение, предлагаемое в настоящем изобретении, описано с помощью химического названия и в виде формулы, то в случае любых различий определяющей является формула. Знак звездочки используется в субформулах для обозначения связи, которая соединена с ядром молекулы, как это определено, например циклопропилметильная группа будет представлена следующей структурой: Стереохимическая конфигурация/сольваты/гидраты. Если специально не указано иное, то в описании и прилагаемой формуле изобретения определенная химическая формула или название соединения включают его таутомеры (например, 1H-бензимидазол можно рассматривать, как идентичный соответствующему соединению, содержащему 3 Н-бензимидазол) и все стереоизомеры, оптические и геометрические изомеры (например, энантиомеры, диастереоизомеры, E/Z-изомеры и т.п.) и рацематы, а также смеси отдельных энантиомеров в разных соотношениях,смеси диастереоизомеров или смеси любых описанных выше форм, в которых существуют такие изомеры и энантиомеры, а также его соли, включая его фармацевтически приемлемые соли и его сольваты,такие как, например, гидраты, включая сольваты свободных соединений или сольваты солей соединения. Соли. Выражение "фармацевтически приемлемое" используется в настоящем изобретении для указания таких соединений, материалов, композиций и/или дозированных форм, которые в соответствии с основными положениями медицины являются подходящими для использования при соприкосновении с тканями людей и животных без проявления чрезмерной токсичности, раздражающего воздействия, аллергической реакции или других затруднений или осложнений при разумном соотношении польза/риск. При использовании в настоящем изобретении "фармацевтически приемлемые соли" означают производные раскрытых соединений, в которых исходное соединение изменено путем образования его солей с кислотой или основанием. Примеры фармацевтически приемлемых солей включают, но не ограничиваются только ими, соли неорганических или органических кислот с основными остатками, такими как аминогруппы; соли щелочных металлов или органических соединений с кислотными остатками, такими как карбоксигруппы и т.п. Например, такие соли включают соли, образованные с аммиаком,L-аргинином, бетаином, бенетамином, бензатином, гидроксидом кальция, холином, деканолом, диэтаноламином (2,2'-имино-бис-(этанол, диэтиламином, 2-(диэтиламино)этанолом, 2-аминоэтанолом, этилендиамином, N-этилглюкамином, гидрабамином, 1H-имидазолом, лизином, гидроксидом магния,-6 021433 4-(2-гидроксиэтил)морфолином, пиперазином, гидроксидом калия, 1-(2-гидроксиэтил)пирролидином,гидроксидом натрия, триэтаноламином (2,2',2-нитрило-трис-(этанол, трометамином, гидроксидом цинка, уксусной кислотой, 2,2-дихлоруксусной кислотой, адипиновой кислотой, альгиновой кислотой,аскорбиновой кислотой, L-аспарагиновой кислотой, бензолсульфоновой кислотой, бензойной кислотой,2,5-дигидроксибензойной кислотой, 4-ацетамидобензойной кислотой, (+)камфорной кислотой,(+)камфор-10-сульфоновой кислотой, угольной кислотой, коричной кислотой, лимонной кислотой, цикламовой кислотой, декановой кислотой, додецилсерной кислотой, этан-1,2-дисульфоновой кислотой,этансульфоновой кислотой, 2-гидроксиэтансульфоновой кислотой, этилендиаминтетрауксусной кислотой, муравьиной кислотой, фумаровой кислотой, галактаровой кислотой, гентизиновой кислотой,D-глюкогептоновой кислотой, D-глюконовой кислотой, D-глюкуроновой кислотой, глутаминовой кислотой, глутаровой кислотой, 2-оксоглутаровой кислотой, глицерофосфорной кислотой, глицином, гликолевой кислотой, гексановой кислотой, гиппуровой кислотой, бромисто-водородной кислотой, хлористоводородной кислотой, изомасляной кислотой, DL-молочной кислотой, лактобионовой кислотой, лауриновой кислотой, лизином, малеиновой кислотой, (-)-L-яблочной кислотой, малоновой кислотой,DL-миндальной кислотой, метансульфоновой кислотой, галактровой кислотой, нафталин-1,5 дисульфоновой кислотой, нафталин-2-сульфоновой кислотой, 1-гидрокси-2-нафтойной кислотой, никотиновой кислотой, азотной кислотой, октановой кислотой, олеиновой кислотой, оротовой кислотой, щавелевой кислотой, пальмитиновой кислотой, памоевой кислотой (эмбоновой кислотой), фосфорной кислотой, пропионовой кислотой, (-)-L-пироглутаминовой кислотой, салициловой кислотой,4-аминосалициловой кислотой, себациновой кислотой, стеариновой кислотой, янтарной кислотой, серной кислотой,дубильной кислотой,(+)-L-винной кислотой,тиоциановой кислотой,п-толуолсульфоновой кислотой и ундециленовой кислотой. Другие фармацевтически приемлемые соли могут быть образованы с катионами металлов, таких как алюминий, кальций, литий, магния, калий, натрий, цинк и т.п. (см. также публикацию Pharmaceuticalsalts, Berge, S.M. et al., J. Pharm. Sci., (1977), 66, 1-19). Фармацевтически приемлемые соли, предлагаемые в настоящем изобретении, можно синтезировать из исходного соединения, которое содержит основный или кислотный фрагмент, по обычным химическим методикам. Обычно такие соли можно получить по реакции этих соединений в форме свободной кислоты или основания с достаточным количеством соответствующего основания или кислоты в воде или органическом растворителе, таком как эфир, этилацетат, этанол, изопропанол или ацетонитрил, или в их смеси. Соли других кислот, отличающиеся от указанных выше, которые, например, применимы для очистки или выделения соединений, предлагаемых в настоящем изобретении (например, трифторацетаты),также входят в объем настоящего изобретения. Термин "галоген" обычно означает фтор, хлор, бром и йод. Термин "C1-Cn-алкил", где n является целым числом от 2 до n, по отдельности или в комбинации с другим радикалом, означает ациклический, насыщенный, обладающий разветвленной или линейной цепью углеводородный радикал, содержащий от 1 до n атомов С. Например, термин C1-C5-алкил включает радикалы H3C-, H3C-CH2-, H3C-CH2-CH2-, H3C-CH(CH3)-, H3C-CH2-CH2-CH2-, H3C-CH2-CH(CH3)-,H3C-CH(CH3)-CH2-,H3C-C(CH3)2-,H3C-CH2-CH2-CH2-CH2-,H3C-CH2-CH2-CH(CH3)-,H3C-CH2-CH(CH3)-CH2-,H3C-CH(CH3)-CH2-CH2-,H3C-CH2-C(CH3)2-,H3C-C(CH3)2-CH2-,H3C-CH(CH3)-CH(CH3)- и H3C-CH2-CH(CH2CH3)-. Термин "С 3-Cn-циклоалкил", где n является целым числом 3, по отдельности или в комбинации с другим радикалом означает циклический, насыщенный углеводородный радикал, содержащий от 3 до n атомов С. Например, термин "C3-C7-циклоалкил" включает циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Термин "циклоалкил" также включает би-, три- или тетрациклические кольцевые структуры, состоящие только из атомов углерода и содержащие от 1 до 4 колец, где такие кольца могут быть присоединены друг к другу с помощью связи или могут быть сконденсированы. Термин "циклоалкил" дополнительно включает спиросистемы и мостиковые системы. Циклический углеводородный радикал также может быть сконденсирован с фенильным кольцом. Таким образом, термин "циклоалкил" включает приведенные ниже типичные структуры, которые не изображены в виде радикалов и в любой форме могут быть присоединены с помощью ковалентной связи к любому атому циклоалкильного кольца при условии, что сохраняются соответствующие валентности: Термин "С 3-Cn-гетероциклоалкил", где n является целым числом 3, по отдельности или в комбинации с другим радикалом означает циклический неароматический моно-, би-, триспироциклический радикал, содержащий от 3 до n кольцевых атомов, где по меньшей мере один кольцевой атом выбран из группы, включающей N, О или S и где n обозначает максимальное количество кольцевых атомов. Циклический углеводородный радикал также может быть сконденсирован с фенильным кольцом. Заместители в гетероциклоалкильных группах, если это возможно, могут находиться на любом атоме кольцевой системы, включая гетероатом. Положением присоединения гетероциклоалкильных радикалов может быть любой атом неароматической кольцевой системы, включая (если это возможно) гетероатом (такой как атом азота) или также включая атом любого сконденсированного неароматического карбоциклического кольцевого фрагмента,который может содержаться в виде части кольцевой системы. Таким образом, термин "гетероциклоалкил" включает приведенные ниже типичные структуры, которые не изображены в виде радикалов и в любой форме могут быть присоединены с помощью ковалентной связи к любому атому при условии, что сохраняются соответствующие валентности: Методики получения. Соединения, предлагаемые в настоящем изобретении, можно получить в соответствии с методиками, которые хорошо известны специалистам в данной области техники, например, так, как это описано ниже в настоящем изобретении и в экспериментальном разделе, или по методикам, аналогичным описанным в WO 2010/034796 и WO 2010/034797. Другим объектом настоящего изобретения является способ получения соединения формулы I, который можно осуществить, например, в соответствии с приведенными ниже схемами A-С.(все переменные группы являются такими, как определено в п.1 формулы изобретения) Реакцию фенилендиамина X с тиоизоционатом XI (стадия а) можно провести при стандартных условиях, известных специалистам в данной области техники, например, по аналогии со способом, описанным в WO 2010/034796, в присутствии подходящего растворителя, такого как диэтиловый эфир (Et2O),диметилформамид (ДМФ), дихлорметан (ДХМ), ацетонитрил (MeCN) и/или тетрагидрофуран (ТГФ). Реакцию предпочтительно проводить в присутствии подходящего реагента, который облегчает протекание стадии циклизации, например CH3-I или соединения на основе карбодиимида, такого как N,N'дициклогексилкарбодиимид (ДЦК), 1-этил-3-(3-диметиламинопропил)карбодиимид (EDCI, или его соль,например гидрохлорид) или N,N'-диизопропилкарбодиимид (ДИК). Реакцию можно проводить при любой подходящей температуре от 0 до 200 С, предпочтительно от комнатной температуры до 100 С. Стадию а) можно провести постадийно с выделением промежуточных тиомочевин XIIa и/или XIIb или по однореакторной методике. Альтернативно, соединения формулы I можно синтезировать в соответствии со схемой В. Схема В(все переменные группы являются такими, как определено в п.1 формулы изобретения, и PG карбоксигруппы обозначает защитную группу карбоксигруппы) Защитная группа PG карбоксигруппы представляет собой известную из литературы защитную группу карбоксигруппы, хорошо известную специалистам в данной области техники, такую как, например, описанную в публикации "Protective Groups in Organic Synthesis", 3rd edition, T.W. GreeneP.G.M. Wutz,-9 021433Wiley-Interscience (1999), например, C1-C5-алкильную, аллильную или бензильную группу. Стадию а) можно провести так, как это представлено на схеме А, но также можно провести в присутствии добавки (такой как 2,2,2-трифтор-N,O-бис-(триметилсилил)ацетамид), если в соединении XIII содержится незащищенная карбоксигруппа. Стадию b) можно провести при известных условиях омыления, например, с помощью LiOH, NaOH или KOH в этаноле (EtOH), метаноле (МеОН), ДМФ, MeCN, ТГФ или диоксане или с помощью Pd/C в МеОН. Образование амида на стадии с) можно провести с использованием дополнительногоin situ активирующего реагента, такого как циклический ангидрид 1-пропилфосфоновой кислоты(HBTU),O-(7-азабензотриазол-1-ил)-N,N,N',N'тетраметилуронийгексафторфосфат (ГАТУ), ДЦК, EDCI, карбонилдиимидазол (КДИ), карбонилдитриазол (КДТ), 1-хлор-2-метилпропенилдиметиламин, оксалилхлорид, или других активирующих реагентов,известных в данной области техники. Реакцию сочетания предпочтительно проводить в присутствии основания, такого как NaOH, KOH,NaHCO3, триэтиламин (ТЭА), N-этилдиизопропиламин (ДИПЭА), пиридин, N,N-диметиламинопиридин(ДМАП), или других подходящих оснований, известных в данной области техники и описанных, например, в публикации Houben-Weyl, "Methods in Organic Synthesis", vol. E22a, p 425ff. Реакции сочетания проводят в подходящем растворителе, например в ДХМ, диоксане, ТГФ, MeCN, ДМФ, диметилацетамиде (ДМА), N-метилпирролидоне (NMP), или в смеси указанных выше растворителей при любой подходящей температуре от 0 до 100 С. Если PG карбоксигруппы представляет собой метильную или этильную группу, то превращение соединения XIV в соединение I также можно провести по однореакторной методике, например, с использованием триметилалюминия или триэтилалюминия в гексане, диоксане, ТГФ при 20-80 С. Альтернативно, соединения формулы I можно синтезировать в соответствии со схемой С. Схема С(все переменные группы являются такими, как определено в п.1 формулы изобретения, и PG аминогруппы обозначает защитную группу аминогруппы бензильного фрагмента) Защитная группа PG аминогруппы в соединении XV представляет собой известную из литературы защитную группу аминогруппы, хорошо известную специалистам в данной области техники, такую как,например, описанную в публикации "Protective Groups in Organic Synthesis", 3rd edition, T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999), например трет-бутоксикарбонильную, бензилоксикарбонильную,этоксикарбонильную, метоксикарбонильную, аллилоксикарбонильную или трифторметилкарбонильную группу. Стадию а) можно провести так, как это представлено на схеме 1. Стадия d): PG аминогруппы в соединении XVI можно удалить по методикам, хорошо известным специалистам в данной области техники и приведенным в качестве примера ниже в настоящем изобретении. Например, в соединении XVI можно удалить защитную группу с использованием соответствующего реагента (в зависимости от защитной группы), такого как, например, растворы трифторуксусной кислоты,HCl или H2SO4, KOH; Ва(ОН)2, палладий на угле (Pd/C), триметилсилилйодид, или при других условиях,как это описано в публикации "Protective Groups in Organic Synthesis", 3rd ed., T.W. GreeneP.G.M. Wutz,Wiley-Interscience (1999). Подходящим сорастворителем для проведения этой стадии является, например,ДХМ, ТГФ, MeCN, ДМФ, ДМА, NMP или смеси указанных выше растворителей, реакцию проводят при любой подходящей температуре от 0 до 100 С. Образование амида на стадии е) можно провести с использованием кислот HO-W-M и дополнительного in situ активирующего реагента, такого как АПФК, TBTU, HBTU, ГАТУ, ДЦК, EDCI, КДИ,- 10021433 КДТ, 1-хлор-2-метилпропенилдиметиламин, оксалилхлорид, или других активирующих реагентов, известных в данной области техники, по аналогии со схемой В, стадия с); или непосредственно с использованием соответствующего хлорангидрида кислоты Cl-W-М при аналогичных условиях без использования дополнительного in situ активирующего реагента. Реакцию сочетания предпочтительно проводить в присутствии основания, такого как NaOH, KOH,NaHCO3, ТЭА, ДИПЭА, пиридин, ДМАП, или других подходящих оснований, известных в данной области техники, и описанных, например, в публикации Houben-Weyl, "Methods in Organic Synthesis",Vol. E22a, p 425ff. Реакции сочетания проводят в подходящем растворителе, например в ДХМ, диоксане,ТГФ, MeCN, ДМФ, ДМА, NMP, или в смеси указанных выше растворителей. Синтез структурных фрагментов X и XIII, в которых A, R6-R8 обладают значениями, определенными в п.1 формулы изобретения, и PG карбоксигруппы обозначает известную из литературы защитную группу карбоксигруппы, как описано выше, можно провести по описанным в литературе методикам, которые хорошо известны специалистам в данной области техники, например по методикам, аналогичным описанным в WO 2010/034796 и WO 2010/034797. Синтез структурных фрагментов XI и XV, в которых все переменные группы являются такими, как определено в п.1 формулы изобретения, и PG аминогруппы обозначает защитную группу аминогруппы бензильного фрагмента, проводят в соответствии со схемой D с использованием стандартных условий проведения реакций, известных специалистам в данной области техники, которые более подробно описаны в качестве примеров в экспериментальном разделе. Схема D(все переменные группы являются такими, как определено в п.1 формулы изобретения, и PG аминогруппы обозначает защитную группу аминогруппы бензильного фрагмента) Стадию f) можно провести по стандартным методикам, описанным в литературе, например, с использованием реагентов, таких как 1,1'-тиокарбонилди-2-пиридон, О,O'-ди-2-пиридилтиокарбонат,1,1'-тиокарбонилдиимидазол, или с использованием тиофосгена в растворителе, таком как, например,ДХМ, диоксан или ДМФ, при температурах 0-150 С и необязательно с добавлением основания, такого как ДМАП или ТЭА. Структурные фрагменты XVII и XVIII можно получить в соответствии со схемой Е.(все переменные группы являются такими, как определено в п.1 формулы изобретения, и PG аминогруппы обозначает защитную группу аминогруппы бензильного фрагмента) Образование амида на стадии g) можно провести по аналогии со стадией с) или стадией е) с получением соединения XVII или с использованием обычных реагентов, использующихся для защиты аминогруппы, например ди-трет-бутилдикарбоната, метил-, этил-, бензил- или аллилхлорформиата, при стандартных условиях проведения реакции, как это описано в публикации "Protective Groups in OrganicSynthesis", 3rd ed., T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999), с получением соединений XVIII. Нитрогруппу в предшественниках XVIIa или XVIIIa можно восстановить с образованием аминогруппы на стадии h) при условиях восстановления, известных из литературы, например, путем гидрирования (предпочтительно при 1-5 бар) в присутствии Pd/C или RaNi в МеОН, EtOH или ТГФ, необязательно в кислой среде в присутствии HCl, или с использованием SnCl2/HCl, Na2S2O4, Zn/HCl, Fe/HCl,порошкообразное Fe/водный раствор NH4Cl, или по методикам, описанным в литературе, например в публикации R. Larock, Comprehensive Organic Transformations, VCH Verlagsgemeinschaft, Weinheim(1989). Подходящим растворителем для проведения этой стадии является, например, ДХМ, ТГФ, MeCN,ДМФ, ДМА, NMP, EtOH, МеОН или смеси указанных выше растворителей, реакцию проводят при любой подходящей температуре от 0 до 100 С. Структурные фрагменты XIX и XX можно получить в соответствии со схемами F-G. Схема F(все переменные группы являются такими, как определено в п.1 формулы изобретения) Стадию i) можно провести путем гидрирования (1-5 бар) с использованием катализатора, такого какPd/C, PtO2 или RaNi, в подходящем растворителе, таком как МеОН или EtOH, необязательно с использованием HCl или NH3 в качестве добавки при температурах 0-60 С или путем восстановления с использованием LiAlH4 или реагентов, содержащих ВН 3, при условиях, известных из литературы. Стадию j) можно провести при условиях реакции сочетания с образованием амида, описанных для стадии е), и с использованием NH3 в качестве компонента реакции сочетания, например в качестве активирующего реагента можно использовать 1-хлор-2-метилпропенилдиметиламин в ТГФ. Стадию k) можно провести с использованием LiAlH4 или реагентов, содержащих ВН 3, при условиях, известных из литературы, например, как это описано в публикации R.C.Larock, Comprehensive Organic Transformations, VCH, 1989, p. 432-433, предпочтительно с использованием LiAlH4 в ТГФ при 080 С. Альтернативно, соединения XIX и XX можно получить в соответствии со схемой G.(все переменные группы являются такими, как определено в п.1 формулы изобретения) Стадию k) можно провести путем перемешивания соединения XXIV с реагентом XXV в концентрированной H2SO4 или F3C-SO3H при температурах 0-150 С, предпочтительно при 20-80 С. Стадию l) можно провести по известным из литературы методикам удаления защитных групп, использующихся для удаления соответствующих защитных групп атома азота, например, путем обработки фталимида гидразином или путем расщепления амидной связи с использованием оснований, таких какNaOH в МеОН или EtOH, при температурах 20-80 С или в кислой среде с использованием водного раствора HCl или раствора HCl в диоксане при температурах 20-80 С. Альтернативно, соединения XIX и XX можно получить в соответствии со схемой Н. Схема Н(все переменные группы являются такими, как определено в п.1 формулы изобретения) Стадию m) можно провести путем перемешивания соединения XXX с HO-NH2 в подходящем растворителе, например MeCN, ДХМ, ТГФ, необязательно с использованием HCl в качестве добавки при температурах 0-60 С. Стадию n) можно провести при известных из литературы условиях восстановления, например путем гидрирования, предпочтительно при давлении Н 2, равном 1-5 бар, в присутствии Pd/C или RaNi в МеОН, EtOH или ТГФ, необязательно с использованием HCl или НОАс в качестве катализатора или с использованием SnCl2/HCl, Zn/HCl, Fe/HCl, порошкообразное Fe/водный раствор NH4Cl или по методикам, описанным в литературе, например в публикации R. Larock, Comprehensive Organic Transformations,VCH Verlagsgemeinschaft, Weinheim (1989). Поэтому другим объектом настоящего изобретения является способ получения соединений формулы I, включающий следующие стадии:(1) реакция соединения формулы XIX в которой R1 и R2 независимо обозначают галоген, -C1-C3-алкил, где последняя алкильная группа необязательно замещена одним или более атомами фтора; с хлорангидридом кислоты формулыCl-W-M,где W обозначает -C(O)-, -C(O)O-, где эти группы присоединены к атому азота фрагмента-C1-C6-алкил, -C3-C7-циклоалкил, обе эти группы необязательно замещены одной или более группа- 13021433 ми, выбранными из -F, -ОН, -CN, -NH2, -NH(C1-C2-алкил), -N(C1-C2-алкил)2, -O-C1-C3-алкила,-C1-C5-алкила, -C3-C4-циклоалкила, где в последних трех группах алкильные или циклоалкильные группы необязательно замещены одним или более атомами фтора; или оксетанил-, тетрагидрофуранил-, тетрагидропиранил-, азетидинил-, пирролидинил-, пиперидинил-,все эти группы необязательно содержат один или более заместителей, выбранных из фтора, -CN,-C1-C3-алкила, где последняя алкильная группа необязательно замещена одним или более атомами фтора; или фенил-, пиридил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил-, оксазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из галогена,-CN или -C1-C3-алкила, где последняя алкильная группа необязательно дополнительно замещена одним или более атомами фтора; или с кислотой формулы HO-W-M в присутствии in situ активирующего реагента,выбранного из группы, включающей циклический ангидрид 1-пропилфосфоновой кислоты (АПФК),O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат (TBTU), O-(бензотриазол-1-ил)N,N,N',N'-тетраметилуронийгексафторфосфат(ТЭА), N-этилдиизопропиламин (ДИПЭА), пиридин, N,N-диметиламинопиридин (ДМАП), в растворителе, выбранном из группы, включающей дихлорметан, диоксан, ТГФ, MeCN, диметилформамид, диметилацетамид (ДМА), N-метилпирролидон (NMP), или в их смеси; при температуре от 0 до 100 С с получением соединения формулы XVII(2) реакция соединения формулы XVII с реагентом, выбранным из группы, включающей 1,1'-тиокарбонилди-2-пиридон, О,О'-ди-2-пиридилтиокарбонат, 1,1'-тиокарбонилдиимидазол и тиофосген, в растворителе, выбранном из группы, включающей дихлорметан, диоксан и ДМФ, при температурах 0-150 С и необязательно в присутствии основания, которым предпочтительно является ДМАП или ТЭА, с получением соединения формулы XI(3) реакция соединения формулы XI с соединением формулы XIIIN,N'-диизопропилкарбодиимид (ДИК); в растворителе, выбранном из группы, включающей диэтиловый эфир (Et2O), диметилформамид (ДМФ), дихлорметан (ДХМ), ацетонитрил (MeCN) и тетрагидрофуран(ТГФ), предпочтительно при температуре от 0 до 100 С. Альтернативный способ получения соединений формулы I включает следующие стадии:(1) реакция соединения формулы XX в которой R1 и R2 независимо обозначают галоген, -C1-C3-алкил, где последняя алкильная группа необязательно замещена одним или более атомами фтора; с хлорангидридом кислоты формулыCl-W-M,где W обозначает -C(O)-, -C(O)O-, где эти группы присоединены к атому азота фрагмента -NH- через атом углерода; М обозначает-C1-C6-алкил, -C3-C7-циклоалкил, обе эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -NH(C1-C2-алкил), -N(C1-C2-алкил)2, -O-C1-C3-алкила, -C1-C5 алкила, -C3-C4-циклоалкила, где в последних трех группах алкильные или циклоалкильные группы необязательно замещены одним или более атомами фтора; или оксетанил-, тетрагидрофуранил-, тетрагидропиранил-, азетидинил-, пирролидинил-, пиперидинил-,все эти группы необязательно содержат один или более заместителей, выбранных из фтора, -CN,-C1-C3-алкила, где последняя алкильная группа необязательно замещена одним или более атомами фтора; или фенил-, пиридил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил-, оксазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из галогена,-CN или -C1-C3-алкила, где последняя алкильная группа необязательно дополнительно замещена одним или более атомами фтора, или с кислотой формулы HO-W-M в присутствии in situ активирующего реагента,выбранного из группы, включающей циклический ангидрид 1-пропилфосфоновой кислоты (АПФК),O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат (TBTU), O-(бензотриазол-1-ил)N,N,N',N'-тетраметилуронийгексафторфосфат(ТЭА), N-этилдиизопропиламин (ДИПЭА), пиридин, N,N-диметиламинопиридин (ДМАП), в растворителе, выбранном из группы, включающей дихлорметан, диоксан, ТГФ, MeCN, диметилформамид, диметилацетамид (ДМА), N-метилпирролидон (NMP), или в их смеси; при температуре от 0 до 100 С с получением соединения формулы XVIIa(2) превращение соединения формулы XVIIa в соединение формулы XVII путем каталитического гидрирования (предпочтительно при 1-5 бар) в присутствии Pd/C или RaNi в МеОН, EtOH или ТГФ, необязательно в кислой среде в присутствии HCl, или путем восстановления с использованием реагента, выбранного из группы, включающей SnCl2/HCl, Na2S2O4, Zn/HCl, Fe/HCl, порошкообразное Fe/водный раствор NH4Cl, в растворителе, выбранном из группы, включающей ДХМ,ТГФ, MeCN, ДМФ, ДМА, NMP, EtOH, МеОН или их смеси, при температуре от 0 до 100 С;(3) реакция соединения формулы XVII с реагентом,выбранным из группы,включающей 1,1'-тиокарбонилди-2-пиридон,О,О'-ди-2-пиридилтиокарбонат, 1,1'-тиокарбонилдиимидазол и тиофосген, в растворителе, выбранном из группы, включающей дихлорметан, диоксан и ДМФ, при температурах 0-150 С и необязательно в присутствии основания, которым предпочтительно является ДМАП или ТЭА, с получением соединения формулы XI(4) реакция соединения формулы XI с соединением формулы XIIIN,N'-диизопропилкарбодиимид (ДИК); в растворителе, выбранном из группы, включающей диэтиловый эфир (Et2O), диметилформамид (ДМФ), дихлорметан (ДХМ), ацетонитрил (MeCN) и тетрагидрофуран(ТГФ), предпочтительно при температуре от 0 до 100 С. Другим объектом настоящего изобретения являются промежуточные соединения формул XI, XVII,XIX и XX: в которых R1 и R2 независимо обозначают галоген, -C1-C3-алкил, где последняя алкильная группа необязательно замещена одним или более атомами фтора;W обозначает -C(O)-, -C(O)O-, где эти группы присоединены к атому азота фрагмента -NH- через атом углерода; М обозначает -C1-C6-алкил, -C3-C7-циклоалкил, обе эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -NH(C1-C2-алкил), -N(C1-C2-алкил)2,-O-C1-C3-алкила, -C1-C5-алкила, -C3-C4-циклоалкила, где в последних трех группах алкильные или циклоалкильные группы необязательно замещены одним или более атомами фтора; или оксетанил-, тетрагидрофуранил-, тетрагидропиранил-, азетидинил-, пирролидинил-, пиперидинил-,все эти группы необязательно содержат один или более заместителей, выбранных из фтора, -CN,-C1-C3-алкила, где последняя алкильная группа необязательно замещена одним или более атомами фтора; или фенил-, пиридил-, тиенил-, пирролил-, пиразолил-, имидазолил-, тиазолил-, оксазолил- или изоксазолил-, все эти группы необязательно содержат один или более заместителей, выбранных из галогена, CN или -C1-C3-алкила, где последняя алкильная группа необязательно дополнительно замещена одним или более атомами фтора. Второй вариант осуществления в качестве предпочтительных промежуточных соединений включает соединения формул XIb, XIc, XVIIb, XVIIc, XIX и XX: в которых R1 и R2 независимо обозначают хлор, фтор или -CH3; М обозначает метил, этил, пропил, изопропил, н-бутил, втор-бутил, трет-бутил, циклопропил,-CH2-циклопропил, циклобутил, циклопентил, все эти группы необязательно замещены одной или более группами, выбранными из -F, -ОН, -CN, -NH2, -OCH3, -CH3, -CF3; или выбран из следующих групп: все эти группы необязательно содержат один или более заместителей, выбранных из -F, -CH3 или-CF3; или выбран из следующих групп: все эти группы необязательно содержат один или более заместителей, выбранных из -F, -Cl, -CH3 или -CF3. Другой вариант осуществления в качестве более предпочтительных промежуточных соединений включает соединения формул XIb, XIc, XVIIb, XVIIc, XIX и XX, а именно: Биологические исследования. Выработка белка mPGES. Микросомы бактерии Е.coli штамма Rosetta, экспрессирующей рекомбинантный mPGES-1 человека, можно получить так, как описано ниже. 5 мл лизогенного бульона (ЛБ), содержащего ампициллин (50 мкг/мл) и хлорамфеникол(34 мкг/мл), инокулируют бактериями замороженной культуры. Инкубируют при 200 об/мин при 37 С в течение 8 ч. Затем 500-1000 мл ЛБ, содержащего ампициллин и хлорамфеникол, инокулируют с помощью 5 мл культуры и выращивают до OD640, составляющего 0,8-1,0. Перед индуцированием культуру охлаждают до 4 С. Культуру индуцируют с помощью IPTG (изопропилтиогалактозид) при конечной концентрации 400 мкМ. Белок экспрессируют при встряхивании при 200 об/мин при комнатной температуре, 18-23 С, в течение ночи. На следующий день можно провести следующие стадии. 1. Клетки осаждают в колбах для центрифугирования объемом 250 мл при 7000 об/мин в течение 15 мин (центрифуга Beckmann Coulte Avanti J-E). 2. Таблетки, полученные из 250 мл культуры, растворяют в 12,5 мл буфера для гомогенизации(15 мМ Tris-HCl (Tris = трис-(гидроксиметиламинометан), рН 8, 1 мМ ЭДТК (этилендиаминтетрауксусная кислота), рН 8, 0,25 мМ сахароза, 2,5 мМ GSH (глутатион), 1 таблетка ингибитора протеазы в 50 мл буфера). 3. Клетки диспергируют с помощью обработки ультразвуком в течение 510 с при амплитуде, составляющей 48%, в устройстве для обработки ультразвуком при мощности 750 Вт. 4. Добавляют 2,5 мл MgCl2 (100 мМ) и 12,5 мкл (0,8 мг/мл) DNase (дезоксирибонуклеаза) и инкубируют на льду в течение 30 мин. 5. Остатки бактерий осаждают при 7000 об/мин в течение 15 мин и собирают надосадочную жидкость. 6. Мембраны, содержащие белок, отделяют от надосадочной жидкости с помощью ультрацентрифугирования при 120000g при 4 С в течение 2 ч (ротор Sorvall T880). 7. Надосадочную жидкость отбрасывают и таблетки растворяют в 20 мМ калий-фосфатном буфере со значением рН 7,4 (KH2PO4 и K2HPO4), с помощью обработки ультразвуком (510 с, амплитуда 30%, в устройстве для обработки ультразвуком при мощности 50 Вт) и фермент делят на аликвоты и хранят при-80 С. Перед проведением каждого эксперимента размораживают аликвоту фермента и затем разводят в 0,1 М калий-фосфатном буфере со значением рН 7,4 (KH2PO4 и K2HPO4), содержащем 2,5 мкМ GSH. Исследование с использованием фермента mPGES-1. Целью этого исследования является определение сродства исследуемого соединения к ферментуmPGES-1. 47 мкл рекомбинантного mPGES-1 человека (0,5 мкг белка/лунка), содержащего микросомальную суспензию, в буфере, содержащем GSH (2,5 ммоль/л восстановленного L-глутатиона, разведенного в 0,1 моль/л фосфатного буфера, рН 7,4), помещают в 384-луночный планшет и затем добавляют 1 мкл исследуемого соединения (соединений) и инкубируют при комнатной температуре в течение 25 мин. Ферментативную реакцию инициируют путем добавления 2 мкл PGH2 (конечная концентрация 2 мкМ),растворенного в безводном диглиме. Через 60 с реакцию останавливают путем добавления останавливающего раствора, содержащего FeCl2 (10 мкл, 0,074 моль/л FeCl2). Образцы разводят в ЗФФ (забуференный фосфатом физиологический раствор) в отношении 1:25. 10 мкл разведенных образцов переносят в малообъемный 384-луночный планшет. Для определения количества образовавшегося PGE2 проводят детектирование PGE2 с помощью однородной флуоресценции с разрешением по времени (HTRF) с использованием имеющегося в продаже набора, выпускающегося фирмой CisBio, в соответствии с инструкциями изготовителя. Это исследование, основанное на использовании HTRF, подробно описано (см. публикацию: Goedken et al., J Biomol Screen, 2008, 13(7), 619-625). Вкратце, методика заключается в следующем: разведенные образцы смешивают с 5 мкл конъюгата PGE2-d2 и 5 мкл конъюгата криптата с анти-PGE2. После инкубирования планшетов в течение ночи флуоресценцию исследуют с использованием соответствующего устройства считывания микропланшетов. Измеряют интенсивность флуоресценции криптата европия (maxex = 307 нм (длина волны возбуждения), maxem = 620 нм (длина волны испускания и PGE2-d2 (maxex = 620 нм, maxem = 665 нм). Конкретные значения HTRF (резонансный перенос энергии флуоресценции) определяют как отношение интенсивности испускания при длине волны 665 нм к интенсивности испускания при длине волны 620 нм, при длине волны импульса возбуждения 320 нм. Планшет для количественного анализа также содержит лунки с PGE2 при различных концентрациях для построения калибровочного графика, предназначенного для расчета концентраций PGE2 по значениям отношений, полученных с помощью HTRF. Во всех исследованиях с использованием фермента mPGES из результатов вычитают фоновое значение и рассчитывают IC50 с помощью нелинейного регрессионного анализа с использованием обычного программного обеспечения. Таблица А Ингибирующее воздействие соединений на mPGES-1 (значения IC50 указаны в нМ) по данным исследования с использованием фермента Исследование с использованием клеток А 549. Несмотря на то что исследование с использованием фермента является высокопроизводительным исследованием, его недостаток заключается в том, что в нем используют рекомбинантный белок, который находится не в его естественной среде. В соответствии с этим разработано исследование с использо- 19021433 ванием клеток, в котором используют линию клеток, полученных от человека (А 549), экспрессирующих белок mPGES-1. Кроме того, для моделирования ситуации, наблюдающейся у людей, у которых соединения могут связываться с белками плазмы, в среду для исследования добавляют 50% сыворотки человека. При использовании комбинации исследуемого mPGES-1 в клеточной среде и присутствия 50% сыворотки человека это исследование является более значимым для определения перспективы терапевтического применения ингибитора mPGES по сравнением с исследованием с использованием только фермента. Клетки А 549 (АТСС: CCL-185) выращивают до слияния, составляющего примерно 90%, в смеси питательных веществ F-12K (среда Kaighn, Gibco), содержащей 10% ФБС (фетальная бычья сыворотка) в инкубаторе с увлажнением при 37 С и в атмосфере, содержащей 5% СО 2. Клетки отделяют с помощью смеси трипсин-ЭДТК. Клетки А 549 высевают в 384-луночный коллагеновый планшет при плотности 7000 клеток/лунка (50 мкл), в среде F-12, содержащей 1% смеси пенициллин-стрептомицин и 50% сыворотки человека. Клеткам дают прилипнуть в течение 3-4 ч. Затем клетки инкубируют в течение 20-24 ч в среде F-12k, к которой добавлены 50% сыворотки человека, 1% смеси пенициллин-стрептомицин и которая содержит IL-1 при конечной концентрации 5 нг/мл, а также 10 нМ арахидоновой кислоты, в присутствии растворителя или исследуемого соединения. Общий объем составляет 100 мкл. Концентрации PGE2 в бесклеточной среде (10 мкл) измеряют с использованием имеющегося в продаже набора для HTRF, выпускающегося фирмой CisBio (так, как описано выше). Количество PGE2, образовавшееся при отсутствии исследуемого соединения, принимают за 100%. Значения IC50 получают из 6-8 результатов, полученных путем титрования, с использованием обычного программного обеспечения. Соединения, перечисленные в табл. В, эффективно блокируют образование PGE2. Поэтому предполагается, что соединения формулы I могут обладать перспективой терапевтического применения для лечения воспалительных заболеваний и связанных патологических состояний, таких как воспалительная/ноцицептивная боль. Таблица В Ингибирующее воздействие соединений на mPGES-1(значения IC50 указаны в нМ) по данным исследования с использованием клеток Данные, приведенные в табл. А-С, показывают, что соединения, обладающие сходным сродством к ферменту mPGES-1, определенным в исследовании с использованием фермента, могут обладать другой активностью по данным исследования с использованием клеток. Предполагается, что сравнение результатов, полученных в фармакологическом исследовании с использованием клеток, с результатами, полученными в исследовании с использованием фермента, позволяет лучше предсказать и рассчитать терапевтически активные концентрации/дозы. Соединения, предлагаемые в настоящем изобретении, обладают высокой активностью по данным обоих исследований. Следовательно, вероятно, что они являются более подходящими для применения in vivo. Способ лечения. Настоящее изобретение относится к соединениям формулы I, которые применимы для предупреждения и/или лечения заболевания и/или патологического состояния, в котором ингибирование простагландин-Е-синтаз, в частности микросомной простагландин-Е 2-синтазы-1 (mPGES-1), оказывает благоприятное терапевтическое воздействие, включая, но не ограничиваясь только ими, лечение и/или предупреждение воспалительных заболеваний и/или связанных патологических состояний. Термин "воспаление" следует понимать, как включающий любое воспалительное заболевание, нарушение или патологическое состояние само по себе, любое патологическое состояние, которое включает связанный с ним воспалительный компонент, и/или любое патологическое состояние, характеризующееся воспалением в качестве симптома, включая, в частности, острое, хроническое, язвенное, специфическое, аллергическое и некротическое воспаление, и другие формы воспаления, известные специалистам в данной области техники. Таким образом, для задач настоящего изобретения этот термин также включает воспалительную боль, боль в целом и/или лихорадку. В случае, если патологическое состояние включает связанный с ним воспалительный компонент или патологическое состояние характеризуется воспалением в качестве симптома, специалист в данной области техники должен понимать, что соединения, предлагаемые в настоящем изобретении, можно применять для устранения симптомов воспаления и/или лечения воспаления, связанного с патологическим состоянием. Соединения, предлагаемые в настоящем изобретении, также могут влиять на проявления, не связанные с воспалением, например уменьшать потерю костной массы у субъекта. Такие патологические состояния включают остеопороз, остеоартрит, болезнь Педжета и/или периодонтальные заболевания. Другим объектом настоящего изобретения является применение соединения формулы I в качестве лекарственного средства. Другим объектом настоящего изобретения является применение соединений формулы I для лечения и/или предупреждения заболевания и/или патологического состояния, в котором ингибированиеmPGES-1 оказывает благоприятное терапевтическое воздействие. Другим объектом настоящего изобретения является применение соединения формулы I для лечения и/или предупреждения воспалительных заболеваний и/или связанных патологических состояний. Настоящее изобретение также относится к применению соединений формулы I для лечения и/или предупреждения следующих заболеваний и патологических состояний. 1. Ревматические заболевания, или аутоиммунные заболевания, или скелетно-мышечные заболевания: все формы ревматических заболеваний, включая, например, ревматизм мягких тканей, ревматоидный артрит, ревматическую полимиалгию; реактивный артрит, теносиновит, подагра или обменный артрит, бурсит, тендинит, хронический полиартрит у детей, спондилоартропатия, такая как, например,спондилит, анкилозирующий спондилоартрит, псориатическая артропатия; саркоидоз, фибромиалгия,миозит, полимиозит, остеоартрит, травматический артрит, коллагенозы любой этиологии, например, системная красная волчанка, склеродермия, дерматомиозит, болезнь Стилла, синдром Шегрена, синдром Фелти; ревматический полиартрит и ревматическая болезнь сердца, заболевания кровеносных сосудов,такие как васкулит, нодозный полиартрит, синдром Бехчета, гигантоклеточный артрит, гранулематоз Вегенера, пурпура Шенлейна-Геноха; псориатический артрит, грибковый артрит, в частности включая боль, связанную с любым из вышеуказанных патологических состояний. 2. Головная боль, такая как мигрень с аурой и без нее, головная боль напряжения, сильная приступообразная головная боль с периодическими рецидивами и головная боль различной этиологии. 3. Симпатически поддерживаемая боль, такая как комплексный региональный болевой синдром типа I и II. 4. Невропатическая боль, такая как боль в нижней части спины, боль в бедре, боль в ноге, негерпетическая невралгия, постгерпетическая невралгия, диабетическая невропатия, боль, вызванная поражением нерва, невропатическая боль, связанная с синдромом приобретенного иммунодефицита (СПИД),травма головы, поражения нервов, вызванные токсином и химиотерапией, фантомные боли в ампутированных конечностях, рассеянный склероз, травматический вывих зуба, болезненная травматическая мононевропатия, болезненная полиневропатия, синдром таламической боли, боль после удара, поражение центральной нервной системы, послеоперационная боль, запястный синдром, тригеминальная невралгия,постмастэктомический синдром, постторакотомический синдром, боль в культе, повторяющаяся боль при движении, невропатическая боль, связанная с гипералгезией и аллодинией, боль, обусловленная алкоголизмом и другая обусловленная действием лекарственных средств боль. 5. Боль, вызванная раком или связанная с опухолями, такими как опухоли костей, лимфолейкоз; болезнь Ходжкина, злокачественная лимфома; лимфогранулематоз; лимфосаркома; солидные злокачественные опухоли; обширные метастазы. 6. Нарушения внутренних органов, такие как хроническая тазовая боль, панкреатит, пептическая язва, интерстициальный цистит, цистит, почечная колика, ангина, дисменорея, менструация, гинекологическая боль, синдромом раздраженной толстой кишки, воспалительная болезнь кишечника, болезнь Крона и язвенный колит, нефрит, простатит, вульводиния, неязвенная диспепсия, экстракардиальная боль в груди, боль, ишемия миокарда. 7. Связанные с воспалением заболевания уха, носа, рта и горла, такие как грипп, и вирусные/бактериальные инфекции, такие как простуда, аллергический ринит (сезонный и круглогодичный),фарингит, тонзиллит, гингивит, ларингит, синусит и вазомоторный ринит, лихорадка, сенная лихорадка,тиреоидит, отит, патологические состояния зубов, такие как зубная боль, периоперационные и постоперационные патологические состояния, тригеминальная невралгия, увеит; ирит, аллергический кератит,конъюнктивит, блефарит, неврит зрительного нерва, хориоидит, глаукома и симпатическая офтальмия, а также боль, связанная с этими заболеваниями. 8. Неврологические заболевания, такие как отек головного мозга и ангионевротический отек, деменция головного мозга, такая как, например, болезнь Паркинсона и болезнь Альцгеймера, старческое слабоумие; рассеянный склероз, эпилепсия, эпилепсия, устойчивая к лекарственным средствам, удар,злокачественная миастения, инфекции мозга и мозговой оболочки, такие как энцефаломиелит, менингит,- 23021433 включая ВИЧ (вирус иммунодефицита человека), а также шизофрения, бредовые нарушения, аутизм,аффективные расстройства и связанные с тиком нарушения. 9. Профессиональные заболевания, такие как пневмокониоз, включая алюминоз, антракоз, асбестоз,халикоз, птилоз, сидероз, силикоз, табакоз и биссиноз. 10. Заболевания легких, такие как астма, включая аллергическую астму (атопическую и неатопическую), а также бронхостеноз напряжения, профессиональную астму, вирусное или бактериальное обострение астмы, другие неаллергические типы астмы и "бронхит младенцев", хроническое обструктивное заболевание легких (ХОЗЛ), включая эмфизему, респираторный дистресс-синдром у взрослых, бронхит,пневмонию, респираторный дистресс-синдром у взрослых, болезнь голубятников, аллергический альвеолит у сельскохозяйственных рабочих. 11. Заболевания кожи, такие как псориаз и экзема, дерматит, солнечный ожог, ожоги, а также растяжения связок и сухожилий и травмы тканей. 12. Сосудистые или сердечные заболевания, которые связаны с воспалением, такие как артериосклероз, включая атеросклероз, связанный с трансплантами сердца, нодозный панартериит, нодозный периартериит, преходящий артериит, гранулематоз Вегенера, гигантоклеточный артрит, реперфузионное поражение и нодозная эритема, тромбоз (например, тромбоз глубоких вен, тромбоз почечной, печеночной, воротной вены); заболевание коронарной артерии, аневризма, отторжение трансплантата сосудов,инфаркт миокарда, эмболия, удар, тромбоз, включая венозный тромбоз, стенокардия, включая нестабильную стенокардию, воспаление, связанное с коронарными бляшками, вызванное бактериями воспаление, включая воспаление, вызванное хламидиями, вызванное вирусами воспаление и воспаление, связанное с хирургическими операциями, такими как операция по установке трансплантата сосудов, включая операцию аортокоронарного шунтирования, операции по замене кровеносных сосудов, включая ангиопластику, установку стента, эндартерэктомию, или другие инвазивные процедуры, в которые вовлечены артерии, вены и капилляры, рестеноз артерии. 13. Симптомы, связанные с диабетом, такие как диабетическая васкулопатия, диабетическая невропатия, диабетическая ретинопатия, последующая резистентность капилляров, или симптомы диабета,связанные с инсулином (например, гипергликемия, диурез, протеинурия и повышенное выведение нитритов и калликреина с мочой). 14. Доброкачественные и злокачественные опухоли и неоплазия, включая рак, такой как колоректальный рак, рак мозга, рак кости, эпителиальную образовавшуюся в клетках неоплазию (эпителиальная карцинома), такую как базальноклеточную карциному, аденокарциному, желудочно-кишечный рак, такой как рак губы, рак полости рта, рак пищевода, рак тонкой кишки, рак желудка, колоректальный рак,рак печени, рак мочевого пузыря, рак поджелудочной железы, рак яичников, рак шейки матки, рак легких, рак молочной железы, рак кожи, такой как плоскоклеточный и базально-клеточный рак, рак предстательной железы, почечно-клеточная карцинома, и другие известные типы рака, влияющие на эпителиальные клетки всего организма; неоплазии, такие как желудочно-кишечный рак, язва пищевода Баррета,рак печени, рак мочевого пузыря, рак поджелудочной железы, рак яичников, рак предстательной железы,рак шейки матки, рак легких, рак молочной железы и рак кожи; аденоматозный полипоз, включая наследственный аденоматозный полипоз (НАП), а также предупреждение образования полипов у пациентов с риском заболевания НАП. 15. Другие заболевания и патологические состояния, такие как эпилепсия, септический шок, например, при котором применяют антигиповолемические и/или антигипотензивные средства, сепсис, остеопороз, доброкачественную гиперплазию предстательной железы и гиперактивность мочевого пузыря,нефрит, прурит, витилиго, нарушения висцеральной подвижности в респираторной, мочеполовой, желудочно-кишечной или сосудистой системах, раны, аллергические реакции кожи, смешанные васкулярные и аваскулярные синдромы, септический шок, связанный с бактериальными инфекциями или с травмой,поражение центральной нервной системы, повреждения тканей и послеоперационная лихорадка, синдромы, сопровождающиеся зудом. В контексте настоящего изобретения предпочтительным является применение соединения формулыI для лечения и/или предупреждения боли; в частности боли, связанной с любым из приведенных выше заболеваний или патологических состояний. Другим объектом настоящего изобретения является способ лечения и/или предупреждения описанных выше заболеваний и патологических состояний, который включает введение человеку соединения формулы I в эффективном количестве. Дозировка. Диапазон доз соединений формулы I, вводимых в сутки, обычно составляет от 0,01 до 5000 мг,предпочтительно от 1 до 2000 мг, более предпочтительно от 5 до 500 мг, наиболее предпочтительно от 10 до 250 мг. Предпочтительно, если каждая дозированная форма содержит от 2 до 500 мг, предпочтительно от 5 до 250 мг. Реальное терапевтически эффективное количество или терапевтическая доза, разумеется, будет зависеть от факторов, известных специалистам в данной области техники, таких как возраст и масса тела пациента, путь введения и тяжесть заболевания. В любом случае комбинацию вводят в таких дозах и та- 24021433 ким образом, чтобы при этом в соответствии с индивидуальным состоянием пациента осуществлялась доставка фармацевтически эффективного количества. Фармацевтические препараты. Подходящие препараты для введения соединений формулы I известны специалистам с общей подготовкой в данной области техники, и они включают, например, таблетки, пилюли, капсулы, суппозитории, пастилки, лепешки, растворы, сиропы, эликсиры, облатки, средства для инъекции, средства для ингаляции, порошки и т.п. Содержание фармацевтически активного соединения (соединений) должно находится в диапазоне от 1 до 99 мас.%, предпочтительно от 10 до 90 мас.%, более предпочтительно от 20 до 70 мас.% от массы композиции в целом. Подходящие таблетки можно изготовить, например, путем смешивания одного или большего количества соединений формулы I с известными инертными наполнителями, например инертными разбавителями, носителями, разрыхлителями, вспомогательными веществами, поверхностно-активными веществами, связующими и/или смазывающими веществами. Таблетки также могут содержать несколько слоев. Другим объектом настоящего изобретения является фармацевтический препарат, включающий соединение формулы I в смеси с фармацевтически приемлемым вспомогательным веществом, разбавителем или носителем. Комбинированная терапия. Соединения, предлагаемые в настоящем изобретении, можно использовать в комбинации с другими известными средствами лечения, использующимися в данной области техники в связи с лечением любого из патологических состояний, лечение которого является задачей настоящего изобретения. В число таких средств лечения, которые считаются подходящими для комбинации со способом лечения, предлагаемым в настоящем изобретении, входят: нестероидные противовоспалительные лекарственные средства (НСПВС), включая ингибиторы СОХ-2; антагонисты опиатного рецептора; антагонисты каннабиноидного рецептора или ингибиторы эндоканнабиноидного пути; блокаторы натриевых каналов; блокаторы кальциевых каналов N-типа; серотонинергические и норадренергические модуляторы; кортикостероиды; антагонисты гистаминового рецептора H1; антагонисты гистаминового рецептора Н 2; ингибиторы протонного насоса; антагонисты лейкотриена и ингибиторы 5-липоксигеназы; местные анестетики; агонисты и антагонисты VR1; агонисты никотинового ацетилхолинового рецептора; антагонисты рецептора Р 2 Х 3; агонисты и антагонисты NGF или антитела к NGF; антагонисты NK1 и NK2; антагонисты брадикинина В 1; антагонисты CCR2; ингибиторы iNOS, или nNOS, или eNOS; антагонисты NMDA; модуляторы калиевых каналов; модуляторы GABA; серотонинергические и норадренергические модуляторы; лекарственные средства для борьбы с мигренью; лекарственные средства для борьбы с невропатической болью, такие как прегабалин или дулоксетин. Указанный список не считается ограничивающим. Ниже приведены типичные примеры таких средств лечения. Нестероидные противовоспалительные лекарственные средства (НСПВС), включая ингибиторы СОХ-2: производные пропионовой кислоты (алминопрофен, беноксапрофен, буклоксиновая кислота,карпрофен, фенбуфен, фенопрофен, флурбипрофен, ибупрофен, индопрофен, кетопрофен, миропрофен,напроксен, оксапрозин, пирпрофен, пранопрофен, супрофен, тиапрофеновая кислота и тиоксапрофен),производные уксусной кислоты (индометацин, ацеметацин, алклофенак, клиданак, диклофенак, фенклофенак, фенклозиновая кислота, фентиазак, фурофенак, ибуфенак, изоксепак, окспинак, сулиндак, тиопинак, толметин, зидометацин и зомепирак), производные фенамовой кислоты (меклофенамовая кислота,мефенамовая кислота и толфенамовая кислота), производные бифенилкарбоновой кислоты, оксикамы нилбутазон), коксибы (целекоксиб, валекоксиб, рофекоксиб и эторикоксиб) и т.п. Противовирусные лекарственные средства, такие как ацикловир, теновир, плеконарил, перамивир,проконазол и т.п. Антибиотики, такие как гентамицин, стрептомицин, гелданамицин, дорипенем, цефалексин, цефаклор, цефтазихин, цефепим, эритромицин, ванкомицин, азтреонам, амоксициллин, бацитрацин, эноксацин, мафенид, доксициклин, хлорамфеникол и т.п. Антагонисты опиатного рецептора: морфин, пропоксифен (дарвон), трамадол, бупренорфин и т.п. Глюкокортикостероиды, такие как бетаметазон, будезонид, дексаметазон, гидрокортизон, метилпреднизолон, преднизолон, преднизон, триамцинолон и дефлазакорт. Иммунодепрессивные, иммуномодулирующие или цитостатические лекарственные средства, включая, но не ограничиваясь только ими, гидроксихлорохин, D-пеницилламин, сульфазалицин, ауранофин,препараты золота, меркаптопурин, такролимус, сиролимус, микофенолятмофетил, циклоспорин, лефлуномид, метотрексат, азатиоприн, циклофосфамид, глатирамерацетат, новантрон, финголимод (FTY720),миноциклин, талидомид и т.п. Антитела к TNF или антагонисты рецептора TNF, такие как, но не ограничивающиеся только ими,этанерцепт, инфликсимаб, адалимумаб (D2E7), CDP 571 и Ro 45-2081 (ленерцепт), или биологические средства, действие которых направлено на мишени, такие как, но не ограничиваясь только ими, CD-4,CTLA-4, LFA-1, IL-6, ICAM-1, C5, и натализумаб и т.п. Антагонисты рецептора IL-1, такие как, но не ограничиваясь только им, кинерет. Блокаторы натриевых каналов: карбамазепин, мексилетин, ламотригин, тектин, лакозамид и т.п. Блокаторы кальциевых каналов N-типа: зиконотид и т.п. Серотонинергические и норадренергические модуляторы: пароксетин, дулоксетин, клонидин, амитриптилин, циталопрам. Антагонисты гистаминового рецептора H1: бромфенирамин, хлорфенирамин, дексхлорфенирамин,трипролидин, клемастин, дифенгидрамин, дифенилпиралин, трипеленнамин, гидроксизин, метдиазин,прометазин, тримепразин, азатидин, ципрогептадин, антазолин, фенирамин, пириламин, астемизол, терфенадин, лоратадин, цетиризин, деслоратадин, фексофенадин, левоцетиридин и т.п. Антагонисты гистаминового рецептора Н 2: циметидин, фамотидин, ранитидин и т.п. Ингибиторы протонного насоса: омепразол, пантопразол, эзомепразол и т.п. Антагонисты лейкотриена и ингибиторы 5-липоксигеназы: зафирлукаст, монтелукаст, пранлукаст,зилеутон и т.п. Местные анестетики, такие как амброксол, лидокаин и т.п. Модуляторы калиевых каналов: такие как ретигабин. Модуляторы GABA: лакозамид, прегабалин, габапентин и т.п. Лекарственные средства для борьбы с мигренью: суматриптан, золмитриптан, наратриптан, элетриптан, телцегепант и т.п. Антитела NGF, такие как RI-724 и т.п. Комбинированная терапия также возможна в новых подходах к лечению боли, например, с помощью антагонистов Р 2 Х 3, антагонистов VR1, антагонистов NK1 и NK2, антагонистов NMDA, антагонистов mGluR и т.п. Комбинация соединений предпочтительно является синергетической комбинацией. Синергизм, как описано, например, в публикации Chou and Talalay, Adv. Enzyme Regul. 22:27-55 (1984), возникает в случае, если воздействие соединений при их введении в комбинации является более сильным, чем суммарное воздействие соединений при их введении по отдельности в виде отдельных средств. Обычно синергетический эффект наиболее четко проявляется при использовании соединений в субоптимальных концентрациях. Синергизм может проявляться в более низкой цитотоксичности, усиленном фармакологическом действии или каком-либо другом более благоприятном свойстве комбинации, по сравнению с отдельными компонентами. Экспериментальный раздел. Примеры получения соединений общей формулы I. Если не указано иное, то одну или более таутомерных форм соединений, приведенных в примерах,описанных ниже в настоящем изобретении, можно получить in situ и/или выделить. Все таутомерные формы соединений, приведенных в примерах, описанных ниже в настоящем изобретении, следует рассматривать, как раскрытые. Настоящее изобретение проиллюстрировано приведенными ниже примерами, в которых могут быть использованы следующие аббревиатуры. Аналитические методики. Для всех соединений, указанных ниже в примерах, получены корректные масс-спектры, соответствующие теоретическим спектрам изотопов. По практическим соображениям в качестве типичных результатов в масс-спектрах в каждом случае приведен только один из главных пиков изотопа. Данные ТСХ получают с использованием приведенных ниже пластин для ТСХ.a) Пластины с силикагелем 60 F254 Merck No 1.05714.0001, в экспериментальной части обозначены как "силикагель".b) Пластины для хроматографии с обращенной фазой: RP-8F 254s Merck No: 1.15684.0001, в экспериментальной части обозначены как "RP-8".c) Пластины с оксидом алюминия 60 F254 Merck 1.05713.0001, в экспериментальной части обозначены как "Alox". Приведенные значения Rf определяют без насыщения атмосферы камеры. Очистку с помощью флэш-хроматографии проводят с использованием силикагеля, выпускающегося фирмой Millipore (MATREX, 35-70 мкм), или Alox (E. Merck, Darmstadt, стандартизованный оксид алюминия 90, 63-200 мкм, Artikel-Nr: 1.01097.9050). Данные ВЭЖХ/МС, когда они приведены, получают при следующих условиях: ХО 1:Agilent HP 1200 с насосом для подачи двух компонентов, Agilent MS 6140, HiPALS1367C. Детектирование с помощью диодной матрицы проводят в диапазоне длин волн 190-400 нм. Диапазон масс-спектрометрического детектирования: от m/z 100 до m/z 1000. ХО 2:Waters SQD MS, Acquity UPLC. Детектирование с помощью диодной матрицы проводят в диапазоне длин волн 210-500 нм. Диапазон масс-спектрометрического детектирования: от m/z 120 до m/z 820. ХО 3:Agilent LC/MSD SL 61956 В; Agilent 1100; насос для подачи четырех компонентов. Детектирование с помощью диодной матрицы проводят в диапазоне длин волн 190-400 нм. Диапазон масс-спектрометрического детектирования: от m/z 100 до m/z 1000. ХО 4:Agilent HP 100 с насосом для подачи двух компонентов, Waters ZQ2000. Детектирование с помощью диодной матрицы проводят в диапазоне длин волн 210-500 нм. Диапазон масс-спектрометрического детектирования: от m/z 120 до m/z 820. ХО 5:Acquity UPLC, Waters SQD MS. Детектирование с помощью диодной матрицы проводят в диапазоне длин волн 210-500 нм. Диапазон масс-спектрометрического детектирования: от m/z 120 до m/z 820. Используют следующие методики (если не указано иное, температура колонки равна 25 С). Методика А (ХО 2). Неподвижная фаза (температура колонки: постоянная, 60 С): Sunfire C18, 2,5 мкм, 2,150 мм. Подвижная фаза: Е 1: вода с добавлением 0,1% НСООН, Е 2: MeCN с добавлением 0,1% НСООН. Элюирование в градиентом режиме:
МПК / Метки
МПК: A61K 31/4184, A61P 29/00, A61P 11/00, C07D 235/30
Метки: качестве, mpges-1, соединения, ингибиторов, микросомной, простагландин-е2-синтазы-1
Код ссылки
<a href="https://eas.patents.su/30-21433-soedineniya-v-kachestve-ingibitorov-mikrosomnojj-prostaglandin-e2-sintazy-1-mpges-1.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения в качестве ингибиторов микросомной простагландин-е2-синтазы-1 (mpges-1)</a>
Предыдущий патент: N-[3-(4-нитрофениламино)индол-2-илметилен]аминогуанидина гидрохлорид, обладающий противовоспалительной активностью
Следующий патент: Очистительное устройство
Случайный патент: Устройство обнаружения для ворот для регистрации объекта, пересекающего плоскость ворот












