Способы получения 3-бензазепинов
Номер патента: 16485
Опубликовано: 30.05.2012
Авторы: Эстрада Скотт А., Эйтс Шелли, Сенгупта Дипанджан, Рей Макс, Джилсон Чарльз А.III, Смит Брайан, Вайгль Ульрих, Бербаум Беверли В.
Формула / Реферат
1. Способ получения соединения формулы V
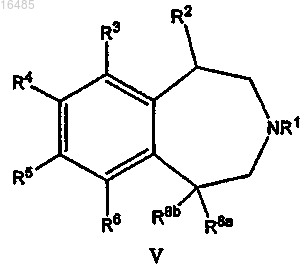
или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый независимо, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил;
включающий:
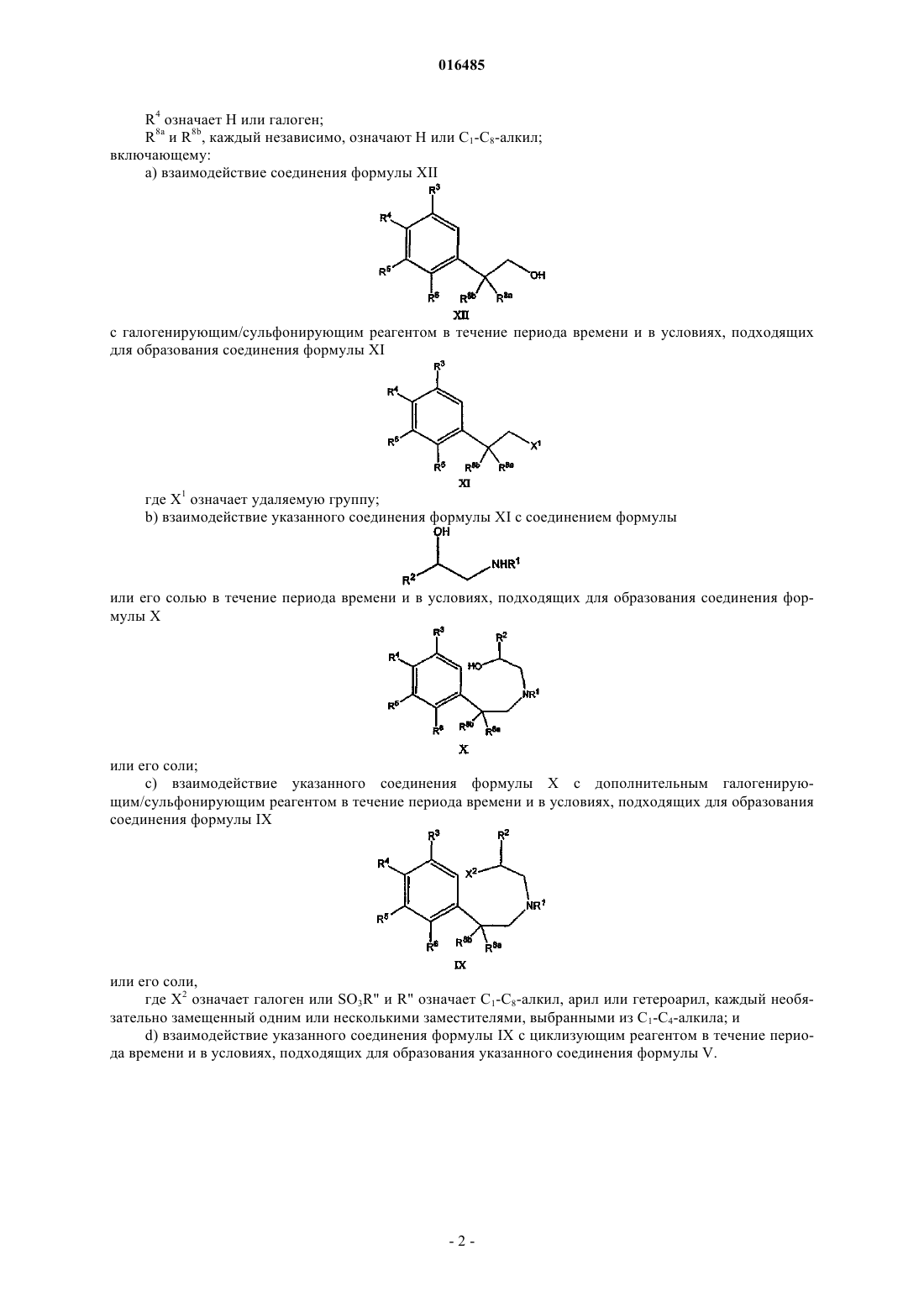
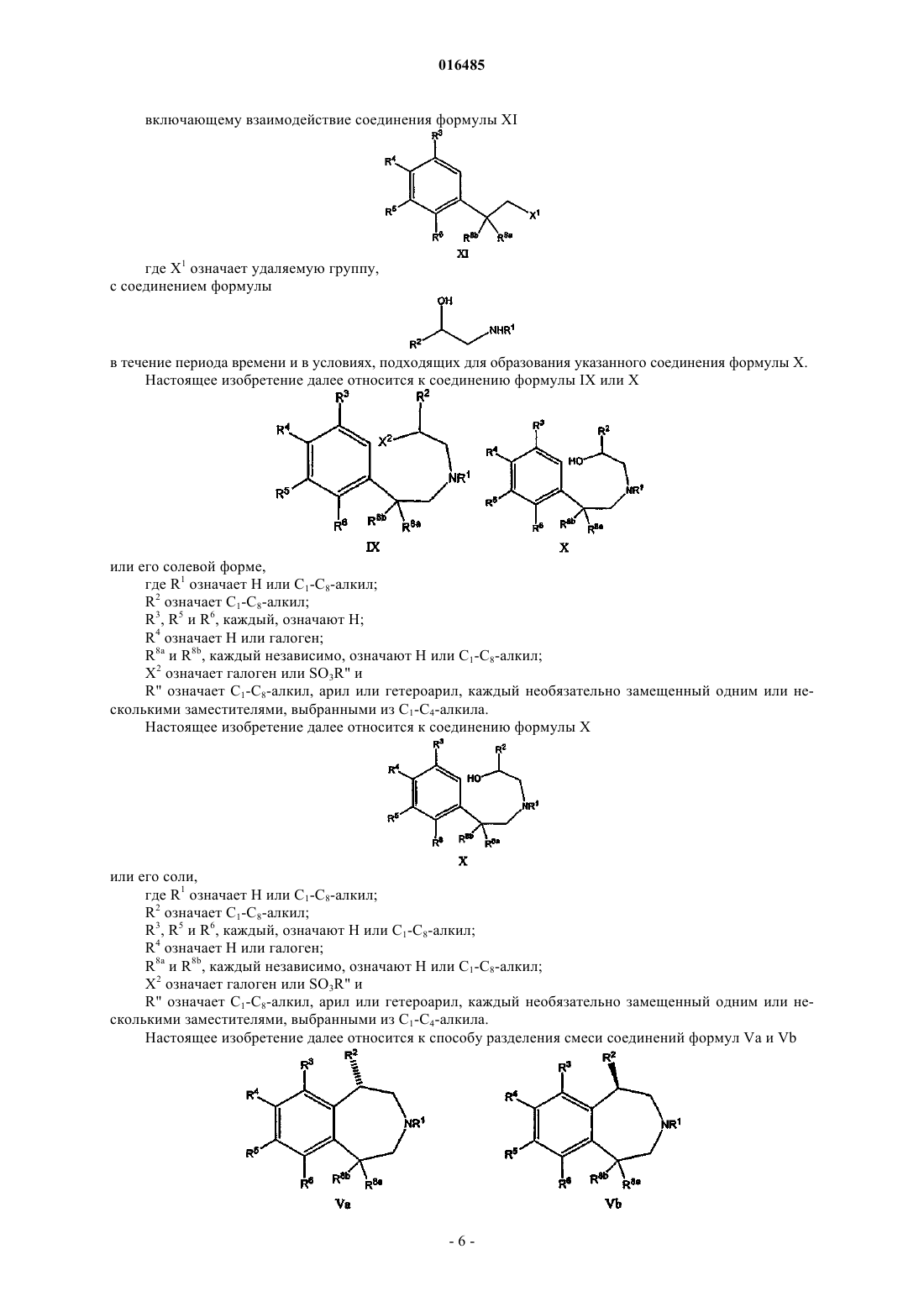
а) взаимодействие соединения формулы XII
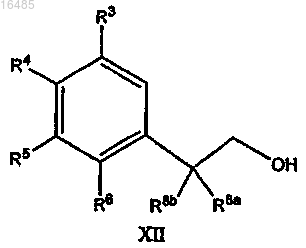
с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы XI
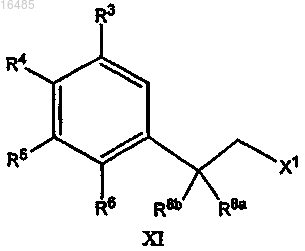
где X1 означает удаляемую группу;
b) взаимодействие указанного соединения формулы XI с соединением формулы
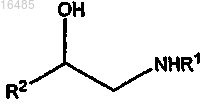
или его солью в течение периода времени и в условиях, подходящих для образования соединения формулы X
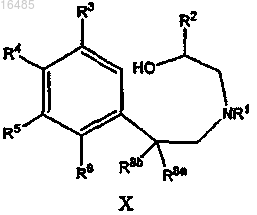
или его соли;
с) взаимодействие указанного соединения формулы X с дополнительным галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы IX
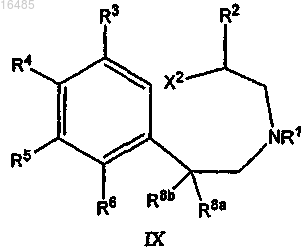
или его соли;
где X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; и
d) взаимодействие указанного соединения формулы IX с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V.
2. Способ по п.1, в котором указанным циклизующим реагентом является AlCl3.
3. Способ по п.1, в котором указанным галогенирующим реагентом является PBr3 или PCl3.
4. Способ по п.1, в котором указанным дополнительным галогенирующим/сульфонирующим реагентом является SOBr2 или SOCl2.
5. Способ по п.1, в котором X2 означает Br.
6. Способ по п.1, в котором X1 означает Br.
7. Способ по любому одному из пп.1-6, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R7a, R7b, R8a и R8b, каждый, означают Н.
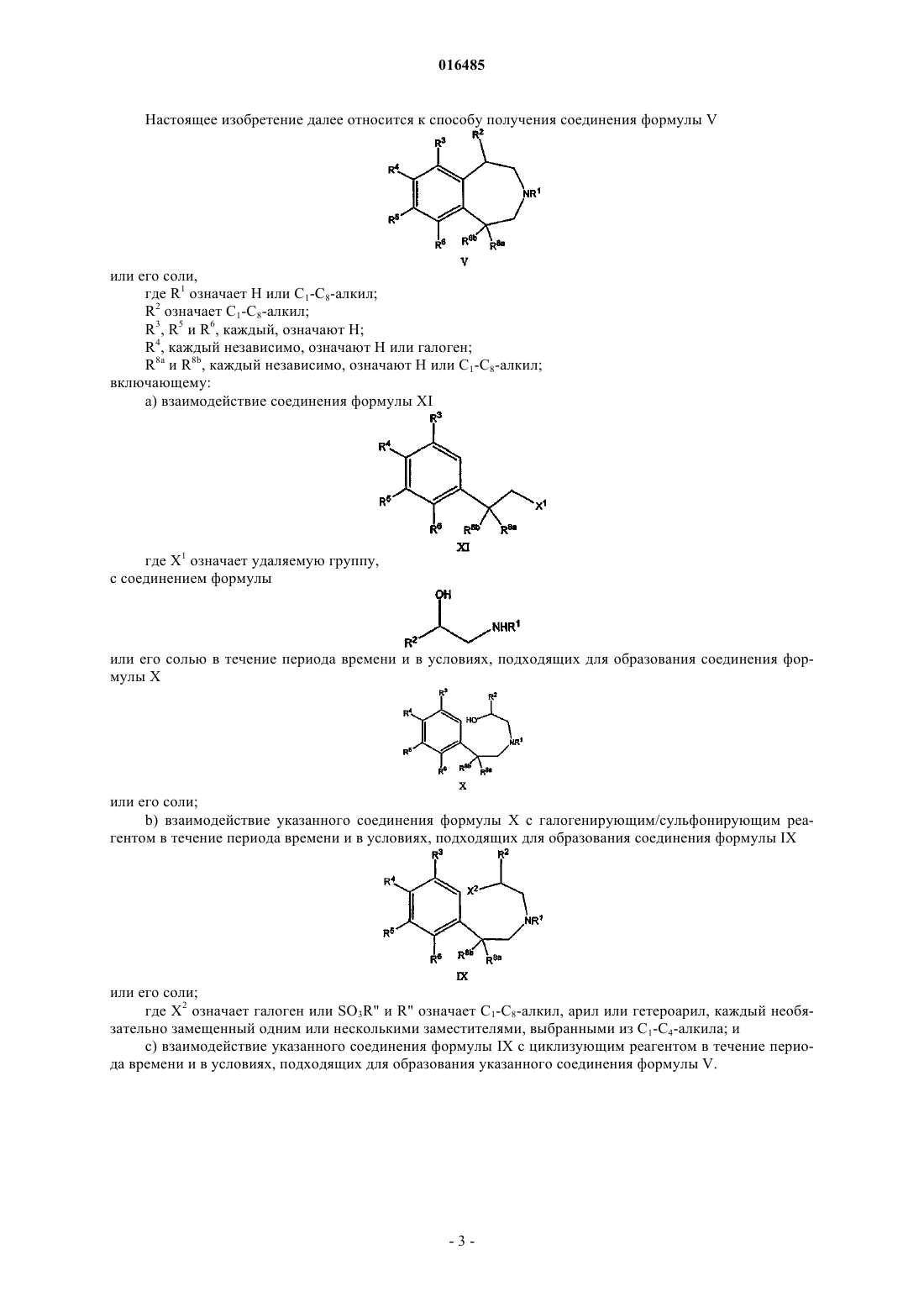
8. Способ получения соединения формулы V
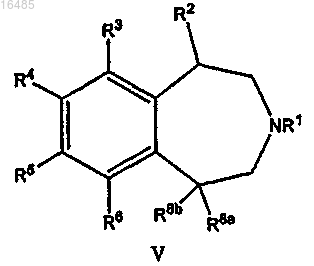
или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил,
включающий:
а) взаимодействие соединения формулы XI

где X1 означает удаляемую группу,
с соединением формулы
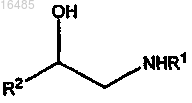
или его солью в течение периода времени и в условиях, подходящих для образования соединения формулы X
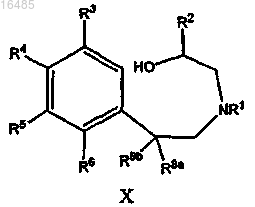
или его соли;
b) взаимодействие указанного соединения формулы X с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы IX
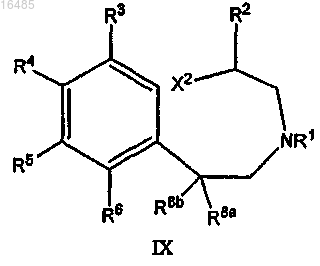
или его соли,
где X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; и
с) взаимодействие указанного соединения формулы IX с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V.
9. Способ по п.8, в котором указанным циклизующим реагентом является AlCl3.
10. Способ по п.8, в котором указанным галогенирующим реагентом является SOBr2 или SOCl2.
11. Способ по п.8, в котором X2 означает Cl.
12. Способ по п.8, в котором X1 означает Br.
13. Способ по любому одному из пп.8-12, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
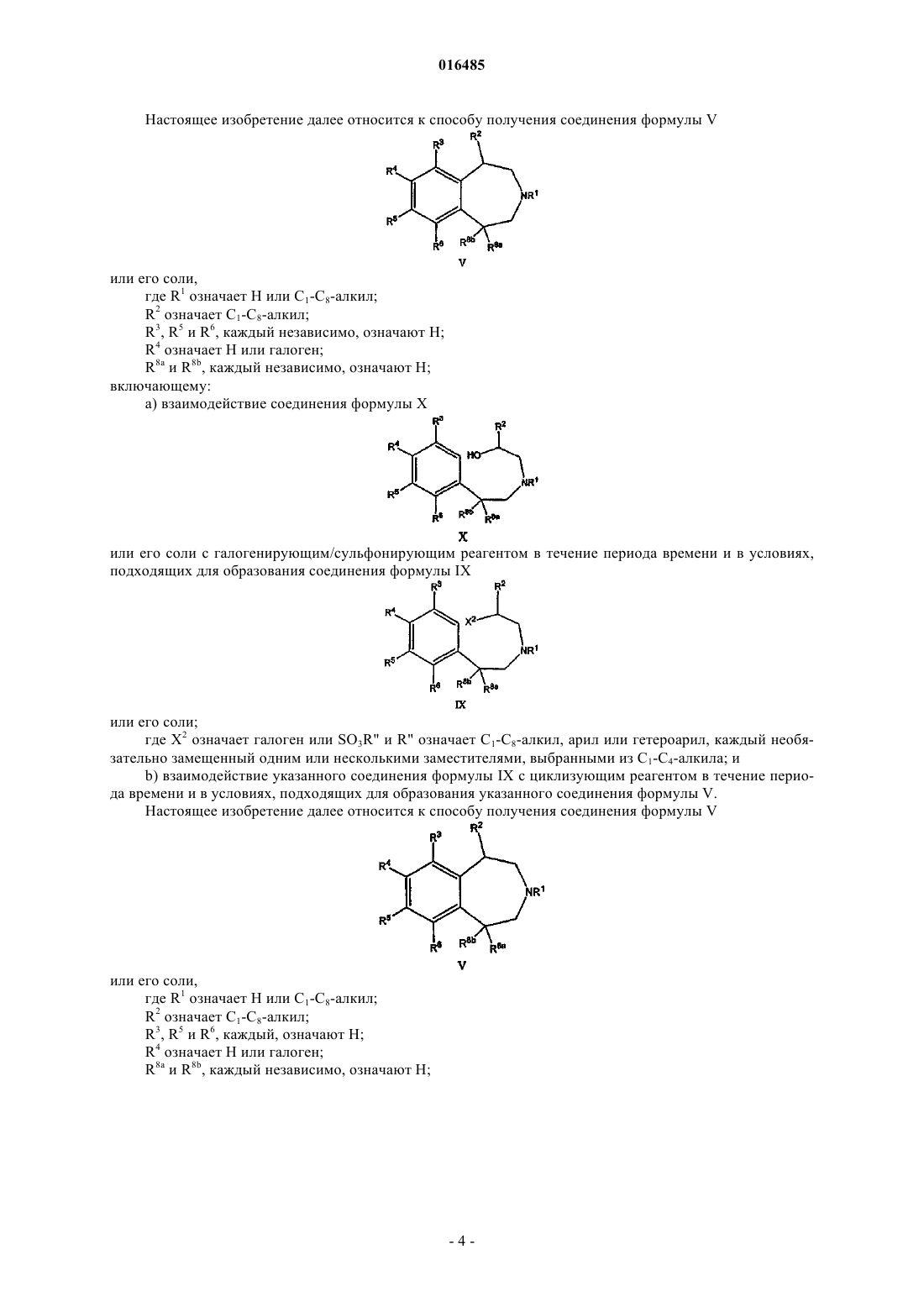
14. Способ получения соединения формулы V
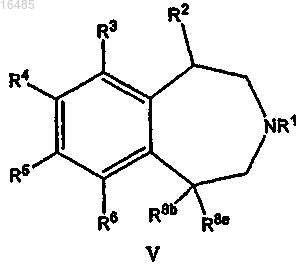
или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый независимо, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил,
включающий:
а) взаимодействие соединения формулы X
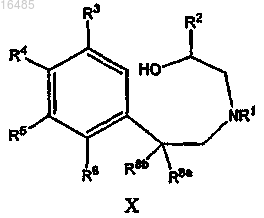
или его соли; с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы IX
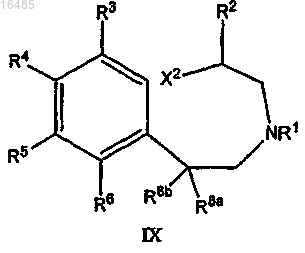
или его соли;
где X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; и
b) взаимодействие указанного соединения формулы IX с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V.
15. Способ по п.14, в котором указанным циклизующим реагентом является AlCl3.
16. Способ по п.14, в котором указанное взаимодействие на стадии (b) осуществляют в присутствии 1,2-дихлорбензола.
17. Способ по п.14, в котором указанным галогенирующим реагентом является SOBr2 или SOCl2.
18. Способ по п.14, в котором X2 означает Cl.
19. Способ по п.14, в котором указанное взаимодействие на стадии (а) осуществляют в присутствии растворителя.
20. Способ по п.19, в котором указанный растворитель содержит диметилформамид или толуол.
21. Способ по любому одному из пп.14-20, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
22. Способ получения соединения формулы V

или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил,
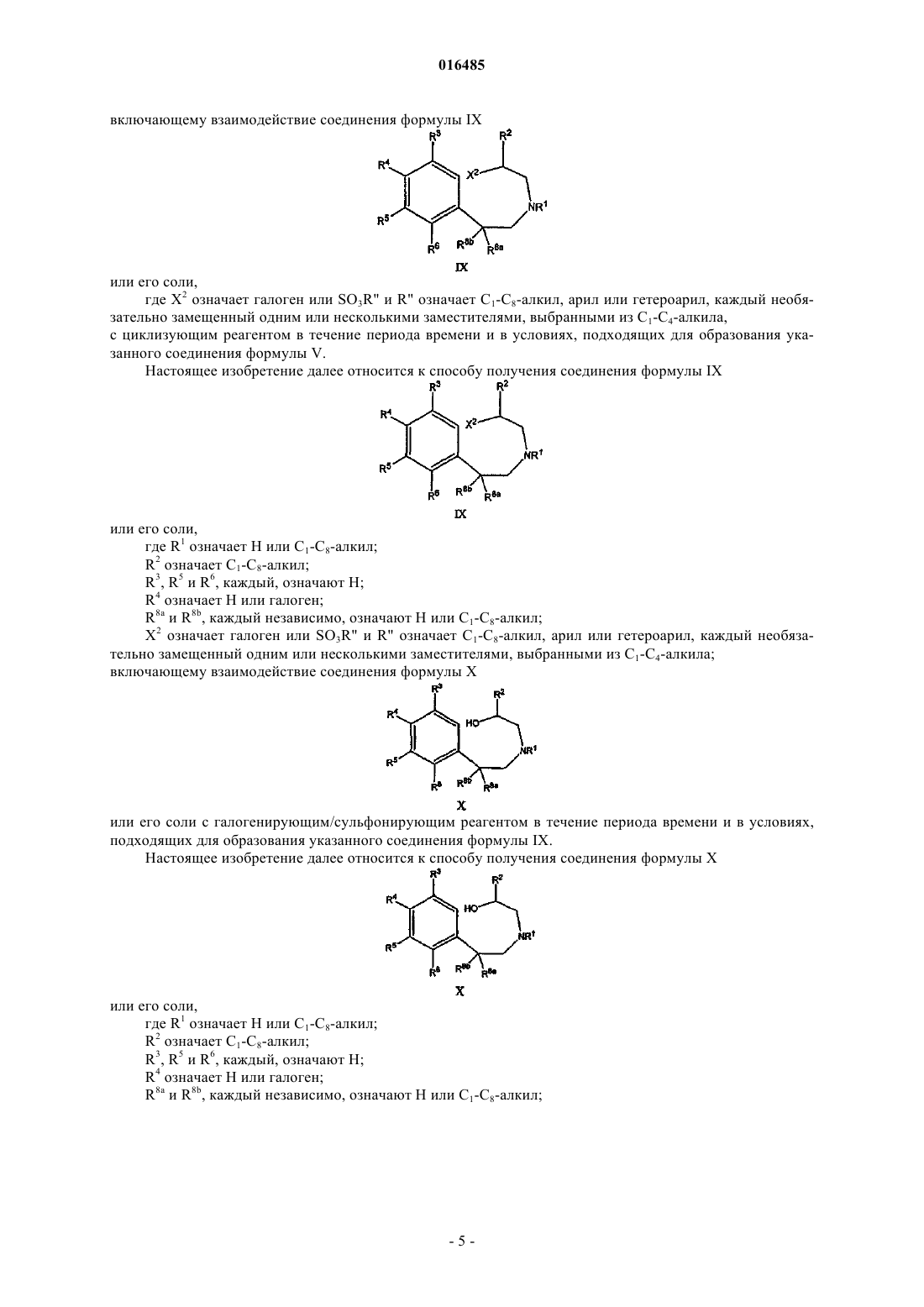
включающий взаимодействие соединения формулы IX
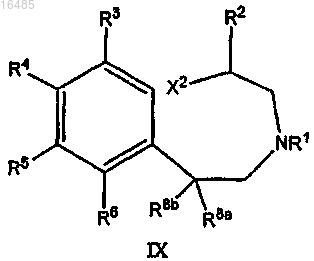
или его соли,
где X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила,
с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V.
23. Способ по п.22, в котором указанным циклизующим реагентом является AlCl3.
24. Способ по п.22, в котором указанное взаимодействие осуществляют в присутствии 1,2-дихлорбензола.
25. Способ по п.22, в котором указанное взаимодействие осуществляют при температуре примерно от 100 до 150°С.
26. Способ по п.22, в котором X2 означает Cl.
27. Способ по любому одному из пп.22-26, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
28. Способ получения соединения формулы IX
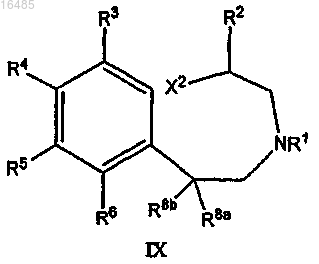
или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил;
X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила,
включающий взаимодействие соединения формулы X
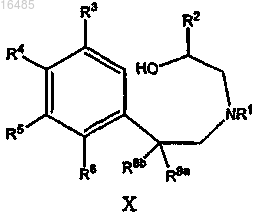
или его соли с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы IX.
29. Способ по п.28, в котором указанным галогенирующим/сульфонирующим реагентом является SOBr2 или SOCl2.
30. Способ по п.28, в котором X2 означает Br.
31. Способ по п.28, в котором X2 означает Cl.
32. Способ по п.28, в котором указанное взаимодействие осуществляют в присутствии растворителя, содержащего диметилформамид или толуол.
33. Способ по п.28, в котором указанная повышенная температура составляет примерно от -40 до 80°С.
34. Способ по любому одному из пп.28-33, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
35. Способ получения соединения формулы X
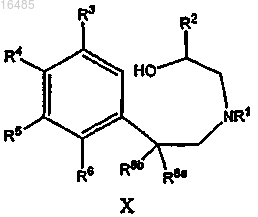
или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил,
включающий взаимодействие соединения формулы XI
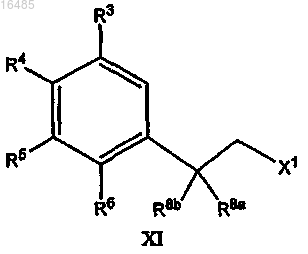
где X1 означает удаляемую группу,
с соединением формулы
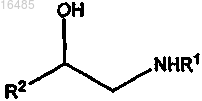
в течение периода времени и в условиях, подходящих для образования указанного соединения формулы X.
36. Способ по п.35, в котором X1 означает Br.
37. Способ по п.35, в котором указанная температура составляет примерно от 80 до 110°С.
38. Способ по любому одному из пп.35-37, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
39. Соединение формулы IX
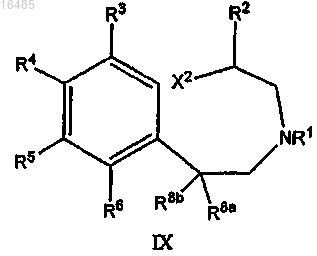
или его солевая форма,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил;
X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила.
40. Соединение по п.39, в котором X2 означает Cl.
41. Соединение формулы X

или его соли,
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н или C1-C8-алкил;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил;
X2 означает галоген или SO3R", R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила.
42. Соединение по п.40 или 41, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
43. Способ разделения смеси соединений формул Va и Vb:
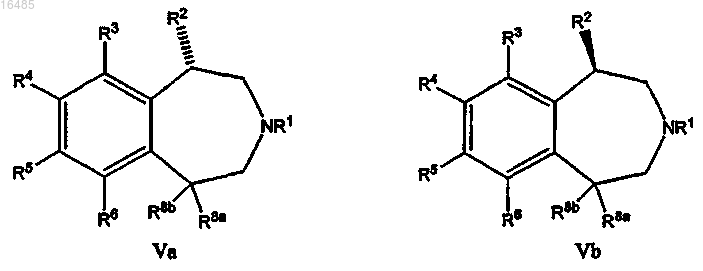
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н,
включающий
контактирование указанной смеси соединений с хиральной разделяющей кислотой с образованием солей хиральной разделяющей кислоты и указанных соединений, где указанная хиральная разделяющая кислота, главным образом, содержит один стереоизомер; и
осаждение указанных солей, образованных хиральной разделяющей кислотой и указанными соединениями, где получаемый в результате осадок обогащен солью хиральной разделяющей кислоты и одного из указанных соединений формулы Va или Vb.
44. Способ по п.43, в котором указанной хиральной разделяющей кислотой является винная кислота.
45. Способ по п.43, в котором указанной хиральной разделяющей кислотой является L-(+)-винная кислота.
46. Способ по п.43, в котором указанный осадок обогащен солью хиральной разделяющей кислоты и указанного соединения формулы Vb.
47. Способ по любому одному из пп.43-46, в котором R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
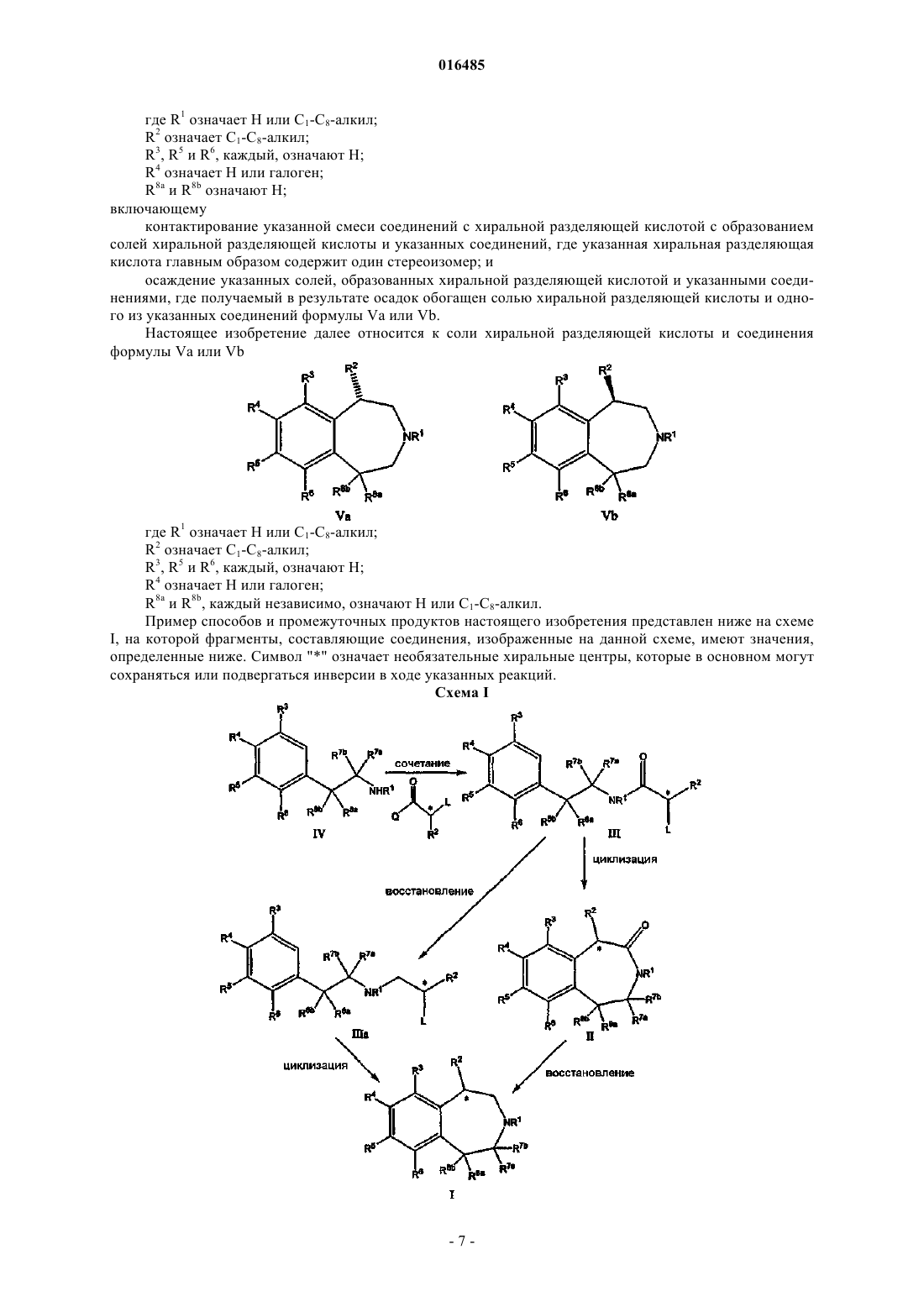
48. Соль хиральной разделяющей кислоты и соединения формулы Va или Vb:
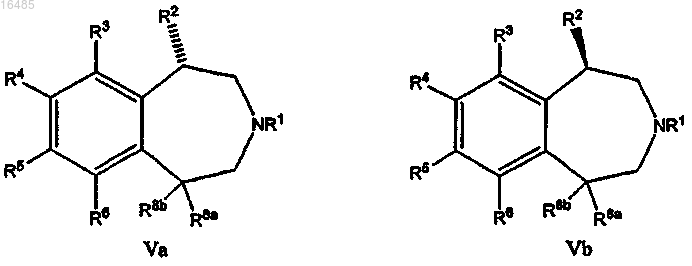
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил.
49. Соль по п.48, в котором указанной солью является соль винной кислоты.
50. Соль по п.48, в котором указанной винной кислотой является L-(+)-винная кислота.
51. Соль по п.48, имеющая формулу Vb.
52. Соль по любому одному из пп.48-51, в которых R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
53. Фармацевтическая композиция, содержащая по меньшей мере одну соль хиральной разделяющей кислоты по п.52.
54. Композиция по п.53, в которой указанная композиция содержит указанную виннокислую солевую форму соединения формулы Va и указанную виннокислую солевую форму соединения формулы Vb, где указанная композиция обогащена одной из форм: либо указанной виннокислой солевой формой соединения формулы Va, либо указанной виннокислой солевой формой соединения формулы Vb.
55. Соль хлористо-водородной кислоты и соединения формулы Va или Vb:
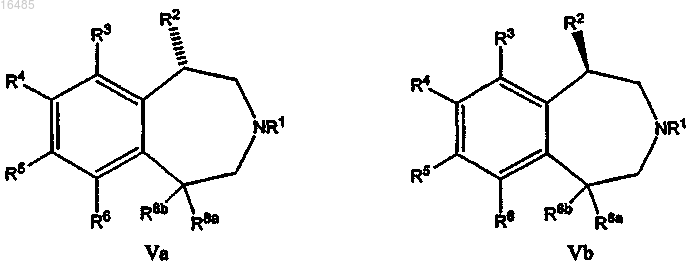
где R1 означает Н или C1-C8-алкил;
R2 означает C1-C8-алкил;
R3, R5 и R6, каждый, означают Н;
R4 означает Н или галоген;
R8a и R8b, каждый независимо, означают Н или C1-C8-алкил.
56. Соль по п.55, имеющая формулу Vb.
57. Соль по п.55 или 56, где R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R7a, R7b, R8a и R8b, каждый, означают Н.
58. Соль по п.55, имеющая формулу Vb, в которой R1 означает Н; R2 означает Me; R3 означает Н; R4 означает Cl; R5, R6, R8a и R8b, каждый, означают Н.
59. Композиция, содержащая по меньшей мере одну соль хлористо-водородной кислоты по п.58.
60. Способ лечения или профилактики 5-HT2C опосредованных заболеваний, включающий введение нуждающемуся пациенту терапевтически эффективного количества соли по п.58.
61. Способ лечения или профилактики ожирения, включающий введение нуждающемуся пациенту терапевтически эффективного количества соли по п.58.
62. Применение соединения по п.58 для производства лекарственного средства для применения для лечения 5-HT2C опосредованных заболеваний.
63. Применение соединения по п.58 для производства лекарственного средства для применения для лечения ожирения.
Текст
Настоящее изобретение относится к способам и промежуточным продуктам получения 3 бензазепинов и их солей, которые могут быть применимы в качестве агонистов рецептора серотонина (5-НТ) для лечения, например, расстройств центральной нервной системы, таких как ожирение. 016485 Область техники, к которой относится изобретение Настоящее изобретение, в общем, относится к способам и промежуточным продуктам получения 3-бензазепинов и их солей, которые могут быть полезны в качестве агонистов рецептора серотонина(5-HT) для лечения, например, расстройств центральной нервной системы, таких как ожирение. Уровень техники Нейропередача серотонина (5-HT) играет важную роль в многочисленных физиологических процессах как в здоровом состоянии, так и при психиатрических расстройствах. Например, 5-HT вовлечен в регуляцию пищевого поведения. Предполагается, что 5-HT оказывает действие, вызывая чувство наполнения или насыщения, так что поглощение пищи прекращается раньше и потребляется меньше калорий. Показано, что стимулирующее действие 5-HT на рецептор 5-HT2C играет важную роль в регуляции потребления пищи и эффекте D-фенфлурамина, направленном против ожирения. Так как рецептор 5-HT2C экспрессируется с высокой плотностью в головном мозге (особенно в лимбических структурах, экстрапирамидальных путях, таламусе и гипоталамусе, т.е. PVN и DMH, и преимущественно в хориоидном сплетении) и экспрессируется с низкой плотностью или отсутствует в периферических тканях, то избирательный агонист рецептора 5-HT2C может быть более эффективным и безопасным средством против ожирения. Также мыши, нокаутированные по 5-HT2C, имеют избыточный вес с когнитивным нарушением и подвержены судорожным припадкам. Таким образом, рецептор 5-HT2C считают хорошо подходящей рецепторной мишенью для лечения ожирения, психиатрических и других расстройств. Обнаружено, что 3-бензазепины являются агонистами рецептора 5-HT2C и проявляют эффективность в снижении ожирения на моделях животных (см., например, заявку на патент США 60/479280 и заявку на патент США 10/410991, каждая из которых включена в данное описание посредством ссылки во всей своей полноте). Сообщалось о различных путях синтеза 3-бензазепинов, и обычно в них используют фенилсодержащий исходный продукт, на котором строят амин- или амидсодержащую цепь,которая способна к циклизации с образованием конденсированного 7-членного кольца бензазепинового ядра. Синтез 3-бензазепинов и их промежуточных продуктов описан в заявке на патент США 60/479280 и заявке на патент США 10/410991, а также Nair et al., в Indian J. Chem., 1967, 5, 169;Hasan et al., Indian J. Chem., 1971, 9(9), 1022; Nagle et al., Tetrahedron Letters, 2000, 41, 3011; Robert, et al.,J. Org. Chem., 1987, 52, 5594 и Deady et al., J. Chem Soc., Perkin Trans. I, 1973, 782. Другие пути получения 3-бензазепинов и родственных соединений описаны Ladd et al., в J. Med.al., Bioorg. Med. Chem. Letters, 1992, 2, 399. Ввиду растущей потребности в соединениях для лечения расстройств, связанных с рецептором 5-HT2C, необходимы новые и более эффективные способы получения 3-бензазепинов. Способы и соединения, приведенные в данном описании, помогают удовлетворить указанные и другие потребности. Сущность изобретения Способы и промежуточные продукты настоящего изобретения полезны при получении терапевтических средств для лечения или профилактики опосредованных 5-HT расстройств, таких как ожирение и другие расстройства центральной нервной системы. Настоящее изобретение далее относится к способу получения соединения формулы VR8a и R8b, каждый независимо, означают Н или C1-C8-алкил; включающему: а) взаимодействие соединения формулы XII с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы XIb) взаимодействие указанного соединения формулы XI с соединением формулы или его солью в течение периода времени и в условиях, подходящих для образования соединения формулы X или его соли; с) взаимодействие указанного соединения формулы X с дополнительным галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы IX или его соли,где X2 означает галоген или SO3R" и R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; иd) взаимодействие указанного соединения формулы IX с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V.-2 016485 Настоящее изобретение далее относится к способу получения соединения формулы VR8a и R8b, каждый независимо, означают Н или C1-C8-алкил; включающему: а) взаимодействие соединения формулы XI или его солью в течение периода времени и в условиях, подходящих для образования соединения формулы Xb) взаимодействие указанного соединения формулы X с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы IX или его соли; где X2 означает галоген или SO3R" и R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; и с) взаимодействие указанного соединения формулы IX с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V.-3 016485 Настоящее изобретение далее относится к способу получения соединения формулы VR8a и R8b, каждый независимо, означают Н; включающему: а) взаимодействие соединения формулы X или его соли с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях,подходящих для образования соединения формулы IX или его соли; где X2 означает галоген или SO3R" и R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; иb) взаимодействие указанного соединения формулы IX с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V. Настоящее изобретение далее относится к способу получения соединения формулы V-4 016485 включающему взаимодействие соединения формулы IX или его соли,где X2 означает галоген или SO3R" и R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила,с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования указанного соединения формулы V. Настоящее изобретение далее относится к способу получения соединения формулы IXX2 означает галоген или SO3R" и R" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила; включающему взаимодействие соединения формулы X или его соли с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях,подходящих для образования указанного соединения формулы IX. Настоящее изобретение далее относится к способу получения соединения формулы X-5 016485 включающему взаимодействие соединения формулы XI в течение периода времени и в условиях, подходящих для образования указанного соединения формулы X. Настоящее изобретение далее относится к соединению формулы IX или X или его солевой форме,где R1 означает Н или C1-C8-алкил;X2 означает галоген или SO3R" иR" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила. Настоящее изобретение далее относится к соединению формулы XX2 означает галоген или SO3R" иR" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из C1-C4-алкила. Настоящее изобретение далее относится к способу разделения смеси соединений формул Va и VbR8a и R8b означают Н; включающему контактирование указанной смеси соединений с хиральной разделяющей кислотой с образованием солей хиральной разделяющей кислоты и указанных соединений, где указанная хиральная разделяющая кислота главным образом содержит один стереоизомер; и осаждение указанных солей, образованных хиральной разделяющей кислотой и указанными соединениями, где получаемый в результате осадок обогащен солью хиральной разделяющей кислоты и одного из указанных соединений формулы Va или Vb. Настоящее изобретение далее относится к соли хиральной разделяющей кислоты и соединения формулы Va или VbR8a и R8b, каждый независимо, означают Н или C1-C8-алкил. Пример способов и промежуточных продуктов настоящего изобретения представлен ниже на схемеI, на которой фрагменты, составляющие соединения, изображенные на данной схеме, имеют значения,определенные ниже. Символ означает необязательные хиральные центры, которые в основном могут сохраняться или подвергаться инверсии в ходе указанных реакций. Схема I-7 016485 В первом аспекте изобретения предлагаются способы, приведенные в качестве примера на схеме I,в которых используют соединения формул I, Ia, Ib, II, III, IIIa и IV или их солевые формы, гдеR3, R4, R5 и R6, каждый независимо, означают Н, галоген, C1-C8-алкил, C2-C8-алкенил,C2-C8-алкинил, C3-C7-циклоалкил, C1-C8-галогеналкил, гидроксигруппу, меркаптогруппу, OR9, SR9, алкоксиалкил, С(О)-алкил, С(О)О-алкил, С(О)NH-алкил, гидроксиалкил, NR10R11, CN, NO2, гетероциклоалкил, арил или гетероарил, где указанный арил и гетероарил могут быть замещены одним или несколькими заместителями, выбранными из C1-C8-алкила, галогена, C1-C8-галогеналкила и алкоксигруппы; илиR4 и R5 вместе с атомами, с которыми они связаны, образуют 5- или 6-членное гетероциклическое кольцо, имеющее один атом О;R10 и R11, каждый независимо, означают Н, C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил,C3-C7-циклоалкил, C1-C8-галогеналкил, аралкил, арил, гетероарил, гетероарилалкил или аллил илиR означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из галогена, цианогруппы, нитрогруппы, C1-C4-алкила,C1-C4-галогеналкила, C1-C4-алкоксигруппы или C1-C4-галогеналкокигруппы иR2 означает C1-C8-алкил, -СН 2-О-(C1-C8-алкил), С(O)O-(C1-C8-алкил), -C(O)NH-(C1-C8-алкил), ОН или СН 2 ОН;R4 и R5, каждый независимо, означают Н, галоген, C1-C8-галогеналкил, гидроксигруппу, OR9, SR9,алкоксиалкил, NHR10, NR10R11, арил или гетероарил, где указанный арил может иметь до двух заместителей, выбранных из C1-C8-алкила, галогена, C1-C8-галогеналкила и алкоксигруппы и указанный гетероарил необязательно может иметь до двух заместителей, выбранных из галогена и C1-C8-алкила; илиR4 и R5 вместе с атомами, с которыми они связаны, образуют 5- или 6-членное гетероциклическое кольцо, имеющее один атом О;R10 и R11, каждый независимо, означают C1-C8-алкил, C2-C8-алкенил, C1-C8-галогеналкил, арил, гетероарил, аралкил, гетероарилалкил или аллил. В некоторых вариантах (А), если R2 означает метил и R4 означает Н, то R5 не является тиазолом, замещенным тиазолом или производным тиазола. В некоторых вариантах (В), если R7a означает Н и R7b является группой, отличной от Н, то ни R4, ни 5R не могут быть Н. В некоторых вариантах (С), если R1 и R2 означают метил и R5 означает Н, то R4 не является NHR10 или NR10R11. В некоторых вариантах (D), если R1 и R2 означают метил и R5 означает Н, то R4 не является имидазолилом, замещенным имидазолилом или производным имидазола. В некоторых вариантах (Е), если R1 означает Н или СН 3 и R2 означает СН 3 или ОН, то все R3, R4, R5 6 и R не могут быть Н. В некоторых вариантах (F), если R1 означает Н и R2 означает изопропил или ОН, то R4 и R5 не могут быть ОСН 3 или ОН. В некоторых вариантах (G), если R1 означает СН 3 и R2 означает н-пропил, то R4 не может быть ОН,5R не может быть Cl и R3 и R6, оба, не могут быть Н.-8 016485 В следующих вариантах R1 означает Н. В следующих вариантах R1 означает C1-C8-алкил. В следующих вариантах R2 означает метил, этил, н-пропил или изопропил. В следующих вариантах R2 означает метил. В следующих вариантах R4 означает Cl, Br, галогеналкил, CF3, тиофенил, фуранил, пирролил, пиразолил или имидазолил. В следующих вариантах R4 означает Cl. В следующих вариантах R5 означает метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, аллилоксигруппу, тиофенил, фуранил, пирролил, пиразолил, имидазолил или фенил, где указанный имидазолил необязательно замещен одним или несколькими заместителями, выбранными из галогена или метила и указанный фенил необязательно имеет до двух заместителей, выбранных изR , оба, не являются Н. В некоторых вариантах (I), если R2 означает СН 3, то R3, R4 и R6, каждый, означают Н и R5 не является Н или изопропилом. В следующих вариантах R1 означает Н. В следующих вариантах R1 означает C1-C8-алкил. В следующих вариантах R2 означает C1-C4-алкил или C1-C4-галогеналкил. В следующих вариантах R2 означает метил, этил, изопропил, н-бутил или CF3. В следующих вариантах R3, R4, R5 и R6, каждый независимо, означают Н, метил, NH2, CN, галоген,CF3, NO2 или ОН. В следующих вариантах изобретения R7a, R7b, R8a и R8b, каждый, означают Н. В следующих вариантах изобретения R3 и R6, каждый, означают Н. В следующих вариантах изобретения R3, R5 и R6, каждый, означают Н. В следующих вариантах изобретения R4 означает галоген. В следующих вариантах изобретения R4 означает Cl. В следующих вариантах изобретения R2 означает C1-C4-алкил. В следующих вариантах изобретения R2 означает метил. В следующих вариантах изобретения R1 означает Н. В следующих вариантах изобретения R1 означает Н или C1-C4-алкил, R2 означает C1-C4-алкил, R3 означает Н, R4 означает галоген, R5 означает Н, R6 означает Н, R7a означает Н, R7b означает Н, R8a означает Н и R8b означает Н. В следующих вариантах изобретения R1 означает Н, R2 означает Me, R3 означает Н, R4 означает Cl,5R означает Н, R6 означает Н, R7a означает Н, R7b означает Н, R8a означает Н и R8b означает Н. В следующих вариантах изобретения L означает галоген. В следующих вариантах изобретения L означает гидроксигруппу. В следующих вариантах изобретения L означает Cl. В следующих вариантах изобретения L означает Br. В следующих вариантах изобретения L означает -OSO2R, например сульфонаты (например, мезилат, трифторметансульфонат, метилсульфонат). В следующих вариантах изобретения L означает -OSi(R')3, например триметилсилилоксигруппу. В следующих вариантах изобретения соединение формулы I может иметь S-конфигурацию по атому углерода, несущему R2. В следующих вариантах изобретения соединение формулы I может иметь R-конфигурацию по атому углерода, несущему R2. Настоящее изобретение относится к способу получения соединения формулы I-9 016485 или его солевой форме, включающему взаимодействие соединения формулы II с восстановителем необязательно в присутствии кислоты Льюиса в течение периода времени и в условиях, подходящих для образования соединения формулы I или его солевой формы. В некоторых вариантах восстановитель содержит боран, такой как ВН 3. В следующих вариантах восстановитель содержит гидрид металла, такой как борогидрид или алюмогидрид. В некоторых вариантах восстановителем является ВН 3:ТТФ. Подходящими могут быть другие восстановители, и они могут быть выбраны специалистом в данной области. Примером подходящих восстановителей являются соединения, которые избирательно восстанавливают амидный остаток соединения формулы II. В следующих вариантах кислота Льюиса может быть представлена в реакции в количестве, достаточном для увеличения скорости реакции. Подходящие кислоты Льюиса включают борсодержащие кислоты Льюиса, такие как BF3 и ее аддукты, включая BF3:TBME (трет-бутилметиловый эфир); BF3:OEt2;BF3:O(CH2CH2CH2CH3)2; BF3: ТГФ и т.п. Подходящие количества включают примерно от 0,01 до примерно 1 экв. по сравнению с количеством соединения формулы II. Вследствие возможной чувствительности восстановителя к воздуху реакцию можно проводить в инертной атмосфере. Реакцию можно осуществлять в любом инертном растворителе, таком как диалкиловый эфир или циклический эфир (например, ТГФ), при любой подходящей температуре, например при комнатной температуре. Продолжительность восстановления может составлять любое количество времени, определяемое специалистом в данной области. В некоторых вариантах продолжительность реакции достаточна для того, чтобы обеспечить возможность протекания реакции, по существу, до полного завершения. Например, продолжительность реакции может быть в пределах примерно от 10 мин до 48 ч. В некоторых вариантах продолжительность реакции составляет примерно 8-12 ч. Завершение реакции можно контролировать, например, ЖХ/МС. Количество присутствующего восстановителя обычно достаточно, чтобы обеспечить, по меньшей мере, достаточное количество в эквивалентах, чтобы восстановить соединение формулы II до требуемого продукта. Например, может быть использован избыток восстановителя, такой как примерно 10, примерно 5, примерно 3 или примерно 2 избыток восстановителя в эквивалентах. В случае боранов и родственных восстановителей молярное отношение восстановителя к соединению формулы II может составлять, например, примерно 2:1, примерно 3:1, примерно 5:1 или примерно 10:1. В некоторых вариантах молярное отношение составляет примерно 3:1. В некоторых вариантах выход реакции восстановления (на основе количества соединения формулыII) составляет более чем примерно 50, примерно 60, примерно 70, примерно 80 или примерно 90%. Настоящее изобретение далее относится к способу получения соединения формулы II или его солевой формы, включающему взаимодействие соединения формулы III или его солевой формы с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы II или его солевой формы. В некоторых вариантах L соединения формулы III означает галоген. В следующих вариантах L соединения формулы III означает Cl. В некоторых вариантах циклизующие реагенты включают кислоту Льюиса, например, такую какC1-C8-алкилалюминийгалогенид (например, метилалюминийхлорид, этилалюминийхлорид и т.д.), C2-C16 диалкилалюминийгалогенид (например, диметилалюминийхлорид, диэтилалюминийхлорид и т.д.), триалкилалюминий, AlCl3 или AlBr3. В некоторых вариантах циклизующим реагентом является AlCl3. Другие подходящие циклизующие реагенты включают кислоты, такие как серная кислота.- 10016485 Циклизация может быть осуществлена в отсутствие растворителя или в присутствии растворителя. Подходящие растворители включают неполярные или слабополярные растворители, такие как декагидронафталин или 1,2-дихлорбензол. Другие подходящие растворители включают галогеналканы и другие галогенированные ароматические соединения, такие как 1,3-дихлорбензол и 1,4-дихлорбензол. Циклизующий реагент может присутствовать в количестве, подходящем для максимизации выхода циклизованного продукта. В некоторых вариантах циклизующий реагент может присутствовать в молярном избытке по сравнению с количеством соединения формулы III. Примеры молярных отношений циклизующего реагента к соединению формулы III включают примерно 2:1, примерно 3:1, примерно 5:1 или примерно 10:1. В некоторых вариантах молярное отношение равно примерно 3:1. В следующих вариантах циклизацию осуществляют при повышенной температуре, такой как примерно от 80 до 160 С. В некоторых вариантах циклизацию осуществляют примерно при 150 С. Реакцию циклизации можно контролировать ЖХ/МС. Продолжительность реакции практически до завершения может составлять примерно от 10 мин до 24 ч. В некоторых вариантах продолжительность реакции составляет примерно от 3 до 15 ч. В некоторых вариантах выход реакции циклизации (на основе количества соединения формулы III) составляет более чем примерно 40, примерно 50, примерно 60, примерно 70, примерно 80 или примерно 90%. Настоящее изобретение далее относится к получению соединения формулы III, включающему взаимодействие соединения формулы IV или его солевой формы с соединением формулы где Q означает удаляемую группу,в течение периода времени и в условиях, подходящих для образования соединения формулы III или его солевой формы. Согласно некоторым вариантам Q означает гидроксигруппу, алкоксигруппу, галоген или O(CO)RQ,где RQ является C1-C8-алкилом, C3-C7-циклоалкилом, арилом, гетероарилом или гетероциклоалкилом. В некоторых вариантах Q означает галоген, такой как Cl. В других вариантах Q означает гидроксигруппу. В следующих вариантах Q означает алкоксигруппу, такую как метоксигруппа, этоксигруппа или третбутоксигруппа. Образование амида необязательно можно осуществлять в присутствии основания, такого как амин (например, NMe3, NEt3, морфолин, пиридин, диизопропилэтиламин, пиперидин,N,N-диметиламинопиперидин и подобные). Другие подходящие основания включают неорганические основания, такие как NaOH, KOH, CsOH и подобные. Относительные количества реагентов, подходящие для осуществления реакции, включают примерно молярные эквиваленты каждого. Например, реакцию образования амида можно осуществлять с молярным отношением соединения формулы IV к соединению формулы составляющим 1:1. В следующих вариантах также может быть включено эквивалентное количество основания (например, молярное отношение примерно 1:1:1). В следующих вариантах основание может быть добавлено в избытке по отношению к количеству соединения формулы IV. В следующих вариантах реакцию образования амида можно осуществлять в растворителе, таком как полярный растворитель. Примером полярного растворителя является ацетонитрил. Температура реакции может быть примерно от -10 до 30 С. В некоторых вариантах реакция может начинаться при температуре ниже комнатной температуры, такой как примерно 0 С, и в ходе реакции возрастает примерно до комнатной температуры. Протекание реакции можно контролировать, например, ТСХ, и период времени до завершения может составлять примерно от 10 мин до 5 ч, в зависимости, например, от масштаба- 11016485 реакции. В некоторых вариантах выход реакции образования амида (на основе количества соединения формулы IV) составляет более чем примерно 40, примерно 50, примерно 60, примерно 70, примерно 80 или примерно 90%. В альтернативном способе получения соединений формулы I настоящее изобретение относится к способу получения соединения формулы I или его солевой формы, включающему взаимодействие соединения формулы IIIa с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы I. В некоторых вариантах L соединения формулы IIIa означает галоген. В следующих вариантах L соединения формулы IIIa означает Br или Cl. В некоторых вариантах циклизующие реагенты включают кислоту Льюиса, например, такую как C1-C8-алкилалюминийгалогенид (например, метилалюминийхлорид, этилалюминийхлорид и т.д.),C2-C16-диалкилалюминийгалогенид (например, диметилалюминийхлорид, диэтилалюминийхлорид и т.д.), триалкилалюминий, AlCl3 или AlBr3. Другие подходящие циклизующие реагенты включают кислоты, такие как серная кислота. Циклизация может быть осуществлена в отсутствие растворителя или в присутствии растворителя. Подходящие растворители включают неполярные или слабополярные растворители, такие как декагидронафталин или 1,2-дихлорбензол. Другие подходящие растворители включают галогеналканы и другие галогенированные ароматические соединения, такие как 1,3-дихлорбензол и 1,4-дихлорбензол. Циклизующий реагент может присутствовать в количестве, подходящем для максимизации выхода циклизованного продукта. В некоторых вариантах циклизующий реагент может присутствовать в молярном избытке по сравнению с количеством соединения формулы IIIa. Примеры молярных отношений циклизующего реагента к соединению формулы IIIa включают примерно 2:1, примерно 3:1, примерно 5:1 или примерно 10:1. В некоторых вариантах молярное отношение равно примерно 3:1. В следующих вариантах циклизацию осуществляют при повышенной температуре, такой как примерно от 80 до 160 С. В некоторых вариантах циклизацию осуществляют примерно при 140 С. Реакцию циклизации можно контролировать ЖХ/МС. Продолжительность реакции до завершения может составлять примерно от 10 мин до 24 ч. В некоторых вариантах продолжительность реакции составляет примерно от 3 до 15 ч. В некоторых вариантах выход реакции циклизации (на основе количества соединения формулыIIIa) составляет более чем примерно 40, примерно 50, примерно 60, примерно 70, примерно 80 или примерно 90%. Настоящее изобретение далее относится к способу получения соединения формулы IIIa или его солевой формы, которое заключается во взаимодействии соединения формулы III- 12016485 с восстановителем необязательно в присутствии кислоты Льюиса в течение периода времени и в условиях, подходящих для образования указанного соединения формулы IIIa. В некоторых вариантах восстановление III может быть осуществлено так, чтобы стереохимия одного или нескольких хиральных центров, присутствующих в соединении формулы III, в основном сохранялась в восстановленном продукте (формулы IIIa). В следующих вариантах восстановление IIIa может быть осуществлено с использованием, по существу, чистого стереоизомера IIIa. В следующих вариантах восстановление IIIa может быть осуществлено с использованием, по существу, чистого стереоизомераIIIa и приводит, по существу, к чистому стереоизомеру III. Например, соединение формулы III, имеющее избыток энантиомера (ее) более чем примерно 80, примерно 90 или примерно 95%, может восстанавливаться с образованием соединения формулы IIIa, имеющего аналогичный ее. В некоторых вариантах восстановитель содержит боран, такой как ВН 3. В следующих вариантах восстановитель содержит гидрид металла, такой как борогидрид или алюмогидрид. В некоторых вариантах восстановительным агентом является ВН 3:ТГФ. Подходящими являются и другие восстановители, и они могут быть выбраны специалистом в данной области. Примером подходящих восстановителей являются соединения, которые избирательно восстанавливают амидный остаток соединения формулы II. В следующих вариантах кислота Льюиса может присутствовать в реакции в количестве, достаточном для увеличения скорости реакции. Подходящие кислоты Льюиса включают борсодержащие кислоты Льюиса, такие как BF3 и ее аддукты, включая BF3:ТВМЕ (трет-бутилметиловый эфир); BF3:OEt2;BF3:O(CH2CH2CH2CH3)2; BF3:ТГФ и т.п. Подходящие количества включают примерно от 0,01 до примерно 1 экв. по сравнению с количеством соединения формулы III. Вследствие возможной чувствительности восстановителя к воздуху реакцию можно проводить в инертной атмосфере. Реакцию восстановления можно осуществлять в любом инертном растворителе, таком как диалкиловый эфир или циклический эфир (например, ТГФ), при любой подходящей температуре, например при комнатной температуре. Продолжительность восстановления может составлять любое количество времени. В некоторых вариантах продолжительность реакции достаточна для того, чтобы обеспечить возможность протекания реакции, по существу, до полного завершения. Например, продолжительность реакции может быть в пределах примерно от 10 мин до 72 ч. В некоторых вариантах продолжительность реакции составляет примерно 8-12 ч. Завершение реакции можно контролировать, например, ЖХ/МС. Количество присутствующего восстановителя обычно достаточно, чтобы обеспечить, по меньшей мере, достаточное количество в эквивалентах, чтобы восстановить соединение формулы II до требуемого продукта. Например, может быть использован избыток восстановителя, такой как примерно 10, примерно 5, примерно 3 или примерно 2 избыток восстановителя в эквивалентах. В случае боранов и родственных восстановителей молярное отношение восстановителя к соединению формулы II может составлять, например, примерно 2:1, примерно 3:1, примерно 5:1 или примерно 10:1. В некоторых вариантах молярное отношение составляет примерно 3:1. В некоторых вариантах выход реакции восстановления (на основе количества соединения формулыIII) составляет более чем примерно 50, примерно 60, примерно 70, примерно 80 или примерно 90%. Настоящее изобретение далее относится к способам, представленным ниже на схемах Ia, Ib и Ic, где составляющие фрагменты изображенных на них структур имеют значения, определенные выше.- 15016485 В следующих вариантах настоящее изобретение относится к способу разделения смеси соединений формул Ia и Ib: контактированием смеси соединений с хиральной разделяющей кислотой, обогащенной одним стереоизомером (например, ее более чем примерно 50, примерно 75, примерно 90 или примерно 95%), с образованием солей хиральной разделяющей кислоты и соединений смеси, и затем осаждением солей хиральной разделяющей кислоты. Полученный в результате осадок обычно обогащен солью хиральной разделяющей кислоты и одного из соединений формулы Ia или Ib (например, ее 50%). В некоторых вариантах осадок обогащен формой соли хиральной разделяющей кислоты и соединения формулы Ia. В некоторых вариантах осадок обогащен формой соли хиральной разделяющей кислоты и соединения формулы Ib. В следующих вариантах хиральной разделяющей кислотой является стереоизомер толуоилвинной кислоты, камфорной кислоты, кетогулоновой кислоты или винной кислоты. В следующих вариантах хиральной разделяющей кислотой является стереоизомер винной кислоты, такой как L-(+)-винная кислота. Контактирование соединений с хиральной разделяющей кислотой может быть осуществлено в растворе. Подходящие растворители обеспечивают растворение как хиральной разделяющей кислоты, так и соединений формул Ia и Ib. Некоторые примеры растворителей включают полярные растворители или смешивающиеся с водой растворители, такие как спирты (например, метанол, этанол, изопропанол, третбутанол и подобные), изопропилацетат, вода и их смеси. В следующих вариантах растворитель содержит смесь трет-бутанола и воды. Некоторые примеры смесей содержат примерно 5-25% воды и примерно 75-95% трет-бутанола. В некоторых вариантах растворитель содержит примерно 8-12% воды и примерно 88-92% трет-бутанола. Осадок, содержащий формы солей хиральной разделяющей кислоты, может быть образован осаждением из любого подходящего растворителя, который растворяет соли, такого как растворитель, в котором осуществляли контактирование. Осаждение может быть индуцировано любым способом, известным в данной области, таким как нагревание раствора, содержащего смесь солей, с последующим охлаждением. Осадок может быть отделен от растворителя, например, фильтрованием. Обогащение осадка одной хиральной солью по сравнению с другой можно охарактеризовать избытком энантиомера (ее), составляющим более чем примерно 50, примерно 60, примерно 70, примерно 80, примерно 90, примерно 95,примерно 98 или примерно 99%. В некоторых вариантах ее составляет примерно более 80%. Осаждение можно повторять один или несколько раз, чтобы увеличить долю хиральной соли в осадке, повторным растворением и повторным осаждением ранее полученного осадка. Настоящее изобретение далее относится к соли хиральной разделяющей кислоты и соединения формулы Ia или Ib: где составляющие фрагменты имеют значение, определенное выше. Композиции настоящего изобретения могут содержать как форму соли соединения формулы Ia, так и форму соли соединения формулы Ib или одну из них. В некоторых вариантах форма соли соединения формулы Ia присутствует в композиции в большем количестве, чем форма соли соединения формулы Ib. В других вариантах форма соли соединения формулы Ib присутствует в композиции в большем количестве, чем форма соли соединения формулы Ia. Следующие примеры способов и промежуточных продуктов настоящего изобретения представлены ниже на схеме II, где составляющие фрагменты изображенных соединений имеют значения, определенные ниже. Символ означает необязательные хиральные центры, которые в основном могут сохраняться или подвергаться инверсии в ходе указанных реакций. Во втором аспекте настоящего изобретения предлагаются способы, приведенные в качестве примера на схеме II, в которые вовлечены соединения формул V, Va, Vb, IX, X, XI и XII или их солевые формы,где R1 означает Н или C1-C8-алкил;R3, R4, R5 и R6, каждый независимо, означают Н, галоген, C1-C8-алкил, C2-C8-алкенил,C2-C8-алкинил, C3-C7-циклоалкил, C1-C8-галогеналкил, гидроксигруппу, OR9, алкоксиалкил, С(O)-алкил,С(О)О-алкил, С(О)NH-алкил, гидроксиалкил, NR10R11, CN, NO2, гетероциклоалкил, арил или гетероарил,где указанный арил и гетероарил могут быть замещены одним или несколькими заместителями, выбранными из C1-C8-алкила, галогена, C1-C8-галогеналкила и алкоксигруппы; илиR4 и R5 вместе с атомами, с которыми они связаны, образуют 5- или 6-членное гетероциклическое кольцо, имеющее один атом О;R9 означает Н, C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил, C3-C7-циклоалкил, C1-C8-галогеналкил,аралкил, арил, гетероарил, гетероарилалкил или аллил иR10 и R11, каждый независимо, означают Н, C1-C8-алкил, C2-C8-алкенил, C2-C8-алкинил,C3-C7-циклоалкил, C1-C8-галогеналкил, аралкил, арил, гетероарил, гетероарилалкил или аллил илиX2 означает галоген или SO2R" иR" означает C1-C8-алкил, арил или гетероарил, каждый необязательно замещенный одним или несколькими заместителями, выбранными из галогена, цианогруппы, нитрогруппы, C1-C4-алкила,C1-C4-галогеналкила, C1-C4-алкоксигруппы или C1-C4-галогеналкоксигруппы. В некоторых вариантах изобретенияR2 означает C1-C8-алкил, -СН 2-О-(C1-C8-алкил), С(O)O-(C1-C8-алкил), -C(O)NH-(C1-C8-алкил), ОН или СН 2 ОН;R4 и R5, каждый независимо, означают Н, галоген, C1-C8-галогеналкил, гидроксигруппу, OR9, SR9,алкоксиалкил, NHR10, NR10R11, арил или гетероарил, где указанный арил может иметь до двух заместителей, выбранных из C1-C8-алкила, галогена, C1-C8-галогеналкила и алкоксигруппы, и указанный гетероарил необязательно может иметь до двух заместителей, выбранных из галогена и C1-C8-алкила; илиR4 и R5 вместе с атомами, с которыми они связаны, образуют 5- или 6-членное гетероциклическое кольцо, имеющее один атом О;R10 и R11, каждый независимо, означают C1-C8-алкил, C2-C8-алкенил, C1-C8-галогеналкил, арил, гетероарил, аралкил, гетероарилалкил или аллил. В некоторых вариантах (А), если R2 означает метил и R4 означает Н, то R5 не является тиазолом, замещенным тиазолом или производным тиазола. В некоторых вариантах (В), если R7a означает Н и R7b является группой, отличной от Н, то ни R4, ни 5R не могут быть Н. В некоторых вариантах (С), если R1 и R2 означают метил и R5 означает Н, то R4 не является NHR10 или NR10R11. В некоторых вариантах (D), если R1 и R2 означают метил и R5 означает Н, то R4 не является имидазолилом, замещенным имидазолилом или производным имидазола. В некоторых вариантах (Е), если R1 означает Н или СН 3 и R2 означает СН 3 или ОН, то все R3, R4, R5 6 и R не могут быть Н. В некоторых вариантах (F), если R1 означает Н и R2 означает изопропил или ОН, то R4 и R5 не могут быть ОСН 3 или ОН. В некоторых вариантах (G), если R1 означает СН 3 и R2 означает н-пропил, то R4 не может быть ОН,5R не может быть Cl и R3 и R6, оба, не могут быть Н. В следующих вариантах R1 означает Н. В следующих вариантах R1 означает C1-C8-алкил. В следующих вариантах R2 означает метил, этил, н-пропил или изопропил. В следующих вариантах R2 означает метил. В следующих вариантах R4 означает Cl, Br, галогеналкил, CF3, тиофенил, фуранил, пирролил, пиразолил или имидазолил. В следующих вариантах R4 означает Cl. В следующих вариантах R5 означает метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, аллилоксигруппу, тиофенил, фуранил, пирролил, пиразолил, имидазолил или фенил, где указанный имидазолил необязательно замещен одним или несколькими заместителями: галогеном или метилом, и указанный фенил необязательно имеет до двух заместителей, выбранных из C1-C8-алкила,C1-C8-галогеналкила, галогена и алкоксигруппы. В следующих вариантах R5 означает Н. В некоторых вариантахR , оба, не являются Н. В некоторых вариантах (I), если R2 означает СН 3, то R3, R4 и R6, каждый, означают Н и R5 не является Н или изопропилом. В следующих вариантах R1 означает Н. В следующих вариантах R1 означает C1-C8-алкил. В следующих вариантах R2 означает C1-C8-алкил, -СН 2-О-(C1-C8-алкил), С(О)О-(C1-C8-алкил),-С(О)NH-(C1-C8-алкил) или C1-C4-галогеналкил. В следующих вариантах R2 означает C1-C4-алкил или C1-C4-галогеналкил. В следующих вариантах R2 означает метил, этил, изопропил, н-бутил или CF3. В следующих вариантах R3, R4, R5 и R6, каждый независимо, означают Н, метил, NH2, CN, галоген,CF3, NO2 или ОН. В следующих вариантах изобретения R7a, R7b, R8a и R8b, каждый, означают Н. В следующих вариантах изобретения R3 и R6, каждый, означают Н. В следующих вариантах изобретения R3, R5 и R6, каждый, означают Н. В следующих вариантах изобретения R4 означает галоген. В следующих вариантах изобретения R4 означает Cl. В следующих вариантах изобретения R2 означает C1-C4-алкил. В следующих вариантах изобретения R2 означает метил. В следующих вариантах изобретения R1 означает Н. В следующих вариантах X1 означает галоген. В следующих вариантах X1 означает Br. В следующих вариантах X1 означает Cl.- 18016485 В следующих вариантах X2 означает галоген. В следующих вариантах X2 означает Br. В следующих вариантах X2 означает Cl. В следующих вариантах изобретения R1 означает Н или C1-C4-алкил, R2 означает C1-C4-алкил,3R означает Н, R4 означает галоген, R5 означает Н, R6 означает Н, R7a означает Н, R7b означает Н, R8a означает Н и R8b означает Н. В следующих вариантах изобретения R1 означает Н, R2 означает Me, R3 означает Н, R4 означает Cl,5R означает Н, R6 означает Н, R7a означает Н, R7b означает Н, R8a означает Н и R8b означает Н. В следующих вариантах изобретения соединение формулы V может иметь S-конфигурацию по атому углерода, несущему R2. В следующих вариантах изобретения соединение формулы V может иметь R-конфигурацию по атому углерода, несущему R2. Настоящее изобретение относится к способу получения соединения формулы V или его соли взаимодействием соединения формулы IX или его соли с циклизующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы V. В некоторых вариантах циклизующие реагенты включают кислоту Льюиса, например, такую как C1-C8-алкилалюминийгалогенид (например, метилалюминийхлорид, этилалюминийхлорид и т.д.),C2-C16-диалкилалюминийгалогенид (например, диметилалюминийхлорид, диэтилалюминийхлорид и т.д.), триалкилалюминий, AlCl3 или AlBr3. Другие подходящие циклизующие реагенты включают кислоты, такие как серная кислота. Циклизующий реагент может присутствовать в количестве, подходящем для максимизации выхода циклизованного продукта. В некоторых вариантах циклизующий реагент может присутствовать в молярном избытке по сравнению с количеством соединения формулы IX. Примеры молярных отношений циклизующего реагента к соединению формулы IX включают примерно 1,5:1, примерно 2:1, примерно 3:1,примерно 5:1 или примерно 10:1. В некоторых вариантах молярное отношение равно примерно 1,5:1. Взаимодействие может быть осуществлено в присутствии любого подходящего растворителя (или в отсутствие растворителя), такого как неполярный или слабополярный растворитель или высококипящий растворитель (температура кипения выше, чем температура кипения воды). В некоторых вариантах взаимодействие осуществляют в присутствии 1,2-дихлорбензола. В следующих вариантах взаимодействие осуществляют в присутствии декалина. Температура реакции может быть равна любой подходящей температуре, такой как температуры,которые не приводят к быстрой деградации реагентов, однако максимизируют эффективность реакции и/или минимизируют время реакции. В некоторых вариантах взаимодействие осуществляют при повышенной температуре, например, такой как примерно от 80 до 170 С. В некоторых вариантах повышенная температура составляет примерно от 100 до 150, примерно от 120 до 150 или примерно 140 С. Реакцию циклизации можно контролировать ЖХ/МС. Продолжительность реакции до завершения составляет примерно от 10 мин до 24 ч. В некоторых вариантах продолжительность реакции составляет примерно от 3 до 15 ч. В следующих вариантах продолжительность реакции составляет примерно от 2 до 5 ч. В некоторых вариантах выход реакции циклизации (на основе количества соединения формулы IX) составляет более чем примерно 40, примерно 50, примерно 60, примерно 70, примерно 80 или примерно 90%.- 19016485 Настоящее изобретение далее относится к способу получения соединения формулы IX или его соли взаимодействием соединения формулы X или его соли с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях,подходящих для образования соединения формулы XI. Подходящие галогенирующие/сульфонирующие реагенты способны заменять остаток ОН в соединении формулы X атомом галогена или остатком сульфоната. В некоторых вариантах галогенирующим/сульфонирующим реагентом является SOBr2 или SOCl2. Галогенирующий/сульфонирующий реагент может присутствовать в количестве, достаточном для получения теоретически максимального выхода. Подходящие молярные отношения галогенирующего/сульфонирующего реагента к соединению формулы X включают отношения примерно 10:1, примерно 5:1, примерно 3:1, примерно 2:1 или примерно 1,5:1. В некоторых вариантах молярное отношение равно примерно от 1,06:1 до 1,4:1. Взаимодействие можно осуществлять в любом подходящем растворителе или в отсутствие растворителя, таком как растворители, способные растворять по меньшей мере одно из соединения формулы X или галогенирующего/сульфонирующего реагента. В некоторых вариантах растворитель содержит ДМФА (диметилформамид). В следующих вариантах растворитель содержит толуол. В следующих вариантах растворитель содержит дихлорметан. В некоторых вариантах растворитель содержит диметилформамид и толуол, и в следующих вариантах растворитель содержит диметилформамид и дихлорметан. Подходящей является любая температура реакции, при которой исходные вещества, растворитель или продукты существенно не разлагаются. В некоторых вариантах взаимодействие осуществляют при таких температурах, как примерно от -40 до примерно 80 С, примерно от -10 до 30 С или примерно от 0 С до комнатной температуры. В некоторых вариантах выделяют соединение формулы XI, например, перекристаллизацией из подходящего растворителя. Выход может составлять более чем примерно 20, более чем примерно 30, более чем примерно 40 или более чем примерно 50%. В некоторых вариантах выход составляет более чем примерно 50%. Настоящее изобретение также относится к способу получения соединения формулы X или его соли, включающему взаимодействие соединения формулы XI в течение периода времени и в условиях, подходящих для образования соединения формулы X. Взаимодействие можно осуществлять, например, при повышенной температуре, такой как примерно от 80 до примерно 110 С или от 90 до примерно 100 С. В некоторых вариантах взаимодействие осуществляют примерно при 95 С. Можно использовать любой подходящий инертный растворитель, и в некоторых вариантах взаимодействие осуществляют в отсутствие растворителя. В реакции может быть использовано достаточное количество соединения формулы чтобы получить максимальный теоретический или практический выход. Примерные количества могут быть в диапазоне по меньшей мере примерно от 1 мол.экв. до любого количества, которое может быть в молярном избытке (например, примерно 10 или 15) по сравнению с количеством соединения формулы XI. Примерная продолжительность реакции может составлять приблизительно от 3 до 5 ч. Настоящее изобретение далее относится к способу получения соединения формулы XI взаимодействием соединения формулы XII с галогенирующим/сульфонирующим реагентом в течение периода времени и в условиях, подходящих для образования соединения формулы XI. Галогенирующим/сульфонирующим реагентом может быть любой подходящий реагент, способный заменять гидроксильный остаток соединения формулы XII подходящей удаляемой группой, такой как атом галогена или остаток сульфоната. В некоторых вариантах галогенирующим/сульфонирующим реагентом, например, является PBr3 или PCl3. Можно использовать любой подходящий растворитель или взаимодействие можно осуществлять в отсутствие растворителя. Температуру реакции легко может выбрать специалист в данной области. В некоторых вариантах взаимодействие осуществляют при пониженных температурах, таких как примерно от -20 до примерно 15 С, примерно от -10 до примерно 10 С или примерно при 0 С. В некоторых вариантах температура реакции составляет примерно ниже 10 С. Галогенирующий/сульфонирующий реагент может присутствовать в количестве, достаточном для получения максимального теоретического выхода. Например, молярное отношение галогенирующего/сульфонирующего реагента к соединению формулы XII может быть в пределах примерно от 20:1 до примерно 0,2:1. В некоторых вариантах галогенирующий/сульфонирующий реагент присутствует в небольшом избытке, таком как при соотношении примерно 1:1 или примерно 0,5:1. Выход реакции может составлять более чем примерно 75, более чем примерно 85, более чем примерно 90, более чем примерно 95 или более чем примерно 98%. В некоторых вариантах выход составляет примерно от 95 до примерно 100%. В следующих вариантах настоящее изобретение относится к способу разделения смеси соединений формул Va и Vb: контактированием смеси соединения с хиральной разделяющей кислотой, обогащенной по одному сте- 21016485 реоизомеру (например, ее более чем примерно 50, примерно 75, примерно 90 или примерно 95%), с образованием солей хиральной разделяющей кислоты и соединений смеси и затем осаждением солей хиральной разделяющей кислоты. Полученный в результате осадок обычно обогащен солью хиральной разделяющей кислоты и одного из соединений формул Va или Vb (например, ее 50%). В некоторых вариантах осадок обогащен формой соли хиральной разделяющей кислоты и соединения формулы Va. В некоторых вариантах осадок обогащен формой соли хиральной разделяющей кислоты и соединения формулы Vb. В следующих вариантах хиральная разделяющая кислота является стереоизомером толуоилвинной кислоты, камфорной кислоты, кетогулоновой кислоты или винной кислоты. В следующих вариантах хиральной разделяющей кислотой является винная кислота, такая как L-(+)-винная кислота. Контактирование соединений формул Va и Vb с хиральной разделяющей кислотой может быть осуществлено в растворе. Подходящие растворители обеспечивают растворение как хиральной разделяющей кислоты, так и соединений формул Va и Vb. Некоторые примеры растворителей включают полярные растворители или смешивающиеся с водой растворители, такие как спирты (например, метанол,этанол, изопропанол, трет-бутанол и подобные), изопропилацетат, тетрагидрофуран, ацетон, метилизобутилкетон, вода и их смеси. В следующих вариантах растворитель содержит смесь спирта и воды. В следующих вариантах растворитель содержит смесь трет-бутанола и воды. Некоторые примеры смесей содержат примерно 5-25% воды и примерно 75-95% трет-бутанола. В некоторых вариантах растворитель содержит примерно 8-12% воды и примерно 88-92% трет-бутанола. В некоторых вариантах растворитель содержит смесь ацетона и воды. Осадок, содержащий формы солей хиральной разделяющей кислоты, может быть получен осаждением из любого подходящего растворителя, который растворяет соли, такого как растворитель, в котором осуществляли контактирование. Осаждение может быть индуцировано любым способом, известным в данной области, таким как нагревание раствора, содержащего смесь солей, с последующим охлаждением. Осадок может быть отделен от растворителя, например, фильтрованием. Обогащение осадка одной хиральной солью по сравнению с другой можно охарактеризовать избытком энантиомера (ее), составляющим более чем примерно 50, примерно 60, примерно 70, примерно 80, примерно 90, примерно 95,примерно 98 или примерно 99%. В некоторых вариантах ее составляет более чем примерно 80%. Осаждение можно повторять один или несколько раз, чтобы увеличить долю хиральной соли в осадке, повторным растворением и повторным осаждением ранее полученного осадка. Настоящее изобретение далее относится к соли хиральной разделяющей кислоты и соединения формул Va или Vb: где составляющие фрагменты имеют значение, определенное выше. Композиции настоящего изобретения могут содержать как форму соли соединения формулы Va,так и форму соли соединения формулы Vb или одну из них. В некоторых вариантах форма соли соединения формулы Va присутствует в композиции в большем количестве, чем форма соли соединения формулы Vb. В других вариантах форма соли соединения формулы Vb присутствует в композиции в большем количестве, чем форма соли соединения формулы Va. Настоящее изобретение далее относится к соли хлористо-водородной кислоты и соединения формулы Va или Vb и их композициям. Понятно, что некоторые отличительные признаки изобретения, которые для ясности описаны в контексте отдельных вариантов, также могут быть представлены в комбинации в одном варианте. Наоборот, различные отличительные признаки изобретения, которые для краткости описаны в контексте одного варианта, также могут быть представлены по отдельности или в любой подходящей подкомбинации. Как использовано в данном описании, термин "алкил" относится к насыщенному углеводороду, который может иметь прямую или разветвленную цепь. Примеры алкильных групп включают метил (Me),этил (Et), пропил (например, н-пропил и изопропил), бутил (например, н-бутил, изобутил, трет-бутил),пентил (например, н-пентил, изопентил, неопентил) и т.п. Алкильная группа может содержать от 1 до примерно 20, от 2 до примерно 20, от 1 до примерно 10, от 1 до примерно 8, от 1 до примерно 6, от 1 до примерно 4 или от 1 до примерно 3 атомов углерода.- 22016485 Как использовано в данном описании, "алкенил" относится к алкильной группе, имеющей одну или несколько двойных углерод-углеродных связей. Примеры алкенильных групп включают этенил, пропенил, циклогексенил и подобные. Как использовано в данном описании, "алкинил" относится к алкильной группе, имеющей одну или несколько тройных углерод-углеродных связей. Примеры алкинильных групп включают этинил, пропинил и подобные. Как использовано в данном описании, "галогеналкил" относится к алкильной группе, имеющей один или несколько заместителей в виде атомов галогена. Примеры галогеналкильных групп включаютCF3, C2F5, CHF2, CCl3, CHCl2, C2Cl5 и подобные. Алкильную группу, в которой все атомы водорода заменены атомами галогена, можно назвать "пергалогеналкил". Как использовано в данном описании, "арил" относится к моноциклическим или полициклическим ароматическим углеводородам, например, таким как фенил, нафтил, антраценил, фенантренил, инданил,инденил и подобные. В некоторых вариантах арильные группы имеют от 6 до примерно 20 атомов углерода. Как использовано в данном описании, "циклоалкил" относится к неароматическим углеводородам,включая циклические алкильные, алкенильные и алкинильные группы. Циклоалкильные группы могут включать моно-, би- или полициклические кольцевые системы, а также содержат двойные и тройные связи. Примеры циклоалкильных групп включают циклопропил, циклобутил, циклопентил, циклогексил,циклогептил, циклопентенил, циклогексенил, циклогексадиенил, циклогептатриенил, норборнил, норпинил, норкарнил, адамантил и подобные. Также в определение циклоалкила включены остатки, которые имеют один или несколько ароматических колец, конденсированных (т.е. имеющих общую связь) с циклоалкильным кольцом, например бензопроизводные пентана и подобные. Как использовано в данном описании, "гетероарильные" группы означают моноциклические и полициклические ароматические углеводороды, которые имеют по меньшей мере один гетероатомный член кольца, такой как атом серы, кислорода или азота. Гетероарильные группы включают без ограничения пиридил, пиримидинил, пиразинил, пиридазинил, триазинил, фурил, хинолил, изохинолил, тиенил,имидазолил, тиазолил, индолил, пиррил, оксазолил, бензофурил, бензотиенил, бензтиазолил, изоксазолил, пиразолил, триазолил, тетразолил, индазолил, 1,2,4-тиадиазолил, изотиазолил, бензотиенил, пуринил,карбазолил,бензимидазолил,2,3-дигидробензофуранил,2,3-дигидробензотиенил,2,3 дигидробензотиенил-S-оксид, 2,3-дигидробензотиенил-S-диоксид, бензоксазолин-2-онил, индолинил,бензодиоксоланил, бензодиоксан и подобные. В некоторых вариантах гетероарильные группы могут иметь от 1 до примерно 20 атомов углерода и в следующих вариантах примерно от 3 до примерно 20 атомов углерода. В некоторых вариантах гетероарильные группы имеют от 1 до примерно 4, от 1 до примерно 3 или от 1 до 2 гетероатомов. Как использовано в данном описании, "гетероциклоалкил" относится к циклоалкильной группе, где один или несколько образующих кольцо атомов углерода заменены гетероатомом, таким как атом О, S,N или Р. Также в определение гетероциклоалкила включены остатки, которые имеют одно или несколько ароматических колец, конденсированных (т.е. имеющих общую связь) с неароматическим гетероциклическим кольцом, например фталимидил, нафталимидил, пиромеллитовый диимидил, фталанил и бензопроизводные насыщенных гетероциклов, таких как группы индолена и изоиндолена. Как использовано в данном описании, "гало" или "галоген" включает фтор, хлор, бром и йод. Как использовано в данном описании, "алкоксигруппа" относится к -О-алкильной группе. Примеры алкоксигрупп включают метокси-, этокси-, пропокси- (например, н-пропокси- и изопропокси-), третбутоксигруппу и подобные. Как использовано в данном описании, "тиоалкоксигруппа" относится к алкоксигруппе, в которой атом О заменен атомом S. Как использовано в данном описании, "арилоксигруппа" относится к -О-арильной группе. Примером арилоксигруппы является феноксигруппа. Как использовано в данном описании, "тиоарилоксигруппа" относится к арилоксигруппе, в которой атом О заменен атомом S. Как использовано в данном описании, "аралкил" относится к алкильному остатку, замещенному арильной группой. Примеры аралкильных групп включают бензильную, фенетильную и нафтилметильную группы. В некоторых вариантах арилалкильные группы имеют от 7 до 20 или от 7 до 11 атомов углерода. Как использовано в данном описании, "гидроксиалкил" относится к алкильной группе, замещенной гидроксигруппой. Как использовано в данном описании, "алкоксиалкил" относится к алкильной группе, замещенной алкоксигруппой. Как использовано в данном описании, термин "реакция/взаимодействие" применяют так, как известно в данной области, и в общем термин относится к объединению химических реагентов вместе таким образом, чтобы обеспечить их взаимодействие на молекулярном уровне для достижения химического или физического превращения.- 23016485 Как использовано в данном описании, термин "замещенный" относится к замене водородного остатка в молекуле или группе неводородным остатком. Как использовано в данном описании, термин "производное тиазола" относится к остатку, содержащему группу тиазолила. Как использовано в данном описании, термин "производное имидазола" относится к остатку, содержащему группу имидазолила. Как использовано в данном описании, термин "контактирование" относится к объединению веществ вместе так, чтобы они могли взаимодействовать на молекулярном уровне. Как использовано в данном описании, термин "восстановитель" применяют так, как известно в данной области, и термин относится к любому химическому реагенту, который осуществляет восстановление другого химического реагента. В некоторых вариантах восстановление, осуществляемое восстановителем, включает уменьшение количества связей атома (например, атома С атом) с атомом кислорода или серы. Например, восстановитель может превращать (или восстанавливать) кетон в спирт. В некоторых вариантах восстановитель превращает амид в амин. В данной области известно множество восстановителей, и они могут быть идентифицированы при сравнении окислительно-восстановительного потенциала восстановителя и восстанавливаемого вещества. Обычно восстановитель может иметь более низкий потенциал восстановления, чем восстанавливаемое вещество. Способы измерения окислительновосстановительных потенциалов хорошо известны в данной области. В других вариантах восстановитель может быть акцептором кислорода. Примеры восстановителей включают гидриды металлов, такие как борогидриды (например, NaBH4, LiBH4, NaBH3CN) и алюмогидриды (например, LiAlH4), включая, например, C1-C8-алкилалюмогидриды, C2-C16-диалкилалюмогидриды, алкоксиалюмогидриды (например,моно-, ди- и триалкоксиалюмогидриды). Другие подходящие восстановители включают бораны, такие как ВН 3 или В 2 Н 6 и их аддукты. Примеры аддуктов боранов включают, например, диалкилсульфидбораны (например, ВН 3: CH3SCH3), амин-бораны (например, ВН 3:триэтиламин), диалкиловый эфир-бораны(например,ВН 3:тетрагидрофуран), C1-C8-алкилбораны, C2-C16-диалкилбораны, C3-C24-триалкилбораны (например,9-борабицикло[3.3.1]нонан), циклические бораны (например, бороланы) и т.п. Кроме того, примеры восстановителей включают Red-Al и Н 2 необязательно в присутствии катализатора, такого как Pd/C. Как использовано в данном описании, термин "циклизующий реагент" относится к любому химическому реагенту, который может быть использован в реакции циклизации линейной или разветвленной молекулы или части молекулы. В некоторых вариантах настоящего изобретения циклизация линейного или разветвленного остатка, связанного с арильным соединением, может быть осуществлена с использованием, например, кислоты Льюиса. Как известно в данной области, к кислотам Льюиса относится молекула, которая может акцептором неподеленной пары электронов. Примеры кислот Льюиса включают ион водорода (протон), производные бора, такие как ВН 3 и BF3, и производные алюминия, такие как AlCl3. Некоторые примеры кислот Льюиса включают C1-C8-алкилалюминийгалогенид (например, метилалюминийхлорид, этилалюминийхлорид и т.д.), С 2-С 16-диалкилалюминийгалогенид (например, диметилалюминийхлорид, диэтилалюминийхлорид и т.д.) и триалкилалюминий. В некоторых вариантах циклизация может быть осуществлена по реакции алкилирования ФриделяКрафтса, которая, как известно, сопровождается общим превращением: ArH+RCH2ClArCH2R (Ar означает арил и R означает, например, любой алкил, аминогруппу или другую группу) в присутствии такого реагента, как кислота Льюиса. Реакции Фриделя-Крафтса обычно осуществляют в присутствии AlCl3 и необязательно при повышенных температурах. Подходящие кислоты Льюиса включают борсодержащие реагенты и реагенты, содержащие алюминий. Примеры борсодержащих реагентов включают ВН 3, BF3 и их аддукты (например, BF3:TBME и BF3:OEt2). Примеры содержащих алюминий реагентов включают алкилалюминийгалогениды, диалкилалюминийгалогениды, триалкилалюминий и галогениды алюминия(например, AlCl3 и AlBr3). Другие подходящие циклизующие реагенты включают, например, такие кислоты, как серная кислота, сульфоновые кислоты (например, CF3SO3H, CH3SO3H, pTSA), фосфорные кислоты, полифосфорные кислоты (например, Н 3 РО 4/Р 2 О 5) и т.п. Дополнительные подходящие катализаторы алкилирования по Фриделю-Крафтсу включают FeCl3, TiCl4, ZrCl4 и ZnCl4. Как использовано в данном описании, термин "галогенирующий/сульфонирующий реагент" относится к любому химическому реагенту, который можно использовать для того, чтобы заменить водород или химический заместитель в молекуле удаляемой группой, такой как остаток галогена или остаток сульфоната (например, алкилсульфонат, мезилат, тозилат и т.д.). В некоторых вариантах галогенирующий/сульфонирующий реагент заменяет гидроксил остатком галогена или остатком сульфоната. Примеры галогенирующих/сульфонирующих реагентов включают тригалогениды фосфора (например, PBr3),пентагалогениды фосфора, оксигалогениды фосфора, тионилгалогениды (например, SOBr2) и т.п. Другие галогенирующие/сульфонирующие реагенты включают N-бромсукцинимид (NBS), 1,3-дибром-5,5 диметилгидантоин, трибромид пиридиния (pyrHBr3), трифторид диэтиламиносеры (DAST),N-фторбензолсульфонимид и т.п. Кроме того, галогенирующие/сульфонирующие реагенты включают сульфонилгалогениды, такие как мезилхлорид, тозилхлорид и подобные.- 24016485 Как использовано в данном описании, термин "удаляемая группа" относится к остатку, который может быть заменен другим остатком, например, в результате нуклеофильной атаки во время химической реакции. Удаляемые группы хорошо известны в данной области и включают, например, галоген,гидроксигруппу, алкоксигруппу, -O(CO)Ra, -OSO2-Rb и -OSi(Rc)3, где Ra может означать C1-C8-алкил,C3-C7-циклоалкил, арил, гетероарил или гетероциклоалкил, где Rb может означать C1-C8-алкил,арил (необязательно замещенный одним или несколькими группами, выбранными из галогена,цианогруппы,нитрогруппы,C1-C4-алкила,C1-C4-галогеналкила,C1-C4-алкоксигруппы илиC1-C4-галогеналкоксигруппы) или гетероарил (необязательно замещенный одним или несколькими группами, выбранными из галогена, цианогруппы, нитрогруппы, C1-C4-алкила, C1-C4-галогеналкила,C1-C4-алкоксигруппы или C1-C4-галогеналкоксигруппы) и где Rc может означать C1-C8-алкил. Примеры удаляемых групп включают хлор, бром, йод, мезилат, тозилат, триметилсилил и т.п. Как использовано в данном описании, термины "процесс разделения" и "разделение" применяют,как известно в данной области, и термины обычно относятся к разделению смеси изомеров, таких как стереоизомеры (например, оптические изомеры, такие как энантиомеры или диастереомеры). Разделение может включать способы, которые могут увеличивать долю одного стереоизомера относительно другого в смеси стереоизомеров. Смесь стереоизомеров, содержащая большую долю первого стереоизомера по сравнению с другим стереоизомером, может быть названа "обогащенной" по первому стереоизомеру. Как использовано в данном описании, термин "осаждение" применяют, как известно в данной области, и термин обычно относится к образованию твердого вещества (например, осадка) из раствора, в котором растворено твердое вещество. Твердое вещество может быть аморфным, кристаллическим или представлять собой их смесь. Способы осаждения хорошо известны в данной области и заключаются,например, в увеличении доли растворителя, в котором растворяемое вещество является нерастворимым,в снижении температуры, химическом превращении растворенного вещества так, чтобы оно больше не растворялось в данном растворителе, и т.п. Осаждение можно использовать для увеличения доли стереоизомера в смеси стереоизомеров. Процессы, приведенные в данном описании, можно контролировать в соответствии с любым подходящим методом, известным в данной области. Например, за образованием продукта можно следить спектроскопическими методами, такими как ядерная магнитно-резонансная спектроскопия (например, 1 Н или 13 С), инфракрасная спектроскопия, спектрофотометрия (например, УФ и видимая) или массспектрометрия, или хроматографией, такой как высокоэффективная жидкостная хроматография (ВЭЖХ) или тонкослойная хроматография. В некоторых вариантах получение соединений может включать защиту и удаление защиты различных химических групп. Необходимость в защите и удалении защиты и выбор соответствующих защитных групп легко может определить специалист в данной области. Химию защитных групп можно найти,например, в публикации Green and Wuts, et al., Protective Groups in Organic Synthesis, 3rd Ed., Wiley andSons, 1999, которая включена в данное описание посредством ссылки во всей своей полноте. Реакции в описанных в данной публикации способах можно осуществлять в подходящих растворителях, которые легко могут быть выбраны специалистом в области органического синтеза. Подходящие растворители могут быть, по существу, неактивными по отношению к исходным веществам (реагентам),промежуточным продуктам или продуктам при температурах, при которых осуществляют реакции, например при температурах, которые находятся в диапазоне от температуры замерзания растворителя до температуры кипения растворителя. Данная реакция может быть осуществлена в одном растворителе или в смеси более чем одного растворителя. В зависимости от конкретной стадии реакции могут быть выбраны подходящие растворители для конкретной стадии реакции. В некоторых вариантах реакции могут быть осуществлены в отсутствие растворителя, например, когда по меньшей мере один из реагентов является жидкостью или газом. Подходящие растворители могут включать галогенированные растворители, такие как четыреххлористый углерод, бромдихлорметан, дибромхлорметан, бромоформ, хлороформ, бромхлорметан,дибромметан, бутилхлорид, дихлорметан, тетрахлорэтилен, трихлорэтилен, 1,1,1-трихлорэтан,1,1,2-трихлорэтан, 1,1-дихлорэтан, 2-хлорпропан, -трифтортолуол, 1,2-дихлорэтан, 1,2-дибромэтан,гексафторбензол, 1,2,4-трихлорбензол, ортодихлорбензол, хлорбензол, фторбензол, фтортрихлорметан,хлортрифторметан, бромтрифторметан, четырехфтористый углерод, дихлорфторметан, хлордифторметан, трифторметан, 1,2-дихлортетрафторэтан и гексафторэтан. Подходящие эфирные растворители включают диметоксиметан, тетрагидрофуран, 1,3-диоксан,1,4-диоксан, фуран, диэтиловый эфир, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, диметиловый эфир диэтиленгликоля, диэтиловый эфир диэтиленгликоля, диметиловый эфир триэтиленгликоля, анизол или трет-бутилметиловый эфир.- 25016485 Подходящие протонные растворители могут включать в качестве примера и без ограничения воду,метанол, этанол, 2-нитроэтанол, 2-фторэтанол, 2,2,2-трифторэтанол, этиленгликоль, 1-пропанол,2-пропанол, 2-метоксиэтанол, 1-бутанол, 2-бутанол, изобутиловый спирт, трет-бутиловый спирт,2-этоксиэтанол, диэтиленгликоль, 1-, 2- или 3-пентанол, неопентиловый спирт, трет-пентиловый спирт,монометиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликоля, циклогексанол, бензиловый спирт, фенол или глицерин. Подходящие апротонные растворители могут включать в качестве примера и без ограничения тетрагидрофуран (ТГФ), диметилформамид (ДМФА), диметилацетамид (DMAC), 1,3-диметил-3,4,5,6 тетрагидро-2(1 Н)-пиримидинон (DMPU), 1,3-диметил-2-имидазолидинон (DMI), N-метилпирролидинон(NMP), формамид, N-метилацетамид, N-метилформамид, ацетонитрил, диметилсульфоксид, пропионитрил, этилформиат, метилацетат, гексахлорацетон, ацетон, этилметилкетон, этилацетат, сульфолан,N,N-диметилпропионамид, тетраметилмочевина, нитрометан, нитробензол или гексаметилфосфорамид. Подходящие углеводородные растворители включают бензол, циклогексан, пентан, гексан, толуол,циклогептан, метилциклогексан, гептан, этилбензол, мета-, орто- или параксилен, октан, индан, нонан или нафталин. Диоксид углерода в сверхкритическом состоянии также можно использовать в качестве растворителя. Реакции в приведенных в данном описании способах можно осуществлять при подходящих температурах, которые легко может определить специалист в данной области. Температуры реакции будут зависеть, например, от температуры плавления и кипения реагентов и растворителя, если таковой присутствует; термодинамики реакции (например, сильно экзотермические реакции могут требовать осуществления при пониженных температурах) и кинетики реакции (например, при высоком барьере энергии активации могут требоваться повышенные температуры). "Повышенная температура" относится к температурам выше комнатной температуры (примерно 20 С) и "пониженная температура" относится к температурам ниже комнатной температуры. Реакции в способах, приведенных в данном описании, можно осуществлять на воздухе или в инертной атмосфере. Обычно реакции с участием реагентов или продуктов, которые в значительной степени химически активны по отношению к воздуху, можно осуществлять с использованием чувствительных к воздуху способов синтеза, которые хорошо известны специалисту в данной области. В некоторых вариантах получение соединений может включать добавление кислот или оснований,чтобы, например, катализировать требуемую реакцию или осуществить образование солевых форм, таких как кислотно-аддитивные соли. Примерами кислот могут быть неорганические или органические кислоты. Неорганические кислоты включают хлористо-водородную, бромисто-водородную, серную, фосфорную и азотную кислоты. Органические кислоты включают муравьиную, уксусную, пропионовую, бутановую, метансульфоновую, паратолуолсульфоновую, бензолсульфоновую, трифторуксусную, пропионовую, масляную, 2-бутановую, винилуксусную, пентановую, гексановую, гептановую, октановую, нонановую и декановую кислоты. Примеры оснований включают гидроксид лития, гидроксид натрия, гидроксид калия, карбонат лития, карбонат натрия и карбонат калия. Некоторые примеры сильных оснований включают, но не ограничиваясь ими, гидроксид, алкоксиды, амиды металлов, гидриды металлов, диалкиламиды и ариламин металлов, при этом алкоксиды включают литиевые, натриевые и калиевые соли метил-, этил- и третбутилоксидов; амиды металлов включают амид натрия, амид калия и амид лития; гидриды металлов включают гидрид натрия, гидрид калия и гидрид лития; и диалкиламиды металлов включают натриевые и калиевые соли метил-, этил-, н-пропил-, изопропил-, н-бутил-, трет-бутил-, триметилсилил- и циклогексилзамещенные амиды. Соединения, приведенные в данном описании, могут быть асимметричными (например, имеющими один или несколько стереоцентров). Подразумеваются все стереоизомеры, такие как энантиомеры и диастереомеры, если не оговорено особо. Соединения настоящего изобретения, которые содержат асимметрично замещенные атомы углерода, могут быть выделены в оптически активной или рацемической форме. Способы получения оптически активных форм из оптически активных исходных веществ известны в данной области, такие как разделение рацемических смесей или стереоизбирательный синтез. Способы, приведенные в данном описании, могут быть стереоизбирательными, так чтобы в любой данной реакции, исходя из одного или нескольких хиральных реагентов, обогащенных по одной стереоизомерной форме, образовывался продукт, который также обогащен по одному стереоизомеру. Реакцию можно проводить так, чтобы в продукте реакции в основном сохранялся один или несколько хиральных центров, присутствующих в исходных веществах. Реакцию также можно проводить так, чтобы продукт реакции содержал хиральный центр, который главным образом инвертирован по сравнению с соответствующим хиральным центром, присутствующим в исходных веществах.- 26016485 Разделение рацемических смесей соединений можно осуществить любым из множества способов,известных в данной области. Примеры способов включают фракционную перекристаллизацию с использованием "хиральной разделяющей кислоты", которая является оптически активной, солеобразующей органической кислотой. Подходящими разделяющими агентами для способов фракционной перекристаллизации являются, например, оптически активные кислоты, такие как D- и L-формы винной кислоты, диацетилвинной кислоты, дибензоилвинной кислоты, миндальной кислоты, яблочной кислоты, молочной кислоты или различные оптически активные камфорсульфоновые кислоты, такие как-камфорсульфоновая кислота. Другие разделяющие агенты, подходящие для способов фракционной кристаллизации, включают стереомерно чистые формы -метилбензиламина (например, S- иR-формы или диастереомерно чистые формы), 2-фенилглицинола, норэфедрина, эфедрина,N-метилэфедрина, циклогексилэтиламина, 1,2-диаминоциклогексана, камфорной кислоты, -метокси-трифторметилфенилуксусной кислоты (МТРА или кислота Мошера), пирролидон-5-карбоновой кислоты,ди-О-изопропиленкетоглутаминовой кислоты, дитолуоилвинной кислоты и т.п. Разделение рацемических смесей также можно осуществить элюированием на колонке, упакованной оптически активным разделяющим агентом (например, динитробензоилфенилглицином). Подходящая комбинация растворителей для элюирования может быть определена специалистом в данной области. Соединения изобретения также могут содержать все изотопы атомов, встречающихся в промежуточных или конечных соединениях. Изотопы включают атомы, имеющие такое же атомное число, но другие массовые числа. Например, к изотопам водорода относится тритий и дейтерий. Соединения изобретения также могут включать таутомерные формы, такие как кетоенольные таутомеры. Таутомерные формы могут находиться в равновесии или стерически удерживаться в одной форме посредством подходящего замещения. В настоящее изобретение также включены солевые формы соединений, приведенных в данном описании. Примеры солей (или солевых форм) включают, но не ограничиваясь ими, соли неорганических или органических кислот основных остатков, таких как амины, щелочные или органические соли кислотных остатков, таких как карбоновые кислоты, и т.п. В общем солевые формы могут быть получены при взаимодействии свободного основания или кислоты со стехиометрическими количествами или с избытком требуемой солеобразующей неорганической или органической кислоты или основания в подходящем растворителе или в различных комбинациях растворителей. Списки подходящих солей можно найти в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., 1985, p. 1418,описание которой включено в данное описание посредством ссылки во всей своей полноте. При осуществлении получения соединений согласно способам, приведенным в данном описании,можно использовать обычные методы выделения и очистки, такие как концентрирование, фильтрование,экстракция, твердофазная экстракция, перекристаллизация, хроматография и т.п., чтобы выделить требуемые продукты. Изобретение будет описано более подробно с помощью конкретных примеров. Следующие примеры предлагаются в целях иллюстрации и никоим образом не предназначены для ограничения изобретения. Специалистам в данной области будут легко понятны различные некритические параметры, которые могут быть изменены или модифицированы с получением, по существу, таких же результатов. Примеры Пример 1. Получение 2-(4-хлорфенил)этил-N-2-хлорпропионамида В трехгорлую круглодонную колбу объемом 1 л, оборудованную баллоном, содержащим аргон, обратным холодильником и капельной воронкой, последовательно добавляли 2-(4-хлорфенил)этиламин(30 г, 193 ммоль), 400 мл ацетонитрила, триэтиламин (19,5 г, 193 ммоль) и 80 мл ацетонитрила. Прозрачный бесцветный раствор перемешивали и охлаждали до 0 С. Медленно в течение 20 мин добавляли 2-хлорпропионилхлорид (24,5 г, 193 ммоль, дистиллированный) в 5 мл ацетонитрила до выделения белого газа, образования белого осадка и изменения окраски реакционной смеси до слабо-желтой. Дополнительно использовали 10 мл ацетонитрила, чтобы промыть капельную воронку. Смесь перемешивали при 0 С в течение 30 мин, затем нагревали до комнатной температуры и энергично перемешивали еще в течение 1 ч. Желтую реакционную смесь концентрировали на роторном испарителе до твердого вещества,содержащего гидрохлорид триэтиламина (76,36 г). Полученный продукт переносили в 100 мл этилацетата и 200 мл воды и энергично перемешивали. Слои разделяли и водный слой экстрагировали дополнительно 100 мл этилацетата. Объединенные органические слои дважды промывали 25 мл насыщенного раствора соли, сушили над сульфатом магния, фильтровали и концентрировали до светлого желтокоричневого твердого вещества (41,6 г, 88%). ТСХ в смеси этилацетат-гексан, 8:2, выявила основное- 27016485 пятно в положении, составляющем две трети пути на пластине, и небольшое пятно на исходном уровне. Пятно на исходном уровне удаляли следующим образом: полученный продукт переносили в 40 мл этилацетата и добавляли гексан до тех пор, пока раствор не становился мутным. Охлаждение до 0 С давало белое кристаллическое твердое вещество (40,2 г, выход 85%). Продукт является известным соединением (Hasan et al., Indian J. Chem., 1971, 9 (9), 1022) с CAS No 34164-14-2. ЖХ/МС давала продукт в точке 2,45 мин; 246,1 МН+. 1 Н-ЯМР (CDCl3):7,2 (дд, 4 Н, Ar), 6,7 (уш.с, 1 Н, NH), 4,38 (кв, 1 Н, CHCH3), 3,5 (кв, 2 Н,ArCH2CH2NH), 2,8 (т, 2 Н, ArCH2), 1,7 (д, 3H, СН 3). 13 С-ЯМР (CDCl3): 169 (1 С, С=О), 136 (1 С, Ar-Cl), 132 (1 С, Ar), 130 (2 С, Ar), 128 (2 С, Ar), 56 (1 С,СНС 1), 40 (1 С, CHN), 34 (1 С, CHAr), 22 (1 С, СН 3). Пример 2. Получение 8-хлор-1-метил-2,3,4,5-тетрагидро-1 Н-3-бензазепин-2-она(16 г, 119,9 ммоль) добавляли в чистую сухую круглодонную колбу объемом 100 мл, оборудованную баллоном с аргоном, устройством для перемешивания и устройством для нагревания. Белое твердое вещество плавили до желто-коричневого масла при барботировании при 91 С. (Примечание: если используют неочищенные вещества, то может образовываться черная смола, но все же может быть выделен очищенный продукт). Смесь нагревали и перемешивали при 150 С в течение 12 ч. (Примечание: время зависит от масштаба реакции, и его может легко контролировать ЖХ/МС; более высокие температуры могут быть использованы в течение более коротких периодов времени. Например, образец массой 1 г был получен за 5 ч). За реакцией можно следить ЖХ/МС, при этом исходное вещество при 2,45 мин(246,1 МН+), продукт при 2,24 мин (209,6 МН+) при времени реакции 5 мин из смеси 5-95 мас.%/0,01% ТФУ в воде/MeCN (50:50). После охлаждения до комнатной температуры реакционную смесь гасили медленным добавлением 10 мл МеОН, затем 5 мл 5% HCl в воде и 5 мл этилацетата. После разделения полученных в результате слоев водный слой экстрагировали второй раз 10 мл этилацетата. Объединенные органические слои сушили над сульфатом магния, фильтровали и концентрировали до желто-коричневого твердого вещества(6,78 г, выход 80%). ЖХ/МС показала один пик при 2,2 мин и 209,6 MI. Полученный продукт переносили в этилацетат, фильтровали через целит и Kieselgel 60 (рыхлый слой 0,5 дюйма на воронке Бюхнера объемом 60 мл) и отфильтрованное вещество перекристаллизовывали из смеси гексан/этилацетат, получая конечный продукт (4,61 г, выход 54%). 1 Способ А. Очищенный ВЭЖХ 8-хлор-1-метил-2,3,4,5-тетрагидро-1 Н-3-бензазапин-2-он (150 мг, 0,716 ммоль) примера 2 добавляли в круглодонную колбу объемом 50 мл с 2 М раствором боран-тетрагидрофурана(2 мл, 2,15 ммоль). Смесь перемешивали 10 ч при комнатной температуре в атмосфере аргона, поступающего из баллона. ЖХ/МС выявила требуемый продукт в виде основного пика, при этом еще присутствовало примерно 5% исходного вещества. Реакционную смесь гасили 5 мл метанола и растворители удаляли на роторном испарителе. Данную операцию повторяли с добавлением метанола и выпариванием. Смесь упаривали на роторном испарителе, затем 2 ч в вакууме, получая продукт в виде белого твердого вещества (117 мг, выход 70%). ЯМР, ЖХ/МС и данные других анализом представлены ниже.(137 мг,0,653 ммоль) добавляли в круглодонную колбу объемом 50 мл при перемешивании в атмосфере газа азота. В колбу медленно добавляли раствор боран-тетрагидрофурана (1 М, 10 мл), затем раствор трифторид бора-ТВМЕ (1 мл, 8,85 ммоль) с интенсивным выделением газа. Смесь перемешивали в течение 6 ч при комнатной температуре в атмосфере газа азота. ЖХ/МС выявила требуемый продукт. Реакционную смесь гасили 5 мл метанола и 3 мл концентрированной HCl и растворители удаляли на роторном испарителе. Указанную операцию повторяли с добавлением метанола и HCl и выпариванием. Смесь упаривали досуха на роторном испарителе, затем 2 ч с использованием насоса, получая гидрохлорид 8-хлор-1 метил-2,3,4,5-тетрагидро-1 Н-3-бензазапина (106 мг, выход 70%). 1 Н-ЯМР (CDCl3): 10,2 (уш.с, 1 Н), 9,8 (уш.с, 1 Н), 7,14 (дд, 1 Н, J=2, 8 Гц), 7,11 (д, 1 Н, J=2 Гц), 7,03 (д,1 Н, J=8 Гц), 3,6 (м, 2 Н), 3,5 (м, 2 Н), 2,8-3,0 (м, 3 Н), 1,5 (д, 3H, J=7 Гц). ЖХ/МС: 1,41 мин, 196,1 М+Н+ и основной фрагмент 139. Примесей не обнаружено. Пример 4. Получение L-(+)-виннокислой соли (R)-8-хлор-1-метил-2,3,4,5-тетрагидро-1 Н-3 бензазепина В чистую сухую круглодонную колбу объемом 50 мл добавляли 11,5 г (0,06 моль) 8-хлор-1-метил 2,3,4,5-тетрагидро-1 Н-3-бензазепина из примера 3 к 2,23 г (0,015 моль) L-(+)-винной кислоты. Суспензию разбавляли 56 г трет-бутанола и 6,5 мл Н 2 О. Смесь кипятили с обратным холодильником (75-78 С) и перемешивали в течение 10 мин, получая бесцветный раствор. Раствор медленно охлаждали до комнатной температуры (в течение 1 ч) и перемешивали в течение 3 ч при комнатной температуре. Суспензию фильтровали и остаток дважды промывали ацетоном (10 мл). Продукт сушили при пониженном давлении (50 мбар) при 60 С, получая 6,3 г тартратной соли (ее=80). Тартратную соль добавляли к 56 г третбутанола и 6,5 мл Н 2 О. Полученную в результате суспензию кипятили с обратным холодильником и добавляли 1-2 г Н 2 О, получая бесцветный раствор. Раствор медленно охлаждали до комнатной температуры (в течение 1 ч) и перемешивали в течение 3 ч при комнатной температуре. Суспензию фильтровали и остаток дважды промывали ацетоном (10 мл). Продукт сушили при пониженном давлении (50 мбар) при 60 С, получая 4,9 г (выход 48%) продукта (ее 98,9). Если значение ее полученного продукта неудовлетворительно, можно осуществить дополнительную перекристаллизацию, как описано выше. С использованием данного способа можно синтезировать любой энантиомер с высоким значением ее. Пример 5. Превращение солевой формы в свободный амин.L-виннокислую соль 8-хлор-1-метил-2,3,4,5-тетрагидро-1 Н-3-бензазепина (300 мг, 0,87 ммоль) из примера 4 добавляли в круглодонную колбу объемом 25 мл с 50% раствором гидроксида натрия(114 мкл, 2,17 ммоль) с добавлением 2 мл воды. Смесь перемешивали 3 мин при комнатной температуре. Раствор дважды экстрагировали метиленхлоридом (5 мл). Объединенные органические экстракты промывали водой (5 мл) и упаривали досуха, используя насос, получая свободный амин (220 мг грубой массы). ЖХ/МС 196 (М+Н). Пример 6. Получение 2-хлор-N-(4-хлорфенил)пропан-1-амина В сухую круглодонную колбу объемом 100 мл в атмосфере азота при перемешивании добавляли 2-(4-хлорфенил)этил-N-2-хлорпропиониламид (8,8 г, 35,8 ммоль), затем боран в ТГФ (1,8 М, 70 мл,140 ммоль) в течение 10 мин (происходило выделение газа и твердое вещество переходило в раствор). После завершения добавления добавляли трифторид бора в трет-бутилметиловом эфире (8 мл,70,8 ммоль) в течение 10 мин с дополнительным выделением газа. Через 4 ч ЖХ/МС показала завершение реакции. Реакционную смесь гасили 20 мл концентрированной HCl (37%) с дополнительным выделением газа. Реакционную смесь перемешивали при 40 С в течение 2 ч, охлаждали до комнатной температуры и упаривали. Затем белую взвесь переносили в 40 мл этилацетата и 20 мл 2,5 М NaOH, получая желтый раствор над белой взвесью. Желтый органический слой промывали насыщенным раствором соли, сушили над сульфатом магния, фильтровали и упаривали, получая 12,2 г твердого вещества, имею- 29
МПК / Метки
МПК: C07D 223/16, A61K 31/55, A61P 25/00, C07C 233/13
Метки: 3-бензазепинов, способы, получения
Код ссылки
<a href="https://eas.patents.su/30-16485-sposoby-polucheniya-3-benzazepinov.html" rel="bookmark" title="База патентов Евразийского Союза">Способы получения 3-бензазепинов</a>
Предыдущий патент: Способ изготовления огнеупоров
Следующий патент: Обнаружение и мониторинг частичного разряда в линии электропередачи
Случайный патент: Способ проведения клеточной терапии для лечения экспериментального хронического орхоэпидидимита