Низкомолекулярные ингибиторы mdm2 и их применения
Номер патента: 14445
Опубликовано: 30.12.2010
Авторы: Ван Гопин, Николовска-Цолеска Занета, Цинь Дунгуан, Цю Су, Дин Кэ, Кумар Санжеев, Лу Ипинь, Ван Шаомэн
Формула / Реферат
1. Соединение, имеющее формулу X
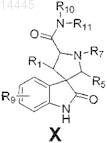
или его фармацевтически приемлемая соль,
где R1представляет собой:
а) C1-18алкил, С3-8циклоалкил или С5-10гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, С5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси, или
б) C6-14арил, необязательно имеющий один или два заместителя, независимо выбранных из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10 гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-С1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, С3-8 гетероцикл-С1-6ацила и С3-8гетероциклалкокси;
R5 представляет собой C1-18алкил или С6-14арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, С6-14арила, С6-14арилокси, C5-10гетероарила, С5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, С6-14арил-С1-6ацилокси, дифенилфосфинилокси, С3-8 гетероцикла, С3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R7 представляет собой водород, C1-18алкил, CONR'R" или CO2R';
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I, C1-3алкил или OR';
каждый R' и R" независимо представляет собой водород, C1-18алкил, С3-8циклоалкил или C5-10гетероцикл;
R10 и R11 независимо представляют собой:
а) водород,
б) C1-18алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, С5-10гетероарилокси, C1-6 алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14 арил-C1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, С3-8гетероцикл-C1-6ацила и С3-8 гетероциклалкокси,
в) (CH2)n-R',
г) (CH2)n-NR'R",
д) (CH2)n-CONR'R",
е) (CH2)n-OR',
ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или
з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либо
R10 и R11 образуют C3-8гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, С5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, С3-8гетероцикл-C1-6ацила и С3-8гетероциклалкокси; и
n, m и р, каждое независимо, равны 1-4.
2. Соединение по п.1, имеющее одну из формул XI-XXVI
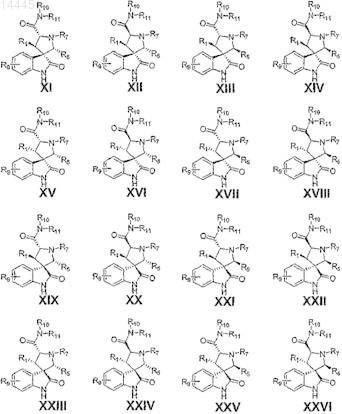
или его фармацевтически приемлемая соль.
3. Соединение по п.2, имеющее формулу XI или XXVI
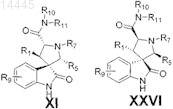
или его фармацевтически приемлемая соль.
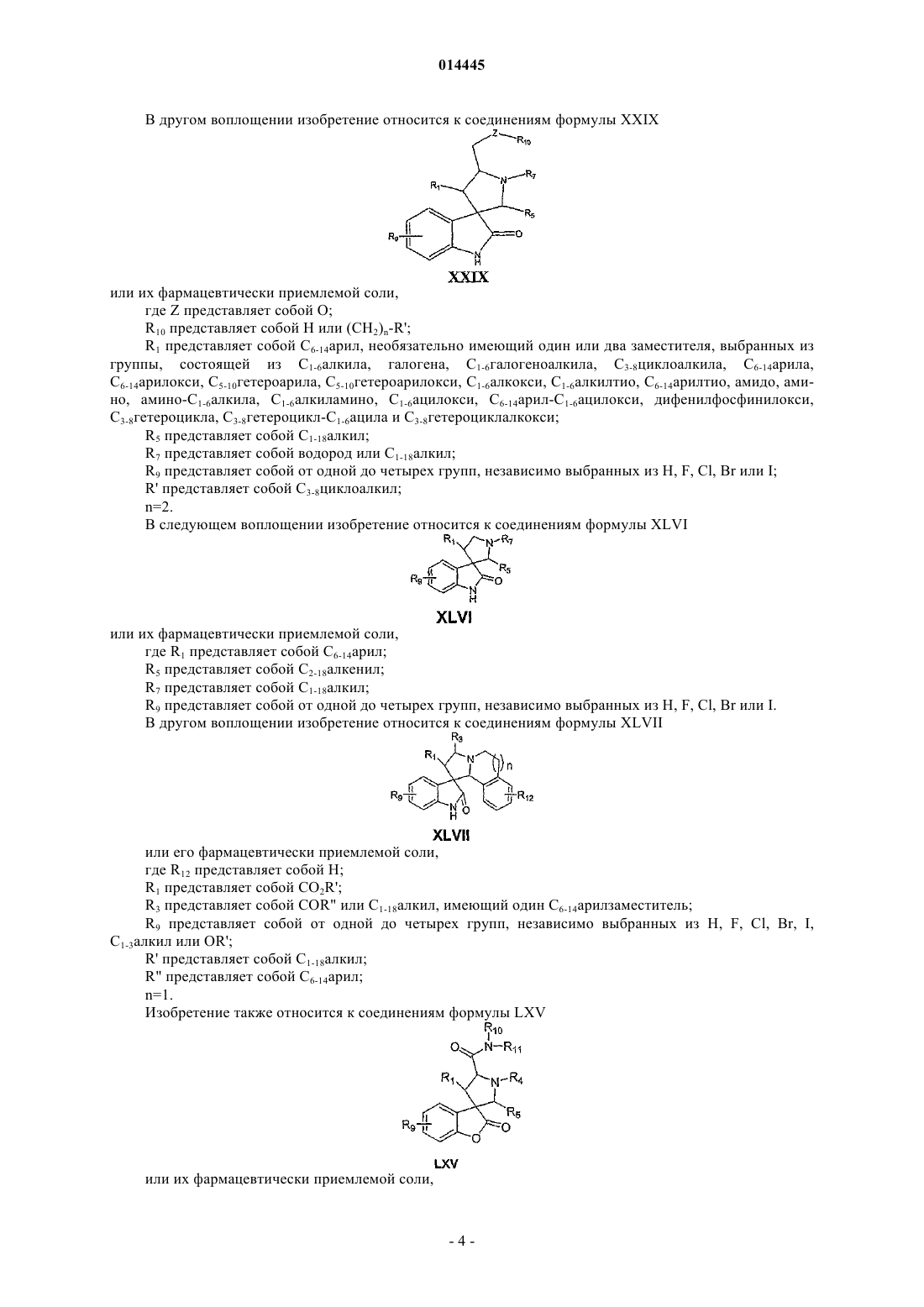
4. Соединение, имеющее формулу XXIX
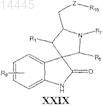
или его фармацевтически приемлемая соль,
где Z представляет собой О;
R10 представляет собой Н или (CH2)n-R';
R1 представляет собой С6-14арил, необязательно имеющий один или два заместителя, выбранных из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, С5-10 гетероарила, С5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, С6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, С6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, С3-8 гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R5 представляет собой C1-18алкил;
R7 представляет собой водород или C1-18алкил;
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I;
R' представляет собой C3-8циклоалкил;
n=2.
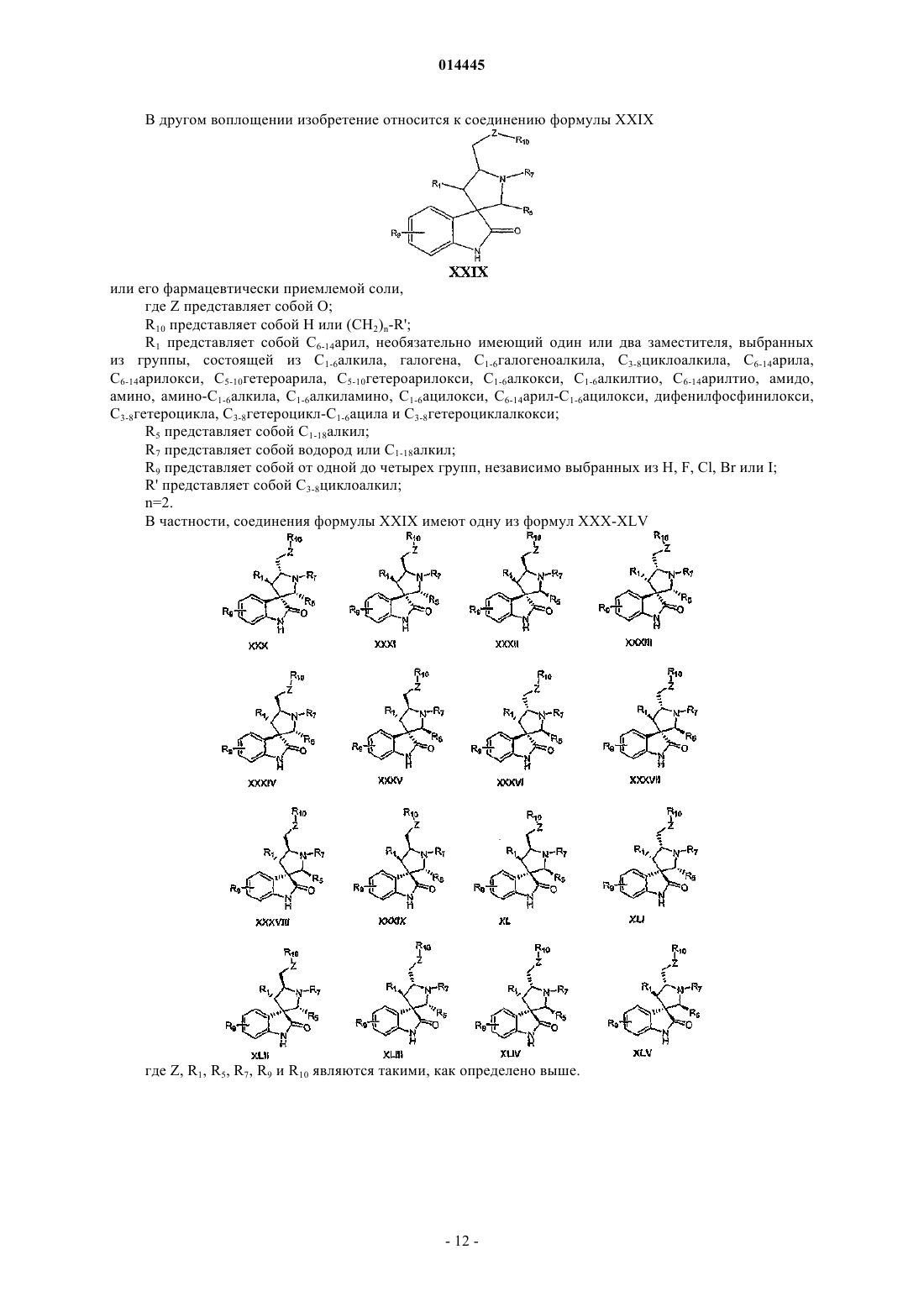
5. Соединение по п.4, имеющее одну из формул XXX-XLV

или его фармацевтически приемлемая соль.
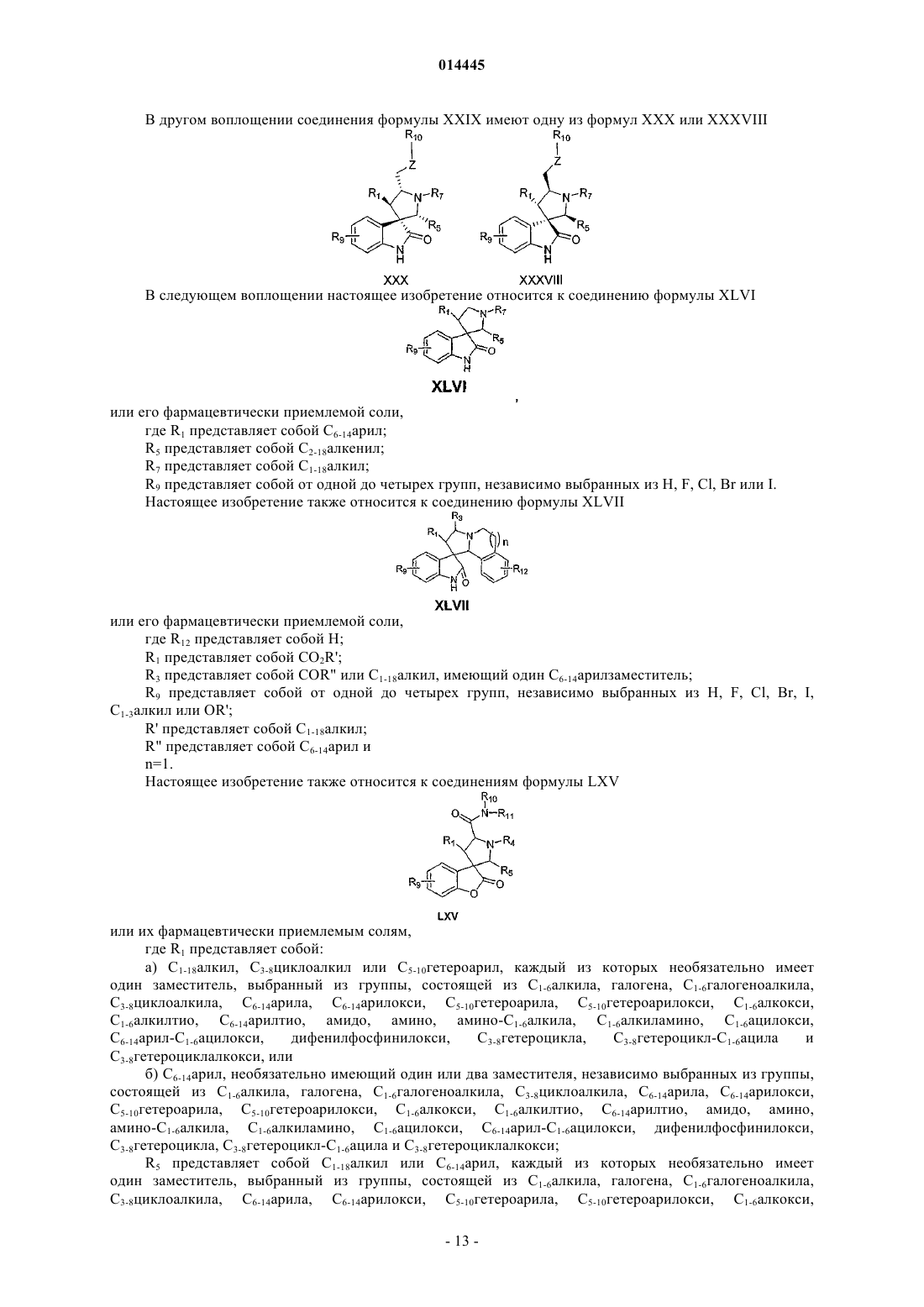
6. Соединение по п.5, имеющее одну из формул XXX или XXXVIII

или его фармацевтически приемлемая соль.
7. Соединение, имеющее формулу XLVI
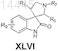
или его фармацевтически приемлемая соль,
где R1представляет собой C6-14арил;
R5 представляет собой С2-18алкенил;
R7 представляет собой C1-18алкил;
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I.
8. Соединение, имеющее формулу XLVII
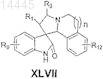
или его фармацевтически приемлемая соль,
где R12 представляет собой Н;
R1 представляет собой CO2R';
R3 представляет собой COR" или C1-18алкил, имеющий один C6-14арилзаместитель;
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I, C1-3алкил или OR';
R' представляет собой С1-18алкил;
R" представляет собой С6-14арил и
n=1.
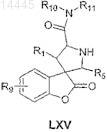
9. Соединение, имеющее формулу LXV
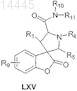
или его фармацевтически приемлемая соль,
где R1представляет собой:
а) C1-18алкил, C3-8циклоалкил или C5-10гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси, или
б) C6-14арил, необязательно имеющий один или два заместителя, независимо выбранных из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10 гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, С1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, C3-8 гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R5 представляет собой C1-18алкил или C6-14арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8 гетероцикла, C3-8гетероцикл-C1-6ацила и С3-8гетероциклалкокси;
R7 представляет собой водород, C1-18алкил, CONR'R" или CO2R';
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I, С1-3алкил или OR';
каждый R' и R" независимо представляет собой водород, C1-18алкил, С3-8циклоалкил или C5-10гетероцикл;
R10 и R11 независимо представляют собой:
а) водород,
б) C1-18алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, C3-8циклоалкила, C6-14арила, С6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6 алкокси, С1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14 арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, C3-8гетероцикл-C1-6ацила и С3-8 гетероциклалкокси,
в) (CH2)n-R',
г) (CH2)n-NR'R",
д) (CH2)n-CONR'R",
е) (CH2)n-OR',
ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или
з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либо
R10 и R11 образуют С3-8гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, С6-14арилтио, амидо, амино, амино-C1-6 алкила, C1-6алкиламино, C1-6ацилокси, С6-14арил-С1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, C3-8 гетероцикл-C1-6ацила и С3-8гетероциклалкокси; и
n, m и p, каждое независимо, равны 1-4.
10. Соединение по п.9, имеющее одну из формул LXVI и LXVII
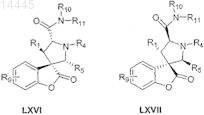
или его фармацевтически приемлемая соль.
11. Соединение, выбранное из группы, состоящей из
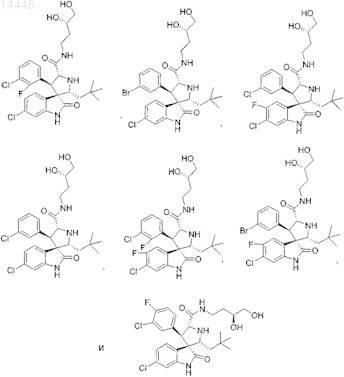
или его фармацевтически приемлемая соль.
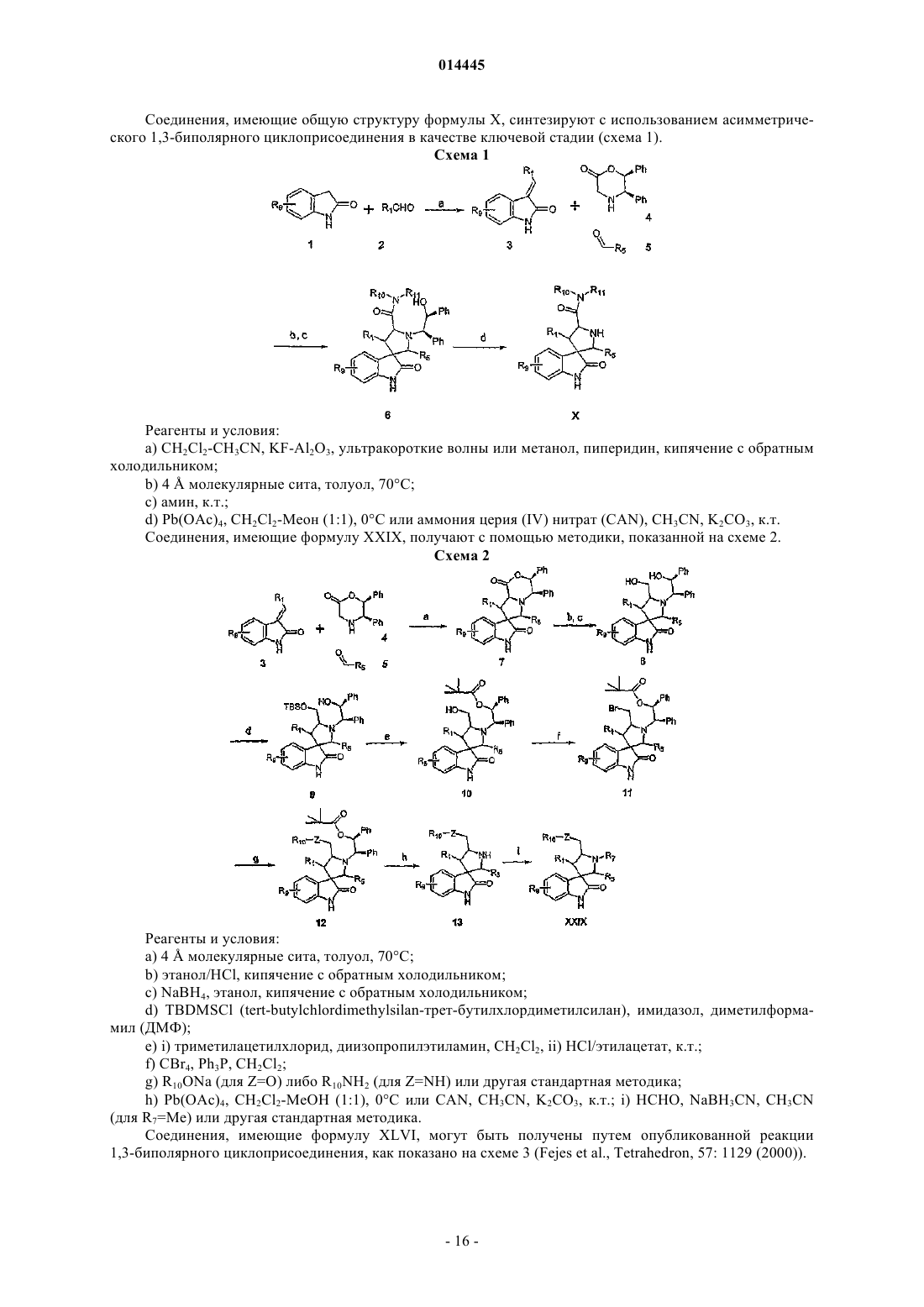
12. Способ получения соединения формулы X, при котором:
а) подвергают конденсации соединение формулы 1 с соединением формулы 2 с образованием соединения формулы 3

б) подвергают конденсации соединение формулы 3 с соединением формулы 4 и с соединением формулы 5 с образованием соединения формулы 6

в) обрабатывают соединение формулы 6 окисляющим агентом с образованием соединения формулы X
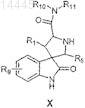
где R1представляет собой:
a) C1-18алкил, C3-8циклоалкил или C5-10гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, С6-14арилокси, С5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси, или
б) C6-14арил, необязательно имеющий один или два заместителя, независимо выбранных из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, С6-14арила, C6-14арилокси, C5-10 гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, С6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, C3-8 гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R5 представляет собой C1-18алкил или C6-14арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, С5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8 гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R7 представляет собой водород, C1-18алкил, CONR'R" или CO2R';
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I, C1-3алкил или OR';
каждый R' и R" независимо представляет собой водород, C1-18алкил, С3-8циклоалкил или C5-10гетероцикл;
R10 и R11 независимо представляют собой:
а) водород,
б) C1-18алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, С5-10гетероарила, C5-10гетероарилокси, C1-6 алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14 арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, С3-8гетероцикл-C1-6ацила и С3-8 гетероциклалкокси,
в) (CH2)n-R',
г) (CH2)n-NR'R",
д) (CH2)n-CONR'R",
е) (CH2)n-OR',
ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или
з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либо
R10 и R11 образуют С3-8гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6 алкила, C1-6алкиламино, C1-6ацилокси, С6-14арил-C1-6ацилокси, дифенилфосфинилокси, С3-8гетероцикла, С3-8 гетероцикл-C1-6ацила и С3-8гетероциклалкокси; и
n, m и p, каждое независимо, равны 1-4.
13. Способ получения соединения формулы LXV, при котором:
а) подвергают конденсации соединение формулы 16 с соединением формулы 2 с образованием соединения формулы 17
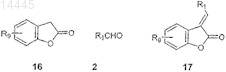
б) подвергают конденсации соединение формулы 17 с соединением формулы 4 и с соединением формулы 5 с образованием соединения формулы 18
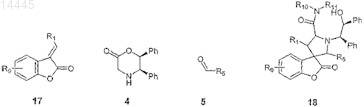
в) обрабатывают соединение формулы 18 окисляющим агентом с образованием соединения формулы LXV
где R1представляет собой:
а) C1-18алкил, C3-8циклоалкил или C5-10гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, С6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси, или
б) C6-14арил, необязательно имеющий один или два заместителя, независимо выбранных из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10 гетероарила, С5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, С6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, С3-8 гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R5 представляет собой C1-18алкил или C6-14арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14арилокси, С5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, С6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8 гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R7 представляет собой водород, C1-18алкил, CONR'R" или CO2R';
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I, C1-3алкил или OR';
каждый R' и R" независимо представляет собой водород, C1-18алкил, C3-8циклоалкил или C5-10гетероцикл;
R10 и R11 независимо представляют собой:
а) водород,
б) C1-18алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, С3-8циклоалкила, C6-14арила, C6-14арилокси, C5-10гетероарила, С5-10гетероарилокси, C1-6 алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14 арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, С3-8гетероцикл-C1-6ацила и C3-8 гетероциклалкокси,
в) (CH2)n-R',
г) (CH2)n-NR'R",
д) (CH2)n-CONR'R",
е) (CH2)n-OR',
ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или
з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либо
R10 и R11 образуют C3-8гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, С3-8циклоалкила, C6-14арила, С6-14арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, C6-14арилтио, амидо, амино, амино-C1-6 алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8гетероцикла, С3-8 гетероцикл-C1-6ацила и С3-8гетероциклалкокси, и
n, m и р, каждое независимо, равны 1-4.
14. Способ получения соединения формулы XXIX, при котором:
а) подвергают конденсации соединение формулы 3 с соединением формулы 4 и с соединением формулы 5 с образованием соединения формулы 7
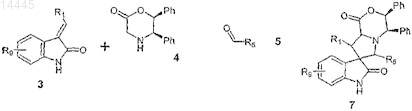
б) нагревают соединение формулы 7 в присутствии кислоты, а затем добавляют восстанавливающий агент с образованием соединения формулы 8
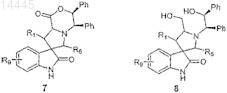
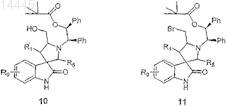
в) подвергают соединение формулы 8 конденсации с блокирующим агентом, после чего обрабатывают триметилацетилхлоридом и затем кислотой с образованием соединения формулы 10
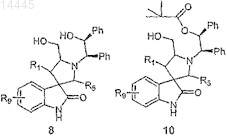
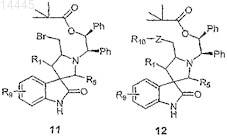
г) обрабатывают соединение формулы 10 галогенирующим агентом с образованием галогеносоединения формулы 11
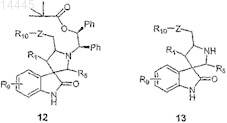
д) замещают галогеновую группу соединения формулы 11 R10ONa или R10NH2с образованием соединения формулы 12
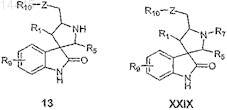
е) обрабатывают соединение формулы 12 окисляющим агентом с образованием соединения формулы 13 и
ж) алкилируют соединение формулы 13 алкилирующим агентом с образованием соединения формулы XXIX
где Z представляет собой О;
R10 представляет собой водород или (CH2)n-R';
R1 представляет собой C6-14арил, необязательно имеющий один или два заместителя, независимо выбранных из группы, состоящей из C1-6алкила, галогена, C1-6галогеноалкила, C3-8циклоалкила, C6-14арила, C6-14 арилокси, C5-10гетероарила, C5-10гетероарилокси, C1-6алкокси, C1-6алкилтио, С6-14арилтио, амидо, амино, амино-C1-6алкила, C1-6алкиламино, C1-6ацилокси, C6-14арил-C1-6ацилокси, дифенилфосфинилокси, C3-8 гетероцикла, C3-8гетероцикл-C1-6ацила и C3-8гетероциклалкокси;
R5 представляет собой C1-18алкил;
R7 представляет собой водород или C1-18алкил;
R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I;
R' представляет собой C3-8гетероцикл и
n=2.
15. Способ ингибирования клеточного роста или деления, индукции апоптоза или индукции остановки клеточного цикла у клетки, при котором клетку приводят в контакт с соединением по любому из пп.1-11.
16. Способ придания клетке чувствительности к дополнительному агенту (агентам), при котором клетку приводят в контакт с соединением по любому из пп.1-11.
17. Способ по п.16, при котором клетку дополнительно приводят в контакт с дополнительным агентом (агентами).
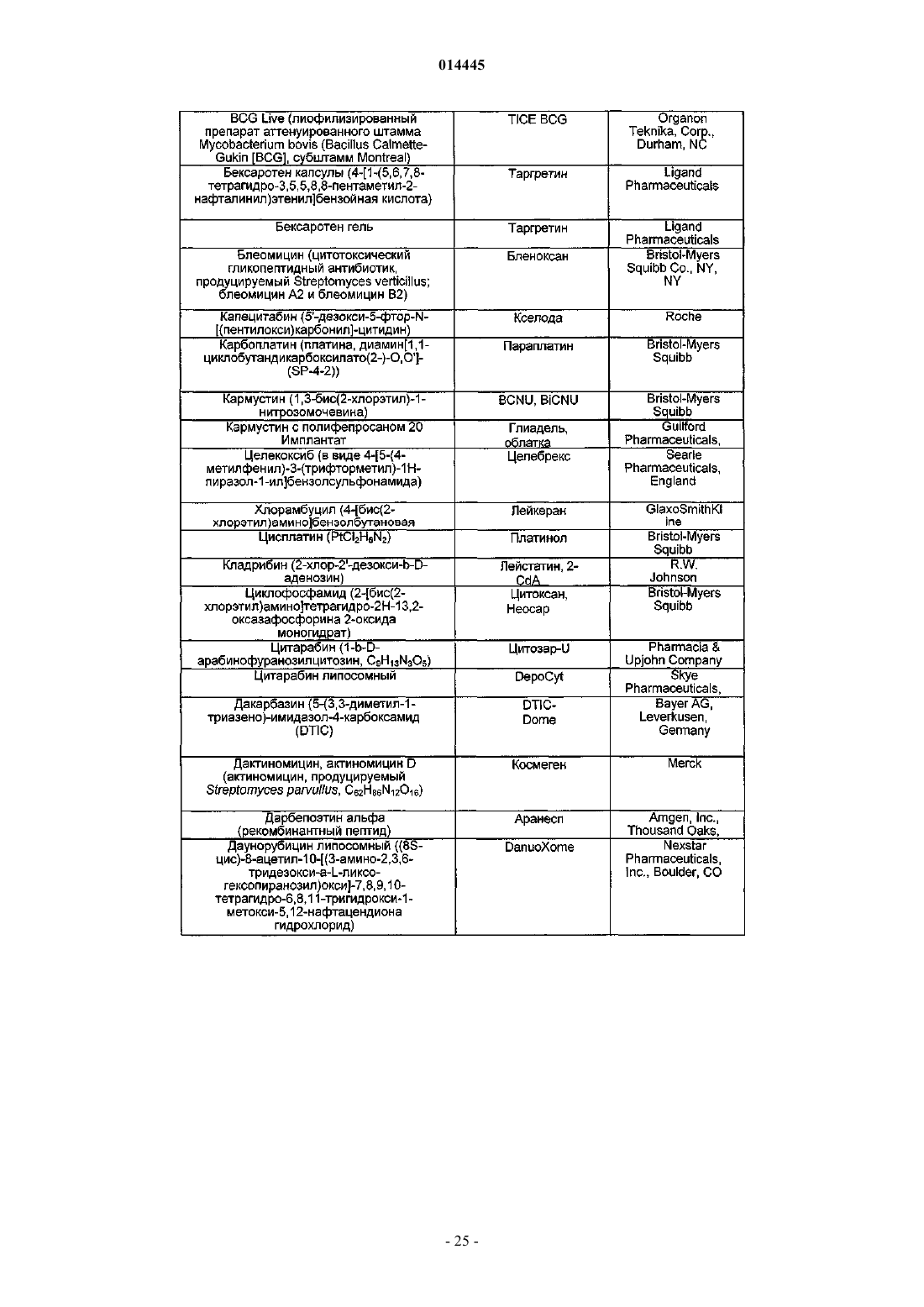
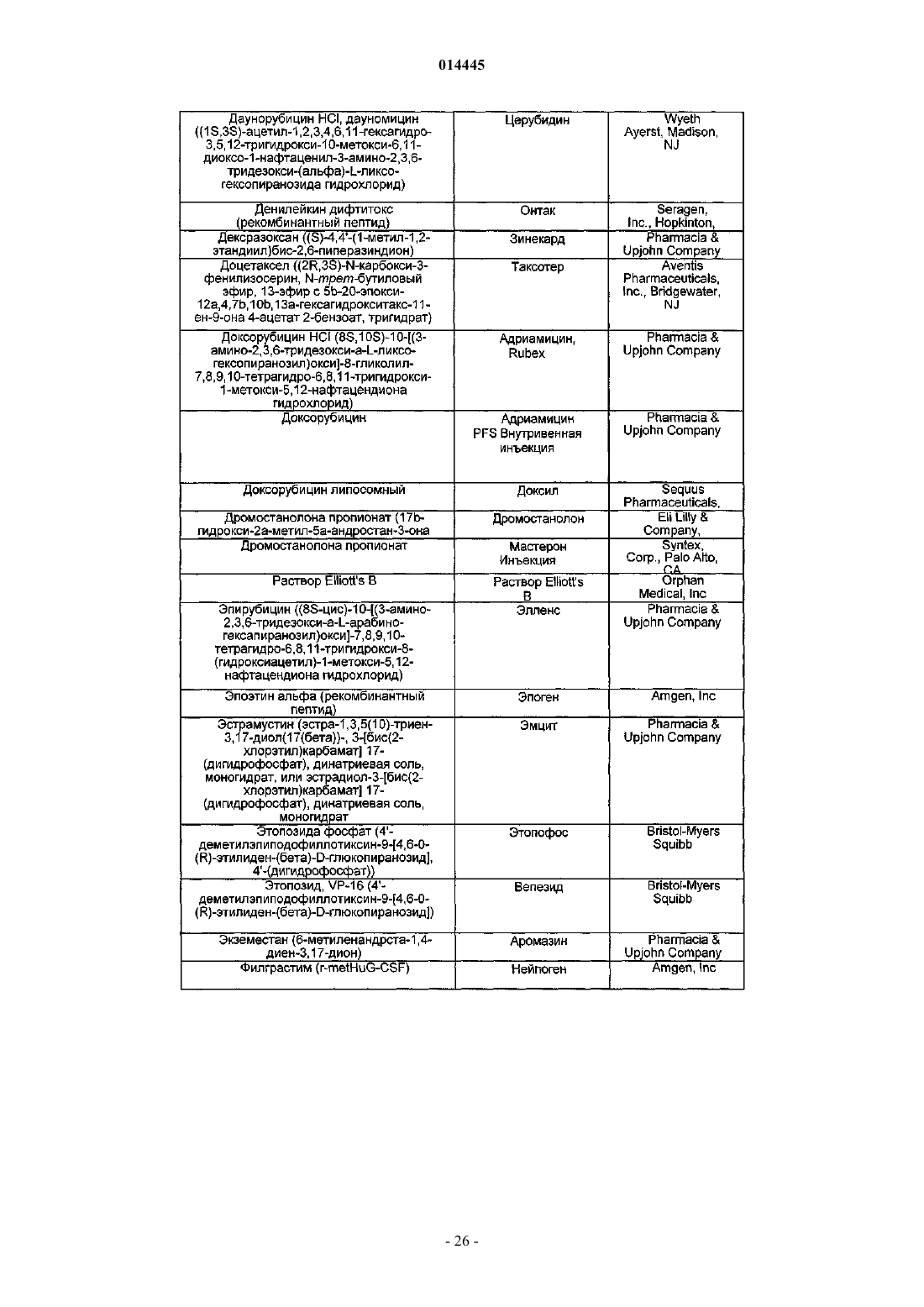
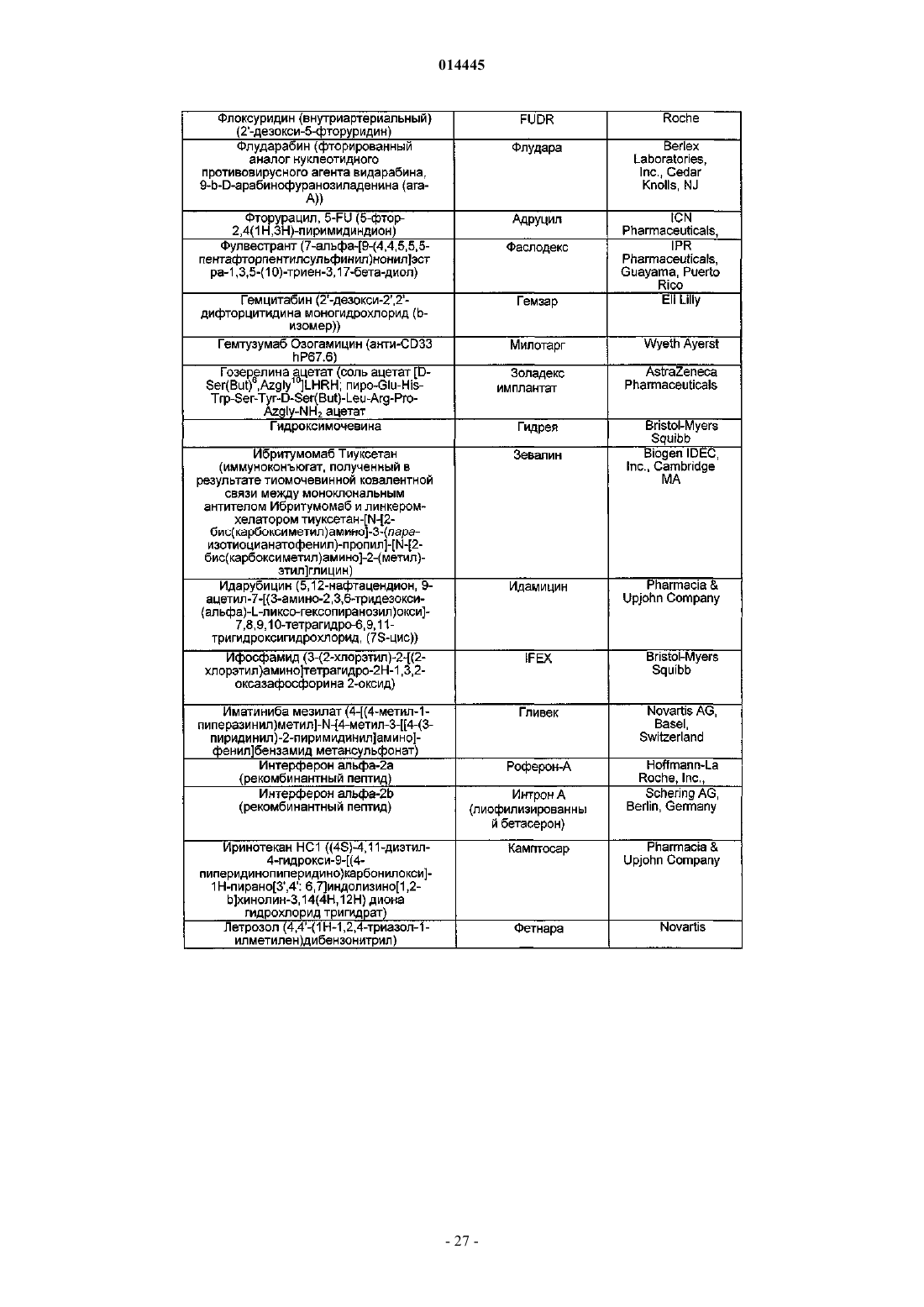
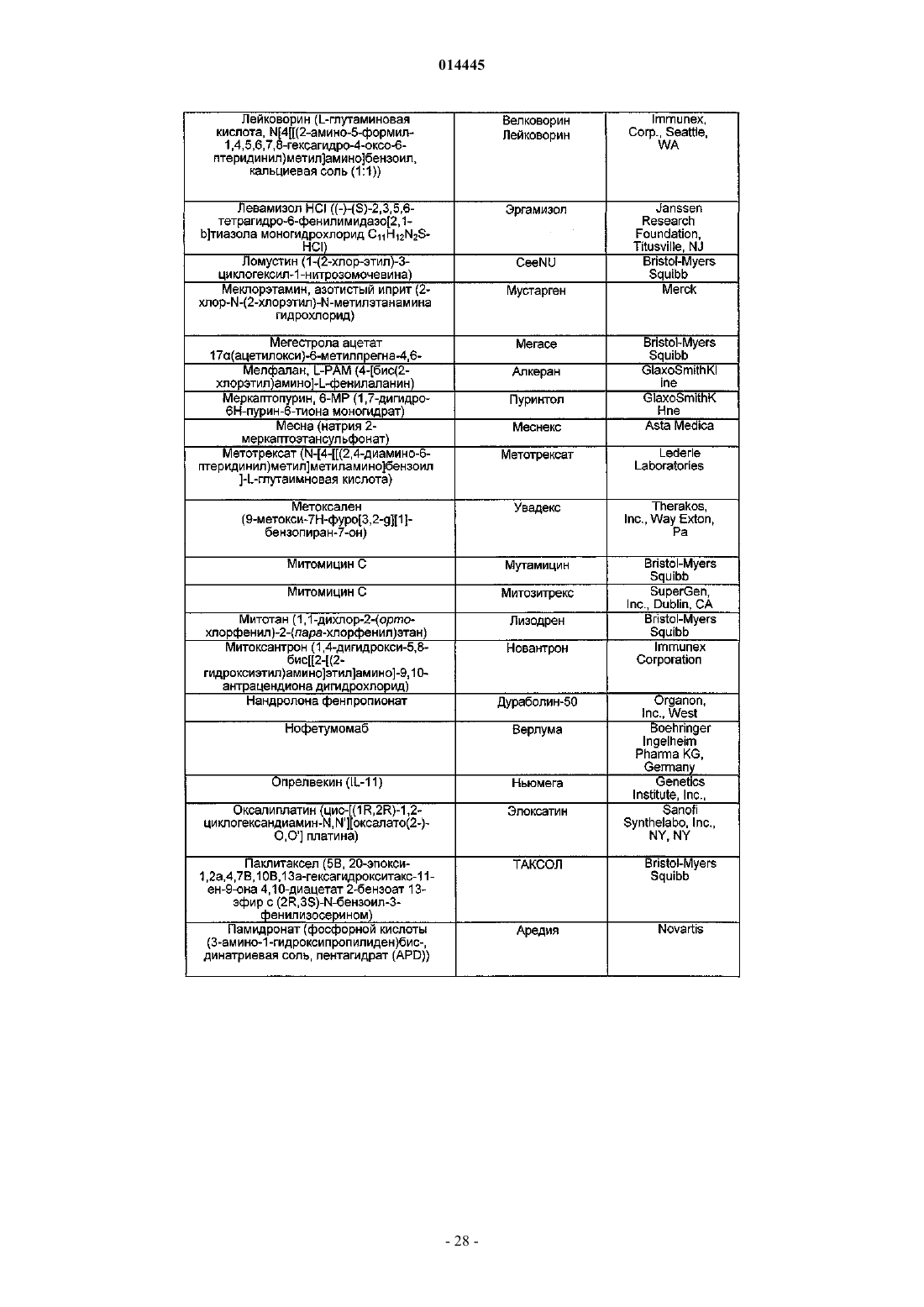
18. Способ по п.17, где указанный дополнительный агент (агенты) представляет собой химиотерапевтический агент.
19. Способ по п.17, где указанный дополнительный агент (агенты) представляет собой облучение.
20. Фармацевтическая композиция для лечения рака у животного, содержащая соединение по любому из пп.1-11 и фармацевтически приемлемый носитель.
21. Способ лечения или облегчения рака у животного, при котором указанному животному вводят терапевтически эффективное количество соединения по любому из пп.1-11.
22. Способ по п.21, при котором дополнительно вводят дополнительный агент (агенты).
23. Способ по п.22, где указанный дополнительный агент (агенты) представляет собой химиотерапевтический агент.
24. Способ по п.22, где указанный дополнительный агент (агенты) представляет собой облучение.
25. Способ по п.22, где указанное соединение по любому из пп.1-11 вводят до указанного дополнительного агента (агентов).
26. Способ по п.22, где указанное соединение по любому из пп.1-11 вводят после указанного дополнительного агента (агентов).
27. Способ по п.22, где указанное соединение по любому из пп.1-11 вводят одновременно с указанным дополнительным агентом (агентами).
28. Способ ингибирования взаимодействия между р53 или родственными р53 белками и MDM2 или родственными MDM2 белками в клетке, при котором клетку подвергают воздействию соединения по любому из пп.1-11.
29. Способ ингибирования роста гиперпролиферативной клетки, содержащей функциональный р53 или родственные р53 белки, при котором клетку подвергают воздействию соединения по любому из пп.1-11.
30. Способ лечения, облегчения или профилактики рака, характеризующегося экспрессией р53 или родственных р53 белков у животного, при котором указанному животному вводят терапевтически эффективное количество соединения по любому из пп.1-11.
31. Способ придания нормальной клетке устойчивости к химиотерапевтическим агентам или лечению, при котором клетку приводят в контакт с соединением по любому из пп.1-11.
32. Способ по п.31, где указанная нормальная клетка содержит р53 дикого типа.
33. Способ защиты нормальных клеток у животного с раком от токсических побочных эффектов химиотерапевтических агентов или лечения, при котором указанному животному вводят соединение по любому из пп.1-11.
34. Способ по п.33, где указанные нормальные клетки содержат р53 дикого типа.
35. Способ по п.33, где указанный рак включает мутацию или делецию р53.
36. Набор, включающий соединение по любому из пп.1-11 и инструкции по введению указанного соединения животному, имеющему рак.
37. Набор по п.36, дополнительно включающий химиотерапевтический агент.
Текст
(71)(73) Заявитель и патентовладелец: ДЗЕ РИДЖЕНТС ОФ ДЗЕ ЮНИВЕРСИТИ ОФ МИЧИГАН (US)(57) Изобретение относится к малым молекулам, которые функционируют как ингибиторы взаимодействия между р 53 и MDM2. Изобретение также относится к применению этих соединений для ингибирования клеточного роста, включая клеточную гибель, индукцию остановки клеточного цикла и/или сенсибилизацию клеток к дополнительному агенту(ам). 014445 Область изобретения Данное изобретение находится в области химии лекарственных средств. В частности, изобретение относится к малым молекулам, которые функционируют как антагонисты взаимодействия между р 53 иMDM2 (Murine Double Minute 2-белок мышиных двойных микрохромосом 2), и к их применению в качестве нового класса терапевтических агентов для лечения рака и других заболеваний. Уровень техники Агрессивный фенотип раковой клетки является результатом ряда генетических и эпигенетических изменений, приводящих к нарушению регуляции внутриклеточных путей передачи сигнала (Ponder,Nature, 411: 336 (2001. Общим для всех раковых клеток, однако, является их неспособность к выполнению апоптотической программы, и отсутствие правильного апоптоза вследствие дефектов в нормальном механизме апоптоза является отличительным признаком рака (Lowe et al., Carcinogenesis, 27: 485 (2000. Неспособность раковых клеток к выполнению апоптотической программы вследствие дефектов в нормальном механизме апоптоза, таким образом, часто связана с устойчивостью к апоптозу, индуцированному химиотерапией, облучением или иммунотерапией. Первичная или приобретенная устойчивость рака человека различного происхождения к современным терапевтическим протоколам вследствие дефектов апоптоза является основной проблемой в современной терапии рака (Lowe et al., Carcinogenesis 27: 485 (2000); Nicholson, Nature, 407: 810 (2000. Соответственно настоящие и будущие усилия в направлении проектирования и разработки новых, специфичных к молекулярной мишени противораковых терапий для улучшения выживаемости и качества жизни больных раком должны включать стратегии,которые специфично направлены на устойчивость раковых клеток к апоптозу. В этом отношении направленность на критические негативные регуляторы, которые играют центральную роль в прямом ингибировании апоптоза в раковых клетках, представляет собой высокоперспективную терапевтическую стратегию для разработки новых противораковых лекарственных средств. Опухолевый супрессор р 53 играет центральную роль в контроле прохождения клеточного цикла и апоптоза (Vogelstem et al., Nature, 408: 307 (2000. Он является привлекательной терапевтической мишенью для разработки противораковых лекарственных средств, поскольку его активность как опухолевого супрессора можно стимулировать для уничтожения опухолевых клеток (Vogelstein et al., Nature, 408: 307(2000); Chene, Nat. Rev. Cancer, 3: 102 (2003. Новым подходом к стимуляции активности р 53 является стимуляция посредством ингибирования его взаимодействия с белком MDM2 с использованием непептидных низкомолекулярных ингибиторов (Chene, Nat. Rev. Cancer, 3: 102 (2003); Vassilev et al., Science,303: 844 (2004. MDM2 и р 53 составляют часть саморегулирующейся петли обратной связи (Wu et al.,Genes Dev. 7: 1126 (1993. Транскрипция MDM2 активируется р 53, и MDM2, в свою очередь, ингибирует активность р 53 посредством по меньшей мере трех механизмов (Wu et al., Genes Dev. 7: 1126 (1993. Во-первых, белок MDM2 непосредственно связывается с доменом трансактивации р 53 и посредством этого ингибирует р 53-опосредованную трансактивацию. Во-вторых, белок MDM2 содержит сигнальную последовательность ядерного экспорта, и при связывании с р 53 индуцирует экспорт р 53 из ядра, предотвращая связывание р 53 с ДНК-мишенями. В-третьих, белок MDM2 является Е 3 убиквитинлигазой, и при связывании с р 53 способен стимулировать распад р 53. Следовательно, посредством функционирования в качестве эффективного эндогенного клеточного ингибитора активности р 53, MDM2 эффективно ингибирует р 53-опосредованный апоптоз, остановку клеточного цикла и репарацию ДНК. Таким образом, низкомолекулярные ингибиторы, которые связываются с MDM2 и блокируют взаимодействие между MDM2 и р 53, могут стимулировать активность р 53 в клетках с функциональным р 53 и стимулировать р 53 опосредованные клеточные эффекты, такие как остановка клеточного цикла, апоптоз или репарация ДНК(Chene, Nat. Rev. Cancer, 3: 102 (2003); Vassilev et al., Science 303: 844 (2004. Хотя высокоаффинные ингибиторы на основе пептидов ранее были успешно сконструированы(Garcia-Echeverria et al., Med. Chem. 43: 3205 (2000, эти ингибиторы являются молекулами, подобными лекарствам, в связи с плохими клеточной проницаемостью и биодоступностью in vivo. Несмотря на интенсивные усилия фармацевтической промышленности, стратегии высокопроизводительного скрининга имели весьма ограниченный успех при идентификации эффективных непептидных низкомолекулярных ингибиторов. Соответственно существует необходимость в непептидных, подобных лекарствам, низкомолекулярных ингибиторах взаимодействия p53-MDM2. Разработка непептидных низкомолекулярных ингибиторов, которые направлены на взаимодействиеp53-MDM2, продолжается в настоящее время, будучи привлекательной стратегией для разработки противораковых лекарственных средств (Chene, Nat. Rev. Cancer, 5: 102 (2003); Vassilev et al., Science, 303: 844 (2004. Структурная основа данного взаимодействия установлена с помощью рентгеновской кристаллографии (Kussie et al., Science, 274: 948 (1996. Кристаллическая структура показывает, что взаимодействие между р 53 и MDM2 прежде всего опосредовано тремя гидрофобными остатками (Phe19,Trp23 и Leu26) p53 и небольшим глубоким гидрофобным углублением MDM2. Это гидрофобное углубление является идеальным сайтом для проектирования низкомолекулярных ингибиторов, которые могут нарушать взаимодействие р 53 и MDM2 (Chene, Nat. Rev. Cancer, 5: 102 (2003.-1 014445 Краткое изложение сущности изобретения В целом считается, что неспособность раковых клеток или их поддерживающих клеток претерпевать апоптоз в ответ на генетические повреждения или воздействия индукторов апоптоза (таких как противораковые агенты и облучение) является главным фактором в возникновении и прогрессировании рака. Индукцию апоптоза в раковых клетках или в их поддерживающих клетках (например, в неоваскулярных клетках сосудистой системы опухоли) считают универсальным механизмом действия практически всех эффективных лекарственных средств для терапии рака или лучевых терапий на рынке или в практике в настоящее время. Одной из причин неспособности клетки претерпевать апоптоз является снижение активности опухолевого супрессора р 53, которое во многих случаях является следствием ингибиторного действия MDM2 на р 53 в опухолевых клетках, содержащих функциональный р 53. Индукция активности р 53 приводит в результате к изменениям в биохимических путях апоптоза, а также регуляции клеточного цикла. Согласно настоящему изобретению предполагается, что воздействие на животных, страдающих раком, терапевтически эффективных количеств лекарственного средства (средств) (например, малых молекул), которое стимулирует функцию(и) р 53 и родственных р 53 белков (например, p63, р 73) посредством ингибирования взаимодействия между р 53 или родственными р 53 белками и MDM2 или родственнымиMDM2 белками (например, MDMX), будет непосредственно ингибировать рост раковых клеток или поддерживающих клеток и/или делать такие клетки, как популяция, более чувствительными к противораковым терапевтическим лекарственным средствам или лучевым терапиям, индуцирующим клеточную гибель. В частности, ингибиторы по изобретению могут продлевать период полураспада р 53, препятствуя взаимодействию р 53 с MDM2, что в норме стимулировало бы распад р 53. Согласно настоящему изобретению предполагается, что ингибиторы взаимодействия между р 53 или родственными р 53 белками иMDM2 или родственными MDM2 белками удовлетворят имеющуюся необходимость в лечении множества типов рака как при введении в качестве монотерапии для индукции ингибирования клеточного роста, апоптоза и/или остановки клеточного цикла в раковых клетках, так при введении во временном взаимодействии с дополнительным агентом(ами), таким как другие противораковые терапевтические лекарственные средства или лучевая терапия, индуцирующие клеточную гибель или прерывающие клеточный цикл (комбинированная терапия), делая чувствительными к осуществлению апоптотической программы долю раковых клеток или поддерживающих клеток, большую по сравнению с соответствующей долей клеток у животного, обработанного только противораковым терапевтическим лекарственным средством или лучевой терапией отдельно. В некоторых воплощениях изобретения комбинированная терапия животных терапевтически эффективным количеством соединения по настоящему изобретению и курсом противоракового агента или лучевой терапии производит более высокий ответ на опухоль и большую клиническую пользу у таких животных по сравнению с животными, которые подвергались лечению соединением или противораковыми лекарственными средствами/лучевой терапией отдельно. Иначе говоря, поскольку эти соединения будут снижать апоптотический порог всех клеток, доля клеток, которые будут успешно выполнять апоптотическую программу в ответ на индуцирующую апоптоз активность противораковых лекарственных средств/облучения, повышается. Альтернативно, соединения по настоящему изобретению будут применять, чтобы обеспечивать возможность введения более низкой и, следовательно, менее токсичной и лучше переносимой дозы противоракового агента и/или облучения для получения такого же ответа на опухоль/клинической пользы, как общепринятая доза противоракового агента и/или облучения отдельно. Поскольку дозы для всех одобренных противораковых лекарственных средств и лучевых терапий известны, в настоящем изобретении рассматриваются их различные комбинации с настоящими соединениями. Также, поскольку соединения по настоящему изобретению могут действовать, по меньшей мере частично, посредством стимуляции проапоптотических и/или ингибирующих клеточный цикл видов активности р 53 и родственных р 53 белков, время воздействия на раковые клетки и поддерживающие клетки терапевтически эффективных количеств этих соединений должно быть подобрано таким образом,чтобы совпадать с попытками клеток осуществить апоптотическую программу в ответ на противораковый агент или лучевую терапию. Таким образом, в некоторых воплощениях введение композиций по настоящему изобретению, связанное определенными временными взаимоотношениями, обеспечивает особенно эффективную терапевтическую практику. В других воплощениях изобретения ингибиторы взаимодействия между р 53 или родственными р 53 белками и MDM2 и родственными MDM2 белками могут защитить нормальные (например, не являющиеся гиперпролиферативными) клетки от токсических эффектов некоторых химиотерапевтических агентов и облучения, возможно, благодаря способности этих ингибиторов индуцировать остановку клеточного цикла. В частности, ингибиторы по изобретению могут вызывать остановку клеточного цикла в клетках, содержащих р 53 дикого типа, не оказывая при этом эффект на раковые клетки, содержащие мутированный или делетированный р 53. Этот дифференциальный защитный эффект может дать возможность более эффективного лечения рака благодаря возможности применения более высоких доз химиотерапевтических агентов или более длительного лечения ими или возможности лечения без повышения токсических побочных эффектов такого лечения.-2 014445 Настоящее изобретение относится к соединениям, которые являются полезными для ингибирования взаимодействия между р 53 или родственными р 53 белками и MDM2 и родственными MDM2 белками и повышения чувствительности клеток к индукторам апоптоза и/или остановки клеточного цикла. В одном конкретном воплощении изобретение относится к соединениям формулы X или их фармацевтически приемлемой соли,где R1 представляет собой:a) С 1-18 алкил, С 3-8 циклоалкил или С 5-10 гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из С 1-6 алкила, галогена, C1-6 галогеноалкила,С 3-8 циклоалкила, С 6-14 арила, С 6-14 арилокси, C5-10 гетероарила, С 5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-С 1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,С 3-8 гетероцикл-C1-6 ацила и С 3-8 гетероциклалкокси, или б) C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы,состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, С 6-14 арила, C6-14 арилокси,C5-10 гетероарила, С 5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,С 3-8 гетероцикла, С 3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R5 представляет собой С 1-18 алкил или C6-14 арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,С 3-8 циклоалкила, С 6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иR9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, CX, Br, X,C1-3 алкила или OR'; каждый R' и R" независимо представляет собой водород, C1-18 алкил, C3-8 циклоалкил или С 5-10 гетероцикл;R10 и R11 независимо представляют собой: а) водород,б) C1-18 алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, С 3-8 циклоалкила, С 6-14 арила, C6-14 арилокси, C5-10 гетероарила,C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-С 1-6 алкила,C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси,в) (CH2)n-R',г) (CH2)n-NR'R",д) (CH2)n-CONR'R",е) (CH2)n-OR'. ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либоR10 и R11 образуют C3-8 гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, С 6-14 арила,C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,С 3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси; и-3 014445 В другом воплощении изобретение относится к соединениям формулы XXIX или их фармацевтически приемлемой соли,где Z представляет собой О;R1 представляет собой С 6-14 арил, необязательно имеющий один или два заместителя, выбранных из группы, состоящей из C1-6 алкила, галогена, С 1-6 галогеноалкила, С 3-8 циклоалкила, C6-14 арила,C6-14 арилокси, С 5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, С 3-8 гетероцикл-C1-6 ацила и С 3-8 гетероциклалкокси;R7 представляет собой водород или C1-18 алкил;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I;n=2. В следующем воплощении изобретение относится к соединениям формулы XLVI или их фармацевтически приемлемой соли,где R1 представляет собой C6-14 арил;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I. В другом воплощении изобретение относится к соединениям формулы XLVII или его фармацевтически приемлемой соли,где R12 представляет собой Н;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I,C1-3 алкил или OR';n=1. Изобретение также относится к соединениям формулы LXV или их фармацевтически приемлемой соли,-4 014445 где R1 представляет собой: а) C1-18 алкил, C3-8 циклоалкил или C5-10 гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,C3-8 циклоалкила, C6-14 арила, С 6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-С 1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иC3-8 гетероциклалкокси, или б) C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы,состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, C6-14 арилокси,C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, C3-8 гетероцикл-С 1-6 ацила и С 3-8 гетероциклалкокси;R5 представляет собой C1-18 алкил или C6-14 арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иR9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I,C1-3 алкил или OR'; каждый R' и R" независимо представляет собой водород, C1-18 алкил, С 3-8 циклоалкил или С 5-10 гетероцикл;R10 и R11 независимо представляют собой: а) водород,б) C1-18 алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, С 3-8 циклоалкила, С 6-14 арила, C6-14 арилокси, С 5-10 гетероарила,C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, С 6-14 арилтио, амидо, амино, амино-C1-6 алкила,C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, С 3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси,в) (CH2)n-R',г) (CH2)n-NR'R",д) (CH2)n-CONR'R",е) (CH2)n-OR,' ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либоR10 и R11 образуют C3-8 гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила,С 6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, С 6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, C3-8 гетероцикл-С 1-6 ацила и C3-8 гетероциклалкокси; и-5 014445 В другом воплощении изобретение относится к соединениям, выбранным из группы, состоящей из или их фармацевтически приемлемой соли. Изобретение относится к соединениям, представленным вышеописанными формулами, которые являются ингибиторами взаимодействия между р 53 или родственными р 53 белками и MDM2 или родственными MDM2 белками. Изобретение относится к применению соединений по изобретению для индукции остановки клеточного цикла и/или апоптоза в клетках, содержащих функциональный белок р 53 или белки, родственные р 53. Изобретение также относится к применению соединений по изобретению для сенсибилизации клеток к дополнительному агенту(ам), такому как индукторы апоптоза и/или остановки клеточного цикла, и химической защиты нормальных клеток посредством индукции остановки клеточного цикла перед лечением химиотерапевтическими агентами. В одном воплощении изобретение относится к способу ингибирования клеточного роста или деления, индукции апоптоза или индукции остановки клеточного цикла у клетки, при котором клетку приводят в контакт с соединением по изобретению. В другом воплощении изобретение относится к способу придания клетке чувствительности к дополнительному агенту (агентам), при котором клетку приводят в контакт с соединением по изобретению. В одном воплощении изобретение относится к способам придания нормальной клетке устойчивости к химиотерапевтическим агентам или лечению, при которых клетку приводят в контакт с соединением по изобретению. В одном воплощении изобретение относится к способам защиты нормальных клеток у животного с раком от токсических побочных эффектов химиотерапевтических агентов или лечения, при которых указанному животному вводят соединение по изобретению. Соединения по изобретению полезны для лечения, облегчения или профилактики расстройств, таких как те, которые способны отвечать на индукцию апоптотической клеточной гибели, например расстройств, характеризующихся нарушением регуляции апоптоза, включая гиперпролиферативные заболевания, такие как рак. В некоторых воплощениях эти соединения могут применяться для лечения, облегчения или профилактики рака, который характеризуется устойчивостью к противораковой терапии (например, тех раковых клеток, которые являются химиорезистентными, радиорезистентными, гормонорезистентными и т.п.). В других воплощениях данное изобретение относится к способу лечения, облегчения или профилактики рака, характеризующегося экспрессией функционального р 53 или родственных р 53 белков у животного, при котором указанному животному вводят терапевтически эффективное количество соединения по изобретению. Настоящее изобретение относится к способу лечения или облегчения рака у животного, при котором указанному животному вводят терапевтически эффективное количество соединения по изобретению. В другом воплощении изобретение относится к способу ингибирования взаимодействия между р 53 или родственными р 53 белками и MDM2 или родственными MDM2 белками в клетке, при котором клет-6 014445 ку подвергают воздействию соединения по изобретению. В следующем воплощении изобретение относится к способу ингибирования роста гиперпролиферативной клетки, содержащей функциональный р 53 или родственные р 53 белки, при котором клетку подвергают воздействию соединения по изобретению. В других воплощениях изобретение относится к применению соединений по изобретению для защиты нормальных (например, не являющихся гиперпролиферативными) клеток от токсических побочных эффектов химиотерапевтических агентов и лечения путем индукции остановки клеточного цикла в этих клетках. В настоящем изобретении предложены фармацевтические композиции для лечения рака у животных, содержащие соединение по изобретению в терапевтически эффективном количестве и фармацевтически приемлемый носитель, для индукции апоптоза в клетках или для сенсибилизации клеток к индукторам апоптоза. Далее в изобретении предложены наборы, содержащие соединения по изобретению, и инструкции по введению соединения животному, имеющему рак. Эти наборы могут возможно содержать другие терапевтические агенты, например противораковые агенты или агенты, модулирующие апоптоз, в частности они могут содержать химиотерапевтические агенты. В изобретении также предложены способы получения соединений формул X, XXIX, LXV. Краткое описание графических материалов/фигур На фиг. 1 показано моделирование нового класса ингибиторов MDM2 на основе спиротрипростатина А. На фиг. 2 А и 2 Б показана предсказанная модель связывания соединений 1 а и 1d с MDM2. На фиг. 3 показана рентгеновская структура (1"R,2"S,2'R,3'R,3S,4'R)-6-хлор-4'-(3-хлор-фенил)-1'-(2 гидрокси-1,2-дифенилэтил)-2'-(3-метилбутил)-2-оксо-1,2-дигидроспиро[индол-3,3'-пирролидин]-5'карбоновой кислоты диметиламида. На фиг. 4 А показана кривая насыщения связывания PMDM6-F с белком MDM2. На фиг. 4 Б показаны кривые конкурентного связывания немеченого флуоресцентного зондаPMDM6 и нативного пептида р 53 с белком MDM2. На фиг. 5 показаны кривые конкурентного связывания и значения Ki ингибиторов MDM2, определенных с использованием анализа связывания на основе ФП (флуоресцентной поляризации). На фиг. 6 показано ингибирование роста клеток рака простаты LNCaP белком р 53 дикого типа, определенное с помощью анализа клеточного роста WST. На фиг. 7 показано ингибирование роста клеток рака простаты PC3 мутантным р 53, определенное с помощью анализа клеточного роста WST. На фиг. 8 показано ингибирование клеточного роста нормальных эпителиальных клеток простаты человека PrEC белком р 53 дикого типа, как определено с помощью анализа клеточного роста WST. На фиг. 9 показаны кривые конкурентного связывания нескольких ингибиторов взаимодействия р 53 и MDM2. На фиг. 10 показано прерывание взаимодействия р 53 и MDM2 с помощью Ke-43. На фиг. 11 показана ингибиторная активность Ke-43 в отношении роста клетках рака ободочной кишки с р 53 дикого типа или без него и в нормальных клетках. На фиг. 12 показан вестерн-блот-анализ экспрессии р 53 и продуктов его гена-мишени MDM2 и р 21 в раковых клетках в ответ на Ke-43. На фиг. 13 А и 13 Б показана клеточная гибель и апоптоз, индуцированный Ke-43 и Ke-61 в раковых клетках и в нормальных клетках. На фиг. 14 показано прогрессирование клеточного цикла клеточных линий рака ободочной кишки,экспрессирующих р 53 дикого типа или мутантный р 53, и нормальных клеток ободочной кишки после обработки Ke-43 и нутлином-3. На фиг. 15 показано, что Ke-63 защищает нормальные клетки при обработке Таксолом (TAXOL). Подробное описание изобретения Настоящее изобретение относится к соединениям, представленным формулами X, XXIX, XLVI,XLVII, LXV, которые функционируют как ингибиторы взаимодействия между р 53 или родственными р 53 белками и MDM2 или родственными MDM2 белками. Посредством ингибирования негативного воздействия MDM2 или родственных MDM2 белков на р 53 или родственные р 53 белки эти соединения сенсибилизируют клетки к индукторам апоптоза и/или остановки клеточного цикла и в некоторых случаях сами индуцируют апоптоз и/или остановку клеточного цикла. Таким образом, изобретение относится к способам сенсибилизации клеток к индукторам апоптоза и/или остановки клеточного цикла и к способам индукции апоптоза и/или остановки клеточного цикла в клетках, включающих приведение клеток в контакт с соединением по изобретению отдельно или в комбинации с дополнительным агентом(ами), например, индуктором апоптоза или веществом, прерывающим клеточный цикл. Изобретение далее относится к способу лечения, облегчения или профилактики рака у животного, при котором животному вводят соединение по изобретению и дополнительный агент(ы), например, индуктор апоптоза. Также изобретение относится к способу лечения, облегчения или профилактики рака у животного, характеризующегося пролиферацией клеток, экспрессирующих функциональный р 53 или родственные р 53 белки, при-7 014445 котором животному вводят соединение по изобретению. В других воплощениях изобретение относится к способам защиты нормальных (например, не гиперпролиферативных) клеток животного от токсических побочных эффектов химиотерапевтических агентов и лечения, при которых животному вводят соединение по изобретению. Изобретение также относится к фармацевтической композиции для лечения рака у животного, содержащей соединение по изобретению и фармацевтически приемлемый носитель. Термины "противораковый агент" и "противораковое лекарственное средство", как их используют здесь, относятся к любым терапевтическим агентам (например, химиотерапевтическим соединениям и/или соединениям для молекулярной терапии), антисенс-терапиям, лучевым терапиям или хирургическим вмешательствам, применяемым при лечении гиперпролиферативных заболеваний, таких как рак(например, у млекопитающих). Термин "фармацевтически приемлемая соль", как его используют здесь, относится к любой соли(например, полученной путем взаимодействия с кислотой или основанием) соединения по настоящему изобретению, которая является физиологически толерантной у животного-мишени (например, млекопитающего). Соли соединений по настоящему изобретению могут быть образованы из неорганических или органических кислот и оснований. Примеры кислот включают, но не ограничиваются указанным, соляную, бромисто-водородную, серную, азотную, перхлорную, фумаровую, малеиновую, фосфорную, гликолевую, молочную, салициловую, янтарную, толуол-пара-сульфоновую, винную, уксусную, лимонную,метансульфоновую, этансульфоновую, муравьиную, бензойную, малоновую, сульфоновую, нафталин-2 сульфоновую, бензолсульфоновую кислоту и т.п. Другие кислоты, такие как щавелевая, хотя сами не являются фармацевтически приемлемыми, могут использоваться при получении солей, полезных в качестве промежуточных соединений при получении соединений по изобретению и их фармацевтически приемлемых солей присоединения кислоты. Примеры оснований включают, но не ограничиваются указанным, гидроксиды щелочных металлов(например, натрия), гидроксиды щелочно-земельных металлов (например, магния), аммиак и соединения формулы NW4, где W представляет собой C1-4 алкил, и т.п. Примеры солей включают, но не ограничиваются указанным, ацетат, адипат, альгинат, аспартат,бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, флюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, хлорид, бромид, йодид, 2-гидроксиэтансульфонат, лактат, малеат, мезилат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, пальмоат, пектинат, персульфат, фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат, ундеканоат и т.п. Другие примеры солей включают анионы соединений по настоящему изобретению, компаундированные с подходящим катионом, таким как Na+, NH4+ и NW4+ (где W представляет собой группу С 1-4 алкил) и т.п. Для терапевтического применения соли соединений по настоящему изобретению рассматривают как фармацевтически приемлемые. Однако соли кислот и оснований, которые не являются фармацевтически приемлемыми, могут также найти применение, например, при получении или очистке фармацевтически приемлемого соединения. Термин "терапевтически эффективное количество", как его используют здесь, относится к количеству терапевтического агента, достаточному для того, чтобы привести в результате к облегчению одного или более симптома расстройства, либо провести профилактику прогрессирования этого расстройства,либо вызвать регрессию этого расстройства. Например, в отношении лечения рака терапевтически эффективное количество предпочтительно обозначает количество терапевтического агента, которое снижает скорость опухолевого роста, уменьшает массу опухоли, уменьшает число метастазов, увеличивает время до прогрессирования опухоли или увеличивает продолжительность жизни по меньшей мере на 5%,предпочтительно по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%,по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%,по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%,по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%,по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 100%. Термины "сенсибилизировать" и "сенсибилизирующий", как их используют здесь, относятся к тому, чтобы придать животному или клетке внутри животного посредством введения первого агента (например, соединения формулы X) большую чувствительность или большую реактивность в отношении биологических эффектов (например, стимуляции или задержки аспекта клеточной функции, включающей, но не ограниченной, деление клетки, клеточный рост, пролиферацию, инвазию, ангиогенез, некроз или апоптоз) второго агента. Сенсибилизирующий эффект первого агента на клетку-мишень можно измерить как разницу требуемых биологических эффектов (например, стимуляции или задержке аспекта клеточной функции, включающей, но не ограниченной, деление клетки, клеточный рост, пролиферацию,инвазию, ангиогенез, некроз или апоптоз), наблюдаемых при введении второго агента с введением и без введения первого агента. Ответ сенсибилизированной клетки может быть повышен по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на-8 014445 90%, по меньшей мере на 100%, по меньшей мере на 150%, по меньшей мере на 200%, по меньшей мере на 350%, по меньшей мере на 300%, по меньшей мере на 350%, по меньшей мере на 400%, по меньшей мере на 450% или по меньшей мере на 500% по сравнению с ответом в отсутствие первого агента. Термин "нарушение регуляции апоптоза", как его используют здесь, относится к любому изменению в способности (например, предрасположенности) клетки претерпевать клеточную гибель посредством апоптоза. Нарушение регуляции апоптоза связано с или вызвано рядом состояний, неограничивающие примеры которых включают аутоиммунные расстройства (например, системную красную волчанку,ревматоидный артрит, болезнь трансплантат против хозяина, тяжелую миастению или синдром Шегрена), хронические воспалительные состояния (например, псориаз, астму или болезнь Крона), гиперпролиферативные расстройства (например, опухоли, В-клеточные лимфомы или Т-клеточные лимфомы), вирусные инфекции (например, герпес, папиллому или ВИЧ) и другие состояния, такие как остеоартрит и атеросклероз. Следует отметить, что, когда нарушение регуляции вызвано вирусной инфекцией или связано с ней, эта вирусная инфекция может быть или может не быть обнаруживаемой в момент, когда возникает или наблюдается нарушение регуляции. То есть индуцированное вирусом нарушение регуляции может возникнуть даже после исчезновения симптомов вирусной инфекции. Термин "функциональный р 53", как его используют здесь, относится к р 53 дикого типа, экспрессируемому на нормальных, высоких или низких уровнях, и к мутантному р 53, который сохраняет по меньшей мере 5% активности р 53 дикого типа, например по меньшей мере 10, 20, 30, 40, 50% или более активности дикого типа. Термин "родственный р 53 белок", как его используют здесь, относится к белкам, которые имеют по меньшей мере 25% гомологии последовательности с р 53, обладают активностью опухолевого супрессора и ингибируются в результате взаимодействия с MDM2 или родственными MDM2 белками. Примеры родственных р 53 белков включают, но не ограничиваются указанным, p63 и р 73. Термин "родственный MDM2 белок", как его используют здесь, относится к белкам, которые имеют по меньшей мере 25% гомологии последовательности с MDM2, и взаимодействуют с р 53 или родственными р 53 белками и ингибируют их. Примеры родственных MDM2 белков включают, но не ограничиваются указанным, MDMX (murine double minute X) и HDM2 (human double minute-белок человеческих двойных микрохромосом 2). Термин "гиперпролиферативное заболевание", как его используют здесь, относится к любому состоянию, при котором локализованная популяция пролиферирующих клеток у животного не управляется обычными ограничениями нормального роста. Примеры гиперпролиферативных расстройств включают опухоли, новообразования, лимфомы и т.п. Новообразование называют доброкачественным, если оно не претерпевает инвазию или метастаз, и злокачественным, если оно претерпевает любое из них."Метастатическая" клетка означает, что эта клетка может проникать в соседние структуры организма и разрушать их. Гиперплазия представляет собой форму клеточной пролиферации, в которую вовлечено увеличение числа клеток в ткани или органе без значительного изменения в структуре или функции. Метаплазия представляет собой форму регулируемого клеточного роста, при которой один тип полностью дифференцированных клеток замещает другой тип дифференцированных клеток. Патологический рост активированных лимфоидных клеток часто приводит в результате к аутоиммунному расстройству или к хроническому воспалительному состоянию. Как его используют здесь, термин "аутоиммунное расстройство" относится к любому состоянию, при котором организм производит антитела или иммунные клетки, которые распознают собственные молекулы, клетки или ткани организма. Неограничивающие примеры аутоиммунных расстройств включают аутоиммунную гемолитическую анемию, аутоиммунный гепатит, болезнь Бергера или lgA-нефропатию, глютеновую энтеропатию, синдром хронической усталости, болезнь Крона, дерматомиозит, фибромиалгию, болезнь трансплантат против хозяина, болезнь Грейвса, тиреоидит Хасимото, идиопатическую тромбоцитопеническую пурпуру,плоский лишай, рассеянный склероз, тяжелую миастению, псориаз, ревматическую лихорадку, ревматоидный артрит, склеродерму, синдром Шегрена, системную красную волчанку, диабет типа 1, неспецифический язвенный колит, витилиго и т.п. Термин "неопластическое заболевание", как его используют здесь, относится к любому аномальному росту клеток, который является либо доброкачественным (нераковым), либо злокачественным (раковым). Термин "нормальная клетка", как его используют здесь, относится к клетке, которая не претерпевает аномальный рост или деление. Нормальные клетки являются нераковыми и не составляют часть какого-либо гиперпролиферативного заболевания или расстройства. Термин "противоопухолевый агент", как его используют здесь, относится к любому соединению,которое задерживает пролиферацию, рост или распространение новообразования-мишени (например,злокачественного). Термины "проводить профилактику", "профилактический" и "профилактика", как их используют здесь, относятся к снижению встречаемости патологических клеток (например, гиперпролиферативных или неопластических клеток) у животного. Профилактика может быть полной, например полное отсутствие патологических клеток у субъекта. Профилактика может быть также частичной, такой, чтобы встре-9 014445 чаемость патологических клеток у субъекта меньше, чем была бы встречаемость без настоящего изобретения. Термин "агенты, модулирующие апоптоз", как его используют здесь, относится к агентам, которые вовлечены в модулирование (например, ингибирование, уменьшение, увеличение, стимуляцию) апоптоза. Примеры агентов, модулирующих апоптоз, включают белки, которые содержат домены клеточной гибели, например, но не ограничиваясь указанным, Fas/CD95, TRAMP (tyrosine-rich acidic matrix proteinбогатый тирозином кислый белок матрикса), TNF-R1 (tumor necrosis factor receptor-рецептор фактора некроза опухоли), DR1 (down regulator of transcription 1-негативный регулятор транскрипции 1), DR2,DR3, DR4, DR5, DR6, FADD (Fas-associated death domain-домен смерти, ассоциированный с Fas) и RIP(receptor-interacting protein-белок, взаимодействующий с рецептором). Другие примеры агентов, модулирующих апоптоз, включают, но не ограничены указанным, TNF- (tumor necrosis factor -фактор некроза опухоли), лиганд Fas, антитела к Fas/CD95 и другим рецепторам семейства TNF, TRAIL (tumornecrosis factor-related apoptosis-inducing ligand-лиганд, индуцирующий апопотоз, связанный с фактором некроза опухоли, также известный как лиганд Аро 2 или Apo2L/TRAIL), антитела к рецепторам TRAIL 1 или 2 (TRAIL-R1 или TRAIL-R2), Bcl-2, р 53, ВАХ, BAD, Akt, CAD, PI3 (инозитол-3-фосфат) киназу, Р 1 и белки каспазы. Модулирующие агенты в широком смысле включают агонисты и антагонисты рецепторов семейства TNF и лиганды семейства TNF. Агенты, модулирующие апоптоз, могут быть растворимыми или связанными с мембраной (например, лиганд или рецептор). Предпочтительные агенты, модулирующие апоптоз, являются индукторами апоптоза, такими как TNF или лиганд, родственный TNF, в частности лиганд TRAMP, лиганд Fas/CD95, лиганд TNF-R1 или TRAIL. Ингибиторы взаимодействия между р 53 и MDM2 по настоящему изобретению представляют собой соединения формулы X или их фармацевтически приемлемые соли,где R1 представляет собой: а) C1-18 алкил, C3-8 циклоалкил или С 5-10 гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,С 3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иC6-14 арил-C1-6 ацилокси,C3-8 гетероциклалкокси, или б) C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы,состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, С 3-8 циклоалкила, С 6-14 арила, C6-14 арилокси,C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, С 6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,С 3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R5 представляет собой C1-18 алкил или C6-14 арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и С 3-8 гетероциклалкокси;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I,C1-3 алкил или OR'; каждый R' и R" независимо представляет собой водород, C1-18 алкил, C3-8 циклоалкил илиR10 и R11 независимо представляют собой: а) водород,б) C1-18 алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, C3-8 циклоалкила, С 6-14 арила, C6-14 арилокси, C5-10 гетероарила,C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила,C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси,в) (CH2)n-R',- 10014445 г) (CH2)n-NR'R",д) (CH2)n-CONR'R",е) (CH2)n-OR',ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либоR10 и R11 образуют C3-8 гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила,C6-14 арилокси, C5-10 гетероарила, С 5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,С 3-8 гетероцикла, С 3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси, иn, m и р, каждое независимо, равны 1-4. В следующем воплощении соединения формулы X имеют одну из формул XI-XXVI где R1, R5, R7, R9, R10 и R11 являются такими, как определено выше. В другом воплощении изобретение относится к соединениям формулы X, имеющим одну из формул XI и XXVI или их фармацевтически приемлемым солям,где R1, R5, R7, R9, R10 и R11 являются такими, как определено выше.- 11014445 В другом воплощении изобретение относится к соединению формулы XXIX или его фармацевтически приемлемой соли,где Z представляет собой О;R1 представляет собой C6-14 арил, необязательно имеющий один или два заместителя, выбранных из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, С 3-8 циклоалкила, C6-14 арила,С 6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо,амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-С 1-6 ацилокси, дифенилфосфинилокси,С 3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R7 представляет собой водород или C1-18 алкил;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I;n=2. В частности, соединения формулы XXIX имеют одну из формул XXX-XLV- 12014445 В другом воплощении соединения формулы XXIX имеют одну из формул XXX или XXXVIII В следующем воплощении настоящее изобретение относится к соединению формулы XLVI или его фармацевтически приемлемой соли,где R1 представляет собой C6-14 арил;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I. Настоящее изобретение также относится к соединению формулы XLVII или его фармацевтически приемлемой соли,где R12 представляет собой Н;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I,C1-3 алкил или OR';n=1. Настоящее изобретение также относится к соединениям формулы LXV или их фармацевтически приемлемым солям,где R1 представляет собой: а) C1-18 алкил, C3-8 циклоалкил или С 5-10 гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,C3-8 циклоалкила, С 6-14 арила, C6-14 арилокси, С 5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, С 6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,С 3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и С 3-8 гетероциклалкокси, или б) C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы,состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, C6-14 арилокси,C5-10 гетероарила, С 5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R5 представляет собой C1-18 алкил или С 6-14 арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,С 3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,- 13014445R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Вг, I,C1-3 алкил или OR'; каждый R' и R" независимо представляет собой водород, C1-18 алкил, С 3-8 циклоалкил илиR10 и R11 независимо представляют собой: а) водород,б) C1-18 алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, С 5-10 гетероарила,C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила,C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси,в) (CH2)n-R',г) (CH2)n-NR'R",д) (CH2)n-CONR'R",е) (CH2)n-OR',ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или з) (CH2)p-(CH2CH2O)n-(CH2)m-OR' либоR10 и R11 образуют С 3-8 гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, С 3-8 циклоалкила, C6-14 арила,С 6-14 арилокси, C5-10 арила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, С 6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси; иn, m и p, каждое независимо, равны 1-4. В другом воплощении соединения формулы LXV имеют одну из формул LXVI и LXVII где R1, R4, R5, R9, R10 и R11 являются такими, как определено выше. В другом воплощении изобретение относится к соединению, выбранному из группы, состоящей из или его фармацевтически приемлемой соли.- 14014445 Полезные алкильные группы включают прямоцепочечные или разветвленные C1-18 алкильные группы, в частности группы метил, этил, пропил, изопропил, трет-бутил, втор-бутил, 3-пентил, адамантил,норборнил и 3-гексил. Полезные алкенильные группы включают прямоцепочечные или разветвленные С 2-18 алкенильные группы, в частности группы этенил, пропенил, изопропенил, бутенил, изобутенил и гексенил. Полезными алкинильными группами являются C2-18 алкинильные группы, в частности группы этинил, пропинил, бутинил и 2-бутинил. Полезными циклоалкильными группами являются группы С 3-8 циклоалкил. Типичные циклоалкильные группы включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Полезные арильные группы включают C6-14 арил, в частности фенил, нафтил, фенантренил, антраценил, инденил, азуленил, дифенил, дифениленил и флуоренил. Полезные гетероарильные группы включают тиенил, бензо[b]тиенил, нафто[2,3-b]тиенил, тиантренил, фурил, пиранил, изобензофуранил, хроменил, ксантенил, феноксантенил, 2 Н-пирролил, пирролил,имидазолил, пиразолил, пиридил, пиразинил, пиримидинил, пиридазинил, индолизинил, изоиндолил,3H-индолил, индолил, индазолил, пуринил, 4 Н-хинолизинил, изохинолил, хинолил, фталазинил, нафтиридинил, хинозалинил, циннолинил, птеридинил, карбазолил, -карболинил, фенантридинил, акридинил,перимидинил, фенантролинил, феназинил, изотиазолил, фенотиазинил, изоксазолил, фуразинил,феноксазинил, 1,4-дигидрохиноксалин-2,3-дион, 7-аминоизокумарин, пиридо[1,2-а]пиримидин-4-он,1,2-бензоизоксазол-3-ил, бензимидазолил, 2-оксиндолил и 2-оксобензимидазолил, где гетероарильная группа содержит атом азота в кольце, такой атом азота может находиться в форме N-оксида, например пиридил-N-оксид, пиразинил-N-оксид, пиримидинил-N-оксид и т.п. Полезные гетероциклические группы включают группы тетрагидрофуранил, пиранил, пиперидинил, пиперизинил, пирролидинил, имидазолидинил, имидазолинил, индолинил, изоиндолинил, хинуклидинил, морфолинил, изохроманил, хроманил, пиразолидинил, пиразолинил, тетроноил, тетрамоил или тетрагидроизохинолинил, а также гетероциклические группы, конденсированные с гетероарильным кольцом, например возможно замещенный 5,6-дигидро-8 Н-[1,2,4]триазоло[4,3-А]пиразинил. Возможные заместители включают один или более из алкила; галогено; галогеноалкила; циклоалкила; арила, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил; арилокси, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил,аминосульфонил, арил или гетероарил; аралкила; гетероарила, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил,арил или гетероарил; гетероарилокси, возможно замещенного одной или более группой: низший алкил,низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил; алкокси; алкилтио; арилтио; амидо; амино; аминоалкила, алкиламино, ацилокси; арилацилокси, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил; дифенилфосфинилокси, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил; гетероцикло, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил, гетероарил,замещенный аминокислотой сульфонил или замещенный производным аминокислоты сульфонил; гетероциклоацила, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил; гетероциклоалкокси, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено,галогеноалкил, аминосульфонил, арил или гетероарил; частично ненасыщенного гетероциклоалкила,возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил или частично ненасыщенного гетероциклоалкилокси, возможно замещенного одной или более группой: низший алкил, низший алкокси, метилендиокси, галогено, галогеноалкил, аминосульфонил, арил или гетероарил. Некоторые из соединений по настоящему изобретению могут существовать в виде стереоизомеров,включая оптические изомеры. В изобретение включены все стереоизомеры как в виде чистых препаратов индивидуального стереоизомера и обогащенных препаратов каждого, так и рацемических смесей таких стереоизомеров, а также индивидуальные энантиомеры, которые можно разделить в соответствии со способами, которые хорошо известны специалистам в данной области техники. Соединения и способы по настоящему изобретению будут лучше понятны в связи с приведенными ниже схемами синтеза, которые иллюстрируют способы, которыми можно получить соединения по изобретению. Исходные вещества могут быть получены из коммерческих источников либо получены с помощью диетально разработанных и описанных в литерартуре способов, известных обычным специалистам в данной области техники. Обычным специалистам в данной области техники будет очевидно, что соединения, определенные выше, можно синтезировать путем замены подходящих реагентов и агентов в способах синтеза, показанных ниже.- 15014445 Соединения, имеющие общую структуру формулы X, синтезируют с использованием асимметрического 1,3-биполярного циклоприсоединения в качестве ключевой стадии (схема 1). Схема 1a) CH2Cl2-CH3CN, KF-Al2O3, ультракороткие волны или метанол, пиперидин, кипячение с обратным холодильником;d) Pb(OAc)4, CH2Cl2-Меон (1:1), 0 С или аммония церия (IV) нитрат (CAN), CH3CN, K2CO3, к.т. Соединения, имеющие формулу XXIX, получают с помощью методики, показанной на схеме 2. Схема 2g) R10ONa (для Z=О) либо R10NH2 (для Z=NH) или другая стандартная методика;(для R7=Me) или другая стандартная методика. Соединения, имеющие формулу XLVI, могут быть получены путем опубликованной реакции 1,3-биполярного циклоприсоединения, как показано на схеме 3 (Fejes et al., Tetrahedron, 57: 1129 (2000. Соединения, имеющие формулу XLVII, могут быть получены путем другой опубликованной реакции 1,3-биполярного циклоприсоединения, как показано на схеме 4 (Fejes et al., Tetrahedron, 57: 1129 Соединения, имеющие формулу LXV, получают способом, подобным получению соединений формулы X (схема 5). Схема 5a) CH2Cl2-CH3CN, KF-Al2O3, ультракороткие волны или метанол, пиперидин, кипячение с обратным холодильником;d) Pb(OAc)4, CH2Cl2-Меон (1:1), 0 С или алюминия церия(IV) нитрат (CAN), CH3CN, K2CO3, к.т. Один аспект изобретения относится к способам получения ингибиторных соединений MDM2. В одном воплощении изобретение относится к способу получения соединения, имеющего формулу X, при котором: а) подвергают соединение формулы 1 конденсации с соединением формулы 2, например, в растворителе или в смеси растворителей (например, CH2Cl2 и CH3CN) под действием ультракоротких волн в присутствии катализатора (например, KF-Al2O3) или в присутствии основания в подходящем растворителе с образованием соединения формулы 3 б) соединение формулы 3 подвергают конденсации с соединением формулы 4 и с соединением формулы 5, например, в неполярном растворителе (например, в толуоле) в присутствии дегидратирующего агента (например, 4 молекулярного сита) при повышенной температуре (например, около 70 С) с образованием соединения формулы 6 в) обрабатывают соединение формулы 6 окисляющим агентом (например, Pb(ОАс)4, нитратом аммония церия) в растворителе или в смеси растворителей (например, CH2Cl2 и Меон, CH3CN) при подходящей температуре (например, приблизительно 0 С или при комнатной температуре) с образованием соединения формулы X где R1 представляет собой: а) C1-18 алкил, C3-8 циклоалкил или С 5-10 гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, С 1-6 галогеноалкила,C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 цилокси,С 6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иC3-8 гетероциклалкокси, или б) C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы,состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, C6-14 арилокси,С 5-10 гетероарила, С 5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, С 6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, С 3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R5 представляет собой C1-18 алкил или C6-14 арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, С 6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,С 6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,С 3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иR9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I,C1-3 алкил или OR'; каждый R' и R" независимо представляет собой водород, C1-18 алкил, C3-8 циклоалкил или С 5-10 гетероцикл;R10 и R11 независимо представляют собой: а) водород,б) C1-18 алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, С 5-10 гетероарила,C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила,C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси,в) (CH2)n-R',г) (CH2)n-NR'R",д) (CH2)n-CONR'R",е) (CH2)n-OR',ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или з) (СН 2)р-(CH2CH2O)n-(CH2)m-OR' либоR10 и R11 образуют C3-8 гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, С 6-14 арила,C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,С 3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси; иn, m и р, каждое независимо, равны 1-4. В другом воплощении изобретение относится к способу получения соединения, имеющего формулуLXV, при котором: а) соединение формулы 16 подвергают конденсации с соединением формулы 2, например, в растворителе или в смеси растворителей (например, CH2Cl2 и CH3CN) в микроволновой печи в присутствии катализатора (например, KF-Al2O3) или в присутствии основания в подходящем растворителе с образованием соединения формулы 17 б) соединение формулы 17 подвергают конденсации с соединением формулы 4 и с соединением формулы 5, например, в неполярном растворителе (например, в толуоле) в присутствии дегидратирующего агента (например, 4 молекулярного сита) при повышенной температуре (например, приблизительно 70 С) с образованием соединения формулы 18 в) обрабатывают соединение формулы 18 окисляющим агентом (например, Pb(ОАс)4, нитратом аммония-церия) в растворителе или в смеси растворителей (например, CH2Cl2 и Меон, CH3CN) при подходящей температуре (например, около 0 С или при комнатной температуре) с образованием соединения формулы LXV где R1 представляет собой: а) C1-18 алкил, C3-8 циклоалкил или С 5-10 гетероарил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,C3-8 циклоалкила, C6-14 арила, C6-14 арилокси, С 5-10 гетероарила, С 5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,С 6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила иC3-8 гетероциклалкокси, или б) C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы,состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, C6-14 арилокси,C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино,амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R5 представляет собой C1-18 алкил или C6-14 арил, каждый из которых необязательно имеет один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила,С 3-8 циклоалкила, C6-14 арила, C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси,C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси,C6-14 арил-C1-6 ацилокси,дифенилфосфинилокси,C3-8 гетероцикла,С 3-8 гетероцикл-C1-6 ацила иR9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br, I,C1-3 алкил или OR'; каждый R' и R" независимо представляет собой водород, C1-18 алкил, C3-8 циклоалкил илиR10 и R11 независимо представляют собой: а) водород,б) C1-18 алкил, необязательно имеющий один заместитель, выбранный из группы, состоящей из галогена, C1-6 галогеноалкила, C3-8 циклоалкила, C6-14 арила, С 6-14 арилокси, C5-10 гетероарила,C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, С 6-14 арилтио, амидо, амино, амино-C1-6 алкила,C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, C3-8 гетероцикла,C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси,в) (CH2)n-R',г) (CH2)n-NR'R",д) (CH2)n-CONR'R",е) (CH2)n-OR',ж) (CH2)p-(CH2CH2O)n-(CH2)m-OH или з) (CH2)p-(CH2CH2O)n-(СН 2)m-OR' либоR10 и R11 образуют С 3-8 гетероцикличное кольцо, необязательно имеющее один заместитель, выбранный из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, С 3-8 циклоалкила, С 6-14 арила,C6-14 арилокси, C5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио, амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, С 6-14 арил-C1-6 ацилокси, дифенилфосфинилокси,C3-8 гетероцикла, C3-8 гетероцикл-С 1-6 ацила и C3-8 гетероциклалкокси; иn, m и p, каждое независимо, равны 1-4. В другом воплощении изобретение относится к способу получения соединения, имеющего формулуXXIX, при котором: а) соединение формулы 3 подвергают конденсации с соединением формулы 4 и с соединением формулы 5, например, в неполярном растворителе (например, в толуоле) в присутствии дегидратирующего агента (например, 4 молекулярного сита) или путем азеотропной перегонки при повышенной температуре (например, около 70 С) с образованием соединения формулы 7 б) нагревают соединение формулы 7 в присутствии кислоты (например, HCl), а затем добавляют восстанавливающий агент (например, NaBH4) с образованием соединения формулы 8 в) соединение формулы 8 подвергают конденсации с блокирующим агентом (например, триалкилсилилгалогенидом, таким как TBDMSCl) в полярном растворителе (например, в диметилформамиде), а затем обрабатывают триметилацетилхлоридом или другими защитными агентами в растворителе или в смеси растворителей (например, диизопропилэтиламина, CH2Cl2) и затем кислотой (например, HCl) с образованием соединения формулы 10- 20014445 г) обрабатывают соединение формулы 10 галогенирующим агентом (например, CBr4 и Ph3P) в растворителе (например, CH2Cl2) с образованием галогеносоединения формулы 11 д) замещают галогеногруппу соединения формулы 11 R10ONa или R10NH2 с образованием соединения формулы 12 е) обрабатывают соединение формулы 12 окисляющим агентом (например, Pb(ОАс)4, нитратом аммония-церия) в растворителе или в смеси растворителей (например, CH2Cl2 и Меон, CH3CN) при подходящей температуре (например, около 0 С или при комнатной температуре) с образованием соединения формулы 13 ж) алкилируют соединение формулы 13 алкилирующим агентом (например, НСНО, NaBH3CN иCH3CN) с образованием соединения формулы XXIXR10 представляет собой водород или (CH2)n-R';R1 представляет собой C6-14 арил, необязательно имеющий один или два заместителя, независимо выбранных из группы, состоящей из C1-6 алкила, галогена, C1-6 галогеноалкила, С 3-8 циклоалкила,C6-14 арила, C6-14 арилокси, С 5-10 гетероарила, C5-10 гетероарилокси, C1-6 алкокси, C1-6 алкилтио, C6-14 арилтио,амидо, амино, амино-C1-6 алкила, C1-6 алкиламино, C1-6 ацилокси, C6-14 арил-C1-6 ацилокси, дифенилфосфинилокси, C3-8 гетероцикла, C3-8 гетероцикл-C1-6 ацила и C3-8 гетероциклалкокси;R7 представляет собой представляет собой водород или C1-18 алкил;R9 представляет собой от одной до четырех групп, независимо выбранных из Н, F, Cl, Br или I;n=2. Важный аспект настоящего изобретения состоит в том, что соединения по изобретению индуцируют остановку клеточного цикла и/или апоптоз, а также потенцируют индукцию остановки клеточного цикла и/или апоптоза либо сами по себе, либо в ответ на дополнительную индукцию сигналов апоптоза. Таким образом, предполагается, что эти соединения сенсибилизируют клетки в отношении индукции остановки клеточного цикла и/или апоптоза, включая и клетки, которые являются устойчивыми к таким индуцирующим стимулам. Ингибиторы взаимодействия между р 53 или родственными р 53 белками иMDM2 или родственными MDM2 белками согласно настоящему изобретению можно применять для ин- 21014445 дукции апоптоза при любом расстройстве, которое можно лечить, облегчать или против которого можно провести профилактику посредством индукции апоптоза. В одном воплощении эти ингибиторы можно использовать для индукции апоптоза в клетках, содержащих функциональный р 53 или родственные р 53 белки. В другом воплощении изобретение относится к модулированию состояния, связанного с апоптозом,которое связано с одним или более агентом, модулирующим апоптоз. Примеры агентов, модулирующих апоптоз, включают, но не ограничены указанным, Fas/CD95, TRAMP, TNF-R1, DR1, DR2, DR3, DR4,DR5, DR6, FADD, RIP, TNF-, лиганд Fas, TRAIL, антитела к TRAIL-R1 или TRAIL-R2, Bcl-2, p53, BAX,BAD, Alct, CAD, PI3 киназу, РР 1 и белки каспазы. Также включены другие агенты, вовлеченные в фазы апоптоза: фазу инициации, эффекторную фазу и фазу деградации. Примеры агентов, модулирующих апоптоз, включают агенты, активность, присутствие или изменение концентрации которых может модулировать апоптоз у субъекта. Предпочтительными агентами, модулирующими апоптоз, являются индукторы апоптоза, такие как TNF или родственный TNF лиганд, в частности лиганд TRAMP, лигандFas/CD95, лиганд TNF-R1 или TRAIL. В некоторых воплощениях композиции и способы по настоящему изобретению применяют для лечения больных клеток, тканей, органов или патологических состояний и/или болезненных состояний у животного (например, млекопитающего, включая, но не ограничиваясь, людей и подвергающихся лечению животных). В этом отношении с применением настоящих способов и композиций поддаются лечению или профилактике различные заболевания и патологии. Неограничивающий перечень примеров этих заболеваний и состояний включает, но не ограничвается указанным, рак молочной железы, рак простаты, лимфому, рак кожи, рак поджелудочной железы, рак ободочной кишки, меланому, злокачественную меланому, рак яичника, рак головного мозга, первичный рак головного мозга, рак головы-шеи,глиому, глиобластому, рак печени, рак мочевого пузыря, немелкоклеточный рак легкого, карциному головы или шеи, карциному молочной железы, карциному яичника, карциному легкого, мелкоклеточный рак легкого, опухоль Вильмса, карциному шейки матки, карциному яичка, карциному мочевого пузыря,карциному поджелудочной железы, карциному желудка, карциному ободочной кишки, карциному простаты, мочеполовую карциному, карциному щитовидной железы, карциному пищевода, миелому, множественную миелому, адренокарциному, почечно-клеточный рак, карциному эндометрия, карциному коры надпочечников, злокачественную инсулиному поджелудочной железы, злокачественную аргентофинному, хориокарциному, грибовидный микоз, злокачественную гиперкальцемию, гиперплазию шейки матки, лейкоз, острый лимфолейкоз, хронический лимфолейкоз, острый миелоидный лейкоз, хронический миелоидный лейкоз, хронический гранулоцитарный лейкоз, острый гранулоцитарный лейкоз, гистиоцитарный ретикулоэндотелиоз, нейробластому, рабдомиосаркому, саркому Капоши, истинную полицитемию, истинный тромбоцитоз, болезнь Ходжкина, неходжкинскую лимфому, саркому мягких тканей,остеогенную саркому, первичную макроглобулинемию и ретинобластому и тому подобное, опосредованные Т- и В-клетками аутоиммунные заболевания; воспалительные заболевания; инфекции; гиперпролиферативные заболевания; СПИД; дегенеративные состояния, сосудистые заболевания и т.п. В некоторых воплощениях раковые клетки, подлежащие лечению, являются метастатическими. В других воплощениях раковые клетки, подлежащие лечению, являются устойчивыми к противораковым агентам. В некоторых воплощениях инфекции, которые можно лечить композициями и способами по настоящему изобретению, включают, но не ограничиваются указанным, инфекции, вызванные вирусами,бактериями, грибами, микоплазмой, прионами и т.п. В некоторых воплощениях настоящего изобретения предложены способы введения эффективного количества соединения по изобретению и по меньшей мере одного дополнительного терапевтического агента (включая, но не ограничиваясь, химиотерапевтические противоопухолевые агенты, агенты, модулирующие апоптоз, противомикробные агенты, антивирусные агенты, противогрибковые агенты и противовоспалительные агенты) и/или применения терапевтической методики (например, хирургического вмешательства и/или лучевых терапий). В способах по настоящему изобретению предполагается применение ряда противораковых агентов. В действительности, настоящее изобретение предполагает, но не ограничивается указанным, введение различных противораковых агентов, таких как агенты, которые индуцируют апоптоз; полинуклеотиды(например, антисмысловые, рибозимы, малые интерферирующие PHK); полипептиды (например, ферменты и антитела); биологические миметики (например, госсипол или ВН 3-миметики); агенты, которые связываются (например, олигомеризуются или образуют комплекс) с белком семейства Bcl-2, таким какBax; алкалоиды; алкилирующие агенты; противоопухолевые антибиотики; антиметаболиты; гормоны; соединения платины; моноклональные или поликлональные антитела (например, антитела, конъюгированные с противораковыми лекарственными средствами, токсинами, дефензинами), токсины; радионуклиды; модификаторы биологического ответа (например, интерфероны (например, IFN-) и интерлейкины (например, IL-2; агенты адаптивной иммунотерапии; гематопоэтические ростовые факторы; агенты,которые индуцируют дифференциацию опухолевых клеток (например, алло-трансретиноевая кислота);B); соединения, имеющие анти-CDK активность (CDK- cyclin-dependent kynase-циклинзависимая киназа), ингибиторы HDAC (hystone deacetylase-деацетилаза тистонов) и т.п. Различные другие примеры химиотерапевтических соединений и противораковых терапий, пригодных для совместного введения или применения с раскрытыми соединениями, известны специалистам в данной области техники. В предпочтительных воплощениях противораковые агенты включают агенты, которые индуцируют или стимулируют апоптоз. Агенты, которые индуцируют апоптоз, включают, но не ограничиваются указанным, облучение (например, рентгеновские лучи, гамма-лучи, УФ); факторы, родственные фактору некроза опухоли (TNF) (например, рецепторные белки семейства TNF, лиганды семейства TNF, TRAIL,антитела к TRAIL-R1 или TRAIL-R2); ингибиторы киназ (например, ингибитор киназы рецептора эпителиального фактора роста (EGFR-epithelial growth factor receptor), ингибитор киназы рецептора сосудистого фактора роста (VGFR-vascular growth factor receptor), ингибитор киназы рецептора фактора роста фибробластов (FGFR-fibroblast growth factor receptor, ингибитор киназы рецептора тромбоцитарного ростового фактора (PDGFR-platelet derived growth factor receptor) и ингибиторы киназы Bcr-Abl (такие как ГЛИВЕК); антисмысловые молекулы; антитела (например, ГЕРЦЕПТИН, РИТУКСАН, ЗЕВАЛИН и АВАСТИН); антиэстрогены (например, ралоксифен и тамоксифен); антиандрогены (например, флутамид, бикалутамид, финастерид, аминоглутетамид, кетоконазол и кортикостероиды); ингибиторы циклооксигеназы 2 (СОХ-2) (например, целекоксиб, мелоксикам, NS-398 и нестероидные противовоспалительные лекарственные средства (НСПВЛ; противовоспалительные лекарственные средства (например,бутазолидин, ДЕКАДРон, ДЕЛЬТАЗон, дексаметазон, дексаметазон интенсол, ДЕКСон, ГЕКСАДРОЛ,гидроксихлорохин, МЕТИКОРТЕН, ОРАДЕКСон, ОРАЗон, оксифенбутазон, ПЕдиАПРЕД, фенилбутазон, ПЛАКВЕНил, преднизолон, преднизон, ПРЕЛон и ТАНДЕРил); и лекарственные средства для химиотерапии рака (например, иринотекан (КАМПТОСАР), СРТ-11, флударабин (ФЛУДАРА), дакарбазин(DTIC), дексаметазон, митоксантрон, МилОТАРГ, VP-16, цисплатин, карбоплатин, оксалиплатин, 5-FU,доксорубицин,гемцитабин,бортезомиб,гефитиниб,бевацизумаб,ТАКСОТЕР или ТАКСОЛ), молекулы клеточной передачи сигнала; церамиды и цитокины; стауроспорин и т.п. В дальнейших воплощениях композиций и способов по настоящему изобретению предусмотрено соединение по изобретению и по меньшей мере один антигиперпролиферативный или противоопухолевый агент, выбранный из алкилирующих агентов, антиметаболитов и натуральных продуктов (например,трав и других соединений растительного и/или животного происхождения). Алкилирующие агенты, пригодные для применения в настоящих композициях и способах, включают, но не ограничены: 1) азотистые иприты (например, мехлорэтамин, циклофосфамид, ифосфамид, мелфалан(L-сарколизин) и хлорамбуцил); 2) этиленимины и метилмеламины (например, гексаметилмеламин и тиотепа); 3) алкилсульфонаты (например, бусульфан); 4) нитрозомочевины (например, кармустин (BCNU); ломустин (CCNU); семустин (метил-CCNU) и стрептозоцин (стрептозотоцин и 5) триазены (например, дакарбазин (DTIC; диметилтриазеноимидазолкарбоксамид). В некоторых воплощениях антиметаболиты, пригодные для применения в настоящих композициях и способах, включают, но не ограничены указанным: 1) аналоги фолиевой кислоты (например, метотрексат (аметоптерин; 2) аналоги пиримидинов (например, фторурацил (5-фторурацил; 5-FU), флоксуридин (флуородоксиуридин; FudR) и цитарабин (цитозин арабинозид и 3) аналоги пуринов (например, меркаптопурин (6-меркаптопурин; 6-МР), тиогуанин (6-тиогуанин;TG) и пентостатин (2'-дезоксикоформицин. Еще в следующих воплощениях химиотерапевтические агенты, пригодные для применения в настоящих композициях и способах, включают, но не ограничены: 1) алкалоиды барвинка розового (например, винбластин (VLB), винкристин); 2) эпиподофиллотоксины (например, этопозид и тенипозид); 3) антибиотики (например, дактиномицин (актиномицин D), даунорубицин (дауномицин; рубидомицин), доксорубицин, блеомицин, пликамицин (митрамицин) и митомицин (митомицин С; 4) ферменты (например, L-аспарагиназа); 5) модификаторы биологического ответа (например, интерферон-альфа); 6) координационные комплексы платины (например, цисплатин (цис-DDP) и карбоплатин); 7) антрацендионы (например, митоксантрон); 8) замещенные мочевины (например, гидроксимочевина); 9) производные метилгидразина (например, прокарбазин (N-метилгидразин; MIH; 10) адренокортикосупрессанты (например, митотан (o,p'-DDD) и аминоглутетимид); 11) адренокортикостероиды (например, преднизон);- 23014445 12) прогестины (например, гидроксипрогестерона капроат, медроксипрогестерона ацетат и мегестрола ацетат); 13) эстрогены (например, диэтилстилбестрол и этинилэстрадиол); 14) антиэстрогены (например, тамоксифен); 15) андрогены (например, тестостерона пропионат и флуоксиместерон); 16) антиандрогены (например, флутамид) и 17) аналоги рилизинг-фактора гонадотропина (например, лепролид). Любой онколитический агент, который, как правило, применяют при терапии рака, может применяться в композициях и способах по настоящему изобретению. Например, Управление по контролю за продуктами и лекарствами США (US FDA-food and drug administration) ведет формуляр онколитических агентов, одобренных к применению в США. Международные агентства-партнеры US FDA ведут подобные формуляры. В табл. 1 приведен перечень примеров противоопухолевых агентов, одобренных к применению в США. Специалистам в данной области техники будет понятно, что одобренные указания, информацию по дозировке, данные токсичности и т.п. для примеров агентов описывает "этикетка продукта", требующаяся на всех одобренных в США химиотерапевтических агентах. Таблица 1
МПК / Метки
МПК: A61K 31/407, C07D 487/12, A61P 35/00, C07D 491/107, C07D 487/10
Метки: низкомолекулярные, применения, ингибиторы
Код ссылки
<a href="https://eas.patents.su/30-14445-nizkomolekulyarnye-ingibitory-mdm2-i-ih-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Низкомолекулярные ингибиторы mdm2 и их применения</a>
Предыдущий патент: Композиция, содержащая статины и омега-3 жирные кислоты
Следующий патент: Твёрдый фармацевтический дозированный состав
Случайный патент: Ингибиторы вируса гепатита с