Тирозиновые производные в качестве модуляторов pparγ
Номер патента: 13227
Опубликовано: 30.04.2010
Авторы: Серра Комас Кармен, Бальса Лопес Долорс, Масип Масип Исабель, Фернандес Серрат Анна, Идальго Родригес Хосе, Лагунас Арналь Кармен, Сальседо Рока Каролина, Фернандес Гарсия Андрес, Катена Руис Хуан Лоренсо
Формула / Реферат
1. Соединение формулы I
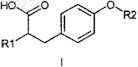
соответствующие стереоизомеры и смеси, соответствующие полиморфы и смеси и фармацевтически приемлемые сольваты и аддитивные соли всех указанных соединений,
где R1 означает радикал 2-бензоилфениламино;
R2 означает -(СН2)s-N(COR3)-A-J-T или -(СН2)s-N(R4)-В;
R3 означает -(C1-С10)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br и -О(C1-C4)алкил; -(С2-С6)алкенил; -(C1-С3)алкилен-Y; -(С2-С3)алкенилен-Y; -(С2-С3)алкинилен-Y или -Y;
R4 означает -(С4-С10)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br и -О(С1-С4)алкил; -(С1-С4)алкилен-Y или -Y;
s равно 2 или 3;
А означает -(С1-С4)алкилен-; -(С1-С4)алкилен-Z-, где алкиленовая часть соединена с атомом N и Z соединен с J, либо -Z-;
В означает фенил или бензил, необязательно замещенный галогеном, метилом, МеО или MeS;
J означает одинарную связь;
Т означает -Н;
Y означает монорадикал, образуемый циклом, выбираемым из группы, включающей (С3-С6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы могут быть, необязательно, замещены одним или более заместителями, выбираемыми из группы, включающей -ОН, -СНО, -SH, -NO2, -CN, -F, -Cl, -Br, -CO(C1-С4)алкил, -COO(C1-C4)алкил, -OCO(C1-C4)алкил, -S(C1-C4)алкил, -SO(C1-C4)алкил, -SO2(C1-C4)алкил, -SO2-O(C1-C4)алкил, -O-SO2(C1-С4)алкил, -NR5R6, -CONR5R6, -(C1-C4)алкил, необязательно замещенный одним или более -ОН или -F, и -О(C1-C4)алкил, необязательно замещенный одним или более -ОН или -F, и где циклы (С3-С6)циклоалкан и бицикл, могут также, необязательно, быть замещены одним или более заместителями оксо;
Z означает бирадикал, образуемый циклом, выбираемым из группы, включающей (С3-С6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы могут быть, необязательно, замещены одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br, -S(C1-C4)алкил, -(C1-C4)алкил, необязательно замещенный одним или более -ОН или -F, и -O(C1-С4)алкил, необязательно замещенный одним или более -ОН или -F;
R5 и R6 независимо означают -Н или -(C1-C4)алкил;
гетероцикл в вышеуказанных определениях означает пяти- или шестичленный ароматический цикл, содержащий от одного до трех гетероатомов, независимо выбираемых из О, S и N, где указанный цикл может быть соединен с остатком молекулы посредством атома углерода или азота; и
бицикл в вышеуказанных определениях означает частично ненасыщенный, насыщенный или ароматический семи-десятичленный цикл, необязательно содержащий от одного до трех гетероатомов, независимо выбираемых из О, S и N, где указанный цикл или циклы могут быть соединены с остатком молекулы посредством атома углерода или азота.
2. Соединение по п.1, где конфигурация хирального углерода, соединенного с R1, соответствует (S), отвечая, таким образом, формуле Ia.
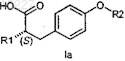
3. Соединение по п.1 или 2, где R2 означает -(CH2)s-N(COR3)-A-J-T.
4. Соединение по п.3, где R3 означает -(С1-С10)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br и -О(C1-C4)алкил-; -(С2-С6)алкенил; -(C1-C3)алкилен-Y; -(С2-С3)алкенилен-Y; -(С2-С3)алкинилен-Y или -Y; и Y в R3 означает монорадикал, образуемый циклом, выбираемым из группы, включающей (С3-С6)циклоалкан, гетероцикл, бензол и бицикл, где все три цикла, необязательно, могут быть замещены, как указано в п.1.
5. Соединение по п.3, где А означает -(С1-С4)алкилен-; -(С1-С4)алкилен-Z- или -Z-; Z в А означает бирадикал, образуемый циклом, выбираемым из группы, включающей (С3-С6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы, необязательно, могут быть замещены одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br, -S(C1-C4)алкил, -(C1-С4)алкил, необязательно замещенный одним или более -ОН или -F, и -О(С1-С4)алкил, необязательно замещенный одним или более
-ОН или -F; J означает одинарную связь и Т означает -Н.
6. Соединение по п.5, где Z в А означает незамещенный бирадикал, образуемый циклом, выбираемым из группы, включающей (С3-С6)циклоалкан и бензол.
7. Соединение по п.1 или 2, где R2 означает -(СН2)s-N(R4)-В.
8. Соединение по п.7, где R4 означает -(С4-С10)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br и -О(С1-С4)алкил; -(C1-C4)алкилен-Y или Y; и Y в R4 означает монорадикал, образуемый циклом, выбираемым из группы, включающей (С3-С6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы могут быть, необязательно, замещены, как указано в п.1.
9. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения формулы I по любому из пп.1-8 вместе с соответствующими количествами фармацевтически приемлемых эксципиентов.
10. Применение соединения формулы I по любому из пп.1-8 для производства лекарственного средства для лечения или профилактики заболеваний, опосредованных PPARy.
11. Применение соединения формулы I по любому из пп.1-8 для производства лекарственного средства для лечения или профилактики нарушений обмена веществ у млекопитающего, включая человека.
12. Применение по п.11, где нарушения обмена веществ выбирают из группы, включающей инсулиннезависимый сахарный диабет и ожирение.
13. Применение соединения формулы I по любому из пп.1-8 для производства лекарственного средства для лечения или профилактики таких заболеваний, как сердечно-сосудистые заболевания, связанные с метаболическим синдромом, воспалительные заболевания, рак, болезни костей, заживление мелких ран на коже, кожные нарушения, связанные с аномальной дифференциацией эпидермических клеток, и другие нарушения, компонентом которых является резистентность к инсулину, у млекопитающего, включая человека.
Текст
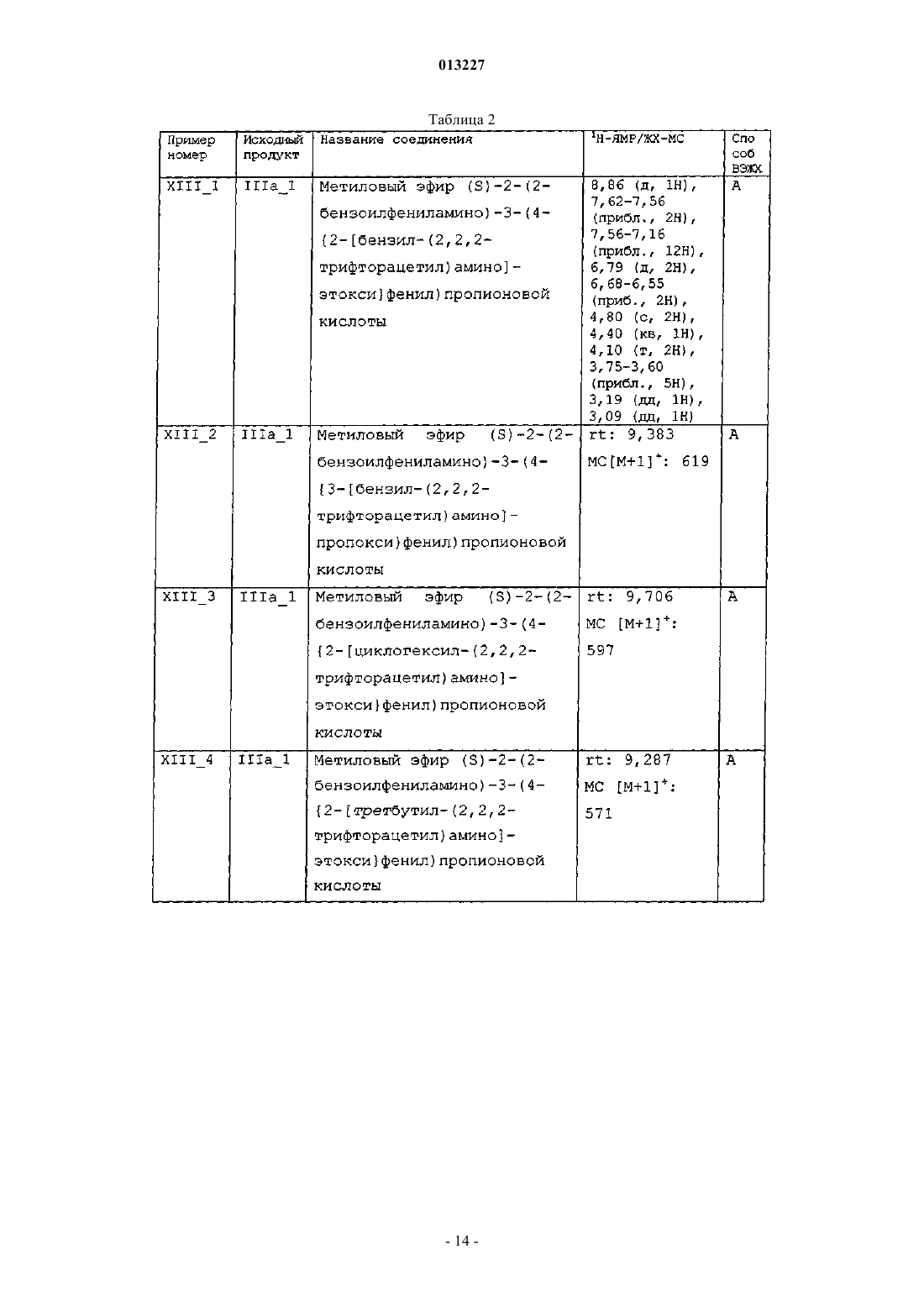
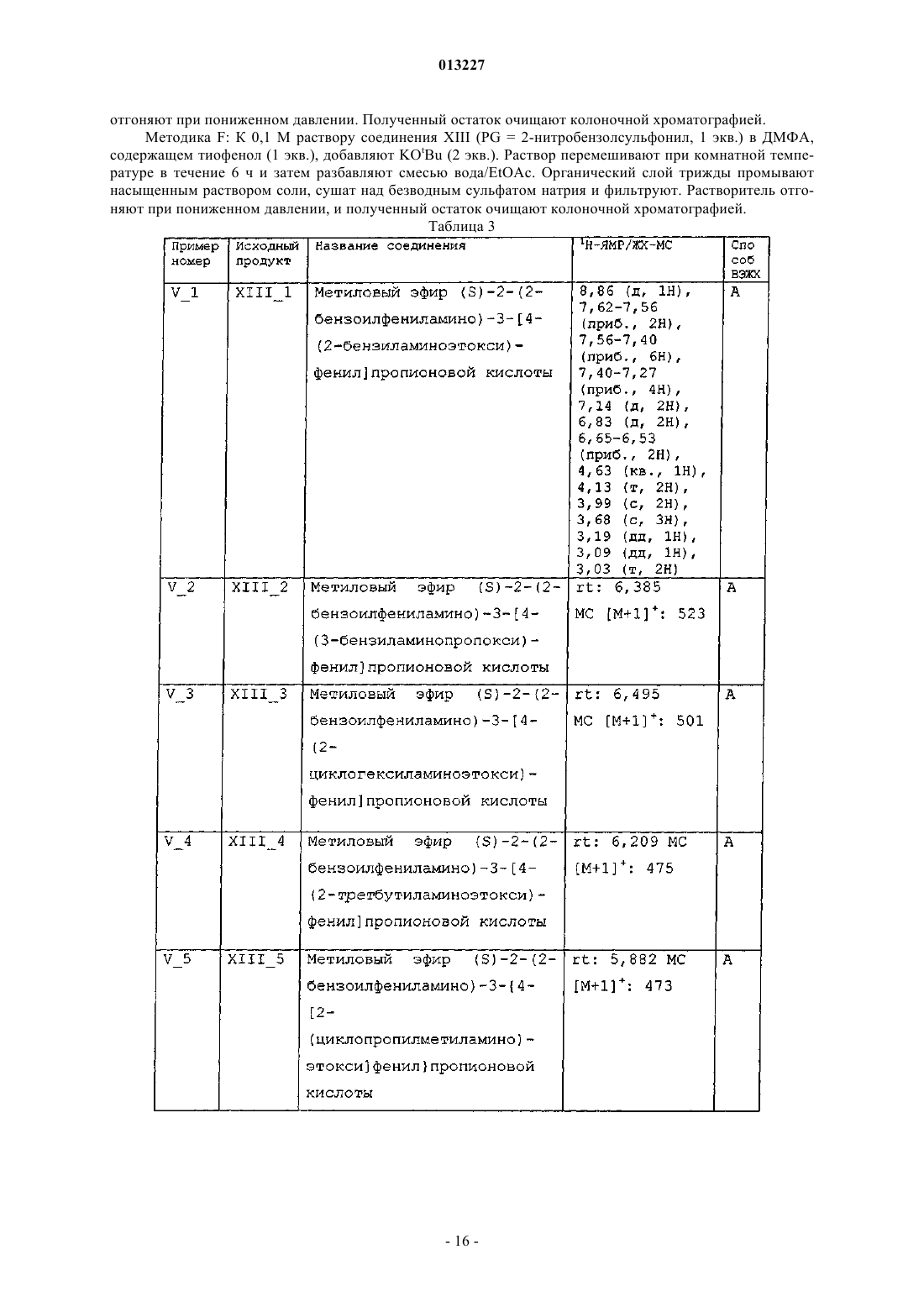
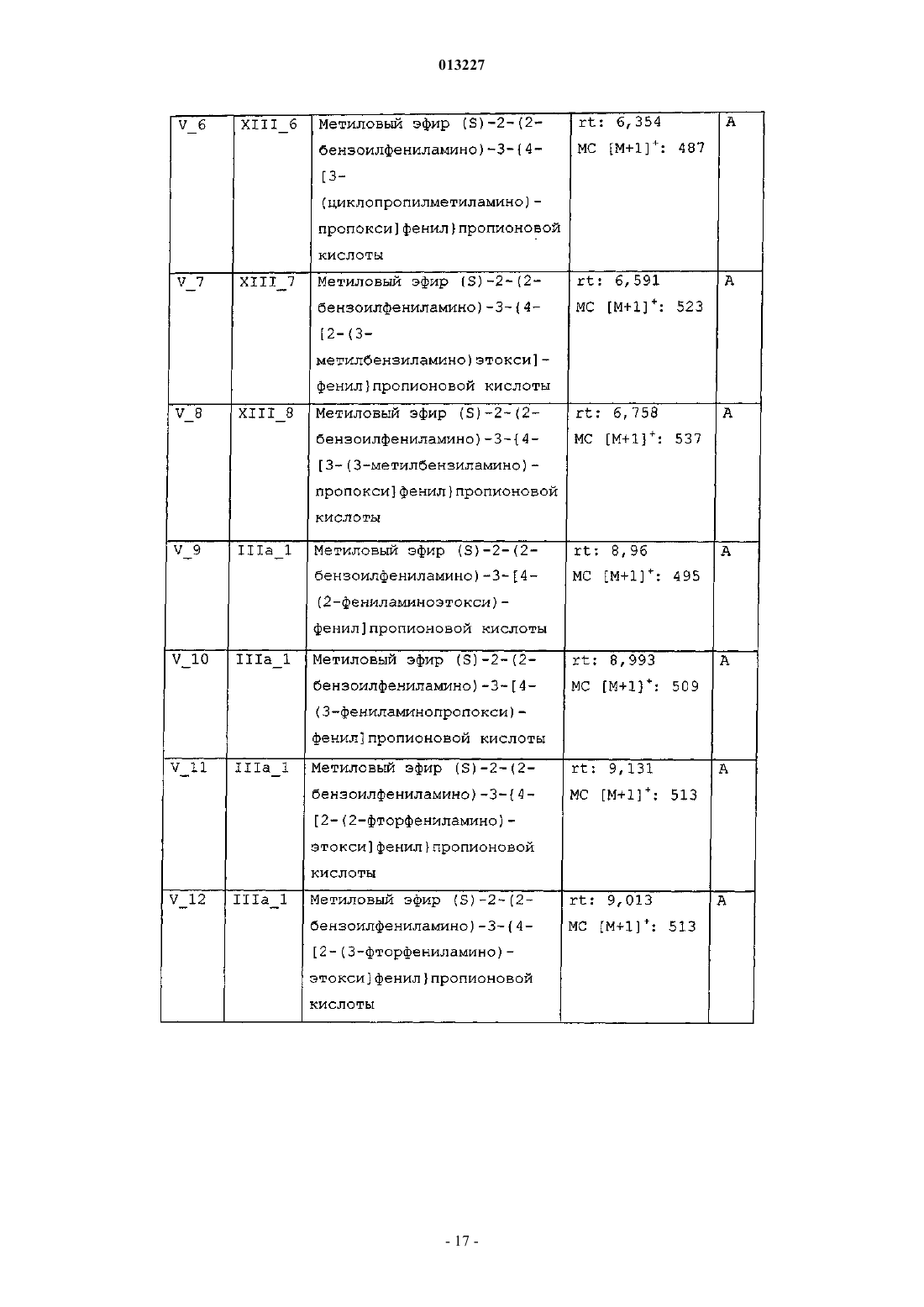
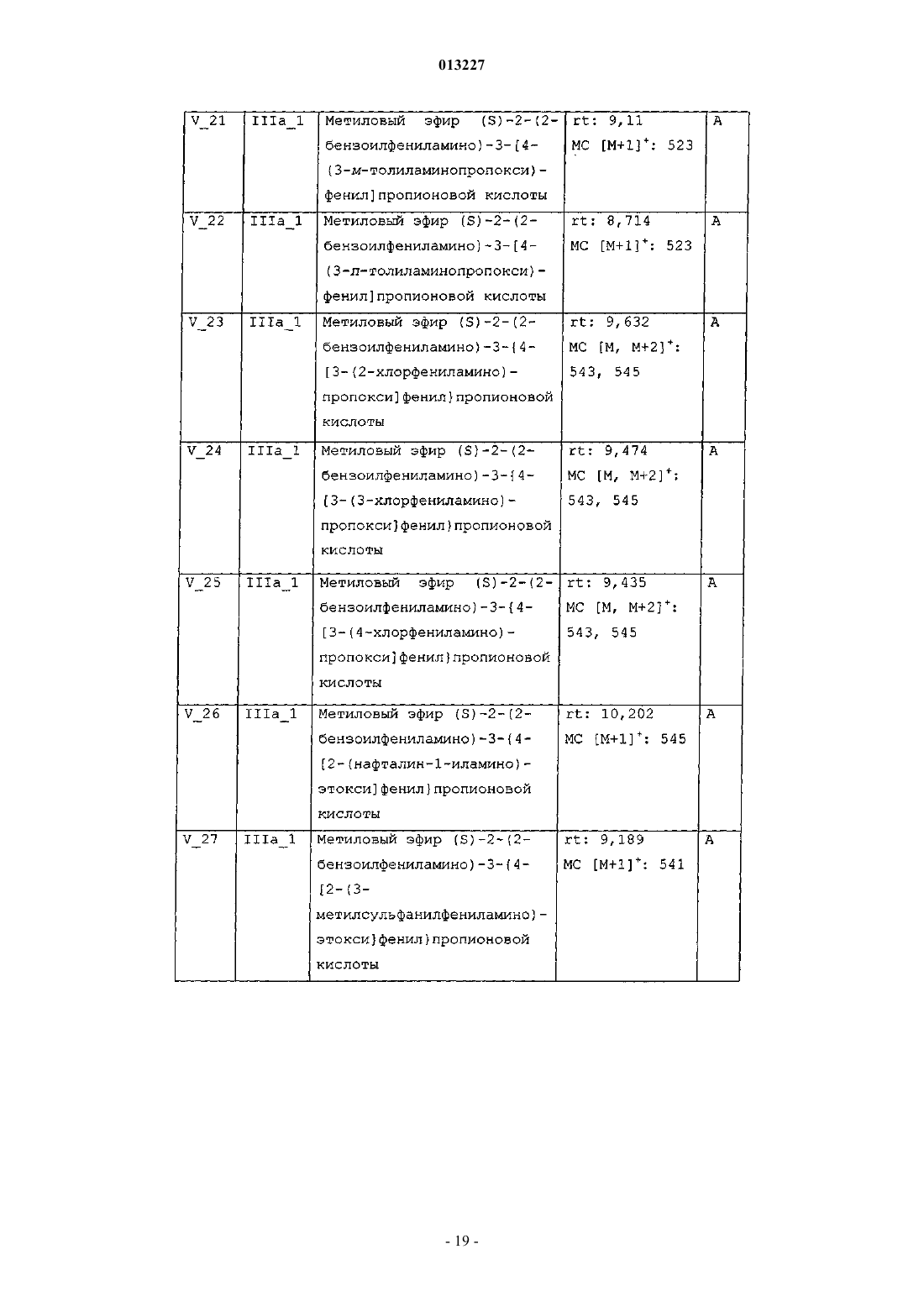
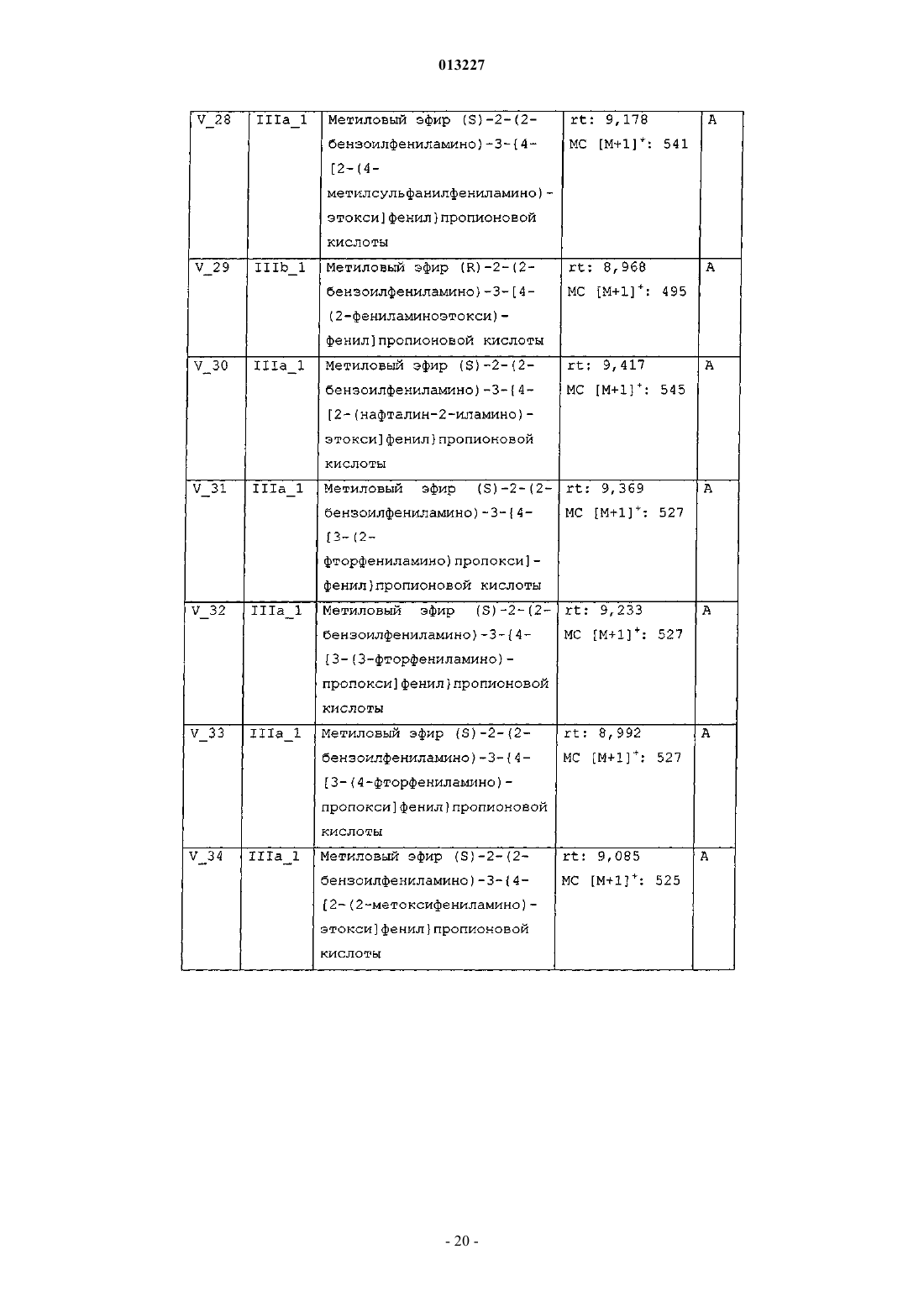
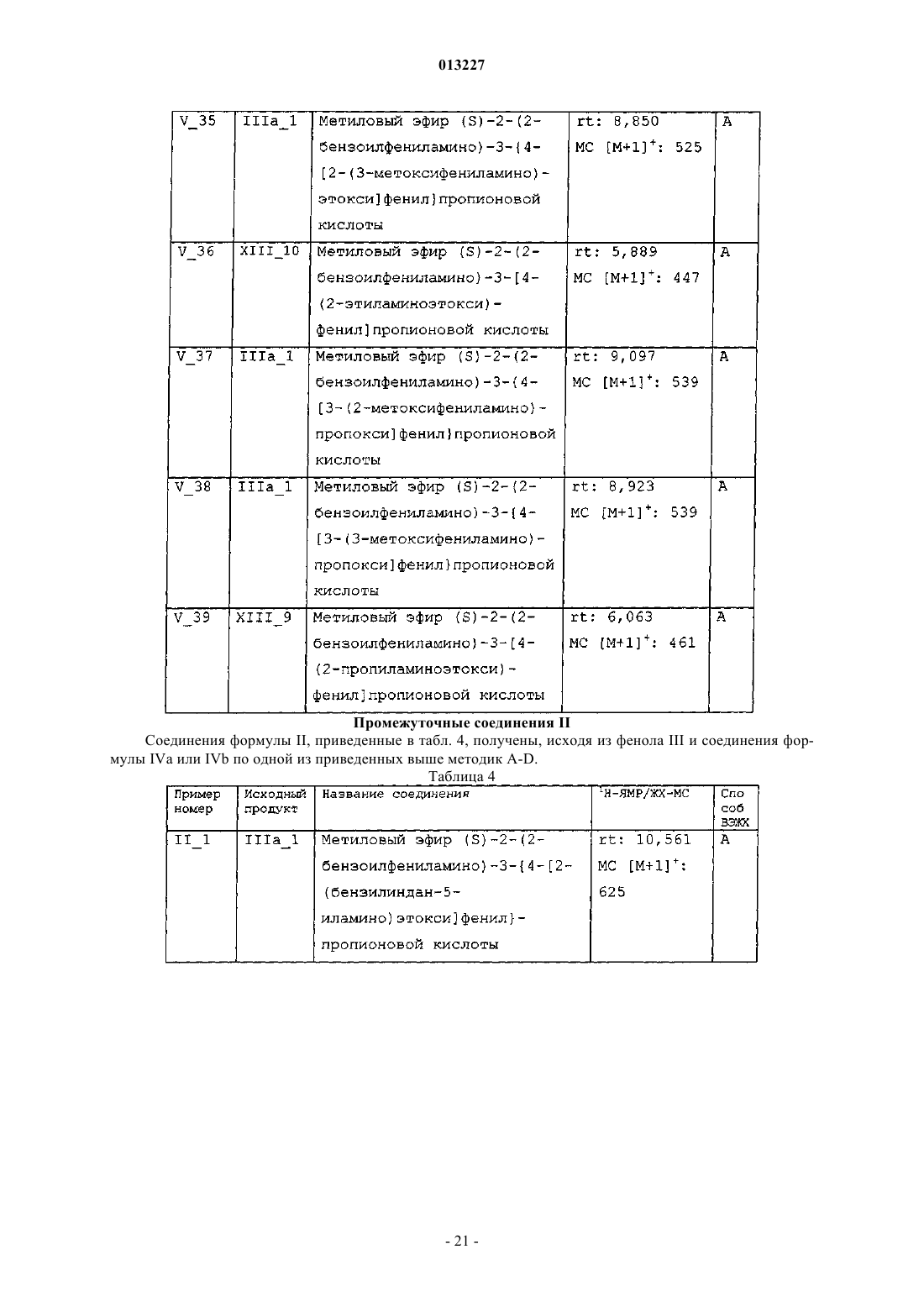
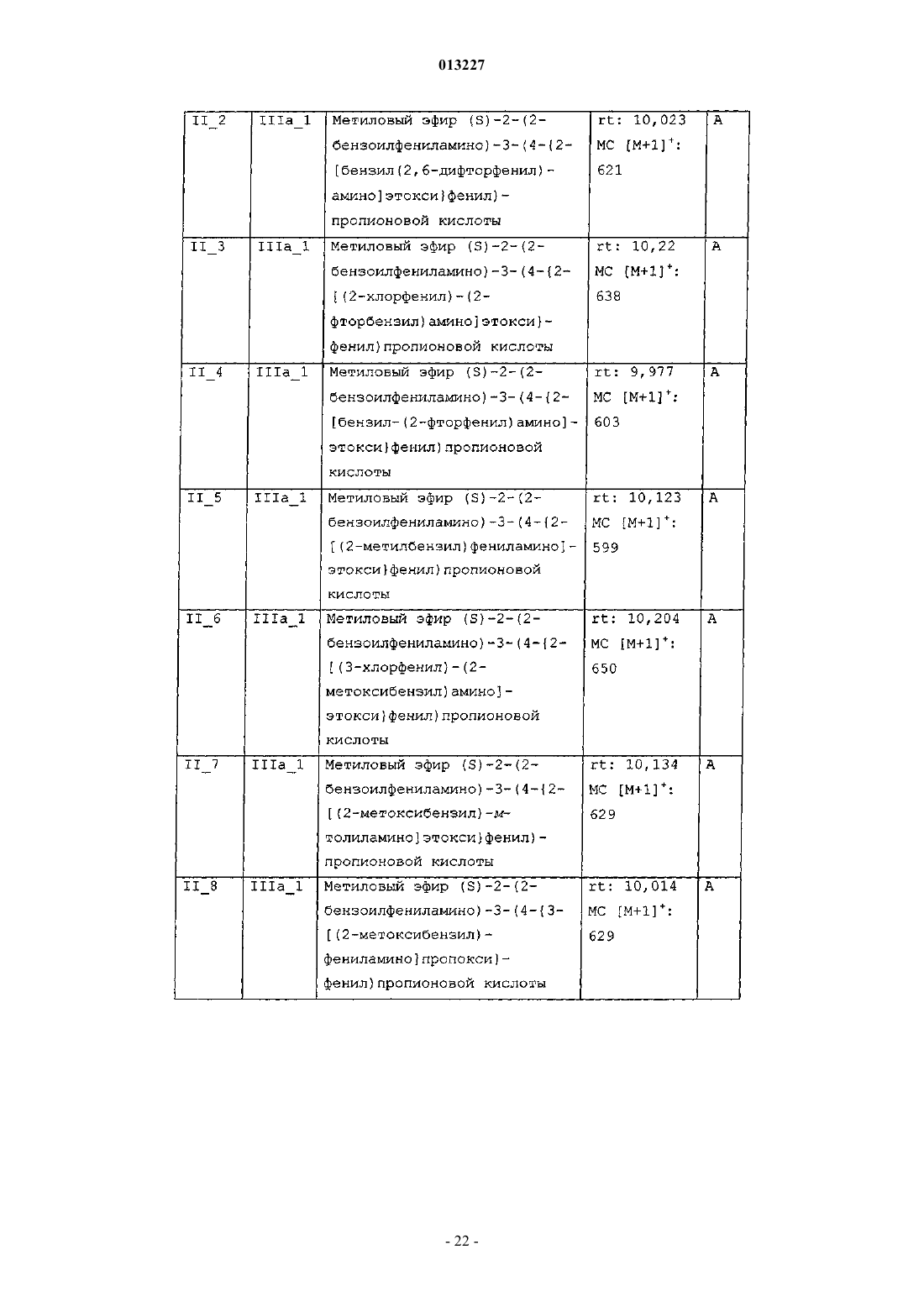
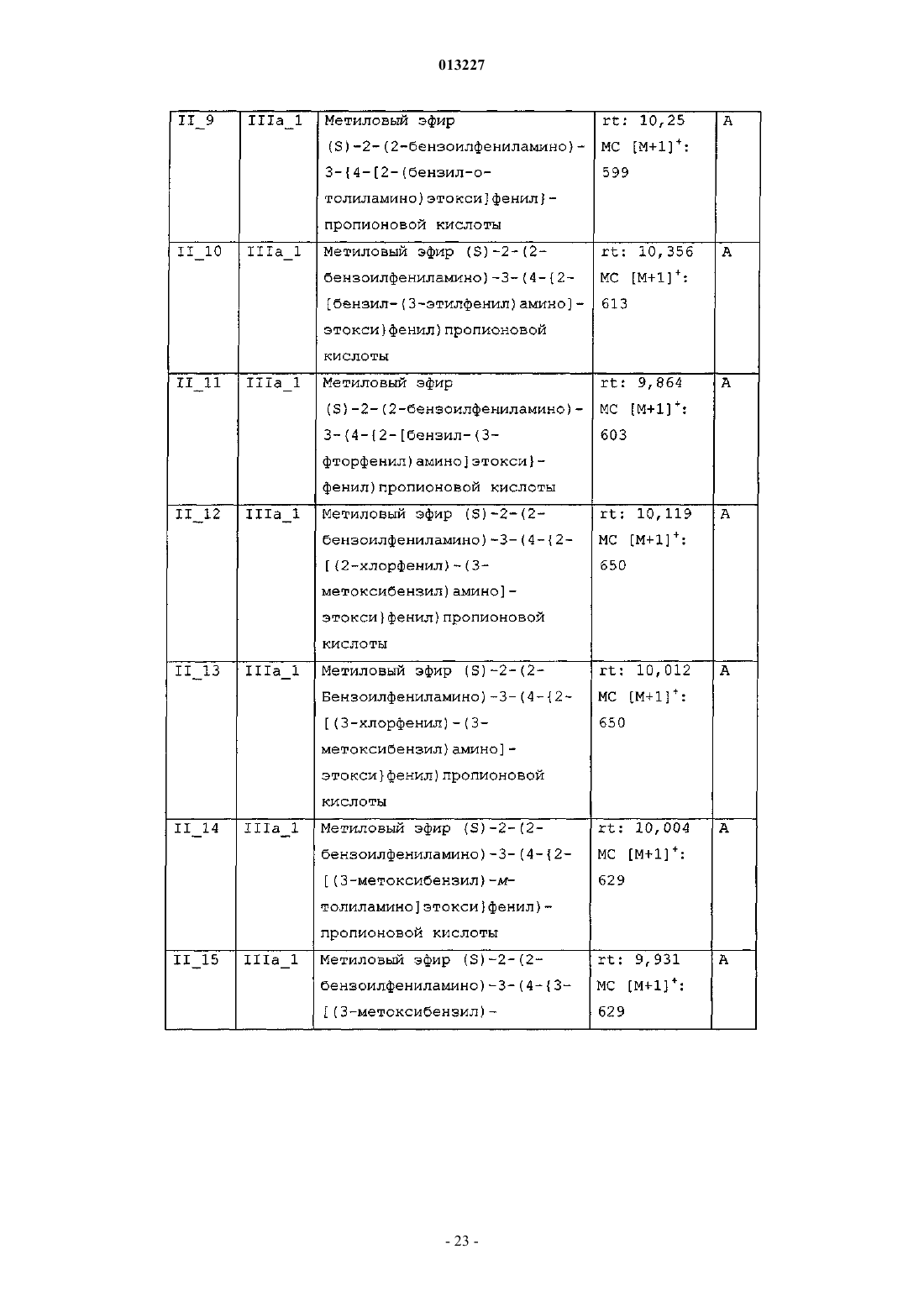
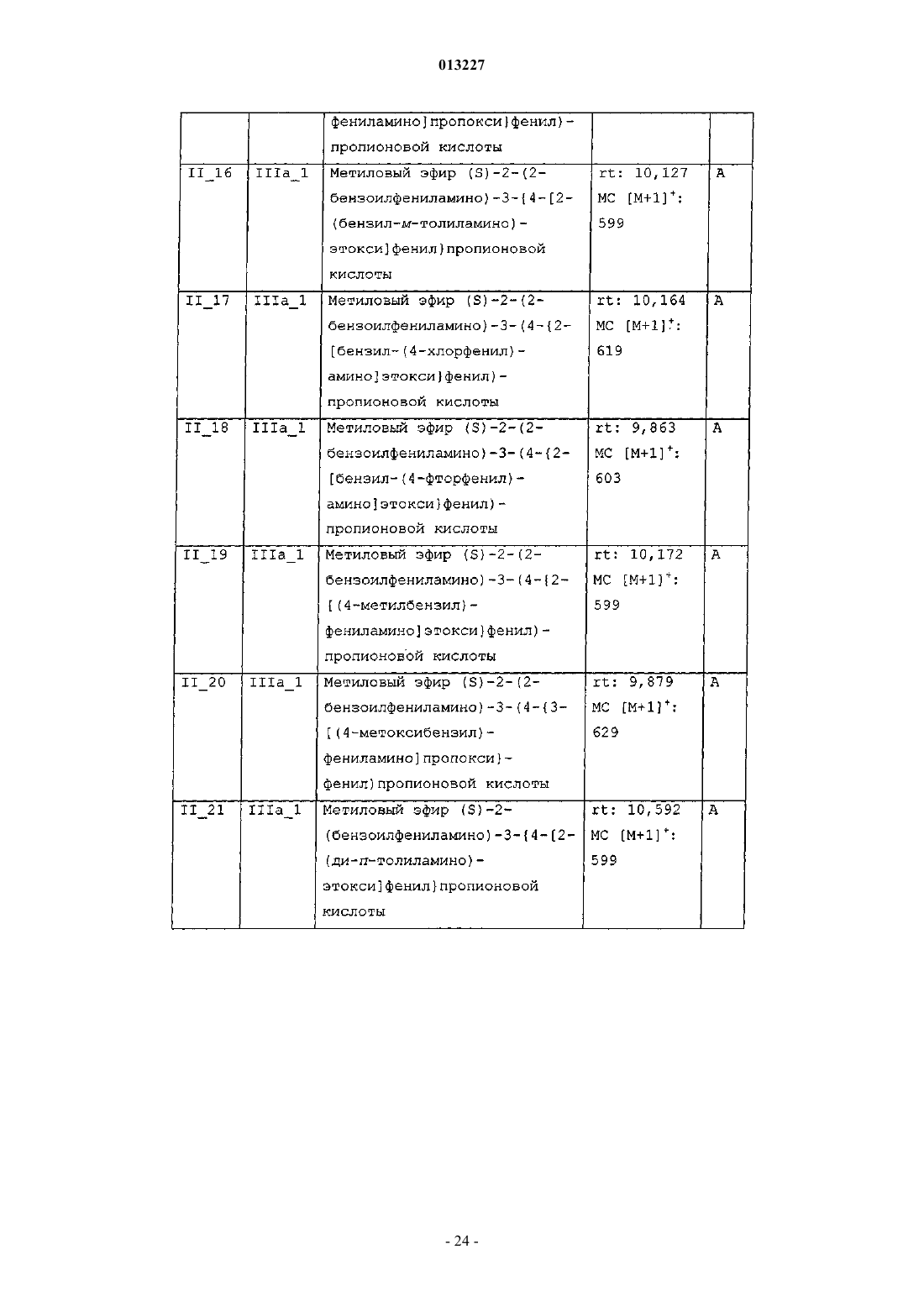
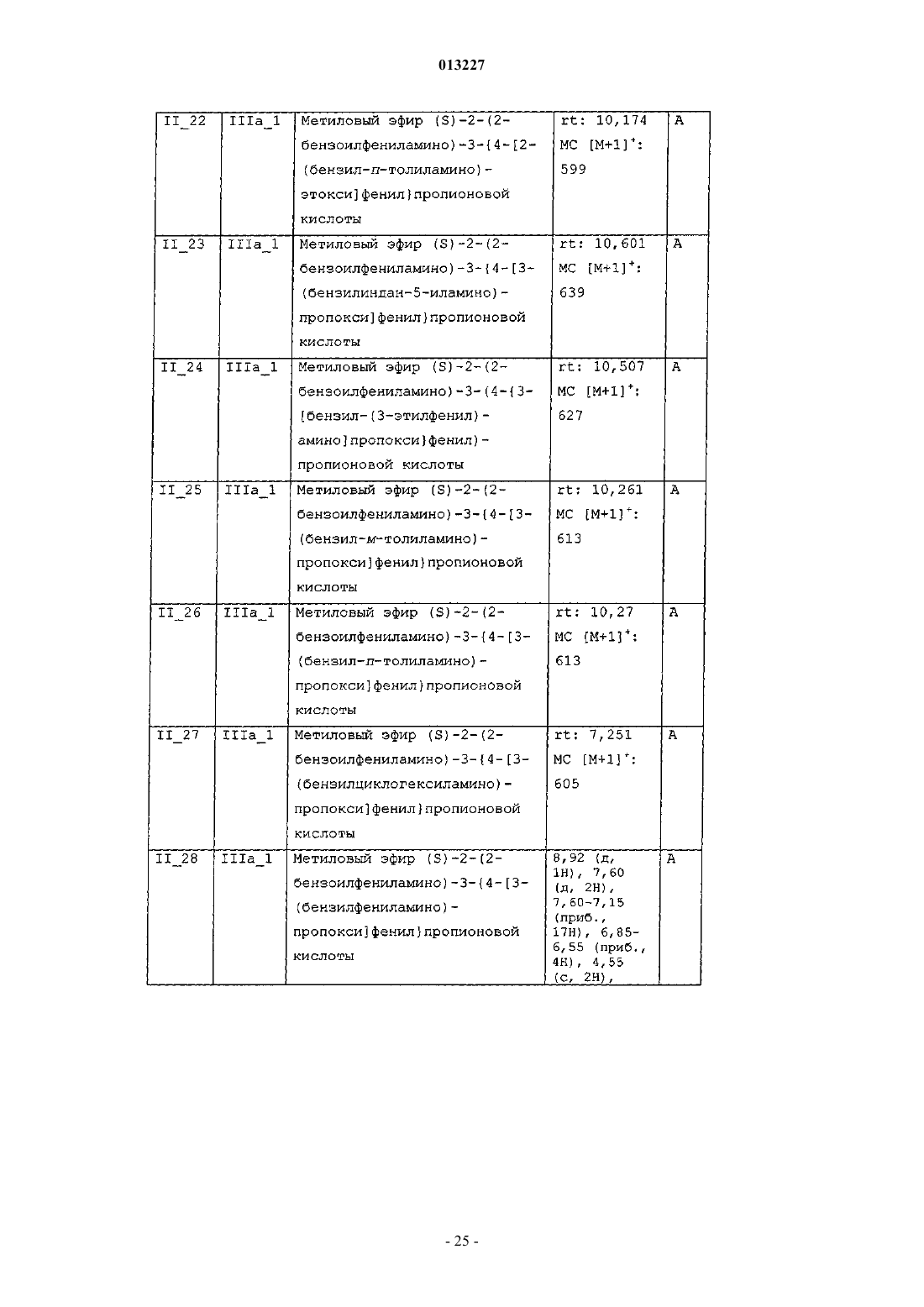
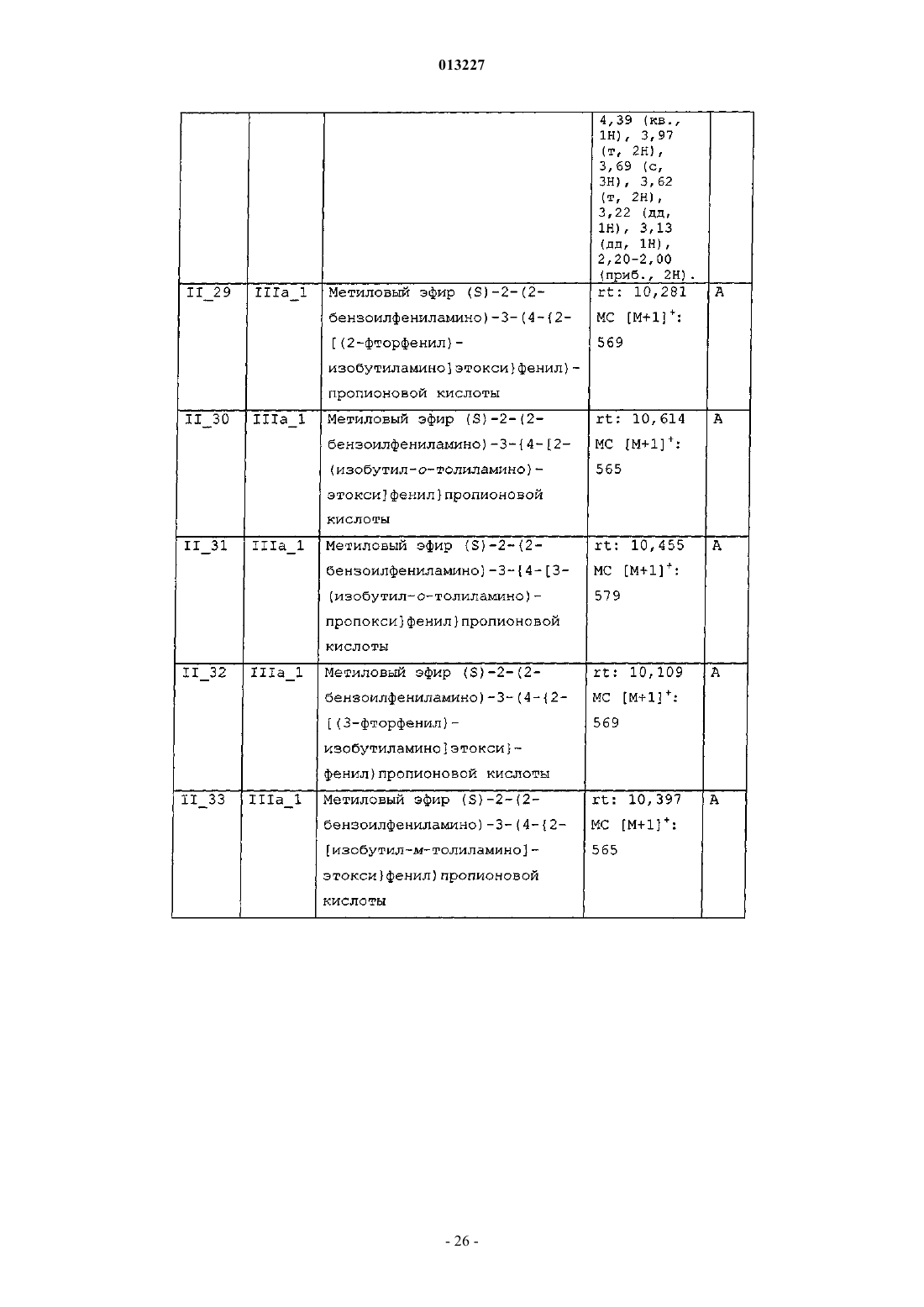
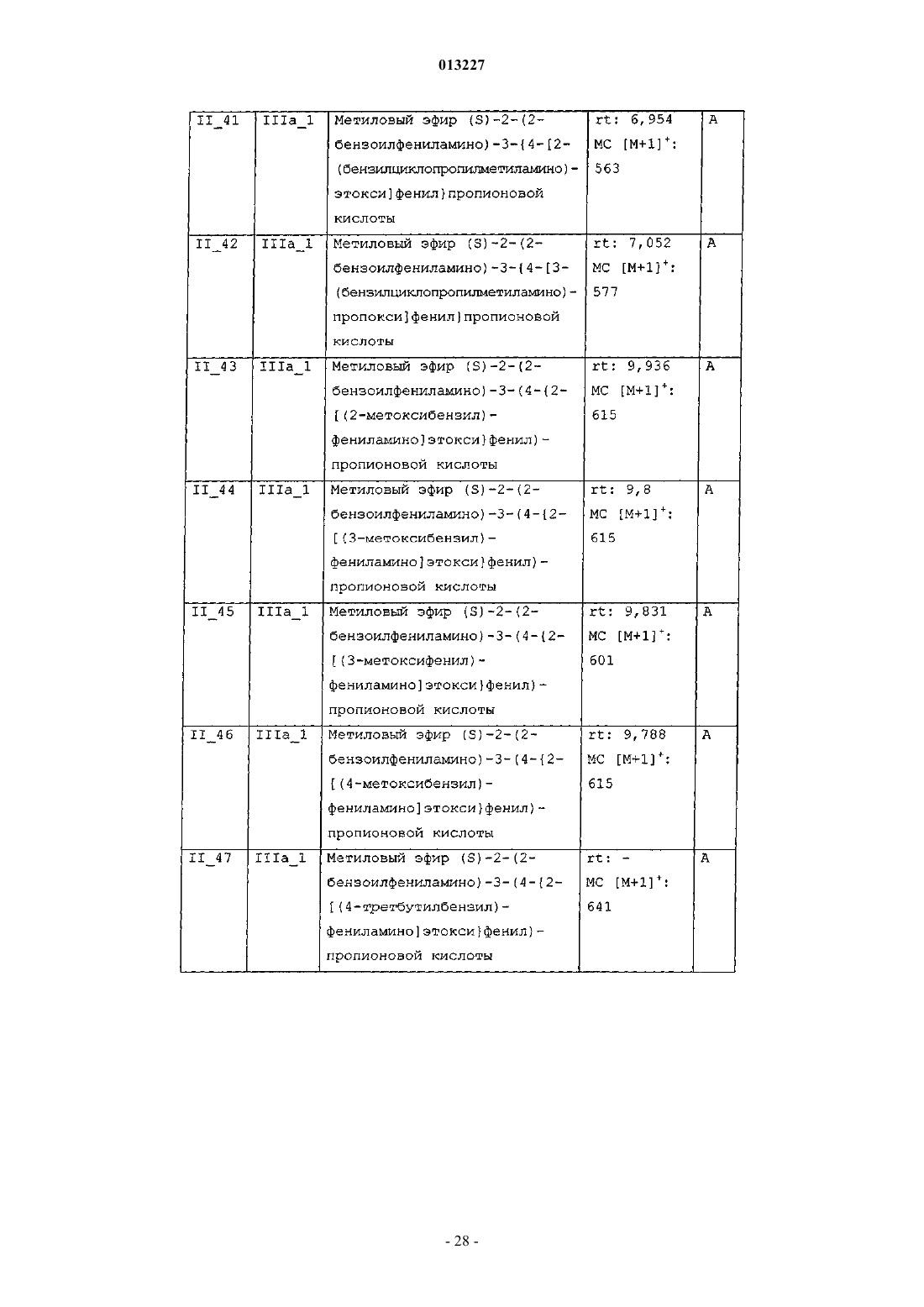
013227 Настоящее изобретение касается новых тирозиновых производных, действующих в качестве модуляторов PPAR, а также способов получения указанных производных и полезных для получения этих производных промежуточных соединений, содержащих указанные производные фармацевтических композиций и применения таких композиций в медицине. Уровень техники Рецепторы, активируемые пролифераторами пероксисом (PPAR) принадлежат к суперсемейству факторов транскрипции, известных как ядерные рецепторы. Это семейство включает рецепторы стероидного, ретиноидного и тиреоидного гормона. Идентифицированы три подтипа PPAR у человека, грызунов и Xenopus laevis. Это PPAR, PPAR/ и PPAR, каждый из которых кодируется иным геном и характеризуется иным распределением в тканях. Ген, кодирующий PPAR, воспроизводится у человека в трех различных изоформах мРНК (PPARl,PPAR2 и PPAR3) посредством различного сплайсинга и использования промотора (Fajas et al., J. Biol.Chem. 1997, vol. 272, p. 18779-18789). Изоформ PPAR1 характеризуется широким распределением в тканях, в то время, как PPAR2 и PPAR3 ограничиваются некоторыми тканями: PPAR2 экспрессируется только в жировой ткани, a PPARy3 в жировой ткани, а также в макрофагах (Fajas et al., FEBS Lett. 1998,vol. 438, p. 55-60). Различия, установленные в отношении распределения в тканях, а также в активационном профиле изоформов PPARy, позволяют предположить, что эти изоформы вовлечены в ряд физиологических функций, играющих основную роль в гомеостазе глюкозы и липидном метаболизме (Vamecq et al., Lancet 1999, vol. 354, p. 141-148). Эти функции включают, например, липидный транспорт в плазме и катаболизм жирных кислот, регуляцию чувствительности к инсулину и уровней глюкозы в крови, дифференциацию макрофагов, образующих атеросклеротические бляшки, воспалительную реакцию, канцерогенез,гиперплазию и дифференциацию адипоцитов, причем последнее является наиболее подтвержденной функцией PPAR (Grimaldi, Prog. Lipid Res. 2001, vol. 40, p. 269-281; Schiller et al., J. Biol. Chem. 2001,vol. 276, p. 14133-14137). Таким образом, обнаружение этих факторов транскрипции обеспечивает новые фармакологические объекты разработки эффективных терапевтических средств, предназначенных для профилактики и лечения нарушений обмена веществ, таких как диабет, ожирение и дислипидемия. Инсулиннезависимый сахарный диабет (NIDDM) или диабет типа 2 характеризуется резистентностью к инсулину в периферических тканях, включая мышцы, печень и жировую ткань. Глитазоны, соединения, являющиеся селективными агонистами PPAR, представляют собой лекарственные средства,снижающие резистентность к инсулину и снижают уровни глюкозы в крови. В настоящее время два продукта, относящихся к этому семейству, розиглитазон и пиоглитазон, апробированы в отношении лечения диабета типа 2 у людей. В последние годы выполнен большой объем исследовательских работ по разработке новых лекарственных средств, улучшающих профиль побочных эффектов исходных глитазонов, обладающих большей аффинностью в качестве лигандов PPAR и повышенной эффективностью в отношении диабета типа 2. Такая рациональная модификация привела к структурно разнообразным соединениям с большей эффективностью и селективностью (например, фарглитазар). Настоящие агонисты PPAR обладают недостатками, снижающими привлекательность этих агонистов, такими как печеночная токсичность (в особенности, троглитазон), прибавление в весе, отек, прибавление сердечной массы (у грызунов) и ожирение, а также ограниченная эффективность в монотерапии диабета типа 2. Приведенные факты служат мотивацией для разработки улучшенных сенсибилизаторов инсулина. Показано, что соединения, полностью или частично блокирующие активность PPAR, ингибируют дифференциацию адипоцитов. Таким образом, полные антагонисты обеспечивают эффективную терапию ожирения. Кроме того, соединения, являющиеся частичными агонистами, в дополнение к тому, что являются антагонистами, в особенности целесообразны, поскольку эффективны не только в лечении ожирения, но также в сдерживании гипергликемии. Кроме того, антагонисты/частичные агонистыPPARy эффективны в лечении ожирения и других симптомов, обычно возникающих при инсулиннезависимом диабете, таких как повышенные уровни глюкозы, триглицеридов и инсулина в плазме. В последнее время поступили сообщения о соединениях, являющихся антагонистами или частичными агонистами PPAR (WO 01/30343, WO 02/08188, WO 2004/020408), полезных для лечения ожирения и диабета типа 2, со сниженными побочными эффектами (Berger et al., Trends Pharmacol. Sci. 2005,vol. 26, p. 244-51). Примерами частичных агонистов, находящихся на стадии клинической разработки, предназначенных для лечения диабета, являются (-)-галофенат (метаглидазен), FK 614 (Minoura et al., Eur. J. Pharmacol. 2004, vol. 494, p. 273-8), T131 (Li et al., 64th Annu. Meet. Sci. Sess. Am. Diabetes Assoc. (Jun 4-Jun 8, Orlando) 2004, Abst 659-P), LY818 (Reifel-Miller et al., Diabetes 2003, 52 (Suppl. 1): Abst 614-P) и телмисартан, блокатор ангиотензина II, апробированный для лечения гипертензии, с PPAR-частичной агонистической активностью при концентрациях, достигаемых на плазматических уровнях в ходе лечения (Kurtz etal., Acta Diabetol. 2005; vol. 42 Suppl 1: S 9-16), указанные частичные агонисты находятся сейчас на вто-1 013227 рой фазе клинической разработки. В Henkel et al., J. Med. Chem. 1998, vol. 41, p. 5020-5036; Collins et al., J. Med. Chem. 1998, vol. 41, p. 5037-5054; Cobb et al., J. Med. Chem. 1998, vol. 41, p. 5055-5069, WO 94/29285 и в WO 97/31907 описаны производные N-(2-бензоилфенил)-L-тирозина в качестве эффективных и селективных агонистов PPAR. В документах WO 03/011814 и WO 03/011834 описаны производные N-(2-бензоилфенил)-L-тирозина как частичные агонисты PPAR. Патент США 6274608 описывает производные N-(2-бензоилфенил)-Lтирозина как полезные при лечении и/или профилактике состояний, опосредованных семействами ретиноид-Х-рецептора (RXR) и PPAR. Несомненно, большой интерес представляет разработка новых терапевтических агентов, модулирующих PPAR. Сущность изобретения Один из аспектов настоящего изобретения касается новых соединений общей формулы I соответствующих стереоизомеров и смесей, соответствующих полиморфов и смесей и фармацевтически приемлемых сольватов и аддитивных солей всех указанных соединений, гдеR3 означает -(C1-С 4)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Сl, -Br и -O(C1-С 4)алкил; -(С 2-С 6)алкенил; -(С 2-С 6)алкинил; -(C1 С 3)алкилен-Y; -(С 2-С 3)алкенилен-Y; -(С 2-С 3)алкинилен-Y или -Y;R4 означает -(С 4-С 10)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Сl, -Br и -O(C1-С 4)алкил; -(С 2-С 6)алкенил; -(С 2-С 6)алкинил; -(C1 С 4)алкилен-Y; -(С 2-С 4)алкенилен-Y; -(С 2-С 4)алкинилен-Y или -Y;s равно 2 или 3; А означает -(C1-С 4)алкилен-; -(С 2-С 4)алкенилен-; -(С 2-С 4)алкинилен-; -(C1-С 4)алкилен-Z-, где алкиленовая часть соединена с атомом N и Z соединен с J; либо -Z-; В означает -(С 4)алкилен-; -(С 2-С 4)алкенилен-; -(С 2-С 4)алкинилен-; -(C1-С 4)алкилен-Z-, где алкиленовая часть соединена с атомом N и Z соединен с J; либо -Z-;J означает одинарную связь или бирадикал, выбираемый из группы, включающей следующее:Y означает монорадикал, образуемый циклом, выбираемым из группы, включающей (С 3 С 6)циклоалкан, циклогексен, гетероцикл, бензол и бицикл, где все эти циклы могут быть, необязательно,замещены одним или более заместителями, выбираемыми из группы, включающей -ОН, -СНО, -SH,-NO2, -CN, -F, -Cl, -Br, -CO(C1-С 4)алкил, -COO(C1-C4)алкил, -ОСО(С 1-С 4)алкил, -S(C1-C4)алкил, -SO(C1C4)алкил, -SO2(C1-C4)алкил, -SO2-O(C1-C4)алкил, -O-SO2(C1-С 4)алкил, -NR5R6, -CONR5R6, -(C1-C4)алкил,необязательно замещенный одним или более -ОН или -F, и -О (C1-C4)алкил, необязательно замещенный одним или более -ОН или -F, и где циклы: (С 3-С 6)циклоалкан, циклогексен и бицикл, могут также, необязательно, быть замещены одним или более заместителями оксо (=O);Z означает бирадикал, образуемый циклом, выбираемым из группы, включающей (С 3 С 6)циклоалкан, циклогексен, гетероцикл, бензол и бицикл, где все эти циклы могут быть, необязательно,замещены одним или более заместителями, выбираемыми из группы, включающей -ОН, -СНО, -SH, NO2, -CN, -F, -Cl, -Br, -CO(C1-C4)алкил, -COO(C1-C4)алкил, -OCO(C1-C4)алкил, -S(C1-C4)алкил, -SO(C1C4)алкил, -SO2(C1-C4)алкил, -SO2-O (C1-C4)алкил, -O-SO2(C1-С 4)алкил, -NR5R6, -CONR5R6, -(C1C4)алкил, необязательно замещенный одним или более -ОН или -F, и -О (C1-C4)алкил, необязательно замещенный одним или более -ОН или -F, и где циклы: (C3-C6)циклоалкан, циклогексен и бицикл, могут также, необязательно, быть замещены одним или более заместителями оксо (=O);R5 и R6 независимо означают -Н или -(C1-C4)алкил; гетероцикл в вышеуказанных определениях означает пяти- или шестичленный ароматический цикл, содержащий от одного до трех гетероатомов, независимо выбираемых из О, S и N, где указанный цикл может быть соединен с остатком молекулы посредством атома углерода или азота; и-2 013227 бицикл в вышеуказанных определениях означает частично ненасыщенный, насыщенный или ароматический семи-десятичленный цикл, необязательно содержащий от одного до трех гетероатомов, независимо выбираемых из О, S и N, где указанный цикл или циклы могут быть соединены с остатком молекулы посредством атома углерода или азота. Соединения формулы I являются PPAR модуляторами и поэтому полезны в качестве активных фармацевтических веществ. Таким образом, другой аспект настоящего изобретения касается фармацевтических композиций,содержащих эффективное количество соединения формулы I или фармацевтически приемлемой соли,или сольвата указанного соединения, и один или более фармацевтически приемлемых эксципиентов. Еще один аспект настоящего изобретения касается применения соединения формулы I для производства лекарственного средства для лечения или профилактики заболеваний, опосредованных PPAR. Другой аспект настоящего изобретения касается применения соединения формулы I для производства лекарственного средства для лечения или профилактики нарушений обмена веществ у нуждающихся в этом пациентов, включая человека. Еще один аспект настоящего изобретения касается применения соединения формулы I или фармацевтически приемлемой соли, или сольвата указанного соединения для производства лекарственного средства для лечения или профилактики нарушений обмена веществ, выбираемых из группы, включающей инсулиннезависимый сахарный диабет и ожирение, у нуждающихся в этом пациентов, включая человека. Другой аспект настоящего изобретения касается применения соединения формулы I или фармацевтически приемлемой соли, или сольвата указанного соединения для производства лекарственного средства для лечения или профилактики таких заболеваний, как сердечнососудистые заболевания, связанные с метаболическим синдромом, воспалительные заболевания, рак,болезни костей, заживление мелких ран на коже, кожные нарушения, связанные с аномальной дифференциацией эпидермических клеток, и другие нарушения, компонентом которых является резистентность к инсулину, у нуждающихся в этом пациентов, включая человека. Другой аспект настоящего изобретения касается способа лечения или профилактики заболеваний,опосредованных PPAR, включающего введение млекопитающему, в том числе человеку, эффективного количества соединения формулы I или фармацевтически приемлемой соли, или сольвата указанного соединения. Еще один аспект настоящего изобретения касается способа лечения или профилактики нарушений обмена веществ, включающего введение млекопитающему, в том числе человеку, эффективного количества соединения формулы I или фармацевтически приемлемой соли, или сольвата указанного соединения. Другой аспект настоящего изобретения касается способа лечения или профилактики нарушений обмена веществ, выбираемых из группы, включающей инсулиннезависимый сахарный диабет и ожирение, включающего введение млекопитающему, в том числе человеку, эффективного количества соединения формулы I или фармацевтически приемлемой соли, или сольвата указанного соединения. Еще один аспект настоящего изобретения касается способа лечения или профилактики таких заболеваний, как сердечно-сосудистые заболевания, связанные с метаболическим синдромом, воспалительные заболевания, рак, болезни костей, заживление мелких ран на коже, кожные нарушения, связанные с аномальной дифференциацией эпидермических клеток, и другие нарушения, компонентом которых является резистентность к инсулину, включающего введение млекопитающему, в том числе человеку, эффективного количества соединения формулы I или фармацевтически приемлемой соли, или сольвата указанного соединения. В приведенных выше определениях термины "алкил" и "алкилен" означают, соответственно, монорадикальную или бирадикальную, линейную или разветвленную, насыщенную углеводородную цепь,содержащую указанное число атомов углерода. Примеры алкила включают, но не в порядке ограничения, метил, этил, пропил, изопропил, бутил, изобутил, вторбутил, третбутил, пентил, изопентил, неопентил, гексил, гептил, октил, нонил, децил и тому подобное. Термины "алкенил" и "алкенилен", как использованы здесь, означают, соответственно, монорадикальную или бирадикальную, линейную или разветвленную, ненасыщенную углеводородную цепь, содержащую указанное число атомов углерода, а также содержащую одну или более двойных связей. Примеры алкенила включают, но не в порядке ограничения, этенил, 1-пропенил, 2-пропенил, 1-бутенил, 2 бутенил, 3-бутенил, 1,3-бутадиенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-гексенил, 2 гексенил, 3-гексенил, 4-гексенил, 5-гексенил и тому подобное. Термины "алкинил" и "алкинилен", как использованы здесь, означают, соответственно, монорадикальную или бирадикальную, линейную или разветвленную, ненасыщенную углеводородную цепь, содержащую указанное число атомов углерода, а также содержащую одну или более тройных связей. Примеры алкинила включают, но не в порядке ограничения, этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2 бутинил, 3-бутинил, 1,3-бутадиинил, 1-пентинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-гексинил, 2 гексинил, 3-гексинил, 4-гексинил, 5-гексинил и тому подобное. Термин гетероцикл, как использован здесь, означает, пяти- или шестичленное, моноциклическое ароматическое кольцо, содержащее от одного до трех гетероатомов, независимо выбираемых из О, S и N. Как упомянуто выше, эти гетероциклы могут быть, необязательно, замещены одним или более замести-3 013227 телями, расположенными в любом доступном положении цикла, и могут быть соединены с остатком молекулы через любой доступный атом углерода или азота. Примеры включают, но не в порядке ограничения, 1,2,4-оксадиазол, 1,2,4-тиадиазол, 1,3,4-оксадиазол, 1,3,4-тиадиазол, фуран, имидазол, изоксазол,изотиазол, оксазол, пиразол, пиррол, тиазол, тиофен, 1,2,3-триазол, 1,2,4-триазол, пиразин, пиридазин,пиридин, пиримидин и тому подобное. Термин (С 3-С 6)циклоалкан, как использован здесь, означает насыщенное, моноциклическое, углеводородное кольцо, содержащее указанное число атомов углерода. Как упомянуто выше, указанный цикл может быть, необязательно, замещен одним или более заместителями, расположенными в любом доступном положении цикла. Примеры (С 3-С 6)циклоалканов включают, но не в порядке ограничения, циклопропан, циклобутан, циклопентан и циклогексан. Термин бицикл, как использован здесь, означает, частично ненасыщенный, насыщенный или ароматический семи-десятичленный цикл, необязательно содержащий от одного до трех гетероатомов, независимо выбираемых из О, S и N, где указанный цикл или циклы могут быть соединены с остатком молекулы через атом углерода или азота. Как упомянуто выше, эти бициклы могут быть, необязательно, замещены одним или более заместителями, расположенными в любом доступном положении цикла. Примеры бициклических групп включают, среди прочего, нафталин, 1,2,3,4-тетрагидронафталин, хинолин,1,2,3,4-тетрагидрохинолин, изохинолин, бензофуран, 2,3-дигидробензофуран, бензотиофен, индол, бензимидазол, бензотриазол, бицикло[2.2.1]гептан, бицикло[3.2.1]октан и бицикло[3.2.2]нонан. Выражение "необязательно замещенный одним или более" означает, что группа может быть незамещенной или замещенной одним или более, предпочтительно 1, 2, 3 или 4 заместителями, при условии что эта группа содержит 1, 2, 3 или 4 доступных для замещения положения. Подразумевается, что во всем тексте описания и приложенных пунктов слово "включает" и вариации слова, такие как "включающий", не означает, что исключаются другие добавки, компоненты, элементы или стадии. Раскрытия сущности изобретения в реферате, приложенном к данной заявке, и в заявке, на основании которой испрашивается приоритет, включены здесь посредством ссылки. Как использован здесь, термин "лечение" включает лечение, профилактику и тактику лечения указанного заболевания. Термин "фармацевтически приемлемый", как использован здесь, означает те соединения, композиции и/или дозированные формы, которые по медицинской оценке пригодны для использования в контакте с тканями людей или животных, не проявляют при этом избыточной токсичности и не вызывают раздражения, аллергической реакции или других проблем или осложнений, соответствуя разумному соотношению польза/риск. Соединения формулы I по настоящему изобретению содержат по меньшей мере один хиральный центр. Настоящее изобретение включает как рацемические соединения, так и энантиомерные соединения, т.е., соединения формулы Ia (где конфигурация хирального углерода, связанного с R1, соответствует В конкретном варианте осуществления изобретения конфигурация хирального углерода, связанного с R1, соответствует (S). В другом варианте осуществления R2 в соединении формулы I или 1 а означает -(СН 2)S-N(COR3) A-J-T. Еще в одном варианте осуществления R2 в соединении формулы I или Ia означает -(СН 2)s-N(R4)B-J-T. В другом варианте осуществления J в соединении формулы I или Ia означает одинарную связь и Т означает -Н. Еще в одном варианте осуществления J в соединении формулы I или Ia означает -(СН 2)1-4-,-O-, -S-, -SO-, -SO2-, -О(С 1-С 4)алкил- или -S(C1-C4)алкил-. В другом варианте осуществления Т в соединении формулы I или Ia означает -Н или -(С 1-С 4)алкил. В другом варианте осуществления R2 в соединении формулы I или Ia означает -(СН 2)S-N(COR3)-AJ-T; R3 означает -(C1-С 10)алкил, необязательно замещенный одним или более заместителями, выбираемыми из группы, включающей -F, -Cl, -Br и -О(С 1-С 4)алкил-; -(С 2-С 6)алкенил; -(С 1-С 3)алкилен-Y; -(С 2 С 3)алкенилен-Y; -(С 2-С 3)алкинилен-Y или -Y; и Y в R3 означает монорадикал, образуемый циклом, выбираемым из группы, включающей (С 3-С 6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы,необязательно, могут быть замещены, как указано выше. В другом варианте осуществления R2 в соединении формулы I или Ia означает -(СН 2)S-N (COR3)-AJ-T; А означает -(С 1-С 4)алкилен-; -(С 1-С 4)алкилен-Z- или -Z-; Z в А означает бирадикал, образуемый циклом, выбираемым из группы, включающей (С 3-С 6) циклоалкан, гетероцикл, бензол и бицикл, где все три цикла, необязательно, могут быть замещены одним или более заместителями, выбираемыми из группы,включающей -F, -Cl, -Br, -S(С 1-С 4)алкил, -(С 1-С 4)алкил, необязательно замещенный одним или более -ОН или -F, и -О(С 1-С 4)алкил, необязательно замещенный одним или более -ОН или -F; J означает одинарную связь и Т означает -Н. В другом варианте осуществления R2 в соединении формулы I или Ia означает -(СН 2)S-N(COR3)-A-4 013227J-T; А означает -(C1-С 4)алкилен-; -(С 1-С 4)алкилен-Z- или -Z-; Z в А означает незамещенный бирадикал,образуемый циклом, выбираемым из группы, включающей (С 3-С 6)циклоалкан и бензол; J означает одинарную связь и Т означает -Н. В другом варианте осуществления R2 в соединении формулы I или Ia означает -(СН 2)S-N(R4)-B-J-T;R4 означает -(С 4-С 10)алкил, необязательно замещенный одним или более заместителями выбираемыми из группы, включающей F, -Cl, -Br и -О(С 1-С 4)алкил; -(С 1-С 4)алкилен-Y или -Y; и Y в R4 означает монорадикал, образуемый циклом, выбираемым из группы, включающей (С 3-С 6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы могут быть необязательно замещены, как указано выше. В другом варианте осуществления R2 в соединении формулы I или Ia означает -(СН 2)S-N(R4)-B-J-T,В означает -(С 1-С 4)алкилен-Z- или -Z-; Z в В означает бирадикал, образуемый циклом, выбираемым из группы, включающей (С 3-С 6)циклоалкан, гетероцикл, бензол и бицикл, где все эти циклы могут быть,необязательно, замещены, как указано выше; J означает одинарную связь и Т означает -Н. Кроме того, все возможные комбинации вышеупомянутых вариантов осуществления также являются частью настоящего изобретения. Соединения по настоящему изобретению могут содержать один или более основных атомов азота и,следовательно, могут образовывать соли с кислотами, которые также являются частью настоящего изобретения. Примеры фармацевтически приемлемых солей включают, среди прочего, аддитивные соли с неорганическими кислотами, такими как хлористо-водородная, бромисто-водородная, иодистоводородная, азотная, перхлорная, серная и фосфорная кислота, а также аддитивные соли с органическими кислотами, такими как уксусная, метансульфоновая, трифторметансульфоновая, этансульфоновая,бензолсульфоновая, n-толуолсульфоновая, бензойная, камфорсульфоновая, миндальная, щавелевая, янтарная, фумаровая, винная и малеиновая кислота. Подобным образом, соединения по настоящему изобретению могут содержать один или более кислотных протонов и, следовательно, могут образовывать соли с основаниями, которые также являются частью настоящего изобретения. Примеры этих солей включают соли с катионами металлов, такими как, например, ион щелочного металла, ион щелочноземельного металла или ион алюминия; либо соединения могут быть координационно связаны с органическим или неорганическим основанием. Приемлемое органическое основание включает, среди прочего,дизтиламин и тризтиламин. Приемлемое неорганическое основание включает гидроксид алюминия, гидроксид кальция, гидроксид калия, карбонат натрия и гидроксид натрия. Может присутствовать более чем один катион или анион, в зависимости от числа несущих заряд функциональностей и от валентности катионов и анионов. Соли, образованные фармацевтически приемлемыми органическими нетоксичными основаниями,включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая замещенные амины природного происхождения, циклических аминов и основных ионообменных смол, таких как аргинин, бетаин, кофеин, холин, N,N-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2 диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперидин,полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и тому подобное. Не существует ограничения по типу соли, которая может быть использована, при условии, что эти соли являются фармацевтически приемлемыми, когда используются в терапевтических целях. Соли могут быть синтезированы из исходного соединения, содержащего основную или кислотную составляющую, по общепринятым химическим методикам. Обычно такие соли могут быть получены при взаимодействии форм свободной кислоты или свободного основания этих соединений со стехиометрическим количеством соответствующего основания или соответствующей кислоты, в воде или в органическом растворителе, таком как диэтиловый эфир, этилацетат, этанол, изопропанол или ацетонитрил, либо в смеси того и другого. Соединения формулы I и соответствующие соли отличаются некоторыми физическими свойствами, но эквивалентны в целях настоящего изобретения. Некоторые из соединений формулы I по настоящему изобретению могут существовать как в несольватированных, так и в сольватированных формах, таких как, например, гидраты. Настоящее изобретение охватывает все такие вышеупомянутые формы, которые являются фармацевтически активными. Некоторые соединения общей формулы I могут проявлять полиморфизм, настоящее изобретение охватывает все возможные полиморфные формы и соответствующие смеси. Различные полиморфы могут быть получены кристаллизацией в различных условиях, либо нагреванием или плавлением соединения с последующим постепенным или быстрым охлаждением. Наличие полиморфов может быть установлено ЯМР-спектроскопией твердого тела, ИК-спектроскопией, дифференциальной сканирующей калориметрией, рентгеновской порошковой дифрактометрией или иными подобными способами. Соединения формулы I по настоящему изобретению содержат по меньшей мере один хиральный центр. Кроме того, соединения формулы I по настоящему изобретению могут иметь дополнительные хиральные центры. Настоящее изобретение включает каждый из возможных стереоизомеров и смеси, в особенности, рацемические смеси стереоизомеров. Отдельный энантиомер может быть получен любым общепринятым способом, например хроматографическим разделением рацемической смеси на непод-5 013227 вижной хиральной фазе, путем разделения рацемической смеси способами фракционированной кристаллизации диастереомерных солей, путем хирального синтеза, путем ферментативного разделения или биотрансформацией. Это разделение может быть выполнено на любом хиральном синтетическом промежуточном соединении или на продуктах общей формулы I. Альтернативно, любой энантиомер соединения общей формулы I может быть получен энантиоспецифическим синтезом с использованием оптически чистых исходных материалов или реагентов известной конфигурации. Некоторые соединения по настоящему изобретению могут существовать в виде нескольких диастереоизомеров, которые могут быть разделены общепринятыми способами такими как хроматография или фракционированная кристаллизация. Некоторые соединения по настоящему изобретению могут существовать в виде цис/транс-изомеров. Настоящее изобретение включает каждый из геометрических изомеров и смеси этих изомеров. Настоящее изобретение охватывает все изомеры и смеси этих изомеров (например рацемические смеси) независимо от того получены смеси синтезом или физическим смешением изомеров. Настоящее изобретение касается способа получения вышеуказанных новых соединений, соответствующих производных, аналогов, таутомерных форм, стереоизомеров, полиморфов или фармацевтически приемлемых солей и сольватов. Соединения по настоящему изобретению могут быть синтезированы с применением описанных ниже способов, а также другими способами известными в области органического синтеза. Предпочтительные способы включают, но не в порядке ограничения, общие способы, представленные на приложенных схемах. Если не оговорено иное, группы Rl, R2, R3, R4, R5, R6, s, А, В, J и Т имеют значения,указанные для общей формулы I. Соединение формулы I может быть получено в общем случае гидролизом соединения формулы II,где R7 означает (С 1-С 4)алкил. Это взаимодействие может быть выполнено в присутствии основания, такого как гидроксид щелочного металла, в растворителе, таком как тетрагидрофуран, водный метанол или смесь указанных растворителей, при температуре, изменяющейся в пределах от комнатной температуры до температуры кипения растворителя, предпочтительно при комнатной температуре. Соединение формулы II может быть получено, как показано на приведенной выше схеме, через синтез простого эфира Williamson'а (см. например Bal-Tembe et al., Bioorg. Med. Chem. 1997, 5, 13811388; Cantello et al., J. Med. Chem. 1994, vol. 37, p. 3977-3985 или ЕР 875510) или в условиях Mitsunobu(Mitsunobu Synthesis 1981, 1; Hughes, Org. React. 1992, 42, 335). В первом случае сложный эфир фенола III может быть подвергнут взаимодействию с R2-LG (IVa),где LG означает уходящую группу, такую как, например, галоген, включая -Cl, -Br, -I, или алкилсульфонат или арилсульфонат, включая мезилат, тозилат или нозилат. Это взаимодействие осуществляют в присутствии основания, такого как NaH, К 2 СО 3 или Cs2CO3, в растворителе, таком как N,Nдиметилформамид, ацетон или этилацетат, при температуре, изменяющейся в пределах от комнатной температуры до температуры кипения растворителя, предпочтительно при нагревании. Во втором случае соединение формулы III может быть подвергнуто взаимодействию со спиртом формулы R2-OH (IVb) с использованием, например, диэтилазодикарбоксилата (DEAD) и трифенилфосфина в тетрагидрофуране, в качестве растворителя, при температуре, изменяющейся в пределах от комнатной температуры до температуры кипения растворителя, предпочтительно при комнатной температуре. Отдельные энантиомерные формы формулы Ia и Ib могут быть получены либо хиральным разделением соединения формулы I, либо исходя из соответствующих хиральных соединений IIIa и IIIb, соответственно. Соединение формулы II, где R2 означает -(СН 2)S-N(COR3)-A-J-Т (т.е., соединение формулы IIa),может быть также получено ацилированием соединения формулы Va с помощью соединения формулы Это взаимодействие осуществляют в присутствии основания, такого как трэтиламин, в растворителе, таком как дихлорметан или этилацетат при температуре, изменяющейся в пределах от комнатной температуры до температуры кипения растворителя. Некоторые соединения формулы IIа могут также быть получены при взаимодействии соединенияVa с соответствующей кислотой формулы VIb (см. например, Elmore, Amino Acids Pep. Proteins 2001, 32,107-162). Это взаимодействие осуществляют в присутствии связующего агента, такого как комбинация 1-(3-диметиламинопропил)-3-этилкарбодиимид (EDC) и 1-гидроксибензотриазол (НОВТ), в присутствии основания, такого как триэтиламин, в растворителе, таком как этилацетат или тетрагидрофуран, при температуре, изменяющейся в пределах от комнатной температуры до температуры кипения растворителя. Некоторые соединения формулы II, где R2 означает -(CH2)S-N(R4)-B-J-T (т.е., соединения формулыIIb), могут также быть получены при взаимодействии соединения формулы Vb с алкилирующим агентом формулы R4-LG (VII), где LG имеет вышеуказанные значения. Это взаимодействие осуществляют в присутствии основания, такого как K2CO3, в подходящем растворителе, таком как N,N-диметилформамид или ацетон, при температуре, изменяющейся в пределах от комнатной температуры до температуры кипения растворителя, предпочтительно при комнатной температуре. Альтернативно, соединения формулы II могут быть получены твердофазным синтезом с использованием различных типов полимерных твердых смол, таких как Wang или 2-хлортритиловые смолы(Collins et at. J. Med. Chem. 1998, 41, 5037-5054). Соединения формулы III могут быть получены по методикам, аналогичным описанным в Cobb et al., J. Med. Chem. 1998, 41, 5055-69. Соединения IVa и IVb, где R2 означает -(CH2)S-N(R4)-B-J-T (т.е., соединения формулы IVaa и IVba,соответственно) могут быть получены, как показано на следующей схеме: Соединение VIII ацилируют с помощью соединения формулы IX, получая соединение формулы X,где R9 означает -СО 2(С 1-С 4)алкил или -ОСО(С 1-С 4)алкил, в тех же условиях, что и в случае взаимодействия соединения Va с VIa, получая соединение IIа. Восстановление соединения X с помощью восстанавливающего агента, такого как литийалюмогидрид, в диэтиловом эфире дает соединение IVba. Альтернативно, соединение VIII может быть подвергнуто взаимодействию с алкилирующим аген-7 013227 том формулы XI, что приводит к образованию соединения IVba (Daoud et al., J. Indian Chem. Soc. 1989,66, 316-318). Соединение формулы IVaa получают, превращая гидроксильную группу соединения IVba в уходящую группу. Это взаимодействие может быть осуществлено с использованием сульфонилгалогенида, такого как метансульфонилхлорид, в присутствии основания, такого как пиридин или триэтиламин, в растворителе, таком как дихлорметан или хлороформ. Альтернативно, соединение IVba может быть подвергнуто взаимодействию с галогенирующим агентом, таким как SOCl2, в растворителе, таком как тетрагидрофуран. Соединение VIII может также быть превращено непосредственно в соединение формулы IVaa путем осуществления взаимодействия с соединением формулы XII, где каждый LG независимо означает уходящую группу, как указано выше, в тех же условиях, что указаны для превращения VIII в IVba. Соединение формулы V (включая соединения формулы Va и Vb) может быть получено с использованием двух различных синтетических последовательностей, как показано на следующей схеме: Фенол III может быть подвергнут взаимодействию с защищенным амином формулы XIVa илиXIVb, что приводит к образованию соединения формулы XIII, где R8 означает -A-J-T или -B-J-T, LG означает уходящую группу, как указано выше, и PG означает защитную группу, такую как, например,трифторацетил или 2-нитробензолсульфонил. Взаимодействие осуществляют в тех же условиях, что указаны для превращения соединения формулы III в соединение формулы II. Соединение V получают впоследствии путем снятия защиты соединения XIII. Это взаимодействие осуществляют в различных условиях, в зависимости от характера защитной группы (см. например, Harland et al. Synthesis 1984, 941-43,Hirschmann et al. J. Amer. Chem. Soc. 1993, 12550-12568, для группы трифторацетамид и Lin et al. Tetrahedron Letters 2000, 3309-3313 для группы 2-нитробензолсульфониламид). Альтернативно, соединение формулы V может быть получено при взаимодействии фенола III с вторичным амином формулы XVa согласно синтезу простого эфира Williamson'а. Соединения формулы VIII промышленно доступны, либо могут быть получены способами, аналогичными описанным, например, вWO 03/53966 или ЕР 875510. Соединения XIVa и XIVb могут быть получены при взаимодействии соответствующего незащищенного амина формулы XV и защитной группы (см., Protective Groups in OrganicSynthesis, John WileySons, 3rd Edition, 1999). Соединение формулы XV может быть получено с применением следующей синтетической схемы: Соединение XVI ацилируют, получая соединение XVII, в условиях, соответствующих условиям взаимодействия соединения Va и VIa, что дает соединение IIа. Восстановление соединения XVII дает соединение XVb, в условиях, указанных для восстановления соединения X. Соединения XVb, где аминогруппа менее реакционноспособна, чем гидроксильная группа, могут быть превращены в соединенияXVa, в условиях, указанных для превращения IVba в IVaa. Кроме того, соединение формулы XVc может быть получено, исходя из соединения формулы Данное превращение может быть осуществлено при взаимодействии с альдегидом формулы R10CHO (XIX), где R10 означает R8, в котором группой, связанной с N, является -СН 2, в присутствии восстанавливающего агента, такого как триацетоксиборгидрид или цианоборгидрид, в растворителе, таком как 1,2-дихлорэтан. Альтернативно, соединение XVIII может быть подвергнуто взаимодействию с соединением XX или производным указанного соединения, что дает соответствующий амид, как указано выше. Восстановление полученного продукта приводит к соединению формулы XVc. Соединения VIa,VIb, VII, IX, XI, XII, XVI, XVIII, XIX и XX промышленно доступны или могут быть легко получены общепринятыми способами. Как очевидно для специалиста в данной области, некоторые из вышеуказанных взаимодействий могут также быть выполнены на соединениях формулы I. Соединения по настоящему изобретению являются лигандами рецептора PPAR. Поэтому такие соединения в особенности полезны для лечения или профилактики состояния, опосредованного PPAR, у нуждающегося в этом пациента, включая человека. Таким образом, настоящее изобретение касается применения этих соединений для получения лекарственного средства для лечения или профилактики таких заболеваний, как нарушения обмена веществ, сердечно-сосудистые заболевания, связанные с метаболическим синдромом (включая сосудистый рестеноз), воспалительные заболевания, рак, болезни костей (в особенности, остеопороз), заживление мелких ран на коже, кожные нарушения, связанные с аномальной дифференциацией эпидермических клеток, в особенности, образование келоидов, и другие нарушения, компонентом которых является резистентность к инсулину, включая синдром X. Например, нарушения обмена веществ, которые можно лечить или предупредить, включают такие нарушения, как инсулиннезависимый сахарный диабет, ожирение, гиперхолестеринемия (включая повышение уровней HDL), дислипидемия (включая гиперлипидемию и гипертриглицеридемию) и другие липид-опосредованные патологии. Например, воспалительные заболевания, которые можно лечить или предупредить, включают ревматоидный артрит, атеросклероз, псориаз, воспалительные заболевания кишечника и панкреатит. Описанные здесь соединения могут быть использованы для лечения этих заболеваний или состояний раздельно, либо могут быть использованы для лечения указанных заболеваний или состояний одновременно с лечением ожирения. Настоящее изобретение также касается фармацевтических композиций, содержащих соединение формулы I или фармацевтическую соль, или сольват указанного соединения, вместе с одним или более фармацевтически приемлемыми эксципиентами, либо в виде разовой дозы, либо в виде многократных доз. Приведенные ниже примеры эксципиентов даны исключительно с целью иллюстрации и не рассматриваются как ограничивающие объем изобретения. Соединения по настоящему изобретению могут быть введены в форме любого фармацевтического-9 013227 препарата. Технология приготовления фармацевтического препарата зависит от характера активного соединения и способа введения. Может быть использован любой способ введения, например, такой как пероральный, буккальный, пульмональный, местный, парентеральный (включая подкожный, внутримышечный и внутривенный), трансдермальный, окулярный (офтальмологический), ингаляционный, интраназальный, ушной, через слизистую, методом имплантата или ректального введения. Однако предпочтительными являются пероральное, местное или парентеральное введение. Твердые композиции для перорального введения включают, среди прочего, таблетки, грануляты и твердые желатиновые капсулы, составленные в виде препаратов немедленного высвобождения или препаратов модифицированного высвобождения. Способ получения может быть основан на простом смешивании, сухой грануляции, мокрой грануляции или лиофилизации активного соединения с эксципиентами. Этими эксципиентами могут быть связующие агенты, такие как сироп, камедь, желатин, сорбит, трагакантовая камедь, кукурузный крахмал или поливинилпирролидон; наполнители, такие как лактоза, сахар, микрокристаллическая целлюлоза,маисовый крахмал, фосфат кальция или сорбит; лубриканты, такие как стеарат магния, стеариновая кислота, тальк, полиэтиленгликоль или диоксид кремния; дезинтегранты, такие как картофельный крахмал,альгиновая кислота или крахмалгликолят натрия; смачивающие вещества, такие как лаурилсульфат натрия, подсластители, такие как сахароза, лактоза, декстроза, маннит, сорбит или сахарин; биоадгезивные средства, такие как гидроксипропилцеллюлоза, поли(виниловый спирт), поли(изобутилен), карбоксиметилцеллюлоза натрия; вещества, способствующие скольжению, такие как трисиликат магния, порошкообразная целлюлоза, крахмал, тальк или трехосновный фосфат кальция; вещества, способствующие текучести, такие как коллоидный диоксид кремния; модификаторы высвобождения, такие как ксантановая камедь, этилцеллюлоза, карбомер, гидроксипропилметилцеллюлоза или воск, или осмотические вещества, такие как бикарбонат калия или хлорид натрия. Таблетки могут быть покрыты оболочкой согласно хорошо известным из уровня техники способам,таким как водоэмульсионное покрытие, покрытие с использованием материала с растворителем или сухое покрытие. Активное соединение может также быть включено путем нанесения оболочки на инертные пеллеты, с использованием пленкообразующих веществ, путем экструзии и сферонизации, путем пеллетизации методом горячего плавления, либо может быть использована форма пастилок или лепешек. Когда единичная дозированная форма представляет собой капсулу, эта капсула может содержать, в дополнение к материалам вышеуказанного типа, жидкий носитель, такой как жирное масло или воск. Порошки и грануляты для получения пероральных суспензий путем добавления воды могут быть получены смешением активного соединения с диспергирующими или смачивающими агентами; суспендирующими средствами, средствами против спекания или слеживания, буферными веществами и консервантами. Могут быть добавлены также другие эксципиенты, например подсластители корригенты и красители. Альтернативно, соединения по настоящему изобретению могут быть включены в пероральные жидкие препараты, такие как эмульсии, растворы, дисперсии, суспензии, сиропы, эликсиры, или препараты в форме мягких желатиновых капсул. Указанные препараты могут содержать общеупотребимые инертные разбавители, такие как очищенная вода, этанол, сорбит, глицерин, полиэтиленгликоли (макроголы) и пропиленгликоль. Вспомогательные композиции могут также содержать такие вспомогательные средства, как смачивающие, суспедирующие средства, подсластители, корригенты, консерванты, буферные вещества, хелатирующие средства и антиоксиданты. Растворы или суспензии могут быть получены в воде, соответственно смешанной с поверхностноактивным веществом, таким как лаурилсульфат натрия. Дисперсии могут также быть получены в глицерине, жидких полиэтиленгликолях и смесях указанных веществ с маслами. В обычных условиях хранения и применения эти препараты содержат консервант для предупреждения роста микроорганизмов. Кроме того, содержащие такие соединения композиции могут быть в виде сухого продукта, смешиваемого с водой или другим подходящим растворителем перед употреблением. Препараты для инъекций, предназначенные для парентерального введения, включают стерильные растворы, суспензии или эмульсии в масляных или водных растворителях, и могут содержать вспомогательные средства, такие как суспендирующие, стабилизирующие, тонизирующие средства или диспергирующие средства. Препарат для назального применения может содержать соединение формулы I, растворенное или суспендированное в жидком носителе, в особенности, в водном носителе, предусмотренное для аэрозольного применения. Носитель может содержать добавки, такие как солюбилизирующие средства, например, пропиленгликоль, поверхностно-активные вещества, усилители всасывания, такие как лецитин(фосфатидилхолин) или циклодекстрин, или консерванты, такие как парабены. Соединение может также быть составлено в препарат для местного применения. Препараты включают кремы, лосьоны, гели, порошки, растворы, препараты в виде шампуней, пероральную пасту, препараты для полоскания полости рта и пластыри, где соединение диспергировано или растворено в подходящих эксципиентах. Этими эксципиентами могут быть противомикробные консерванты, такие как ими- 10013227 домочевина, пропилпарабен, пропиленгликоль или метилпарабен; эмульгирующие средства, такие как цетиловый спирт, метилцеллюлоза, полоксамер или триглицериды со средней длиной цепи; стабилизаторы эмульсий, такие как глицерилмоностеарат, магнийалюмосиликат, циклодекстрины или воск; увлажнители, такие как триацетин, глицерин, пропиленгликоль или сорбит; вещества, усиливающие смачивание, такие как изопропилмиристат; буферные вещества, такие как яблочная кислота, цитрат калия или двухосновный форсфат натрия; поверхностно-активные вещества, такие как докузат натрия, лаурилсульфат натрия, полисорбаты или эфиры сорбита; загустители, такие как гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза или полиэтиленоксид. Эффективная дозировка активного ингредиента может изменяться в зависимости от конкретного вводимого соединения, способа введения, характера или тяжести заболевания, которое лечат, а также возраста, общего состояния и массы тела пациента, наряду с прочими факторами. Типичным примером подходящей дозировки является дозировка, изменяющаяся в пределах приблизительно от 0,001 до 100 мг/кг массы тела в день, которая может быть введена в виде одной или разделенных доз. Однако вводимая дозировка обычно выбирается по усмотрению лечащего врача. Испытание на связывание PPAR2 кДНК, кодирующую открытую рамку считывания hPPAR2, амплифицируют PCR (полимеразной цепной реакцией) и вставляют в плазмиду pGEX-4T-2. Эту конструкцию (pGEX-hPPAR) вводят в Е. coli,где указанная конструкция сверхпродуцируется и частично очищается как слитый белок с глутатион-Sтрансферазой (GST) (Elbrecht et al., J. Biol. Chem. 1999, 274, 7913-7922). Связывание соединений с GSThPPAR2 определяют, используя модификации способа, описанного Lehmann et al. (J. Biol. Chem. 1995,270, 12953-12957). Рецепторы (2,5 мкг) инкубируют в 96-луночных планшетах в присутствии или в отсутствии продуктов с [3H]BRL-49853 (100 нМ) в течение 3 ч при 4 С, в конечном объеме 200 мкл буфераTris-HCl, 10 мМ, рН:8,0, содержащего 50 мМ KCl и 10 мМ DTT. Неспецифическое связывание определяют в присутствии 100 мкМ BRL-49853. Реакционную смесь переносят в микропланшет MultiscreenDurapore (Millipore), содержащий в каждой лунке глутатион-сефарозу 4 В. Реакционную смесь оставляют инкубироваться со смолой на 10 мин и затем центрифугируют при 735 g в течение 2 мин. Чтобы вызвать диссоциацию связи рецептора со смолой, добавляют 10 мМ восстановленный глутатион и инкубируют в течение 10 мин. Рецептор извлекают центрифугированием. Затем добавляют сцинтилляционную жидкость для элюцирования и содержащуюся радиоактивность определяют количественно с помощью жидкостной сцинтилляционной спектроскопии (Microbeta Wallac, Perkin Elmer). Испытание на трансактивацию LBD-hPPARoв Клетки COS-7 культивируют в 24-луночных планшетах и транс-инфицируют плазмидами pFACMV,которые кодируют рекомбинантные белки, содержащие домен связывания ДНК GAL4, слитый с LBDPPAR. Репортерной плазмидой для вышеуказанных конструкций является pFR-Luc, содержащая пять повторяющихся групп GAL4-чувствительного элемента, в присутствии промотера, регулирующего транскрипцию гена люциферазы. Липофектамин используют в качестве агента трансфекции. Плазмиды химерных рецепторов и ген репортера внедряют в клетки путем транзиторной трансфекции в клеткахCOS-7 в культуре. Когда продукты добавляют к культуре на момент времени 48 ч, активность люциферазы отражает влияние модуляции активности PPAR на транскрипцию конструкции репортера (Wright etal., J. Biol. Chem. 2000, 275, 1873). Клонирование PPAR2 человека кДНК PPAR человека амплифицируют посредством RT-PCR. Для hPPAR2, РНК получают из белой жировой ткани человека. Каждый амплифицированнный фрагмент клонируют в pBluescript(Stratagene(R и определяют последовательность аминокислотных остатков. Выбирают один клон для каждого построения и используют как матрицу для дальнейшего субклонирования и амплификации PCR. Конструкция GST-слитого белка Для создания этого химерного белка полную кДНК для PPAR человека клонируют в pGEX4T2(Amersham Biosciences). Фрагмент получают из pBluescript-кДНК клонов, дигестированных эндонуклеазами. Для оценки идентичности плазмид и обеспечения синфазного клонирования белков, определяют последовательность аминокислотных остатков конструкции pGEX. Слитый белок GST-hPPAR2 создают в Escherichia coli (DE3 штамм BL21). Клетки культивируют в среде LB до плотности А 600= 1,6 ед.опт.пл. и индуцируют сверхэкспрессию путем добавления индуцированных изопропил-1-тиоDгалактопиранозидом (IPTG) культур до конечной концентрации 0,5 мМ. IPTG-индуцированные культуры выращивают при комнатной температуре в течение ночи, после чего клетки собирают центрифугированием при 5000 g в течение 15 мин. После обработки ультразвуком GST-слитый белок очищают от дебриса, используя гранулы глутатион-сефароза согласно рекомендации производителя (Amersham PharmaciaBiotech). Избыток глутатиона удаляют в течение ночи путем диализа при 4 С. Чистоту рецептора определяют визуально с помощью SDS-PAGE и содержание белка определяют методом Bradford'а. Аликвоты рецептора хранят при -80 С до употребления. В табл. 1 приведены данные по аффинности и функциональной активности для некоторых соединений по настоящему изобретению.: Ki500 нМ, : 500 нМ Ki 1500 нМ, + : Ki 1500 нМ Дополнительные объекты, преимущества и признаки новизны настоящего изобретения отчасти приведены в описании, отчасти станут очевидными для специалиста в данной области при изучении описания или могут быть обнаружены при практическом применении изобретения. Настоящее изобретение дополнительно иллюстрируется следующими примерами. Примеры приведены исключительно с целью иллюстрации и не рассматриваются в качестве ограничивающих объем настоящего изобретения. Номенклатура различных соединений, используемых в настоящем документе, базируется на программном обеспечении AUTONOM (Automatic Nomenclature) от Beilstein Institute, где использована систематическая номенклатура ИЮПАК. Спектр ЖХ-МС получен с применением следующего хроматографического оборудования: HewlettPackard, модель 1100, снабженный селективным детектором массы, модель 1100 VL, автоматической пипеткой, ChemStation software и лазерным принтером (метод масс-спектрометрической ионизации: ионизация при атмосферном давлении с детектированием положительных ионов), и используются следующие хроматографические способы. Способ А: Колонка Kromasil 100 С 18, 404,0 мм, 3,5 мкм, скорость потока: 0,7 мл/мин, элюент: АUNITY-300 МГц, и химические сдвиги выражают через м.д.относительно внутреннего эталона TMS. Масс-спектр получают, используя масс-спектрометр Agilent 1100 VL. В примерах использованы следующие обозначения:TMS: триметилсилан Промежуточные соединения IIIa и IIIb Соединения формул IIIa и IIIb могут быть получены по методикам, аналогичным описанным в Cobbrt: 7,357, МС [М+1]+: 376. Промежуточные соединения XIII Соединения формулы XIII, приведенные в табл. 2, получены, исходя из фенола III и производного амина формулы XIVa или XIVb по одной из приведенных ниже методик A-D. Методика А: 0,5 М суспензию фенола III (1 экв) в EtOAc, содержащем безводный карбонат калия (3 экв.) и соединение XIVa (1,3 экв.) при температуре кипения с обратным холодильником в течение 18 ч. Затем суспензии дают охладиться, и белый твердый продукт отделяют фильтрованием. Растворитель отгоняют при пониженном давлении, и полученный остаток очищают колоночной хроматографией. Методика В: 0,5 М суспензию фенола III (1 экв.) в безводном ДМФА, содержащем карбонат цезия(3 экв.), соединение XIVa (1,3 зкв.) и иодид калия (каталитическое количество) нагревают при 80 С в течение 18 ч. Затем суспензии дают охладиться до комнатной температуры и обрабатывают водой иEtOAc. Органический слой трижды промывают насыщенным раствором соли, сушат над безводным сульфатом натрия и фильтруют. Растворитель отгоняют при пониженном давлении, и полученный остаток очищают колоночной хроматографией. Методика С: К 0,1 М раствору фенола III (1 экв.) в безводном ДМФА, содержащем каталитическое количество иодида калия, добавляют гидрид натрия (60%, 1,1 экв.). Полученную суспензию перемешивают при комнатной температуре в течение 1 ч и затем добавляют соединение XIVa (1,1 экв.). Реакционную смесь перемешивают при 80 С в течение 18 ч и затем дают охладиться до комнатной температуры. После обработки водой и EtOAc органический слой трижды промывают насыщенным раствором соли,сушат над безводным сульфатом натрия и фильтруют. Растворитель отгоняют при пониженном давлении, и полученный остаток очищают колоночной хроматографией. Методика D: К 0,2 М раствору фенола III (1 экв.) в ТГФ, содержащем соединение XIVb (2,2 экв.) и трифенилфосфин (2,2 экв.), добавляют в инертной атмосфере DEAD (2,2 экв.). Раствор перемешивают при комнатной температуре 18 ч. Затем растворитель отгоняют при пониженном давлении и полученный остаток очищают колоночной хроматографией. Промежуточные соединения V Соединения формулы V, приведенные в табл. 3, получены, исходя из фенола III и производного амина формулы XVa по одной из приведенных выше методик А-С или, альтернативно, исходя из соединения XIII с использованием приведенных ниже методик E-F. Методика Е: К 0,1 М раствору соединения XIII (1 экв.) (PG = трифторацетил) в смеси ТГФ:метанол(3:1) добавляют 1 М водный раствор гидроксида лития (5 экв.). Раствор перемешивают в течение 18 ч при комнатной температуре, затем разбавляют смесью вода/EtOAc, после чего подкисливают до рН 5 с помощью 1 н HCl. Органический слой сушат над безводным сульфатом натрия и фильтруют. Растворитель отгоняют при пониженном давлении, и полученный остаток повторно растворяют в метаноле, что приводит к 0,1 М раствору, который обрабатывают тионилхлоридом (3,2 экв.). Раствор нагревают до температуры кипения в течение 18 ч и затем дают охладиться до комнатной температуры. Растворитель- 15013227 отгоняют при пониженном давлении. Полученный остаток очищают колоночной хроматографией. Методика F: К 0,1 М раствору соединения XIII (PG = 2-нитробензолсульфонил, 1 экв.) в ДМФА,содержащем тиофенол (1 экв.), добавляют KOtBu (2 экв.). Раствор перемешивают при комнатной температуре в течение 6 ч и затем разбавляют смесью вода/EtOAc. Органический слой трижды промывают насыщенным раствором соли, сушат над безводным сульфатом натрия и фильтруют. Растворитель отгоняют при пониженном давлении, и полученный остаток очищают колоночной хроматографией. Таблица 3 Промежуточные соединения II Соединения формулы II, приведенные в табл. 4, получены, исходя из фенола III и соединения формулы IVa или IVb по одной из приведенных выше методик A-D. Таблица 4
МПК / Метки
МПК: C07D 307/54, A61P 3/04, A61K 31/4406, C07C 233/69, C07C 233/88, A61K 31/198, A61P 3/10, C07D 213/56, C07C 229/36, A61K 31/341, C07C 233/20
Метки: качестве, ppar&gamma, тирозиновые, производные, модуляторов
Код ссылки
<a href="https://eas.patents.su/30-13227-tirozinovye-proizvodnye-v-kachestve-modulyatorov-ppargamma.html" rel="bookmark" title="База патентов Евразийского Союза">Тирозиновые производные в качестве модуляторов pparγ</a>
Предыдущий патент: Гербицидные смеси
Случайный патент: Портативное устройство связи, система и способ связи между локальным терминалом и множеством портативных устройств