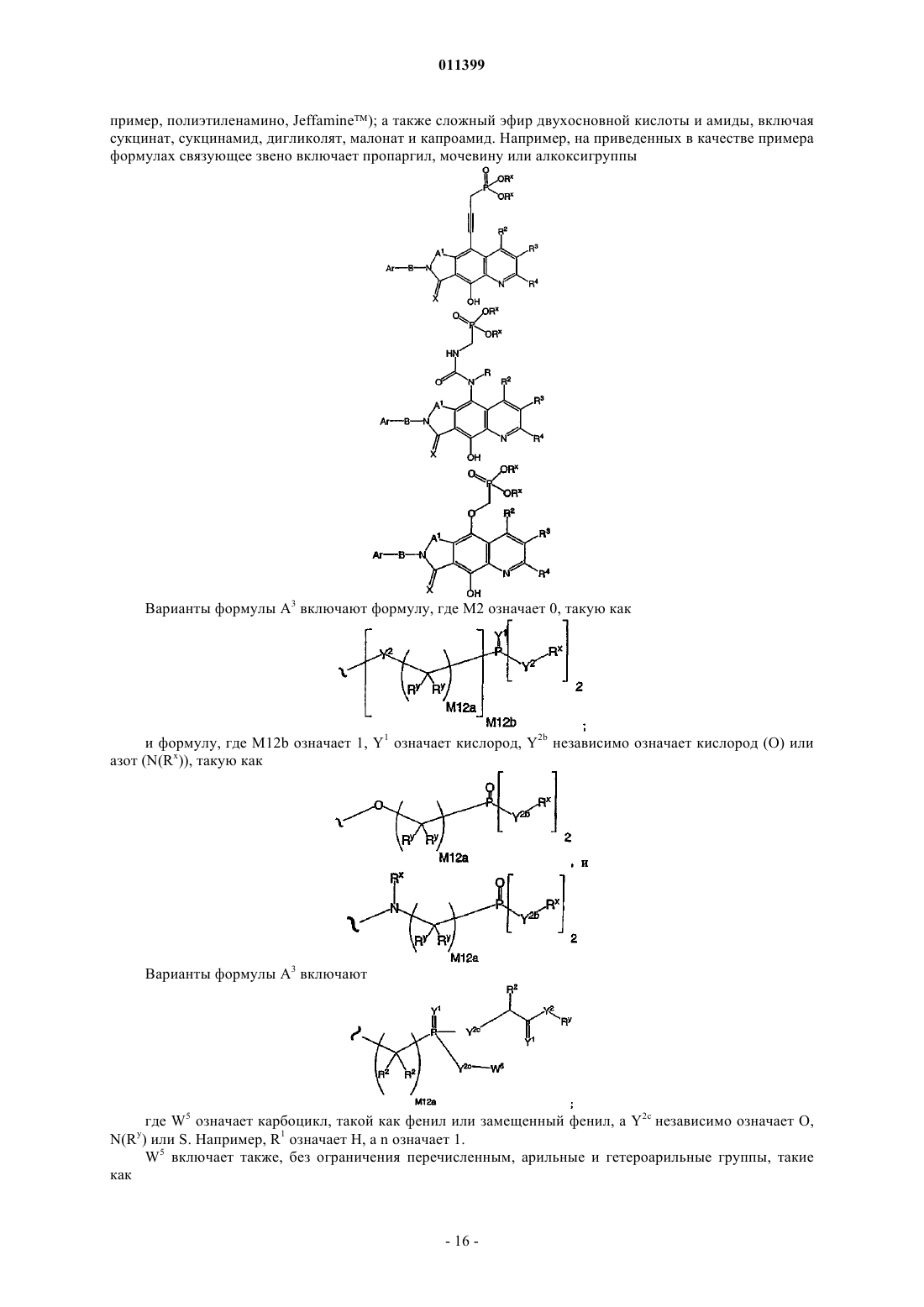
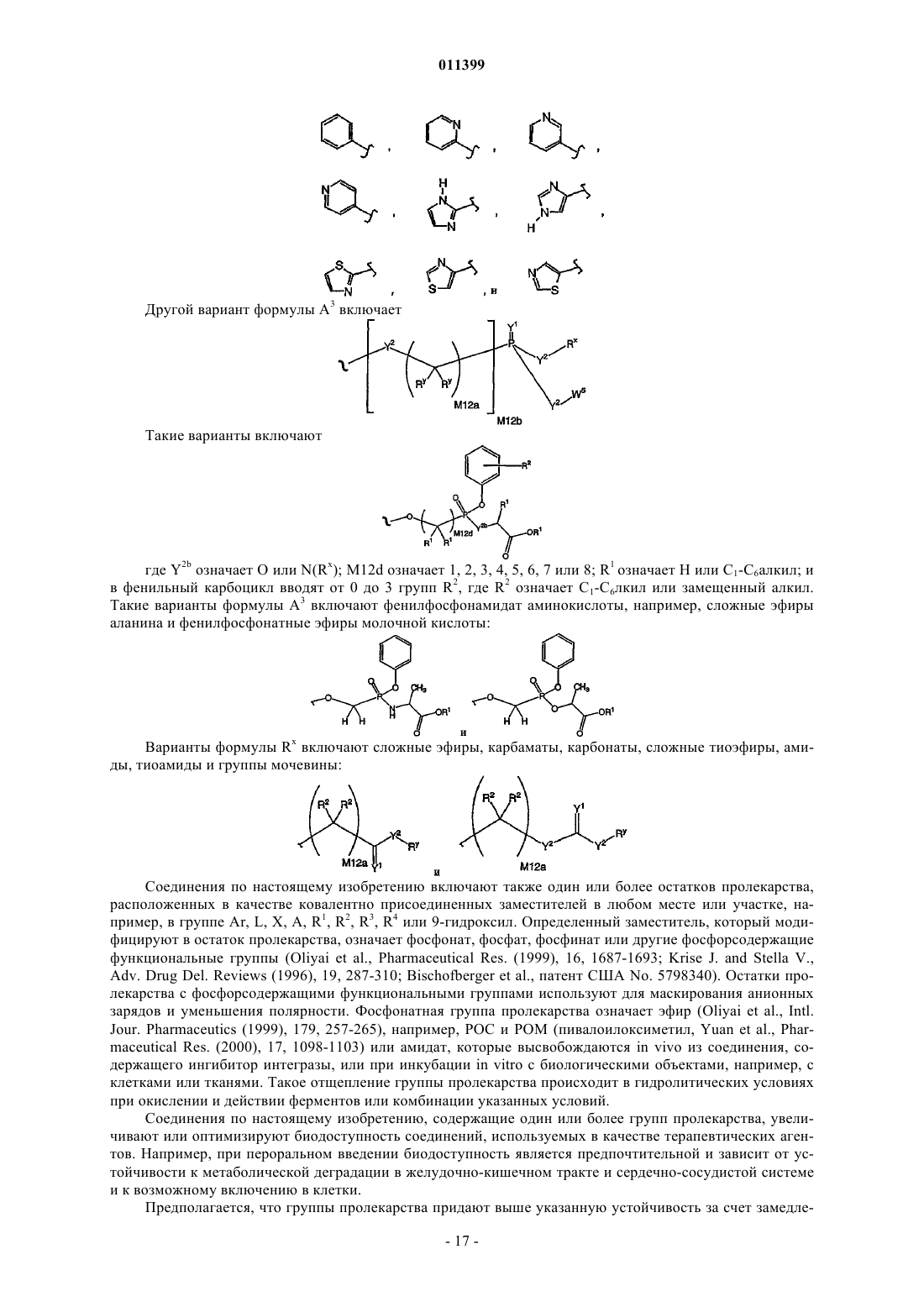
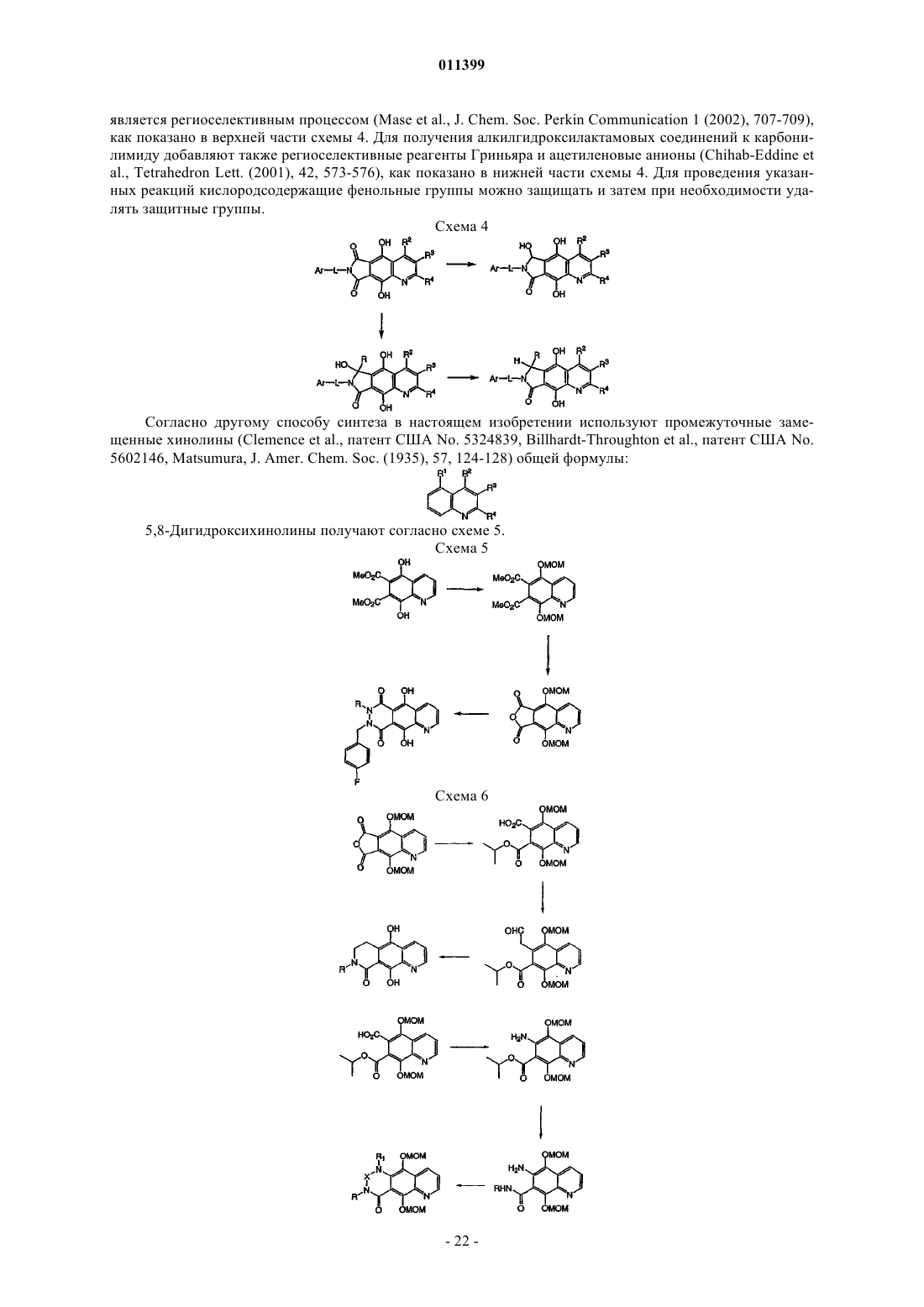
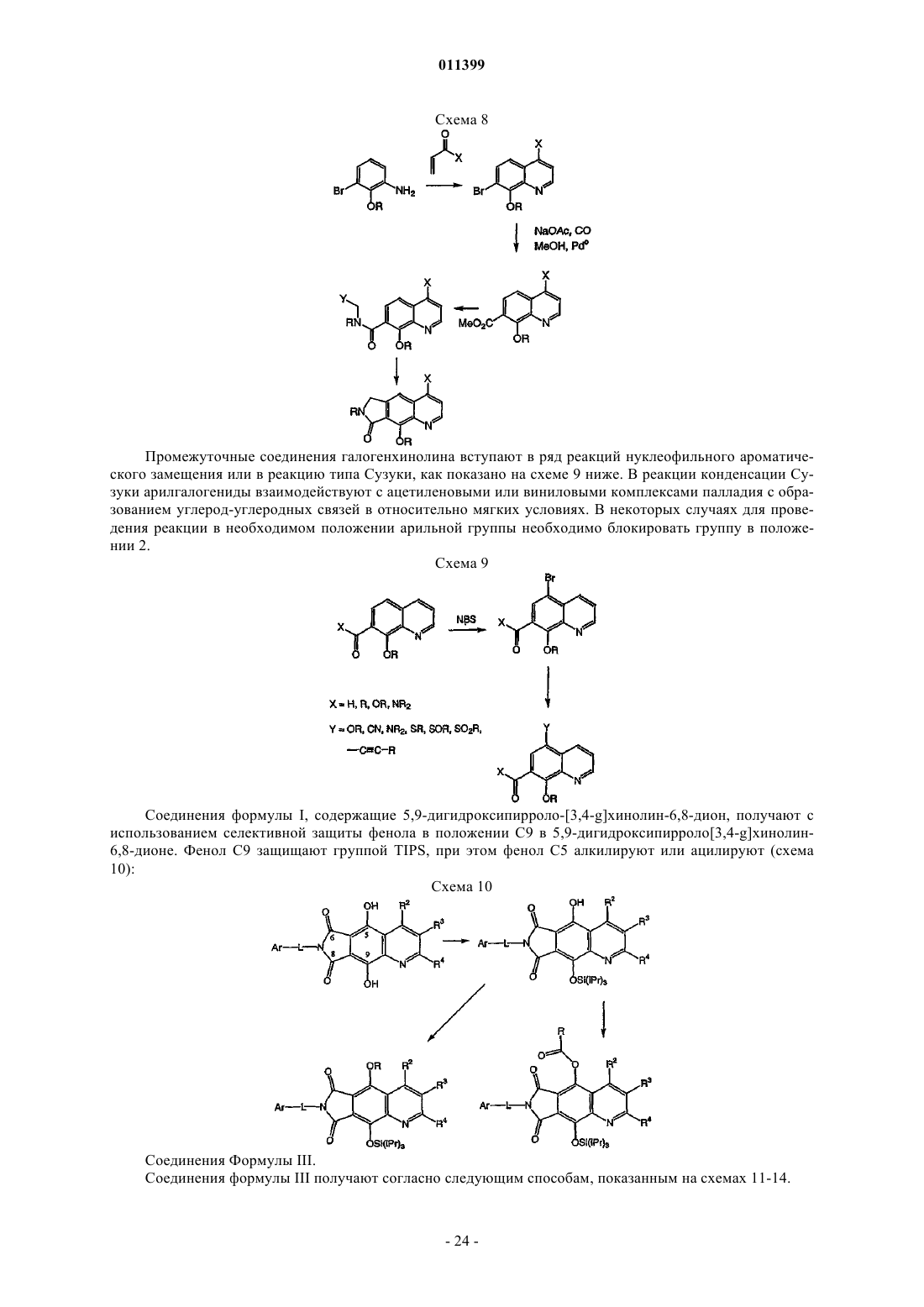
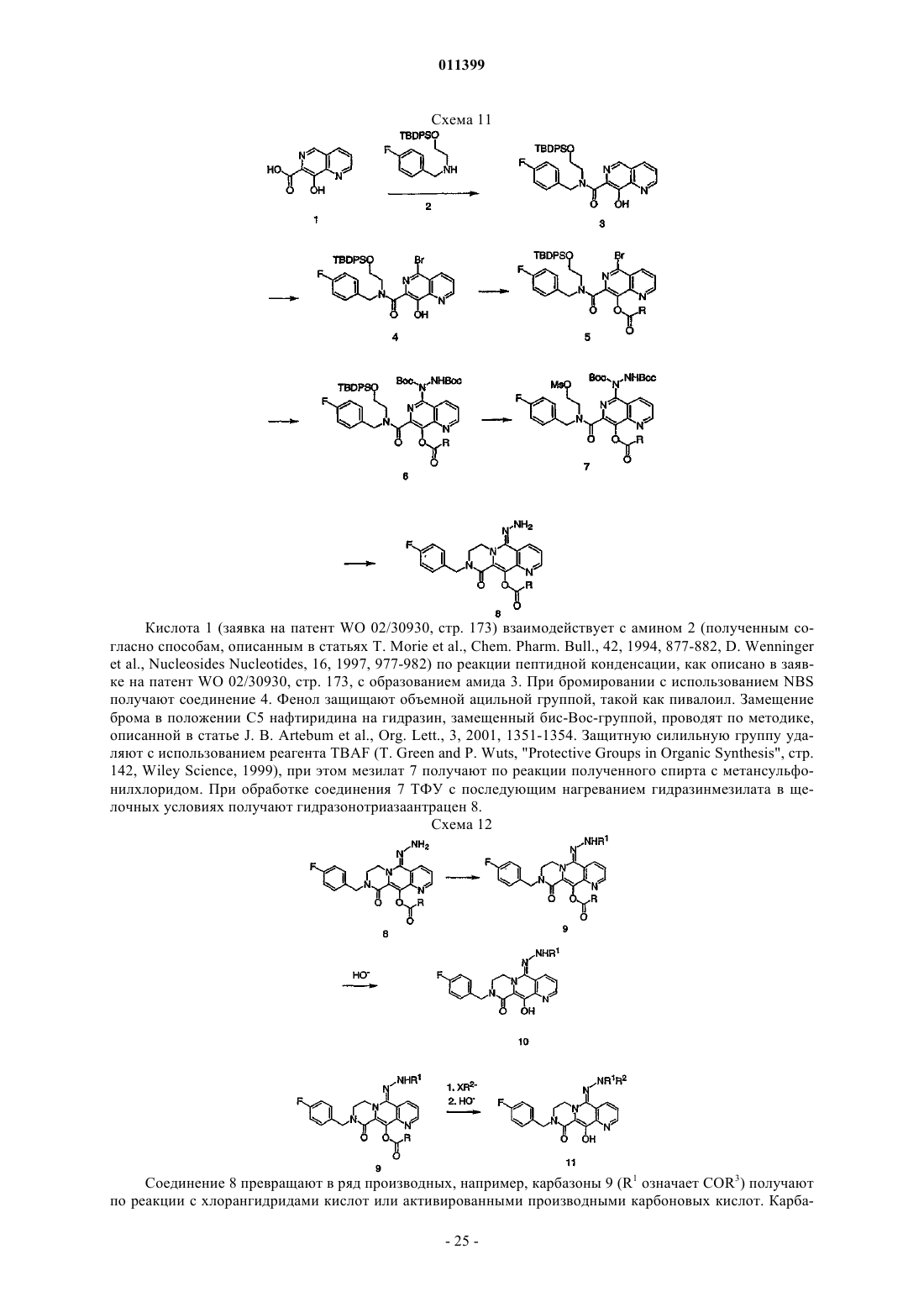
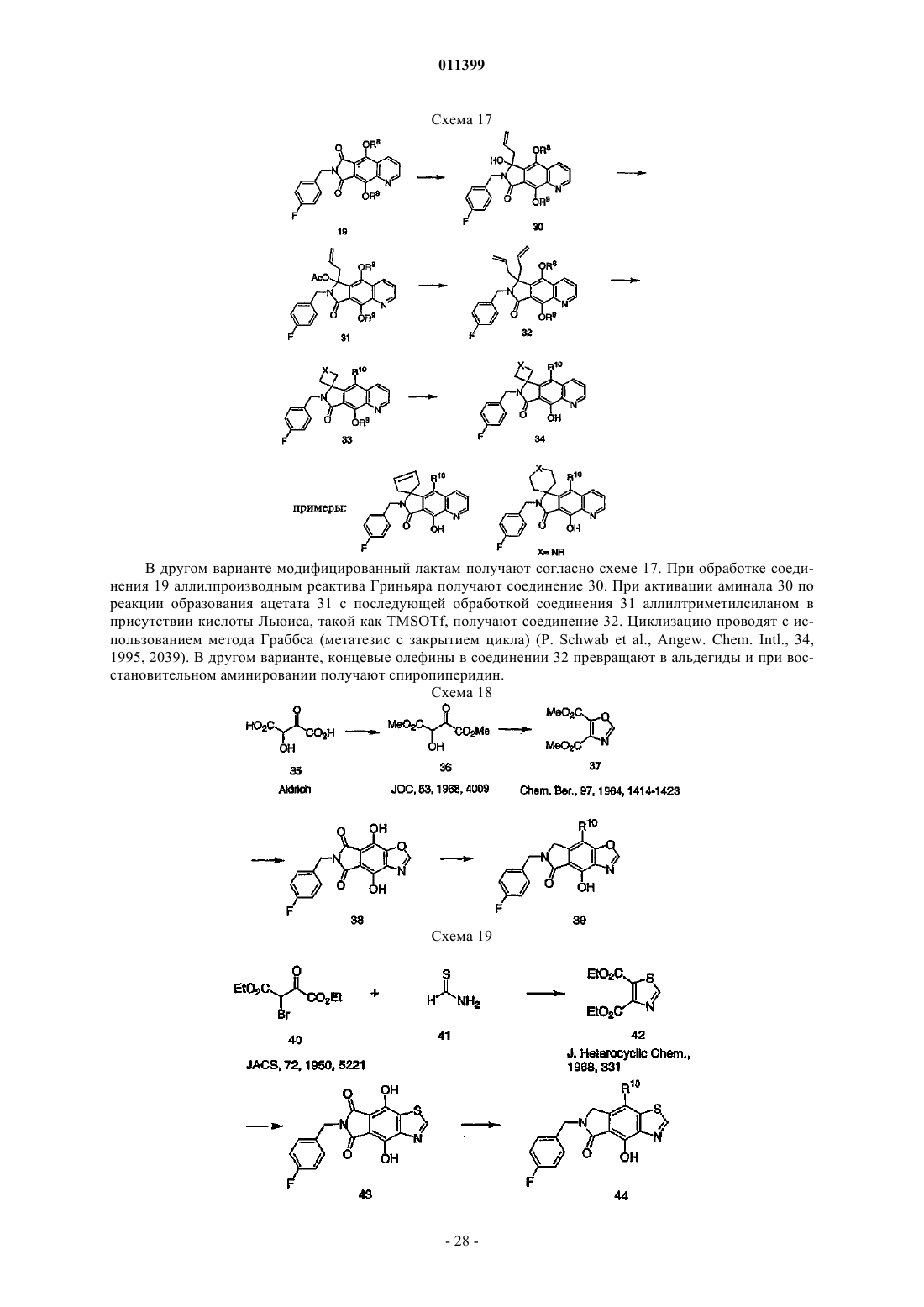
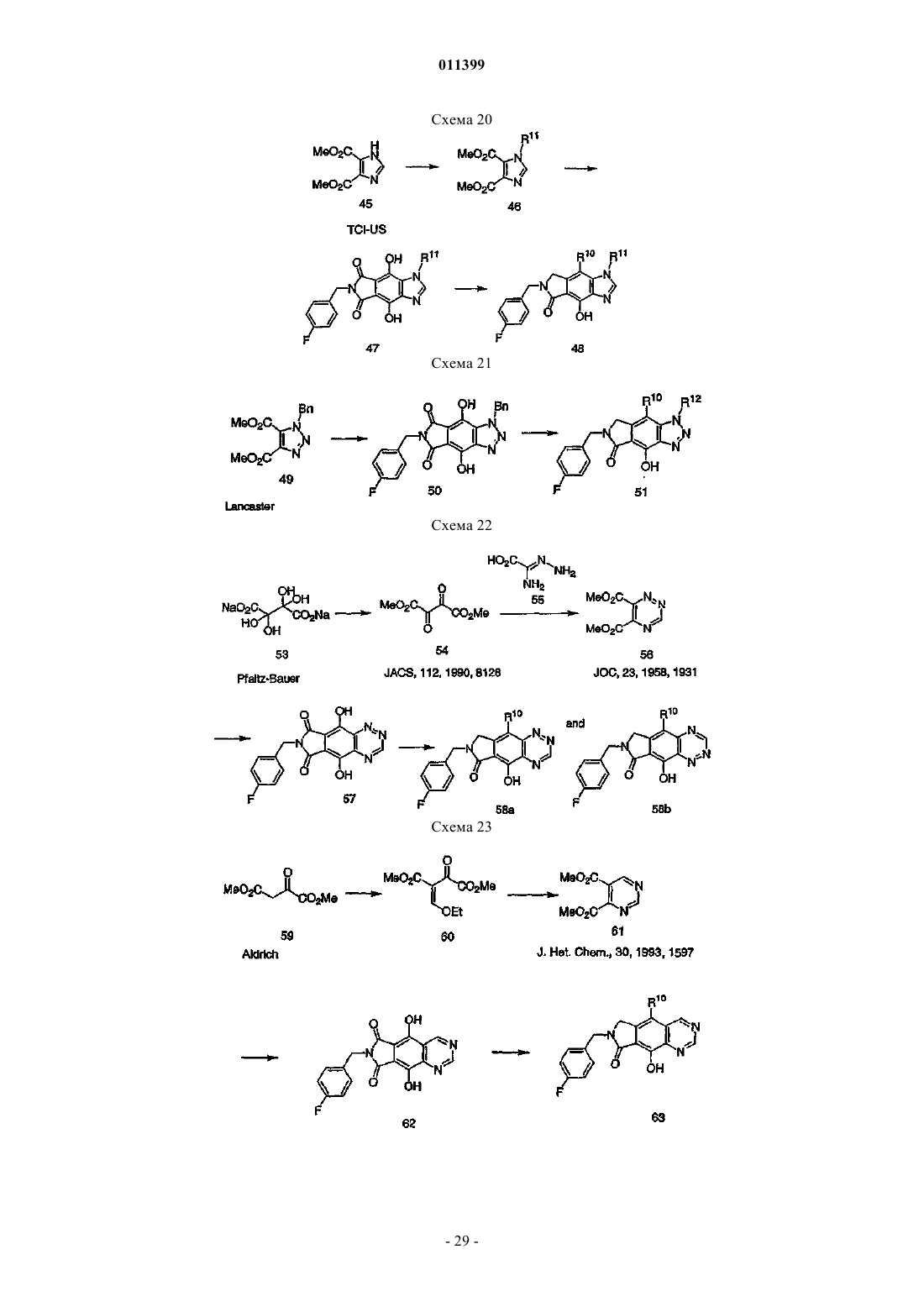
Трициклические соединения – ингибиторы интегразы вич, способ их получения (варианты), фармацевтическая композиция на их основе, способ ее получения и способы их использования в лечении болезней
Номер патента: 11399
Опубликовано: 27.02.2009
Авторы: Ким Чанг Ю., Чен Джеймс М., Чен Сяову, Шахерер Лаура Н., Джин Хаолун, Фардис Мерайя
Формула / Реферат
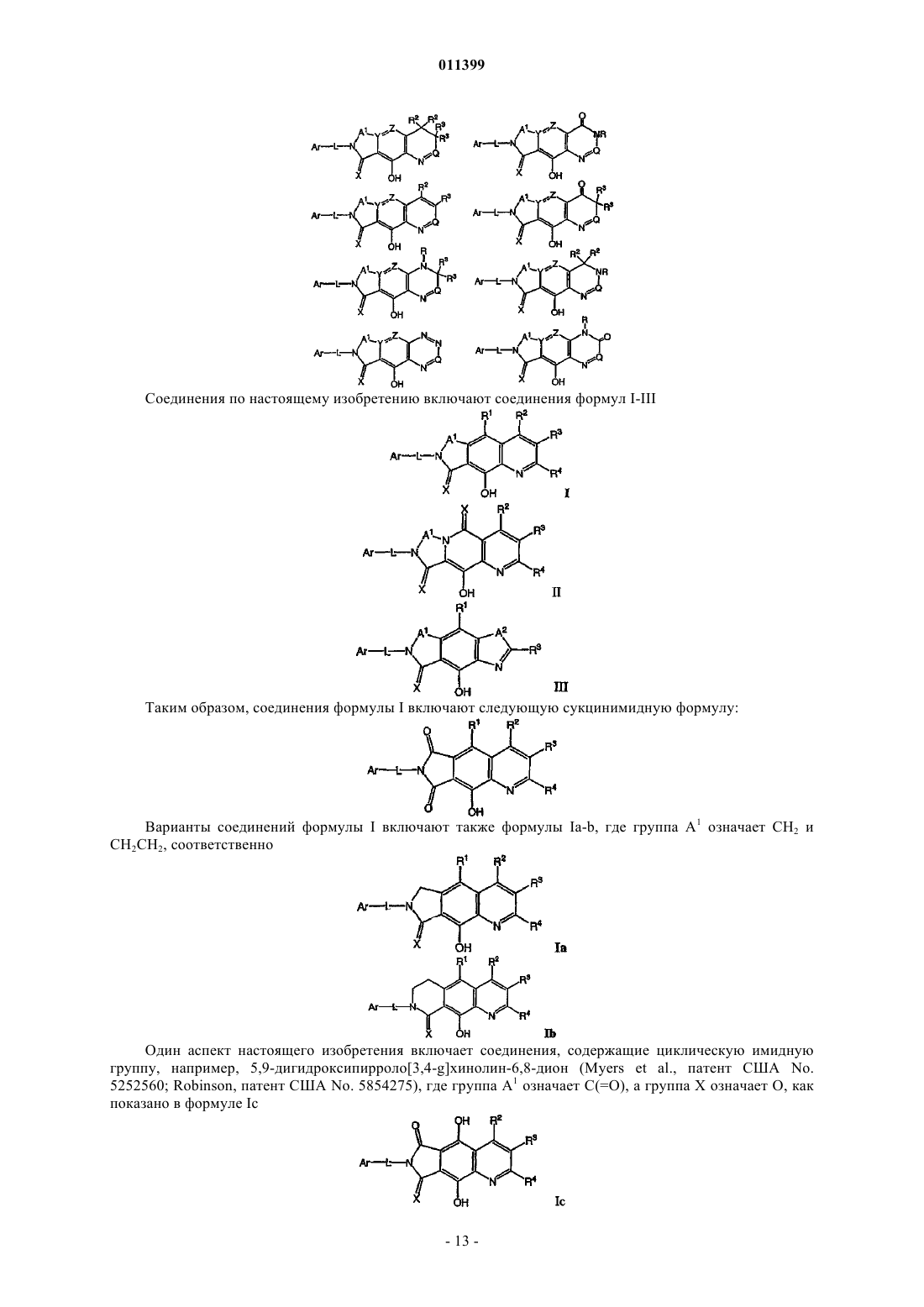
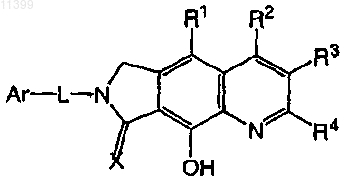
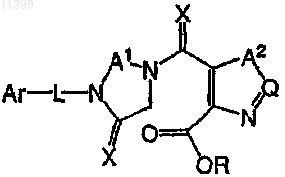
1. Соединение формулы
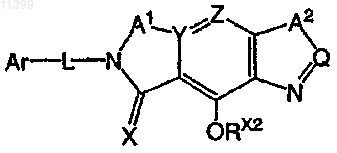
где
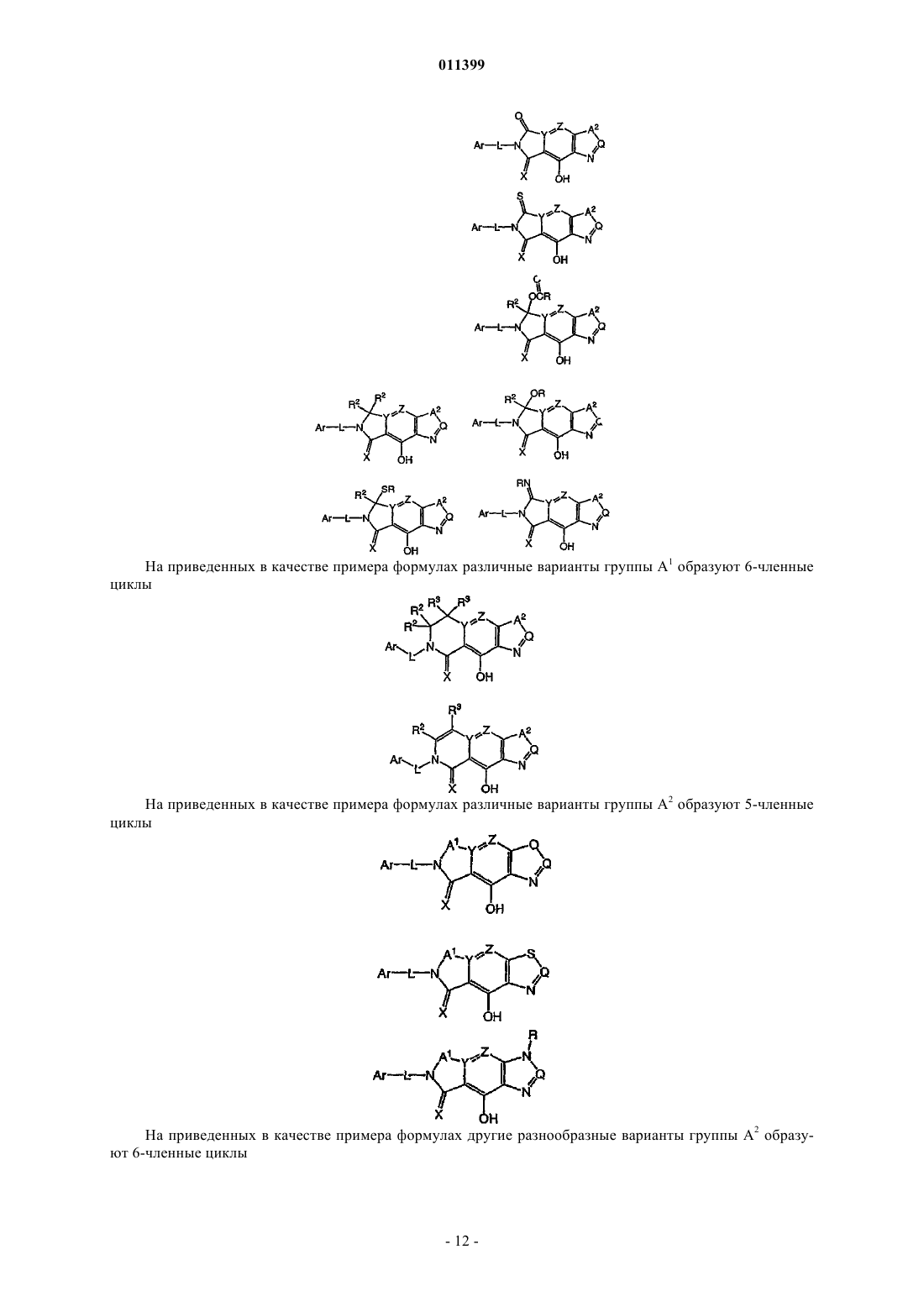
А1 независимо выбирают из ряда: C(R2)2, CR2OR, CR2OC(=O)R, C(=O), C(=S), CR2SR, C(=NR);
А2 независимо выбирают из ряда: О, S, NR, C(R2)2-C(R3)2, C(R2)=C(R3), C(=O)C(R3)2, NR-C(R3)2, N=C(R3), N=N или C(R2)=N;
Q означает N или CR4;
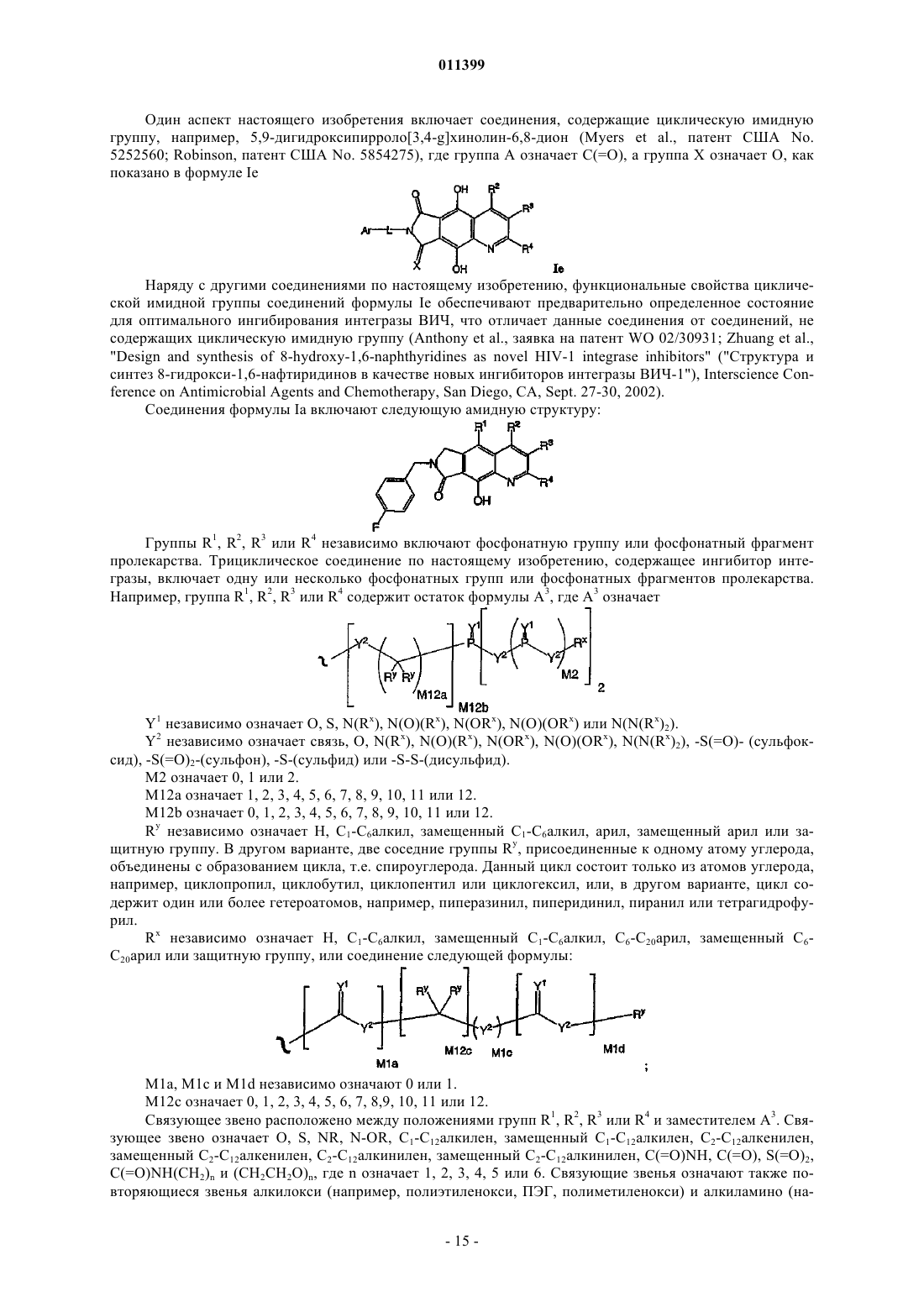
L выбирают из ряда: связь, О, S, S-S, S(=O), S(=O)2, S(=O)2NR, NR, N-OR, C1-С12алкилен, замещенный C1-C12алкилен, С2-С12алкенилен, замещенный С2-С12алкенилен, С2-С12алкинилен, замещенный С2-С12 алкинилен, C(=O)NH, OC(=O)NH, NHC(=O)NH, С(=O), C(=O)NH(CH2)n или (CH2CH2O)n, где n означает 1, 2, 3, 4, 5 или 6;
X выбирают из ряда: О, S, NH, NR, N-OR, N-NR2, N-CR2OR и N-CR2NR2;
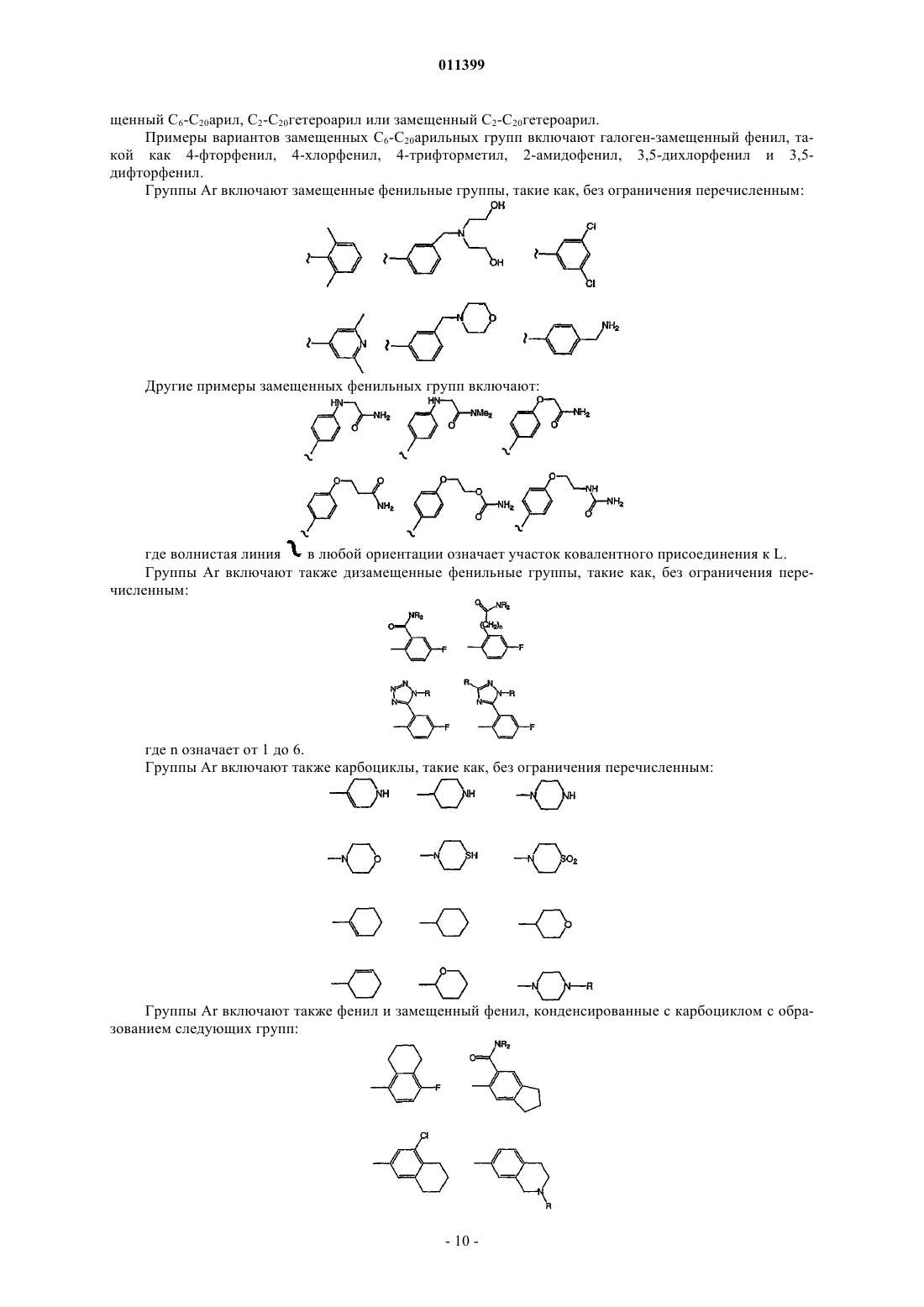
Ar выбирают из ряда: С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, или насыщенного, ненасыщенного или ароматического цикла или циклической системы, включающей моно- или бициклический карбоцикл или гетероцикл, содержащий от 3 до 12 циклических атомов;
каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2,
-NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, С1-С8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8алкокси, C1-C8трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20 арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства; две группы R2 или две группы R3, присоединенные к одному атому углерода, могут быть объединены с образованием спироцикла;
R1 независимо выбирают из ряда: CR3, NRSO2R, OC(=O)NR2, OC(=O)R, SR, H, F, Cl, Br, I, OH, -NH2, -NH3+, -NHR, -NR2, -NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-C8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8алкокси, C1-C8 трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства;
R независимо выбирают из ряда: Н, C1-C8алкил, замещенный C1-C8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства;
Rx2 независимо выбирают из ряда: Н, C1-C8алкил, замещенный C1-C8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат, остаток пролекарства и защитная группа;
причем замещенный алкилен, замещенный алкенилен, замещенный алкинилен, замещенный арил и замещенный гетероарил независимо друг от друга замещены по меньшей мере одним заместителем, выбранным из группы, включающей F, Cl, Br, I, ОН, амино (-NH2), аммоний (-NH3+), алкиламино, диалкиламино, триалкиламмоний, C1-C8алкил, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-C8алкилгидроксил, C1-C8алкилтиол, алкилсульфон (-SO2R), арилсульфон (-SO2Ar), арилсульфоксид (-SOAr), арилтио (-SAr), сульфонамид (-SO2NR2), алкилсульфоксид (-SOR), сложный эфир (-CO2R), амидо (-C(=O)NR2), 5-7-членный циклический лактам, 5-7-членный циклический лактон, нитрил (-CN), азидо (-N3), нитро (-NO2), C1-С8алкокси (-OR), C1-C8алкил, замещенный С1-С8алкил, С6-С20 арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, фосфонат, фосфат, полиэтиленокси и остаток пролекарства;
при этом, остаток пролекарства независимо выбран из группы, включающей -CH2OC(=O)R9 и
-CH2OC(=O)OR9, где R9 означает C1-C6алкил, замещенный C1-C6алкил, С6-С20арил или замещенный С6-С20арил или выбран из группы, включающей
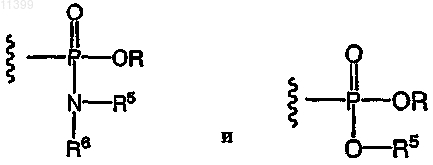
где R5 означает -CR2CO2R7, где R6 и R7 независимо означают Н или C1-С8алкил;
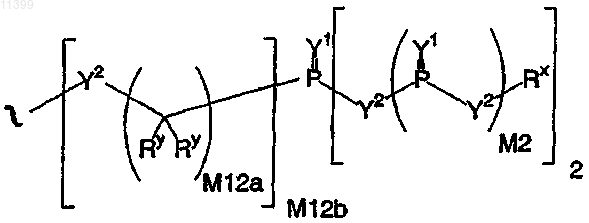
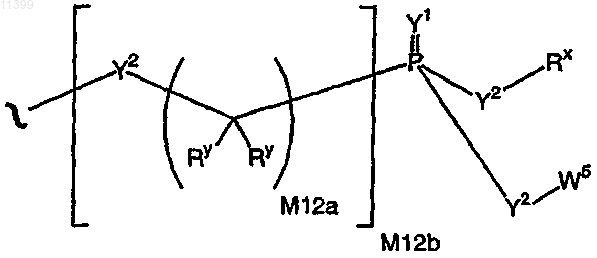
где
Y1 независимо означает О, S, N(Rx), N(O)(Rx), N(ORx), N(O)(ORx) или N(N(Rx)2),
Y2 независимо означает связь, О, N(Rx), N(O)(Rx), N(ORx), N(O)(ORx), N(N(Rx)2), -S(O)- (сульфоксид), -S(O)2- (сульфон), -S- (сульфид) или -S-S- (дисульфид),
M2 означает 0, 1 или 2,
М12а означает 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12,
М12b означает 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12,
Ry независимо означает Н, C1-C6алкил, замещенный С1-С6алкил, С6-С20арил, замещенный С6-С20 арил или защитную группу, или две соседние группы Ry, присоединенные к одному атому углерода, объединены с образованием карбоцикла или гетероцикла и
Rx независимо означает Н, C1-C6алкил, замещенный C1-C6алкил, С6-С20арил, замещенный С6-С20 арил или защитную группу, или следующую структурную формулу:
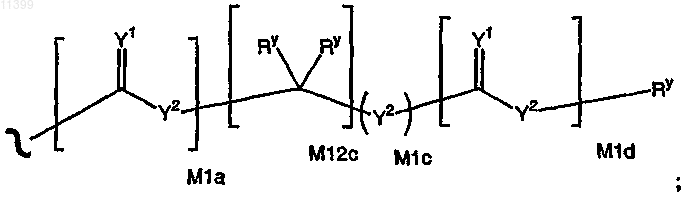
где
М1а, М1c и M1d независимо означают 0 или 1,
М12с означает 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12; и
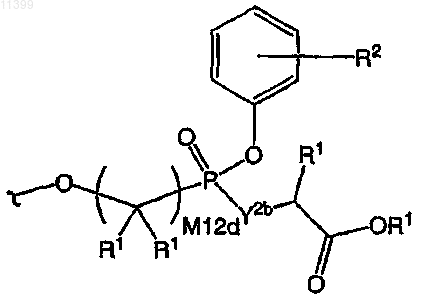
где Y2b означает О или N(Rx), M12d означает 1, 2, 3, 4, 5, 6, 7 или 8, R1 означает Н или C1-C6алкил, а фенильный карбоцикл содержит в качестве заместителей от 0 до 3 групп R2, где R2 означает C1-C6алкил или замещенный алкил; а также таутомеры, соли, сольваты, индивидуальные энантиомеры и их очищенные диастереомеры;
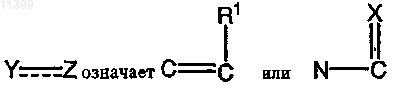
при условии, что, если Y=Z означает С=С(ОН), X означает О, А1 означает С(=O), А2 означает C(R2)=C(R3), и Q означает СН, то L не означает связь.
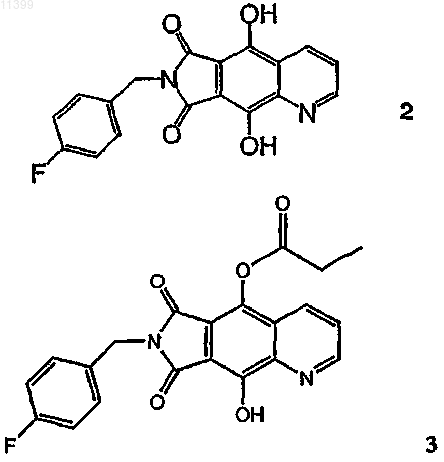
2. Соединение по п.1, которое выбрано из группы, включающей соединения следующих формул:
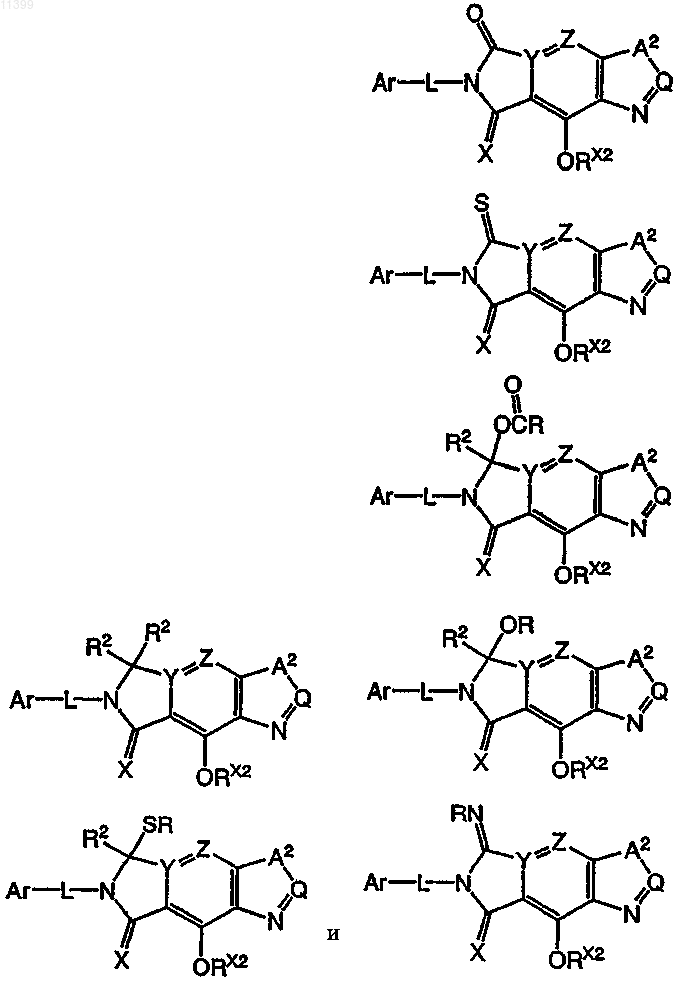
3. Соединение по п.1, которое выбрано из группы, включающей соединения следующих формул:
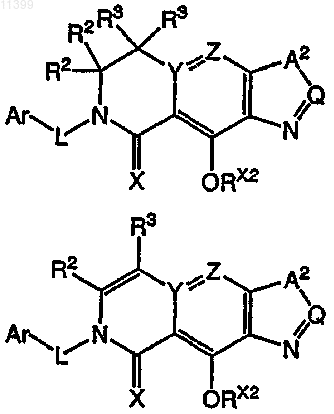
4. Соединение по п.1, в котором R1 выбрано из группы, включающей R, OR, NR2, NHR, NHSO2R и NRSO2R.
5. Соединение по п.1, которое выбрано из группы, включающей соединения следующих формул:

6. Соединение по п.1, которое выбрано из группы, включающей соединения следующих формул:

7. Соединение по п.1, в котором RX2 представляет собой защитную группу, выбранную из группы, включающей бензгидрил (CHPh2), триалкилсилил (R3Si), 2-триметилсилоксиэтил, алкоксиметил (CH2OR) и сложный эфир (C(=O)R).
8. Соединение по п.6 формулы

9. Соединение по п.6 формулы I

в которой RX2 означает Н и X означает О.
10. Соединение по п.6, в котором L не означает связь.
11. Соединение по п.6 формулы III
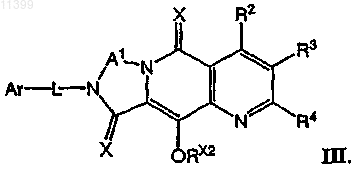
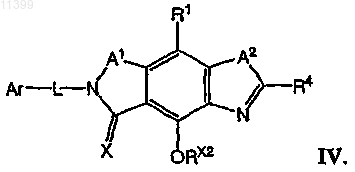
12. Соединение по п.1 формулы IV
13. Соединение по п.1, имеющее по крайней мере одну фосфонатную группу.
14. Соединение по п.1, в котором замещенный алкил, замещенный алкилен, замещенный алкенилен, замещенный алкинилен, замещенный карбоцикл, замещенный арил и замещенный гетероарил независимо замещены одним или более заместителями, которые выбирают из ряда: F, Cl, Br, I, ОН, -NH2, -NH3+,
-NHR, -NR2, -NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-С8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8алкокси, C1-C8трифторалкил, C1-C8алкил, С3-С12карбоцикл, С6-С20арил, С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства.
15. Соединение по п.1, где А1 выбрано из группы, включающей СН2, С(СН3)2, 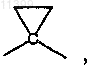 СН2-СН2 или С(СН3)2-СН2.
СН2-СН2 или С(СН3)2-СН2.
16. Соединение по п.9, где X означает О, L означает СН2, а Ar означает замещенный фенил.
17. Соединение по п.16, где Ar означает 4-фторфенил.
18. Соединение по п.9, где X означает О, a R2, R3 и R4 каждый означает Н.
19. Соединение по п.9, где X означает О, А1 означает СН2, a R2, R3 и R4 каждый означает Н.
20. Соединение по п.1, где Ar-L выбрано из группы, включающей следующие формулы:

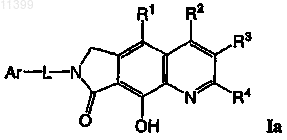
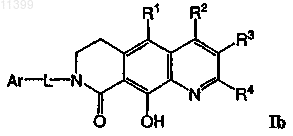
21. Соединение по п.9, имеющее формулу Ia или Ib
22. Соединение по п.9 формулы
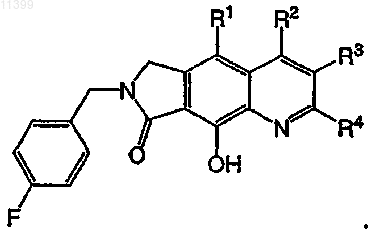
23. Соединение по п.22, которое выбрано из группы, включающий соединения следующих формул:
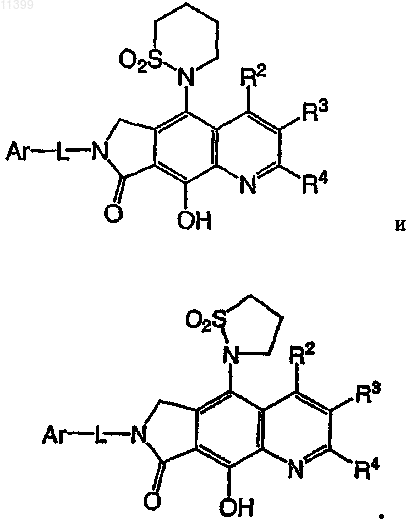
24. Соединение по п.9, в котором Ar-L означает парафторбензил.
25. Соединение по п.9 формулы
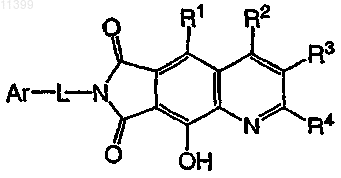
при условии, что если R1 означает ОН, R2, R3 и R4 означают Н, то L не означает связь.
26. Соединение по п.1, где
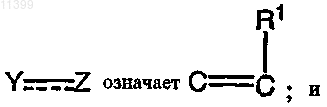
R1 означает CR3, C(=O)NR2, OC(=O)OR, OC(=O)NR2, OC(=O)R, OSO2NR2 (сульфамат), NR2, NRSO2R, SR, S(O)R, SO2R или SO2NR2 (сульфонамид).
27. Соединение по п.26, где по крайней мере один R означает остаток пролекарства.
28. Соединение по п.1, где по крайней мере один из R1, R2, R3 и R4 выбран из группы, включающей следующие формулы:
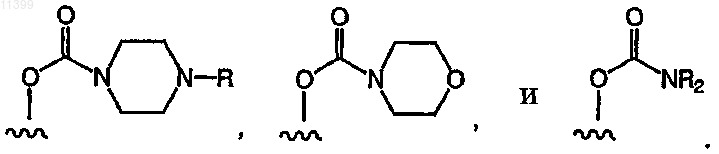
29. Соединение по п.1, где по крайней мере один из R1, R2, R3 и R4 выбран из группы, включающей следующие формулы:
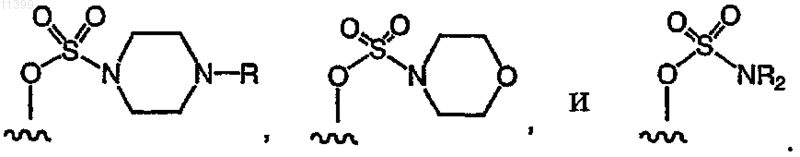
30. Соединение по п.1, где по крайней мере один из R1, R2, R3 и R4 выбран из группы, включающей следующие формулы:
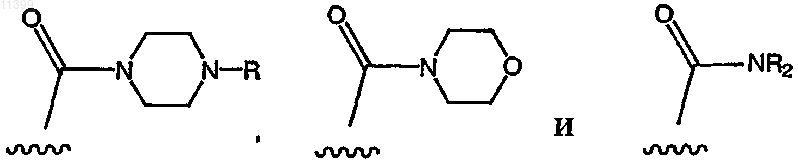
31. Соединение по п.1, где по крайней мере один из R1, R2, R3 и R4 означает лактам, выбранный из группы, включающей следующие формулы
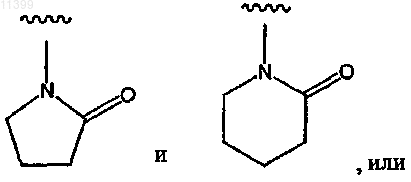
или сультам, выбранный из группы, включающей следующие формулы:
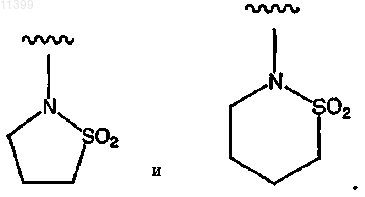
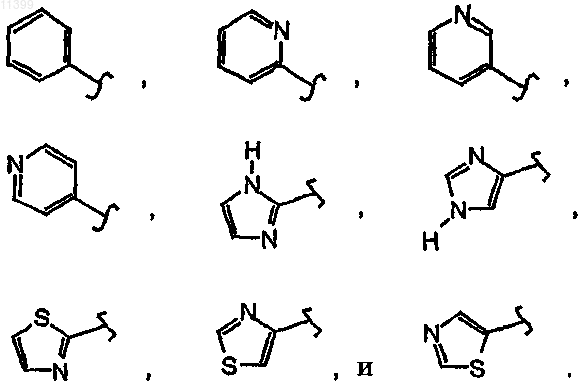
32. Соединение по п.1, где Ar выбрано из группы, включающей следующие формулы:
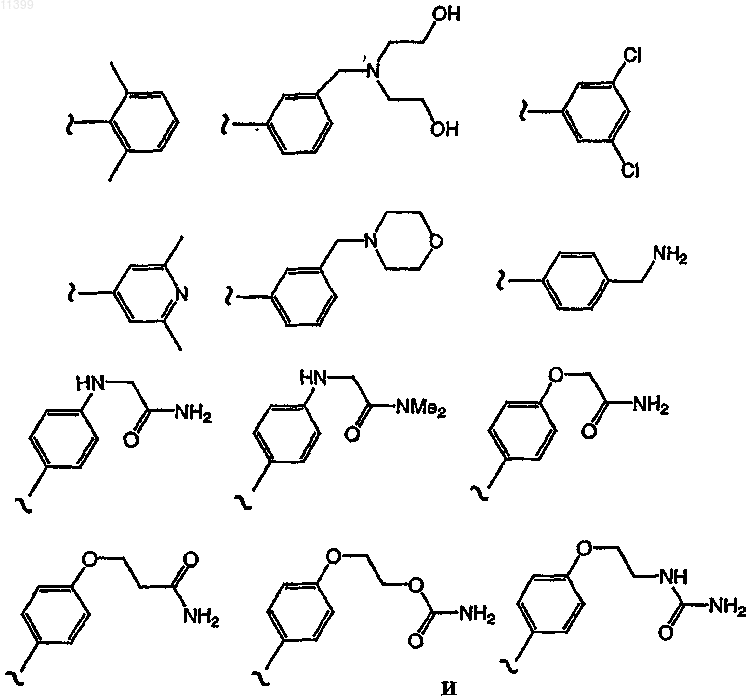
где волнистая линия ![]() указывает участок ковалентного присоединения к заместителю L.
указывает участок ковалентного присоединения к заместителю L.
33. Соединение по п.1, где Ar выбрано из группы, включающей следующие формулы:
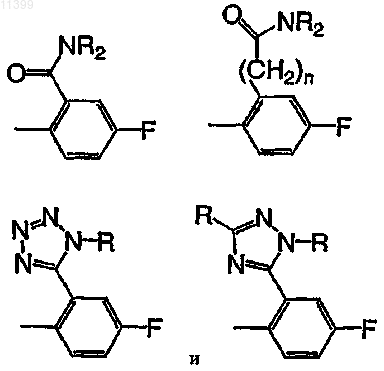
где n равно от 1 до 6.
34. Соединение по п.1, где Ar выбрано из группы, включающей следующие формулы:
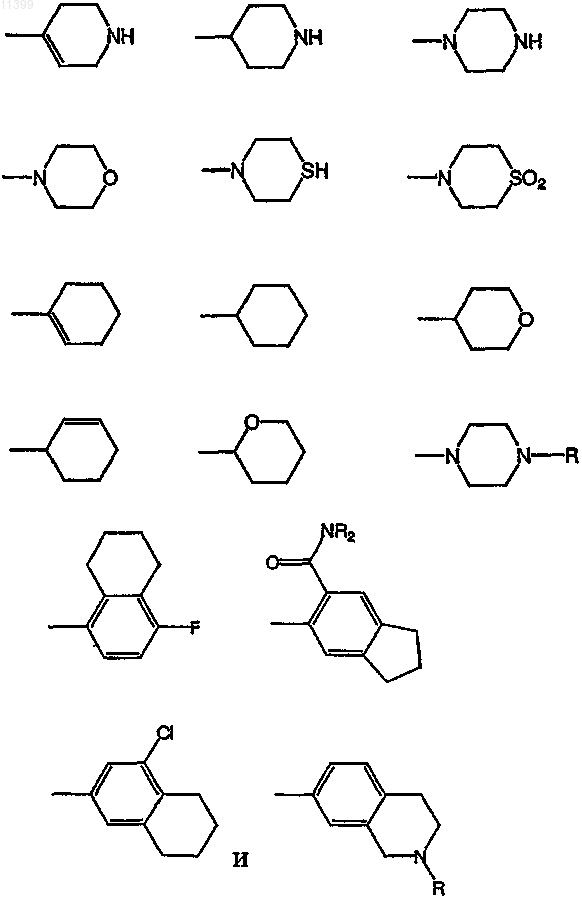
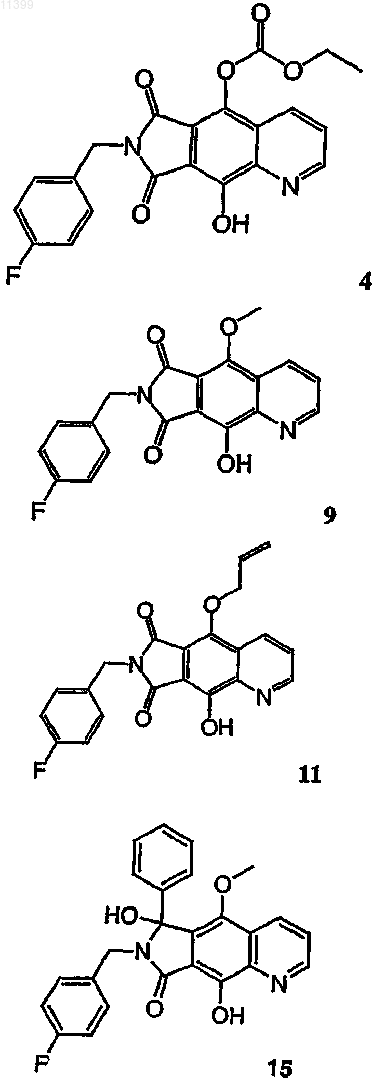
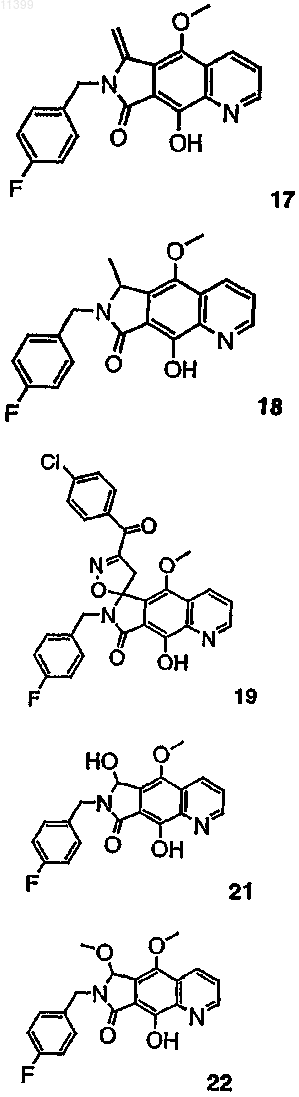
35. Соединение по п.9, выбранное из группы, включающей соединения следующих формул:

36. Соединение по п.11, выбранное из группы, включающей соединения следующих формул:
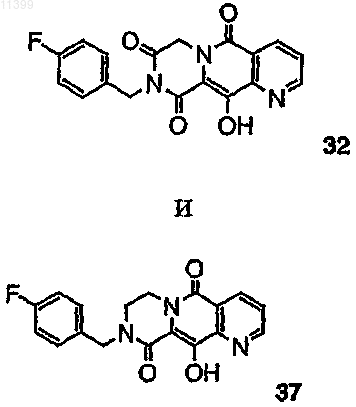
37. Соединение по п.1, выбранное из группы, включающей соединения следующих формул:
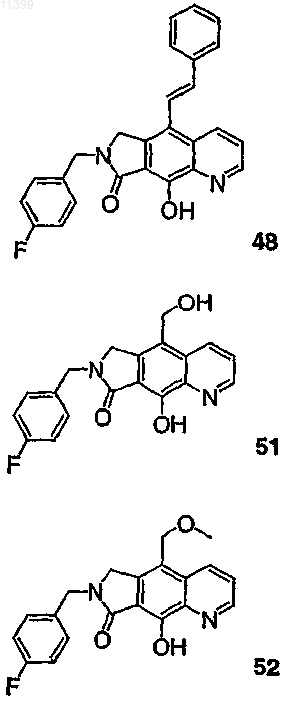
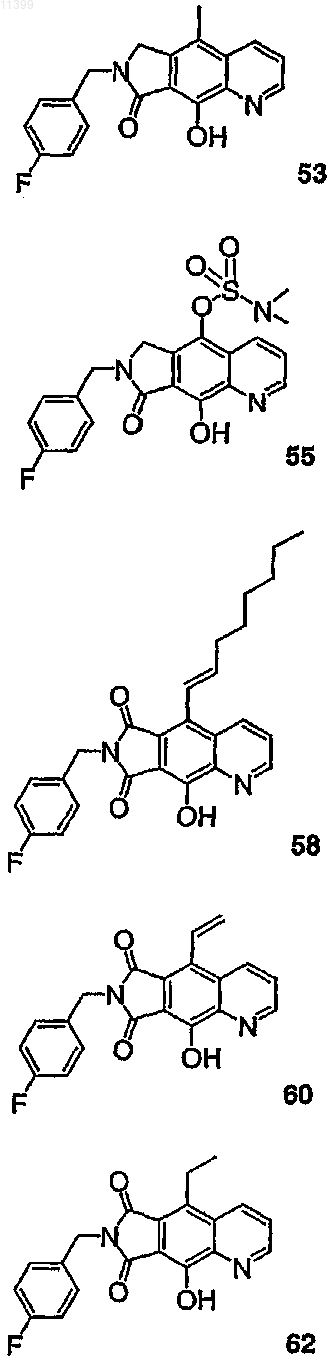
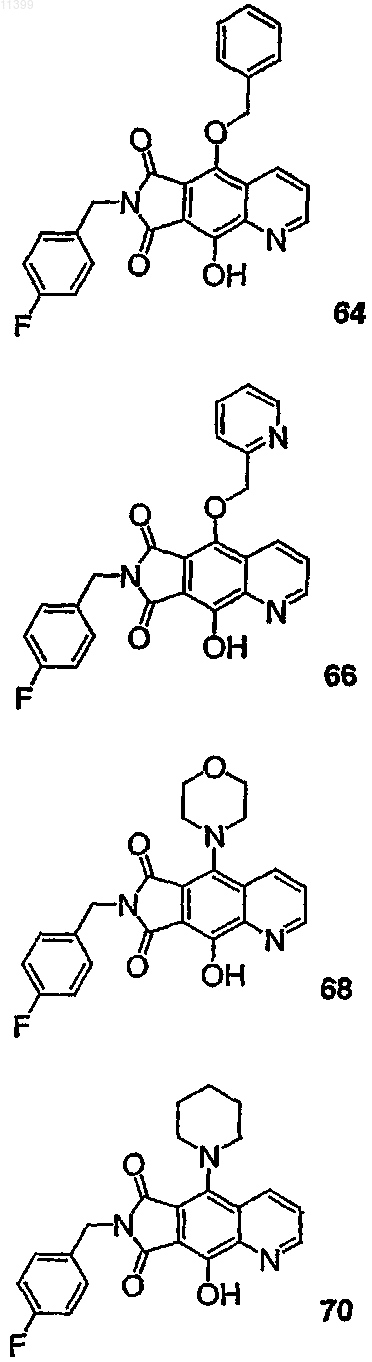
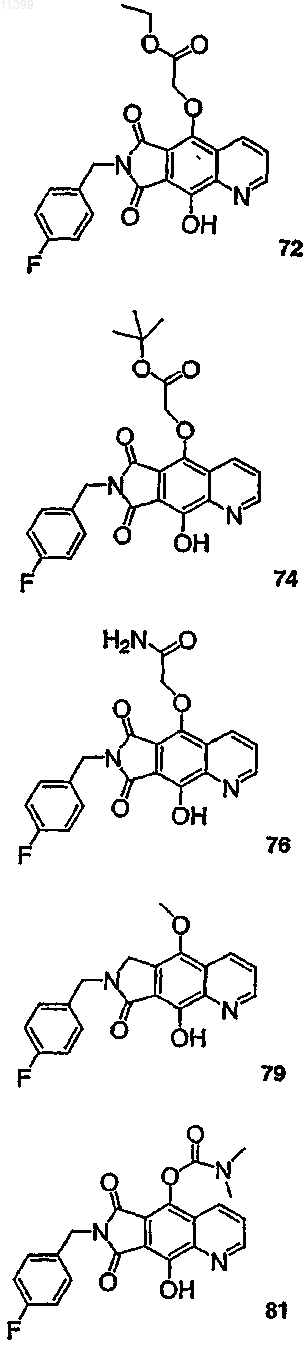
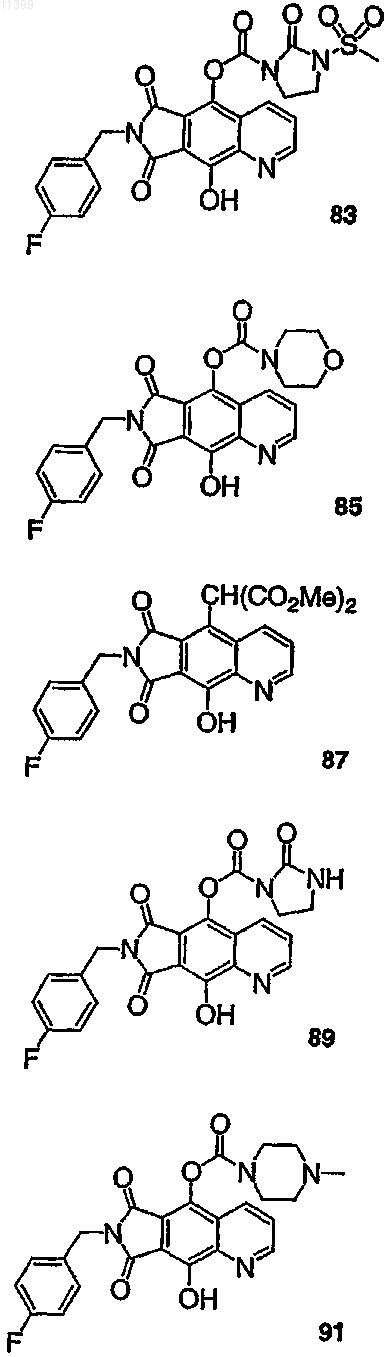
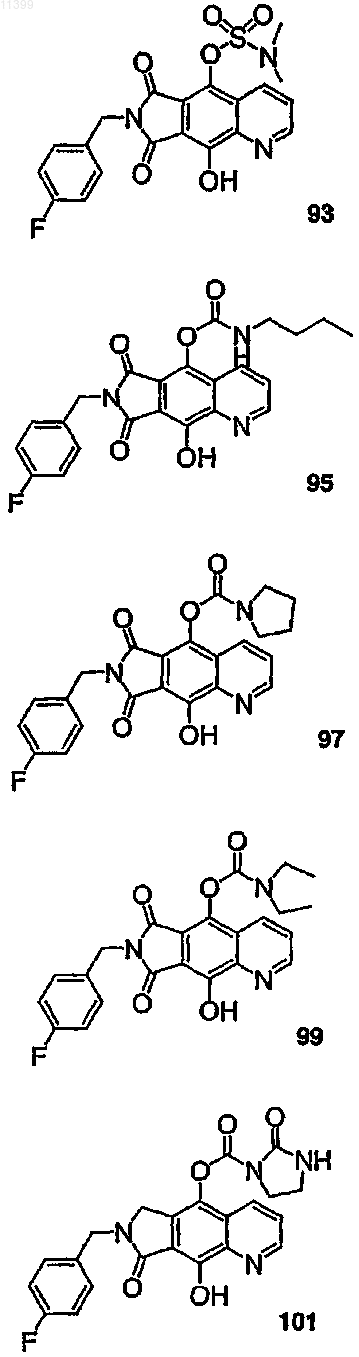
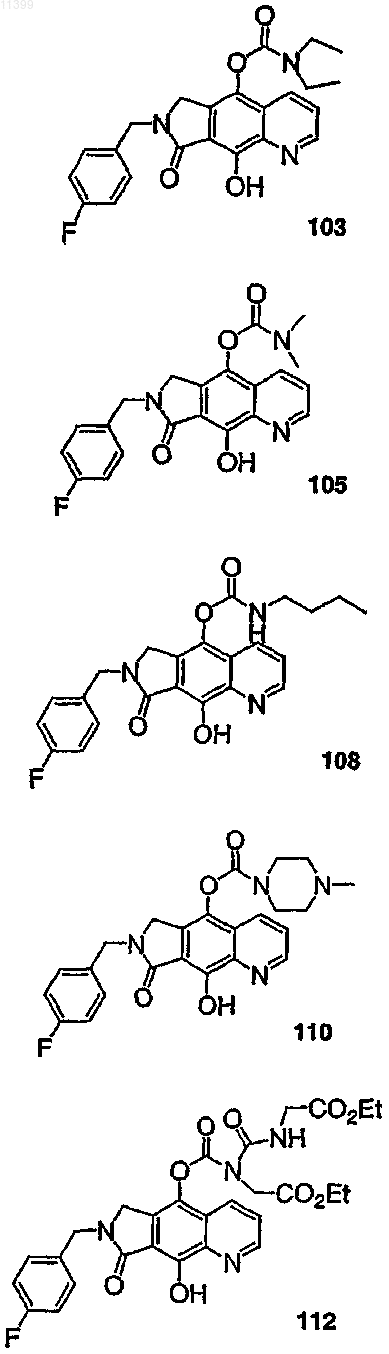
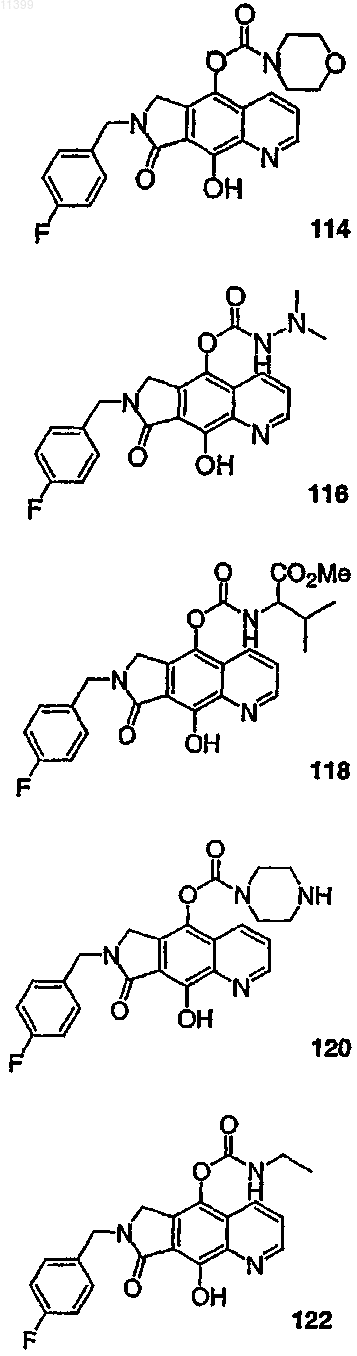
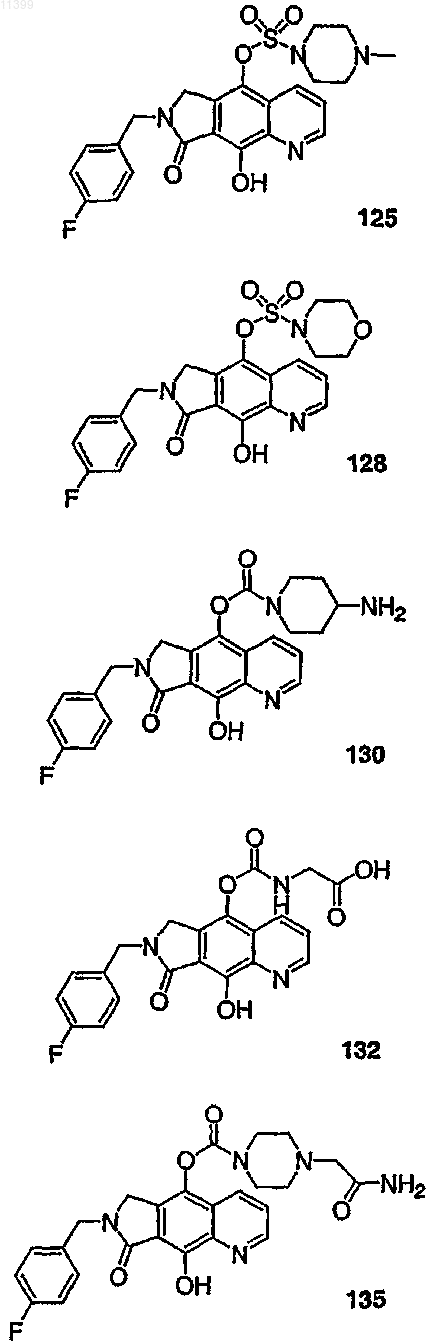
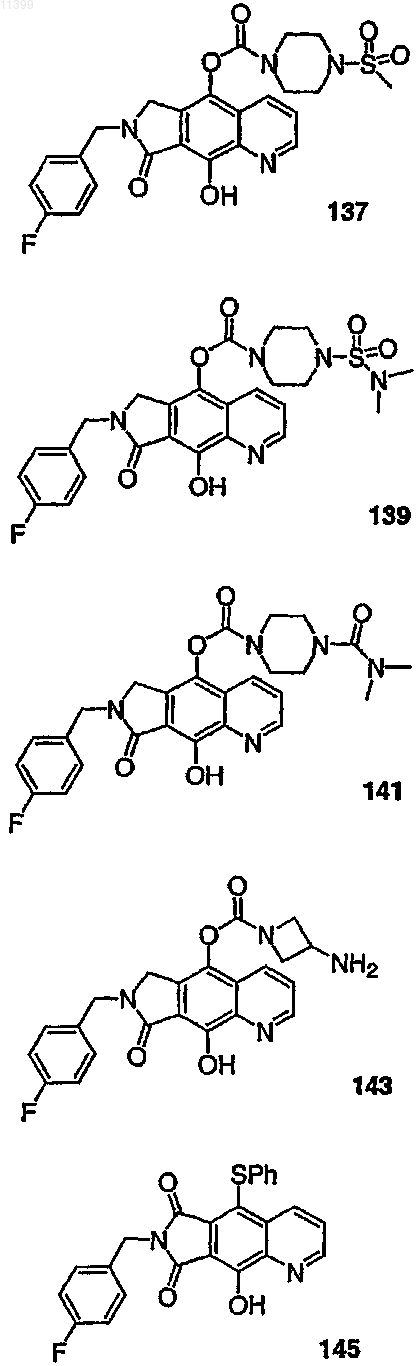
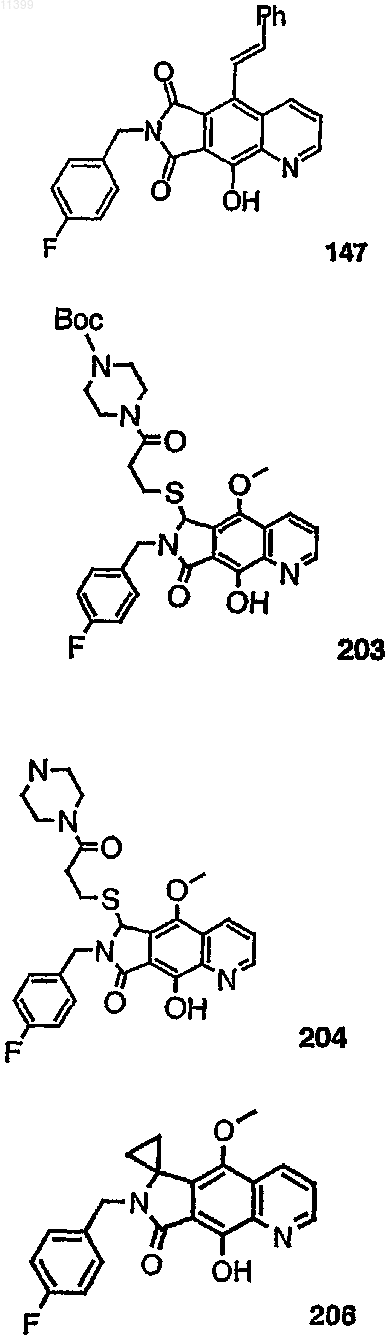
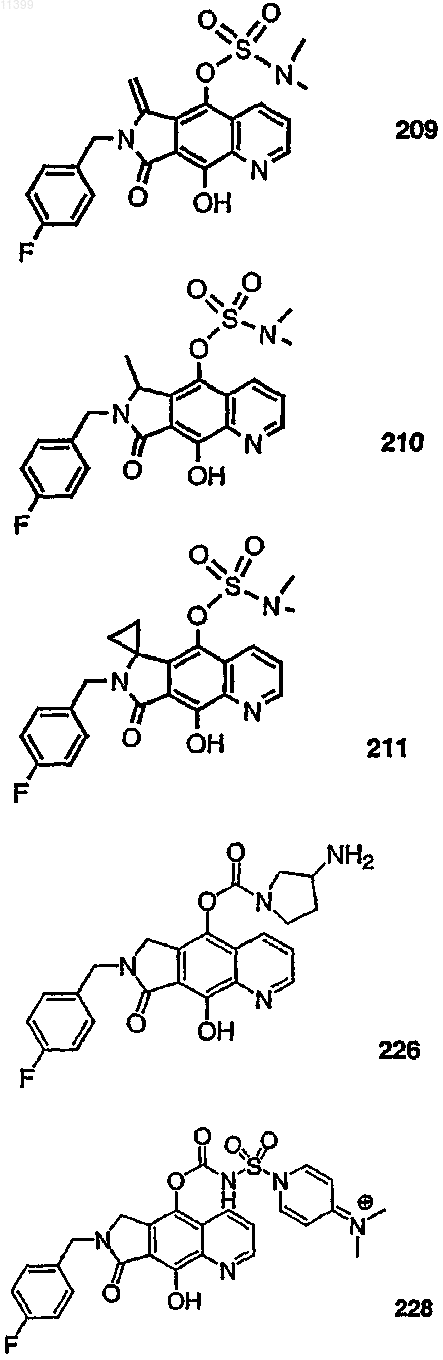
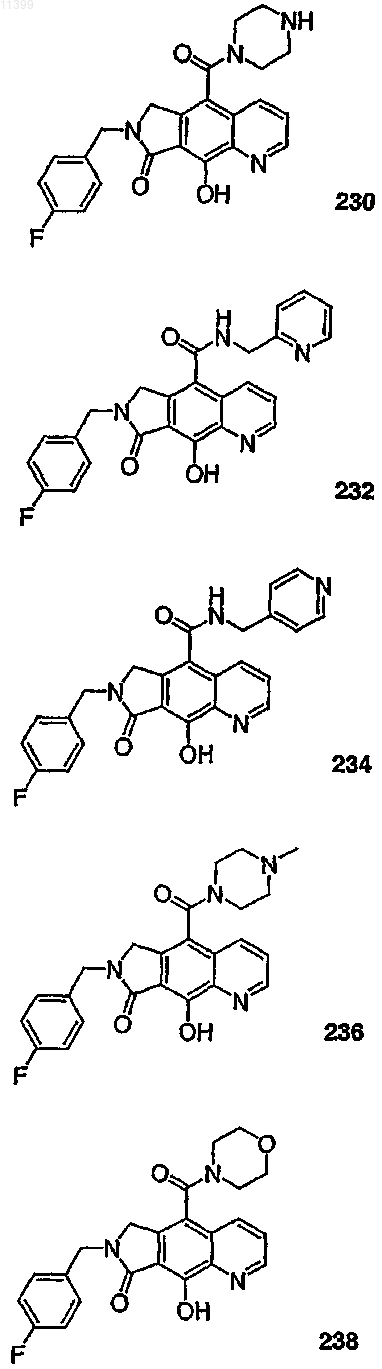
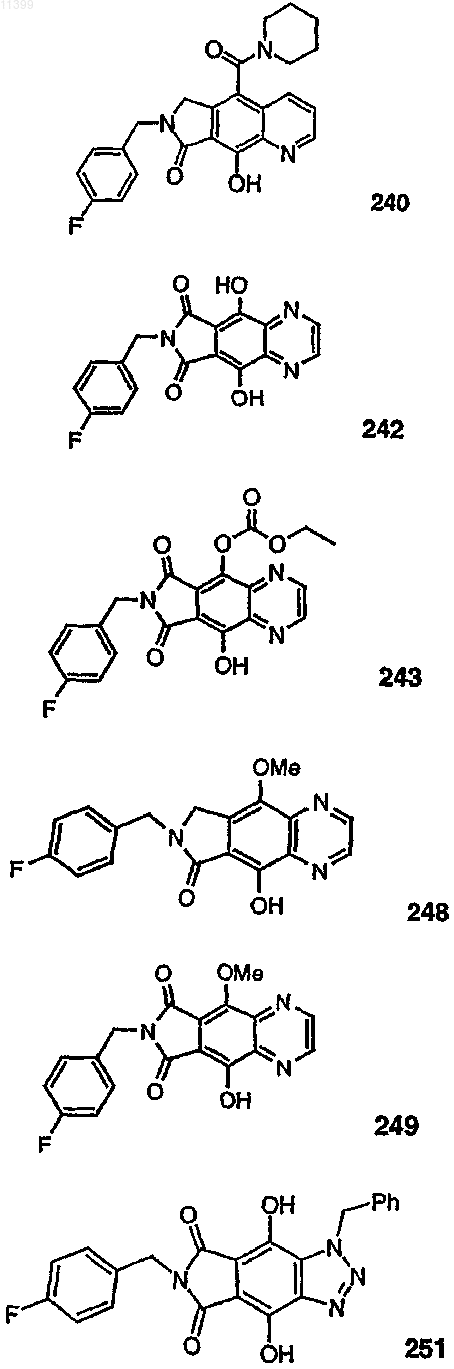
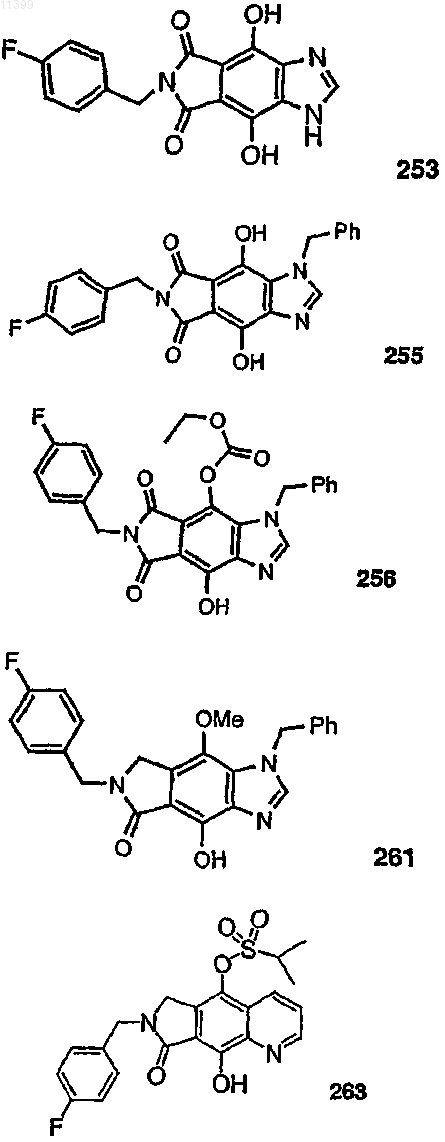
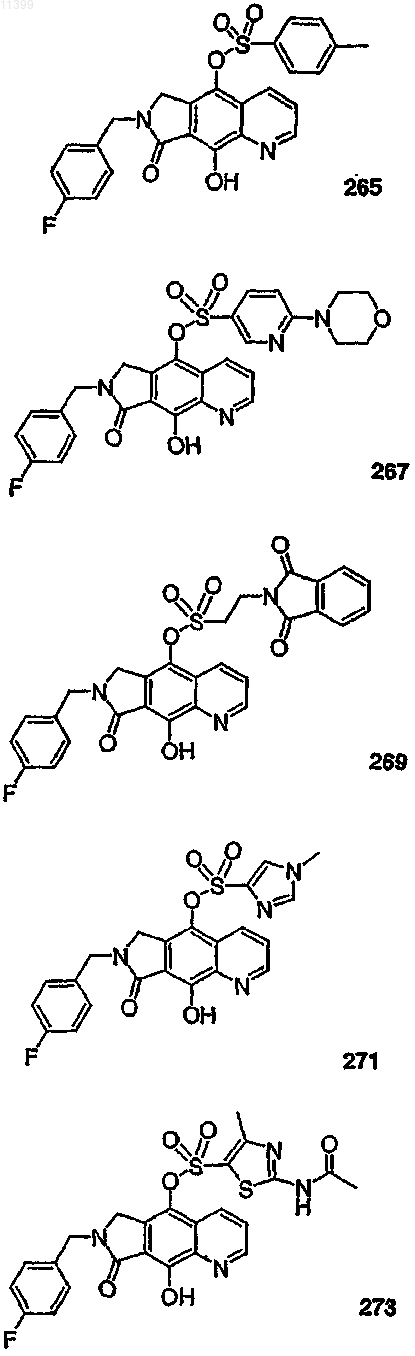
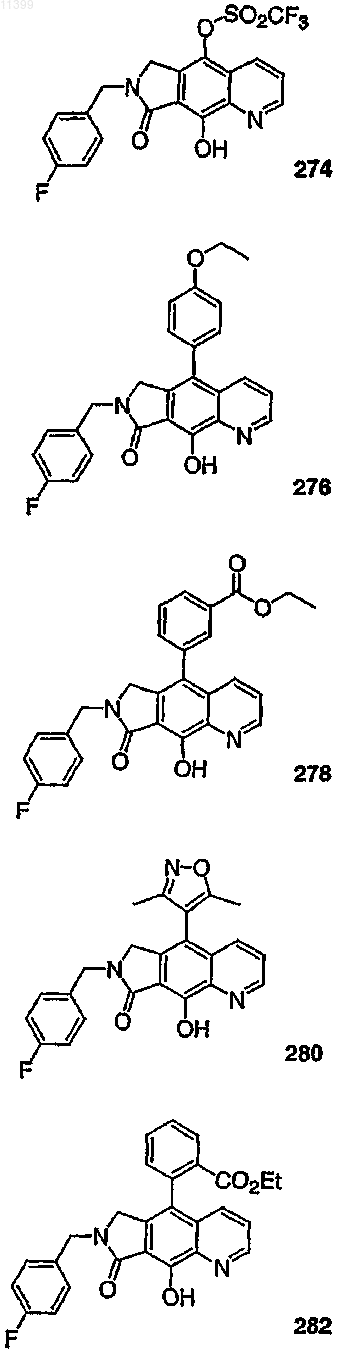
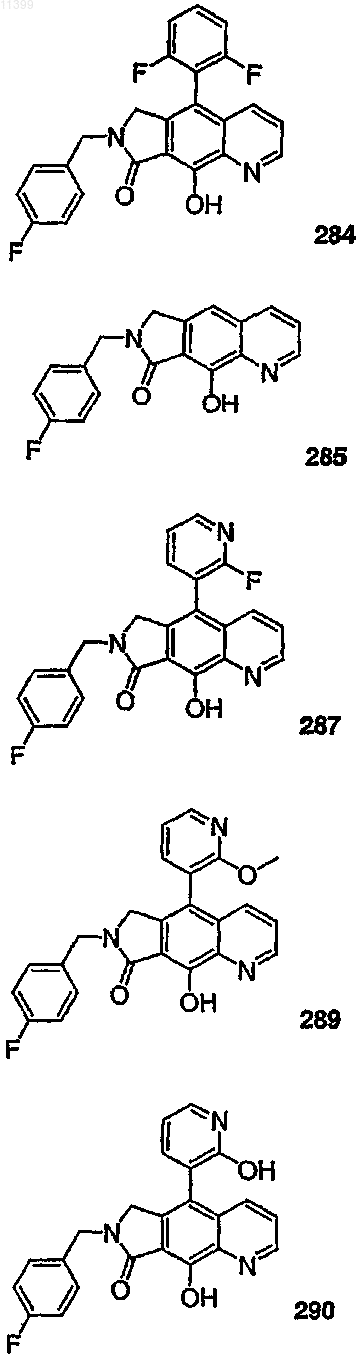
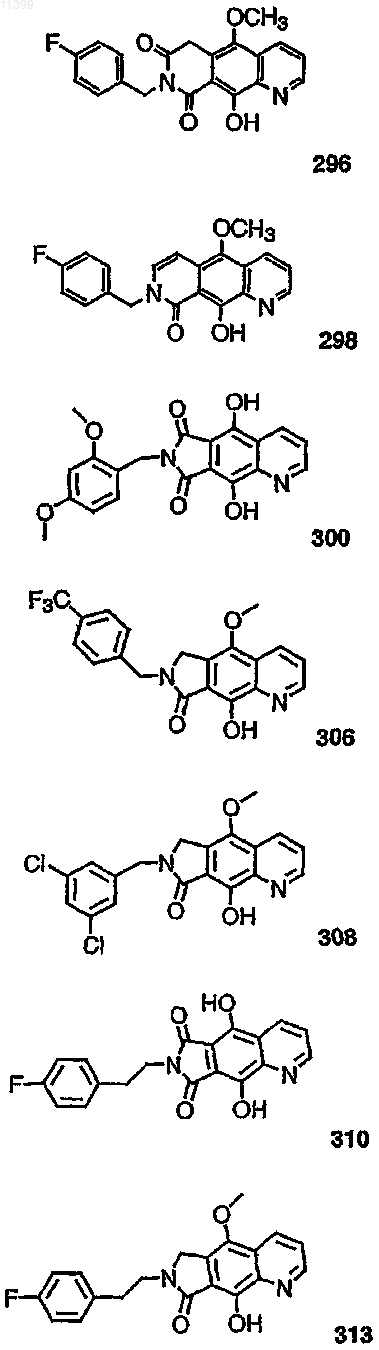

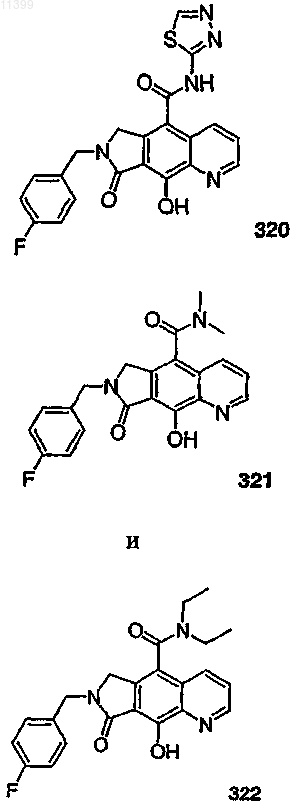
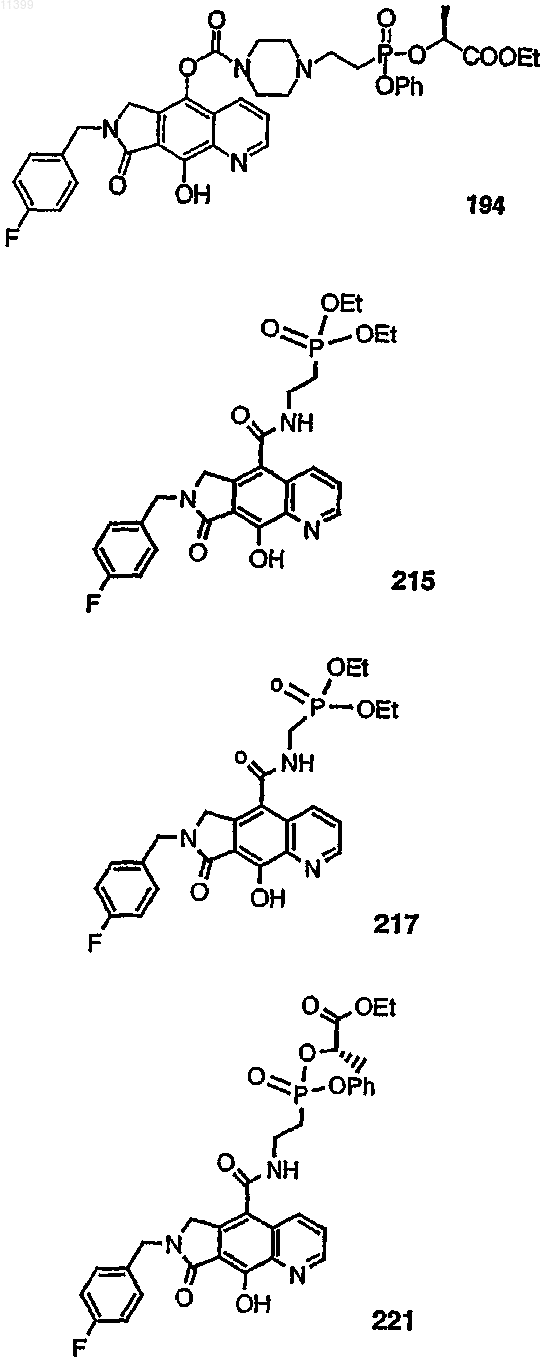
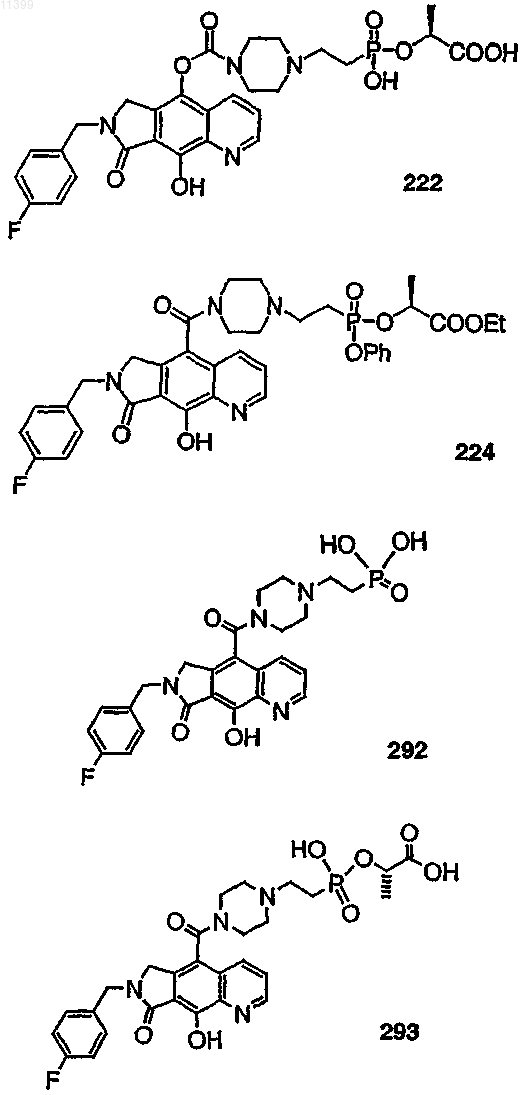
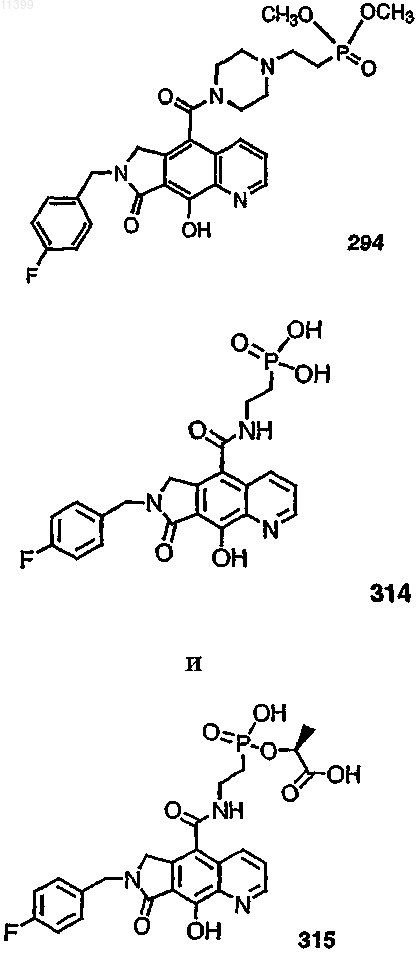
38. Соединение по п.13, выбранное из группы, включающей соединения следующих формул:
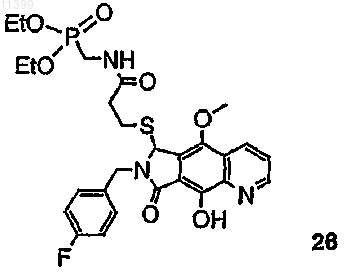
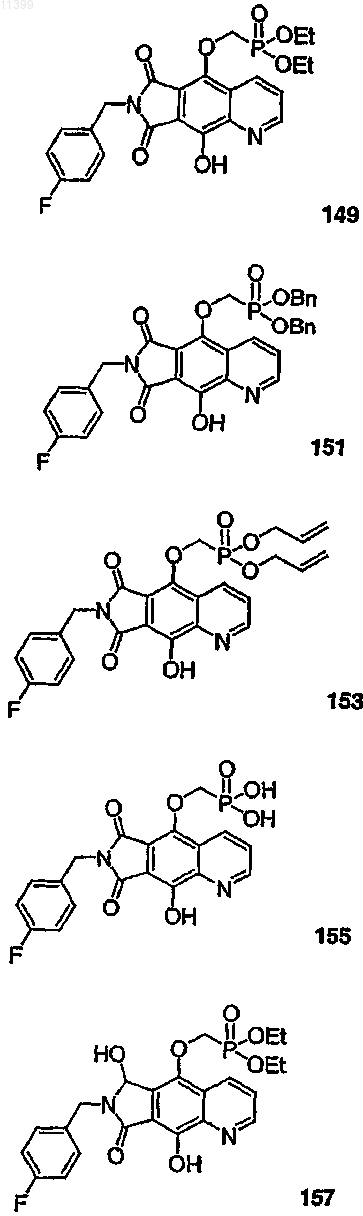
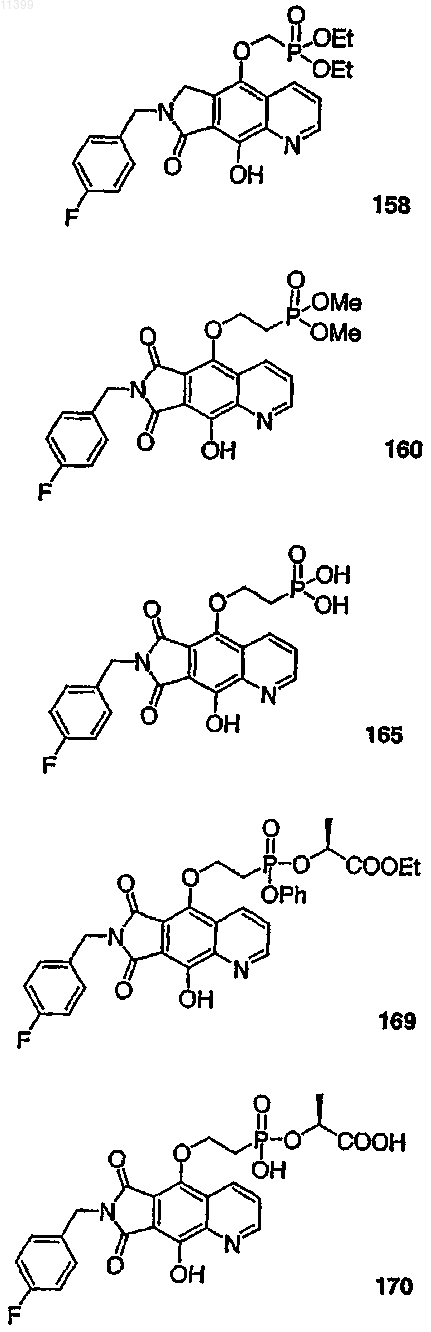
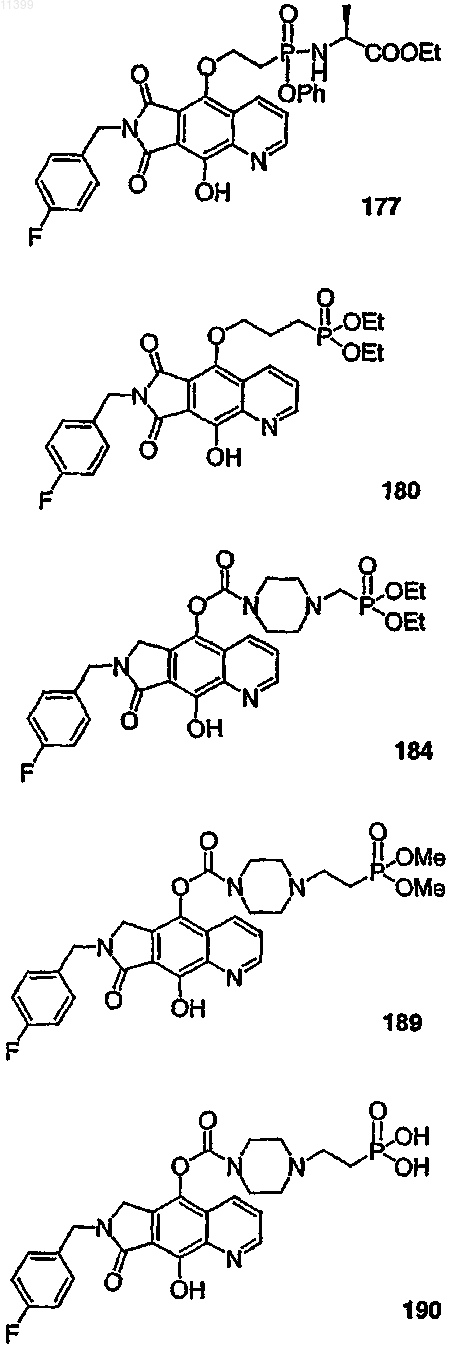
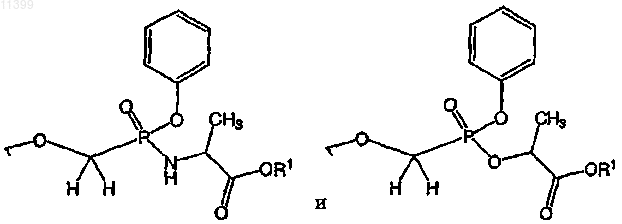
39. Соединение по п.1, в котором остаток пролекарства представлен следующей структурной формулой:
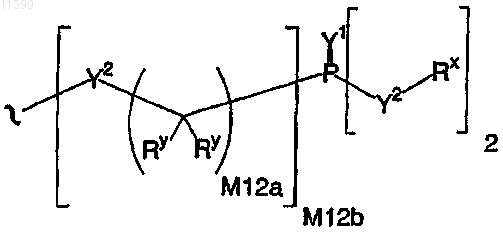
40. Соединение по п.39, в котором остаток пролекарства выбран из группы, включающей следующие структурные формулы:
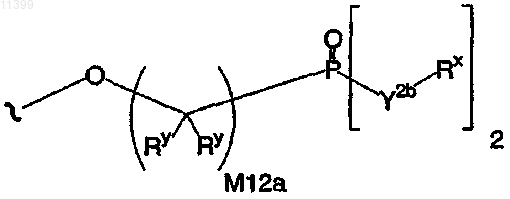
где Y2b означает О или N(Rx);

где W5 означает карбоцикл, выбранный из группы:
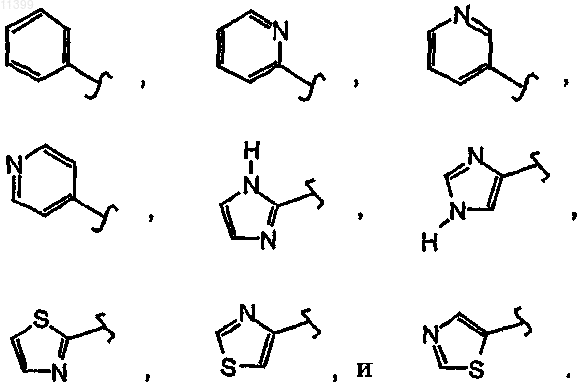
a Y2c представляет собой О, N(Ry) или S;
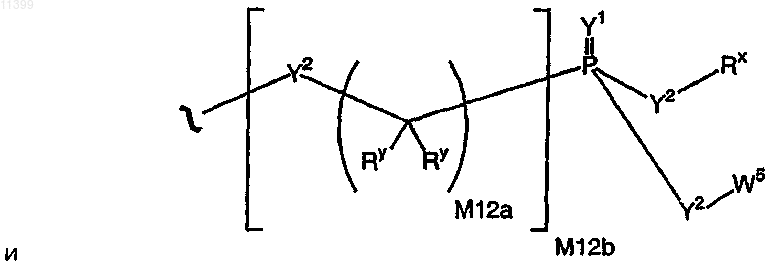
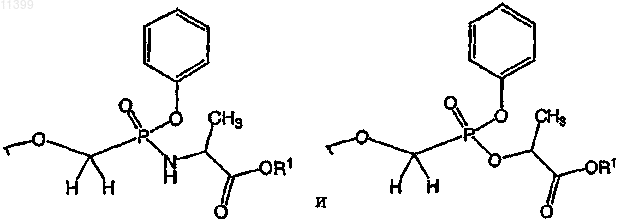
41. Соединение по п.1, в котором заместитель Rx у остатка пролекарства выбран из группы, включающей следующие структурные формулы:

42. Соединение по пп.1, 39-41, которое характеризуется способностью накапливаться в клетках РВМС человека.
43. Соединение по п.42, которое характеризуется внутриклеточным периодом полураспада соединения или внутриклеточного метаболита указанного соединения в клетках РВМС человека, увеличенным по крайней мере на приблизительно 50% по сравнению с аналогом соединения, не содержащим фосфонат.
44. Соединение по п.43, которое характеризуется периодом полураспада, увеличенным по крайней мере приблизительно на 100%.
45. Соединение по п.1 формулы
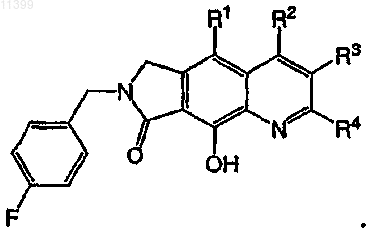
где R1 независимо выбирают из ряда: R, OR, NR2, NHR, NHSO2R и NRSO2R;
каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2,
-NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-С8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, С1-С8алкокси, C1-C8трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20 арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства; и
R независимо выбирают из ряда: Н, C1-C8алкил, замещенный C1-C8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства; и таутомеры, соли, сольваты, индивидуальные энантиомеры и их очищенные диастереомеры.
46. Соединение по п.1 формулы
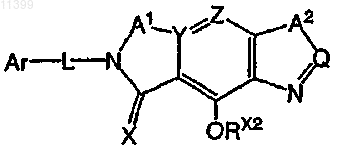
где А1 независимо выбирают из ряда: C(R2)2, CR2OR, CR2OC(=O)R, С(=O), C(=S), CR2SR и C(=NR);
А2 независимо выбирают из ряда: C(R2)2-C(R3)2, C(R2)=C(R3) и C(=O)C(R3)2;
Q означает CR4;

L выбирают из ряда: связь, О, S, S-S, S(=O), S(=O)2, S(=O)2NR, NR, N-OR, С1-С12алкилен, замещенный С1-С12алкилен, С2-С12алкенилен, замещенный С2-С12алкенилен, С2-С12алкинилен, замещенный С2-С12 алкинилен, C(=O)NH, OC(=O)NH, NHC(=O)NH, С(=O), C(=O)NH(CH2)n или (CH2CH2O)n, где n означает 1, 2, 3, 4, 5 или 6;
X выбирают из ряда: О, S, NH, NR, N-OR, N-NR2, N-CR2OR и N-CR2NR2;
Ar выбирают из ряда: С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, или насыщенного, ненасыщенного или ароматического цикла или циклической системы, включающей моно- или бициклический карбоцикл или гетероцикл, содержащий от 3 до 12 циклических атомов; каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2, -NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, С1-С8алкиламино, 4-диалкиламинопиридиний, C1-C8алкилгидроксил, С1-С8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2,
-SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3,
-NO2, C1-C8алкокси, C1-C8трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20 гетероарил, полиэтиленокси, фосфонат и фосфат;
две группы R2 или две группы R3, присоединенные к одному атому углерода, могут быть объединены с образованием спироцикла; R1 независимо выбирают из ряда: CR3, NRSO2R, OC(=O)NR2, OC(=O)R, SR, H, F, Cl, Br, I, OH, -NH2, -NH3+, -NHR, -NR2, -NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-C8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2,
-SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3,
-NO2, C1-C8алкокси, C1-C8трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20 гетероарил, полиэтиленокси, фосфонат и фосфат;
R независимо выбирают из ряда: Н, C1-C8алкил, замещенный C1-C8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат и фосфат;
RX2 независимо выбирают из ряда: Н, C1-C8алкил, замещенный С1-С8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и защитная группа; и таутомеры, соли, сольваты, индивидуальные энантиомеры и их очищенные диастереомеры;
при условии, что если Y=Z означает С=С(ОН), X означает О, А1 означает С(=O), А2 означает C(R2)=C(R3), и Q означает СН, то L не означает связь.
47. Соединение по п.46, в котором А1 означает СН2 или 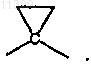
48. Соединение по п.46 формулы I
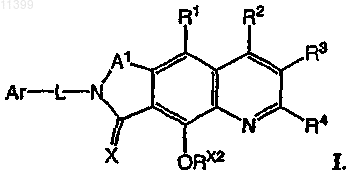
где X означает О.
49. Соединение по п.48, где L означает СН2 и Ar означает замещенный фенил.
50. Соединение по п.48, где А1 означает СН2, a R2, R3 и R4 каждый означает Н.
51. Соединение по п.46 формулы
где X означает О.
52. Соединение по п.51, где L означает СН2 и Ar означает замещенный фенил.
53. Соединение по п.52, где R2, R3 и R4 каждый означает Н.
54. Соединение формулы

где А1 независимо выбирают из ряда: C(R2)2, CR2OR, CR2OC(=O)R, C(=O), C(=S), CR2SR, C(=NR),
А2 независимо выбирают из ряда: О, S, NR, C(R2)2-C(R3)2, C(R2)=C(R3), C(=O)C(R3)2, NR-C(R3)2, N=C(R3), N=N или C(R2)=N;
Q означает N или CR4;
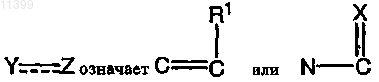
L выбирают из ряда: связь, О, S, S-S, S(=O), S(=O)2, S(=O)2NR, NR, N-OR, C1-C12алкилен, замещенный С1-С12алкилен, С2-С12алкенилен, замещенный С2-С12алкенилен, С2-С12алкинилен, замещенный С2-С12 алкинилен, C(=O)NH, OC(=O)NH, NHC(=O)NH, С(=O), C(=O)NH(CH2)n или (CH2CH2O)n, где n означает 1, 2, 3, 4, 5 или 6;
X выбирают из ряда: О, S, NH, NR, N-OR, N-NR2, N-CR2OR и N-CR2NR2;
Ar выбирают из ряда: С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил; или насыщенного, ненасыщенного или ароматического цикла или циклической системы, включающей моно- или бициклический карбоцикл или гетероцикл, содержащий от 3 до 12 циклических атомов;
каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2,
-NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-С8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8алкокси, C1-C8трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства;
две группы R2 или две группы R3, присоединенные к одному атому углерода, могут быть объединены с образованием спироцикла;
R1 независимо выбирают из ряда: CR3, NRSO2R, OC(=O)NR2, OC(=O)R, SR, H, F, Cl, Br, I, OH, -NH2, -NH3+, -NHR, -NR2, -NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-C8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8алкокёш, C1-C8трифторалкил, C1-C8алкил, замещенный С1-С8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства;
R независимо выбирают из ряда: Н, C1-C8алкил, замещенный C1-C8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства;
причем замещенный алкилен, замещенный алкенилен, замещенный алкинилен, замещенный арил и замещенный гетероарил независимо друг от друга замещены одним или более заместителями, выбранными из группы, включающей F, Cl, Br, I, ОН, амино (-NH2), аммоний (-NH3+), алкиламино, диалкиламино, триалкиламмоний, С1-С8алкил, С1-С8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-C8алкилгидроксил, C1-C8алкилтиол, алкилсульфон (-SO2R), арилсульфон (-SO2Ar), арилсульфоксид
(-SOAr), арилтио (-SAr), сульфонамид (-SO2NR2), алкилсульфоксид (-SOR), сложный эфир (-CO2R), амидо (-C(=O)NR2), 5-7-членный циклический лактам, 5-7-членный циклический лактон, нитрил (-CN), азидо (-N3), нитро (-NO2), C1-C8алкокси (-OR), C1-C8алкил, замещенный С1-С8алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, фосфонат, фосфат, полиэтиленокси и остаток пролекарства;
при этом, остаток пролекарства независимо выбран из группы, включающей -CH2OC(=O)R9 и -CH2OC(=O)OR9, где R9 означает C1-C6алкил, замещенный C1-C6алкил, С6-С20арил или замещенный С6-С20арил или выбран из группы, включающей

где R5 означает -CR2CO2R7, где R6 и R7 независимо означают Н или C1-С8алкил;
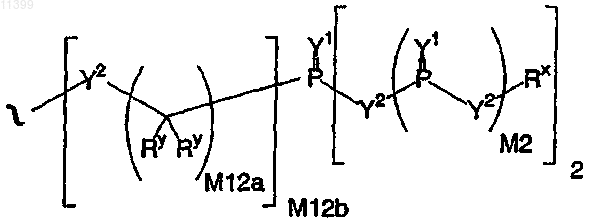
где
Y1 независимо означает О, S, N(Rx), N(O)(Rx), N(ORx), N(O)(ORx) или N(N(Rx)2),
Y2 независимо означает связь, О, N(Rx), N(O)(Rx), N(ORx), N(O)(ORx), N(N(Rx)2), -S(O)-(сульфоксид), -S(O)2-(сульфон), -S-(сульфид) или -S-S-(дисульфид),
M2 означает 0, 1 или 2,
М12а означает 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12,
М12b означает 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12,
Ry независимо означает Н, C1-C6алкил, замещенный C1-C6алкил, С6-С20арил, замещенный С6-С20 арил, или защитную группу, или две соседние группы Ry, присоединенные к одному атому углерода, объединены с образованием карбоцикла или гетероцикла и
Rx независимо означает Н, C1-C6алкил, замещенный C1-C6алкил, С6-С20арил, замещенный С6-С20 арил, или защитную группу, или следующую структурную формулу:
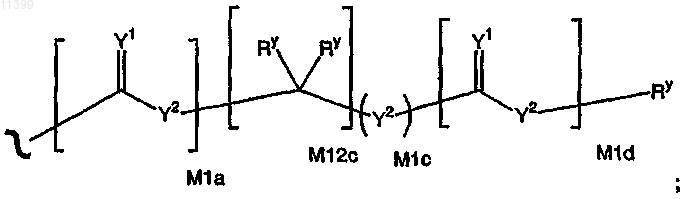
где М1а, М1c и M1d независимо означают 0 или 1, М12с означает 0, 1, 2, 3, 4, 5, 6, 7, 8, , 10, 11 или 12; и
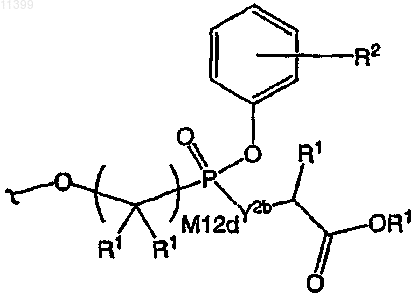
где Y2b означает О или N(Rx), M12d означает 1, 2, 3, 4, 5, 6, 7 или 8, R1 означает Н или C1-C6алкил, а фенильный карбоцикл содержит в качестве заместителей от 0 до 3 групп R2, где R2 означает C1-C6алкил или замещенный алкил; а также таутомеры, соли, сольваты, индивидуальные энантиомеры и их очищенные диастереомеры;
при условии, что если Y=Z означает С=С(ОН), X означает О, А1 означает С(=O), А2 означает C(R2)=C(R3) и Q означает СН, то L не означает связь; и Р означает защитную группу, выбранную из ряда: бензгидрил (CHPh2), триалкилсилил (R3Si), 2-триметилсилоксиэтил, алкоксиметил (CH2OR) и сложный эфир (C(=O)R).
55. Соединение по п.54, в котором остаток пролекарства представлен следующей формулой:
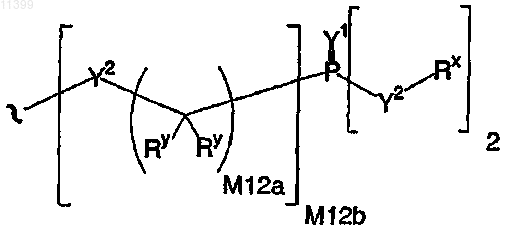
56. Соединение по п.55, в котором остаток пролекарства выбран из группы, включающей
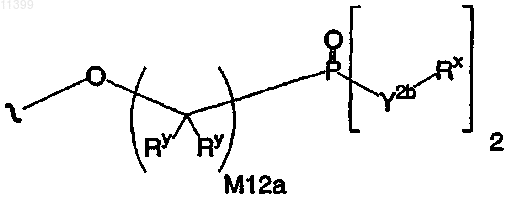
где Y2b означает О или N (Rx);
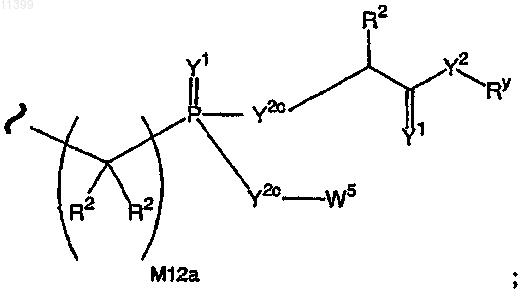
где W5 означает карбоцикл, выбранный из группы
a Y2c означает О, N(Ry) или S;
и
57. Соединение по п.54, в котором заместитель Rx у остатка пролекарства выбран из группы, включающей следующие структурные формулы:

58. Способ получения соединения следующей формулы:
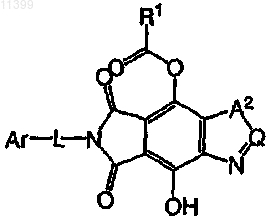
отличающийся тем, что осуществляют взаимодействие производного сукцинимида следующей формулы:
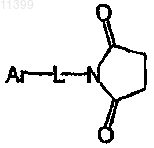
с гетероциклом следующей формулы:
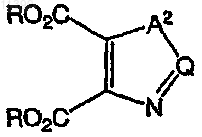
и затем взаимодействие с ацилирующим агентом, который выбирают из соединений следующих формул:
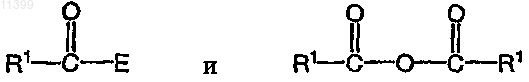
где
А2 выбирают из ряда: О, S, NR, C(R2)2, CR2OR, CR2OC(=O)R, C(=O), C(=S), CR2SR, C(=NR), C(R2)2-C(R3)2, C(R2)=C(R3), N=C(R3), N=N, SO2-NR, C(=O)C(R3)2, C(=O)NR, C(R2)2-C(R3)2-C(R3)2, C(R2)=C(R3)-C(R3)2, C(R2)C(=O)NR, C(R2)C(=S)NR, C(R2)=N-C(R3)2, C(R2)=N-NR и N=C(R3)-NR;
Q означает N, +NR или CR4;
L выбирают из ряда: связь, О, S, NR, N-OR, C1-C12алкилдиил, замещенный C1-C12алкилдиил, C(=O)NH, C(=O), S(=O), S(=O)2, C(=O)NH(CH2)n и (CH2CH2O)n, где n находится в диапазоне от 1 до 6,
Ar выбирают из ряда: С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20 гетероарил;
R1 выбирают из ряда: R, OR, NR2, NHR, NHSO2R ш NRSO2R,
E выбирают из ряда: Cl, имидазол и гидроксибензотриазол, каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2, -NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, С1-С8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, С1-С8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr,
-SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон,
-CN, -N3, -NO2, C1-C8алкокси, C1-C8трифторалкил, С1-С8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства;
R независимо выбирают из ряда: C1-C6алкил, замещенный C1-C6алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил, замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства.
59. Способ по п.58, отличающийся тем, что Q означает CR4, а А2 означает C(R2)=C(R3).
60. Способ получения соединения формулы
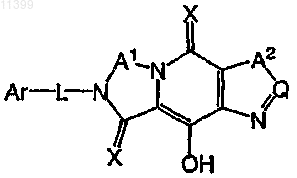
отличающийся тем, что осуществляют взаимодействие соединения формулы
с основным реагентом, включающим гидроксид, алкоксид или амин, где
А1 и А2 независимо выбирают из ряда: О, S, NR, C(R2)2, CR2OR, CR2OC(=O)R, С(=O), C(=S), CR2SR, C(=NR), C(R2)2-C(R3)2, C(R2)=C(R3), NR-C(R3)2, N=C(R3), N=N, SO2-NR, C(=O)C(R3)2, C(=O)NR, C(R2)2-C(R3)2-C(R3)2, C(R2)=C(R3)-C(R3)2, C(R2)C(=O)NR, C(R2)C(=S)NR, C(R2)=N-C(R3)2, C(R2)=N-NR и N=C(R3)-NR;
Q означает N, +NR или CR4;
X выбирают из ряда: О, S, NH, NR, N-OR, N-NR2, N-CR2OR и N-CR2NR2;
L выбирают из ряда: связь, О, S, NR, N-OR, C1-C12алкилдиил, замещенный С1-С12алкилдиил, C(=O)NH, С(=O), S(=O), S(=O)2, C(=O)NH(CH2)n и (CH2CH2O)n, где n находится в диапазоне от 1 до 6,
Ar выбирают из ряда: С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20 гетероарил;
каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2,
-NR3+, C1-C8алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, C1-C8алкилсульфонат, C1-C8алкиламино, 4-диалкиламинопиридиний, C1-С8алкилгидроксил, C1-C8алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8алкокси, C1-C8трифторалкил, C1-C8алкил, замещенный C1-C8алкил, С3-С12карбоцикл, замещенный С3-С12карбоцикл, С6-С20арил, замещенный С6-С20 арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства; и R выбирают из ряда: C1-C6алкил, замещенный C1-C6алкил, С6-С20арил, замещенный С6-С20арил, С2-С20гетероарил и замещенный С2-С20гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства.
61. Способ получения соединения формулы 115
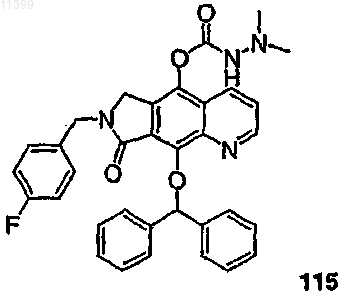
отличающийся тем, что осуществляют взаимодействие соединения формулы 44
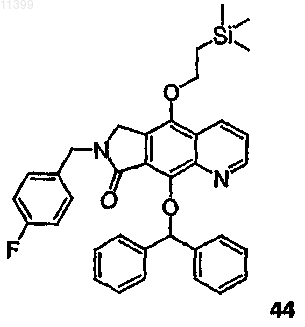
с фторидом тетрабутиламмония с образованием десилилированного промежуточного производного и последующее взаимодействие полученного промежуточного соединения с трифосгеном (бис(трихлорметил)карбонатом), а затем с диметилгидразином.
62. Фармацевтическая композиция, включающая терапевтически эффективное количество соединения по п.1 и фармацевтически приемлемый носитель.
63. Композиция по п.62, которая дополнительно содержит терапевтически эффективное количество агента для лечения СПИД, выбранного из группы, включающей ингибитор ВИЧ, противоинфекционный агент и иммуномодулятор.
64. Композиция по п.63, в которой ингибитором ВИЧ является ингибитор протеазы ВИЧ.
65. Композиция по п.63, в которой ингибитором ВИЧ является нуклеозидный ингибитор обратной транскриптазы.
66. Композиция по п.63, в которой ингибитором ВИЧ является ненуклеозидный ингибитор обратной транскриптазы.
67. Способ получения фармацевтической композиции, отличающийся тем, что смешивают соединение по п.1 и фармацевтически приемлемый носитель.
68. Способ ингибирования интегразы ВИЧ, отличающийся тем, что млекопитающему, нуждающемуся в таком лечении, вводят терапевтически эффективное количество соединения по п.1.
69. Способ лечения инфекции ВИЧ или лечения СПИД или СПИД-ассоциированного комплекса, отличающийся тем, что млекопитающему, нуждающемуся в таком лечении, вводят терапевтически эффективное количество соединения по п.1.
70. Способ лечения нарушения, влияющего на лейкоциты крови, отличающийся тем, что пациенту, нуждающемуся в обработке лейкоцитов в качестве мишени, вводят соединение по п.42.
Текст
011399 Область техники, к которой относится изобретение Настоящее изобретение в основном относится к соединениям, обладающим антивирусной активностью и, более подробно, ингибирующими свойствами в отношении интегразы ВИЧ. Уровень техники Инфекция, вызванная вирусом иммунодефицита человека (ВИЧ), и связанные с ней заболевания представляют основную проблему здравоохранения во всем мире. Кодируемый вирусом белок - интеграза опосредует специфическое включение и интеграцию вирусной ДНК в геном организма хозяина. Интеграция необходима для вирусной репликации. В связи с этим при разработке способов лечения инфекции ВИЧ и связанных с ней заболеваний важной задачей является ингибирование интегразы ВИЧ. Вирус иммунодефицита типа 1 (ВИЧ-1) кодирует три фермента, необходимых для вирусной репликации: обратную траскриптазу, протеазу и интегразу. Хотя лекарственные средства, действующие на обратную транскриптазу и протеазу, широко распространены и показана их эффективность, прежде всего, если их используют в комбинации, их применение ограничено из-за токсичности и развития устойчивых штаммов (см. статьи Palella et al., N. Engl. J. Med. (1998) 338:853-860; Richman D.D., Nature (2001) 410:995-1001). Следовательно, существует необходимость в разработке новых агентов, действующих на различных этапах развития вируса. Интеграза является перспективной мишенью в связи с ее необходимостью для устойчивой инфекции и в связи с отсутствием гомологичных ферментов в организме хозяина(см. статью LaFemina et al., J. Virol. (1992) 66:7414-7419). Функция интегразы заключается в катализе интеграции провирусной ДНК, обраующейся в результате обратной транскрипции вирусной PHK в геноме организма хозяина, причем последний процесс происходит за счет постадийного процессинга провирусной ДНК эндонуклеазами в цитоплазматическом преинтеграционном комплексе (названного 3'процессингом или 3'-Р) поспецифичным последовательностям в концевых фрагментах ДНК ВИЧ-1 (а именно, в вирусных длинноцепных концевых повторяющихся фрагментах (LTR, с последующей транслокацией комплекса в ядре, где происходит интеграция провирусной ДНК, образующейся просле 3'процессинга, с ДНК организма хозяина по реакции типа "перенос цепей" (ST) (см. статьи Hazuda et al.,Science (2000) 287:646-650; Katzman et al., Adv. Virus Res. (1999) 52:371-395; Asante-Applah et al., Adv.Virus Res. (1999) 52:351-369). Несмотря на то, что мночисленные агенты ингибируют процессы 3'-Р и ST при анализе в безклеточной среде с использованием рекомбинантной интегразы и вирусных длинноцепных повторяющихся фрагментов, в большинстве случаев такие ингибиторы не проявляют ингибирующую активность при анализе с использованием полностью собранного преинтеграционного комплекса или не обладают антивирусной активностью против ВИЧ-инфицированных клеток (см. статьи Pommieretal., Adv. Virus Res. (1999) 52:427-458; Farnet et al., Proc. Natl. Acad. Sci. U.S.A. (1996) 93:9742-9747; Pommier et al., Antiviral Res. (2000) 47:139-148). Известны определенные ингибиторы интегразы ВИЧ, которые ингибируют интеграцию в бесклеточных средах и проявляют достаточно высокую противовирусную активность в отношении ВИЧ-инфицированных клеток (Anthony et al., WO 02/30426; Anthony et al., WO 02/30930; Anthony et al., WO 02/30931; WO 02/055079; Zhuang et al., WO 02/36734; US 6395743; US 6245806; US 6271402; Fujishita et al., WO 00/039086; Uenaka et al., WO 00/075122; Selnick et al., WO 99/62513; Young et al., WO 99/62520; Payne et al., WO 01/00578; Jing et al., Biochemistry (2002) 41:53975403; Pais et al., Jour. Med. Chem. (2002) 45:3184-94; Goldgur et al., Proc. Natl. Acad. Sci. U.S.A. (1999) 96:13040-13043; Espeseth et al., Proc. Natl. Acad. Sci. U.S.A. (2000) 97:11244-11249). В связи с этим существует необходимость в соединениях-ингибиторах интегразы ВИЧ с улучшенными противовирусными и фармакокинетическими свойствами, включая повышенную активность против развития устойчивости к ВИЧ, повышенную пероральную биодоступность, более высокую эффективность действия in vivo и более продолжительный период полувыведения in vivo (Nair V., "HIV integrase as a target for antiviral chemotherapy" Reviews in Medical Virology (2002) 12(3): 179-193). Количественные исследования зависимости трехмерной структуры от активности и структурного моделирования(Buolamwini et al., Jour. Med. Chem. (2002) 45:841-852;) ингибиторов интегразы циннамоильного типа с заторможенной конформацией (Artico et al., Jour. Med. Chem. (1998) 41:3948-3960) показали зависимость различия в ингибирующей активности соединений от способности к образованию водородных связей. Особое внимание при исследованиях в течение многих лет уделялось улучшению доставки лекарственных средств и других агентов к клеткам-мишеням и тканям-мишеням. Несмотря на многисленные попытки разработки эффективных способов для доставки биологически активных молекул в клетки, какin vivo, так и in vitro, ни один из подходов полностью не удовлетворяет предъявляемым требованиям. В большинстве случаев оптимизация ассоциации ингибирующего лекарственного средства с внутриклеточной мишенью с одновременным сведением к минимуму межклеточного распределения лекарственного средства, то есть в соседних клетках, оказывается затруднительной или неэффективной. В настоящее время многие агенты, введенные пациенту парентерально, не достигают мишени, что приводит к системной доставке агента в клетки и ткани организма, в которые доставка либо не требуется и в большинстве случаев нежелательна. В результате наблюдается отрицательное действие лекарственного средства и в большинстве случаев при этом ограничивается вводимая доза лекарственного средства(например, цитотоксических агентов и других противопухолевых или противовирусных лекарственных средств). Несмотря на то, что по сравнению с указанным выше способом введения, пероральный способ-1 011399 введения лекарственных средств в основном считается наиболее удобным и экономичным способом,пероральное введение может привести либо (а) к проникновению лекарственного средства через клеточные и тканевые барьеры, например, кровь/мозг, эпителиальные и клеточные мембраны, что в свою очередь приводит к нежелательному системному распределению, либо (б) к временному удерживанию лекарственного средства в желудочно-кишечном тракте. В связи с этим основная задача заключается в разработке способов специфичной доставки агентов к клеткам-мишеням или тканям-мишеням. Доставка внутрь клеток может быть достигнута способами и композициями, которые обеспечивают накопление или удерживание биологически активных соединений в клетках. Сущность изобретения Настоящее изобретение относится к композициям и способам ингибирования интегразы ВИЧ. Один аспект изобретения относится к соединению формулы где А 1 независимо выбирают из ряда: C(R2)2, CR2OR, CR2OC(=O)R, C(=O), C(=S), CR2SR, C(=NR); А 2 независимо выбирают из ряда: О, S, NR, C(R2)2-C(R3)2, C(R2)=C(R3), C(=O)C(R3)2, NR-C(R3)2,N=C(R3), N=N или C(R2)=N;Ar выбирают из ряда: С 3-С 12 карбоцикл, замещенный С 3-С 12 карбоцикл, С 6-С 20 арил, замещенный С 6 С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, или насыщенный, ненасыщенный или ароматический цикл или циклическая система, включающая моно- или бициклический карбоцикл или гетероцикл, содержащий от 3 до 12 циклических атомов; каждый из R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR, -NR2,+-NR3 , С 1-С 8 алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный циклический сультам, С 1-С 8 алкилсульфонат, С 1-С 8 алкиламино, 4-диалкиламинопиридиний, С 1-С 8 алкилгидроксил, С 1 С 8 алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, С 1-С 8 алкокси, C1-C8 трифторалкил, C1-C8 алкил,замещенный C1-C8 алкил, С 3-С 12 карбоцикл, замещенный С 3-С 12 карбоцикл, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства; две группы R2 или две группы R3, присоединенные к одному атому углерода, могут быть объединены с образованием спироцикла;R1 независимо выбирают из ряда: CR3, NRSO2R, OC(=O)NR2, OC(=O)R, SR, H, F, Cl, Br, I, OH, -NH2,+R независимо выбирают из ряда: Н, C1-C8 алкил, замещенный C1-C8 алкил, C6-C20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат и фрагмент пролекарства;RX2 независимо выбирают из ряда: Н, C1-C8 алкил, замещенный C1-С 8 алкил, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат, пролекарство, фармацевтически приемлемое пролекарство, фрагмент пролекарства, защитная группа и фосфонатный фрагмент пролекарства; и соли, сольваты, индивидуальные энантиомеры и их очищенные диастереомеры; при условии, если Y=Z означает С=С(ОН), X означает О, А 1 означает С(=O), А 2 означаетC(R2)=C(R3), и Q означает СН, то L не означает связь. Один аспект изобретения включает трициклические соединения, представленные следующей формулой: Соединения по настоящему изобретению характеризуются трициклической структурой-каркасом и включают активный участок или фрагмент связывания с металлом, показанный в нижней части приведенной выше формулы, включающий амидную функциональную группу, т.е. группу N-С(=Х) в левом цикле, ароматический гидроксил в среднем цикле и атом азота в правом цикле. Соединения по настоящему изобретению содержат участок связывания, т.е. содержат атом азота, гидроксил и Х-карбонил в предварительно определенной конфигурации, которая позволяет оптимизировать ингибирующие свойства в отношении интегразы ВИЧ. Каждая из групп А 1 и А 2 независимо означает остаток, образующий 5-, 6- или 7-членный цикл. Q означает N, замещенный атом азота (NR), СН или замещенный атом углерода. L означает связь или связующее звено, соединяющее циклический атом группы Ar с атомом N. X означает О, S, NH или замещенный атом азота (NR). Ar означает карбоцикл, арильную или гетероарильную группу. R означает заместитель, включая Н, алкил, арил, гетероарил и замещенные формы указанных соединений, а также полиэтиленокси, фосфонат, фосфат или фрагмент пролекарства. На представленной выше формуле указаны Y и Z в положениях 5 и 6, соответственно. Химическая связь между Y и Z означает простую связь,двойную связь или связь енольного таутомерного типа в зависимости от заместителя Z, т.е. R1 или X. Структура Y и Z показана ниже: Соединения по настоящему изобретению включают фрагменты пролекарства, ковалентно присоединенные к любому участку. Фрагмент пролекарства может означать фосфонатную группу. Настоящее изобретение включает также фармацевтическую композицию, содержащую терапевтически эффективное количество соединения по настоящему изобретению или его фармацевтически приемлемую соль в комбинации с фармацевтически приемлемым разбавителем или носителем. Настоящее изобретение включает также фармацевтическую композицию, содержащую терапевтически эффективное количество соединения по настоящему изобретению или его фармацевтически приемлемую соль в комбинации с фармацевтически эффективным количеством агента для лечения СПИД,который выбирают из группы, включающей ингибитор ВИЧ, противоинфекционный агент и имуномодулятор. Ингибитор ВИЧ включает ингибитор протеазы ВИЧ или нуклеозидный ингибитор обратной транскриптазы или ненуклеозидный ингибитор обратной транскриптазы. Настоящее изобретение включает также способы предотвращения пролиферации вируса ВИЧ, лечения СПИД, замедления проявления симптомов СПИД или СПИД-ассоциированного комплекса и основного ингибирования интегразы ВИЧ. Способы включают введение млекопитающему, инфицированному ВИЧ (ВИЧ положительному), соединения по настоящему изобретению в количестве терапевтически эффективной дозы или введение для ингибирования роста ВИЧ-инфицированных клеток млекопитающего. В другом аспекте настоящего изобретения активность интегразы ВИЧ ингибируют способом, включающим стадию обработки образца, предположительно содержащего вирус ВИЧ, соединением или композицией по настоящему изобретению. Настоящее изобретение включает также способы и новые промежуточные соединения, описанные в данном контексте, которые используют для получения соединений по настоящему изобретению. Некоторые из соединений по настоящему изобретению используют для получения других соединений по настоящему изобретению. Настоящее изобретение включает также способы увеличения накопления в клетках, биодоступности или удерживания лекарственных средств, что повышает их терапевтическое и диагностическое значение, причем способы включают введение фосфонатной пролекарственной формы соединения по настоящему изобретению. В другом аспекте настоящего изобретения описан способ ингибирования активности интегразы ВИЧ, включающий стадию контактирования образца, предположительно содержащего вирус ВИЧ, с вариантами композиции по настоящему изобретению. В других аспектах описаны новые способы синтеза, анализа, разделения, выделения, кристаллизации, очистки, характеризации, разделения изомеров, включая энантиомеры и диастереомеры, и испытания соединений по настоящему изобретению. Сведения, подтверждающие возможность осуществления изобретения Следует подробно описать некоторые варианты воплощения изобретения, примеры которых представлены в описании, структурах и формулах. В то время как изобретение будет описано в сочетании с пронумерованными вариантами воплощения, изобретение не ограничивается перечисленным. Наоборот,-3 011399 в объем изобретения включены все варианты, модификации и эквиваленты, которые могут быть внесены в объем настоящего изобретения, определенный в пунктах формулы изобретения. Определения Если не указано иное, следующие термины и выражения, использованные в настоящем описании,имеют следующие значения. Термин "фосфонат или фосфонатная группа" означает функциональную группу или остаток в составе молекулы, который содержит по крайней мере одну связь фосфор-углерод и по крайней мере одну двойную связь фосфор-кислород. Кроме того, атом фосфора замещен группами, содержащими кислород,серу и азот. Как определено в данном описании "фосфонат" и "фосфонатная группа" включают молекулы, содержащие функциональные группы фосфоновой кислоты, моноэфира фосфоновой кислоты, диэфира фосфоновой кислоты, фосфонамидата, фосфондиамидата и фосфонтионата. Термин "пролекарство", использованный в данном описании, означает любое соединение, которое при введении в биологическую систему образует субстанцию лекарственного средства, то есть активный компонент, который образуется в результате химической реакции (реакций), ферментативных химических реакций, фотолиза и/или метаболической химической реакции (реакций). Таким образом, пролекарство означает ковалентно модифицированный аналог или латентную форму терапевтически активного соединения."Фармацевтически приемлемое пролекарство" означает соединение, которое превращается в процессе метаболизма в организме хозяина, например, гидролизуется или окисляется под действием фермента или кислотного или основного сольволиза с образованием активного компонента. Типичные примеры пролекарств соединений по настоящему изобретению содержат лабильные защитные группы в функциональном остатке соединения. Пролекарства включают соединения, которые могут модифицироваться в результате окисления, восстанавления, аминирования, деаминирования, этерификации, омыления, алкилирования, деалкилирования, ацилирования, деацилирования, фосфорилирования, дефосфорилирования или изменения или превращения других функциональных групп, включая образование или разрыв химических связей в пролекарстве."Остаток пролекарства" означает лабильную функциональную группу, которая отделяется от активного ингибитора в процессе метаболизма по системному механизму, внутри клетки, в результате гидролиза, ферментативного расщепления или по иному механизму (см. книгу Bundgaard Hans "Design andApplication of Prodrugs" (Конструирование и применение пролекарств), Textbook of Drug Design and Development (Учебник по созданию и разработке лекарственных средств) (1991), под ред. P.KrogsgaardLarsen and H.Bundgaard, Harwood Academic Publishers, стр.113-191). Ферменты, способные осуществлять ферментативную активацию пролекарств, содержащих фосфонат, по настоящему изобретению включают, без ограничения перечисленным, амидазы, эстеразы, микробные ферменты, фосфолипазы, холинэстеразы и фосфазы. Остатки пролекарства могут увеличивать растворимость, всасывание и липофильность, что позволит оптимизировать доставку лекарственного средства, а также его биодоступность и эффективность. Примеры остатков пролекарств включают чувствительные к гидролизу или лабильные ацилоксиметиловые эфиры -CH2OC(=O)R9 и ацилоксиметилкарбонаты -CH2OC(=O)OR9, где R9 означает C1-С 6 алкил,замещенный C1-С 6 алкил, С 6-С 20 арил или замещенный С 6-С 20 арил. Первоначально ацилоксиалкиловый эфир был использован при разработке пролекарств на основе карбоновых кислот, а затем применен к фосфатам и фосфонатам, как описано в статье Farquhar et al., J.Pharm. Sci., (1983) 72:324, и в патентах США NoNo 4816570, 4968788, 5663159 и 5792756. Позднее ацилоксиалкиловый эфир был использован для доставки фосфоновых кислот через клеточные мембраны и для повышения пероральной биодоступности. Родственный вариант ацилоксиалкилового эфира, то есть алкоксикарбонилоксиалкиловый эфир(карбонат), также может повышать пероральную биодоступность, если использовать его в качестве остатка пролекарства в соединениях, входящих в состав комбинации по настоящему изобретению. Пример ацилоксиметилового эфира включает пивалоилоксиметокси (РОМ) -СН 2 ОС(=O)С(СН 3)3. Пример ацилоксиметилкарбонатного остатка пролекарства включает пивалоилоксиметилкарбонат (РОС) -СН 2 ОС(=O) ОС(СН 3)3. Фосфонатная группа может означать фосфонатный остаток пролекарства. Остаток пролекарства может означать чувствительные к гидролизу группы, такие как, без ограничения перечисленным, пивалоилоксиметилкарбонатная (РОС) или РОМ-группы. В другом варианте остаток пролекарства может быть чувствительным к расщеплению ферментами, то есть содержать остатки эфира молочной кислоты или фосфонамидат-эфирные группы. Ариловые эфиры фосфорсодержащих групп, прежде всего, фениловые эфиры повышают пероральную биодоступность, как описано DeLambert et al., J.Med.Chem., (1994), 37:498. Описаны также фениловые эфиры, содержащие эфир карбоновой кислоты в орто-положении по отношению к фосфатной группе(см. статью Khamnei and Torrence, J.Med.Chem., (1996), 39:4109-4115). Описаны бензиловые эфиры, из которых образуется исходная фосфоновая кислота. В некоторых случаях заместители в орто- или параположении могут ускорять гидролиз. Бензиловые аналоги, содержащие ацилированный фенол или алкилированный фенол, при действии ферментов, например, эстераз, оксидаз и т.п. могут образовывать фе-4 011399 нольное соединение, которое в свою очередь расщепляется по бензильной связи С-O с образованием фосфорной кислоты и промежуточного хинонметида. Примеры этого класса пролекарств описаны в статье Mitchel et al., J.Chem.Soc.Perkin Trans. (1992) I 2345; в заявке Brook et al., WO 91/19721. Описаны также другие бензильные пролекарства, содержащие остатки эфиров карбоновых кислот, присоединенные к метиленовой группе в составе бензильной группы (Glazier et al., WO 91/19721). Описаны тиосодержащие пролекарства, которые используют для внутриклеточной доставки фосфонатных лекарственных средств. Такие проэфиры содержат этилтиогруппу, в которой тиольная группа либо этерифицирована ацильной группой, либо объединена с другой тиольной группой с образованием дисульфида. Омыление или восстановление дисульфидов приводит к образованию промежуточного производного со свободной тиогруппой, которая затем отщепляется с образованием фосфорной кислоты и эписульфида (Puech et al.,Antiviral Res. (1993), 22:155-174; Banzaria et al., J.Med.Chem. (1996), 39:4958). Циклические фосфонатные эфиры также описаны в качестве пролекарств на основе фосфорсодержащих соединений (Erion et al.,патент США No 6312662)."Защитная группа" означает остаток в соединении, который блокирует или изменяет свойства функциональной группы или свойства соединения в целом. Химическая структура защитной группы изменяется в широком диапазоне. Одной из функций защитной группы является получение производных при синтезе исходной лекарственной субстанции. Структура защитных групп и стратегия введения/удаления защитных групп известны в данной области техники. См. в книге "Protective Groups in Organic Chemistry", Theodora W. Greene (John Wiley and Sons, Inc., New York, 1991). В большинстве случаев защитные группы используют для блокирования реакционной способности функциональных групп с целью повышения эффективности требуемых химических реакций, например, для создания и расщепления химических связей по предназначенному и запланированному механизму реакции. Введение защитных групп в соединение наряду с изменением реакционной способности защищенной функциональной группы приводит к изменению других физических свойств, таких как полярность, липофильность (гидрофобность) и других свойств, которые можно определить с использованием обычных методов анализа. Сами по себе защищенные промежуточные соединения могут обладать биологической активностью или являются неактивными. Защищенные соединения могут также проявлять измененные и в некоторых случаях оптимизированные in vitro и in vivo свойства, такие как проникновение через клеточную мембрану и устойчивость к ферментативному расщеплению или секвестрации (изоляции). В этом смысле защищенные соединения с предназначенным терапевтическим действием можно назвать пролекарствами. Другой функцией защитной группы является превращение исходного лекарственного средства в пролекарство, причем исходное лекарственное средство высвобождается после превращения пролекарства in vivo. Так как активные пролекарства могут впитываться более эффективно по сравнению с исходным лекарственным средством,пролекарства могут обладать более высокой активностью in vivo по сравнению с исходным лекарственным средством. Защитные группы удаляют либо in vitro, например в случае химических производных,либо in vivo в случае пролекарств. Наличие физиологической приемлемости в случае химических производных после удаления защитных групп, например, спиртов, не имеет существенного значения, хотя в основном желательно, чтобы продукты являлись фармацевтически безопасными. Любое упоминание любого соединения по настоящему изобретению включает упоминание его физиологически приемлемой соли. Примеры физиологически приемлемых солей соединений по настоящему изобретению включает соли, полученные с использованием соответствующего основания, такие как соли щелочного металла (например, натрия), щелочно-земельного металла (например, магния), аммония и NX4+ (где X означает C1-C4 алкил). Физиологически приемлемые соли по водородному атому или аминогруппе включают соли органических карбоновых кислот, таких как уксусная, бензойная, молочная,фумаровая, винная, малеиновая, малоновая, яблочная, изетионовая, лактобионовая и янтарная кислоты; органических сульфокислот, таких как метансульфокислота, этансульфокислота, бензолсульфокислота и паратолуолсульфокислота; и неорганических кислот, таких как хлористо-водородная, серная, фосфорная и сульфаминовая кислоты. Физиологически приемлемые соли соединения по гидроксильной группе включают анион упомянутого соединения в комбинации с подходящим катионом, таким как Na+ и NX4+(где X независимо выбирают из водорода и С 1-С 4 алкильной группы). Соли активных компонентов соединений по настоящему изобретению, предназначенные для терапевтического применения, должны быть физиологически приемлемыми, то есть представлять собой соли, полученные из физиологически приемлемых кислоты или основания. Однако можно также использовать соли физиологически неприемлемых кислот и оснований, например, при получении или очистке физиологически приемлемого соединения. Все соли, независимо от того, является ли соль или основание физиологически приемлемыми, включены в объем настоящего изобретения."Алкил" означает С 1-С 18 углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода. Примеры включают метил (Me, -CH3), этил (Et, -CH2CH3), 1-пропил (n-Pr, нпропил, -СН 2 СН 2 СН 3), 2-пропил (i-Pr, изопропил, -СН 2(СН 3)2, 1-бутил (n-Bu, н-бутил, -СН 2 СН 2 СН 2 СН 3),2-метил-1-пропил (i-Bu, изобутил, -СН 2 СН(СН 3)2, 2-бутил (s-Bu, вторбутил, -СН 2(СН 3)СН 2 СН 3), 2-метил 2-пропил (t-Bu, трет-бутил, -С(СН 3)3), 1-пентил (н-пентил, -СН 2 СН 2 СН 2 СН 2 СН 3), 2-пентил (-СН(СН 3)"Алкенил" означает С 2-С 18 углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода и по крайней мере одну ненасыщенную связь, то есть углерод-углеродную sp2 двойную связь. Примеры включают, без ограничения перечисленным, этилен или винил (-СН=СН 2), аллил (-СН 2 СН=СН 2), циклопентил (С 5 Н 7) и 5-гексенил (-СН 2 СН 2 СН 2 СН 2 СН=СН 2)."Алкинил" означает С 2-С 18 углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода и по крайней мере одну ненасыщенную связь, то есть углерод-углеродную sp тройную связь. Примеры включают, без ограничения перечисленным ацетиленовую (-CСН) и пропаргиловую (-СН 2 ССН) группы. Термины "алкилен" и "алкилдиил" означают насыщенный, разветвленный или неразветвленный,или циклический углеводородный радикал, содержащий от 1 до 18 атомов углерода и включающий два моновалентных радикала, полученных при удалении двух атомов водорода от одного или двух разных атомов углерода в исходном алкане. Типичные алкиленовые радикалы включают, без ограничения перечисленным, метилен (-СН 2-), 1,2-этил (-СН 2 СН 2-), 1,3-пропил (-СН 2 СН 2 СН 2-), 1,4-бутил (-СН 2 СН 2 СН 2 СН 2-) и т.п."Алкенилен" означает ненасыщенный углеводородный радикал с разветвленной или прямой цепью или циклический радикал, содержащий 2-18 атомов углерода и две валентности, образующиеся при удалении двух атомов водорода у одного и того же атома углерода или у двух различных атомов углерода в исходном алкене. Типичные алкениленовые радикалы включают, без ограничения перечисленным, 1,2 этилен (-СН=СН-)."Алкинилен" означает ненасыщенный углеводородный радикал с разветвленной или прямой цепью или циклический радикал, содержащий 2-18 атомов углерода и две валентности, образующиеся при удалении двух атомов водорода у одного и того же атома углерода или у двух различных атомов углерода в исходном алкине. Типичные алкиниленовые радикалы включают, без ограничения перечисленным, ацетилен (-CC-), пропаргил (-CH2CC-) и 4-пентинил (-CH2CH2CH2CCH)."Арил" означает моновалентный ароматический углеводородный радикал, содержащий 6-20 атомов углерода, образующийся при удалении одного атома водорода у одного атома углерода в исходной ароматической кольцевой системе. Типичные арильные группы включают, без ограничения перечисленным,производные бензола, замещенного бензола, нафталина, антрацена, бифенила и т.п. Термин "гетероарил" означает моновалентный ароматический радикал, состоящий из одного или более атомов углерода и одного или более атомов, выбранных из N, О, S или Р, полученный при удалении одного атома водорода от одного циклического атома в исходной ароматической системе. Гетероарильные группы включают моноцикл, содержащий от 3 до 7 атомов в цикле (от 2 до 6 атомов углерода и от 1 до 3 гетероатомов, выбранных из N, О, Р и S), или бицикл, содержащий от 7 до 10 атомов в цикле (от 4 до 9 атомов углерода и от 1 до 3 гетероатомов, выбранных из N, О, Р и S). Гетероарильные бициклы содержат от 7 до 10 атомов в цикле (от 6 до 9 атомов углерода и от 1 до 2 гетероатомов, выбранных из N,О и S), расположенных в виде бициклической системы [4,5], [5,5], [5,6] или системы [6,6], или от 9 до 10 атомов в цикле (от 8 до 9 атомов углерода и от 1 до 2 гетероатомов, выбранных из N и S), расположенных в виде бициклической системы [5,6] или [6,6]. Гетероарильную группу присоединяют к структурекаркасу лекарственного средства пригодной ковалентной связью через атом углерода, азота, серы, фосфора или другой атом. Гетероарильные группы включают, например, пиридил, изомеры дигидропиридила, пиридазинил,пиримидинил, пиразинил, s-триазинил, оксазолил, имидазолил, тиазолил, изоксазолил, пиразолил, изотиазолил, фуранил, тиофуранил, тиенил и пирролил."Арилалкил" означает ациклический алкильный радикал, в котором один из атомов водорода, присоединенный к атому углерода, обычно к терминальному или sp3 атому углерода, заменен на арильный радикал. Типичные арилалкильные радикалы включают, без ограничения перечисленным, бензил, 2 фенилэтан-1-ил, 2-фенилэтен-1-ил, нафтилметил, 2-нафтилэтан-1-ил, 2-нафтилэтен-1-ил, нафтобензил, 2 нафтофенилэтан-1-ил и т.п. Арилалкильная группа включает от 6 до 20 атомов углерода, например, алкильный остаток, включающий алканильные, алкенильные или алкинильные группы, причем арилалкильная группа содержит от 1 до 6 атомов углерода, а арильный остаток от 5 до 14 атомов углерода. Замещенные заместители, такие как "замещенный алкил", "замещенный арил" и "замещенный арилалкил" означают алкил, арил и арилалкил, соответственно, в которых один или более атомов водорода каждый независимо замещен заместителем. Типичные заместители включают, без ограничения перечисленным, -X, -R, -О-, -OR, -SR, -S-, -NR2, -NR3, =NR, -CX3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2,=N2, -N3, NC(=O)R, -C(=O)R, -C(=O)NRR, -S(=O)2O-, -S(=O)2OH, -S(=O)2R, -OS(=O)2OR, -S(=O)2NR,-6 011399-S(=O)R, -OP(=O)O2RR, -P(=O)O2RR, -P(=O)(O-)2, -P(=O)(OH)2, -C(=O)R, -C(=O)X, -C(S)R, -C(O)OR,-C(O)O-, -C(S)OR, -C(O)SR, -C(S)SR, -C(O)NRR, -C(S)NRR, -C(NR)NRR, где каждый X независимо означает галоген, F, Cl, Br или I, a каждый R независимо означает -Н, алкил, арил, гетероцикл или остаток пролекарства. Алкилен, алкенилен и алкинилен могут быть также аналогичным образом замещены. Термин "гетероцикл" означает насыщенную, ненасыщенную или ароматическую циклическую систему, включающую по крайней мере один атом N, О, S или Р. Таким образом, гетероцикл включает гетероарильные группы. Термин "гетероцикл", использованный в данном описании, включает, например, без ограничения перечисленным, гетероциклы, описанные в книгах Paquette Leo A., "Priciples of Modern Heterocyclic Например, гетероцикл, связанный через атом углерода, присоединен, без ограничения перечисленным, в положениях 2, 3, 4, 5 или 6 пиридина, в положениях 3, 4, 5 или 6 пиридазина, в положениях 2, 4, 5 или 6 пиримидина, в положениях 2, 3, 5 или 6 пиразина, в положениях 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, в положениях 2, 4 или 5 оксазола, имидазола или тиазола, в положениях 3, 4 или 5 изоксазола, пиразола или изотиазола, в положениях 2 или 3 азиридина, в положениях 2, 3 или 4 азетидина, в положениях 2, 3, 4, 5, 6, 7 или 8 хинолина или в положениях 1, 3, 4, 5, 6, 7 или 8 изохинолина. Наиболее типичные гетероциклы, связанные через атом углерода,включают 2-пиридил, 3-пиридил, 4-пиридил, 5-пиридил, 6-пиридил, 3-пиридазинил, 4-пиридазинил, 5 пиридазинил, 6-пиридазинил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 6-пиримидинил, 2 пиразинил, 3-пиразинил, 5-пиразинил, 6-пиразинил, 2-тиазолил, 4-тиазолил или 5-тиазолил. Например, гетероцикл, связанный через атом азота, присоединен, без ограничения перечисленным,в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола,имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1 Н-индазола, в положении 2 изоиндола или изоиндолина, в положении 4 морфолина и в положении 9 карбазола или -карболина. Наиболее типичные гетероциклы,связанные через атом азота, включают 1-азиридил, 1-азетедил, 1-пирролил, 1-имидазолил, 1-пиразолил и 1-пиперидинил."Карбоцикл" означает насыщенное, ненасыщенное или ароматическое кольцо, содержащее от 3 до 7 атомов углерода в форме моноцикла или от 7 до 12 атомов углерода в форме бицикла. Моноциклические карбоциклы содержат от 3 до 6 циклических атомов, более типично, 5 или 6 циклических атомов. Бициклические карбоциклы содержат от 7 до 12 циклических атомов, например, образующих бицикло[4,5],[5,5], [5,6] или [6,6] систему, или содержат 9 или 10 циклических атомов, образующих бицикло[5,6] или[6,6] систему. Примеры моноциклических карбоциклов включают циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1 циклогекс-2-енил, 1-циклогекс-3-енил, фенил, спирил и нафтил. Таким образом, карбоцикл включает некоторые арильные группы."Связующее звено" или "связь" означает химический остаток, включающий ковалентную связь или цепочку атомов, через которые фосфонатная группа ковалентно присоединена к лекарственному средству. Связующие звенья включают L, расположенный между группой Ar и атомом азота в трициклических соединениях по настоящему изобретению. На формулах, приведенных в данном контексте, связующие звенья обозначены как "link" или "L". Связующие звенья расположены также между фосфорсодержащей-7 011399 группой А 3 и положением группы R1, R2, R3 или R4 в соединениях по настоящему изобретению. Связующие звенья включают, без ограничения перечисленным, такие остатки, как О, S, NR, N-OR, C1-С 12 алкилен, замещенный C1-C12 алкилен, С 2-С 12 алкенилен, замещенный С 2-С 12 алкенилен, С 2-С 12 алкинилен, замещенный С 2-С 12 алкинилен, C(=O)NH, С(=O), S(=O)2, C(=O)NH(CH2)n и (CH2CH2O)n, где n означает 1, 2, 3,4, 5 или 6. Связующие звенья включают также повторяющиеся звенья алкилокси (например, полиэтиленокси, PEG, полиметиленокси) и алкиламино (например, полиэтиленамино, Jeffamine), и сложные эфиры и амиды двухосновных кислот, включающих сукцинат, сукцинамид, дигликолят, малонат и капроамид. Термин "хиральный" относится к молекулам, структура которых не совпадает с их зеркальным отражением, а термин "ахиральный" относится к молекулам, структура которых совпадает с их зеркальным отражением. Термин "стереоизомеры" относится к соединениям с одинаковой химической структурой, но которые отличаются расположением атомов или групп в пространстве."Диастереомер" означает стереоизомер, содержащий два или более центров хиральности, а его молекулы не являются зеркальным отражением друг друга. Диастереомеры отличаются по физическим свойствам, например, характеризуются различными температурами плавления, температурами кипения,спектральными характеристиками и реакционной способностью. Смеси диастереомеров можно разделять с использованием высокоэффективных аналитических методов, таких как электрофорез и хроматография."Энантиомеры" означают два стереоизомера соединения, структуры которых не совпадают с зеркальными отражениями друг друга. Для описания стереохимических определений и терминов использовали рекомендации, представленные в книгах под ред. S.P.Parker, McGraw-Hill Dictionary of Chemical Terms (1984), McGraw-Hill BookSons, Inc., New York. Многие органические соединения существуют в оптически активной форме, то есть они способны вращать плоскость поляризованного света. При описании оптически активных соединений буквы D и L или R и S используют для обозначения абсолютной конфигурации молекулы в хиральном центре (центрах). Знаки d и I, D и L или (+) и (-) используют для обозначения знака вращения плоскополяризованного света соединением, причем знак I или (-) означают, что соединение является левовращающим, а знак (+) или d означает, что соединение является правовращающим. В случае данной химической структуры эти соединения, называемые стереоизомерами, являются идентичными, за исключением случая, когда они являются зеркальным отражением друг друга. Специфический стереоизомер называется также энантиомером, а смесь таких изомеров в большинстве случаев называют энантиомерной смесью. Смесь энантиомеров 50:50 называют рацемической смесью или рацематом, которые не проявляют стереоспецифичность или стереоселективность в химической реакции или процессе. Термины "рацемическая смесь" и "рацемат" относятся к эквимолярной смеси двух энантиомеров, не проявляющей оптическую активность. Соединения, содержащие ингибитор интегразы ВИЧ Описаны новые трициклические соединения, обладающие ингибирующей активностью в отношении интегразы ВИЧ, включая любые фармацевтически приемлемые соли указанных соединений. Один аспект настоящего изобретения включает соединение следующей формулы: где А 1 и А 2 независимо выбирают из ряда: О, S, NR, C(R2)2, CR2OR, CR2OC(=O)R, C(=O), C(=S), CR2SR,C(=NR), C(R2)2-C(R3)2, C(R2)=C(R3), C(R2)2-O, NR-C(R3)2, N=C(R3), N=N, SO2-NR, C(=O)C(R3)2, C(=O)NR,C(R2)2-C(R3)2-C(R3)2, C(R2)=C(R3)-C(R3)2, C(R2)C(=O)NR, C(R2)C(=S)NR, C(R2)=N-C(R3)2, C(R2)=N-NR иAr выбирают из ряда: С 3-С 12 карбоцикл, замещенный С 3-С 12 карбоцикл, С 6-С 20 арил, замещенный С 6 С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил; каждый из R1, R2, R3 и R4 независимо выбирают из ряда: Н, F, Cl, Br, I, ОН, -NH2, -NH3+, -NHR,-NR2, -NR3+, C1-C8 алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7-членный цикличе-8 011399 ский сультам, C1-C8 алкилсульфонат, C1-C8 алкиламино, 4-диалкиламинопиридиний, С 1-С 8 алкилгидроксил, C1-C8 алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7-членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8 алкокси, C1-C8 трифторалкил,C1-C8 алкил, замещенный C1-C8 алкил, С 3-С 12 карбоцикл, замещенный С 3-С 12 карбоцикл, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат и фрагмент пролекарства; две группы R2 или две группы R3, присоединенные к одному атому углерода, могут быть объединены с образованием спироцикла; иR независимо выбирают из ряда: Н, C1-C8 алкил, замещенный С 1-С 8 алкил, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат и фрагмент пролекарства;RX2 независимо выбирают из ряда: Н, C1-C8 алкил, замещенный С 1-С 8 алкил, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат, пролекарство, фармацевтически приемлемое пролекарство, фрагмент пролекарства, защитная группа и фосфонатный фрагмент пролекарства; и соли, сольваты, индивидуальные энантиомеры и их очищенные диастереомеры; при условии, если Y=Z означает С=С(ОН), X означает О, А 1 означает С(=O), А 2 означаетC(R2)=C(R3), и Q означает СН, то L не означает связь. Один аспект настоящего изобретения включает соединения в предварительно определенной конфигурации с ограниченным набором конформаций, который включает активную форму соединения, позволяющую ингибировать нуклеарную интеграцию ДНК после обратной транскрипции ВИЧ. Настоящее изобретение включает трициклические соединения, представленные следующей формулой: Каждая из групп А 1 и А 2 независимо означает остаток, образующий 5-, 6- или 7-членный цикл. Группы А 1 и А 2 независимо выбирают из ряда: О, S, MR, C(R2)2, CR2OR, CR2OC(=O)R, C(=O), C(=S),CR2SR, C(=NR), C(R2)2-C(R3)2, C(R2)=C(R3), C(R2)2-O, NR-C(R3)2, N=C(R3), N=N, SO2-NR, C(=O)C(R3)2,C(=O)NR, C(R2)2-C(R3)2-C(R3)2, C(R2)=C(R3)-C(R3)2, C(R2)C(=O)NR, C(R2)C(=S)NR, C(R2)=N-C(R3)2,C(R2)=N-NR и N=C(R3)-NR. Две группы R2 или две группы R3, присоединенные к одному атому углерода, могут быть объединены с образованием спироцикла.L означает связь или любое связующее звено, через которое группа Ar коваленто присоединена к трициклической структуре-каркасу. Например, L означает связь, О, S, S-S (дисульфид), S(=O) (сульфоксид), S(=O)2 (сульфон), S(=O)2NR (сульфонамид), NR, N-OR, C1-C12 алкилен, замещенный С 1-С 12 алкилен,С 2-С 12 алкенилен, замещенныйС 2-С 12 алкенилен, С 2-С 12 алкинилен, замещенный С 2-С 12 алкинилен,C(=O)NH, OC(=O)NH, NHC(=O)NH, C(=O), C(=O)NH(CH2)n или (CH2CH2O)n, где n означает 1, 2, 3, 4, 5 или 6. Замещенный алкилен, замещенный алкенилен, замещенный алкинилен, замещенный арил и замещенный гетероарил независимо замещены одним или более заместителями, которые выбирают из ряда:X выбирают из ряда: О, S, NH, NR, N-OR, N-NR2, N-CR2OR или N-CR2NR2. Группы Ar означают любой насыщенный, ненасыщенный или ароматический цикл, или систему циклов, включающую моно- или бициклический карбоцикл или гетероцикл, например, цикл, содержащий от 3 до 12 циклических атомов. Циклы, содержащие 3 атома, являются насыщенными; циклы, содержащие 4 атома, являются насыщенными или моно-ненасыщенными; циклы, содержащие 5 атомов,являются насыщенными или моно-, или диненасыщенными; и циклы, содержащие 6 атомов, являются насыщенными, моно- или диненасыщенными, или ароматическими. Например, группа Ar означает С 3-С 12 карбоцикл, замещенный С 3-С 12 карбоцикл, С 6-С 20 арил, заме-9 011399 щенный С 6-С 20 арил, С 2-С 20 гетероарил или замещенный С 2-С 20 гетероарил. Примеры вариантов замещенных С 6-С 20 арильных групп включают галоген-замещенный фенил, такой как 4-фторфенил, 4-хлорфенил, 4-трифторметил, 2-амидофенил, 3,5-дихлорфенил и 3,5 дифторфенил. Группы Ar включают замещенные фенильные группы, такие как, без ограничения перечисленным: Другие примеры замещенных фенильных групп включают: где волнистая линия в любой ориентации означает участок ковалентного присоединения к L. Группы Ar включают также дизамещенные фенильные группы, такие как, без ограничения перечисленным: Группы Ar включают также фенил и замещенный фенил, конденсированные с карбоциклом с образованием следующих групп:R независимо выбирают из ряда: Н, C1-C8 алкил, замещенный C1-C8 алкил, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства; группы R1, R2, R3 и R4 могут также принимать значения: -OC(=O)OR, -OC(=O)NR2, -OC(=S)NR2,-OC(=O)NRNR2, -OC(=O)R, -C(=O)OR, -C(=O)NR2, -C(=O)NRNR2, -C(=O)R, -OSO2NR2 (сульфамат), -NR2,-NRSO2R, -NRC(=S)NR2, -SR, -S(O)R, -SO2R, -SO2NR2 (сульфонамид), -OSO2R (сульфонат), -P(=O)(OR)2,-P(=O)(OR)(NR2), -P(=O)(NR2)2, -P(=S)(OR)2, -P(=S)(OR)(NR2), -P(=S)(NR2)2, a также включают замещенные пролекарственные формы указанных соединений. Группа R1 независимо означает: CR3, NRSO2R, OC(=O)NR2, OC(=O)R, SR, H, F, Cl, Br, I, OH, -NH2,+-NH3 , -NHR, -NR2, -NR3+, C1-C8 алкилгалогенид, карбоксилат, сульфат, сульфамат, сульфонат, 5-7 членный циклический сультам, C1-C8 алкилсульфонат, C1-C8 алкиламино, 4-диалкиламинопиридиний, C1C8 алкилгидроксил, C1-C8 алкилтиол, -SO2R, -SO2Ar, -SOAr, -SAr, -SO2NR2, -SOR, -CO2R, -C(=O)NR2, 5-7 членный циклический лактам, 5-7-членный циклический лактон, -CN, -N3, -NO2, C1-C8 алкокси, C1C8 трифторалкил, С 1-С 8 алкил, замещенный C1-C8 алкил, С 3-С 12 карбоцикл, замещенный С 3-С 12 карбоцикл,С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси,фосфонат, фосфат и остаток пролекарства. Примеры вариантов групп R1, R2, R3 и R4 включают следующие формулы: где волнистая линия указывает участок ковалентного присоединения к трициклической структуре.R независимо выбирают из ряда: Н, C1-C8 алкил, замещенный C1-C8 алкил, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил, замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат и остаток пролекарства. Две группы R могут быть объединены с образованием цикла, например, две группы R,присоединенные к атому азота, образуют цикл, такой как азиридинил, азетидинил, пирролидинил, пиразинил, имидазолил, пиперидил, пиперазинил, пиридиний или морфолино. Следующие варианты групп А 1 и А 2 в соединениях по настоящему изобретению включают, без ограничения перечисленным, следующие формулы. На приведенных в качестве примера формулах различные варианты группы А 1 образуют 5-членные циклы На приведенных в качестве примера формулах различные варианты группы А 1 образуют 6-членные циклы На приведенных в качестве примера формулах различные варианты группы А 2 образуют 5-членные циклы На приведенных в качестве примера формулах другие разнообразные варианты группы А 2 образуют 6-членные циклы Соединения по настоящему изобретению включают соединения формул I-III Таким образом, соединения формулы I включают следующую сукцинимидную формулу: Варианты соединений формулы I включают также формулы Ia-b, где группа А 1 означает СН 2 и СН 2 СН 2, соответственно Один аспект настоящего изобретения включает соединения, содержащие циклическую имидную группу, например, 5,9-дигидроксипирроло[3,4-g]хинолин-6,8-дион (Myers et al., патент США No. 5252560; Robinson, патент США No. 5854275), где группа А 1 означает С(=O), а группа X означает О, как показано в формуле Ic- 13011399 Наряду с другими соединениями по настоящему изобретению, функциональные свойства циклической имидной группы соединений формулы Ic обеспечивают предварительно определенное состояние для оптимального ингибирования интегразы ВИЧ, что отличает данные соединения от соединений, не содержащих циклическую имидную группу (Anthony et al., заявка на патент WO 02/30931; Zhuang et al.,"Design and synthesis of 8-hydroxy-1,6-naphthyridines as novel HIV-1 integrase inhibitors" ("Структура и синтез 8-гидрокси-1,6-нафтиридинов в качестве новых ингибиторов интегразы ВИЧ-1"), Interscience Conference on Antimicrobial Agents and Chemotherapy, San Diego, CA, Sept. 27-30, 2002). Соединения формулы Ia включают следующую амидную структуру: Группы R1, R2, R3 или R4 независимо включают фосфонатную группу или фосфонатный остаток пролекарства. Трициклическое соединение по настоящему изобретению, содержащее ингибитор интегразы, включает одну или несколько фосфонатных групп или фосфонатных остатков пролекарства. Например, группа R1, R2, R3 или R4 содержит остаток формулы А 3, где А 3 означаетRy независимо означает Н, C1-C6 алкил, замещенный C1-C6 алкил, арил, замещенный арил или защитную группу. В другом варианте, две соседние группы Ry, присоединенные к одному атому углерода,объединены с образованием цикла, т.е. спироуглерода. Данный цикл состоит только из атомов углерода,например, циклопропил, циклобутил, циклопентил или циклогексил, или, в другом варианте, цикл содержит один или более гетероатомов, например, пиперазинил, пиперидинил, пиранил или тетрагидрофурил. Варианты соединений формулы I включают также формулы Ia-с, где группа А означает СН 2,СН 2 СН 2 и СН 2 СН 2 СН 2, соответственно Если группа А образует 7-членный цикл, то данный 7-членный цикл содержит вторую амидную группу, как показано на примере формулы Id- 14011399 Один аспект настоящего изобретения включает соединения, содержащие циклическую имидную группу, например, 5,9-дигидроксипирроло[3,4-g]хинолин-6,8-дион (Myers et al., патент США No. 5252560; Robinson, патент США No. 5854275), где группа А означает С(=O), а группа X означает О, как показано в формуле Ie Наряду с другими соединениями по настоящему изобретению, функциональные свойства циклической имидной группы соединений формулы Ie обеспечивают предварительно определенное состояние для оптимального ингибирования интегразы ВИЧ, что отличает данные соединения от соединений, не содержащих циклическую имидную группу (Anthony et al., заявка на патент WO 02/30931; Zhuang et al.,"Design and synthesis of 8-hydroxy-1,6-naphthyridines as novel HIV-1 integrase inhibitors" ("Структура и синтез 8-гидрокси-1,6-нафтиридинов в качестве новых ингибиторов интегразы ВИЧ-1"), Interscience Conference on Antimicrobial Agents and Chemotherapy, San Diego, CA, Sept. 27-30, 2002). Соединения формулы Ia включают следующую амидную структуру: Группы R1, R2, R3 или R4 независимо включают фосфонатную группу или фосфонатный фрагмент пролекарства. Трициклическое соединение по настоящему изобретению, содержащее ингибитор интегразы, включает одну или несколько фосфонатных групп или фосфонатных фрагментов пролекарства. Например, группа R1, R2, R3 или R4 содержит остаток формулы А 3, где А 3 означаетRy независимо означает Н, C1-C6 алкил, замещенный C1-C6 алкил, арил, замещенный арил или защитную группу. В другом варианте, две соседние группы Ry, присоединенные к одному атому углерода,объединены с образованием цикла, т.е. спироуглерода. Данный цикл состоит только из атомов углерода,например, циклопропил, циклобутил, циклопентил или циклогексил, или, в другом варианте, цикл содержит один или более гетероатомов, например, пиперазинил, пиперидинил, пиранил или тетрагидрофурил.Rx независимо означает Н, C1-C6 алкил, замещенный C1-C6 алкил, С 6-С 20 арил, замещенный С 6 С 20 арил или защитную группу, или соединение следующей формулы: М 1 а, М 1c и M1d независимо означают 0 или 1. М 12 с означает 0, 1, 2, 3, 4, 5, 6, 7, 8,9, 10, 11 или 12. Связующее звено расположено между положениями групп R1, R2, R3 или R4 и заместителем А 3. Связующее звено означает О, S, NR, N-OR, C1-С 12 алкилен, замещенный C1-C12 алкилен, С 2-С 12 алкенилен,замещенный С 2-С 12 алкенилен, С 2-С 12 алкинилен, замещенный С 2-С 12 алкинилен, C(=O)NH, С(=O), S(=O)2,C(=O)NH(CH2)n и (CH2CH2O)n, где n означает 1, 2, 3, 4, 5 или 6. Связующие звенья означают также повторяющиеся звенья алкилокси (например, полиэтиленокси, ПЭГ, полиметиленокси) и алкиламино (на- 15011399 пример, полиэтиленамино, Jeffamine); а также сложный эфир двухосновной кислоты и амиды, включая сукцинат, сукцинамид, дигликолят, малонат и капроамид. Например, на приведенных в качестве примера формулах связующее звено включает пропаргил, мочевину или алкоксигруппы и формулу, где М 12b означает 1, Y1 означает кислород, Y2b независимо означает кислород (О) или азот (N(Rx, такую как где W5 означает карбоцикл, такой как фенил или замещенный фенил, a Y2c независимо означает О,N(R ) или S. Например, R1 означает Н, а n означает 1. Другой вариант формулы А 3 включает где Y2b означает О или N(Rx); M12d означает 1, 2, 3, 4, 5, 6, 7 или 8; R1 означает Н или C1-C6 алкил; и в фенильный карбоцикл вводят от 0 до 3 групп R2, где R2 означает C1-C6 лкил или замещенный алкил. Такие варианты формулы А 3 включают фенилфосфонамидат аминокислоты, например, сложные эфиры аланина и фенилфосфонатные эфиры молочной кислоты: Соединения по настоящему изобретению включают также один или более остатков пролекарства,расположенных в качестве ковалентно присоединенных заместителей в любом месте или участке, например, в группе Ar, L, X, A, R1, R2, R3, R4 или 9-гидроксил. Определенный заместитель, который модифицируют в остаток пролекарства, означает фосфонат, фосфат, фосфинат или другие фосфорсодержащие функциональные группы (Oliyai et al., Pharmaceutical Res. (1999), 16, 1687-1693; Krise J. and Stella V.,Adv. Drug Del. Reviews (1996), 19, 287-310; Bischofberger et al., патент США No. 5798340). Остатки пролекарства с фосфорсодержащими функциональными группами используют для маскирования анионных зарядов и уменьшения полярности. Фосфонатная группа пролекарства означает эфир (Oliyai et al., Intl.Jour. Pharmaceutics (1999), 179, 257-265), например, РОС и РОМ (пивалоилоксиметил, Yuan et al., Pharmaceutical Res. (2000), 17, 1098-1103) или амидат, которые высвобождаются in vivo из соединения, содержащего ингибитор интегразы, или при инкубации in vitro c биологическими объектами, например, с клетками или тканями. Такое отщепление группы пролекарства происходит в гидролитических условиях при окислении и действии ферментов или комбинации указанных условий. Соединения по настоящему изобретению, содержащие один или более групп пролекарства, увеличивают или оптимизируют биодоступность соединений, используемых в качестве терапевтических агентов. Например, при пероральном введении биодоступность является предпочтительной и зависит от устойчивости к метаболической деградации в желудочно-кишечном тракте и сердечно-сосудистой системе и к возможному включению в клетки. Предполагается, что группы пролекарства придают выше указанную устойчивость за счет замедле- 17011399 ния некоторых гидролитических или ферментативных метаболических процессов. Липофильные группы пролекарства могут также ускорять активный или пассивный транспорт соединений по настоящему изобретению через клеточные мембраны (Darby G., Antiviral Chem. and Chemotherapy (1995), Supp. 1, 6, 5463).RX2 независимо выбирают из ряда: Н, C1-C8 алкил, замещенный C1-С 8 алкил, С 6-С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил и замещенный С 2-С 20 гетероарил, полиэтиленокси, фосфонат, фосфат, пролекарство, фармацевтически приемлемое пролекарство, остаток пролекарства, защитная группа и фосфонатный остаток пролекарства; предпочтительно Н, пролекарство или защитная группа; более предпочтительно Н или пролекарство; еще более предпочтительно RX2 означает Н. Примеры вариантов воплощения настоящего изобретения включают пролекарства в виде фосфонамидатов и фосфорамидатов (обозначаемых как "амидаты") пролекарств. Основные формулы фосфонамидатов и фосфорамидатов пролекарств включают: Атом фосфора фосфонамидатной группы присоединен к атому углерода. Заместитель R5, присоединенный к атому азота, означает сложно эфирную, амидную или карбаматную функциональную группу. Например, R5 означает -CR2C(=O)OR', где R' означает Н, C1-C6 алкил, замещенный C1-C6 алкил, С 6 С 20 арил, замещенный С 6-С 20 арил, С 2-С 20 гетероарил или замещенный С 2-С 20 гетероарил. Примеры фосфонамидатов и фосфорамидатов пролекарств включают: где группа R5 означает -CR2CO2R7, где R6 и R7 независимо означают Н или C1-C8 алкил. Атом азота может входить в состав аминокислотного остатка пролекарства, такого как глицин, аланин или сложный эфир валина (например, валацикловир, см.: Beauchamp et. al., Antiviral Chem. Chemotherapy (1992) 3:157-164), такие, как соединения общей формулы: где R' означает боковую цепь аминокислоты, например, Н, СН 3, СН(СН 3)2 и т.д. Пример варианта фосфонамидата пролекарства означает: Другой вариант воплощения настоящего изобретения включает трициклическое соединение по настоящему изобретению, содержащее ингибитор интегразы ВИЧ, которое обладает способностью накапливаться в клетках РВМС человека (периферических мононуклеарах крови). РВМС означает клетки крови, содержащие сферические лимфоциты и моноциты. С физиологической точки зрения РВМС являются ключевыми компонентами в механизме противодействия инфекции. Клетки РВМС выделяют из гепаринизированной цельной крови здоровых доноров или из лейкоцитных пленок стандартным центрифугированием в градиенте плотности с последующим сбором клеток на разделе фаз и промывкой (например,фосфатно-солевым раствором), и хранят в замороженном состоянии. Клетки РВМС культивируют в многолуночных планшетах. При культивировании в различные периоды времени супернатант отбирают для анализа, либо собирают для исследования (Smith R. et al., (2003) Blood, 102 (7), 2532-2540). Соединения по настоящему изобретению включают также фосфонат или фосфонатное пролекарство. Обычно фосфонат или фосфонатное пролекарство характеризуется формулой А 3, как описано в данном контексте.- 18011399 По выбору, соединение по данному варианту воплощения настоящего изобретения характеризуется повышенным периодом полупревращения соединений или продуктов их метаболизма внутри клеток РВМС человека по сравнению с аналогами соединений, не содержащих фосфонат или фосфонатное пролекарство. Обычно, период полупревращения повышается по крайней мере приблизительно на 50%, или более предпочтительно в интервале 50-100%, еще более предпочтительно по крайней мере приблизительно на 100%, наиболее предпочтительно более 100%. В другом варианте воплощения настоящего изобретения внутриклеточный период полупревращения метаболитов соединения в клетках РВМС человека увеличивается по сравнению с аналогичным соединением, не содержащим фосфоната или фосфонатного лекарства. В таких вариантах воплощения настоящего изобретения метаболит обычно образуется внутри клетки, более предпочтительно внутри клеток РВМС человека. Еще более предпочтительно метаболит является продуктом расщепления фосфонатного пролекарства внутри РВМС человека. Наиболее предпочтительно фосфонатное пролекарство расщепляется с образованием метаболита, характеризующегося по крайней мере одним отрицательным зарядом при физиологической величине рН. Наиболее предпочтительно фосфонатное пролекарство отщепляется под действием фермента внутри клеток РВМС человека с образованием фосфоната, содержащего по крайней мере один активный атом водорода в форме Р-ОН. Соединения по настоящему изобретению можно модифицировать по участку связывания и таким образом оптимизировать связывающую способность других известных ингибиторов интегразы ВИЧ. При связывании ингибитора с активным центром фермента-мишени интегразы ВИЧ, ингибитор приобретает конформацию с низкой энергией (называемую также конформацией связывания) и взаимодействует в пределах активного центра. В основном, лиганды молекул, содержащих несколько ротационных связей,существуют в нескольких конформационных состояниях, большинство из которых не связывается с активным центром. Чем больше число возможных конформаций лиганда, тем ниже эффективность энтропийного вклада в свободную энергию связывания и, таким образом, ниже способность связывания. Один аспект при создании предварительно определенных соединений, содержащих ингибитор интегразы, заключается в введении конформационных ограничений, которые уменьшают общее число конформационных состояний и позволяют получить ингибитор с высокой связывающей способностью (Lam P.Y.S. etal., Jour. Amer. Chem. Soc. (2000), 122, 9648-9654; Chen J.M. et al., патент США 6187907; Chen J.M. et al.,Bio. Org. Med. Chem. Letters (2002), 12, 1195-1198). С учетом одной или более предпочтительных, т.е. низкоэнергетических конформаций участка связывания можно рационально планировать синтез активных соединений и исключить получение неактивных производных. Специалистам в данной области техники известно, что соединения по настоящему изобретению существуют в различных протонированных состояниях в зависимости от рН раствора и других факторов. В то время, как на структурных формулах, приведенных в данном контексте, соединения показаны только в одном из возможных протонированных состояний, следует понимать, что данные формулы приведены только для иллюстрации, и настоящее изобретение не ограничивается каким-либо определенным протонированным производным, и в область настоящего изобретения включены все протонированные формы данных соединений. Соединения по настоящему изобретению по выбору включают соли соединений, указанных в данном контексте, прежде всего фармацевтически приемлемые нетоксичные соли, содержащие, например,Na+, Li+, K+, Ca+2 и Mg+2. Такие соли включают соли, образованные при присоединении подходящих катионов, таких как ионы щелочных или щелочно-земельных металлов или ионы аммония и четвертичных аминов, к остатку аниона кислоты, как правило, карбоновой кислоты. Соединения по настоящему изобретению могут содержать несколько положительных или отрицательных зарядов. Полный заряд соединений по настоящему изобретению может быть как положительным, так и отрицательным. Тип связанных противоионов, в основном, зависит от способа синтеза и/или выделения, с помощью которых получают данные соединения. Типичные противоионы включают, без ограничения перечисленным, аммоний,натрий, калий, литий, галогениды, ацетат, трифторацетат и т.д., и их смеси. Следует понимать, что идентификация любого связанного противоиона не является определяющим признаком настоящего изобретения, и в объем настоящего изобретения включены соединения, содержащие противоион любого типа. Более того, так как соединения могут существовать в различных формах, настоящее изобретение включает не только формы соединений, которые содержат связанный противоион (например, сухие соли), но и формы соединений, которые не связаны с противоионами (например, водные или органические растворы). Соли металлов, в основном, получают при взаимодействии гидроксида металла с соединением по настоящему изобретению. Примерами солей металлов, которые получают этим способом, являются соли,содержащие Li+, Na+ и K+. Менее растворимые соли металлов осаждают из раствора более растворимой соли при добавлении пригодного соединения металла. Кроме того, соли получают в виде кислотноаддитивных солей, полученных при взаимодействии органических и неорганических кислот, например,HCl, HBr, H2SO4, H3PO4 или органических сульфокислот с основными фрагментами, например, с аминами или с кислотными группами. Таким образом композиции, указанные в данном контексте, включают- 19011399 соединения по настоящему изобретению в их ионизованной форме, а также в цвиттерионной форме и в комбинации со стехиометрическими количествами воды в форме гидратов. Настоящее изобретение включает также соли исходных соединений, полученные при взаимодействии с одной или более аминокислотами, прежде всего природными аминокислотами, которые являются компонентами белков. К аминокислотам, в основном, относятся соединения, в боковой цепи которых содержится группа, обладающая основными или кислотными свойствами, например, лизин, аргинин или глутаминовая кислота, или нейтральная группа, такая как глицин, серин, треонин, аланин, изолейцин или лейцин. Соединения по настоящему изобретению в некоторых случаях образуют также как таутомерные резонансные изомеры. Как правило, на формулах, приведенных в данном контексте, в качестве примера показана только одна таутомерная или резонансная форма соединений. Например, гидразины, оксимы,гидразоны показаны либо в син-, либо в антиконфигурациях. Подразумевается также соответствующая альтернативная конфигурация. Настоящее изобретение включает все таутомерные и резонансные формы. Определенный энантиомер соединения по настоящему изобретению выделяют в чистой форме, в основном не содержащей противоположного энантиомера, например, с использованием оптически активных индивидуальных агентов для разделения изомеров (Stereochemistry of Carbon Compounds (1962),E.L. Eliel, McGraw Hill, Lochmuller C.H., J. Chromatogr. (1975), 113 (3), 283-302). Разделение рацемической смеси диастереомеров проводят любым пригодным способом, включая: (1) образование ионных диастереомерных солей с хиральными соединениями и их разделение фракционной кристаллизацией или другими способами, (2) образование диастереомерных соединений с хиральными производными, разделение диастереомеров и превращение их в чистые энантиомеры. В другом варианте энантиомеры разделяют непосредственно в хиральных условиях, способ (3). Согласно способу (1) диастереомерные соли получают по реакции энантиомерно чистых хиральных оснований, таких как бруцин, хинин, эфедрин, стрихнин, -метилфенилэтиламин (амфетамин) и т.п. с ассиметричными соединениями, обладающими кислотными свойствами, такими как карбоновая кислота и сульфокислота. Разделение диастереомерных солей проводят фракционной кристаллизацией или ионной хроматографией. При разделении оптических изомеров аминосоединений добавление хиральных карбоновых или сульфокислот, таких как, камфорсульфокислота, винная кислота, миндальная кислота или молочная кислота, приводит к образованию диастереомерных солей. В другом варианте согласно способу (2) выделяемый субстрат взаимодействует с одним энантиомером хирального соединения с образованием диастереомерной пары (Eliel E. and Wilen S. (1994), Stereochemistry of Organic Compounds, John WileySons, Inc., стр. 322). Диастереомерные соединения получают по реакции ассиметричных соединений с энантиомерно чистыми производными хиральных реагентов, такими как производные ментила, с последующим разделением диастереомеров и гидролизом для получения чистого обогащенного энантиомером ксантена. Способ определения оптической чистоты включает получение хиральных сложных эфиров, таких как сложный эфир ментила или эфир Мошера,-метокси(трифторметил)фенилацетат (Jacob III (1982), J. Org. Chem., 47, 4165), из рацемической смеси и анализ ЯМР-спектра для определения присутствия двух атропизомерных диастереомеров. Стабильные диастереомеры фракционируют и выделяют обычной и обращенно-фазной хроматографией с использованием методов разделения атропизомеров нафтилизохинолинов (Ноуе Т., заявка на патент WO 96/15111). Согласно способу (3) рацемическую смесь двух ассиметричных энантиомеров разделяют хроматографией с использованием хиральной стационарной фазы (Chiral Liquid Chromatography (1989) W. J.phase", J. of Chromatogr., 513, 375-378). Энантиомеры идентифицируют способами, используемыми для идентификации других хиральных молекул с ассиметричным атомом углерода, такими как оптическое вращение и круговой дихроизм. Получение соединений, содержащих ингибитор интегразы ВИЧ Соединения по настоящему изобретению получают различными способами синтеза, известными специалистам в данной области техники. Настоящее изобретение включает также способы получения соединений по настоящему изобретению. Соединения получают по любой подходящей методике органического синтеза. В данной области техники известно много способов синтеза. Множество методик описано в сборниках: "Compendium of Organic Synthetic Methods", John Wiley and Sons, New York, т.1, IanYork, 1985; "Comprehensive Organic Synthsis. Selectivety, Strategy and Efficiency in Modern Organic Chemistry" (9 томов) Barry M. Trost, гл. изд. (Editor-in-Chief), Pergamon Press, New York, 1993. В данном контексте в качестве примеров приведен ряд способов получения соединений формул IIV по настоящему изобретению. Данные способы приведены для иллюстрации сущности изобретения и- 20011399 не ограничивают объем изобретения. Для защиты реакционноспособных функциональных групп и блокирования региоселективных реакций используют защитные группы (Green et al. (1991), "Protective Groups in Organic Synthesis", 2-ое издание, John Wiley and Sons). Например, защитные группы, используемые для 8-гидроксильной группы и других гидроксильных заместителей, включают метил, MOM (метоксиметил), триалкилсилил, бензил,бензоил, тритил и тетрагидропиранил. Для предотвращения замещения блокируют определенные положения арильного кольца, например, положение 2 защищают от фторирования. Соединения формулы I На схемах 1-10 и 15-17, представленных ниже в качестве примеров, показаны способы синтеза соединений формулы I. Один способ синтеза соединений формулы I по настоящему изобретению заключается в циклизации сукцинимидного производного с пиридиндикарбоксилатом с образованием трициклических соединений (Murray and Semple, Synthesis (1996), 11, 80-82, Jones and Jones, Jour. Chem. Soc,Perkin Transactions I (1973), 26-32) согласно схеме 1. Схема 1 В другом варианте сукцинимид с лабильной защитной группой (Р), присоединенной к атому азота,взаимодействует пиридиндикарбоксилатом. Группа Р означает защитную группу, такую как триалкилсилил, которая отщепляется в кислотных условиях. Триалкилсилильные группы удаляют также в присутствии фторсодержащих реагентов. После удаления Р, различные группы Ar-L ковалентно присоединяют согласно схеме 2: Схема 2 Имидные соединения восстанавливают растворимыми восстановителями на основе металлов, например, Zn, или гидридными реагентами, например, NaBH4, с образованием лактама. Примеры региоселективных превращений показаны на схеме 3: Схема 3 Имидные соединения восстанавливают также в мягких условиях до гидроксилактама. Показано, что восстановление ассиметричных имидов с использованием боргидрида натрия и солей церия или самария- 21011399 является региоселективным процессом (Mase et al., J. Chem. Soc. Perkin Communication 1 (2002), 707-709),как показано в верхней части схемы 4. Для получения алкилгидроксилактамовых соединений к карбонилимиду добавляют также региоселективные реагенты Гриньяра и ацетиленовые анионы (Chihab-Eddine etal., Tetrahedron Lett. (2001), 42, 573-576), как показано в нижней части схемы 4. Для проведения указанных реакций кислородсодержащие фенольные группы можно защищать и затем при необходимости удалять защитные группы. Схема 4 Согласно другому способу синтеза в настоящем изобретении используют промежуточные замещенные хинолины (Clemence et al., патент США No. 5324839, Billhardt-Throughton et al., патент США No. 5602146, Matsumura, J. Amer. Chem. Soc. (1935), 57, 124-128) общей формулы: 5,8-Дигидроксихинолины получают согласно схеме 5. Схема 5- 22011399 Циклический ангидрид, показанный ниже, в региоселективных условиях этерифицируют с образованием соединений по настоящему изобретению, например, согласно схеме 6, где MOM означает метоксиметил, а X означает, например, С(=O), CRC(=O), C(=O)C(=O) и SO2. См. статью Ornstein et al., Jour.Med. Chem. (1989), 32, 827-833. Аналогичные химические реакции проводят при синтезе 5-членного лактама в контролируемых региоселективных условиях, как показано на схеме 7: Схема 7 Циклический имид алкилируют стандартным способом, ацилируют или другим образом вводят в реакцию с образованием множества соединений, содержащих группы Ar-L: Группу Ar-L присоединяют в качестве реакционноспособной группы, например, в качестве алкилирующего реагента типа бензилбромида (Ar означает фенил, L означает СН 2) или сульфонирующего агента типа 4-метоксифенилсульфонилхлорида (Ar означает 4-метоксифенил, L означает S(=O)2). В другом варианте группу Ar-L присоединят по многостадийному процессу. Например, имидный атом азота взаимодействует с сульфирующим реагентом, таким как 2,2-дипиридилдисульфид с образованием Nсульфидного промежуточного соединения (Ar означает 2-пиридил, L означает S). Такое промежуточное соединение далее превращают в различные группы Ar-L, где L означает S, S(=O) или S(=O)2. Другой вариант синтеза соединений по настоящему изобретению включает получение 7 замещенных промежуточных соединений 8-хинолинола (Zhuang et al., заявка на патент WO 02/36734,Vaillancourt et al., патент США No. 6310211, Hodel, патент США No. 3113135), соответствующих общем формулам, включая арилзамещенные соединения: Образование третьего 5-7-членного цикла проводят при соответствующем выборе арильных заместителей циклической хинолиновой системы, используя известные синтетические превращения для получения соединений формулы I. Например, в данной области техники известны способы конденсации карбоновых кислот и других активированных ацильных групп с аминами с образованием карбоксамидов(March J., Advanced Organic Chemistry. 3-е издание, Jonh Wiley and Sons, 1985, стр. 370-376). Пример циклизации включает следующее превращение: На схеме 8 ниже показан другой вариант синтеза соединений по настоящему изобретению, т.е. соединений формулы I. Данный способ включает циклизацию 2-О-защищенного соединения 3-галогенанилина с ,-ненасыщенным карбонильным соединением с образованием функционально-активного хинолина. ,-Ненасыщенное карбонильное соединение является альдегидом (X означает Н), кетоном (X означает R), сложным эфиром (X означает OR), амидом (X означает NR2), ацилгалогенидом (X означаетCl) или ангидридом. При карбонилировании над палладиевым катализатором получают сложный эфир,который превращают в функциональное амидное соединение, которое циклизуют для получения 5-, 6 или 7-членного цикла. Группа R, присоединенная к атому кислорода фенольного кольца, является лабильной защитной группой, которая, например, означает триалкилсилил или тетрагидропиранил, и которую удаляют на определенной стадии синтеза, или заместителем, который содержится в соединении,содержащем ингибитор интегразы. Промежуточные соединения галогенхинолина вступают в ряд реакций нуклеофильного ароматического замещения или в реакцию типа Сузуки, как показано на схеме 9 ниже. В реакции конденсации Сузуки арилгалогениды взаимодействуют с ацетиленовыми или виниловыми комплексами палладия с образованием углерод-углеродных связей в относительно мягких условиях. В некоторых случаях для проведения реакции в необходимом положении арильной группы необходимо блокировать группу в положении 2. Схема 9 Соединения формулы I, содержащие 5,9-дигидроксипирроло-[3,4-g]хинолин-6,8-дион, получают с использованием селективной защиты фенола в положении С 9 в 5,9-дигидроксипирроло[3,4-g]хинолин 6,8-дионе. Фенол С 9 защищают группой TIPS, при этом фенол С 5 алкилируют или ацилируют (схема 10): Схема 10 Соединения Формулы III. Соединения формулы III получают согласно следующим способам, показанным на схемах 11-14.et al., Nucleosides Nucleotides, 16, 1997, 977-982) по реакции пептидной конденсации, как описано в заявке на патент WO 02/30930, стр. 173, с образованием амида 3. При бромировании с использованием NBS получают соединение 4. Фенол защищают объемной ацильной группой, такой как пивалоил. Замещение брома в положении С 5 нафтиридина на гидразин, замещенный бис-Вос-группой, проводят по методике,описанной в статье J. В. Artebum et al., Org. Lett., 3, 2001, 1351-1354. Защитную силильную группу удаляют с использованием реагента TBAF (Т. Green and P. Wuts, "Protective Groups in Organic Synthesis", стр. 142, Wiley Science, 1999), при этом мезилат 7 получают по реакции полученного спирта с метансульфонилхлоридом. При обработке соединения 7 ТФУ с последующим нагреванием гидразинмезилата в щелочных условиях получают гидразонотриазаантрацен 8. Схема 12 Соединение 8 превращают в ряд производных, например, карбазоны 9 (R1 означает COR3) получают по реакции с хлорангидридами кислот или активированными производными карбоновых кислот. Карба- 25011399 маты 9 (R1 означает COOR3) получают по реакции соединения 8 с хлорформиатами ClCOOR3. Семикарбазоны 9 (R1 означает CONR2R3) получают с использованием изоцианатов или N,N-диалкилхлорформиатов. Тиосемикарбазоны 9 (R1 означает CSNR3R4) получают по реакции с тиоизоцианатами. Сульфонилмочевины 9 (R1 означает CO2NR3R4) получают по реакции соединения 8 с сульфамоилхлоридами с использованием методик, опубликованных в статье М. L. Matier et al., J. Med. Chem., 15, 1972, 538-541. Простые сульфонамиды получают по реакции соединения 8 с сульфонилхлоридами. Сложно-эфирную группу в соединениях 9 удаляют при омылении и получают соединение 10. В другом варианте ряд производных гидразона 9 алкилируют с последующим омылением и получают соединения 11. Схема 13 Соединение 5, показанное на схеме 11, взаимодействует с замещенным гидроксиламином или амином (R5 означает Boc, R6 означает ORa или алкил) по аналогичной методике, описанной в статье L. A.Carpino et al., Org. Lett., 3, 2001, 2793-2795, при этом получают производное 12. После превращения гидроксильной группы, защищенной силильной группой, в соединении 12 в уходящую группу, такую как мезилат в соединении 13, проводят циклизацию при нагревании в присутствии основания и получают соединение 14. После заключительного удаления защитной группы гидролизом соединения 14 получают соединение 15. Схема 14 Если группа R6 в соединении 14 означает ORa, группу Ra удаляют и получают оксим 16, который затем обрабатывают рядом реагентов и получают соединение 17. При гидролизе сложно-эфирной группы получают соединение 18. Например, при обработке соединения 16 алкилгалогенидом (R7-X) или спиртом в условиях реакции Мицунобу получают простой эфир 18. При использовании изоцианата или тиоизоцианата получают карбамат или тиокарбамат 18 (R7 означает C(=O)NHR8 или С(=S)NHR8). N,NДизамещенный карбамат 18 (R7 означает C(=O)NR2R3) получают при взаимодействии хлорформиатаClC(=O)NR2R3 с соединением 16. Аналогичным образом, при обработке соединения 16 сульфамоилхлоридами получают сульфамат 18 (R7 означает SO2NR1R2). На схеме 15 показан один из способов получения лактама, содержащего спироциклопропан, который конденсируют с образованием хинолина, являющийся вариантом формулы I. При этом используют фенол 19 с защитными группами различного типа, где R8 означает удаляемую эфирную группу, такую как триметилсилиэтиловый эфир, a R9 означает объемную группу, такую как дифенилметиловый или трет-бутиловый эфир. Карбонил С 6 превращают в олефин в региоселективных условиях при обработке соединения 19 метилмагний бромидом с последующей дегидратацией аминала с образованием соединения 20. При введении карбена по реакции Симмонс-Смита (например, как описано в статье Y. Biggs etal., JOC, 57, 1992, 5568-5573) получают циклопропан 21. При селективном удалении R8 с использованием реагента TBAF с последующей модификацией по методикам, описанным в многочисленных примерах,получают соединение 24. Схема 16 Диметилзамещенный лактам получают по реакции соединения 19 с реактивом Гриньяра с последующим превращением аминала 25 в ацетат 26 и обработкой соединения 26 реагентами Me3Al/MSOTf по методике, описанной в статье C.U. Kim et al., Tetrahedron Letters, 35, 1994, 3017-3020, при этом получают соединение 27. Другой способ используют при восстановлении циклопропана 21 над PtO2/Н 2, как описано в статье С.K. Cheung et al., JOC, 54, 1989, 570-573, при этом получают соединение 27. В другом варианте модифицированный лактам получают согласно схеме 17. При обработке соединения 19 аллилпроизводным реактива Гриньяра получают соединение 30. При активации аминала 30 по реакции образования ацетата 31 с последующей обработкой соединения 31 аллилтриметилсиланом в присутствии кислоты Льюиса, такой как TMSOTf, получают соединение 32. Циклизацию проводят с использованием метода Граббса (метатезис с закрытием цикла) (P. Schwab et al., Angew. Chem. Intl., 34,1995, 2039). В другом варианте, концевые олефины в соединении 32 превращают в альдегиды и при восстановительном аминировании получают спиропиперидин. Схема 18 Многие трициклические соединения содержат гетероцикл, за исключением 9-гидрокси-6,7 дигидропирроло[3,4-g]хинолин-8-она, т.е. соединения формулы IV. Некоторые примеры и методики получения соединений формулы IV показаны выше на схемах 18-24. Получение промежуточных эфиров фосфоновой кислоты Iaa-IVcc Ниже представлены структуры промежуточных эфиров фосфоновой кислоты Iaa-IVcc, где заместители R1, R2, R3, R4, А 1 и А 2 определены выше. Группы А 1 а и А 2 а имеют одинаковое значение, как и группы А 1 и А 2, за исключением того, что присоединено замещенное связующее звено P(O)(OR5)2. Заместитель R5 означает водород, алкил, алкенил, аралкил или арил. Дальнейшая химическая модификация соединений Iaa-Vcc, как описано в данном контексте, позволяет получить конечные соединения по настоящему изобретению. Промежуточные соединения Iaa-IVcc включают фосфонатный остаток (R5O)2P(O), соединенный с центральной структурой через различные связующие группы, обозначенные в прилагаемых формулах термином "link" (связующее звено). Далее представлены примеры связующих групп в формулах Iaa-IVcc. На схемах А 1-А 33 показан синтез промежуточных фосфонатных соединений по настоящему изобретению, Iaa-IVcc, и промежуточных производных, необходимых для их синтеза. Для получения субстратов I-V используют модифицированные методики для введения фосфонатных заместителей, известные специалистам в данной области. Например, для получения фосфонатов IIaa,IIIaa или IVaa используют модифицированную последовательность реакций, описанную для получения фосфонатов Iaa. Для получения каждой формулы каркаса I-V используют методики, описанные ниже для присоединения фосфонатных групп к реакционноспособным заместителям, таким как ОН, NH2, CH2Br,СООН, СНО и т.д. На схеме А 34 описаны методы взаимных превращений производных фосфонатных диэфиров, моноэфиров и кислот. Структуры фосфонатных эфиров Iaa-IVcc
МПК / Метки
МПК: C07D 498/20, C07D 487/04, C07D 471/04
Метки: получения, использования, композиция, способ, болезней, фармацевтическая, основе, лечении, вич, способы, интегразы, ингибиторы, трициклические, соединения, варианты
Код ссылки
<a href="https://eas.patents.su/30-11399-triciklicheskie-soedineniya-ingibitory-integrazy-vich-sposob-ih-polucheniya-varianty-farmacevticheskaya-kompoziciya-na-ih-osnove-sposob-ee-polucheniya-i-sposoby-ih-ispolzovaniya-v.html" rel="bookmark" title="База патентов Евразийского Союза">Трициклические соединения – ингибиторы интегразы вич, способ их получения (варианты), фармацевтическая композиция на их основе, способ ее получения и способы их использования в лечении болезней</a>
Предыдущий патент: Система и способ управления по меньшей мере одним устройством
Следующий патент: Лекарственные формы модафинила с модифицированным высвобождением
Случайный патент: Способ и установка для промывки кусков мяса.