Производные эстрогена в качестве ингибиторов стероидной сульфатазы
Номер патента: 11123
Опубликовано: 30.12.2008
Авторы: Рид Майкл Джон, Ньюман Саймон Пол, Журден Фабрис, Пурохит Алан, Чандер Суриндер Кумар, Поттер Барри Виктор Ллойд, Лис Маттью
Формула / Реферат
1. Соединение, включающее стероидную циклическую систему
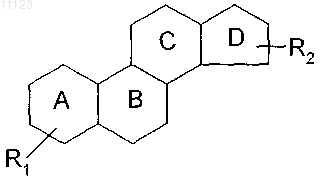
и необязательно группу R1, выбранную из гидроксигруппы и сульфаматной группы;
где цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, в которой L является необязательной мостиковой группой, представляющей собой (C1-C10)алкиленовую группу, a R3 выбран из группы, включающей
нитрильную группу,
спирт С0-С40-ОН,
сложный эфир -C(O)OR17,
простой эфир, выбранный из группы, состоящей из -OR10, -O-(CR14R15)p(CH2)q-CR10, -O-(CR14R15)p(CH2)q-OR16, -O-(CR14R15)p(CH2)q-S-R16, -O-(CR14R15)pNR11R12, -O-(CR14R15)pCуN, -O-CH=CH2,
-OSO2R9, -(CH2)qO-R16, -(CH2)qS-R16, =CH-OR10, =CH-(CR14Rl5)pOR10, =CH-(CR14R15)p(CH2)q-O-R16, =CH-(CR14R15)p(CH2)q-S-R16, NR13(CR14R15)pOR10, NR13(CR14R15)p(CH2)q-O-R16, NR13(CR14R15)p(CH2)q-S-R16,
амин, выбранный из группы, состоящей из NR13(CR14R15)pSO2R9, NR13(CRl4R15)pOR10, NR13(CR14R15)pC(O)OR17, NR13(CR14R15)pCуN, NRl3(CRl4R15)p(CH2)qO-R16, NR13(CR14R15)p(CH2)qS-R16, NRl3(CR14R15)pNR11R12, NR13(CR14R15)pCуCH, NR13(CR14R15)pCH=CH2, =CH-(CR14R15)pNR11R12, -O-(CRl4Rl5)pNR11R12 и -NR11R12, и
алкен, выбранный из группы, состоящей из =CH-(CR14R15)pSO2R9, =CH-(CRl4Rl5)pOR10, =CH-(CR14R15)pC(O)OR17, =CH-(CR14R15)p(CH2)qO-R16, =CH-(CR14R15)p(CH2)qS-R16, =CH-(CR14Rl5)p CуN, =CH-(CR14R15)pNR11R12, =CH-(CRl4Rl5)pCуCH, =CH-(CR14R15)pCH=CH2-O-(CR14R15)pCH=CH2, NR13(CR14R15)pCH=CH2,
где R10 выбирают из атома водорода и (С1-C20)алкила; R11 и R12 независимо друг от друга выбирают из (C1-C10)алкила или они вместе образуют морфолин, пирролидин или пиперидин;
где R13 выбирают из атома водорода и (С1-C20)алкила; R14 и R15 независимо друг от друга выбирают из атома водорода и (С1-C20)алкила; R16 выбирают из атома водорода и (С1-C20)алкила и R17 представляет собой (C1-C10)алкил,
q является целым числом от 0 до 20;
р является целым числом от 0 до 20;
при том условии, что когда R3 является спиртом или включает его, L наличествует; и
цикл А, принадлежащий к стероидной циклической системе, замещен по положению 2 группой R4, где R4 выбирают из атома водорода, (С1-C6)алкила и (C1-C6)алкокси.
2. Соединение по п.1 формулы II
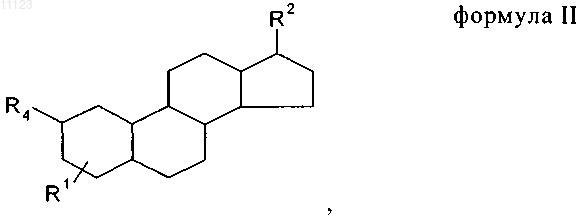
где R1 является необязательной группой, выбранной из -ОН и сульфаматной группы.
3. Соединение по п.1 формулы III
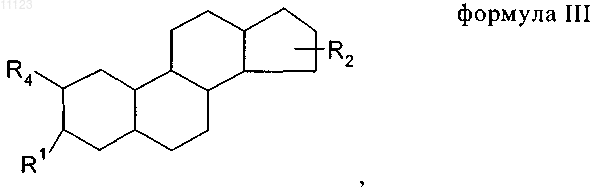
где R1 является необязательной группой выбранной из -ОН и сульфаматной группы.
4. Соединение по п.1 формулы IV

где R1 является необязательной группой, выбранной из -ОН и сульфаматной группы.
5. Соединение по любому из предшествующих пунктов, в котором R4 представляет собой метоксигруппу.
6. Соединение по любому из пп.1-4, в котором R4 является этилом.
7. Соединение по любому из предшествующих пунктов, в котором в тех случаях, когда цикл А замещен группами R1 и R4, R4 находится в орто-положении по отношению к R1.
8. Соединение по любому из предшествующих пунктов, в котором R1 присутствует.
9. Соединение по любому из предшествующих пунктов, в котором R1 представляет собой -ОН.
10. Соединение по любому из пп.1-7, в котором R1 представляет собой сульфаматную группу.
11. Соединение по п.10, в котором R1 представляет собой сульфаматную группу формулы

в котором R5 и R6 независимо выбирают из атома водорода, (С1-C20)алкильной, (С3-С6)циклоалкильной, (С2-C10)алкенильной, и арильных, таких как фенильная или толильная, групп или их комбинаций, причем алкильная, или циклоалкильная, или алкенильная, или арильная группы, или каждая из этих групп необязательно содержат один или более гетероатом или группу, выбранную из -О- или -NH-.
12. Соединение по п.11, в котором по меньшей мере одна из групп R5 и R6 представляет собой атом водорода.
13. Соединение по п.12, в котором каждая из групп R5 и R6 представляет собой атом водорода.
14. Соединение по любому из предшествующих пунктов, в котором R3 представляет собой нитрильную группу или включает ее.
15. Соединение по любому из предшествующих пунктов, в котором R3 представляет собой группу формулы
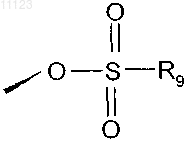
где R9 выбирают из Н и (С1-C20)алкила.
16. Соединение по любому из предшествующих пунктов, в котором R3 является группой формулы
-(R7)n(CR14R15)pR8, в которой
n принимает значения 0 или 1, а р обозначает целое число от 0 до 20;
R7 выбирают из =СН-, -О- и NR13;
R8 выбирают из -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CуN, -NR11R12 и -CH=CH2;
R9 представляет собой замещенный шыш незамещенный амин;
R10 выбирают из Н и (С1-C20)алкила;
R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин;
R13 выбирают из атома водорода и (С1-C20)алкила;
R14 и R15, каждый независимо друг от друга, выбирают из атома водорода и (С1-C20)алкила;
q является целым числом от 0 до 20;
X обозначает О или S;
R16 выбирают из атома водорода и (С1-C20)алкила; и
R17 выбирают из атома водорода и (С1-С2)алкила.
17. Соединение по любому из предшествующих пунктов, в котором R3 является группой формулы
-(CR14R15)pR8, где р обозначает число от 0 до 20; R8 выбирают из -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16,
-CуN, -NR11R12 и -CH=CH2; R9 представляет собой замещенный или незамещенный амин; R10 выбирают из Н и (С1-C20)алкила; R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин; R14 и R15, каждый независимо друг от друга, выбирают из атома водорода и (С1-C20)алкила; q является целым числом от 0 до 20; X обозначает О или S; R16 выбирают из атома водорода и (С1-C20)алкила; и R17 выбирают из атома водорода и (С1-C20)алкила.
18. Соединение по любому из предшествующих пунктов, в котором R3 является группой формулы
-(CH2)pR8, где р обозначает число от 0 до 20; R8 выбирают из -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16,
-CуN, -NR11R12 и -СН=СН2; R9 представляет собой замещенный или незамещенный амин; R10 выбирают из Н и (С1-C20)алкила; R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин; q является целым числом от 0 до 20; X обозначает О или S; R16 выбирают из атома водорода и (С1-C20)алкила; и R17 выбирают из атома водорода и (С1-C20)алкила.
19. Соединение по любому из пп.1-15, в котором R3 является группой формулы -(R7)nR8, где n принимает значения 0 или 1; R7 выбирают из =СН-, -О- и NR13; R8 выбирают из -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CуN, -NR11R12, -CуCH и -CH=CH2; R9 представляет собой замещенный или незамещенный амин; R10 выбирают из Н и (С1-C20)алкила; R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин; R13 выбирают из атома водорода и (С1-C20)алкила; q является целым числом от 0 до 20; X обозначает О или S; R16 выбирают из атома водорода и (С1-C20)алкила; и R17 выбирают из атома водорода и (С1-C20)алкила.
20. Соединение по любому из пп.16-19, в котором р принимает значения от 0 до 5.
21. Соединение по любому из пп.16-20, в котором р принимает значение 0, 1 или 2.
22. Соединение по любому из пп.16-21, в котором R8 представляет собой -SO2-R9.
23. Соединение по любому из пп.16-22, в котором R10 выбирают из атома водорода и (C1-C10)алкила.
24. Соединение по любому из пп.16-23, в котором R10 представляет собой атом водорода или -CH3.
25. Соединение по любому из пп.16-24, в котором R11 и R12 независимо выбирают из атома водорода и (C1-C10)алкила.
26. Соединение по любому из пп.16-25, в котором R11 и R12 независимо выбирают из атома водорода и -CH3.
27. Соединение по любому из пп.16-26, в котором R13 выбирают из атома водорода и (С1-C10)алкила.
28. Соединение по любому из пп.16-27, в котором R13 является атомом водорода.
29. Соединение по любому из предшествующих пунктов, в котором R3 представляет собой группу, выбранную из =CHC(O)OEt, -CH2C(O)OEt, =CHCH2OH, -СН2СН2ОН, -CH2CуN, =CHCуN,
-NHCH2CH2N(Me)2, -OCH2CH2-OMe.
30. Соединение по любому из предшествующих пунктов, в котором L представляет собой (С1-С5)алкилен.
31. Соединение по любому из предшествующих пунктов, в котором L представляет собой С1 или С2 алкилен.
32. Соединение по любому из пп.1-29, в котором R2 представляет собой группу формулы -R3.
33. Соединение по любому из предшествующих пунктов, в котором группа R2 находится в a-конформации.
34. Соединение по любому из предшествующих пунктов, в котором группа R2 находится в a-конформации в положении 17 цикла D.
35. Соединение по п.1, которое представляет собой
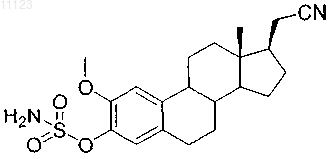
36. Соединение по п.1, которое представляет собой
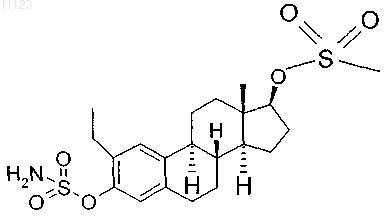
37. Фармацевтическая композиция, включающая:
i) соединение, как оно определено в любом из предшествующих пунктов; и
ii) модификатор биологической ответной реакции.
38. Композиция по п.37, в которой модификатор биологической ответной реакции является цитокином.
39. Композиция по п.38, в которой цитокин представляет собой фактор некроза опухолей (TNF).
40. Композиция по п.39, в которой TNF представляет собой TNFa.
41. Фармацевтическая композиция, включающая:
(а) (i) соединение, как оно определено в любом из пп.1-36 или (ii) композицию, как она определена в любом из пп.37-40, и
(б) фармацевтически приемлемый носитель, разбавитель, наполнитель или адъювант.
42. Применение соединения, как оно определено в любом из пп.1-36, для приготовления лекарственного средства, предназначенного для профилактики и/или ингибирования роста опухолей.
43. Применение соединения, как оно определено в любом из пп.1-36, для приготовления лекарственного средства, предназначенного для применения в лечении состояния или заболевания, связанного с одним или более из следующих факторов: активностью стероидной сульфатазы (STS); протеканием клеточного цикла; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек; и апоптозом.
44. Применение соединения, как оно определено в любом из пп.1-36, для приготовления лекарственного средства, предназначенного для применения в лечении состояния или заболевания, связанного с одним или более из следующих факторов: неблагоприятной активностью стероидной сульфатазы (STS); протеканием клеточнюую цикла; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек и апоптозом.
45. Применение соединения, как оно определено в любом из пп.1-36, для приготовления лекарственного средства, предназначенного для ингибирования активности стероидной сульфатазы (STS); модуляции протекания клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек и стимуляции апоптоза.
46. Применение соединения, как оно определено в любом из пп.1-36, для приготовления лекарственного средства, предназначенного для ингибирования активности стероидной сульфатазы (STS).
47. Применение соединения, как оно определено в любом из пп.1-36, для приготовления лекарственного средства, предназначенного для модуляции клеточного роста.
48. Способ лечения состояния или заболевания, связанного с одним или более из следующих факторов: активностью стероидной сульфатазы (STS); модуляцией протекания клеточного цикла; модуляцией апоптоза; модуляцией роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек и/или стимуляцией апоптоза, включающий введение нуждающемуся в лечении субъекту соединения, как оно определено в любом из пп.1-36.
Текст
011123 Область техники, к которой относится изобретение Объектом настоящего изобретения является соединение. В частности, объектами настоящего изобретения являются соединение и фармацевтическая композиция, включающая соединение. Объектом настоящего изобретения также является применение соединения или композиции в лечебных целях. Предпосылки создания изобретения Имеются свидетельства, указывающие на то, что эстрогены являются главными митогенами, участвующими в промотировании роста опухолей в эндокринзависимых тканях, таких как молочная железа и слизистая оболочка матки. Хотя концентрации эстрогена в плазме одинаковы у женщин как страдающих,так и не страдающих раком молочной железы, уровни эстрона и эстрадиола в опухоли молочной железы существенно выше, чем в нормальной ткани молочной железы и в крови. Считается, что синтез эстрогена in situ дает существенный вклад в высокий уровень эстрогенов в опухолях, поэтому ингибиторы, в особенности специфичные ингибиторы, биосинтеза эстрогена имеют потенциальное значение для лечения эндокринзависимых опухолей. В течение двух последних десятилетий присутствовал существенный интерес к разработке ингибиторов ароматазного метаболического пути, по которому предшественник мужского полового гормона андростендион преобразуется в эстрон. Теперь, однако, имеются свидетельства того, что за производство эстрогенов в опухолях молочной железы отвечают эстронсульфатазный(E1-STS) метаболический путь, т.е. гидролиз эстрон-сульфата до эстрона (E1S до Е 1), и ароматазный метаболический путь (т.е. преобразование андростендиона в эстрон). Фиг. 1 и 2 представляют схематические диаграммы, демонстрирующие некоторые из ферментов,участвующих в синтезе эстрона in situ из эстрон-сульфата, эстрадиола и андростендиона. На фиг. 2, схематически демонстрирующей происхождение эстрогенных стероидов у женщин в постклимактерический период, "ER" обозначает рецептор эстрогена, "DHA-S" обозначает дегидроэпиандростерон-сульфат, "Adiol" обозначает андростендиол, "E1-STS" обозначает эстронсульфатазу, "DHASTS" обозначает дегидроэпиандростеронсульфатазу, "Adiol-STS" обозначает андростендиолсульфатазу, a"17B-HSD" обозначает эстрадиол-17 В-гидроксистероиддегидрогеназу. Как можно заметить, двумя главными ферментами, участвующими в периферийном синтезе эстрогенов являются ароматаза и эстронсульфатаза. Вкратце, фермент ароматаза преобразует андростендион, выделяемый в больших количествах корой надпочечников, в эстрон. Недавние исследования указывают на то, что активность ароматазы могут ингибировать некоторые флавоны. Существенное количество из образующегося таким образом эстрона преобразуется, однако, в эстрон-сульфат (E1S), и в настоящее время имеется большой объем свидетельств, показывающих, что E1S действует в плазме и ткани как резервуар для образования эстрона под действием эстронсульфатазы. В связи с этим, в настоящее время считается, что эстронсульфатазный (Е 1-STS) механизм, т.е. гидролиз эстрон-сульфата до эстрона (E1S до Е 1) является главным источником эстрогена в опухолях молочной железы. В пользу этой теории свидетельствует умеренное снижение концентрации эстрогена в плазме у больных раком молочной железы женщин в постклимактерический период, при лечении ингибиторами ароматазы, такими как 3-(n-аминофенил)-3-этилпиперидин-2,6-дион и 4-гидроксиандростендион, а также тот факт, что концентрация E1S в плазме у подобных пациентов, подвергаемых лечению ингибиторами ароматазы, остается сравнительно высокой. Большой период полураспада E1S в крови (10-12 ч) по сравнению с несопряженными эстрогенами (20 мин) и высокие уровни активности стероидной сульфатазы в печени и нормальных и злокачественных тканях молочной железы также выступают в поддержку данной теории. Таким образом, образование эстрогенов в злокачественных тканях молочной железы и слизистой оболочки матки по сульфатазному механизму вносит главный вклад в высокие концентрации эстрогенов,присутствующих в данных опухолях.PCT/GB 92/01587 описывает новые ингибиторы стероидной сульфатазы и содержащие их фармацевтические композиции для применения в лечении эстронзависимых опухолей, в особенности рака молочной железы. Этими ингибиторами стероидной сульфатазы являются сложные эфиры сульфаминовой кислоты, такие как N,N-диметилэстрон-3-сульфамат и предпочтительно эстрон-3-сульфамат (также известный как "ЕМАТЕ"). ЕМАТЕ имеет следующее строение: Известно, что EMATE является эффективным ингибитором E1-STS и демонстрирует более чем 99% ингибирование активности E1-STS в интактных клетках рака молочной железы MCF-7, при концентрации 0,1 нМ. ЕМАТЕ также ингибирует фермент E1-STS зависящим от времени и концентрации образом,-1 011123 что указывает на его действие как инактиватора, направленного на активный центр. Хотя ЕМАТЕ изначально предназначался для ингибирования E1-STS, он также ингибирует дегидроэпиандростеронсульфатазу (DHA-STS), которая, как считают, является ферментом, играющим центральную роль в регулировании биосинтеза эстрогенного стероида андростендиола. Кроме того, в настоящее время имеются свидетельства, позволяющие предположить, что андростендиол может иметь даже более важное значение в качестве промотора роста опухоли молочной железы. ЕМАТЕ также активен in vivo, на что указывает почти полное ингибирование активности E1-STS (99%) и DHA-STS (99%) в печени крыс при как пероральном, так и подкожном введении. Кроме того, было показано, что ЕМАТЕ приводит к улучшению памяти у крыс. Исследования на мышах указывают на связь между активностью DHA-STS и регуляцией части иммунного ответа. Полагают, что это может иметь место и у человека. Мостиковый атом кислорода сульфаматного остатка в ЕМАТЕ важен с точки зрения ингибирующей активности. Таким образом,когда атом кислорода в положении 3 замещается другими гетероатомами, как это происходит в эстрон-3N-сульфамате и эстрон-3-S-сульфамате, подобные аналоги оказываются более слабыми, не зависящими от времени инактиваторами. Помимо эстрона другим основным стероидом с эстрогенными свойствами, образующимся в организме женщин в постклимактерический период, является андростендиол (см. фиг. 2). Несмотря на то, что андростендиол является мужским половым гормоном, он может связываться с рецептором эстрогена (ER) и может стимулировать рост ER-положительных клеток рака молочной железы и рост вызываемых канцерогенами опухолей груди у крыс. Важно отметить, что у женщин в постклимактерический период 90% образующегося андростендиола происходит из мужского полового гормона дегидроэпиандростерон-сульфата (DHA-S), выделяемого в больших количествах корой надпочечников.DHA-S преобразуется в DHA под действием DHA-сульфатазы, которая может быть аналогичной или отличной от фермента эстронсульфатазы, ответственного за гидролиз E1S. В течение последних 10-15 лет были проведены обширные исследования, имеющие целью разработку эффективных ингибиторов ароматазы, некоторые из которых в настоящее время коммерчески доступны. Однако в трех недавних наблюдениях за больными раком молочной железы женщинами в постклимактерический период, проходившими курс лечения ингибиторами ароматазы, концентрации E1S в плазме оставались на уровне 400-1000 пг/мл. Подводя итоги, синтез эстрогена in situ дает, как полагают, важный вклад в высокие уровни эстрогенов в опухолях, поэтому специфичные ингибиторы биосинтеза эстрогена имеют потенциальное значение для лечения эндокринзависимых опухолей. Более того, хотя образование эстрогена в злокачественных тканях молочной железы и слизистой оболочки матки по сульфатазному механизму вносит основной вклад в высокие концентрации эстрогенов, имеются и другие ферментативные механизмы, вносящие вклад в синтез эстрогена in vivo. Краткое изложение сущности изобретения Настоящее изобретение основано на неожиданном открытии того факта, что стероидные соединения, содержащие в цикле D группу, выбранную среди групп, являющихся нитрильной группой, спиртом,сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп,могут применяться в качестве эффективных ингибиторов стероидной сульфатазы (STS); модуляторов клеточного цикла; модуляторов апоптоза; модуляторов роста клеток; средств, предотвращающих и/или подавляющих поглощение глюкозы; средств, предотвращающих ангиогенез опухоли, или его ингибиторов; разрушителей микротрубочек; и/или средств, вызывающих апоптоз. Таким образом, в настоящем изобретении предлагаются соединения, включающие стероидную циклическую систему и необязательно группу R1, выбранную из гидроксигруппы и сульфаматной группы; где цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, в которой L является необязательной мостиковой группой, представляющей собой (C1-C10)алкиленовую группу, a R3 выбран из группы, включающей нитрильную группу,спирт С 0-С 40-ОН,сложный эфир -C(O)OR17,простой эфир, выбранный из группы, состоящей из -OR10, -O-(CR14R15)p(CH2)q-OR10, -O14 15(CR R )pC(O)OR17, =CH-(CR14R15)p(CH2)qO-R16, =CH-(CR14R15)p(CH2)qS-R16, =CH-(CR14R15)pCN, =CH(CR14R15)pNR11R12, =CH-(CR14R15)pCCH, =CH-(CR14R15)pCH=CH2-O-(CR14R15)pCH=CH2,NR13(CR14R15)pCH=CH2,где R10 выбирают из атома водорода и (С 1-С 20)алкила; R11 и R12 независимо друг от друга выбирают из (C1-C10)алкила или они вместе образуют морфолин, пирролидин или пиперидин; где R13 выбирают из атома водорода и (С 1-C20)алкила; R14 и R15 независимо друг от друга выбирают из атома водорода и (С 1-C20)алкила; R16 выбирают из атома водорода и (С 1-C20)алкила и R17 представляет собой (C1-C10)алкил,q является целым числом от 0 до 20; р является целым числом от 0 до 20; при том условии, что когда R3 является спиртом или включает его, L наличествует; и цикл А, принадлежащий к стероидной циклической системе, замещен по положению 2 группой R4,где R4 выбирают из атома водорода, (С 1-C6)алкила и (С 1-C6)алкокси. Предпочтительными являются соединения формулы II 13 где R1 представляет собой необязательную группу, выбранную из -ОН и сульфаматной группы. Более предпочтительными являются соединения формулы III где R1 представляет собой необязательную группу, выбранную из -ОН и сульфаматной группы. Наиболее предпочтительными являются оединения формулы IV где R1 представляет собой необязательную группу, выбранную из -ОН и сульфаматной группы. Предпочтительными соединениями являются такие, в которых R4 представляет собой метоксигруппу, например этил; цикл А, замещенный группами R1 и R4, R4 находится в орто-положении по отношению к R1; R1 присутствует и представляет собой -ОН или сульфаматную группу формулы в которой R5 и R6 независимо выбирают из атома водорода, (С 1-C20)алкильной, (С 3-C6)циклоалкильной,(С 2-C10)алкенильной, и арильных, таких как фенильная или толильная группы или их комбинаций, причем алкильная, или циклоалкильная, или алкенильная, или арильная группы, или каждая из этих групп необязательно содержат один или более гетероатом или группу, выбранную из -О- или -NH-. Предпочтительно, если по меньшей мере одна из групп R5 и R6 представляет собой атом водорода. Более предпочтительно, если каждая из групп R5 и R6 представляет собой атом водорода. Предпочтительными соединениями являются такие, в которых R3 представляет собой нитрильную группу или включает ее; или R3 представляет собой группу формулы где R9 выбирают из Н и (С 1-C20)алкила; или R3 является группой формулы -(R7)n(CR14R15)pR8, в которойn принимает значения 0 или 1, а р обозначает целое число от 0 до 20;R8 выбирают из -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN, -NR11R12 и -CH=CH2,R9 представляет собой замещенный или незамещенный амин,R10 выбирают из Н и (С 1-C20)алкила;R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С 1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин;R13 выбирают из атома водорода и (С 1-C20)алкила;R14 и R15, каждый независимо друг от друга, выбирают из атома водорода и (С 1-C20)алкила;q является целым числом от 0 до 20;R16 выбирают из атома водорода и (С 1-C20)алкила иR17 выбирают из атома водорода и (С 1-С 2)алкила; или R3 является группой формулы -(CR14R15)pR8, где р обозначает число от 0 до 20; R8 выбирают из-SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN, -NR11R12 и -CH=CH2; R9 представляет собой замещенный или незамещенный амин, R10 выбирают из Н и (С 1-C20)алкила; R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С 1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин; R14 и R15, каждый независимо друг от друга, выбирают из атома водорода и (С 1-C20)алкила; q является целым числом от 0 до 20; X обозначает О или S; R16 выбирают из атома водорода и (С 1C20)алкила; и R17 выбирают из атома водорода и (С 1-С 2)алкила; или R3 является группой формулы -(CH2)pR8, где р обозначает число от 0 до 20; R8 выбирают из-SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN, -NR11R12 и -CH=CH2; R9 представляет собой замещенный или незамещенный амин, R10 выбирают из Н и (С 1-C20)алкила; R11 и R12, каждый независимо друг от друга, выбирают из атома водорода и (С 1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин; q является целым числом от 0 до 20; X обозначает О или S; R16 выбирают из атома водорода и (С 1-C20)алкила; и R17 выбирают из атома водорода и (С 1-С 2)алкила; или R3 является группой формулы -(R7)nR8, где n принимает значения 0 или 1, R7 выбирают из =СН-,-О- и NR13; R8 выбирают из -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN, -NR11R12, -СCH и -СН=СН 2;R9 представляет собой замещенный или незамещенный амин, R10 выбирают из Н и (С 1-C20)алкила; R11 иR12, каждый независимо друг от друга, выбирают из атома водорода и (C1-C20)алкила или они вместе образуют морфолин, пирролидин или пиперидин; R13 выбирают из атома водорода и (С 1-C20)алкила; q является целым числом от 0 до 20; X обозначает О или S; R16 выбирают из атома водорода и (С 1C20)алкила; и R17 выбирают из атома водорода и (C1-C2)алкила. Предпочтительными соединениями являются такие, в которых р принимает значения от 0 до 5, более предпочтительно, когда р принимает значение 0, 1 или 2. Предпочтительными соединениями являются такие, в которых R8 представляет собой -SO2-R9; R10 выбирают из атома водорода и (C1-C10)алкила, предпочтительно из атома водорода или -CH3; R11 и R12 независимо выбирают из атома водорода и (C1-C10)алкила, предпочтительно из атома водорода и -CH3;R13 выбирают из атома водорода и (C1-C10)алкила, предпочтительно из атома водорода. Предпочтительными соединениями являются такие, в которых R3 представляет собой группу, выбранную из =CHC(O)OEt, -CH2C(O)OEt, =СНСН 2 ОН, -СН 2 СН 2 ОН, -CH2CN, =CHCN,-NHCH2CH2N(Me)2, -OCH2CH2-OMe; L представляет собой (С 1-С 5)алкилен, предпочтительно L представляет собой С 1 или С 2 алкилен; R2 представляет собой группу формулы -R3. Предпочтительными соединениями являются такие, в которых группа R2 находится в конформации, особенно предпочтительными являются соединения, в которых группа R2 находится в конформации в положении 17 цикла D. Предпочтительными соединениями являются такие, которые представляют собой Далее настоящее изобретение относится к фармацевтической композиции, включающей: i) соединение, как оно определено выше; и ii) модификатор биологической ответной реакции, причем модификатор биологической ответной реакции является цитокином, который предпочтительно представляет собой фактор некроза опухолей (TNF), особо предпочтительно TNF. Также настоящее изобретение относится к фармацевтической композиции, включающей: (а) (i) соединение, как оно определено выше или (ii) композицию, как она определена выше; и (б) фармацевтически приемлемый носитель, разбавитель, наполнитель или адъювант. Настоящее изобретение относится к применению соединения, как оно определено выше, для приготовления лекарственного средства, предназначенного для профилактики и/или ингибирования роста опухолей. Настоящее изобретение относится к применению соединения, как оно определено выше, для приготовления лекарственного средства предназначенного для применения в лечении состояния или заболевания, связанного с одним или более из следующих факторов: активностью стероидной сульфатазы (STS),особенно ее неблагоприятной активностью; протеканием клеточного цикла; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек; и апоптозом. Настоящее изобретение относится к применению соединения, как оно определено выше, для приготовления лекарственного средства, предназначенного для ингибирования активности стероидной сульфатазы (STS); модуляции протекания клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек; и стимуляции апоптоза. Настоящее изобретение относится к применению соединения, как оно определено выше, для приготовления лекарственного средства, предназначенного для ингибирования активности стероидной сульфатазы (STS). Настоящее изобретение относится к применению соединения, как оно определено выше, для приготовления лекарственного средства, предназначенного для модуляции клеточного роста. Кроме того, настоящее изобретение относится к способу лечения состояния или заболевания, связанного с одним или более из следующих факторов: активностью стероидной сульфатазы (STS); модуляцией протекания клеточного цикла; модуляцией апоптоза; модуляцией роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек; и/или стимуляцией апоптоза, включающий введение нуждающемуся в лечении субъекту соединения, как оно определено выше. Подробное изложение сущности изобретения В перспективе соединения могут предоставлять следующие возможности: включать стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. При этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3,где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Кроме того, в котором цикл А , принадлежащий к стероидной циклической системе, замещен по положению 2 или 4 группой R4, где R4 является гидрокарбильной группой. Одним из вариантов осуществления является композиция, включающая: 1) соединение, как оно определено в контексте; и 2) модификатор биологической ответной реакции. Одним из вариантов осуществления является фармацевтическая композиция, включающая: (а) (1) соединение, как оно определено в контексте, или (2) композицию, как она определена в контексте, и (б) фармацевтически приемлемый носитель, разбавитель, наполнитель или вспомогательное средство. Одним из вариантов осуществления является: (1) соединение, как оно определено в контексте, или(2) композиция, как она определена в контексте для применения в медицине. Одним из вариантов осуществления является применение: (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, в производстве лекарственного средства для предотвращения и/или ингибирования роста опухоли. Одним из из вариантов осуществления является применение: (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, в производстве лекарственного средства для применения в целях лечения состояния или заболевания, связанного с одним или более из следую-5 011123 щих факторов: активностью стероидной сульфатазы (STS); клеточным циклом; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек; и апоптозом. Одним из вариантов осуществления является применение (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, в производстве лекарственного средства для применения в целях лечения состояния или заболевания, связанного с одним или более из следующих факторов: неблагоприятной активностью стероидной сульфатазы (STS); клеточным циклом; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек; и апоптозом. Одним из вариантов осуществления является применение (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, в производстве лекарственного средства для достижения одной или более из следующих целей: ингибирования активности стероидной сульфатазы (STS); модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек; стимуляции апоптоза. Одним из вариантов осуществления является применение: (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, в производстве лекарственного средства для ингибирования активности стероидной сульфатазы (STS). Одним из вариантов осуществления является применение: (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, в производстве лекарственного средства для модуляции роста клеток. Одним из вариантов осуществления является способ лечения, включающий введение нуждающемуся в лечении субъекту (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте. Одним из вариантов осуществления является способ лечения, включающий введение нуждающемуся в лечении субъекту (1) соединения, как оно определено в контексте, или (2) композиции, как она определена в контексте, с целью ингибирования активности стероидной сульфатазы (STS); модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек; и/или стимуляции апоптоза. Одним из вариантов осуществления является способ, включающий: (а) осуществление анализа на один или более из следующих процессов: ингибирование активности стероидной сульфатазы (STS); модуляцию клеточного цикла; модуляцию апоптоза; модуляцию роста клеток; предотвращение и/или подавление поглощения опухолью глюкозы; предотвращение и/или ингибирование ангиогенеза опухоли; разрушение микротрубочек и стимуляцию апоптоза с одним или более из испытуемых соединений, определенных в контексте; (б) установление того, способны ли одно или более из упомянутых испытуемых соединений приводить к какому-либо одному или нескольким из следующих результатов: ингибированию активности стероидной сульфатазы (STS); модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращению и/или подавлению поглощения опухолью глюкозы; предотвращению и/или ингибированию ангиогенеза опухоли; разрушению микротрубочек; и стимуляции апоптоза; и (в) выбор одного или более из упомянутых испытуемых соединений, способных приводить к какомулибо одному или нескольким из следующих результатов: ингибированию активности стероидной сульфатазы (STS); модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращению и/или подавлению поглощения опухолью глюкозы; предотвращению и/или ингибированию ангиогенеза опухоли; разрушению микротрубочек и стимуляции апоптоза. Во всяком из способов может присутствовать одна или более дополнительная стадия. Например,способ может также включать стадию модифицирования идентифицированного испытуемого соединения (с помощью, например, химических и/или ферментативных методов) и необязательную дополнительную стадию тестирования подобного модифицированного соединения на обладание одним или более из следующих эффектов: ингибирование активности стероидной сульфатазы (STS); модуляция клеточного цикла; модуляция апоптоза; модуляция роста клеток; предотвращение и/или подавление поглощения опухолью глюкозы; предотвращение и/или ингибирование ангиогенеза опухоли; разрушение микротрубочек и стимуляция апоптоза. В качестве дальнейших примеров способ может также включать стадию определения строения (с помощью, например, кристаллографических методов) идентифицированного испытуемого соединения с последующим осуществлением исследований методами компьютерного моделирования, имеющих целью, например, дальнейшее усиление его действия. Таким образом, настоящее изобретение также включает компьютер, снабженный набором данных (таких как кристаллографические координаты) для упомянутого идентифицированного испытуемого соединения. Настоящее изобретение также включает подобное идентифицированное испытуемое соединение, показанное на мониторе компьютера для его анализа, такого как исследование связывания с ферментами и/или белками. Одним из вариантов осуществления является соединение, идентифицированное способом по настоящему изобретению.-6 011123 Также раскрываются новые соединения (такие как представленные в контексте), равно как и методики их получения (такие как методики, представленные в контексте), равно как и новые интермедиаты(такие как представленные в контексте) для применения в данных методиках. Одним из расширенных вариантов является применение соединения в производстве лекарственного средства для применения в целях лечения состояния или заболевания, связанного с одним или более из следующих факторов: клеточным циклом; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек и апоптозом. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группойR2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Одним из расширенных вариантов осуществления является применение композиции в производстве лекарственного средства для применения в целях лечения состояния или заболевания, связанного с одним или более из следующих факторов: клеточным циклом; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек и апоптозом. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Одним из расширенных вариантов является применение соединения в производстве лекарственного средства для применения в целях лечения состояния или заболевания, связанного с одним или более из следующих факторов: неблагоприятным протеканием клеточного цикла; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек и апоптозом. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1,выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Одним из расширенных вариантов осуществления является применение композиции в производстве лекарственного средства для применения в целях лечения состояния или заболевания, связанного с одним или более из следующих факторов: неблагоприятным протеканием клеточного цикла; апоптозом; ростом клеток; поглощением опухолью глюкозы; ангиогенезом опухоли; образованием микротрубочек; и апоптозом. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Еще одним из расширенных вариантов осуществления является применение соединения в производстве лекарственного средства для достижения одной или более из следующих целей: модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек и стимуляции апоптоза. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы,фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой,спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует.-7 011123 Еще одним из расширенных вариантов осуществления настоящего изобретения, его объектом является применение композиции в производстве лекарственного средства для достижения одной или более из следующих целей: модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек и стимуляции апоптоза. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Согласно расширенному варианту осуществления является применение соединения в производстве лекарственного средства для модуляции роста клеток. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы-L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Согласно расширенному варианту осуществления является применение композиции в производстве лекарственного средства для модуляции роста клеток. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Согласно расширенному варианту осуществления является способ лечения, включающий введение нуждающемуся в лечении субъекту соединения с целью модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек и/или стимуляции апоптоза. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром,простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии,что когда R3 является спиртом или включает его, L наличествует. Согласно расширенному варианту осуществления является способ лечения, включающий введение нуждающемуся в лечении субъекту композиции с целью модуляции клеточного цикла; модуляции апоптоза; модуляции роста клеток; предотвращения и/или подавления поглощения опухолью глюкозы; предотвращения и/или ингибирования ангиогенеза опухоли; разрушения микротрубочек и/или стимуляции апоптоза. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Одним из расширенных вариантов осуществления является применение соединения в производстве лекарственного средства для применения в лечении состояния или заболевания, связанного с карбоангидразой. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стеро-8 011123 идную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром,простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии,что когда R3 является спиртом или включает его, L наличествует. Одним из расширенных вариантов осуществления является применение композиции в производстве лекарственного средства для применения в лечении состояния или заболевания, связанного с карбоангидразой. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Еще одним из расширенных вариантов осуществления является применение соединения в производстве лекарственного средства для применения в лечении состояния или заболевания, связанного с неблагоприятной активностью углеродной ангидразы. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы-L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Еще одним из расширенных вариантов осуществления является применение композиции в производстве лекарственного средства для применения в лечении состояния или заболевания, связанного с неблагоприятной активностью карбоангидразы. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Еще одним из расширенных вариантов осуществления является применение соединения в производстве лекарственного средства для модуляции активности карбоангидразы. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1, выбранной среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Еще одним из расширенных вариантов осуществления является применение композиции в производстве лекарственного средства для модуляции активности карбоангидразы. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Согласно расширенному варианту осуществления является способ лечения, включающий введение нуждающемуся в лечении субъекту соединения с целью модуляции активности карбоангидразы. При этом упомянутое соединение включает стероидную циклическую систему и необязательную группу R1,выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3-9 011123 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Согласно расширенному варианту осуществления является способ лечения, включающий введение нуждающемуся в лечении субъекту композиции с целью модуляции активности карбоангидразы. При этом упомянутая композиция включает: 1) соединение, включающее стероидную циклическую систему и необязательную группу R1, выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы,сульфогруппы или сульфонамидной группы; при этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром,амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует; и 2) модификатор биологической ответной реакции. Для удобства рассмотрения материала, эти и дальнейшие аспекты обсуждаются ниже в разделах с соответствующими названиями. Однако представленные в каждом из разделов идеи не обязательно ограничиваются каждым отдельным разделом. Некоторые преимущества изобретения Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут ингибировать активность стероидной сульфатазы (STS). Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут осуществлять модуляцию клеточного цикла. Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут модулировать апоптоз. Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут модулировать рост клеток. Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут предотвращать и/или подавлять поглощение глюкозы опухолью. Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут предотвращать и/или ингибировать ангиогенез опухоли. Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изобретению могут разрушать микротрубочки. По этому поводу следует заметить, что микротрубочки, совместно с микрофиламентами и промежуточными филаментами, образуют часть цитоскелетной системы клетки. Микротрубочки отвечают за многие из клеточных движений; примеры включают пульсацию ресничек и жгутиков и транспорт мембранных везикул в цитоплазме. Все эти движения являются результатом полимеризации и деполимеризации микротрубочек или действий моторных белков микротрубочек динеина и кинезинов. Некоторые другие клеточные движения, такие как выстраивание и разделение хромосом в процессе мейоза и митоза,являются результатами действия обоих механизмов. Микротрубочки также направляют клеточные движения, но в некоторых случаях микротрубочки несут чисто структурные функции. Микротрубочка построена из субъединиц, в качестве которых выступают гетеродимеры мономеров-тубулина и -тубулина. Существуют две популяции микротрубочек: стабильные долгоживущие микротрубочки и динамичные короткоживущие микротрубочки. Динамичные микротрубочки находят тогда,когда структурам из микротрубочек необходимо быстро соединяться и разъединяться. Например, во время митоза цитозольная сеть микротрубочек, характерная для клеток в интерфазе, исчезает, а происходящий из нее тубулин используется для формирования веретена, распределяющего хромосомы поровну по дочерним клеткам. По завершении митоза веретено распадается, а интерфазная сеть микротрубочек образуется снова. Лекарственные средства, ингибирующие митоз, предоставляют удобные способы манипуляции микротрубочками в клетке. Три лекарственных средства, колхицин, розевин и таксол, все выделенные из растений, являются, как оказалось, весьма мощными средствами зондирования деятельности микротрубочек, отчасти потому, что они связываются только с тубулином или микротрубочками и не связываются с другими белками, а также потому, что их концентрации в клетках можно легко контролировать. Вследствие их влияния на митоз, ингибиторы микротрубочек широко используются для лечения заболеваний и в последнее время в качестве противораковых средств, поскольку блокада образования веретена будет предпочтительно ингибировать быстро делящиеся клетки, такие как раковые клетки. Высокоэффективным средством против рака яичников является таксол. В клетках рака яичников, которые подвержены процессу быстроклеточного деления, при воздействии таксола митоз блокируется, тогда как остальные функции, осуществляемые неповрежденными микротрубочками, не затрагиваются. Подробный обзор, посвященный микротрубочкам, можно найти в книге "Молекулярная клеточная биология"(под ред. Lodish и др., 1995 WH Freeman and Co., New York, стр. 1051-1122). Одним из преимуществ настоящего изобретения является то, что соединения по настоящему изо- 10011123 бретению могут стимулировать апоптоз. Апоптоз вызывают действующие на микротрубочки лекарственные средства, причем этот процесс может включать фосфорилирование (и инактивацию) регулятора апоптоза, белка bcl-2 (Haider, Cancer Res. 57: 229, 1997). Настоящее изобретение основывается на неожиданном открытии того факта, что соединение обеспечивает эффективное лечение рака. Другое преимущество соединений по настоящему изобретению состоит в том, что они могут быть действенны in vivo. Некоторые из соединений по настоящему изобретению могут быть неэстрогенными соединениями. Термин неэстрогенный означает в контексте не проявляющий или почти не проявляющий никакой эстрогенной активности. Термин неэстрогенный означает в контексте не проявляющий или почти не проявляющий никакой системной эстрогенной активности, такой как определяемая по методике 4. Для некоторых применений соединения обладают эстрогенным эффектом. Другое преимущество состоит в том, что некоторые из соединений не могут быть преобразованы в ходе обмена веществ в соединения, обладающие гормональной активностью или вызывающие ее. Для некоторых применений соединения предпочтительно обладают обратимым действием. Для некоторых применений соединения предпочтительно обладают необратимым действием. Некоторые из соединений по настоящему изобретению обладают также тем преимуществом, что могут быть активны при пероральном введении. Некоторые из соединений по настоящему изобретению могут быть применимы для профилактики и/или лечения рака, такого как рак молочной железы, равно как (или альтернативно) и незлокачественные состояния, как то профилактика и/или лечение воспалительных состояний, таких как состояния, связанные с одним или более из следующих заболеваний: аутоиммунитет, включая, например, ревматоидный артрит, диабет типа I и II, системную красную волчанку, рассеянный склероз, злокачественную миастению, тиреодит, васкулит, язвенный колит и болезнь Крона, кожные расстройства, например угри,псориаз, контактный дерматит; реакция трансплантат против хозяина; экзема, астма и отторжение органов после трансплантации. Соединения по настоящему изобретению применимы, в частности, в тех случаях, когда введение медикамента необходимо осуществлять с раннего возраста. В одном из вариантов осуществления настоящего изобретения соединения по настоящему изобретению применимы для лечения рака молочной железы. Таким образом, некоторые из соединений по настоящему изобретению, как также полагают, обладают иными лечебными применениями помимо лечения эндокринзависимых видов рака, такими как лечение аутоиммунных заболеваний. Для удобства рассмотрения материала, эти и дальнейшие аспекты настоящего изобретения обсуждаются ниже в разделах с соответствующими названиями. Однако представленные в каждом из разделов идеи изобретения не обязательно ограничиваются каждым отдельным разделом. Предпочтительные аспекты Соединение. Прежде всего, соединение, включающее стероидную циклическую систему и необязательную группу R1, в выбранную среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. При этом цикл D, входящий в стероидную циклическую систему, замещен группой R2 формулы -L-R3, где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп, при том условии, что когда R3 является спиртом или включает его, L наличествует. Кроме того, цикл А, принадлежащий к стероидной циклической системе, замещен по положению 2 или 4 группой R4, где R4 является гидрокарбильной группой. В одном из предпочтительных вариантов соединение обладает одним или более из следующих эффектов: ингибирование активности стероидной сульфатазы (STS); модуляция клеточного цикла; модуляция апоптоза; модуляция роста клеток; предотвращение и/или подавление поглощения опухолью глюкозы; предотвращение и/или ингибирование ангиогенеза опухоли; разрушение микротрубочек; и стимуляция апоптоза. Стероидная циклическая система. Соединение содержит стероидную циклическую составляющую, а именно циклопентанофенантреновый скелет или его биоизостереомеры. Как хорошо известно специалистам в соответствующей области, классическая стероидная циклическая структураимеет следующую общую формулу: В вышеприведенной формуле циклы обозначены и пронумерованы общепринятым способом. В одном из вариантов осуществления стероидная циклическая структура может содержать какойлибо один или более из следующих атомов: углерода, водорода, кислорода, азота, фосфора, галогена(включая хлор, бром и йод), серы и фосфора. По крайней мере одна из циклических групп стероидной циклической структуры может быть гетероциклической группой (гетероциклом) или негетероциклической группой. По крайней мере одна из циклических групп стероидной циклической структуры может быть насыщенной циклической структурой или ненасыщенной циклической структурой (такой как арильная группа). Предпочтительно по крайней мере одна из циклических групп стероидной циклической структуры является ароматическим циклом. Примером биоизостереомера является тот случай, когда какой-либо один или более из циклов А, В,С и D является гетероциклом и/или когда какой-либо один или более из циклов А, В, С и D замещен и/или когда какой-либо один или более из циклов А, В, С и D модифицирован; но при этом биоизостереомер обладает стероидными свойствами. Учитывая вышесказанное, структура предпочтительной стероидной циклической системы может быть представлена в следующем виде: где А', В', С' и D' независимо друг от друга являются гетероциклами или негетероциклическими кольцами, каковые циклы могут быть независимо друг от друга замещенными или незамещенными, насыщенными или ненасыщенными. В качестве примера какой-либо один или более из циклов А', В', С' и D' может быть независимо замещен подходящими группами, такими как алкильная группа, аллильная группа, гидроксигруппа, галоид, гидрокарбильная группа, оксигидрокарбильная группа и т.д. Термин гидрокарбильная группа, как он используется в контексте, означает группу, которая включает, по крайней мере, атом углерода и атом водорода и может необязательно включать один или более из иных подходящих заместителей. Примеры таких заместителей могут включать галоид, алкоксигруппу, нитрогруппу, углеводородную группу, N-ацильную группу, циклическую группу и т.д. В дополнение к той возможности, что заместитель является циклической группой, комбинация заместителей может образовывать циклическую группу. Если гидрокарбильная группа включает более одного атома углерода, такие атомы углерода не должны быть обязательно связаны друг с другом. Например, по крайней мере два из атомов углерода могут быть связаны посредством подходящего элемента или группы. Таким образом, гидрокарбильная группа может содержать гетероатомы. Подходящие гетероатомы должны быть очевидны специалистам в соответствующей области и включают, например, серу, азот и кислород. В одном из предпочтительных вариантов осуществления гидрокарбильная группа является углеводородной группой. Термин углеводород означает в контексте какую-либо из алкильной группы, алкенильной группы, алкинильной группы, ацильной группы, каковые группы могут быть неразветвленными, разветвленными или циклическими, или арильной группы. Термин углеводород также включает эти группы в тех случаях, когда они необязательно замещены. Если углеводород является разветвленной структурой, содержащей заместитель или заместители, то замещение может иметь место или по основной углеводородной цепи, или по побочной; альтернативно, может иметь место замещение и по основной, и по побочной углеводородной цепи. В одном из предпочтительных вариантов осуществления гидрокарбильная группа является оксигидрокарбильной группой. Термин оксигидрокарбильная группа, как он используется в контексте, означает группу, которая включает, по крайней мере, атом углерода, атом водорода и атом кислорода и может необязательно включать один или более из иных подходящих заместителей. Примеры таких заместителей могут включать галоид, алкоксигруппу, нитрогруппу, алкильную группу, циклическую группу, и т.д. В дополнение к той возможности, что заместитель является циклической группой, комбинация заместителей может образовывать циклическую группу. Если оксигидрокарбильная группа включает более одного атома уг- 12011123 лерода, такие атомы углерода не должны быть обязательно связаны друг с другом. Например, по крайней мере два из атомов углерода могут быть связаны посредством подходящего элемента или группы. Таким образом, оксигидрокарбильная группа может содержать гетероатомы. Подходящие гетероатомы должны быть очевидны специалистам в соответствующей области и включают, например, серу и азот. В одном из предпочтительных вариантов осуществления оксигидрокарбильная группа является оксиуглеводородной группой. Термин оксиуглеводород означает в контексте какую-либо из алкоксигруппы, оксиалкенильной группы, оксиалкинильной группы, каковые группы могут быть неразветвленными, разветвленными или циклическими, или оксиарильной группы. Термин оксиуглеводород также включает эти группы в тех случаях, когда они необязательно замещены. Если оксиуглеводород является разветвленной структурой, содержащей заместитель или заместители, то замещение может иметь место или по основной углеводородной цепи, или по побочной; альтернативно, может иметь место замещение и по основной, и по побочной углеводородной цепи. Предпочтительно оксигидрокарбильная группа является алкоксигруппой. Предпочтительно оксигидрокарбильная группа имеет формулу C1-6O (как, например, С 1-3 О). Примером D' служит 5- или 6-членное негетероциклическое кольцо, содержащее по крайней мере один заместитель. В одном из предпочтительных вариантов осуществления цикл D' замещен этинильной группой. Если какой-либо из циклов А', В', С' и D' является гетероциклом, то этот гетероцикл предпочтительно включает комбинацию атомов углерода по крайней мере с одним атомом азота и/или по крайней мере одним атомом кислорода. В цикле могут присутствовать и другие гетероциклические атомы. Примеры подходящих предпочтительных циклов A'-D' стероидного ядра в соединениях по настоящему изобретению включают циклы A-D эстрона и дегидроэпиандростерона. Примеры подходящих предпочтительных циклов A'-D' стероидного ядра в соединениях включают циклы A-D следующих соединений: эстронов и замещенных эстронов, а именно: эстрона,2-ОН-эстрона,2-алкоксиэстрона (как, например, (С 1-C6)алкоксиэстрон, такой как 2-метоксиэстрон),4-ОН-эстрона,6-ОН-эстрона,7-ОН-эстрона,16-ОН-эстрона,16-ОН-эстрона; эстрадиолов и замещенных эстрадиолов, а именно 2-ОН-17-эстрадиола,2-алкокси-17-эстрадиола (как, например, (С 1-C6)алкокси-17-эстрадиол, такой как 2-метокси-17 эстрадиол),4-ОН-17-эстрадиола,6-OH-17-эстрадиола,7-OH-17-эстрадиола,2-ОН-17-эстрадиола,2-алкокси-17-эстрадиола (как, например, (С 1-C6)алкокси-17-эстрадиол, такой как 2-метокси-17 эстрадиол),4-ОН-17-эстрадиола,6-ОН-17-эстрадиола,7-ОН-17-эстрадиола,16-ОН-17-эстрадиола,16-ОН-17-эстрадиола,16-ОН-17-эстрадиола,16-ОН-17-эстрадиола,17-эстрадиола,17-эстрадиола,17-этинил-17-эстрадиола,17-этинил-17-эстрадиола; эстриолов и замещенных эстриолов, а именно: эстриола, 2-ОНэстриола,2-алкоксиэстриола (как, например, (С 1-C6)эстриол, такой как 2-метоксиэстриол),4-ОН-эстриола, 6-ОН-эстриола, 7-ОН-эстриола; дегидроэпиандростеронов и замещенных дегидроэпиандростеронов, а именно дегидроэпиандростеронов, 6-ОН-дегидроэпиандростерона, 7-ОН-дегидроэпиандростерона, 16 ОН-дегидроэпиандростерона, 16-ОН-дегидроэпиандростерона.- 13011123 В целом, циклическая система A'B'C'D' может содержать множество разнообразных не создающих друг другу помех заместителей. В частности, циклическая система A'B'C'D' может содержать какой-либо один или более из следующих заместителей: гидроксигруппу, алкильную группу, в особенности,низш.(C1-C6)алкил, например, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, нпентил и другие изомеры пентила, а также н-гексил и другие изомеры гексила, алкоксигруппу, в особенности, низш.(C1-C6)алкоксигруппу, например, метоксигруппу, этоксигруппу, пропоксигруппу и т.д., алкинильную группу, например, этинил, или галоид, например фтор. В альтернативном варианте осуществления полициклическое соединение может не содержать стероидного ядра или не иметь его в основе. Подобное полициклическое соединение может содержать или иметь в основе нестероидную циклическую систему, такую как диэтилстильбэстрол, стильбэстрол, кумарины и другие циклические системы. Другие подходящие нестероидные соединения для применения в композиции или в качестве композиции по настоящему изобретению могут быть найдены в патенте США 5567831.R1 и R2. В одном из предпочтительных вариантов осуществления соединение отвечает формуле I в которой R1 является необязательной группой, выбранной среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. В одном из предпочтительных вариантов осуществления соединение отвечает формуле II в которой R1 является необязательной группой, выбранной среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. В одном из предпочтительных вариантов осуществления соединение отвечает формуле III в которой R1 является необязательной группой, выбранной среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. В одном из предпочтительных вариантов осуществления соединение отвечает формуле IV в которой R1 является необязательной группой, выбранной среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. Понятно, что цикл А циклической стероидной системы в формулах I-IV дополнительно замещен по положению 2 или 4 группой R4.R1. Специалисты в данной области должны понимать, что R1 является необязательной группой, которая может как присутствовать, так и не присутствовать. В одном из предпочтительных вариантов осуществления присутствует. В этом случае R1 является группой, выбранной среди гидроксигруппы, сульфаматной группы, фосфонатной группы, тиофосфонатной группы, сульфогруппы или сульфонамидной группы. Сульфаматная группа. В одном из вариантов осуществления R1 является необязательной сульфаматной группой. Термин сульфамат включает сложный эфир сульфаминовый кислоты, или сложный эфир Nзамещенного производного сульфаминовой кислоты, или их соль. В одном из вариантов осуществления R1 является сульфаматной группой. В этом случае соединение может именоваться сульфаматным соединением.- 14011123 Предпочтительно сульфаматная группа R1 является сульфаматной группой формулы в которой R5 и R6 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы. Предпочтительно R5 и R6 независимо выбраны среди атома водорода, алкильной, циклоалкильной,алкенильной, ацильной и арильной групп, или их комбинаций, или совместно являются алкиленовой группой, причем алкильная, или циклоалкильная, или алкенильная, или арильная группы, или каждая из этих групп необязательно содержат один или более гетероатом или группу. В случае замещенных соединений N-замещенные соединения по настоящему изобретению могут содержать один или два N-алкильных, N-алкенильных, N-циклоалкильных, N-ацильных или N-арильных заместителя, предпочтительно содержащих совместно или по отдельности не более 10 атомов углерода. В тех случаях, когда R5 и/или R6 является алкилом, предпочтительными вариантами являются такие, когда R5 и R6 независимо друг от друга выбраны среди низш.алкильных групп, содержащих от 1 до 5 атомов углерода, т.е. метильной, этильной, пропильной и т.д. Предпочтительно и R5, и R6 являются метильными группами. В тех случаях, когда R5 и/или R6 являются арильными группами, типичными вариантами являются фенильная и толильная группы (-PhCH3; о-, м- или п-). В тех случаях, когда R5 и R6 представляют собой циклоалкильную группу, типичными вариантами являются циклопропил, циклопентил,циклогексил и т.д. В тех случаях, когда R5 и R6 объединены, они, как правило, представляют собой алкиленовую группу с цепочкой из от 4 до 6 атомов углерода, необязательно прерываемой одним или более гетероатомом или группой, например -О- или -NH-, что приводит к 5-, 6- или 7-членному гетероциклу,например морфолину, пирролидину или пиперидину. В круг возможных вариантов алкильных, циклоалкильных, алкенильных, ацильных и арильных групп мы включаем замещенные группы, содержащие в качестве заместителей одну или более групп, не влияющих на активность рассматриваемого соединения в ингибировании стероидной сульфатазы. Примеры не влияющих на активность заместителей включают гидроксигруппу, аминогруппу, галоид, алкоксигруппу, алкильную группу и арильную группу. Примером гидрокарбильной группы, не ограничивающим круг возможных вариантов, является ацильная группа. В некоторых вариантах осуществления сульфаматная группа может образовывать циклическую структуру путем замыкания (или связывания с) одним или более атомами в или на стероидной циклической системе. В некоторых вариантах осуществления может наличествовать более одной сульфаматной группы. В качестве примера может присутствовать два сульфамата (т.е. бис-сульфаматные соединения). В некоторых предпочтительных вариантах осуществления по крайней мере одна из групп R5 и R6 является атомом водорода. В некоторых предпочтительных вариантах осуществления каждая из групп R5 и R6 являются атомом водорода. В некоторых предпочтительных вариантах осуществления R1 является сульфаматной группой, а соединение пригодно для применения в качестве ингибитора эстронсульфатазы (Е.С. 3.1.6.2). В некоторых предпочтительных вариантах осуществления в тех случаях, когда сульфаматная группа в сульфаматном соединении должна быть заменена сульфатной группой с образованием сульфатного соединения, такое сульфатное соединение подвержено гидролизу ферментом стероидной сульфатазой(Е.С. 3.1.6.2). В некоторых предпочтительных вариантах осуществления, если бы сульфаматная группа в сульфаматном соединении была заменена сульфатной группой с образованием сульфатного соединения, а последнее было бы инкубировано с ферментом стероидной сульфатазой (Е.С. 3.1.6.2) при рН 7,4 и температуре 37 С, такое соединение характеризовалось бы величиной Km менее 50 мМ. В некоторых предпочтительных вариантах осуществления, если бы сульфаматная группа в сульфаматном соединении была заменена сульфатной группой с образованием сульфатного соединения, а последнее было бы инкубировано с ферментом стероидной сульфатазой (Е.С. 3.1.6.2) при рН 7,4 и температуре 37 С, такое соединение характеризовалось бы величиной Km менее 50 мкМ. Фосфонатная группа. Если соединение включает фосфонатную группу, то соединение именуется фосфонатным соединением. В типичном случае, фосфонатная группа имеет формулу (R18)-Р(O)(ОН)-O-, где R18 предпочтительно является атомом водорода, алкильной, циклоалкильной, алкенильной, ацильной или арильной группой или их комбинациями, причем каждая алкильная, или циклоалкильная, или алкенильная, или арильная группа необязательно содержит один или более гетероатом или группу. В тех случаях, когда R18 является алкильной группой, R18 может быть низш.алкильными группами,- 15011123 содержащими от 1 до 6 атомов углерода, т.е. метильной, этильной, пропильной и т.д. В качестве примераR18 может быть метилом. В тех случаях, когда R18 является арильной группой, типичными вариантами являются фенильная и толильная группы (-PhCH3; о-, м- или п-). В тех случаях, когда R18 представляет собой циклоалкильную группу, типичными вариантами являются циклопропил, циклопентил, циклогексил и т.д. R18 может даже включать алкиленовую группу с цепочкой из от 4 до 6 атомов углерода, необязательно прерываемой одним или более гетероатомом или группой, являясь, например, 5-членным гетероциклом, например морфолином, пирролидином или пиперидином. В круг возможных вариантов алкильных, циклоалкильных, алкенильных, ацильных и арильных групп мы включаем замещенные группы, содержащие в качестве заместителей одну или более групп, не влияющих на активность рассматриваемого соединения в ингибировании стероидной сульфатазы. Примеры не влияющих на активность заместителей включают гидроксигруппу, аминогруппу, галоид, алкоксигруппу, алкильную группу и арильную группу. В некоторых вариантах осуществления фосфонатная группа может образовывать циклическую структуру путем замыкания (или связывания с) одним или более атомами в или на стероидной циклической системе. В некоторых вариантах осуществления может наличествовать более одной фосфонатной группы. В качестве примера может присутствовать два фосфоната (т.е. бис-фосфонатные соединения). Если такие соединения имеют в своей основе стероидное ядро, вторая (или по крайней мере одна из дополнительных) фосфонатная группа предпочтительно присоединена по 17 положению стероидного ядра. Такие группы не должны быть обязательно одинаковы. Тиофосфонатная группа. Если соединение включает тиофосфонатную группу, то соединение именуется тиофосфонатным соединением. В типичном случае, фосфонатная группа имеет формулу (R18)-P(S)(OH)-O-, где R18 предпочтительно является атомом водорода, алкильной, циклоалкильной, алкенильной, ацильной или арильной группой или их комбинациями, причем каждая алкильная, или циклоалкильная, или алкенильная, или арильная группа необязательно содержит один или более гетероатом или группу. В тех случаях, когда R18 является алкильной группой, R18 может быть низш.алкильными группами,содержащими от 1 до 6 атомов углерода, т.е. метильной, этильной, пропильной и т.д. В качестве примераR18 может быть метилом. В тех случаях, когда R18 является арильной группой, типичными вариантами являются фенильная и толильная группы (-PhCH3; о-, м- или п-). В тех случаях, когда R18 представляет собой циклоалкильную группу, типичными вариантами являются циклопропил, циклопентил, циклогексил и т.д. R18 может даже включать алкиленовую группу с цепочкой из от 4 до 6 атомов углерода, необязательно разрываемой одним или более гетероатомом или группой, являясь, например, 5-членным гетероциклом, например морфолином, пирролидином или пиперидином. В круг возможных вариантов алкильных, циклоалкильных, алкенильных, ацильных и арильных групп мы включаем замещенные группы, содержащие в качестве заместителей одну или более групп, не влияющих на активность рассматриваемого соединения в ингибировании стероидной сульфатазы. Примеры не влияющих на активность заместителей включают гидроксигруппу, аминогруппу, галоид, алкоксигруппу, алкильную группу и арильную группу. В некоторых вариантах осуществления тиофосфонатная группа может образовывать циклическую структуру путем замыкания (или связывания с) одним или более атомам в или на стероидной циклической системе. В некоторых вариантах осуществления может наличествовать более одной тиофосфонатной группы. В качестве примера может присутствовать два тиофосфоната (т.е. бис-тиофосфонатные соединения). Если такие соединения имеют в своей основе стероидное ядро, вторая (или по крайней мере одна из дополнительных) тиофосфонатная группа предпочтительно присоединена по 17 положению стероидного ядра. Такие группы не должны быть обязательно одинаковы. Сульфогруппа. Если соединение включает сульфогруппу, то соединение именуется сульфонатным соединением. В типичном случае сульфогруппа имеет формулу (R20)-S(O)(O)-O-, где R20 предпочтительно является атомом водорода, алкильной, циклоалкильной, алкенильной, ацильной или арильной группой или их комбинациями, причем каждая алкильная, или циклоалкильная, или алкенильная, или арильная группа необязательно содержит один или более гетероатом или группу. В тех случаях, когда R20 является алкильной группой, R20 может быть низш.алкильными группами,содержащими от 1 до 6 атомов углерода, т.е метильной, этильной, пропильной и т.д. В качестве примераR20 может быть метилом. В тех случаях, когда R20 является арильной группой, типичными вариантами являются фенильная и толильная группы (-PhCH3; о-, м- или п-). В тех случаях, когда R20 представляет собой циклоалкильную группу, типичными вариантами являются циклопропил, циклопентил, циклогексил и т.д. R20 может даже включать алкиленовую группу с цепочкой из от 4 до 6 атомов углерода, необязательно прерываемой одним или более гетероатомом или группой, являясь, например, 5-членным гетероциклом, например морфолином, пирролидином или пиперидином.- 16011123 В круг возможных вариантов алкильных, циклоалкильных, алкенильных, ацильных и арильных групп мы включаем замещенные группы, содержащие в качестве заместителей одну или более групп, не влияющих на активность рассматриваемого соединения в ингибировании стероидной сульфатазы. Примеры не влияющих на активность заместителей включают гидроксигруппу, аминогруппу, галоид, алкоксигруппу, алкильную группу и арильную группу. В некоторых вариантах осуществления сульфогруппа может образовывать циклическую структуру путем замыкания (или связывания с) одним или более атомами в или на стероидной циклической системе. В некоторых вариантах осуществления может наличествовать более одной сульфогруппы. В качестве примера, может присутствовать два сульфоната (т.е. бис-сульфонатные соединения). Если такие соединения имеют в своей основе стероидное ядро, вторая (или по крайней мере одна из дополнительных) сульфогруппа предпочтительно присоединена по 17 положению стероидного ядра. Такие группы не должны быть обязательно одинаковы. Другие заместители. Соединение может иметь иные заместители, нежели включенные в формулу I. В качестве примера подобные иные заместители могут быть каким-либо одним или более среди следующих: одна или более сульфаматная группа(группы), одна или более фосфонатная группа(группы), одна или более тиофосфонатная группа(группы), одна или более сульфогруппа(группы), одна или более сульфонамидная группа(группы), одна или более галоидная группа, одна или более группа в виде атома кислорода, одна или более гидроксигруппа. одна или более аминогруппа, одна или более серосодержащая группа(группы),одна или более гидрокарбильная группа(группы), такая как оксигидрокарбильная группа. Цикл D стероидной циклической системы соединения замещен группой R2 формулы -L-R , где L является необязательной мостиковой группой, a R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп. В некоторых предпочтительных вариантах осуществления R2 имеет формулу -R3; иными словами,группа L отсутствует. В некоторых предпочтительных вариантах осуществления группа R2 имеет -конформацию. Предпочтительно группа R2 находится в -конформации и присоединена по 17 положению в цикле D.L. В некоторых вариантах осуществления L является гидрокарбильной группой. В некоторых вариантах осуществления L является углеводородной группой, такой как алкиленовая группа. В типичных случаях, L может быть (C1-C10)алкиленом, (C1-С 5)алкиленом, C1- или C2-алкиленом.R3. Как обсуждалось выше, R3 выбрана среди групп, являющихся нитрильной группой, спиртом, сложным эфиром, простым эфиром, амином и алкеном или включающих одну из перечисленных групп. В некоторых предпочтительных вариантах осуществления R3 выбрано среди следующих групп: нитрила,спирта, сложного эфира, простого эфира, амина или алкена. Предпочтительно R3 является нитрильной группой или включает ее. Предпочтительно R3 является нитрильной группой.R3 может быть циклической группой или нециклической группой. В тех случаях, когда R3 является циклической группой, она может образовывать цикл, конденсированный с циклом D стероида или не конденсированный с циклом D стероида. В тех случаях, когда R3 является циклической группой, конденсированной с циклом D стероида, R3 предпочтительно образует цикл, присоединенный по соседним положениям в цикле D; более предпочтительно, R3 образует цикл, присоединенный к циклу D по положениям 16 и 17. В некоторых предпочтительных вариантах осуществления R3 выбрана из групп формулы =СН 2,=СН-СН 3, =C(CN)2, =C(CH3)(CN) и -(R7)n(CR14R15)pR8, где n принимает значения 0 или 1, р является целым числом, R7 выбрана среди =СН-, -О- и NR13; R8 выбрана среди -SO2-R9, -C(O)OR17, -OR10, (CH2)q-XR16, -CN, -NR11R12-CCH и -СН=СН 2; R9 выбрана среди атома водорода и гидрокарбильной группы, R10 выбрана среди атома водорода и гидрокарбильной группы; R11 и R12 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы; R13 выбрана среди атома водорода и гидрокарбильной группы, R14 и R15 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, q является целым числом, X является кислородом или серой, R16 выбрана среди атома водорода и гидрокарбильной группы и R17 выбрана среди атома водорода и гидрокарбильной группы. В некоторых предпочтительных вариантах осуществления R3 является группой формулы 7R9 выбрана среди атома водорода и гидрокарбильной группы, R10 выбрана среди атома водорода и гидрокарбильной группы; R11 и R12 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы; R13 выбрана среди атома водорода и гидрокарбильной группы, R14 и R15 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, q является целым числом, X- 17011123 является кислородом или серой, R16 выбрана среди атома водорода и гидрокарбильной группы и R17 выбрана среди атома водорода и гидрокарбильной группы. В некоторых предпочтительных вариантах осуществления R3 является группой формулы 14 15-(CR R )pR8, р является целым числом; R8 выбрана среди -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN,-NR11R12 -ССН и -CH=CH2; R9 выбрана среди атома водорода и гидрокарбильной группы, R10 выбрана среди атома водорода и гидрокарбильной группы; R11 и R12 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, R14 и R15 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, q является целым числом, X является кислородом или серой, R16 выбрана среди атома водорода и гидрокарбильной группы и R17 выбрана среди атома водорода и гидрокарбильной группы. В некоторых предпочтительных вариантах осуществления R3 является группой формулы -(CH2)pR8,р является целым числом; R8 выбрана среди -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN, -NR11R12,-CCH и -СН=СН 2; R9 выбрана среди атома водорода и гидрокарбильной группы, R10 выбрана среди атома водорода и гидрокарбильной группы; R11 и R12 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, q является целым числом, X является кислородом или серой, R16 выбрана среди атома водорода и гидрокарбильной группы и R17 выбрана среди атома водорода и гидрокарбильной группы. В некоторых предпочтительных вариантах осуществления R3 является группой формулы -(R7)nR8,где n принимает значения 0 или 1, R7 выбрана среди =СН-, -О- и NR13; R8 выбрана среди -SO2-R9,-C(O)OR17, -OR10, (CH2)q-X-R16, -C=N, -NR11R12-CCH и -CH=CH2; R9 выбрана среди атома водорода и гидрокарбильной группы, R10 выбрана среди атома водорода и гидрокарбильной группы; R11 и R12 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы; R13 выбрана среди атома водорода и гидрокарбильной группы, q является целым числом, X является кислородом или серой, R16 выбрана среди атома водорода и гидрокарбильной группы и R17 выбрана среди атома водорода и гидрокарбильной группы. Число р может принимать любое целое значение. Число р может лежать в пределах от 0 до 20. Число р может лежать в пределах от 0 до 10. В типичных случаях, р находится в пределах от 0 до 5. В одном из вариантов осуществления р принимает значения 0, 1 или 2. Число q может принимать любое целое значение. Число q может лежать в пределах от 0 до 20. Число q может лежать в пределах от 0 до 10. В типичных случаях q находится в пределах от 0 до 5. В одном из вариантов осуществления q принимает значения 0, 1 или 2.R8 выбрана среди -SO2-R9, -C(O)OR17, -OR10, (CH2)q-X-R16, -CN, -NR11R12, -CCH и -СН=СН 2. В одном из предпочтительных вариантов осуществления R8 является -SO2-R9. В одном из предпочтительных вариантов осуществления R8 является -SO2-R9, где R9 является гидрокарбильной группой. Предпочтительно в данном варианте осуществления R7 является -О-, n принимает значение 1 и р принимает значение 0, таким образом, что R3 является -O-SO2R9.R9 выбрана среди атома водорода и гидрокарбильной группы. В одном из вариантов осуществления 9R является гидрокарбильной группой. В одном из предпочтительных вариантов осуществления R9 выбрана среди какой-либо из следующих групп: атома водорода, (С 1-C20)гидрокарбильной, (С 1C10)гидрокарбильной, (С 1-С 5)гидрокарбильной, (С 1-C3)гидрокарбильной групп, углеводородных групп,(С 1-C20)углеводородной, (C1-C10)углеводородной, (С 1-С 5)углеводородной, (С 1-C3)углеводородной групп,алкильных групп, (С 1-C20)алкильной, (C1-C10)алкильной, (C1-С 5)алкильной и (C1-C3)алкильной групп. В одном из вариантов осуществления R9 выбрана среди атома водорода и (C1-C10)алкила. В одном из вариантов осуществления настоящего изобретения R9 является (C1-C10)алкилом. В одном из вариантов осуществления R9 выбрана среди атома водорода и (C1-С 5)алкила. В одном из вариантов осуществленияR9 является (С 1-С 5)алкилом. В одном из вариантов осуществления R9 выбрана среди атома водорода и(С 1-C3)алкила. В одном из вариантов осуществления R9 является (С 1-C3)алкилом. Предпочтительно R9 является этилом. В одном из вариантов осуществления R9 является замещенным или незамещенным амином. В случае наличия замещения N-замещенные соединения могут содержать один или два N-алкильных, Nалкенильных, N-циклоалкильных, N-ацильных или N-арильных заместителя, предпочтительно содержащих вместе или по отдельности не более 10 атомов углерода. В предпочтительном варианте осуществления R9 является незамещенным амином, т.е. R9 является NH2.R10 выбрана среди атома водорода и гидрокарбильной группы. В одном из предпочтительных вариантов осуществления R10 выбрана среди какой-либо из следующих групп: атома водорода, (С 1C20)гидрокарбильной, (С 1-C10)гидрокарбильной, (С 1-С 5)гидрокарбильной, (С 1-C3)гидрокарбильной групп,углеводородных групп, (C1-C20)углеводородной, (C1-C10)углеводородной, (С 1-С 5)углеводородной, (C1C3)углеводородной групп, алкильных групп, (C1-C20)алкильной, (C1-C10)алкильной, (C1-С 5)алкильной и(С 1-C3)алкильной групп. В одном из вариантов осуществления R10 выбрана среди атома водорода и (C1-C10)алкила. В одном из вариантов осуществления R10 выбрана среди атома водорода и (С 1-С 5)алкила. В одном из вариантов- 18011123 осуществления R10 выбрана среди атома водорода и (C1-C3)алкила. В одном из вариантов осуществленияR10 является (C1-C3)алкилом. Предпочтительно R10 является водородом или метилом. Как было упомянуто выше, R11 и R12, принадлежащие NR11R12, независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы. В случае наличия замещения N-замещенные соединения по настоящему изобретению могут содержать один или два N-алкильных, N-алкенильных, Nциклоалкильных, N-ацильных или N-арильных заместителя, предпочтительно содержащих вместе или по отдельности не более 10 атомов углерода. В тех случаях, когда R11 и/или R12 являются акильными группами, предпочтительными вариантами являются такие, когда R11 и R12 независимо друг от друга выбраны среди низш.алкильных групп, содержащих от 1 до 5 атомов углерода, т.е. метильной, этильной, пропильной и т.д. Предпочтительно и R11, и R12 являются метильными группами. В тех случаях, когда R11 и/или R12 являются арильными группами, типичными вариантами являются фенильная и толильная группы (-PhCH3; о-, м- или п-). В тех случаях, когда R11 и R12 представляют собой циклоалкильную группу,типичными вариантами являются циклопропил, циклопентил, циклогексил и т.д. В тех случаях, когда R11 и R12 объединены, они, как правило, представляют собой алкиленовую группу с цепочкой из от 4 до 6 атомов углерода, необязательно прерываемой одним или более гетероатомом или группой, например, -Оили -NH-, что приводит к 5-, 6- или 7-членному гетероциклу, например, морфолину, пирролидину или пиперидину. В одном из вариантов осуществления R11 и R12 независимо друг от друга являются гидрокарбильными группами. В одном из предпочтительных вариантов осуществления настоящего изобретения R11 иR12 независимо друг от друга выбраны среди какой-либо из следующих групп: атома водорода, (С 1C20)гидрокарбильной, (C1-C10)гидрокарбильной, (С 1-С 5)гидрокарбильной, (С 1-C3)гидрокарбильной групп,углеводородных групп, (C1-C20)углеводородной, (C1-C10)углеводородной, (С 1-С 5)углеводородной, (C1C3)углеводородной групп, алкильных групп, (C1-C20)алкильной, (C1-C10)алкильной, (С 1-С 5)алкильной и(C1-C3)алкильной групп. В одном из вариантов осуществления R11 и R12 независимо друг от друга выбраны среди атома водорода и (C1-C10)алкила. В одном из вариантов осуществления R11 и R12 независимо друг от друга являются (С 1-C10)алкильными группами. В одном из вариантов осуществления R11 и R12 независимо друг от друга выбраны среди атома водорода и (С 1-С 5)алкила. В одном из вариантов осуществления R11 и R12 независимо друг от друга являются (С 1-С 5)алкильными группами. В одном из вариантов осуществленияR11 и R12 независимо друг от друга выбраны среди атома водорода и (С 1-C3)алкила. В одном из вариантов осуществления R11 и R12 независимо друг от друга являются (С 1-C3)алкильными группами. Предпочтительно R11 и R12 независимо друг от друга выбраны среди атома водорода и метильной группы.R13 выбрана среди атома водорода и гидрокарбильной группы. В одном из предпочтительных вариантов осуществления R13 выбрана среди какой-либо из следующих групп: атома водорода, (C1C20)гидрокарбильной, (C1-C10)гидрокарбильной, (С 1-C5)гидрокарбильной, (С 1-C3)гидрокарбильной групп,углеводородных групп, (С 1-C20)углеводородной, (C1-C10)углеводородной, (C1-С 5)углеводородной, (С 1C3)углеводородной групп, алкильных групп, (С 1-C20)алкильной, (C1-C10)алкильной, (С 1-С 5)алкильной и(C1-C3)алкильной групп. В одном из вариантов осуществления R13 выбрана среди атома водорода и (C1-C10)алкила. В одном из вариантов осуществления R13 выбрана среди атома водорода и (C1-С 5)алкила. В одном из вариантов осуществления R13 выбрана среди атома водорода и (С 1-C3)алкила. В одном из вариантов осуществленияR14 и R15 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы. В одном из вариантов осуществления R14 и R15 независимо друг от друга являются гидрокарбильными группами. В одном из предпочтительных вариантов осуществления R14 и R15 независимо друг от друга выбраны среди какой-либо из следующих групп: атома водорода, (C1-С 20)гидрокарбильной, (C1C10)гидрокарбильной, (C1-С 5)гидрокарбильной, (C1-C3)гидрокарбильной групп, углеводородных групп,(С 1-C20)углеводородной, (C1-C10)углеводородной, (С 1-C5)углеводородной, (С 1-C3)углеводородной групп,алкильных групп, (С 1-C20)алкильной, (C1-C10)алкильной, (С 1-С 5)алкильной и (С 1-C3)алкильной групп. В одном из вариантов осуществления R14 и R15 независимо друг от друга выбраны среди атома водорода и (C1-C10)алкила. В одном из вариантов осуществления R14 и R15 независимо друг от друга являются (C1-C10)алкильными группами. В одном из вариантов осуществления R14 и R15 независимо друг от друга выбраны среди атома водорода и (С 1-С 5)алкила. В одном из вариантов осуществления R14 и R15 независимо друг от друга являются (С 1-С 5)алкильными группами. В одном из вариантов осуществленияR14 и R15 независимо друг от друга выбраны среди атома водорода и (С 1-C3)алкила. В одном из вариантов осуществления R14 и R15 независимо друг от друга являются выбрана среди атома водорода и (С 1C3)алкильными группами. Предпочтительно R14 и R15 независимо друг от друга выбраны среди атома водорода и метильной группы.X выбрана среди атомов кислорода или серы. В одном из вариантов осуществления X является атомом серы. В одном из вариантов осуществления X является атомом кислорода.R16 выбрана среди атома водорода и гидрокарбильной группы. В одном из предпочтительных вариантов осуществления R16 выбрана среди какой-либо из следующих групп: атома водорода, (C1- 19011123(C1-C3)алкильной групп. В одном из вариантов осуществления R16 выбрана среди атома водорода и (C1-C10)алкила. В одном из вариантов осуществления R16 выбрана среди атома водорода и (С 1-С 5)алкила. В одном из вариантов осуществления R16 выбрана среди атома водорода и (С 1-C3)алкила. В одном из вариантов осуществленияR16 является (С 1-C3)алкилом. Предпочтительно R16 является атомом водорода. В одном из особенно предпочтительных вариантов осуществления R3 является группой, выбранной среди =CHC(O)OEt, -CH2C(O)OEt, =CHCH2OH, -СН 2 СН 2 ОН, -CH2CN, =CHCN, -NHCH2CH2N(Me)2,-OCH2CH2-OMe. Наиболее предпочтительные группы R3 выбраны среди представленных ниже вариантов замещения в цикле D В одном из вариантов осуществления R3 может быть выбрана среди показанных ниже вариантов замещения в цикле D, причем каждая Q независимо друг от друга выбрана среди атома кислорода, атома серы, NH и CH2, а y является целым числом, принимающим значения от 3 до 8, предпочтительно 5, 6, 7 и 8. Как было упомянуто выше, цикл А стероидной циклической системы замещен группой R4, где R4 является гидрокарбильной группой. В одном из предпочтительных вариантов осуществления R4 является оксигидрокарбильной группой. Как это обсуждалось выше, термин оксигидрокарбильная группа, как он используется в контексте в отношении R4, означает группу, которая включает, по крайней мере, атомы углерода, водорода и кислорода и может необязательно включать один или более из иных подходящих заместителей. Примеры таких заместителей могут включать галоид, алкоксигруппу, нитрогруппу, алкильную группу, циклическую группу и т.д. В дополнение к той возможности, что заместитель является циклической группой,комбинация заместителей может образовывать циклическую группу. Если оксигидрокарбильная группа включает более одного атома углерода, такие атомы углерода не должны быть обязательно связаны друг с другом. Например, по крайней мере два из атомов углерода могут быть связаны посредством подходящего элемента или группы. Таким образом, оксигидрокарбильная группа может содержать гетероатомы. Подходящие гетероатомы должны быть очевидны специалистам в соответствующей области и включают, например, серу и азот. В одном из предпочтительных вариантов осуществления R4 является оксиуглеводородной группой. Термин оксиуглеводород означает в контексте (или R4 является) какую-либо из алкоксигруппы,оксиалкенильной группы, оксиалкинильной группы, каковые группы могут быть неразветвленными, разветвленными или циклическими, или оксиарильной группы. Термин оксиуглеводород также включает эти группы в тех случаях, когда они необязательно замещены. Если оксиуглеводород является разветвленной структурой, содержащей заместитель или заместители, то замещение может иметь место или по- 20011123 основной углеводородной цепи, или по побочной; альтернативно, может иметь место замещение и по основной, и по побочной углеводородной цепи. Предпочтительно оксигидрокарбильная группа R4 является алкоксигруппой. Предпочтительно оксигидрокарбильная группа R4 отвечает формуле С 1-6 О (такой, как С 1-3 О). Предпочтительно, оксигидрокарбильная группа R4 отвечает формуле -O(CH2)1-10CH3, -O(CH2)1-5CH3, -O(CH2)1-2CH3. В особенно предпочтительном варианте осуществления R4 является метоксигруппой. Предпочтительно оксигидрокарбильная группа R4 является простой эфирной группой. Предпочтительно оксигидрокарбильная группа R4 отвечает формуле C1-6OC1-6 (такой как C1-3OC1-3). Предпочтительно оксигидрокарбильная группа R4 отвечает формуле -(CH2)1-10O(CH2)1-10CH3, -(CH2)1-5O(CH2)1-5CH3,-(СН 2)1-2O(СН 2)1-2CH3. В особенно предпочтительном варианте осуществления R4 является -СН 2 ОСН 3. В одном из предпочтительных вариантов осуществления R4 является углеводородной группой. Предпочтительно R4 является алкильной группой. Предпочтительно алкильная группа является (С 1C6)алкильной группой (такой как (С 1-C3)алкильная группа). Предпочтительно гидрокарбильная группаR4 отвечает формуле -(CH2)1-10CH3, -(СН 2)1-5CH3, -(CH2)1-2CH3. В особенно предпочтительном варианте осуществления R4 является этилом. В одном из предпочтительных вариантов осуществления R4 выбрана среди какой-либо из следующих групп: (C1-C10)гидрокарбильной, (С 1-С 5)гидрокарбильной, (С 1-C3)гидрокарбильной групп, углеводородных групп, (C1-С 10)углеводородной, (С 1-С 5)углеводородной, (С 1-C3)углеводородной групп, алкильных групп, (C1-C10)алкильной, (C1-С 5)алкильной и (C1-C3)алкильной групп. В одном из предпочтительных вариантов осуществления R4 является гидрокарбилсульфанильной группой. Термин гидрокарбилсульфанил означает группу, включающую, по крайней мере, гидрокарбильную группу (как она определена в контексте) и серу. Эта серосодержащая группа может быть необязательно окислена. Предпочтительно гидрокарбилсульфанильная группа отвечает формуле -S-гидрокарбил, где гидрокарбильная группа является такой, как описано в контексте. Термин гидрокарбилсульфанильная группа, как он используется в контексте в отношении R4, означает группу, которая включает, по крайней мере, атомы углерода, водорода и серы и может необязательно включать один или более из иных подходящих заместителей. Примеры таких заместителей могут включать галоид, алкоксигруппу, нитрогруппу, алкильную группу, циклическую группу и т.д. В дополнение к той возможности, что заместитель является циклической группой, комбинация заместителей может образовывать циклическую группу. Если гидрокарбилсульфанильная группа включает более одного атома углерода, такие атомы углерода не должны быть обязательно связаны друг с другом. Например, по крайней мере два из атомов углерода могут быть связаны посредством подходящего элемента или группы. Таким образом, гидрокарбилсульфанильная группа может содержать и другие гетероатомы. Подходящие гетероатомы должны быть очевидны специалистам в соответствующей области и включают, например, азот. В одном из предпочтительных вариантов осуществления R4 является гидрокарбилсульфанильной группой. Термин гидрокарбилсульфанильная группа, как он используется в контексте в отношении R4,означает группу, состоящую из атомов углерода, водорода и серы. Предпочтительно гидрокарбилсульфанильная группа отвечает формуле -S-углеводород, где углеводородная группа является такой, как описано в контексте. Предпочтительно гидрокарбилсульфанильная группа R4 отвечает формуле C1-6S (такой как C1-3S). Предпочтительно гидрокарбилсульфанильная группа R4 отвечает формуле -S(CH2)1-10CH3, -S(CH2)1-5CH3,-S(CH2)1-2CH3. В особенно предпочтительном варианте осуществления R4 является -S-Me. Как было упомянуто выше, R4 находится в положении 2 или 4 в цикле А. Таким образом, соединение может отвечать формуле Предпочтительно R4 находится в положении 2 в цикле А. Еще в одном предпочтительном варианте осуществления настоящего изобретения, в тех случаях,когда цикл А замещен группами R1 и R4, R4 находится в орто-положении по отношению к R1. В предпочтительном варианте осуществления соединение отвечает формуле где R4 является гидрокарбильной группой, R14 и R15 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, а р является целым числом. В предпочтительном варианте осуществления соединение отвечает формуле где R4 является оксиуглеводородной группой или углеводородной группой, R14 и R15 независимо друг от друга выбраны среди атома водорода и (C1-C10)алкильной группы, а р является целым числом, принимающим значения от 0 до 5. В этом варианте осуществления R4 предпочтительно является алкоксигруппой, такой как группа С 1-6 О, или алкильной группой, такой как (С 1-C6)алкильная группа. Предпочтительно R4 является метоксигруппой или этилом. В этом варианте осуществления R14 и R15 предпочтительно выбраны независимо друг от друга среди атома водорода и метильной группы; более предпочтительно и R14, и R15 являются атомами водорода. В этом варианте осуществления р предпочтительно принимает значения 0, 1, или 2. Более предпочтительно р принимает значение 1. В особенно предпочтительном варианте осуществления соединение отвечает формуле В предпочтительном варианте осуществления соединение отвечает формуле где R4 является гидрокарбильной группой, R14 и R15 независимо друг от друга выбраны среди атома водорода и гидрокарбильной группы, а р является целым числом. В предпочтительном варианте осуществления соединение отвечает формуле где R4 является оксиуглеводородной группой или углеводородной группой, R14 и R15 независимо друг от друга выбраны среди атома водорода и (C1-C10)алкильной группы, а р является целым числом, принимающим значения от 0 до 5. В этом варианте осуществления R4 предпочтительно является алкоксигруппой, такой как группа С 1-6 О, или алкильной группой, такой как (С 1-C6)алкильная группа. Предпочтительно R4 является метоксигруппой или этилом. В этом варианте осуществления R14 и R15 предпочтительно выбраны независимо друг от друга среди атома водорода и метильной группы; более предпочтительно и R14, и R15 являются атомами водорода. В этом варианте осуществления р предпочтительно принимает значения 0, 1, или 2. Более предпочтительно р принимает значение 1. В особенно предпочтительном варианте осуществления соединение отвечает формуле Наиболее предпочтительные соединения представлены ниже и могут быть выбраны среди следующих:- 23011123 Композиция. Как это было описано выше, одним из вариантов осуществления является фармацевтическая композиция, включающая: (а) (1) соединение, как оно определено в контексте, или (2) композицию, как она определена в контексте, и (б) фармацевтически приемлемый носитель, разбавитель, наполнитель или адъювант. Композиция может включать более одного модификатора биологической ответной реакции. Термин модификатор биологической ответной реакции включает цитокины, иммуномодуляторы,факторы роста, факторы регуляции гемопоэза, колониестимулирующий фактор, хемотаксические, гемолитические и тромболитические факторы, рецепторы клеточной поверхности, лиганды, лейкоцитарные адгезивные молекулы, моноклональные антитела, профилактические и лечебные вакцины, гормоны,компоненты внеклеточного матрикса, фибронектин и т.д. Модификаторы биологической ответной реакции могут играть роль в модуляции иммунного и воспалительного ответа при расстройствах. Примеры модификаторов биологической ответной реакции включают фактор некроза опухолей (TNF), гранулоцитарный колониестимулирующий фактор, эритропоэтин, инсулиноподобный фактор роста (IGF), фактор роста эпидермиса (EGF), трансформирующий фактор роста (TGF), тромбоцитарный фактор роста (PDGF), интерфероны (IFNs), интерлейкины, тканевые активаторы плазминогена, Р-, Е- и L-селектины, эндотелиальные межклеточные адгезивные молекулы (ICAM-1), васкулярные клеточные адгезивные молекулы (VCAM), селектины, адрессины и т.д. Предпочтительно модификатор биологической ответной реакции является цитокином. Цитокин является молекулой, зачастую - растворимым белком, которая позволяет иммунокомпетентным клеткам обмениваться между собой информацией. Эти молекулы осуществляют свои биологические функции через посредство специфических рецепторов, экспрессированных на поверхности клеток-мишеней. Связывание рецепторов инициирует подачу каскада биохимических сигналов, производящих глубокое воздействие на поведение несущей рецептор клетки (Poole, S 1995 TibTech 13: 81-82). Многие цитокины и их рецепторы идентифицированы на молекулярном уровне (Paul и Sedar 1994, Cell 76: 241-251) и являются подходящими молекулами, имеющими терапевтическое значение, равно как и являются сами по себе мишенями для терапевтического воздействия. Более подробную информацию о цитокинах можно найти в Molecular Biology and Biotechnology(изд. VCH, под ред. Meyers, 1995, стр. 202, 203, 394, 390, 475, 790). Примеры цитокинов включают интерлейкины (IL), такие как IL-1, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7,IL-8, IL-9, IL-10, IL-11, IL-12, IL-19; фактор некроза опухолей (TNF), такой как TNF-; интерфероны ,и ; трансформирующий фактор роста TGF-. Для настоящего изобретения цитокин предпочтительно является фактором некроза опухолей (TNF). Более предпочтительно цитокин является TNF-.TNF является цитокином, вырабатываемым макрофагами и лимфоцитами, который служит посредником в воспалительных и иммунопатологических ответах. TNF вовлечен в процесс развития заболеваний, которые включают иммуномодуляционное расстройство, инфекцию, пролиферацию клеток, ангиогенез, неоваскуляризацию, метастаз опухоли, апоптоз, сепсис и эндотоксемию, но не ограничиваются перечисленным. Омертвевающее действие TNF in vivo в основном относится к повреждению капилляров. TNF вызывает некроз не только в опухолевых тканях, но и в грануляционной ткани. Он вызывает морфологические изменения в ингибировании роста культивируемых клеток сосудистого эндотелия и цитотоксичности в их отношении (Haranka и др. 1987 Ciba Found Symp 131: 140-153). В предпочтительном варианте осуществления TNF может быть любого типа, такой как TNF-,TNF-, включая их производные и смеси. Положения, имеющие отношение к TNF, могут быть найдены в документах, относящихся к данной области, таких как международные заявки на патент WO-А-98/08870 и WO-A-98/13348.TNF может быть получен химическим путем или экстрагирован из содержащих его источников. Предпочтительно TNF получают по методикам, использующим рекомбинантные ДНК. В этом варианте осуществления композиции более эффективны in vivo, чем соединения сами по себе или TNF сам по себе. Более того, комбинация соединений и TNF в некоторых отношениях более эффективны, чем можно было бы ожидать, исходя из эффективности соединения самого по себе, т.е. между соединениями и TNF существуют синергические взаимоотношения. Кроме того, рассматривается композиция, содержащая также индуктор модификатора биологической ответной реакции, такой как индуктор модификатора биологической ответной реакции in vivo. Компоненты композиции могут быть добавлены в общую смесь, одновременно или последовательно. Кроме того, согласно настоящему изобретению может оказаться возможным сформировать по крайней мере часть композиции in situ (как, например, in vivo) путем индуцирования экспрессии или увеличения экспрессии одного из компонентов. Например, может оказаться возможным индуцировать экспрессию или увеличить экспрессию модификатора биологической ответной реакции, такого как TNF. В качестве примера, может оказаться возможным индуцировать экспрессию или увеличить экспрессиюTNF путем добавления бактериального липополисахарида (LPS) и мурамилдипептида (MDP). В этом случае, бактериальный LPS и MDP в комбинации могут стимулировать производство TNF клетками селезенки мышей in vitro и регрессия опухоли in vivo (Fuks и др. Bull Exp Biol Med 1987 104: 497-499). В способе лечения субъект предпочтительно является млекопитающим, более предпочтительно человеком. Для некоторых применений человек предпочтительно является женщиной. Также описаны новые промежуточные вещества, применимые в получении соединений, например новые спирты - предшественники соединений. В качестве дальнейшего примера описаны бисзащищенные предшественники соединений. Примеры каждого из таких предшественников приводятся в настоящей заявке. Описаны также способ синтеза соединений, включающий любой из этих предшественников или их оба. Стероидная сульфатаза. Стероидная сульфатаза, именуемая иногда стероидной сульфатазой, или стерилсульфатазой, или,для краткости, STS, гидролизует ряд сульфатированных стероидов, таких как эстрон-сульфат, дегидроэпиандростерон-сульфат и холестерин-сульфат. В классификации ферментов STS имеет номер ЕС 3.1.6.2.STS является ферментом, вовлеченным в ряд болезненных состояний. В качестве примера исследователи обнаружили, что общий недостаток STS приводит к ихтиозу. Согласно некоторым исследователям, недостаток STS весьма широко распространена в Японии. Те же исследователи (Sakura и др., Inherit Metab Dis, ноябрь 1997; 20(6):807-10) сообщают также, что аллергические заболевания, такие как бронхиальная астма, аллергические риниты или диффузный нейродерматит, могут быть связаны с недостатком стероидной сульфатазы. Вдобавок к болезненным состояниям, возникающим при посредстве общего недостатка активностиSTS, повышенный уровень активности STS может также вызывать болезненные состояния. В качестве примера, как было указано выше, существуют серьезные свидетельства в поддержку того, что STS играет роль в развитии рака молочной железы и метастаз.Genet, март 1999; 29(2): 131-6) обнаружили, что может существовать генетическая корреляция между концентрацией стероидной сульфатазы и инициацией агрессивного поведения у мышей. Авторы заключают, что сульфатирование стероидов может быть первичной движущей силой сложной сети, включающей гены, связанные, как показано, с агрессией при посредстве мутагенеза. Ингибирование STS. Полагают, что некоторые болезненные состояния связаны с активностью STS вследствие преобразования неактивного сульфатированного эстрона в активный несульфатированный эстрон. При болезненных состояниях, связанных с активностью STS, было бы желательно осуществить ингибирование активности STS. Термин ингибировать здесь включает снижение, и/или устранение, и/или маскирование, и/или предотвращение вредного действия STS. Ингибитор STS. Согласно настоящему изобретению соединение по настоящему изобретению способно действовать в качестве ингибитора STS. Термин ингибитор, как он используется в контексте в отношении соединения по настоящему изобретению, означает здесь соединение, которое может ингибировать активность STS, как то снизить,и/или устранить, и/или маскировать, и/или предотвратить вредное действие STS. Ингибитор STS может действовать в качестве антагониста. Способность соединений ингибировать эстронсульфатазу может быть определена с использованием неповрежденных клеток трофобластической опухоли JEG3 или плацентарных микросом. Кроме того,может быть использована экспериментальная модель на животных. Подробная информация о подходящих методиках анализа представлена в нижеследующих разделах. Следует отметить, что другие анализы также могут быть использованы для определения активности STS и, таким образом, ингибирования STS. Например, можно также сослаться на положения, описанные в международной заявке на патент WO-A99/50453. В одном из вариантов осуществления для некоторых применений соединение дополнительно характеризуется тем свойством, что если бы сульфаматная группа была заменена сульфатной группой с образованием сульфатного производного, то такое сульфатное производное могло бы быть гидролизуемо ферментом, обладающим активностью стероидной сульфатазы (Е.С. 3.1.6.2), т.е. при инкубировании со стероидной сульфатазой ЕС 3.1.6.2 при pH 7,4 и температуре 37 С. В одном из предпочтительных вариантов осуществления, если бы сульфаматная группа была заменена сульфатной группой с образованием сульфатного соединения, то такое сульфатное соединение могло бы быть гидролизуемо ферментом, обладающим активностью стероидной сульфатазы (Е.С. 3.1.6.2), и характеризовалось бы величиной Km менее 200 мМ, предпочтительно менее 150 мМ, предпочтительно- 25011123 менее 100 мМ, предпочтительно менее 75 мМ, предпочтительно менее 50 мМ при инкубировании со стероидной сульфатазой ЕС 3.1.6.2 при pH 7.4 и температуре 37 С. В предпочтительном варианте осуществления соединение не гидролизуемо ферментом, обладающим активностью стероидной сульфатазы (Е.С. 3.1.6.2). Для некоторых применений соединение предпочтительно обладает по крайней мере приблизительно 100-кратной селективностью в отношении целевой мишени (т.е. STS и/или ароматазы), предпочтительно по крайней мере приблизительно 150-кратной селективностью в отношении целевой мишени,предпочтительно по крайней мере приблизительно 200-кратной селективностью в отношении целевой мишени, предпочтительно по крайней мере приблизительно 250-кратной селективностью в отношении целевой мишени, предпочтительно по крайней мере приблизительно 300-кратной селективностью в отношении целевой мишени, предпочтительно по крайней мере приблизительно 350-кратной селективностью в отношении целевой мишени. Следует отметить, что соединение может иметь и другие полезные свойства помимо или вместо способности ингибировать активность STS и/или ароматазы. Анализ для определения активности STS с использованием раковых клеток (методика 1) Ингибирование активности стероидной сульфатазы в клетках JEG3. Активность стероидной сульфатазы измеряют in vitro с использованием неповрежденных клеток трофобластической опухоли JEG3. Эта линия клеток может быть использована для изучения контроля роста клеток рака молочной железы человека. Она характеризуется значительной активностью стероидной сульфатазы (Boivin и др., J. Med. Chem., 2000, 43: 4465 - 4478) и может быть получена из Американской Коллекции Типовых Культур (АТСС). Клетки содержат в минимальной эссенциальной среде (Minimal Essential Medium, MEM) (Flow(HEPES), 5% эмбриональной бычьей сыворотки, 2 мМ глутамина, не относящиеся к незаменимым аминокислоты и 0,075% гидрокарбоната натрия. Производится параллельный посев в 25 см 2 колбы для тканевых культур в количестве до 30 при плотности посева около 1105 клеток на колбу и с использованием вышеописанной среды. Клетки выращивают до 80% слияния, а среду переменяют каждые третьи сутки. Неповрежденные монослои клеток JEG3 во взятых по три 25 см 2 колбах для тканевых культур промывают сбалансированным солевым раствором Эрла (Earle's Balanced Salt Solution, EBSS, производства компании ICN Flow, High Wycombe, Великобритания) и инкубируют в течение 3-4 ч при температуре 37 С с 5 пмоль (7105 распадов в минуту) [6,7-3 Н]эстрон-3-сульфата (специфическая активность 60 кюри/моль, производства компании New England Nuclear, Бостон, Массачусетс, США) в бессывороточнойMEM (2,5 мл) вместе с эстрон-3-сульфаматом (5 концентраций: 1, 10, 100, 1000 нМ и 10 мкМ). После инкубирования каждую колбу охлаждают и переводят среду (1 мл) с помощью пипеток в отдельные пробирки, содержащие [14 С]эстрон (7103 распадов в минуту) (специфическая активность 97 кюри/моль,производства компании Amersham International Radiochemical Centre, Amersham, Великобритания). Смесь тщательно встряхивают в течение 30 с с толуолом (5 мл). Эксперименты показывают, что более 90%[14 С]эстрона и менее 0,1% [3 Н]эстрон-3-сульфата удаляется из водной фазы при такой обработке. Часть органической фазы (2 мл) удаляют, выпаривают и определяют содержание 3 Н и 14 С в остатке с помощью сцинтилляционной спектрометрии. Массу гидролизованного эстрон-3-сульфата рассчитывают, исходя из полученного числа отсчетов для 3 Н (поправленного на использование объемы среды и органической фазы и обратное выделение добавленного [14 С]эстрона) и специфической активности субстрата. Каждая серия экспериментов включает инкубирование микросом, полученных из сульфатаза-положительной человеческой плаценты (позитивный контроль) и колбы без клеток (для определения степени видимого неферментативного гидролиза субстрата). Число клеточных ядер на колбу определяют с помощью счетчика Coulter после обработки монослоев клеток запонином. Одну колбу из каждой серии используют для определения состояния и жизнеспособности клеточной мембраны с использованием метода вытеснения трипанового синего (Phillips, H.J. (1973) в: Tissue culture and applications, [под ред. Kruse, D.F. и Patterson,M.K.]; стр. 406-408; Academic Press, New York). Результаты для активности стероидной сульфатазы выражают в виде средней величиныстандартное отклонение общего количества продукта (эстрон + эстрадиол), образованного в течение периода инкубации (3-4 ч), в пересчете на 10 клеток и для величин, демонстрирующих статистическую значимость,в виде процентного снижения (ингибирования) в сравнении с опытами, проведенными в отсутствие эстрон-3-сульфамата. Для оценки статистической значимости результатов используют непарный tкритерий Стьюдента. Анализ для определения активности STS с использованием плацентарных микросом (методика 2) Ингибирование активности стероидной сульфатазы в плацентарных микросомах. Сульфатаза-положительную человеческую плаценту, полученную от беременностей нормального срока, тщательно измельчают ножницами и однократно промывают холодным фосфатным буферным раствором (pH 7,4, 50 мМ), после чего заново суспендируют в холодном фосфатном буферном растворе(5 мл на грамм ткани). Гомогенизацию доводят до конца с помощью гомогенизатора Ultra-Turrax тремя- 26011123 10-секундными импульсами, разделенными 2-минутными периодами охлаждения во льду. Ядра и остатки клеток удаляют посредством центрифугирования (4 С) при ускорении 2000g в течение 30 мин и сохраняют надосадочную жидкость в виде порций (2 мл) при температуре 20 С. Концентрацию белка в надосадочной жидкости определяют по методу Брэдфорда (Anal. Biochem., 72, 248-254 (1976. Инкубирование (1 мл) осуществляют с использованием концентрации белка 100 мг/мл, концентрации субстрата 20 мМ [6,7-3 Н]эстрон-3-сульфата (специфическая активность 60 кюри/моль, производства компании New England Nuclear, Бостон, Массачусетс, США) при времени инкубирования 20 мин при температуре 37 С. При необходимости используют шесть концентраций соединений: 0,1, 1,0, 10, 100,1000 нМ и 10 мкМ. После инкубирования каждый образец охлаждают и переносят среду (1 мл) с помощью пипеток в отдельные пробирки, содержащие [14 С]эстрон (7103 распадов в минуту) (специфическая активность 97 кюри/моль, производства компании Amersham International Radiochemical Centre, Amersham, Великобритания). Смесь тщательно встряхивают в течение 30 с с толуолом (5 мл). Эксперименты показывают, что более 90% [14 С]эстрона и менее 0,1% [3 Н]эстрон-3-сульфата удаляется из водной фазы при такой обработке. Часть органической фазы (2 мл) удаляют, выпаривают и определяют содержание 3 Н и 14 С в остатке с помощью сцинтилляционной спектрометрии. Массу гидролизованного эстрон-3 сульфата рассчитывают, исходя из полученного числа отсчетов для 3 Н (поправленного на использование объемы среды и органической фазы и обратное выделение добавленного [14 С]эстрона) и специфической активности субстрата. Анализ для определения активности STS с использованием экспериментальной модели на животных (методика 3) Ингибирование активности эстронсульфатазы in vivo. Соединения по настоящему изобретению могут быть исследованы с использованием экспериментальной модели на животных, в частности на крысах с удаленными яичниками. В этой модели соединения, являющиеся эстрогенными, стимулируют маточный рост. Соединение (0,1 мг на килограмм веса в день в течение 5 дней) вводят крысам перорально, тогда как другая группа животных получает только носитель (пропиленгликоль). По завершении исследования получают образцы ткани печени и анализируют активность эстронсульфатазы с использованием[3 Н]эстрон-сульфата в качестве субстрата, как это описано ранее (см. PCT/GB 95/02638). Анализ с использованием экспериментальной модели на животных для определения эстрогенной активности (методика 4) Соединения по настоящему изобретению могут быть исследованы с использованием экспериментальной модели на животных, в частности на крысах с удаленными яичниками. В этой модели соединения, являющиеся эстрогенными, стимулируют маточный рост. Соединение (0,1 мг на килограмм веса в день в течение 5 дней) вводят крысам перорально, тогда как другая группа животных получает только носитель (пропиленгликоль). По завершении исследования удаляют матку и взвешивают ее, выражая результаты в виде отношения массы матки к общей массе тела,умноженного на 100. Соединения, не оказывающие существенного влияния на рост матки, не являются эстрогенными. Биотехнологические анализы для определения активности STS (методика 5) Способность соединений ингибировать активность эстронсульфатазы также может быть оценена с помощью последовательностей аминокислот или последовательностей нуклеотидов, кодирующих STS,или их активные фрагменты, производные, гомологи или варианты, например, с помощью высокопроизводительного скрининга. Для идентификации агента, способного модулировать STS, с помощью любой из множества методик лекарственного скрининга может быть использована какая-либо одна или более из подходящих мишеней, таких как последовательность аминокислот и/или последовательность нуклеотидов. Мишень, используемая в таком испытании, может находиться в свободной форме в растворе, быть прикрепленной к твердому носителю, находиться на поверхности клетки или располагаться в межклеточном пространстве. При этом может быть измерено снижение активности мишени или образование связанных комплексов между мишенью и исследуемым агентом. Анализ по настоящему изобретению может являться скринингом, с помощью которого испытывают несколько агентов. В одном из вариантов осуществления настоящего изобретения способ анализа по настоящему изобретению является высокопроизводительным скринингом. Методики лекарственного скрининга могут быть основаны на способе, описанном Geysen в европейская заявке на патент 84/03564, опубликованной 13 сентября 1984 г. Излагая кратко, большое количество различных небольших пептидных соединений, подвергаемых испытанию, синтезируют на твердом субстрате, таком как пластиковые стержни или какая-либо другая поверхность. Подвергаемые испытанию пептидные соединения вводят в реакцию с подходящей мишенью или ее фрагментом и промывают. После этого детектируют связанные вещества, например, с помощью подходящим образом приспособленных способов, известных в данной области. Очищенную мишень можно также нанести непосредственно на планшеты, применяемые в методиках лекарственного скрининга. Альтернативно, для захвата пептида и его иммобилизации на твердом носители можно использовать ненейтрализующие антитела.- 27011123 Настоящее изобретение также распространяется на применение анализов с конкурентным скринингом препаратов, в рамках которых способные к специфическому связыванию с мишенью нейтрализующие антитела конкурируют с исследуемым соединением за связывание с мишенью. Другая основанная на скрининге методика предусматривает высокопроизводительный скрининг(HTS) агентов, обладающих подходящим сродством к связыванию с соединениями, и основана на способе, подробно описанном в международной заявке на патент WO 84/03564. Ожидается, что способы анализа по настоящему изобретению окажутся пригодными как для мелкомасштабного, так и для крупномасштабного скрининга исследуемых соединений, равно как и в количественных анализах. В одном из предпочтительных вариантов осуществления настоящего изобретения объектом настоящего изобретения является способ идентификации агентов, селективно модулирующих STS, каковые агенты отвечают формуле (I). Репортерные соединения В способах анализа (равно как и скрининге) по настоящему изобретению может быть использовано большое разнообразие репортерных соединений, причем предпочтительными репортерными соединениями будут такие, сигналы от которых удобно детектировать (например, с помощью спектроскопии). В качестве примера репортерный ген может кодировать белок, катализирующий реакцию, под влиянием которой изменяются светопоглощающие свойства. Другие методики включают твердофазный иммуноферментный анализ (ELISA), радиоиммунологический анализ (RIA) и активируемый флуоресценцией клеточный сортинг (FACS). Может даже быть применен двухстадийный, основанный на моноклональных антителах иммуноферментный анализ, использующий моноклональные антитела, реакционноспособные по отношению к двум невзаимодействующим антигенным детерминантам. Эти и другие анализы описаны, помимо прочих источников, в Hampton R и др. (1990, Serological Methods, A Laboratory Manual,APS Press, St Paul MN) и Maddox DE и др. (1983, J Exp Med 15 8:121 1). Примеры репортерных молекул включают -галактозидазу, инвертазу, белок с зеленой флуоресценцией, люциферазу, левомицетин, ацетилтрансферазу, -глюкуронидазу, экзоглюканазу и глюкоамилазу, но не ограничиваются перечисленными. Альтернативно, можно ввести радиоактивно меченные или содержащие флуоресцентную метку нуклеотиды в возникающие транскрипты, которые впоследствии идентифицируют, когда они связаны с олигонуклеотидными зондами. В качестве дальнейших примеров ряд компаний, таких как Pharmacia Biotech (Piscataway, NJ),Promega (Madison, WI) и US Biochemical Corp (Cleveland, ОН) поставляют коммерчески доступные наборы и методики для различных способов анализа. Подходящие репортерные молекулы или метки включают радионуклиды, ферменты, флуоресцентные, хемилюминесцентные или вызывающие окраску агенты, равно как и субстраты, кофакторы, ингибиторы, магнитные частицы и прочие подобные вещества. Патенты, содержащие положения, относящиеся к применению подобных меток, включают патенты US3817837; 3850752; 3939350; 3996345; 4277437; 4275149 и 4366241. Клетки-хозяева Термин клетка-хозяин, как он относится к настоящему изобретению, включает всякую клетку,которая может содержать мишень для агента по настоящему изобретению. Таким образом, объектами дальнейших вариантов осуществления настоящего изобретения являются клетки-хозяева, подвергнутые преобразованию или трансфекции полинуклеотидом, являющимся мишенью но настоящему изобретению или экспрессирующим ее. Предпочтительно такой нуклеотид переносится в векторе для репликации и экспрессии полинуклеотидов, которые должны быть мишенью или должны экспрессировать мишень. Выбирают такие клетки, которые совместимы с данным вектором и могут, например, быть прокариотическими (например, бактериальными), грибковыми, дрожжевыми или клетками растений. В качестве клетки-хозяина для гетерологичной экспрессии генов широко используют грамотрицательную бактерию E.coli. Однако большие количества гетерологичного белка имеют тенденцию накапливаться внутри клетки. Последующая очистка целевого белка от массы межклеточных белков E.coli иногда бывает непростой. В противоположность E.coli, бактерии, относящиеся к роду бациллы (Bacillus), оказываются весьма пригодны в качестве гетерологичных организмов-хозяев вследствие их способности выделять белок в культуральную среду. Другие бактерии, пригодные в качестве организмов-хозяев, относятся к родам стрептомицеты (Streptomyces) и псевдомонады (Pseudomonas). В зависимости от природы полинуклеотида, кодирующего полипептид по настоящему изобретению, и/или желательности дальнейшего процессинга экспрессируемого белка, могут оказаться предпочтительны эукариотические клетки-хозяева, такие как дрожжи или иные грибы. В целом, дрожжевые клетки являются предпочтительными по сравнению с клетками грибов, поскольку с ними проще осуществлять различные манипуляции. Однако некоторые белки либо плохо выделяются дрожжевыми клетками, либо, в некоторых случаях, не вырабатываются правильным образом (например, гипергликозилирование в дрожжах). В таких случаях необходимо выбрать другой грибковый организм-хозяин.- 28011123 Примерами подходящих организмов-хозяев для экспрессии, находящихся в сфере настоящего изобретения, являются грибы, такие как грибы вида аспергиллы (Aspergillus) (такие как описанные в европейских патентах 0184438 и 0284603) и вида триходермы (Trichoderma); бактерии, такие как бактерии вида бациллы (Bacillus) (такие как описанные в европейских патентах 0134048 и 0253455), вида стрептомицеты (Streptomyces) и вида псевдомонады (Pseudomonas); а также дрожжи, такие как дрожжи вида Kluyveromyces (такие как описанные в европейских патентах 0096430 и 0301670) и вида Saccharomyces. В качестве примера типичные организмы-хозяева для экспрессии могут быть выбраны средиAspergillus niger, Aspergillus niger var. tubigenis, Aspergillus niger var. awamori, Aspergillus aculeatis, Aspergillus nidulans, Aspergillus orvzae, Trichoderma reesei, Bacillus subtilis, Bacillus licheniformis, Bacillus amyloliquefaciens, Kluyveromyces lactis и Saccharomyces cerevisiae. Использование подходящих клеток-хозяев, таких как клетки-хозяева дрожжей, грибов и растений может предусматривать посттрансляционные модификации (например, миристоилирование, гликозилирование, усечение, лапидацию и фосфорилирование тирозина, серина или треонина), как то может требоваться для придания оптимальной биологической активности рекомбинантным экспрессионным продуктам по настоящему изобретению. Организм. Термин организм, как он относится к настоящему изобретению, включает любой организм, который может содержать мишень согласно настоящему изобретению и/или получаемые из нее продукты. Примеры организмов могут включать грибок, дрожжи или растение. Термин трансгенный организм, как он относится к настоящему изобретению, включает любой организм, который содержит мишень согласно настоящему изобретению и/или получаемые продукты. Преобразование клеток-хозяев/организмов-хозяев. Как указывалось ранее, организм-хозяин может быть прокариотическим или эукариотическим организмом. Примеры подходящих прокариотов-хозяев включают E.coli и Bacillus subtilis. Идеи, относящиеся к преобразованию прокариотов-хозяев подробно описаны специалистами в данной области, см.,например, Sambrook и др. (Molecular Cloning: A Laboratory Manual, 2-е издание, 1989, Cold Spring HarborLaboratory Press) и Ausubel и др., Current Protocols in Molecular Biology (1995), John WileySons, Inc. Если используется прокариот-хозяин, то может потребоваться подходящим образом модифицировать последовательность нуклеотидов перед преобразованием, например, путем удаления интронов. В другом варианте осуществления настоящего изобретения трансгенным организмом могут быть дрожжи. В этом отношении следует отметить, что дрожи широко используются в качестве носителя для экспрессии гетерологичных генов. Дрожжи вида Saccharomyces cerevisiae имеют долгую историю промышленного применения, включая применение для экспрессии гетерологичных генов. Обзоры, посвященные экспрессии гетерологичных генов в Saccharomyces cerevisiae можно найти в Goodey и др. (1987,Yeast Biotechnology, под ред. D.R. Berry и др., стр. 401-429, Allen and Unwin, London) и в King и др. (1989,Molecular and Cell Biology of Yeasts, под ред. Е.F. Walton и G.T. Yarronton, стр. 107-133, Blackie, Glasgow). По ряду причин Saccharomyces cerevisiae хорошо подходит для экспрессии гетерологичных генов. Во-первых, они не патогенны для человека и неспособны вырабатывать определенные эндотоксины. Вовторых, они имеют долгую историю безопасного применения вслед за веками коммерческой эксплуатации в различных целях. Это обусловило их широкое применение населением. В-третьих, интенсивное коммерческое применение и обширные исследования, посвященные организму, обеспечили богатый объем знаний о генетике и физиологии, равно как и о характеристиках крупномасштабного брожения Saccharomyces cerevisiae. Обзор основ экспрессии гетерологичных генов в Saccharomyces cerevisiae и секреции генных продуктов дан в Е. Hinchcliffe, E. Kenny (1993, "Yeast as a vehicle for the expression of heterologous genes",Yeasts, т. 5, под ред. Anthony H. Rose и J. Stuart Harrison, 2-е издание, Academic Press Ltd.). Доступен ряд типов векторов дрожжей, включая интегративные векторы, требующие для своего сохранения рекомбинации с геномом организма-хозяина, и автономно реплицирующиеся векторы плазмид. Для получения трансгенных Saccharomyces, экспрессионные конструкции приготовляют путем встраивания последовательности нуклеотидов в конструкцию, созданную для экспрессии в дрожжах. Разработаны несколько типов конструкций, используемых для гетерологической экспрессии. Конструкции содержат сшитый с последовательностью нуклеотидов промотор, активный в дрожжах; обычно используют промотор дрожжевого происхождения, такой как промотор галактокиназы(GAL1). Как правило, используют сигнальную последовательность дрожжевого происхождения, такую как последовательность, кодирующую репортерный белок SUC2. Экспрессионная система оканчивается активным в дрожжах терминатором. Для преобразования дрожжей разработан ряд методик преобразования. Например, трансгенные Saccharomyces по настоящему изобретению могут быть получены, следуя идеям, описанным в Hinnen и др.(1978, Proceedings of the National Academy of Sciences of the USA 75, 1929); Beggs, J.D. (1978, Nature, London, 275, 104); и Ito, H. и др. (1983, J Bacteriology 153, 163-168). Преобразованные дрожжевые клетки отбирают с помощью различных селективных генов- 29011123 маркров. Среди используемых для трансформации маркеров присутствует ряд ауксотрофных геновмаркров, таких как LEU2, HIS4 и TRP1, и доминантные гены-маркры, обеспечивающие устойчивость к антибиотикам, такие как гены-маркры аминогликозидных антибиотиков, например, G418. Другим организмом-хозяином является растение. Основной принцип конструирования генетически модифицированных растений состоит во вставке генетической информации в геном растения таким образом, чтобы обеспечить стабильное существование вставленного генетического материала. Существует ряд методик для вставки генетической информации, причем двумя основными подходами являются прямое введение генетической информации и введение генетической информации посредством использования векторной системы. Обзор общих методик можно найти в статьях Potrykus (Annu Rev Plant PhysiolPlant Mol Biol [1991] 42:205-225) и Christou (Agro-Food-Industry Hi-Tech March/April 1994 17-27). Дальнейшие положения, относящиеся к преобразованию растений, можно найти в европейском патенте 0449375. Таким образом, объектом настоящего изобретения также является способ преобразования клеткихозяина с помощью последовательности нуклеотидов, которая будет являться мишенью или экспрессировать мишень. Клетки-хозяева, преобразованные с помощью нуклеотидной последовательности, могут выращиваться в условиях, пригодных для экспрессии кодированного белка. Белок, вырабатываемый рекомбинантной клеткой, может проявляться на поверхности клетки. При соответствующем желании, как известно специалистам в данной области, экспрессирующие векторы, содержащие кодирующие последовательности, синтезированы с сигнальными последовательностями, направляющими выделение кодирующих последовательностей через определенную мембрану прокариотичекой или эукариотической клетки. Другие рекомбинантные конструкции могут объединять кодирующую последовательность с последовательностью нуклеотидов, кодирующей полипептидный домен, который обеспечит очистку растворимых белков (Kroll D.J. и др. (1993) DNA Cell Biol 12:441-53). Варианты/гомологи/производные В дополнение к упомянутым в контексте специфическим последовательностям аминокислот и нуклеотидов настоящее изобретение также включает использование их вариантов, гомологов и производных. Здесь термин гомология может быть приравнен к идентичности. В настоящем контексте подразумевается, что гомологическая последовательность включает такую аминокислотную последовательность, которая может быть по крайней мере на 75, 85 или 90% идентичной, предпочтительно по крайней мере на 95 или 98% идентичной. Хотя гомология может также рассматриваться в терминах сходства (т.е. аминокислотные остатки, обладающие сходными химическими свойствами/функциями), в контексте настоящего изобретения гомология предпочтительно выражается в терминах идентичности последовательностей. Сравнения гомологии могут быть осуществлены невооруженным глазом или, как делают чаще, с помощью легкодоступных программ для сравнения последовательностей. Эти коммерчески доступные компьютерные программы могут рассчитать процент гомологии между двумя или более последовательностями. Процент гомологии может быть рассчитан для соседствующих последовательностей, т.е. совместно выстраивают в линию одну и другую последовательности и непосредственно сравнивают каждую аминокислоту из одной последовательности с соответствующей аминокислотой из другой последовательности, один остаток за один раз. Эту процедуру называют безразрывным выстраивание. Как правило,подобные безразрывные выстраивания осуществляют только для сравнительно малого числа остатков. Хотя этот метод весьма прост и последователен, он не может принять во внимание, например, то, что одна вставка или один пропуск в идентичной во всем остальном паре последовательностей приведет к тому, что последующие аминокислотные остатки будут выведены из выстроенного состояния, что может потенциально привести к большому снижению процента гомологии в случае осуществления глобального выстраивания. Как следствие, большинство методов сравнения последовательностей устроены таким образом, чтобы обеспечить оптимальные выстраивания, учитывающие возможные вставки и пропуски без чрезмерного ухудшения общей степени гомологии. Это достигается путем включения разрывов в выстраивание последовательности в попытке максимизировать локальную гомологию. Однако эти более сложные методы приписывают штраф за разрыв каждому встречающемуся в выстраивании разрыву таким образом, что для одинакового количества идентичных аминокислот выстраивание последовательности с минимально возможным числом разрывов, что отражает большую степень взаимосвязи между двумя сравниваемыми последовательностями, будет характеризоваться более высокой степенью гомологии, чем последовательность со многими разрывами. Как правило, используется система аффинных штрафов за разрыв, которая назначает сравнительно высокий штраф за существование разрыва и меньший штраф за каждый последующий остаток в разрыве. Это наиболее общепринятая система оценки. Высокие штрафы за разрыв будут, конечно, приводить к оптимизированным выстраиваниям с меньшим числом разрывов. Большинство программ для выстраивания позволяет варьировать штраф за разрыв. Однако при использовании таких программ для сравнения последовательностей предпочитают использовать значения по умолчанию. Например, при использовании программного пакета GCG Wisconsin Bestflt (см. ниже) штраф за разрыв для последовательностей аминокислот по умолча- 30
МПК / Метки
МПК: C07J 43/00, A61K 31/56, A61P 35/00, C07J 41/00
Метки: качестве, стероидной, производные, эстрогена, сульфатазы, ингибиторов
Код ссылки
<a href="https://eas.patents.su/30-11123-proizvodnye-estrogena-v-kachestve-ingibitorov-steroidnojj-sulfatazy.html" rel="bookmark" title="База патентов Евразийского Союза">Производные эстрогена в качестве ингибиторов стероидной сульфатазы</a>












