5-фенилпиримидины, способ их получения, содержащие их средства и их применение
Номер патента: 10628
Опубликовано: 30.10.2008
Авторы: Райнхаймер Йоахим, Штирль Райнхард, Грамменос Вассилиос, Шэфер Петер, Аммерманн Эберхард, Гипзер Андреас, Шивек Франк, Розе Инго, Лоренц Гизела, Швёглер Аня, Тормо И Бласко Хорди, Штратманн Зигфрид, Гевер Маркус, Мюллер Бернд, Гроте Томас
Формула / Реферат
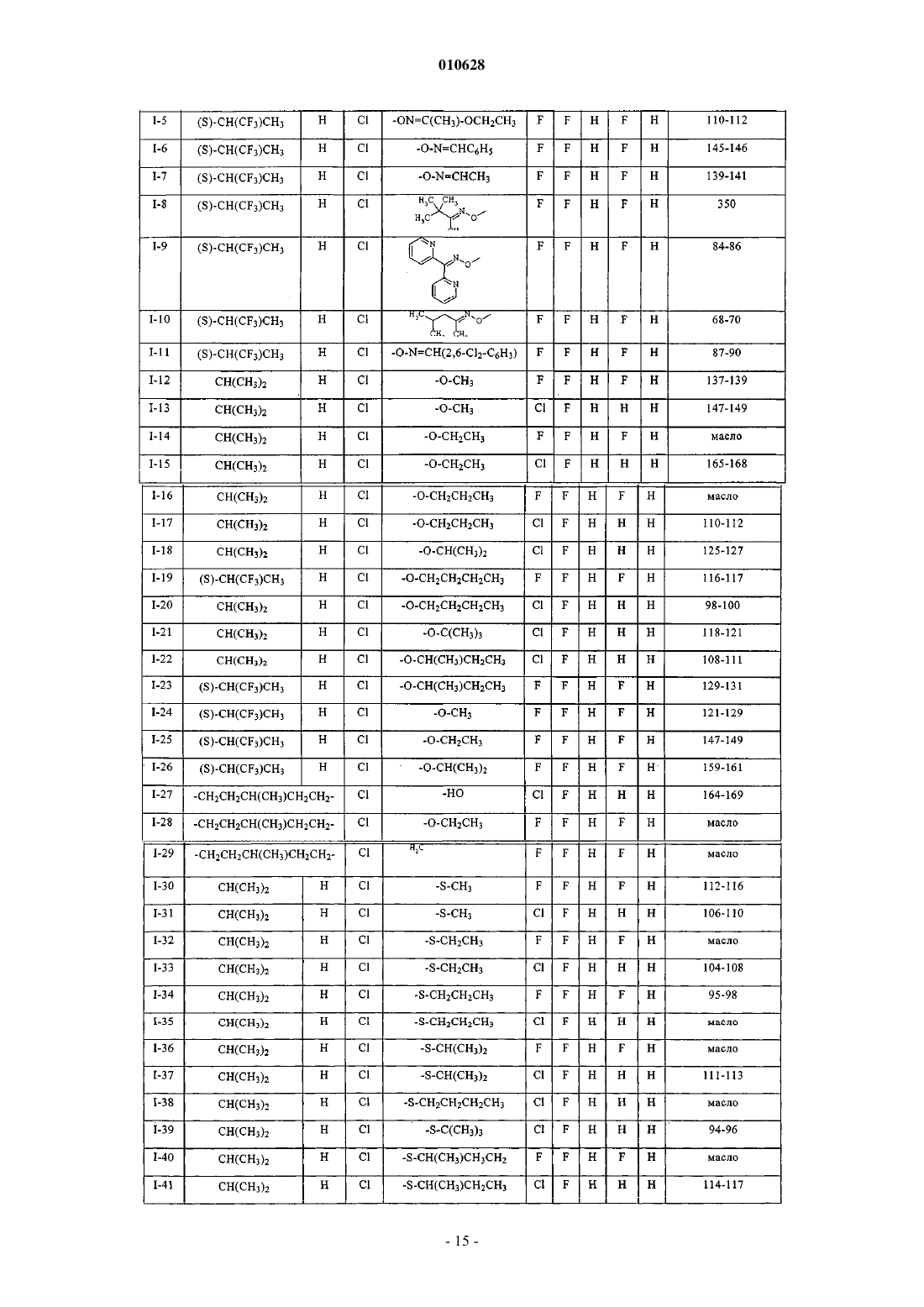
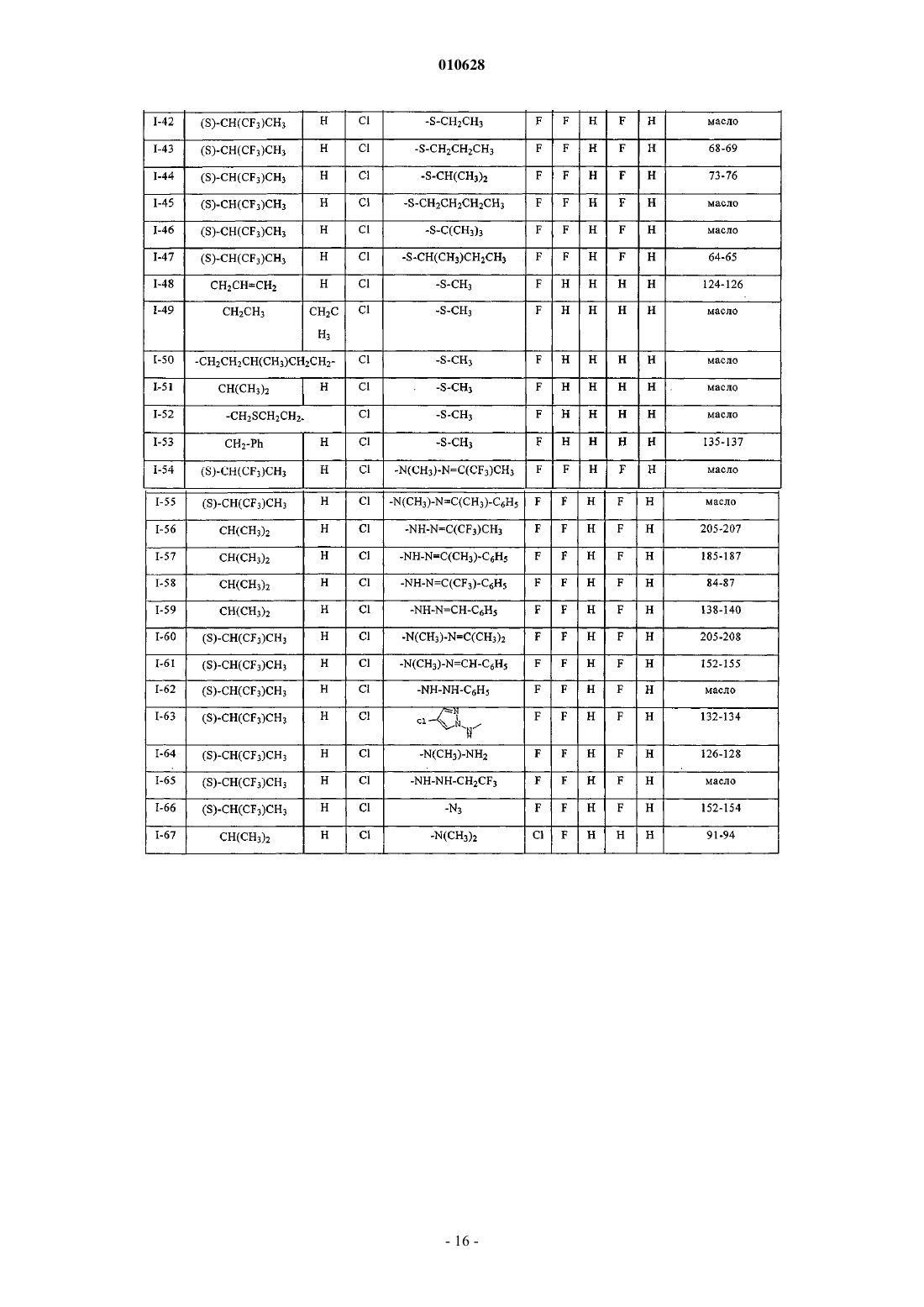
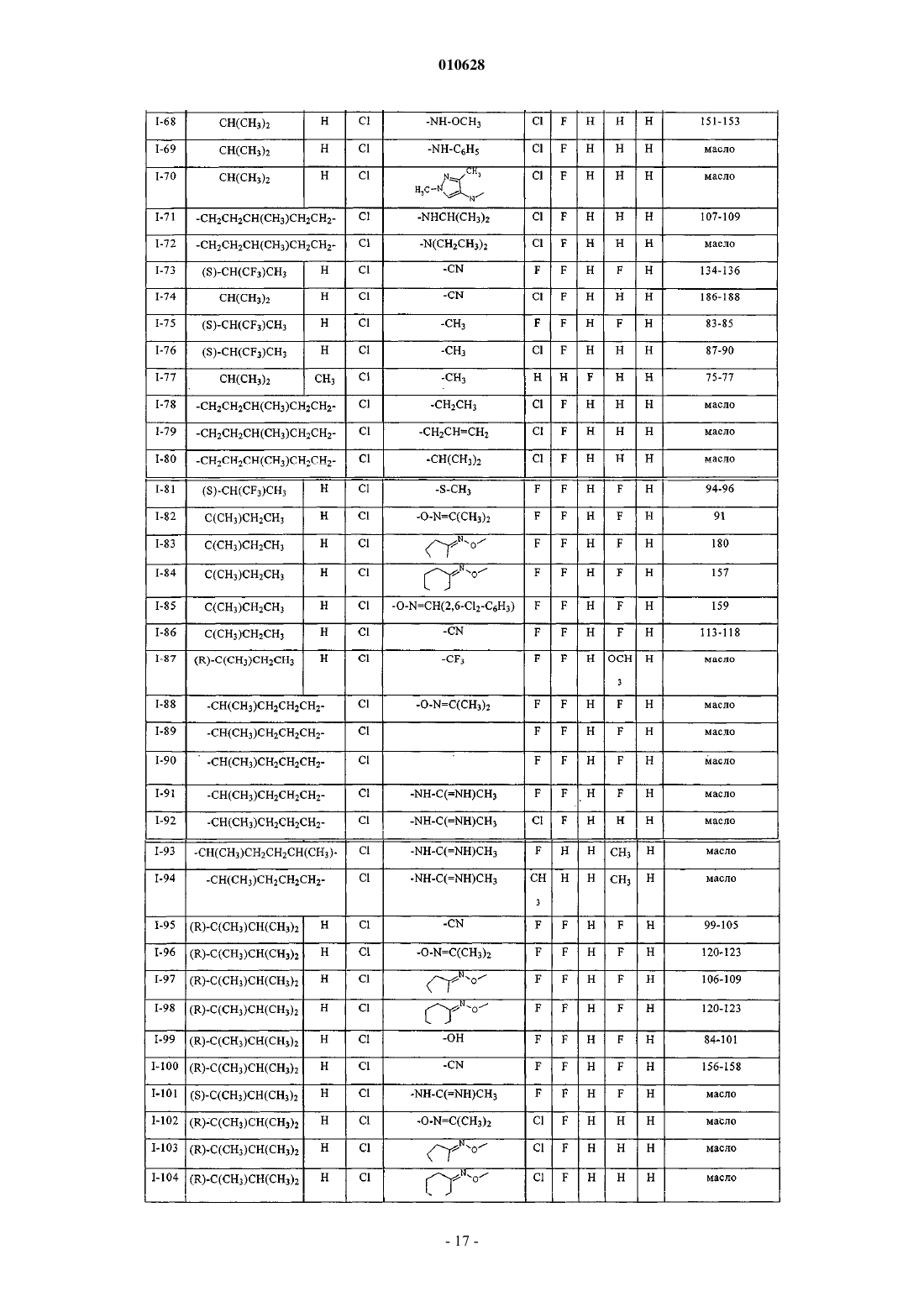
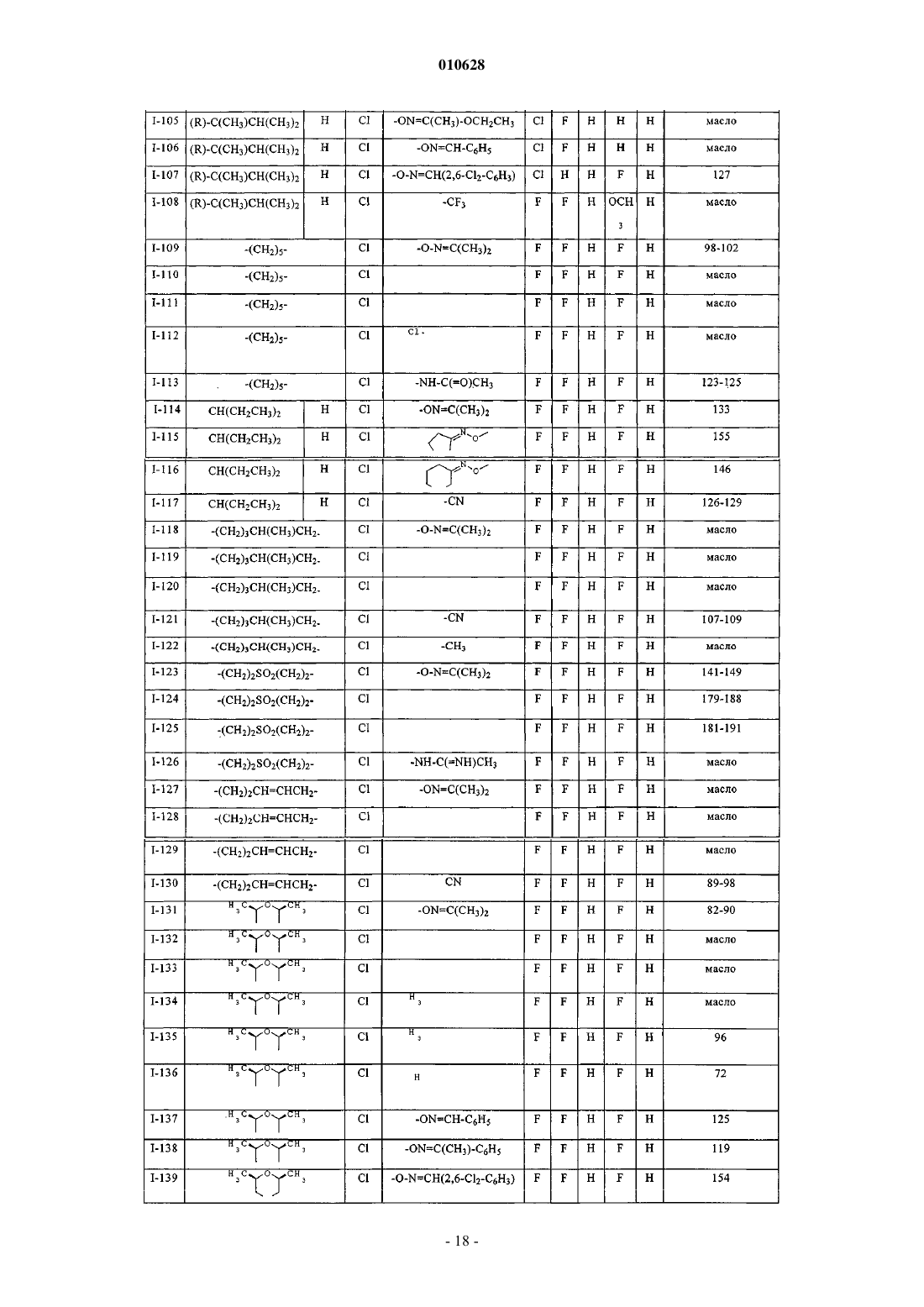
1. 5-Фенилпиримидины формулы I
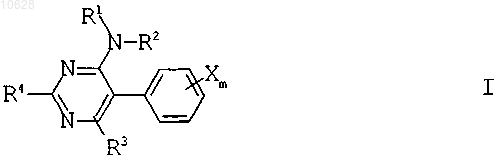
в которой заместители и индекс имеют следующие значения:
R1 - C1-C6алкил, C1-C6галогеналкил, C3-C6циклоалкил, C3-C6галогенциклоалкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил;
R2 - водород или группы, значения которых определены для R1;
R1 и R2 могут образовывать также с атомом азота, с которым они связаны, насыщенный или ненасыщенный 5- или 6-членный цикл, который может быть прерван группой эфиро- (-O-), тио- (-S-), сульфоксил- (-S[=O]-) или сульфонил- (-SO2-) и/или может быть замещен посредством 1-4 групп Ra и/или Rb;
Ra, Rb означают независимо друг от друга водород, C1-C6алкил, С2-С8алкенил, С2-С8алкинил, C1-C6галогеналкил, C1-C6алкокси, С1-С6галогеналкокси, С3-С10циклоалкил, фенил или 5-10-членный насыщенный, частично ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов из группы, включающей О, N или S, причем циклические остатки могут быть частично или полностью замещены следующими группами Rx:
Rx независимо друг от друга означают циано, нитро, амино, аминокарбонил, аминотиокарбонил, галоген, гидрокси, C1-C6алкил, C1-C6галогеналкил, C1-C6алкилкарбонил, C1-C6алкилсульфонил, C1-C6алкилсульфоксил, C3-C6циклоалкил, C1-C6алкокси, C1-C6галогеналкокси, C1-C6алкилоксикарбонил, C1-C6алкилтио, C1-C6алкиламино, ди-C1-C6алкиламино, C1-C6алкиламинокарбонил, ди-C1-C6алкиламинокарбонил, C1-C6алкиламинотиокарбонил, ди-C1-C6алкиламинотиокарбонил, C2-C6алкенил, C2-C6алкенилокси, фенил, фенокси, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6-членный гетарилокси, C(=NORa)-ORb или OC(Ra)2-C(Rb)=NORb,
причем циклические группы, в свою очередь, незамещены или замещены от 1-3 остатков Ry:
Ry означает циано, нитро, галоген, гидрокси, амино, аминокарбонил, аминотиокарбонил, C1-C6алкил, C1-C6галогеналкил, C1-C6алкилсульфонил, C1-C6алкилсульфоксил, C3-C6циклоалкил, C1-C6алкокси, C1-C6галогеналкокси, C1-C6алкоксикарбонил, C1-C6алкилтио, C1-C6алкиламино, ди-С1-C6алкиламино, C1-C6алкиламинокарбонил, ди-С1-C6алкиламинокарбонил, C1-C6алкиламинотиокарбонил, ди-С1-C6алкиламинотиокарбонил, C2-C6алкенил, C2-C6алкенилокси, C3-C6циклоалкил, C3-C6циклоалкенил, фенил, фенокси, фенилтио, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6-членный гетарилокси или C(=NORa)-ORb;
Ra, Rb означают водород или C1-C6алкил;
Ra и Rb могут также совместно образовывать через алкиленовую или алкениленовую цепь со связывающим мостиком атомом насыщенный или ненасыщенный 5- или 6-членный цикл;
Rc означает одну из приведенных для Ra и Rb одновалентных групп;
R3 - водород, галоген, циано, C1-C6алкил, C1-C6галогеналкил, C1-C6алкокси, C1-C6галогеналкокси или C3-C8алкенилокси;
R4 - циано, гидрокси, меркапто, азидо, С2-С8алкенил, C2-C8алкинил, C1-C6галогеналкил, C1-C6алкокси, C3-C8алкенилокси, -ON=CRaRb, -CRc=NORa, -NRcN=CRaRb, -NRcNRaRb, -NHORa, -NRcC(=NRc')NRaRb, -NRcC(=O)NRaRb, -NRaC(=O)Rc, -NRaC(=NORc)Rc', -OC(=O)Rc, -C(=NORc)NRaRb, -CRc(=NNRaRb), -C(=O)NRaRb или -C(=O)Rc;
X - галоген, C1-C6алкил или C1-C6алкокси и
m равно целому числу от 1 до 5.
2. 5-Фенилпиримидины формулы I
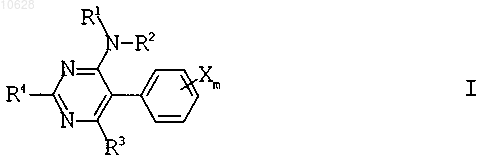
в которой заместители и индекс имеют следующие значения:
R1 - C1-C6алкил, C1-C6галогеналкил, С3-С6циклоалкил, С3-С6галогенциклоалкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил;
R2 - водород или группы, значения которых определены для R1;
R1 и R2 могут образовывать также вместе атомом азота, с которым они связаны, насыщенный или ненасыщенный 5- или 6-членный цикл, который может быть прерван атомом кислорода и может иметь C1-C6алкильный заместитель или в котором 2 смежных углеродных кольцевых члена могут быть связаны мостиком посредством C1-C4алкиленовой группы;
R3 - водород, галоген, циано, C1-C6алкил, C1-C6галогеналкил, C1-C6алкокси, C1-C6галогеналкокси или С3-С8алкенилокси;
R4 - циано, гидрокси, меркапто, азидо, C2-C8алкенил, C2-C8алкинил, C1-C6галогеналкил, C1-C6алкокси, C3-C8алкенилокси, -ON=CRaRb, -CRa=NORb, -NRaN=CRaRb, -NRaNRaRb или -NHORa;
Ra, Rb независимо друг от друга означают водород, C1-C6алкил, С2-С8алкенил, С2-С8алкинил, C1-C6галогеналкил, С1-С6алкокси, С1-С6галогеналкокси, С3-C10циклоалкил, фенил или 5-10-членный насыщенный, частично ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов из группы, включающей О, N или S, причем циклические остатки могут быть замещены частично или полностью следующими группами Rx:
Rx независимо друг от друга означают циано, нитро, амино, аминокарбонил, аминотиокарбонил, галоген, гидрокси, C1-C6алкшы, C1-C6галогеналкил, C1-C6алкилкарбонил, C1-C6алкилсульфонил, C1-C6алкилсульфоксил, C3-C6циклоалкил, C1-C6алкокси, C1-C6галогеналкокси, C1-C6алкилоксикарбонил, C1-C6алкилтио, C1-C6алкиламино, ди-C1-C6алкиламино, C1-C6алкиламинокарбонил, ди-C1-C6алкиламинокарбонил, C1-C6алкиламинотиокарбонил, ди-C1-C6алкиламинотиокарбонил, C2-C6алкенил, С2-C6алкенилокси, фенил, фенокси, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6-членный гетарилокси, C(=NORa)-ORb или OC(Ra)2-C(Rb)=NORb,
причем цикличные группы, в свою очередь, замещены или незамещены посредством 1-3 остатков Ry:
Ry означает циано, нитро, галоген, гидрокси, амино, аминокарбонил, аминотиокарбонил, C1-C6алкил, C1-C6галогеналкил, C1-C6алкилсульфонил, C1-C6алкилсульфоксил, C3-C6циклоалкил, C1-C6алкокси, C1-C6галогеналкокси, C1-C6алкоксикарбонил, C1-C6алкилтио, C1-C6алкиламино, ди-C1-C6алкиламино, C1-C6алкиламинокарбонил, ди-C1-C6алкиламинокарбонил, C1-C6алкиламинотиокарбонил, ди-C1-C6алкиламинотиокарбонил, C2-C6алкенил, С2-C6алкенилокси, C3-C6циклоалкил, C3-C6циклоалкенил, фенил, фенокси, фенилтио, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6-членный гетарилокси или C(=NORa)-ORb;
Ra, Rb означают водород или C1-C6алкил;
X - галоген, C1-C6алкил, C1-C6алкокси или C1-C6галогеналкил и
m равно целому числу от 1 до 5.
3. Соединения формулы I по п.1, в которой
R4 - циано, азидо, C2-C8алкенил, C2-C8алкинил, C1-C6галогеналкил, -CRc=NORc, -ON=CRaRb, или
-NRcN=CRaRb, или -C(=NORc)NRaRb.
4. Соединения формулы I по п.1, в которой R4 означает -ON=CRaRb.
5. Соединения формулы I по п.1, в которой R4 означает -CRc=NORa.
6. Способ получения соединений формулы I по п.1, в которой R4 означает циано или связанную через гетероатом группу, взаимодействием сульфонов формулы II
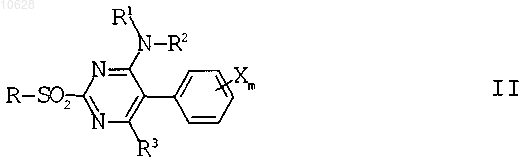
где R означает C1-C4алкил, с соединениями формулы III
![]()
где R4 имеет вышеприведенное значение, в щелочных условиях.
7. Способ получения соединений формулы I по п.1, где R3 означает галоген и R4 - алкенил, алкинил или галогеналкил, взаимодействием сложных фенилмалоновых эфиров формулы IV

с амидинами формулы V

где R4 имеет вышеприведенное значение, и галогенированием образовавшихся дигидроксипиримидинов формулы VI

агентом галогенирования с получением дигалогенпиримидинов формулы VII
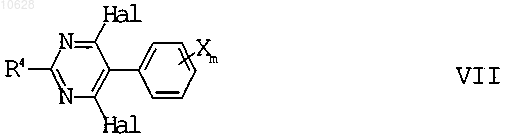
где Hal означает бром или хлор, который подвергают взаимодействию с аминами формулы VIII

где R1 и R2 имеют приведенное для формулы I значение, с получением соединений формулы I.
8. Способ получения соединений формулы I по п.1, где R3 означает циано, C1-C6алкокси, C1-C6галогеналкокси или C3-C8алкенилокси, взаимодействием пиримидинов формулы I, где R3 означает галоген, с соединениями формулы IX
![]()
где R3 имеет вышеприведенное значение, в щелочных условиях.
9. Способ получения соединений формулы I по п.1, где R3 означает C1-C6алкил, взаимодействием пиримидинов формулы I, где R3 означает галоген, с металлорганическими соединениями формулы X
![]()
где М означает группу Mg-Hal, Zn-R3 или B(OR)2, причем Hal означает атом галогена, и R означает водород или С1-С4алкил, и R3 означает C1-C6алкил.
10. Фунгицидное средство, содержащее твердый или жидкий носитель и соединение формулы I по пп.1-5.
11. Способ борьбы с фитопатогенными грибами, отличающийся тем, что грибы или подлежащие защите от них материалы, растения, почву или посевной материал обрабатывают эффективным количеством соединения формулы I по пп.1-5.
12. [6-Хлор-2-(диметиламино)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(1-метилэтил)амин;
[6-хлор-2-(фениламино)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(1-метилэтил)амин;
[6-хлор-2-(1-метилэтиламино)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-(диэтиламино)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-метил-5-(2,4,6-трифторфенил)пиримидин-4-ил]-((S)-1-(трифторметил)этиламин);
[6-хлор-2-метил-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-((S)-1-(трифторметил)этиламин);
[6-хлор-2-метил-5-(3-фторфенил)пиримидин-4-ил]-(N-(1-метилэтил)-N-метил)амин;
[6-хлор-2-этил-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-(1-метилэтил)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-метил-5-(2,4,6-трифторфенил)пиримидин-4-ил]-(3-метилпиперидин);
[6-хлор-2-метил-5-(2,4,6-трифторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-этил-5-(2,4,6-трифторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-диэтиламино-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-этил-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-(1-метилэтил)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(4-метилпиперидин);
[6-хлор-2-(диметиламино)-5-(2,4,6-трифторфенил)пиримидин-4-ил]-(1-(трифторметил)этил)амин.
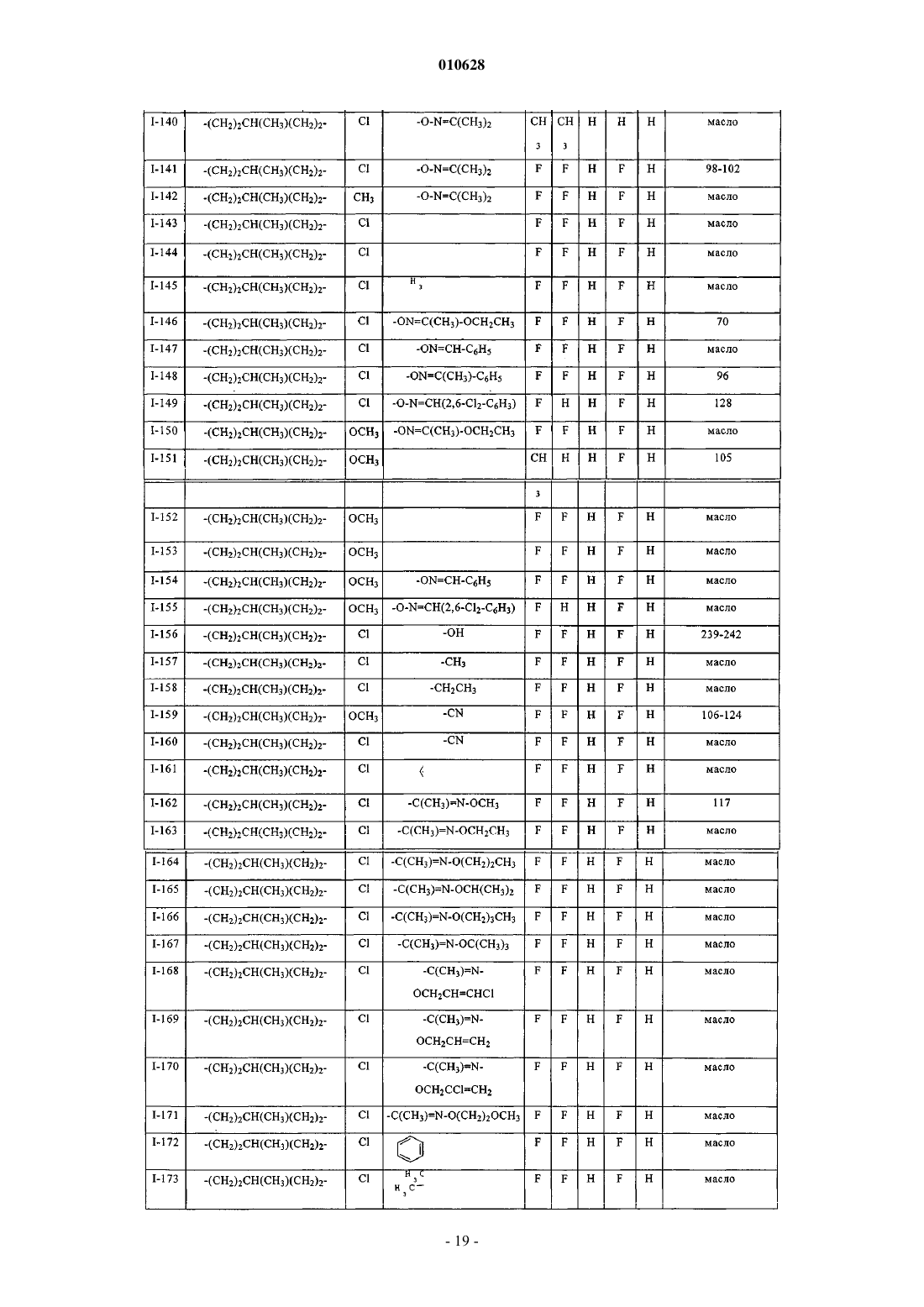
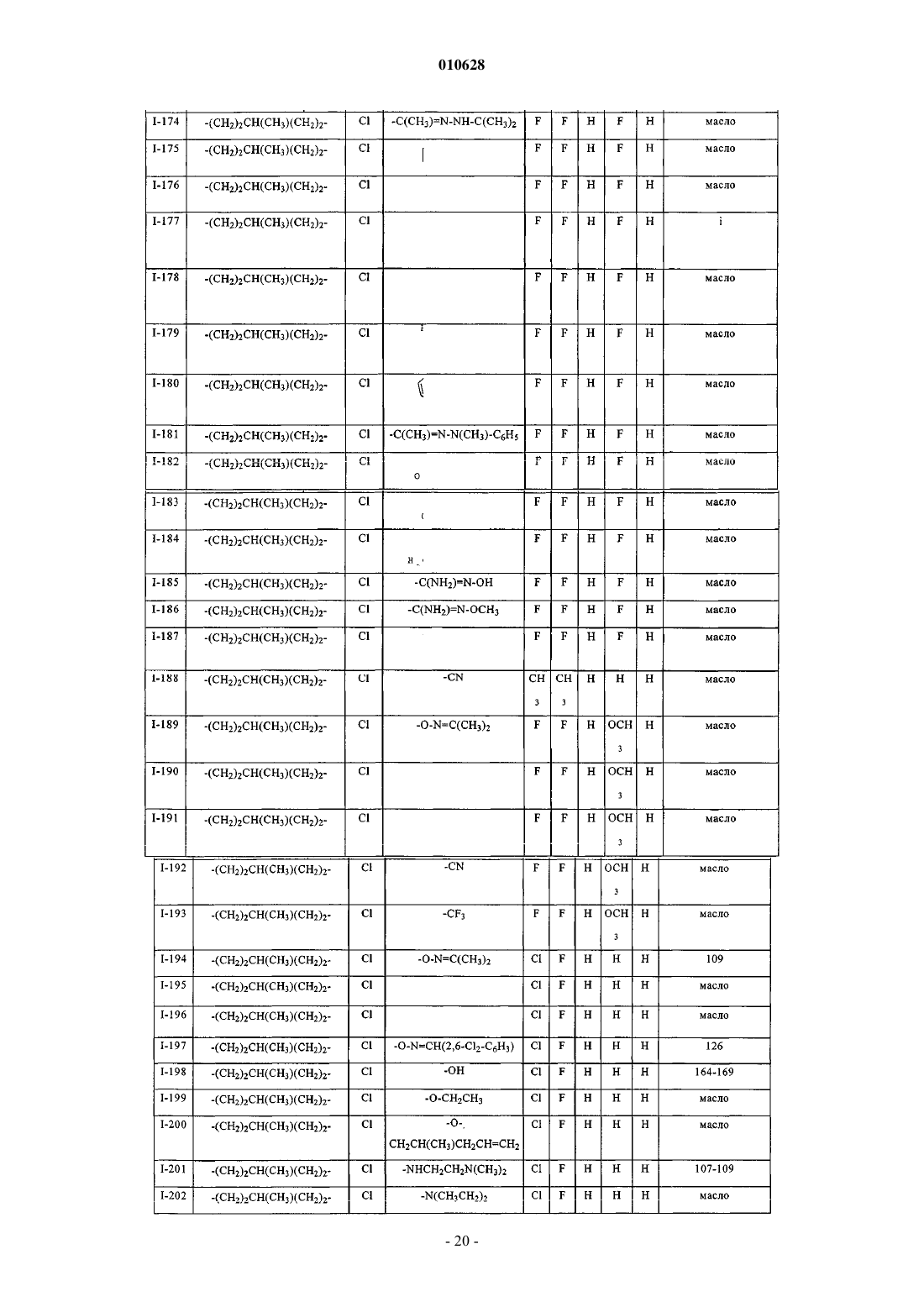
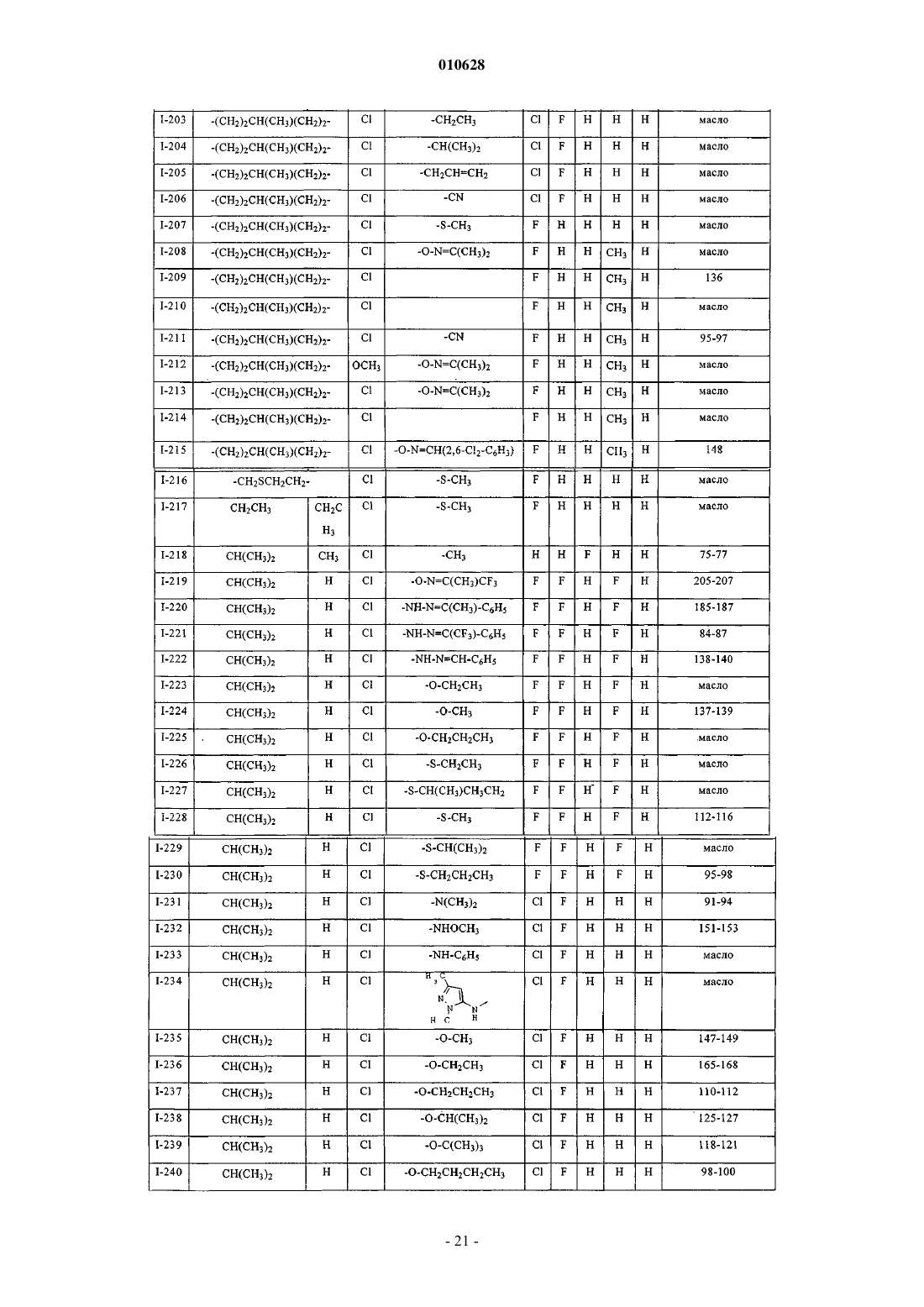
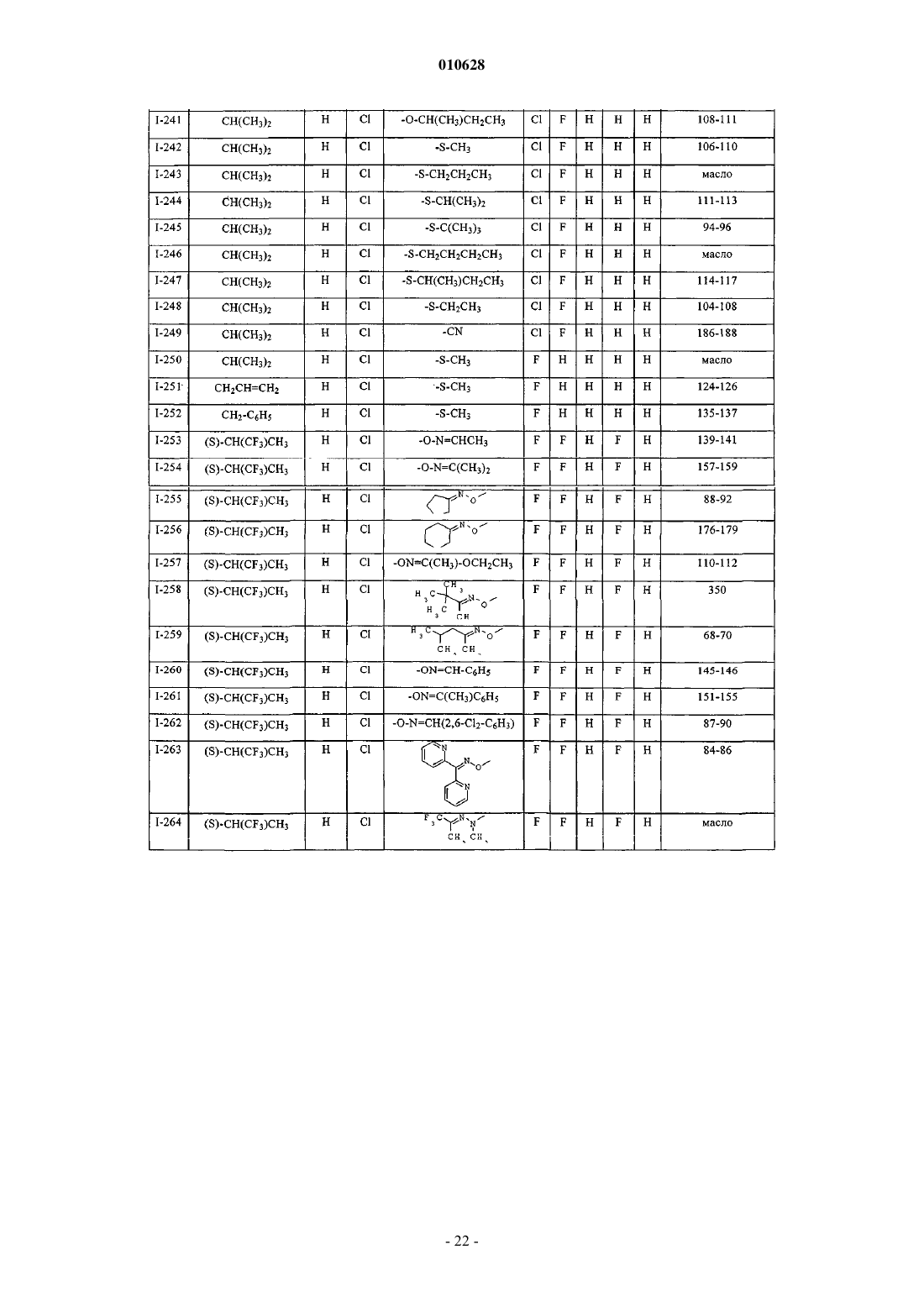
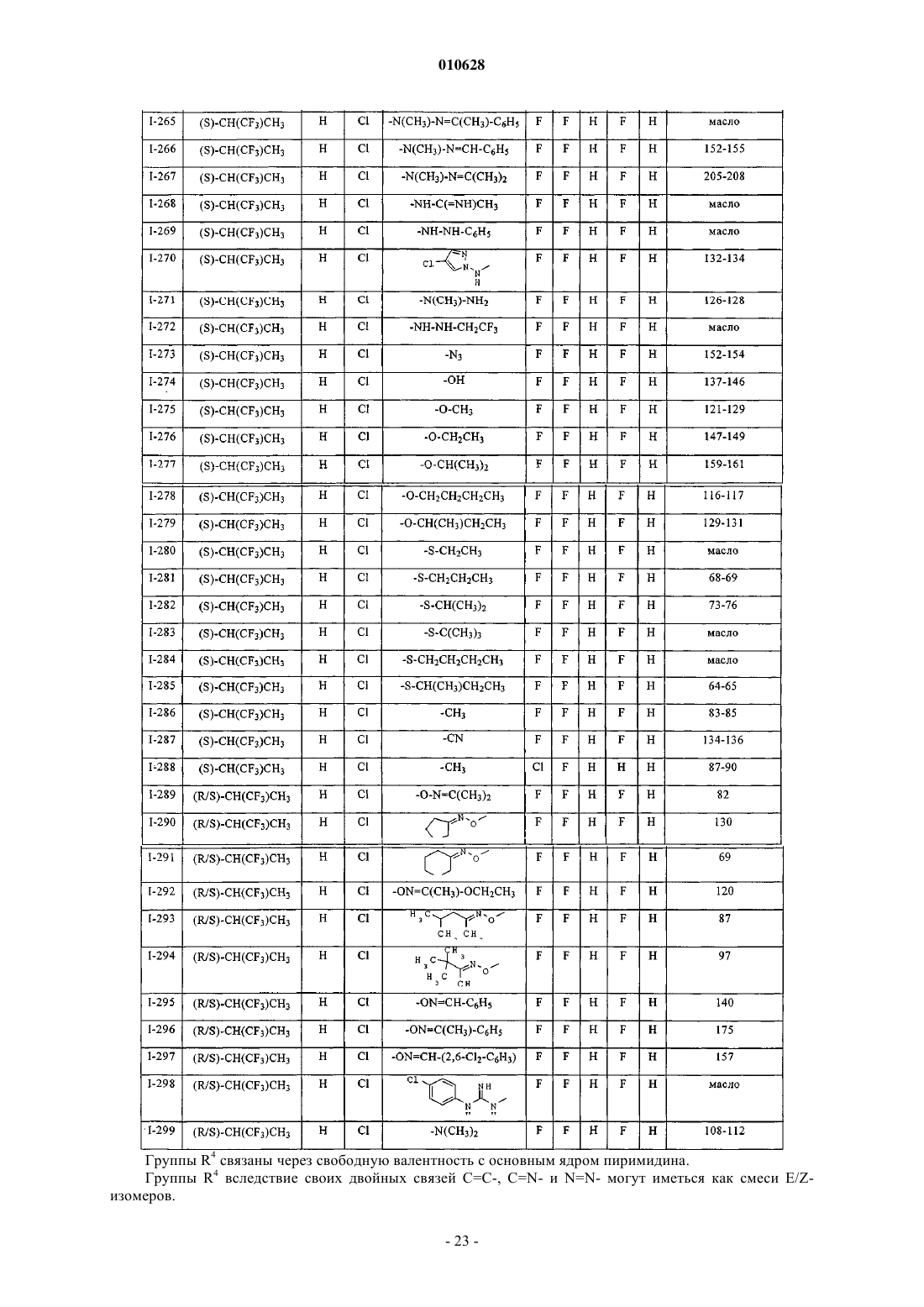
Текст
010628 Настоящее изобретение относится к 5-фенилпиримидинам формулы I в которой заместители и индекс имеют следующее значение:R1, R2 означают независимо друг от друга водород, C1-C6 алкил, C1-C6 галогеналкил, C3-C6 циклоалкил,C3-C6 галогенциклоалкил, C2-C6 алкенил, C2-C6 галогеналкенил, C2-C6 алкинил или C2-C6 галогеналкинил,R1 и R2 могут образовывать также с атомом азота, с которым они связаны, насыщенный или ненасыщенный 5- или 6-членный цикл, который может быть прерван групой эфиро- (-О-), тио- (-S-), сульфоксил- (-S[=O]-) или сульфонил- (-SO2-) и/или может быть замещен посредством 1-4 групп Ra и/или Rb;Ra, Rb означают независимо друг от друга водород, C1-C6 алкил, C2-C8 алкенил, C2-C8 алкинил, C1C6 галогеналкил, C1-C6 алкокси, C1-C6 галогеналкокси, C3-C10 циклоалкил, фенил или от 5- до 10-членный,насыщенный, частично ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов из группы, включающей О, N или S, причем циклические остатки могут быть частично или полностью замещены следующими группами Rx:Rx означают независимо друг от друга циано, нитро, амино, аминокарбонил, аминотиокарбонил, галоген, гидрокси, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 алкилкарбонил, C1-C6 алкилсульфонил, C1-C6 алкилсульфоксил, C3-C6 циклоалкил, C1-C6 алкокси, C1-C6 галогеналкокси, C1-C6 алкилоксикарбонил, C1-C6 алкилтио, C1-C6 алкиламино, ди-C1-C6 алкиламино, C1-C6 алкиламинокарбонил, ди-C1-C6 алкиламинокарбонил, C1-C6 алкиламинотиокарбонил, ди-C1-C6 алкиламинотиокарбонил, C2-C6 алкенил, C2-C6 алкенилокси,фенил, фенокси, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6 членный гетарилокси, C(=NOR)-OR или OC(R)2-C(R)=NOR,причем циклические группы, в свою очередь, незамещены или замещены посредством 1-3 остаков Ry:Ra и Rb могут совместно образовывать через алкиленовую или алкениленовую цепь со связывающим мостиком атомом насыщенный или ненасыщенный 5- или 6-членный цикл;Rc означает одну из приведенных для Ra и Rb одновалентных групп;m равно целому числу от 1 до 5. Кроме того, изобретение относится к способу получения таких соединений, к содержащим их средствам, а также к их применению для борьбы с фитопатогенными грибами. Производные пиридилпиримидина с фунгицидным действием известны из ЕР-А 407899, DE-A 4227811 и WO-A 92/10490. Производные тетрагидропиримидинов с фунгицидным действие известны из GB-A 2277090. Описанные в вышеприведенных публикациях соединения пригодны в качестве средств защиты растений для борьбы с фитопатогенными грибами. Их действие, однако, во многих случаях не удовлетворительно. Поэтому задачей изобретения является разработка соединений с усовершенствованным действием. В соответствии с этим были разработаны вышеприведенные производные фенилпиримидинов формулы I. Кроме того, были разработаны способы их получения, а также содержащие их средства для борьбы с фитопатогенными грибами и их применение в этом смысле. Соединения формулы I имеют по сравнению с известными соединениями повышенную эффективность против фитопатогенных грибов. Соединения формулы I могут быть получены различным образом. Предпочтительно для получения соединений формулы I, в которой R4 означает циано или связанную через гетероатом группу, исходят из сульфонов формулы II. В формуле II заместители Xm и R1 до R3 имеют такие же значения, что и в формуле I, и R означает С 1-С 4 алкил, предпочтительно метил. Сульфо-1 010628 ны формулы II подвергают взаимодействию с соединениями формулы III при щелочных условиях. Из практических соображений альтернативно можно применять соль щелочных металлов, щелочно-земельных металлов или аммониевую соль соединения III. Это взаимодействие осуществляют обычно при температуре от 25 до 250 С, предпочтительно от 40 до 210 С, в инертном органическом растворителе в присутствии основания (см. DE-A 3901084; публикацииChimia, том 50, стр. 525-530 (1996); Khim. Geterotsikl. Soedin., том 12, стр. 1696-1697 (1998. Пригодными растворителями являются галогенированные углеводороды, простой эфир, такой как диэтиловый эфир, диизопропиловый эфир, трет.-бутилметиловый эфир, 1,2-диметоксиэтан, диоксан, анизол и тетрагидрофуран, а также диметилсульфоксид, диметилформиамид и диметилацетамид. Особенно предпочтительны этанол, дихлорметан, ацетонитрил и тетрагидрофуран. Могут также применяться смеси приведенных растворителей. В качестве оснований, в общем, пригодны неорганические соединения, такие как гидроксиды щелочных и щелочно-земельных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, карбонаты щелочных и щелочно-земельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция. Основания применяются, в общем, в каталитических количествах, однако, они могут также применяться в избытке. Исходные продукты подвергаются взимодействию друг с другом, в общем, в эквимолярных количествах. Для повышения выхода преимущество может обеспечивать применение соединения формулы III в количестве до десятикратного, в частности до трехкратного, избытка в пересчете на соединение II. Соединения формулы I, в которых R4 означает водород, алкил, алкенил, алкинил или галогеналкил,получают из сложного фенилмалонового эфира формулы IV взаимодействием с амидинами формулы V. Это взаимодействие осуществляют при известных из публикации J. Chem. Soc. (1943) S. 388 и J.Org. Chem. (1952) Bd. 17, S. 1320 условиях. Сложный фенилмалоновый эфир формулы IV извествен из ЕР-А 1002788. Гидроксипиримидины формулы VI переводят в галогеновые соединения формулы VII (см. публикации J. Chem. Soc. (1943) S. 383; Helv. Chim. Acta (1981) Bd. 64, S. 113-152). В качестве средств галогенирования пригодны, в частности, такие соединения, как POCl3 и POBr3. Из галогенпиримидинов формулы VII взаимодействием с аминами формулы VIII получают соединения формулы I. Это взаимодействие осуществляют предпочтительно при описанных в публикации J. Chem. Soc.(1943) S. 383 и Chem. Eur. J. (1999) Bd. 5 (12), S. 3450-3458 условиях. Фенилпиримидины формулы I, в которой R3 означает циано или связанные через кислород группы,получают преимущественно из соответствующих галогеновых соединений формулы I взаимодействием с соединениями формулы IX при щелочных условиях. Из практических соображений альтернативно можно применять непосредственно соль щелочного металла, щелочно-земельного металла или аммониевую соль соединений IX. Это взаимодействие осуществляют обычно при температуре от 25 до 250 С, предпочтительно от 40 до 210 С, в инертном органическом растворителе, в случае необходимости, в присутствии основания (см.Reel. Trav. Chim. Pays-Bas (1942) Bd. 61, S. 291; J. Heterocycl. Chem. (1993) Bd. 30 (4), S. 993-995). При-2 010628 годными растворителями являются простой эфир, сульфоксиды, амиды, особенно предпочтительно диметилсульфоксид, N,N-диметилформамид, N-метилпирролидон, N,N-диметилацетамид, простой диэтиловый эфир, тетрагидрофуран, 1,2-диметоксиэтан. Могут применяться смеси приведенных растворителей. В качестве оснований, в общем, пригодны неорганические соединения, такие как гидроксиды щелочных и щелочно-земельных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, карбонаты щелочных и щелочно-земельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция. Основания применяются, в общем, в каталитическом количестве, они могут также применяться в избытке. Фенилпиримидины формулы I, где R3 означает C1-C6 алкил или C1-C6 галогеналкил, получают предпочтительно из соответствующих галогенных соединений формулы I взаимодействием с металлорганическими соединениями формулы X, где М означает группу Mg-Hal, Zn-R3 или B(OR)2, причем Hal означает атом галогена, и R - водород или С 1-С 4 алкил, и R3 означает C1-C6 алкил. Взаимодействие осуществляют обычно при температуре от -25 до 250C, предпочтительно от 0 до 150 С, в инертном органическом растворителе, в случае необходимости, в присутствии катализатора на основе переходного металла (см. публикации Chem. and Pharm. Bull. (1980) Bd. 28, Nr. 2, S. 571-577; TetrahedronLett. (1996) Bd. 37 (8), S. 1309; Tetrahedron Lett. (1994) Bd. 35 (19), S. 3155; Synlett. (1999) Bd. 7, S. 1145). Подходящими растворителями являются алифатические углеводороды, ароматические углеводороды,простые эфиры, в частности предпочтительны диэтиловый эфир, тетрагидрофуран, 1,2-диметоксиэтан,бензол, толуол и ксилол. Могут также применяться смеси приведенных растворителей. В качестве катализатора на основе переходного металла пригодны соединения железа, кобальта, никеля, родия, платины или палладия, в частности соединения никеля(0), никеля(II), палладия(0) и палладия(II). При этом могут применяться соли, такие как хлорид палладия, или ацетат палладия, или же комплексы палладия. Предпосылкой является только то, что лиганды на палладии при условиях реакции могут вытесняться с основы. Исходные продукты подвергаются взаимодействию друг с другом, в общем, в эквимолярных количествах. Для обеспечения высокого выхода преимущество дает применение соединения X в количестве от одного до десятикратного избытка, в частности до трехкратного избытка в пересчете на соединение I. Требуемые для получения соединений формулы I исходные вещества формулы II могут быть получены известными в публикациях методами, например следующим синтезом. Исходя из сложных алкиловых эфиров фенилмалоновой кислоты формулы XI и тиомочевины, получают соединения формулы XII причем в формуле XI R означает C1-C6 алкил. Реакцию осуществляют обычно в протонном растворителе, таком как спирты, в частности этанол, в случае необходимости, в присутствии основания, такого как Na2CO3 и NaHCO3. Температура реакции составляет предпочтительно от 70 до 220 С (см. публикации Collect. Czech. Chem. Commun., Bd. 48, S. 137-143 (1983); Heteroat. Chem., Bd. 10, S. 17-23 (1999);Czech. Chem. Commun., Bd. 58, S. 2215-2221 (1993. Требуемые сложные эфиры малоновой кислоты формулы XI известны из ЕР-А 1002788. Соединения XII превращаются алкилирующим агентом формулы XIII в производные тиобарбитуровой кислоты. В формуле XIII остаток R означает С 1-С 6 алкил и X нуклеофильно отщепляемую, уходящую группу. Формула XIII относится, в общем, к таким алкилирующим агентам, как метилхлорид и метилбромид, диметилсульфат или сложный метиловый эфир метансульфокислоты. Реакция может быть проведена в воде или же в диполярном апротонном растворителе, таком как,например, N,N-диметилформамид (см. патент US 5250689), она протекает предпочтительно в присутствии основания, такого как, например, KOH, NaOH, NaHCO3 и Na2CO3 или пиридин. Температура реакции находится предпочтительно в интервале 10-60 С. Соединения формулы XIV переводятся в дихлорпиримидины формулы XV (см. ЕР-А 745593; WO-3 010628 В качестве хлорирующего агента [Cl] пригодны, например, POCl3, PCl3/Cl2 или PCl5. Реакция может протекать обычно в избыточном хлорирующем агенте (POCl3) или в инертном растворителе. Эта реакция обычно осуществляется при температуре в интервале от 10 и до 180 С. Аминированием соединением формулы XVI соединения дихлора формулы XV переводятся в соединения формулы XVII. Эта реакция взаимодействия происходит предпочтительно при температуре от 20 до 120 С (см. J. Chem.Res. S (7), S. 286-287 (1995); Liebigs Ann. Chem., S. 1703-1705 (1995 в инертном растворителе, в случае необходимости в присутствии вспомогательного основания, такого как NaHCO3, Na2CO3 или трет.-амины. Амины формулы XVI могут приобретаться на рынке или же могут быть получены известными из литературных источников методами. Тиосоединения формулы XVII окисляются с получением сульфонов формулы II. Реакцию проводят предпочтительно при температуре в интервале от 10 до 50 С в присутствии протонного или апротонного растворителя (см. В. Kor. Chem. Soc., Bd. 16, S. 489-492 (1995); Z. Chem., Bd. 17, S. 63 (1977. Пригодным окислительным агентом может быть перекись водорода или 3-хлорпербензойная кислота. Введение отличных от хлора групп R3 в сульфоны формулы II может осуществляться аналогично соединениям формулы I. Соединения формулы I, где R4 означает группировки -C(=O)Rc, -C(=O)NRaRb, -C(=NORc)NRaRb,-C(=NNRaRb)Rc или -C(=NORa)Rc, получают предпочтительно из соединений формулы I, где R4 означает циано. Соединения формулы I, где R4 означает -C(=O)NRaRb или -C(=NORc)NRaRb, получают из соответствующих нитрилов (R4=циано) омылением с получением карбоновых кислот формулы Ia при кислотных или щелочных условиях и амидированием аминами HNRaRb. Омыление осуществляется обычно в инертном полярном растворителе, таком как вода или спирты, предпочтительно с органическим основанием,таким как гидроксиды щелочных и щелочно-земельных металлов, в частности NaOH. Это взаимодействие осуществляют преимущественно при известных из публикации Chem. andPharm. Bull. 1982, Bd. 30, N 12, S. 4314 условиях. Из амидов формулы Ib оксимированием замещенными гидроксиаминами H2N-ORc при щелочных условиях получают соединения формулы I, при которых R4 означает -C(=NORc)NRaRb (см. патент US 4876252). Замещенные гидроксиамины могут применяться как свободные основания или предпочтительно в форме своих солей присоединения кислот. Из практических соображений при этом особенно пригодны галогениды, такие как хлориды или сульфаты. Альтернативно амидоксимы формулы Ic, где Ra и Rb означают водород, могут быть получены также из соответствующих нитрилов (R4=циано) посредством взаимодействия с гидроксиламином и после-4 010628 дующего алкилирования. Это взаимодействие осуществляют преимущественно при описанных в патентной заявке DE-A 19837794 условиях. Соединения формулы I, где R4 означает -C(=O)Rc, получают из соответствующих нитрилов (R4=циано) посредством взаимодействия с соединениями Гриньяра Rc-Mg-Hal, где Hal означает атом галогена, в частности хлор или бром. Взаимодействие осуществляется предпочтительно при известных из публикации J. Heterocycl.Chem. 1994, Bd. 31 (4), S. 1041 условиях. Заместители и индексы в формулах Ia, Ib и Ic соответствуют их значениям в формуле I. Соединения формулы I, где R4 означает -C(=NNRaRb)Rc, доступны через карбонильные соединения. Они получаются взаимодействием соединения формулы Id с гидразинами H2NNRaRb, предпочтительно при известных из публикации J. Org. Chem. 1966, Bd. 31, S. 677 усолвиях. Соединения формулы I, где R4 означает -C(=NORa)Rc, доступны через оксимирование карбонильных соединений формулы Id. Оксимирование соединения формулы Id осуществляют аналогично оксимированию соединений формулы Ib. Реакционные смеси обрабатывают обычным образом, например смешиванием с водой, разделением фаз и, в случае необходимости, хроматографической очисткой сырых продуктов. Промежуточные и конечные продукты имеются частично в форме бесцветных или слегка коричневатых вязких масел, которые при сниженном давлении и при умеренно повышенной температуре освобождаются от летучих составных частей и очищаются. Если промежуточные и конечные продукты имеются как твердые вещества, очистка может осуществляться посредством перекристаллизации или дигерирования. Если отдельные соединения формулы I не доступны вышеописанным путем, они могут быть получены дериватизизацией других соединений формулы I. При указанных в вышеприведенных формулах определениях символов применяются общие понятия, которые, в общем, представляют следующие заместители. Галоген означает фтор, хлор, бром и йод. Алкил означает насыщенные, прямолинейные или разветвленные углеводородные остатки с 1-4 или 6 атомами углерода, например C1-C6 алкил, такой как метил, этил, пропил, 1-метилэтил, бутил, 1-метилпропил, 2-метилпропил, 1,1-диметилэтил, пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 2,2-диметилпропил, 1-этилпропил, гексил, 1,1-диметилпропил, 1,2-диметилпропил, 1-метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2-триметилпропил, 1,2,2 триметилпропил, 1-этил-1-метилпропил и 1-этил-2-метилпропил. Галогеналкил означает прямолинейные или разветвленные алкильные группы с 1-6 атомами углерода (как приведено выше), причем в этих группах атомы водорода могут быть частично или полностью заменены атомами галогена, как приведено выше, например C1-C2 галогеналкил, такой как хлорметил,бромметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлордифторметил, 1-хлорэтил, 1-бромэтил, 1-фторэтил, 2-фторэтил, 2,2-дифторэтил,2,2,2-трифторэтил, 2-хлор-2-фторэтил, 2-хлор-2,2-дифтороэтил, 2,2-дихлор-2-фторэтил, 2,2,2-трихлорэтил и пентафторэтил. Алкокси означает прямолинейные или разветвленные алкильные группы с 1-10 атомами углерода(как приведено выше), которые связаны со скелетом через атом кислорода (-O-). Алкилтио означает прямолинейные или разветвленные алкильные группы с 1-10 или 1-4 атомами углерода (как приведено выше), которые связаны со скелетом через атом серы (-S-). Алкенил означает ненасыщенные, прямолинейные или разветвленные углеводородные остатки с 24, 6 или 8 атомами углерода и двойной связью в любом положении, например C2-C6 алкенил, такой как этенил, 1-пропенил, 2-пропенил, 1-метилэтенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-метил-1-пропенил, 2 метил-1-пропенил, 1-метил-2-пропенил, 2-метил-2-пропенил, 1-пентенил, 2-пентенил, 3-пентенил, 4-пентенил, 1-метил-1-бутенил, 2-метил-1-бутенил, 3-метил-1-бутенил, 1-метил-2-бутенил, 2-метил-2-бутенил,3-метил-2-бутенил, 1-метил-3-бутенил, 2-метил-3-бутенил, 3-метил-3-бутенил, 1,1-диметил-2-пропенил,1,2-диметил-1-пропенил, 1,2-диметил-2-пропенил, 1-этил-1-пропенил, 1-этил-2-пропенил, 1-гексенил, 2 гексенил, 3-гексенил, 4-гексенил, 5-гексенил, 1-метил-1-пентенил, 2-метил-1-пентенил, 3-метил-1-пентенил,4-метил-1-пентенил, 1-метил-2-пентенил, 2-метил-2-пентенил, 3-метил-2-пентенил, 4-метил-2-пентенил,1-метил-3-пентенил, 2-метил-3-пентенил, 3-метил-3-пентенил, 4-метил-3-пентенил, 1-метил-4-пентенил,2-метил-4-пентенил, 3-метил-4-пентенил, 4-метил-4-пентенил, 1,1-диметил-2-бутенил, 1,1-диметил-3 бутенил, 1,2-диметил-1-бутенил, 1,2-диметил-2-бутенил, 1,2-диметил-3-бутенил, 1,3-диметил-1-бутенил,1,3-диметил-2-бутенил, 1,3-диметил-3-бутенил, 2,2-диметил-3-бутенил, 2,3-диметил-1-бутенил, 2,3-диме-5 010628 тил-2-бутенил, 2,3-диметил-3-бутенил, 3,3-диметил-1-бутенил, 3,3-диметил-2-бутенил, 1-этил-1-бутенил,1-этил-2-бутенил, 1-этил-3-бутенил, 2-этил-1-бутенил, 2-этил-2-бутенил, 2-этил-3-бутенил, 1,1,2-триметил-2-пропенил, 1-этил-1-метил-2-пропенил, 1-этил-2-метил-1-пропенил и 1-этил-2-метил-2-пропенил. Галогеналкенил означает ненасыщенные, прямолинейные или разветвленные углеводородные остатки с 2-8 атомами углерода и двойной связью в любом положении (как приведено выше), причем в этих группах атомы водорода могут быть частично или полностью заменены атомами галогена, как приведено выше, в частности фтором, хлором и бромом. Алкинил означает прямолинейные или разветвленные углеводородные группы с 2-4, 6 или 8 атомами углерода и тройной связью в любом положении, например С 2-C6 алкинил, такой как этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-метил-2-пропинил, 1-пентинил, 2-пентинил, 3-пентинил, 4-пентинил, 1-метил-2-бутинил, 1-метил-3-бутинил, 2-метил-3-бутинил, 3-метил-1-бутинил, 1,1 диметил-2-пропинил, 1-этил-2-пропинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил, 5-гексинил, 1 метил-2-пентинил, 1-метил-3-пентинил, 1-метил-4-пентинил, 2-метил-3-пентинил, 2-метил-4-пентинил,3-метил-1-пентинил, 3-метил-4-пентинил, 4-метил-1-пентинил, 4-метил-2-пентинил, 1,1-диметил-2-бутинил, 1,1-диметил-3-бутинил, 1,2-диметил-3-бутинил, 2,2-диметил-3-бутинил, 3,3-диметил-1-бутинил, 1 этил-2-бутинил, 1-этил-3-бутинил, 2-этил-3-бутинил и 1-этил-1-метил-2-пропинил. Галогеналкинил: ненасыщенные, прямолинейные или разветвленные углеводородные остатки с 2-8 атомами углерода и тройной связью с любом положении (как приведено выше), причем в этих группах атомы водорода могут быть частично или полностью заменены на атомы галогена, как приведено выше,в частности на фтор, хлор и бром. Алкинилокси: ненасыщенные, прямолинейные или разветвленные углеводородные остатки с 3-8 атомами углерода и тройной связью в любом, не смежном с гетероатомом положении (как приведено выше), которые связаны со скелетом через атом кислорода (-О-). Циклоалкил: моноцикличные, насыщенные углеводородные группы с 3-6, 8 или 10 углеродными кольцевыми членами, например C3-C8 циклоалкил, такой как циклопропил, циклобутил, циклопентил,циклогексил, циклогептил и циклооктил. 5- или 6-членный гетероциклил, содержащий наряду с углеродными кольцевыми членами от 1 до 3 атомов азота, и/или 1 атом кислорода или серы, или 1 или 2 атома кислорода и/или серы, например 2-тетрагидрофуранил, 3-тетрагидрофуранил, 2-тетрагидротиенил, 3-тетрагидротиенил, 2-пирролидинил, 3 пирролидинил, 3-изоксазолидинил, 4-изоксазолидинил, 5-изоксазолидинил, 3-изотиазолидинил, 4-изотиазолидинил, 5-изотиазолидинил, 3-пиразолидинил, 4-пиразолидинил, 5-пиразолидинил, 2-оксазолидинил, 4-оксазолидинил, 5-оксазолидинил, 2-тиазолидинил, 4-тиазолидинил, 5-тиазолидинил, 2-имидазолидинил, 4-имидазолидинил, 1,2,4-оксадиазолидин-3-ил, 1,2,4-оксадиазолидин-5-ил, 1,2,4-тиадиазолидин 3-ил, 1,2,4-тиадиазолидин-5-ил, 1,2,4-тиазолидин-3-ил, 1,3,4-оксадиазолидин-2-ил, 1,3,4-тиадиазолидин 2-ил, 1,3,4-триазолидин-2-ил, 2,3-дигидрофур-2-ил, 2,3-дигидрофур-3-ил, 2,4-дигидрофур-2-ил, 2,4-дигидрофур-3-ил, 2,3-дигидротиен-2-ил, 2,3-дигидротиен-3-ил, 2,4-дигидротиен-2-ил, 2,4-дигидротиен-3-ил,2-пирролин-2-ил, 2-пирролин-3-ил, 3-пирролин-2-ил, 3-пирролин-3-ил, 2-изоксазолин-3-ил, 3-изоксазолин 3-ил, 4-изоксазолин-3-ил, 2-изоксазолин-4-ил, 3-изоксазолин-4-ил, 4-изоксазолин-4-ил, 2-изоксазолин-5-ил,3-изоксазолин-5-ил, 4-изоксазолин-5-ил, 2-изотиазолин-3-ил, 3-изотиазолин-3-ил, 4-изотиазолин-3-ил, 2 изотиазолин-4-ил, 3-изотиазолин-4-ил, 4-изотиазолин-4-ил, 2-изотиазолин-5-ил, 3-изотиазолин-5-ил, 4 изотиазолин-5-ил, 2,3-дигидропиразол-1-ил, 2,3-дигидропиразол-2-ил, 2,3-дигидропиразол-3-ил, 2,3-дигидропиразол-4-ил, 2,3-дигидропиразол-5-ил, 3,4-дигидропиразол-1-ил, 3,4-дигидропиразол-3-ил, 3,4-дигидропиразол-4-ил, 3,4-дигидропиразол-5-ил, 4,5-дигидропиразол-1-ил, 4,5-дигидропиразол-3-ил, 4,5-дигидропиразол-4-ил, 4,5-дигидропиразол-5-ил, 2,3-дигидрооксазол-2-ил, 2,3-дигидрооксазол-3-ил, 2,3-дигидрооксазол-4-ил, 2,3-дигидрооксазол-5-ил, 3,4-дигидрооксазол-2-ил, 3,4-дигидрооксазол-3-ил, 3,4-дигидрооксазол-4-ил, 3,4-дигидрооксазол-5-ил, 3,4-дигидрооксазол-2-ил, 3,4-дигидрооксазол-3-ил, 3,4-дигидрооксазол-4-ил, 2-пиперидинил, 3-пиперидинил, 4-пиперидинил, 1,3-диоксан-5-ил, 2-тетрагидропиранил, 4-тетрагидропиранил, 2-тетрагидротианил, 3-гексагидропиридазинил, 4-гексагидропиридазинил, 2 гексагидропиримидинил, 4-гексагидропиримидинил, 5-гексагидропиримидинил, 2-пиперазинил, 1,3,5 гексагидротриазин-2-ил и 1,2,4-гексагидротриазин-3-ил. 5- или 6-членный гетероарил, который наряду с углеродными кольцевыми членами может содержать гетероатомы из группы кислорода, серы и азота: арил, как приведено выше, или 1- или 2-ядерный гетероарил, например 5-членный гетероарил, содержащий от 1 до 4 атомов азота или от 1 до 3 атомов азота и 1 атом серы или 1 атом кислорода: 5-кольцевые гетероарильные группы, которые наряду с атомами углерода могут содержать от 1 до 4 атомов азота или от 1 до 3 атомов азота и 1 атом серы или кислорода в качестве кольцевых членов, например 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 2-пирролил, 3-пирролил, 3-изоксазолил,4-изоксазолил, 5-изоксазолил, 3-изотиазолил, 4-изотиазолил, 5-изотиазолил, 3-пиразолил, 4-пиразолил, 5 пиразолил, 2-оксазолил, 4-оксазолил, 5-оксазолил, 2-тиазолил, 4-тиазолил, 5-тиазоллли, 2-имидазолил, 4 имидазолил, 1,2,4-оксадиазол-3-ил, 1,2,4-оксадиазол-5-ил, 1,2,4-тиадиазол-3-ил, 1,2,4-тиадиазол-5-ил,1,2,4-тиазол-3-ил, 1,3,4-оксадиазол-2-ил, 1,3,4-тиадиазол-2-ил и 1,3,4-триазол-2-ил; бензоконденсированный 5-членный гетероарил, содержащий от 1 до 3 атомов азота или 1 атом азо-6 010628 та и 1 атом кислорода или серы: 5-кольцевые гетероарильные группы, которые наряду с атомами углерода могут содержать от 1 до 4 атомов азота или от 1 до 3 атомов азота и 1 атом серы или кислорода в качестве кольцевых членов и в которых два смежных углеродных кольцевых члена или 1 атом азота и 1 смежный углеродный кольцевой член могут быть связаны мостиком бута-1,3-диен-1,4-дииловой группы; 6-членный гетероарил, содержащий от 1 до 3, соответственно, от 1 до 4 атомов азота: 6-кольцевые гетероарильные группы, которые наряду с углеродными атомами могут содержать от 1 до 3, соответственно, от 1 до 4 атомов азота в качестве кольцевых членов, например 2-пиридинил, 3-пиридинил, 4-пиридинил, 3-пиридазинил, 4-пиридазинил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, 2-пиразинил,1,3,5-триазин-2-ил и 1,2,4-триазин-3-ил. Алкилен: двухвалентные неразветвленные цепи из 1-4 СН 2-групп, например СН 2, СН 2 СН 2,СН 2 СН 2 СН 2 и СН 2 СН 2 СН 2 СН 2. Оксиалкилен: двухвалентная неразветвленная цепь из 2-4 СН 2-групп, причем валентность связана через атом кислорода со скелетом, например ОСН 2 СН 2, ОСН 2 СН 2 СН 2 и ОСН 2 СН 2 СН 2 СН 2. Оксиалкиленокси: двухвалентные неразветвленные цепи из 1-3 СН 2-групп, причем обе валентности связаны через атом кислорода со скелетом, например OCH2O, OCH2CH2O и OCH2CH2CH2O. Алкенилен: двухвалентные неразветвленные цепи из 1-3 СН 2-групп и СН=СН-группы в любом положении, например СН=СНСН 2, СН 2 СН=СНСН 2, СН=СНСН 2 СН 2, СН 2 СН=СНСН 2 СН 2 и СН=СНСН 2 СН 2 СН 2. Относительно определяемого изобретением применения фенилпиримидинов формулы I особенно предпочтительны следующие значения заместителей, а именно как в отдельности, так и в комбинации. В частности, предпочтительны соединения формулы I, при которых R1 означает водород. В одинаковой степени особенно предпочтительны соединения формулы I, при которых R1 и R2 независимо друг от друга означают C1-C6 алкил, C1-C6 галогеналкил, C3-C6 циклоалкил, С 2-C6 алкенил. В особенности предпочтительны соединения формулы I, при которых R1 означает С 1-С 4 алкил и R2 водород. Особенно предпочтительны соединения формулы I, при которых R1 и R2 образуют совместно с соединяющим мостиком атомом азота насыщенное или ненасыщенное 5- или 6-членное кольцо, которое может быть прервано группами простой эфир- (-O-), тио- (-S-), сульфоксил- (-S[=O]-) или сульфонильной группой (-SO2-) и/или может быть замещено 1 или 2 метил- или галогенметиловыми группами или в котором 2 смежных атома углерода связаны мостиком через метиленовую группу. Замещение 1 или 2 метил- или галогенметиловыми группами, в частности 1 или 2 метиловыми группами, является особенно предпочтительным. Кроме того, предпочтительны соединения формулы I, при которых R1 и R2 совместно образуют бутиленовую, пентиленовую или пентениленовую цепь, которая может быть замещена алкиловой, в частности метиловой, группой или может быть относительно 2 смежных атомов углерода связана мостиком посредством метиленовой группы. Далее предпочтительны соединения формулы I, при которых R1 и R2 образуют совместно пентиленовую или пентениленовую цепь, которая замещена метиловой группой. Особенно предпочтительны соединения формулы I, при которых R1 и R2 образую совместно со связывающим мостиком атомом азота 3- или 4-метилпиперидиниловую группу или 2-метилпирролидиновую группу. Наряду с этим особенно предпочтительны соединения формулы I, при которых R3 означает галоген, в частности хлор. В одинаковой степени предпочтительны соединения формулы I, при которых R4 означает водород,циано, азидо, C1-C6 алкил, C2-C8 алкенил, C2-C8 алкинил, C1-C6 галогеналкил, -ON=CRaRb, или -NRcN=CRaRb,или -C(=NORc)NRaRb. В частности, предпочтительны соединения формулы I, при которых R4 означает циано, -CRaNORb или -ON=CRaRb, и в частности -ON=CRaRb. Наряду с этим предпочтительны соединения формулы I, при которых R4 означает -NH(=NH)NHRc,-NHC(=O)NHRa, -NHC(=O)Ra, -OC(=O)Ra, -C(=NORc)NH2 или -CRc(=NNRaRb). Далее предпочтительны соединения формулы I, при которых R4 означает -NRcN=CRaRb. В одинаковой степени предпочтительны соединения формулы I, при которых R4 означает-C(=NORc)NRaRb, в частности -C(=NORc)NH2. Наряду с этим особенно предпочтительны соединения формулы I, при которых R4 означает C1-C6 алкенил или азидо. Кроме того, предпочтительны соединения формулы I, при которых Ra и Rb одинаковы или различны и означают водород, C1-C6 алкил, С 1-С 4 алкокси, фенил или 5- или 6-членный ароматической цикл, причем кольца, в случае необходимости, могут быть замещены посредством 1-3 групп Rx; причем их значения водород, алкил, алкокси и, в случае необходимости, замещенный фенил, особенно предпочтительны. Особенно предпочтительными значениями для остатков Ra и Rb являются С 1-С 4 алкил, C1-C2 галогеналкил, С 1-С 4 алкокси-С 1-С 2 алкил, C3-C6 алкенил, C3-C6 галогеналкенил, С 1-С 4 алкокси, С 1 галогеналкокси,пиридил, пиразолил, фенил или бензил, или Ra и Rb совместно образуют бутиленовую или пентиленовую цепь, причем циклические группы могут быть замещены посредством до 4 заместителей, выбранных из группы, включающей галоген, С 1-С 4 алкил, C1 галогеналкил, С 1-С 4 алкокси и/или С 1-С 4 алкокси-С 1-С 2 алкил.-7 010628 Предпочтительно Rc означает водород. В одинаковой степени предпочтительны соединения формулы I, при которых X означает хлор,фтор, метил, трифторметил или метокси. Кроме того, особенно предпочтительны соединения формулы I, при которых 1 или 2 заместителя X находятся в орто-положении относительно места связи с пиримидиновым кольцом. Наряду с этим особенно предпочтиельны соединения формулы IAX2, Х 3, Х 4, Х 5 означают водород или одну из приведенных для X1 и X2 групп. В частности, предпочтительны соединения формулы IA, при которыхX3, Х 4, Х 5 означают водород или одну из приведенных для X1 и X2 групп. Кроме того, особенно предпочтительны соединения формулы I, при которых Xm означает F5, 2-Cl,2-F, 2-СН 3, 2-ОСН 3, 2,6-Cl2, 2,6-F2, 2-Cl-6-F, 2-Br-6-F, 2-CH3-4-Cl, 2-CH3-4-F, 2-CH3-5-F, 2-CH3-6-F, 2 СН 3-4-ОСН 3, 2-CF3-4-F, 2-CF3-5-F, 2-CF3-6-F, 2-CF3-4-OCH3, 2-OCH3-6-F, 2,4,6-Cl3, 2,3,6-F3, 2,4,6-F3,2,4,6-(CH3)3, 2,6-F2-4-CH3, 2,6-F2-4-OCH3, 2,4-F2-6-OCH3, 2,6-(CH3)2-4-OCH3 и 2,6-(CH3)2-4-F. В частности, предпочтительны соединения формулы I, при которых Xm означает F5, 2,6-Cl2, 2,6-F2, 2-Cl-6-F, 2CH3-4-F, 2-CH3-6-F, 2-СН 3-4-С 1 и 2,4,6-F3. Соединения I пригодны в качестве фунгицидов. Они отличаются прекрасной активностью против широкого спектра фитопатогенных грибов, в частности из класса аскомецетов, дейтеромицетов, фикомицетов и базидиомицетов. Они являются частично систематически активными и могут применяться при защите растений в качестве почвенных и лиственных фунгицидов. Они имеют особое значение при борьбе с рядом фитопатогенных грибов на различных культурных растениях, таких как пшеница, рожь,ячмень, овес, рис, кукуруза, злаки, бананы, хлопчатник, соевые, кофе, сахарный тростник, виноград,плодовые и декоративные растения, и на овощных культурах, таких как огурцы, бобовые, томаты, картофель и тыквенные, а также на семенах этих растений. Особенно они пригодны для борьбы против следующих болезней растений: виды Alternaria, Podosphaera, Sclerotinia, Physalospora canker на овощных и плодовых растениях,Botrytis cinerea (серая гниль) на клубничных, овощных, декоративных культурах и на виноградных лозах,Corynespora cassiicola на огурцах,виды Colletotrichum на плодовых и овощных,Diplocarpon rosae на розах,Elsinoe fawcetti и Diaporhe citri на цитрусовых фруктах,виды Sphaerotheca на тыквенных, клубнике и розах,Cercospora arachidicola на земляных орехах, сахарной свекле и баклажанах,Erysiphe cichoracearum на тыквенных,Leveillula taurica на перце, томатах и баклажанах,Phyllactinia kakicola, Gloesporium kaki на японских абрикосовых,Gymnasporangium yamadae, Leptothyrium pomi, Podosphaera leucutricha и Gloedes pomigena на яблоневых,Cladosporium carpophilum на грушевых и японских абрикосовых,виды Phomopsis на грушевых,виды Phytophtora на цитрусовых, картофеле, луке, в частности Phytopphtora infestans на картофеле и томатах,Blumeria graminis (мучнистая роса) на зерновых культурах,виды Fusarium и Verticillium на различных растениях,Glomerella cingulata на чае,виды Drechslera и Bipolaris на зерновых культурах и рисе,виды Mycosphaerella на бананах и земляном орехе,Plasmopara viticola на виноградных лозах,виды Personospora на луке, шпинате и хризантемах,Phaeoisariopsis vitis и Sphaceloma ampelina на цитрусовых,Pseudocercosporella herpotrichoides на зерновых культурах и ячмене,виды Pseudoperonospora на огурцах и хмеле,Phytophthora infestans на картофеле и томатах,виды Puccinia и Typhula на зерновых и дернине,Pyricularia oryzae на рисе,-8 010628 виды Rhizoctonia на хлопчатнике, рисе и дернине,Stagonospa nodorum и Septoria tritici на пшенице,Uncinula necator на виноградных лозах,виды Ustilago на зерновых и сахарном тростнике, а также виды Venturia (парша) на яблоневых и грушевых. Кроме того, соединения формулы I пригодны для борьбы с такими фитопатогенными грибами, какPaecilomyces variotii, при защите материалов (например, древесины, бумаги, в дисперсиях для покрытий,волокон, соответственно, тканей) и при защите складируемых запасов. Соединения формулы I применяются таким образом, что грибы или подлежащие защите от поражения ими растения, материалы или почву обрабатывают фунгицидно активным количеством действущего вещества. Применение может осуществляться как перед, так и после поражения грибами материалов, растений или семян. Фунгицидные средства содержат, в общем, между 0,1 и 95, предпочтительно между 0,5 и 90 мас.% действующего вещества. Нормы расхода составляют при применении для защиты растений в зависимости от желаемого эффекта между 0,01 и 2,0 кг действующего вещества на гектар. При обработке посевного зерна, в общем, требуется количества действующего вещества от 0,001 до 0,1 г, предпочтительно от 0,01 до 0,05 г на кг посевного материала. При применении для защиты материалов, соответственно, складируемых запасов норма расхода ориентируется на область применения и на желаемый эффект. Обычные нормы расхода при защите материалов составляют, например, от 0,001 г до 2 кг, предпочтительно от 0,005 г до 1 кг действующего вещества на кубометр обрабатываемого материала. Соединения формулы I могут быть переведены в обычные препаративные формы, например растворы, эмульсии, суспензии, тонкие порошки, порошки, пасты и гранулят. Препаративная форма зависит от цели применения, она должна в любом случае обеспечивать тонкое и равномерное распределение соединения по изобретению. Препаративные формы получают известным образом, например путем разбавления действующего вещества в растворителях и/или наполнителях, по желанию с применением эмульгаторов или диспергаторов, причем при применении в качестве разбавителя воды также и другие органические растворители могут применяться в качестве вспомогательных агентов. В качестве впомогательных агентов пригодны, в основном, растворители, такие как ароматы (например, ксилол), хлорированные ароматы (например,хлорбензолы), парафины (например, фракции нефти), спирты (например, метанол, бутанол), кетоны (например, циклогексанон), амины (например, этаноламин, диметилформамид) и вода; наполнители, такие как естественные измельченные породы (например, каолин, глинозем, тальк, мел) и искуственные измельченные породы (например, высокодисперсная кремниевая кислота, соли кремниевой кислоты); эмульгаторы, такие как неионогенные и анионные эмульгаторы (например, полиоксиэтиленовый эфир спирта жирного ряда, алкилсульфонаты и арилсульфонаты) и диспергаторы, такие как лигнинсульфитная отработанная щелочь и метилцеллюлоза. В качестве поверхностно-активных веществ применяются соли щелочных, щелочно-земельных металлов и аммониевые соли лигнинсульфокислоты, нафталинсульфокислоты, фенолсульфокислоты, дибутилнафталинсульфокислоты, алкиларилсульфонаты, алкилсульфаты, алкилсульфонаты, сульфаты спиртов жирного ряда, кислоты жирного ряда, а также их соли щелочных и щелочно-земельных металлов, соли сульфатированного гликолевого эфира жирного ряда, продукты конденсации сульфонированного нафталина и производных нафталина с формальдегидом, продукты конденсации нафталина, соответственно, нафталинсульфокислот с фенолом и формальдегидом, полиоксиэтиленоктилфенольный эфир, этоксилированный изооктилфенол, октилфенол, нонилфенол, алкилфенолполигликолевый эфир, трибутилфенилполигликолевый эфир, алкиларилполиэфирные спирты, изотридециловый спирт, продукты конденсации этиленоксида жирных спиртов, этоксилированное касторовое масло, полиоксиэтиленалкиловый эфир, этоксилированный полиоксипропилен, ацеталь поликликолевого эфира лаурилового спирта жирного ряда, сложный эфир сорбита, лигнинсульфитные отработанные щелочи и метилцеллюлоза. Для получения предназначенных для непосредственного разбрызгивания растворов, эмульсий, паст или маслянных дисперсий применяются фракции минеральных масел со средней и высокой точками кипения, такие как керосин или дизельное топливо (масло), дегтярные масла растительного или животного происхождения, алифатические, циклические и ароматические углеводороды, например бензол, толуол,ксилол, парафин, тетрагидронафталин, алкилированные нафталины или их производные, метанол, этанол,пропанол, бутанол, хлороформ, тетрахлоруглерод, циклогексанол, циклогексанон, хлорбензол, изоформ,сильно полярные растворители, например диметилформамид, диэтилсульфоксид, N-метилпирролидон, вода. Порошковые препараты, препараты для опыливания и опудривания могут быть изготовлены путем смешения или совместного промеливания действующих веществ с твердым наполнителем. Гранулят, например оболочковый, импрегнированный или гомогенный гранулят, может быть получен путем связывания действующего вещества с твердыми наполнителями. Твердыми наполнителями могут быть, например, минеральные земли, такие как силикагель, кремниевые кислоты, силикаты, тальк,каолин, аттаклау, известняк, известь, мел, болюс, лесс, глина, доломит, диатомовоя земля, сульфат каль-9 010628 ция и магния, окись магния, измельченная пластмасса, удобрения, такие как сульфат аммония, фосфат аммония, нитрат аммония, мочевины и растительные продукты, такие как зерновая мука, мука древесной коры, древесная мука и мука ореховой скорлупы, порошок целлюлозы и другие твердые наполнители. Препаративные формы содержат, в общем, между 0,01 и 95 мас.%, предпочтительно между 0,1 и 90 мас.% действующего вещества. Действующие вещества имеют при этом чистоту от 90 до 100%, предпочтительно от 95 до 100% (по спектру ЯМР). Примеры препаративных формI. 5 вес.долей соединения согласно изобретению тщательно перемешивают с 95 вес.долями тонкого каолина. Таким образом получают средство опыливания, содержащее 5 мас.% действующего вещества.II. 30 вес.долей соединения согласно изобретению тщательно перемешивают с 92 вес.долями порошкового силикагеля и 8 вес.долями парафинового масла, которое напрыскивают на поверхность этого силикагеля. Таким образом получают препаративную форму действующего вещества с хорошей адгезионной способностью (содержание действующего вещества 23 мас.%).III. 10 вес.долей соединения согласно изобретению растворяют в смеси, которая состоит из 90 вес.долей ксилола, 6 вес.долей продукта присоединения 8-10 молей этиленоксида к 1 молю N-моноэтаноламида олеиновой кислоты, 2 вес.долей кальциевой соли додецилбензолсульфокислоты и 2 вес.долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла (содержание действующего вещества 9 мас.%).IV. 20 вес.долей соединения согласно изобретению растворяют в смеси, которая состоит из 60 вес.долей циклогексанона, 30 вес.долей изобутанола, 5 вес.долей продукта присоединения 7 молей этиленоксида к 1 молю изооктилфенола и 5 вес.долей продукта присоединения 40 молей этиленоксида к 1 молю кастрового масла (содержание действующего вещества 16 мас.%).V. 80 вес.долей соединения согласно изобретению хорошо перемешивают с 3 вес.долями натриевой соли диизобутилнафталин-альфа-сульфокислоты, 10 вес.долями натриевой соли лигнинсульфокислоты из сульфитного отработанного щелока и 7 вес.долями порошкового силикагеля и перемалывают в молотковой мельнице (содержание действующего вещества 80 мас.%).VI. Перемешивают 90 вес.долей соединения согласно изобретению с 10 вес.долями N-метилпирролидона и получают раствор, который пригоден для применения в форме мельчайших капель (содержание действующего вещества 90 мас.%).VII. 20 вес.долей соединения согласно изобретению растворяют в смеси, состоящей из 40 вес.долей циклогексанона, 30 вес.долей изобутанола, 20 вес.долей продукта присоединения 7 молей этиленоксида к 1 молю изооктилфенола и 10 вес.долей продукта присоединения 40 молей этиленоксида к 1 молю касторового масла. Путем концентрации и тонкого распределения раствора в 100000 вес.долей воды получают водную дисперсию, содержащую 0,02 вес.% действующего вещества.VIII. 20 вес.долей соединения согласно изобретению хорошо перемешивают с 3 вес.долями натриевой соли диизобутилнафталинсульфокислоты, 17 вес.долями натриевой соли лигнинсульфокислоты из сульфитного отработанного щелока и 60 вес.долями порошкового силикагеля и перемалывают в молотковой мельнице. Путем тонкого распределения смеси в 20000 вес.долях воды получают раствор для опрыскивания, который содержит 0,1 мас.% действующего вещества. Действующие вещества могут применяться как таковые, в их препаративной форме или же в приготовленной из них форме применения, например в форме подлежащих непосредственному распылению растворов, порошков, суспензий или дисперсий, эмульсий, маслянных дисперсий, паст, препаратов для опыливания, препаратов для опудривания, гранулятов путем опрыскивания, мелкокапельного опрыскивания,опыливания, опудривания или полива. Используемые формы зависят от цели применения, но во всех случаях должно быть обеспечено максимально тонкое распределение действующих веществ по изобретению. Водные препаративные формы могут быть приготовлены из концентратов эмульсий, паст или смачиваемых порошков (порошки для разбрызгивания, масляные дисперсии) путем добавки воды. Для изготовления эмульсий, паст или масляных дисперсий вещества как таковые, или же растворенные в масле,могут гомогенизироваться в воде с помощью смачивающих агентов, активаторов адгезии, диспергаторов или эмульгаторов. Могут также приготовляться состоящие из действующего вещества, смачивающего агента, активатора адгезии, диспергатора или эмульгатора и, возможно, из растворителя и масла концентраты, которые можно разбавлять водой. Концентрация действующего вещества в готовых к применению препаратах может варьироваться в широких пределах. В общем, она составляет от 0,0001 до 10%, предпочтительно от 0,01 до 1%. Действующие вещества могут применяться с успехом при особенно низких нормах расхода, причем имеется возможность использовать препараты с более чем 95 мас.% действующего вещества или даже применять действующее вещество без добавок. К действующим веществам могут добавляться масла различного типа, гербициды, фунгициды, другие средства борьбы с вредителями, бактерициды, в случае необходимости, также и непосредственно перед применением (смеси в баке). Эти средства могут примешиваться к соединениям по изобретению в весовом соотношении от 1:10 до 10:1.- 10010628 Соединения по изобретению в форме применения как фунгициды могут применяться вместе с другими действующими веществами, например гербицидами, инсектицидами, регуляторами роста, фунгицидами или же удобрениями. При смешении соединений I, соответственно, содержащих их фунгицидных средств с другими фунгицидами во многих случаях обеспечивается увеличение спектра фунгицидного действия. Нижеприведенный перечень фунгицидов, которые можно применять вместе с соединениями по изобретению, поясняет возможности их комбинирования, однако, не ограничивает их. К таким фунгицидам относятся следующие: сера, дитиокарбонаты и их производные, такие как ферридиметилдитиокарбамат, цинкдиметилдитиокарбамат, цинкдиметилдитиокабамат, марганецэтилен-бис-дитиокарбамат, марганеццинкэтилендиамин-бис-дитиокарбамат, тетраметилтиурамдисульфиды, аммиачный комплекс цинк(N,N-этилен-бис-дитиокарбамата), аммиачный комплекс цинк(N,N'-пропилен-бис-дитиокарбамата), полимер цинк(N,N'-пропилен-бис-дитиокарбамата), N,N'-пропилен-бис(тиокарбамоил)дисульфид; нитропроизводные, такие как динитро(1-метилгептил)фенилкротонат, 2-втор.-бутил-4,6-динитрофенил-3,3-диметилакрилат, 2-втор.-бутил-4,6-динитрофенилизопропилкарбонат, диизопропиловый эфир 5 нитроизофталевой кислоты; гетероциклические соединения, такие как 2-гептадецил-2-имидазолинацетат, 2,4-дихлор-6-(о-хлоранилино)-s-триазин, O,O-диэтилфталимидофосфонотиоат, 5-амино-1-[бис(диметиламино)фосфинил]-3 фенил-1,2,4-триазол, 2,3-дициано-1,4-дитиоантрахинон, 2-тио-1,3-дитиоло[4,5-b]хиноксалин, метиловый эфир 1-(бутилкарбамоил)-2-бензимидазолкарбаминовой кислоты, 2-метоксикарбониламинобензимидазол, 2-(фурил-(2-бензимидазол, 2-(тиазолил-(4-бензимидазол, N-(1,1,2,2-тетрахлорэтилтио)тетрагидрофталимид, N-трихлорметилтиотетрагидрофталимид, N-трихлорметилтиофталимид; диамид N-дихлорфторметилтио-N,N'-диметил-N-фенилсерной кислоты, 5-этокси-3-трихлорметил 1,2,3-тиадиазол, 2-роданметилтиобензтиазол, 1,4-дихлор-2,5-диметоксибензол, 4-(2-хлорфенилгидразоно)-3-метил-5-изоксазолон, пиридин-2-тио-1-оксид, 8-гидроксихинолин, соответственно, его медная соль, 2,3-дигидро-5-карбоксанилидо-6-метил-1,4-оксатиин, 2,3-дигидро-5-карбоксанилидо-6-метил-1,4 оксатиин-4,4-диоксид, анилид 2-метил-5,6-дигидро-4 Н-пиран-3-карбоновой кислоты, анилид 2-метилфуран-3-карбоновой кислоты, анилид 2,5-диметилфуран-3-карбоновой кислоты, анилид 2,4,5-триметилфуран-3-карбоновой кислоты, циклогексиламид 2,5-диметилфуран-3-карбоновой кислоты, амид N-циклогексил-N-метокси-2,5-диметилфуран-3-карбоновой кислоты, 2-анилид метилбензойной кислоты, анилид 2-йодбензойной кислоты, N-формил-N-морфолин-2,2,2-трихлорэтилацеталь, пиперазин-1,4-диил-бис-1(2,2,2-трихлорэтил)формамид, 1-(3,4-дихлоранилино)-1-формиламино-2,2,2-трихлорэтан, 2,6-диметил-Nтридецилморфолин, соответственно, его соли, 2,6-диметил-N-циклододецилморфолин, соответственно,его соли, N-[3-(п-трет.-бутилфенил)-2-метилпропил]-цис-2,6-диметилморфолин, N-[3-(п-трет.-бутилфенил)-2-метилпропил]пиперидин, 1-[2-(2,4-дихлорфенил)-4-этил-1,3-диоксолан-2-илэтил]-1 Н-1,2,4-триазол,1-[2-(2,4-дихлорфенил)-4-н-пропил-1,3-диоксолан-2-илэтил]-1 Н-1,2,4-триазол, N-(н-пропил)-N-(2,4,6-трихлорфеноксиэтил)-N'-имидазолилмочевина, 1-(4-хлорфенокси)-3,3-диметил-1-(1 Н-1,2,4 триазол-1-ил)-2 бутанон, 1-(4-хлорфенокси)-3,3-диметил-1-(1 Н-1,2,4-триазол-1-ил)-2-бутанол, (2RS,3RS)-1-[3-(2-хлорфенил)-2-(4-фторфенил)оксиран-2-илметил]-1 Н-1,2,4-триазол, -(2-хлорфенил)(4-хлорфенил)-5-пиримидинметанол, 5-бутил-2-диметиламино-4-гидрокси-6-метилпиримидин, бис-(п-хлорфенил)-3-пиридинметанол, 1,2-бис-(3-этоксикарбонил-2-тиоуреидо)бензол, 1,2-бис-(3-метоксикарбонил-2-тиоуреидо)бензол; стробилурины, такие как метил (Е)-2-2-[6-(2-цианофенокси)пиримидин-4-илокси]фенил-3-метоксиакрилат, (Е)-2-(метоксиимино)-N-метил-2-[-(2,5-ксилилокси)-о-толуол]ацетат, 2-[6-(2-хлорофенокси)-5-фторопиримидин-4-илокси]фенил(5,6-дигидро-1,4,2-диоксазин-3-ил)метанон О-метилоксим, метил (Е)-метоксиимино[-(о-толуолокси)-о-толуол]ацетаты, (Е)-2-(метоксиимино)-N-метил-2-(2-феноксифенил)ацетамид,(2 Е)-2-(метоксиимино)-2-2-[(3 Е,5 Е,6 Е)-5-(метоксиимино)-4,6-диметил-2,8-диокса-3,7-диазанона-3,6-диен 1-ил]фенил-N-метилацетамид, метил-(Е)-3-метокси-2-2-[6-(трифторметил)-2-пиридилоксиметил]фенил акрилат, метил-N-2-[1-(4-хлорофенил)-1 Н-пиразол-3-илоксиметил]фенил(N-метокси)карбамат, метил(Е)-метоксиимино-(Е)[1-(-трифторо-м-толуол)этилиденаминоокси]-о-толулацетат; анилинопиримидины, такие как N-(4,6-диметилпиримидин-2-ил)анилин, N-[4-метил-6-(1-пропинил) пиримидин-2-ил]анилин, N-[4-метил-6-циклопропилпиримидин-2-ил]анилин; фенилпирролы, такие как 4-(2,2-дифтор-1,3-бензодиоксол-4-ил)пиррол-3-карбонитрил; амиды коричной кислоты, такие как морфолид 3-(4-хлорфенил)-3-(3,4-диметоксифенил)акриловой кислоты, морфолид 3-(4-фторфенил)-3-(3,4-диметоксифенил)акриловой кислоты; а также различные фунгициды, такие как додецилнуанидинацетат, 1-(3-бром-6-метокси-2-метилфенил)-1-(2,3,4-триметокси-6-метилфенил)метанон, 3-[3-(3,5-диметил-2-оксициклогексил)-2-гидроксиэтил] глютаримид, гексахлорбензол, DL-метил-N-(2,6-диметилфенил)-N-фуроил(2)аланинат, метиловый эфир- 11010628 ацетамид, 1-[2-(2,4-дихлорфенил)пентил]-1 Н-1,2,4-триазол, 2,4-дифтор(1 Н-1,2,4-триазолил-1-метил) бензгидриловый спирт, N-(3-хлор-2,6-динитро-4-трифторметилфенил)-5-трифторметил-3-хлор-2-аминопиридин, 1-бис-(4-фторфенил)метилсилил)метил)-1 Н-1,2,4-триазол, амид 5-хлор-2-циано-4-п-толуолимидазол-1-сульфокислоты, 3,5-дихлор-N-(3-хлор-1-этил-1-метил-2-оксопропил)-4-метилбензамид. Примеры синтеза Отраженные в нижеследующих примерах синтеза стадии использовались при соответствующем изменении исходных соединений для получения других соединений формулы I. Полученные таким образом соединения приведены в нижеследующей таблице с физическими данными. Пример 1. Получение [6-хлор-2-(N'-изопропилиденгидразино)-5-(2,4,6-трифторфенил)пиримидин-4 ил]-S)-1-трифторметилэтил)амина [I-1]. 0,065 г (2,4 ммоль) гидрида натрия смешивают в 10 мл диметилформамида с 0,16 г (2,2 ммоль) ацетоноксима. После перемешивания в течение 1 ч при температуре от 20 до 25 С добавляют 1,0 г (2,2 ммоль)[6-хлор-2-метансульфонил-5-(2,4,6-трифторфенил)пиримидин-4-ил]-S)-1-трифторметилэтил)амина (сокращенно сульфон 1). После перемешивания еще в течение 14 ч при температуре от 20 до 25C реакционную смесь выливают на воду и экстрагируют дихлорметаном. Собранные органические фазы промывают водой, потом сушат и освобождают от растворителя. Остается 0,6 г приведенного в заголовке соединения с т.пл. 157-159 С. Пример 2. Получение [6-хлор-2-метокси-5-(2,4,6-трифторфенил)пиримидин-4-ил]-S)-1-трифторметилэтил)амина [I-24]. Раствор из 282 мг (0,65 ммоль) сульфона 1 в 4 мл безводного диметилформамида смешивают с 294 мг(1,30 ммоль) метилата натрия (90% в метаноле). После перемешивания в течение 16 ч при температуре от 20 до 25C реакционную смесь разбавляют метил-трет.-бутиловым эфиром, промывают водой и потом сушат. После отгонки растворителя и хроматографии на силикагеле получают 0,14 г приведенного в заголовке соединения с т.пл. 121-129 С. Пример 3. Получение [6-хлор-2-метилсульфанил-5-(2,4,6-трифторфенил)пиримидин-4-ил]изопропиламина [1-30]. Раствор из 216 мг (0,5 моль) [6-хлор-2-метансульфонил-5-(2,4,6-трифторметил)пиримидин-4-ил]изо пропиламина (сокращенно сульфон 2) в 2 мл безводного диметилформамида смешивают с 70 мг (1,0 ммоль) тиометилата натрия, растворенного в 3 мл безводного тетрагидрофурана. После перемешивания в течение 16 ч при 20-25 С реакционную смесь разбавляют метил-трет.-бутиловым эфиром (МТВЕ), промывают водой и потом сушат. После отгонки растворителя и хроматографии на силикагеле получают 0,21 г приведенного в заголовке соединения с т.пл. 112-116 С. Пример 4. Получение [6-хлор-2-гидразино-5-(2,4,6-трифторфенил)пиримидин-4-ил]-S)-1-трифторметилэтил)амина. Этанольный раствор из 0,5 г (1,15 ммоль) сульфона 1 и 0,13 г (2,54 ммоль) гидрата гидразина перемешивают в течение 2 ч при температуре от 20 до 25 С. После отгонки растворителя и кипячения остат- 12010628 ка в простом диизопропиловом эфире остаток отфильтровывают и промывают смесью диизопропилового эфира и гексана в соотношении 1:1. Пример 5. Получение [6-хлор-2-[N'-(1-трифторметилэтилиден)гидразино]-5-(2,4,6-трифторфенил) пиримидин-4-ил]-S)-1-трифторметилэтил)амина [I-56]. Раствор из 0,8 г (2,07 ммоль) гидразина из примера 4 и 0,28 г (2,49 ммоль) 1,1,1-трифторацетона в ацетонитриле перемешивают в течение 16 ч при температуре от 20 до 25 С. Осадок отфильтровывают, из фильтрата получают после хроматографии на силикагеле (циклогексан СН:МТВЕ 95:5) 0,3 г приведенного в заголовке соединения с т.пл. 205-207 С. Пример 6. Получение [6-хлор-2-(N-фенилгидразино)-5-(2,4,6-трифторфенил)пиримидин-4-ил]-S)1-трифторметилэтил)амина [I-62]. Этанольный раствор 0,5 г (1,15 ммоль) сульфона 1 и 0,15 г (1,38 ммоль) фенилгидразина кипятят с обратным холодильником в течение 16 ч. После охлаждения, отгонки растворителя и хроматографии на силикагеле (циклогексан:метил-трет.-бутиловый эфир 95:5) получают 0,36 г приведенного в заголовке соединения. Пример 7. Получение [2-азидо-6-хлор-5-(2,4,6-трифторфенил)пиримидин-4-ил]-S)-1-трифторметилэтил)амина [I-66]. Суспензию из 2,9 г бутиллития (15% раствор в гексане) в 15 мл тетрагидрофурана смешивают при-70 С с 0,62 г (6,6 ммоль) анилина, потом перемешивают еще в течение 1 ч при -70 С. После добавки 1,0 г(2,64 ммоль) [6-хлор-5-(2-хлорфторфенил)-2-метансульфонилпиримидин-4-ил]изопропиламина (сокращенно сульфон 3) реакционную смесь нагревают до температуры от 20 до 25 С. Реакционную смесь выливают на ледяную воду и подкисляют соляной кислотой. Затем реакционную смесь экстрагируют посредством 240 мл МТВЕ, из собранных органических фаз после сушки и отгонки растворителя получают 1,0 г приведенного в заголовке соединения. Пример 9. Получение 4-хлор-6-S)-1-трифторметилэтиламино)-5-(2,4,6-трифторфенил)пиримидин 2-карбонитрила [I-73]. Раствор из 0,5 г (1,15 ммоль) сульфона 1 и 0,36 г (2,31 ммоль) цианида тетраэтиламмония в дихлорэтане перемешивают в течение 20 ч при температуре от 20 до 25 С. После отгонки растворителя и хроматографии на силикагеле (циклогексан [СН]:МТВЕ 9:1) получают 0,18 г приведенного в заголовке соединения с т.пл. 134-136 С. Пример 10. Получение 4-хлор-5-(2-хлор-6-фторфенил)-6-изопропиламинопиримидин-2-карбонитрила [I-74]. Раствор из 1,0 г (2,63 ммоль) сульфона 3 и 0,21 г (3,16 моль) цианида калия в ацетонитриле перемешивают в течение 5 дней при температуре от 20 до 25C. Растворитель отгоняют и остаток дегидрируют в смеси из метил-трет.-бутиловом эфира и этилацетата в соотношении 9:1. После фильтрации и концентрации фильтрата получают 0,61 г приведенного в заголовке соединения с т.пл. 186-188 С. Группы R4 связаны через свободную валентность с основным ядром пиримидина. Группы R4 вследствие своих двойных связей С=С-, C=N- и N=N- могут иметься как смеси E/Zизомеров.- 23010628 Примеры действия против фитопатогенных грибов Фунгицидное действие соединений общей формулы I демострируются следующими тестами. Из действующих веществ, по отдельности или вместе, были подготовлены композиции в виде 10% эмульсии в смеси из 70 мас.% циклогексанона, 20 мас.% Nekanil LN (Lutensol AP6, смачивающий агент на основе этоксилированных алкилфенолов, имеющий свойства эмульгатора и диспергатора) и 10 мас.%Wettol EM (неионогенный эмульгатор на основе этоксилированного касторового масла) и разведены водой до необходимой концентрации. Пример применения 1. Эффективность против вызванной Septoria пятнистости листьев пшеницы(Septoria tritici). Листья выращенных в горшках проростков пшеницы сорта "Riband" опрыскивают до образования капель водной композицией действующего вещества, которая приготовлена из основного раствора, состоящего из 10% действующего вещества, 85% циклогесанона и 5% эмульгатора. Через 24 ч после подсыхания напрысканного слоя его инокулируют водной суспензией спор Septoria tritici. Суспензия содержит 2,0106 мпор/мл. Тестуемые растения помещают в теплицу при температуре между 18 и 22 С и при относительной влажности воздуха около 100%. Через 2 недели определяют степень развития болезни визуально в % поражения общей поверхности листьев. В этом тесте обработанные посредством 250 млн д. действующего вещества 1, 12-15, 18, 19,21, 24-26, 30, 32, 33, 54, 55, 60-65, 86, 160, 223, 224, 226, 228, 235-239, 248, 254, 264, 265, 269-272 и 275278 вышеприведенной таблицы растения показывают максимальное поражение 7%, в то время как необработанные растения имеют поражение в 90%. Пример применения 2. Эффективность против сетчатой пятнистости листьев ячменя (Pyrenophora teres). Листья выращенных в горшках проростков ячменя сорта "Igri" опрыскивают до образования капель водной композицией действующего вещества, которая приготовлена из основного раствора, состоящего из 10% действующего вещества, 85% циклогесанона и 5% эмульгатора, и через 24 ч после подсыхания напрысканного слоя инокулируют его водной суспензией Pyrenophora (Drechslera) teres, возбудителя сетчатой пятнистости листьев ячменя. Затем тестируемые растения помещают в теплицу при температуре между 20 и 24 С и при относительной влажности воздуха до 100%. Через 6 дней определяют визуально степень развития болезни в % поражения общей поверхности листьев. В этом тесте обработанные посредством 250 млн д. действующего вещества 1, 55, 60, 64, 73,88, 130, 134, 160, 163, 165, 168, 171, 185, 186, 254, 255, 265, 267, 271, 274, 276-278 и 287 вышеприведенной таблицы растения проявили поражение не более 15%, в то время как необработанные рстения имели поражение в 100%. Пример применения 3. Защитное действие против вызванной Sphaerotheca fuliginea мучнистой росы огурцов. Листья выращенных в горшках проростков огурцов сорта "Chinesische Schlange" на стадии зародышевого листка опрыскивают водной композицией действующего вещества, приготовленной из основного раствора, состоящего из 10% действующего вещества, 85% циклогексанона и 5% эмульгатора, до образования капель. Спустя 20 ч после подсыхания напрысканного раствора растения инокулируют водной суспензией спор мучнистой росы огурцов (Sphaerotheca fuliginea). После этого растения культивируют в теплице при температуре от 20 и 24 С и относительной влажности от 60 до 80% в течение 7 дней. Потом определяют степень развития мучнистой росы в % поражения поверхности зародышевого листа. В этом тесте обработанные посредством 250 млн д. действующего вещества 86, 88, 100, 121,130, 141, 160, 163, 168, 171, 185, 186, 189, 206, 220, 249, 253-261, 265, 266, 271, 273, 275, 276, 287 и 299 вышеприведенной таблицы растения имели поражение не более 10%, в то время как необработанные растения имели поражение в 85%. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. 5-Фенилпиримидины формулы I в которой заместители и индекс имеют следующие значения:R2 - водород или группы, значения которых определены для R1;R1 и R2 могут образовывать также с атомом азота, с которым они связаны, насыщенный или ненасыщенный 5- или 6-членный цикл, который может быть прерван группой эфиро- (-O-), тио- (-S-), сульфоксил- (-S[=O]-) или сульфонил- (-SO2-) и/или может быть замещен посредством 1-4 групп Ra и/или Rb;Ra, Rb означают независимо друг от друга водород, C1-C6 алкил, С 2-С 8 алкенил, С 2-С 8 алкинил, C1-C6 галогеналкил, C1-C6 алкокси, С 1-С 6 галогеналкокси, С 3-С 10 циклоалкил, фенил или 5-10-членный насыщенный, частично ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов из группы, включающей О, N или S, причем циклические остатки могут быть частично или полностью замещены следующими группами Rx:Rx независимо друг от друга означают циано, нитро, амино, аминокарбонил, аминотиокарбонил, галоген, гидрокси, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 алкилкарбонил, C1-C6 алкилсульфонил, C1-C6 алкилсульфоксил, C3-C6 циклоалкил, C1-C6 алкокси, C1-C6 галогеналкокси, C1-C6 алкилоксикарбонил, C1-C6 алкилтио, C1-C6 алкиламино, ди-C1-C6 алкиламино, C1-C6 алкиламинокарбонил, ди-C1-C6 алкиламинокарбонил,C1-C6 алкиламинотиокарбонил, ди-C1-C6 алкиламинотиокарбонил, C2-C6 алкенил, C2-C6 алкенилокси, фенил, фенокси, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6 членный гетарилокси, C(=NOR)-OR или OC(R)2-C(R)=NOR,причем циклические группы, в свою очередь, незамещены или замещены от 1-3 остатков Ry:R, R означают водород или C1-C6 алкил;Ra и Rb могут также совместно образовывать через алкиленовую или алкениленовую цепь со связывающим мостиком атомом насыщенный или ненасыщенный 5- или 6-членный цикл;Rc означает одну из приведенных для Ra и Rb одновалентных групп;m равно целому числу от 1 до 5. 2. 5-Фенилпиримидины формулы I в которой заместители и индекс имеют следующие значения:R2 - водород или группы, значения которых определены для R1;R1 и R2 могут образовывать также вместе атомом азота, с которым они связаны, насыщенный или ненасыщенный 5- или 6-членный цикл, который может быть прерван атомом кислорода и может иметьC1-C6 алкильный заместитель или в котором 2 смежных углеродных кольцевых члена могут быть связаны мостиком посредством C1-C4 алкиленовой группы;Ra, Rb независимо друг от друга означают водород, C1-C6 алкил, С 2-С 8 алкенил, С 2-С 8 алкинил, C1-C6 галогеналкил, С 1-С 6 алкокси, С 1-С 6 галогеналкокси, С 3-C10 циклоалкил, фенил или 5-10-членный насыщенный, частично ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 гетероатомов из группы, включающей О, N или S, причем циклические остатки могут быть замещены частично или полностью следующими группами Rx:Rx независимо друг от друга означают циано, нитро, амино, аминокарбонил, аминотиокарбонил, галоген, гидрокси, C1-C6 алкил, C1-C6 галогеналкил, C1-C6 алкилкарбонил, C1-C6 алкилсульфонил, C1-C6 алкилсульфоксил, C3-C6 циклоалкил, C1-C6 алкокси, C1-C6 галогеналкокси, C1-C6 алкилоксикарбонил, C1-C6 алкилтио, C1-C6 алкиламино, ди-C1-C6 алкиламино, C1-C6 алкиламинокарбонил, ди-C1-C6 алкиламинокарбонил,C1-C6 алкиламинотиокарбонил, ди-C1-C6 алкиламинотиокарбонил, C2-C6 алкенил, С 2-C6 алкенилокси, фенил,- 25010628 фенокси, бензил, бензилокси, 5- или 6-членный гетероциклил, 5- или 6-членный гетарил, 5- или 6-членный гетарилокси, C(=NORa)-ORb или OC(Ra)2-C(Rb)=NORb,причем цикличные группы, в свою очередь, замещены или незамещены посредством 1-3 остатков Ry:R, R означают водород или C1-C6 алкил;m равно целому числу от 1 до 5. 3. Соединения формулы I по п.1, в которой-NRcN=CRaRb, или -C(=NORc)NRaRb. 4. Соединения формулы I по п.1, в которой R4 означает -ON=CRaRb. 5. Соединения формулы I по п.1, в которой R4 означает -CRc=NORa. 6. Способ получения соединений формулы I по п.1, в которой R4 означает циано или связанную через гетероатом группу, взаимодействием сульфонов формулы II где R означает C1-C4 алкил, с соединениями формулы III где R4 имеет вышеприведенное значение, в щелочных условиях. 7. Способ получения соединений формулы I по п.1, где R3 означает галоген и R4 - алкенил, алкинил или галогеналкил, взаимодействием сложных фенилмалоновых эфиров формулы IV где R4 имеет вышеприведенное значение, и галогенированием образовавшихся дигидроксипиримидинов формулы VI агентом галогенирования с получением дигалогенпиримидинов формулы VII где Hal означает бром или хлор, который подвергают взаимодействию с аминами формулы VIII где R1 и R2 имеют приведенное для формулы I значение, с получением соединений формулы I. 8. Способ получения соединений формулы I по п.1, где R3 означает циано, C1-C6 алкокси, C1-C6 галогеналкокси или C3-C8 алкенилокси, взаимодействием пиримидинов формулы I, где R3 означает галоген, с- 26010628 соединениями формулы IX где R3 имеет вышеприведенное значение, в щелочных условиях. 9. Способ получения соединений формулы I по п.1, где R3 означает C1-C6 алкил, взаимодействием пиримидинов формулы I, где R3 означает галоген, с металлорганическими соединениями формулы X где М означает группу Mg-Hal, Zn-R3 или B(OR)2, причем Hal означает атом галогена, и R означает водород или С 1-С 4 алкил, и R3 означает C1-C6 алкил. 10. Фунгицидное средство, содержащее твердый или жидкий носитель и соединение формулы I по пп.1-5. 11. Способ борьбы с фитопатогенными грибами, отличающийся тем, что грибы или подлежащие защите от них материалы, растения, почву или посевной материал обрабатывают эффективным количеством соединения формулы I по пп.1-5. 12. [6-Хлор-2-(диметиламино)-5-(2-хлор-6-фторфенил)пиримидин-4-ил]-(1-метилэтил)амин;
МПК / Метки
МПК: C07D 239/46, C07D 239/52, A01N 43/54, C07D 403/12, C07D 239/48, C07D 239/42
Метки: содержащие, применение, способ, получения, 5-фенилпиримидины, средства
Код ссылки
<a href="https://eas.patents.su/28-10628-5-fenilpirimidiny-sposob-ih-polucheniya-soderzhashhie-ih-sredstva-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">5-фенилпиримидины, способ их получения, содержащие их средства и их применение</a>
Предыдущий патент: Совокупность дозированных лекарственных форм, содержащих опиоид
Следующий патент: Композиция для аэрозольной ингаляции, содержащая антихолинергическое средство
Случайный патент: Инфузионный и инъекционный раствор леводопа