Фенилпропионамидные соединения и их применение
Формула / Реферат
1. Соединение формулы I
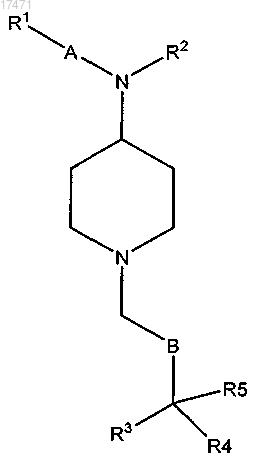
где А обозначает фенил;
R1 обозначает Н или галоген либо -O-С1-6алкил;
R2 обозначает С1-6алкил, С2-6алкенил, С2-6алкинил, -С(=О)С1-6алкил, -С(=О)-С2-6алкенил, С(=О)-С2-6алкинил или -СО2С1-6алкил;
В обозначает (СН2)m, где m обозначает 1, 2 или 3;
R3 и R4, каждый, представляют собой фенил;
R5 обозначает Н, С1-6алкил, -С(=О)NHC1-6алкил, -С(=O)N(С1-6алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1-пиперидинилкарбонила и N-метилпиперазинилкарбонила;
или его фармацевтически приемлемая соль или сольват.
2. Соединение по п.1, отличающееся тем, что R1 обозначает:
а) Н, F или Cl;
б) -O-C1-6алкил.
3. Соединение по пп.1 и 2, отличающееся тем, что R2 обозначает:
а) -С(=О)С1-6алкил или
б) С(=О)-С2-6алкенил или -С(=О)-С2-6алкинил.
4. Соединение по пп.1-3, отличающееся тем, что R2 обозначает С(=О)СН2СН3.
5. Соединение по п.1, выбранное из
N-(1-(3,3-дифенилпропил)пиперидин-4-ил)-N-фенилпропионамида;
N,N-(диметил-2,2-дифенил-4-(4-N-фенилпропионамидо)пиперидин-1-ил)бутанамида;
N-(1-(4-оксо-3,3-дифенил-4-(пирролидин-1-ил)бутилпиперидин-4-ил))-N-фенилпропионамида, или
его фармацевтически приемлемая соль или сольват.
6. Фармацевтическая композиция, содержащая соединение по пп.1-5 и по меньшей мере один фармацевтически приемлемый эксципиент.
7. Способ лечения, предупреждения или ослабления интенсивности боли или рвоты у животного путем активации опиоидного рецептора, включающий введение эффективного количества соединения формулы I животному, где соединение формулы I представляет собой
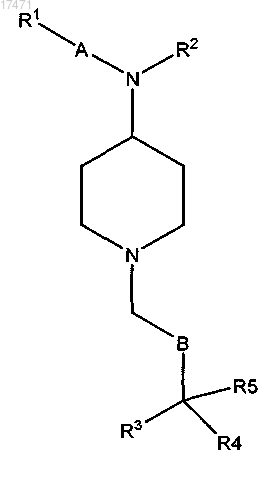
где А обозначает фенил;
R1 обозначает Н или галоген либо -O-C1-6алкил;
R2 обозначает C1-6алкил, С2-6алкенил, С2-6алкинил, -С(=О)С1-6алкил, -С(=О)-С2-6алкенил, С(=О)-С2-6алкинил или -CO2C1-6алкил;
В обозначает (СН2)m, где m обозначает 1, 2 или 3;
R3 и R4, каждый, представляют собой фенил;
R5 обозначает Н, циано, C1-6алкил, -C(=O)NHC1-6алкил, -C(=O)N(C1-6алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1-пиперидинилкарбонила и N-метилпиперазинилкарбонила; или
его фармацевтически приемлемую соль или сольват.
8. Способ по п.7, отличающийся тем, что соединение активирует m-опиоидный рецептор.
9. Способ по п.8, отличающийся тем, что соединение селективно активирует m-опиоидный рецептор.
10. Способ по пп.7-9, отличающийся тем, что боль выбирают из группы, состоящей из хронической боли, невропатической боли, боли при воспалении, боли при остеоартрите, боли при артрите, боли при ревматоидном артрите, боли при раке, боли, вызванной поражением спинного мозга, боли, вызванной хирургическим вмешательством, послеоперационной боли или острой боли.
11. Способ по пп.7-10, дополнительно включающий введение эффективного количества опиоидного аналгетика, неопиоидного аналгетика, агента против мигрени, противоэпилептического агента, противодиарейного агента и противорвотного агента (антиэметика).
12. Применение соединения формулы I по пп.1-5 для изготовления лекарственного средства для лечения, предупреждения или ослабления интенсивности боли или рвоты.
13. Применение соединения формулы I для лечения, предупреждения или ослабления интенсивности боли или рвоты у животного путем активации опиоидного рецептора, где соединение формулы I представляет собой
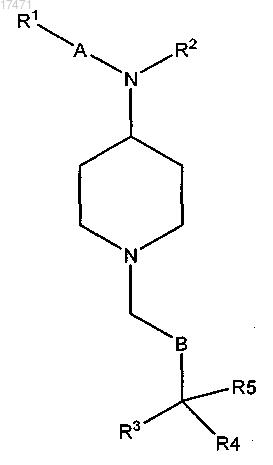
где А обозначает фенил;
R1 обозначает Н или галоген либо -O-C1-6алкил;
R2 обозначает C1-6алкил, С2-6алкенил, С2-6алкинил, -С(=О)С1-6алкил, -С(=О)-С2-6алкенил, С(=О)-С2-6алкинил или -СО2С1-6алкил;
В обозначает (CH2)m, где m обозначает 1, 2 или 3;
R3 и R4, каждый, представляют собой фенил;
R5 обозначает Н, циано, С1-6алкил, -C(=O)NHC1-6алкил, -С(=O)N(С1-6алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1-пиперидинилкарбонила и N-метилпиперазинилкарбонила; или
его фармацевтически приемлемую соль или сольват.
14. Применение соединения формулы I для лечения, предупреждения или ослабления боли, выбранной из хронической боли, невропатической боли, боли при воспалении, боли при остеоартрите, боли при артрите, боли при ревматоидном артрите, боли при раке, боли, вызванной поражением спинного мозга, боли, вызванной хирургическим вмешательством, послеоперационной боли или острой боли, где соединение формулы I представляет собой

где А обозначает фенил;
R1 обозначает Н или галоген либо -O-C1-6алкил;
R2 обозначает С1-6алкил, С2-6алкенил, С2-6алкинил, -С(=О)С1-6алкил, -С(=О)-С2-6алкенил, С(=О)-С2-6алкинил или -СО2С1-6алкил;
В обозначает (CH2)m, где m обозначает 1, 2 или 3;
R3 и R4, каждый, представляют собой фенил;
R5 обозначает Н, циано, C1-6алкил, -С(=О)NHC1-6алкил, -С(=O)N(С1-6алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1-пиперидинилкарбонила и N-метилпиперазинилкарбонила; или
его фармацевтически приемлемую соль или сольват.
Текст
Изобретение относится к фенилпропионамидным соединениям формулы (I) и их фармацевтически приемлемым солям и сольватам, где А, В, R1, R2, R3, R4 и R5 имеют значения, определенные в описании. Изобретение также относится к применению соединений формулы (I) для лечения,предупреждения или ослабления интенсивности расстройства, отвечающего на активацию опиоидных рецепторов, в частности -опиоидных рецепторов. Соединения по настоящему изобретению особенно применимы для лечения боли. 017471 Область, к которой относится изобретение Данное изобретение относится к области медицинской химии. Изобретение относится к новым соединениям фенилпропионамида, которые действуют как агонисты опиоидов. Предпосылки создания изобретения Боль является наиболее обычным симптомом, по поводу которого пациенты обращаются за медицинским советом и лечением. Боль может быть острой и хронической. В то время как острая боль обычно является самоограничивающейся, хроническая боль может длиться в течение 3 месяцев или дольше и приводить к значительным изменениям личностных свойств, образа жизни, профессиональной квалификации и общего качества жизни пациента (K.M. Foley, Pain, в Cecil Textbook of Medicine 100-107, J.C.Bennet and Plum eds., 20th ed. 1996). Традиционно боль лечат с применением неопиоидного аналгетика, включая, но без ограничения,ацетилсалициловую кислоту, холина магния трисалицилат, ацетаминофен, ибупрофен, фенопрофен,дифлузинал и напроксен; или опиоидного аналгетика, включая, но без ограничения, морфин, гидроморфон, метадон, леворфанол, фентанил, оксикодон и оксиморфон. Id. В патентах США No. 6576650, 6166039 и 5849761, принадлежащих Yaksh, и в патенте США No. 6573282, принадлежащем Yaksh et al., описаны производные 1,4-замещнного пиперидина для применения в качестве антигипералгетических опиатов периферического действия. В патенте США No. 6362203 В 1, принадлежащем Mogi et al., описаны производные 4-гидрокси-4 фенилпиперидина, которые оказывают периферическое аналгетическое действие. В канадском патенте No. 949560, принадлежащем Carron et al., описаны производные пиперидина для применения в качестве аналгетиков. В опубликованной Международной заявке WO 02/38185 А 2, поданной Dunn et al., описаны 1,4 замещнные пиперидины для применения в качестве антигипералгетических опиатов. В опубликованной Международной заявке WO 01/70689 А 1, поданной Dunn et al., описаны производные пиперидина для применения в качестве агонистов -опиоидных рецепторов. Традиционные опиоидные аналгетики проявляют свою фармакологическую активность, если только они прошли через гематоэнцефалический барьер (ВВВ). Но прохождение через гематоэнцефалический барьер может привести к нежелательным побочным эффектам, опосредованным центральной нервной системой (ЦНС), таким как респираторная депрессия, повышенная толерантность к лекарствам, повышенная лекарственная зависимость, констипация и нежелательная эйфория. Остатся потребность в новых лекарствах, которые можно использовать для лечения или предупреждения боли и, следовательно, для того, чтобы ослабить или избежать одного или более побочных эффектов, обусловленных традиционной терапией. Сущность изобретения Настоящее изобретение относится к применению соединений фенилпропионамида, представленных ниже формулой I, и их фармацевтически приемлемых солей и сольватов в качестве агонистов опиоидных рецепторов. Предполагается, что некоторые соединения формулы I проявят селективность в отношении-опиоидного рецептора. Предполагается, что некоторые соединения формулы I с трудом проходят через ВВВ и, следовательно, фактически остаются на периферии. Настоящее изобретение относится также к лечению, предупреждению и уменьшению интенсивности расстройства, реагирующего на активацию опиоидных рецепторов у млекопитающих, страдающих таким расстройством, путм введения эффективного количества соединения формулы I, или его фармацевтически приемлемой соли или сольвата по данному описанию. Более конкретно, изобретение относится к лечению, предупреждению или уменьшению интенсивности расстройства, реагирующего на активацию опиоидных рецепторов вне ЦНС (т.е. в периферической нервной системе), у млекопитающего,страдающего таким расстройством, путм введения эффективного количества соединения формулы I или его фармацевтически приемлемой соли либо сольвата по данному описанию. В одном аспекте настоящее изобретение относится к лечению, предупреждению и уменьшению интенсивности расстройства, реагирующего на активацию опиоидных рецепторов у млекопитающих, страдающих таким расстройством, путм введения эффективного количества соединения формулы I или его фармацевтически приемлемой соли либо сольвата по данному описанию. В частности, предпочтительными расстройствами, которые можно лечить, предупредить или ослабить путм активации опиоидного рецептора, являются боль, такая как хроническая боль, невропатическая боль, боль при воспалении, боль при остеоартрите, боль при ревматоидном артрите, боль при раке, боль, вызванная поражением спинного мозга, боль, вызванная хирургическим вмешательством, или острая боль, диарея, неврологические расстройства, такие как болезнь Паркинсона, хорея Хантингтона, болезнь Альцгеймера, тревога, депрессия,стрессовые расстройства, потеря памяти, например, вследствие болезни Альцгеймера и/или при деменции или эпилепсии. Кроме того, соединения по настоящему изобретению можно использовать в качестве анестетиков, нейропротективных агентов, агентов для лечения неврологических расстройств, таких как болезнь Паркинсона, анксиолитиков, антидепрессантов, агентов для лечения стрессовых расстройств,агентов для лечения потери памяти, например, вследствие болезни Альцгеймера и/или деменции, проти-1 017471 воэпилептических или противосудорожных (антиконвульсантов) агентов. В одном аспекте настоящее изобретение включает новые соединения формулы I и их фармацевтически приемлемые соли и сольваты. В другом аспекте настоящее изобретение включает фармацевтические композиции, применимые для лечения, предупреждения или ослабления интенсивности расстройства, реагирующего на активацию опиоидных рецепторов, причм указанная фармацевтическая композиция содержит эффективное количество соединения формулы I или его фармацевтически приемлемую соль либо сольват, необязательно в смеси с одним или более фармацевтически приемлемыми носителями или эксципиентами. В другом аспекте настоящее изобретение включает способ лечения, предупреждения или ослабления боли (например, хронической боли, невропатической боли, боли при воспалении, боли при хирургическом вмешательстве или острой боли), или диареи путм введения эффективного количества соединения формулы I или его фармацевтически приемлемой соли либо сольвата нуждающемуся в таком лечении, предупреждении или ослаблении млекопитающему. В другом аспекте настоящее изобретение включает способ модуляции активности опиоидного рецептора, заключающийся в экспозиции рецептора с эффективным количеством по меньшей мере одного соединения формулы I или его фармацевтически приемлемой соли или сольвата. В другом аспекте настоящее изобретение включает применение соединения формулы I или его фармацевтически приемлемой соли либо сольвата для приготовления лекарственного препарата для лечения,предупреждения или ослабления боли (например, хронической боли, невропатической боли, боли при воспалении, боли при хирургическом вмешательстве или острой боли) у млекопитающего или для лечения, предупреждения или ослабления диареи у млекопитающего. В другом аспекте настоящее изобретение включает меченные радиоизотопами соединения формулы I и применение таких соединений или их фармацевтически приемлемых солей или сольватов в качестве радиолигандов для связывания с опиоидным рецептором. Используя такие меченные радиоактивными изотопами (например, меченные 3 Н, 11C или 14 С) соединения, настоящее изобретение включает,помимо этого, способ скрининга на предполагаемое соединение-кандидат по способности связываться с опиоидным рецептором. Этот способ включает: а) введение фиксированной концентрации радиомеченного соединения в рецептор в условиях, способствующих связыванию радиомеченного соединения с рецептором с образованием комплекса; б) титрование комплекса соединением-кандидатом и в) определение связывания соединения-кандидата с указанным рецептором. Дополнительные варианты и преимущества изобретения частично представлены в нижеприведнном описании и вытекают из описания или их можно узнать при практическом применении изобретения. Варианты изобретения можно осуществить, а преимуществ изобретения можно достичь с помощью элементов и комбинаций, особо указанных в прилагаемой "Формуле изобретения". Следует принять к сведению, что как вышеописанная сущность изобретения, так и представленное ниже подробное описание даны только в качестве иллюстрации и пояснения и не ограничивают изобретение в соответствии с "Формулой изобретения". Подробное описание изобретения Настоящее изобретение включает соединения формулы I по определению ниже и их фармацевтически приемлемые соли или сольваты, причм эти соединения применимы в качестве агонистов опиоидных рецепторов. Предполагается, что соединения формулы I и их фармацевтически приемлемые соли или сольваты селективно активируют -опиоидные рецепторы и, следовательно, применимы для лечения,предупреждения или ослабления интенсивности расстройств, восприимчивых к селективной активации-опиоидных рецепторов. Таким образом, настоящее изобретение включает соединения, представленные формулой IR1 обозначает Н или галоген либо -O-C1-6 алкил;R5 обозначает Н, С 1-6 алкил, -С(=О)NHC1-6 алкил, -С(=О)N(С 1-6 алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1 пиперидинилкарбонила и N-метилпиперазинилкарбонила; и его фармацевтически приемлемые соли и сольваты. В другом варианте изобретения R1 обозначает Н или галоген. В другом варианте изобретения R2 обозначает -C(=O)C1-6 алкил. Примеры таких заместителей включают карбонилметил, карбонилэтил, карбонилпропил, карбонилбутил и карбонилпентил, карбонилгексил. В другом варианте изобретения R2 обозначает -С(=О)С 2-6 алкенил или С(=О)С 2-6 алкинил. В другом варианте изобретения m обозначает 1, 2 или 3. Применимые соединения по настоящему изобретению включаютN-(1-(4-оксо-3,3-дифенил-4-(пирролидин-1-ил)пиперидин-4-ил-N-фенилпропионамид и их фармацевтически приемлемые соли и сольваты. Термин "циклоалкил" по данному описанию относится к группе, выбранной из С 3-С 12 циклоалкила,и предпочтительно С 5-С 9 циклоалкила. Типичные циклоалкильные группы включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и циклононил. Термин "гетероциклоалкил" по данному описанию относится к группе, выбранной из насыщенных 3-12-членных моноциклов, которые содержат атомы углерода и от одного до четырх гетероатомов, независимо выбранных из группы, состоящей из О, N и/или S. Примеры гетероциклических систем включают пиперидин, пирролидин, пиперазин, морфолин, имидазолин, пиразолидин, бензодиазепины и т.п. Термин "арил" по данному описанию относится к группе, выбранной из С 6-С 14 арила, в особенности С 6-С 10 арила. Типичные С 6-С 14 арильные группы включают фенильную, нафтильную, фенантр(ен)ильную,антрац(ен)ильную, инденильную, азуленильную, бифенильную, бифениленильную и флуоренильную группы. Термин "гетероарил" по данному описанию относится к группе, содержащей от 5 до 14 атомов в циклическом фрагменте; 6, 10 или 14 общих (делокализованных)электронов в циклическом фрагменте; и содержащей углеродные атомы и 1, 2 или 3 гетероатома, а именно атома кислорода, азота и/или серы. Примеры гетероарильных групп включают тиенил, бензо[b]тиенил, нафта[2,3-b]тиенил, тиантренил, фурил, бензофурил, пиранил, изобензофуранил, бензооксазолил, хроменил, ксантенил, 2H-пирролил, пирролил, имидазолил, пиразолил, пиридил, пиразинил, пиримидинил, пиридазинил, изоиндолил, 3 Ниндолил, индолил, индазолил, пуринил, изохинолил, фталазинил, нафтиридинил, хинолинил, хиназолинил, птеридинил, 4 аН-карбазолил, карбазолил, -карболинил, фенантридинил, акридинил, пиримидинил,фенантролинил, феназинил, тиазолил, изотиазолил, фенотиазолил, изоксазолил, фуразанил и феноксазинил. Термин "галоген" или "галоид" по данному описанию обозначает фтор, хлор, бром или иод."C1-С 6 алкил" по данному описанию выбирают из линейных и разветвлнных нециклических углеводородов, содержащих от 1 до 6 атомов углерода. Типичные линейные С 1-С 6 алкильные группы включают -метил, -этил, -н-пропил, -н-бутил, -н-пентил и -н-гексил. Типичные разветвлнные C1-С 6 алкильные группы включают -изопропил, -втор-бутил, -изобутил, -трет-бутил, -изопентил, -неопентил, 1 метилбутил, 2-метилбутил, 3-метилбутил, 1,1-диметилпропил, 1,2-диметилпропил, 1-метилпентил, 2 метилпентил, 3-метилпентил, 4-метилпентил, 1-этилбутил, 2-этилбутил, 3-этилбутил, 1,1-диметилбутил,1,2-диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил и 3,3-диметилбутил."C2-С 6 алкенил" по данному описанию выбирают из линейных и разветвлнных нециклических углеводородов, содержащих от 2 до 6 атомов углерода и включающих по меньшей мере одну углеродуглеродную двойную связь. Примеры линейных и разветвлнных С 2-С 6 алкенильных групп включают"С 2-С 6 алкинил" по данному описанию выбирают из линейных и разветвлнных нециклических углеводородов, содержащих от 2 до 6 атомов углерода и включающих по меньшей мере одну углеродуглеродную тройную связь. Примеры линейных и разветвлнных C2-С 6 алкинильных групп включают-ацетиленил, -пропинил, -1-бутинил, -2-бутинил, -1-пентинил, -2-пентинил, -3-метил-1-бутинил, -4 пентинил, -1-гексинил, -2-гексинил и 5-гексинил. Термин "амино" или "аминогруппа" по данному описанию относится к -NH2. Применимые алкиламинокарбонильные группы включают N-метиламинокарбонил, Nэтиламинокарбонил, N-пропиламинокарбонил, N-бутиламинокарбонил, N-пентиламинокарбонил, Nгексиламинокарбонил и N-октиламинокарбонил. Применимые диалкиламинокарбонильные группы включают N,N-диметиламинокарбонил, N,N-3 017471 диэтиламинокарбонил, N,N-дипропиламинокарбонил и N-этил-N-метиламинокарбонил. Применимые циклоаминокарбонильные группы включают 1-азиридинилкарбонил,1 азетидинилкарбонил, 1-пирролидинилкарбонил, 1-пиперидинилкарбонил и N-метилпиперазинилкарбонил. Выражение "необязательно замещнный" по данному описанию относится к группе, которая является незамещнной или замещнной, содержащей один или более заместителей. Например, если группы С 1-С 6 алкил, С 2-С 6 алкенил, С 2-С 6 алкинил, -О-С 1-С 6 алкил, -О-С 2-С 6 алкенил и -О-С 2-С 6 алкинил описываются как необязательно замещнные, то они могут быть или не быть замещнными. Будучи замещнными, они могут иметь в качестве заместителя группу, выбранную из следующих групп: галоген, галоген(C1-6)алкил, галоген 2(С 1-6)алкил, галоген 3(С 1-6)алкил, арил, гетероарил, циклоалкил, гетероциклоалкил,C1-6 алкил, С 2-6 алкенил, С 2-6 алкинил, арил(С 1-6)алкил, арил(С 2-6)алкенил, арил(С 2-6)алкинил, циклоалкил(С 1-6)алкил, гетероцикло(С 1-6)алкил, гидрокси(С 1-6)алкил, амино(С 1-6)алкил, карбокси(С 1-6)алкил, алкокси(С 1-6)алкил, нитро, амино, уреидо, циано, алкилкарбониламино, гидроксил, тиол, алкилкарбонилокси, азидо, алкокси, карбокси, аминокарбонил и C1-6 алкилтиол. Предпочтительные необязательные заместители включают галоген, галоген(С 1-6)алкил, галоген 2(С 1-6)алкил, галоген 3(С 1-6)алкил, гидрокси(С 1-6)алкил, амино(С 1-6)алкил, гидроксил, нитро, C1-6 алкил, C1-6 алкокси и амино. Предпочтительное число необязательных заместителей составляет 1, 2 или 3. Изобретение по данному описанию охватывает также меченные изотопами (т.е. "радиомеченные",меченные радиоактивной меткой) соединения формулы I. Примеры изотопов, которые можно вводить в раскрываемые соединения, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2 Н, 3 Н, 11 С, 13 С, 14 С, 15N, 18 О, 17 О, 31 Р, 32 Р, 35S, 18F и 36Cl соответственно и предпочтительно 3 Н, 11 С и 14 С. Меченные изотопами (т.е. "радиомеченные", меченные радиоактивной меткой) соединения по настоящему изобретению можно получать методами, известными в уровне техники. Например,тритийсодержащие соединения формулы I можно получать, вводя тритий в конкретное соединение формулы I, например, каталитическим дегалогенированием в присутствии трития. Этот метод может включать реакцию соответствующего галогензамещнного предшественника соединения формулы I с газообразным тритием в присутствии подходящего катализатора, например Pd/C, в присутствии или в отсутствие основания. Другие подходящие методы получения тритийсодержащих соединений можно найти вFiler, Isotopes in the Physical and Biomedical Sciences, vol. 1, Labeled Compounds (Part A), Chapter 6 (1987). Соединения, меченные 14 С, можно получать из исходных, содержащих углерод 14 С. Настоящее изобретение относится также к применению меченных радиоактивной меткой соединений формулы I, а также их фармацевтически приемлемых солей и сольватов в качестве радиолигандов для их сайта связывания на опиоидном рецепторе. Меченное радиоактивной меткой соединение формулы I можно применять для того, чтобы охарактеризовать специфическое рецепторное связывание тестируемого соединения или соединения-кандидата. Такие анализы связывания соединений с радиоактивной меткой могут явиться альтернативой испытанию на животных для определения соотношения структураактивность. В неограничивающем варианте настоящее изобретение охватывает метод скрининга соединения-кандидата на способность связываться с опиоидным рецептором, включающий: а) добавление(введение) к рецептору соединения с радиоактивной меткой в фиксированной концентрации в условиях,способствующих связыванию соединения с радиоактивной меткой с рецептором с образованием комплекса; б) титрование комплекса с помощью соединения-кандидата и в) определение связывания соединения-кандидата с указанным рецептором. Некоторые соединения, раскрываемые в данном описании, могут содержать один или более асимметрических центров и, следовательно, могут приводить к получению энантиомеров, диастереомеров и других стереоизомерных форм. Предполагается, что настоящее изобретение охватывает все возможные такие формы, а также их рацемические и разрешнные (разделнные) формы и их смеси, и их применение. Индивидуальные энантиомеры можно разделять методами, известными рядовым специалистам в данной области техники, с учтом настоящего раскрытия. Если соединения по данному описанию содержат олефиновые (ненасыщенные) двойные связи или другие центры геометрической асимметрии, и если не указано иначе, то предполагается, что они включаю Е и Z геометрические изомеры. Предполагается, что данное изобретение также охватывает все таутомеры. Термин "стереоизомер" по данному описанию является общим термином для всех изомеров индивидуальных молекул, которые отличаются только ориентацией их атомов в пространстве. Он включает энантиомеры и изомеры соединений, имеющих более одного хирального центра, которые не являются зеркальными изображениями друг друга (диастереомерами). Термин "хиральный центр" относится к углеродному атому, с которым связаны четыре различные группы. Термины "энантиомер" и "энантиомерный" относятся к молекуле, которую нельзя наложить на сво зеркальное изображение и поэтому является оптически активной, причм энантиомер вращает плоскость поляризованного света в одном направлении, а соединение, являющееся его зеркальным изображением,вращает плоскость поляризованного света в противоположном направлении. Термин "рацемический" относится к смеси равных частей энантиомеров, и эта смесь является опти-4 017471 чески неактивной. Термин "разрешение" относится к разделению, или к концентрации, или к истощению одной из двух энантиомерных форм молекулы. Изобретение по данному описанию охватывает также все соли раскрываемых соединений. В одном варианте настоящее изобретение включает все без исключения нетоксические фармацевтически приемлемые соли раскрываемых соединений. Примеры фармацевтически приемлемых солей включают соли присоединения неорганических и органических кислот и основные соли. Фармацевтически приемлемые соли включают, но без ограничения, соли (щелочных) металлов, такие как натриевая соль, калиевая соль,цезиевая соль и т.п.; соли щелочно-земельных металлов, такие как кальциевая соль, магниевая соль и т.п.; соли органических аминов, такие как соль триэтиламина, соль пиридина, соль пиколина, соль этаноламина, соль триэтаноламина, соль дициклогексиламина, соль N,N'-дибензилэтилидендиамина и т.п.; соли неорганических кислот, такие как гидрохлорид, гидробромид, фосфат, сульфат и т.п.; соли органических кислот, такие как цитрат, лактат, тартрат, малеат, фумарат, манделат (соль миндальной кислоты),ацетат, дихлорацетат, трифторацетат, оксалат, формиат и т.п.; сульфонаты, такие как метансульфонат,бензолсульфонат, п-толуолсульфонат и т.п.; и соли аминокислот, такие как аргинат, глутамат и т.п. Соли присоединения кислоты можно получать, смешивая раствор конкретного соединения по настоящему изобретению с раствором фармацевтически приемлемой нетоксической кислоты, такой как соляная кислота, фумаровая кислота, малеиновая кислота, янтарная кислота, уксусная кислота, лимонная кислота, винная кислота, карбоновая кислота, фосфорная кислота, щавелевая кислота, дихлоруксусная кислота и т.п. Основные соли можно получать, перемешивая раствор конкретного соединения по настоящему изобретению и фармацевтически приемлемого нетоксического основания, такого как гидроксид натрия, гидроксид калия, холин, карбонат натрия и т.п. Изобретение по данному описанию охватывает также сольваты раскрываемых соединений. Одним из типов сольвата является гидрат. Сольваты обычно не оказывают заметного влияния на физиологическую активность или токсичность соединений и в силу этого могут вести себя как фармакологические эквиваленты. Так как соединения формулы I могут применяться в качестве агонистов опиоидных рецепторов, то с помощью этих соединений можно лечить ряд заболеваний и состояний, опосредуемых активацией опиоидных рецепторов. Поэтому настоящее изобретение включает способ лечения, предупреждения или ослабления боли (например, хронической боли, невропатической боли, боли при воспалении, боли при хирургическом вмешательстве или острой боли) или диареи у млекопитающего. В одном варианте изобретение включает способ лечения боли. В другом варианте изобретения тип боли представляет собой хроническую боль. В другом варианте изобретения тип боли представляет собой хроническую невропатическую боль. В другом варианте изобретения тип боли представляет собой хроническую боль при воспалении. В другом варианте изобретения тип боли представляет собой боль, вызванную хирургическим вмешательством. В другом варианте изобретения тип боли представляет собой острую боль. В каждом случае такой метод лечения, предупреждения или ослабления интенсивности требует введения млекопитающему, нуждающемуся в таком лечении, предупреждении или ослаблении интенсивности, некоторого количества соединения по настоящему изобретению, терапевтически эффективного для достижения заданного результата (а именно лечения, предупреждения или ослабления интенсивности). В одном варианте изобретения количество такого соединения представляет собой количество, эффективное для активации опиоидных рецепторов in vivo. Хроническая боль включает, но без ограничения, боль, вызванную воспалением, послеоперационную боль, боль при раковом заболевании, боль при остеоартрите, невралгию тройничного нерва, диабетическую нейропатию, острую герпетическую и постгерпетическую невралгию, каузалгию, авульсию плечевого сплетения, затылочную невралгию, симпатическую рефлекторную дистрофию, фибромиалгию, подагру, фантомную боль в конечностях, боль при ожоге и другие формы невралгии, невропатических и идиопатеческих болевых синдромов. Хроническая соматическая боль обычно возникает в результате воспалительных реакций на поражение тканей, такое как ущемление нерва, хирургические процедуры, рак или артрит (Brower, NatureBiotechnology 2000; 18: 387-391). Воспалительный процесс представляет собой сложную последовательность биохимических и клеточных событий, активируемую в ответ на поражение ткани или присутствие чужеродных вещества (Levine, Inflammatory Pain; В: Textbook of Pain, Wall and Melzack eds., 3rd ed., 1994). Воспаление часто возникает в месте поврежднной ткани или чужеродного материала и способствует процессу восстановления и заживления ткани. Основные признаки воспаления включают эритему (покраснение), повышение температуры, эдему (отк), боль и утрату функции. Большинство пациентов, испытывающих боль, вызванную воспалением, чувствуют ее не постоянно, а скорее испытывают более сильную боль, когда воспалнный участок смещается или когда его трогают. Боль, вызванная воспалением, включает, но без ограничения,остеоартрит и ревматоидный артрит. Хроническая невропатическая боль является гетерогенным болезненным состоянием неясного происхождения. При хронической невропатической боли боль может быть обусловлена участием различных-5 017471 механизмов. Этот тип боли обычно возникает при поражении ткани периферической или центральной нервной системы. Синдромы включают боль, обусловленную повреждением спинного мозга, рассеянным склерозом, постгерпетической невралгией, невралгией тройничного нерва (тригеминальной невралгией), фантомную боль, каузалгию и симпатическую рефлекторную дистрофию и боль в нижнем отделе спины. Хроническая боль отличается от острой боли тем, что пациенты с хронической невропатической болью испытывают аномальные болевые ощущения, которые можно описать как спонтанную боль, хронический поверхностный ожог и/или как сильную ноющую боль. Боль может быть вызвана температурной (тепловой), холодовой и механической гипералгезией или температурной (тепловой), холодовой и механической аллодинией. Хроническая невропатическая боль может быть вызвана поражением или инфекцией периферических сенсорных нервов. Она включает, но без ограничения, боль, вызванную травмой периферического нерва, герпес-вирусной инфекцией, сахарным диабетом, каузалгией, авульсией сплетения, невромой,ампутацией конечности и васкулитом. Невропатическая боль может также быть вызвана поражением нерва в результате хронического алкоголизма, инфицирования вирусом иммунодефицита человека, гипотиреоза, уремии или витаминной недостаточности. Нарушение кровообращения (головного или спинного мозга) и поражение позвоночника может также вызывать невропатическую боль. Невропатическая боль, вызванная раковым заболеванием, возникает в результате сжатия растущей опухолью прилегающих нервов, мозга или позвоночника. Кроме того, терапия рака, включая химиотерапию и лучевую терапию, может вызывать поражение нервов. Невропатическая боль включает, но без ограничения, боль, вызванную поражением нервов, например, такую как боль, которой страдают диабетики. Острая боль представляет собой любую боль, которая длится менее 3 месяцев подряд, и включает,но без ограничения, боль, испытываемую в результате хирургического вмешательства, при небольших порезах, растяжении связок голеностопного сустава, небольшом ожоге или при ударе о предмет. В более общем смысле настоящее изобретение относится также к способу лечения расстройства,которое можно лечить путм активации опиоидных рецепторов и, в частности, селективной активации опиоидных рецепторов, у животных, страдающих указанным расстройством, причм указанный способ заключается во введении животному некоторого количества соединения формулы I или его фармацевтически приемлемой соли либо сольвата, которые могут активировать опиоидные рецепторы, и, более конкретно, которые могут активировать -опиоидные рецепторы. Полагают, что соединение формулы I селективно к активации -опиоидных рецепторов, если Ki (константа ингибирования) для -опиоидных рецепторов (по определению в in vitro анализах, аналогичных анализам, описанным ниже) ниже, чем Ki для - и -опиоидных рецепторов. В одном варианте изобретения соединения формулы I имеют Ki для и -опиоидных рецепторов, которая по меньшей мере примерно в 5 выше, чем в случае -опиоидных рецепторов. В другом варианте изобретения соединения формулы I имеют Ki для - и -опиоидных рецепторов, которая по меньшей мере примерно в 10 выше, чем в случае -опиоидных рецепторов. В другом варианте изобретения соединения формулы I имеют Ki для - и -опиоидных рецепторов, которая по меньшей мере примерно в 100 выше, чем в случае -опиоидных рецепторов. В другом варианте изобретения соединения формулы I имеют Ki для - и -опиоидных рецепторов, которая по меньшей мере примерно в 500 выше, чем в случае -опиоидных рецепторов. В другом варианте изобретения соединения формулы I имеют Ki для - и -опиоидных рецепторов, которая по меньшей мере примерно в 1000 выше, чем в случае -опиоидных рецепторов. В другом варианте изобретения соединения формулы I имеютKi для - и -опиоидных рецепторов, которая по меньшей мере примерно в 10000 выше, чем в случае опиоидных рецепторов. Настоящее изобретение включает также применение соединения формулы I или его фармацевтически приемлемой соли либо сольвата, для получения лекарственного препарата для лечения расстройства,которое можно лечить путм активации опиоидных рецепторов у животного, страдающего указанным расстройством. В одном варианте изобретения расстройство можно лечить селективной активацией опиоидных рецепторов. В другом варианте изобретения расстройство представляет собой боль или диарею. Синтез соединений. Соединения по настоящему изобретению можно получать методами, известными специалистам в данной области техники, с учтом данного раскрытия. Например, соединения формулы I, где А обозначает фенил, R1 обозначает Н, R2 обозначает МеСН 2 СО, В обозначает CH2, R3 и R4, каждый, обозначают фенил, a R5 обозначает Н, CN, CONMe2 или CON(CH2)4, можно получать, как показано на схеме. где W обозначает CR3R4 и каждый Z обозначает (С 1-С 4 алкильную) группу. Тестирование соединений. In vitro анализы связывания -опиоидных рецепторов. Методика проведения анализов связывания -опиоидных рецепторов. В анализах связывания -опиоидных рецепторов с замещением дозы радиолиганда используют 0.2 нМ [3 Н]-дипренорфина (NEN, Boston, Mass.) с 5-20 мг мембранного белка/лунка в конечном объме 500 мкл связывающего буфера (10 мМ MgCl2, 1 мМ EDTA, 5% DMSO, 50 мМ HEPES, рН 7.4). Реакции проводят в отсутствие или в присутствии увеличивающихся концентраций немеченого налоксона. Все реакции проводят в 96-глубоколуночных полипропиленовых планшетах в течение 1-2 ч при комнатной температуре. Реакции связывания прекращают быстрой фильтрацией с помощью 96-луночных фильтрпланшетов Unifilter GF/C (Packard, Meriden, Conn.), предварительно смоченных 0.5% раствором полиэтиленимина, используя 96-луночный харвестер для тканей (Brandel, Gaithersburg, Md.), с последующей трхкратной фильтрационной промывкой с применением 500 мкл ледяного связывающего буфера. Затем фильтр-планшеты сушат при 50 С в течение 2-3 ч. Добавляют сцинтилляционный коктейль BetaScint(Wallac, Turku, Finland) (50 мкл/лунка) и планшеты считают с помощью Packard Top-Count со скоростью 1 мин/лунка. Данные анализируют, используя функции для построения односайтовой конкурентной кривой в GraphPad PRISM v. 3.0 (San Diego, Calif.) или собственную функцию для построения односайтовой конкурентной кривой. Результаты связывания -опиоидного рецептора. Обычно чем ниже значение Ki, тем более эффективно фенилпропионамидные соединения лечат боль или диарею. Как правило, значение Ki (нМ) фенилпропионамидных соединений равно примерно 300 или ниже для связывания с -опиоидными рецепторами. В одном варианте изобретения фенилпропионамидные соединения имеют Ki (нМ) около 100 или ниже. В одном варианте изобретения фенилпропионамидные соединения имеют Ki (нМ) около 50 или ниже. В одном варианте изобретения фенилпропионамидные соединения имеют Ki (нМ) около 20 или ниже. В другом варианте фенилпропионамидные соединения по настоящему изобретению имеют Ki (нМ) около 10 или ниже. Ещ в одном варианте фенилпропионамидные соединения по настоящему изобретению имеют Ki (нМ) около 1 или ниже. Ещ в одном варианте фенилпропионамидные соединения по настоящему изобретению имеют Ki (нМ) около 0.1 или ниже. N-(1-(4-Оксо-3,3-дифенил-4-(пирролидин-1-ил)пиперидин-4-ил-N-фенилпропионамид,типичное фенилпропионамидное соединение, имеет значение Ki (нМ) 19.17 для связывания с опиоидными рецепторами.In vitro анализ связывания ORL-1 рецептора. Методика анализа связывания ORL-1 рецептора. Мембраны рекомбинантных HEK-293 клеток, экспрессирующих рецептор, подобный человеческому опиоидному рецептору (ORL-1) (Receptor Biology), получают, лизируя клетки в ледяном гипотоническом буфере (2.5 мМ MgCl2, 50 мМ HEPES, рН 7.4) (10 мл/10 см плашка), с последующей гомогенизацией с помощью измельчителя тканей (гомогенизатора)/тефлонового пестика. Мембраны собирают центрифугированием при 30000g в течение 15 мин при 4 С и пеллеты (осадок) ресуспендируют в гипотоническом буфере до конечной концентрации 1-3 мг/мл. Концентрации белка определяют, используя реагент для анализа белка BioRad и альбумин бычьей сыворотки в качестве стандарта. Аликвоты ORL-1 рецепторных мембран хранят при -80 С. В анализах связывания радиолигандов (скрининг и замещение дозы) используют 0.1 нМ [3 Н]ноцицептина (NEN; 87.7 Ки/ммоль) с 10-20 мкг мембранного белка в конечном объме 500 мкл связывающего буфера (10 мМ MgCl2, 1 мМ EDTA, 5% DMSO, 50 мМ HEPES, рН 7.4). Неспецифическое связывание определяют в присутствии 10 нМ немеченого ноцицептина (American Peptide Company). Все реакции проводят в 96-глубоколуночных полипропиленовых планшетах в течение 1 ч при комнатной температуре. Реакции связывания прекращают быстрой фильтрацией с помощью 96-луночных фильтрпланшетов Unifilter GF/C (Packard), предварительно смоченных 0.5% раствором полиэтиленимина(Sigma). Сбор осуществляют, используя 96-луночный харвестер тканей (Packard), с последующей трхкратной фильтрационной промывкой с помощью 500 мкл ледяного связывающего буфера. Затем фильтрпланшеты сушат при 50 С в течение 2-3 ч. Добавляют сцинтилляционный коктейль (BetaScint; Wallac)(50 мкл/лунка) и планшеты считают с помощью Packard Top-Count со скоростью 1 мин/лунка. Результаты экспериментов по скринингу и замещению дозы анализируют, используя Microsoft Excel и функции для построения кривой в GraphPad PRISM v. 3.0 соответственно или собственную функцию для построения односайтовой конкурентной кривой. Результаты связывания ORL-1 рецептора. Как правило, значение Ki (нМ) фенилпропионамидных соединений равно примерно 300 или ниже для связывания с ORL-1 рецепторами. В одном варианте изобретения фенилпропионамидные соединения имеют Ki (нМ) около 100 или ниже. В одном варианте изобретения фенилпропионамидные соединения имеют Ki (нМ) около 50 или ниже. В одном варианте изобретения фенилпропионамидные соединения имеют Ki (нМ) около 20 или ниже. В другом варианте фенилпропионамидные соединения по настоящему изобретению имеют Ki (нМ) около 10 или ниже. Ещ в одном варианте фенилпропионамидные соединения по настоящему изобретению имеют Ki (нМ) около 1 или ниже. Ещ в одном варианте фенилпропионамидные соединения по настоящему изобретению имеют Ki (нМ) около 0.1 или ниже.In vitro функциональные анализы -опиоидных рецепторов. Методика функциональных анализов -опиоидных рецепторов. Функциональные анализы [35S]GTPS проводят, используя свежеоттаявшие -рецепторные мембраны. Реакционные смеси для анализов готовят, последовательно добавляя к связывающему буферу(100 мМ NaCl, 10 мМ MgCl2, 20 мМ HEPES, рН 7.4) на льду следующие реагенты (указаны конечные концентрации): мембранный белок (0.026 мг/мл), сапонин (10 мг/мл), ГДФ (GDP, 3 мМ) и [35S]GTPS(0.20 нМ; NEN). Приготовленный раствор мембран (190 мкл/лунка) переносят в 96-луночный полипропиленовый планшет с мелкими лунками, содержащий 10 мкл с концентрацией 20 исходного раствора агониста DAMGO, приготовленного в диметилсульфоксиде (DMSO). Планшеты инкубируют в течение 30 мин при комнатной температуре при встряхивании. Реакции прекращают быстрой фильтрацией с помощью 96-луночных фильтр-планшетов Unifilter GF/C (Packard, Meriden, Conn.), используя 96-луночный харвестер для тканей (Brandel, Gaithersburg, Md.), с последующей трхкратной фильтрационной промывкой с применением 200 мкл ледяного буфера для промывки (10 мМ NaH2PO4, 10 мМ Na2HPO4, рН 7.4). Затем фильтр-планшеты сушат при 50 С в течение 2-3 ч. Добавляют сцинтилляционный коктейль BetaScint (Wallac, Turku, Finland) (50 мкл/лунка) и планшеты считают с помощью Packard Top-Count со скоростью 1 мин/лунка. Данные анализируют, используя функции для построения сигмоидальной кривой зависимости эффекта от дозы в GraphPad PRISM v. 3.0 (San Diego, Calif.) или собственную функцию для построения нелинейной сигмоидальной кривой зависимости эффекта от дозы. Результаты функционального анализа -опиоидного рецептора.GTP EC50 обозначает концентрацию соединения, обеспечивающую 50% максимального отклика на соединение у -опиоидного рецептора. Фенилпропионамидные соединения, имеющие, как правило,GTP EC50 (нМ) около 5000 или менее, стимулируют рецепторную функцию -опиодного рецептора. В одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 1000 или менее. В одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 500 или менее. В одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 200 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 100 или менее. В одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 60 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 10 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 1 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеютGTP EC50 (нМ) около 0.1 или менее.GTP Emax % обозначает максимальный эффект, выявляемый соединением, по сравнению с эффектом, выявляемым [D-Ala2, N-метил-Phe4 Gly-ол 5]энкефалином (DAMGO), стандартнымагонистом. Обычно величинаGTP Emax (%) показывает эффективность соединения в лечении и предупреждении боли или диареи. Как правило, фенилпропионамидные соединения по данному изобретению имеютGTP Emax (%) более 50%. В одном варианте изобретения фенилпропионамидные соединения по данному изобретению имеютGTP Emax более 75%. Ещ в одном варианте изобретения фенилпропионамидные соединения по данному изобретению имеютGTP Emax более 88%. Ещ в одном варианте изобретения фенилпропионамидные соединения по данному изобретению имеютGTP Emax более 100%.In vitro функциональный анализ ORL-1 рецептора. Методика анализа [35]GTPS связывания ORL-1 рецептора. Мембраны рекомбинантных HEK-293 клеток, экспрессирующих рецептор, подобный человеческому опиоидному рецептору (ORL-1) (Receptor Biology), получают, лизируя клетки в ледяном гипотониче-8 017471 ском буфере (2.5 мМ MgCl2, 50 мМ HEPES, рН 7.4) (10 мл/10 см плашка), с последующей гомогенизацией с помощью измельчителя тканей (гомогенизатора)/тефлонового пестика. Мембраны собирают центрифугированием при 30000g в течение 15 мин при 4 С и пеллеты (осадок) ресуспендируют в гипотоническом буфере до конечной концентрации 1-3 мг/мл. Концентрации белка определяют, используя реагент для анализа белка BioRad и альбумин бычьей сыворотки в качестве стандарта. Аликвоты ORL-1 рецепторных мембран хранят при -80 С. Анализы функционального связывания. Раствор ORL-1 мембран готовят, последовательно добавляя конечные концентрации 0.066 мкг/мклORL-1 мембранного белка, 10 нг/мл сапонина, 3 мкМ GDP и 0.20 нМ [35S]GTPS к связывающему буферу (100 мМ NaCl, 10 мМ MgCl2, 20 мМ HEPES, рН 7.4) на льду. Полученный раствор мембран (190 мкл/лунка) переносят в 96-луночные полипропиленовые планшеты с мелкими лунками, содержащие 10 мкл с концентрацией 20 исходного раствора агониста/ноцицептина, приготовленного в DMSO. Планшеты инкубируют в течение 30 мин при комнатной температуре при встряхивании. Реакции прекращают быстрой фильтрацией на 96-луночных фильтр-планшетах Unifilter GF/C (Packard), используя 96 луночный харвестер для тканей (Packard), с последующей трхкратной фильтрационной промывкой с применением 200 мкл ледяного буфера для промывки (10 мМ NaH2PO4, 10 мМ Na2HPO4, pH 7.4). Затем фильтр-планшеты сушат при 50 С в течение 2-3 ч. Добавляют сцинтилляционный коктейль (BetaScint;Wallac) (50 мкл/лунка) и планшеты считают на Packard Top-Count со скоростью 1 мин/лунка. Данные анализируют, используя функции для построения сигмоидальной кривой зависимости эффекта от дозы вGraphPad PRISM v. 3.0 или собственную функцию для построения нелинейной сигмоидальной кривой зависимости эффекта от дозы. Результаты функционального анализа ORL-1 рецептора.ORL-1 GTP EC50 обозначает концентрацию соединения, обеспечивающую 50% максимального отклика на соединение у ORL-1 рецептора. Фенилпропионамидные соединения, имеющие, как правило,ORL-1 GTP EC50 (нМ) около 5000 или менее, стимулируют ORL-1 рецепторную функцию. В одном варианте фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP EC50 (нМ) около 1000 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP EC50 (нМ) около 100 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP EC50 (нМ) около 10 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP EC50 (нМ) около 1 или менее. Ещ в одном варианте фенилпропионамидные соединения по данному изобретению имеют ORL-1ORL-1 GTP Emax % обозначает максимальный эффект, выявляемый соединением, по сравнению с эффектом, выявляемым ноцицептином, стандартным агонистом ORL-1. Как правило, фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP Emax (%) более 50%. В одном варианте изобретения фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP Emax более 88%. Ещ в одном варианте изобретения фенилпропионамидные соединения по данному изобретению имеют ORL-1 GTP Emax более 100%.In vivo фармакология. Соединения по настоящему изобретению можно проверять на их антиноцицептиновую активность на модели формалина, которая описана S. Hunskaar, О.В. Fasmer and K. Hole, J. Neurosci Methods. 14: 6976 (1985). Во всех экспериментах можно использовать самцов мышей Swiss Webster NIH (20-30 г; Harlan,San Diego, CA). В день эксперимента пищу отбирают. Мышей помещают в камеры из плексигласа по меньшей мере на 1 ч, чтобы они привыкли к обстановке. После периода акклиматизации мышей взвешивают и дают либо соединение по изобретению и.п. или п.о., или соответствующий объм носителя (10% Твин-80) в качестве контроля. Через 15 мин после введения и.п. дозы и через 30 мин после введения п.о. дозы мышам инъецируют формалин (20 мкл 5% раствора формальдегида в физиологическом солевом растворе) в дорсальную область правой задней лапы. Мышей переносят в камеры из плексигласа и контролируют время, в течение которого мыши лижут и кусают лапу после инъекции. Периоды лизания и укусов регистрируют с 5-минутными интервалами в течение 1 ч после инъекции формалина. Все эксперименты делают слепым методом в течение светового цикла. Раннюю фазу реакции на формалин определяют как лизание/укусы через 0-5 мин, а позднюю фазу определяют через 15-50 мин после инъекции формалина. Разницу между группами, получавшими носитель и лекарство, можно анализировать с помощью однофакторного дисперсионного анализа (ANOVA). Величину р 0.05 полагают значимой. Соединения считаются эффективными для лечения острой и хронической боли, если они активно блокируют как раннюю, так и вторую фазу вызванной формалином активности лизания лапы. Соединения можно проверять на их способность лечить хроническую боль (т.е. их антиаллодиническую и антигипертензивную активность), используя модель периферической нейропатии Чанга (Chung)(Kim and Chung, Pain 50: 355-363 (1992. Самцов крыс Sprague-Dawley весом 200-225 г анестезируют галотаном (1-3% в смеси 70% воздуха и 30% кислорода) и контролируют температуру их тела под наркозом, используя гомеотермическое одеяло. Затем делают дорсальный медиальный разрез 2 см в области-9 017471 спинно-мозговых нервов L5 и L6 и группу околопозвоночных мышц оттягивают назад с двух сторон. Затем спинно-мозговые нервы L5 и L6 обнажают, изолируют и крепко перевязывают шлковой нитью 60 или 7-0. Имитацию операции проводят, обнажая спинно-мозговые нервы L5 и L6 на противоположной стороне, без перевязывания, в качестве негативного контроля. Тактильная аллодиния. Чувствительность к нетоксическим механическим раздражителям можно измерять у животных для оценки тактильной аллодинии. Крыс переносят в приподнятую клетку для испытаний с полом из проволочной сетки и оставляют для акклиматизации на 5-10 мин. Ряд хирургических мононитей фон Фрая(von Frey) прикладывают (помещают) к подошве задней лапы, чтобы определить порог отдргивания животного. Первая используемая нить деформируется при весе 9.1 г (величина log 0.96) и прикладывается до пяти раз, чтобы посмотреть, действительно ли она выявляет реакцию отдргивания. Если у животного наблюдается реакция отдргивания, тогда следующую наиболее лгкую (тонкую) в ряду нить прикладывают до пяти раз, чтобы проверить, может ли она вызвать реакцию. Эту процедуру повторяют с последующими меньшими нитями до тех пор, пока реакция не перестанет наблюдаться и регистрируют характеристики наиболее лгкой нити, которая выявляет реакцию. Если животное не проявляет реакции отдргивания от начальной нити 9.1 г, тогда последующие нити берут с повышенным весом до тех пор,пока нить выявляет реакцию, и характеристики этой нити регистрируют. Для каждого животного в каждой временной точке делают три определения, чтобы получить среднее пороговое значение отдргивания. Испытания проводят до и через 1, 2, 4 и 24 ч после введения лекарства. Механическая гипералгезия. Чувствительность к вредным механическим раздражителям можно определять у животных, используя тест давления на лапу для оценки механической гипералгезии. У крыс пороговые значения отдргивания задней лапы ("PWT"), измеряемые в граммах, в ответ на вредные механические раздражители определяют, используя анальгезиметр (модель 7200 фирмы Ugo Basile of Italy), описанный в Stein (BiochemistryBehavior 31: 451-455 (1988. Лапу крысы помещают на малую платформу (небольшой столик) и прилагаемый вес постепенно увеличивают до максимального веса 250 г. За конечную точку бертся вес, при котором лапа целиком отдргивается. PWT определяют один раз для каждой крысы в каждой временной точке. PWT можно измерять только на непоражнной лапе или как на поражнной, так и на непоражнной лапе. В одном неограничивающем варианте изобретения на крысах можно определять механическую гипералгезию, ассоциированную с болью, индуцированной поражением нерва (невропатическая боль). Крыс тестируют перед хирургическим вмешательством для определения базовых, или нормальных, значений PWT. Крыс проверяют снова через 2-3 недели после хирургического вмешательства, до, и в различное время после (например, через 1, 3, 5 и 24 ч) после введения лекарства. ПовышениеPWT после введения лекарства показывает, что тестируемое соединение снижает механическую гипералгезию. Фармацевтические композиции. Хотя соединение по настоящему изобретению можно вводить млекопитающему в виде чистого соединения без примеси других компонентов, предпочтительно это соединение вводят как часть фармацевтической композиции, содержащей соединение в смеси с подходящим фармацевтически приемлемым носителем. Такой носитель можно выбрать из фармацевтически приемлемых эксципиентов и вспомогательных веществ. Фармацевтические композиции в объме настоящего изобретения включают все композиции, в которых соединение по настоящему изобретению находится в смеси с фармацевтически приемлемым носителем. В предпочтительном варианте изобретения соединение присутствует в композиции в количестве,эффективном для достижения предполагаемой терапевтической цели. Хотя индивидуальные требования могут варьироваться, определение оптимальных интервалов эффективных количеств каждого соединения находится в компетенции специалиста. Как правило, соединения можно вводить млекопитающему,например человеку, перорально в дозе примерно от 0.0025 примерно до 1500 мг на 1 кг веса тела млекопитающего или эквивалентное количество его фармацевтически приемлемой соли или сольвата в день для лечения, предупреждения или ослабления конкретного расстройства. Применимая пероральная доза соединения по настоящему изобретению, вводимая млекопитающему, составляет примерно от 0.025 примерно до 50 мг на 1 кг веса тела млекопитающего, или эквивалентное количество его фармацевтически приемлемой соли или сольвата. Для внутримышечной инъекции доза обычно составляет около половины пероральной дозы. Унифицированная (стандартная, разовая) пероральная доза содержит примерно от 0.01 примерно до 50 мг и предпочтительно около 0.1-10 мг соединения. Разовую дозу можно вводить один или более раз в сутки, например, в виде одной или более таблеток или капсул, причм каждая из них содержит примерно 0.01-50 мг соединения или эквивалентное количество его фармацевтически приемлемой соли либо сольвата. Фармацевтическую композицию по настоящему изобретению можно вводить любому животному,которое может испытывать благотворное действие соединения по настоящему изобретению. Главными среди таких животных являются млекопитающие, например человек и животные-компаньоны, хотя изо- 10017471 бретение не претендует на такое ограничение. Фармацевтическую композицию по настоящему изобретению можно вводить любым способом, который позволяет достичь предполагаемой цели. Например, вводить можно пероральным, парентеральным, подкожным, внутривенным, внутримышечным, интраперитонеальным, трансдермальным, интраназальным, трансмукозным, ректальным, интравагинальным или трансбуккальным способами или с помощью ингаляции. Вводимая доза и способ введения меняются в зависимости от состояния конкретного субъекта и с учтом таких факторов, как возраст, состояние здоровья и вес реципиента, состояние или расстройство, которое следует лечить, характера одновременно проводимого лечения, если таковое проводится, частоты лечения и характера ожидаемого эффекта. В одном варианте фармацевтическую композицию по настоящему изобретения можно вводить перорально и е готовят в виде таблеток, драже, капсул или перорального жидкого препарата. В одном варианте изобретения пероральный препарат содержит экструдированные макрочастицы, содержащие соединение по изобретению. В другом варианте фармацевтическую композицию по настоящему изобретению готовят для ректального введения, а именно в виде суппозиториев. В другом варианте фармацевтическую композицию по настоящему изобретению готовят для введения в виде инъекции. В другом варианте изобретения композицию по настоящему изобретению готовят для трансдермального введения, например, в виде пэтчей (пластырей). В другом варианте изобретения композицию по настоящему изобретению готовят для введения с помощью ингаляции или с помощью интраназального или трансмукозного введения. В другом варианте изобретения композицию по настоящему изобретению готовят для интравагинального введения. Фармацевтическая композиция по настоящему изобретению может содержать примерно 0.01-99 вес.% и предпочтительно примерно 0.25-75 вес.% активного соединения (активных соединений). Фармацевтическую композицию по настоящему изобретению предпочтительно получают способом, который сам по себе известен, с учтом настоящего раскрытия, например обычным смешиванием,грануляцией, изготовлением драже, растворением, экструзией или лиофилизацией. Так, фармацевтические композиции для перорального применения можно получать смешением активного соединения с тврдыми эксципиентами, необязательным измельчением полученной смеси и обработкой смеси гранул,после добавления подходящих вспомогательных веществ, при желании или при необходимости, получая таблетки или ядра драже. Подходящие эксципиенты включают наполнители, такие как сахариды (например, лактозу, сахарозу, манит или сорбит), препараты целлюлозы, фосфаты кальция (например, трикальцийфосфат или кальция гидрофосфат), а также связующие, такие как крахмальная паста (использующая, например, маисовый(кукурузный) крахмал, пшеничный крахмал, рисовый крахмал или картофельный крахмал), желатин,трагакант, метилцеллюлозу, гидроксипропилметилцеллюлозу, натрий карбоксиметилцеллюлозу и/или поливинилпирролидон. При необходимости можно добавить одно или более веществ, способствующих измельчению, таких как вышеуказанные крахмалы, а также карбоксиметилкрахмал, сшитый поливинилпирролидон, агар или альгиновая кислота или е соль, такая как альгинат натрия. Вспомогательные вещества, как правило, являются агентами, регулирующими текучесть, и смазками, такими как, например, диоксид кремния, тальк, стеариновая кислота или е соли (например, стеарат магния или стеарат кальция) и полиэтиленгликоль. Ядра драже выпускают с подходящими оболочками(покрытиями), резистентными к желудочному соку. Для этой цели можно применять концентрированные растворы сахаридов, которые, необязательно, могут содержать аравийскую камедь, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, растворы лака и подходящие органические растворители или смеси растворителей. Для получения оболочек, резистентных к желудочному соку, можно применять растворы подходящих препаратов целлюлозы, таких как фталат ацетилцеллюлозы или фталат гидроксипропилметилцеллюлозы. В таблетки или оболочки драже можно добавлять красители или пигменты, например, для идентификации или для того, чтобы охарактеризовать комбинации доз активного соединения. Примеры других фармацевтических препаратов, которые можно применять перорально, включают желатиновые капсулы из двух плотно насаженных друг на друга половин (тврдые) или мягкие герметичные капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. Капсулы с плотной посадкой (тврдые желатиновые капсулы) могут содержать соединение в виде гранул, которые могут быть смешаны с наполнителями, такими как лактоза, связующими, такими как крахмалы,и/или смазками, такими как тальк или стеарат магния, и, необязательно, стабилизаторами, или в виде экструдированных макрочастиц. В мягких капсулах активные соединения предпочтительно растворены или суспендированы в подходящих жидкостях, таких как нелетучие жидкие масла или жидкий парафин. Кроме того, могут быть добавлены стабилизаторы. Вероятные фармацевтические препараты для ректального применения включают, например, суппозитории, которые состоят из комбинации одного или более активных соединений с основой для суппози- 11017471 ториев. Подходящие основы для суппозиториев включают, среди прочего, природные или синтетические триглицериды и парафиновые углеводороды. Возможно также использовать желатиновые ректальные капсулы, состоящие из комбинации активного соединения с материалом основы, например, таким как жидкий триглицерид, полиэтиленгликоль или парафиновый углеводород. Подходящие препараты для парентерального введения включают водные растворы активного соединения в водорастворимой форме, например, такой как водорастворимая соль, щелочной раствор или кислый раствор. Или же, суспензию активного соединения можно приготовить в виде масляной суспензии. Подходящие липофильные растворители или носители для такой суспензии могут включать нелетучие жидкие масла (например, кунжутное масло), синтетические эфиры нелетучих жидких кислот (например, этилолеат), триглицериды или полиэтиленгликоль, такой как полиэтиленгликоль-400 (ПЭГ-400). Водная суспензия может содержать одно или более веществ, повышающих вязкость суспензии, включая,например, натрий карбоксиметилцеллюлозу, сорбит и/или декстран. Суспензия может, необязательно,содержать стабилизаторы. В одном варианте фармацевтические композиции по изобретению готовят, включая соединения формулы I в препарат с контролируемым высвобождением, тем самым можно поддерживать равновесные уровни соединения формулы I в плазме. Другим способом, позволяющим получать эти равновесные уровни соединения в плазме, является применение походящих технологий, например препаратов с контролируемым высвобождением, выбранным для того, чтобы обеспечить подходящий профиль высвобождения. Примеры единичных систем доставки включают, но без ограничения, таблетки в восковой матрице (восковые таблетки), таблетки в гидрофильной матрице и таблетки с покрытием с контролируемым высвобождением. Примеры систем с макрочастицами включают, но без ограничения, матричные системы, такие как макрочастицы, экструдированные из расплава (MEM), или системы на основе покрытий с контролируемым высвобождением,такие как гранулы (бусы) с оболочкой (покрытием). В одном варианте фармацевтические композиции по настоящему изобретению обеспечивают терапевтические равновесные уровни соединения формулы I в плазме в течение примерно от 12 до 24 ч после перорального введения. В другом варианте фармацевтические композиции по настоящему изобретению обеспечивают терапевтические равновесные уровни соединения формулы I в плазме в течение примерно от 6 до 12 ч после перорального введения. Способ по настоящему изобретению, такой как способ лечения, предупреждения или ослабления расстройства, которое можно лечить, предупредить или ослабить путм активации опиоидных рецепторов нуждающемуся в этом животному, может дополнительно включать введение нуждающемуся в этом животному второго терапевтического агента в комбинации с соединением по настоящему изобретению. В одном варианте изобретения другой терапевтический агент вводят в эффективном количестве. Эффективные количества других терапевтических агентов, зависящие от свойств другого терапевтического агента, известны специалистам в данной области техники. Однако в компетенции опытного специалиста в данной области техники находится определение оптимальных интервалов эффективных количеств. Соединение по настоящему изобретению (а именно первый терапевтический агент) и второй терапевтический агент могут действовать аддитивно или, в одном варианте изобретения синергично. В одном варианте изобретения соединение по настоящему изобретению вводят одновременно со вторым терапевтическим агентом; например, можно вводить композицию для разового прима, содержащую как эффективное количество соединения формулы I, так и эффективное количество второго терапевтического агента. Соответственно настоящее изобретение включает далее фармацевтическую композицию, содержащую комбинацию соединения по настоящему изобретению, второй терапевтический агент и фармацевтически приемлемый носитель. Или же, можно одновременно вводить первую фармацевтическую композицию, содержащую эффективное количество соединения формулы I, и вторую фармацевтическую композицию, содержащую эффективное количество второго терапевтического соединения. В другом варианте изобретения эффективное количество соединения по настоящему изобретению вводят до или после введения эффективного количества второго терапевтического агента. В данном варианте соединение по настоящему изобретению вводят в то время, как второй терапевтический агент проявляет свой терапевтический эффект, или второй терапевтический агент вводят в то время, когда соединение по настоящему изобретению проявляет свой терапевтический эффект, для лечения, предупреждения или ослабления расстройства или состояния. Второй терапевтический агент может представлять собой опиоидный агонист, неопиоидный аналгетик и нестероидный противовоспалительный агент, агент против мигрени, противорвотный агент, ингибитор Сох-II, блокатор -адренергических рецепторов, противосудорожный агент, антидепрессант,противораковый агент, агент для лечения аддиктивного расстройства, агент для лечения болезни Паркинсона и паркинсонизма, агент для лечения состояния тревоги, агент для лечения эпилепсии, агент для лечения эпилептических припадков, агент для лечения удара, агент для лечения состояния зуда, агент для лечения психоза, агент для лечения ALS (амиотрофического бокового склероза), агент для лечения когнитивного расстройства, агент для лечения мигрени, агент для лечения рвоты, агент для лечения дис- 12017471 кинезии, агент для лечения депрессии или агент для лечения диареи или их смесь. Примеры применимых опиоидных агонистов включают, но без ограничения, альфентанил, аллилпродин, альфапродин, анилеридин, бензилморфин, безитрамид, бупренорфин, буторфанол, клонитазен,кодеин, дезоморфин, декстроморамид, дезоцин, диампромид, диаморфон, дигидрокодеин, дигидроморфин, дименоксадол, димефептанол, диметилтиамбутен, диоксафетилбутират, дипипанон, эптазоцин, этогептазин, этилметилтиамбутен, этилморфин, этонитазен, фентанил, героин, гидрокодон, гидроморфон,гидроксипетидин, изометадон, кетобемидон, леворфанол, левофенацилморфан, лофентанил, меперидин,мептазинол, метазоцин, метадон, метопон, морфин, мирофин, налбуфин, нарцеин, никоморфин, норлеворфанол, норметадон, налорфин, норморфин, норпипанон, опий, оксикодон, оксиморфон, папаверетум,пентазоцин, фенадоксон, феноморфан, феназоцин, феноперидин, пиминодин, пиминодин, пиритрамид,прогептазин, промедол, проперидин, пропирам, пропоксифен, суфетанил, тилидин, трамадол, их фармацевтически приемлемые соли и их смеси. В некоторых вариантах изобретения опиоидный агонист выбирают из кодеина, гидроморфона, гидрокодона, оксикодона, дигидрокодеина, дигидроморфина, морфина, трамадола, оксиморфона, их фармацевтически приемлемых солей и их смесей. Примеры применимых неопиоидных аналгетиков включают нестероидные противовоспалительные агенты, такие как аспирин, ибупрофен, диклофенак, напроксен, беноксапрофен, флурбипрофен, фенопрофен, флубуфен, кетопрофен, индопрофен, пиропрофен, карпрофен, оксапрозин, прамопрофен, муропрофен, триоксапрофен, супрофен, аминопрофен, тиапрофеновую кислоту, флупрофен, буклоксовую кислоту, индометацин, сулиндак, толмецин, зомепирак, тиопинак, зидометацин, ацеметацин, фентиазак,клиданак, окспинак, мефенамовую кислоту, меклофенамовую кислоту, флуфенамовую кислоту, нифлуминовую кислоту, толфенамовую кислоту, дифлунизал, пироксикам, судоксикам, изоксикам, их фармацевтически приемлемые соли и их смеси. Примеры других подходящих неопиоидных аналгетиков включают, без ограничения, следующие классы аналгетических, антипиретических, нестероидных противовоспалительных лекарств: производные салициловой кислоты, включая аспирин, салицилат натрия, трисалицилат холина магния, сальсалат, дифлунизал, салицилсалициловую кислоту, сульфасалазин и оксалазин; производные пара-аминофенола, включая ацетаминофен и фенацетин; индол- и инденуксусные кислоты, включая индометацин, сулиндак и этодолак; гетероарилуксусные кислоты, включая толмецин,диклофенак и кеторолак; антраниловые кислоты (фенаматы), включая мефенамовую кислоту и меклофенамовую кислоту; енолсодержащие кислоты, включая оксикамы (пироксикам, теноксикам), и пиразолидиндионы (фенилбутазон, оксифентартазон); и алканоны, включая набуметон. Более подробное описание НСПВС см. в Paul Insel, Analgesic Antipyretic and Anti-inflammatory Agents and Drags, Employed in theMolinhoff and Raymond W. Ruddon eds., 9th ed. 1996) и Glen R. Hanson, Analgesic Antipyretic and Anti Inflammatory Drugs in Remington: The Science and Practice of Pharmacy, vol. II 1196-1221 (A.R. Gennaro ed. 19th ed. 1995), которые вводятся в данное описание ссылкой во всей полноте. Подходящие ингибиторы Сох-II и ингибиторы 5-липоксигеназы, а также их комбинации описаны в патенте США No. 6136831,вводимом в данное описание ссылкой во всей полноте. Примеры ингибиторов Сох-II включают, но без ограничения, рофекоксиб и целекоксиб. Примеры применимых агентов против мигрени включают, но без ограничения, алпироприд, бромокриптин, дигидроэрготамин, долазетрон, эргокорнин, эргокорнинин, эргокриптин, эргоновин, эргот,эрготамин, флумедроксона ацетат, фоназин, кетансерин, лизурид, ломеризин, метилэргоновин, метилсергид, метопролол, наратрипан, оксеторон, пизотилин, пропранолол, рисперидон, ризатрипан, суматрипан,тимолол, тразодон, золмитрипан и их смеси. Примеры применимых блокаторов -адренергических рецепторов включают, но без ограничения,ацебутолол, алпренолол, амосулабол, аротинолол, атенолол, бефунолол, бетаксолол, бевантолол, бисопролол, бопиндолол, букумолол, буфетолол, буфуралол, бунитролол, бупранолол, бутиридин гидрохлорид, бутофилолол, каразолол, картеолол, карведилол, целипролол, цетамолол, клоранолол, дилевалол,эпанолол, эсмолол, инденолол, лабеталол, левобунолол, мепиндолол, метипранолол, метопролол, мопролол, надолол, надоксолол, небивалол, нифеналол, нипрадилол, окспренолол, пенбутолол, пиндолол,практолол, пронеталол, пропранолол, соталол, сульфиналол, талинолол, тертатолол, тилизолол, тимолол,толипролол и ксибенолол. Примеры применимых антиконвульсантов включают, но без ограничения, ацетилфенетурид, албутоин, алоксидон, аминоглутетимид, 4-амино-3-гидроксимасляную кислоту, атролактамид, бекламид, бурамат, бромид кальция, карбамазепин, цинромид, клометиазол, клоназепам, децимемид, диэтадион, диметадион, доксенитроин, этеробарб, этадион, этозуксимид, этотоин, фелбамат, флуорезон, габапентин, 5 гидрокситриптофан, ламотригин, бромид магния, сульфат магния, мефенитоин, мефобарбитал, метабарбитал, мететоин, метсуксимид, 5-метил-5-(3-фенантрил)гидантоин, 3-метил-5-фенилгидантоин, наркобарбитал, ниметазепам, нитразепам, оксабазепин, параметадион, фенацемид, фенетарбитал (phenetharbital), фенетурид, фенсуксимид, фенилметилбарбитуровую кислоту, фенитоин, фетенилат (fethenylate) натрий, бромид калия, прегабалин, примидон, прогабин, бромид натрия, соланум, бромид стронция, суклофенид, султиам, тетрантоин, тиагабин, топирамат, триметадион, вальпроевую кислоту, вигабатрин и зо- 13017471 нисамид. Примеры применимых антидепрессантов включают, но без ограничения, бинедалин, кароксазон,циталопрам, (S)-циталопрам, диметазан, фенкамин, индальпин, инделоксазина гидрохлорид, нефорам,номифензин, окситриптан, оксипертин, пароксентин, сертралин, тиазезим, тразодон, бенмоксин, ипроклозид, ипрониазид, изокарбоксазид, ниаламид, октамоксин, фенелзин, котинин, ролициприн, ролипрам,мапротилин, метралиндол, миансерин, миртазепин, адиназолам, амитриптилин, амитриптилиноксид,амоксапин, бутриптилин, кломипрамин, демексиптилин, дезипрамин, дибензепин, диметакрин, дотиепин, флуацизин, имипрамин, имипрамин N-оксид, иприндол, лофепрамин, мелитрацен, метапрамин, нортриптилин, ноксиптилин, опипрамол, пизотилин, пропизепин, протриптилин, хинупрамин, тинпентин,тианептин, тримипрамин, адрафанил, бенактизин, бупропион, бунацетин, диоксадрол, дулоксетин, этоперидон, фемоклсетин, фенпентадиол, флуксицин, флувоксамин, гематопорфирин, гиперицин, левофацетоперан, медифоксамин, милнаципран, минаприн, моклобемид, нефазодон, оксафлозан, пибералин, пролинтан, пиросукцидеанол, ритансерин, роксиндол, хлорид рубидия, сульпирид, тандоспирон, тозалинон,тофенацин, толоксатон, транилципромин, L-триптофан, веналфаксин, вилоксазин и зимелдин. Примеры применимых противораковых агентов включают, но без ограничения, ацивицин, акларубицин, акодазола гидрохлорид, акронин, адозелезин, альдеслейкин, альтретамин, амбомицин, аметантрона ацетат, аминоглутетимид, амсакрин, анастрозол, антрамицин, аспарагиназу, аспрелин, азацитидин,азетепу, азотомицин, батимастат, бензодепу, бикалутамид, бензантрена гидрохлорид, биснафид димезилат, бизелезин, бломицина сульфат, бреквинар натрия, бропиримин, бусульфан, кактиномицин, калустерон, карацемид, карбетимер, карбоплатин, кармустин, карубицина гидрохлорид, карзелезин, цедефингол,клорамбуцил, циролемицин и цисплатин. Терапевтические агенты, применимые для лечения или предупреждения аддиктивного расстройства, включают, но без ограничения, метадон, дезипрамин, амантадин, флуоксетин, бупренорфин, опиатный агонист, 3-феноксипиридин или антагонист серотонина. Примеры подходящих терапевтических агентов для лечения или предупреждения болезни Паркинсона и паркинсонизма включают, но без ограничения, карбидопу/леводопу, перголид, бромокриптин,ропинирол, прамипексол, энтакапон, толкапон, селегилин, амантадин и тригексифенидила гидрохлорид. Примеры применимых терапевтических агентов для лечения или предупреждения страха, тревоги включают, но без исключения, бензодиазепины, такие как алпразолам, бротизолам, хлордиазепоксид,клобазам, клоназепам, клозепат, демоксепам, диазепам, эстазолам, флумазенил, флуразепам, галазепам,лоразепам, мидозалам, нитразепам, нордазепам, оксазепам, празепам, квазепам, темазепам и триазолам; небензодиазепиновые агенты, такие как буспирон, гепирон, ипсапирон, тиоспирон, золпикон, золпидем и залеплон; транквилизаторы, такие как барбитураты, например амобарбитал, апробарбитал, бутабарбитал,буталбитал, мефобарбитал, метогекситал, пентобарбитал, фенобарбитал, секобарбитал и тиопентал; и пропандиолкарбаматы, такие как мепробамат и тибамат. Примеры подходящих терапевтических агентов для лечения или предупреждения эпилепсии или эпилептического припадка включают, но без ограничения, карбамазепин, этозуксимид, габапентин, ламотригин, фенобарбитал, фенитоин, примидон, вальпроевую кислоту, триметадион, бензодиазепины,гамма-винил-ГАМК (GABA), ацетазоламид и фелбамат. Примеры подходящих терапевтических агентов для лечения или предупреждения удара включают,но без ограничения, антиконвульсанты, такие как гепарин, агенты, которые разрушают тромбы (сгустки),такие как стрептокиназа или тканевый плазминогенный активатор, агенты, которые уменьшают припухлости (опухания), такие как манит или кортикостероиды, и ацетилсалициловую кислоту. Примеры подходящих терапевтических агентов для лечения или предупреждения зуда включают,но без ограничения, налтрексон; налмефен; даназол; трициклические соединения, такие как амитриптилин, имипрамин и доксепин; антидепрессанты, такие как приведнные ниже; ментол; камфару; фенол; прамоксин; капсаицин; дготь; стероиды и антигистаминные препараты. Примеры подходящих терапевтических агентов для лечения или предупреждения психоза включают, но без ограничения, фенотиазины, такие как хлорпромазина гидрохлорид, мезоридазина безилат и торидазина гидрохлорид; тиоксантены, такие как хлоропротиксена и тиотиксена гидрохлорид; клозапин; рисперидон; оланзапин; кветиапин; кветиапина фумарат; галоперидол; галоперидола деканоат; локсапина сукцинат; молиндона гидрохлорид; пимозид и зипразидон. Примеры подходящих терапевтических агентов для лечения или предупреждения ALS (амиотрофического бокового склероза) включают, но без ограничения, баклофен, нейротрофические факторы, рилузол, тизанидин, бензодиазепины, такие как клоназепам и дантролен. Примеры подходящих терапевтических агентов для лечения или предупреждения когнитивных расстройств включают, но без ограничения, агенты для лечения или предупреждения деменции, такие как такрин; донепезил; ибупрофен; нейролептики, такие как тиоридазин и галоперидол; и антидепрессанты,такие как приведнные ниже. Примеры подходящих терапевтических агентов для лечения или предупреждения мигрени включают, но без ограничения, суматрипан; метизергид; эрготамин; кофеин и бета-блокаторы, такие как пропранолол, верапамил и дивалпроэкс.- 14017471 Примеры подходящих терапевтических агентов для лечения или предупреждения рвоты включают,но без ограничения, 5-НТ 3 рецепторные антагонисты, такие как ондасетрон, доласетрон, гранисетрон и трописетрон; рецепторные антагонисты дофамина (допамина), такие как прохлорперазин, тиэтилперазин,хлорпромазин, метоклопамид и домперидон; глюкокортикоиды, такие как дексаметазон; и бензодиазепины, такие как лоразепам и алпразолам. Примеры подходящих терапевтических агентов для лечения или предупреждения дискинезии включают, но без ограничения, резерпин и тетрабеназин. Примеры подходящих терапевтических агентов для лечения или предупреждения депрессии включают, но без ограничения, трициклические антидепрессанты, такие как амитриптилин, амоксапин, бупропион, кломипрамин, дезипрамин, доксепин, имипрамин, мапротилин, нефазадон, нортриптилин, протриптилин, тразодон, тримипрамин и венлафаксин; селективные ингибиторы обратного захвата серотонина, такие как циталопрам, (S)-циталопрам, флуоксетин, флувоксамин, пароксетин и сертралин; ингибиторы моноаминоксидазы, такие как изокарбоксазид, паргилин, фенелзин и транилципромин; и психостимуляторы, такие как декстроамфетамин и метилфенидат. Примеры подходящих противодиарейных агентов включают, но без ограничения, лоперамид, дифеноксилат с атропином, клинидин, октреотид и холестирамин. Нижеприведнные примеры являются иллюстративными, но не ограничивающими соединения,композиции и методы по настоящему изобретению. Подходящие модификации и варианты различных условий и характеристик, встречающиеся обычно в клинической терапии и очевидные специалистам в данной области техники с учтом данного раскрытия, соответствуют сущности и входят в объм изобретения. Примеры Пример 1. N-(1-(3-Циано-3,3-дифенилпропил)пиперидин-4-ил)-N-фенилпропионамид(1.5 мл) при комнатной температуре прибавляют триэтиламин (2.87 ммоль). Смесь перемешивают при 60 С в течение ночи. Флеш-хроматографией смеси (70% гексана/30% EtOAc/3% Et3N) получают заданный продукт в виде тврдого вещества белого цвета с выходом 75%. Соединение (1): чистота (ВЭЖХ) 97%; MS: m/z 452.1 (М+1); 1H ЯМР (CDCl3):7.40-7.24 (м, 13 Н),7.06 (м, 2 Н), 4.62 (м, 1H), 2.86 (м, 2H), 2.52 (м, 2H), 2.38 (м, 2H), 2.08 (дт, 2H, J=2.0, 11.9 Гц), 1.91 (кв, 2H,J=7.5, 14.9 Гц), 1.75 (м, 2H), 1.33 (дкв, 2H, J=3.7, 12.3 Гц), 1.00 (т, 3 Н, J=7.6 Гц) м.д. Пример 2. N-(1-(3,3-Дифенилпропил)пиперидин-4-ил)-N-фенилпропионамид К раствору (А) (0.5 ммоль) и (С) (Acros Organics USA) (0.5 ммоль) в MeCN (1.5 мл) при комнатной температуре прибавляют триэтиламин (2.87 ммоль). Смесь перемешивают при 60 С в течение ночи. Флеш-хроматографией смеси (70% гексана/30% EtOAc/3% Et3N) получают заданный продукт в виде тврдого вещества белого цвета с выходом 75%. Соединение (2): чистота (ВЭЖХ) 97%; MS: m/z 427.1 (М+1); 1H ЯМР (CDCl3):7.37 (м, 3 Н), 7.257.12 (м, 10 Н), 7.06 (м, 2 Н), 4.62 (м, 1H), 3.88 (т, 1H, J=7.3 Гц), 2.87 (д, 2 Н, J=11.3 Гц), 2.19 (м, 4 Н), 2.02 4-Бром-2,2-дифенилмасляную кислоту (D) (Aldrich Chemical Company, Inc.) (23 г, 72 ммоль) суспендируют в хлороформе (150 мл) и по каплям прибавляют хлористый тионил (20 мл). После добавления хлористого тионила прибавляют DMF (ДМФА, 0.2 мл) и полученный раствор кипятят 4 ч. Затем реакционную смесь упаривают в вакууме, получают хлорангидрид 4-бром-2,2-дифенилмасляной кислоты (Е) в виде бледно-розового масла, которое используют на следующей стадии без дополнительной очистки. К раствору диметиламина (2 М в THF, 50 мл) и насыщенного водного раствора Na2CO3 (100 мл) по каплям при 0 С прибавляют раствор соединения (Е) в толуоле (100 мл), полученный, как описано выше. Полученную смесь оставляют перемешиваться в течение 12 ч. Смесь экстрагируют толуолом (130 мл) и хлороформом (3100 мл). Объединнные органические вытяжки промывают водой (130 мл), сушатK2CO3. Упаривают досуха, кристаллизуют из метилизобутилкетона, получают заданный продукт (F) диметил(тетрагидро-3,3-дифенил-2-фурилиден)аммония бромид с выходом 53%. К раствору (А) (0.5 ммоль) и (F) (0.5 ммоль) в MeCN (1.5 мл) при комнатной температуре прибавляют триэтиламин (2.87 ммоль). Смесь перемешивают при 60 С в течение ночи. Флеш-хроматографией смеси (70% гексана/30% EtOAc/3% Et3N) получают заданный продукт в виде тврдого вещества белого цвета с выходом 75%. Соединение (3): чистота (ВЭЖХ) 97%; MS: m/z 498.1 (М+1); 1 Н ЯМР (CDCl3):7.38-7.22 (м, 13 Н),7.06 (м, 2 Н), 4.56 (м, 1H), 2.96 (м, 2H). 2.78 (м, 2H), 2.32 (м, 4H), 1.96 (м, 5H), 1.88 (кв, 2H, J=7.5, 14.8 Гц),1.64 (с, 3 Н), 1.29 (дкв, 2 Н, J=3.3, 7.2 Гц), 0.98 (т, 3 Н, J=7.4 Гц) м.д. Пример 4. N-(1-(4-Оксо-3,3-дифенил-4-(пирролидин-1-ил)бутил)пиперидин-4-ил)-N-фенилпропионамид Соединение (G), 1-(3,3-дифенилдигидрофуран-2-илиден)пирролидиния бромид, получают с пирролидином после реакции, аналогичной реакции получения соединения (F), диметил(тетрагидро-3,3 дифенил-2-фурилиден)аммония бромида. К раствору (А) (0.5 ммоль) и (G) (0.5 ммоль) в MeCN (1.5 мл) при комнатной температуре прибавляют триэтиламин (2.87 ммоль). Смесь перемешивают при 60 С в течение ночи. Флеш-хроматографией смеси (70% гексана/30% EtOAc/3% Et3N) получают заданный продукт в виде тврдого вещества белого цвета с выходом 75%. Соединение (4): чистота (ВЭЖХ) 97%; MS: m/z 524.1 (M+1); 1H ЯМР (CDCl3):7.37-7.22 (м, 13 Н),7.06 (м, 2 Н), 4.56 (м, 1H), 3.56 (т, 2 Н, J=7.0 Гц), 2.80 (уш д, 2 Н, J=11.8 Гц), 2.44 (т, 2 Н, J=6.4 Гц), 2.37 (м,2 Н), 2.00 (м, 4 Н), 1.88 (кв, 2 Н, J=7.4, 14.8 Гц), 1.66 (м, 4 Н), 1.50 (м, 2 Н), 1.29 (дкв, 2 Н, J=3.9, 12.3 Гц), 0.98(т, 3 Н, J=7.2 Гц) м.д. Пример 5. Соединения по настоящему изобретению проверяют на связывание -опиоидных рецепторов и функцию. В табл. 1 приводятся данные связывания и функциональные данные для некоторых соединений. Пример 6. Соединения по настоящему изобретению проверяют на связывание ORL-1 рецептора и функцию. В табл. 2 приводятся данные связывания и функциональные данные для тех же соединений, что и в табл. 1. Теперь после полного описания данного изобретения рядовой специалист в данной области техники понимает, что то же самое можно осуществить в широком и эквивалентном интервале условий, рецептур и других характеристик, не изменяя объм изобретения или какой-либо из его вариантов. Другие варианты изобретения будут очевидны для специалистов в данной области техники после анализа описания и практического осуществления раскрываемого в данном описании изобретения. Предполагается, что описание и примеры даются только в качестве иллюстрации, причм действительный объм и сущность изобретения представлены в нижеприведнной "Формуле изобретения". Все патенты и публикации, цитируемые в данном описании, полностью включены в данное описание ссылкой во всей полноте. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы IR1 обозначает Н или галоген либо -O-С 1-6 алкил;R5 обозначает Н, С 1-6 алкил, -С(=О)NHC1-6 алкил, -С(=O)N(С 1-6 алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1 пиперидинилкарбонила и N-метилпиперазинилкарбонила; или его фармацевтически приемлемая соль или сольват. 2. Соединение по п.1, отличающееся тем, что R1 обозначает:N-(1-(4-оксо-3,3-дифенил-4-(пирролидин-1-ил)бутилпиперидин-4-ил-N-фенилпропионамида,или его фармацевтически приемлемая соль или сольват. 6. Фармацевтическая композиция, содержащая соединение по пп.1-5 и по меньшей мере один фармацевтически приемлемый эксципиент. 7. Способ лечения, предупреждения или ослабления интенсивности боли или рвоты у животного путм активации опиоидного рецептора, включающий введение эффективного количества соединения формулы I животному, где соединение формулы I представляет собойR1 обозначает Н или галоген либо -O-C1-6 алкил;R5 обозначает Н, циано, C1-6 алкил, -C(=O)NHC1-6 алкил, -C(=O)N(C1-6 алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1 пиперидинилкарбонила и N-метилпиперазинилкарбонила; или его фармацевтически приемлемую соль или сольват. 8. Способ по п.7, отличающийся тем, что соединение активирует -опиоидный рецептор. 9. Способ по п.8, отличающийся тем, что соединение селективно активирует -опиоидный рецептор. 10. Способ по пп.7-9, отличающийся тем, что боль выбирают из группы, состоящей из хронической боли, невропатической боли, боли при воспалении, боли при остеоартрите, боли при артрите, боли при ревматоидном артрите, боли при раке, боли, вызванной поражением спинного мозга, боли, вызванной хирургическим вмешательством, послеоперационной боли или острой боли. 11. Способ по пп.7-10, дополнительно включающий введение эффективного количества опиоидного аналгетика, неопиоидного аналгетика, агента против мигрени, противоэпилептического агента, противодиарейного агента и противорвотного агента (антиэметика). 12. Применение соединения формулы I по пп.1-5 для изготовления лекарственного средства для лечения, предупреждения или ослабления интенсивности боли или рвоты. 13. Применение соединения формулы I для лечения, предупреждения или ослабления интенсивности боли или рвоты у животного путм активации опиоидного рецептора, где соединение формулы I представляет собойR1 обозначает Н или галоген либо -O-C1-6 алкил;R5 обозначает Н, циано, С 1-6 алкил, -C(=O)NHC1-6 алкил, -С(=O)N(С 1-6 алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1 пиперидинилкарбонила и N-метилпиперазинилкарбонила; или его фармацевтически приемлемую соль или сольват. 14. Применение соединения формулы I для лечения, предупреждения или ослабления боли, выбранной из хронической боли, невропатической боли, боли при воспалении, боли при остеоартрите, боли при артрите, боли при ревматоидном артрите, боли при раке, боли, вызванной поражением спинного мозга, боли, вызванной хирургическим вмешательством, послеоперационной боли или острой боли, где соединение формулы I представляет собойR1 обозначает Н или галоген либо -O-C1-6 алкил;R5 обозначает Н, циано, C1-6 алкил, -С(=О)NHC1-6 алкил, -С(=O)N(С 1-6 алкил)2 или циклоаминокарбонил, выбранный из 1-азиридинилкарбонила, 1-азетидинилкарбонила, 1-пирролидинилкарбонила, 1 пиперидинилкарбонила и N-метилпиперазинилкарбонила; или его фармацевтически приемлемую соль или сольват.
МПК / Метки
МПК: A61K 45/06, A61P 25/04, C07D 211/58, C07D 401/06, A61P 29/02
Метки: применение, фенилпропионамидные, соединения
Код ссылки
<a href="https://eas.patents.su/20-17471-fenilpropionamidnye-soedineniya-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Фенилпропионамидные соединения и их применение</a>
Предыдущий патент: Электрический коммутационный блок
Следующий патент: Удаление магнитных частиц из текучей среды
Случайный патент: Способ получения 5-[2-циклопропил-1-(2-фторфенил)-2-оксоэтил]-4,5,6,7-тетрагидротиено[3,2-с]пиридин-2-ила ацетата (прасугреля)
























