Новые полиморфные формы n-[4-(трифторметил)бензил]-4- метоксибутирамида
Формула / Реферат
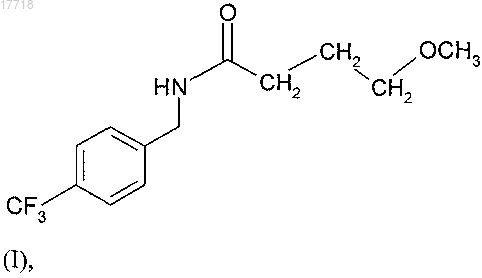
1. Полиморфная форма А N-[4-(трифторметил)бензил]-4-метоксибутирамида формулы (I)
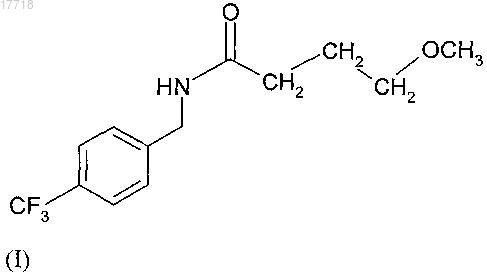
характеризующаяся следующими углами дифракции пиков на порошковой дифрактограмме: 9,7; 12,0; 18,0; 24,1; 25,9±0,2°2θ.
2. Полиморфная форма А по п.1, характеризующаяся следующими пиками углов дифракции на порошковой дифрактограмме ±0,2:
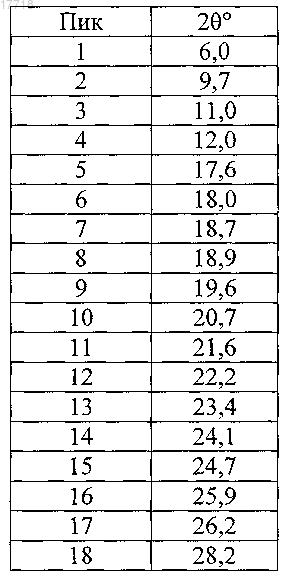
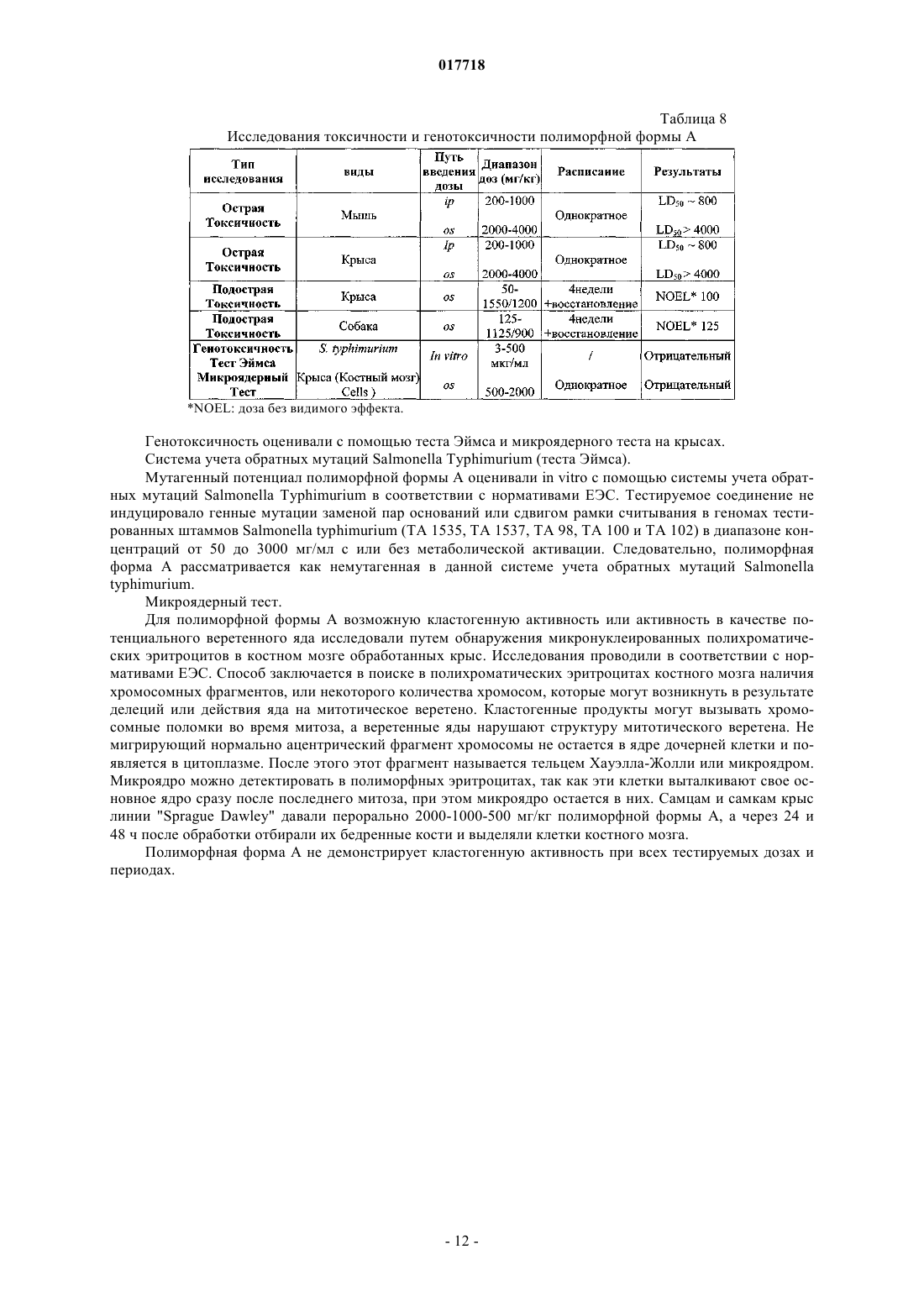
3. Полиморфная форма А по любому из пп.1, 2, характеризующаяся представленной на фиг. 1 порошковой дифрактограммой.
4. Полиморфная форма В N-[4-(трифторметил)бензил]-4-метоксибутирамида формулы (I)
характеризующаяся следующими углами дифракции пиков на порошковой дифрактограмме: 11,7; 19,8; 22,3; 23,6±0,2°2θ.
5. Полиморфная форма В по п.4, характеризующаяся следующими пиками углов дифракции на порошковой дифрактограмме ±0,2:
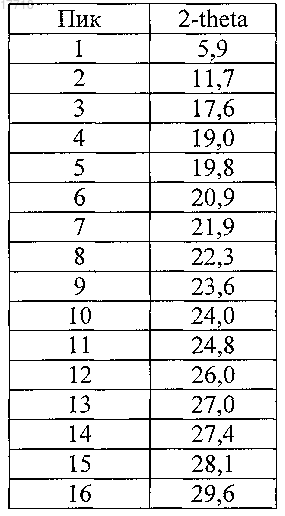
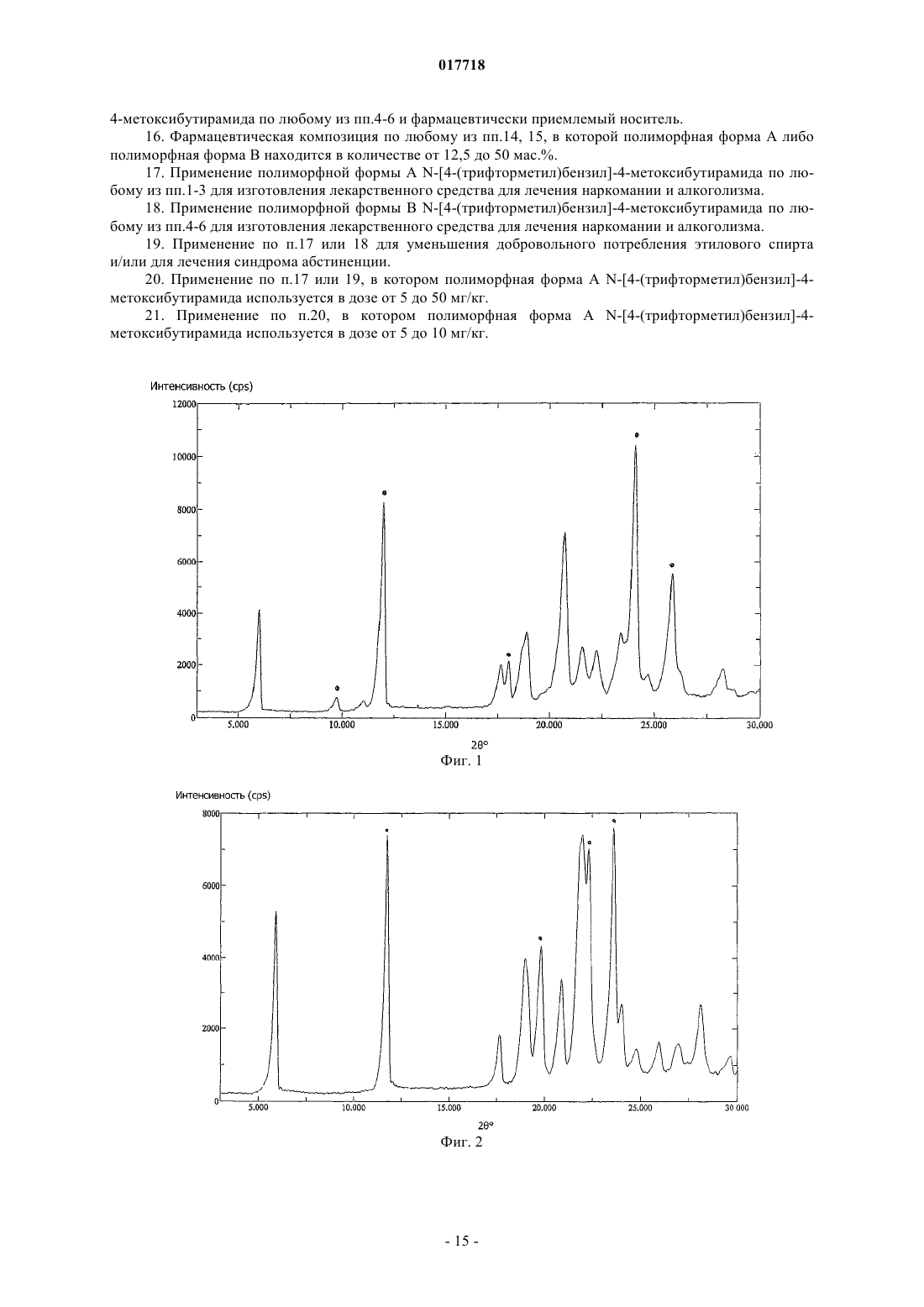
6. Полиморфная форма В по любому из пп.4, 5, характеризующаяся представленной на фиг. 2 порошковой дифрактограммой.
7. Способ получения полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.1-3, включающий следующие стадии:
i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;
ii) получение кристаллической полиморфной формы А из раствора неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливают полиморфной формой А N-[4-(трифторметил)бензил]-4-метоксибутирамида.
8. Способ получения полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.4-6, включающий следующие стадии:
i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;
ii) получение кристаллической полиморфной формы В из раствора неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливают полиморфной формой В N-[4-(трифторметил)бензил]-4-метоксибутирамида.
9. Способ по п.7 или 8, в котором 4-трифторметилбензиламин получают реакцией 4-трифторметилбензальдегида с гидрохлоридом гидроксиламина по следующей схеме:
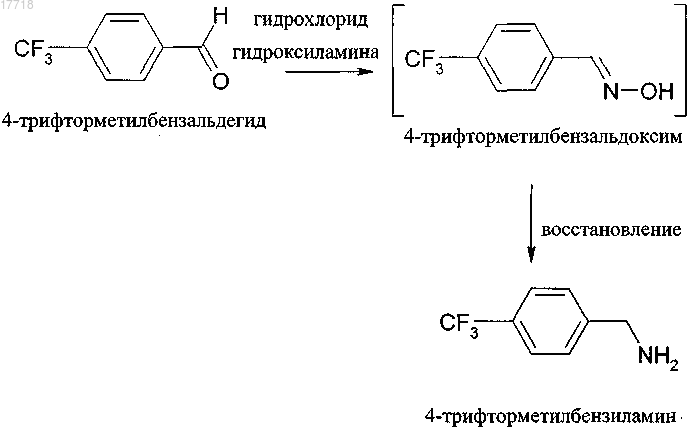
10. Способ по любому из пп.7-9, согласно которому на стадии (i) катализатором является 30% раствор метилата натрия в метаноле.
11. Способ по любому из пп.7-10, согласно которому органический растворитель выбирают из толуола и смеси этилацетата/н-гексана.
12. Способ по п.11, согласно которому органический растворитель является смесью этилацетата/н-гексана.
13. Способ по п.12, согласно которому смесь этилацетата:н-гексана имеет соотношение от 1:4 до 1:2, предпочтительно около 1:3.
14. Фармацевтическая композиция для лечения наркомании или алкоголизма, содержащая в качестве активного ингредиента эффективное количество полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.1-3 и фармацевтически приемлемый носитель.
15. Фармацевтическая композиция для лечения наркомании или алкоголизма, содержащая в качестве активного ингредиента эффективное количество полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.4-6 и фармацевтически приемлемый носитель.
16. Фармацевтическая композиция по любому из пп.14, 15, в которой полиморфная форма А либо полиморфная форма В находится в количестве от 12,5 до 50 мас.%.
17. Применение полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.1-3 для изготовления лекарственного средства для лечения наркомании и алкоголизма.
18. Применение полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.4-6 для изготовления лекарственного средства для лечения наркомании и алкоголизма.
19. Применение по п.17 или 18 для уменьшения добровольного потребления этилового спирта и/или для лечения синдрома абстиненции.
20. Применение по п.17 или 19, в котором полиморфная форма А N-[4-(трифторметил)бензил]-4-метоксибутирамида используется в дозе от 5 до 50 мг/кг.
21. Применение по п.20, в котором полиморфная форма А N-[4-(трифторметил)бензил]-4-метоксибутирамида используется в дозе от 5 до 10 мг/кг.
Текст
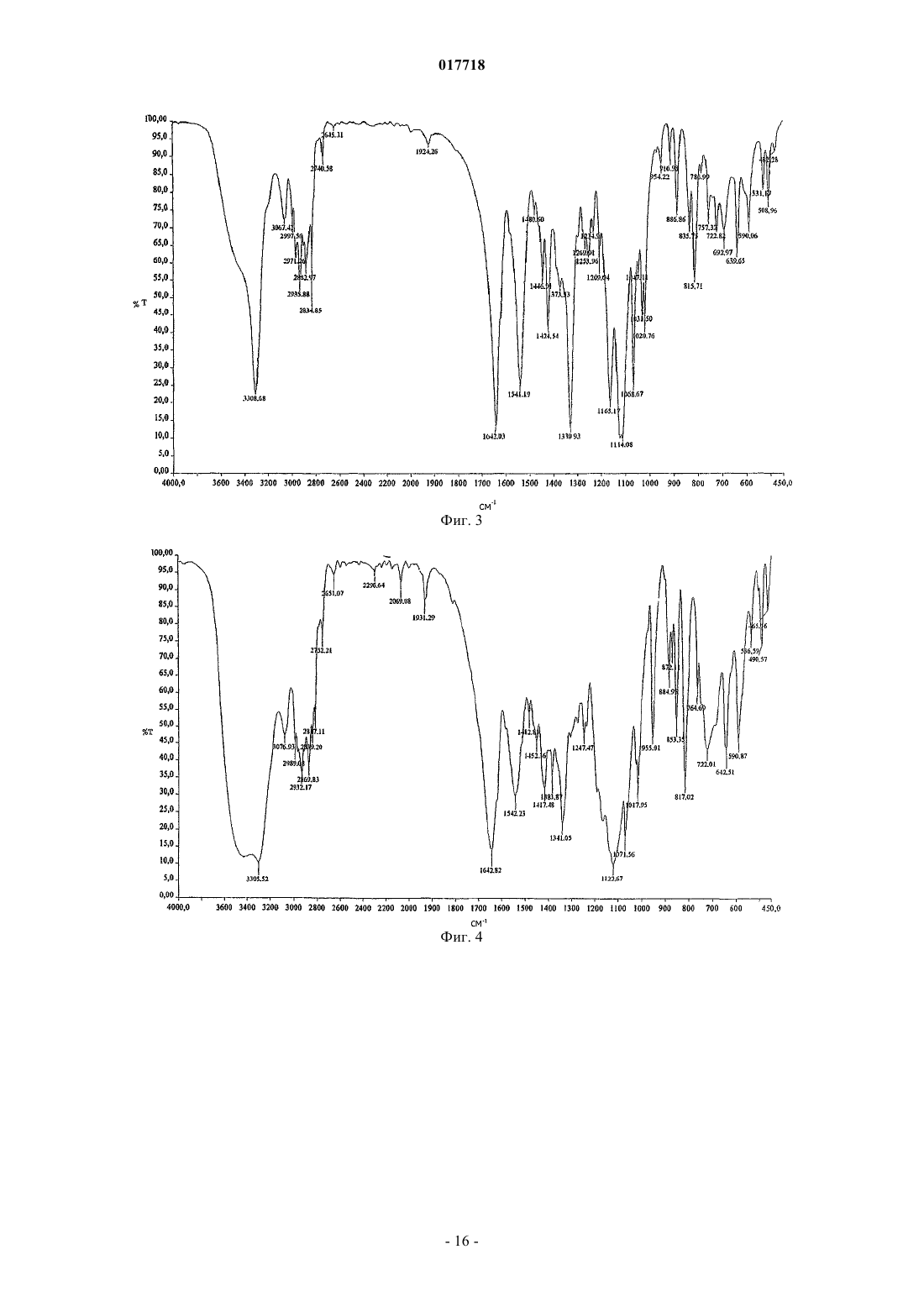
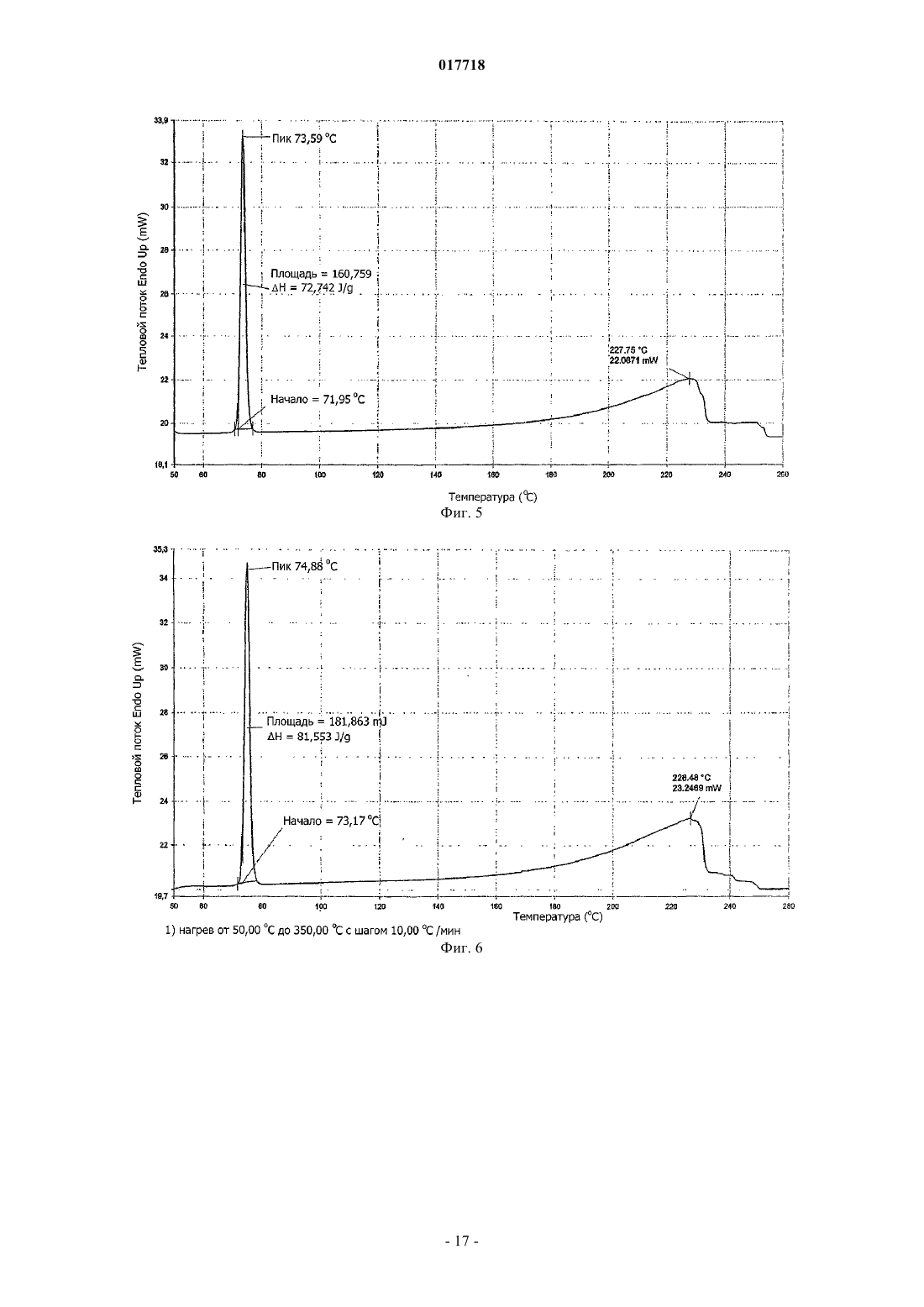
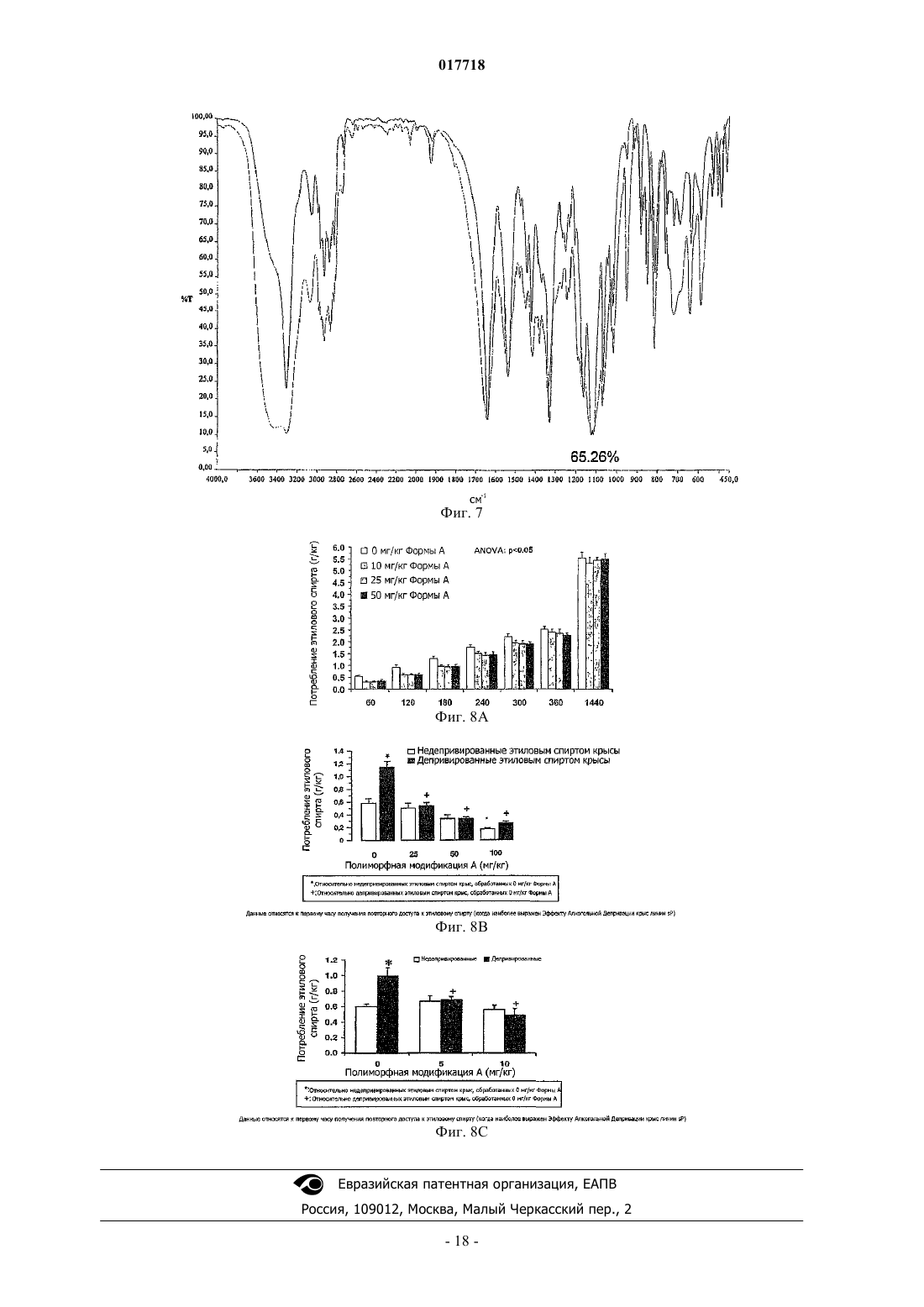
ИСПРАВЛЕННОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ЕВРАЗИЙСКОМУ ПАТЕНТУ 2008.11.12 НОВЫЕ ПОЛИМОРФНЫЕ ФОРМЫ N-[4-(ТРИФТОРМЕТИЛ)БЕНЗИЛ]-4 МЕТОКСИБУТИРАМИДА Приведено описание кристаллических полиморфных форм N-[4-(трифторметил)бензил]-4 метоксибутирамида. Две полиморфные формы, называемые полиморфная форма А и полиморфная форма В, могут быть использованы при лечении наркомании и алкоголизма и обладают очень хорошей стабильностью. Также приведено описание способа получения полиморфных форм. Примечание: библиография отражает состояние при переиздании Область техники, к которой относится изобретение Настоящее изобретение относится к двум новым полиморфным формам соединения формулы (I) а именно N-[4-(трифторметил)бензил]-4-метоксибутирамида, и к их применению при лечении наркомании и особенно при лечении алкоголизма. Предшествующий уровень техникиN-[4-(Трифторметил)бензил]-4-метоксибутирамид впервые был раскрыт в европейском патенте ЕР 0932597 В 1 как часть группы амидов, полезных при лечении наркомании и алкоголизма. В соответствии с этим патентом содержащий 4-трифторметилбензильную группуN-[4-(трифторметил)бензил]-4-метоксибутирамид демонстрировал оптимальные свойства по показателю нейрофармакологической активности, по сравнению с широко известными при лечении алкоголизма солями -оксимасляной кислоты (ГОМК). В частности, данное соединение продемонстрировало большую по сравнению с ГОМК и по сравнению с другими амидами с различными группами в структуре эффективность и длительность действия при оценке воздействия на двигательную активность крыс. Ввиду оптимальной нейрофармакологической активности данного соединения для использования в фармакологии потребовался N-[4-(трифторметил)бензил]-4-метоксибутирамид с высокой чистотой и с высоким выходом. Сначала изобретатели настоящего изобретения попытались получить N-[4-(трифторметил)бензил]4-метоксибутирамид, следуя описанной в патенте прописи. В частности, в соответствии с ЕР 0932597 В 1 соединение было приготовлено, следуя описанному на стр. 8 патента основному способу синтеза, который предусматривает следующие этапы: А) реакцию эфира 4-алкоксимасляной кислоты с подходящим амином в присутствии NH4Cl при температуре 160-170 С, для получения неочищенного продукта; В) хроматография неочищенного продукта на силикагеле с элюцией циклогексаном/этилацетатом и,наконец; С) кристаллизация из CH2Cl2/Et2O. Следуя этой процедуре, однако, изобретатели обнаружили, что даже если они и получали искомое соединение, то оно каждый раз обладало различными физико-химическими характеристиками. Основной способ синтеза, указанный в ЕР 0932597 В 1, следовательно, продемонстрировал плохую воспроизводимость, а из-за этапа очистки В) также оказался очень дорогим и, следовательно, не подходящим для получения N-[4-(трифторметил)бензил]-4-метоксибутирамида в промышленных масштабах. Сущность изобретения Пытаясь решить проблему воспроизводимости способа получения N-[4-(трифторметил)бензил]-4 метоксибутирамида, изобретатели, к своему удивлению, обнаружили, что соединение может находиться в различных полиморфных формах. В частности, при разработке способа получения, при дистилляции и при каждом анализе полученного продукта изобретатели обнаружили две новые полиморфные формыN-[4-(трифторметил)бензил]-4-метоксибутирамида, форму А и форму В, обладающие различной кристаллической упаковкой. Следовательно, настоящее изобретение обеспечивает в одном аспекте полиморфную форму А характеризующуюся углами дифракции пиков (2) на порошковой дифрактограмме 9,7; 12,0; 18,0; 24,1; 25,90,2. В дальнейшем аспекте настоящее изобретение обеспечивает полиморфную форму В соединения формулы (I), характеризующуюся углами дифракции пиков (2) на порошковой дифрактограмме 11,7; 19,8; 22,3; 23,60,2. Более того, изобретатели также нашли способ для воспроизводимого и стабильного получения двух новых полиморфных форм А и В с высокой чистотой без необходимости проведения этапа очистки хроматографией. В еще одном дополнительном аспекте, в силу вышесказанного настоящее изобретение касается способа получения полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида, содержащего следующие стадии:i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;ii) получение кристаллической полиморфной формы А из раствора неочищенногоN-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливается полиморфной формой А N-[4-(трифторметил)бензил]-4-метоксибутирамида. В еще одном дополнительном аспекте настоящее изобретение касается способа получения полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида, содержащего следующие стадии:i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;ii) получение кристаллической полиморфной формы В из раствора неочищенногоN-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливается полиморфной формой В N-[4-(трифторметил)бензил]-4-метоксибутирамида. Полиморфные формы А и В N-[4-(трифторметил)бензил]-4-метоксибутирамида полезны при лечении наркомании и алкоголизма. Конкретнее, они нужны для сокращения добровольного потребления этилового спирта при лечении синдрома абстиненции. Более того, вышеупомянутые полиморфные формы А и В также полезны при лечении кризисов абстиненции от формирующих зависимость препаратов,таких как героин, кокаин, морфин и психоактивные препараты. Таким образом, также настоящее изобретение касается полиморфной формы AN-[4-(трифторметил)бензил]-4-метоксибутирамида для применения в качестве лекарственного средства,а также касается полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида для применения в качестве лекарственного средства. В другом аспекте настоящее изобретение также относится к фармацевтической композиции, содержащей эффективное количество полиморфной формы АN-[4-(трифторметил)бензил]-4 метоксибутирамида в качестве активного ингредиента и фармацевтически приемлемый носитель, а также относится к фармацевтической композиции, содержащей эффективное количество полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида в качестве активного ингредиента и фармацевтически приемлемый носитель. Перечень чертежей На фигурах покано: на фиг. 1 - порошковая дифрактограмма кристаллической полиморфной формы АN-[4-(трифторметил)бензил]-4-метоксибутирамида; на фиг. 2 - порошковая дифрактограмма кристаллической полиморфной формы ВN-[4-(трифторметил)бензил]-4-метоксибутирамида; на фиг. 3 - инфракрасный спектр кристаллической полиморфной формы А- инфракрасный спектр кристаллической полиморфной формы ВN-[4-(трифторметил)бензил]-4-метоксибутирамида; на фиг. 5 - спектр дифференциальной сканирующей калориметрии полиморфной формы АN-[4-(трифторметил)бензил]-4-метоксибутирамида; на фиг. 6 - спектр дифференциальной сканирующей калориметрии полиморфной формы ВN-[4-(трифторметил)бензил]-4-метоксибутирамида; на фиг. 8 А - результаты модели спонтанного потребления этилового спирта у недепривированных крыс линии sP после введения полиморфной формы А; на фиг. 8 В - результаты модели эффекта алкогольной депривации у недепривированных крыс линииsP после введения высоких доз полиморфной формы А; на фиг. 8 С - результаты модели эффекта алкогольной депривации у недепривированных крыс линииsP после введения низких доз полиморфной формы А. Сведения, подтверждающие возможность осуществления изобретения Изобретение касается новых полиморфных форм А и В N-[4-(трифторметил)бензил]-4 метоксибутирамида, характеризующихся различными углами дифракции релевантных пиков (2 в угловых градусах 0,2) на порошковой дифрактограмме, в частности 9,7, 12,0, 18,0, 24,1, 25,9 для полиморфной формы А и 11,7, 19,8, 22,3, 23,6 для полиморфной формы В. Более конкретно, полиморфная форма А характеризуется 18 пиками углов дифракции на показанной на фиг. 1 порошковой дифрактограмме с интенсивностью, представленной в табл. 1. Таблица 1 Пики полиморфной формы А В соответствии с настоящим изобретением полиморфная форма А N-[4-(трифторметил)бензил]-4 метоксибутирамида может быть получена способом, включающим следующие стадии:i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;ii) получение кристаллической полиморфной формы А из раствора неочищенногоN-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливается полиморфной формой А N-[4-(трифторметил)бензил]-4-метоксибутирамида. 4-Трифторметилбензиламин этапа (i) может быть получен в соответствии с известными способами синтеза ароматических аминов. Предпочтительно, если 4-трифторметилбензиламин получают с помощью реакции 4-трифторметилбензальдегида с гидроксиламином по следующей схеме: По этой схеме 4-трифторметилбензиламин предпочтительно может быть получен с выходом 90%. В соответствии с настоящим изобретением на стадии (i) 4-трифторметилбензиламин вступает в реакцию с 4-метилметоксибутиратом в присутствии катализатора, которым предпочтительно является 30%-ный раствор метилата натрия в метаноле, но также могут быть использованыN,N-диметиламинопиридин и хлорид аммония. Предпочтительно, чтобы стадия (i) проводилась при температуре от 95 до 135 С, более предпочтительно от 110 до 120 С. В конце реакции неочищенныйN-[4-(трифторметил)бензил]-4-метоксибутирамид может быть выделен путем изоляции обычными методами, такими как дистилляция в органических растворителях. Предпочтительно, если стадия (i) позволяет получать около 70% неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида. Полученный таким образом неочищенный N-[4-(трифторметил)бензил]-4-метоксибутирамид кристаллизуют в полиморфную форму А на стадии (ii), во-первых, путем приготовления раствора неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, а затем путем затравки полиморфной формы А в указанном растворе. Таким растворителем может быть любой подходящий органический растворитель, способный содействовать кристаллизации полиморфной формы А. Предпочтительно, если такой органический растворитель выбирается из толуола и смеси этилацетата и н-гексана. Более предпочтительно, если раствор неочищенного N-[4-(трифторметил)бензил]-4 метоксибутирамида готовится на смеси этилацетат:н-гексан. Предпочтительно, когда неочищенный продукт солюбилизируют в смеси этилацетат:н-гексан, в которой соотношение этилацетат:н-гексан составляет от 1:4 до 1:2, более предпочтительно около 1:3. Раствор неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида в растворителе предпочтительно образуется при нагревании до температуры от 35 до 70 С, еще более предпочтительно от 40 до 60 С, перед затравкой полиморфной формой А. Осаждение осадка полиморфной формы А предпочтительно происходит при температуре от 0 до 35 С, более предпочтительно от 10 до 20 С. Предпочтительно, если стадия (ii) позволяет получать около 95% полиморфной формы А N-[4(трифторметил)бензил]-4-метоксибутирамида. В соответствии с другим воплощением настоящего изобретения обеспечивается полиморфная форма В. Полиморфная форма В характеризуется 16 пиками углов дифракции на показанной на фиг. 2 порошковой дифрактограмме с интенсивностью, представленной в табл. 2. Таблица 2 Пики полиморфной формы В В соответствии с настоящим изобретением полиморфная форма В N-[4-(трифторметил)бензил]-4 метоксибутирамида может быть получена способом, включающим следующие стадии:i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;ii) получение кристаллической полиморфной формы В из раствора неочищенного N-[4(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливается полиморфной формой В N-[4-(трифторметил)бензил]-4-метоксибутирамида. Все указанные выше предпочтительные аспекты способа получения полиморфной формы А, а именно получение бензиламина на стадии (i) и все предпочтительные особенности обеих стадий (i) и (ii),тождественны аспектам способа получения полиморфной формы В и названы здесь в качестве ссылки. В соответствии с настоящим изобретением полиморфную форму А и полиморфную форму В предпочтительно получали простым способом, который также позволял избежать применения хроматографии для получения чистой кристаллической формы и, что более предпочтительно, который, являясь воспроизводимым, позволяет получать выборочно желаемую кристаллическую форму в стабильной форме. Кристаллические полиморфные формы А и В могут, в частности, различаться порошковыми дифрактограммами, представленными на фиг. 1 и 2 соответственно, но также их можно различить по инфракрасным спектрам, что будет видно в экспериментальной части. Обе кристаллические полиморфные формы А и В являются термодинамически стабильными, без преобразования друг в друга. Анализ на растворимость проводили для каждой полиморфной модификации, и обе формы, А и В, не продемонстрировали каких-либо различий в свойствах растворимости. Обе формы также продемонстрировали удивительную фармакологическую активность при лечении наркомании и особенно алкоголизма. Благодаря таким свойствам, кристаллические полиморфные формы А и В могут применяться в качестве лекарственных средств. В силу вышесказанного в соответствии с настоящим изобретением обеспечивается фармацевтическая композиция, содержащая либо полиморфную форму А, либо полиморфную форму В и фармацевтически приемлемые эксципиенты. Композиция по настоящему изобретению предпочтительно содержит от 12,5 до 50 мас.% либо полиморфной формы А, либо полиморфной формы В. Такие композиции могут быть получены с помощью обычных растворителей или вспомогательных веществ и методов, известных в области изготовления галеновых препаратов. Фармацевтические композиции, содержащие полиморфные формы А и В, могут быть введены любым подходящим путем, например перорально или парентерально. Фармацевтические композиции для перорального введения предпочтительно могут быть в твердой форме, такой как порошки, гранулы, таблетки, необязательно шипучих, спрессованных или покрытых пилюль, драже, саше, твердых или мягких капсул, или могут быть в жидкой форме, такой как растворы,суспензии или эмульсии. Фармацевтические композиции для парентерального введения могут быть в форме водных или неводных растворов, суспензий или эмульсий. В твердых композициях форма А или форма В могут быть объединены с любыми подходящими твердыми эксципиентами, например, выбранными из смазывающих и разрыхляющих агентов, наполнителей и т.п. В жидких композициях форма А и форма В могут быть растворены, например, в воде, органических растворителях или спиртах. Полиморфная форма А и полиморфная форма В предпочтительно могут быть использованы для лечения наркомании и для лечения алкоголизма. Для этих целей полиморфные модификации предпочтительно могут быть введены в дозах от 5 до 50 мг/кг. Несмотря на то что обе полиморфные модификации обладают схожими особенностями и схожей активностью, в соответствии с настоящим изобретением для использования в качестве лекарственного средства предпочтительной является полиморфная форма А N-[4-(трифторметил)бензил]-4 метоксибутирамида. Собственно говоря, полиморфная форма А продемонстрировала оптимальные физические свойства, такие как сжимаемость и плотность, что, таким образом, придает ей лучшую технологичность и обрабатываемость, которые критически важны при разработке и изготовлении продукта. Более того, как это будет видно из экспериментальной части, полиморфная форма А продемонстрировала удивительную терапевтическую активность при алкогольной зависимости, даже в очень низких фармакологических дозах от 5 до 10 мг/кг. Форма А также была протестирована на фармакологическую, токсикологическую и генотоксическую безопасность и была признана безопасной с очень низкими профилями токсичности и генотоксичности, что показано ниже. Теперь изобретение будет описано более подробно с помощью неограничивающих примеров для того, чтобы лучше охарактеризовать как форму А, так иформу В и их физико-химические и фармакологические особенности. Пример 1. Получение полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида. А) Получение 4-трифторметилбензиламина. В реактор загружали 15 кг дистиллированной воды, 2,50 кг ацетата натрия, 2,30 кг гидрохлорида гидроксиламина, 4,00 кг метанола. При комнатной температуре добавляли 5 кг трифторметилбензальдегида и сначала перемешивали смесь около 30 мин, а затем дистиллировали под вакуумом 5 кг растворителя. Затем добавляли 12,0 кг 80% уксусной кислоты, после чего порционно добавляли 4,5 кг цинка, тем самым давая температуре экзотермически подняться до 60-80 С. Такая температура затем поддерживалась охлаждением. В конце реакции для удаления солей цинка добавляли 10,0 кг толуола и 15,0 кг 30% аммиака. Полученную таким образом массу перемешивали при 50-60 С, после чего отбрасывали нижнюю водную фазу. После дистилляции в вакууме примерно до половины объема раствор толуола, содержащий 4 трифторметилбензиламин, восстанавливали и использовали на последующей стадии (i). Было получено 4,00 кг 4-трифторметилбензиламина, что установлено потенциометрическим титрованием. Выход: 79,5%B) Стадия i) получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида. Толуоловый раствор, полученный на стадии А (4,00 кг 4-трифторметилбензиламина), загружали в реактор. После дистилляции до получения масляного остатка добавляли 3,20 кг 4-метоксибутирата,0,40 кг 30% метилата натрия. Раствор затем нагревали до температуры 110-120 С, дистиллировали при атмосферном давлении для удаления всего метанола (также метанол удаляется из реакции) и поддерживали такую температуру по меньшей мере в течение 2 ч. Реактор при температуре 110-120 С затем помещали в вакуум по меньшей мере на 1 ч. В конце реакции к массе добавляли 12,0 кг толуола, 2,0 кг во-5 017718 ды и 0,40 кг 80% уксусной кислоты. После перемешивания нижнюю водную фазу отделяли и отбрасывали. Органическую фазу затем дистиллировали в вакууме до масляного остатка. К этому остатку добавляли 4,00 кг этилацетата, 12,0 кг н-гексана и нагревали целевую массу до 40-60 С до получения полного раствора. Затем температуру раствора доводили до 20-30 С и выдерживали при этой температуре до получения хорошего осадка. Массу затем охлаждали до 0-10 С, центрифугировали с промыванием смесью 0,80 кг этилацетата, 4,00 кг н-гексана. Полученный влажный продукт использовали на следующей стадии. Было получено около 3,8 кг неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида. Выход: 60,5%C) Стадия (ii) кристаллизации полиморфной формы А N-[4-(трифторметил)бензил]-4 метоксибутирамида. В реактор помещали 3,8 кг неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида (соответствующий влажный продукт), 3,8 кг этилацетата и 11,4 кг н-гексана. Массу нагревали до 40-60 С до полного растворения, после чего температуру раствора доводили до 25-35 С. В качестве затравки использовали 0,038 кг полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида. Температуру массы поддерживали на уровне 25-35 С в течение по меньшей мере 1 ч, а затем охлаждали до температуры 10-20 С, которую также поддерживали по меньшей мере в течение 1 ч. Массу затем центрифугировали для отмывания с помощью предварительно полученной смеси, содержащей 0,76 кг этилацетата, 2,28 кг н-гексана. Полученный продукт сушили при 40-50 С. Было получено около 3,4 кг полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамид. Выход: 89,5%. Пример 2. Получение полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида. Неочищенный N-[4-(трифторметил)бензил]-4-метоксибутирамид был получен по той же процедуре и с использованием тех же количеств экспериментальных частей А) и В), что и в примере 1. С) Стадия (ii) кристаллизации полиморфной формы В N-[4-(трифторметил)бензил]-4 метоксибутирамида. В лабораторную колбу помещали 34,0 г N-[4-(трифторметил)бензил]-4-метоксибутирамида, 34,0 г этилацетата, 102 г н-гексана. Массу затем нагревали до 40-60 С до полного растворения. Затем раствор охлаждали до 25-35 С, а в качестве затравки использовали 0,35 г полиморфной формы В N-[4(трифторметил)бензил]-4-метоксибутирамида. Температуру массы поддерживали на уровне 25-35 С в течение по меньшей мере 1 ч, а затем охлаждали до температуры 10-20 С, которую также поддерживали по меньшей мере в течение 1 ч. Массу затем центрифугировали для отмывания с помощью предварительно полученной смеси, содержащей 6,8 г этилацетата, 20,4 г н-гексана. Полученный продукт сушили при 40-50 С. Было получено около 31 г полиморфной формы В N-[4-(трифторметил)бензил]-4 метоксибутирамида. Пример 3. Анализ полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида. Во-первых, кристаллический продукт примера 1 анализировали для подтверждения того, что он является N-[4-(трифторметил)бензил]-4-метоксибутирамидом. Образец примера 1 был подвергнут масс-спектрометрическому анализу методом ионизации электрораспылением +)ESI) с помощью прибора "Thermo-Finnigam LCQ-Advantage". Молекулярная масса составила 275, а результаты паттерна фрагментации тандемной массспектрометрии представлены в табл. 3. Таблица 3 Результаты паттерна фрагментации тандемной масс-спектрометрии Молекулярная масса и паттерн фрагментации тандемной масс-спектрометрии подтвердили структуру N-[4-(трифторметил)бензил]-4-метоксибутирамида. 1 Н-ЯМР анализ с помощью растворителей CDCl3 и CDCl3+D2O на приборе "Variant Geminy 200" на частоте 200 МГц. Спектр ЯМР подтвердил структуру N-[4-(трифторметил)бензил]-4-метоксибутирамида в соответствии со следующими результатами. Элементный анализ. Образец дал следующие элементные значения, которые соответствуют расчетным. Таблица 5 Элементные значения для C13H16NO2F3 Пример 4. Анализ полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида. Масс-спектрометрический, 1 Н-ЯМР и элементный анализы повторили с образцом кристаллизованного продукта, полученного в соответствии с примером 2, с помощью тех же методов и инструментов. Все полученные данные подтвердили, что продуктом примера 2 был N-[4-(трифторметил)бензил]-4 метоксибутирамид. Пример 5. Определение полиморфизма N-[4-(трифторметил)бензил]-4-метоксибутирамида. Два образца кристаллизованных продуктов примеров 1 и 2 были проанализированы с помощью порошковой рентгеновской дифрактометрии на приборе "Rigaku MiniFlex" с применением Cu-1 излучения и Cu-2-излучения; дифференциальной сканирующей калориметрии на приборе "Perkin-Elmer DSC 6" при скорости сканирования 10 С/мин в диапазоне температур 50-260 С; инфракрасного анализа на приборе "Perkin-Elmer FT-IR Spectrum-one", в котором анализируемый образец находится в состоянии суспензии в KBr. Порошковая дифрактограмма образца полиморфной формы А примера 1 представлена на фиг. 1, а все значения 2 и интенсивности (cps) представлены в табл. 1. Порошковая дифрактограмма образца полиморфной формы В примера 2 представлена на фиг. 2, а все значения 2 и интенсивности (cps) представлены в табл. 2. ИК-спектр полиморфной формы А (пример 1) представлен на фиг. 3. На фиг. 3 показаны следующие ИК-полосы (см-1): 3308,68, 3067,42, 2997,56, 2971,26, 2935,88, 2882,97, 2834,85, 2740,58, 1924,26,1642,03, 1541,19, 1480,60, 1446,91, 1424,54, 1373,53, 1330,93, 1253,96, 1234,94, 1209,04, 1165,17, 1114,08,1068,67, 1047,11, 1031,50, 1020,76, 954,22, 916,98, 886,86, 835,75, 815,71, 757,32, 722,82, 692,97, 639,65,590,06, 531,17, 508,96, 482,28. ИК-спектр полиморфной формы В (пример 2) представлен на фиг. 4. На фиг. 4 показаны следующие ИК-полосы (см-1): 3305,52, 3076,93, 2989,08, 2932,17, 2869,83, 2839,20, 2817,11, 2752,21, 2651,07,2296,64, 2069,08, 1931,29, 1642,82, 1542,23, 1482,83, 1452,36, 1417,48, 1383,87, 1341,05, 1247,47, 1122,67,1071,56, 1017,95, 955,01, 884,95, 872,11, 853,35, 817,02, 764,69, 722,01, 642,51, 590,87, 536,59, 490,57,465,16. Спектры дифференциальной сканирующей калориметрии для полиморфной формы А (полученной в примере 1) и полиморфной формы В (полученной в примере 2) представлены на фиг. 5 и 6 соответственно, на которых отмечены температуры начала разложения и максимальные температуры. На всех фиг. 1-6 ясно видно, что и форма А, и форма В состоят из изоморфных кристаллов. Тем не менее, исходя из полученных значений различных анализов, видно, что полиморфная форма А и полиморфная форма В имеют различную кристаллическую структуру. Для того чтобы более четко подчеркнуть различие в структуре, ИК-спектр образца примера 1 (форма А), представленный на фиг. 3, и ИК-спектр образца примера 2 (форма В), представленный на фиг. 4,наложили друг на друга, как показано на фиг. 7, и вычислили их корреляцию. Значение корреляции составило 65,26%. Этот результат и фиг. 7 подтвердили тот факт, что форма А и форма В являлись двумя различными полиморфными модификациями N-[4-(трифторметил)бензил]-4-метоксибутирамида. Пример 6. Оценка физико-химических характеристик образцов полиморфной формы А и полиморфной формы В. Анализировали полученный, как описано в примере 1, образец полиморфной формы А, состоящий из частиц с размером менее чем 10 мкм. Результаты анализа приведены в табл. 6. Таблица 6 Физико-химические характеристики полиморфных форм А и форм В Обе полиморфные модификации оказались кристаллами высокой чистоты. Более того, полиморфная форма А оказалась полностью кристаллическим порошком. Благодаря этой особенности, с которой может быть достигнута лучшая технологичность и обрабатываемость, полиморфная форма А признана лучшим кандидатом для изготовления фармацевтических композиций. Оба образца порошка (форма А и форма В) были использованы для оценки свойств растворимости двух полиморфных модификаций при различных значениях рН. Оба образца были протестированы в условиях со следующими значениями рН: солянокислый буфер при рН 1,2; уксусная кислота при рН 3,0; фосфатный буфер при рН 3,0; фосфатный буфер при рН 4,6; фосфатный буфер при рН 6,0; фосфатный буфер при рН 7,4; щелочной фосфатный буфер при рН 8,0. 0,5 г каждого образца растворяли в стеклянной колбе в 100 мл соответствующего буфера. Оба образца затем перемешивали в течение 30 минт. Если образцы полностью растворялись, то в колбу добавляли дополнительный 1 г и перемешивали в течение 30 мин. Процедуру повторяли до появления нерастворенного продукта на дне колбы. После такой процедуры растворения образцы сохраняли в течение 24 ч, а затем растворенное количество формы А и формы В соответственно определяли с помощью ВЭЖХ анализа. Результаты представлены в табл. 7. Таблица 7 Растворимость полиморфной формы А и полиморфной формы В при различных значениях рН Обе полиморфные модификации не показали особых различий в свойствах растворения. рН не влияла на растворимость обоих соединений, а минимальные различия в данном случае не являлись значимыми. Растворимость была низкой, тем самым подтверждая высокую стабильность двух полиморфных модификаций. После 24 ч инкубации растворимость повысилась на 10-30% при различных значениях рН. В соответствии с этим тестом как форма А, так и форма В могут быть использованы для изготовления лекарственных средств. Пример 7. Фармакологические тесты. А) Оценка полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида при лечении алкогольной зависимости. Тесты проводили на линии крыс сардинийская, предпочитающая этиловый спирт" ("SardinianAlcohol preferring" (sP, т.е. на грызунах, генетически отобранных за их спонтанное потребление этилового спирта. Эти животные были приняты в качестве основной специальной модели в исследовательской программе в связи с тем, что эти крысы (содержащиеся в режиме свободного выбора между водой и 10% раствором этанола) потребляют большое количество этилового спирта (6-7 г/кг/сутки), что важно для тестируемого соединения (80-100%). В соответствии со стандартом эти крысы подвергались содержанию в домашних клетках в режиме свободного выбора между поилкой с 10% спиртом и поилкой с водой с неограниченным доступом(24 ч/сутки) и демонстрировали следующие особенности: суточная доза потребления спирта около 6 г/кг; предпочтительное соотношение (спиртовой раствор относительно общей жидкости) выше 80%; разбивка ежедневного потребления этилового спирта на 3-4 запоя, достижение уровня этилового спирта в крови(BALs-Blood Alcohol Levels) выше 50 мг% в каждом запое; индукцию фармацевтических эффектов (анксиолиз, стимуляция моторной деятельности) и регуляцию центрального механизма достижения гедонического уровня. Тест проводили в соответствии со следующими моделями. 1. Спонтанный прием этилового спирта недепривированными крысами линии sP. Согласно этой модели потребление этилового спирта в режиме выбора из двух поилок имитирует фазу человеческого алкоголизма "активное пьянство". Следовательно, протестированные активные соединения должны уменьшать склонность к употреблению этилового спирта у крыс. Исчерпывающие результаты этой модели демонстрируют, что полиморфная форма А в широком диапазоне доз (10-100 мг/кг) уменьшает потребление этилового спирта. Важно подчеркнуть, что антиалкогольный эффект был специфичным, что уменьшение потребления этилового спирта не было связано с седативным эффектом, о чем свидетельствует компенсаторное увеличение потребления крысами линииsP воды и нормальное потребление ими пищи (данные не приведены). На фиг. 8 А показаны результаты отдельного эксперимента. В частности, вводили дозы в 10, 20, 25 и 50 мг/кг полиморфной формы А, после чего оценивали потребление этилового спирта. Удивительно, но даже такие низкие дозы, как 10 мг/кг, значительно снижали потребление этилового спирта 2. Эффект алкогольной депривации у депривированных крыс линии sP. Для того чтобы более полно охарактеризовать антиалкогольный эффект полиморфной формы А,это соединение оценивали по эффекту алкогольной депривации (Alcohol Deprivation Effect (ADE. Эффект алкогольной депривации является хорошо описанным, временным увеличением потребления этилового спирта, которое происходит после периода абстиненции и является моделью характерного для рецидивов у алкоголиков компульсивного, неконтролируемого поиска этилового спирта и рискованного поведения. В соответствии с этой моделью крыс линии sP с опытом потребления этилового спирта подвергали двухнедельному периоду абстиненции, в течении которого они не получали доступа к этанолу. После этого периода перед отбоем животным вводили полиморфную форму А, а затем снова открывали доступ к этиловому спирту. Потребление этилового спирта измеряли через 1 ч после отбоя. Результаты приведены на фиг. 8 В и 8 С для высоких и низких доз кристаллической полиморфной формы А соответственно. Полиморфная форма А полностью подавляла эффект алкогольной депривации,демонстрируя очень хорошую активность в диапазоне доз 5-100 мг/кг. Более того, даже дозы ниже чем 5 мг/кг были способны полностью отменить излишнее потребление этилового спирта. Пример 8. Оценка фармакологической безопасности, токсикологических и генотоксических характеристик полиморфной формы А. 1. Фармакологическое исследование безопасности. Возможные негативные эффекты полиморфной формы А на ЦНС, сердечно-сосудистые, дыхательные и иммунные функции оценивали in vitro и in vivo (на крысах и собаках) в различных экспериментальных моделях. В in vivo тестах тестируемое соединение всегда давалось однократно перорально в дозах 100, 300 и 1000 мг/кг. А) ЦНС. Тест Ирвина и температура тела крыс. Нейроповеденческие эффекты полиморфной формы А исследовали в соответствии с тестом Ирвина с использованием стандартной батареи для наблюдений, которая позволяет оценивать активность как периферической, так и центральной нервной системы (например, двигательную активность, двигательную координацию, соматические сенсорные/двигательные рефлекторные ответы, автономные ответы); температуру тела измеряли посредством электронного термометра. При 100 мг/кг соединение индуцировало временное понижение спонтанной локомоторной активности; при более высоких дозах эффект на локомоцию был более выраженным, был более длительным и был ассоциирован с миорелаксантным эффектом и ослаблением восприятия. При 1000 мг/кг крысы демонстрировали следующие типы поведения: вставали на цыпочки, впадали в атаксию с последующим переходом в лежачее или распластанное положение; при этом все эффекты были обратимыми. 100 мг/кг не влияла на температуру тела, хотя при более высоких дозах было отмечено понижение температуры тела с длительностью вплоть до 4 ч. Продолжительность сна у крыс после введения гексобарбитала. Тест заключается в измерении длительности сна, индуцированного гексобарбиталом; субстанции с седативным или противосонным действием вызывают увеличение или уменьшение соответственно длительности сна, индуцированного гексобарбиталом. При минимальной дозе (100 мг/кг) не было отмечено каких-либо статистически значимых эффектов на время засыпания или на длительность сна. При промежуточной дозе было зафиксировано незначительное сокращение длительности сна, а при максимальной дозе наблюдалось значительное сокращение времени засыпания и длительности сна. Проконвульсивная активность у крыс. В этом исследовании изучали возможный проконвульсивный эффект полиморфной формы А, введенной в комбинации с дозой пентилентетразола, который индуцирует конвульсии; предварительная обработка субстанциями с проконвульсивными свойствами ведет к более быстрому появлению конвульсий. Полиморфная форма А во всех введенных дозах не показала статистически значимого проконвульсивного эффекта, хотя дозы от 100 до 300 мг/кг индуцировали увеличение времени появления конвульсий, что предполагает возможный антиконвульсивный эффект. В) Сердечно-сосудистая система.HERG клетки (клетки с геном специфических калиевых каналов сердца человека). Исследовали возможный блокирующий эффект полиморфной формы А на следовой ток HERG канала, фиксируемый в клетках HEK-293 (Human Embryonic Kidney cells - Человеческие эмбриональные почечные клетки) в стабильно трансфицированных кДНК гена HERGG-1. Способ заключается в измерении следового тока HERG каналов с помощью метода фиксации потенциала на целой клетке. Ингибирующие ток HERG каналов соединения распознавали по продленному кардиальному потенциалу действия и увеличенному QT-интервалу. Полученные данные показали, что полиморфная форма А не индуцирует статистически значимого ингибирования следового тока HERG каналов при 10-7 М; при концентрациях от 10-6 и 10-5 М наблюдалось незначительное и дозонезависимое снижение и только при максимальной протестированной концентрации, равной 10-4 М, снижение составило около 50%. Это четко говорит о том, что ингибирование никогда не достигнет значения 70%, которое считается пороговым значением для рассмотрения активности соединения в этом тесте. Волокна Пуркинье. Возможный негативный эффект полиморфной формы А на кардиальный потенциал действия оценивали на изолированных собачьих волокнах Пуркинье. Трансмембранный потенциал действия измеряли методом внутриклеточного микроэлектрода; этот способ рекомендуется для детекции способности вещества индуцировать пролонгацию QT-интервала. Полиморфная форма А в концентрациях 10-7, 10-6 и 10-5 М не обладает статистически значимым влиянием на параметры потенциала действия в соответствии либо с нормальной, либо с низкой частотой стимуляции; при очень высокой концентрации, 10-4 М, наблюдалось значительное сокращение длительности потенциала действия. При всех тестируемых концентрациях не было зафиксировано ни ранней, ни поздней следовой деполяризации. Эти результаты говорят о том, что, исходя из электрофизиологического профиля полиморфной формы А, не следует ожидать пируэтной желудочковой тахикардии (TDP (Torsade de Pointes или пролонгации QT-интервала; а полиморфная форма А может быть классифицирована среди препаратов, не способных индуцировать пируэтную желудочковую тахикардию или пролонгацию QT-интервала у человека.In vivo. Оценка деятельности сердечно-сосудистой системы бодрствующих собак. Оценивали любой возможный эффект перорально введенной полиморфной формы А в дозах 100,300 и 1000 мг/кг на кровяное давление, частоту сердечных сокращений и электрокардиограмму у бодрствующих собак, предварительно оборудованных телеметрическими передатчиками и способных свободно перемещаться. В первой части исследования фиксировали только телеметрические измерения; запись параметров начинали по меньшей мере за 24 ч до введения соединения и продолжали в течение 24 ч после приема. Во второй части исследования вводили только максимальную дозу в 1000 мг/кг и проводили перед обработкой и в течение 3 ч после обработки комплементарные исследования, такие как электрокардиограмма в 6 отведениях (отведения I, II, III, aVL, aVR и aVF), отбор проб крови и наблюдения за животными. Первая часть: Полиморфная форма А в дозе 100 мг/кг не индуцировала соответствующих изменений кровяного давления, частоты сердечных сокращений и электрокардиограммы (в частности, не было каких-либо изменений в морфологии Т-зубца). При введении доз 300 и 1000 мг/кг были отмечено небольшое повышение артериального давления (среднего, систолического и диастолического артериального давления), некоторое снижение длительности PR- и PQ-интервалов и небольшое увеличение длитель- 10017718 ности QT-интервала с поправкой на частоту сердечных сокращений по методу Сарма. Изменения, наблюдаемые при 300 мг/кг, были очень незначительными и изолированными и вследствие этого не связанными с фармакологически релевантным эффектом полиморфной формы А, таким как наблюдаемые при 1000 мг/кг изменения длительностей PR- и PQ-интервалов, в то же время увеличение длительностиQT-интервала скорректированного с частотой сердечных сокращений было ясно связано с эффектом полиморфной формы А, что свидетельствует об увеличении длительности вентрикулярной реполяризации. При всех тестируемых дозировках не наблюдалось каких-либо нарушений в электрокардиограмме (II отведение) и, в частности, не наблюдалось каких-либо изменений в морфологии Т-зубца. Вторая часть: Никаких нарушений не наблюдалось в электрокардиограмме в 6 отведениях перед и в течение 3 ч после введения полиморфной формы А в концентрации 1000 мг/кг. Всех животных вырвало в интервале между 0,5 и 17 ч после введения дозы. Анализ плазмы подтвердил присутствие полиморфной формы А в плазме в течение 3 ч после введения. Эти результаты показывают, что полиморфная форма А, введенная перорально в дозах 100, 300 и 1000 мг/кг, только в дозе 1000 мг/кг индуцирует небольшую гипертензию, связанную с увеличением длительности вентрикулярной реполяризации. С) Система дыхания. Оценка системы дыхания у бодрствующих крыс. Эффект полиморфной формы А на параметры дыхательной системы (частота дыхания, максимальные скорости вдоха и выдоха, время вдоха и выдоха, индекс сопротивления дыхательных путей, минутный объем и дыхательный объем) оценивали у бодрствующих крыс после однократного перорального введения. Параметры дыхательной системы измеряли методом общей плетизмографии. Полиморфная форма А в концентрации 100 мг/кг не оказывала какого-либо релевантного эффекта на параметры дыхательной системы, а в концентрации 300 и 1000 мг/мл индуцировала тахипноэ, связанное с временным уменьшением дыхательного объема. Не было выявлено каких-либо статистически значимых изменений в максимальных скоростях вдоха и выдоха, в минутном объеме и в индексе сопротивления дыхательных путей, что позволяет предположить, что тестируемое соединение не вызывает каких-либо угнетающих дыхательную систему либо бронхосуживающих эффектов.D) Иммунная система. Анализ бляшкообразующих клеток у крыс. Возможный эффект полиморфной формы А на иммунную систему оценивали способом бляшкообразующих клеток (Plaque Forming Cells (PCF на крысах, после перорального введения в течение 28 дней доз 150, 250 и 500 мг/кг. Способ основан на стимуляции иммунной системы антигенами (эритроцитами овечьей крови) и на оценке воздействия тестового объекта на иммунный ответ. Иммунный ответ оценивали путем измерения пропорции спленоцитов, продуцирующих антитела относительно антигена (бляшкообразующих клеток) в присутствии комплемента. Полученные в данном исследовании результаты показали, что полиморфная форма А обладает небольшой и дозонезависимой иммуносупрессирующей активностью; при низких протестированных дозах (150 и 250 мг/кг) существует сравнимый пограничный эффект, который только при максимальной дозе (500 мг/кг) становится ярко выраженным. Фактически,статистический анализ свидетельствует о статистической значимости только для 150 мг/кг, но не для 250 мг/кг; и эти данные указывают на то, что наблюдаемые при этих дозах эффекты могут быть связаны с обычно присутствующей в этом тесте вариабельностью, так как гетерогенность иммунного ответа часто наблюдается, что, вероятно, связано с индивидуальными различиями в иммунной чувствительности. Все упомянутые выше фармакологические исследования безопасности были проведены по правилам GLP в соответствии с руководством ICH S7A по фармакологической безопасности. 2. Токсикология и генотоксичность. Для поддержки клинического испытания тестируемого соединения, т.е. полиморфной формы А,проводили исследования по токсичности однократно или многократно введенных доз на грызунах и не грызунах. Исследования токсичности однократно введенной дозы проводили на мышах и крысах интраперитонеально (ip) и перорально (os). Исследования многократно введенных доз (введение в течение 28 дней, с последующим 14-дневным восстановительным периодом) проводили на крысах и собаках. Проводили тест Эймса и микроядерный тест для исследования генотоксического потенциала соединения. В табл. 8 просуммированы результаты исследований, проведенных с полиморфной формой А. Таблица 8 Исследования токсичности и генотоксичности полиморфной формы АNOEL: доза без видимого эффекта. Генотоксичность оценивали с помощью теста Эймса и микроядерного теста на крысах. Система учета обратных мутаций Salmonella Typhimurium (теста Эймса). Мутагенный потенциал полиморфной формы А оценивали in vitro с помощью системы учета обратных мутаций Salmonella Typhimurium в соответствии с нормативами ЕЭС. Тестируемое соединение не индуцировало генные мутации заменой пар оснований или сдвигом рамки считывания в геномах тестированных штаммов Salmonella typhimurium (ТА 1535, ТА 1537, ТА 98, ТА 100 и ТА 102) в диапазоне концентраций от 50 до 3000 мг/мл с или без метаболической активации. Следовательно, полиморфная форма А рассматривается как немутагенная в данной системе учета обратных мутаций Salmonellatyphimurium. Микроядерный тест. Для полиморфной формы А возможную кластогенную активность или активность в качестве потенциального веретенного яда исследовали путем обнаружения микронуклеированных полихроматических эритроцитов в костном мозге обработанных крыс. Исследования проводили в соответствии с нормативами ЕЭС. Способ заключается в поиске в полихроматических эритроцитах костного мозга наличия хромосомных фрагментов, или некоторого количества хромосом, которые могут возникнуть в результате делеций или действия яда на митотическое веретено. Кластогенные продукты могут вызывать хромосомные поломки во время митоза, а веретенные яды нарушают структуру митотического веретена. Не мигрирующий нормально ацентрический фрагмент хромосомы не остается в ядре дочерней клетки и появляется в цитоплазме. После этого этот фрагмент называется тельцем Хауэлла-Жолли или микроядром. Микроядро можно детектировать в полиморфных эритроцитах, так как эти клетки выталкивают свое основное ядро сразу после последнего митоза, при этом микроядро остается в них. Самцам и самкам крыс линии "Sprague Dawley" давали перорально 2000-1000-500 мг/кг полиморфной формы А, а через 24 и 48 ч после обработки отбирали их бедренные кости и выделяли клетки костного мозга. Полиморфная форма А не демонстрирует кластогенную активность при всех тестируемых дозах и периодах. характеризующаяся следующими углами дифракции пиков на порошковой дифрактограмме: 9,7; 12,0; 18,0; 24,1; 25,90,22. 2. Полиморфная форма А по п.1, характеризующаяся следующими пиками углов дифракции на порошковой дифрактограмме 0,2: 3. Полиморфная форма А по любому из пп.1, 2, характеризующаяся представленной на фиг. 1 порошковой дифрактограммой. 4. Полиморфная форма В N-[4-(трифторметил)бензил]-4-метоксибутирамида формулы (I) характеризующаяся следующими углами дифракции пиков на порошковой дифрактограмме: 11,7; 19,8; 22,3; 23,60,22. 5. Полиморфная форма В по п.4, характеризующаяся следующими пиками углов дифракции на порошковой дифрактограмме 0,2: 6. Полиморфная форма В по любому из пп.4, 5, характеризующаяся представленной на фиг. 2 порошковой дифрактограммой. 7. Способ получения полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.1-3, включающий следующие стадии:i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;ii) получение кристаллической полиморфной формы А из раствора неочищенногоN-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливают полиморфной формой А N-[4-(трифторметил)бензил]-4-метоксибутирамида. 8. Способ получения полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.4-6, включающий следующие стадии:i) реакцию 4-трифторметилбензиламина с 4-метилметоксибутиратом в присутствии катализатора для получения неочищенного N-[4-(трифторметил)бензил]-4-метоксибутирамида;ii) получение кристаллической полиморфной формы В из раствора неочищенногоN-[4-(трифторметил)бензил]-4-метоксибутирамида в органическом растворителе, в котором упомянутый раствор затравливают полиморфной формой В N-[4-(трифторметил)бензил]-4-метоксибутирамида. 9. Способ по п.7 или 8, в котором 4-трифторметилбензиламин получают реакцией 4-трифторметилбензальдегида с гидрохлоридом гидроксиламина по следующей схеме: 10. Способ по любому из пп.7-9, согласно которому на стадии (i) катализатором является 30% раствор метилата натрия в метаноле. 11. Способ по любому из пп.7-10, согласно которому органический растворитель выбирают из толуола и смеси этилацетата/н-гексана. 12. Способ по п.11, согласно которому органический растворитель является смесью этилацетата/нгексана. 13. Способ по п.12, согласно которому смесь этилацетата:н-гексана имеет соотношение от 1:4 до 1:2, предпочтительно около 1:3. 14. Фармацевтическая композиция для лечения наркомании или алкоголизма, содержащая в качестве активного ингредиента эффективное количество полиморфной формы А N-[4-(трифторметил)бензил]4-метоксибутирамида по любому из пп.1-3 и фармацевтически приемлемый носитель. 15. Фармацевтическая композиция для лечения наркомании или алкоголизма, содержащая в качестве активного ингредиента эффективное количество полиморфной формы В N-[4-(трифторметил)бензил]- 14017718 4-метоксибутирамида по любому из пп.4-6 и фармацевтически приемлемый носитель. 16. Фармацевтическая композиция по любому из пп.14, 15, в которой полиморфная форма А либо полиморфная форма В находится в количестве от 12,5 до 50 мас.%. 17. Применение полиморфной формы А N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.1-3 для изготовления лекарственного средства для лечения наркомании и алкоголизма. 18. Применение полиморфной формы В N-[4-(трифторметил)бензил]-4-метоксибутирамида по любому из пп.4-6 для изготовления лекарственного средства для лечения наркомании и алкоголизма. 19. Применение по п.17 или 18 для уменьшения добровольного потребления этилового спирта и/или для лечения синдрома абстиненции. 20. Применение по п.17 или 19, в котором полиморфная форма А N-[4-(трифторметил)бензил]-4 метоксибутирамида используется в дозе от 5 до 50 мг/кг. 21. Применение по п.20, в котором полиморфная форма А N-[4-(трифторметил)бензил]-4 метоксибутирамида используется в дозе от 5 до 10 мг/кг.
МПК / Метки
МПК: A61P 25/30, C07C 235/06, A61K 31/165
Метки: новые, метоксибутирамида, полиморфные, n-[4-(трифторметил)бензил]-4, формы
Код ссылки
<a href="https://eas.patents.su/19-17718-novye-polimorfnye-formy-n-4-triftormetilbenzil-4-metoksibutiramida.html" rel="bookmark" title="База патентов Евразийского Союза">Новые полиморфные формы n-[4-(трифторметил)бензил]-4- метоксибутирамида</a>
Предыдущий патент: Высокоэффективный котел
Следующий патент: Способ гербицидной обработки
Случайный патент: Трансгенный вектор, содержащий гуманизированный локус ig, и его применение для получения трансгенных животных