Способ синтеза соединений, пригодных для лечения гепатита с
Номер патента: 17173
Опубликовано: 30.10.2012
Авторы: Смит Майкл Дж., Дженг Пенг, Пэк Шон К., Хэмм Джейсон
Формула / Реферат
1. Способ получения соединения формулы (I)
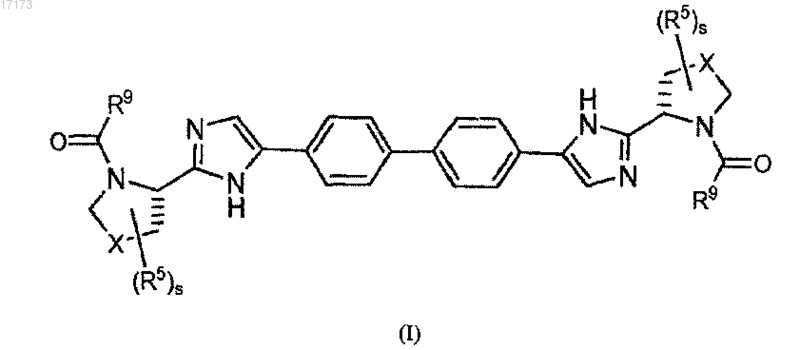
где s равен 0 или 1;
X выбран из СН2 или CHR5;
когда s равен 1, R5 представляет собой С1-С6алкил, где С1-С6алкил необязательно может образовывать конденсированное трехчленное кольцо с соседним атомом углерода;
при условии, что два гетероциклических кольца, замещающих имидазольные кольца, являются идентичными;
R9 представляет собой (NRcRd)С1-С6алкил;
Rc и Rd независимо выбраны из водорода, С2-С6алкенилоксикарбонила, С1-С6алкоксиС1-С6алкилкарбонила, С1-С6алкоксикарбонила, С1-С6алкила, C1-С6алкилкарбонила, С1-С6алкилсульфонила, арила, арилС1-С6алкоксикарбонила, арилС1-С6алкила, арилС1-С6алкилкарбонила, арилкарбонила, арилоксикарбонила, арилсульфонила, С3-С7циклоалкила, С3-С7циклоалкилсульфонила, формила, галоидС1-С6алоксикарбонила, гетероциклила, гетероциклилС1-С6алкоксикарбонила, гетероциклилС1-С6алкила, гетероциклилС1-С6алкилкарбонила, гетероциклилкарбонила, гетероциклилоксикарбонила, гидроксиС1-С6алкилкарбонила, (NReRf)С1-С6алкила, (NReRf)С1-С6алкилкарбонила, (NReRf)карбонила, (NReRf)сульфонила, -C(NCN)OR' и
-C(NCN)NRxRy, где R' выбран из С1-С6алкила и незамещенного фенила и где алкильная часть арилС1-С6алкила, арилС1-С6алкилкарбонила, гетероциклилС1-С6алкила, а также гетероциклилС1-С6алкилкарбонила, в свою очередь, могут быть замещены одним -NReRf и где арил, арильная часть арилоксикарбонила, арилС1-С6алкила, арилС1-С6алкилкарбонила, арилкарбонила, арилоксикарбонила и арилсульфонила, гетероциклил и гетероциклическая часть гетероциклилС1-С6алкоксикарбонила, гетероциклилС1-С6алкила, гетероциклилС1-С6алкилкарбонила, гетероциклилкарбонила и гетероциклилоксикарбонила также могут быть замещены одним, двумя или тремя заместителями, независимо выбранными из C1-С6алкокси, С1-С6алкила, циано, галоида, галоидС1-С6алкокси, галоидС1-С6алкила и нитро;
Re и Rf независимо выбраны из водорода, алкила, незамещённого арила, незамещённого арилалкила, незамещённого циклоалкила, незамещённого (циклоалкил)алкила, незамещённого гетероциклила, незамещённого гетероциклилалкила, (NRxRy)алкила и (NRxRy)карбонила;
Rx и Ry независимо выбраны из водорода, алкоксикарбонила, алкила, алкилкарбонила, незамещённого арила, незамещённого арилалкоксикарбонила, незамещённого арилалкила, незамещённого циклоалкила, незамещённого гетероциклила и (NRx'Ry')карбонила, при этом Rx' и Ry' независимо выбраны из водорода и алкила;
при этом арил относится к фенильной группе или к бициклической конденсированной кольцевой системе, состоящей из фенильной группы, конденсированной с 4-6-членным ароматическим или неароматическим карбоциклическим кольцом;
гетероциклил относится к 4-, 5-, 6- или 7-членному кольцу, содержащему один, два, три или четыре гетероатома, независимо выбранных из азота, кислорода или серы, а также к бициклическим группам, в которых гетероциклическое кольцо является конденсированным с другим моноциклическим гетероциклом или 4-6-членным ароматическим или неароматическим карбоциклическим кольцом; а также мостиковым бициклическим группам и может присоединяться к родительской молекуле через любой атом углерода или атом азота в группе;
при этом способ включает:
(а) взаимодействие соединения формулы (3)
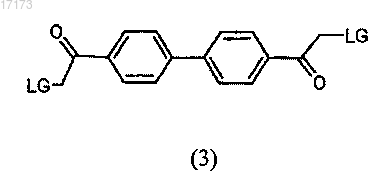
где LG - удаляемая группа;
с соединением формулы (4)
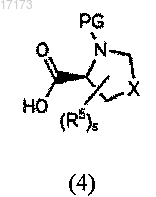
где PG - группа, защищающая атом азота;
(б) обработку продукта со стадии (а) реагентом, выбранным из ацетата аммония, формиата аммония, сульфамата аммония, фосфата аммония, цитрата аммония, карбамата аммония и аммиака; и
(в) обработку продукта со стадии (б) агентом, снимающим защиту с получением соединения формулы (7)
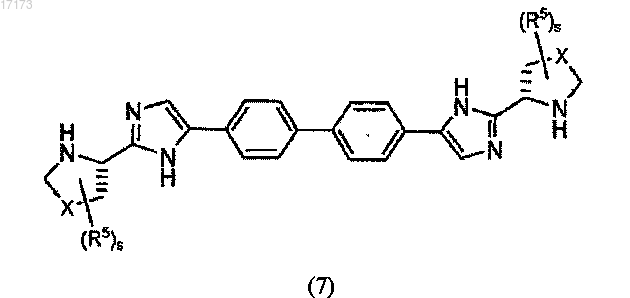
(г) обработку соединения формулы (7) соединением формулы (8)

где R9 обозначает радикалы, указанные выше.
2. Способ получения соединения формулы (7)
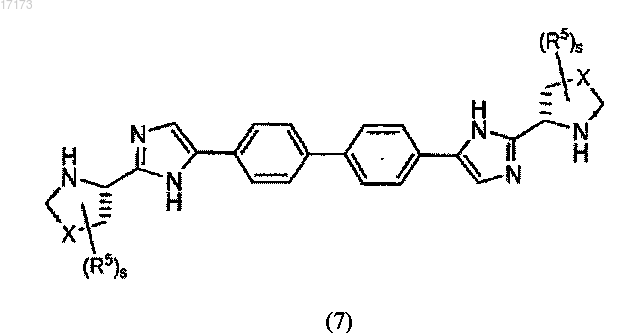
или его фармацевтически приемлемой соли,
где s равен 0 или 1;
X выбран из CH2 или CHR5;
когда s равен 1, R5 представляет собой С1-С6алкил, где С1-С6алкил необязательно может образовывать конденсированное трехчленное кольцо с соседним атомом углерода;
при условии, что два гетероциклических кольца, замещающих имидазольные кольца, являются идентичными; причем указанный способ включает:
(а) взаимодействие соединения формулы (3)
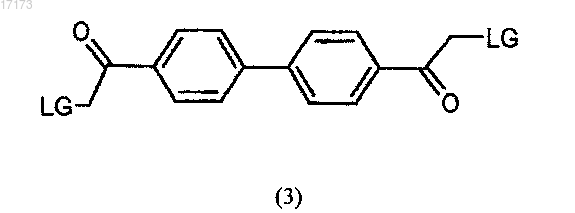
где LG - удаляемая группа;
с соединением формулы (4)
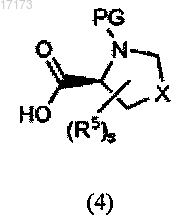
где PG - группа, защищающая атом азота;
(б) обработку продукта со стадии (а) реагентом, выбранным из ацетата аммония, формиата аммония, сульфамата аммония, фосфата аммония, цитрата аммония, карбамата аммония и аммиака; и
(в) обработку продукта со стадии (б) агентом, снимающим защиту.
3. Способ по п.1 или 2, отличающийся тем, что s равен 0 и X обозначает CH2.
4. Способ по п.1 или 2, отличающийся тем, что LG обозначает галоид.
5. Способ по п.4, отличающийся тем, что галоид представляет собой бром.
6. Способ по п.1 или 2, отличающийся тем, что стадию (а) проводят в присутствии основания.
7. Способ по п.6, отличающийся тем, что основание представляет собой диизопропилэтиламин.
8. Способ по п.1 или 2, отличающийся тем, что реагент, применяемый на стадии (б), представляет собой ацетат аммония.
9. Способ по п.1 или 2, отличающийся тем, что PG обозначает формулу
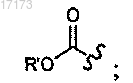 где
гдеобозначает точку присоединения к родительской молекуле и
R' выбран из С1-С6алкила, арила и арилС1-С6алкила.
10. Способ по п.9, отличающийся тем, что PG обозначает трет-бутоксикарбонил.
11. Способ по п.10, отличающийся тем, что агент для снятия защиты на стадии (в) представляет собой кислоту.
12. Способ по п.11, отличающийся тем, что кислота представляет собой соляную кислоту.
Текст
СПОСОБ СИНТЕЗА СОЕДИНЕНИЙ, ПРИГОДНЫХ ДЛЯ ЛЕЧЕНИЯ ГЕПАТИТА С Изобретение относится к способу синтеза гидрохлоридной соли метил-1S)-1-2S)-2-(5-(4'-(22S)-2-метоксикарбонил)амино)-3-метилбутаноил)-2-пирролидинил)-1H-имидазол-5-ил)-4-бифенилил)-1H-имидазол-2-ил)-1-пирролидинил)карбонил)-2-метилпропил)карбамата. Изобретение относится также к промежуточным соединениям, применяемым при осуществлении этого способа. 017173 Данное изобретение относится, в общем, к способу синтеза метил-1S)-1-2S)-2-(5-(4'-(2-2S)-2 метоксикарбонил)амино)-3-метилбутаноил)-2-пирролидинил)-1H-имидазол-5-ил)-4-бифенилил)-1H-имидазол-2-ил)-1-пирролидинил)карбонил)-2-метилпропил)карбамат дигидрохлорида. Оно относится также к промежуточным соединениям, используемым при осуществлении этого способа. Вирус гепатита С (HCV) представляет собой основной патоген человека, поражающий 170 млн людей по всему миру - почти в 5 раз больше, чем количество людей, инфицированных вирусом иммунодефицита человека типа I. У значительной части этих инфицированных HCV людей развивается серьзное прогрессирующее заболевание печени, включая цирроз и печеночно-клеточную карциному. В настоящее время наиболее эффективная терапия HCV использует комбинацию альфаинтерферона и рибавирина, которая приводит к эффективному результату в 40% случаев. Недавние клинические результаты показывают, что пэгилированный альфа-интерферон превосходит немодифицированный альфа-интерферон в случае монотерапии. Однако даже при использовании экспериментальных схем прима, включающих комбинации пэгилированного альфа-интерферона и рибавирина у значительной части пациентов не наблюдается существенного снижения вирусной нагрузки. Следовательно, существует чткая и неудовлетворнная потребность в создании эффективных терапевтических средств для лечения инфекции HCV. Соединение метил-1S)-1-2S)-2-(5-(4'-(2-2S)-2-метоксикарбонил)амино)-3-метилбутаноил)-2 пирролидинил)-1H-имидазол-5-ил)-4-бифенилил)-1H-имидазол-2-ил)-1-пирролидинил)карбонил)-2-метилпропил)карбамат дигидрохлорид пригодно для лечения инфекции HCV Для промышленного производства необходимо разработать способ синтеза соединения (I) и родственных аналогов, являющийся эффективным, экономичным и обеспечивающим высокий выход этого соединения. Согласно первому аспекту данное изобретение предусматривает способ получения соединения формулы (7) или его фармацевтически приемлемой соли,где s равен 0 или 1;X выбран из CH2 или CHR5; когда s равен 1, R5 представляет собой С 1-С 6 алкил, где С 1-С 6 алкил необязательно может образовывать конденсированное трехчленное кольцо с соседним атомом углерода; при условии, что два гетероциклических кольца, замещающих имидазольные кольца, являются идентичными; причм указанный способ включает:(а) взаимодействие соединения формулы (3)(б) обработку продукта со стадии (а) реагентом, выбранным из ацетата аммония, формиата аммония, сульфамата аммония, фосфата аммония, цитрата аммония, карбамата аммония и аммиака; и(в) обработку продукта со стадии (б) агентом, снимающим защиту. Согласно первому варианту осуществления способа s равен 0 и X обозначает СН 2. По второму варианту LG обозначает галоид. По третьему варианту галоид является бромом. По четвртому варианту осуществления изобретения стадию (а) проводят в присутствии основания. Согласно пятому варианту осуществления изобретения основание является диизопропилэтиламином. По шестому варианту осуществления изобретения реагент, применяемый на стадии (б), представляет собой ацетат аммония. Согласно седьмому варианту осуществления изобретения PG обозначает формулу где обозначает точку присоединения к части родительской молекулы иR' выбран из алкила, арила и арилалкила. Согласно восьмому варианту PG обозначает трет-бутоксикарбонил. Агент для снятия защиты на стадии (в) является кислотой, в частности соляной кислотой. Согласно второму аспекту данного изобретения предусмотрен способ получения соединения формулы (I)X выбран из CH2 или CHR5 и когда s равен 1, R5 представляет собой С 1-С 6 алкил, где С 1-С 6 алкил необязательно может образовывать конденсированное трехчленное кольцо с соседним атомом углерода; при условии, что два гетероциклических кольца, замещающих имидазольные кольца, являются идентичными;Rc и Rd независимо выбраны из водорода, С 2-С 6 алкенилоксикарбонила, C1-С 6 алкоксиС 1 С 6 алкилкарбонила, С 1-С 6 алкоксикарбонила, С 1-С 6 алкила, С 1-С 6 алкилкарбонила, С 1-С 6 алкилсульфонила,арила, арилС 1-С 6 алкоксикарбонила, арилС 1-С 6 алкила, арилС 1-С 6 алкилкарбонила, арилкарбонила, арилоксикарбонила, арилсульфонила, C3-С 7 циклоалкила, C3-С 7 циклоалкилсульфонила, формила, галоидС 1 С 6 алоксикарбонила, гетероциклила, гетероциклилС 1-С 6 алкоксикарбонила, гетероциклилС 1-С 6 алкила,гетероциклилС 1-С 6 алкилкарбонила, гетероциклилкарбонила, гетероциклил оксикарбонила, гидроксиС 1 С 6 алкилкарбонила,(NReRf)С 1-С 6 алкила,(NReRf)С 1-С 6 алкилкарбонила,(NReRf)карбонила,e f(NR R )сульфонила, -C(NCN)OR' и -C(NCN)NR R , где R' выбран С 1-С 6 алкила и незамещенного фенила и где алкильная часть арилС 1-С 6 алкила, арилС 1-С 6 алкилкарбонила, гетероциклилС 1-С 6 алкила, а также гетероциклилС 1-С 6 алкилкарбонила, в свою очередь, может быть замещена одним -NReRf и где арил, арильная часть арилоксикарбонила, арилС 1-С 6 алкила, арилС 1-С 6 алкилкарбонила, арилкарбонила, арилоксикарбонила и арилсульфонила,гетероциклил и гетероциклическая часть гетероциклилС 1 С 6 алкоксикарбонила, гетероциклилС 1-С 6 алкила, гетероциклилС 1-С 6 алкилкарбонила, гетероциклилкарбонила и гетероциклилоксикарбонила также могут быть замещены одним, двумя или тремя заместителями,независимо выбранными из С 1-С 6 алкокси, С 1-С 6 алкила, циано, галоида, галоидС 1-С 6 алкокси, галоидС 1 С 6 алкила и нитро;Re и Rf независимо выбраны из водорода, алкила, незамещнного арила, незамещнного арилалкила, незамещнного циклоалкила, незамещнного (циклоалкил)алкила, незамещнного гетероциклила,незамещнного гетероциклилалкила, (NRxRy)алкила и (NRxRy)карбонила;Rx и Ry независимо выбраны из водорода, алкоксикарбонила, алкила, алкилкарбонила, незамещнного арила, незамещнного арилалкоксикарбонила, незамещнного арилалкила, незамещнного циклоалкила, незамещнного гетероциклила и (NRx'Ry')карбонила, при этом Rx' и Ry' независимо выбраны из водорода и алкила; при этом арил относится к фенильной группе или к бициклической конденсированной кольцевой системе, состоящей из фенильной группы, конденсированной с 4-6-членным ароматическим или неароматическим карбоциклическим кольцом; гетероциклил относится к 4-, 5-, 6- или 7-членному кольцу, содержащему один, два, три или четыре-2 017173 гетероатома, независимо выбранных из азота, кислорода или серы, а также к бициклическим группам, в которых гетероциклическое кольцо является конденсированным с другим моноциклическим гетероциклом или 4-6-членным ароматическим или неароматическим карбоциклическим кольцом; а также мостиковым бициклическим группам, и может присоединяться к родительской молекуле через любой атом углерода или атом азота в группе; при этом способ включает:(а) взаимодействие соединения формулы (3)(б) обработку продукта со стадии (а) реагентом, выбранным из ацетата аммония, формиата аммония, сульфамата аммония, фосфата аммония, цитрата аммония, карбамата аммония и аммиака; и(в) обработку продукта со стадии (б) агентом, снимающим защиту с получением соединения формулы (7)(г) обработку соединения формулы (7) соединением формулы (8) где R9 обозначает радикалы, указанные выше. Согласно первому варианту второго способа по изобретению s равен 0 и X обозначает CH2. По второму варианту LG обозначает галоид. По третьему варианту галоидом является бром. По четвртому варианту второго способа по изобретению стадию (а) проводят в присутствии основания. Согласно пятому варианту основание является диизопропилэтиламином. По шестому варианту реагент, применяемый на стадии (б), представляет собой ацетат аммония. Согласно седьмому варианту второго способа PG обозначает формулу где обозначает точку присоединения к части родительской молекулы иR' выбран из алкила, арила и арилалкила. Согласно пятому варианту второго аспекта PG обозначает трет-бутоксикарбонил. Согласно восьмому варианту агент для снятия защиты на стадии (в) является кислотой, в частности соляной кислотой. Другие варианты данного изобретения могут включать комбинации двух или более описанных здесь вариантов и/или аспектов. Дальнейшие варианты и аспекты данного изобретения станут очевидны из описания, приведнного ниже. Соединения согласно данному изобретению существуют как таутомеры; следовательно, изобретение охватывает все таутомерные формы заявленных соединений. В данном описании используются термины, имеющие следующие значения. Термины "алкенил" относится к линейной или разветвлнной группе, содержащей 2-6 атомов углерода и по меньшей мере одну двойную связь.-3 017173 Термин "алкенилокси", применяемый в данной заявке, относится к алкенильной группе, присоединнной к родительской молекуле через атом кислорода. Термин "алкенилоксикарбонил" в данной заявке относится к алкенильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "алкокси" в данной заявке относится к алкильной группе, присоединнной к родительской молекуле через атом кислорода. Термин "алкоксиалкил" в данной заявке относится к алкильной группе, замещнной одной, двумя или тремя алкоксигруппами. Термин "алкоксиалкилкарбонил" в данной заявке относится к алкоксиалкильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "алкоксикарбонил" в данной заявке относится к алкоксигруппе, присоединнной к родительской молекуле через карбонильную группу. Термин "алкоксикарбонилалкил" в данной заявке относится к алкильной группе, замещнной одной, двумя или тремя алкоксикарбонильными группами. Термин "алкил" в данной заявке относится к группе на основе линейного или разветвлнного углеводорода, содержащего 1-6 атомов углерода. В соединениях по изобретению, когда m и/или n равен 1 или 2; X или Y обозначают CHR5 и/или CHR6 соответственно, и R5 и/или R6 обозначают алкил, и каждый алкил может образовать конденсированное 3-6-членное кольцо вместе с соседним атомом углерода с образованием одной из структур, показанных ниже:R50 обозначает алкил. Когда w равен 2, два R50 могут быть одинаковыми или разными. Термин "алкилкарбонил" в данной заявке относится к алкильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "алкилкарбонилалкил" в данной заявке относится к алкильной группе, замещнной одной,двумя или тремя алкилкарбонильными группами. Термин "алкилкарбонилокси" в данной заявке относится к алкилкарбонильной группе, присоединнной к родительской молекуле через атом кислорода. Термин "алкилсульфанил" в данной заявке относится к алкильной группе, присоединнной к родительской молекуле через атом серы. Термин "алкилсульфонил" в данной заявке относится к алкильной группе, присоединнной к родительской молекуле через сульфонильную группу. Термин "арил", применяемый в данной заявке, относится к фенильной группе или к бициклической конденсированной кольцевой системе, в которой одно или оба кольца представляют собой фенильную группу. Бициклические конденсированные кольцевые системы состоят из фенильной группы, конденсированной с 4-6-членным ароматическим или неароматическим карбоциклическим кольцом. Арильные группы могут быть присоединены к родительской молекуле через любой способный к замещению атом углерода в группе. Примеры арильных групп включают, но без ограничения, инданил, инденил, нафтил,фенил и тетрагидронафтил. Арильные группы согласно данному изобретению могут быть замещены одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранными из алкокси, алкоксиалкила, алкоксикарбонила, алкила, алкилкарбонила, второй арильной группы, арилалкокси, арилалкила,арилкарбонила, циано, гало, галоидалкокси, галоидалкила, гетероциклила, гетероциклилалкила, гетероциклилкарбонила, гидрокси, гидроксиалкила, нитро, -NRxRy, (NRxRy)алкила, оксо и -P(O)OR2, где каждый R независимо выбран из водорода и алкила, где алкильная часть арилалкила и гетероциклилалкила является незамещнной и где вторая арильная группа, арильная часть арилалкила, арильная часть арилкарбонила, гетероциклил и гетероциклическая часть гетероциклилалкила и гетероциклилкарбонила могут быть замещены одним, двумя или тремя заместителями, независимо выбранными из алкокси, алкила,циано, гало, галоидалкокси, галоидалкила и нитро. Термин "арилалкенил" в данной заявке относится к алкенильной группе, замещнной одной, двумя или тремя арильными группами. Термин "арилокси", применяемый в данной заявке, относится к арильной группе, присоединнной к родительской молекуле через группу алкокси. Термин "арилалкоксиалкил" в данной заявке относится к алкильной группе, замещнной одной,двумя или тремя арилоксильными группами.-4 017173 Термин "арилалкоксиалкилкарбонил", применяемый в данной заявке, относится к арилалкоксиалкильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "арилалкоксикарбонил" в данной заявке относится к арилалкоксильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "арилалкил" в данной заявке относится к алкильной группе, замещнной одной, двумя или тремя арильными группами. Алкильная часть арилалкильной группы может быть замещена одной или двумя дополнительными группами, независимо выбранными из алкокси, алкилкарбонилокси, галоида,галоидалкокси, галоидалкила, гетероциклила, гидрокси и -NRcRd, где гетероциклил может быть замещн одним или двумя заместителями, независимо выбранными из алкокси, алкила, незамещнного арила,незамещнного арилалкокси, незамещнного арилалкоксикарбонила, галоида, галоидалкокси, галоидалкила, гидрокси и -NRxRy. Термин "арилалкилкарбонил" в данной заявке относится к арилалкильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "арилкарбонил" в данной заявке относится к арильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "арилокси" в данной заявке относится к арильной группе, присоединнной к родительской молекуле через атом кислорода. Термин "арилоксиалкил" в данной заявке относится к алкильной группе, замещнной одной, двумя или тремя группами арилокси. Термин "арилоксикарбонил", применяемый в данной заявке, относится к арилоксигруппе, присоединнной к родительской молекуле через карбонильную группу. Термин "арилсульфонил", применяемый в данной заявке, относится к арильной группе, присоединнной к родительской молекуле через сульфонильную группу. Термин "основание" в данной заявке относится к реагенту, способному присоединять протоны во время реакции, не действующему как нуклеофил. Примеры оснований включают дисилиламиды, такие как гексаметилдисилазид лития, не нуклеофильные амины, такие как триэтиламин, диизопропилэтиламин и диизопропиламин гетероциклические амины, такие как имидазол, пиридин, пиридазин и пиримидин, и бициклические амины, такие как DBN (1,5-диазабицикло[4.3.0]нон-5-ен) и DBU (1,8 диазабицикло[5.4.0]ундец-7-ен). Выбор основания для конкретной реакции превращения зависит от природы исходных материалов, растворителя или растворителей, в которых проводится реакция, и температуры, при которой проводится реакция. Термин "карбонил" в данной заявке относится к -С(О)-. Термин "карбокси" в данной заявке относится к -CO2H. Термин "циано" в данной заявке относится к -CN. Термин "циклоалкил" в данной заявке относится к насыщенному моноциклическому углеводородному кольцевому фрагменту, содержащему 3-7 атомов углерода и не содержащему гетероатомов. Примеры циклоалкильных групп включают, но без ограничения, циклопропил, циклопентил и циклогексил. Циклоалкильные группы согласно изобретению могут быть замещены одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранными из алкокси, алкила, арила, циано, галоида, галоидалкила, гетероциклила, гидрокси, гидроксиалкила, нитро и -NRxRy, причм арил и гетероциклил также могут быть замещены одним, двумя или тремя заместителями, независимо выбранными из алкокси, алкила,арила, циано, галоида, галоидалкокси, галоидалкила, гидрокси и нитро. Термин "(циклоалкил)алкенил" в данной заявке относится к алкенильной группе, замещнной одной, двумя или тремя циклоалкильными группами. Термин "(циклоалкил)алкил" в данной заявке относится к алкильной группе, замещнной одной,двумя или тремя циклоалкильными группами. Алкильная часть (циклоалкил)алкила также может быть замещена одной или двумя группами, независимо выбранными из гидрокси и -NRcRd. Термин "циклоалкилокси", применяемый в данной заявке, относится к циклоалкильной группе,присоединнной к родительской молекуле через атом кислорода. Термин "циклоалкилоксиалкил" в данной заявке относится к алкильной группе, замещнной одной,двумя или тремя циклоалкилоксигруппами. Термин "циклоалкилсульфонил", применяемый в данной заявке, относится к циклоалкильной группе, присоединнной к родительской молекуле через сульфонильную группу. Термин "агент для снятия защиты", применяемый в данной заявке, относится к веществу, способному к удалению группы, защищающей атом азота. Примеры агентов для снятия защиты включают кислоты, такие как трифторуксусная кислота и соляная кислота, силилирующие агенты, такие как триметилсилилйодид, и циклические амины, такие как морфолин. Дополнительные примеры агентов для снятия защиты, а также примеры защитных групп, которые удаляются при помощи этих агентов, можно найти в Greene, Т.W. and Wuts, P.G.M., "Protective Groups in Organic Synthesis", 3rd edition. Термин "формил", применяемый в данной заявке, относится к -СНО. Термины "гало" и "галоид", применяемые в данной заявке, относятся к F, Cl, Br или I. Термин "галоидалкокси", применяемый в данной заявке, относится к галоидалкильной группе, при-5 017173 соединнной к родительской молекуле через атом кислорода. Термин "галоидалкоксикарбонил", применяемый в данной заявке, относится к галоидалкоксильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "галоидалкил", применяемый в данной заявке, относится к алкильной группе, замещнной одним, двумя, тремя или четырьмя атомами галоида. Термин "гетероциклил", применяемый в данной заявке, относится к 4-, 5-, 6- или 7-членному кольцу, содержащему один, два, три или четыре гетероатома, независимо выбранных из азота, кислорода или серы. В четырхчленном кольце нет двойных связей, кольцо с пятью членами имеет 0-2 двойных связи и кольца с шестью и семью членами содержат 0-3 двойных связи. Термин "гетероциклил" включает также бициклические группы, в которых гетероциклическое кольцо является конденсированным с другим моноциклическим гетероциклом или 4-6-членным ароматическим или неароматическим карбоциклическим кольцом; а также мостиковые бициклические группы, такие как 7-азабицикло[2.2.1]гепт-7-ил, 2 азабицикло[2.2.2]окт-2-ил и 2-азабицикло[2.2.2]окт-3-ил. Гетероциклические группы согласно изобретению могут присоединяться к родительской молекуле через любой атом углерода или атом азота в группе. Примеры гетероциклических групп включают, но без ограничения, бензотиенил, фурил, имидазолил,индолинил, индолил, изотиазолил, изоксазолил, морфолинил, оксазолил, пиперазинил, пиперидинил,пиразолил, пиридинил, пирролидинил, пирролопиридинил, пирролил, тиазолил, тиенил, тиоморфолинил,7-азабицикло[2.2.1]гепт-7-ил, 2-азабицикло[2.2.2]окт-2-ил и 2-азабицикло[2.2.2]окт-3-ил. Гетероциклические группы согласно изобретению могут быть замещены одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранными из алкокси, алкоксиалкила, алкоксикарбонила, алкила, алкилкарбонила, арила, арилалкила, арилкарбонила, циано, галоида, галоидалкокси, галоидалкила, второго гетероциклила, гетероциклилалкила, гетероциклилкарбонила, гидрокси, гидроксиалкила, нитро,-NRxRy, (NRxRy)алкила и оксо, при этом алкильные части арилалкила и гетероциклилалкила являются незамещнными и арил, арильная часть арилалкила, арильная часть арилкарбонила второй гетероциклической группы и гетероциклическая часть гетероциклилалкила и гетероциклилкарбонила, в свою очередь, могут быть замещены одним, двумя или тремя заместителями, независимо выбранными из алкокси,алкила, циано, галоида, галоидалкокси, галоидалкила и нитро. Термин "гетероциклилалкенил", применяемый в данной заявке, относится к алкенильной группе,замещнной одной, двумя или тремя гетероциклическими группами. Термин "гетероциклилалкокси", применяемый в данной заявке, относится к гетероциклической группе, присоединнной к родительской молекуле через алкоксильную группу. Термин "гетероциклилалкоксикарбонил", применяемый в данной заявке, относится к гетероциклилалкоксильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "гетероциклилалкил", применяемый в данной заявке, относится к алкильной группе, замещнной одной, двумя или тремя гетероциклическими группами. Алкильная часть гетероциклилалкила, в свою очередь, может быть замещена одной или двумя дополнительными группами, независимо выбранными из алкокси, алкилкарбонилокси, арила, галоида, галоидалкокси, галоидалкила, гидрокси и -NRcRd, при этом арил может быть замещн одним или двумя заместителями, независимо выбранными из алкокси, алкила, незамещнного арила, незамещнного арилалкокси, незамещнного арилалкоксикарбонила, галоида, галоидалкокси, галоидалкила, гидрокси и-NRxRy. Термин "гетероциклилкарбонил", применяемый в данной заявке, относится к гетероциклической группе, присоединнной к родительской молекуле через карбонильную группу. Термин "гетероциклилокси", применяемый в данной заявке, относится к гетероциклической группе,присоединнной к родительской молекуле через атом кислорода. Термин "гетероциклилоксиалкил", применяемый в данной заявке, относится к алкильной группе,замещнной одной, двумя или тремя гетероциклилокси группами. Термин "гетероциклилоксикарбонил", применяемый в данной заявке, относится к гетероциклилоксигруппе, присоединнной к родительской молекуле через карбонильную группу. Термин "гидрокси" в данной заявке относится к -ОН. Термин "гидроксиалкил" в данной заявке относится к алкильной группе, замещнной одной, двумя или тремя гидроксильными группами. Термин "гидроксиалкилкарбонил" в данной заявке относится к гидроксиалкильной группе, присоединнной к родительской молекуле через карбонильную группу. Термин "удаляемая группа", применяемый в данной заявке, относится к группе, которая способна замещаться нуклеофилом в реакции SN2. Примеры удаляемых групп включают сульфонаты, такие как тозилат, мезилат и бензилсульфонат; и атомы галоида, такие как бром, хлор и йод. Термин "нитро" относится к -NO2. Термин "-NRcRd", применяемый в данной заявке, относится к двум группам, Rc и Rd, которые присоединены к родительской молекуле через атом азота. Rc и Rd независимо выбраны из водорода, алкенилоксикарбонила, алкоксиалкилкарбонила, алкоксикарбонила, алкила, алкилкарбонила, алкилсульфонила,арила, арилалкоксикарбонила, арилалкила, арилалкилкарбонила, арилкарбонила, арилоксикарбонила,-6 017173 арилсульфонила, циклоалкила, циклоалкилсульфонила, формила, галоидалоксикарбонила, гетероциклила, гетероциклилалкоксикарбонила, гетероциклилалкила, гетероциклилалкилкарбонила, гетероциклилкарбонила,гетероциклилоксикарбонила,гидроксиалкилкарбонила,(NReRf)алкила,e f(NR R )алкилкарбонила, (NR R )карбонила, (NR R )сульфонила, -C(NCN)OR' и -C(NCN)NRxRy, где R' выбран из алкила и незамещнного фенила и где алкильная часть арилалкила, арилаклилкарбонила, гетероциклилалкила, а также гетероциклилалкилкарбонила, в свою очередь, могут быть замещены одним-NReRf и где арил, арильная часть арилоксикарбонила, арилалкила, арилалкилкарбонила, арилкарбонила,арилоксикарбонила и арилсульфонила, гетероциклил и гетероциклическая часть гетероциклилалкоксикарбонила, гетероциклилалкила, гетероциклилалкилкарбонила, гетероциклилкарбонила и гетероциклилоксикарбонила также могут быть замещены одним, двумя или тремя заместителями, независимо выбранными из алкокси, алкила, циано, галоида, галоидалкокси, галоидалкила и нитро. Термин "(NRcRd)алкенил", применяемый в данной заявке, относится к алкенильной группе, замещнной одной, двумя или тремя группами -NRcRd. Термин "(NRcRd)алкил", применяемый в данной заявке, относится к алкильной группе, замещнной одной, двумя или тремя группами -NRcRd. Алкильная часть (NRcRd)алкила также может быть замещена одной или двумя дополнительными группами, выбранными из алкокси, алкоксиалкилкарбонила, алкоксикарбонила, алкилсульфанила, арилалкоксиалкилкарбонила, карбокси, гетероциклила, гетероциклилкарбонила, гидрокси и (NReRf)карбонила; при этом гетероциклил может быть также может быть замещн одним, двумя, тремя, четырьмя или пятью заместителями, независимо выбранными из алкокси, алкила,циано, галоида, галоидалкокси, галоидалкила и нитро. Термин "(NRcRd)карбонил", применяемый в данной заявке, относится к группе NRcRd, присоединнной к родительской молекуле через карбонильную группу. Термин "-NReRf", применяемый в данной заявке, относится к двум группам, Re и Rf, которые присоединены к родительской молекуле через атом азота. Re и Rf независимо выбраны из водорода, алкила,незамещнного арила, незамещнного арилалкила, незамещнного циклоалкила, незамещнного (циклоалкил)алкила, незамещнного гетероциклила, незамещнного гетероциклилалкила, (NRxRy)алкила и(NRxRy)карбонила. Термин "(NReRf)алкил", применяемый в данной заявке, относится к алкильной группе, замещнной одной, двумя или тремя группами -NReRf. Термин "(NReRf)алкилкарбонил", применяемый в данной заявке, относится к группе (NReRf)алкил,присоединнной к родительской молекуле через карбонильную группу. Термин "(NReRf)карбонил", применяемый в данной заявке, относится к группе -NReRf, присоединнной к родительской молекуле через карбонильную группу. Термин "(NReRf)сульфонил", применяемый в данной заявке, относится к группе -NReRf, присоединнной к родительской молекуле через сульфонильную группу. Термин "-NRxRy", применяемый в данной заявке, относится к двум группам, Rx и Ry, присоединнным к родительской молекуле через атом азота. Rx и Ry независимо выбраны из водорода, алкоксикарбонила, алкила, алкилкарбонила, незамещнного арила, незамещнного арилалкоксикарбонила, незамещнного арилалкила, незамещнного циклоалкила, незамещнного гетероциклила и (NRxRy)карбонила,при этом Rx и Ry независимо выбраны из водорода и алкила. Термин "(NRxRy)алкил", применяемый в данной заявке, относится к алкильной группе, замещнной одной, двумя или тремя группами -NRxRy. Термин "(NRxRy)карбонил" в данной заявке относится к группе -NRxRy, присоединнной к родительской молекуле через карбонильную группу. Термин "оксо" в данной заявке относится к =O. Термин "группа, защищающая атом азота" в данной заявке относится к группе, которая должна защищать аминогруппу от нежелательных реакций во время синтеза. Обычные группы, защищающие атом азота, включают ацильные группы, такие как ацетил, бензоил, 2-бромацетил, 4-бромбензоил, третбутилацетил, карбоксальдегидную группу, 2-хлорацетил, 4-хлорбензоил, -хлорбутирил, 4 нитробензоил, о-нитрофеноксиацетил, фталил, пивалоил, пропионил, трихлорацетил и трифторацетил; сульфонильные группы, такие как бензосульфонил и п-толуолсульфонил; группы, образующие карбаматы, такие как бензилоксикарбонил (Cbz), трет-бутилоксикарбонил (Boc), п-хлор-бензилоксикарбонил, пметилоксибензилоксикарбонил и т.п. Термин "сульфонил" в данной заявке относится к -SO2-. Все способы согласно данному изобретению могут проводиться непрерывно. Термин "непрерывный способ", применяемый в данной заявке, означает, что стадии процесса осуществляются без выделения промежуточного продукта. Схема иллюстрирует синтез соединений формулы (I). Соединения формулы (3), которые могут быть получены способом, описанным в примерах, могут реагировать с соединениями формулы (4) (которые доступны коммерчески или получены способами, известными специалисту) в присутствии ненуклеофильного основания с получением соединений формулы (5). Примеры ненуклеофильных оснований включают диизопропилэтиламин, триэтиламин, гексаметилдисилан, а также диизопропиламин. Примеры растворителей, применяемых в этой реакции, включают ацетонитрил, терагидрофуран, этилацетат, изопропилацетат, бутилацетат, толуол, тетрагидропиран, ацетон, DMSO, DMF, DMA, NMP и дихлорметан. Реакцию обычно проводят при температуре от около 20 до около 40C, время реакции обычно составляет от примерно 1 до примерно 12 ч. Соединения формулы (5) могут быть превращены в соединения формулы (6) путм обработки ацетатом аммония, формиатом аммония, сульфаматом аммония, фосфатом аммония, цитратом аммония,карбаматом аммония или аммиаком. Примеры растворителей, применяемых в данной реакции, включают толуол, ксилол, мезитилен и уксусную кислоту. Реакцию обычно проводят при температуре от около 85 до около 110C, время реакции обычно составляет от примерно 10 до примерно 20 ч. Соединения формулы (7) могут быть получены путм снятия защиты с защищенной группы, содержащейся в соединениях формулы (6). Примеры агентов для снятия защиты включают HCl (для групп,защищенных при помощи трет-бутоксикарбонила), триметилсилилйодид (для групп, защищенных метокси- и этоксикарбонилом) и морфолин (в случае 9-флуоренилметоксикарбонила в качестве защитной группы). Условия реакции и время меняются в зависимости от вида агента для снятия защиты и известны специалисту в данной области. Соединения формулы (7) могут быть превращены в соединения формулы (1) путм сочетания с соответствующим образом замещнной аминокислотой в присутствии агентов сочетания, таких как 1,1'карбонилдиимидазол, бис-(2-оксо-3-оксазолидинил)фосфинхлорид, 1-гидрокси-7-азабензотриазол, 1 гидроксибензотриазола гидрат, 3-гидрокси-1,2,3-бензотриазин-4-(3H)-он, 1-(3-диметиламинопропил)-3 этилкарбодиимид гидрохлорид,4-нитрофенол,пентафторфенол,2-гидроксипиридин,Nгидроксисукцинимид, N-гидроксифталамид, 2-меркаптобензоксазол, триметилацетилхлорид, изобутилхлорформиат, хлордиметокситриазол, оксалилхлорид, 2-гидроксипиридин-N-оксид, 5-нитро-2 гидроксипиридин, Boc-L-валиновый ангидрид и их смеси. Примеры растворителей включают изопропилацетат, ацетон, NMP, дихлорметан, 2-метилтетрагидрофуран, этилацетат и ацетонитрил. Конкретные условия меняются в зависимости от природы агента сочетания и известны специалисту в данной области. Следующие ниже примеры иллюстрируют данное изобретение. Примеры Получение соединения (3). В 3-горлую круглодонную колбу объмом 1 л, снабжнную линией для подвода азота, мешалкой и-8 017173 термопарой, загружали 20 г (83,9 ммоль, 1 экв.) 1,1'-(бифенил-4,4'-диил)диэтанона, 200 мл CH2Cl2 и 8,7 мл (27,1 г, 169,3 ммоль, 2,02 экв.) брома. Смесь перемешивали в атмосфере азота в течение примерно 20 ч в условиях окружающей среды. В полученную суспензию загружали 200 мл CH2Cl2 и концентрировали до объма около 150 мл путм отгонки под вакуумом. Затем растворитель в суспензии заменяют тетрагидрофураном (THF) до объма, равного 200 мл, путм перегонки под вакуумом. Суспензию охлаждали до 20-25C в течение 1 ч и перемешивали ещ 1 ч при 20-25C. Кристаллическое вещество неправильного белого цвета отфильтровывали и промывали 150 мл CH2Cl2. Полученный продукт сушили под вакуумом при 60C с получением 27,4 г (69,2 ммоль, 82%) желаемого продукта. 1H NMR (400 МГц, CDCl3)7,95-7,85 (m, 4H), 7,60-7,50 (m, 4H), 4,26 (s, 4H); 13 С NMR (100 МГц, CDCl3)191,0, 145,1, 133,8, 129,9,127,9, 30,8; IR (KBr cm-1) 3007, 2950, 1691, 1599, 1199; рассчитано для C16H12Br2O2: С, 48,52; H, 3,05; Br 40,34. Найдено: C, 48,53; Н, 3,03; Br 40,53. HRMS рассчитано для C16H13Br2O2: (М + Н; DCI+): 394,9282. Найдено: 394,9292. т.пл. 224-226C. Получение соединения (5). В колбу объмом 500 мл с рубашкой, снабжнную линией для подачи азота, мешалкой и термопарой, загружали 20 г (50,5 ммоль, 1 экв.) Соединения 3, 22,8 г (105,9 моль, 2,10 экв.) 1-(третбутоксикарбонил)-L-пролина и 200 мл ацетонитрила. Суспензию охлаждали до 20C и затем добавляли 18,2 мл (13,5 г, 104,4 ммоль, 2,07 экв.) диизопропилэтиламина (DIPEA). Суспензию нагревали до 25C и перемешивали в течение 3 ч. Полученный прозрачный органический раствор промывали 3100 мл 13 вес.% водного раствора NaCl. Обогащенный ацетонитрилом раствор обрабатывали толуолом с обменом на ацетонитрил (до объма, равного 215 мл) с применением вакуумной перегонки до содержания ацетонитрила менее 0,5 об.%. Получение соединения (6). К раствору соединения 5 в толуоле добавляли 78 г (1,011 моль, 20 экв.) ацетата аммония и нагревали до температуры 95-100C. Смесь перемешивали при температуре 95-100C в течение 15 ч. После завершения реакции смесь охлаждали до 70-80C и загружали 7 мл уксусной кислоты, 40 мл н-бутанола и 80 мл 5 об.% водного раствора уксусной кислоты. Полученный двухфазный раствор разделялся при температуре 50C. К обогащенной органикой фазе добавляли 80 мл 5 об.% водного раствора уксусной кислоты, 30 мл уксусной кислоты и 20 мл н-бутанола при температуре 50C. Полученный двухфазный раствор разделялся при температуре 50C и обогащенную органикой фазу промывали дополнительно 80 мл 5 об.% водного раствора уксусной кислоты. Затем растворитель вытесняли толуолом до объма 215 мл с применением вакуумной перегонки. При температуре 60C загружали 64 мл метанола. Полученную суспензию нагревали до 70-75C и выдерживали в течение 1 ч. Суспензию охлаждали до 20-25C в течение 1 ч и выдерживали при этой температуре ещ 1 ч. Суспензию отфильтровывали и осадок промывали 200 мл смеси 10:3 толуол:метанол. Полученный продукт сушили под вакуумом при 70C, получали 19,8 г (31,7 ммоль, 63%) желаемого продукта. 1 Н NMR (400 МГц, DMSO-d6)13,00-11,00 (s, 2H),7,90-7,75 (m, 4H), 7,75-7,60 (m, 4H), 7,60-7,30 (s, 2H), 4,92-4,72 (m, 2H), 3,65-3,49 (m, 2H), 3,49-3,28 (m,2H), 2,39-2,1 (m, 2H), 2,10-1,87 (m, 6H), 1,60-1,33 (s, 8H), 1,33-1,07 (s, 10H); 13 С NMR (100 МГц, DMSOd6)154,1, 153,8, 137,5, 126,6, 125,0, 78,9, 78,5, 55,6, 55,0, 47,0, 46,7, 33,7, 32,2, 28,5, 28,2, 24,2, 23,5; IR Альтернативный способ получения соединения (6). К раствору соединения 5 в толуоле добавляли 78 г (1,011 моль, 20 экв.) ацетата аммония и нагревали до температуры 95-100C. Смесь перемешивали при температуре 95-100C в течение 15 ч. После завершения реакции смесь охлаждали до 50-60C и добавляли 140 мл смеси 2:1 уксусная кислота:вода. Полученный двухфазный раствор разделялся при температуре 50C. Органический слой промывали 70 мл смеси 1:1 уксусная кислота:вода. Обогащенные водой слои соединяли и остаточный толуол удаляли путм вакуумной перегонки. При температуре 50-60C добавляли 50 мл метанола и затем 68 мл 10 NNaOH. Полученную суспензию охлаждали до 20-25C в течение 1 ч и выдерживали ещ 1 ч при этой температуре. Суспензию отфильтровывали, остаток промывали 200 мл воды и затем 75 мл MeOH. Полученный продукт сушили под вакуумом при температуре 70C, получали 27,4 г сырого продукта. В колбу объмом 1 л с рубашкой, снабжнную линией для подачи азота, мешалкой и термопарой, загружали 63 мл NMP и 25 г указанного выше продукта. Смесь нагревали до 50-60C и добавляли 83 мл МеОН. Полученную суспензию перемешивали при температуре 50-60C в течение 18 ч. К суспензии добавляли 208 мл MeOH при температуре 50C. Суспензию охлаждали до температуры окружающей среды в течение 1,5 ч и перемешивали ещ 2 ч. Тврдые вещества отфильтровывали, промывали 75 мл МеОН и высушивали под вакуумом при 70C, получая 18,0 г (28,8 ммоль, 62%) желаемого продукта. Получение соединения (7). В реактор объмом 250 мл, снабжнный линией для подвода азота и мешалкой, загружали 25,0 г соединения 6 (40,01 ммоль, 1 экв.) и затем 250 мл метанола и 32,85 мл (400,1 ммоль, 10 экв.) 6 М водного раствора HCl. Температуру повышали до 50C и перемешивали смесь при температуре 50C в течение 5 ч. Полученную суспензию охлаждали до температуры 20-25C и выдерживали при перемешивании в течение примерно 18 ч. После фильтрации суспензии получали тврдый продукт, который промывали последовательно 100 мл смеси 90% метанол/вода (об./об.) и 2100 мл метанола. Сырой остаток высушивали в вакуумной печи при 50C в течение ночи, получали 18,12 г (31,8 ммоль, 79,4%) желаемого продукта. Альтернативный способ получения соединения (7). В реактор с рубашкой, снабжнный механической мешалкой, термопарой и линией для подачи азота, загружали 2,8 л изопропилового спирта, 1,32 л воды и 1 кг соединения 6 (1,6 М, 1 экв.). Затем к суспензии добавляли 1,31 л (1,58 кг, 16,0 моль, 10 экв.) концентрированной соляной кислоты при комнатной температуре в течение 30 мин. Полученный раствор нагревали до 50C и перемешивали в течение 2,5 ч. Проводили кристаллизацию продукта путм добавления 7,2 л изопропилового спирта и охлаждали суспензию при комнатной температуре. Полученный продукт собирали путм фильтрации и промывали 3,7 л смеси 20% вода/изопропиловый спирт и затем 7,4 л изопропилового спирта. Сырой остаток сушили в вакуумной печи при температуре 50C с получением 0,84 г (1,44 моль, 90%) желаемого продукта). Перекристаллизация соединения (7). В реактор объмом 250 мл, снабжнный линией для подачи азота и мешалкой, загружали 17,8 г указанного выше соединения 7 и затем 72 мл метанола. Полученную суспензию перемешивали при температуре 50C в течение 4 ч, охлаждали до 20-25C и выдерживали в течение 1 ч при перемешивании при температуре 20-25C. После фильтрации получали кристаллический тврдый продукт, который промывали 60 мл метанола. Полученный сырой осадок высушивали в вакуумной печи при температуре 50C в течение 4 дней, получая 14,7 г (25,7 ммоль, 82,6%) очищенного продукта. 1 Н NMR (400 МГц, DMSO-d6)10,5-10,25 (br, 2H), 10,1-9,75 (br, 2H), 8,19 (s, 2H), 7,05 (d, J=8,4, 4 Н), 7,92 (d, J=8,5, 4H), 5,06 (m, 2H),3,5-3,35 (m, 4H), 2,6-2,3 (m, 4H), 2,25-2,15 (m, 2H), 2,18-1,96 (m, 2H); 13C NMR (100 МГц, DMSO-d6)156,6, 142,5, 139,3, 128,1, 127,5, 126,1, 116,9, 53,2, 45,8, 29,8, 24,3; IR (KBr cm-1) 3429, 2627, 1636,- 10017173 1567,1493, 1428, 1028. Рассчитано для C26H32N6C14: С, 54,75; H, 5,65; Cl 24,86; получено 1,9% воды: С,53,71; Н, 5,76; N, 14,46, Cl 24,39. Найдено: С, 53,74; Н, 5,72, N, 14,50, Cl 24,49. KF=1,9. т.пл. 240C (разлагается). Получение соединения (I). В колбу объмом 1 л с рубашкой, снабжнную линией для подвода азота и мешалкой, последовательно загружали 100 мл ацетонитрила, 13,69 г (89,4 ммоль, 2,5 экв.) гидроксибензотриазолгидрата, 15,07 г (86 ммоль, 2,4 экв.) N-(метоксикарбонил)-L-валина, 16,46 г (85,9 ммоль, 2,4 экв.) 1-(3 диметиламинопропил)-3-этилкарбодиимид гидрохлорида и дополнительное количество (100 мл) ацетонитрила. Полученный раствор перемешивали при температуре 20C в течение 1 ч и добавляли 20,4 г(35,8 ммоль, 1 экв.) очищенного соединения 7. Суспензию охлаждали до температуры около 0C и в течение 30 мин добавляли 18,47 г (142,9 ммоль, 4 экв.) диизопропилэтиламина при температуре ниже 10C. Раствор медленно нагревали до 15C в течение 3 ч и выдерживали при 15C в течение 12 ч. В полученный раствор добавляли 120 мл 13 вес.% водного раствора NaCl и нагревали до 50C в течение 1 ч. После охлаждения до температуры 20C добавляли 100 мл изопропилацетата. Двухфазный раствор отфильтровывали через фильтр 0,45 мкм, смесь разделялась. Органическую фазу промывали 2240 мл 0,5 N раствора NaCl, содержащего 13 вес.% NaCl, и затем 120 мл 13 вес.% водного раствора NaCl. В смеси растворитель вытесняли изопропилацетатом с применением вакуумной перегонки до объма, равного 400 мл. Полученный мутный раствор охлаждали до 20C и фильтровали через фильтр 0,45 мкм. Затем в прозрачном растворе растворитель заменяли этанолом с применением вакуумной перегонки до объма, равного 140 мл. При температуре 50C добавляли 66,4 мл (82,3 ммоль, 2,3 экв.) 1,24 М раствора HCl в этаноле. Затем в смесь добавляли 33 мг (0,04 ммоль, 0,001 экв.) затравочных кристаллов соединения (I) (см. пример ниже), полученную суспензию перемешивали при 50C в течение 3 ч. Смесь охлаждали до 20C в течение 1 ч и выдерживали при этой температуре ещ 22 ч. Затем суспензию отфильтровывали и сырой осадок промывали 100 мл смеси 2:1 ацетон:этанол. Тврдый продукт высушивали в вакуумной печи при температуре 70C с получением 22,15 г (27,3 ммоль, 76,3%) желаемого продукта. Альтернативный способ получения соединения (I). В реактор с рубашкой, снабжнный механической мешалкой, термопарой и линией для подачи азота, последовательно загружали 10 л ацетонитрила, 0,671 кг (4,38 моль, 2,50 экв.) 1 гидроксибензотриазола, 0,737 кг (4,21 моль, 2,40 экв.) N-(метоксикарбонил)-L-валина и 0,790 кг (4,12 моль, 2,35 экв.) 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорида. Смесь перемешивали при температуре 20C в течение 1 ч, охлаждали до 5C и добавляли 1 кг (1,75 моль, 1,00 экв.) соединения 7. При температуре менее 10C добавляли 0,906 кг (7,01 моль, 4 экв.) диизопропилэтиламина. Смесь нагревали до температуры 15-20C в течение 2 ч и перемешивали смесь ещ 2 ч. После завершения реакции смесь промывали один раз 6,0 л 13 вес.% водного раствора NaCl, два раза 6,1 л (6,12 моль, 3,5 экв.) 1,0 М водного раствора NaOH, содержащего 13 вес.% NaCl, и один раз 6,0 л 13 вес.% водного раствора NaCl. Затем из органической фазы удаляли воду путм азеотропной отгонки. Смесь охлаждали до 20C, перемешивали в течение 1 ч и отфильтровывали. Органический раствор обрабатывали этиловым спиртом,вытесняя растворитель, с применением вакуумной перегонки до объма, равного 5 л. При температуре 50C добавляли 3,2 л (4,0 моль, 2,3 экв.) 1,25 М HCl в EtOH. В смесь добавляли затравочные кристаллы 1,6 г соединения (I) (см. пример ниже) и перемешивали при температуре 50C в течение 3 ч. Полученную суспензию охлаждали до 20C и перемешивали в течение по меньшей мере 3 ч. Полученный продукт отфильтровывали и промывали 5 л смеси 2:1 ацетон:EtOH, получали 1,29 кг (примерно 90 вес.%) влажного сырого продукта. В реактор, снабжнный мешалкой, линией для подачи азота и термопарой, загружали 1,11 кг указанного сырого продукта и 7 л метанола. Полученный раствор обрабатывали Cuno ZetaCarbon (TM) 55 SP. Углерод промывали 15 л MeOH и объединнные фильтрат и промывку концентрировали до 4 л путм вакуумной перегонки. Концентрированный раствор обрабатывали 5 л ацетона и добавляли 1,6 г затравочных кристаллов соединения (I) (см. пример ниже), поддерживая температуру, равную 50C. Добавляли ещ 10 л ацетона и перемешивали полученную суспензию при 50C в течение 3 ч. Эту суспензию охлаждали до 20C и перемешивали в течение 3 ч при температуре 20C. Полученный продукт отфильтровывали, промывали 5 л смеси 2:1 ацетон:EtOH и сушили под вакуумом при темпера- 11017173 туре 50-60C, получая 0,900 кг (1,11 моль, 74%) соединения (I). Обработка углм и перекристаллизация соединения (I). Раствор соединения (I) получали путм растворения 3,17 г соединения (I) (см. выше) в 22 мл метанола. Раствор пропускали через угольный фильтр Cuno Zeta Carbon 53SP 47 мм при давлении, равном 5 фунт/дюйм 2 со скоростью потока 58 л/мин. Угольный фильтр промывали 32 мл метанола. Раствор концентрировали до объма 16 мл путм вакуумной отгонки. Поддерживая температуру, равной 40-50C,добавляли 15,9 мл ацетона и 5 мг затравочных кристаллов соединения (I) (см. ниже). В полученную суспензию в течение 30 мин добавляли 32 мл ацетона. Суспензию выдерживали при температуре 50C в течение 2 ч, охлаждали до 20C в течение примерно 1 ч и выдерживали при 20C в течение примерно 20 ч. Отфильтровывали тврдый продукт, промывали 16 мл смеси 2:1 ацетон:метанол и сушили в вакуумной печи при температуре 60C, получая 2,14 г (67,5%) очищенного соединения (I). 1H NMR (400 МГц,DMSO-d6, 80C)8,02 (d, J=8,34 Гц, 4H), 7,97 (s, 2H), 7,86 (d, J=8,34 Гц, 4H), 6,75 (s, 2H), 5,27 (t, J=6,44 Гц, 2H), 4,17 (t, J=6,95 Гц, 2H), 3,97-4,11 (m, 2H), 3,74-3,90 (m, 2H), 3,57 (s, 6H), 2,32-2,46 (m, 2H), 2,092,31 (m, 6H), 1,91-2,07 (m, 2H), 0,88 (d, J=6,57 Гц, 6H), 0,79 (d, J=6,32 Гц, 6 Н); 13 С NMR (75 МГц, DMSOd6)170,9, 156,9, 149,3, 139,1, 131,7, 127,1, 126,5, 125,9, 115,0, 57,9, 52,8, 51,5, 47,2, 31,1, 28,9, 24,9, 19,6,17,7; IR (чист, cm-1) 3385, 2971, 2873, 2669, 1731, 1650. Рассчитано для C40H52N8O6Cl2: C, 59,18; Н, 6,45;N, 13,80; Cl 8,73. Найдено: C, 59,98; Н, 6,80, N, 13,68, Cl 8,77. т.пл. 267C (разлагается). Положения характеристических пиков (20,1) при комнатной температуре для высокого разрешения, полученные при помощи дифрактометра (Cu K) с вращением с углом 2, откалиброванным при помощи другого подходящего стандарта NIST, были следующие: 10,3, 12,4, 12,8, 13,3, 13,6, 15,5, 20,3, 21,2, 22,4, 22,7,23,7. Получение затравочных кристаллов соединения (I). В круглодонную колбу объмом 250 мл загружали 6,0 г (10,5 ммоль, 1 экв.) соединения (5), 3,87 г(22,1 ммоль, 2,1 экв.) N-(метоксикарбонил)-L-валина, 4,45 г (23,2 ммоль, 2,2 экв.) 1-(3 диметиламинопропил)-3-этилкарбодиимид гидрохлорида, 0,289 г (2,14 ммоль, 0,2 экв.) 1 гидроксибензотриазола и 30 мл ацетонитрила. В полученную суспензию затем загружали 7,33 мл (42,03 ммоль, 4 экв.) диизопропилэтиламина и перемешивали при температуре 24-30C в течение примерно 18 ч. В смесь добавляли 6 мл воды и нагревали до температуры 50C в течение примерно 5 ч. Смесь охлаждали и добавляли 32 мл этилацетата и 30 мл воды. Слои разделяли и органический слой промывали 30 мл 10 вес.% водного раствора NaHCO3, 30 мл воды и 20 мл 10 вес.% водного раствора NaCl. Органический слой затем высушивали над MgSO4, фильтровали и концентрировали до получения остатка. Сырой продукт затем очищали методом флэш-хроматографии (силикагель, 0-10% метанола в дихлорметане), получая свободное основание соединения (I). Свободное основание соединения (I) (0,03 г) растворяли в 1 мл изопропанола при температуре 20C. Добавляли безводную HCl (70 мкл, растворнную в этаноле с концентрацией примерно 1,25 М) и реакционную смесь перемешивали. К раствору добавляли метил-трет-бутилового эфира (1 мл) и полученную суспензию энергично перемешивали при температуре от 40 до 50C в течение 12 ч. Суспензию кристаллов охлаждали до 20C и отфильтровывали. Влажный осадок сушили воздухом при температуре 20C. Получали белое кристаллическое вещество (форма N-2 соединения (I. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения соединения формулы (I)X выбран из СН 2 или CHR5; когда s равен 1, R5 представляет собой С 1-С 6 алкил, где С 1-С 6 алкил необязательно может образовывать конденсированное трехчленное кольцо с соседним атомом углерода;- 12017173 при условии, что два гетероциклических кольца, замещающих имидазольные кольца, являются идентичными;Rc и Rd независимо выбраны из водорода, С 2-С 6 алкенилоксикарбонила, С 1-С 6 алкоксиС 1 С 6 алкилкарбонила, С 1-С 6 алкоксикарбонила, С 1-С 6 алкила, C1-С 6 алкилкарбонила, С 1-С 6 алкилсульфонила,арила, арилС 1-С 6 алкоксикарбонила, арилС 1-С 6 алкила, арилС 1-С 6 алкилкарбонила, арилкарбонила, арилоксикарбонила, арилсульфонила, С 3-С 7 циклоалкила, С 3-С 7 циклоалкилсульфонила, формила, галоидС 1 С 6 алоксикарбонила, гетероциклила, гетероциклилС 1-С 6 алкоксикарбонила, гетероциклилС 1-С 6 алкила,гетероциклилС 1-С 6 алкилкарбонила, гетероциклилкарбонила, гетероциклилоксикарбонила, гидроксиС 1 С 6 алкилкарбонила,(NReRf)С 1-С 6 алкила,(NReRf)С 1-С 6 алкилкарбонила,(NReRf)карбонила,e f(NR R )сульфонила, -C(NCN)OR' и -C(NCN)NR R , где R' выбран из С 1-С 6 алкила и незамещенного фенила и где алкильная часть арилС 1-С 6 алкила, арилС 1-С 6 алкилкарбонила, гетероциклилС 1-С 6 алкила, а также гетероциклилС 1-С 6 алкилкарбонила, в свою очередь, могут быть замещены одним -NReRf и где арил,арильная часть арилоксикарбонила, арилС 1-С 6 алкила, арилС 1-С 6 алкилкарбонила, арилкарбонила, арилоксикарбонила и арилсульфонила, гетероциклил и гетероциклическая часть гетероциклилС 1 С 6 алкоксикарбонила, гетероциклилС 1-С 6 алкила, гетероциклилС 1-С 6 алкилкарбонила, гетероциклилкарбонила и гетероциклилоксикарбонила также могут быть замещены одним, двумя или тремя заместителями,независимо выбранными из C1-С 6 алкокси, С 1-С 6 алкила, циано, галоида, галоидС 1-С 6 алкокси, галоидС 1 С 6 алкила и нитро;Re и Rf независимо выбраны из водорода, алкила, незамещнного арила, незамещнного арилалкила,незамещнного циклоалкила, незамещнного (циклоалкил)алкила, незамещнного гетероциклила, незамещнного гетероциклилалкила, (NRxRy)алкила и (NRxRy)карбонила;Rx и Ry независимо выбраны из водорода, алкоксикарбонила, алкила, алкилкарбонила, незамещнного арила, незамещнного арилалкоксикарбонила, незамещнного арилалкила, незамещнного циклоалкила, незамещнного гетероциклила и (NRx'Ry')карбонила, при этом Rx' и Ry' независимо выбраны из водорода и алкила; при этом арил относится к фенильной группе или к бициклической конденсированной кольцевой системе, состоящей из фенильной группы, конденсированной с 4-6-членным ароматическим или неароматическим карбоциклическим кольцом; гетероциклил относится к 4-, 5-, 6- или 7-членному кольцу, содержащему один, два, три или четыре гетероатома, независимо выбранных из азота, кислорода или серы, а также к бициклическим группам, в которых гетероциклическое кольцо является конденсированным с другим моноциклическим гетероциклом или 4-6-членным ароматическим или неароматическим карбоциклическим кольцом; а также мостиковым бициклическим группам и может присоединяться к родительской молекуле через любой атом углерода или атом азота в группе; при этом способ включает:(а) взаимодействие соединения формулы (3)(б) обработку продукта со стадии (а) реагентом, выбранным из ацетата аммония, формиата аммония, сульфамата аммония, фосфата аммония, цитрата аммония, карбамата аммония и аммиака; и(в) обработку продукта со стадии (б) агентом, снимающим защиту с получением соединения формулы (7)(г) обработку соединения формулы (7) соединением формулы (8) где R9 обозначает радикалы, указанные выше. 2. Способ получения соединения формулы (7) или его фармацевтически приемлемой соли,где s равен 0 или 1;X выбран из CH2 или CHR5; когда s равен 1, R5 представляет собой С 1-С 6 алкил, где С 1-С 6 алкил необязательно может образовывать конденсированное трехчленное кольцо с соседним атомом углерода; при условии, что два гетероциклических кольца, замещающих имидазольные кольца, являются идентичными; причем указанный способ включает:(а) взаимодействие соединения формулы (3)(б) обработку продукта со стадии (а) реагентом, выбранным из ацетата аммония, формиата аммония, сульфамата аммония, фосфата аммония, цитрата аммония, карбамата аммония и аммиака; и(в) обработку продукта со стадии (б) агентом, снимающим защиту. 3. Способ по п.1 или 2, отличающийся тем, что s равен 0 и X обозначает CH2. 4. Способ по п.1 или 2, отличающийся тем, что LG обозначает галоид. 5. Способ по п.4, отличающийся тем, что галоид представляет собой бром. 6. Способ по п.1 или 2, отличающийся тем, что стадию (а) проводят в присутствии основания. 7. Способ по п.6, отличающийся тем, что основание представляет собой диизопропилэтиламин. 8. Способ по п.1 или 2, отличающийся тем, что реагент, применяемый на стадии (б), представляет собой ацетат аммония. 9. Способ по п.1 или 2, отличающийся тем, что PG обозначает формулу где обозначает точку присоединения к родительской молекуле иR' выбран из С 1-С 6 алкила, арила и арилС 1-С 6 алкила. 10. Способ по п.9, отличающийся тем, что PG обозначает трет-бутоксикарбонил. 11. Способ по п.10, отличающийся тем, что агент для снятия защиты на стадии (в) представляет собой кислоту. 12. Способ по п.11, отличающийся тем, что кислота представляет собой соляную кислоту.
МПК / Метки
МПК: C07D 403/14
Метки: лечения, гепатита, синтеза, пригодных, соединений, способ
Код ссылки
<a href="https://eas.patents.su/16-17173-sposob-sinteza-soedinenijj-prigodnyh-dlya-lecheniya-gepatita-s.html" rel="bookmark" title="База патентов Евразийского Союза">Способ синтеза соединений, пригодных для лечения гепатита с</a>
Предыдущий патент: Способ получения изоиммунной плазмы крови
Следующий патент: Композиция на основе силиконового геля и лекарственное средство для лечения ран с уменьшенной степенью рубцевания
Случайный патент: Неорганическая плита и способ ее изготовления












