Полиморфы этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты
Номер патента: 14082
Опубликовано: 30.08.2010
Авторы: Зоботта Райнер, Зигер Петер, Шмид Рольф, Хаюль Норберт
Формула / Реферат
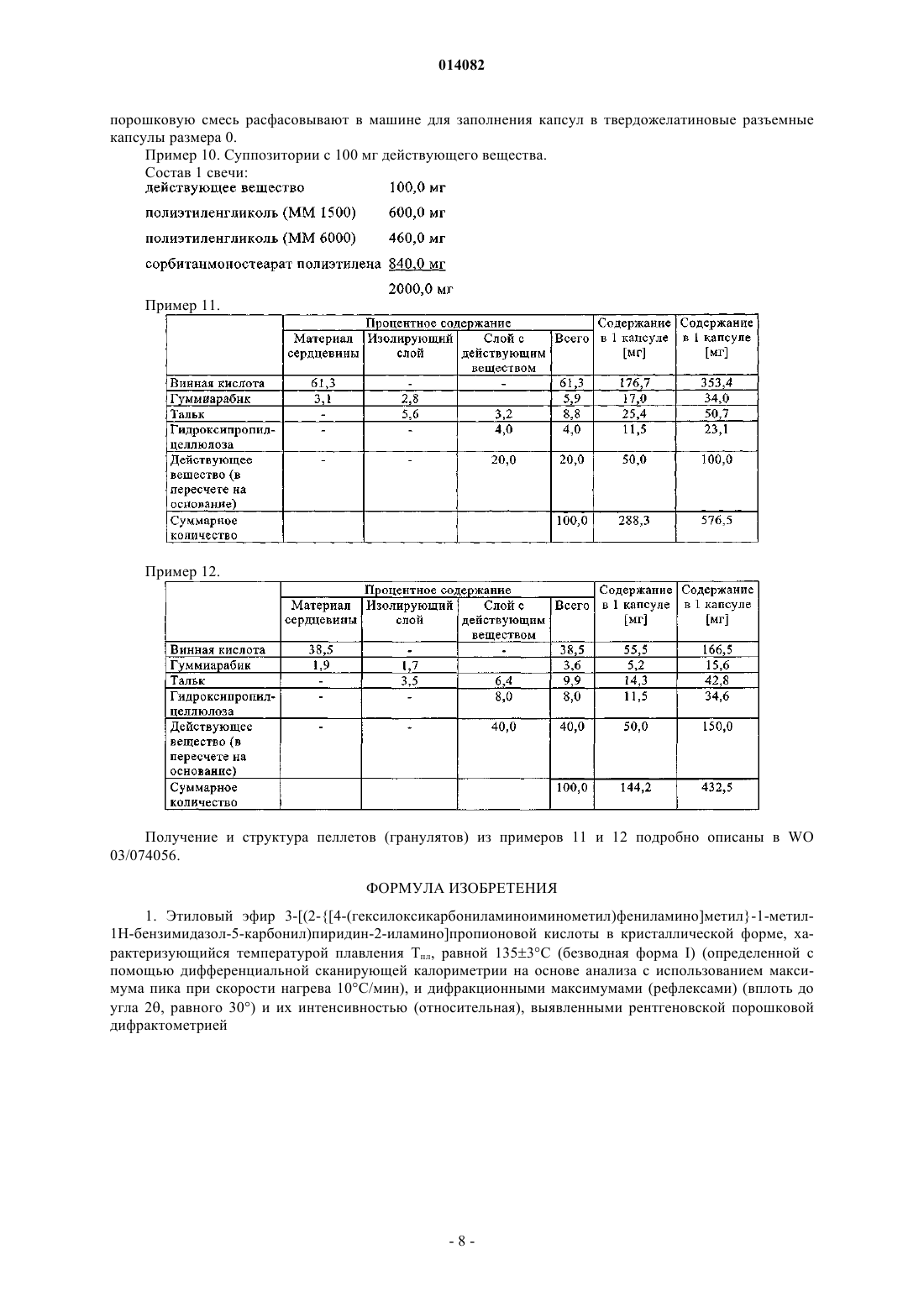
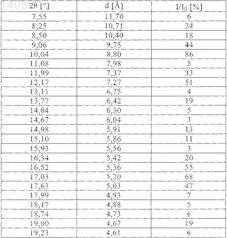
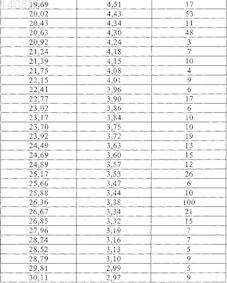
1. Этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в кристаллической форме, характеризующийся температурой плавления Тпл, равной 135±3°С (безводная форма I) (определенной с помощью дифференциальной сканирующей калориметрии на основе анализа с использованием максимума пика при скорости нагрева 10°С/мин), и дифракционными максимумами (рефлексами) (вплоть до угла 2q, равного 30°) и их интенсивностью (относительная), выявленными рентгеновской порошковой дифрактометрией
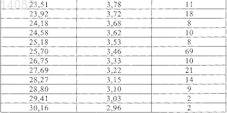
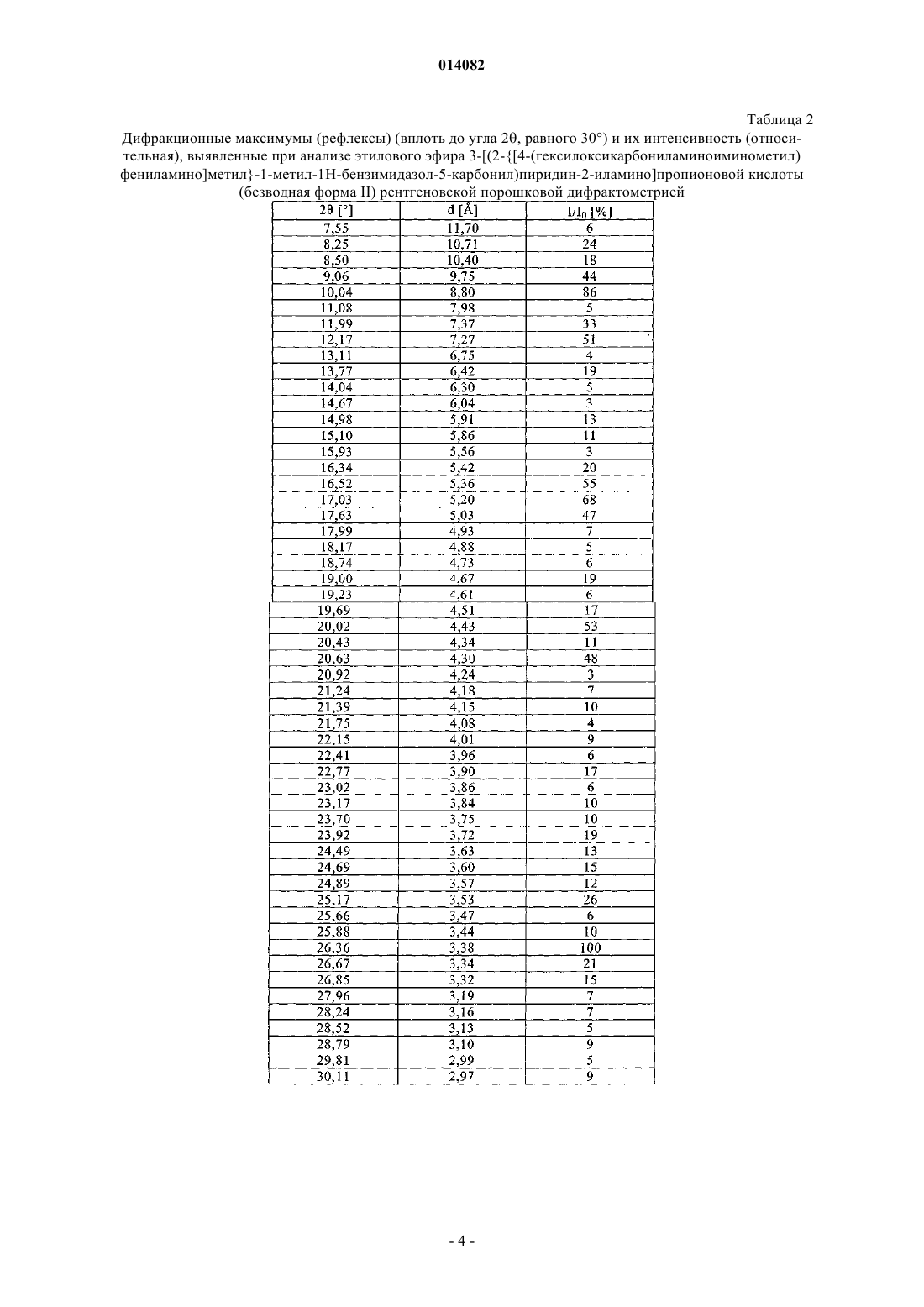
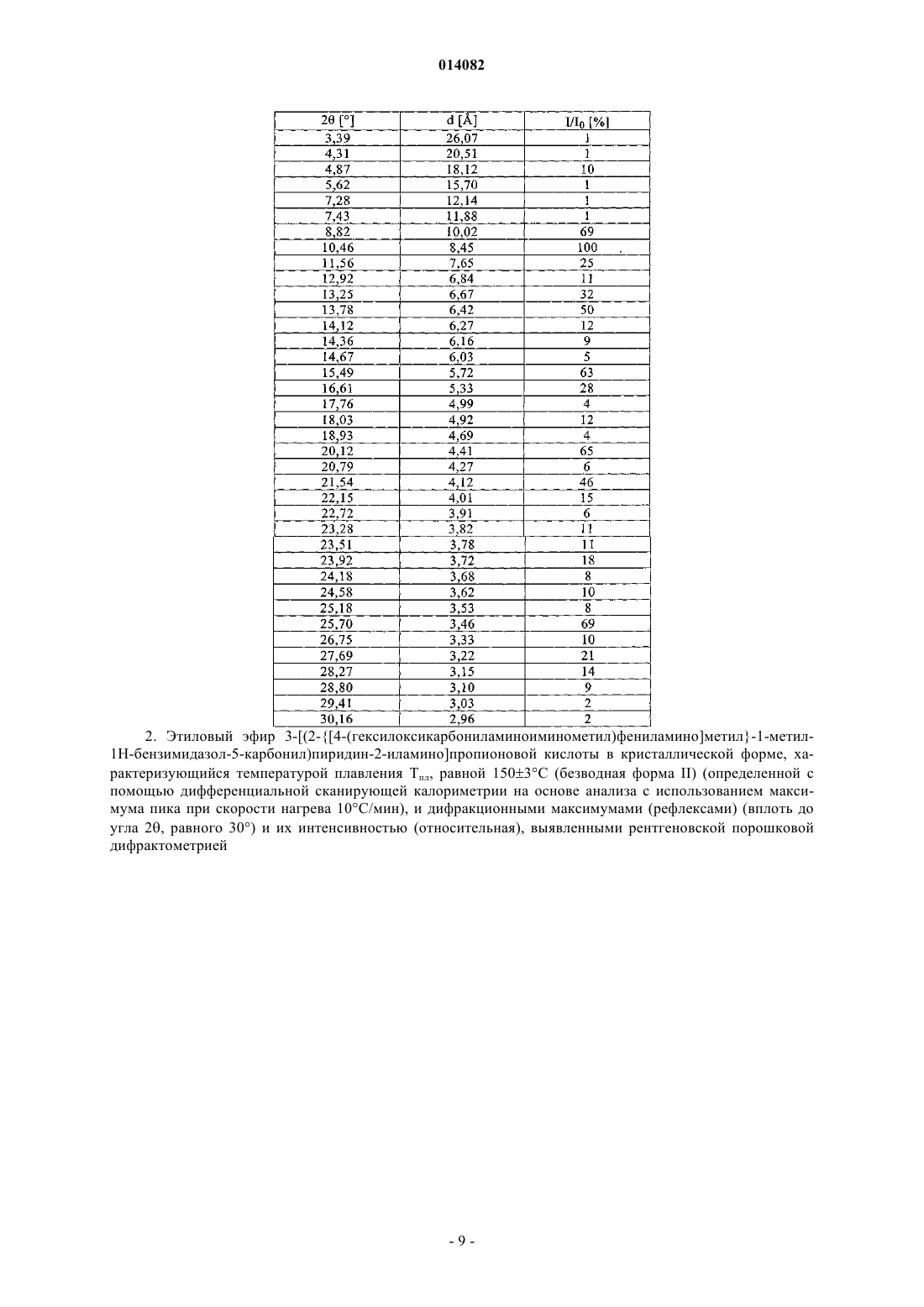
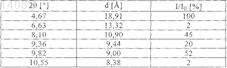
2. Этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в кристаллической форме, характеризующийся температурой плавления Тпл, равной 150±3°С (безводная форма II) (определенной с помощью дифференциальной сканирующей калориметрии на основе анализа с использованием максимума пика при скорости нагрева 10°С/мин), и дифракционными максимумами (рефлексами) (вплоть до угла 2q, равного 30°) и их интенсивностью (относительная), выявленными рентгеновской порошковой дифрактометрией
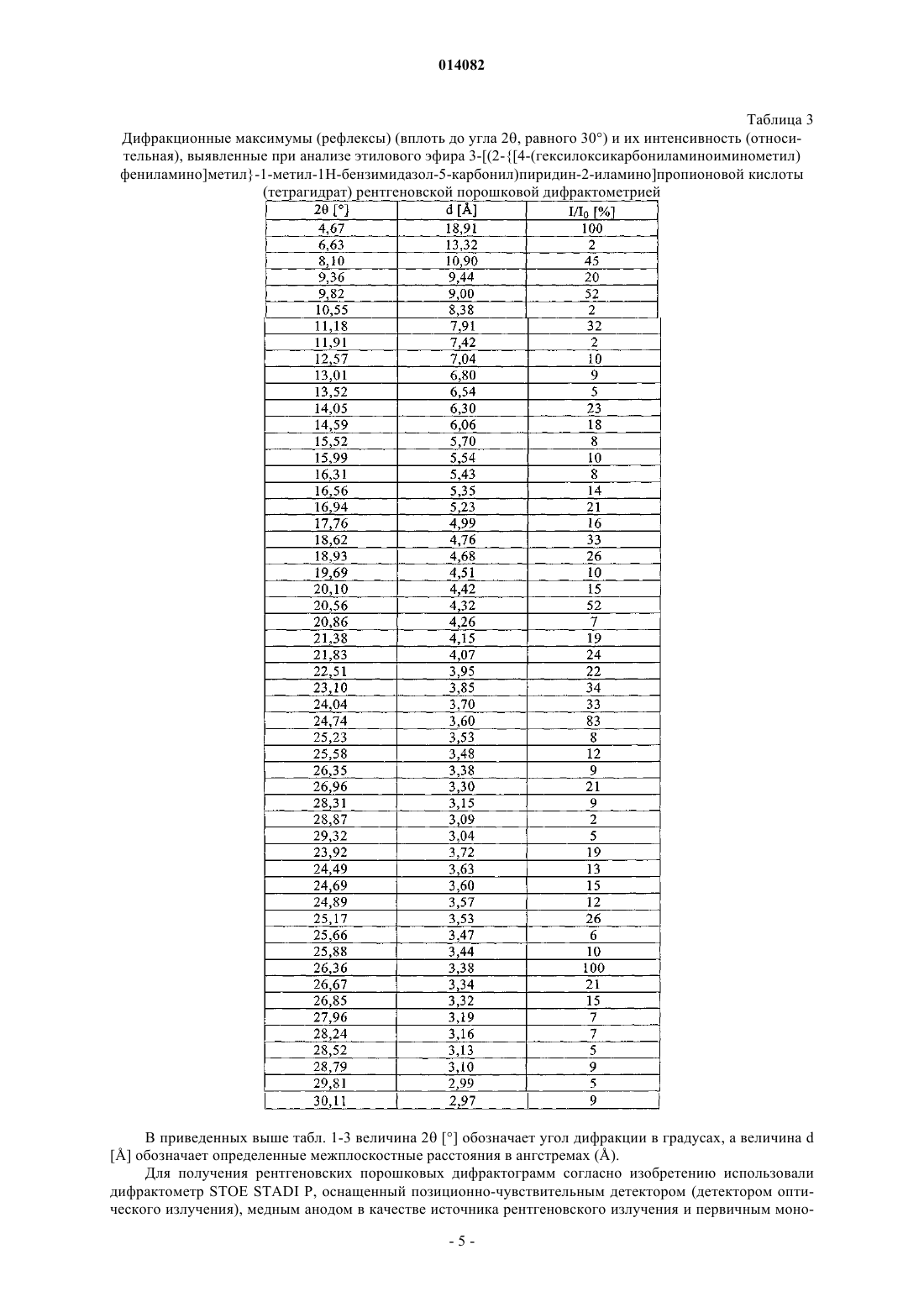
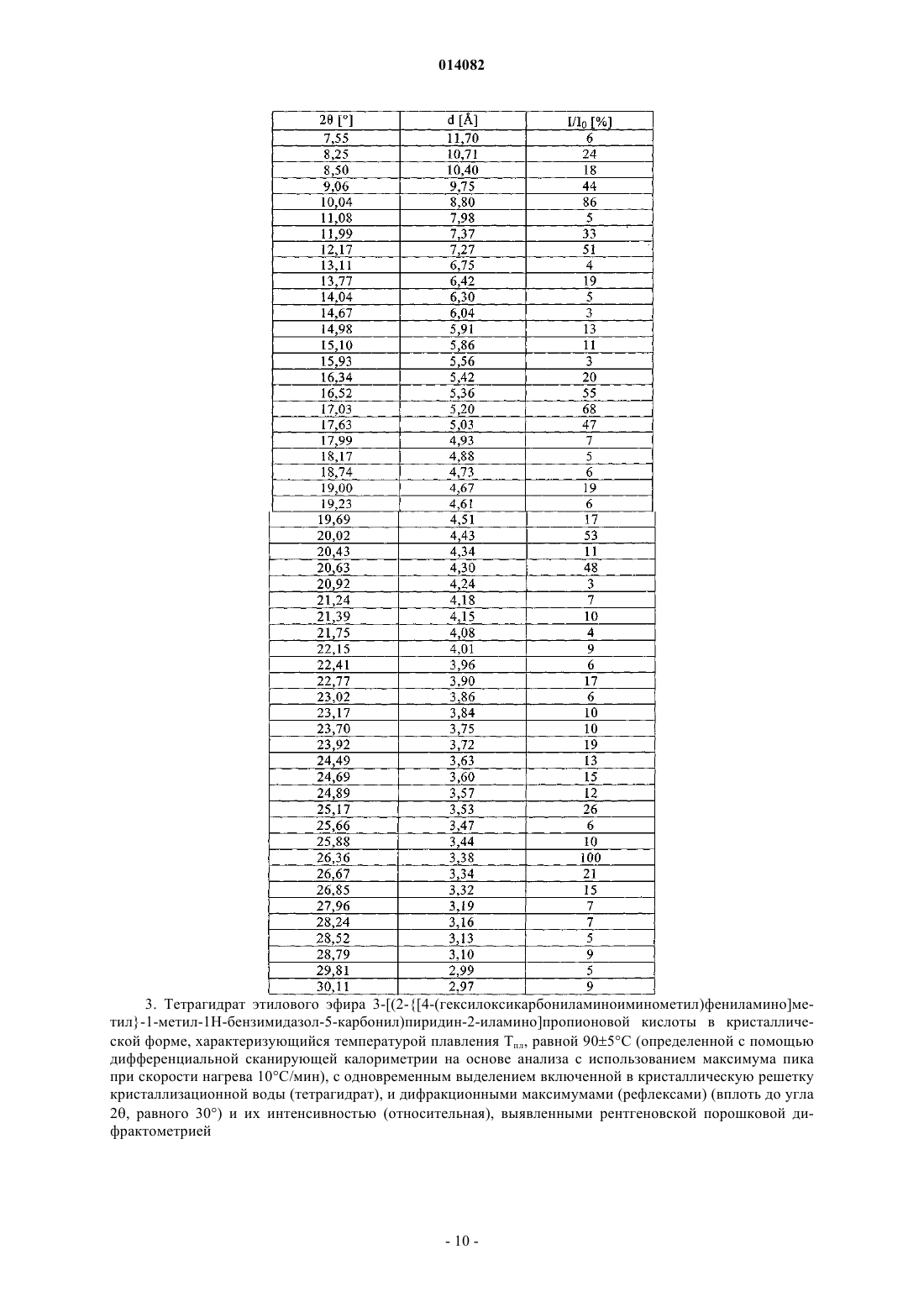
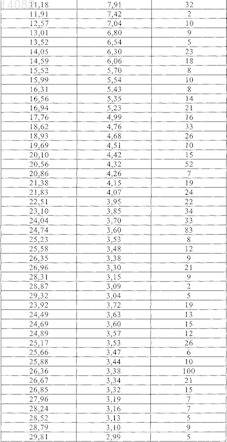
3. Тетрагидрат этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в кристаллической форме, характеризующийся температурой плавления Тпл, равной 90±5°С (определенной с помощью дифференциальной сканирующей калориметрии на основе анализа с использованием максимума пика при скорости нагрева 10°С/мин), с одновременным выделением включенной в кристаллическую решетку кристаллизационной воды (тетрагидрат), и дифракционными максимумами (рефлексами) (вплоть до угла 2q, равного 30°) и их интенсивностью (относительная), выявленными рентгеновской порошковой дифрактометрией
![]()
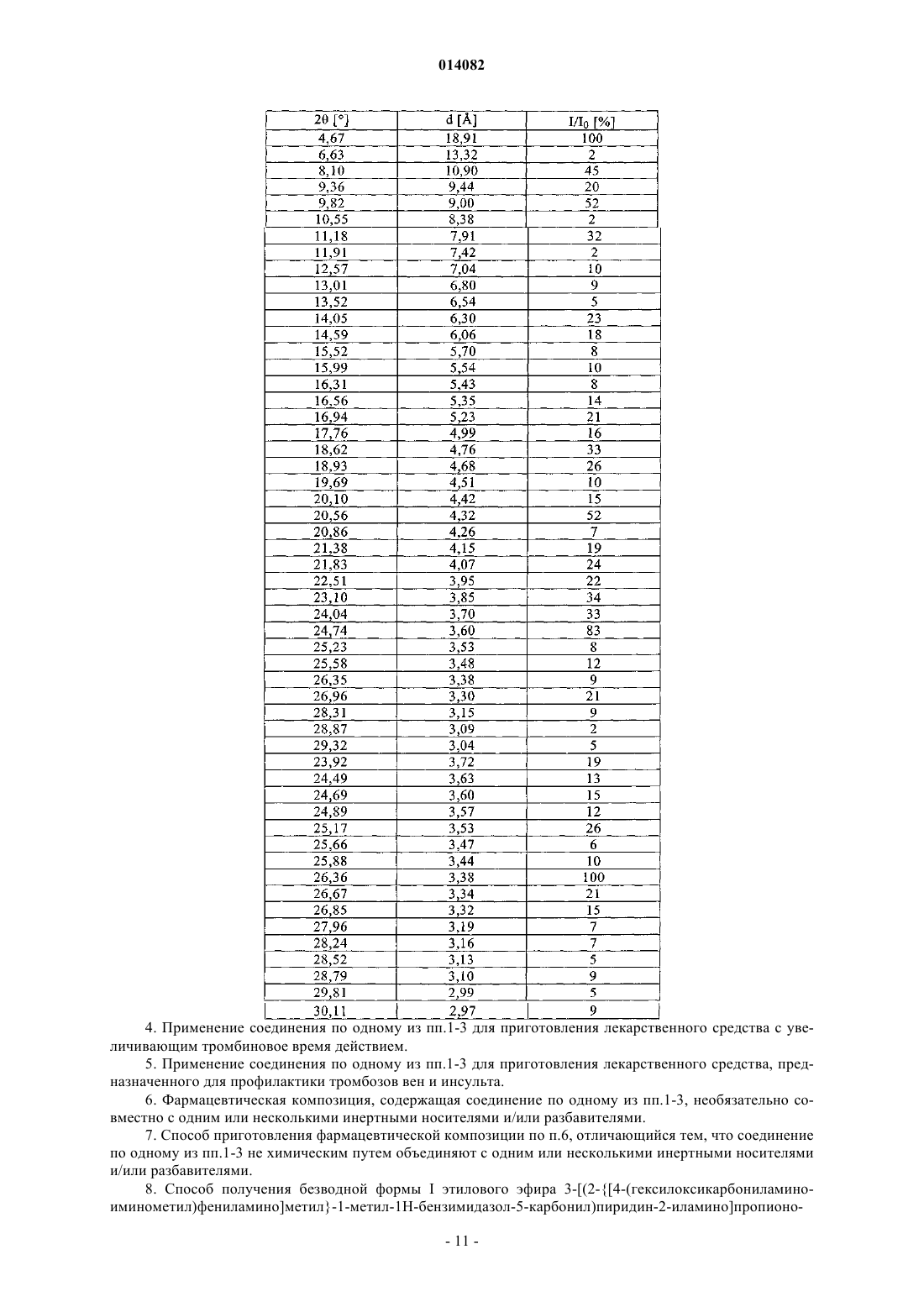
4. Применение соединения по одному из пп.1-3 для приготовления лекарственного средства с увеличивающим тромбиновое время действием.
5. Применение соединения по одному из пп.1-3 для приготовления лекарственного средства, предназначенного для профилактики тромбозов вен и инсульта.
6. Фармацевтическая композиция, содержащая соединение по одному из пп.1-3, необязательно совместно с одним или несколькими инертными носителями и/или разбавителями.
7. Способ приготовления фармацевтической композиции по п.6, отличающийся тем, что соединение по одному из пп.1-3 не химическим путем объединяют с одним или несколькими инертными носителями и/или разбавителями.
8. Способ получения безводной формы I этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил) фениламино]метил}-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, отличающийся тем, что:
а) этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания растворяют при нагревании с обратным холодильником в этилацетате,
б) полученный раствор охлаждают до температуры порядка 30-35°С и перемешивают при этой температуре в течение последующих 60 мин,
в) раствор охлаждают до температуры порядка 15-20°С и затем перемешивают при этой температуре еще в течение примерно 60 мин,
г) выпавшие в осадок кристаллы отделяют вакуум-фильтрацией и промывают этилацетатом и затем
д) полученный таким путем продукт сушат в сушильном шкафу с циркуляцией воздуха при температуре в пределах от 40 до 50°С.
9. Способ получения безводной формы II этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил) фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, отличающийся тем, что:
а) этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания смешивают с небольшим количеством этилацетата,
б) полученную таким путем суспензию нагревают до температуры порядка 80°С с образованием при этом прозрачного раствора,
в) этот раствор в течение примерно одного часа кипятят с обратным холодильником,
г) выпавшие в осадок кристаллы отфильтровывают и
д) полученный таким путем продукт сушат на воздухе.
10. Способ получения тетрагидрата этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил) фениламино]метил}-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, отличающийся тем, что:
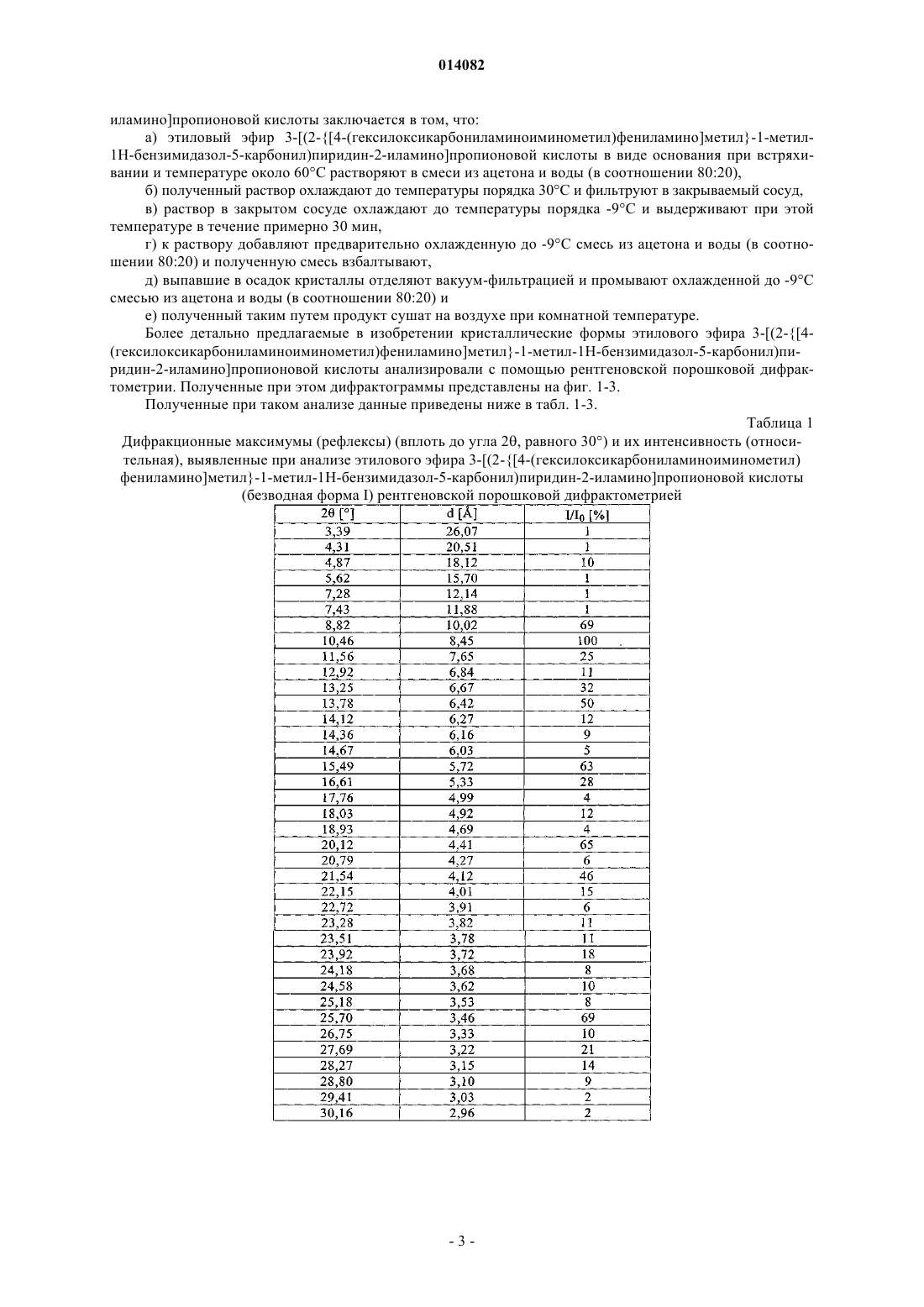
а) этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания при встряхивании и температуре около 60°С растворяют в смеси из ацетона и воды (в соотношении 80:20),
б) полученный раствор охлаждают до температуры порядка 30°С и фильтруют в закрываемый сосуд,
в) раствор в закрытом сосуде охлаждают до температуры порядка -9°С и выдерживают при этой температуре в течение примерно 30 мин,
г) к раствору добавляют предварительно охлажденную до -9°С смесь из ацетона и воды (в соотношении 80:20) и полученную смесь взбалтывают,
д) выпавшие в осадок кристаллы отделяют вакуум-фильтрацией и промывают охлажденной до -9°С смесью из ацетона и воды (в соотношении 80:20) и
е) полученный таким путем продукт сушат на воздухе при комнатной температуре.
11. Этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, представляющий собой безводную форму I и получаемый способом по п.8.
12. Этиловый эфир 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, представляющий собой безводную форму II и получаемый способом по п.9.
13. Тетрагидрат этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, получаемый способом по п.10.
Текст
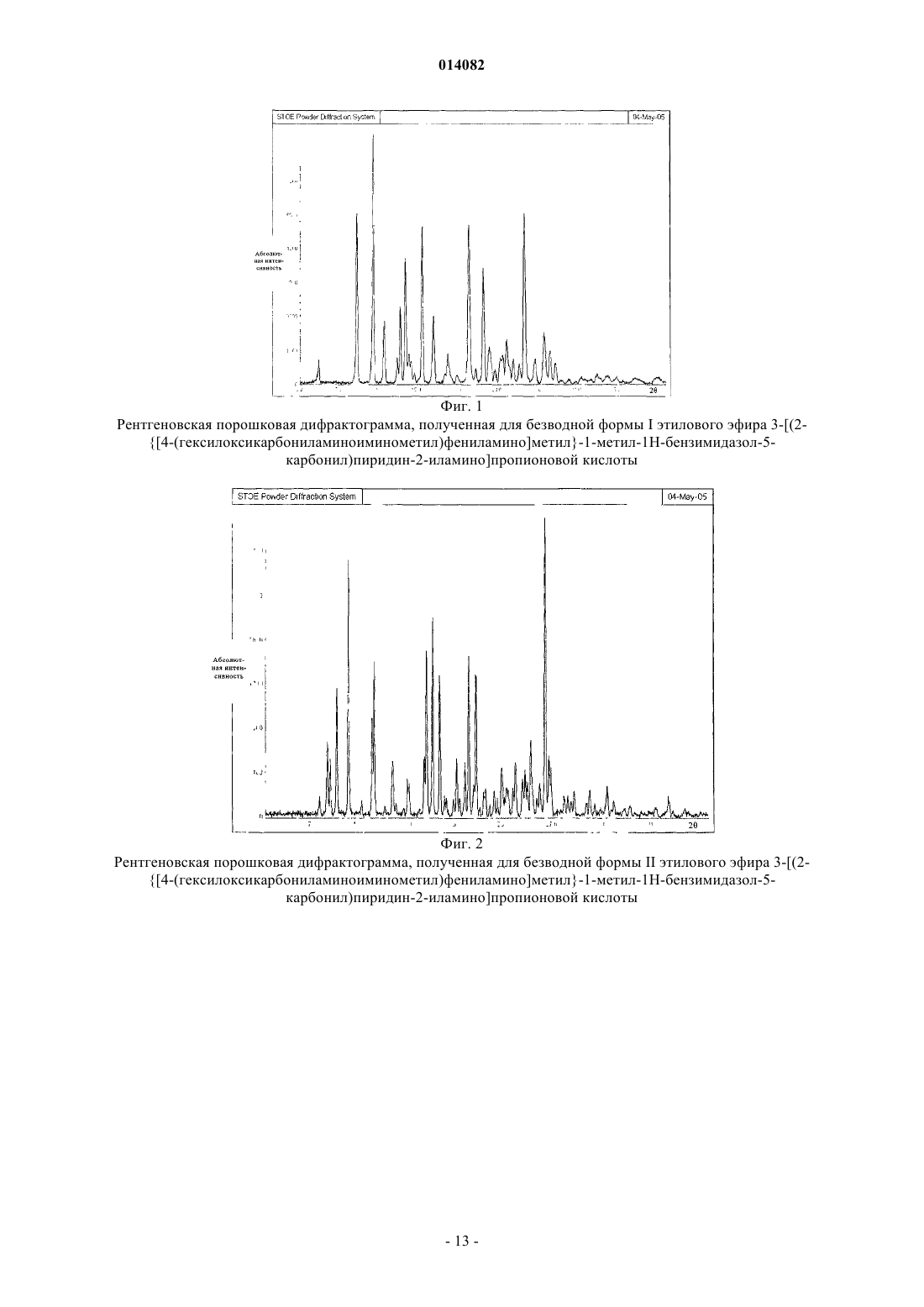
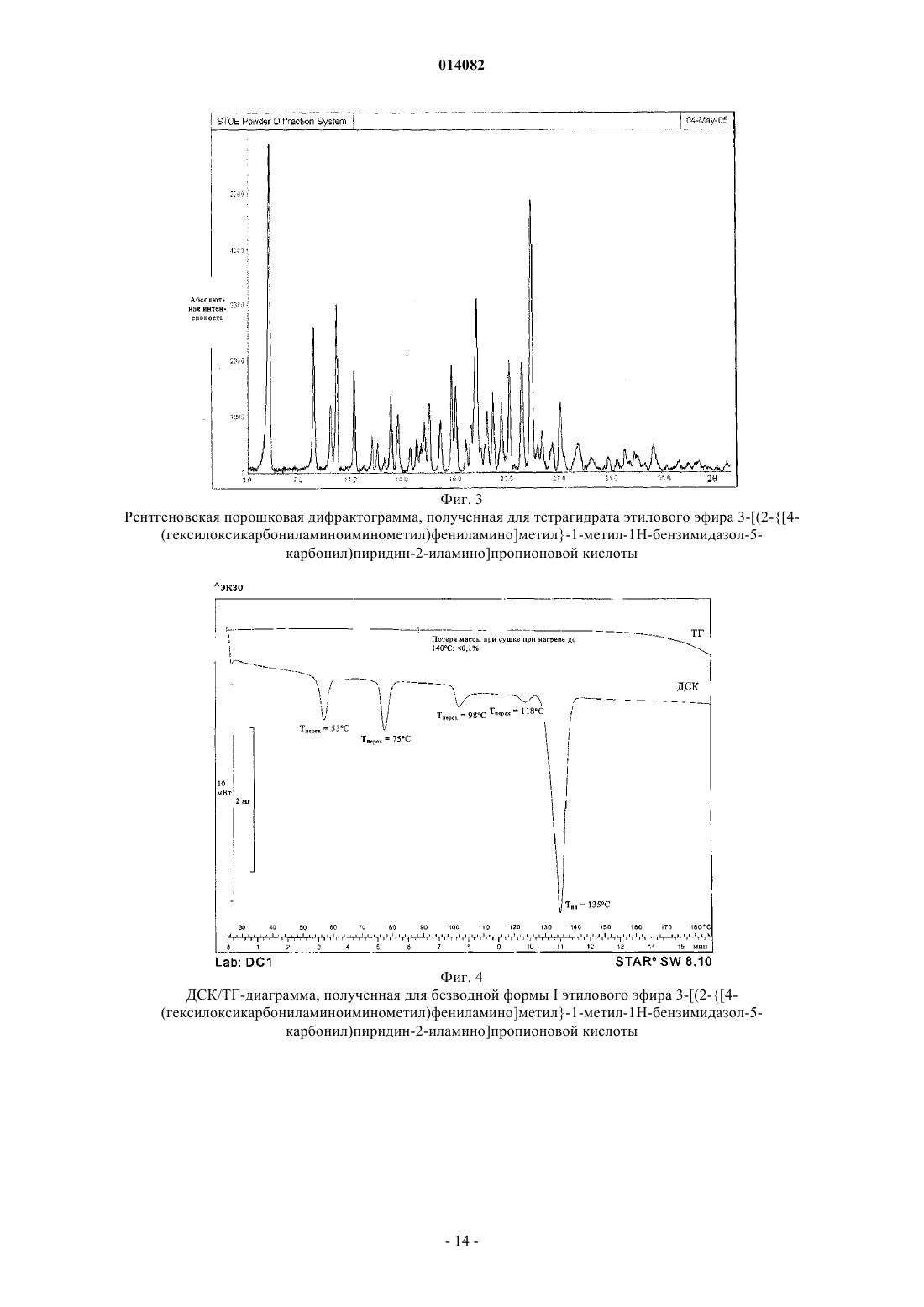
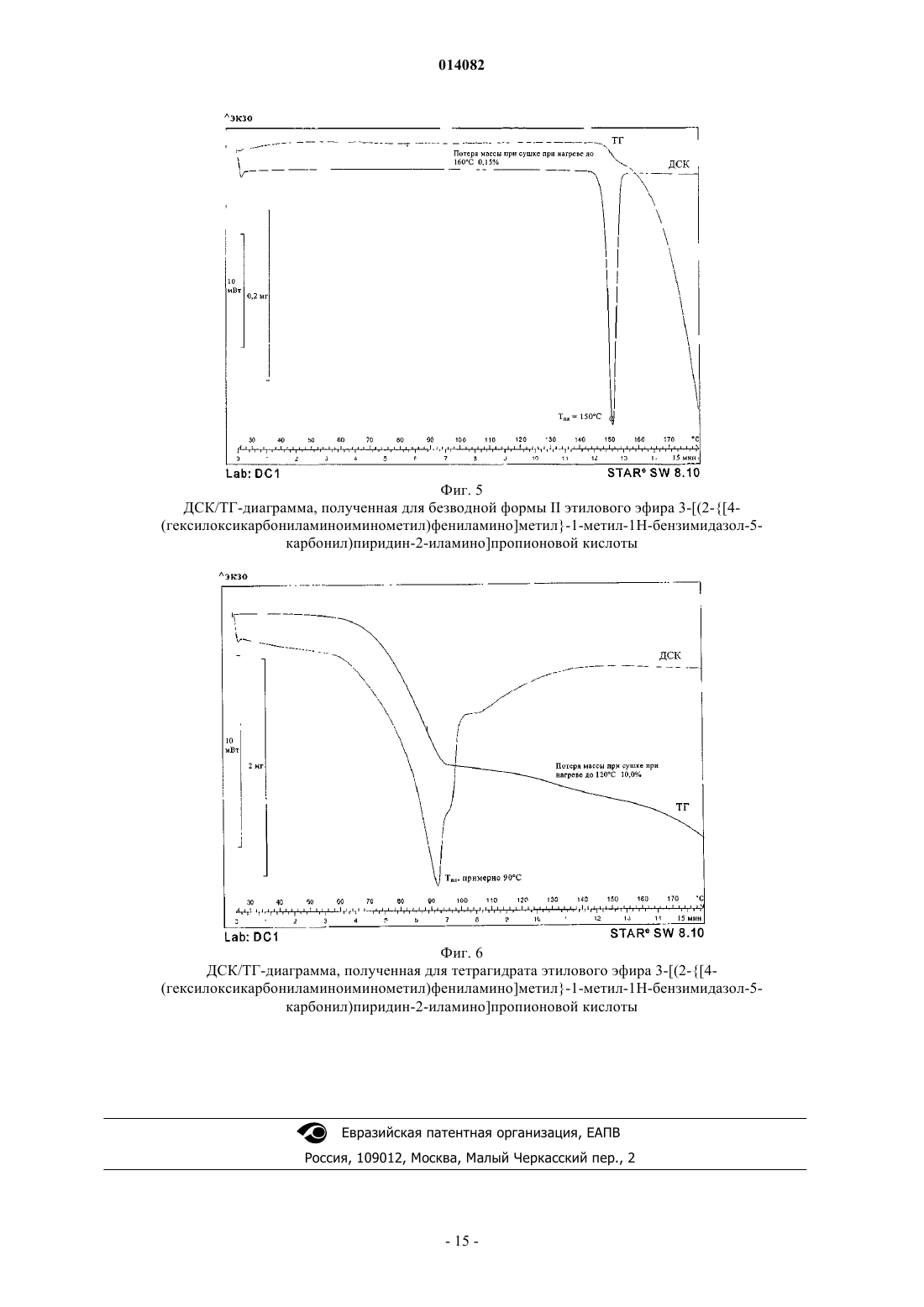
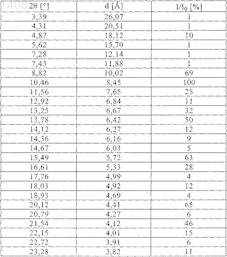
ПОЛИМОРФЫ ЭТИЛОВОГО ЭФИРА 3-[(2-[4-(ГЕКСИЛОКСИКАРБОНИЛАМИНОИМИНОМЕТИЛ)ФЕНИЛАМИНО]МЕТИЛ-1-МЕТИЛ-1 Н-БЕНЗИМИДАЗОЛ-5-КАРБОНИЛ)ПИРИДИН-2-ИЛАМИНО]ПРОПИОНОВОЙ КИСЛОТЫ В изобретении описаны новые полиморфы действующего вещества - этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты, их получение и их применение в качестве лекарственных средств.(71)(73) Заявитель и патентовладелец: БРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНАЦИОНАЛЬ ГМБХ (DE) 014082 Настоящее изобретение относится к новым полиморфам действующего вещества - этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты, к способу их получения и к их применению в качестве лекарственных средств. Это действующее вещество с химической формулой уже известно под названием N-(2-пиридил)-N-(2-этоксикарбонилэтил)амид 1-метил-2-[N-[4-(N-нгексилоксикарбониламидино)фенил]аминометил]бензимидазол-5-илкарбоновой кислоты из публикацииWO 98/37075, в которой описаны соединения с ингибирующим тромбин и увеличивающим тромбиновое время действием. Соединение формулы I представляет собой двойное пролекарственное вещество, являющееся предшественником соединения формулы т.е. соединение формулы I лишь в организме превращается в собственно биологически активное вещество,а именно в соединение формулы II. Основными показаниями к применению соединения химической формулы I являются послеоперационная профилактика тромбозов глубоких вен и профилактика инсультов. Задача настоящего изобретения состояла в получении новых полиморфов соединения формулы I с оптимальным для фармацевтического применения набором свойств. Наличие упомянутых выше фармакологически ценных свойств у известных из уровня техники двузамещенных двухъядерных гетероциклов является основной предпосылкой эффективного применения таких соединений в качестве действующих веществ. Однако наряду с собственно эффективностью при определенном показании действующее вещество для возможности его применения в качестве лекарственного средства по многим критериям должно отвечать и иным требованиям. Подобные критерии большей частью связаны с физико-химическими свойствами действующего вещества. В качестве не ограничивающих примеров подобных критериев можно назвать стабильное сохранение исходным веществом своего действия в различных окружающих условиях, в процессе приготовления фармацевтического препарата и в составе конечных лекарственных средств. Поэтому лекарственное действующее вещество, используемое для приготовления лекарственных композиций, должно обладать высокой стабильностью, сохраняющейся даже в различных окружающих условиях. Обязательное соблюдение этого требования обусловлено необходимостью исключить применение лекарственных композиций, в которых наряду с собственно действующим веществом присутствуют, например, и продукты его разложения. В подобном случае содержание действующего вещества в фармацевтических препаратах может оказаться меньше указанного производителем. В результате абсорбции влаги содержание лекарственного действующего вещества уменьшается изза обусловленного поглощением воды увеличения массы. Поэтому лекарственные средства, проявляющие склонность к поглощению влаги, необходимо на время хранения защищать от влаги, например, за счет добавления соответствующих осушителей либо хранения лекарственного средства в условиях, в которых оно защищено от контакта с влагой. Помимо этого поглощение влаги может привести к уменьшению содержания лекарственного действующего вещества в процессе изготовления фармацевтического препарата, если лекарственное действующее вещество не защищено от контакта с влагой и непосредственно подвергается воздействию факторов окружающей среды. По этой причине лекарственное действующее вещество предпочтительно должно обладать лишь минимально возможной гигроскопичностью. Поскольку для получения лекарственной формы с постоянно воспроизводимым содержанием в ней действующего вещества важное значение имеет его кристаллическая модификация, изначально необходимо получать максимально полную информацию о любом возможном полиморфизме действующего вещества, представленного в кристаллической форме. Если действующее вещество может существовать в различных полиморфных модификациях, то необходимо удостовериться в том, что определенная кристаллическая модификация действующего вещества не претерпит никаких изменений в изготовленном позже на его основе лекарственном препарате. В противном случае подобные полиморфные превращения могут отрицательно сказаться на эффективности медикамента и ее воспроизводимости.-1 014082 Другим критерием, который при определенных условиях может иметь особо важное значение в зависимости от выбранной лекарственной формы или выбранной технологии ее приготовления, является растворимость действующего вещества. Так, например, при приготовлении лекарственных форм в виде растворов (например, для инфузий) обязательным условием является наличие у действующего вещества достаточной растворимости в физиологически совместимых растворителях. Особо важное значение имеет и достаточная растворимость действующего вещества, включаемого в состав лекарственных средств,принимаемых внутрь. В основу настоящего изобретения была положена задача получить лекарственное действующее вещество, которое не только обладало бы высокой фармакологической эффективностью, но и в максимально возможной степени удовлетворяло бы по своим физико-химическим свойствам рассмотренным выше требованиям. При создании изобретения неожиданно было установлено, что указанную выше задачу позволяют решить предлагаемые в изобретении полиморфы соединения формулы I (дабигатрана этексилата), обладающие оптимальным набором свойств. Объектом изобретения в соответствии с этим являются полиморфы этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, обозначаемые соответственно как безводная форма I, безводная форма II и тетрагидрат. Еще одним объектом изобретения являются фармацевтические композиции, содержащие по меньшей мере один из указанных выше полиморфов, а также способ приготовления лекарственных средств, пригодных для профилактики тромбозов вен и инсульта (апоплексического удара) и содержащие предлагаемые в изобретении полиморфы. В соответствии с этим первым объектом настоящего изобретения являются три вышеуказанные полиморфные формы действующего вещества - этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, предпочтительно представленные в кристаллической форме и характеризующиеся температурой плавления Тпл, равной 1353 С (безводная форма I), 1503 С (безводная форма II), соответственно 905 С (тетрагидрат) (определенной с помощью дифференциальной сканирующей калориметрии (ДСК) на основе анализа с использованием максимума пика при скорости нагрева 10 С/мин). Безводная форма I отличается наличием на ее ДСК-диаграмме четырех других слабых эндотермических сигналов, приходящихся на температуры около 53, 75, 98 и 118 С. Эти сигналы обусловлены полностью обратимыми твердофазными переходами, т.е. в интервалах температур от 53 до 75 С, от 75 до 98 С, от 98 до 118 С и от 118 до 135 С существуют четыре другие высокотемпературные фазы безводной формы I. Еще одним объектом настоящего изобретения являются способы избирательного получения трех вышеуказанных полиморфных модификаций, а также получаемые этими способами полиморфные модификации. Согласно изобретению способ получения безводной формы I этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2 иламино]пропионовой кислоты заключается в том, что а) этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания растворяют при нагревании с обратным холодильником в этилацетате,б) полученный раствор охлаждают до температуры порядка 30-35 С и перемешивают при этой температуре в течение последующих 60 мин,в) раствор охлаждают до температуры порядка 15-20 С и затем перемешивают при этой температуре еще в течение примерно 60 мин,г) выпавшие в осадок кристаллы отделяют вакуум-фильтрацией и промывают этилацетатом и затем д) полученный таким путем продукт сушат в сушильном шкафу с циркуляцией воздуха при температуре в пределах от 40 до 50 С. Согласно изобретению способ получения безводной формы II этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2 иламино]пропионовой кислоты заключается в том, что: а) этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания смешивают с небольшим количеством этилацетата,б) полученную таким путем суспензию нагревают до температуры порядка 80 С с образованием при этом прозрачного раствора,в) этот раствор в течение примерно 1 ч кипятят с обратным холодильником,г) выпавшие в осадок кристаллы отфильтровывают и д) полученный таким путем продукт сушат на воздухе. Согласно изобретению способ получения тетрагидрата этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-2 014082 иламино]пропионовой кислоты заключается в том, что: а) этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания при встряхивании и температуре около 60 С растворяют в смеси из ацетона и воды (в соотношении 80:20),б) полученный раствор охлаждают до температуры порядка 30 С и фильтруют в закрываемый сосуд,в) раствор в закрытом сосуде охлаждают до температуры порядка -9 С и выдерживают при этой температуре в течение примерно 30 мин,г) к раствору добавляют предварительно охлажденную до -9 С смесь из ацетона и воды (в соотношении 80:20) и полученную смесь взбалтывают,д) выпавшие в осадок кристаллы отделяют вакуум-фильтрацией и промывают охлажденной до -9 С смесью из ацетона и воды (в соотношении 80:20) и е) полученный таким путем продукт сушат на воздухе при комнатной температуре. Более детально предлагаемые в изобретении кристаллические формы этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты анализировали с помощью рентгеновской порошковой дифрактометрии. Полученные при этом дифрактограммы представлены на фиг. 1-3. Полученные при таком анализе данные приведены ниже в табл. 1-3. Таблица 1 Дифракционные максимумы (рефлексы) (вплоть до угла 2, равного 30) и их интенсивность (относительная), выявленные при анализе этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил) фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты-3 014082 Таблица 2 Дифракционные максимумы (рефлексы) (вплоть до угла 2, равного 30) и их интенсивность (относительная), выявленные при анализе этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил) фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты-4 014082 Таблица 3 Дифракционные максимумы (рефлексы) (вплоть до угла 2, равного 30) и их интенсивность (относительная), выявленные при анализе этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил) фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты В приведенных выше табл. 1-3 величина 2 [] обозначает угол дифракции в градусах, а величина d[] обозначает определенные межплоскостные расстояния в ангстремах . Для получения рентгеновских порошковых дифрактограмм согласно изобретению использовали дифрактометр STOE STADI Р, оснащенный позиционно-чувствительным детектором (детектором оптического излучения), медным анодом в качестве источника рентгеновского излучения и первичным моно-5 014082 хроматором (K1-излучение меди,= 1,54056 , 40 кВ, 40 мА). Краткое описание чертежей На фиг. 1-3 представлены рентгеновские порошковые дифрактограммы, полученные для трех кристаллических форм этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты. На фиг. 4-6 представлены диаграммы, полученные при термоанализе (ДСК/ТГ (термогравиметрия трех кристаллических форм этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты. Примеры Температуры плавления определяли посредством ДСК с использованием для этого прибора фирмыMettler-Toledo (тип DSC 821). Температуре плавления соответствует температурный пик на ДСКдиаграмме. Точность указанных температур плавления составляет примерно 3 С, а для тетрагидрата 5 С, поскольку из тетрагидрата при его плавлении выделяется включенная в кристаллическую решетку кристаллизационная вода, чем обусловлено появление очень широкого эндотермического сигнала. Исходное соединение - этиловый эфир 3-[(2-[4-(аминогексилоксикарбонилиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты можно получать, например, способом, описанным в публикации WO 98/37075, пример 113. Пример 1. Этиловый эфир 3-[(2-[4-(аминогексилоксикарбонилиминометил)фениламино] метил-1 метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты (безводная форма I). 1500 г (2,389 моль) этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания (полученного описанным в WO 98/37075 способом) растворяют при нагревании с обратным холодильником в 12 л этилацетата. Затем полученный раствор охлаждают до 30-35 С. Через несколько минут начинает выкристаллизовываться продукт. Раствор перемешивают еще в течение 60 мин при 3035 С, а также в течение последующих 60 мин при 15-20 С, после чего осадок отделяют вакуумфильтрацией, промывают его 3 л этилацетата и сушат в сушильном шкафу с циркуляцией воздуха при 40-50 С. Выход: 88,5% от теории. Пример 2. Этиловый эфир 3-[(2-[4-(аминогексилоксикарбонилиминометил)фениламино]метил-1 метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты (безводная форма II). 2,0 г этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1 метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания (полученного описанным в WO 98/37075 способом) смешивают с 10 мл этилацетата. Полученную в результате суспензию нагревают до 80 С (при этом вещество переходит в раствор) и в течение 1 ч кипятят с обратным холодильником. Примерно через 30 мин кипячения с обратным холодильником начинает кристаллизоваться форма II. После этого выпавшее в осадок вещество отфильтровывают и сушат на воздухе. Выход: 85% от теории. Пример 3. Тетрагидрат этилового эфира 3-[(2-[4-(аминогексилоксикарбонилиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты. 0,5 г этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1 метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания (полученного описанным в WO 98/37075 способом) при встряхивании и при 60 С растворяют в 5 мл смеси из ацетона и воды в соотношении 80:20. Полученный раствор охлаждают до примерно 30 С, фильтруют,например, через фильтр Sartorius Minisart SRP 15, в 10-милллилитровую склянку и закрывают ее. Затем раствор охлаждают в смеси из льда и этанола до примерно -9 С. При этом вещество начинает самостоятельно кристаллизоваться. После примерно 30-минутной выдержки в ледяной бане добавляют примерно 3 мл охлажденной до -9 С смеси из ацетона и воды (в соотношении 80:20), полученную смесь взбалтывают и затем фильтруют через вакуум-фильтр, например через круглый фильтр SchleicherSchll595. Далее дополнительно промывают еще примерно 5 мл охлажденной до -9 С смеси из ацетона и воды(в соотношении 80:20). Отфильтрованное вещество соскабливают с круглого фильтра в лабораторный кристаллизатор и сушат на воздухе при комнатной температуре. Выход: 97% от теории. Пример 4. Ампула с сухим препаратом, содержащим 75 мг действующего вещества на 10 мл. Состав: Получение. Действующее вещество и маннит растворяют в воде. После расфасовывания в ампулы раствор подвергают сублимационной сушке. Готовый для применения раствор приготавливают растворением сухого состава в воде для инъекций.-6 014082 Пример 5. Ампула с сухим препаратом, содержащим 35 мг действующего вещества на 2 мл. Состав: Получение. Действующее вещество и маннит растворяют в воде. После расфасовывания в ампулы раствор подвергают сублимационной сушке. Готовый для применения раствор приготавливают растворением сухого состава в воде для инъекций. Пример 6. Таблетка с 50 мг действующего вещества. Состав: Получение. Ингредиент (1) смешивают с ингредиентами (2) и (3) и полученную смесь гранулируют с использованием водного раствора ингредиента (4). К высушенному грануляту примешивают ингредиент (5). Из этой смеси прессуют двоякоплоские таблетки с двусторонней фасеткой и односторонней делительной насечкой. Диаметр таблеток: 9 мм. Пример 7. Таблетка с 350 мг действующего вещества. Состав: Получение. Ингредиент (1) смешивают с ингредиентами (2) и (3) и полученную смесь гранулируют с использованием водного раствора ингредиента (4). К высушенному грануляту примешивают ингредиент (5). Из этой смеси прессуют двоякоплоские таблетки с двусторонней фасеткой и односторонней делительной насечкой. Диаметр таблеток: 12 мм. Пример 8. Капсулы с 50 мг действующего вещества. Состав: Получение. Ингредиент (1) растирают совместно с ингредиентом (3). К этой полученной растиранием смеси при интенсивном перемешивании добавляют смесь ингредиентов (2) и (4). В завершение эту порошковую смесь расфасовывают в машине для заполнения капсул в твердожелатиновые разъемные капсулы размера 3. Пример 9. Капсулы с 350 мг действующего вещества. Состав: Получение. Ингредиент (1) растирают совместно с ингредиентом (3). К этой полученной растиранием смеси при интенсивном перемешивании добавляют смесь ингредиентов (2) и (4). В завершение эту-7 014082 порошковую смесь расфасовывают в машине для заполнения капсул в твердожелатиновые разъемные капсулы размера 0. Пример 10. Суппозитории с 100 мг действующего вещества. Состав 1 свечи: Получение и структура пеллетов (гранулятов) из примеров 11 и 12 подробно описаны в WO 03/074056. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в кристаллической форме, характеризующийся температурой плавления Тпл, равной 1353 С (безводная форма I) (определенной с помощью дифференциальной сканирующей калориметрии на основе анализа с использованием максимума пика при скорости нагрева 10 С/мин), и дифракционными максимумами (рефлексами) (вплоть до угла 2, равного 30) и их интенсивностью (относительная), выявленными рентгеновской порошковой дифрактометрией 2. Этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в кристаллической форме, характеризующийся температурой плавления Тпл, равной 1503 С (безводная форма II) (определенной с помощью дифференциальной сканирующей калориметрии на основе анализа с использованием максимума пика при скорости нагрева 10 С/мин), и дифракционными максимумами (рефлексами) (вплоть до угла 2, равного 30) и их интенсивностью (относительная), выявленными рентгеновской порошковой дифрактометрией 3. Тетрагидрат этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в кристаллической форме, характеризующийся температурой плавления Тпл, равной 905 С (определенной с помощью дифференциальной сканирующей калориметрии на основе анализа с использованием максимума пика при скорости нагрева 10 С/мин), с одновременным выделением включенной в кристаллическую решетку кристаллизационной воды (тетрагидрат), и дифракционными максимумами (рефлексами) (вплоть до угла 2, равного 30) и их интенсивностью (относительная), выявленными рентгеновской порошковой дифрактометрией 4. Применение соединения по одному из пп.1-3 для приготовления лекарственного средства с увеличивающим тромбиновое время действием. 5. Применение соединения по одному из пп.1-3 для приготовления лекарственного средства, предназначенного для профилактики тромбозов вен и инсульта. 6. Фармацевтическая композиция, содержащая соединение по одному из пп.1-3, необязательно совместно с одним или несколькими инертными носителями и/или разбавителями. 7. Способ приготовления фармацевтической композиции по п.6, отличающийся тем, что соединение по одному из пп.1-3 не химическим путем объединяют с одним или несколькими инертными носителями и/или разбавителями. 8. Способ получения безводной формы I этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионо- 11014082 вой кислоты, отличающийся тем, что: а) этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания растворяют при нагревании с обратным холодильником в этилацетате,б) полученный раствор охлаждают до температуры порядка 30-35 С и перемешивают при этой температуре в течение последующих 60 мин,в) раствор охлаждают до температуры порядка 15-20 С и затем перемешивают при этой температуре еще в течение примерно 60 мин,г) выпавшие в осадок кристаллы отделяют вакуум-фильтрацией и промывают этилацетатом и затем д) полученный таким путем продукт сушат в сушильном шкафу с циркуляцией воздуха при температуре в пределах от 40 до 50 С. 9. Способ получения безводной формы II этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, отличающийся тем, что: а) этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания смешивают с небольшим количеством этилацетата,б) полученную таким путем суспензию нагревают до температуры порядка 80 С с образованием при этом прозрачного раствора,в) этот раствор в течение примерно одного часа кипятят с обратным холодильником,г) выпавшие в осадок кристаллы отфильтровывают и д) полученный таким путем продукт сушат на воздухе. 10. Способ получения тетрагидрата этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, отличающийся тем, что: а) этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты в виде основания при встряхивании и температуре около 60 С растворяют в смеси из ацетона и воды (в соотношении 80:20),б) полученный раствор охлаждают до температуры порядка 30 С и фильтруют в закрываемый сосуд,в) раствор в закрытом сосуде охлаждают до температуры порядка -9 С и выдерживают при этой температуре в течение примерно 30 мин,г) к раствору добавляют предварительно охлажденную до -9 С смесь из ацетона и воды (в соотношении 80:20) и полученную смесь взбалтывают,д) выпавшие в осадок кристаллы отделяют вакуум-фильтрацией и промывают охлажденной до -9 С смесью из ацетона и воды (в соотношении 80:20) и е) полученный таким путем продукт сушат на воздухе при комнатной температуре. 11. Этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, представляющий собой безводную форму I и получаемый способом по п.8. 12. Этиловый эфир 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил 1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, представляющий собой безводную форму II и получаемый способом по п.9. 13. Тетрагидрат этилового эфира 3-[(2-[4-(гексилоксикарбониламиноиминометил)фениламино] метил-1-метил-1 Н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты, получаемый способом по п.10. Фиг. 1 Рентгеновская порошковая дифрактограмма, полученная для безводной формы I этилового эфира 3-[(2[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты Фиг. 2 Рентгеновская порошковая дифрактограмма, полученная для безводной формы II этилового эфира 3-[(2[4-(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты Фиг. 3 Рентгеновская порошковая дифрактограмма, полученная для тетрагидрата этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты Фиг. 4 ДСК/ТГ-диаграмма, полученная для безводной формы I этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты Фиг. 5 ДСК/ТГ-диаграмма, полученная для безводной формы II этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1 Н-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты Фиг. 6 ДСК/ТГ-диаграмма, полученная для тетрагидрата этилового эфира 3-[(2-[4(гексилоксикарбониламиноиминометил)фениламино]метил-1-метил-1H-бензимидазол-5 карбонил)пиридин-2-иламино]пропионовой кислоты
МПК / Метки
МПК: C07D 401/12, A61K 31/4184, A61K 31/4402, A61P 9/14, A61P 7/02
Метки: полиморфы, этилового, 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой, кислоты, эфира
Код ссылки
<a href="https://eas.patents.su/16-14082-polimorfy-etilovogo-efira-3-2-4-geksiloksikarbonilaminoiminometilfenilaminometil-1-metil-1n-benzimidazol-5-karbonilpiridin-2-ilaminopropionovojj-kisloty.html" rel="bookmark" title="База патентов Евразийского Союза">Полиморфы этилового эфира 3-[(2-{[4-(гексилоксикарбониламиноиминометил)фениламино]метил}-1-метил-1н-бензимидазол-5-карбонил)пиридин-2-иламино]пропионовой кислоты</a>