Производные тетрагидроизохинолилсульфонамидов, их получение и применение в терапии
Номер патента: 10234
Опубликовано: 30.06.2008
Авторы: Диас Мартин Хуан Антонио, Химинес Баргуэно Мария Долорес
Формула / Реферат
1. Соединение формулы I
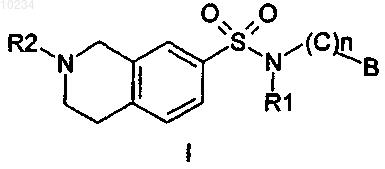
где n может принимать значения от 1 до 6;
-(С)n- представляет собой C1-6-алкилиден, при необходимости замещенный заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино или C1-3-алкокси;
R1 представляет собой атом водорода; C1-6-алкил;
R2 представляет собой атом водорода;
C1-6-алкил или C3-6-циклоалкил, при необходимости замещенные заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси, C3-6-циклоалкила, моноциклического гетероарила, такого как тиенил, фурил или пирролил, или арила, такого как фенил или нафтил; причем арил при необходимости может быть замещен заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила,
C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси или C1-3-алкилидендиоксигруппы;
В представляет собой группу NR3R4, где
R3 и R4 представляют собой независимо друг от друга С1-6-алкил, атом водорода или
R3 и R4 представляют собой совместно C1-6-алкилиден, C2-8-алкенилиден, C1-3-алкилиден-О-C1-3-алкилиден или C1-3-алкилиден-N(R5)-C1-3-алкилиден, где R5 представляет собой атом водорода, C1-3-алкил или C1-6-алкилкарбонил, причем эти C1-3-алкил и С1-6-алкилкарбонил могут быть замещены атомом галогена, гидрокси, C1-3-алкокси, нитро, циано или амино; или
циклический амин, связанный по углероду с группой -NR1-(C)n-, выбранный из азиридина, азетидина, пирролидина, пиперидина и морфолина;
причем группы R3, R4, а также циклический амин при необходимости могут быть замещены заместителями в числе от 1 до 4, выбранными из фенила, бензила, атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила или C1-3-алкокси; атом азота также при необходимости может быть замещен C1-3-алкилом, в виде основания или кислотно-аддитивной соли, также как и в виде гидрата или сольвата,
за исключением соединения, в котором R1 и R2 представляют собой атомы водорода, B представляет собой диметиламиногруппу и -(С)n- представляет собой этилиденовую группу.
2. Соединение по п.1, отличающееся тем, что
n равно 2, 3 или 4; и
R1 представляет собой атом водорода или C1-2-алкил; и
R2 представляет собой атом водорода, C1-4-алкил или С5-6циклоалкил, при необходимости замещенные заместителями в числе от 1 до 4, выбранными из фенила, С3-6-циклоалкила, C1-2-пергалогеналкила, C1-3-галогеналкила или C1-3-алкокси; причем фенил при необходимости может быть замещен заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила, C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси или C1-3-алкилидендиоксигруппы; и
B представляет собой: группу NR3R4, где
R3 и R4 представляют собой независимо друг от друга C1-4-алкил; или
в случае, когда R3 и R4 представляют собой совместно C1-6-алкилиден, C2-8-алкенилиден, C1-3-алкилиден-О-C1-3-алкилиден или C1-3-алкилиден-N(R5)-C1-3-алкилиден, В представляет собой группу
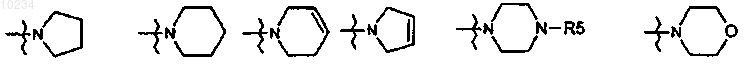
или циклический амин, связанный по углероду с группой -NR1-(C)n-, выбранный из азиридина, азетидина, пирролидина, пиперидина и морфолина;
причем группы R3, R4 и R5, а также циклический амин при необходимости могут быть замещены; в виде основания или кислотно-аддитивной соли, а также в виде гидрата или сольвата.
3. Соединение по п.2, отличающееся тем, что, когда B представляет собой группу NR3R4 и R3 и R4 образуют совместно C1-6-алкилиден, C2-8-алкенилиден, C1-3-алкилиден-О-C1-3-алкилиден или C1-3-алкилиден-N(R5)-C1-3-алкилиден или когда В представляет собой циклический амин, В выбран из следующих групп:
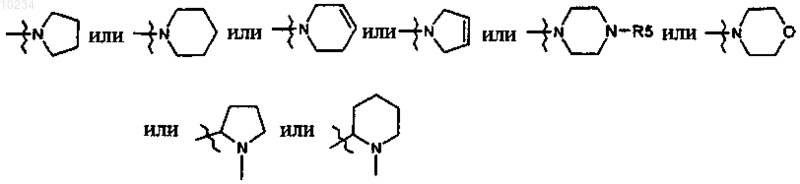
4. Соединение по пп.1, 2 или 3, отличающееся тем, что оно представляет собой
N-[3-(диметиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(диэтиламино)пропил]-2-метил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(диэтиламино)пропил]-N-метил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
2-бензил-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
2-(циклопропилметил)-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
2-(циклогексилметил)-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-N-[3-(2-метилпиперидин-1-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(3,6-дигидропиридин-1(2H)-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(диэтиламино)пропил]-2-изопропил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(диэтиламино)пропил]-2-(2-тиенилметил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(диэтиламино)пропил]-2-(3-тиенилметил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(2,5-дигидро-1H-пиррол-1-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
2-циклогексил-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(циклогексилметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(2,5-дигидро-1H-пиррол-1-ил)пропил]-2-метил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(4-бензилпиперазин-1-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-(3-пирролидин-1-илпропил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-(3-морфолин-4-илпропил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
N-[3-(диметиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
2-(циклогексилметил)-N-(3-пирролидин-1-илпропил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(циклопропилметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-бензил-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(4-изопропилбензил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(1,3-бензодиоксол-5-илметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(-)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+)-2-(циклогексилметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид и
(-)-2-(циклогексилметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид в виде основания или кислотно-аддитивной соли, также как и в виде гидрата или сольвата;
(+/-)-2-(4-бромбензил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(2,5-диметоксибензил)-)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(2-метилбутил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(3-метоксибензил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;
(+/-)-2-(3,5-диметилбензил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид.
5. Соединение формулы II
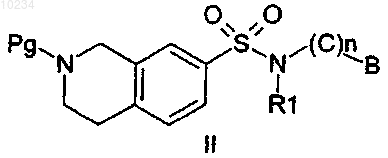
где Pg представляет собой атом водорода или защитную группу и -(С)n- и R1 имеет такие же значения, как и определенные в п.1, а В представляет собой группу NR3R4, где R3 и R4 имеют такие же значения, как и определенные в п.1; или циклический амин, связанный по углероду с группой -NR1-(C)n-, выбранный из азиридина, азетидина, пирролидина, пиперидина или морфолина; причем группы R3, R4, а также циклический амин, при необходимости могут быть замещены так же, как определено в п.1.
6. Фармацевтическая композиция, содержащая соединение формулы I по любому из пп.1-4 или его соль, сольват или гидрат и по меньшей мере один фармацевтически приемлемый эксципиент.
7. Применение соединения формулы I по любому из пп.1-4 или его соли, сольвата или гидрата для получения лекарственного средства, предназначенного для лечения ожирения и диабета.
8. Применение соединения формулы I по любому из пп.1-4 или его соли, сольвата или гидрата для получения лекарственного средства, предназначенного для лечения заболеваний центральной нервной системы, таких как нарушения сна и бессонница, нарколепсия, болезнь Альцгеймера и другие деменции, болезнь Паркинсона, нарушения внимания у детей с гиперкинетическим синдромом, нарушения памяти и способности к обучению, эпилепсия, шизофрения, умеренные когнитивные нарушения, депрессия, тревожные состояния, половые дисфункции, головокружение и транспортная болезнь.
Текст
010234 Объектом настоящего изобретения являются производные сульфонамидов, их получение и применение в терапии, в частности, для лечения нарушений, при которых улучшение состояния обеспечивается модуляцией H3-рецепторов гистамина, таких как ожирение, диабет и заболевания центральной нервной системы, такие как нарушения сна и бессонница. В заявке WO 03/055848 описаны производные мочевины, являющиеся антагонистами VR1. В заявкеWO 2004/019935 описаны производные 3-(сульфонамидоэтил)индола, обладающие глюкокортикоидной активностью, которые могут быть использованы в лечении воспалительных, аллергических и пролиферативных заболеваний. В заявке WO 02/076925 описаны неимидазольные производные арилалкиламинов,которые являются антагонистами H3-рецепторов гистамина. Соответственно, первым объектом настоящего изобретения являются соединения, соответствующие формуле In может принимать значения от 1 до 6;-(С)n- представляет собой C1-6-алкилиден, при необходимости замещенный заместителями в числе от 1 до 4, выбранными из атома галогена, групп гидрокси, нитро, циано, амино, C1-3-моноалкиламино,C2-6-диалкиламино или C1-3-алкокси;R1 представляет собой атом водорода; C1-6-алкил;R2 представляет собой атом водорода; C1-6-алкил или C3-6-циклоалкил, при необходимости замещенные заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино,C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила, C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3 алкокси или C1-3-алкилидендиоксигруппы; В представляет собой группу NR3R4, гдеR3 и R4 представляют собой независимо друг от друга C1-6-алкил, атом водорода; илиR3 и R4 представляют собой совместно С 1-6-алкилиден, С 2-8 алкенилиден, C1-3-алкилиден-О-C1-3 алкилиден или C1-3-алкилиден-N (R5)-C1-3-алкилиден, где R5 представляет собой атом водорода, C1-3 алкил или C1-6-алкилкарбонил, причем эти группы C1-3-алкил и C1-6-алкилкарбонил могут быть замещены атомом галогена, гидрокси, C1-3-алкокси, нитро, циано или амино; или циклический амин, связанный по углероду с группой -NR1-(С)n-, такой как азиридин, азетидин,пирролидин, пиперидин или морфолин; причем группы R3, R4, а также циклический амин, при необходимости могут быть замещены заместителями в числе от 1 до 4, выбранными из фенила, бензила, атома галогена, гидрокси, нитро, циано,амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила или C1-3-алкокси; атом азота при необходимости может быть замещен C1-3-алкилом. В рамках настоящего изобретения подразумевают, чтоCx-z означает углеродную цепочку, которая может содержать от х до z атомов углерода, например,C1-3 означает углеродную цепочку, которая может содержать от 1 до 3 атомов углерода; алкил означает алифатическую насыщенную линейную или разветвленную группу; например, C1-4 алкил представляет собой насыщенную линейную или разветвленную углеродную цепочку, содержащую от 1 до 6 атомов углерода, в частности метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил и т.д.; термин Сх-y-алкилиден означает линейный или разветвленный двухвалентный Сх-у-алкил; термин С 2-8-алкенилиден означает ненасыщенный линейный или разветвленный двухвалентный Сх-у-алкил; Сх-у-алкокси означает алифатическую насыщенную линейную или разветвленную алкоксигруппу,содержащую от х до у атомов углерода; атом галогена означает фтор, хлор, бром или иод;C1-2-пергалогеналкил означает C1-2-алкил, в котором все атомы водорода замещены атомами галогена;C1-3-галогеналкил означает C1-3-алкил, в котором по меньшей мере один атом водорода замещен атомом галогена. Соединения формулы I могут содержать один или несколько асимметрических атомов углерода. Они могут, таким образом, существовать в форме энантиомеров или диастереоизомеров. Эти энантиомеры, диастереоизомеры, а также их смеси, включая рацемические смеси, составляют часть настоящего изобретения. Соединения общей формулы I могут существовать в виде свободных оснований или кислотноаддитивных солей, которые в равной мере составляют часть настоящего изобретения. В эти соли согласно настоящему изобретению включают как соли фармацевтически приемлемых кислот, так и соли мине-1 010234 ральных и органических кислот, применение которых позволяет осуществлять соответствующее разделение или кристаллизацию соединений формулы I. Эти соли могут быть получены способами, известными специалисту в данной области техники, например взаимодействием соединения формулы I в виде основания с кислотой в соответствующем растворителе, таком как спиртовой раствор или органический растворитель, с последующим отделением реакционной среды, содержащей эти соли, выпариванием растворителя или фильтрованием. Соединения формулы I могут существовать равным образом в виде гидратов или сольватов, а именно в виде ассоциатов или комбинаций с одной или несколькими молекулами воды или с растворителем. Такие гидраты и сольваты составляют в равной мере часть изобретения. В рамках настоящего изобретения под защитной группой Pg понимают группу, которая, с одной стороны, защищает в ходе синтеза функциональную группу, такую как гидрокси или аминогруппа, и, с другой стороны, позволяет восстанавливать функциональную группу без изменения в конце синтеза. Примеры защитных групп, а также способы введения и удаления защитных групп, приведены в издании"Protective Groups in Organic Synthesis 3th Ed.", Greene et Wuts (John WileySons, Inc., New York, 1999). Объектом настоящего изобретения в равной мере являются соединения, выбранные из следующих подгрупп, гдеR1 представляет собой атом водорода или группу C1-2-алкил; и/илиR2 представляет собой атом водорода, С 1-4-алкил или С 5-6-циклоалкил, при необходимости замещенные заместителями в числе от 1 до 4, выбранными из фенила, C3-6-циклоалкила, C1-2-пергалогеналкила, C1-3-галогеналкила или C1-3-алкокси; причем фенил при необходимости может быть замещен заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3 моноалкиламино, C2-6-диалкиламино, C1-3-алкила, C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси илиR3 и R4 представляют собой независимо друг от друга C1-4-алкил; или в случае, когда R3 и R4 представляют собой совместно C1-6-алкилиден, C2-8-алкенилиден, С 1-3 алкилиден-O-С 1-3-алкилиден или C1-3-алкилиден-N(R5)-C1-3-алкилиден, В представляет собой группу или циклический амин, связанный по углероду с группой -NR1-(C)n-, такой как азиридин, азетидин,пирролидин, пиперидин или морфолин; причем группы R3, R4 и R5, а также циклический амин, при необходимости могут быть замещены; и, в частности, из подгруппы, где n, R1, R2 и В имеют такие же значения, как и определенные ранее. В частности, когда В представляет собой группу NR3R4 и R3 и R4 образуют совместно C1-6 алкилиден, C2-8-алкенилиден, C1-3-алкилиден-O-C1-3-алкилиден или C1-3-алкилиден-N(R5)-С 1-3-алкилиден или когда В представляет собой циклический амин, тогда В выбирают из следующих групп: Другим объектом настоящего изобретения являются следующие соединения: 1. N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 2. (+/-)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 3. N-[3-(диэтиламино)пропил]-2-метил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 4. N-[3-(диэтиламино)пропил]-N-метил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 5. 2-бензил-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 6. 2-(циклопропилметил)-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 7. 2-(циклогексилметил)-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 8. ( +/-)-N-[3-(2-метилпиперидин-1-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 9. N-[3-(3,6-дигидропиридин-1(2H)-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 10. N-[3-(диэтиламино)пропил]-2-изопропил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 11. N-[3-(диэтиламино)пропил]-2-(2-тиенилметил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 12. N-[3-(диэтиламино)пропил]-2-(3-тиенилметил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 13. N-[3-(2,5-дигидро-1H-пиррол-1-ил)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид; 14. 2-циклогексил-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид;(+/-)-2-(2-метилбутил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамид; 33. (+/-)-2-(3-метоксибензил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамид и 34. (+/-)-2-(3,5-диметилбензил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин 7-сульфонамид. Вторым объектом настоящего изобретения являются способы получения соединений формулы I по настоящему изобретению. Так, соединения формулы I могут быть получены по способам, приведенным на схеме 1. Схема 1 По способу, приведенному на схеме 1, соединения формулы I, где R2 отличается от атома водорода,получают реакцией восстановления амина, приводя во взаимодействие вторичный амин формулы I, гдеR2 представляет собой Н, с альдегидом или кетоном формулы III, где группы R6 и R7 в результате взаимодействия образуют совместно группу R2, такую же, как и определенная для формулы I. Соединения формулы I, где R2 представляет собой атом водорода, могут быть получены удалением защитной группы из соединения формулы II по традиционным способам, известным специалисту в данной области техники. Например, для соединений формулы II в том случае, когда Pg является группой трифторацетил, удаление защитной группы может быть осуществлено в присутствии основания, такого как, например, карбонат натрия или калия, аммиак или гидроксид бария, в протонном растворителе, таком как вода, метанол или смесь таких растворителей, при температуре в интервале от 0 до 100 С. Как альтернатива, удаление защитной группы из соединений формулы II в том случае, когда Pg является группой трифторацетил, может быть осуществлено в присутствии кислоты, такой как, например, соляная кислота, в протон-3 010234 ном или апротонном растворителе, таком как вода, метанол, этанол, этилацетат или смесь таких растворителей, при температуре в интервале от 0 до 100 С. Пояснения к способу приведены в примерах. Соединения, исходные для формулы II, могут быть получены по схеме 2 или синтезированы по традиционным способам, известным специалисту в данной области техники. Схема 2 Согласно этой схеме соединения формулы II, где n, R1 и В такие же, как и определенные для формулы I, могут быть получены взаимодействием амина формулы V, где R1 и В такие же, как и определенные для формулы I, с сульфонилхлоридом формулы IV, где Pg представляет собой соответствующую защитную группу, такую как, например, трифторацетамид, с образованием производного соединения типа сульфонамида формулы II по традиционным способам, известным специалисту в данной области техники, например, взаимодействие может быть осуществлено в протонном или апротонном растворителе, таком как тетрагидрофуран, дихлорметан, этилацетат, N,N-диметилформамид, ацетонитрил или смесь таких растворителей, при температуре в интервале от 0 до 100 С в присутствии основания, такого как,например, карбонат калия, натрия, диизопропилэтиламин или триэтиламин. Как альтернатива, соединения формулы II могут быть получены по реакции Мицунобу согласно схеме 3. Схема 3 Согласно этому альтернативному варианту сульфонамид формулы VII, где группа R1 такая же, как и определенная для формулы I, приводят во взаимодействие с аминоспиртом формулы VIII, где n и В такие же, как и определенные ранее. Взаимодействие может быть осуществлено традиционным образом в присутствии реактива Мицунобу, такого как азопроизводное соединение, например диэтилазодикарбоксилат, диизопропилазодикарбоксилат, дитрет-бутилазодикарбоксилат, 1,1'-(азодикарбонил)дипиперидин или N,N,N',N'-тетраметилазодикарбоксамид, и фосфина, например, трифенилфосфина или трибутилфосфина. Взаимодействие может быть осуществлено в апротонном растворителе, таком как тетрагидрофуран, или диоксан, или смесь таких растворителей, при температуре в интервале от 0 до 100 С с получением соединения формулы II. Сульфонамид формулы VII, где группа R1 такая же, как и определенная для формулы I, может быть получен взаимодействием амина формулы VI, где группа R1 такая же, как и определенная для формулы I, с сульфонилхлоридом формулы IV, где Pg представляет собой соответствующую защитную группу, такую как, например, трифторацетамид, по традиционным способам, известным специалисту в данной области техники, например, взаимодействие может быть осуществлено в протонном или апротонном растворителе, таком как тетрагидрофуран, дихлорметан, этилацетат,N,N-диметилформамид, ацетонитрил или смесь таких растворителей, при температуре в интервале от 0 до 100 С в присутствии основания, такого как, например, карбонат калия, натрия, диизопропилэтиламин или триэтиламин. Исходные соединения формулы IV и амины формул V и VIII имеются непосредственно в продаже или могут быть синтезированы по традиционным способам, известным специалисту в данной области техники или из литературных источников. Например, диамины формулы V, где n равно 3, могут быть получены согласно схеме 4. Схема 4 По этому способу соединения формулы V, где п равно 3, R1 является атомом водорода и В представляет собой аминогруппу, могут быть получены по реакции присоединения между амином формулыX, где R3 и R4 такие же, как и определенные ранее, и акрилонитрилом формулы IX с образованием производного соединения типа аминонитрила формулы XI по традиционным способам, известным специа-4 010234 листу в данной области техники, с последующим восстановлением нитрила. Восстановление может быть осуществлено по способам, известным специалисту в данной области техники, например, в присутствии гидрида диизобутилалюминия при температуре в интервале от -70 до 40 С в апротонном растворителе,таком как дихлорметан, толуол или смесь таких растворителей; восстановление может быть осуществлено также в присутствии восстановителя, такого как водород, в присутствии катализатора, такого, как платина, палладий или никель Ренея, в растворителе, таком как метанол или этилацетат, с получением соединения формулы V, где n равно 3, R1 является атомом водорода и В представляет собой аминогруппу. Соединения формулы V, где R1 представляет собой группу C1-6-алкил, могут быть получены алкилированием соединения формулы V, полученного ранее, по традиционным способам, известным специалисту в данной области техники. Объектом настоящего изобретения являются в равной мере соединения формулы II, когда Pg представляет собой защитную группу или атом водорода, в качестве промежуточных соединений для получения соединения формулы I. Следующие примеры приводятся для иллюстрации соответствующих способов и методик получения по настоящему изобретению, не ограничивая все же пределов формулы изобретения. Пример 1. Гидрохлорид N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамида(0,015 моль) 2-(2,2,2-трифторацетил)-1,2,3,4-тетрагидроизохинолин-7 сульфонилхлорида и 2,00 г (0,015 моль) (+/-)-2-(1-метилпирролидин-2-ил)-этиламина в 50 мл дихлорметана перемешивают в течение ночи при комнатной температуре. Раствор концентрируют досуха. Образовавшееся твердое вещество очищают хроматографией на колонке с силикагелем смесью дихлорметан/метанол (97:3), используемой в качестве элюента, с получением 4,30 г требуемого продукта в виде белого твердого вещества.(+/-)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамида. Раствор 4,30 г (0,0094 моль) 2-(2,2,2-трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамидо-[2-(1-метилпирролидин-2-ил)этил]гидрохлорида в 50 мл метанола, насыщенного хлористым водородом, нагревают в течение двенадцати часов при 60 С. Смесь охлаждают и образовавшееся твердое вещество отфильтровывают, промывают метанолом и сушат. Получают 2,00 г требуемого продукта в виде белого твердого вещества.(2 Н, м), 2,7 (3H, м), 2,1 (1 Н, м), 1,9 (3H, м), 1,6 (2 Н, м), 2,7 (3H, с), 2,9 (2 Н, т). 1.3. Гидрохлорид (+) или (-)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамида. Соединение, полученное на стадии 1.2, разделяют препаративной хроматографией на хиральной фазе с получением упомянутых в подзаголовке энантиомеров. В опыте разделение 15,00 г (+/-)-N-[2-(1 метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамида осуществлено на системе препаративной ВЭЖХ PROCHROM LC50 с неподвижной фазой CHIRALPCK AD и подвижной фазой,образованной смесью изогексан/этанол/метанол (80%:10%:10%)+0,2% диэтиламина, с получением 5,39 г правовращающего продукта в виде белого порошка с энантиомерной чистотой на хиральной фазе 99,67% и 4,89 г левовращающего продукта в виде белого порошка с энантиомерной чистотой на хиральной фазе 99,48%. Оба продукта превращены в соответствующие гидрохлориды обработкой изопропанолом, насыщенным хлористым водородом. Правовращающий энантиомер: PF = 114-117 С; К раствору 2,02 г (0,0063 моль) (+/-)-1,2,3,4-тетрагидроизохинолин-7-сульфонамидо-[2-(1 метилпирролидин-2-ил)этила] и 0,70 г (0,00 63 моль) циклогексанкарбоксальдегида в 100 мл метанола прибавляют 0,32 г (0,0003 моль) палладия на углероде с содержанием 10%. Раствор гидрируют в течение 24 часов в гидрогенизаторе Паара при давлении 45 фунт/кв. дюйм. Катализатор удаляют фильтрованием и отфильтрованный раствор выпаривают досуха. Полученное неочищенное маслоподобное вещество(2,90 г) очищают хроматографией на колонке с силикагелем смесью дихлорметан/метанол (95:5), используемой в качестве элюента. Получают требуемый продукт (1,62 г; 62%) в виде маслоподобного вещества. Полученное маслоподобное вещество растворяют в 20 мл этанола, затем прибавляют 0,77 г (0,0086 моль) щавелевой кислоты, растворенной в 15 мл этанола. Осадок отфильтровывают и промывают холодным этанолом. Получают 2,01 г требуемого продукта в виде белого твердого вещества.PF = 142-147 С. ЯМР 1 Н (ДМСО-d6)(м.д.): 7,5 (2 Н, м), 7,29 (1 Н, м), 3,84 (2 Н, с), 3,35 (2 Н, м), 3,1 (1 Н, м), 2,9 (1 Н,м), 2,8 (2 Н, с), 2,7 (1 Н, м), 2,6 (3H, с), 2,5 (2 Н, м), 2,1-1,4 (13 Н, м), 1,15 (4 Н, м), 0,8 (2 Н, м). Пример 3. Оксалат (1,5:1) (+)-2-(циклогексилметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4 тетрагидроизохинолин-7-сульфонамида. По способу, аналогичному способу примера 2, из 1,00 г (0,0031 моль) (+)-N-[2-(1-метилпирролидин 2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамида и 0,35 г (0,0031 моль) циклогексанкарбоксальдегида в 50 мл метанола в качестве исходных продуктов получают 0,46 г основания, которое затем превращают в соответствующий полуторный гидрооксалат в виде твердого белого вещества.[]20D = +12 (с = 0,5; метанол). Пример 4. Оксалат (2:1) (-)-2-(циклогексилметил)-N- [2-(1-метилпирролидин-2-ил)этил]-1,2,3,4 тетрагидроизохинолин-7-сульфонамида. По способу, аналогичному способу примера 2, из 1,00 г (0,0031 моль) (-)-N-[2-(1-метилпирролидин 2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамида и 0,35 г (0,0031 моль) циклогексанкарбоксальдегида в 50 мл метанола в качестве исходных продуктов получают 0,90 г основания, которое затем превращают в соответствующий дигидрооксалат в виде твердого белого вещества. 5.1. Гидрохлорид N-[2-(3-диэтиламинопропил)-2-(2,2,2-трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-сульфонамида. Раствор 1,00 г (0,0031 моль) 2-(2,2,2-трифторацетил)-1,2,3,4-тетрагидроизохинолин-7-сульфонилхлорида и 0,61 г (0,0047 моль) N,N-диэтил-N-аминопропиламина в 25 мл дихлорметана перемешивают в течение ночи при комнатной температуре. Раствор концентрируют досуха и полученное маслоподобное вещество очищают хроматографией на коленке с силикагелем смесью дихлорметан/метанолPF = маслоподобное вещество. 5.2. Гидрохлорид N-[(3-диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамида. Раствор 5,39 г (0,013 моль) гидрохлорида N-[2-(3-диэтиламинопропил)-2-(2,2,2-трифторацетил)1,2,3,4-тетрагидроизохинолин-7-сульфонамида, растворенного в 60 мл метанола, насыщенного хлористым водородом, нагревают в течение двенадцати часов при 60 С. Смесь охлаждают и образовавшееся твердое вещество отфильтровывают, промывают метанолом и сушат. Остаток растворяют в водном растворе гидроксида натрия. Водную фазу экстрагируют несколько раз диэтиловым эфиром. Органические фракции объединяют и сушат над безводным сульфатом магния. Полученное маслоподобное вещество(2,80 г) используют без дополнительной очистки.PF = маслоподобное вещество. 5.3. Оксалат (2:1) 2-бензил-N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7-сульфона-6 010234 мида. К суспензии 0,45 г (0,0014 моль) N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамида и 0,149 г (0,0014 моль) бензальдегида в 12 мл тетрагидрофурана прибавляют 1,5 мл уксусной кислоты. Суспензию перемешивают в течение 1 ч при комнатной температуре и затем прибавляют 0,14 г (0,0021 моль) цианоборогидрида натрия. Смесь перемешивают в течение ночи. Концентрируют досуха, остаток обрабатывают водой и промывают диэтиловым эфиром. Водную фазу подщелачивают до рН=10 и экстрагируют несколько раз диэтиловым эфиром. Органические фракции объединяют и сушат над безводным сульфатом магния. Полученное маслоподобное вещество очищают хроматографией на колонке с силикагелем смесью дихлорметан/метанол (95:5), используемой в качестве элюента. Получают требуемый продукт (0,13 г; 22%) в виде маслоподобного вещества. Полученное маслоподобное вещество растворяют в 5 мл этанола, затем прибавляют 0,06 г (0,0007 моль) щавелевой кислоты, растворенной в 5 мл этанола. Осадок отфильтровывают и промывают холодным этанолом. Получают 0,12 г требуемого продукта в виде белого твердого вещества. 6.1. N-[2-(3-Диэтиламинопропил)-N-метил-2-(2,2,2-трифторацетил)-1,2,3,4-тетрагидроизохинолин 7-сульфонамид. К раствору 0,91 г (0,0021 моль) N-[2-(3-диэтиламинопропил)-2-(2,2,2-трифторацетил)-1,2,3,4 тетрагидроизохинолин-7-сульфонамида (полученного по способу, описанному на стадии 5.1 примера 5) в 17 мл диметилформамида, охлажденного до 0 С, прибавляют 0,09 г (0,0022 моль) дисперсии гидрида натрия (60%) в минеральном масле. Смесь перемешивают в течение часа и прибавляют 0,060 г (0,0042 моль) метилиодида. Смесь перемешивают в течение ночи при комнатной температуре, затем раствор концентрируют досуха. Остаток обрабатывают водой. Водную фазу экстрагируют несколько раз этилацетатом. Органические фракции объединяют и сушат над безводным сульфатом магния. Полученное маслоподобное вещество после фильтрования и выпаривания растворителя очищают хроматографией на колонке с силикагелем смесью дихлорметан/метанол (95:5), используемой в качестве элюента, с получением 0,31 г требуемого продукта в виде маслоподобного вещества.PF = маслоподобное вещество. 6.2. N-[2-(3-Диэтиламинопропил)-N-метил-1,2,3,4-тетрагидроизохинолин-7-сульфонамид. Раствор 0,20 г (0,0004 6 моль) N-[2-(3-диэтиламинопропил)-N-метил-2-(2,2,2-трифторацетил)1,2,3,4-тетрагидроизохинолин-7-сульфонамида, растворенного в 10 мл метанола, насыщенного хлористым водородом, нагревают в течение двенадцати часов при 60 С. Раствор концентрируют досуха и остаток обрабатывают водой. Водную фазу экстрагируют несколько раз диэтиловым эфиром. Органические фракции объединяют, сушат над безводным сульфатом магния и раствор концентрируют досуха с получением 0,02 г требуемого продукта в виде маслоподобного вещества. К суспензии 1,7 0 г (0,0050 моль) N-[3-(диэтиламино)пропил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамида (полученного по способу, описанному на стадии 3.2 примера 3) и 0,98 г (0,0014 моль) циклогексанона в 50 мл тетрагидрофурана прибавляют 5 мл уксусной кислоты. Смесь перемешивают в течение 3 ч при комнатной температуре и затем прибавляют 0,47 г (0,0075 моль) цианоборогидрида натрия. Смесь перемешивают в течение ночи. Концентрируют досуха. Остаток обрабатывают водой и промывают диэтиловым эфиром. Водную фазу подщелачивают до рН=10 и экстрагируют несколько раз диэтиловым эфиром. Органические фракции объединяют и сушат над безводным сульфатом магния. Полученное маслоподобное вещество очищают хроматографией на колонке с силикагелем смесью дихлорметан/метанол (95:5), используемой в качестве элюента. Получают требуемый продукт (0,22 г; 11%) в виде маслоподобного вещества.-7 010234 Полученное маслоподобное вещество растворяют в 5 мл этанола, затем прибавляют раствор 0,11 г(0,0012 моль) щавелевой кислоты, растворенной в 5 мл этанола. Осадок отфильтровывают и промывают холодным этанолом. Получают 0,32 г требуемого продукта в виде белого твердого вещества. 8.1. 1-(2-цианоэтил)пирролин. К раствору 1,00 г (0,0014 моль) пирролина в метаноле прибавляют при 0 С 0,95 мл (0,0014 моль) акрилонитрила. Смесь перемешивают в течение ночи при комнатной температуре и концентрируют досуха с получением 1,65 г требуемого продукта в виде маслоподобного вещества.PF = маслоподобное вещество. 8.2. 1-(3-аминопропил)пирролин. К раствору 1,00 г (0,0089 моль) 1-(2-цианоэтил)пирролина в 20 мл дихлорметана прибавляют 0,024 г гидрида диизобутилалюминия в виде 1 М раствора в толуоле. Смесь перемешивают в течение ночи при комнатной температуре. Раствор обрабатывают десятиводным сульфатом натрия. Перемешивают в течение получаса. Неорганическую фазу отфильтровывают и фильтрат концентрируют досуха с получением 1,00 г бесцветного маслоподобного вещества.PF = маслоподобное вещество. ЯМР 1 Н (CD3Cl)(м.д.): 5,75 (2 Н, с), 3,47 (4 Н, с), 2,75 (2 Н, т), 2,56 (2 Н, т), 1,69 (2 Н, кв). Таблица, приведенная далее, дана для иллюстрации химической структуры и физических свойств некоторых соединений по настоящему изобретению. Результаты элементного микроанализа и ЯМР, ИК или масс-спектры подтверждают структуру полученных соединений. Аббревиатурой PF в таблице обозначена температура плавления соединений формулы I. Таблица 1 Соединения формулы I по настоящему изобретению были объектом фармакологических испытаний, которые показали их пригодность в качестве терапевтически активных веществ. В частности, соединения по настоящему изобретению являются антагонистами рецептора гистамина типа H3. Рецепторы типа Н 3 известны специалисту в данной области техники и их терапевтическая полезность описана в литературе ("Histamine H3 receptor antagonists" Exp. Opinion Ther. Patents (2000) 10(7): 1045-1055). Так, соединения формулы I по настоящему изобретению были подвергнуты испытаниям на сродство in vitro к нативному рецептору гистамина типа Н 3 в мембранном препарате мозга взрослой крысы по специфическому связыванию [3H]-Nметилгистамина с этим рецептором согласно методикам, описанным Korte А. и др. в публикации Biochem. Biophys. Res. Commun. 168, 979-986 (1990) и West R.E. Jr. и др. в публикации Mol. Pharmacol. 38, 610-613 (1990). Константы Ki для соединений по настоящему изобретению в отношении рецепторов H3 составляют от 0,1 нМ до 5,0 мкМ и, в частности, для (+/-)-2-(циклогексилметил)-N-[2-(1-метилпирролидин-2 ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамида (соединение 15; таблица 1) Ki составляет 0,3 нМ. Соединения формулы I по настоящему изобретению были подвергнуты также испытаниям на образование сАМР на человеческом рецепторе гистамина типа Н 3, трансфицированном в клетки СНО, по ингибированию агонизма, вызываемого специфическим связыванием Rметилгистамина с этим рецептором, по методикам, описанным Lovenberg T.W. и др. в публикации J. Pharmacol. Exp. Ther. 293, 771-778(2000). Концентрации CI50 для соединений по настоящему изобретению в отношении рецепторов гистамина типа Н 3 составляют от 0,1 нМ до 5,0 мкМ. Например, для соединения 15, включенного в таблицу 1, CI50 составляет менее 10 нМ, при использовании набора EIA (Amersham) для определения образования сАМР, на человеческом рецепторе гиста-9 010234 мина типа Н 3, трансфицированном в клетки СНО, по ингибированию агонизма, вызываемого специфическим связыванием Rметилгистамина с этим рецептором. Соединения по настоящему изобретению обладают селективной активностью к рецептору гистамина типа H3. Действительно, Ki для указанных соединений составляет более 7,0 мкМ в тесте на сродство invitro на нативном рецепторе гистамина типа Hi в мембранном препарате мозга взрослой крысы по специфическому связыванию [3 Н]-пириламина с этим рецептором по методикам, описанным Liu Y.Q. и др. в публикации J. Pharmacol. Exp. Ther. 268, 959 (1994). С другой стороны, соединения формулы I по настоящему изобретению были объектом испытанийin vivo, которые показали их способность уменьшать прием пищи крысами, не получавшими пищу в течение 24 ч. Эксперименты были осуществлены на крысах Wistar. Крысы были помещены раздельно в пластмассовые прозрачные клетки с размерами 4826,521,5 см. Клетки были установлены в изолированном от любого шума месте при температуре от 20 до 22 С с периодом освещения с 7 ч утра до 7 ч вечера; крысы имели свободный доступ к воде и пище. Перед проведением эксперимента крысы не получали пищу в течение 24 ч при свободном доступе к воде. В день проведения эксперимента жидкостный наполнитель, содержавший соединение по настоящему изобретению, вводили интраперитонеально (i.p.) или перорально (р.о.) за 15 или 30 мин до дачи известного количества пищи (30 г). Через каждый час в течение 6 ч определяли количество съеденной крысой пищи. Было показано, что активные дозы DA50 (мг/кг i.p. или р.о.) для соединений по настоящему изобретению в отношении приема пищи могут быть менее 10. Например, (+/-)-2-(4-изопропилбензил)-N-[2-(1 метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7-сульфонамид (соединение 24; таблица 1) уменьшает на 54% прием пищи в течение первого часа после введения продукта i.p. с дозой 10 мг/кг. Результаты испытаний показывают, что соединения по настоящему изобретению позволяют уменьшить прием пищи животными. Таким образом, они позволяют контролировать увеличение массы тела,излечивать ожирение или помогать при уменьшении массы тела у животных и равным образом у человека. Таким образом, настоящее изобретение в одном из других его аспектов относится к лекарственным средствам, содержащим соединение формулы I или аддитивную соль этого соединения с фармацевтически приемлемой кислотой или также гидрат или сольват соединения формулы I. Эти лекарственные средства находят применение в терапии, в частности, при лечении патологий,при которых антагонисты рецептора гистамина типа H3 оказывают полезное терапевтическое действие. В частности, такими патологиями являются ожирение и диабет. Равным образом, эти соединения могут быть использованы при лечении заболеваний центральной нервной системы, таких как нарушения сна и бессонница, нарколепсия, болезнь Альцгеймера и другие деменции, болезнь Паркинсона, нарушения внимания у детей с гиперкинезией, нарушения памяти и способности к обучению, эпилепсия, шизофрения, умеренные когнитивные нарушения, депрессия и состояние тревожности. Состояния депрессии и тревожности включают в себя, например, состояние тревожности опережающего типа (перед хирургическим вмешательством, перед лечением зубов и т.д.), состояние тревожности, обусловленное зависимостью или вынужденным воздержанием от алкоголя, наркотиков, мания, сезонные аффективные расстройства, мигрени и тошнота. Они могут быть использованы также при лечении половых дисфункций,головокружения и укачивания. Применение соединений по настоящему изобретению для получения лекарственного средства, предназначенного для лечения ранее упомянутых патологий, является составной частью настоящего изобретения. Настоящее изобретение в одном из других его аспектов относится к фармацевтическим композициям, включающим в себя в качестве действующего вещества по меньшей мере одно соединение по настоящему изобретению. Эти фармацевтические композиции содержат эффективную дозу по меньшей мере одного соединения по настоящему изобретению или фармацевтически приемлемой соли, гидрата или сольвата упомянутого соединения, а также по меньшей мере один или несколько фармацевтически приемлемых эксципиентов. Эти эксципиенты выбирают из традиционных эксципиентов, известных специалисту в данной области техники, в соответствии с требуемыми фармацевтической формой и способом введения. В фармацевтических композициях по настоящему изобретению, предназначенных для введения перорально, сублингвально, подкожно, внутримышечно, внутривенно, наружно, местно, интратрахеально,интраназально, чрескожно или ректально, ранее упомянутое действующее вещество формулы I или его возможных соли, сольвата или гидрата может вводиться в лекарственной форме стандартной дозы в смеси с традиционными фармацевтическими эксципиентами животным и людям для профилактики или лечения ранее упомянутых нарушений или заболеваний. Соответствующие лекарственные формы стандартной дозы для введения включают в себя формы для перорального приема, такие как таблетки, капсулы с мягкой или твердой желатиновой оболочкой,порошки, гранулы и растворы или суспензии для приема внутрь, формы для приема сублингвально,- 10010234 трансбуккально, интратрахеально, интраназально, путем ингаляции, формы для введения наружно, чрескожно, подкожно, внутримышечно или внутривенно, формы для введения ректально и имплантаты. Для наружного применения соединения по настоящему изобретению можно использовать в виде кремов, гелей, помад или лосьонов. Для получения требуемого профилактического или терапевтического эффекта доза действующего вещества может варьировать в интервале от 0,1 мкг до 50 мг на кг массы тела в день. Каждая разовая доза может содержать от 0,1 до 1000 мг, предпочтительно от 1 до 500 мг действующего вещества в комбинации с фармацевтическим эксципиентом. Такая разовая доза может быть назначена для приема от 1 до 5 раз в день в зависимости от назначения суточной дозы в интервале от 0,5 до 5000 мг, предпочтительно в интервале от 1 до 2500 мг. Могут иметь место особые случаи, в которых дозы устанавливают увеличенными или уменьшенными. Такие дозы в равной мере составляют часть настоящего изобретения. По принятой практике соответствующие дозы для каждого больного определяются врачом в соответствии со способом введения,массой тела и реакцией больного. Пример лекарственной формы разовой дозы соединения по настоящему изобретению: Соединение по настоящему изобретению 50,0 мг Маннит 223,75 мг Натрия кроскарамеллоза 6,0 мг Крахмал кукурузный 15,0 мг Гидроксипропилметилцеллюлоза 2,25 мг Магния стеарат 3,0 мг Настоящее изобретение в одном из других его аспектов в равной мере относится к способу лечения ранее упомянутых патологий, который включает в себя введение пациенту эффективной дозы соединения по настоящему изобретению, или одной из его фармацевтически приемлемых солей, или гидратов,или сольватов. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы I где n может принимать значения от 1 до 6;-(С)n- представляет собой C1-6-алкилиден, при необходимости замещенный заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6 диалкиламино или C1-3-алкокси;R1 представляет собой атом водорода; C1-6-алкил;R2 представляет собой атом водорода;C1-6-алкил или C3-6-циклоалкил, при необходимости замещенные заместителями в числе от 1 до 4,выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6 диалкиламино, C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси, C3-6-циклоалкила, моноциклического гетероарила, такого как тиенил, фурил или пирролил, или арила, такого как фенил или нафтил; причем арил при необходимости может быть замещен заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила,C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси или C1-3-алкилидендиоксигруппы; В представляет собой группу NR3R4, гдеR3 и R4 представляют собой независимо друг от друга С 1-6-алкил, атом водорода илиR3 и R4 представляют собой совместно C1-6-алкилиден, C2-8-алкенилиден, C1-3-алкилиден-О-C1-3 алкилиден или C1-3-алкилиден-N(R5)-C1-3-алкилиден, где R5 представляет собой атом водорода, C1-3 алкил или C1-6-алкилкарбонил, причем эти C1-3-алкил и С 1-6-алкилкарбонил могут быть замещены атомом галогена, гидрокси, C1-3-алкокси, нитро, циано или амино; или циклический амин, связанный по углероду с группой -NR1-(C)n-, выбранный из азиридина, азетидина, пирролидина, пиперидина и морфолина; причем группы R3, R4, а также циклический амин при необходимости могут быть замещены заместителями в числе от 1 до 4, выбранными из фенила, бензила, атома галогена, гидрокси, нитро, циано,амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила или C1-3-алкокси; атом азота также при необходимости может быть замещен C1-3-алкилом, в виде основания или кислотно-аддитивной соли, также как и в виде гидрата или сольвата,за исключением соединения, в котором R1 и R2 представляют собой атомы водорода, B представляет собой диметиламиногруппу и -(С)n- представляет собой этилиденовую группу.R1 представляет собой атом водорода или C1-2-алкил; иR2 представляет собой атом водорода, C1-4-алкил или С 5-6 циклоалкил, при необходимости замещенные заместителями в числе от 1 до 4, выбранными из фенила, С 3-6-циклоалкила, C1-2-пергалогеналкила,C1-3-галогеналкила или C1-3-алкокси; причем фенил при необходимости может быть замещен заместителями в числе от 1 до 4, выбранными из атома галогена, гидрокси, нитро, циано, амино, C1-3-моноалкиламино, C2-6-диалкиламино, C1-3-алкила, C1-2-пергалогеналкила, C1-3-галогеналкила, C1-3-алкокси или C1-3 алкилидендиоксигруппы; иR3 и R4 представляют собой независимо друг от друга C1-4-алкил; или в случае, когда R3 и R4 представляют собой совместно C1-6-алкилиден, C2-8-алкенилиден, C1-3 алкилиден-О-C1-3-алкилиден или C1-3-алкилиден-N(R5)-C1-3-алкилиден, В представляет собой группу или циклический амин, связанный по углероду с группой -NR1-(C)n-, выбранный из азиридина, азетидина, пирролидина, пиперидина и морфолина; причем группы R3, R4 и R5, а также циклический амин при необходимости могут быть замещены; в виде основания или кислотно-аддитивной соли, а также в виде гидрата или сольвата. 3. Соединение по п.2, отличающееся тем, что, когда B представляет собой группу NR3R4 и R3 и R4 образуют совместно C1-6-алкилиден, C2-8-алкенилиден, C1-3-алкилиден-О-C1-3-алкилиден или C1-3 алкилиден-N(R5)-C1-3-алкилиден или когда В представляет собой циклический амин, В выбран из следующих групп: 4. Соединение по пп.1, 2 или 3, отличающееся тем, что оно представляет собой(-)-2-(циклогексилметил)-N-[2-(1-метилпирролидин-2-ил)этил]-1,2,3,4-тетрагидроизохинолин-7 сульфонамид в виде основания или кислотно-аддитивной соли, также как и в виде гидрата или сольвата; где Pg представляет собой атом водорода или защитную группу и -(С)n- и R1 имеет такие же значения,как и определенные в п.1, а В представляет собой группу NR3R4, где R3 и R4 имеют такие же значения,как и определенные в п.1; или циклический амин, связанный по углероду с группой -NR1-(C)n-, выбранный из азиридина, азетидина, пирролидина, пиперидина или морфолина; причем группы R3, R4, а также циклический амин, при необходимости могут быть замещены так же, как определено в п.1. 6. Фармацевтическая композиция, содержащая соединение формулы I по любому из пп.1-4 или его соль, сольват или гидрат и по меньшей мере один фармацевтически приемлемый эксципиент. 7. Применение соединения формулы I по любому из пп.1-4 или его соли, сольвата или гидрата для получения лекарственного средства, предназначенного для лечения ожирения и диабета. 8. Применение соединения формулы I по любому из пп.1-4 или его соли, сольвата или гидрата для получения лекарственного средства, предназначенного для лечения заболеваний центральной нервной системы, таких как нарушения сна и бессонница, нарколепсия, болезнь Альцгеймера и другие деменции,болезнь Паркинсона, нарушения внимания у детей с гиперкинетическим синдромом, нарушения памяти и способности к обучению, эпилепсия, шизофрения, умеренные когнитивные нарушения, депрессия, тревожные состояния, половые дисфункции, головокружение и транспортная болезнь.
МПК / Метки
МПК: C07D 217/04, A61K 31/496, C07D 405/06, C07D 401/12, C07D 409/06, A61K 31/472, C07D 217/06, A61P 3/04, A61K 31/5377, C07D 217/02, A61K 31/4725
Метки: тетрагидроизохинолилсульфонамидов, терапии, получение, производные, применение
Код ссылки
<a href="https://eas.patents.su/14-10234-proizvodnye-tetragidroizohinolilsulfonamidov-ih-poluchenie-i-primenenie-v-terapii.html" rel="bookmark" title="База патентов Евразийского Союза">Производные тетрагидроизохинолилсульфонамидов, их получение и применение в терапии</a>
Предыдущий патент: Противопаразитарные терпеновые алкалоиды
Следующий патент: Способ корректировки погрешностей уровня пути
Случайный патент: Способ литья объектов со стояком усовершенствованной конструкции












