Дейтерированные производные катехоламина и лекарственные средства, содержащие указанные соединения
Формула / Реферат
1. Дейтерированные производные катехоламина общей формулы I
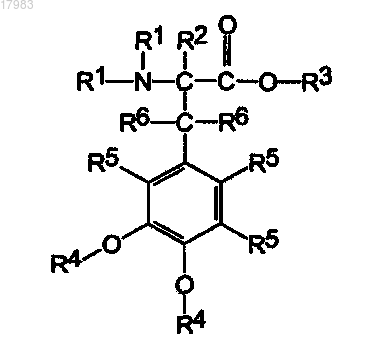
где R1 представляет собой H;
R2 представляет собой D;
R3 представляет собой H, метил или этил;
R4 представляет собой H;
R5 представляет собой Н или D;
R6 представляет собой Н или D, где оба остатка R6 не являются одновременно D и где оба остатка R6 не являются одновременно H,
их стереоизомеры, энантиомеры или диастереомеры в оптически чистой форме, а также их физиологически приемлемые соли.
2. Дейтерированное производное катехоламина по п.1, где
R1 представляет собой H;
R2 представляет собой D;
R3 представляет собой метил;
R4 представляет собой H;
R5 представляет собой D;
R6 представляет собой Н или D, при условии, что оба остатка R6 не являются одновременно D, и при условии, что оба остатка R6 не являются одновременно H.
3. Дейтерированное производное катехоламина по п.1, где
R1 представляет собой H;
R2 представляет собой D;
R3 представляет собой этил;
R4 представляет собой H;
R5 представляет собой D;
R6 представляет собой Н или D, при условии, что оба остатка R6 не являются одновременно D, и при условии, что оба остатка R6 не являются одновременно H.
4. Дейтерированное производное катехоламина по п.1, выбранное из
S/R-2-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты,
метилового эфира S/R-2-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты,
этилового эфира S/R-2-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты,
S/S-2-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты,
метилового эфира S/S-2-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты,
этилового эфира S/S-2-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты,
S/R-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты,
метилового эфира S/R-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты,
этилового эфира S/R-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты,
S/S-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты,
метилового эфира S/S-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты,
этилового эфира S/S-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты.
5. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для лечения болезней, вызываемых недостатком допамина, которые основываются на нарушении передачи тирозина или на нарушении активности тирозиндекарбоксилазы, выбранных из болезни Паркинсона, синдрома беспокойных ног и дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии.
6. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 в комбинации с одним или с несколькими ингибиторами ферментов, выбранных из ингибитора декарбоксилазы, ингибитора катехол-O-метилтрансферазы, ингибитора моноаминоксидазы и ингибитора β-гидроксилазы, для лечения болезней, вызываемых недостатком допамина, которые основываются на нарушении передачи тирозина или на нарушении активности тирозиндекарбоксилазы, выбранных из болезни Паркинсона, синдрома беспокойных ног и дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии.
7. Применение по п.6, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-α-гидразино-3,4-дигидрокси-α-метилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4-тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемых солей.
8. Применение по п.6, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей.
9. Применение по п.6, где ингибитор моноаминоксидазы выбран из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли.
10. Применение по п.6, где ингибитор β-гидроксилазы выбран из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей.
11. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для производства фармацевтического препарата для лечения болезни Паркинсона, синдрома беспокойных ног, бокового амиотрофического склероза и множественной системной атрофии.
12. Фармацевтическая композиция для лечения болезни Паркинсона, синдрома беспокойных ног, дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4 в комбинации с фармацевтически приемлемыми обычными твердыми или жидкими связующими веществами или разбавителями.
13. Фармацевтическая композиция для лечения болезни Паркинсона, синдрома беспокойных ног, дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4, а также один или более ингибиторов ферментов, включающих ингибиторы декарбоксилазы и/или ингибиторы катехол-O-метилтрансферазы, и/или ингибиторы моноаминоксидазы, и/или ингибиторы β-гидроксилазы, в комбинации с фармацевтически приемлемыми обычными твердыми или жидкими связующими веществами или разбавителями.
14. Фармацевтическая композиция по п.13, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-α-гидразино-3,4-дигидрокси-α-метилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4-тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемых солей.
15. Фармацевтическая композиция по п.13, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей.
16. Фармацевтическая композиция по п.13, где ингибитор моноаминоксидазы выбран из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли.
17. Фармацевтическая композиция по п.13, где ингибитор β-гидроксилазы выбран из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей.
18. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для получения фармацевтической композиции для профилактики психозов.
19. Применение по п.18, при котором психозом является шизофрения.
20. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для лечения острых психозов.
21. Применение по п.20, при котором острым психозом является шизофрения.
22. Применение по п.21, при котором шизофрения характеризуется негативной симптоматикой.
23. Применение дейтерированных производных катехоламина по любому из пп.1-4, а также их физиологически приемлемых солей в комбинации с одним или несколькими ингибиторами ферментов, выбранных из ингибитора декарбоксилазы, ингибитора катехол-O-метилтрансферазы, ингибитора моноаминоксидазы и ингибитора β-гидроксилазы, для профилактики психозов, а также для лечения острых психозов при негативной симптоматике.
24. Применение по п.23, при котором острым психозом является шизофрения.
25. Применение по п.23, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-α-гидразино-3,4-дигидрокси-α-метилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4-тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемых солей.
26. Применение по п.23, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей.
27. Применение по п.23, где ингибитор моноаминоксидазы выбран из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли.
28. Применение по п.23, где ингибитор β-гидроксилазы выбран из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей.
29. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для производства фармацевтического препарата для профилактики психозов, а также для лечения острых психозов при негативной симптоматике.
30. Фармацевтическая композиция для профилактики психозов, а также для лечения острых психозов при негативной симптоматике, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4 в комбинации с фармацевтически приемлемыми обычными твердыми или жидкими связующими веществами или разбавителями.
31. Фармацевтическая композиция для профилактики психозов и для лечения острых психозов при негативной симптоматике, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4, а также один или несколько ингибиторов ферментов, выбранных из ингибитора декарбоксилазы, ингибитора катехол-O-метилтрансферазы, ингибитора моноаминоксидазы и ингибитора β-гидроксилазы в комбинации с фармацевтически приемлемыми обычными твердыми или жидкими связующими веществами или разбавителями.
32. Фармацевтическая композиция по п.31, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-α-гидразино-3,4-дигидрокси-α-метилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4-тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемых солей.
33. Фармацевтическая композиция по п.31, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей.
34. Фармацевтическая композиция по п.31, где ингибитор моноаминоксидазы выбран из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли.
35. Фармацевтическая композиция по п.31, где ингибитор β-гидроксилазы выбран из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей.
Текст
ДЕЙТЕРИРОВАННЫЕ ПРОИЗВОДНЫЕ КАТЕХОЛАМИНА И ЛЕКАРСТВЕННЫЕ СРЕДСТВА, СОДЕРЖАЩИЕ УКАЗАННЫЕ СОЕДИНЕНИЯ Настоящее изобретение относится к дейтерированным производным катехоламина общей формулы I а также к фармацевтическим средствам, содержащим эти соединения. В дополнение к этому изобретение относится к использованию дейтерированных производных катехоламина, а также их фармацевтически приемлемых солей и фармацевтических композиций, которые содержат эти соединения, также в комбинации с ингибиторами ферментов, для лечения болезней, вызываемых недостатком допамина, или болезней, которые основываются на нарушении передачи тирозина или нарушении тирозиндекарбоксилазы, а также других расстройств.(71)(73) Заявитель и патентовладелец: БЕДС ФАРМА ГМБХ БЕРОЛИНА ИННОВЕЙТИВ РЕСЧ ЭНД ДЕВЕЛОПМЕНТ СВИСИЗ (DE) Настоящее изобретение относится к дейтерированным производным катехоламина, а также к фармацевтическим препаратам, содержащим эти соединения. Известные представители катехоламинов, такие как L-допа (леводопа), а также их эфиры карбоновой кислоты используются, в том числе, для лечения болезни Паркинсона и синдрома беспокойных ног. Таким фармацевтическим препаратом, который содержит леводопу, является, например, Dopaflex.L-допа воздействует на концентрацию допамина в нейронах мозга. В отличие от самого допамина она может проходить через гематоэнцефалический барьер и превращаться в мозгу в допамин. Кроме того, леводопа вводится в комбинации с активными добавками, являющимися фармацевтическими средствами. Леводопа используется в комбинации с ингибиторами периферической декарбоксилазы, с ингибиторами фермента катехол-O-метилтрансферазы (СОМТ), с ингибиторами фермента моноаминоксидазы (МАО) и с ингибиторами допамин -гидроксилазы. В этой связи использующимися ингибиторами декарбоксилазы являются, например, D,L-серин-2(2,3,4-гидроксибензил)гидразид (бенсеразид), (-)-Lгидразино-3,4-дигидроксиметилгидрокоричная кислота (карбидопа), L-серин-2-(2,3,4-гидроксибензил)гидразид, глицин-2-(2,3,4-гидроксибензил)гидразид и L-тирозин-2-(2,3,4-гидроксибензил)гидразид. Примеры комбинаций препаратов леводопы и ингибиторов декарбоксилазы включают, в том числе, Madopar (леводопа и бенсеразида гидрохлорид), а также Nacom (леводопа и карбидопа). Примерами ингибиторов СОМТ являются энтакапон (Comtan) и каберголин, а часто применяющимися ингибиторами МАО являются гидрохлорид селегилина, моклобемид и транилципромин. 5-Бутилпиколинат кальция и 5-пентилпиколинат кальция описываются в качестве ингибиторов для допамингидроксилазы (DE 2049115). В WO-A 20004/056724 описывается дейтерированный катехоламин, включающий два атома дейтерия в -позиции. Эти соединения показывают улучшенные фармакокинетические и/или фармакодинамические свойства по сравнению с недейтерированными соединениями и по сравнению с соединением LДОПА. Целью данного изобретения является получение дейтерированных производных катехоламина, которые обладают улучшенными фармакокинетическими и/или фармакодинамическими свойствами по сравнению с известными соединениями, а также получение производных катехоламина, которые могут применяться для профилактики психозов, включая шизофрению, и которые могут использоваться для получения фармацевтических препаратов для профилактики психозов. Неожиданно было установлено, что дейтерированные производные катехоламина в соответствии с изобретением обладают существенно улучшенными фармакокинетическими и/или фармакодинамическими свойствами по сравнению с недейтерированными соединениями и ,-дидейтерированными соединениями, известными в уровне техники, и они также могут использоваться для профилактики психозов и для производства лекарственных средств для профилактики психозов. В соответствии с изобретением эта цель достигается получением соединений общей формулы IR6=Н или D, где оба остатка R5 не являются одновременно D и где оба остатка R6 не являются одновременно H,их стереоизомеров, энантиомеров или диастереомеров в оптически чистой форме, а также их физиологически приемлемых солей. Преимущественными являются соединения в соответствии с общей формулой I, в которых оба остатка R6 не являются дейтерием (D). Группы, которые легко гидролитически или ферментативно расщепляются в физиологических условиях, известны специалистам в данной области. Эти группы являются обычными защитными группами, которые применяются при синтезе, или такими группами, которые приводят к так называемым пролекарствам. Эти соединения могут выбираться из группы, включающей метил, предейтерометил, этил, предейтероэтил, пропил, предейтеропропил, бутил, предейтеробутил, C1-C6-алкил, который может быть разветвленным или неразветвленным, или C5-C6-циклоалкил, дейтерированный или частично дейтерированный C1-C6-алкил, который может быть разветвленным или неразветвленным, или дейтерированный или частично дейтерированный C5-C6-циклоалкил. В соответствии с изобретением преимущественными являются дейтерированные производные катехоламина формулы I, у которыхR6=Н или D, при условии, что оба остатка R6 не являются одновременно D и при условии, что оба остатка R5 не являются одновременно H. Преимущественными являются дейтерированные производные катехоламина формулы I, у которыхR6=H или D, при условии, что оба остатка R6 не являются одновременно D и при условии, что оба остатка R5 не являются одновременно H. Преимущественными являются дейтерированные производные катехоламина формулы I, а именноS/R-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты,этиловый эфир S/R2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты. Другим воплощений изобретения является применение дейтерированных производных катехоламина в соответствии с изобретением, а также их физиологически приемлемых солей, для лечения болезней, вызываемых недостатком допамина, которые основываются на нарушении передачи тирозина или нарушении тирозиндекарбоксилазы, таких как болезнь Паркинсона, синдром беспокойных ног, дистония, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии. Преимущественно использовать дейтерированные производные катехоламина, а также их физиологически приемлемые соли в комбинации с ингибитором фермента или с несколькими ингибиторами ферментов для лечения болезней, вызываемых недостатком допамина, которые основываются на нарушении передачи тирозина или нарушении тирозиндекарбоксилазы, таких как болезнь Паркинсона, синдром беспокойных ног, дистония, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем,бокового амиотрофического склероза и множественной системной атрофии. Преимущественным является случай, когда ингибитор фермента или ингибиторы фермента включают ингибиторы декарбоксилазы, и/или ингибиторы катехол-О-метилтрансферазы, и/или ингибиторы моноаминоксидазы, и/или ингибиторы -гидроксилазы. Особо преимущественным является случай, когда ингибитор декарбоксилазы выбирается из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид),(-)-Lгидразино-3,4-дигидроксиметилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4 тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4 тригидроксибензил)гидразид, а также их физиологически приемлемые соли. В частности, преимущественно также, если ингибитор катехол-O-метилтрансферазы выбирается из энтакапона и каберголина, а также их физиологически приемлемых солей. Преимущественно также, если ингибитор моноаминоксидазы выбирается из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. Кроме того, особо преимущественно, если ингибитор -гидроксилазы выбирается из 5 бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей. Другим объектом изобретения является применение дейтерированных производных катехоламина в соответствии с изобретением, а также их физиологически приемлемых солей для производства фармацевтических препаратов для лечения болезней, вызываемых недостатком допамина, или болезней, которые основываются на нарушении передачи тирозина или нарушении тирозиндекарбоксилазы, таких как болезнь Паркинсона, синдром беспокойных ног, дистония, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии. Другим объектом настоящего изобретения является фармацевтическая композиция, которая содержит дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли для лечения болезней, вызываемых недостатком допамина, или болезней, которые основываются на нарушении передачи тирозина или нарушении тирозиндекарбоксилазы, таких как болезнь Паркинсона, синдром беспокойных ног, дистония, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии в дополнение к фармацевтически приемлемым вспомогательным лекарственным веществам и добавкам. Особо преимущественной является фармацевтическая композиция, которая содержит дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, для лечения болезни Паркинсона, синдрома беспокойных ног, дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии, а также содержит один или более ингибиторов ферментов, в дополнение к приемлемым вспомогательным лекарственным веществам и добавкам. Особо преимущественной является фармацевтическая композиция, в которой ингибитор или ингибиторы ферментов включают ингибиторы декарбоксилазы, и/или ингибиторы катехол-Oметилтрансферазы, и/или ингибиторы моноаминоксидазы, и/или ингибиторы -гидроксилазы. Дополнительным преимуществом обладает фармацевтическая композиция, у которой ингибитор декарбоксилазы выбирается из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4 тригидроксибензил)гидразид (бенсеразид), (-)-Lгидразино-3,4-дигидроксиметилгидрокоричная кислота(карбидопа),L-серин 2-(2,3,4-тригидроксибензил)гидразид,глицин 2-(2,3,4 тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемые соли. Особо преимущественной является фармацевтическая композиция, в которой ингибитор катехол-Oметилтрансферазы выбирается из энтакапона и каберголина, а также их физиологически приемлемых солей. Дополнительным преимуществом обладает фармацевтическая композиция, в которой ингибитор моноаминоксидазы выбирается из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. Кроме того, преимущественной является фармацевтическая композиция, в которой ингибитор гидроксилазы выбирается из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей. Другим объектом изобретения является применение дейтерированных производных катехоламина в соответствии с изобретением, а также их физиологически приемлемых солей, для профилактики психозов, в особенности у предрасположенных пациентов, для профилактики рецидивов и также, в частности,для лечения острых психозов, например, при негативной симптоматике. Особенно преимущественно применять дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, в комбинации с одним или более ингибиторами ферментов для профилактики психозов и при острых психозах, преимущественно психозов с негативной симптоматикой. Особенно преимущественно использовать дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, если ингибитор или ингибиторы ферментов включают ингибиторы декарбоксилазы, и/или ингибиторы катехол-Oметилтрансферазы, и/или ингибиторы моноаминоксидазы, и/или ингибиторы -гидроксилазы. Особенно преимущественно применять дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, если ингибитор декарбоксилазы выбирается из группы, включающей D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-гидразино-3,4-дигидроксиметилгидрокоричная кислота тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4 тригидроксибензил)гидразид, а также их физиологически приемлемые соли. Преимущественно применять дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, если ингибитор катехол-O-метилтрансферазы выбирается из энтакапона и каберголина, а также их физиологически приемлемых солей. Кроме того, преимущественно использовать дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, если ингибитор моноаминоксидазы выбирается из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. Применение дейтерированных производных катехоламина в соответствии с изобретением, а также их физиологически приемлемых солей, обладает особым преимуществом, если ингибитор гидроксилазы выбирается из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей. Другим объектом изобретения является применение дейтерированных производных катехоламина в соответствии с изобретением, а также их физиологически приемлемых солей, при производстве фармацевтических препаратов для использования в профилактике психозов. Еще одним объектом изобретения является фармацевтическая композиция, которая содержит дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, для использования в профилактике психозов и лечении острых психозов, в дополнение к фармацевтически приемлемым вспомогательным лекарственным веществам и добавкам. Особенно преимущественной является фармацевтическая композиция, которая содержит дейтерированные производные катехоламина в соответствии с изобретением, а также их физиологически приемлемые соли, для профилактики психозов и для лечения острых психозов, а также один или более ингибиторов ферментов, в дополнение к фармацевтически приемлемым вспомогательным лекарственным веществам и добавкам. Особенно преимущественной является фармацевтическая композиция, в которой ингибиторы фермента включают ингибитор или ингибиторы декарбоксилазы, и/или ингибиторы катехол-Oметилтрансферазы, и/или ингибиторы моноаминоксидазы, и/или ингибиторы -гидроксилазы. Дополнительным преимуществом обладает фармацевтическая композиция, в которой ингибитор декарбоксилазы выбирается из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4 тригидроксибензил)гидразид (бенсеразид), (-)-Lгидразино-3,4-дигидроксиметилгидрокоричная кислота(карбидопа),L-серин 2-(2,3,4-тригидроксибензил)гидразид,глицин 2-(2,3,4 тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемые соли. Особенно преимущественной является фармацевтическая композиция, в которой ингибитор катехол-O-метилтрансферазы выбирается из энтакапона и каберголина, а также их физиологически приемлемых солей. Особенно преимущественной является также фармацевтическая композиция, в которой ингибитор моноаминоксидазы выбирается из группы, включающей селегелин, моклобемид и транилципромин, а также их физиологически приемлемые соли. Особенно преимущественной является фармацевтическая композиция, в которой ингибитор гидроксилазы выбирается из 5-бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей. Способы получения соединений в соответствии с изобретением известны специалистам в данной области техники. Могут использоваться аналогичные способы производства, которые описываются, например, в документе DE-A 10262807. Для получения физиологически приемлемых солей дейтерированных производных катехоламина в соответствии с изобретением могут использоваться обычные физиологически приемлемые неорганические и органические кислоты, такие как соляная кислота, бромисто-водородная кислота, ортофосфорная кислота, серная кислота, щавелевая кислота, малеиновая кислота, фумаровая кислота, молочная кислота,винная кислота, яблочная кислота, лимонная кислота, салициловая кислота, адипиновая кислота и бензойная кислота. Дополнительные кислоты, которые могут использоваться, описываются, например, в Fortschritte derPharmaceutical Sciences, том 66, с. 1-5 (1977). Дополнительные соли кислот обычно получают известным путем, смешивая свободные основания или их растворы с соответствующими кислотами или их растворами в органическом растворителе, например, в низшем спирте, таком как метанол, этанол, н-пропанол или изопропанол, или в низшем кетоне,таком как ацетон, метилэтилкетон или метилизобутилкетон, или в простом эфире, таком как диэтиловый эфир, тетрагидрофуран или диоксан. Для лучшего осаждения кристаллов могут использоваться смеси указанных растворителей. Кроме того, физиологически приемлемые водные растворы дополнительных солей кислот соединений, использующихся в соответствии с изобретением, могут получаться из водных растворов кислот. Дополнительные соли кислот соединений в соответствии с изобретением могут обращаться в свободные основания известным путем, например, с использованием щелочей или ионообменных смол. Дополнительные соли могут получаться из свободных оснований реакцией с неорганическими или органическими кислотами, в особенности с теми, которые пригодны для формирования солей, которые могут применяться терапевтически. Эти, а также другие соли новых соединений, такие как, например, пикраты,могут также использоваться для очистки свободной базы, обращая свободное основание в соль, отделяя эту соль и снова высвобождая основание из соли. Объектом настоящего изобретения являются также фармацевтические препараты для орального,буккального, подъязычного, назального, ректального, подкожного, внутривенного или внутримышечного введения, а также для ингаляции, которые, в дополнение к обычным связующим веществам и разбавителям, содержат также соединение формулы I или его дополнительную соль кислоты в качестве активного ингредиента. Фармацевтические препараты в соответствии с изобретением производятся обычным путем и в требующейся дозе с обычными твердыми или жидкими связующими веществами или разбавителями, а обычные вспомогательные фармацевтические или технические вещества добавляются в зависимости от типа введения. Преимущественно препараты состоят из компонентов, при которых они соответствуют оральной форме введения. Такие формы введения включают, например, таблетки, таблетки для сосания,пленочные таблетки, драже, капсулы, пилюли, порошки, растворы, аэрозоли, суспензии или медленно высвобождающиеся формы. Конечно, могут также применяться парентеральные препараты, такие как растворы для инъекций. Кроме того, предлагались также в качестве препаратов, например, и суппозитории. Соответствующие таблетки могут получаться, например, смешиванием активного вещества с известными вспомогательными веществами, например с инертными разбавителями, такими как декстроза, сахар, сорбит, маннитол,поливинилпирролидон, с разрушающими агентами, такими как кукурузный крахмал или альгиновая кислота, со связующими веществами, такими как крахмалы или желатины, со скользящими веществами,такими как стеарат магния или тальк, и/или с веществами, обеспечивающими медленное высвобождение,такими как карбоксиполиметилен, карбоксиполиметилцеллюлоза, ацетатфталат или поливинилацетат целлюлозы. Таблетки могут также состоять из нескольких слоев. Могут также производиться драже соответственно для регулируемого или задерживаемого высвобождения форм препарата путем покрытия ядра, которое получают аналогично таблеткам, веществами,использующимися обычно в покрытиях для драже, например поливинилпирролидоном или шеллаком,аравийской камедью, тальком, диоксидом титана или сахаром. Оболочка драже может также состоять из нескольких слоев, в которых могут использоваться вспомогательные вещества, указанные выше для таблеток. Растворы или суспензии, содержащие активное вещество, использующееся в соответствии с изобретением, могут дополнительно включать вещества для улучшения вкуса, такие как сахарин, цикламат или сахар, а также, например, усилители вкуса, такие как ваниль или апельсиновый экстракт. Они могут также содержать вспомогательные вещества для формирования суспензии, такие как карбоксиметилцеллюлоза натрия, или консерванты, такие как p-гидроксибензоат. Капсулы, содержащие активные вещества, могут производиться, например, смешиванием активных веществ с инертными связующими веществами, такими как лактоза или сорбит, и помещение этой смеси в желатиновую капсулу. Соответствующие суппозитории могут производиться, например, смешиванием связующего вещества,применяющегося в препарате, с нейтральными жирами, полиэтиленгликолем или его производными. Производство фармацевтических препаратов в соответствии с изобретением известно в уровне техники и описывается в справочниках, известных специалистам в данной области, например, в Hager'sHandbuch [Справочник] (5-е издание) 2, 622-1045; List и др., Arzneiformenlehre [Инструкции по производству лекарственных форм], Штутгарт, Wiss. Verlagsges, 1985; Sucker и др., Pharmazeutische Technologie[Фармацевтические технологии], Штутгарт, Thieme, 1991; Ullmann's Enzyklopadie [Энциклопедия] (5-е издание) А 19, 241-271; Voigt, Pharmazeutische Technologie [Фармацевтические технологии], Берлин, Ullstein Mosby, 1995. Как известно из WO-A 2004/056724, L-2-амино-2,3,3-тридейтеро-3-(3,4-дигидроксифенил)пропионовая кислота является селективно дейтерированным производным L-DOPA с улучшенными фармакокинетическими и фармакодинамическими свойствами по сравнению с L-DOPA. Введение L-2-амино-2,3,3-тридейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты самцам крыс Уистара увеличивало содержание допамина в стриатуме значительно больше по сравнению с недейтерированной L-DOPA. Неожиданно было установлено,чтоL-2-амино-2,3-дидейтеро-3-(3,4 дигидрооксифенил)пропионовая кислота увеличивала допамин в стриатуме в значительно большей степени, чем L-2-амино-2,3,3-тридейтеро-3-(3,4-дигидрооксифенил)пропионовая кислота, хотя соединение имеет меньше дейтерия в бета-положении боковой цепи ее молекулы (пример 15 и таблица). Кроме того, в то время как L-2-амино-2,3,3-тридейтеро-3-(3,4-дигидрооксифенил)пропионовая кислота снижает стриарный выход артеренола по сравнению с L-DOPA, L-2-амино-2,3-дидейтеро-3-(3,4 дигидрооксифенил)пропионовая кислота не блокирует формирование артеренола. В связи с этим L-2-амино-2,3-дидейтеро-3-(3,4-дигидрооксифенил)пропионовая кислота имеет два преимущества - она обеспечивает больше допамина и достаточное количество артеренола, который, как было доказано, играет важную роль в компенсации потерь допаминергической функции (Archer иFredriksson, 2006, Нейронная передача, 113(9): 1119-29; Cathala и др., 2002, Нейробиология, 115(4): 105965; Tong и др., 2006, Arch Neurol, 63(12): 1724-8). Было показано, что хорошо растворимый метиловый эфир L-DOPA действует как пролекарство LDOPA. В экспериментах на животных метиловый эфир L-DOPA, вводившийся орально или интраперитонеально, был эквивалентен на молярной основе L-DOPA. Однако терапевтическая эквивалентность не сохранялась при непрерывном внутривенном вливании пациентам с болезнью Паркинсона с четко выраженными возвратами. Оптимальный уровень вливания метилового эфира L-DOPA был в 2,7 раз выше уровня, требовавшегося для L-DOPA (Stocchi и др., 1992, Расстройства движения, 7: 249-256). Неожиданно было установлено,что метиловый эфирL-2-амино-2,3-дидейтеро-3-(3,4 дигидрооксифенил)пропионовой кислоты терапевтически эквивалентен L-2-амино-2,3-дидейтеро-3-3,4 дигидрооксифенил)пропионовой кислоте при непрерывном внутривенном вливании. Следующие далее примеры приводятся для того, чтобы пояснить настоящее изобретение более детально, но они не должны интерпретироваться как ограничения объема изобретения. Пример 1.D,L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)пропионовая кислота. 2,5 г леводопы растворяются в 60 мл CH3CO2D в атмосфере аргона и затем вступают в реакцию с 0,25 мл бензальдегида при орошении. После удаления уксусной кислоты и бензальдегида дистилляцией в вакууме, добавляется 2 мл этанола. Полученный продукт медленно осаждается с помощью этилацетата/толуола (1:1). После сушки в вакууме изолируется 2,2 г D,L-2-амино-2-дейтеро-3-(3,4 дигидрооксифенил)пропионовой кислоты. Выход: 87,6%. Пример 2.D,L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)метилпропионат. 2,0 г D,L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)пропионовой кислоты растворяются в 30 мл метанола и охлаждаются до -10C и взаимодействуют по каплям с 1 мл тионолхлорида. Затем реакционная смесь нагревается до 40C в течение 15 ч. Летучие вещества реакционной смеси удаляются в вакууме, добавляется 10 мл воды, 15 мл раствора 0,8 г гидрокарбоната натрия, 1 г сульфата натрия и 1 мг аскорбиновой кислоты. pH раствора доводится до 7 добавлением разбавленного раствора гидроксида натрия Полученный продукт переводится в органическую фазу с помощью этилацетата, не содержащего кислорода, который включает 0,01% 2,6-ди-трет-бутил-4-метоксифенола. Органическая фаза сушится, а затем растворитель удаляется отгонкой. К остатку добавляется 50 мг диэтилового эфира, не содержащего кислорода, и после того, как этот материал оставляется на ночь отстаиваться, D,L-2-амино-2-дейтеро-3(3,4-дигидрооксифенил)метилпропионат выпадает в осадок. После рекристаллизации из смеси метанол/диэтиловый эфир, свободной от кислорода, которая комбинируется с 2,6-ди-трет-бутил-4 метоксифенолом, выделяется 1,8 г продукта. Выход: 84,9%. Пример 3.L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)пропионовая кислота. 1,15 г D,L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)метилпропионата растворяются в 30 мл раствора 0,2-молярного раствора бикарбоната натрия (pH 8,2). Добавляется 200 мкл алкалазы, и pH раствора поддерживается на этом уровне с помощью карбонат-бикарбонатного буфера. Ход реакции отслеживается с помощью жидкостной хроматографии высокого разрешения (HPLC) и реакция прекращается при добавлении соляной кислоты, когда концентрация пропионата уменьшается на половину. Дейтерированная аминокислота, содержащаяся в растворе, отделяется от дейтерированного метилового эфира хроматографически с использованием системы растворителей ацетонитрил/0,1% водная трифторуксусная кислота (15:85), и отделяется 0,51 г L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)пропионовой кислоты. Выход: 95% (основан на пропорции L-энантиомера). Точка плавления: 287-290C.L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)метилпропионат. 2,0 г L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)пропионовой кислоты растворяются в 30 мл метанола, охлаждаются до -10C и взаимодействуют по каплям с 1 мл тионилхлорида. Затем реакционная смесь нагревается до 40C в течение 15 ч. Летучие вещества реакционной смеси удаляются в вакууме и добавляется 10 мл воды, 15 мл раствора 0,8 г гидрокарбоната натрия, 1 г сульфата натрия и 1 мг аскорбиновой кислоты. pH раствора доводится до 7 добавлением разбавленного раствора гидроксида натрия. Полученный продукт переводится в органическую фазу экстрагированием с этилацетатом, не содержащим кислорода, который включает 0.01% 2,6-ди-трет-бутил-4-метоксифенола. Органическая фаза сушится, а затем растворитель удаляется отгонкой. К остатку добавляется 50 мг диэтилового эфира, не содержащего кислорода, и после того, как этот материал оставляется на ночь отстаиваться, L-2-амино-2 дейтеро-3-(3,4-дигидрооксифенил)метилпропионат выпадает в осадок. После рекристаллизации из смеси метанол/диэтиловый эфир, свободной от кислорода, которая комбинируется с 2,6-ди-трет-бутил-4 метоксифенолом, выделяется 1,9 г продукта. Выход: 89.6%.L-2-Амино-2-дейтеро-3-(3,4-дигидрооксифенил)этилпропионат. 2,0 г L-2-амино-2-дейтеро-3-(3,4-дигидрооксифенил)пропионовой кислоты растворяются в 30 мл этанола, охлаждаются до -10C и взаимодействуют по каплям с 1 мл тионилхлорида. Затем реакционная смесь нагревается до 40C в течение 15 ч. Летучие вещества реакционной смеси удаляются в вакууме и добавляется 10 мл воды, 15 мл раствора 0,8 г гидрокарбоната натрия, 1 г сульфата натрия и 1 мг аскорбиновой кислоты. pH раствора доводится до 7 добавлением разбавленного раствора гидроксида натрия. Полученный продукт переводится в органическую фазу экстрагированием с этилацетатом, не содержащим кислорода, который включает 0.01% 2,6-ди-трет-бутил-4-метоксифенола. Органическая фаза сушится, а затем растворитель удаляется отгонкой. К остатку добавляется 50 мг диэтилового эфира, не содержащего кислорода, и после того, как этот материал оставляется на ночь отстаиваться, L-2-амино-2 дейтеро-3-(3,4-дигидрооксифенил)этилпропионат выпадает в осадок. После рекристаллизации из смеси этанол/диэтиловый эфир, свободной от кислорода, которая комбинируется с 2,6-ди-трет-бутил-4 метоксифенолом, выделяется 2 г продукта. Выход: 88.5%.L-2-Амино-2,3(S)-дидейтеро-3-(3,4-дигидроксифенил)пропионовая кислота. 2,5 г N-ацетил-3-метокси-4-ацетоксикоричной кислоты растворяются в 30 мл метанола, содержащего 0,027 г гидроксида натрия, и помещаются в автоклав. Кислород заменяется азотом перед заполнением реактора газообразным дейтерием. В то же время 0,5 г катализатора Monsanto готовится в 2,5 мл толуола обработкой газообразным дейтерием. После добавления катализатора в автоклав начинается "гидрогенизация" при 60C и 4-5 барах. После 4 ч излишек газообразного дейтерия удаляется и растворитель отгоняется. Соль натрия дейтерированного продукта выделяется и рекристаллизуется. Выход: 2,4 г (94%). 0,9 г соли натрия растворяются в 2,5 мл бромисто-водородной кислоты (23%) и нагреваются для дефлегмации при около 105-110C. После этого реакционная смесь охлаждается до 25-30C и pH доводится до 3 добавлением концентрированного раствора гидроксида натрия для осаждения L-2-амино 2,3(S)-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты. Осадок промывается холодной водой и рекристаллизуется в горячей воде при использовании защитного газа. После рекристаллизации выделяется 0,51 г продукта. Выход: 85.1%. Точка плавления: 286-299C.L-2-амино-2,3(S)-дидейтеро-3-(3,4-дигидроксифенил)метилпропионат. Соединение получают в соответствии с описанием для монодейтерированного соединения (см. пример 4). Выход: 91%.L-2-Амино-2,3(S)-дидейтеро-3-(3,4-дигидроксифенил)этилпропионат. Соединение получают в соответствии с описанием для монодейтерированного соединения (см. пример 5). Выход: 93%, C11H13D2NO4. Расчетные данные: С 58.14%, Н 5.77%; N 6.16%; O 28.16%; D 1.77%; Фактические данные: С 58.10%; H+D 7.48%; N 6.10%; 1 Н-ЯМР (400 MHz, d6-DMSO): 6.59 (d, 1H); 6.54 (s, 1H); 6.48 (d, 1H); 2.72 (m, 1H); 4.17 (q, 2H); 1.22L-2-Амино-2-дейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовая кислота. 0,2 г L-2-амино-2-дейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты помещается в автоклав,куда добавляется 10 мл D2O. Из автоклава удаляется воздух, и он нагревается до 190C в течение 24 ч. Удаляется растворитель и добавляется этиловый эфир уксусной кислоты. Растворитель отгоняется, а остаток промывается холодным ацетоном. После этого выделяется 0,17 г продукта. Выход: 84%.L-2-Амино-2-дейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)метилпропионат. Соединение получают в соответствии с описанием для монодейтерированного соединения (см. пример 4). Выход: 89%.L-2-Амино-2-дейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)этилпропионат. Соединение получают в соответствии с описанием для монодейтерированного соединения (см. пример 5). Выход: 92% C11H11NO4D4. Расчетные данные: С 57.63%; Н 4.84%; N 6.11%; О 27.91%; D 3.51%. Фактические данные: С 57.57%; H+D 8.31%; N 6.15%. 1 Н-ЯМР (400 MHz, d6-DMSO): 4.17 (q, 2H); 3.06 (d, 1H); 2.88 (d, 1 Н); 1.21 (t, 3H). Пример 12.L-2-Амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовая кислота. 0,2 г L-2-амино-2-дейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты помещается в автоклав,куда добавляется 10 мл D2O. Из автоклава удаляется воздух, и он нагревается до 190C в течение 24 ч. Удаляется растворитель и добавляется этиловый эфир уксусной кислоты. Растворитель отгоняется, а остаток промывается холодным ацетоном. После этого выделяется 0,16 г продукта. Выход: 79.2%.L-2-Амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)метилпропионат. Соединение получают в соответствии с описанием для монодейтерированного соединения (см. пример 4). Выход: 90%.L-2-Амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)этилпропионат. Соединение получают в соответствии с описанием для монодейтерированного соединения (см. пример 5). Выход: 93%.C11H10D5NO4. Расчетные данные: С 57.38%; Н 4.38%; N 6.08%; O 27.79%; D 4.37%. Фактические данные: С 57.34%; H+D 8.71%; N 6.04%. 1 Н-ЯМР (400 MHz, d6-DMSO): 4.15 (q, 2H); 2.75 (m, 1H); 1.21 (t, 3H). Пример 15. Выход стриарного допамина, измеренный с помощью микродиализа. Выход стриарного допамина измерялся у самцов крыс Уистара после интраперитонеального введения 50 мг/кг L-2-амино-3-(3,4-дигидроксифенил)пропионовой кислоты (L-DOPA), L-2-амино-2,3,3 тридейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты (WO-A 2004/056724, пример 6) и L-2-амино 2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты (пример 6). Самцы крыс Уистара (ВК Universal, Sollentuna, Sweden) массой около 300 г во время проведения эксперимента анестезировались смесью, содержащей фентанилцитрат (0,39 мг/кг), меторин (12,5 мг/кг, Hypnorm, Janssen-Cilag) и мидазолам (6,25 мг/кг, Dormicum, Roche), разбавленные дистиллированной водой (1:1:2; 5 мл/кг), и крепились в стереотаксической рамке. Пробы диализа имплантировались в дорсолатеральный стриатум (AP: +0.6:Watson (1998. Диализ происходил через полупроницаемую мембрану (Filtral AN69, Hospal Industrie,Франция) с длиной активной поверхности 3,5 мм. Эксперименты по диализу проводились приблизительно через 48 ч после хирургического вмешательства на свободно движущихся крысах. Крысы получали 10 мг/кг Кардидопы за 30 мин до введения тестовых веществ. Пробы для диализа вводились с физиологическим раствором для перфузии (Apoteksbolaget, Швеция) со скоростью 2,5 мл/мин с помощью микроинфузионного насоса (Harvard Apparatus, Hollis-ton, MA). Диализат собирался с интервалом в 15 мин и автоматически инжектировался в систему жидкостной хроматографии высокого разрешения. Определение количества допамина в диализате осуществлялось электрохимическим детектором (ESA, Cheimsford,MA). Расположение проб для микродиализа определялось в срезах зафиксированной формалином ткани,помеченных природным красным пигментом. Строились графики базисной скорректированной концентрации (моль/мин) во времени. Сравнение значений AUCo-t (площадь под кривой) показало, что повышение содержания допамина в стриатуме после введения 50 мг/кг L-2-амино-2,3,3-тридейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты было приблизительно в два раза больше по сравнению с L-2-амино-3-(3,4 дигидроксифенил)пропионовой кислотой (L-DOPA), как показано в таблице. Повышение содержания стриарного допамина после введения 50 мг/кг 1-амино-2,3-дидейтеро-3-(3,4-дигидроксифенил)пропионовой кислоты (пример 6) было даже в три раза выше по сравнению с содержанием, изменнным после введения L-DOPA. Базисный скорректированный выход допамина в стриатуме ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Дейтерированные производные катехоламина общей формулы IR6 представляет собой Н или D, где оба остатка R6 не являются одновременно D и где оба остатка 6R не являются одновременно H,их стереоизомеры, энантиомеры или диастереомеры в оптически чистой форме, а также их физиологически приемлемые соли. 2. Дейтерированное производное катехоламина по п.1, гдеR6 представляет собой Н или D, при условии, что оба остатка R6 не являются одновременно D, и при условии, что оба остатка R6 не являются одновременно H. 3. Дейтерированное производное катехоламина по п.1, гдеR6 представляет собой Н или D, при условии, что оба остатка R6 не являются одновременно D, и при условии, что оба остатка R6 не являются одновременно H. 4. Дейтерированное производное катехоламина по п.1, выбранное изS/S-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5 дигидроксифенил)пропионовой кислоты,этилового эфира S/S-2-амино-2,3-дидейтеро-3-(2,3,6-тридейтеро-4,5-дигидроксифенил)пропионовой кислоты. 5. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для лечения болезней, вызываемых недостатком допамина, которые основываются на нарушении передачи тирозина или на нарушении активности тирозиндекарбоксилазы, выбранных из болезни Паркинсона, синдрома беспокойных ног и дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии. 6. Применение дейтерированных производных катехоламина и их физиологически приемлемых со- 10017983 лей по любому из пп.1-4 в комбинации с одним или с несколькими ингибиторами ферментов, выбранных из ингибитора декарбоксилазы, ингибитора катехол-O-метилтрансферазы, ингибитора моноаминоксидазы и ингибитора -гидроксилазы, для лечения болезней, вызываемых недостатком допамина, которые основываются на нарушении передачи тирозина или на нарушении активности тирозиндекарбоксилазы,выбранных из болезни Паркинсона, синдрома беспокойных ног и дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии. 7. Применение по п.6, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-Lгидразино-3,4 дигидроксиметилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4-тригидроксибензил)гидразид,глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемых солей. 8. Применение по п.6, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей. 9. Применение по п.6, где ингибитор моноаминоксидазы выбран из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. 10. Применение по п.6, где ингибитор -гидроксилазы выбран из 5-бутилпиколината кальция и 5 пентилпиколината кальция, а также их физиологически приемлемых солей. 11. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для производства фармацевтического препарата для лечения болезни Паркинсона, синдрома беспокойных ног, бокового амиотрофического склероза и множественной системной атрофии. 12. Фармацевтическая композиция для лечения болезни Паркинсона, синдрома беспокойных ног,дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4 в комбинации с фармацевтически приемлемыми обычными тврдыми или жидкими связующими веществами или разбавителями. 13. Фармацевтическая композиция для лечения болезни Паркинсона, синдрома беспокойных ног,дистонии, для ингибирования секреции пролактина, для стимуляции высвобождения гормона роста, для лечения неврологических симптомов хронической интоксикации марганцем, бокового амиотрофического склероза и множественной системной атрофии, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4, а также один или более ингибиторов ферментов, включающих ингибиторы декарбоксилазы и/или ингибиторы катехол-O-метилтрансферазы,и/или ингибиторы моноаминоксидазы, и/или ингибиторы -гидроксилазы, в комбинации с фармацевтически приемлемыми обычными тврдыми или жидкими связующими веществами или разбавителями. 14. Фармацевтическая композиция по п.13, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-гидразино-3,4-дигидроксиметилгидрокоричная кислота(карбидопа),L-серин 2-(2,3,4 тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4 тригидроксибензил)гидразид, а также их физиологически приемлемых солей. 15. Фармацевтическая композиция по п.13, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей. 16. Фармацевтическая композиция по п.13, где ингибитор моноаминоксидазы выбран из группы,включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. 17. Фармацевтическая композиция по п.13, где ингибитор -гидроксилазы выбран из 5 бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей. 18. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для получения фармацевтической композиции для профилактики психозов. 19. Применение по п.18, при котором психозом является шизофрения. 20. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для лечения острых психозов. 21. Применение по п.20, при котором острым психозом является шизофрения. 22. Применение по п.21, при котором шизофрения характеризуется негативной симптоматикой. 23. Применение дейтерированных производных катехоламина по любому из пп.1-4, а также их физиологически приемлемых солей в комбинации с одним или несколькими ингибиторами ферментов, выбранных из ингибитора декарбоксилазы, ингибитора катехол-O-метилтрансферазы, ингибитора моноаминоксидазы и ингибитора -гидроксилазы, для профилактики психозов, а также для лечения острых психозов при негативной симптоматике. 24. Применение по п.23, при котором острым психозом является шизофрения. 25. Применение по п.23, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-Lгидразино-3,4 дигидроксиметилгидрокоричная кислота (карбидопа), L-серин 2-(2,3,4-тригидроксибензил)гидразид,глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4-тригидроксибензил)гидразид, а также их физиологически приемлемых солей. 26. Применение по п.23, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей. 27. Применение по п.23, где ингибитор моноаминоксидазы выбран из группы, включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. 28. Применение по п.23, где ингибитор -гидроксилазы выбран из 5-бутилпиколината кальция и 5 пентилпиколината кальция, а также их физиологически приемлемых солей. 29. Применение дейтерированных производных катехоламина и их физиологически приемлемых солей по любому из пп.1-4 для производства фармацевтического препарата для профилактики психозов,а также для лечения острых психозов при негативной симптоматике. 30. Фармацевтическая композиция для профилактики психозов, а также для лечения острых психозов при негативной симптоматике, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4 в комбинации с фармацевтически приемлемыми обычными тврдыми или жидкими связующими веществами или разбавителями. 31. Фармацевтическая композиция для профилактики психозов и для лечения острых психозов при негативной симптоматике, содержащая дейтерированные производные катехоламина и их физиологически приемлемые соли по любому из пп.1-4, а также один или несколько ингибиторов ферментов, выбранных из ингибитора декарбоксилазы, ингибитора катехол-O-метилтрансферазы, ингибитора моноаминоксидазы и ингибитора -гидроксилазы в комбинации с фармацевтически приемлемыми обычными тврдыми или жидкими связующими веществами или разбавителями. 32. Фармацевтическая композиция по п.31, где ингибитор декарбоксилазы выбран из группы, состоящей из следующих соединений: D,L-серин 2-(2,3,4-тригидроксибензил)гидразид (бенсеразид), (-)-L-гидразино-3,4-дигидроксиметилгидрокоричная кислота(карбидопа),L-серин 2-(2,3,4 тригидроксибензил)гидразид, глицин 2-(2,3,4-тригидроксибензил)гидразид и L-тирозин 2-(2,3,4 тригидроксибензил)гидразид, а также их физиологически приемлемых солей. 33. Фармацевтическая композиция по п.31, где ингибитор катехол-O-метилтрансферазы выбран из энтакапона и каберголина, а также их физиологически приемлемых солей. 34. Фармацевтическая композиция по п.31, где ингибитор моноаминоксидазы выбран из группы,включающей селегилин, моклобемид и транилципромин, а также их физиологически приемлемые соли. 35. Фармацевтическая композиция по п.31, где ингибитор -гидроксилазы выбран из 5 бутилпиколината кальция и 5-пентилпиколината кальция, а также их физиологически приемлемых солей.
МПК / Метки
МПК: C07B 59/00, C07C 229/26
Метки: средства, катехоламина, содержащие, соединения, дейтерированные, производные, лекарственные, указанные
Код ссылки
<a href="https://eas.patents.su/13-17983-dejjterirovannye-proizvodnye-kateholamina-i-lekarstvennye-sredstva-soderzhashhie-ukazannye-soedineniya.html" rel="bookmark" title="База патентов Евразийского Союза">Дейтерированные производные катехоламина и лекарственные средства, содержащие указанные соединения</a>
Предыдущий патент: Фармацевтическая композиция на основе транскаротиноидов и способы лечения опухоли
Следующий патент: Кристаллические безводные формы лактата n-гидрокси-3-[4-[[[2-(2-метил-1h-индол-3-ил)этил]амино]метил]фенил]-2e-2-акриламида
Случайный патент: Устройство и способ для отбора и первичной подготовки проб ткани для молекулярной генной диагностики

















