Способ получения хинолин-3-карбоксамидов
Номер патента: 21171
Опубликовано: 30.04.2015
Авторы: Хольмберг Пер Хеннинг, Янссон Карл-Эрик, Бок Лиллемор Мария
Формула / Реферат
1. Способ получения соединения формулы (I)

в которой
R1 представляет собой этил, R2 представляет собой этил и R3 представляет собой Н; или
R1 представляет собой хлор, R2 представляет собой этил и R3 представляет собой Н; или
R1 представляет собой метокси, R2 представляет собой метил и R3 представляет собой трифторметил;
содержащий стадии, на которых:
(i) соединение формулы (II)
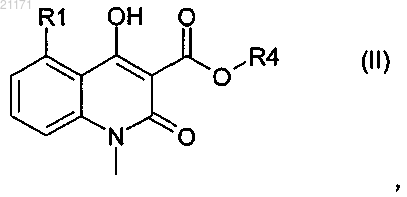
в которой R1 представляет собой этил, хлор или метокси и R4 представляет собой (С1-С4)алкил,
вводят в реакцию с соединением формулы (III)
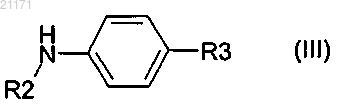
в которой R2 представляет собой этил и R3 представляет собой Н; или R2 представляет собой метил и R3 представляет собой трифторметил;
при кипячении в смеси, содержащей алифатический растворитель или смесь алифатических растворителей, причем указанный(е) алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 68-191°C;
(ii) пары кипящей смеси конденсируют;
(iii) конденсированные пары обрабатывают поглотителем спирта, выбранным из молекулярных сит, или поглотителем спирта, который представляет собой смесь молекулярных сит; и
(iv) конденсированные пары возвращают в реакционную смесь.
2. Способ по п.1, в котором алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 80-150°C.
3. Способ по п.1, в котором алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 95-130°C.
4. Способ по п.1, в котором поглотитель спирта выбран из молекулярных сит 3Å, 4Å, 5Å, 13Х или представляет собой смесь любых из указанных молекулярных сит.
5. Способ по любому из пп.1-4, в котором алифатический(е) растворитель(и) выбирают из разветвленных или линейных алканов и циклоалканов С6-С10.
6. Способ по любому из пп.1-5, в котором алифатический(е) растворитель(и) выбирают из разветвленных или линейных алканов и циклоалканов С7-С8.
7. Способ по п.6, в котором алифатический(е) растворитель(и) выбирают из н-гептана, н-октана, метилциклогексана, 2,2,4-триметилпентана и циклооктана.
8. Способ по п.7, в котором алифатический(е) растворитель(и) выбирают из н-гептана и н-октана.
9. Способ по любому из пп.1-8, в котором R4 выбирают из метила, этила, н-пропила, изопропила и н-бутила.
10. Способ по п.9, в котором R4 выбирают из метила и этила.
11. Способ по п.1, в котором R1 представляет собой этил, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил или этил; поглотитель спирта представляет собой молекулярные сита 3Å, 4Å, 5Å или 13Х или представляет собой их смесь и алифатический(е) растворитель(и) выбирают из н-гептана и н-октана.
12. Способ по п.1, в котором R1 представляет собой хлор, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил, поглотитель спирта представляет собой молекулярные сита 3Å, 4Å, 5Å или 13Х и алифатический(е) растворитель(и) выбирают из н-гептана и н-октана.
13. Способ по п.1, в котором R1 представляет собой метокси, R2 представляет собой метил, R3 представляет собой трифторметил, R4 представляет собой метил или этил; поглотитель спирта представляет собой молекулярные сита 3Å, 4Å, 5Å или 13Х или представляет собой их смесь и алифатический растворитель представляет собой н-октан.
Текст
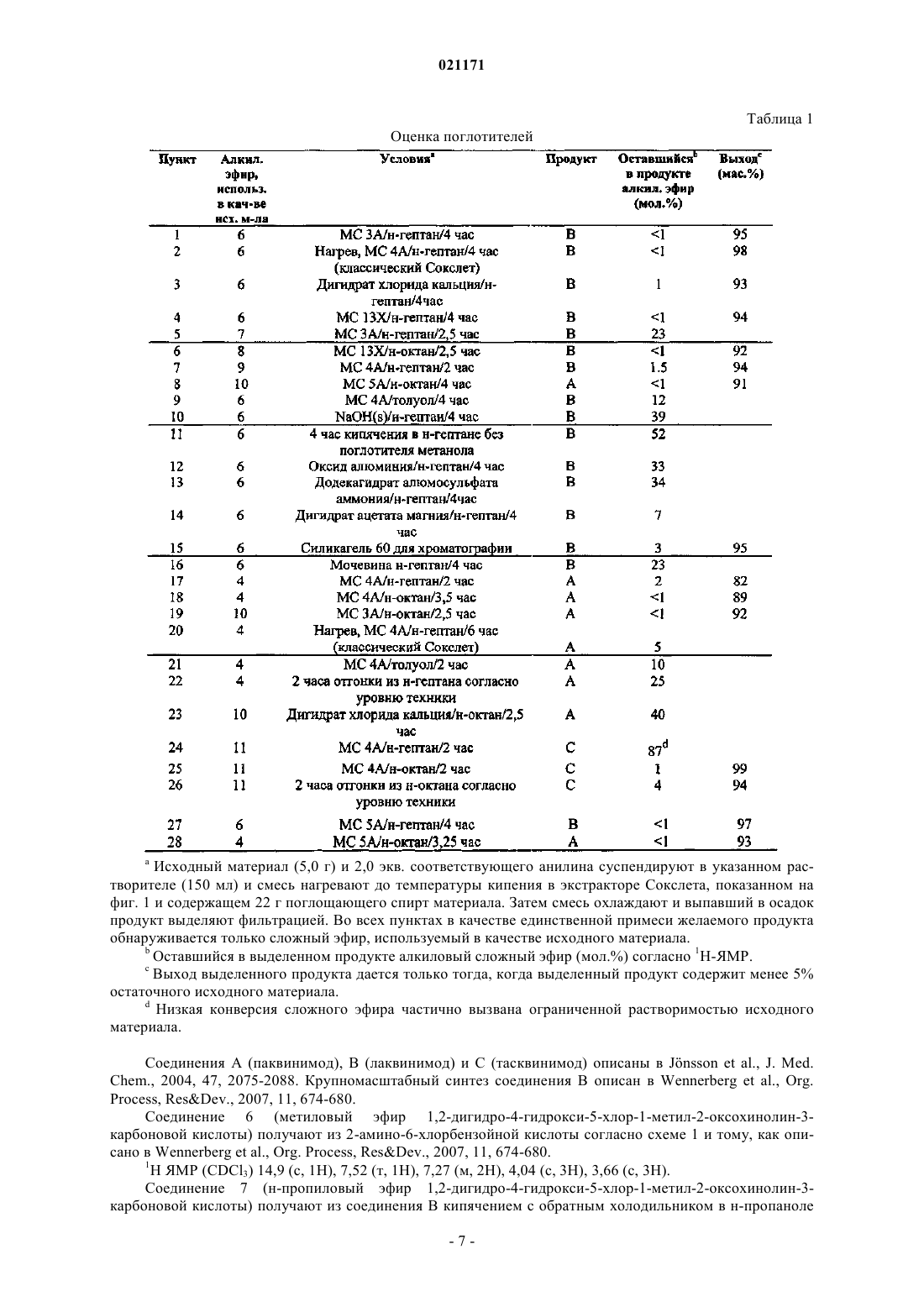
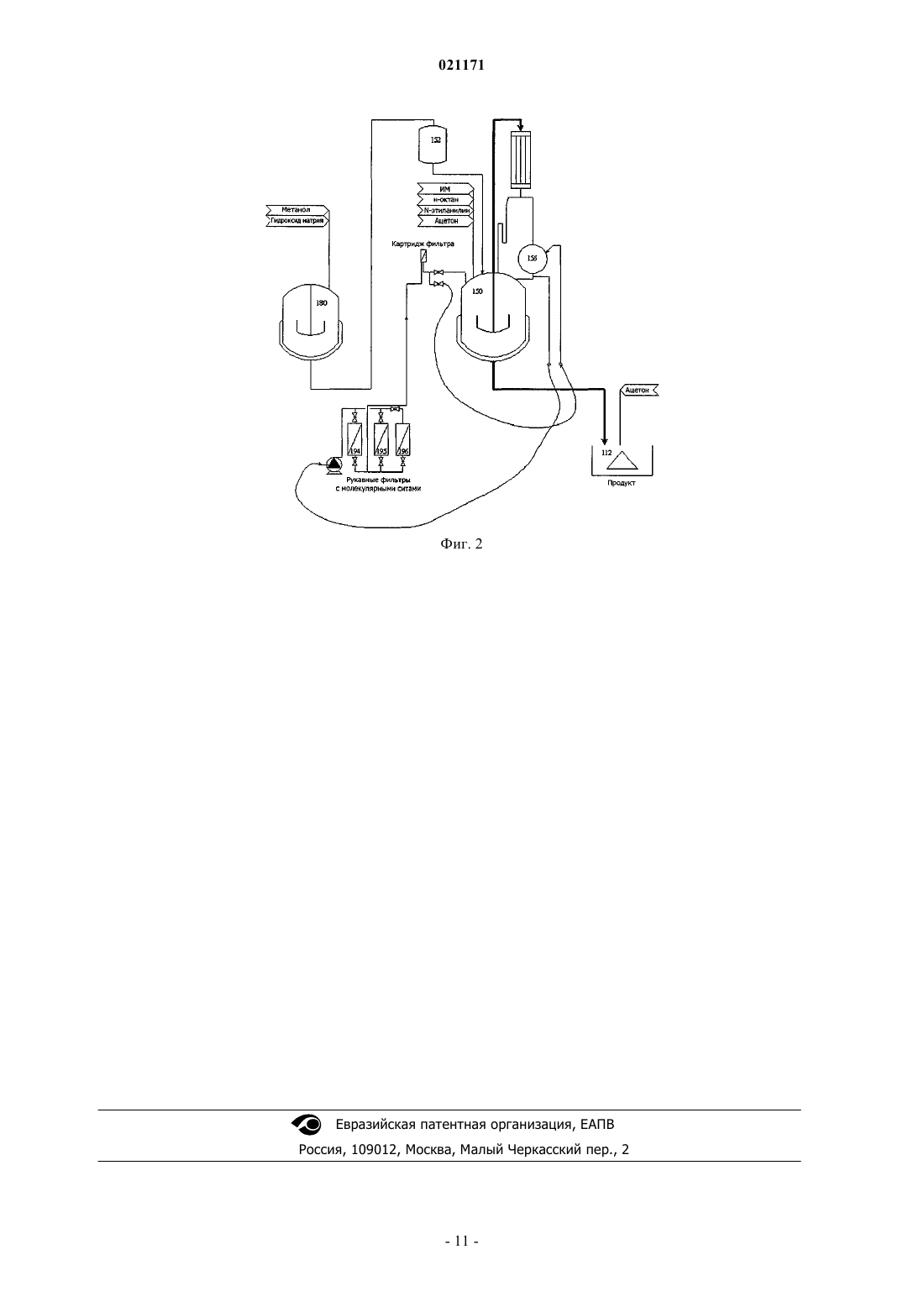
Описывается способ получения соединения формулы (I) путем реакции соответствующего алкилового сложного эфира и производного анилина в кипящей смеси, содержащей алифатический растворитель или смесь алифатических растворителей, имеющих температуру кипения в интервале 68-191C; конденсации паров кипящей смеси; обработки конденсированных паров поглотителем спирта или смесью поглотителей спирта и возвращения конденсированных паров обратно в реакционную смесь.(71)(73) Заявитель и патентовладелец: ЭКТИВ БАЙОТЕК АБ (SE) Область техники, к которой относится изобретение Настоящее изобретение относится к области органического синтеза. В частности, изобретение относится к области химического синтеза некоторых производных N-алкил-N-фенилхинолин-3 карбоксамидов. Уровень техникиN-алкил-N-фенилхинолин-3-карбоксамиды представляют собой перспективный класс соединений,проходящих клинические испытания против различных типов заболеваний, таких как, например, аутоиммунные заболевания и рак.N-алкил-N-фенилхинолин-3-карбоксамиды, такие как паквинимод (в настоящем документе ниже обозначаемый также как А), лаквинимод (в настоящем документе ниже обозначаемый также как В) и тасквинимод (в настоящем документе ниже обозначаемый также как С), получают способом, включающим отгонку летучих веществ из смеси, содержащей сложный эфир, анилин и алифатический растворитель, такой как н-гептан или н-октан. Этот способ описан в патенте США 6875869. Известная из уровня техники (Wennerberg et al., Org. Process, ResDev., 2007, 11, 674-680) методика синтеза N-алкил-N-фенилхинолин-3-карбоксамидов, таких как паквинимод (А), лаквинимод (В) и тасквинимод (С), иллюстрируется примером синтеза паквинимода по схеме 1. Синтез начинается с антраниловой кислоты 1, которую превращают в изатовый ангидрид 2. Изатовый ангидрид метилируют и получают 3, который конденсируют с диметилмалонатом для получения соответствующего метилового эфира 4. Затем метиловый эфир конденсируют с соответствующим анилином с получением желаемого конечного соединения. Схема 1 Путь синтеза N-алкил-N-фенилхинолин-3-карбоксамидов на примере синтеза паквинимода (А) через соответствующий метиловый эфир 4 Такой способ получения короток и позволяет избежать использования дорогостоящих реагентов. Все промежуточные соединения устойчивы и легко выделяются с высокой чистотой путем осаждения и фильтрации. Основной примесью на конечной стадии конденсации является оставшийся алкиловый сложный эфир. Другие способы, такие как опосредуемое карбодиимидом сочетание между карбоновой кислотой и анилином или конденсация метилового эфира N-алкил-N-фенилмалонаминовой кислоты с изатовым ангидридом (патент США 5912349), или являются более длительными, или дают продукт меньшей чистоты. Конечная стадия конденсации соответствует равновесию (схема 2), сдвинутому в сторону алкилового сложного эфира, и убедительные данные указывают на механизм реакции с участием промежуточного кетена 5 (Jansson et al., J. Org. Chem., 2006, 71, 1658-1667 и Lu Jin et al., J. Phys. Chem. A 2008, 112,4501-4510). Обычно для образования амидов из сложных эфиров и анилинов требуются весьма высокие температуры, которые также приводят к образованию значительного количества побочных продуктов. Вышеуказанная реакция может проходить при умеренных температурах за счет способности 4 к мономолекулярному образованию промежуточного кетена 5 вместо тетраэдрического промежуточного соединения. Способ, описанный в патенте США 6875869, включает загрузку в реактор соответствующего сложного эфира и производного анилина в алифатическом растворителе, таком как н-гептан или н-октан. Равновесие сдвигается в сторону желаемого продукта путем отгонки растворителя и всех образующихся спиртов. После завершения реакции смесь охлаждают и выпавший в осадок сырой продукт реакции извлекают путем фильтрации. В отличие от большинства других реакций, в которых сложные эфиры превращаются в термодинамически более устойчивые амиды, в данной конкретной реакции для того, чтобы получить высокий выход, требуется весьма эффективное удаление образовавшегося спирта. Описанный выше способ используется для получения паквинимода, лаквинимода и тасквинимода в рамках GMP (Good Manufacturing Practice, надлежащая практика организации производства). Раскрытие изобретения Как отмечалось выше в данном описании, в реакции, описанной в Wennerberg et al., Org. ProcessResDev., 2007, 11, 674-680, при получении N-алкил-N-фенилхинолин-3-карбоксамида основной примесью в выделенном сыром продукте является алкиловый сложный эфир, используемый в качестве исходного материала на конечной стадии конденсации. Конденсацию можно представить следующей общей схемой реакции: В реакции, представленной выше в данном описании, оставшийся сложный эфир (II) можно легко удалить из продукта перекристаллизацией, если этот эфир присутствует в небольших количествах. С другой стороны, авторы настоящего изобретения обнаружили, что если в сыром продукте присутствуют большие количества остаточного сложного эфира, только одной перекристаллизации может быть недостаточно для получения чистого продукта. Следовательно, важно сдвинуть равновесие в сторону продукта настолько, насколько это возможно, путем удаления спирта (IV), образующегося в реакции в качестве побочного продукта. Авторы настоящего изобретения также обнаружили другую проблему - что процесс удаления спирта (IV) зависит от масштаба синтеза. Таким образом, когда реакция конденсации осуществляется в небольшом масштабе (например, менее 20 г), большая часть эфира (II) превращается в продукт (I) за несколько часов дистилляции. В таком случае выпавший в осадок продукт содержит только небольшие(приемлемые) количества сложного эфира в качестве примеси. Однако в более крупномасштабном синтезе, например, в килограммовом масштабе, процесс становится менее предсказуемым, и в некоторых случаях существенные количества эфира (II) остаются в смеси даже после 20 ч дистилляции. В таких случаях необходимо добавить еще растворитель и продолжать дистилляцию до тех пор, пока большая часть эфира (II) не превратится в нужный продукт (I). Способ, в рамках которого для того, чтобы достичь полной конверсии, расходуются большие и непредсказуемые количества алифатического растворителя,далек от оптимального в случае получения лекарственных средств. Поэтому авторы настоящего изобретения приступили к задаче разработки усовершенствованного способа получения соединения формулы (I), определенной в настоящем документе, с высоким выходом и преимущественно без вышеуказанных недостатков. В частности, такой способ должен дать возможность получать соединение формулы (I) в большом масштабе с высоким выходом и высокой чистотой продукта и преимущественно без необходимости продолжительного времени реакции и избыточного расхода растворителя и энергии. Соответственно, предлагается способ получения соединения формулы (I)R1 представляет собой этил, R2 представляет собой этил и R3 представляет собой Н; илиR1 представляет собой хлор, R2 представляет собой этил и R3 представляет собой Н; илиR1 представляет собой метокси, R2 представляет собой метил и R3 представляет собой трифторметил,путем(i) реакции соединения формулы (II)R1 представляет собой этил, хлор или метокси и R4 представляет собой (С 1-С 4)алкил,с соединением формулы (III)R2 представляет собой этил и R3 представляет собой Н; илиR2 представляет собой метил и R3 представляет собой трифторметил; при кипячении в смеси, содержащей алифатический растворитель или смесь алифатических растворителей, причем указанный(е) алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 68-191C;(ii) конденсации паров кипящей смеси;(iii) обработки конденсированных паров поглотителем спирта или смесью поглотителей спирта и(iv) возврата конденсированных паров в реакционную смесь. Авторы настоящего изобретения обнаружили, что способ, описанный в настоящем документе, позволяет достичь более высоких значений выхода реакции за более короткое время по сравнению со способами из уровня техники. Это, в свою очередь, приводит к снижению расхода энергии, что вместе с уменьшенным расходом растворителя во время реакции является крайне выгодным с экономической точки зрения и с точки зрения окружающей среды. Более того, способ по настоящему изобретению позволяет получить продукт реакции с более высокой чистотой. Весьма выгодно то, что продукт реакции с более высоким выходом и улучшенной чистотой получают за более короткое время реакции и с меньшим расходом растворителя и энергии, чем в способах из уровня техники, особенно, когда реакцию выполняют в большом масштабе. Другими преимуществами настоящего изобретения являются такие преимущества, что использование поглотителя спирта позволяет достичь более высокой скорости дистилляции без уменьшения объема реакционной смеси; таким образом, получают более короткое время реакции; расход растворителя снижается до минимума за счет его рециркуляции; отсутствует необходимость в тщательном контроле за скоростью дистилляции, и имеет место почти полная конверсия сложного эфира, что приводит к большей чистоте выделяемого продукта. Краткое описание чертежей Фиг. 1 иллюстрирует модифицированный экстрактор Сокслета, используемый в экспериментах с поглотителями и фиг. 2 иллюстрирует компоновку оборудования в опытной установке для получения паквинимода. Осуществление изобретения Поглотитель спирта. В способе по настоящему изобретению дистиллят обрабатывают поглотителем спирта перед возвратом в реакционную смесь. Поглотитель спирта можно выбирать, например, из молекулярных сит, силикагеля и дигидрата хлорида кальция или смеси любых из них. Авторы настоящего изобретения испытали множеством поглотителей спирта в комбинации с различными растворителями и обнаружили, что молекулярные сита являются особенно полезными для получения соединений формулы (I), описанных в настоящем документе. Молекулярные сита представляют собой кристаллические алюмосиликаты металлов, имеющие трехмерную переплетающуюся сетку тетраэдров диоксида кремния и оксида алюминия. Молекулярные сита способны абсорбировать различные полярные соединения в образуемых сеткой полостях. Существуют молекулярные сита различного качества, такие как порошок сит 3, 4, 5 и 13 Х, которые можно закупить, например, у Sigma-Aldrich Co. В одном предпочтительном варианте осуществления поглотитель спирта выбирают из молекулярных сит или смеси молекулярных сит. Например, поглотитель спирта можно выбирать из молекулярных сит 3, 4, 5, 13 Х, или он может представлять собой смесь любых указанных молекулярных сит. Состав молекулярных сит 3 приблизительно соответствует следующему: 0,6 K2O:0,40 Na2O:1 Al2O3:2,00,1 SiO2:xH2O. Эту форму получают заменой катионами калия свойственных структуре 4 ионов натрия, что приводит к получению пор размерами приблизительно 3. Молекулярные сита 3 используются главным образом для удаления влаги. Молекулярные сита 4 имеют состав, приблизительно соответствующий 1 Na2O:1 Al2O3:2,00,1SiO2:xH2O. Молекулярные сита 4 имеют эффективное отверстие поры примерно 4 (0,4 нм). Такие сита, как правило, рассматриваются как универсальный осушитель в полярных и неполярных средах. Молекулярные сита 5 имеют состав, приблизительно соответствующий 0,80 CaO:0,20 Na2O:1Al2O3:2,00,1 SiO2:xH2O, а размер их пор составляет примерно 5. Молекулярные сита 13 Х имеют состав, приблизительно соответствующий 1 Na2O:1 Al2O3:2,80,2SiO2:xH2O. Размер пор молекулярных сит 13 Х примерно равен 10. Также могут быть использованы и другие молекулярные сита, и предполагается, что специалист в данной области техники может с помощью простых экспериментов определить те молекулярные сита или смесь молекулярных сит, которые подходят для использования в настоящем изобретении. Дополнительные сведения о молекулярных ситах можно найти в книге Molecular Sieves, R. Szostak, ed., BlackieAcademicProfessional (ISBN 0 75140480 2). Количество поглотителя спирта, используемого в способе по изобретению, предпочтительно является таким, что массовое отношение поглотителя спирта к сложному эфиру (II) составляет по меньшей мере 1:1. Предпочтительно поглотитель спирта используют в избытке относительно сложного эфира (II),например, при массовом отношении поглотителя спирта к сложному эфиру (II) 2:1, или 3:1, или 5:1, или даже выше. Алифатический растворитель. Алифатический растворитель или смесь алифатических растворителей для использования в способе по настоящему изобретению должны иметь температуру кипения в интервале 68-191C, предпочтительно 80-150C, более предпочтительно 95-130C. Такие растворители выбирают, например, из разветвленных или линейных алканов и циклоалканов С 6-С 10, например разветвленных или линейных алканов и циклоалканов С 7 или С 8. Для целей настоящего изобретения разветвленный или линейный алкан или циклоалкан С 6-С 10 означает алкан или циклоалкан, имеющий в совокупности от 6 до 10 атомов углерода. Разветвленный или линейный алкан С 7 или С 8 означает алкан, имеющий в совокупности 7 или 8 атомов углерода, например н-гептан, н-октан, 2,2,4-триметилпентан и т.д. Циклоалкан может быть моно- или полициклическим, например бициклическим. Кроме того, циклоалкан может быть или незамещенным, или замещенным (т.е. разветвленным) одной или несколькими разветвленными или линейными алкильными группами, причем следует иметь ввиду, что общее число атомов углерода в цикле и любом алкильном заместителе, взятых вместе, равно 6-10, в частности 7 или 8. Примером циклоалкана С 10 является декалин (т.е. декагидронафталин). Примерами циклоалканов С 7-С 8 являются метилциклогексан и циклооктан. Также можно использовать и другие изомеры алканов и циклоалканов, которые легко может вспомнить специалист, при условии, что выполняется указанное выше требование по температуре кипения. В одном варианте осуществления алифатический растворитель выбирают из н-гептана, н-октана,метилциклогексана, 2,2,4-триметилпентана и циклооктана или смеси любых из них. В другом варианте осуществления алифатический растворитель выбирают из н-гептана и н-октана или их смеси. Соединение формулы (II). В соединении формулы (II)R4 выбирают из (С 1-С 4)алкила, и он может быть разветвленным или линейным. В одном варианте осуществления R4 выбирают из метила, этила, н-пропила, изопропила и нбутила. В другом варианте осуществления R4 представляет собой (С 1-С 3)алкил, т.е. метил, этил, нпропил и изопропил. В еще одном варианте осуществления R4 представляет собой метил или этил, например R4 представляет собой метил. В реакции конденсации между соединениями (II) и (III) алифатический спирт (IV) образуется как побочный продукт, и такой алифатический спирт удаляют из конденсированных паров, содержащих алифатический растворитель или смесь алифатических растворителей, обработкой конденсированных паров поглотителем спирта или смесью поглотителей спирта. Некоторыми неограничивающими примерами сложных эфиров формулы (II) являются соединения 6-11, представленные ниже. Если в качестве исходного соединения (II) использовать, например, 4, образующийся спирт (IV) будет представлять собой метанол, если в качестве исходного соединения (II) использовать, например, 10,образующийся спирт (IV) будет представлять собой этанол, и т.д. Соединение формулы (I). Продукт, получаемый способом по изобретению, представляет собой соединение формулы (I)R1 представляет собой этил, R2 представляет собой этил и R3 представляет собой Н; илиR1 представляет собой хлор, R2 представляет собой этил и R3 представляет собой Н; илиR1 представляет собой метокси, R2 представляет собой метил и R3 представляет собой трифторметил. В одном варианте осуществления изобретения R1 представляет собой этил, R2 представляет собой этил и R3 представляет собой Н, т.е. полученное соединение представляет собой паквинимод. В другом варианте осуществления изобретения R1 представляет собой хлор, R2 представляет собой этил и R3 представляет собой Н, т.е. полученное соединение представляет собой лаквинимод. В еще одном варианте осуществления изобретения R1 представляет собой метокси, R2 представляет собой метил и R3 представляет собой трифторметил, т.е. полученное соединение представляет собой тасквинимод. Некоторые предпочтительные воплощения В одном подходящем варианте осуществления изобретения R1 представляет собой этил, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил или этил; поглотителем спирта являются молекулярные сита 3, 4, 5 или 13 Х или их смесь; и алифатический(е) растворитель(и) выбирают из н-гептана и н-октана. В одном конкретном варианте осуществления R1 представляет собой этил, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил; поглотителем спирта являются молекулярные сита 4, и алифатаческий(е) растворитель(и) выбирают из н-гептана и н-октана. В другом конкретном варианте осуществления R1 представляет собой этил, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой этил, поглотителем спирта являются молекулярные сита 5, и алифатический растворитель представляет собой н-октан. В еще одном варианте осуществления R1 представляет собой этил, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой этил, поглотителем спирта являются молекулярные сита 3, и алифатический растворитель представляет собой н-октан. В другом варианте осуществления R1 представляет собой хлор, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил, поглотителем спирта являются молекулярные сита 3, 4, 5 или 13 Х, и алифатический(е) растворитель(и) выбирают из н-гептана и н-октана, и, в частности,алифатический растворитель представляет собой н-гептан. В еще одном варианте осуществления R1 представляет собой метокси, R2 представляет собой метил, R3 представляет собой трифторметил, R4 представляет собой метил или этил, поглотителем спирта являются молекулярные сита 3, 4, 5 или 13 Х или их смесь; и алифатический растворитель представляет собой н-октан. В одном конкретном варианте осуществления R1 представляет собой метокси, R2 представляет собой метил, R3 представляет собой трифторметил, R4 представляет собой метил, поглотителем спирта являются молекулярные 4, и алифатический растворитель представляет собой н-октан. Ниже в настоящем документе изобретение поясняется некоторыми неграничивающими примерами и примерами сравнения, при этом алкиловые сложные эфиры формулы (II), используемые в качестве исходного материала, будут обозначаться цифрами, указанными в настоящем документе выше (т.е. соединения 4 и 6-11). Примеры Начальные эксперименты проводят в 5-граммовом масштабе с использованием оборудования, показанного на фиг. 1. Для оценки создают специальный экстрактор Сокслета (не является частью изобретения). Такой экстрактор Сокслета охлаждает дистиллят до пропускания его через материал, поглощающий спирт. В классическом экстракторе Сокслета в адсорбционной камере температура на несколько градусов ниже температуры кипения растворителя. Как подтверждают эксперименты, молекулярные сита являются более эффективными поглотителями при более низких температурах. При использовании модифицированного экстрактора Сокслета в круглодонную колбу загружают сложный эфир, соответствующий анилин и растворитель. Смесь нагревают до температуры кипения, и в двух охлаждаемых жидкостью холодильниках образуется конденсат. Конденсат самотеком проходит через слой молекулярных сит и затем обратно в реакционную смесь. Результаты суммированы в табл. 1. Молекулярные сита лучше поглощают спирты, например метанол, при более низких температурах (пп.17 и 20). Поглощение спирта протекает более эффективно из алифатических растворителей, чем из ароматических растворителей, например толуола. Это можно увидеть из пп.2 и 9 или пп.17 и 21. Процесс с молекулярными ситами идет быстрее, расходует меньше растворителя, легче контролируется и дает продукт более высокой чистоты, чем способ из уровня техники(пп.17 и 22 или пп.25 и 26, примеры 1 и 4 в экспериментальной части, и патент США 6875869). Метиловые сложные эфиры дают превосходный результат с молекулярными ситами типов 3, 4, 5 и 13 Х(пп.1, 2, 4, 17, 18, 25, 27 и 28). Молекулярные сита типа 3 и 5 также являются эффективными при использовании с этиловым сложным эфиром (пп.8 и 19). Превосходный результат при конденсации метилового или этилового сложного эфира (пп.1 и 19) в присутствии молекулярных сит 3 имеет место, несмотря на несоответствие между размером молекул метанола и этанола и полостью в 3 в ситах. Теоретически критические диаметры молекул метанола и этанола соответственно, слишком велики для молекулярных сит 3. Однако молекулярные сита 3 не эффективны, когда в качестве исходного материала используется н-пропиловый сложный эфир (п.5). Когда при реакции конденсации используют н-бутиловый сложный эфир, эффективны молекулярные сита 13 Х (п.6). Молекулярные сита оказались весьма эффективными в качестве поглощающего спирт материала при сравнении с другими испытанными материалами. Из испытанных поглощающих материалов дигидрат хлорида кальция также дает удовлетворительный результат с метиловым сложным эфиром, но менее эффективен, когда используют этиловый сложный эфир(пп.3 и 23). Силикагель для хроматографии удовлетворительно работает в качестве поглощающего спирт материала, но менее эффективен, чем молекулярные сита (п.15). Исходный материал (5,0 г) и 2,0 экв. соответствующего анилина суспендируют в указанном растворителе (150 мл) и смесь нагревают до температуры кипения в экстракторе Сокслета, показанном на фиг. 1 и содержащем 22 г поглощающего спирт материала. Затем смесь охлаждают и выпавший в осадок продукт выделяют фильтрацией. Во всех пунктах в качестве единственной примеси желаемого продукта обнаруживается только сложный эфир, используемый в качестве исходного материала.b Оставшийся в выделенном продукте алкиловый сложный эфир (мол.%) согласно 1 Н-ЯМР.c Выход выделенного продукта дается только тогда, когда выделенный продукт содержит менее 5% остаточного исходного материала.d Низкая конверсия сложного эфира частично вызвана ограниченной растворимостью исходного материала. Соединения А (паквинимод), В (лаквинимод) и С (тасквинимод) описаны в Jnsson et al., J. Med.Chem., 2004, 47, 2075-2088. Крупномасштабный синтез соединения В описан в Wennerberg et al., Org.Process, ResDev., 2007, 11, 674-680. Соединение 6 (метиловый эфир 1,2-дигидро-4-гидрокси-5-хлор-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из 2-амино-6-хлорбензойной кислоты согласно схеме 1 и тому, как описано в Wennerberg et al., Org. Process, ResDev., 2007, 11, 674-680. 1H ЯМР (CDCl3) 14,9 (с, 1 Н), 7,52 (т, 1 Н), 7,27 (м, 2 Н), 4,04 (с, 3H), 3,66 (с, 3H). Соединение 7 (н-пропиловый эфир 1,2-дигидро-4-гидрокси-5-хлор-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из соединения В кипячением с обратным холодильником в н-пропаноле-7 021171 в течение ночи и добавлением разбавленной соляной кислоты для осаждения соединения 7. 1 Н ЯМР(CDCl3) 15,06 (с, 1 Н), 7,50 (т, 1 Н), 7,27 (д, 1H), 7,23 (д, 1H), 4,39 (т, 2 Н), 3,64 (с, 3H), 1,87 (пентет, 2 Н),1,07 (т, 3H). Соединение 8 (н-бутиловый эфир 1,2-дигидро-4-гидрокси-5-хлор-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из соединения В нагреванием в н-бутаноле при 100C в течение ночи и добавлением разбавленной соляной кислоты для осаждения соединения 8. 1 Н ЯМР (CDCl3) 15,08 (с, 1 Н),7,50 (т, 1H), 7,28 (д, 1 Н), 7,24 (д, 1 Н), 4,43 (т, 2 Н), 3,64 (с, 3H), 1,82 (пентет, 2 Н), 1,52 (секстет, 2 Н), 0.98(т, 3H). Соединение 4 (метиловый эфир 1,2-дигидро-4-гидрокси-5-этил-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из 2-амино-6-этилбензойной кислоты согласно схеме 1 и тому, как описано для соединения 6 в Wennerberg et al., Org. Process, ResDev., 2007, 11, 674-680. 1H ЯМР (CDCl3) 14,9(с, 1 Н), 7,57 (т, 1 Н), 7,22 (д, 1 Н), 7,08 (д, 1H), 4,06 (с, 3H), 3,68 (с, 3H), 3,27 (к, 2 Н), 1,31 (т, 3H). Соединение 10 (этиловый эфир 1,2-дигидро-4-гидрокси-5-этил-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из соединения А кипячением с обратным холодильником в этаноле в течение ночи и добавлением холодной разбавленной соляной кислоты для осаждения соединения 10. 1 Н ЯМР (CDCl3) 15,02 (с, 1 Н), 7,53 (т, 1 Н), 7,18 (д, 1 Н), 7,04 (д, 1 Н), 4,50 (к, 2 Н), 3,64 (с, 3H), 3,25 (к, 2 Н),1,48 (т, 3H), 1,28 (т, 3H). Соединение 11 (метиловый эфир 1,2-дигидро-4-гидрокси-5-метокси-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из 2-метиламино-6-метоксибензойной кислоты (патент США 6133285) согласно схеме 1 и тому, как описано для соединения 6 в Wennerberg et al., Org. Process, ResDev., 2007,11, 674-680. 1H ЯМР (CDCl3) 13,8 (с, 1 Н), 7,57 (т, 1H), 6,93 (д, 1H), 6,73 (д, 1 Н), 4,02 (с, 3H), 4,01 (с, 3H),3,63 (с, 3H). Соединение 9 (изопропиловый эфир 1,2-дигидро-4-гидрокси-5-хлор-1-метил-2-оксохинолин-3 карбоновой кислоты) получают из соединения В кипячением с обратным холодильником в 2-пропаноле в течение ночи и добавлением разбавленной соляной кислоты для осаждения соединения 9. 1 Н ЯМР(CDCl3) 15,2 (с, 1 Н), 7,51 (т, 1H), 7,28 (д, 1 Н), 7,24 (д, 1 Н), 5,37 (септет, 1 Н), 3,67 (с, 3H), 1,47 (д, 6 Н). Пример 1. Получение соединения А (п.17). Смесь 4 (5,00 г) и N-этиланилина (4,7 г) в н-гептане (200 мл) кипятят в экстракторе Сокслета (фиг. 1), содержащем молекулярные сита 4 (22,9 г). Кипячение прекращают через 2,0 ч и смесь охлаждают до комнатной температуры. Суспензию кристаллов фильтруют. Осадок промывают н-гептаном и сушат в вакууме с получением 5,53 г (82%) N-этил-N-фенил-5-этил-1,2-дигидро-4-гидрокси-1-метил-2 оксохинолин-3-карбоксамида (А). Анализ выделенного продукта методом 1 Н-ЯМР показывает 2% остаточного сложного эфира. 1 Н-ЯМР (d-ДМСО), все пики уширенные; 11,1 (1 Н), 7.41 (1 Н), 7,29 (2 Н), 7,21(3H), 7,14 (1 Н), 6,96 (1H), 3,80 (2 Н), 3,42 (3H), 3,08 (2 Н), 1,07 (3H), 1,06 (3H). Когда ту же реакцию выполняли с традиционной отгонкой из н-гептана (п.22) в течение 2 ч согласно уровню техники (патент США 6875869), продукт извлекали с выходом 85% (относительно соединения А) и методом 1 Н-ЯМР обнаруживали смесь соединения А (75%) и сложного эфира, используемого в качестве исходного материала (25 мол.%). Пример 2. Получение соединения В (п.2). Смесь 6 (5,00 г) и N-этиланилина (5,0 г) в н-гептане (150 мл) кипятят в течение 4,0 ч в экстракторе Сокслета, содержащем молекулярные сита 4 (22,9 г). После охлаждения смеси продукт извлекают так,как описано выше, и получают 6,54 г (98%) N-этил-N-фенил-5-хлор-1,2-дигидро-4-гидрокси-1-метил-2 оксохинолин-3-карбоксамида (В). 1 Н-ЯМР анализ выделенного продукта показал отсутствие примесей. 1 Н-ЯМР (CDCl3) 12,6 (с, 1 Н), 7,41 (т, 1 Н), 7,08-7,26 (м, 7 Н), 3,98 (к, 2 Н), 3,30 (с, 3H), 1.22 (т, 3H). Пример 3. Получение соединения В (п.3). Смесь 6 (5,00 г) и N-этиланилина (5,0 г) в н-гептане (150 мл) кипятят в течение 4,0 ч в экстракторе Сокслета, содержащем дигидрат хлорида кальция (хлопья, предназначенные для осушения, 22,0 г). После охлаждения смеси продукт извлекают так, как описано выше, и получают 6,20 г (93%) N-этил-N-фенил 5-хлор-1,2-дигидро-4-гидрокси-1-метил-2-оксохинолин-3-карбоксамида (В). Анализ методом 1 Н-ЯМР выделенного продукта показал 1% остаточного сложного эфира. Пример 4. Получение соединения С (п.25). Смесь 11 (5,00 г, 18,9 ммоль), N-метил-п-трифторметиланилина (5,13 г, 28,4 ммоль) и н-октана (200 мл) кипятят в экстракторе Сокслета, содержащем молекулярные сита 4 (22,9 г), в течение 2 ч. После охлаждения смеси продукт извлекают так, как описано выше, и получают 7,6 г (99%) 4-гидрокси-5 метокси-N,1-диметил-2-оксо-N-[(4-трифторметил)фенил]-1,2-дигидрохинолин-3-карбоксамида (С). Анализ методом 1 Н-ЯМР выделенного продукта не показал иных примесей, кроме 1 мол.% остаточного сложного эфира 11. 1 Н-ЯМР (CDCl3) 9,9 (с, 1 Н), 7,50 (ушс, 4 Н), 7,46 (т, 1H), 6,94 (д, 1 Н), 6,70 (д, 1 Н), 4,06(с, 3H), 3,54 (с, 3H), 3,48 (с, 3H). Когда такую же реакцию выполняли с традиционной отгонкой из н-октана (п.26) в течение 2 ч согласно уровню техники (патент США 6875869), продукт извлекали с выходом 94% и анализом методом 1 Н-ЯМР определяли смесь, состоящую из соединения С (96 мол.%) и исходного материала 11 (4 мол.%). Пример 5. Крупномасштабное получение соединения А. В крупномасштабном получении паквинимода используют установку, показанную на фиг. 2. В футерованный стеклом реактор через люк загружают 4 (11,6 кг) и затем добавляют н-октан (212 кг) и нэтиланилин (13,4 кг). Смесь нагревают до температуры кипения, т.е. 125C. н-Октан отгоняют в стеклянную сферу (156) при атмосферном давлении. Когда объем становится 70 л, дистиллят в 156 перекачивают насосом через рукавный фильтр (194), заполненный молекулярными ситами 4 (7,5 кг). Дистилляцию продолжают на протяжении операции. Дистиллят подают на рецикл обратно в реактор, а также в стеклянную сферу для обеспечения непрерывного потока через фильтр. Через 7 ч смесь охлаждают до 60C. Проводят контроль за процессом (IPC) для оценки конверсии согласно спецификации. Сразу же после отбора образцов смесь нагревают до температуры кипения. Дистилляцию и рециркуляцию продолжают через второй рукавный фильтр (195), заполненный молекулярными ситами (7,5 кг). Так как первый образец не был одобрен, отбирали второй образец после дополнительной рециркуляции в течение 4,5 ч. Образец 2 был признан соответствующим спецификации. Результаты приведены в табл. 2. Таблица 2 Результаты IPC Дополнительную дистилляцию и рециркуляцию через третий рукавный фильтр (196), заполненный молекулярными ситами (7 кг), начинают до получения результатов анализа IPC. Так как результат оказался удовлетворительным, рециркуляцию прерывают. Дистилляцию продолжают до установленного в реакторе объема (11010 л). В другой операции получения А с использованием способа из уровня техники в реактор загружают 4 (6,3 кг), н-октан (124 кг) и н-этиламин (6,9 кг). После отгонки 88 кг растворителя в течение 16 ч IPC показывает, что осталось 2,7% 4. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения соединения формулы (I)R1 представляет собой этил, R2 представляет собой этил и R3 представляет собой Н; илиR1 представляет собой хлор, R2 представляет собой этил и R3 представляет собой Н; илиR1 представляет собой метокси, R2 представляет собой метил и R3 представляет собой трифторметил; содержащий стадии, на которых: в которой R1 представляет собой этил, хлор или метокси и R4 представляет собой (С 1-С 4)алкил,вводят в реакцию с соединением формулы (III) в которой R2 представляет собой этил и R3 представляет собой Н; или R2 представляет собой метил и R3 представляет собой трифторметил; при кипячении в смеси, содержащей алифатический растворитель или смесь алифатических растворителей, причем указанный(е) алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 68-191C;(ii) пары кипящей смеси конденсируют;(iii) конденсированные пары обрабатывают поглотителем спирта, выбранным из молекулярных сит,или поглотителем спирта, который представляет собой смесь молекулярных сит; и(iv) конденсированные пары возвращают в реакционную смесь. 2. Способ по п.1, в котором алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 80-150C. 3. Способ по п.1, в котором алифатический(е) растворитель(и) имеет(ют) температуру кипения в интервале 95-130C. 4. Способ по п.1, в котором поглотитель спирта выбран из молекулярных сит 3, 4, 5, 13 Х или представляет собой смесь любых из указанных молекулярных сит. 5. Способ по любому из пп.1-4, в котором алифатический(е) растворитель(и) выбирают из разветвленных или линейных алканов и циклоалканов С 6-С 10. 6. Способ по любому из пп.1-5, в котором алифатический(е) растворитель(и) выбирают из разветвленных или линейных алканов и циклоалканов С 7-С 8. 7. Способ по п.6, в котором алифатический(е) растворитель(и) выбирают из н-гептана, н-октана, метилциклогексана, 2,2,4-триметилпентана и циклооктана. 8. Способ по п.7, в котором алифатический(е) растворитель(и) выбирают из н-гептана и н-октана. 9. Способ по любому из пп.1-8, в котором R4 выбирают из метила, этила, н-пропила, изопропила и н-бутила. 10. Способ по п.9, в котором R4 выбирают из метила и этила. 11. Способ по п.1, в котором R1 представляет собой этил, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил или этил; поглотитель спирта представляет собой молекулярные сита 3, 4, 5 или 13 Х или представляет собой их смесь и алифатический(е) растворитель(и) выбирают из н-гептана и н-октана. 12. Способ по п.1, в котором R1 представляет собой хлор, R2 представляет собой этил, R3 представляет собой Н, R4 представляет собой метил, поглотитель спирта представляет собой молекулярные сита 3, 4, 5 или 13 Х и алифатический(е) растворитель(и) выбирают из н-гептана и н-октана. 13. Способ по п.1, в котором R1 представляет собой метокси, R2 представляет собой метил, R3 представляет собой трифторметил, R4 представляет собой метил или этил; поглотитель спирта представляет собой молекулярные сита 3, 4, 5 или 13 Х или представляет собой их смесь и алифатический растворитель представляет собой н-октан.
МПК / Метки
МПК: C07D 215/56
Метки: получения, хинолин-3-карбоксамидов, способ
Код ссылки
<a href="https://eas.patents.su/12-21171-sposob-polucheniya-hinolin-3-karboksamidov.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения хинолин-3-карбоксамидов</a>
Предыдущий патент: Соединения, модулирующие андрогеновые рецепторы
Следующий патент: Держатель интраокулярной линзы
Случайный патент: Способ лечения синдрома дефицита внимания/гиперактивности