Производные розувастатина
Номер патента: 20591
Опубликовано: 30.12.2014
Авторы: Хайндли Стивен, Джексон Питер, Линдсэй Дерек, Бхамра Индер
Формула / Реферат
1. Соединение формулы (I) и его фармацевтически приемлемые соли и сольваты
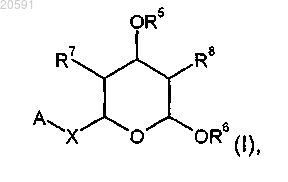
где А представляет собой
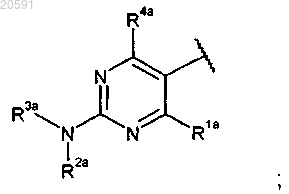
где R1a представляет собой изопропил;
R2a представляет собой -S(O)2Me;
R3a представляет собой метил и
R4a - 4-фторфенил;
R5 выбирают из группы, включающей водород, С1-6-алкил, С1-6-галоалкил, С2-6-алкенил, арил, С1-6-алкиларил и С1-6-алканоилгетероарил;
R6 выбирают из группы, состоящей из С2-6-алкила, С2-6-алкенила и арила;
R7 и R8 представляют собой Н;
X представляет собой -(CRaRb)m(CRa=CRb)n(CRaRb)o-, где Ra и Rb представляют собой Н и m, n и о независимо равны 0 или 1; и
где арильные группы включают ароматические циклические системы, содержащие 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 атомов углерода в цикле;
гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы;
каждая из указанных групп R5 и R6 может быть, если это возможно химически, независимо и необязательно замещена 1-5 группами, которые выбирают независимо в каждом случае из групп, включающих галоген,
C1-3-алкил, C1-3-галоалкил, C1-3-алкокси, C1-3-галоалкокси, гидрокси и циано.
2. Соединение по п.1, в котором R5 выбирают из группы, включающей водород, С1-6-алкил, арил, С1-6-алкиларил и С1-6-алканоилгетероарил.
3. Соединение по п.2, в котором R5 является водородом.
4. Соединение по п.2, в котором R5 выбирают из группы, включающей -C1-алкил-Ph, -C2-алкил-Ph,
-C3-алкил-Ph и -С4-алкил-Ph.
5. Соединение по п.4, в котором R5 является бензилом.
6. Соединение по п.2, в котором R5 является C1-6-алканоилпиридином.
7. Соединение по п.6, в котором R5 является 3-метаноилпиридином.
8. Соединение по любому из предшествующих пунктов, в котором R6 выбирают из группы, включающей
С2-6-алкил и С2-6-алкенил.
9. Соединение по п.8, в котором R6 выбирают из группы, включающей этил, пропил, бутил и пропилен.
10. Соединение по любому из предшествующих пунктов, в котором R6 представляет необязательно замещенный арил.
11. Соединение по п.10, в котором R6 выбирают из группы, включающей С1-6-алкоксизамещенный фенил и галогензамещенный фенил.
12. Соединение по п.10, в котором R6 выбирают из группы, включающей 2,4,6-трифторфенил и 2,4-диметоксифенил.
13. Соединение по п.8, в котором R6 выбирают из группы, включающей этил, пропил, бутил и аллил.
14. Соединение по п.1, в котором R5 представляет водород и R6 является арильной группой.
15. Соединение по п.1,
в котором R5 является бензилом и R6 является С2-6-алкилом или С2-6-алкенилом; или
R5 представляет собой С1-6-алканоилгетероарил и R6 представляет собой С2-6-алкил; или
R5 является водородом и R6 является С2-6-алкилом или арилом.
16. Соединение по любому из предшествующих пунктов, в котором m=0, n=1 и o=0.
17. Соединение по любому из пп.1-16, в котором m=1, n=0 и о=1.
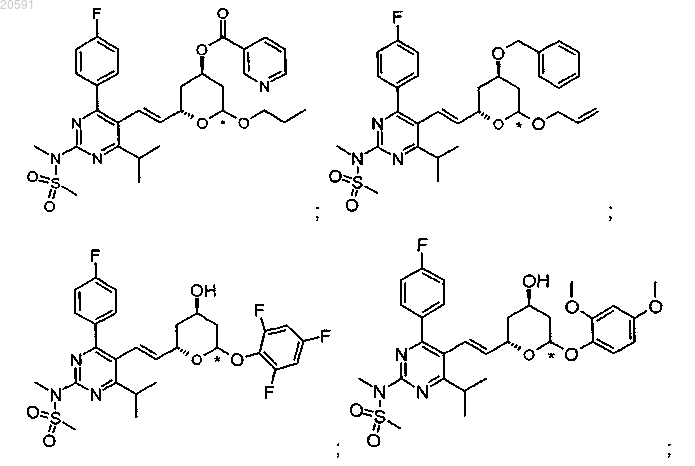
18. Соединение по п.1 со структурой, которую выбирают из
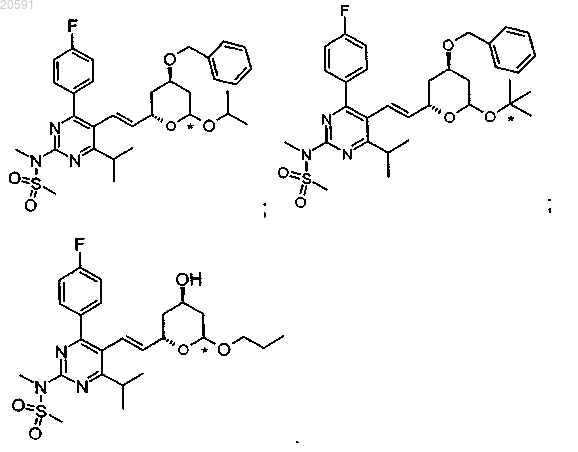
Текст
Изобретение относится к аналогам розувастатина общей формулы (I) и их фармацевтически приемлемым солям и сольватам а остальные заместители имеют значения, приведенные в описании. Соединения изобретения активны в ингибировании фермента 3-гидрокси-3-метилглютарил-коэнзим А редуктазы (редуктазыHMG-CoA) и могут быть использованы для лечения болезненных состояний, которые модулируются редуктазой HMG-CoA.(71)(73) Заявитель и патентовладелец: РЕДКС ФАРМА ЛИМИТЕД (GB) Область техники, к которой относится изобретение Настоящее изобретение относится к новым лактольным производным розувастатина. Сведения о предшествующем уровне техники Розувастатин - 7-[4-(4-фторфенил)-6-(1-метилэтил)-2-(метилметансульфон-амидо)пиримидин-5-ил]3,5-диоксигептен-6-оевая кислота - и его применение для ингибирования биосинтеза холестерина были впервые описаны в ЕР 0521471. Розувастатин является сильным ингибитором фермента HMG-CoA. Транс-6-[2-(3- или 4-карбоксамидопиррол-1-ил)алкил]-4-оксипиран-2-оны являются лактонами, которые впервые были описаны в патенте США 4681893. Однако сами по себе лактоны, по-видимому, не активны. Соответствующие эквивалентные кислоты с разомкнутым циклом используют в качестве ингибиторов биосинтеза холестерина благодаря их активности по отношению к HMG-CoA. В патенте США 4681893 также приведены способы производства таких соединений. В работе Clin Invest Med, Volume 24, No 5, p. 258-72, 2001 (Baker and Tamopolsky) было обнаружено, что в то время как статины с открытой конформацией оксикислоты проявляют активность, его циклический аналог - лактон - не активен. Протекающий в печени гидролиз при щелочном рН приводит к размыканию цикла и таким образом происходит in vivo активация лактоновых пролекарств ловастатина и симвастатина путем образования активных форм с разомкнутым циклом. Однако проблема таких соединений состоит в том, что экстенсивный пресистемный метаболизм приводит к быстрому выведению образующегося циклического статина из организма. Аналогично в работе Trends in Pharmacological Sciences, Volume 19, Issue 1, 1 January 1998, р. 26-37 описано, что лактоны, неактивные в ингибировании редуктазы HMG-CoA, должны подвергаться метаболизму в соответствующие разомкнутые формы оксикислот. С лактоном и его активной формой с разомкнутым циклом связаны также проблемы устойчивости в течение длительного периода времени. Эта проблема важна для производства главного активного вещества или при его длительном хранении в аптеке. Например, вследствие дегидратации может удаляться гидроксильная группа. Полученный продукт разложения может иметь двойную связь, сопряженную с карбонильной группой лактона, что облегчает процесс возможного разложения. Аналогично в случае формы с разомкнутым циклом один из возможных продуктов разложения может также содержать двойную связь, сопряженную с карбонильной группой кислоты. Сущность изобретения Поэтому целью настоящего изобретения является предложение новых фармацевтически активных лактольных производных розувастатина. Целью изобретения также является предложение соединений,обладающих повышенной устойчивостью. В идеале такие соединения должны иметь длительный срок годности при хранении. Целью данного изобретения является предложение соединений, которые можно получить синтетическими способами, пригодными для использования в промышленном масштабе. Изобретение также ставит целью предложить соединения, которые можно получать экономичным и надежным способом. Также целью являются соединения с хорошей растворимостью и/или биодоступностью. Данное изобретение предлагает соединения, с помощью которых можно решить одну или несколько из указанных задач. Согласно одному варианту настоящее изобретение предлагает соединение формулы (I) и его фармацевтически приемлемые соли и сольватыR3a представляет собой метил и где арильные группы включают ароматические циклические системы, содержащие 6, 7, 8, 9, 10, 11,12, 13, 14, 15 или 16 атомов углерода в цикле; гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы; каждая из указанных групп R5 и R6 может быть, если это возможно химически, независимо и необязательно замещена 1-5 группами, которые независимо выбирают из группы, включающей галоген,C1-3-алкил, C1-3-галоалкил, C1-3-алкоксил, C1-3-галоалкоксил, гидроксил и цианогруппу. Соединения по данному изобретению могут быть активны сами по себе или в некоторых случаях могут подвергаться размыканию цикла в физиологических условиях и образовывать соответствующие соединения, обладающие ингибирующей активностью. Сопровождающий чертеж иллюстрирует уровень концентрации триглицеридов в плазме крыс после введения розувастатина (перорально 25 мг/кг) и четырех аналогов розувастатина (25 мг/кг). Фармацевтически приемлемые соли соединений формулы (I) включают соли присоединения кислоты и соли присоединения основания. Подходящие соли кислот образуются из кислот, образующих нетоксичные соли. Примеры включают следующие соли: ацетат, бензоат, безилат, бикарбонат/карбонат, бисульфат/сульфат, борат, камсилат,цитрат, эдизилат, эзилат, формиат, фумарат, глюцептат, глюконат, глюкуронат, гексафторфосфат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидроиодид/иодид, изетионат, лактат, малат, малеат, малонат, мезилат, метилсульфат, нафтилат, 1,5-нафталиндисульфонат, 2-напсилат, никотинат, нитрат, оротат, оксалат, пальмитат, памоат, фосфат/однозамещенный фосфат/двузамещенный фосфат, сахарат, стеарат, сукцинат, тартрат, тозилат и трифторацетат. Подходящие основные соли получают из оснований, которые образуют нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина, глицина,лизина, магния, меглюмина, оламина, калия, натрия, трометамина и цинка. Могут образоваться также частично замещенные соли кислот и оснований, например гемисульфат и частично замещенные соли кальция. Обзор пригодных солей см. "Handbook of Pharmaceutical Salts: Properties, Selection, and Use" byStahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002). Фармацевтически приемлемые соли соединений формулы (I) можно получить одним или несколькими из трех способов:(i) по реакции соединения формулы (I) с соответствующей кислотой или основанием;(ii) путем удаления кислотной или основной лабильной защитной группы из подходящего предшественника соединения формулы (I) или раскрытия цикла в подходящем циклическом предшественнике,например лактоне или лактаме, с помощью соответствующей кислоты или основания или(iii) путем превращения одной соли соединения формулы (I) в другую по реакции с соответствующей кислотой или основанием или с использованием подходящей ионообменной колонки. Все три реакции обычно проводят в растворе. Полученную соль можно осадить и выделить путем фильтрации или выпаривания растворителя. Степень ионизации полученной соли может варьироваться от полной ионизации до почти неионизованной формы. Соединения по данному изобретению могут существовать как в несольватированной, так и в сольватированной форме. Термин "сольват" использован здесь для описания молекулярного комплекса,включающего соединение по изобретению и стехиометрическое количество одной или нескольких молекул фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" используют, когда указанным растворителем является вода. В объем настоящего изобретения включены также комплексы типа клатратов, т.е. комплексы включения лекарство-хозяин, в котором в отличие от указанных выше сольватов лекарство и хозяин присутствуют в стехиометрическом или нестехиометрическом количествах. Также включены комплексы лекарства, содержащие два или несколько органических и/или неорганических компонентов, которые могут присутствовать в стехиометрическом или нестехиометрическом количествах. Полученные комплексы могут быть ионизированными или неионизированными. Обзор таких комплексов см. J. Pharm. Sci, 64 (8),1269-1288 by Haleblian (August 1975). Далее все ссылки на соединения формулы (I) включают ссылки на соли, сольваты и их комплексы,сольваты и комплексы их солей. Соединения по данному изобретению включают указанные выше соединения формулы (I), в том числе их полиморфные модификации и кристаллические формы, пролекарства и изомеры (включая оптические, геометрические изомеры и таутомерные формы), как указано ниже, и изотопно меченные соединения формулы (I). Соединения по настоящему изобретению могут существовать перед очисткой в виде смеси энантиомеров в зависимости от метода синтеза. Например, соединения по данному изобретению могут существовать в виде смеси энантиомеров с соотношением от 2:1 до 3:1, хотя могут быть и другие соотношения. Энантиомеры можно разделить известными специалистам традиционными методами. Таким образом, данное изобретение включает индивидуальные энантиомеры, а также их смеси. В случае, когда опи-2 020591 санные здесь химические структуры включают символ , это означает, что присутствует смесь энантиомеров с соотношением от 2:1 до 3:1. На некоторых стадиях в способе получения соединений (I) бывает необходимо защитить потенциально реакционноспособные группы, которые нежелательно вводить в реакции, и в дальнейшем удалить такие защитные группы. В таком случае можно использовать любые совместимые защитные радикалы. В качестве конкретных способов защиты и снятия защиты можно использовать способы, описанные T.W.(Protecting groups, Georg Thieme Verlag, 1994). Все вышеуказанные реакции и способы получения новых исходных веществ, использованные в предшествующих способах, являются традиционными, и соответствующие реагенты и условия реакций для их осуществления, а также методики выделения целевых продуктов хорошо известны специалистам в данной области, знакомым с литературными прецедентами и примерами получения. Кроме того, соединения формулы (I) так же, как промежуточные соединения в их синтезе, можно очищать разными хорошо известными способами, например кристаллизацией или хроматографией. Авторы установили, что соединения по данному изобретению весьма активны в ингибированииHMG-CoA. Эти соединения слаборастворимы в воде и доступны для метаболизма. В этом отношении,несмотря на присутствие объемной группы во 2 положении лактольного производного, соединения все же подвергаются метаболизму в результате потери заместителя, окислению и последующему раскрытию цикла с образованием ингибиторов HMG-CoA. Кроме того, эти соединения обладают собственной активностью. Оба эти вывода оказались неожиданными и парадоксальными. Поэтому можно ожидать, что эти соединения продемонстрируют более устойчивый профиль высвобождения in vivo. Также можно ожидать, что эти соединения будут обладать более длительным периодом полупревращения и/или увеличенным периодом действия. Удивительно, но предполагалось, что эти типы соединений с закрытым циклом вообще не активны Кроме того, можно ожидать, что присутствие заместителя окажется препятствием к окислению и последующему превращению в активное соединение путем раскрытия цикла. В одном варианте R6 выбирают из группы, включающей C2-6-алкил, C2-6-алкенил и арил. В одном варианте А представляет собой В одном варианте R5 выбирают из группы, включающей водород, С 1-6-алкил, арил, С 1-6-алкиларил и С 1-6-алканоилгетероарил. В другом варианте R5 выбирают из группы, включающей: водород и С 1-6-алкиларил. В другом варианте R5 представляет С 1-6-алкиларил. В еще одном варианте R5 представляет С 1-6-алканоилгетероарил, например метаноилгетероарил. В предпочтительном варианте R5 представляет метаноилпиридил, например 2-метанолилпиридин, 3-метанолилпиридин или 4-метанолилпиридин,предпочтительно 3-метанолилпиридин. В другом варианте R5 является водородом. В альтернативном варианте R5 является бензилом. В одном варианте R6 выбирают из группы, включающей С 2-6-алкил, С 2-6-алкенил и арил. В одном варианте R6 является С 2-6-алкилом. В другом варианте R6 представляет этил, пропил, изопропил, бутил, втор-бутил, изобутил или трет-бутил. В одном варианте R6 представляет изопропил или трет-бутил. В одном варианте R6 представляет собой С 2-6-алкенил. В еще одном варианте R6 представляет собой проп-2-ен. В одном варианте R6 представляет собой необязательно замещенный арил. В еще одном варианте 6R является 2,4,6-трифторфенилом или 2,4-диметоксифенилом. В одном варианте m=0, n=1 и o=0. В другом варианте m=1, n=1 и o=0 или m=0, n=1 и o=1. В следующем варианте n равно 0. В еще одном варианте m=1, n=0 и о=1. В еще одном варианте m=1, n=0 иo=0. В предпочтительном варианте X представляет собой В альтернативном предпочтительном варианте X представляет собой Предпочтительно, чтобы одна или несколько указанных групп были замещенными, причем каждый необязательный заместитель является независимо выбранным атомом галогена. Среди них предпочтительны хлор и фтор.R1a представляет собой изопропил; R2a представляет собой -S(O)2R9a, где R9a представляет собой метил; R3a представляет собой метил и R4a представляет собой 4-фторфенил. В одном варианте R5 представляет собой водород или бензил и R6 представляет собой С 2-6-алкил,предпочтительно пропил или бутил, или C2-6-алкенил, предпочтительно проп-2-енил. В предпочтитель-3 020591 ном варианте R5 представляет собой бензил и R6 является С 2-6-алкилом, предпочтительно пропилом, изопропилом, бутилом, изобутилом или трет-бутилом. В предпочтительном варианте R5 представляет собой бензил и R6 представляет собой С 2-6-алкенил, предпочтительно проп-2-енил. В предпочтительном варианте R5 представляет собой водород и R6 является необязательно замещенным арилом, предпочтительно 2,4,6-трифторфенилом или 2,4-диметоксифенилом. В предпочтительном варианте R5 представляет собой водород и R6 является С 2-6-алкилом, предпочтительно н-пропилом. В другом предпочтительном вариантеR5 представляет собой метаноилпиридил, например 2-метанолилпиридин, 3-метанолилпиридин или 4 метанолилпиридин, предпочтительно 3-метанолилпиридин, и R6 является С 2-6-алкилом, предпочтительно этилом или пропилом. Арильные группы включают ароматические циклические системы, содержащие 6, 7, 8, 9, 10, 11, 12,13, 14, 15 или 16 атомов углерода в цикле. Арильные группы могут содержать один цикл, но могут включать полициклические системы с двумя или несколькими циклами, из которых по меньшей мере один является ароматическим. Арильные группы включают фенил, нафтил, флуоренил, азуленил, инденил и антрил. В одном варианте арильная группы представляет собой фенил. Гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы. Такая группа может представлять собой полициклическую систему с двумя или несколькими циклами, из которых по меньшей мере один цикл является ароматическим, но чаще это бывает моноциклическая система. Предпочтительными являются моноциклические гетероарильные группы, содержащие 5-6 атомов в цикле. Гетероарильные группы включают пирролил,пиразолил, имидазолил, пиразинил, оксазолил, изоксазолил, тиазолил, фурил, тиофенил, пиридил, пиримидил, бензимидазолил, индолил, изохинолил, хиноксалинил и хинолил. В одном варианте гетероарильную группу выбирают из группы, включающей пиридин, пиримидин,пиразин, пиразол и оксазол. Предпочтительной гетероарильной группой является пиридин. В одном варианте соединение имеет структуру, которую выбирают из следующих: Способы получения соединений по настоящему изобретению описаны в WO2005/012246, в частности в примерах. Описание патента WO2005/012246 в отношении методик синтеза составляет часть описания настоящего изобретения. Для краткости подробности этих методик синтеза не воспроизводятся здесь, но включены ссылкой в описание этого документа. Помимо указанных вариантов настоящее изобретение также относится к применению лактольных производных розувастатина в производстве препаратов для лечения некоторых заболеваний. С помощью соединений по настоящему изобретению можно лечить болезненные состояния, которые модулируются ферментом 3-гидрокси-3-метилглютарил-коэнзим А редуктазой (редуктазой HMG-CoA). Поэтому ингибирование этого фермента представляет собой важную терапию многих заболеваний. Примеры болезненных состояний, которые можно лечить ингибированием редуктазы HMG-CoA,включают гиперхолестеринемию, атеросклероз и гиперлипидемию. Статины используют для вторичной профилактики сердечно-сосудистых заболеваний или для первичного предотвращения сердечнососудистых заболеваний, когда возрастает риск сердечно-сосудистых заболеваний. Поэтому ожидается,что соединения по настоящему изобретению найдут применение в лечении или профилактике сердечнососудистых заболеваний благодаря их ингибиторной активности. Примеры сердечно-сосудистых заболеваний, которые можно лечить соединениями по настоящему изобретению, включают ишемическую бо-4 020591 лезнь сердца, инфаркт миокарда, инсульт и болезни периферических артерий. Кроме того, эти соединения могут быть весьма полезны в лечении воспалений, деменции, рака, ядерной катаракты, диабета и гипертонии. Болезненные состояния, которые можно лечить путем ингибирования редуктазы HMG-CoA, могут наблюдаться у человека и животных. Эти соединения особенно предназначены для людей. Настоящее изобретение также включает синтез всех фармацевтически приемлемых изотопно меченных соединений формулы (I), в которых один или несколько атомов замещены атомами с тем же атомным номером, но атомной массой или массовым числом, отличными от атомной массы или массового числа, обычно встречающихся в природе. Примеры пригодных для введения изотопов в соединения по данному изобретению включают изотопы водорода, такие как 2 Н и 3 Н, углерода, такие как 11 С, 13 С и 14 С, хлора, такие как 36Cl, фтора, такие как 18F, иода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15 О, 17 О и 18 О, фосфора,такие как 32 Р, и серы, такие как 35S. Некоторые меченные изотопами соединения, например, такие, которые включают радиоактивный изотоп, полезны при изучении распределения лекарства и/или тканей субстрата. Особенно полезны для этой цели радиоактивные изотопы: тритий, т.е. 3 Н, и углерод-14, т.е. 14 С, ввиду легкости их введения и детектирования. Замещение более тяжелыми изотопами типа дейтерия, т.е. 2 Н, может иметь некоторые терапевтические преимущества, обусловленные повышенной метаболической устойчивостью, например повышенным временем полупревращения in vivo или пониженным требованием к дозе, и, следовательно, при некоторых обстоятельствах может быть предпочтительным. Замещение позитрон-активными изотопами, такими как 11 С, 18F, 15O и 13N, можно использовать для исследования степени занятости рецептора субстратом методом позитронной эмиссионной томографии(ПЭТ). Меченные изотопами соединения обычно можно синтезировать традиционными методами, известными специалистам в данной области, или способами, аналогичными описанным, с применением соответствующих меченных изотопами реагентов вместо применявшихся раньше немеченых реагентов. Во всем описании и формуле единственное число охватывает множественное, если контекст не требует другого. В частности, при использовании неопределенного артикля описание следует понимать как включающее множественность так же, как единственность, если контекст не требует иного. Признаки, целые числа, характеристики, соединения, химические фрагменты или группы, описанные в связи с конкретным аспектом, вариантом или примером изобретения, следует понимать как применимые к любому другому описанному здесь аспекту, варианту или примеру, за исключением случая их несовместимости. Сведения, подтверждающие возможность осуществления изобретения Общая методика Все анализы проводили в реакционном буфере, содержащем 100 нМ KxPO4 при рН 7.2, 1 мМ ЭДТА,500 мМ KCl и 1 мг/мл BSA. Концентрации каждого из NADPH и HMG-CoA составляли 200 мкМ. Концентрация используемого фермента не известна, хотя эта концентрация в 10 раз ниже концентрации исходного продажного раствора. Ингибиторы растворяли в 75% ДМСО. Когда было установлено, что ингибиторы не растворяются или только частично растворяются в 75% ДМСО, использовали 100% ДМСО. Реакцию активировали путем добавления фермента и после добавления встряхивали в течение 12 с. Затем каждые 20 с следили за поглощением в течение 600 с. В начальных тестах концентрацию каждого ингибитора устанавливали на уровне 50 нМ для идентификации лучших ингибиторов по сравнению с известным ингибитором правастатином. После такой идентификации анализы проводили, варьируя их концентрации от 0 до 50 нМ, и рассчитывали величины IC50. Пример 1. Применяли следующую методику с использованием набора для анализа редуктазы HMG-CoA отSigma-Aldrich (номер в каталоге CS1090). Анализ основан на спектрофотометрическом определении уменьшения поглощения при 340 нм от NADPH в растворе. Уменьшение поглощения вызвано окислением NADPH под действием каталитической субъединицы HMGR в присутствии субстрата HMG-CoA. Эффективное ингибирование HMG-CoA ведет к уменьшению окисления NADPH, которое, в свою очередь, ведет к меньшему снижению поглощения при 340 нм во времени. Это проиллюстрировано следующей схемой реакции:HMG-CoA+2NADPH+2 Н+мевалонат+2NADPCoA-SH. Соединениями, проявляющими наилучшую ингибирующую активность, являются те, которые минимально уменьшают поглощение. Приготовление раствора для анализа. Для приготовления реагентов и во время опытов использовали воду сверхвысокой чистоты (с удельным сопротивлением 17 M-см или е эквивалент). Вначале приготовили буферный раствор следующим образом: 0.2 мл аналитического буферного раствора (номер в каталоге А 5981) 5-кратного с помощью 0.8 мл сверхчистой воды. Полученный буферный раствор для дальнейшего использования держали на льду или хранили при -20 С. Затем 25 мг NADPH (номер в каталоге N6505) разбавили 1.5 мл буферного раствора. Рабочие дозы полученного раствора NADPH хранили при -20 С. В течение всего анализа раствор субстрата HMG-CoA (номер в каталоге S7447), редуктазу HMGCoA (номер в каталоге Н 8789) и раствор ингибитора (например, правастатина, номер в каталоге I5909) держали на льду. 1. Перед началом анализа на спектрофотометре установили кинетическую программу: 37 С, мониторинг при 340 нм, 1 мл образца, замер через каждые 20 с в течение 10 мин. 2. Добавили соответствующие объемы реакционных растворов согласно табл. 1 (1 мл анализ). Таблица 1 Объемы реакции на 1 мл образца Реагенты добавляли в следующем порядке: а) добавить буферный раствор ко всем образцам;b) добавить ингибитор (тестируемое соединение/правастатин) к ингибируемому образцу; с) добавить разбавленный раствор NADPH ко всем образцам;d) добавить раствор субстрата (HMG-CoA) ко всем образцам; е) добавить редуктазу HMG-CoA (HMGR) к активным и ингибируемым образцам;f) тщательно смешать образцы. 3. Сразу запустили кинетическую программу. Активность продукта рассчитывали по следующему уравнению: Пример 2. В следующей таблице приведены величины IC50 для конкретных соединений розувастатина по настоящему изобретению: Пример 4. Следующий пример демонстрирует эффективность соединений розувастатина по данному изобретению. Пример демонстрирует эффект лечения дважды в день в течение 3-5 суток четырьмя соединениями розувастатина по настоящему изобретению и розувастатином (все по 25 мг/кг перорально) на уровень триглицеридов в плазме крыс через 16 ч после последнего приема дозы. Считается, что определение изменения в уровне триглицеридов в плазме крыс является хорошим тестом на активность редуктазы(свет включали в 07.00 ч) и свободном доступе к пище (обычная лабораторная еда) и воде. Животные массой 148-183 г были распределены по 8 особей на испытуемые группы по массе тела и тестирование выравнивали по клеткам. Четыре аналога розувастатина были приготовлены в растворе 10% PEG300/10% кремафор/80% метилцеллюлоза (0.5%) (носитель 1) с концентрацией 5 мг/мл. Использовали следующие соединения розувастатина: н-пропилацеталь розувастатин лактола (диастереомерное соотношение 2/1)(BPL001); никотиноиловый эфир н-пропилацеталя розувастатин лактола (диастереомерное соотношение 2/1)(BPL002); бензиловый эфир изопропилацеталя розувастатин лактола (BPL003) и никотиноиловый эфир метилацеталя розувастатин лактола (диастереомерное соотношение 2/1)(BPL004). Приготовили препарат розувастатина с 0.5% Tween в 0.5% растворе метилцеллюлозы (носитель 2) в виде суспензии с концентрацией 5 мг/кг. Крысам вводили перорально носитель 1, один из четырех аналогов розувастатина в носителе 1 (25 мг/кг), носитель 2 или розувастатин в носителе 2 (25 мг/кг перорально) дважды в сутки в течение 3-5 дней. Через 16 ч после введения последней дозы взяли последние образцы плазмы, выдержали при -20C и перенесли на сухом льду для анализа на уровень триглицеридов. Для каждой временной точки проводили однофакторный дисперсионный анализ (1-факторныйANOVA) и апостериорный тест Даннетта. Результаты представлены на фиг. 1, из которых следует, что введение розувастатина (25 мг/кг перорально) дважды в сутки в течение 3-5 дней вызывает заметное уменьшение содержания триглицеридов в плазме. Все четыре аналога розувастатина также значительно уменьшили содержание триглицеридов в плазме после введения препарата дважды в сутки в течение 3-5 дней. Все животные хорошо переносили обработку розувастатином без признаков отрицательных эффектов. Эффект от аналогов розувастатина был эквивалентен эффекту от розувастатина. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) и его фармацевтически приемлемые соли и сольватыR3a представляет собой метил иX представляет собой -(CRaRb)m(CRa=CRb)n(CRaRb)o-, где Ra и Rb представляют собой Н и m, n и о независимо равны 0 или 1; и где арильные группы включают ароматические циклические системы, содержащие 6, 7, 8, 9, 10, 11,12, 13, 14, 15 или 16 атомов углерода в цикле; гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы; каждая из указанных групп R5 и R6 может быть, если это возможно химически, независимо и необязательно замещена 1-5 группами, которые выбирают независимо в каждом случае из групп, включающих галоген, C1-3-алкил, C1-3-галоалкил, C1-3-алкокси, C1-3-галоалкокси, гидрокси и циано. 2. Соединение по п.1, в котором R5 выбирают из группы, включающей водород, С 1-6-алкил, арил,С 1-6-алкиларил и С 1-6-алканоилгетероарил.-9 020591 3. Соединение по п.2, в котором R5 является водородом. 4. Соединение по п.2, в котором R5 выбирают из группы, включающей -C1-алкил-Ph, -C2-алкил-Ph,-C3-алкил-Ph и -С 4-алкил-Ph. 5. Соединение по п.4, в котором R5 является бензилом. 6. Соединение по п.2, в котором R5 является C1-6-алканоилпиридином. 7. Соединение по п.6, в котором R5 является 3-метаноилпиридином. 8. Соединение по любому из предшествующих пунктов, в котором R6 выбирают из группы, включающей С 2-6-алкил и С 2-6-алкенил. 9. Соединение по п.8, в котором R6 выбирают из группы, включающей этил, пропил, бутил и пропилен. 10. Соединение по любому из предшествующих пунктов, в котором R6 представляет необязательно замещенный арил. 11. Соединение по п.10, в котором R6 выбирают из группы, включающей С 1-6-алкоксизамещенный фенил и галогензамещенный фенил. 12. Соединение по п.10, в котором R6 выбирают из группы, включающей 2,4,6-трифторфенил и 2,4 диметоксифенил. 13. Соединение по п.8, в котором R6 выбирают из группы, включающей этил, пропил, бутил и аллил. 14. Соединение по п.1, в котором R5 представляет водород и R6 является арильной группой. 15. Соединение по п.1,в котором R5 является бензилом и R6 является С 2-6-алкилом или С 2-6-алкенилом; илиR5 является водородом и R6 является С 2-6-алкилом или арилом. 16. Соединение по любому из предшествующих пунктов, в котором m=0, n=1 и o=0. 17. Соединение по любому из пп.1-16, в котором m=1, n=0 и о=1. 18. Соединение по п.1 со структурой, которую выбирают из
МПК / Метки
МПК: A61K 31/505, A61P 9/00, A61K 31/40, A61P 9/10, A61P 3/06
Метки: розувастатина, производные
Код ссылки
<a href="https://eas.patents.su/12-20591-proizvodnye-rozuvastatina.html" rel="bookmark" title="База патентов Евразийского Союза">Производные розувастатина</a>
Предыдущий патент: Способы улучшения жизнеспособности растений
Следующий патент: Печь для сжигания твердого топлива
Случайный патент: Эктопаразитицидные водные суспензионные препараты спинозинов












