3-замещенное-[1,2,3]-бензотриазиноновое соединение для увеличения глутаматергических синаптических ответов
Формула / Реферат
1. Соединение формулы
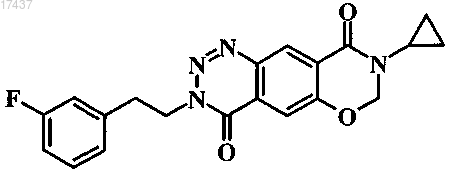
которое представляет собой 8-циклопропил-3-[2-(3-фторфенил)этил]-7,8-дигидро-3H-[1,3]оксазино[6,5-g][1,2,3]бензотриазин-4,9-дион или его фармацевтически приемлемую соль присоединения кислоты или основания.
2. Способ лечения млекопитающего пациента, где пациент страдает гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых снижены память или другие познавательные функции, упомянутый способ включает введение упомянутому пациенту в фармацевтически приемлемом носителе эффективного количества соединения согласно п.1.
3. Способ лечения млекопитающего, где пациент страдает гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых происходит кортикальный/стриарный дисбаланс, приводящий к шизофрении или шизофреноформному поведению, упомянутый способ включает введение упомянутому пациенту в фармацевтически приемлемом носителе эффективного количества соединения по п.1.
4. Способ по п.3, в котором упомянутое патологическое состояние является шизофренией.
5. Способ по п.2, в котором упомянутое патологическое состояние является болезнью Паркинсона.
6. Способ по п.2, в котором упомянутое патологическое состояние является болезнью Альцгеймера.
7. Фармацевтическая композиция, включающая эффективное количество соединения по п.1 в комбинации с фармацевтически приемлемым носителем, добавкой или вспомогательным веществом.
8. Композиция по п.7, в которой соединение составляет от около 0,5 до около 75 мас.% композиции и носитель, добавка или инертный наполнитель составляет от около 25 до около 95,5% композиции.
9. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении млекопитающего пациента, где пациент страдает гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых снижены память или другие познавательные функции.
10. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении шизофрении.
11. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении болезни Паркинсона.
12. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении СДВГ.
13. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении синдрома Ретта.
14. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении синдрома ломкой Х-хромосомы.
15. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении болезни Альцгеймера.
Текст
3-ЗАМЕЩННОЕ-[1,2,3]-БЕНЗОТРИАЗИНОНОВОЕ СОЕДИНЕНИЕ ДЛЯ УВЕЛИЧЕНИЯ ГЛУТАМАТЕРГИЧЕСКИХ СИНАПТИЧЕСКИХ ОТВЕТОВ Это изобретение относится к предотвращению и лечению мозговой недостаточности, включая увеличение функционирования рецептора в синапсах в ячеистых структурах мозга, ответственных за поведения более высокого порядка. Эти ячеистые структуры мозга включены в познавательные способности, связанные с нарушением памяти, такого как наблюдается при различных слабоумиях,и в дисбалансе в нейронной активности между разными участками мозга, который предполагается в нарушениях, таких как болезнь Паркинсона, шизофрения и аффективные нарушения. В особенном объекте настоящее изобретение относится к соединению формулы пригодному для лечения таких патологических состояний, и способам применения этих соединений для такого лечения.(71)(73) Заявитель и патентовладелец: ЛЕ ЛАБОРАТУАР СЕРВЬЕ (FR) 017437 Область изобретения Это изобретение относится к соединению, фармацевтическим композициям и способам для применения в предотвращении и лечении мозговой недостаточности, включая увеличение функционирования рецепторов в синапсах в ячеистых структурах мозга, ответственных за поведения более высокого порядка. Эти ячеистые структуры мозга, которые вовлечены в познавательные способности, связаны с нарушением памяти, например таким, которое наблюдается при старении, и различное слабоумие, в дисбалансе в нейронной активности между разными участками мозга, что предполагается в нарушениях, таких как болезнь Паркинсона, шизофрения, дефицит внимания и аффективные нарушения или расстройства настроения, и в нарушениях, в которых вовлечен дефицит в нейротрофических факторах. В особенном объекте настоящее изобретение относится к соединениям, пригодным для лечения таких патологических состояний, и способам применения этих соединений для такого лечения. Родственные заявки Эта заявленная формула изобретения имеет преимущество приоритета U.S. предварительных заявок US 60/878503, поданной 3 января 2007 г., и US 60/921433, поданной 2 апреля 2007 г., релевантные части этих заявок включены сюда посредством ссылки. Уровень техники изобретения Высвобождение глютамата в синапсах во многих сайтах в переднем мозгу млекопитающего стимулирует два класса постсинаптических, ионотропических рецепторов. Эти классы, как правило, называются как АМРА/квисквалатный и N-метил-D-аспарагиновокислотный (NMDA) рецепторы. АМРА/квисквалатные рецепторы содействуют потенциалонезависимому быстрому возбудительному постсинаптическому току (быстрый ВПСТ), тогда как NMDA рецепторы генерируют потенциалозависимый, медленный возбудительный ток. Исследования, выполненные в долях гиппокампа или коры головного мозга, указывают, что АМРА рецептор, содействующий быстрому ВПСТ, является безусловно основным доминирующим компонентом в большинстве глутаматергических синапсов. АМРА рецепторы равномерно не распределены в мозгу, но по большей части в значительной степени ограничены в мозговом пузыре и мозжечке. Эти рецепторы найдены в высокой концентрации в поверхностных слоях новой коры головного мозга, в каждой из главных синаптических зон гиппокампа и в стриарном комплексе, как сообщается Monaghan et al., в Brain Research 324:160-164 (1984). Исследования на животных и людях указывают, что эти структуры организовывают комплекс перцептивно-моторных процессов и обеспечивают субстраты для поведений более высокого порядка. Таким образом, АМРА рецепторы содействуют трансмиссии в такие ячеистые структуры мозга, ответственные за реципиента познавательной деятельности. По причинам, сформулированным выше, лекарства, которые модулируют и, таким образом, увеличивают функционирование АМРА рецепторов, могли бы иметь значительную пользу для познавательной и умственной деятельности. Такие лекарства должны также облегчить кодирование памяти. Экспериментальные исследования, такие как те, о которых сообщает Arai и Lynch, Brain Research 598:173-184 (1992),указывают, что увеличивая размер АМРА рецептора, содействующего синаптическому ответу(ам), увеличивается индукция долговременного потенцирования (LTP). LTP означает устойчивое увеличение интенсивности синаптических контактов, которая следует за повторной физиологической активностью типа, известного для наблюдаемого в мозге во время изучения. Соединения, которые увеличивают функционирование АМРА формы рецепторов глютамата, облегчают индукцию LTP и достижение изученных проблем на грызунах и людях, как оценено на многочисленных образцах. См., например, Granger et al., Synapse 15:326-329 (1993); Staubli et al., PNAS 91:777781 (1994); Arai et al., Brain Res. 638:343-346 (1994); Staubli et al., PNAS 91:11158-11162 (1994); Shors etRogers, US Patent 5747492. Существует значительный корпус результатов, показывающий, что LTP составляет субстрат памяти. Например, соединения, которые блокируют LTP, сталкиваются с формированием памяти у животных, и определенные лекарства, которые разрушают изучение у людей, вызывают антагонизм стабилизации LTP, как сообщается del Cerro и Lynch, Neuroscience 49: 1-6 (1992). Изучение простой задачи вызывает LTP в гиппокампе, которое мешает LTP, генерированному при помощи высокочастотной стимуляции (Whitlock et al., Science 313:1093-1097 (2006, и механизм, который подтверждает, что LTP поддерживает пространственную память (Pastalkova, et al., Science 313:1141-1144 (2006. Важное значение для области изучения имеет то, что найдено, что in vivo лечения модулятором положительного рецептора глютамата АМРА-типа восстанавливает стабилизацию основного дендритного LTP у животных среднего возраста (Rex, et al., J. Neurophysiol. 96:677-685 (2006. Возбудительная синаптическая трансмиссия обеспечивает основной путь, при помощи которого нейротрофические факторы увеличиваются в конкретных участках мозга. Также потенцирование функции АМРА рецептора модуляторами было найдено, чтобы увеличить уровни нейротрофинов, особенно производимый мозгом нейротрофический фактор или BDNF. См., например, Lauterborn, et al., J. Neurosci. 20:8-21 (2000); Gall, et al., U.S. Patent-1 017437 6030968; Lauterborn, et al., JPET 307:297-305 (2003) и Mackowiak, et al., Neuropharmacology 43:1-10 (2002). Другие исследования связывают уровни BDNF со многими неврологическими нарушениями, такими как болезнь Паркинсона, синдром дефицита внимания и гиперактивности (СДВГ), аутизм, синдром ломкой Х-хромосомы и синдром Ретта (RTT). См., например, O'Neill, et al., Eur. J. Pharmacol. 486:163-174 (2004);al., Neuron 49:341-348(2006). Таким образом, потенцирующие средства АМРА рецептора, могут быть полезными для лечения этих, так же как и других неврологических болезней, которые являются результатом глутаматергического дисбаланса или дефицита в нейротрофических факторах. Прототип соединения, которое увеличивает функцию АМРА рецептора, был описан Ito et al., J.Physiol. 424:533-543 (1990). Эти авторы нашли, что ноотропное лекарство анирацетам (N-анизоил-2 пирролидинон) увеличивает ток, установленный мозговыми АМРА рецепторами, выраженный в ооцитах Ксенопуса, без влияния на ответы -аминобутировокислотными (GABA), каиновокислотными (KA) илиNMDA рецепторами. Инфузия анирацетама в доли гиппокампа, как также показано, существенно увеличила размер быстрых синаптических потенциалов, не изменяя мембранных свойств в состоянии покоя. С тех пор подтверждено, что анирацетам увеличивает синаптические ответы в некоторых сайтах в гиппокампе и что он не имеет никакого эффекта на связывающие потенциалы NMDA-рецептора (Staubli et al.,Psychobiology 18:377-381 (1990) и Xiao et al., Hippocampus 1:373-380 (1991. Было найдено, что анирацетам имеет чрезвычайно быстрое проявление и вымывание и может неоднократно применяться без очевидных длительных эффектов, которые являются желательными особенностями для схожих по поведению лекарств. Тем не менее, анирацетам имеет некоторые недостатки. Внешнее введение анирацетама вряд ли будет влиять на мозговые рецепторы. Лекарство работает только при высоких концентрациях (приблизительно 1000 мкМ), и около 80% лекарства переходят в анизоилGABA после внешнего введения людям (Guenzi и Zanetti, J. Chromatogr. 530:397-406 (1990. Было найдено, что метаболит, анизоил-GABA, имеет меньшую синаптическую активность, чем анирацетам. В дополнение к этим проблемам, анирацетам имеет предполагаемые эффекты на множество других нейромедиаторов и ферментативных целей в мозге, что делает сомнительным механизм любого требуемого терапевтического эффекта лекарства. См., например, Himori, et al., Pharmacology Biochemistry and Behavior 47:219-225 (1994); Pizzi et al., J. Neurochem. 61:683-689 (1993); Nakamura и Shirane, Eur. J. Pharmacol. 380: 81-89 (1999); Spignoli и Pepeu, Pharmacol. Biochem. Behav. 27:491-495 (1987); Hall и Von Voigtlander,Neuropharmacology 26:1573-1579 (1987) и Yoshimoto et al., J. Pharmacobiodyn. 10:730-735 (1987). Был описан класс АМРА рецептор-модулирующих соединений, который не показывает низкие потенциальные возможности и присущую особенность неустойчивости анирацетама (Lynch и Rogers, USPatent 5747492). Эти соединения, названные "Ампакины", могут быть замещенными бензамидами, которые включают, например, 1-(хиноксалин-6-илкарбонил)пиперидин (СХ 516; Ampalex). Как правило,они химически более устойчивы чем анирацетам и показывают улучшенное бионакопление. СХ 516 является активным в тестах животных, используемых, чтобы обнаружить эффективные лекарства для лечения нарушения памяти, шизофрении, и депрессивного синдрома. В трех отдельных клинических испытаниях СХ 516 продемонстрировал эффективность в улучшении различных форм человеческой памятиIngvar et al., Exp. Neurology 146:553-559 (1997. Другой класс Ампакинов, бензоксазинов, как обнаруживали, имеет очень высокую активность в invitro и in vivo моделях для оценки вероятности продуцирования повышения познания (Rogers и Lynch;US Patent5736543). Замещенные бензоксазины являются устойчивыми бензамидными аналогами с разными рецепторомодулирующими свойствами гибкого бензамида, СХ 516. Некоторые замещенные бензофуразановые и бензотиадиазоловые соединения, как было найдено,были значительно и неожиданно с более большим потенциалом в животных моделях шизофрении, чем предыдущие соединения, а также эффективны при повышении познания. Эти соединения структурно подобны соединениям, раскрытым в Lynch и Rogers, US Patent5736543. Ранее раскрыты структуры, которые содержат 1,3-бензоксазин-4-оновый фармакофор, замещенные в бензольной части при помощи гетероатомов, таких как азот или кислород (US Patents5736543 и 5962447), при помощи замещенных алкильных групп (US Patents5650409 и 5783587), или незамещенные (WO 99/42456). Еще другие классы 1,3-бензоксазиновых соединений содержат внешнюю карбонильную группу в оксазиновом кольце (US Patent6124278), но не в качестве заместителя в бензольном кольце. В настоящее время был обнаружен, новый класс триазиноновых соединений, которые показывают значительное действие на гиппокампальные синаптические ответы и нейрональный ток целой клетки,содействующий АМРА рецепторам. 3-Замещенные бензо[1,2,3]триазин-4-оновые соединения являются потенциальными модуляторами АМРА рецепторов, которые значительно более метаболитически стабильнее, чем соответствующие бис-бензоксазиноны. Биологическая активность триазинона была неожиданной и эффективность на АМРА рецепторы поразительно высокой; наиболее сильнодействующие триазиноны этого класса удваивают ток АМРА рецептора при концентрации уже 3 нМ. Бензо[1,2,3]триазин-4-оновое соединение раскрыто в этом документе в качестве модулятора АМРА рецептора. Краткое изложение сущности изобретения Настоящее изобретение включает в одном объекте соединение, как показано структурой I и описано в разделе II детального описания, которые следуют далее. Было найдено, что введение соединений этого класса увеличивает синаптические ответы, опосредованные АМРА рецепторами. Соединение настоящего изобретения значительно и неожиданно более эффективное, чем описанные ранее соединения в усилении функции АМРА рецептора в первичных нейронных культурах и в срезах гиппокампа крыс и в увеличении познавательной деятельности, такой как деятельность в задержанной совместимости для образцовой задачи. Эта неожиданная активность переводит в фармацевтические соединения и соответствующие способы применения, включая способы лечения, которые используют значительно меньшие концентрации (в пересчете моль-на-моль) настоящих соединений по сравнению с композициями предыдущего уровня техники. Способность соединения изобретения увеличивать опосредуемые АМРА рецептором ответы делает соединения пригодными для множества целей. Они включают облегчение изучения поведений, зависящих от глутаматных рецепторов, условий лечения, в которых АМРА рецепторы или синапсы, использующие эти рецепторы, уменьшаются в количестве или эффективности, и усилении возбудительной синаптической активности с целью восстановить равновесие между подобластями мозга или увеличить уровни нейротрофических факторов. В другом аспекте изобретение включает способ лечения млекопитающего, страдающего гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых память или другие познавательные функции снижены. Такие условия могут также вызвать кортикальный/стриарный дисбаланс, приводящий к шизофрении или шизофреноформному поведению. Согласно способу такого пациента лечат эффективным количеством соединения, как показано структурой I и описано в разделе II детального описания далее, в фармацевтически приемлемом носителе. Эти и другие объекты и признаки изобретения будут более очевидными после прочтения последующего детального описания изобретения в сочетании с прилагаемыми чертежами. Детальное описание изобретения Определения Термины ниже имеют следующие определения, если не указано иначе. Другие термины, которые использованы в описании настоящего изобретения, имеют такие же определения, как такие же термины,которые обычно используются в таком уровне техники. Термин "алкил" использован здесь для ссылки к полностью насыщенному одновалентному радикалу, содержащему углерод и водород, который может быть неразветвленной цепью, разветвленной или циклической. Примерами алкильной группы являются метил, этил, н-бутил, н-гептил, изопропил, 2 метилпропил, циклопропил, циклопропилметил, циклобутил, циклопентил, циклопентилэтил и циклогексил. Термин "алкенил" использован здесь для ссылки к одновалентному радикалу, содержащему углерод и водород, который содержит один или два участка ненасыщености и который может быть неразветвленной цепью, разветвленной или циклической. Примерами алкильной группы являются этенил, нбутенил, н-гептенил, изопропенил, циклопентенил, циклопентенилэтил и циклогексенил. Термин "замещенный алкил" относится к алкилу, как такой, который только что описан, включающему одну или более функциональную группу, такую как низший алкил, содержащий 1-6 атомов углерода, арил, замещенный арил, ацил, галоген (т.е. галоалкилы, например CF3), гидроксигруппа, алкоксигруппа, алкоксиалкил, аминогруппа, алкил и диалкиламиногруппа, акриламиногруппа, ацилоксигруппа,арилоксигруппа, арилоксиалкил, карбоксиалкил, карбоксамидогруппа, тиогруппа, тиоэфиры, насыщенные и ненасыщенные циклические углеводороды, гетероциклы и т.п. Термин "арил" относится к замещенному или незамещенному одновалентному ароматическому радикалу, имеющему одно кольцо (например, фенил) или множество конденсированных колец (например, нафтил). Другие примеры включают гетероциклические ароматические группы, имеющие один или более атом азота, кислорода или серы в кольце, такие как оксазолил, изоксазолил, пиразолил, тиазолил, тиадиазолил,тетразолил, пиридазинил, пиримидил, бензофурил, бензотиенил, бензимидазолил, бензоксазолил, бензотиазолил, хинолил, изохинолил, имидазолил, фурил, пирролил, пиридил, тиенил и индолил.-3 017437 Термин "замещенные", как использовано в термине "замещенный арил, замещенный ароматический, замещенный гетороарил или замещенный гетероароматический", здесь означает, что может находиться один или более заместителей, упомянутые заместители выбирают из атомов и групп, которые,если присутствуют, не препятствуют функционированию соединений в качестве усилителя функции АМРА рецептора. Примеры заместителей, которые могут находиться в замещенной ароматической или гетероароматической группе, включают, но не ограничиваются ими, группы, такие как (С 1-С 7)алкил, (С 1 С 7)ацил, арил, гетороарил, замещенный арил и гетороарил, галоген, цианогруппу, нитрогруппу, (С 1-С 7) алкилгалогениды (например, CF3), гидроксигруппу, (С 1-С 7)алкоксигруппу, алкоксиалкил, аминогруппу,алкил и диалкиламиногруппу, акриламиногруппу, ацилоксигруппу, арилоксигруппу, арилоксиалкил,карбоксиалкил, карбоксамидогруппу, тиогруппу, тиоэфиры, насыщенные и ненасыщенные (С 3-С 8)циклические углеводороды, (С 3-С 8)гетероциклы и т.п."Гетероцикл" или "гетероциклический" относится к циклическому кольцу, где один или более атомов углерода замещены на один или более гетероатомов, таких как азот, кислород или сера. Примеры гетероциклов включают, но не ограничиваются ими, пиперидин, пирролидин, морфолин, тиоморфолин,пиперазин, тетрагидрофуран, тетрагидропиран, 2-пирролидинон, 5-валеролактам, 6-валеролактон и 2 кетопиперазин. Термин "замещенный гетероцикл" относится к гетероциклу как такой, который только что описан,который содержит одну или более функциональную группу, такую как низший алкил, ацил, арил, цианогруппа, галоген, гидроксигруппа, алкоксигруппа, алкоксиалкил, аминогруппа, алкил и диалкиламиногруппа, акриламиногруппа, ацилоксигруппа, арилоксигруппа, арилоксиалкил, карбоксиалкил, карбоксамидогруппа, тиогруппа, тиоэфиры, насыщенные и ненасыщенные циклические углеводороды, гетероциклы и т.п. Термин "соединение" использован здесь для ссылки к конкретному химическому соединению, раскрытому в этом документе. В рамках его применения в контексте термин как правило относится к отдельному соединению, но в некоторых случаях может также относиться к стереоизомерам и/или оптическим изомерам (включая рацемические смеси) раскрытых соединений. Термин "эффективное количество" относится к количеству выбранного соединения формулы I, которое использовано для увеличения глутаматергического синаптического ответа увеличением активности АМРА рецептора. Конкретное используемое количество меняется в зависимости от конкретного выбранного соединения и его целевого применения, возраста и веса пациента, пути введения и т.д., но может быть легко определено при помощи обычного эксперимента. В случае лечения патологического состояния или болезненного состояния, эффективное количество является таким количеством, которое применяется для эффективного лечения специфического патологического состояния или болезненного состояния. Термин "фармацевтически приемлемый носитель" относится к носителю или инертному наполнителю, который не является неприемлемо токсическим для пациента, которому его вводят. Фармацевтически приемлемые инертные наполнители подробно описаны E.W. Martin в "Remington's Pharmaceutical"Фармацевтически приемлемая соль" соединения амина такого, как рассмотренные в текущем изобретении, является солью аммония, имеющей как противоион неорганический анион, такой как хлорид,бромид, йодид, сульфат, сульфит, нитрат, нитрит, фосфат и т.п., или органический анион, такой как ацетат, малонат, пируват, пропионат, фумарат, циннамат, тозилат и т.п. Термин "больной" или "пациент" использован во всем описании для описания животного, главным образом относящегося к млекопитающему животному, включая человека, для которого предназначается лечение или применение соединений или композиций согласно настоящему изобретению. Для лечения или применения в/или таких патологических состояний или болезненных состояний, которые являются специфическими для конкретного животного (особенно, например, человеческого пациента или больного), термин "больной" или "пациент" относится к такому особому животному. Термин "сенсомоторные нарушения" использован для описания проблемы, которая возникает у больного или пациента из-за неспособности объединить внешнюю информацию, полученную из пяти известных чувств таким путем, как непосредственные соответствующие физические ответы, включающие движение и действие. Термин "задача познавательного характера" или "познавательная функция" использован для описания усилия или процесса, осуществляемого больным или пациентом, которое вовлекает мышление или познание. Разнообразные функции ассоциации коры головного мозга теменной, височной и лобных долей большого мозга, которые составляют приблизительно 75% всей ткани человеческого мозга, ответственны за большую часть обработки информации, которая проходит между сенсорным входом и двигательной реакцией. Разнообразные функции ассоциации коры головного мозга часто упоминаются как познание, которое буквально означает процесс, которым мы познаем мир. Выборочные проявления внимания по специфическому стимулу, распознавая и идентифицируя эти соответствующие особенности стимула и планирование и преодоление ответа, являются некоторыми из процессов или способностей,установленных человеческим мозгом, которые связаны с познанием.-4 017437 Термин "ячеистая структура мозга" использован для описания разных анатомических участков мозга, которые сообщаются друг с другом через синаптическую активность нейронных клеток. Термин "АМРА рецептор" относится к скоплению белков, найденных в некоторых мембранах, которое позволяет положительным ионам пересекать мембрану в ответ на связывание глютамата или АМРА (DLамино-3-гидрокси-5-метил-4-изоксазолпропионовая кислота), но не NMDA. Термин "возбудительный синапс" использован для описания соединения клетка-клетка, в котором высвобождение химической информационной РНК одной клеткой вызывает деполяризацию внешней мембраны другой клетки. Возбудительный синапс описывает постсинаптический нейрон, у которого есть потенциал аннулирования, который более положителен чем пороговый потенциал и, следовательно, в таком синапсе нейромедиатор увеличивает вероятность, что возбудительный постсинаптический потенциал будет результативным (нейрон запустит продуцирование потенциала действия). Потенциалы аннулирования и пороговые потенциалы определяют постсинаптическое возбуждение и ингибирование. Если потенциал аннулирования для постсинаптического потенциала (PSP) более положителен, чем порог потенциала действия, эффект нейромедиатора является возбудительным и производит возбудительный постсинаптический потенциал (EPSP) и запускает потенциал действия при помощи нейрона. Если потенциал аннулирования для постсинаптического потенциала более отрицателен, чем порог потенциала действия, нейромедиатор является ингибирующим и может производить ингибирующие постсинаптические потенциалы (IPSP), таким образом, уменьшая вероятность, что синапс запустит потенциал действия. Общим правилом для постсинаптического действия является то, что если потенциал аннулирования более положителен, чем порог, результаты - возбуждение; ингибирование происходит, если потенциал аннулирования более отрицателен, чем порог. См., например, Chapter 7, NEUROSCIENCE, под ред. DalePurves, Sinauer Associates, Inc., Sunderland, MA 1997. Термин "задача на выполнение движений" использован для описания усилия, взятого больным или пациентом, которое включает движение или действие. Термин "задача на восприятие" использован для описания действия больным или пациентом, чтобы уделить внимание сенсорным входам. Термин "синаптический ответ" использован для описания биофизических реакций в одной клетке как следствие высвобождения химической информационной РНК другой клетки, с которой она находится в тесном контакте. Термин "гипоглутаматергическое патологическое состояние" использован для описания состояния или патологического состояния, в котором трансмиссия, опосредованная глютаматом (или связанными возбудительными аминокислотами) уменьшена ниже нормальных уровней. Трансмиссия состоит из высвобождения глютамата, связывания с постсинаптическими рецепторами, и открытие интеграла каналов на те рецепторы. Конечной точкой гипоглутаматергического патологического состояния является уменьшение возбудительного постсинаптического тока. Это может быть результатом любого из трех выше отмеченных фаз трансмиссии. Патологические состояния или болезненные состояния, которые считают гипоглутаматергическими патологическими состояниями и которые могут лечиться с использованием соединений, композиций и способов согласно настоящему изобретению, включают, например,потерю памяти, слабоумие, депрессивный синдром, нарушения внимания, сексуальную дисфункцию,нарушения движений, включающие болезнь Паркинсона, шизофрению или шизофреноформное поведение, нарушения памяти и обучения, включающие такие нарушения, которые возникают вследствие старения, травмы, удара и нейродегенеративных нарушений, таких как те, которые связаны с вызванными лекарствами состояниями, нейротоксическими агентами, болезнью Альцгеймера и старением. Эти патологические состояния являются легко узнаваемыми и диагностируемыми средним специалистом в данной области техники. Термин "кортикостриарный дисбаланс" использован для описания состояния, в котором баланс нейронной активности в связанной коре головного мозга и лежащий в основе стриарного комплекса обычно отклоняется от найденного. Активность может быть оценена электрической регистрацией или молекулярными биологическими методами. Дисбаланс может быть установлен, применяя эти измерения к этим двум структурам или при помощи функциональных (поведенческих или физиологических) критериев. Термин "аффективное нарушение" или "расстройство настроения" описывает патологическое состояние, когда печаль или восторг чрезмерно интенсивны и продолжаются вне ожидаемого воздействия стрессового случая жизни или возникают эндогенно. Как используется здесь, термин "аффективное нарушение" охватывает все типы расстройства настроения, как описано, например, в Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition (DSM IV), pages 317-391. Термин "шизофрения" использован для описания патологического состояния, которое является общим типом психоза, характеризующегося беспорядком в интеллектуальных процессах, таких как заблуждение и галлюцинации, обширная потеря интереса человека к другим людям и внешнему миру и замыкание интересов в его или ее собственном мире. Шизофрению теперь считают группой нарушений психики, а не одиночным случаем, и различие сделано между острой и непрерывно текущей шизофренией. Как используется здесь, термин шизофрения или "шизофреноформный" охватывает все типы шизофре-5 017437 нии, включая амбулаторную шизофрению, кататоническую шизофрению, гебефреническую шизофрению, латентную шизофрению, непрерывно текущую шизофрению, псевдоневротическую шизофрению,острую шизофрению, простую шизофрению, и связанные психические расстройства, которые подобны шизофрении, но которые не обязательно диагностированы как шизофрении per se. Шизофрения и другие психическое расстройства могут быть диагностированы, используя методические рекомендации, установленные, например, в Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition (DSM IV) Sections 293.81, 293.82, 295.10, 295.20, 295.30, 295.40, 295.60, 295.70, 295.90, 297.1, 297.3, 298.8. Термин "функция мозга" использован для описания комбинированных задач восприятия, интегрирования, фильтрования и ответа на внешние стимулы и внутренние мотивационные процессы. Термин "сниженный" использован для описания функции, работающей на уровне, который менее чем нормальный. Сниженные функции могут быть значительно ослаблены так, что функция едва выполняется, фактически не существуя или работает создавая видимость, которая значительно менее чем нормальная. Сниженные функции могут быть также недостаточными. Снижение функции изменяется по серьезности от больного к больному и патологического состояния, которое будет лечиться. Соединения, которые увеличивают функцию АМРА рецептора Настоящее изобретение направлено в одном объекте на соединение, имеющее свойство увеличивать функцию АМРА рецептора. Обусловленные соединения этого изобретения имеют структуру I ниже Синтез соединения изобретения 8-циклопропил-3-[2-(3-фторфенил)этил]-7,8-дигидро-3H-[1,3]оксазино[6,5-g][1,2,3]бензотриазин-4,9-диона предпочтительно проводят согласно следующей синтетической схеме, где синтез замещенного салициламида хорошо известен специалисту в области органического синтеза. Схема 1 На схеме 1 стадия А может быть проведена при обычных условиях, в том числе катализируемое кислотой включение синтона формальдегида. Например, салициламид (1) растворяют и нагревают в подходящем органическом растворителе вместе с триоксаном и серной или хлористо-водородной кислотой. Стадия В является реакцией нитрования, которая может проводиться в мягких условиях, известных специалисту в области органического синтеза и детально описанных в таких объемах в Reagents for OrganicSynthesis (Fieser and Fieser) и Organic Syntheses (см. веб-сайт http://www.orgsyn.org/). Стадия С включает 2-стадийное окисление метильной группы соединения 3 до карбоновой кислоты через промежуточный альдегид, применяя N,N-диметилформамид диметилацеталь и перйодат натрия, а затем оксон. Стадия D включает сочетание первичного амина с нитрокислотой, которое может быть выполнено с использованием множества конденсирующих агентов, известных специалисту химику. Некоторые неограничивающие примеры широко используют тионилхлорид, оксалилхлорид или карбонилдиимидазол. Стадия Е является восстановлением арильной нитрогруппы до анилина и может быть произведена при помощи восстановления с использованием множества катализаторов, включая, но не ограничиваясь ими, Pd, или Pt, илиNi Реннея и водород, или Zn/Cu. Стадия F формирует триазиноновое кольцо и может проводиться присоединением изоамилнитрита в DMF. Все композиции, раскрытые в настоящем изобретении, могут быть синтезированы вышеописанными способами, используя аналогичные синтетические стадии для отдельных представленных в примерах-6 017437 соединений, описанные в этом документе так же как и те, которые известны в уровне техники. Также заявленными являются все их соли присоединения с фармацевтически приемлемой кислотой или основанием. Способ лечения Согласно одному объекту изобретения способ предназначается для лечения млекопитающего пациента, страдающего гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов. У такого пациента память или другие познавательные функции могут быть сниженными или может произойти кортикальный/стриарный дисбаланс, приводящий к потере памяти, слабоумию, депрессивному синдрому, нарушению внимания, сексуальной дисфункции, нарушению движений, шизофрении или шизофреноформному поведению. Нарушения памяти и нарушения обучения, которые поддаются лечению согласно настоящему изобретению,включают те нарушения, которые являются результатом старения, травмы, удара и нейродегенеративного нарушения. Примеры нейродегенеративного нарушения включают, но не ограничиваются теми, которые относятся к медикаментозным состояниям, нейротоксические агенты, болезнь Альцгеймера и старение. Эти патологические состояния легко устанавливаются и диагностируются средним специалистом в данной области техники и лечатся введением больному эффективного количества одного или более соединений согласно настоящему изобретению. В настоящем изобретении способ лечения включает введение пациенту, который нуждается в лечении, в фармацевтически приемлемом носителе эффективного количества 8-циклопропил-3-[2-(3 фторфенил)этил]-7,8-дигидро-3H-[1,3]оксазино[6,5-g][1,2,3]бензотриазин-4,9-диона, имеющего формулу или его фармацевтически приемлемой соли присоединения кислоты или основания. Как отмечалось выше, лечение пациента согласно способу изобретения пригодно для увеличения активности АМРА рецептора и, таким образом, может быть применено для облегчения изучения поведений, зависящих от АМРА рецепторов, и для лечения патологических состояний, таких как нарушение памяти, в котором АМРА рецепторы или синапсы, использующие эти рецепторы, уменьшаются в количестве или эффективности. Способ также пригоден для увеличения возбудительной синаптической активности для восстановления равновесия между подобластями мозга, которое может выражаться в шизофрению или шизофреноформное поведение или другое поведение, как описано выше. Было найдено,что соединения, применяемые в соответствии со способом, являются более эффективными, чем описанные ранее соединения, в усилении активности АМРА рецептора, как показано в in vitro и in vivo тестах,описанных ниже. Биологическая активность Усиление функции АМРА рецептора Синаптические ответы, опосредованные АМРА рецепторами, увеличиваются согласно способу изобретения при применении соединения, описанного в этом документе. Соединение продемонстрировано,чтобы быть существенно более мощным, чем ранее описанные соединения, в усилении опосредования АМРА токов всей клетки в выращенных нейронах. Анализ in vitro описан следующим образом. Кортикальные клетки получали из 18-19-дневного эмбриона крысы Sprague-Dawley и регистрировали после 3-дневного культивирования. Внеклеточный раствор (ВКР) содержит (в мМ): NaCl (145), KCl(5,4), HEPES (10), MgCl2 (0,8), CaCl2 (1,8), глюкоза (10), сахароза (30); рН (7,4). Чтобы заблокировать потенциалзависимые потоки натрия, к указанному раствору добавляли 40 нМ ТТХ. Внутриклеточный раствор содержит (в мМ): K-глюконат (140), HEPES (20), EGTA (1,1), фосфокреатин (5), MgATP (3), GTP(0,3), MgCl2 (5) и CaCl2 (0,1); рН (7,2). Все тестируемые соединения и глютаматные растворы были добавлены во внеклеточный раствор. Ток всей клетки измеряли фиксирующим потенциал амплификатором (Axopatch 200 В), фильтровали при 2 кГц, дискретизировали при 5 кГц и записывали на ПК с pClamp 8. Клетки были фиксированы потенциалом при -80 мВ. Растворы были применены DAD-12 системой. Ответ начального уровня для каждой клетки записывали, используя 1 с выброс 500 мкМ глютамата, растворенного в ВКР. Ответы на исследуемые соединения были потом оценены применением 10 с выброса исследуемого соединения с последующим 1 с выбросом такой же концентрации исследуемого соединения плюс 500 мкМ глютамата и затем 10 с солевого раствора. Эту последовательность выбросов повторяли до тех пор, пока не получили стабильное считывание или пока не были измерены удовлетворительные частные значения, позволяющие экстраполяцию для измерения максимального измерения. Средняя величина стабилизированного тока между 600 и 900 мс после применения глютамата или исследуемого соединения плюс глютамат была вычислена и использована как параметр для измерения лекарственного эффекта. Стабилизированные ответы в присутствии различных концентраций исследуемого соединения были разделены на ответ начального уровня, чтобы вычислить процентное увеличение.-7 017437 Соединения считают активным в этом исследовании, если при исследуемой концентрации 3 мкМ или меньше они вызывают более чем 100%-ное увеличение величины измеренного установившегося тока,вызванного только применением глютамата. Концентрация, при которой вызванный глютаматом ток увеличивается на 100%, обычно называется как ЕС 2 х величина. Соединение этого изобретения 8-циклопропил-3-[2-(3-фторфенил)этил]-7,8-дигидро-3H[1,3]оксазино[6,5-g][1,2,3]бензотриазин-4,9-дион демонстрирует ЕС 2 х величину 0,1 мкМ. Введение, дозы и препарат Как отмечалось выше, соединение и способ изобретения увеличивает АМРА рецепторсодействующие ответы и пригодны для лечения гипоглутаматергических патологических состояний. Соединение также пригодно для лечения патологических состояний, таких как нарушение памяти или другие познавательные функции, вызванные дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов. Соединение может также быть применено в лечении шизофрении или шизофреноформного поведения, появившихся в результате кортикального/стриарного дисбаланса, и в помощи изучения поведений, зависящих от АМРА рецептора. У больных, которым назначается лечение соединениями настоящего изобретения, фармацевтическими композициями и способами, могут быть снижены память или другие познавательные функции,или может быть кортикальный/стриарный дисбаланс, приводящий к потере памяти, слабоумию, депрессивному синдрому, нарушениям внимания, сексуальной дисфункции, нарушениям движений, шизофрении или шизофреноформному поведению. Нарушения памяти и нарушения обучения, которые поддаются лечению согласно настоящему изобретению, включают такие нарушения, которые являются результатом старения, травмы, удара и нейродегенеративного нарушения. Примеры нейродегенеративного нарушения включают, но не ограничиваются такими, которые связаны с вызванными лекарствами состояниями, нейротоксическими агентами, болезнью Альцгеймера и старением. Эти патологические состояния легко устанавливаются и диагностируются средним специалистом в данной области техники и лечатся введением больному эффективного количества одного или более соединений согласно настоящему изобретению. В общем, дозы и пути введения соединений должны быть определены согласно размеру и патологическому состоянию пациента согласно стандартным фармацевтическим методам. Используемые уровни дозы могут изменяться в широких пределах и могут быть легко определены специалистом в данной области техники. Как правило, используются количества в миллиграммах вплоть до количества грамма. Композиция может быть введена пациенту различными путями, например перорально, трансдермально,периневрально или парентерально, которые представляют собой внутривенные, подкожные, внутрибрюшинные или внутримышечные инъекции, среди прочих, включающие трансбуккальное, ректальное и трансдермальное введение. Пациенты, рассматриваемые для лечения согласно способу изобретения,включают людей, сопутствующих животных, лабораторных животных и т.п. Препараты, содержащие соединение согласно настоящему изобретению, могут принимать твердую форму, полутвердую, форму лиофилизированного порошка или жидких лекарственных форм, таких как,например, таблетки, капсулы, порошки, препараты длительного выпуска, растворы, суспензии, эмульсии,суппозитории, кремы, мази, лосьоны, аэрозоли, пластинки или т.п., предпочтительно в единичных лекарственных формах, подходящих для простого введения точных дозировок. Фармацевтические композиции согласно настоящему изобретению, как правило, включают общепринятый фармацевтический носитель или инертный наполнитель и могут дополнительно включать другие лекарственные средства, носители, адъюванты, добавки и т.п. Предпочтительно композиция имеет содержание приблизительно 0,5-75 мас.% соединения или соединений изобретения с остатком, состоящим в основном из подходящих фармацевтических инертных наполнителей. Для перорального введения такие инертные наполнители включают маннит, лактозу, крахмал, стеарат магния, сахарин натрия, тальк,целлюлозу, глюкозу, желатин, сахарозу, карбонат магния фармацевтических классов и т.п. Если желательно, композиция может также содержать незначительные количества не токсических вспомогательных веществ, таких как смачивающие агенты, эмульгирующие агенты или буферы. Жидкие композиции могут быть получены растворением или диспергированием соединений (от около 0,5 до около 20 мас.% или более) и необязательно фармацевтических адъювантов в носителе, таком как, например, водный солевой раствор, водная D-глюкоза, глицерин или этанол, для получения раствора или суспензии. Для применения в пероральном жидком препарате, композиция может быть приготовлена в виде раствора, суспензии, эмульсии или сиропа, поставляясь или в жидкой форме, или в высушенной форме, подходящей для гидратации в воде или нормальном солевом растворе. Когда композицию применяют в виде твердых препаратов для перорального введения, препараты могут быть таблетками, гранулами, порошками, капсулами или т.п. В таблетированном препарате композиция обычно формируется с добавками, например инертным наполнителем, таким как сахаридный или целлюлозный препарат, связующим, таким как крахмальный клейстер или метилцеллюлоза, наполнительным веществом, дезинтегратором и другими добавками, обычно применяемыми в производстве медицинских препаратов. Инъецируемая композиция для парентерального введения обычно содержит соединение в подхо-8 017437 дящем внутривенном (в.в.) растворе, таком как стерильный физиологический солевой раствор. Композиция может также быть сформированной в виде суспензии, в липидной или фосфолипидной, в липосомной суспензии или в водной эмульсии. Способы приготовления таких лекарственных форм известны или будут очевидны для специалиста в данной области техники; например, см. Remington's Pharmaceutical Sciences (17th Ed., Mack Pub. Co.,1985). Композиция, которая будет вводиться, должна содержать количество выбранного соединения в фармацевтически эффективном количестве для того, чтобы произвести увеличение токов АМРА рецепторов у пациента. Следующие примеры иллюстрируют изобретение, но в любом случае, не предназначены для его ограничения. Если не указано иное, все температуры представлены в градусах Цельсия. Если не указано иное, все данные ЯМР спектра являются данными 1 Н ЯМР спектра и были получены в дейтерохлороформе или дейтерированном DMSO как растворитель, применяя тетраметилсилан как внутренний стандарт. Название соединения примера соответствует номенклатуре IUPAC в соответствии с программным обеспечением ChemSketch, предоставленным ACD Labs. Пример 1. 8-Циклопропил-3-[2-(3-фторфенил)этил]-7,8-дигидро-3H-[1,3]оксазино[6,5-g][1,2,3]бензотриазин-4,9-дион 4-Метилсалициловую кислоту (21,3 г, 140 ммоль) растворяли в метиленхлориде (120 мл), а затем порциями прибавляли CDI (22,7 г, 140 ммоль). Смесь перемешивали при комнатной температуре в течение 24 ч и затем непродолжительно нагревали при кипении. К смеси прибавляли раствор циклопропиламина (8,0 г, 140 ммоль) в триэтиламине (5 мл, 36 ммоль) и перемешивали в течение 3 дней. Прибавляли воду (200 мл) и рН доводили до 2, применяя 12 М хлористо-водородную кислоту. Фазы разделяли и водную фазу экстрагировали хлороформом (200 мл). Объединенные органические фазы промывали раствором бикарбоната натрия (100 мл) и сушили над сульфатом натрия. Выпаривание дает 22,7 г амида в виде беловатого порошка. Амид (22,7 г, 119 ммоль) и триоксан (36 г, 0,4 моль) растворяли в хлороформе (250 мл) и перемешивали при комнатной температуре. Прибавляли сульфат натрия (32 г) и концентрированную серную кислоту (80 капель) и смесь кипятили в течение 30 мин, после чего дополнительно прибавляли 40 капель конц. серной кислоты. Через 90 мин осадок удаляли фильтрованием и промывали этилацетатом. Объединенные растворители удаляли в вакууме с образованием 30 г масла. Масло очищали при помощи флэш-хроматографии (250 г силикагеля, этилацетат:гексан 30:70, затем 40:60) с образованием 20,1 г 7-метилбензоксазинона в виде бесцветного масла. Бензоксазинон (16 г, 79 ммоль) растворяли в метиленхлориде (200 мл), к которому прибавляли уксусную кислоту (30 мл). Смесь охлаждали до 0 С при помощи ледяной бани и по каплям прибавляли азотную кислоту (14 мл, 90%) в течение 15 мин, в результате образуя оранжевый раствор. Реакционную смесь перемешивали в течение 90 мин и затем выливали в смесь измельченного льда/воды (300 мл). Медленно прибавляли раствор гидроксида натрия до тех пор, пока рН не достигнет 5. Реакционную смесь экстрагировали хлороформом (200 мл), сушили над сульфатом натрия и концентрировали в вакууме до 40 мл. Прибавляли этилацетат (200 мл) и смесь концентрировали в вакууме до 60 мл. Полученные кристаллы отфильтровывали с образованием 8,1 г (33 ммоль, выход 41%) желаемого 6-нитроизомера в виде беловатого порошка. Маточный раствор концентрировали и кристаллизовали дополнительное количество продукта (1,2 г) в виде беловатого порошка. Затем из маточного раствора были выделены другие 5 г смеси изомеров, эта смесь использовалась в следующей стадии. Твердую смесь изомеров с предыдущей стадии (5 г, 20 ммоль) суспендировали в диметилацеталеN,N-диметилформамида (30 мл) и DMF (10 мл) и нагревали при 125 С в течение 16 ч. Растворитель удаляли в вакууме с образованием темно-коричневого остатка. Остаток растворяли в THF (100 мл). Перйодат натрия (11 г, 51 ммоль) растворяли в воде (100 мл) и прибавляли к реакционной смеси, которую перемешивали в течение 15 мин при комнатной температуре. Бежевую суспензию экстрагировали хлороформом (200 мл), затем сушили над сульфатом натрия и разбавляли этилацетатом (200 мл). Растворителям позволяли медленно испаряться, что в результате привело к кристаллизации желаемого изомера (2,0 г, 7,6 ммоль) в виде беловатого порошка. Промежуточный нитроальдегид (524 мг, 2,0 ммоль) растворяли в DMF (10 мл) при 40 С. После этого раствор охлаждали до комнатной температуры, прибавляли оксон(1,47 г, 2,4 ммоль) и смесь перемешивали всю ночь. Прибавление воды (25 мл) и этилацетата (30 мл) дает две фазы, которые разделяли и органическую фазу фильтровали и промывали водой. Водную фазу экстрагировали этилацетатом и объединенные органические фазы промывали дважды водой, сушили над сульфатом магния и концентрировали в вакууме с образованием влажного желтого остатка (0,54 г, 1,9 ммоль), который использовали без дополнительной очистки.-9 017437 Раствор промежуточной нитрокислоты (0,54 г, 1,9 ммоль) в метиленхлориде объединяли с тионилхлоридом (1,4 мл, 20 ммоль) вместе с несколькими каплями DMF и перемешивали при комнатной температуре всю ночь. Смесь концентрировали в вакууме и повторно растворяли в метиленхлориде (10 мл). 3 Фторфенэтиламин (0,56 мл, 4,3 ммоль) и триэтиламин (1,1 мл, 7,9 ммоль) растворяли в метиленхлориде(15 мл), к которому прибавляли свежеприготовленный раствор хлорангидрида кислоты. После перемешивания в течение 2 ч раствор промывали водной HCl (1 М) и нас. бикарбонатом натрия и сушили над сульфатом магния. Полученный раствор концентрировали в вакууме с образованием желтого порошка,который растирали в этилацетате с образованием светло-бежевых кристаллов (0,53 г, 1,3 ммоль). Бежевый порошок с предыдущей стадии (0,53 г, 1,3 ммоль) растворяли в смеси THF (20 мл) и метанола (20 мл) и прибавляли к свежеприготовленному Zn/Cu реагенту (10 г, см. ниже). Прибавляли муравьиную кислоту (10 капель) и смесь перемешивали при комнатной температуре всю ночь, после чего ТСХ показала окончание реакции. После прибавления DMF (2 мл) смесь перемешивали в течение 10 мин и затем фильтровали через силикагель (2 см). Силикагель промывали смесью THF/метанол (1:1) и объединенные фильтрат и промывной раствор концентрировали в вакууме. Прибавляли хлороформ и упаривали для удаления всей остаточной воды. Прибавляли DMF (2 мл) и избыток изоамилнитрита (5 мл) и смесь перемешивали в течение 2,5 ч, после чего ТСХ показала окончание реакции. Прибавление диэтилового эфира(5 мл) приводит к осаждению продукта, который промывали этилацетатом и сушили на воздухе с образованием 0,29 г желтого порошка со следующими свойствами: Т пл. 181-182 С; 1 Н ЯМР (300 МГц,CDCl3)8.78 (1 Н, s), 7.82 (1 Н, s), 7.3-6.8 (4 Н, m), 5.33 (2 Н, s), 4.67 (2 Н, m), 3.21 (2 Н, m), 2.76 (1 Н, m), 1.02Zn/Cu реагент (использованный выше) был свежеприготовлен следующим образом. Конц. HCl (3 мл) прибавляли к 10 г цинка в 100 мл воды во время интенсивного перемешивания. Перемешивание продолжали в течение 2 мин (начали образовываться комки), после чего воду декантировали. Дополнительно 100 мл воды прибавляли при интенсивном перемешивании. Все остаточные куски разрушали при помощи шпателя. Прибавляли конц. HCl (3 мл) и перемешивание продолжали в течение 2 мин. После удаления воды декантированием осадок промывали дополнительно 100 мл воды. К осадку прибавляли воду (50 мл) и перемешивание продолжали между тем, как медленно прибавляли раствор CuSO4 (300 мг в 50 мл воды). После того как цинк стал черным, воду удаляли декантированием. Остаток последовательно промывали метанолом (50 мл) и THF (50 мл). Пример 2. In vivo физиологическое испытание. Физиологическое действие соединения изобретения испытывали in vivo на анестезированных животных согласно следующим процедурам. Животные поддерживались под наркозом при помощи введения фенобарбитала, используя шприцевой насос Гамильтона. Возбуждающий и регистрирующий электроды вставляли в перфорирующий путь и зубчатую извилину гиппокампа соответственно. Как только электроды были внедрены, устанавливался стабильный исходный уровень вызванных ответов при помощи одиночных монофазных импульсов (длительность импульсов 100 мкс), поставляемых при 3/мин возбуждающего электрода. Поле EPSP контролировали до достижения стабильного исходного уровня (около 20-30 мин), после чего внутрибрюшинно вводили раствор исследуемого соединения в HPCD и регистрировали вызванные потенциалы поля. Вызванные потенциалы регистрировали в течение приблизительно 2 ч после введения лекарства или до тех пор, пока амплитуда поля EPSP не вернется до исходного уровня. В последнем случае это означает, что внутрижелудочное введение также осуществляется соответствующей дозой того же исследуемого соединения. 8-Циклопропил-3-[2-(3-фторфенил)этил]-7,8-дигидро-3H-[1,3]оксазино[6,5-g][1,2,3]бензотриазин 4,9-дион вызывает увеличение амплитуды поля EPSP на 10% при дозе 5 мг/кг после внутрижелудочного введения. В то время как изобретение было описано в отношении определенных способов и вариантов осуществления, должно быть принято во внимание, что могут быть произведены различные модификации без отклонения от изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы которое представляет собой 8-циклопропил-3-[2-(3-фторфенил)этил]-7,8-дигидро-3H-[1,3]оксазино[6,5g][1,2,3]бензотриазин-4,9-дион или его фармацевтически приемлемую соль присоединения кислоты или основания. 2. Способ лечения млекопитающего пациента, где пациент страдает гипоглутаматергическим забо- 10017437 леванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых снижены память или другие познавательные функции, упомянутый способ включает введение упомянутому пациенту в фармацевтически приемлемом носителе эффективного количества соединения согласно п.1. 3. Способ лечения млекопитающего, где пациент страдает гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых происходит кортикальный/стриарный дисбаланс, приводящий к шизофрении или шизофреноформному поведению, упомянутый способ включает введение упомянутому пациенту в фармацевтически приемлемом носителе эффективного количества соединения по п.1. 4. Способ по п.3, в котором упомянутое патологическое состояние является шизофренией. 5. Способ по п.2, в котором упомянутое патологическое состояние является болезнью Паркинсона. 6. Способ по п.2, в котором упомянутое патологическое состояние является болезнью Альцгеймера. 7. Фармацевтическая композиция, включающая эффективное количество соединения по п.1 в комбинации с фармацевтически приемлемым носителем, добавкой или вспомогательным веществом. 8. Композиция по п.7, в которой соединение составляет от около 0,5 до около 75 мас.% композиции и носитель, добавка или инертный наполнитель составляет от около 25 до около 95,5% композиции. 9. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении млекопитающего пациента, где пациент страдает гипоглутаматергическим заболеванием или дефицитом в количестве или интенсивности возбудительных синапсов или в количестве АМРА рецепторов таких, при которых снижены память или другие познавательные функции. 10. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении шизофрении. 11. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении болезни Паркинсона. 12. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении СДВГ. 13. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении синдрома Ретта. 14. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении синдрома ломкой Х-хромосомы. 15. Применение соединения по п.1 в производстве лекарственного средства для применения в лечении болезни Альцгеймера.
МПК / Метки
МПК: A61K 31/675, A61K 31/535, A01N 57/00
Метки: соединение, увеличения, синаптических, ответов, глутаматергических, 3-замещенное-[1,2,3]-бензотриазиноновое
Код ссылки
<a href="https://eas.patents.su/12-17437-3-zameshhennoe-123-benzotriazinonovoe-soedinenie-dlya-uvelicheniya-glutamatergicheskih-sinapticheskih-otvetov.html" rel="bookmark" title="База патентов Евразийского Союза">3-замещенное-[1,2,3]-бензотриазиноновое соединение для увеличения глутаматергических синаптических ответов</a>
Предыдущий патент: Новые составы, стабилизирующие иммуногенные композиции и ингибирующие их осаждение
Следующий патент: Способ переработки сырья, содержащего благородные металлы и сульфиды
Случайный патент: Конденсированные гетероциклические производные и их применение












