Способ получения цитопротекторного средства
Формула / Реферат
Способ получения цитопротекторного средства, заключающийся в том, что надземную часть солянки холмовой (Salsola collina Pall. ex Spreng.) измельчают до размера частиц 2+0,1 мм, удаляют липофильные вещества экстракцией сжиженным диоксидом углерода (CO2) при регулируемом давлении 63+1 атм и температуре 23+0,5шС в течение 20 ч, из оставшегося растительного сырья после CO2-экстракции извлекают 60%-ным этанолом целевой продукт, сумму флавоноидов, которую подвергают лиофильной сушке при температуре +65шС, давлении не менее 5 атм в течение 24 ч, затем высушенный продукт измельчают до порошкообразного состояния на шаровой мельнице, объединяют с вспомогательными веществами для получения цитопротекторного средства в количественном соотношении сухой продукт солянки холмовой:крахмал:стеарат кальция:тальк:лактоза 1:0,3:0,03:0,05:1,6 соответственно и таблетируют методом прямого прессования.
Текст
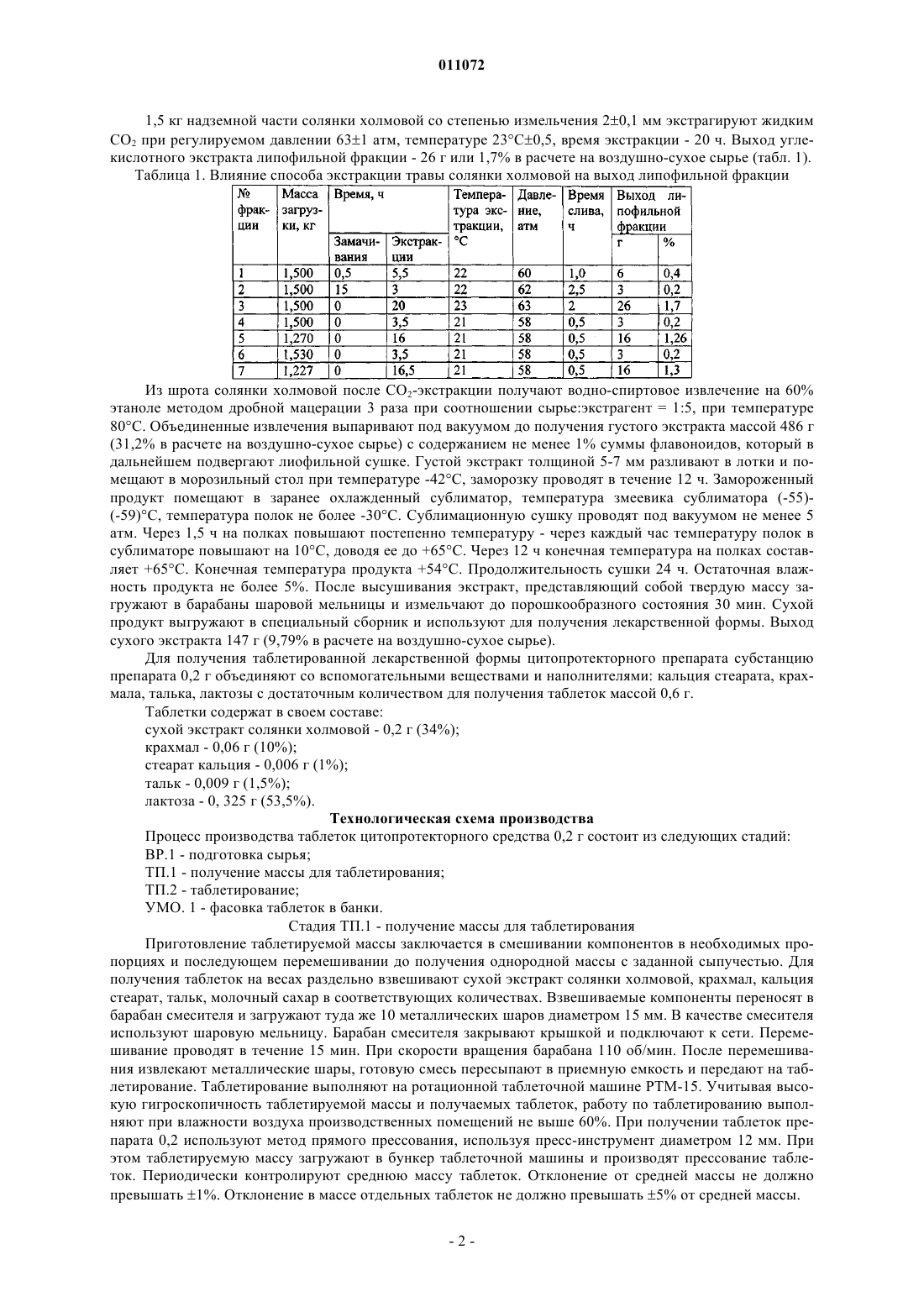
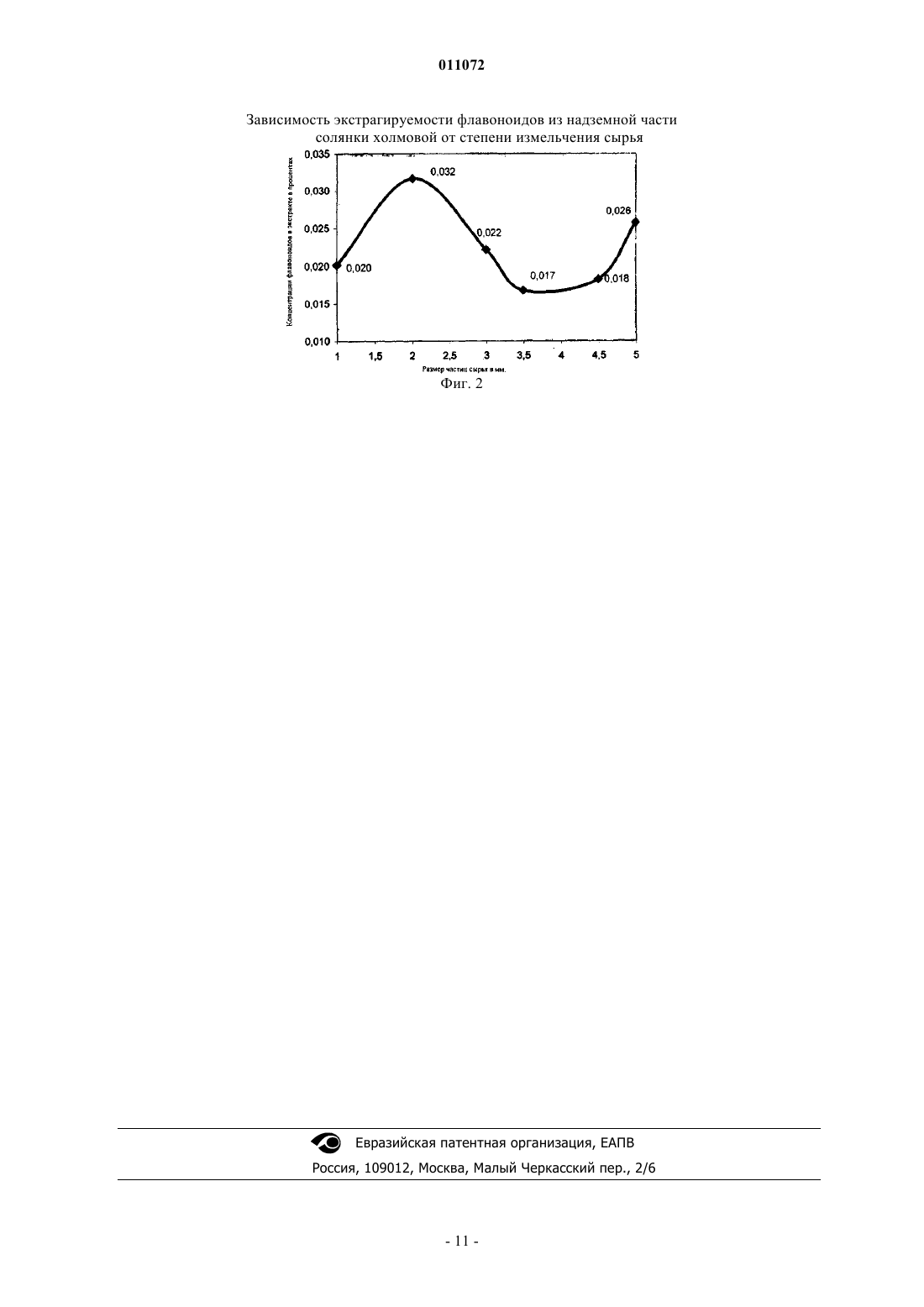
011072 Изобретение относится к лекарственным препаратам растительного происхождения, в частности к способу получения препарата из солянки холмовой, обладающего цитопротекторной активностью и может быть использовано в медицине при лечении заболеваний печени и желчевыводящих путей. Известен способ получения суммы экстрактивных веществ из солянки холмовой (патент РФ 2046604. Саратиков А.С., Чучалин B.C., Чупин С.П. Способ получения средства, обладающего гепатопротекторной активностью). Недостатками данного метода является то, что соотношение сырье : экстрагент 1:2 не обеспечивает полного извлечения экстрактивных веществ сырья солянки холмовой (3,2% на воздушно-сухое сырье), также в данном способе не извлечение липофильной фракции и применение вакуумной фильтрации делает процесс продолжительным в течение 2-3 суток. Известны средства растительного происхождения, обладающие цитопротекторным действием. Так,например силибинин - флавоноидное вещество, выделенное из Silybum marianum и улучшающее обменные процессы в печени (Машковский М.Д. Лекарственные средства. Харьков: 1997 - т.1.-с.788). Препарат ЛИВ-52, представляющий собой сухой остаток, изготовленный из смеси соков и отваров ряда растений, таких как Achillea millefolium, Capparis spinosa, Terminalia arjuna и др., используемый при токсических гепатитах (Машковский М.Д. Лекарственные средства. Харьков: 1997 - т.1.-с.715). Наиболее близким по характеру фармакологического действия к заявляемому средству является Эссенциале - препарат, содержащий "эссенциальные" фосфолипиды - диглицериновые эфиры холинфосфорной кислоты и ненасыщенные жирные кислоты вместе с витаминами (Машковский М.Д. Лекарственные средства. Харьков: 1997-т.1-с.516). Однако эти препараты дорогостоящие и труднодоступные, так как требуют использования дефицитного сырья, изготавливаются в основном из растений, не произрастающих на территории Республики Казахстан, производятся за рубежом. Известен способ получения препарата Салсоколлин (Патент РК 5696 Гепатопротекторное и антиоксидантное средство Салсоколлин. Опубл.: Официальный бюллетень Промышленная собственность 1 15.01.1998 г. МПК А 61 K 35/78.). Аналог имеет ряд существенных недостатков: экстракцию проводят хлороформом, хлороформ является дорогостоящим материалом и обладает токсическим действием; фармакокинетические исследования выявили низкую абсолютную биодоступность твердой лекарственной формы данного препарата. Целью заявляемого изобретения является способ получения нового цито-протекторного средства изSalsola collina Pall, ex Spreng. (солянка холмовая). Технический результат заявляемого способа заключается в извлечении липофильных веществ из сырья растения Salsola collina Pall, ex Spreng. (солянка холмовая) со степенью измельчения сырья 20,1 мм методом CO2 -экстракции при давлении 631 атм, температуре 230,5 С, времени экстракции 20 ч,извлечением целевого продукта - суммы флавоноидов 60% этанолом, с последующей лиофильной сушкой субстанции при температуре +65 С, давлении не менее 5 атм, продолжительности сушки 24 ч, конечной температурой продукта +54 С. Извлечение липофильной фракции способствует повышению выхода целевого продукта - флавоноидов из солянки холмовой. Для установления оптимальной концентрации спирта при экстрагировании биологически активных веществ из травы солянки холмовой в качестве экстрагента использовали 20; 30; 40; 50; 60; 70; 80% этиловый спирт. Результаты Результаты исследований показали, что соотношение спирт - вода незначительно влияет на процесс извлечения флавоноидов в диапазонах концентраций этанола до 30%. Заметное увеличение наблюдается при концентрации этанола от 40 до 60%. Сумма флавоноидов в экстракте при экстрагировании травы солянки холмовой этанолом 20 и 60% равна 0,021 и 0,032% соответственно. Наблюдается снижение содержания флавоноидов в экстракте при использовании этанола в концентрации 70% и выше. Максимальное значение экстрагируемости флавоноидов 0,032% в расчете на воздушно-сухое сырье определили при концентрации этанола 60% (фиг. 1). Это явилось определяющим при выборе экстрагента для выделения действующего вещества препарата. Также была исследована зависимость выхода флавоноидов от степени измельчения сырья. Из фиг. 2 видно, что при использовании для экстракции солянки холмовой со степенью измельчения 2 мм отмечается количественный выход флавоноидов. Таким образом, максимальный выход целевого продукта - суммы флавоноидов обеспечивается при измельчении сырья солянки холмовой 20,1 мм и экстракции 60% этанолом. Для оптимизации таблетированной формы препарата и улучшения показателя биодоступности субстанция из солянки холмовой объединяется с вспомогательными веществами в количественном соотношении : сухой экстракт растения : крахмал : стеарат кальция : тальк : лактоза = 1:0,3:0,03:0,05:1,6. Способ осуществляется совместным измельчением на центробежной мельнице вспомогательных веществ и сухого экстракта растения, с последующим прессованием на таблет-машине РТМ-15. Цель достигается следующим способом:-1 011072 1,5 кг надземной части солянки холмовой со степенью измельчения 20,1 мм экстрагируют жидкимCO2 при регулируемом давлении 631 атм, температуре 23 С 0,5, время экстракции - 20 ч. Выход углекислотного экстракта липофильной фракции - 26 г или 1,7% в расчете на воздушно-сухое сырье (табл. 1). Таблица 1. Влияние способа экстракции травы солянки холмовой на выход липофильной фракции Из шрота солянки холмовой после CO2-экстракции получают водно-спиртовое извлечение на 60% этаноле методом дробной мацерации 3 раза при соотношении сырье:экстрагент = 1:5, при температуре 80 С. Объединенные извлечения выпаривают под вакуумом до получения густого экстракта массой 486 г(31,2% в расчете на воздушно-сухое сырье) с содержанием не менее 1% суммы флавоноидов, который в дальнейшем подвергают лиофильной сушке. Густой экстракт толщиной 5-7 мм разливают в лотки и помещают в морозильный стол при температуре -42 С, заморозку проводят в течение 12 ч. Замороженный продукт помещают в заранее охлажденный сублиматор, температура змеевика сублиматора (-55)(-59)С, температура полок не более -30 С. Сублимационную сушку проводят под вакуумом не менее 5 атм. Через 1,5 ч на полках повышают постепенно температуру - через каждый час температуру полок в сублиматоре повышают на 10 С, доводя ее до +65 С. Через 12 ч конечная температура на полках составляет +65 С. Конечная температура продукта +54 С. Продолжительность сушки 24 ч. Остаточная влажность продукта не более 5%. После высушивания экстракт, представляющий собой твердую массу загружают в барабаны шаровой мельницы и измельчают до порошкообразного состояния 30 мин. Сухой продукт выгружают в специальный сборник и используют для получения лекарственной формы. Выход сухого экстракта 147 г (9,79% в расчете на воздушно-сухое сырье). Для получения таблетированной лекарственной формы цитопротекторного препарата субстанцию препарата 0,2 г объединяют со вспомогательными веществами и наполнителями: кальция стеарата, крахмала, талька, лактозы с достаточным количеством для получения таблеток массой 0,6 г. Таблетки содержат в своем составе: сухой экстракт солянки холмовой - 0,2 г (34%); крахмал - 0,06 г (10%); стеарат кальция - 0,006 г (1%); тальк - 0,009 г (1,5%); лактоза - 0, 325 г (53,5%). Технологическая схема производства Процесс производства таблеток цитопротекторного средства 0,2 г состоит из следующих стадий: ВР.1 - подготовка сырья; ТП.1 - получение массы для таблетирования; ТП.2 - таблетирование; УМО. 1 - фасовка таблеток в банки. Стадия ТП.1 - получение массы для таблетирования Приготовление таблетируемой массы заключается в смешивании компонентов в необходимых пропорциях и последующем перемешивании до получения однородной массы с заданной сыпучестью. Для получения таблеток на весах раздельно взвешивают сухой экстракт солянки холмовой, крахмал, кальция стеарат, тальк, молочный сахар в соответствующих количествах. Взвешиваемые компоненты переносят в барабан смесителя и загружают туда же 10 металлических шаров диаметром 15 мм. В качестве смесителя используют шаровую мельницу. Барабан смесителя закрывают крышкой и подключают к сети. Перемешивание проводят в течение 15 мин. При скорости вращения барабана 110 об/мин. После перемешивания извлекают металлические шары, готовую смесь пересыпают в приемную емкость и передают на таблетирование. Таблетирование выполняют на ротационной таблеточной машине РТМ-15. Учитывая высокую гигроскопичность таблетируемой массы и получаемых таблеток, работу по таблетированию выполняют при влажности воздуха производственных помещений не выше 60%. При получении таблеток препарата 0,2 используют метод прямого прессования, используя пресс-инструмент диаметром 12 мм. При этом таблетируемую массу загружают в бункер таблеточной машины и производят прессование таблеток. Периодически контролируют среднюю массу таблеток. Отклонение от средней массы не должно превышать 1%. Отклонение в массе отдельных таблеток не должно превышать 5% от средней массы.-2 011072 Стадия УМО. 1 - фасовка таблеток в банки Готовые таблетки упаковывают в стеклянные стерилизованные банки вместимостью 2 кг, маркируют и передают на участок фасовки. Контролер ОТК отбирает из банок среднюю пробу и направляет в лабораторию контроля качества. При соответствии таблеток препарата 0,2 г требованиям ФС РК 42-65104 таблетки фасуют по 25 или 50 штук в банки типа БДС или БВ. Определение биодоступности цитопротекторного препарата В экспериментальных исследованиях использованы 60 белых беспородных половозрелых крыссамцов, массой 160-180 г. Животные разделены на группы с внутривенным, внутрижелудочным введением препарата и контрольную. Внутривенно вводилась субстанция сухого экстракта солянки холмовой,внутрижелудочно таблетки 1 (ранее разработанная форма с содержанием субстанции 0,4 г), 2 (оптимизированная форма с содержанием субстанции 0,2 г) в дозе 40 мг/кг (табл. 2). Пробы крови у декапитированных крыс отбирались в разные сроки (n = 3) на протяжении 24 ч после введения препарата. Для исследований использовали сыворотку крови животных. Количественный анализ заявляемого препарата проводили по суммарному содержанию флавоноидов спектрофотометрическим методом на спектрометре Helios(Великобритания) при длине волны 347 нм. Фармакокинетические параметры по программе PHARM. После внутривенного введения препарата животным, максимальная концентрация суммы флавоноидов определяется в первой пробе Cmax =1,3 мкг/мл, с последующим двухфазным снижением. При внутрижелудочном введении максимальная концентрация достигается к 1 ч и соответствует 0,56 мкг/мл(форма 1) и 0,60 мкг/мл (форма 2), дальнейшая динамика фармакокинетической кривой имеет аналогичный характер. Площадь под фармакокинетической кривой "Концентрация - время" (AUC) при внутривенном введении составляет 6,13 мкг/млч, что значительно превышает таковую при внутрижелудочном введении,для формы 1 AUC = 3,92, для формы 2 - 5,05 мкг/млч. Абсолютную биодоступность таблеток препарата для крыс рассчитывали по формуле: где AUCBB - площадь под фармакокинетической кривой при внутривенном введении препарата,AUCВЖ - площадь под фармакокинетической кривой при внутривенном введении препарата таблеток 1 или 2.f для таблеток 1 составила 63,4%, для оптимизированных - 79,4%. Таблица 2. Динамика концентрации суммы флавоноидов цитопротекторного препарата в сыворотке крови у крыс Клиническое испытание цитопротекторного препарата при хронических гастритах. Клиническое испытание препарата проведено на базе областной детской клинической больницы (г. Караганда). Под наблюдением находились 154 ребенка в возрасте от 5 до 17 лет, находившихся на лечении в стационарах города Караганды. Установление диагноза основывалось на данных общепринятых унифицированных лабораторных и инструментальных методов диагностики. Для контроля эффективности нового препарата при лечении хронического гастрита обследованные дети были объединены в две группы: 34 ребенка основной группы получали препарат в сочетании со стандартной терапией хронического гастрита из расчета 40 мг/кг при двукратном применении в течение 20 дней. В контрольной группе (120 детей) пациенты получали базисную терапию ХГ (антибиотики, антисекреторный препарат в составе классической двойной или тройной или квадротерапии в зависимости от тяжести заболевания.). Симптоматика ХГ характеризовалась болевым (82,6%), диспептическим (76%) и астеновегетативным (у двух третей детей) синдромами. По данным эндоскопического исследования чаще встречались поверхностный (42,2-65%), эрозивный (31,8-49%), атрофический формы гастрита (18,8-29%), значительно реже констатированы гиперпластический (3,2-5%) и аутоиммунный (3,8-6%) гастрит.-3 011072 По окончании лечения у пациентов исследуемых групп наблюдали различные сроки купирования общеклинических, биохимических, морфологических проявлений заболевания. Если дети группы сравнения отмечали субъективное улучшение состояния в среднем на 5-7 сутки, то пациенты основной группы указывали на отсутствие диспепсических жалоб на 3-4 день лечения. Болевой синдром отсутствовал на 14 и 10 день лечения соответственно. Наряду с более ускоренной положительной динамикой общеклинических симптомов эндоскопически регистрировали обратное развитие воспалительных проявлений со стороны слизистой желудка у детей основной группы. В промежуточный момент (14 сутки наблюдения) сочетание традиционной терапии с новым препаратом купировало локальные признаки воспаления в виде отека гиперемии, при этом слизистая практически у всех больных (89%) соответствовала физиологическим нормам. В то же время в контрольной группе на указанный момент описанная симптоматика сохранялась более чем у 40% детей. К окончанию наблюдения (25-28 день) эндоскопическая картина имела вид здоровой ткани у всех пациентов основной группы и у 87% детей группы сравнения. Изучение состояния биополимеров соединительной ткани в слизи и слизистой оболочке выявило изменения в их количественном отношении. Установлена зависимость изменения уровня биополимеров соединительной ткани от морфологической формы хронического гастрита среди обследованных детей с помощью сравнительного анализа количественного содержания гексуроновой кислоты и гексозаминов в составе слизи (табл. 3). Исходя из представленных данных в таблице, можно сказать, что содержание как гексозаминов, так и гексуроновой кислоты изменяется при различных морфологических типах хронического гастрита. Причем, наибольшее снижение уровня биополимеров соединительной ткани имело место при аутоиммунном, атрофическом и эрозивном гастрите (расположены по степени убывания показателей). При поверхностном гастрите также выявлялась тенденция снижения исследованных показателей, однако, менее выраженная по сравнению с вышеуказанными формами гастрита. При гиперпластическом гастрите имело место повышение содержания гексозаминов и гексуроновой кислоты по сравнению с контрольной группой, вероятно это связано с компенсаторной реакцией со стороны соединительной ткани. Таблица 3. Сравнительная характеристика концентрации ГАГ в зависимости от морфологической формы гастрита Характеризуя состояние общеклинических симптомов и морфологических показателей при хроническом гастрите видно, что включение нового препарата независимо от степени выраженности воспаления и активности патологического процесса положительно влияет на клиническую картину хронического гастрита, болевой, диспептический синдромы купировались в среднем на 20,5 дней раньше по сравнению с контрольными данными; состояние соединительной ткани в виде значительного снижения содержания гликозаминогликанов в слизистой оболочке желудка (0,26-0,38). на динамику эндоскопических изменений и активности патологического процесса, у детей основной группы регресс наблюдали раньше, чем у детей группы сравнения; у части детей отмечались в эндоскопической картине признаки паразитоза. Клинические испытания цитопротекторного препарата на больных с заболеваниями печени и желчевыводящих путей Для изучения терапевтической активности нового препарата при хронических диффузных заболеваниях печени обследовано в динамике и пролечено 138 больных (мужчин - 111, женщин - 27), в том числе 20 больных получавших препарат - плацебо по 1 таблетке 3 раза в день. Последние были представлены следующими нозологическими единицами: хронический вирусный гепатит - 54 (39,1%), хронический алкогольный гепатит - 18 (13,1%), циррозы печени различной этиологии - 32, из них 20 (14,5%) - в стадии компенсации и 12 (8,7%) - в стадии декомпенсации, а также 34 больных с токсическим гепатитом на фоне ожоговой болезни. Контрольную группу составили больные (51 человек), получавшие Эссенциале по 1 капсуле 3 раза в день. Новый препарат применяли в суточной дозе 1,2 г (по 0,2 г 3 раза в день) в течение 20-30 дней (соответственно срокам пребывания в стационаре). У 14 больных проведено-4 011072 длительное лечение в течение 3-х месяцев и у 5 больных в течение 6 месяцев в условиях амбулаторного наблюдения. Исследуемые группы больных были репрезентативны по полу, возрасту, длительности болезни, нозологическим единицам. При поступлении в клинику у больных отмечались боли и тяжесть в правом подреберье, связанные с приемом пищи или физической нагрузкой (у 86 больных), диспептические расстройства: тошнота (у 21 больных), горечь во рту (у 13 больных), плохой аппетит (у 38 больных), метеоризм (у 41 больных), пониженная работоспособность (у 45 больных), быстрая утомляемость (у 24 больных), апатия, слабость (у 78 больных). При объективном исследовании выявлены гепатомегалия у всех больных, спленомегалия (у 43 больных), иктеричность склер (у 18 больных), желтуха (у 19 больных), кожный зуд (у 15 больных),асцит (у 12 больных). В качестве контроля эффективности использованы общеклинические данные; показатели функционального состояния печени: цитолиза - АсАТ, АлАТ, холестаза - билирубин с фракциями, ЩФ, ГГТП,печеночно-клеточной недостаточности - общий белок с фракциями, холинэстераза, фибриноген, ПТИ,показатели активности свободно-радикального состояния и системы антиоксидантной защиты - ДК,МДА, КТ, ГПО, СОД; состояние желчеобразовательной и желчевыделительной системы - многомоментное фракционное дуоденальное зондирование с микроскопическим, физико-химическим исследованием пузырной и печеночной порций желчи. При оценке эффективности лечения препаратами учитывалась динамика клинических симптомов и синдромов (табл. 4): болевого, диспептического, астеноневротического, геморрагического, гепатолиенального, холестаза, портальной гипертензии, печеночно-клеточной недостаточности. Диагноз верифицировали в каждом конкретном случае с учетом клиникоанамнестических данных результатов лабораторных показателей и инструментальных методов исследований. При установлении диагноза хронического гепатита использовали классификации, рекомендованные Международным конгрессом гастроэнтерологов в Лос-Анжелесе (1994 г.), диагноз цирроза печени ставили на основании рекомендаций экспертов Всемирной ассоциации по изучению заболеваний печени(1978 г.). Таблица 4. Динамика основных клинических симптомов и синдромов у больных с хроническими диффузными заболеваниями печени Результаты клинического обследования оценивали по условному коэффициенту, который является частным от деления суммы результатов лечения на число случаев. Результаты лечения оценивали следующим образом: нормализация изучаемого показателя 3 балла, значительное улучшение - 2 балла, незначительное улучшение - 0 баллов. Клиническое обследование до лечения выявило у всех больных нарушение функционального состояния печени, что проявилось наличием диспротеинемии с явлениями гипоальбуминемии и гипергаммаглобулинемии. Активность воспалительного процесса была умеренной: содержание ГГТП составило 239+10,2 н/моль/сл (при норме 50,4 + 7,6) (р 0,001), тимоловой пробы 8,7 + 0,3 ед. при норме 4,0 +0,5(р 0,001), уровень гаммаглобулина был повышен до 29,7+1,9% при норме 15,8+1,3% (р 0,01). Цитолитический синдром характеризовался умеренной гипертрансфераземией (5-кратное повышение нормы) у больных циррозами печени. Гипертрансфераземия была более выраженной (8-кратное повышение нормы) у больных с хроническим вирусным гепатитом, а также у больных с алкогольным гепатитом. В результате проведенной терапии новым препаратом отмечена существенная положительная динамика субъективных и объективных клинических симптомов. Монотерапия (хронические вирусные,алкогольные гепатиты с минимальной степенью активности воспалительного процесса), а также применение препарата на фоне базисных средств позволило купировать болевой синдром у 2/3 больных на 4-5 день, у остальных к 7-10 дню, а к концу второй недели боли сохранялись только у 21 больных. У 4 больных умеренные боли сохранялись и после лечения. Диспепсические симптомы также регрессировали у больных, принимавших препарат на 2-3 дня раньше по сравнению с контрольной. У больных, получав-5 011072 ших плацебо, отмечалось значительное запаздывание положительной динамики клинических симптомов,наличие которой можно объяснить базисной терапией. У 70% больных к концу курса лечения сохранялись боли в правом подреберье различной степени выраженности, диспетические проявления, значительная гепатомегалия. Кроме того, улучшилась белково-синтетическая функция печени, уменьшилась диспротеинемия,выраженность воспалительного и гепатодепрессивного синдромов. В контрольной и плацебо-группе отмечена аналогичная динамика клинических проявлений заболевания и лабораторных показателей, однако выявлено определенное запаздывание положительных изменений, о чем свидетельствовали достоверные различия параклинических показателей больных основной, контрольной и плацебо-групп в конце стационарного периода. Результаты лечения больных с хроническими диффузными заболеваниями печени представлены в табл. 5, из которой видно, что коэффициент терапевтической эффективности был наиболее высокий в группе больных, получавших новый препарат. Таблица 5. Результаты лечения больных хроническими диффузными заболеваниями печени Поддерживающая терапия новым препаратом больных при декомпенсированном циррозе печени не только алкогольной, но и вирусной этиологии оказала благоприятное влияние на качество жизни и функциональные показатели печени (билирубин, аминотрансферазы, ЩФ, холестерин, ПТИ). Результаты исследования состояния ПОЛ в процессе лечения заявляемым препаратом показали(табл. 6), что наиболее выраженные положительные сдвиги отмечены в эритроцитах (МДА). В плазме уровень продуктов ПОЛ по сравнению с исходными, снизился вследствие уменьшения диеновых коньюгат. При анализе динамики АОЗ обращает внимание достоверное увеличение ГПО в эритроцитах, активности каталазы в эритроцитах, СОД (р 0,05). Сопоставление положительной динамики показателей ПОЛ и АОЗ свидетельствуют о большой степени влияния нового препарата на антиоксидантную защиту клеток. Таблица 6. Влияние препарата на состояние процессов ПОЛ-АОЗ у больных с хроническими диффузными заболеваниями печени р 0,05 Результаты проведенных исследований свидетельствуют о том, что препарат обладает довольно широким спектром действия на различные клинические симптомы и синдромы, включая лабораторные показатели, являющиеся ведущими в клинической картине заболеваний печени. Отмечается избирательность влияния нового препарата в отношении ряда клинико-лабораторных данных: уменьшилась выраженность диспепсического, болевого, астенического, цитолитического и холестатического синдромов, а также билиарной недостаточности; улучшался пигментный, белковый, липидный обмен, кроме того,препарат оказывает антиоксидантный эффект. Применение препарата привело к снижению продуктов ПОЛ и повышению активности каталазы. Применение Эссенциале способствовало снижению МДА ниже контроля, что трудно расценить как однозначно позитивный фактор, так как МДА в физиологических концентрациях является нормальным метаболитом и играет определенную роль в биохимии желчи. Применение препарата оправдано его как гепатопротекторным, так и антиоксидантным эффектами, заключающиеся в инактивации свободных радикалов и торможении процессов ПОЛ. Полученные данные показали, что механизм действия нового препарата отличается от механизма действия Эссенциале. Механизм действия Эссенциале связан с репарацией мембран гепатоцитов. Механизм действия нового препарата направлен на стимуляцию репаративных, а также на перехват и инактивацию свободных радикалов. Входящие в его состав полифенолы могут образовывать хелатные комплексы с ионами железа, выключая их из процессов ПОЛ. Заявляемый препарат потенциирует функцию эндогенных антиоксидантов - витамина Е и глутатионпероксидазы и способствует сохранению высокого уровня восстановленного глутатиона. Терапевтическая эффективность цитопротекторного средства при патологии билиарной системы. Обследовано и пролечено в динамике 161 больных с патологией билиарной системы (50 больных с-6 011072 дискинезиями желчевыводящих путей (ДЖВП) и 111 - с хроническими бескаменными холециститами(ХБХ. Характеристика больных представлена в табл. 7. Таблица 7. Характеристика обследованных больных при патологии билиарной системы Применение нового препарата при дискинезии желчевыводящих путей позволило купировать болевой синдром к 3-му дню от начала лечения у 2/3 больных, а к 10-му дню боли сохранялись лишь у 17% ,к концу курса лечения только у 4,7% больных. Положительные "пузырные" симптомы, отмеченные практически у всех пациентов до лечения (96,8%) к концу курса лечения были выявлены у 3-х больных(5,9%). Диспептические явления в виде тошноты, рвоты к концу лечения не обнаруживались, горечь во рту сохранялась у 2,8%, метеоризм у 6,7% больных. Запоры после терапии отмечены только у 3,9% больных с выраженными дискинезиями толстого кишечника (табл. 8). Таблица 8. Клиническая эффективность нового препарата при ДЖВП (частота симптомов,%) Данные многомоментного фракционного дуоденального зондирования, ультразвукового исследования желчного пузыря и желчевыводящих путей после курса лечения свидетельствовали о значительном улучшении как моторной функции желчного, так и сфинктерного аппарата билиарной системы. Наряду с улучшением оттока желчи практически в равной степени наблюдалось и снижение тонуса сфинктеров Одди, Люткенса, что свидетельствует о холеспазмолитическом действии препарата (табл. 9). Таблица 9. Функциональное состояние билиарной системы при ДЖВП по данным МФДЗ и УЗИ Таким образом, назначение нового препарата, обладающего холеретическим, холеспазмолитическим действием может быть рекомендовано широкому кругу больных с различными дискинезиями желчевыводящих путей. Терапевтичесая эффективность цитопротекторного препарата при хронических бескаменных холециститах. Больные поступали в клинику с жалобами на боли в правом подреберье, у 14 с типичной иррадиацией вверх и вправо, ощущение горечи во рту, тошноту плохую переносимость жирной и острой пищи, а также склонность к запорам и метеоризму. При физическом обследовании у большинства больных (95%) определялись положительные пузырные симптомы: Алиева, Кера, Мерфи, Боаса, Маккензи, Ортнера. У 13 больных выявлен правосторонний реактивный вегетативный синдром, указывающий на длительность и тяжесть течения патологического процесса, у 4 - холецистокардиальный синдром. Анализ пузырной порции желчи до лечения показал, что у всех больных примерно в одинаковой степени отмечались изменения как микроскопической картины: лейкоцитоиды более 10, заключенные в хлопья слизи, клетки цилиндрического эпителия, кристаллы холестерина, жирных кислот, билирубинат кальция в умеренном или большом количестве, так и физико-химических свойств: снижение удельного(в достаточной мере отражающий изменения фосфолипидов желчи). Положительная реакция на Среактивный белок свидетельствовала об активном воспалительном процессе. Одновременно изучали функциональные пробы печени, состояние процессов ПОЛ и АОЗ. У большинства больных (92%) содержание в крови билирубина, ферментов (АсАТ, АлАТ, ЩФ, ГГТП), общего белка отмечены умеренные сдвиги со стороны неспецифических тестов активности воспалительного процесса. Увеличение СОЭ отмечено у 12 больных, умеренный лейкоцитоз - у 7 больных. Критерием эффективности лечения служила положительная динамика основных клинических симптомов обострения ХБХ и купирование болевого синдрома. Так, включение в комплекс лечения нового препарата позволило купировать болевой синдром у 2/3 больных на 4-5 день от начала терапии, у остальных - к 7-10 дню, а к концу лечения боли сохранялись только у 4 больных с длительным и часто рецидивирующим течением заболевания, однако интенсивность их уменьшилась. В контрольной группе для купирования болевого синдрома приходилось прибегать к назначению спазмолитиков, у 7 пациентов умеренные боли в правом подреберье сохранялись и после лечения. Диспепсические расстройства также регрессировали быстрее в группе больных, получавших препарат. Важно отметить, что практически у всех больных данной группы, страдающих запорами нормализовался стул. Прием нового препарата все больные переносили хорошо, побочных реакций не отмечено. Наряду с купированием болевого и диспепсического синдрома у большинства больных ХБХ на фоне лечения препаратом исчезли пузырные симптомы. Функциональное состояние различных отделов желчевыделительной системы чаще нормализовывалось в группе больных, принимавших новый препарат (от 7% до лечения до 64% после лечения и от 6 до 23%, соответственно). У оставшихся больных нарушения моторики, тонуса желчного пузыря и сфинктерного аппарата сохранялись, однако они были менее выраженными. Применение нового препарата способствовало усилению скорости секреции желчи в 1,7 раз, в группе, получавших плацебо в 1,3 раза. Терапевтическая эффективность хронического генерализованного пародонтита с цитопротекторным препаратом Исследование противовоспалительных свойств фитопленки с новым препаратом проводили у 80 больных обоего пола в возрасте от 17 до 60 лет с хроническим генерализованным пародонтитом легкой,средней и тяжелой степени. С соблюдением принципа рандомизации (каждый четный пациент с верифицированным диагнозом хронический генерализованный пародонтит) больные распределены на основную(30 человек) и группу сравнения (50). Наблюдаемые больные были рандомизированны и распределены на группы: основную и контрольную. В контрольную группу (n=30) были включены пациенты в возрасте от 20 до 55 лет. Легкая степень пародонтита выявлена у 10 больных (33%) от числа обследованных; средняя степень - у 12 (40%); тяжелая - у 8 (27%) больных. Всем больным производилась обработка слизистой оболочки полости рта растворами антисептиков(перекись водорода, хлоргекседин, фурациллин), затем тщательно удалялись зубные отложения с последующим полированием поверхности зуба. Далее производилась медикаментозная обработка пародонтального кармана с использованием преимущественно сильных антисептических средств или антимикробных препаратов широкого спектра действия (хлоргекседин, метронидазол, сангвиритрин). После высушивания слизистой использовали мазь метилурацила в виде тампонирования препарата в пародонтальные карманы и аппликаций на десну. В основную группу из 50 человек вошли пациенты в возрасте от 17 до 60 лет. Легкая степень поражения тканей пародонта выявлена у 20 (40%) больных от числа обследованных, средняя степень - у 25(50%), тяжелая - у 5 (10%) больных соответственно. После соответствующей антисептической обработки слизистой оболочки полости рта и пародонтальных карманов узкие сегменты фитопленок вводились в пародонтальные карманы, широкие сегменты апплицировались на десну. Клинические наблюдения показали, что до начала лечения основные жалобы больных хроническим генерализованным пародонтитом сводились к появлению выраженной кровоточивости десен при чистке зубов и приеме пищи, болезненности десен, зуда, подвижностью зубов и неприятного запаха изо рта. Регистрировали симптомы ХГП с выраженным цианозом десны, кровоточивостью и серозно-гнойным отделяемым из пародонтальных карманов при зондировании. Глубина карманов составила в среднем 4,5-4,7 мм, патологическая подвижность зубов I-III степени. Вышеперечисленные симптомы соответствовали изучаемым функциональным пробам. Так, пародонтальный индекс (ПИ) составил 3,721,05 и соответствовал средней степени воспаления. Комплексный пародонтальный индекс составил в среднем 3,621,05. Прежде всего, необходимо отметить, что в группе, где применяли фотопленку с новым препаратом не было зафиксировано ни одного случая токсического эффекта препаратов для местного лечения пародонтитов. По субъективным оценкам больных применение фитопленки не сопровождалось какими-либо неприятными ощущениями в области поражения десны или изменениями в общем состоянии. Большин-8 011072 ство больных отмечали купирование зуда и болевого синдрома на 2-3 день использования препарата. Объективные данные также не позволили зафиксировать токсический или побочный эффект исследуемой фитопленки. Комплексное лечение больных пародонтитами во всех группах наблюдения способствовало сначала уменьшению, а затем полному исчезновению субъективных ощущений. Однако сроки устранения этих симптомов во всех группах оказались разными. Так, если в контрольной группе кровоточивость десен прекратилась в среднем через 5,30,12 дней, то в группе, где применяли фитопленку с препаратом, данные сроки были короче и в среднем составили 3,30,15 дней. Неприятный запах изо рта, нормализация цвета десны и отделяемое из пародонтальных карманов перестали беспокоить больных контрольной группы через 6,20,15 дней. Аппликации пленок с новым препаратом ликвидировали эти симптомы быстрее, составляя в среднем 4,30,09 суток. Аналогичная динамика отмечена и при анализе сроков убывания симптомов боли и зуда в десне. В контрольной группе составила в среднем 4,60,13, тогда как при применении пленочной формы нового препарата 2,90,11. В основной группе нормализация клинической картины при лгкой степени достигали через 3-5 дней лечения, при средней степени тяжести через 5-7 дней, при тяжлой степени - 7-10 дней. В контрольной группе клиническая картина нормализовалась на 5-7 сутки при лгкой степени тяжести заболевания; на 7-10 сутки у пациентов со средней степенью тяжести; на 10-14 сутки при тяжлой степени соответственно. Положительная динамика с использованием фитопленки с новым препаратом в терапии хронического генерализованного пародонтита выявлена и при анализе специальных методов исследования. Десна имела бледно-розовую окраску, не кровоточила при зондировании, глубина карманов до 1,8-2,0 мм. Пародонтальный индекс соответствовал легкой степени воспаления 1,310,06. К концу наблюдения (7 сутки) слизистая ротовой полости здоровой окраски, плотно прилежит к поверхности резцов. Подтверждена эффективность фитопленки в виде положительной динамики пародонтальных индексов. Так, ПИ при использовании фитопленки изменялся от 3,721,05 до лечения и 0,290,12 после лечения (1,1-1,5-легкое воспаление). Положительная динамика была отмечена и в группе контроля, но в меньшей степени, пародонтальный индекс изменялся с 3,540,08 до 0,360,06. При оценке гигиенического индекса по Федорову-Володкиной (1,1-1,4-хорошая гигиена) в основной группе до проведенного лечения индекс составил 3,540,67 и снизился до 1,250,08. В группе, где применяли мазь метилурацила, гигиенический индекс составил 3,470,58 и 1,30,06 до и после лечения соответственно. Проба Ясиновского (в норме 16013,6) имела выраженную тенденцию к снижению в основной группе, где она изменялась от 420 до 180, тогда как при применении мази метилурацила терапевтический эффект был менее выражен, показатель изменялся от 398 до 296 после лечения. Проводились исследования цитологический активности с целью оценки эффективности лечения хронического генерализованного пародонтита при использовании традиционного и модифицированного способов лечения. На фоне традиционного лечения, где в качестве местной терапии использовали тампонирование мази метилурацила, достигали существенного очищения поля зрения в мазках-отпечатках. На 7 сутки в цитограммах сохранялась лейкоцитарные инфильтраты в виде сгустков, но их количество существенно отличалось от аналогичных цитограмм не леченных больных. Эпителиальные клетки встречались в виде конгломератов в количестве более 4-5- клеток. Как известно, метилурацил применяют с целью стимуляции лейкопоэза, что и было регистрировано в мазках по наличию зрелых зернистых гранулоцитов. К окончанию наблюдения поле зрения было представлено мононуклеарами, что характеризует падение остроты заболевания. Цитологическая характеристика больных основной группы отличалась картиной, соответствующей состоянию интактного пародонта. Цитограммы в основном характеризовались присутствием эпителиальных клеток различных типов, небольшим количеством моноцитов и лимфоцитов. Сохранялись признаки контаминирования клеток микроорганизмами, видимо за счет плохого гигиенического состояния полости рта (плохая чистка зубов). Анализ представленных результатов демонстрирует эффективность использования лекарственных пленок с содержанием заявляемого препарата при лечении воспалительных заболеваний пародонта(Р 0,05 по сравнению с группой сравнения). Реализации терапевтического действия препарата, очевидно,способствуют местное применение нового средства, с достаточным временем адгезии и комплаэнтными условиями лечения для больного при высоких фармакологических свойствах субстанции препарата. Преимущества способа получения нового цитопротекторного препарата 1. Доступность растительного сырья - солянка холмовая (Salsola collina Pall, ex Spreng.) широко распространена на территории Казахстана, возделывается в опытном хозяйстве Института фитохимии на площади 2 га, с ежегодным производством 4,0 т сырья. 2. Доступность и простота способа выделения суммы экстрактивных веществ из сырья солянки-9 011072 холмовой, заключающийся в экстракции растительного сырья со степенью измельчения 20,1 мм методом CO2 - экстракции при регулируемом давлении 631 атм и температуре 230,5 С, времени экстракции 20 ч, извлечением целевого продукта - суммы флавоноидов 60% этанолом, с последующей лиофильной сушкой субстанции при температуре +65 С, давлении не менее 5 атм, продолжительности сушки 24 ч,конечной температурой продукта +54 С. 3. Способ является экологически чистым, так как жидкий диоксид углерода и 60% этанол являются нетоксичными экстрагентами. 4. Экономическая эффективность заявляемого способа получения нового препарата заключается в сокращении продолжительности процесса получения до 20 ч. 5. Препарат обладает высоким лечебно-профилактическим эффектом при заболеваниях печени и желчевыводящих путей в сравнении с известными препаратами Легалон, Эссенциале, Карсил. При хроническом гастрите болевой, диспептический синдромы купируются в среднем на 20,5 дней раньше по сравнению с контрольными данными, регресс эндоскопических изменений и активности патологического процесса, у основной группы наблюдается раньше, чем у группы сравнения. При заболеваниях печени и желчевыводящих путей применение нового препарата способствует положительной динамике физико-химических показателей протоковой желчи и снижению содержания первичных и вторичных продуктов перекисного окисления липидов, усиливается скорость секреции желчи в 1,7 раз. При включении фитопленки с сухим экстрактом солянки холмовой в стандартную схему лечения хронического генерализованного пародонтита сокращаются сроки лечения на 2-3 суток. 6. Заявляемый лекарственный препарат имеет фармацевтические показатели, соответствующие требованиям фармакопейной статьи (ВФС РК 42-331-2000) ГФ, в том числе содержание остаточной влаги в таблетке составляет 3,7% (тогда как по стандартным требованиям не должно превышать 5%), время распадаемости 10,06 мин (не должно превышать 15 мин). 7. Абсолютная биодоступность препарата 79,4%. ФОРМУЛА ИЗОБРЕТЕНИЯ Способ получения цитопротекторного средства, заключающийся в том, что надземную часть солянки холмовой (Salsola collina Pall. ex Spreng.) измельчают до размера частиц 20,1 мм, удаляют липофильные вещества экстракцией сжиженным диоксидом углерода (CO2) при регулируемом давлении 631 атм и температуре 230,5 С в течение 20 ч, из оставшегося растительного сырья после CO2-экстракции извлекают 60%-ным этанолом целевой продукт, сумму флавоноидов, которую подвергают лиофильной сушке при температуре +65 С, давлении не менее 5 атм в течение 24 ч, затем высушенный продукт измельчают до порошкообразного состояния на шаровой мельнице, объединяют с вспомогательными веществами для получения цитопротекторного средства в количественном соотношении сухой продукт солянки холмовой:крахмал:стеарат кальция:тальк:лактоза 1:0,3:0,03:0,05:1,6 соответственно и таблетируют методом прямого прессования. Зависимость экстрагируемости флавоноидов из надземной части солянки холмовой от концентрации этилового спирта- 10011072 Зависимость экстрагируемости флавоноидов из надземной части солянки холмовой от степени измельчения сырья
МПК / Метки
МПК: A61P 1/16, A61P 1/04, A61K 36/185, A61P 1/02, A61K 9/20
Метки: способ, средства, получения, цитопротекторного
Код ссылки
<a href="https://eas.patents.su/12-11072-sposob-polucheniya-citoprotektornogo-sredstva.html" rel="bookmark" title="База патентов Евразийского Союза">Способ получения цитопротекторного средства</a>
Предыдущий патент: Устройство и способ для восстановления бурового раствора на нефтяной основе
Следующий патент: Напитки и пищевые продукты, устойчивые к изменению вкуса под действием света, способы их получения и композиции, обеспечивающие такую устойчивость
Случайный патент: Композиция для нанесения на кожу и ее применение