Применение аторвастатин лактолов в лечении состояний, которые модулируются 3-гидрокси-3-метилглютарил-коэнзим а редуктазой
Формула / Реферат
1. Применение соединения формулы (I) или его фармацевтически приемлемой соли или сольвата
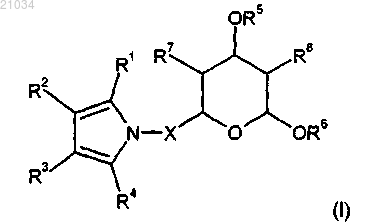
в лечении болезненного состояния, выбранного из группы, состоящей из гиперхолестеринемии, атеросклероза, гиперлипидемии, сердечно-сосудистого заболевания, ишемической болезни сердца, инфаркта миокарда, инсульта, заболевания периферических артерий, воспаления, деменции, рака, ядерной катаракты, диабета и гипертонии, в котором
R1, R4 и один из R2 и R3 независимо выбирают из группы, состоящей из C1-6-алкила и арила;
другой из R2 и R3 представляет собой -CONR9R10, где R9 и R10 независимо выбирают из группы, состоящей из водорода и арила;
R5 и R6 независимо выбирают из группы, состоящей из водорода, C1-6-алкила, C2-6-алкенила, C3-6-циклоалкила, арила, C1-6-алкиларила и C1-6-алканоилгетероарила, при условии, что всегда R5 и R6 оба не являются водородом;
R7 и R8 представляют собой Н;
X представляет собой -(CRaRb)m(CRa=CRb)n(CRaRb)o-, где Ra и Rb представляют собой Н и m, n и о независимо равны 0 или 1 при условии, что m+n+о не более 3, и где арильные группы включают ароматические циклические системы, содержащие 6-15 или 16 атомов углерода в цикле;
гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5-15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы;
каждая из приведенных групп R1-R10 может быть, если это возможно химически, независимо и необязательно замещена 1-5 группами, которые независимо выбирают из группы, состоящей из галогена, C1-3-алкила, гало-С1-3-алкила, C1-3-алкоксила, C1-3-галоалкоксила, гидроксила и цианогруппы.
2. Применение по п.1, где R1 представляет собой C1-6-алкил.
3. Применение по п.1 или 2, где R2 представляет собой -CONR9R10, где R9 является Н и R10 является арилом.
4. Применение по любому из пп.1-3, где R3 является арилом.
5. Применение по любому из предшествующих пунктов, где R4 является необязательно замещенным арилом.
6. Применение по любому из предшествующих пунктов, где R1 представляет собой изопропил, R2 представляет -CONHPh, R3 представляет собой фенил и R4 представляет собой 4-фторфенил.
7. Применение по любому из предшествующих пунктов, где R5 выбирают из группы, состоящей из водорода, арила, C1-6-алкиларила и C1-6-алканоилгетероарила.
8. Применение по п.7, где R5 является водородом.
9. Применение по п.7, где R5 выбирают из группы, состоящей из -C1-алкил-Ph, -С2-алкил-Ph, -C3-алкил-Ph и -С4-алкил-Ph.
10. Применение по п.9, где R5 представляет собой бензил.
11. Применение по п.7, где R5 представляет собой C1-6-алканоилпиридин.
12. Применение по п.11, где R5 представляет собой 3-метаноилпиридин.
13. Применение по любому из предшествующих пунктов, где R6 выбирают из группы, состоящей из водорода, C1-6-алкила, C2-6-алкенила, C3-6-циклоалкила, необязательно замещенного арила и C1-6-алкиларила.
14. Применение по п.13, где R6 выбирают из группы, состоящей из C1-6-алкила, C3-6-циклоалкила, C2-6-алкенила и необязательно замещенного арила.
15. Применение по п.14, где R6 выбирают из группы, состоящей из метила, этила, пропила, бутила, циклогексила и аллила.
16. Применение по п.13, где R6 представляет собой необязательно замещенный арил.
17. Применение по п.16, где R6 выбирают из группы, состоящей из C1-6-алкоксизамещенного фенила.
18. Применение по п.16, где R6 представляет собой 2,4-диметоксифенил.
19. Применение по любому из пп.1-6, где R5 является водородом и R6 является C1-6-алкилом, C3-6-циклоалкилом или необязательно замещенным арилом.
20. Применение по любому из пп.1-6, где R5 является необязательно замещенным бензилом и R6 является необязательно замещенным C1-6-алкилом или необязательно замещенным C2-6-алкенилом.
21. Применение по любому из пп.1-6, где R5 представляет собой C1-6-алканоилгетероарил и R6 представляет собой необязательно замещенный C1-6-алкил.
22. Применение по любому из предшествующих пунктов, где каждый Ra представляет собой Н, каждый Rb представляет собой Н и m=1, n=0 и о=1.
23. Применение по п.1, где структуру соединения выбирают из следующих:

Текст
ПРИМЕНЕНИЕ АТОРВАСТАТИН ЛАКТОЛОВ В ЛЕЧЕНИИ СОСТОЯНИЙ, КОТОРЫЕ МОДУЛИРУЮТСЯ 3-ГИДРОКСИ-3-МЕТИЛГЛЮТАРИЛ-КОЭНЗИМ А РЕДУКТАЗОЙ Изобретение относится к открытию новых аналогов аторвастатина. Более конкретно изобретение относится к новым аналогам аторвастатина, которые применяют в лечении болезненных состояний, которые поддаются лечению путем ингибирования HMG-CoA редуктазы. Новые аналоги аторвастатина представляют собой соединения формулы (I)(71)(73) Заявитель и патентовладелец: РЕДКС ФАРМА ЛИМИТЕД (GB) Область техники, к которой относится изобретение Настоящее изобретение относится к аторвастатин лактолам. В частности, изобретение относится к применению аторвастатин лактолов в производстве лекарственных препаратов для лечения некоторых болезненных состояний. К числу болезненных состояний, поддающихся лечению соединениями по настоящему изобретению, относятся состояния, которые модулируются ферментом 3-гидрокси-3 метилглютарил-коэнзим А редуктазой (редуктазой HMG-СоА). Поэтому ингибирование фермента является важной терапией многих заболеваний. В изобретении используют производные 6-(3- или 4 карбоксамидозамещенный пиррол-1-ил)-4-гидрокси-3,5-дигидропиран-2-ола. Сведения о предшествующем уровне техники транс-6-[2-(3- или 4-Карбоксамидопиррол-1-ил)алкил]-4-оксипиран-2-оны являются лактонами, которые впервые были описаны в патенте США 4681893. В этом документе также описаны их эквиваленты - соответствующие кислоты с разомкнутым циклом. Сами по себе лактоны, по-видимому,не активны. Однако соответствующие эквивалентные кислоты с разомкнутым циклом используют в качестве ингибиторов биосинтеза холестерина. В патенте США 4681893 также приведены способы производства таких соединений. Аторвастатин, который является R-изомером кислоты с разомкнутым циклом транс-5-(4 фторфенил)-2-(1-метилэтил)-N,4-дифенил-1-[2-тетрагидро-4-окси-6-оксо-2 Н-пиран-2-ил)этил]-1 Нпиррол-3-карбоксамида, и его применение в ингибировании биосинтеза холестерина были впервые описаны в ЕР 0409281. Аторвастатин как в рацемической форме, так и в виде [R-(R,R)]-изомера является сильным ингибитором фермента HMG-CoA. В работе Clin. Invest Med., Volume 24, No 5, p. 258-72, 2001 (Baker and Tamopolsky) было обнаружено, что в то время как статины с открытой конформацией оксикислоты проявляют активность, его циклический аналог лактон не активен. Протекающий в печени гидролиз при щелочном рН приводит к размыканию цикла и таким образом происходит in vivo активация лактоновых пролекарств ловастатина и симвастатина. Однако проблема таких соединений состоит в том, что экстенсивный пресистемный метаболизм приводит к быстрому выведению этих статинов. Аналогично, в работе Trends in Pharmacological Sciences, Volume 19, Issue 1, 1 January 1998, p. 26-37 показано, что для ингибирования редуктазы HMG-CoA неактивные лактоны должны подвергаться метаболизму в соответствующие разомкнутые формы оксикислот. С лактоном и его активной формой с разомкнутым циклом связаны также проблемы устойчивости в течение длительного периода времени. Эта проблема важна для производства активного вещества или при его длительном хранении в аптеке. Например, вследствие дегидратации может удаляться гидроксильная группа. Полученный продукт разложения может иметь двойную связь, сопряженную с карбонильной группой лактона, что облегчает процесс возможного разложения. Аналогично в случае формы с разомкнутым циклом один из возможных продуктов разложения может также содержать двойную связь,сопряженную с карбонильной группой кислоты. Сущность изобретения Поэтому целью настоящего изобретения является предложение соединений, способных ингибировать HMG-CoA редуктазу. Аторвастатин является весьма сильным ингибитором HMG-CoA редуктазы. Поэтому целью настоящего изобретения является также предложение соединений, способных ингибировать редуктазу HMG-CoA, характеризующихся величиной IC50, сравнимой с аторвастатином или выше. Было бы идеально, чтобы эти соединения обладали повышенной устойчивостью и биодоступностью по сравнению с аторвастатином. Целью изобретения также является предложение соединений, обладающих повышенной устойчивостью. В идеале такие соединения должны иметь длительный срок годности при хранении. Целью данного изобретения является предложение соединений, способных ингибироватьHMG-CoA редуктазу, обладающих повышенным сроком хранения. Таким образом, целью настоящего изобретения является предложение соединений, способных ингибировать редуктазу HMG-CoA, обладающих повышенной биодоступностью. Также целью настоящего изобретения является предложение соединений, способных ингибировать редуктазу HMG-CoA и усиливать промотирование липопротеинов высокой плотности (HDL). Также целью настоящего изобретения является предложение соединений,способных понижать уровень липопротеинов низкой плотности (LDL) и усиливать промотирование липопротеинов высокой плотности (HDL). Конкретно, целью настоящего изобретения является предложение соединений, способных понижать уровень липопротеинов низкой плотности (LDL) и усиливать промотирование липопротеинов высокой плотности (HDL) более чем на 10%, предпочтительно более чем на 15% или более. Таким образом, данное изобретение посвящено поиску способов терапии для ингибирования биосинтеза холестерина. Также целью изобретения является лечение группы заболеваний, при которых ингибируется образование холестерина. Данное изобретение предлагает соединения, которые отвечают одной или нескольким указанным целям. Согласно одному варианту настоящее изобретение предлагает соединение формулы (I) и его фармацевтически приемлемые соли и сольваты для лечения болезненного состояния, выбранного из группы, состоящей из гиперхолестеринемии,атеросклероза, гиперлипидемии, сердечно-сосудистого заболевания, ишемической болезни сердца, инфаркта миокарда, инсульта, заболевания периферических артерий, воспаления, деменции, рака, ядерной катаракты, диабета и гипертонии, в которомR1, R4 и один из R2 и R3 независимо выбирают из группы, включающей C1-6-алкил и арил; другие R2 и R3 представляют собой -CONR9R10, где R9 и R10 независимо выбирают из группы,включающей водород и арил;R5 и R6 независимо выбирают из группы, включающей водород, C1-6-алкил, C2-6-алкенил,C3-6-циклоалкил, арил, C1-6-алкиларил и C1-6-алканоилгетероарил, при условии, что всегда оба R5 и R6 не являются водородом;X представляет собой -(CRaRb)m(CRa=CRb)n(CRaRb)o-, где Ra и Rb представляют собой Н и m, n и о независимо равны 0 или 1 при условии, что m+n+о не более 3, и где арильные группы включают ароматические циклические системы, содержащие 6-15 или 16 атомов углерода в цикле; гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5-15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы; каждая из приведенных групп R1-R10 может быть, если это возможно химически, независимо и необязательно замещена 1-5 группами, которые независимо выбирают из группы, включающей галоид,C1-3-алкил, гало-С 1-3-алкил, C1-3-алкоксил, C1-3-галоалкоксил, гидроксил и цианогруппу. Обычно болезненные состояния, которые модулируются HMG-CoA редуктазой, это те состояния,которые можно было бы лечить путем ингибирования фермента с помощью соединений по настоящему изобретению. Согласно другому варианту настоящее изобретение предлагает соединение формулы (I) и его фармацевтически приемлемые соли и сольваты для изготовления лекарственного средства для лечения болезненных состояний, которые поддаются лечению путем ингибирования фермента 3-окси-3-метилглютарил-коэнзим А редуктазы (HMG-CoA редуктаза), в котором R1-R10, Ra, Rb, X, m, n и о определены выше. Согласно другому варианту настоящее изобретение предлагает способ лечения болезненных состояний, которые поддаются лечению путем ингибирования фермента 3-окси-3-метилглютарил-коэнзим А редуктазы (HMG-CoA редуктаза), включающий введение эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли или сольвата, в котором R1-R10, Ra, Rb, X, m, n и о определены выше. Соединения по данному изобретению могут быть активными сами по себе или в некоторых случаях могут подвергаться размыканию цикла в физиологических условиях с образованием соответствующих соединений, обладающих ингибирующей активностью. Фармацевтически приемлемые соли соединений формулы (I) включают соли присоединения кислоты и соли присоединения основания. Подходящие соли присоединения кислот получают из кислот, образующих нетоксичные соли. Примеры включают следующие соли: ацетат, бензоат, безилат, бикарбонат/карбонат, бисульфат/сульфат,борат, камсилат, цитрат, эдизилат, эзилат, формиат, фумарат, глюцептат, глюконат, глюкуронат, гексафторфосфат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидроиодид/иодид, изетионат, лактат,малат, малеат, малонат, мезилат, метилсульфат, нафтилат, 1,5-нафталиндисульфонат, 2-напсилат, никотинат, нитрат, оротат, оксалат, пальмитат, памоат, фосфат/однозамещенный фосфат/двузамещенный фосфат, сахарат, стеарат, сукцинат, тартрат, тозилат и трифторацетат. Подходящие основные соли получают из оснований, которые образуют нетоксичные соли. Примеры включают соли алюминия, аргинина, бензатина, кальция, холина, диэтиламина, диоламина, глицина,лизина, магния, меглюмина, оламина, калия, натрия, трометамина и цинка. Могут образовываться также частично замещенные соли кислот и оснований, например гемисульфат, и частично замещенные соли кальция. Обзор пригодных солей см. в "Handbook of Pharmaceutical Salts: Properties, Selection, and Use" byStahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002). Фармацевтически приемлемые соли соединений формулы (I) можно получить одним или несколькими из трех способов:(i) по реакции соединения формулы (I) с нужной кислотой или основанием;(ii) путем удаления кислотной или основной лабильной защитной группы из подходящего предшественника соединения формулы (I) или раскрытия цикла в подходящем циклическом предшественнике,например лактоне или лактаме, с помощью нужной кислоты или основания или(iii) путем превращения одной соли соединения формулы (I) в другую по реакции с соответствующей кислотой или основанием или с помощью подходящей ионообменной колонки. Все три реакции обычно проводят в растворе. Полученную соль можно осадить и выделить путем фильтрации или выпариванием растворителя. Степень ионизации полученной соли может варьироваться от полной ионизации до почти не ионизированной формы. Соединения по данному изобретению могут существовать как в несольватированной, так и сольватированной форме. Термин "сольват" использован здесь для описания молекулярного комплекса, включающего соединение по изобретению и стехиометрическое количество одной или нескольких молекул фармацевтически приемлемого растворителя, например этанола. Термин "гидрат" используют, когда указанным растворителем является вода. В объем изобретения включены также комплексы типа клатратов, т.е. комплексов включения лекарство-хозяин, в которых в отличие от указанных выше сольватов лекарство и хозяин присутствуют в стехиометрическом или нестехиометрическом количествах. Также сюда включены комплексы лекарства,содержащие два или несколько органических и/или неорганических компонентов, которые могут присутствовать в стехиометрическом или нестехиометрическом количествах. Полученные комплексы могут быть ионизированы, частично ионизированы или не ионизированы. Обзор таких комплексов см. J.Pharm. Sci, 64 (8), 1269-1288 by Haleblian (August, 1975). Все приведенные далее ссылки на соединения формулы (I) включают ссылки на их соли, сольваты и комплексы, сольваты и комплексы их солей. Соединения по данному изобретению включают указанные выше соединения формулы (I), в том числе их полиморфные модификации и кристаллические формы, пролекарства и изомеры (включая оптические, геометрические изомеры и таутомерные формы), как указано ниже, и изотопно меченные соединения формулы (I). Соединения по настоящему изобретению могут существовать перед очисткой в виде смеси энантиомеров в зависимости от метода синтеза. Например, соединения по данному изобретению могут существовать в виде смеси энантиомеров с соотношением от 2:1 до 3:1, хотя могут быть и другие соотношения. Энантиомеры можно разделить известными специалистам традиционными методами. Таким образом, данное изобретение включает индивидуальные энантиомеры, а также их смеси. В случае, когда описанные здесь химические структуры включают символ , это означает, что присутствует смесь энантиомеров с соотношением от 2:1 до 3:1. На некоторых стадиях способа получения соединений (1) бывает необходимо защитить потенциально реакционноспособные группы, которые нежелательно вводить в реакции, и в дальнейшем удалить такие защитные группы. В таком случае можно использовать любые совместимые защитные радикалы. В качестве конкретных способов введения защитных групп и снятия защиты можно использовать способы,описанные T.W. Greene (Protective Groups in Organic Synthesis, A. Wiley-Interscience Publication, 1981) или Р.J. Kocienski (Protecting groups, Georg Thieme Verlag, 1994). Все вышеуказанные реакции и способы получения новых исходных веществ, использованные в предшествующих способах, являются традиционными, и соответствующие реагенты и условия реакций для их осуществления, а также методики выделения целевых продуктов хорошо известны специалистам в данной области, знакомым с литературными прецедентами и примерами синтеза. Кроме того, соединения формулы (I) так же, как промежуточные соединения в их синтезе, можно очищать разными хорошо известными способами, например кристаллизацией или хроматографией. В одном варианте R1 представляет собой C1-6-алкил. В одном варианте R1 представляет собой метил,этил, пропил или бутил. В другом варианте R1 является изопропильным радикалом.-3 021034 В одном варианте R2 представляет собой -CONR9R10. В одном варианте R3 представляет собой арил. В одном варианте R3 является фенилом. В одном варианте R4 представляет собой арил, причем указанная группа может быть необязательно замещена, как это было рассмотрено выше в связи с первым вариантом. В одном варианте R4 является фенилом. В следующем варианте R4 замещен галогеном, предпочтительно фтором. В одном варианте R4 представляет собой 4-фторфенил. В одном варианте R5 выбирают из группы, включающей водород, C1-6-алкил, арил, C1-4-алкиларил. В другом варианте R5 выбирают из группы, включающей водород и C1-4-алкиларил. В альтернативном варианте R5 представляет C1-6-алканоилгетероарил, например метаноилгетероарил. В предпочтительном варианте R5 представляет собой метаноилпиридил, например 2-метаноилпиридин, 3-метаноилпиридин или 4-метаноилпиридин, предпочтительно 3-метаноилпиридин. В одном варианте R5 является водородом. В альтернативном варианте R5 представляет собой C1-4-алкиларил, например -C1-алкил-Ph,-C2-алкил-Ph, -C3-алкил-Ph или -С 4-алкил-Ph. В одном варианте R5 является бензилом. В одном варианте R6 такой же, как R5. В одном варианте R6 выбирают из группы, включающей C1-6-алкил, C2-6-алкенил, C3-6-циклоалкил и арил. В одном варианте R6 является C1-6-алкилом. В другом варианте R6 представляет собой метил, этил,н-пропил или трет-бутил. В альтернативном варианте R6 представляет собой C2-6-алкенил. В следующем альтернативном варианте R6 является аллилом. В еще одном варианте R6 представляет собой С 3-6-циклоалкил. В другом предпочтительном варианте R6 представляет собой циклогексил. В следующем варианте R6 представляет собой арил, такой как необязательно замещенный фенил. В одном варианте R9 представляет собой водород. В одном варианте R10 представляет собой арил. В другом варианте R10 выбирают из группы, включающей арил и C1-4-алкиларил. В альтернативном варианте R10 выбирают из группы, включающей гетероарил и C1-4-алкилгетероарил. В еще одном варианте R10 является фенилом. В одном варианте n равен 0. В другом варианте m=1, n=0 и о=1. В альтернативном варианте m=1,n=0 и о=0. В еще одном варианте m=1, n=1 и о=0 или m=0, n=1 и о=1. Арильные группы включают ароматические циклические системы, содержащие 6-15 или 16 атомов углерода в цикле. Арильные группы могут содержать один цикл, но это могут быть полициклические системы с двумя или несколькими циклами, из которых по меньшей мере один является ароматическим. Арильные группы включают фенил, нафтил, флуоренил, азуленил, инденил и антрил. В одном варианте арил является фенилом. Гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5-15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы. Такая группа может представлять собой полициклическую систему с двумя или несколькими циклами, из которых по меньшей мере один цикл является ароматическим, но чаще это бывает моноциклическая система. Предпочтительными являются моноциклические гетероарильные группы, содержащие 5-6 атомов в цикле. Гетероарильные группы включают пирролил, пиразолил, имидазолил, пиразинил, оксазолил, изоксазолил, тиазолил, фурил, тиофенил, пиридил, пиримидил, бензимидазолил,индолил, изохинолил, хиноксалинил и хинолил. В одном варианте гетероарильную группу выбирают из группы, включающей пиридин, пиримидин,пиразин, пиразол и оксазол. Предпочтительной гетероарильной группой является пиридин. В случае, когда одна или несколько из указанных групп являются необязательно замещенными,предпочтительно, чтобы каждый необязательный заместитель был независимо выбранным атомом галогена. Среди них предпочтительны хлор и фтор. Предпочтительно, чтобы атомы галогена, когда их более одного, были одинаковыми. В одном варианте R1 представляет собой C1-4-алкил, предпочтительно изопропил, и R4 представляет собой необязательно замещенный арил, предпочтительно 4-фторфенил. В другом варианте R2 представляет -CONR9R10, в которой R9 представляет собой необязательно замещенный арил, предпочтительно фенил; R10 является водородом и R3 представляет собой необязательно замещенный арил, предпочтительно фенил. В следующем варианте R1 представляет собой C1-4-алкил, предпочтительно изопропил; R2 представляет собой -CONR9R10, в которой R9 представляет собой необязательно замещенный арил, предпочтительно фенил; R10 явяется водородом; R3 представляет собой необязательно замещенный арил, предпочтительно фенил, и R4 является необязательно замещенным арилом, предпочтительно 4-фторфенилом. Соотношение между группами R5 и R6 является важным для активности соединений. Таким образом, R5 и R6 оба не могут быть водородом. В одном варианте R5 не является водородом. В другом варианте R6 не является водородом. В другом варианте R5 представляет собой необязательно замещенный бензил и R6 представляет собой необязательно замещенный C1-6-алкил. В этом варианте предпочтительно, чтобы алкильная группа представляла собой пропил или бутил, предпочтительно изопропил или трет-бутил. В другом вариантеR5 представляет собой необязательно замещенный бензил и R6 представляет собой необязательно замещенный C2-6-алкенил. В этом варианте предпочтительно, чтобы алкенильная группа была аллилом.-4 021034 В другом варианте R5 представляет собой Н и R6 является необязательно замещенным C1-6-алкилом. В этом варианте предпочтительно, чтобы алкильная группа была пропилом. В еще одном варианте R5 представляет Н и R6 представляет собой C3-6-циклоалкил. В этом варианте предпочтительно, чтобы циклоалкильная группа была циклогексилом. В другом варианте R5 представляет собой Н и R6 является необязательно замещенным арилом. В этом варианте предпочтительно, чтобы необязательно замещенный арил представлял собой необязательно замещенный фенил, например фенил, замещенный алкокси (например, метокси). В одном варианте R5 представляет собой C1-6-алканоилгетероарил и R6 представляет собой необязательно замещенный C1-6-алкил. В этом варианте предпочтительно, чтобы алкильная группа представляла собой метил и C1-6-алканоилгетероарильная группа представляла собой метаноилгетероарил (например,метаноилпиридин). В одном варианте соединение имеет структуру, которую выбирают из следующих: Как указано выше, известно, что статины, имеющие конформацию открытой оксикислоты, обладают эффектом ингибирования HMG-CoA редуктазы. Известно также, что лактон - аналог такой оксикислоты с замкнутым кольцом - не активен в ингибировании HMG-CoA редуктазы, и для активации лактона необходима его дециклизация. Однако авторы установили, что функционализированные лактолы по настоящему изобретению сами по себе оказывают значительное ингибирующее действие на HMG-CoA редуктазу. Это удивительно ввиду того, что эти молекулы в замкнутой циклической форме имеют конформационное напряжение. Примеры болезненных состояний, которые можно лечить ингибированием редуктазы HMG-CoA,включают гиперхолестеринемию, атеросклероз и гиперлипидемию. Статины используют для вторичной профилактики сердечно-сосудистых заболеваний или для первичного предотвращения сердечнососудистых заболеваний в случае, когда возрастает риск сердечно-сосудистых заболеваний. Поэтому ожидается, что соединения по настоящему изобретению найдут применение в лечении или профилактике сердечно-сосудистых заболеваний благодаря их ингибиторной активности. Примеры сердечнососудистых заболеваний, которые можно лечить соединениями по настоящему изобретению, включают ишемическую болезнь сердца, инфаркт миокарда, инсульт и болезни периферических артерий. Кроме того, эти соединения могут быть весьма полезны в лечении воспалений, деменции, рака, ядерной ката-5 021034 ракты, диабета и гипертонии. Болезненные состояния, которые можно лечить путем ингибирования редуктазы HMG-CoA, могут наблюдаться у человека и животных. Эти соединения особенно предназначены для людей. Производные аторвастатина по настоящему изобретению можно анализировать по следующей методике, в которой определяют уровень триглицеридов в плазме после лечения крыс соединением по настоящему изобретению (или аторвастатином). Считается, что определение изменения в уровне триглицеридов в плазме крыс является хорошим тестом на активность редуктазы HMG СоА. Использовали следующую методику: самцы крыс SD (Harlan) содержали в группах по 6 особей при 12-часовых циклах свет-темнота (свет включали в 07.00 ч) и свободном доступе к пище (обычная лабораторная еда) и воде. Животные массой 148-183 г были распределены для лечения по 8 особей по массе тела и тесты выравнивали по клеткам. Приготовили растворы четырех аналогов аторвастатина с концентрацией 5 мг/мл (например, в смеси 10% PEG300/10% кремафор/80% метилцеллюлоза (0.5% и суспензию, содержащую 5 мг/кг аторвастатина (в смеси с 0.5% Tween в 0.5% метилцеллюлозе). Крысам вводили перорально один из четырех аналогов аторвастатина (25 мг/кг) или аторвастатин(25 мг/кг перорально) дважды в сутки в течение 3-5 дней. Через 16 ч после введения последней дозы взяли последние образцы плазмы, выдержали при -20 С и перенесли на сухом льду для анализа на уровень триглицеридов. Для каждой временной точки проводили однофакторный дисперсионный анализ (однофакторнымANOVA) и апостериорный тест Даннетта. Способы синтеза соединений по настоящему изобретению описаны в WO2005/012246, в частности в примерах. Описание патента в WO2005/012246 в отношении методик синтеза составляет часть описания настоящего изобретения. Для краткости подробности этих методик синтеза здесь не воспроизводятся, но включены ссылкой в описание данного документа. Настоящее изобретение также включает синтез всех фармацевтически приемлемых изотопно меченных соединений формулы (I), в которых один или несколько атомов замещены атомами с тем же атомным номером, но атомной массой или массовым числом, отличными от атомной массы или массового числа, обычно встречающихся в природе. Примеры изотопов, пригодных для введения в соединения по данному изобретению, включают изотопы водорода, такие как 2 Н и 3 Н, углерода, такие как 11 С, 13 С и 14 С, хлора, такие как 36Cl, фтора, такие как 18F, иода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15 О, 17 О и 18 О, фосфора,такие как 32 Р, и серы, такие как 35S. Некоторые изотопно меченные соединения, например, такие, которые включают радиоактивный изотоп, полезны при изучении лекарства и/или его распределения в тканях субстрата. Особенно полезны для этой цели радиоактивные изотопы: тритий, т.е. 3 Н, и углерод-14, т.е. 14 С, ввиду легкости их введения и детектирования. Замещение более тяжелыми изотопами типа дейтерия, т.е. 2 Н, может иметь некоторые терапевтические преимущества, обусловленные повышенной метаболической устойчивостью, например увеличенным временем полупревращения in vivo или пониженным требованием к дозе, и, следовательно, при некоторых обстоятельствах может быть предпочтительным. Замещение позитрон-активными изотопами, такими как 11 С, 18F, 15O и 13N, можно использовать для исследования степени занятости рецептора субстратом методом позитронной эмиссионной топографии(ПЭТ). Изотопно меченные соединения обычно можно синтезировать традиционными методами, известными специалистам в данной области, или способами, аналогичными описанным, с применением соответствующих изотопно меченных реагентов вместо применявшихся раньше немеченых реагентов. Во всем описании и формуле термины "включать" или "содержать" и их варианты, например"включающий" и "содержащий", означают "включающий, но не ограничивающийся этим" и не исключают другие фрагменты, добавки, компоненты, целые числа или стадии. Во всем описании и формуле единственное число охватывает множественное, если контекст не требует другого. В частности, при использовании неопределенного артикля описание следует понимать как включающее множественность так же, как единственность, если контекст не требует иного. Особенности, целые числа, характеристики, соединения, химические фрагменты или группы, описанные в связи с конкретным вариантом, вариантом или примером изобретения, следует понимать как применимые к любому другому описанному здесь аспекту, варианту или примеру, за исключением случая их несовместимости. Сведения, подтверждающие возможность осуществления изобретения Общая методика. Все анализы проводили в реакционном буфере, содержащем 100 нМ KxPO4 при рН 7.2, 1 мМ ЭДТА,500 мМ KCl и 1 мг/мл BSA. Концентрации каждого из NADPH и HMG-CoA составляли 200 мкМ. Концентрация используемого фермента не известна, хотя эта концентрация в 10 раз ниже концентрации исходного продажного раствора. Ингибиторы растворяли в 75% ДМСО. Когда устанавливали, что ингибиторы не растворяются или только частично растворяются в 75% ДМСО, использовали 100% ДМСО. Реакцию активировали путем добавления фермента и после этого встряхивали в течение 12 с. Затем каждые 20 с следили за поглощением в течение 600 с. В начальных тестах концентрацию каждого ингибитора устанавливали на уровне 50 нМ для идентификации лучших ингибиторов по сравнению с известным ингибитором правастатином. После такой идентификации проводили анализы, варьируя концентрации ингибиторов от 0 до 50 нМ, и рассчитывали величины IC50. Пример 1. Применили следующую методику с использованием набора для анализа редуктазы HMG-CoA отSigma-Aldrich (номер в каталоге CS1090). Анализ основан на стектрофотометрическом определении уменьшения поглощения раствора NADPH при 340 нм. Уменьшение поглощения вызвано окислениемNADPH под действием каталитической субъединицы HMGR в присутствии субстрата HMG-СоА. Эффективное ингибирование HMG-CoA ведет к уменьшению окисления NADPH, которое, в свою очередь,ведет к меньшему снижению поглощения при 340 нм во времени. Это проиллюстрировано следующей схемой реакции: Соединениями, проявляющими наибольшую ингибирующую активность, являются те, которые минимально уменьшают поглощение. Приготовление раствора для анализа. Для приготовления реагентов и в ходе опытов использовали воду сверхвысокой чистоты (с удельным сопротивлением 17 M-см) или ее эквивалент. Вначале приготовили буферный аналитический раствор следующим образом: 0.2 мл 5-кратного аналитического буферного раствора (номер в каталоге А 5981) с помощью 0.8 мл сверхчистой воды. Полученный буферный раствор для дальнейшего использования держали на льду или хранили при -20C. Затем 25 мг NADPH (номер в каталоге N6505) разбавили 1.5 мл буферного раствора. Рабочие дозы полученного раствора NADPH хранили при -20C. В ходе всего анализа раствор субстрата HMG-CoA (номер в каталоге S7447), редуктазу HMG-CoA(номер в каталоге Н 8789) и раствор ингибитора (например, правастатина, номер в каталоге I5909) держали на льду. 1. Перед началом анализа на спектрофотометре установили кинетическую программу: 37C, мониторинг при 340 нм, 1 мл образца, замер через каждые 20 с в течение 10 мин. 2. Добавили соответствующие объемы реакционных растворов согласно табл. 1 (1 мл анализ). Таблица 1 Объемы реакции на 1 мл образцаa) добавить буферный раствор ко всем образцам;c) добавить разбавленный раствор NADPH ко всем образцам;d) добавить раствор субстрата (HMG-CoA) ко всем образцам;f) тщательно перемешать образцы. 3. Сразу запустили кинетическую программу. Активность продукта рассчитывали по следующему уравнению:TV - общий объем реакции в мл (1 мл в кюветах);LP - длина оптического пути в см (1 см кювета). Пример 2. В следующей таблице приведены величины IC50 для конкретных соединений аторвастатина по настоящему изобретению. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Применение соединения формулы (I) или его фармацевтически приемлемой соли или сольватаR1, R4 и один из R2 и R3 независимо выбирают из группы, состоящей из C1-6-алкила и арила; другой из R2 и R3 представляет собой -CONR9R10, где R9 и R10 независимо выбирают из группы, состоящей из водорода и арила;R5 и R6 независимо выбирают из группы, состоящей из водорода, C1-6-алкила, C2-6-алкенила,C3-6-циклоалкила, арила, C1-6-алкиларила и C1-6-алканоилгетероарила, при условии, что всегда R5 и R6 оба не являются водородом;X представляет собой -(CRaRb)m(CRa=CRb)n(CRaRb)o-, где Ra и Rb представляют собой Н и m, n и о независимо равны 0 или 1 при условии, что m+n+о не более 3, и где арильные группы включают ароматические циклические системы, содержащие 6-15 или 16 атомов углерода в цикле; гетероарильные группы включают ароматические гетероциклические циклические системы, содержащие 5-15 или 16 атомов в цикле с 1-4 гетероатомами, которые независимо выбирают из азота, кислорода и серы; каждая из приведенных групп R1-R10 может быть, если это возможно химически, независимо и необязательно замещена 1-5 группами, которые независимо выбирают из группы, состоящей из галогена,C1-3-алкила, гало-С 1-3-алкила, C1-3-алкоксила, C1-3-галоалкоксила, гидроксила и цианогруппы. 2. Применение по п.1, где R1 представляет собой C1-6-алкил.-9 021034 3. Применение по п.1 или 2, где R2 представляет собой -CONR9R10, где R9 является Н и R10 является арилом. 4. Применение по любому из пп.1-3, где R3 является арилом. 5. Применение по любому из предшествующих пунктов, где R4 является необязательно замещенным арилом. 6. Применение по любому из предшествующих пунктов, где R1 представляет собой изопропил, R2 представляет -CONHPh, R3 представляет собой фенил и R4 представляет собой 4-фторфенил. 7. Применение по любому из предшествующих пунктов, где R5 выбирают из группы, состоящей из водорода, арила, C1-6-алкиларила и C1-6-алканоилгетероарила. 8. Применение по п.7, где R5 является водородом. 9. Применение по п.7, где R5 выбирают из группы, состоящей из -C1-алкил-Ph, -С 2-алкил-Ph,-C3-алкил-Ph и -С 4-алкил-Ph. 10. Применение по п.9, где R5 представляет собой бензил. 11. Применение по п.7, где R5 представляет собой C1-6-алканоилпиридин. 12. Применение по п.11, где R5 представляет собой 3-метаноилпиридин. 13. Применение по любому из предшествующих пунктов, где R6 выбирают из группы, состоящей из водорода, C1-6-алкила, C2-6-алкенила, C3-6-циклоалкила, необязательно замещенного арила иC1-6-алкиларила. 14. Применение по п.13, где R6 выбирают из группы, состоящей из C1-6-алкила, C3-6-циклоалкила,C2-6-алкенила и необязательно замещенного арила. 15. Применение по п.14, где R6 выбирают из группы, состоящей из метила, этила, пропила, бутила,циклогексила и аллила. 16. Применение по п.13, где R6 представляет собой необязательно замещенный арил. 17. Применение по п.16, где R6 выбирают из группы, состоящей из C1-6-алкоксизамещенного фенила. 18. Применение по п.16, где R6 представляет собой 2,4-диметоксифенил. 19. Применение по любому из пп.1-6, где R5 является водородом и R6 является C1-6-алкилом,C3-6-циклоалкилом или необязательно замещенным арилом. 20. Применение по любому из пп.1-6, где R5 является необязательно замещенным бензилом и R6 является необязательно замещенным C1-6-алкилом или необязательно замещенным C2-6-алкенилом. 21. Применение по любому из пп.1-6, где R5 представляет собой C1-6-алканоилгетероарил и R6 представляет собой необязательно замещенный C1-6-алкил. 22. Применение по любому из предшествующих пунктов, где каждый Ra представляет собой Н, каждый Rb представляет собой Н и m=1, n=0 и о=1. 23. Применение по п.1, где структуру соединения выбирают из следующих:
МПК / Метки
МПК: A61K 31/40, A61P 3/06, A61P 9/10, A61P 9/00
Метки: лечении, которые, аторвастатин, применение, модулируются, редуктазой, состояний, 3-гидрокси-3-метилглютарил-коэнзим, лактолов
Код ссылки
<a href="https://eas.patents.su/11-21034-primenenie-atorvastatin-laktolov-v-lechenii-sostoyanijj-kotorye-moduliruyutsya-3-gidroksi-3-metilglyutaril-koenzim-a-reduktazojj.html" rel="bookmark" title="База патентов Евразийского Союза">Применение аторвастатин лактолов в лечении состояний, которые модулируются 3-гидрокси-3-метилглютарил-коэнзим а редуктазой</a>











