Новый способ получения функционализированных бензоциклобутенов и их применение в синтезе ивабрадина и его аддитивных солей с фармацевтически приемлемой кислотой
Номер патента: 17503
Опубликовано: 30.01.2013
Авторы: Пиккарди Рикардо, Пегльон Жан-Луи, Шомонте Манон, Одик Никола, Бодуан Оливье
Формула / Реферат
1. Способ получения соединений формулы (IV)

где R1, R2, R3 и R4, которые могут быть идентичными или различными, каждый, представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, атом фтора, атом хлора, защищенную аминогруппу, защищенную гидроксильную группу, алкоксикарбонильную группу, в которой алкоксильная группа является линейной или разветвленной (C1-C6), или CF3-группу, или R1=R4=H и R2 и R3 вместе с несущими их атомами углерода образуют группу 1,3-диоксолана;
R5 представляет собой насыщенную или ненасыщенную, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)гидроксиалкильную группу, в которой гидроксильная группа является защищенной, или CO2R7-группу, в которой R7 представляет собой линейную или разветвленную (C1-C6)алкильную группу;
R6 представляет собой группу циано или группу CO2R8, в которой R8 является линейной или разветвленной (C1-C6)алкильной группой,
при этом способ характеризуется тем, что соединение формулы (V)

где R1, R2, R3, R4, R5, R6 являются такими, как определено выше; и
X представляет собой атом галогена, предпочтительно атом брома, или группу трифлата,
подвергают реакции циклизации в присутствии системы катализатор/лиганд, включающей палладиевый катализатор и органический фосфин, выбранный из три-трет-бутилфосфина, 2-бифенил-ди-трет-бутилфосфина, 1,2,3,4,5-пентафенил-1'-(ди-трет-бутилфосфино)ферроцена и трис-(4-метокси-2-метилфенил)фосфина или соли фосфония упомянутых фосфинов, в присутствии основания, в органическом растворителе.
2. Способ получения в соответствии с п.1, характеризующийся тем, что палладиевый катализатор является выбранным из Pd(OAc)2, Pd(dba)2, Pd2(dba)3, PdCl2, PdCl2(CH3CN)2, PdBr2 и трет-ди-(m-ацетат)-бис-[o-(ди-o-толилфосфин)бензил]дипалладия.
3. Способ получения в соответствии с любым из пп.1 или 2, характеризующийся тем, что палладиевый катализатор представляет собой Pd(OAc)2.
4. Способ получения в соответствии с любым из пп.1-3, характеризующийся тем, что органический фосфин представляет собой три-трет-бутилфосфин.
5. Способ получения в соответствии с любым из пп.1-4, характеризующийся тем, что соль фосфония представляет собой тетрафторборат, гексафторфосфат или гексафторантимонат фосфония.
6. Способ получения в соответствии с п.5, характеризующийся тем, что соль фосфония представляет собой тетрафторборат три-трет-бутилфосфония.
7. Способ получения в соответствии с любым из пп.1-6, характеризующийся тем, что используемое основание является выбранным из K2CO3, Cs2CO3, Na2CO3, K3PO4, KHCO3, t-BuCO2Na, t-BuCO2K и
t-BuCO2Cs.
8. Способ получения в соответствии с п.7, характеризующийся тем, что используемое основание представляет собой K2CO3.
9. Способ получения в соответствии с любым из пп.1-8, характеризующийся тем, что используемый органический растворитель является выбранным из ДМФ, N,N-диметилацетамида, N-метилпирролидина, ксилена и мезитилена.
10. Способ получения в соответствии с п.9, характеризующийся тем, что используемый органический растворитель представляет собой ДМФ.
11. Способ получения в соответствии с любым из пп.1-10, характеризующийся тем, что температура реакции составляет от 100 до 150°C.
12. Способ получения соединений формулы (VIIa)
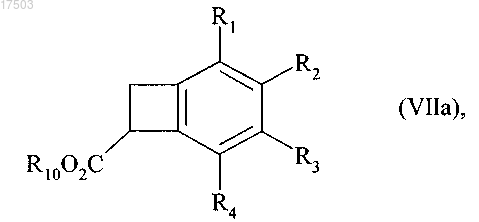
где R1, R2, R3 и R4 являются такими, как определено в п.1; и
R10 представляет собой атом водорода или линейную или разветвленную (C1-C6)алкильную группу,
характеризующийся тем, что соединения формулы (Va), частный случай соединений формулы (V), в которых R5=CO2R7 и R6=CO2R8:
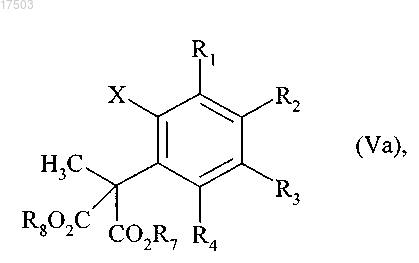
где R1, R2, R3, R4, R7, R8 и X являются такими, как определено в п.1,
превращают в соединения формулы (IVa), частный случай соединений формулы (IV), в которых R5=CO2R7 и R6=CO2R8:

где R1, R2, R3, R4, R7 и R8 являются такими, как определено в п.1,
в соответствии со способом п.1,
затем соединение формулы (IVa) превращают в соединение формулы (VIa)
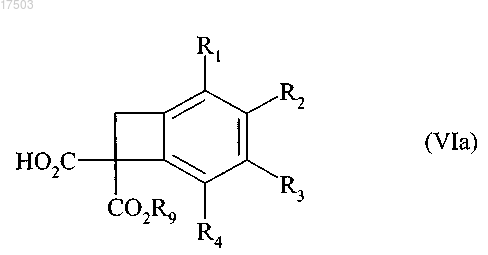
где R1, R2, R3 и R4 являются такими, как определено в п.1; и
R9 представляет собой линейную или разветвленную (C1-C6)алкильную группу,
путем реакции омыления эстера или реакции гидролиза, а соединение формулы (VIa) приводит к получению соединения формулы (VIIa) посредством реакции декарбоксилирования.
13. Способ в соответствии с п.12 для получения соединений формулы (VIIb), частного случая соединений формулы (VIIa), где R1=R4=H и R2=R3=OCH3.
14. Соединение формулы (IVa)

где R1, R2, R3 и R4, которые могут быть идентичными или различными, каждый, представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, атом фтора, атом хлора, аминогруппу, защищенную группой, выбранной из нозила, тозила, мезила, ацетила, трет-бутоксикарбонила, бензила и фталимида, гидроксильную группу, защищенную группой, выбранной из триизопропилсилила, трет-бутилдиметилсилила, тетрагидропирана, бензила, параметоксибензила, тритила, ацетила и пивалоила, алкоксикарбонильную группу, в которой алкоксильная группа является линейной или разветвленной (C1-C6), или CF3-группу, или R1=R4=H и R2 и R3 вместе с несущими их атомами углерода образуют группу 1,3-диоксолана;
R7 и R8, которые могут быть идентичными или различными, каждый, представляют собой линейную или разветвленную (C1-C6)алкильную группу.
15. Соединение формулы (VIb)
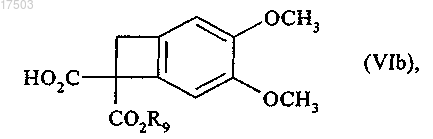
где R9 представляет собой линейную или разветвленную (C1-C6)алкильную группу.
16. Соединение формулы (VIIc)
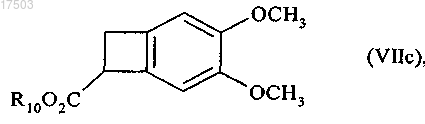
где R10 представляет собой линейную или разветвленную (C1-C6)алкильную группу.
17. Способ синтеза ивабрадина, его фармацевтически приемлемых солей и их гидратов, характеризующийся тем, что соединение формулы (Vb)
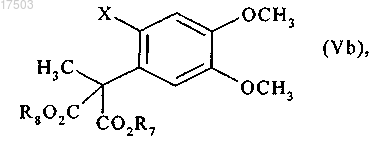
где R7, R8 и X являются такими, как определено в п.1,
превращают в соответствии со способом п.13 в соединение формулы (VIIb)
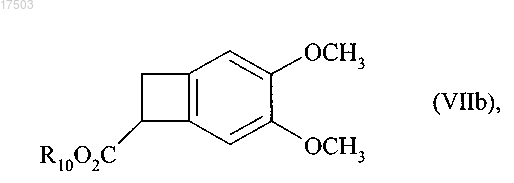
где R10 является таким, как определено в п.12,
затем соединение формулы (VIIb) превращают в соединение формулы (VIII)
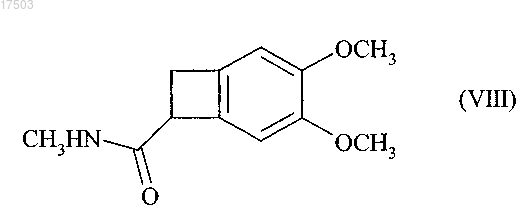
путем реакции с метиламином, восстановление которого обеспечивает получение соединения формулы (III)
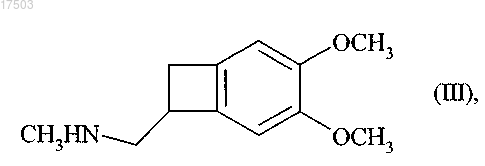
разделение которого в присутствии камфорсульфоновой кислоты обеспечивает получение соединения формулы (II)
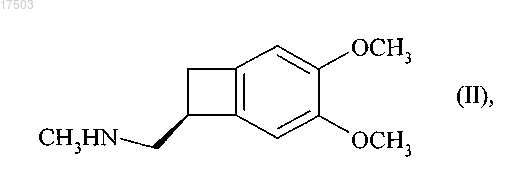
которое превращают в ивабрадин формулы (I)
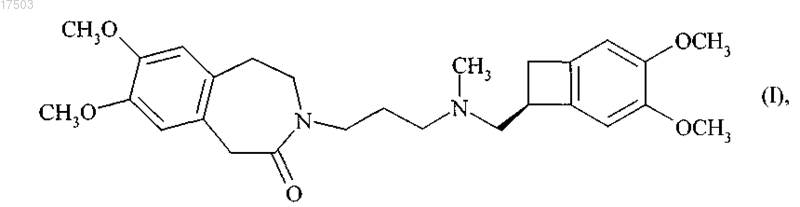
который может быть необязательно превращен в его аддитивные соли с фармацевтически приемлемой кислотой, выбранной из хлористо-водородной, бромисто-водородной, серной, фосфорной, уксусной, трифторуксусной, молочной, пировиноградной, малоновой, янтарной, глутаровой, фумаровой, виннокаменной, малеиновой, лимонной, аскорбиновой, щавелевой, метансульфоновой, бензолсульфоновой и камфорной кислот, и в их гидраты.
Текст
НОВЫЙ СПОСОБ ПОЛУЧЕНИЯ ФУНКЦИОНАЛИЗИРОВАННЫХ БЕНЗОЦИКЛОБУТЕНОВ И ИХ ПРИМЕНЕНИЕ В СИНТЕЗЕ ИВАБРАДИНА И ЕГО АДДИТИВНЫХ СОЛЕЙ С ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМОЙ КИСЛОТОЙ Изобретение относится к способу получения соединений формулы (IV) где R1, R2, R3 и R4, которые могут быть идентичными или различными, каждый, представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, атом фтора, атом хлора, защищенную аминогруппу,защищенную гидроксильную группу, алкоксикарбонильную группу, в которой алкоксильная группа является линейной или разветвленной (C1-C6), или CF3-группу, или R1=R4=H и R2 иR3 вместе с несущими их атомами углерода образуют группу 1,3-диоксолана; R5 представляет собой насыщенную или ненасыщенную, линейную или разветвленную (C1-C6)алкильную группу,линейную или разветвленную (C1-C6)гидроксиалкильную группу, в которой гидроксильная группа является защищенной, или CO2R7-группу, в которой R7 представляет собой линейную или разветвленную (C1-C6)алкильную группу; R6 представляет собой группу циано или CO2R8 группу, в которой R8 является линейной или разветвленной (C1-C6)алкильной группой, Кроме того, изобретение относится к применению в синтезе ивабрадина, его аддитивных солей с фармацевтически приемлемой кислотой и их гидратов.(71)(73) Заявитель и патентовладелец: ЛЕ ЛАБОРАТУАР СЕРВЬЕ; САНТР НАСЬОНАЛЬ ДЕ ЛЯ РЕШЕРШ СЬЕНТИФИК; УНИВЕРСИТЕ КЛОД БЕРНАР ЛИОН 1 (FR) 017503 Настоящее изобретение относится к способу получения функционализированных бензоциклобутенов и к их применению в синтезе ивабрадина, его аддитивных солей с фармацевтически приемлемой кислотой. Ивабрадин формулы (I) или 3-3-(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил(метил)амино]пропил-7,8 диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-он, а также его аддитивные соли с фармацевтически приемлемой кислотой, в частности гидрохлорид, имеют весьма ценные фармакологические и терапевтические свойства, в частности брадикардические свойства, которые делают эти соединения полезными в лечении и предотвращении различных клинических случаев миокардиальной ишемии, таких как стенокардия, инфаркт миокарда и ассоциированные нарушения сердечного ритма, а также при различных патологиях, которые вовлекают расстройства сердечного ритма, в частности при наджелудочковых расстройствах ритма, и при сердечной недостаточности. Способ получения и терапевтическое применение ивабрадина и его аддитивных солей с фармацевтически приемлемой кислотой, в частности его гидрохлорида, были описаны в европейской патентной заявке EP 0534859. Описание к патенту представляет синтез ивабрадина при использовании в качестве исходного материала соединения формулы (II) Соединение формулы (II) получают путем разделения с помощью камфорсульфоновой кислоты соединения формулы (III) Соединение формулы (II) является важным промежуточным соединением синтеза ивабрадина. Настоящее изобретение относится к способу получения функционализированных бензоциклобутенов и к их применению в синтезе ивабрадина, его аддитивных солей с фармацевтически приемлемой кислотой и их гидратов при использовании соединения формулы (II). Способ получения функционализированных бензоциклобутенов был описан в Angewandte Chemie,International Edition. 2003, 42, 5736-5740. Эта публикация описывает возможность использования активации C(sp3)-H связи для способа получения функционализированных бензоциклобутенов при использовании каталитической системы палладия. В частности, настоящее изобретение относится к способу получения соединений формулы (IV) где R1, R2, R3 и R4, которые могут быть идентичными или различными, каждый, представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, атом фтора, атом хлора, защищенную аминогруппу, защищенную гидроксигруппу, алкоксикарбонильную группу, в которой алкоксигруппа является линейной или разветвленной(C1-C6), или CF3-группу, или R1=R4=H и R2 и R3 вместе с несущими их атомами углерода образуют группу 1,3-диоксолана;R5 представляет собой насыщенную или ненасыщенную, линейную или разветвленную(C1-C6)алкильную группу, линейную или разветвленную (C1-C6)гидроксиалкильную группу, в которой гидроксильная группа является защищенной, или CO2R7-группу, в которой R7 представляет собой линейную или разветвленную (C1-C6)алкильную группу;R6 представляет собой группу циано или CO2R8-группу, в которой R8 является линейной или разветвленной (C1-C6)алкильной группой,-1 017503 при этом способ характеризуется тем, что соединение формулы (V)X представляет собой атом галогена, предпочтительно атом брома, или группу трифлата,подвергают реакции циклизации в присутствии системы катализатор/лиганд, включающей палладиевый катализатор и органический фосфин, выбранный из три-трет-бутилфосфина, 2-бифенил-ди-третбутилфосфина,1,2,3,4,5-пентафенил-1'-(ди-трет-бутилфосфино)ферроцена и трис-(4-метокси-2 метилфенил)фосфина, или соли фосфония упомянутых фосфинов, в присутствии основания, в органическом растворителе. Защищенная гидроксильная группа или защищенная гидроксильная функция означает гидроксильную функцию, замещенную защитной группой, обычной для этой функции. Среди таких защитных групп, которые могут быть упомянуты, без какого-либо ограничения следует упомянуть группы, содержащие силил, такие как триизопропилсилил и трет-бутилдиметилсилил, и группы тетрагидропирана,бензила, параметоксибензила, тритила, ацетила и пивалоила. Защищенная аминогруппа означает функцию амина, замещенную защитной группой, обычной для этой функции. Среди таких защитных групп, которые могут быть упомянуты, без какого-либо ограничения следует упомянуть группы нозила, тозила, мезила, ацетила, трет-бутоксикарбонила, бензила и фталимида. Среди палладиевых катализаторов, которые могут быть использованы, следует упомянуть без какого-либо ограничения Pd(OAc)2, Pd(dba)2, Pd2(dba)3, PdCl2, PdCl2(CH3CN)2, PdBr2 или трет-ди-(-ацетат)бис-[o-(ди-o-толилфосфин)бензил]дипалладий (катализатор Германа). Предпочтительно используемый палладиевый катализатор представляет собой Pd(OAc)2. Предпочтительно используемый органический фосфин представляет собой три-трет-бутилфосфин. Среди фосфониевых солей, которые могут использоваться, следует упомянуть без какого-либо ограничения тетрафторбораты фосфония, гексафторфосфаты фосфония и гексафторантимонаты фосфония. Предпочтительно используемая соль фосфония представляет собой тетрафторборат три-третбутилфосфония. Среди оснований, которые могут использоваться, следует упомянуть без какого-либо ограниченияK2CO3, Cs2CO3, Na2CO3, K3PO4, KHCO3, t-BuCO2Na, t-BuCO2K и t-BuCO2Cs. Предпочтительно используемое основание представляет собой K2CO3. Среди растворителей, которые могут использоваться, следует упомянуть без какого-либо ограничения ДМФ, N,N-диметилацетамид, N-метилпирролидин, ксилен и мезитилен. Предпочтительно используемый растворитель представляет собой ДМФ. Температура реакции предпочтительно составляет от 100 до 150C. В соответствии с предпочтительным воплощением настоящее изобретение относится к способу получения соединений формулы (IVa), частных случаев соединений формулы (IV), в которых R5=CO2R7 и где R1, R2, R3, R4, R7 и R8 являются такими, как определено выше,начиная от соединений формулы (Va), частных случаев соединений формулы (V), в которых R5=CO2R7 и-2 017503 В соответствии с другим предпочтительным воплощением настоящее изобретение относится к способу получения соединений формулы (IVb), частных случаев соединений формулы (IVa), в которых где R7 и R8 являются такими, как определено выше,начиная от соединений формулы (Vb), частных случаев соединений формулы (Va), в которых R1=R4=H и где R7, R8 и X являются такими, как определено выше. Соединения формулы (IVa), полученные в соответствии со способом в соответствии с изобретением, могут использоваться для получения соединений формулы (VIa)R9 представляет собой линейную или разветвленную (C1-C6)алкильную группу,путем реакции омыления эстера или реакции гидролиза, потом из соединений формулы (VIa) получают соединения формулы (VIIa)R10 представляет собой атом водорода или линейную или разветвленную (C1-C6)алкильную группу,посредством реакции декарбоксилирования. Гидролиз или омыление функции эстера соединений формулы (IVb) приводят к получению соединений формулы (VIb), частных случаев соединений формулы (VIa), в которых R1=R4=H и R2=R3=OCH3: где R9 является таким, как определено выше. Декарбоксилирование соединений формулы (VIb) потом приводит к получению соединений формулы (VIIb), частных случаев соединений формулы (VIIa), в которых R1=R4=H и R2=R3=OCH3: где R10 является таким, как определено выше. Соединения формулы (VIIb), полученные в соответствии со способом в соответствии с изобретением, являются полезными в синтезе ивабрадина, его аддитивных солей с фармацевтически приемлемой кислотой и их гидратов.-3 017503 Например, их реакция с метиламином приводит к образованию соединений формулы (VIII) восстановление которых приводит к получению соединений формулы (III) растворение которых при использовании камфорсульфоновой кислоты приводит к получению соединений формулы (II) или 3-3-(7S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил]метил(метил)амино]пропил-7,8 диметокси-1,3,4,5-тетрагидро-2H-3-бензазепин-2-он, который может быть необязательно превращен в его аддитивные соли с фармацевтически приемлемой кислотой, выбранной из хлористо-водородной,бромисто-водородной, серной, фосфорной, уксусной, трифторуксусной, молочной, пировиноградной,малоновой, янтарной, глутаровой, фумаровой, виннокаменной, малеиновой, лимонной, аскорбиновой,щавелевой, метансульфоновой, бензолсульфоновой и камфорной кислот, и в их гидраты. Среди способов, известных для осуществления превращения соединений формулы (II) в ивабрадин,могут быть упомянуты те, которые описаны в патентных заявках EP 0534859 и EP 1589005. Получение соединений формулы (IVb) с хорошим выходом, таким образом, является особенно полезным в синтезе ивабрадина, его аддитивных солей с фармацевтически приемлемой кислотой и их гидратов. Соединения формулы (IVa), которые представляют собой частные случаи соединений формулы(IV), где R5=CO2R7 и R6=CO2R8, а также соединений формулы (VIb), а также соединений формулы (VIIc),которые представляют собой частные случаи соединений формулы (VIIb), где R10 представляет собой линейную или разветвленную (C1-C6)алкильную группу, являются новыми продуктами, которые полезны в качестве промежуточных соединений синтеза в химической или фармацевтической промышленности, в частности в синтезе ивабрадина, его аддитивных солей с фармацевтически приемлемой кислотой и их гидратов, и, как таковые, составляют цельную часть настоящего изобретения. Используемый список сокращений:dba - дибензилиденацетон; ДМФ - N,N-диметилформамид; ДМСО - диметилсульфоксид; экв. - эквивалент; ТГФ - тетрагидрофуран. Примеры, приведенные ниже, иллюстрируют изобретение. Общая процедура А для получения бензоциклобутенов с помощью активации C-H связи. Вводили арилбромид (1 ммоль), Pd(OAc)2 (0,1 экв.), P(t-Bu)3HBF4 (0,2 экв.) и безводный K2CO3(1,3 экв.) в сухой герметически запечатываемый сосуд Шленка, оснащенный магнитной мешалкой. Очищали сосуд Шленка и помещали под аргон. Прибавляли 4 мл безводного ДМФ в атмосфере аргона и герметически закрывали сосуд Шленка, а потом подвергали перемешиванию на масляной бане, предварительно нагретой до 140C, до полного исчезновения арилбромида в ГХ/МС. После возвращения к условиям комнатной температуры реакционную смесь разводили диэтиловым этером и фильтровали через целит. Органический раствор промывали с помощью насыщенного водного раствора NaCl и высушивали над MgSO4, а оставшийся растворитель выпаривали при сниженном давлении. Сырьевой продукт реакции очищали с помощью флэшхроматографии с получением бензоциклобутена.-4 017503 Общая процедура В для получения бензоциклобутенов с помощью активации C-H связи. Вводили арилбромид (1 ммоль), Pd(OAc)2 (0,05 экв.), P(t-Bu)3HBF4 (0,1 экв.) и безводный K2CO3(1,3 экв.) в сухой герметически запечатываемый сосуд Шленка, оснащенный магнитной мешалкой. Очищали сосуд Шленка и помещали под аргон. Прибавляли 4 мл безводного ДМФ в атмосфере аргона и герметически закрывали сосуд Шленка, а потом подвергали перемешиванию на масляной бане, предварительно нагретой до 120C, до полного исчезновения арилбромида в ГХ/МС. После возвращения к условиям комнатной температуры реакционную смесь разводили диэтиловым этером и фильтровали через целит. Органический раствор промывали с помощью насыщенного водного раствора NaCl и высушивали над MgSO4, a оставшийся растворитель выпаривали при сниженном давлении. Сырьевой продукт реакции очищали с помощью флэш-хроматографии с получением бензоциклобутена. Пример 1. Диметил 7-метилбицикло[4.2.0]окта-1,3,5-триен-3,7-дикарбоксилат. В соответствии с общей процедурой A и при использовании метил 3-бром-4-(2-метокси-1,1 диметил-2-оксоэтил)бензоата в качестве исходного материала получали указанное в заглавии соединение с выходом 92%. ИК (пленка):= 2952, 1714, 1433, 1275, 1146, 1079, 768 см-1. Пример 2. Метил 7-метил-4-(трифторметил)бицикло[4.2.0]окта-1,3,5-триен-7-карбоксилат. В соответствии с общей процедурой A и при использовании метил 2-[2-бром-5-(трифторметил)фенил]-2-метилпропаноата в качестве исходного материала получали указанное в заглавии соединение с выходом 81%. ИК (пленка):= 2955, 1731, 1315, 1143, 1113, 826, 685 см-1. Пример 3. 7-Изопропилбицикло[4.2.0]окта-1,3,5-триен-7-карбонитрил. В соответствии с общей процедурой A и при использовании 2-(2-бромфенил)-2,3 диметилбутанонитрила в качестве исходного материала получали указанное в заглавии соединение с выходом 72%. ИК (пленка):= 2964, 1458, 748, 715 см-1. Пример 4. Диметил 3-метилбицикло[4.2.0]окта-1,3,5-триен-7,7-дикарбоксилат. В соответствии с общей процедурой A и при использовании диметил 2-(2-бром-4-метилфенил)-2 метилмалоната в качестве исходного материала получали указанное в заглавии соединение с выходом 87%. ИК (пленка):=2952, 1731 см-1. Пример 5. Диметил 3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7,7-дикарбоксилат. Указанное в заглавии соединение получали в соответствии с общей процедурой A при использовании диметил 2-(2-бром-4,5-диметоксифенил)-2-метилмалоната в качестве исходного материала. ИК (чист.):= 3007, 2960, 1730, 1591, 1239, 1116, 1090, 878, 758 см-1. Пример 6. трет-Бутилметил 3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7,7-дикарбоксилат. В соответствии с общей процедурой A и при использовании трет-бутилметил 2-(2-бром-4,5 диметоксифенил)-2-метилмалоната в качестве исходного материала получали указанное в заглавии соединение с выходом 69%. ИК (чист.):= 2977, 2936, 1728, 1591, 1464, 1249, 1115, 840 см-1. Пример 7. Метил 7-4-[(триизопропилсилил)окси]бутилбицикло[4.2.0]окта-1,3,5-триен-7-карбоксилат. В соответствии с общей процедурой A и при использовании метил 2-(2-бромфенил)-2-метил-6[(триизопропилсилил)окси]гексаноата в качестве исходного материала получали указанное в заглавии соединение с выходом 82%. ИК (пленка):= 2940, 2863, 1731, 1457, 1253, 1103, 881, 678 см-1. Пример 8. Метил 7-метилбицикло[4.2.0]окта-1,3,5-триен-7-карбоксилат. В соответствии с общей процедурой В и при использовании метил 2-(2-бромфенил)-2 метилпропаноата в качестве исходного материала получали указанное в заглавии соединение с выходом 81%. ИК (чист.):= 2972, 2952, 2930, 1729, 1457, 1433, 1277, 1140, 740, 711 см-1. Пример 9. (R,S)-3,4-Диметоксибицикло[4.2.0]окта-1,3,5-триен-7-карбоновая кислота. 638 мг (2,28 ммоль) диметил 3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7,7-дикарбоксилата, полученного в примере 5, растворяли в 18 мл ДМСО и прибавляли 445 мг (6,84 ммоль) KCN в один прием. Смесь перемешивали в атмосфере аргона при 130C в течение 12 ч. После возвращения к условиям комнатной температуры к реакционной смеси прибавляли 25 мл водного раствора 1 н. HCl и 20 мл диэтилового этера (ВНИМАНИЕ: образование HCN) и смесь перемешивали в течение 1 ч. Органическую фазу промывали с помощью 1 н. водного раствора NaOH (310 мл). Водные фазы соединяли, потом подкисляли до значения pH 2 при использовании 6 н. водного раствора HCl при комнатной температуре и экстрагировали при использовании диэтилового этера (315 мл). Органические фазы высушивали над MgSO4 и оставшиеся растворители выпаривали при сниженном давлении. Сырьевой продукт реакции очищали с помощью флэш-хроматографии (гексан/этилацетат: 85/15) с получением указанного в заглавии соединения.-5 017503 ИК (чист.):= 3227, 2842, 2835, 1725, 1593, 1486, 1302, 1160, 1140, 970, 753 см-1. Пример 10. Метил (R,S)-3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7-карбоксилат. 424 мг (1,31 ммоль) трет-бутил метил 3,4-диметоксибицикло[4.2.0]окта-1,3,5-триен-7,7 дикарбоксилата, полученного в примере 6, растворяли в 2,1 мл трифторуксусной кислоты (99%) и смесь нагревали при кипении в течение 1,5 ч. После возвращения к условиям комнатной температуры смесь выпаривали при сниженном давлении с получением метилмоноэстера монокарбоновой кислоты. Сырьевое соединение растворяли в 4,34 мл смеси 30:1 ДМФ/пиридин и раствор нагревали при 120C в течение 2 ч в атмосфере аргона и потом возвращали в условия комнатной температуры. Реакционную смесь подвергали гидролизу при использовании насыщенного водного раствора NH4Cl и водную фазу экстрагировали с помощью этилацетата (310 мл). Органические фазы соединяли, промывали с помощью насыщенного водного раствора NaCl (20 мл), высушивали над MgSO4 и выпаривали при сниженном давлении. Сырьевой продукт реакции очищали с помощью флэш-хроматографии (гексан/AcOEt: 8/2) с получением указанного в заглавии продукта. ИК (чист.):= 2950, 2834, 1729, 1464, 1207, 1068, 729 см-1. Пример 11. (R,S)-3,4-Диметокси-N-метилбицикло[4.2.0]окта-1,3,5-триен-7-карбоксамид. 0,05 мл серной кислоты (d=1,83) прибавляли к раствору 2,5 г (12 ммоль) (R,S)-3,4 диметоксибицикло[4.2.0]окта-1,3,5-триен-7-карбоновой кислоты, полученной в примере 9, в 40 мл метанола. Смесь нагревали при кипении в течение 2 ч и потом охлаждали до 10C. Прибавляли 40 мл 40% раствора метиламина в воде в течение 15 мин и смесь перемешивали в течение 2 ч. Выпаривали метанол при сниженном давлении и прибавляли 40 мл воды. После экстракции с помощью CH2Cl2 объединенные органические фазы последовательно промывали водой, 1 н. HCl и насыщенным раствором NaCl, а потом высушивали над MgSO4. После выпаривания растворителей при сниженном давлении получали 2,2 г указанного в заглавии продукта в виде бежевого твердого вещества (выход: 83%). Точка плавления: 142-147C. Пример 12. (R,S)-1-(3,4-Диметоксибицикло[4.2.0]окта-1,3,5-триен-7-ил)-N-метилметанамин гидрохлорид. 20 мл молярного раствора BH3 в ТГФ прибавляли при комнатной температуре к смеси 2,2 г(10 ммоль) продукта, полученного в примере 11, в 45 мл ТГФ. После перемешивания в течение 1 ч прибавляли 10 мл раствора BH3 в ТГФ. После перемешивания в течение ночи при комнатной температуре прибавляли по каплям 20 мл этанола и смесь перемешивали до прекращения выделения газа (приблизительно 1 ч). Потом по каплям прибавляли 20 мл раствора HCl в этаноле. После перемешивания в течение 4 ч отфильтровывали полученный осадок (1,2 г указанного в заглавии продукта). Концентрировали фильтрат и дополнительно получали 0,65 г указанного в заглавии продукта путем превращения в твердое вещество в смеси 80:20 AcOEt/этанол. Соединяли два преципитата с получением 1,85 г указанного в заглавии продукта (выход 77%). Точка плавления: 174-177C. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения соединений формулы (IV) где R1, R2, R3 и R4, которые могут быть идентичными или различными, каждый, представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, атом фтора, атом хлора, защищенную аминогруппу, защищенную гидроксильную группу, алкоксикарбонильную группу, в которой алкоксильная группа является линейной или разветвленной (C1-C6), или CF3-группу, или R1=R4=H и R2 и R3 вместе с несущими их атомами углерода образуют группу 1,3-диоксолана;R5 представляет собой насыщенную или ненасыщенную, линейную или разветвленную(C1-C6)алкильную группу, линейную или разветвленную (C1-C6)гидроксиалкильную группу, в которой гидроксильная группа является защищенной, или CO2R7-группу, в которой R7 представляет собой линейную или разветвленную (C1-C6)алкильную группу;R6 представляет собой группу циано или группу CO2R8, в которой R8 является линейной или разветвленной (C1-C6)алкильной группой,при этом способ характеризуется тем, что соединение формулы (V)X представляет собой атом галогена, предпочтительно атом брома, или группу трифлата,подвергают реакции циклизации в присутствии системы катализатор/лиганд, включающей палладиевый катализатор и органический фосфин, выбранный из три-трет-бутилфосфина, 2-бифенил-ди-третбутилфосфина,1,2,3,4,5-пентафенил-1'-(ди-трет-бутилфосфино)ферроцена и трис-(4-метокси-2 метилфенил)фосфина или соли фосфония упомянутых фосфинов, в присутствии основания, в органическом растворителе. 2. Способ получения в соответствии с п.1, характеризующийся тем, что палладиевый катализатор является выбранным из Pd(OAc)2, Pd(dba)2, Pd2(dba)3, PdCl2, PdCl2(CH3CN)2, PdBr2 и трет-ди-(-ацетат)бис-[o-(ди-o-толилфосфин)бензил]дипалладия. 3. Способ получения в соответствии с любым из пп.1 или 2, характеризующийся тем, что палладиевый катализатор представляет собой Pd(OAc)2. 4. Способ получения в соответствии с любым из пп.1-3, характеризующийся тем, что органический фосфин представляет собой три-трет-бутилфосфин. 5. Способ получения в соответствии с любым из пп.1-4, характеризующийся тем, что соль фосфония представляет собой тетрафторборат, гексафторфосфат или гексафторантимонат фосфония. 6. Способ получения в соответствии с п.5, характеризующийся тем, что соль фосфония представляет собой тетрафторборат три-трет-бутилфосфония. 7. Способ получения в соответствии с любым из пп.1-6, характеризующийся тем, что используемое основание является выбранным из K2CO3, Cs2CO3, Na2CO3, K3PO4, KHCO3, t-BuCO2Na, t-BuCO2K иt-BuCO2Cs. 8. Способ получения в соответствии с п.7, характеризующийся тем, что используемое основание представляет собой K2CO3. 9. Способ получения в соответствии с любым из пп.1-8, характеризующийся тем, что используемый органический растворитель является выбранным из ДМФ, N,N-диметилацетамида, N-метилпирролидина,ксилена и мезитилена. 10. Способ получения в соответствии с п.9, характеризующийся тем, что используемый органический растворитель представляет собой ДМФ. 11. Способ получения в соответствии с любым из пп.1-10, характеризующийся тем, что температура реакции составляет от 100 до 150C. 12. Способ получения соединений формулы (VIIa)R10 представляет собой атом водорода или линейную или разветвленную (C1-C6)алкильную группу,характеризующийся тем, что соединения формулы (Va), частный случай соединений формулы (V), в которых R5=CO2R7 и R6=CO2R8: где R1, R2, R3, R4, R7, R8 и X являются такими, как определено в п.1,превращают в соединения формулы (IVa), частный случай соединений формулы (IV), в которых где R1, R2, R3, R4, R7 и R8 являются такими, как определено в п.1,в соответствии со способом п.1,затем соединение формулы (IVa) превращают в соединение формулы (VIa)R9 представляет собой линейную или разветвленную (C1-C6)алкильную группу,путем реакции омыления эстера или реакции гидролиза, а соединение формулы (VIa) приводит к получению соединения формулы (VIIa) посредством реакции декарбоксилирования. 13. Способ в соответствии с п.12 для получения соединений формулы (VIIb), частного случая соединений формулы (VIIa), где R1=R4=H и R2=R3=OCH3. 14. Соединение формулы (IVa) где R1, R2, R3 и R4, которые могут быть идентичными или различными, каждый, представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, линейную или разветвленную (C1-C6)алкоксигруппу, атом фтора, атом хлора, аминогруппу, защищенную группой. выбранной из нозила, тозила, мезила, ацетила, трет-бутоксикарбонила, бензила и фталимида, гидроксильную группу,защищенную группой. выбранной из триизопропилсилила, трет-бутилдиметилсилила, тетрагидропирана,бензила, параметоксибензила, тритила, ацетила и пивалоила, алкоксикарбонильную группу, в которой алкоксильная группа является линейной или разветвленной (C1-C6), или CF3-группу, или R1=R4=H и R2 иR3 вместе с несущими их атомами углерода образуют группу 1,3-диоксолана;R7 и R8, которые могут быть идентичными или различными, каждый, представляют собой линейную или разветвленную (C1-C6)алкильную группу. 15. Соединение формулы (VIb) где R9 представляет собой линейную или разветвленную (C1-C6)алкильную группу. 16. Соединение формулы (VIIc) где R10 представляет собой линейную или разветвленную (C1-C6)алкильную группу. 17. Способ синтеза ивабрадина, его фармацевтически приемлемых солей и их гидратов, характеризующийся тем, что соединение формулы (Vb) где R7, R8 и X являются такими, как определено в п.1,превращают в соответствии со способом п.13 в соединение формулы (VIIb) путем реакции с метиламином, восстановление которого обеспечивает получение соединения формулы разделение которого в присутствии камфорсульфоновой кислоты обеспечивает получение соединения формулы (II) который может быть необязательно превращен в его аддитивные соли с фармацевтически приемлемой кислотой, выбранной из хлористо-водородной, бромисто-водородной, серной, фосфорной, уксусной,трифторуксусной, молочной, пировиноградной, малоновой, янтарной, глутаровой, фумаровой, виннокаменной, малеиновой, лимонной, аскорбиновой, щавелевой, метансульфоновой, бензолсульфоновой и камфорной кислот, и в их гидраты.
МПК / Метки
МПК: C07C 213/08, C07D 223/16, C07C 217/56, C07C 213/02, C07C 217/58, C07C 213/10
Метки: применение, фармацевтически, приемлемой, кислотой, аддитивных, бензоциклобутенов, новый, получения, солей, способ, синтезе, функционализированных, ивабрадина
Код ссылки
<a href="https://eas.patents.su/10-17503-novyjj-sposob-polucheniya-funkcionalizirovannyh-benzociklobutenov-i-ih-primenenie-v-sinteze-ivabradina-i-ego-additivnyh-solejj-s-farmacevticheski-priemlemojj-kislotojj.html" rel="bookmark" title="База патентов Евразийского Союза">Новый способ получения функционализированных бензоциклобутенов и их применение в синтезе ивабрадина и его аддитивных солей с фармацевтически приемлемой кислотой</a>
Предыдущий патент: Способ закалки матриц разделительных штампов
Следующий патент: Подгузник одноразового использования
Случайный патент: Устройство и способ анализа размера, формы и угловатости, а также состава минералов и частиц горных пород












