Олигосахариды,способ их получения и содержащие их фармацевтические композиции
Номер патента: 4046
Опубликовано: 25.12.2003
Авторы: Перрэн Элизабет, Мурье Пьер, Штутцманн Жан-Мари, Висков Кристиан, Валь Флоранс
Формула / Реферат
1. Олигосахариды формулы
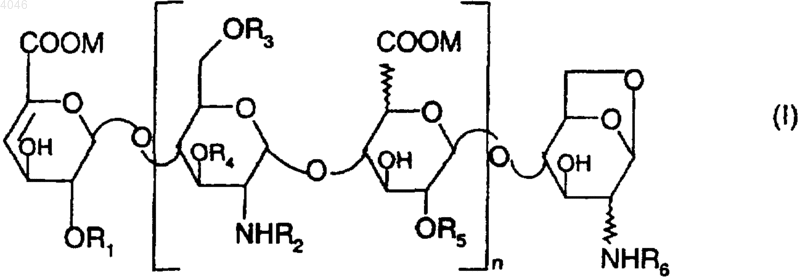
в которой n является целым числом от 0 до 25; R1, R3, R4 и R5, одинаковые или разные, обозначают атом водорода или радикал SO3M; R2 и R6, одинаковые или разные, обозначают атом водорода или радикал SO3M или COCH3 и M обозначает натрий, кальций, магний или калий, смесь этих олигосахаридов и их диастереоизомеры.
2. Олигосахариды формулы I по п.1, у которых R4 обозначает атом водорода, смесь этих олигосахаридов и их диастереоизомеры.
3. Олигосахариды формулы I по одному из пп.1 или 2, у которых n является целым числом от 0 до 10, смесь этих олигосахаридов и их диастереоизомеры.
4. Олигосахариды формулы I по одному из пп.1 или 2, у которых n является целым числом от 0 до 6, смесь этих олигосахаридов и их диастереоизомеры.
5. Олигосахариды формулы I по одному из пп.1 или 2, у которых n является целым числом от 1 до 6, смесь этих олигосахаридов и их диастереоизомеры.
6. Способ получения олигосахаридов формулы I по п.1, отличающийся тем, что гидроксид щелочного металла или четвертичного аммония вводят во взаимодействие с олигосахаридами формулы
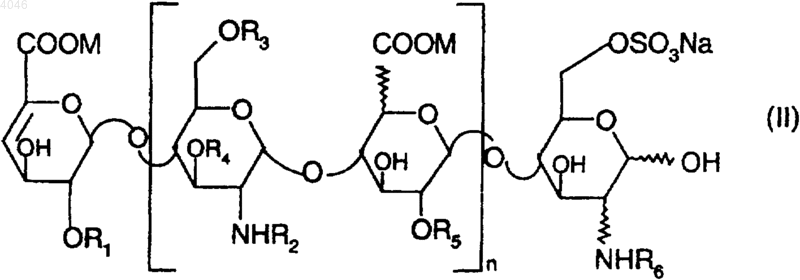
в которой n является целым числом от 0 до 25; R1, R3, R4 и R5, одинаковые или разные, обозначают атом водорода или радикал SO3M; R2 и R6, одинаковые или разные, обозначают атом водорода или радикал SO3M или COCH3 и M обозначает натрий, кальций, магний или калий, или их смеси, и выделяют олигосахариды или их смеси.
7. Способ по п.6, отличающийся тем, что реакцию проводят в водной среде при температуре от 40 до 80шC и pH от 10 до 13.
8. Способ по одному из пп.6 или 7, отличающийся тем, что используют 1-5%-ный водный раствор гидроксида щелочного металла или четвертичного аммония.
9. Способ по одному из пп.6-8, отличающийся тем, что реакцию проводят при температуре от 60 до 70шC.
10. Способ по одному из пп.6-9, отличающийся тем, что pH реакционной среды составляет от 11 до 12,5.
11. Способ по пп.6-10, отличающийся тем, что гидроксидом щелочного металла или четвертичного аммония является гидроксид натрия, гидроксид калия, гидроксид лития, цезия или гидроксид тетрабутиламмония.
12. Фармацевтические композиции, содержащие в качестве активного начала по меньшей мере один олигосахарид по п.1.
13. Фармацевтические композиции, содержащие в качестве активного начала по меньшей мере один олигосахарид по одному из пп.1-5.
14. Применение олигосахаридов формулы I по одному из пп.1-5 для получения лекарственного средства, пригодного для профилактики или лечения заболеваний, связанных с воспалительным процессом, при котором происходит образование закиси азота (NO).
15. Применение олигосахаридов формулы I по п.14 для получения лекарственного средства, пригодного для профилактики и лечения церебральных, сердечных или периферических сосудистых ишемий, остеоартритов, повреждений центральной нервной системы, черепных, спинно-мозговых и черепно-спинно-мозговых травм, рассеянного склероза, невропатических болей и периферических невропатий, заболеваний двигательных нейронов, бокового амиотрофического склероза, нейро-СПИДа, болезни Альцгеймера, болезни Паркинсона и хореи Гентингтона.
Текст
1 Настоящее изобретение относится к олигосахаридам формулы их смесям, их диастереоизомерам, способу их получения и содержащим их фармацевтическим композициям. Дисахариды-сульфаты, имеющие на восстановительном конце структуру 1,6-ангидро,были описаны H.P. Wessel, J.CarbohydrateChemistry, 11(8), 1039-1052 (1992). Ни о какой их фармакологической активности не упоминалось. В патенте ЕР 84999 и авторами Y. Ichikawa с сотр., Carbohydr. Res., 141, 273-282 (1985), были также описаны трисахариды-сульфаты со звеном 1,6-ангидро в качестве промежуточных продуктов для получения высших олигосахаридов. Эти трисахариды обладают слабой активностью анти-Ха. В формуле I является целым числом от 0 до 25; R1, R3, R4 и R5, одинаковые или разные,обозначают атом водорода или радикал SО 3 М;R2 и R6, одинаковые или разные, обозначают атом водорода или радикал SО 3 М или СОСН 3; и М обозначает натрий, кальций, магний или калий. Эти олигосахариды содержат, таким образом, четное число сахаридов.R4 в формуле I является преимущественно атомом водорода, а n преимущественно является целым числом от 0 до 10, предпочтительно от 0 до 6 и еще более предпочтительно от 1 до 6. Олигосахариды формулы I могут быть получены действием гидроксида щелочного металла или четвертичного аммония на олигосахариды формулы в которой n является целым числом от 0 до 25;R1, R3, R4 и R5, одинаковые или разные, обозначают атом водорода или радикал SО 3 М; R2 и R6,одинаковые или разные, обозначают атом водорода или радикал SО 3 М или СОСН 3; и М обозначает натрий, кальций, магний или калий, или их смеси. Названную реакцию проводят в водной среде при температуре от 40 до 80 С и рН от 10 до 13. В качестве возможно используемого гидроксида щелочного металла можно назвать гидроксид натрия, гидроксид калия, гидроксид лития и гидроксид цезия. В качестве возможно используемого гидроксида четвертичного аммония можно назвать гидроксид тетрабутиламмония. 2 Количество гидроксида щелочного металла или четвертичного аммония должно быть достаточным для того, чтобы рН реакционной среды в процессе реакции сохранялся постоянным. Для этой цели гидроксид щелочного металла или четвертичного аммония необходимо добавлять непрерывно в течение всей реакции. Гидроксид щелочного металла или четвертичного аммония используется преимущественно в виде 1-5%-ного водного раствора. Реакцию проводят преимущественно при температуре от 60 до 70 С. рН реакционной среды преимущественно равен 11-12,5. Реакцию останавливают путем подкисления реакционной среды, например добавлением кислой смолы, такой как смола Amberlite IR120R(Fluka). Олигосахариды формулы I могут быть при необходимости очищены с помощью гельпроникающей хроматографии на геле типа полиакриламидагароза, таком как гель, поставляемый под маркой Ultrogel ACA202R (Biosepra), в соответствии с прописью, приведенной ниже для разделения промежуточных олигосахаридов формулы II. Олигосахариды формулы I, у которых n равно 0 или 1, также могут быть в случае необходимости очищены на колонке с окисью алюминия с использованием в качестве элюента смеси вода-этанол. Промежуточные олигосахариды формулыII и их смеси могут быть получены разделением с помощью гелевой хроматографии смеси олигосахаридов III, полученной ферментативной деполимеризацией гепарина или щелочной деполимеризацией бензилового эфира гепарина или полусинтетического бензилового эфира гепарина. Названную выше хроматографию проводят на колонках, заполненных гелем типа полиакриламид-агароза, поставляемым под маркойUltrogel АСА 202R (Biosepra). Преимущественно используют батарею колонок с полиакриламидагарозным гелем. Число используемых колонок зависит от объема, геля и разделяемых олигосахаридов. Смесь элюируют с помощью раствора,содержащего фосфатный буфер и хлорид натрия. Фосфатный буфер представляет собой преимущественно 0,02 моль/л раствор NaH2PO4/Na2HPO4 (pH 7), содержащий 0,1 моль/л хлорида натрия. Детекцию различных фракций осуществляют с помощью УФ спектрометрии (254 нм) и ионной спектрометрии (IBF). Получаемые при этом фракции могут быть затем при необходимости очищены, например с помощью хроматографии SAX (strong anion exchange) с использованием известных специалистам способов, в частности способов, описанных К.G. Rice и R.J. Linhardt, Carbohydrate Research, 190, 219233 (1989), A. Larnkjaer, S.H. Hansen и P.B. 3 Фракции после этого лиофилизируют и затем обессоливают на заполненной гелем колонке,такой как колонка с гелем Sephadex G10R (Pharmacia Biochemicals). Если очистку осуществляют, не прибегая к помощи хроматографии SAX, лиофилизаты могут быть очищены простым осаждением или подвергнуты фракционированию с помощью известных специалистам способов, в частности с помощью способа, описанного в патенте FR 2548672. В общем случае операции проводят в соответствии со следующей прописью. Очищаемую лиофилизированную фракцию растворяют при 25 С в приблизительно десяти объемах дистиллированной воды. С помощью добавки метанола или этанола осаждают желаемый олигосахарид, контролируя его чистоту с помощью хроматографии ЖХВР (жидкостной хроматографии высокого разрешения). Добавку метанола или этанола определяют в зависимости от желаемых чистоты и выхода олигосахарида. Эта операция может быть проведена в несколько последовательных этапов, исходя из начального раствора лиофилизата. С этой целью высаливающий агент (метанол или этанол) добавляют малыми порциями, отделяя после каждого добавления образующийся осадок. Полученные таким образом осадки анализируют с помощью хроматографии ЖХВР. В зависимости от желаемых чистоты и выхода собирают соответствующие им фракции осадка. Для промежуточных продуктов формулыII, у которых n=0, 1 или 2, целесообразно исходить из смеси III, получаемой с помощью ферментативной деполимеризации. Эту деполимеризацию проводят с использованием гепариназы I (ЕС 4.2.2.7) в растворе фосфатного буфера с рН 7 в присутствии хлорида натрия и БСА (бычьего сывороточного альбумина) при температуре в пределах от 10 до 18 С, предпочтительно при 15 С, в течение 8-10 суток, предпочтительно 9 суток. Деполимеризация может быть остановлена, например, нагреванием реакционной среды до 100 С в течение 2 мин, а смесь может быть выделена лиофилизацией. На 25 г гепарина предпочтительно используют 7 меж.ед. гепариназы I. Фосфатный буфер обычно содержит 0,05 моль/л NaH2PO4/Na2HPO4 (рН 7) в присутствии 0,1 моль/л хлорида натрия. Концентрация БСА обычно составляет 2%. Для промежуточных продуктов формулыII, у которых n=0, 1, 2, 3 или 4, целесообразно исходить из смеси III, получаемой деполимеризацией бензилового эфира гепарина. Бензиловый эфир гепарина может быть получен с помощью методов, описанных в патентах US 5389618, ЕР 40144, FR 2548672. Степень эстерификации в этом случае составляет от 50 до 100%, преимущественно от 70 до 90%. Деполимеризацию проводят в водной среде с помощью гидроксида щелочного металла(например, гидроксида лития, гидроксида натрия, гидроксида калия или гидроксида цезия) или гидроксида четвертичного аммония (например, гидроксида тетрабутиламмония) преимущественно в молярной концентрации от 0,1 до 0,2 моль/л при температуре от 40 до 80 С в течение времени от 5 до 120 мин. В предпочтительном варианте реакцию проводят в течение 5-15 мин при температуре от 60 до 70 С с использованием 0,15 моль/л раствора гидроксида натрия. Реакцию деполимеризации останавливают с помощью нейтрализации, добавляя кислоту, такую как уксусная кислота. После добавления 10% мас./об. ацетата натрия смесь олигосахаридов осаждают добавкой метанола преимущественно в количестве 2 об. на 1 об. реакционной среды, после чего смесь отфильтровывают. В соответствии с предпочтительным аспектом изобретения, смесь олигосахаридов, полученную после химической деполимеризации в виде водного раствора, обогащают с помощью ультрафильтрации на мембранах с соответствующим номинальным пределом разделения(типа Pellicon из регенерированной целлюлозы,поставляемых фирмой Millipore), причем тип мембраны подбирают в соответствии с типом выделяемых обогащенных олигосахаридов. Для олигосахаридов II, у которых n=0, используют мембрану с номинальным пределом разделения 1 кДа, для олигосахаридов II, у которых n=1,используют мембрану 1 кДа или 3 кДа, для олигосахаридов II, у которых n=2, используют мембрану 3 кДа, для олигосахаридов II, у которыхn=3 или 4, используют мембрану 5 кДа. В процессе этой операции собирают фильтрат, а задержанный материал отбрасывают. В результате операции фракция обогащенного продукта может составлять от 50 до 10% исходной смеси олигосахаридов, при этом она содержит не менее 80% желаемого олигосахарида. Для промежуточных продуктов формулыII, у которых n= от 0 до 25, целесообразно исходить из смеси III, получаемой деполимеризацией полусинтетического бензилового эфира полисахарида-сульфата. Полусинтетический бензиловый эфир полисахарида-сульфата получают из полусинтетических полисахаридов-сульфатов, получаемых из полисахарида К 5 с помощью методов, описанных в патентах WO 94/29352 и WO 96/14425. Условия эстерификации, деполимеризации и выделения такие же,как те, которые описаны выше для бензилового эфира гепарина. Во всех описанных выше способах исходный гепарин может быть получен от свиньи,овцы, козы или быка и может быть взят из слизи, легких или кожи животных. Преимущественно используют гепарин из слизи свиньи, овцы или из легких быка, причем предпочтительнее из слизи свиньи. 5 Олигосахариды формулы I обладают противовоспалительными свойствами и могут, таким образом, быть использованы для профилактики или лечения болезней, связанных с воспалительным процессом, при котором происходит продукция цитотоксических веществ, таких как закись азота (NO), индуцируемая форма которых высвобождается, в частности, нейтрофилами или макрофагами, когда последние мигрируют и активируются в ткани. Активация, миграция, слипание и инфильтрация нейтрофилов происходят в затронутых ишемией зонах ткани в результате закупорки или спазма артерии, питающей эту ткань. Такие ишемии могут возникать либо в головном мозге (нарушение мозгового кровообращения), либо в сердечной мышце(инфаркт миокарда), либо в нижних конечностях (так называемые периферические ишемии). Олигосахариды формулы I могут быть, таким образом, использованы для профилактики и/или лечения нейродегенеративных заболеваний, в случае которых воспаление мозга играет разрушающую роль с возможным летальным исходом, из которых можно назвать церебральные ишемии, ишемии сердца (инфаркт миокарда),периферические ишемии, повреждения центральной нервной системы и, в частности, черепные, спинно-мозговые и черепно-спинномозговые травмы, рассеянный склероз, невропатические боли и периферические невропатии,заболевания двигательных нейронов, в том числе боковой амиотрофический склероз, нейроСПИД, болезнь Альцгеймера, болезнь Паркинсона и хорея Гентингтона, и некоторые формы остеоартритов, в частности локализованных в суставах. Противовоспалительная активность этих продуктов доказана in vivo в тесте на продукцию NOx (нитрит и нитрат), индуцируемую липополисахаридом (LPS), полученным от E.coli способом, описанным M.Yamashita с сотр., Eur.Shellito с сотр., Am. J. Respir. Cell Mol. Biol., 13,1, 45-53 (1995). Мышам-самцам CDI (Charles River, 25-35 г) вводят внутривенно в момент времени Т 0 0,5 мг/кг олигосахарида в виде шариков, в момент времени Т+15 мин подкожно 1 или 2 мг/кг олигосахарида. В момент времени Т+30 мин вводят 100 мг/кг липополисахарида (LPS), полученного от E.coli (Sigma L3129, серотип 0127:В 8). В момент времени Т+3 час вновь вводят подкожно 1 или 2 мг/кг олигосахарида. В момент времени Т+5 ч 30 мин с помощью глазной пункции отбирают пробу крови и определяют концентрации NOx (нитрит и нитрат) в плазме, используя колориметрический метод Грисса после восстановления нитрата в нитрит с помощью нитратредуктазы следующим образом: 12 л образца плазмы смешивают с 88 л деионизованной воды и инкубируют в темноте в течение 1 ч при 6 комнатной температуре с 40 л фосфатного буфера (0,31 М, рН 7,5), 20 л -НАДФН (восстановленный никотинамидадениндинуклеотидфосфат) (0,86 мМ), 20 л ФДА (флавинадениндинуклеотид) (0,11 мМ) и 20 л нитратредуктазы (2 ед./мл) (Boehringer Mannheim). Добавляют 10 л ZnSO4 (1M) для осаждения белков и после смешения образцы центрифугируют при 20000g в течение 5 мин. В заключение 50 л супернатанта инкубируют 10 мин при комнатной температуре со 100 л реактива Грисса (1%-ный раствор сульфаниламида в 0,1%-ном растворе смеси фосфорная кислота/нафтилэтилендиамин в деионизованной воде (об./об Оптические плотности замеряют при 540 нм на микропластинчатом спектрофотометре, производя по два замера на каждую точку. В качестве стандарта в колориметрическом методе используют KNО 3 иNaNO2. Олигосахариды изобретения в названном испытании ингибируют образование NOx более чем на 50%. Из предпочтительных олигосахаридов формулы I можно, в частности, назвать олигосахариды, у которых:SО 3Nа и М обозначает натрий, и смесь его диастереоизомеров,- n равно 1, R1, R2, R3, R5 и R6 обозначают радикал SО 3Nа, R4 обозначает атом водорода и М обозначает натрий, и смесь его диастереоизомеров,- n равно 2, R1, R2, R3, R5 и R6 обозначают радикал SО 3Nа, R4 обозначает атом водорода и М обозначает натрий, и смесь его диастереоизомеров,- n равно 2, R1, R2, R3 и R6 обозначают радикал SО 3Nа, R5 обозначает атом водорода или радикал SO3Na, R4 обозначает атом водорода и М обозначает натрий, и смесь его диастереоизомеров (производное 1,6-ангидро-Is-Is-IIs). Получение олигосахаридов формулы I и промежуточных продуктов иллюстрируют следующие примеры. В этих примерах используют следующие значения сокращений:IIIs: (2-сульфоL-идопиранозилурониевая кислота)-(14)-2-дезокси-2-сульфамино-D-глюкопираноза, тринатриевая соль, или -LIdoAp2S-(14)D-GlcNp2S,IdoAp: идопиранозилурониевая кислота,GlcNp: 2-дезокси-2-аминоглюкопираноза,UAp: 4-дезоксиL-треогексенпиранозилурониевая кислота,S: сульфат. Примеры получения смесей формулы II Пример А. Получение олигосахаридов формулы II, у которых n=0, 1 и 2, ферментативной деполимеризацией и разделением. Растворяют 25 г гепарина в 250 мл раствора фосфатного буфера, содержащего 0,05 моль/л(ЕС 4.2.2.2.7), охлаждают полученный раствор до 15 С и выдерживают при этой температуре в течение всей реакции деполимеризации. За протеканием реакции следят путем ступенчатого отбора проб, анализируемых с помощью гель проникающей хроматографии. По истечении 9 суток ферментативную реакцию останавливают,нагревая реакционную среду в течение двух минут при 100 С. Смесь после этого охлаждают и лиофилизируют, получая таким образом смесь олигосахаридов III. Полученную смесь олигосахаридов III хроматографируют по следующей методике: хроматографию проводят на колонках, заполненных полиакриламид-агарозным гелем, известным под названием Ultrogel АСА 202, и элюируют смесь раствором, содержащим фосфатный буфер (0,02 моль/л NaH2PO4/Na2HPO4),рН=7, и 0,1 моль/л хлорида натрия. Детекцию осуществляют с помощью УФ спектрометрии(254 нм) и ионной спектрометрии (IBF). Продукты могут быть затем при необходимости очищены с помощью хроматографии SAX(strong anion exchange) или фракционным осаждением по методу, описанному в патенте FR 2548672. Выделенные фракции продукта лиофилизируют и затем обессоливают на колонке,заполненной гелем Sephadex G10R (PharmaciaBiochemicals). Используя эту методику, получают 3 г дисахарида Is и 1100 мг смеси гексасахарида, содержащего, как правило, 55% производного IsIs-Is, 35% Is-Is-IIs и 10% Is-Is-IIIs. Эта смесь может быть очищена с использованием известных специалистам способов, позволяющих выделение каждого из компонентов, или использована как таковая для превращения в 1,6 ангидро-производные формулы I. Следует отметить, что в процессе этого превращения гексасахарид Is-Is-IIIs не может дать соединений формулы I. Пример В. Получение олигосахаридов формулы II, у которых n=0, 1, 2, 3 или 4, депо 004046 8 лимеризацией бензилового эфира гепарина и разделением. а. Получение бензилового эфира гепарина. Бензиловый эфира гепарина получают как описано в примере 2 патента US 5389618.b. Деполимеризация. Растворяют 100 г бензилового эфира гепарина в 1,9 л деминерализованной воды. Смесь нагревают до 60 С при перемешивании. После образования гомогенного раствора вводят в один прием приблизительно 35 мл 23%-ного раствора гидроксида натрия. После проведения реакции в течение 10 мин раствор охлаждают и нейтрализуют 80 мл приблизительно 2 н. раствора уксусной кислоты. К полученному раствору добавляют 10% мас./об. ацетата натрия. Смесь олигосахаридов осаждают добавлением приблизительно 2 объемов метанола. Осадок отделяют фильтрацией, дважды промывают метанолом и сушат при 50 С и пониженном давлении. После сушки получают 73,8 г смеси олигосахаридов II. с. Обогащение олигосахарида с n=1. Растворяют 30 г полученной выше смеси олигосахаридов в приблизительно 35 объемах воды. Этот раствор подвергают ультрафильтрации на мембране 3 кДа (Pellicon). После получения 600 мл фильтрата задержанную часть разбавляют 500 мл воды. Продолжают операцию до получения дополнительных 450 мл фильтрата. Обе фракции фильтрата объединяют и затем досуха упаривают при пониженном давлении. Получают 6,1 г желтовато-белого твердого вещества. Анализ этого вещества с помощью гельпроникающей хроматографии указывает на содержание в нем приблизительно 30% олигосахаридов формулы II, у которых n=1.d. Фракционирование подвергнутых ультрафильтрации смесей олигосахаридов. Обогащенную смесь фракционируют на колонках,заполненных полиакриламидагарозным гелем, известным под названием Ultrogel АСА 202 (используют 4 последовательно расположенных колонки с диаметром 10 см и высотой 50 см). 5 г обогащенной ультрафильтрацией смеси растворяют в 25 мл воды, после чего элюируют 0,2 моль/л раствором хлорида натрия со скоростью 5 мл/мин. Отбирают с низа колонки фракции по 25 мл. Детекцию продуктов осуществляют с помощью УФ спектрометрии(254 нм) и ионной спектрометрии (IBF). Фракции продукта с n=1 выделяют, лиофилизируют и затем обессоливают на колонке, заполненной гелем Sephadex G10. После лиофилизации получают 1 г тетрасахарида, содержащего, как правило, 70% производного Is-Is формулы II (R1,R2, R3, R5, R6 = SО 3Nа; R4 = Н и М = Na). Производное Is-Is может быть при необходимости очищено с помощью хроматографии SAX(strong anion exchange) или, что является предпочтительным, фракционным осаждением по методу, описанному в патенте FR 2548672. 9 Пример 1. В реактор при температуре 66 С загружают 5 мл 0,0063 моль/л раствора гидроксида натрия. Измеряют рН раствора и принимают его значение в качестве целевого (рН 11,35). Добавляют при перемешивании в один прием 30 мг олигосахарида формулы II, у которого n равно 0, R1 и R6 обозначают радикалSО 3Nа и М обозначает натрий. После этого корректируют рН и поддерживают его равным 11,35 с помощью непрерывного добавления 0,5 моль/л раствора гидроксида натрия. Через 10 ч добавление гидроксида натрия прекращают и реакционную смесь охлаждают до 25 С. После этого доводят рН раствора до 6-7, добавляя смолу Amberlite IR 120. Смесь фильтруют на мембране Whatman GF/B и досуха упаривают при пониженном давлении (2,7 кПа) при температуре, близкой к 25 С. Продукт забирают 0,5 мл дистиллированной воды и лиофилизируют, получая 29 мг смеси диастериоизомеров олигосахарида формулы I, у которого n равно 0, R1 и R6 обозначают радикал SO3Na и М обозначает натрий [(4-дезокси-2-O-сульфоL-трео-гекс-4 енпиранозилурониевая кислота)-(14)-1,6-ангидро-2-дезокси-2-сульфаминоD-маннопираноза, тринатриевая соль: спектр ПМР в D2O, 400 МГц, Т=298 К,в м.д.: 3,15(1 Н, с, Н 2), 3,75(2 Н,м, Н 6 и Н 3), 3,88(1 Н, м, Н 4), 4,20(1 Н, д, J=8 Гц,Н 6), 4,22(1 Н, т, J=5 Гц, Н 3'), 4,58(1 Н, м, Н 2'),4,75(1 Н, м, Н 5), 5,53(1 Н, с, H1), 5,60(1 Н, дд, J=6 и 1 Гц, Н 1'), 6,03(1 Н, д, J=5 Гц, Н 4');(4-дезокси-2-O-сульфоL-трео-гекс-4 енпиранозилурониевая кислота)-(14)-1,6-ангидро-2-дезокси-2-сульфаминоD-глюкопираноза, тринатриевая соль): спектр ПМР в D2O,400 МГц, Т=298 К,в м.д.: 3,34(1 Н, дд, J=7 и 2 Гц, Н 2), 3,72(1 Н, т, J=8 Гц, Н 6), 3,90(1 Н, м, Н 3),4,03(1 Н, с, Н 4), 4,20(1 Н, д, J=8 Гц, Н 6), 4,23(1 Н,т, J=5 Гц, Н 3'), 4,58(1 Н, м, Н 2'), 4,78(1 Н, м, Н 5),5,50(1 Н, с, H1), 5,60(1 Н, дд, J=6 и 1 Гц, Н 1'),6,03(1 Н, д, J=5 Гц, Н 4')]. Пример 2. В реактор при температуре 62 С загружают 33,3 мл 0,0063 моль/л раствора гидроксида натрия. Измеряют рН раствора и принимают его значение в качестве целевого (рН 11,15). Добавляют при перемешивании в один прием 200 мг олигосахарида формулы II, у которого n равно 1, R1, R2, R3, R5 и R6 обозначают радикал SO3Na, R4 обозначает атом водорода и М обозначает натрий. После этого корректируют рН и поддерживают его равным 11,15 с помощью непрерывного добавления 0,5 моль/л раствора гидроксида натрия. Через 12 ч добавление гидроксида натрия прекращают и реакционную смесь охлаждают до 25 С. После этого доводят рН раствора до 6-7, добавляя смолуAmberlite IR 120. Смесь фильтруют на мембранеWhatman GF/B и досуха упаривают при пониженном давлении (2,7 кПа) при температуре,близкой к 25 С. Продукт забирают 3 мл дистиллированной воды и лиофилизируют, получая 10 230 мг олигосахарида формулы I, у которого n равно 1, R1, R2, R3, R5 и R6 обозначают радикалSO3Na, R4 обозначает атом водорода и М обозначает натрий, в виде смеси диастереоизомеров(1 Н, м, H1), 5,94(1 Н, д, J=5 Гц, Н 4)]. Пример 3. В реактор при температуре 62 С загружают 16,7 мл 0,0063 моль/л раствора гидроксида натрия. Измеряют рН раствора и принимают его значение в качестве целевого (рН 11,7). Добавляют при перемешивании в один прием 100 мг олигосахарида формулы II, у которого n равно 2, R1, R2, R3, R5 и R6 обозначают радикал SO3Na, R4 обозначает атом водорода и М обозначает натрий. После этого корректируют рН и поддерживают его равным 11,7 с помощью непрерывного добавления 0,5 моль/л раствора гидроксида натрия. Через 10 ч добавление гидроксида натрия прекращают и реакционную смесь охлаждают до 25 С. После этого доводят рН раствора до 6-7, добавляя смолуAmberlite IR 120. Смесь фильтруют на мембранеWhatman GF/B и досуха упаривают при пониженном давлении (2,7 кПа) при температуре,близкой к 25 С. Продукт забирают 3 мл дистиллированной воды и лиофилизируют, получая 108 мг олигосахарида формулы I, у которого n равно 2, R1, R2, R3, R5 и R6 обозначают радикалSO3Na, R4 обозначает атом водорода и М обозначает натрий, в виде смеси диастереоизомеров. Отмечают символами от А до F сахара,которые образуют гексасахариды, где А представляет собой остаток 1,6-анигидро и F-остаток ненасыщенной урониевой кислоты.(А, 5,95 (1 Н, д, J=5 Гц, Н 4 (F. Пример 4. В реактор при температуре 62 С загружают 4 мл 0,0316 моль/л раствора гидроксида натрия. Измеряют рН раствора и принимают его значение в качестве целевого (рН 11,8). Добавляют при перемешивании в один прием 100,8 мг смеси олигосахаридов формулыII, у которых n равно 2, содержащей 55% производного Is-Is-Is (R1, R2, R3, R5 и R6 обозначают радикал SO3Na, R4 обозначает атом водорода и М обозначает натрий), 35% Is-Is-IIs (R1, R2, R3 и R6 обозначают радикал SО 3Nа, R5 обозначает радикал SO3Na или атом водорода, R4 обозначает атом водорода и М обозначает натрий) и 10%Is-Is-IIIs (R1, R2, R3, R5 и R6 обозначают радикал SO3Na, R4 обозначает атом водорода и М обозначает натрий, причем функция SО 3 М у углерода С 6 заменена водородом). После этого корректируют рН и поддерживают его равным 11,8 с помощью непрерывного добавления 0,5 моль/л раствора гидроксида натрия. Через 11 ч добавление гидроксида натрия прекращают и реакционную смесь охлаждают до 25 С. После этого доводят рН раствора до 6-7, добавляя смолу Amberlite IR 120. Смесь фильтруют на мембране Whatman GF/B и досуха упаривают при пониженном давлении (2,7 кПа) при температуре, близкой к 25 С. Продукт забирают 1,5 мл 12 дистиллированной воды и лиофилизируют, получая 110 мг смеси олигосахаридов формулы I,у которых n равно 2, содержащей, в частности,производное 1,6-ангидро-Is-Is-Is (R1, R2, R3, R5 и R6 обозначают радикал SO3Na, R4 обозначает атом водорода и М обозначает натрий) и производное 1,6-ангидро-Is-Is-IIs (R1, R2, R3 и R6 обозначают радикал SO3Na, R5 обозначает радикал SO3Na или атом водорода, R4 обозначает атом водорода и М обозначает натрий). Анализ с помощью ЖХВР (жидкостной хроматографии высокого разрешения) в режиме ионных пар позволяет следить за превращением производных формулы I. Полученные данные ЖХВР указывают на то, что превращение осуществляется с производными Is-Is-Is и Is-Is-IIs. Пример 5. В реактор при температуре 66 С загружают 8,6 мл 0,025 моль/л раствора гидроксида лития. Измеряют рН раствора и принимают его значение в качестве целевого (рН 11,68). Добавляют при перемешивании в один прием 50 мг олигосахарида формулы II, у которого n равно 0, R1 и R6 обозначают радикалSO3Na и М обозначает натрий. После этого корректируют рН и поддерживают его равным 11,68 с помощью непрерывного добавления 0,466 моль/л раствора гидроксида лития. Через 8 ч добавление гидроксида лития прекращают и реакционную смесь охлаждают до 25 С. Анализ с помощью ЖХВР (жидкостной хроматографии высокого разрешения) в режиме ионных пар позволяет следить за превращением производного формулы I, у которого n равно 0, R1 и R6 обозначают радикал SO3Na и М обозначает натрий или литий. Полученные данные ЖХВР указывают на то, что превращение осуществляется на 100%. Выход на основании сравнения с эталонными данными составляет 81,2%. Пример 6. В реактор при температуре 66 С загружают 8,3 мл 0,0063 моль/л раствора гидроксида калия. Измеряют рН раствора и принимают его значение в качестве целевого (рН 11,1). Добавляют при перемешивании в один прием 50 мг олигосахарида формулы II, у которого n равно 0, R1 и R6 обозначают радикал SO3Na и М обозначает натрий. После этого корректируют рН и поддерживают его равным 11,1 с помощью непрерывного добавления 0,515 моль/л раствора гидроксида калия. Через 24 ч добавление гидроксида калия прекращают и реакционную смесь охлаждают до 25 С. Анализ с помощью ЖХВР(жидкостной хроматографии высокого разрешения) в режиме ионных пар позволяет следить за превращением производного формулы I, у которого n равно 0, R1 и R6 обозначают радикалSО 3Nа и М обозначает натрий или калий. Полученные данные ЖХВР указывают на то, что превращение осуществляется на 100%. Выход на основании сравнения с эталонными данными составляет 75,6%. 13 Пример 7. В реактор при температуре 66 С загружают 8,3 мл 0,0063 моль/л раствора гидроксида цезия. Измеряют рН раствора и принимают его значение в качестве целевого (рН 10,75). Добавляют при перемешивании в один прием 50 мг олигосахарида формулы II, у которого n равно 0, R1 и R6 обозначают радикал SO3Na и М обозначает натрий. После этого корректируют рН и поддерживают его равным 10,75 с помощью непрерывного добавления 0,476 моль/л раствора гидроксида цезия. Через 20 ч добавление гидроксида цезия прекращают и реакционную смесь охлаждают до 25 С. Анализ с помощью ЖХВР (жидкостной хроматографии высокого разрешения) в режиме ионных пар позволяет следить за превращением производного формулы I, у которого n равно 0, R1 и R6 обозначают радикал SO3Na и М обозначает натрий или цезий. Полученные данные ЖХВР указывают на то, что превращение осуществляется на 90,3%. Выход на основании сравнения с эталонными данными составляет 73%. Пример 8. В реактор при температуре 66 С загружают 8,3 мл 0,0063 моль/л раствора гидроксида тетрабутиламмония. Измеряют рН раствора и принимают его значение в качестве целевого (рН 10,95). Добавляют при перемешивании в один прием 50 мг олигосахарида формулыII, у которого n равно 0, R1 и R6 обозначают радикал SО 3Nа и М обозначает натрий. После этого корректируют рН и поддерживают его равным 10,95 с помощью непрерывного добавления 0,521 моль/л раствора гидроксида тетрабутиламмония. Через 16 ч добавление гидроксида цезия прекращают и реакционную смесь охлаждают до 25 С. Анализ с помощью ЖХВР (жидкостной хроматографии высокого разрешения) в режиме ионных пар позволяет следить за превращением производного формулы I, у которогоn равно 0, R1 и R6 обозначают радикал SО 3Nа и М обозначает натрий или тетрабутиламмоний. Полученные данные ЖХВР указывают на то, что превращение осуществляется на 96,7%. Выход на основании сравнения с эталонными данными составляет 65%. Лекарственные средства по изобретению содержат в качестве активного начала по меньшей мере один олигосахарид формулы I или смесь олигосахаридов формулы I в виде композиции, в которой активное начало ассоциировано с любым другим фармацевтически совместимым продуктом, который может быть как инертным, так и физиологически активным. Лекарственные средства по изобретению могут применяться внутривенно, подкожно, перорально, ректально, местно и пульмонарно (ингаляцией). Стерильные композиции для внутривенного и подкожного применения обычно являются водными растворами. Эти композиции могут также содержать адъюванты, в частности смачивающие, изотонизирующие, эмульгирующие, 004046 14 диспергирующие и стабилизирующие агенты. Стерилизация может быть осуществлена различными способами, например асептической фильтрацией, введением в композицию стерилизующих агентов, облучением. Эти композиции могут быть также приготовлены в виде твердых стерильных композиций, которые непосредственно перед применением могут быть растворены в стерильной воде или любой другой пригодной для инъекций стерильной среде. В качестве твердых композиций для перорального применения могут быть использованы таблетки, пилюли, порошки (желатиновые капсулы, крахмальные облатки) или гранулы. Активное начало в композициях смешивают в токе аргона с одним или несколькими инертными разбавителями, такими как крахмал, целлюлоза,сахароза, лактоза или кремнезем. Эти композиции могут также содержать другие, отличные от разбавителей, вещества, например одно или несколько маслянистых материалов, таких как стеарат магния или тальк, агент, способствующий всасыванию при пероральном применении,краситель, оболочка (драже) или лак. В качестве жидких композиций для перорального применения можно использовать фармацевтически приемлемые растворы, суспензии,эмульсии, сиропы и эликсиры, содержащие инертные разбавители, такие как вода, этиловый спирт, глицерин, растительные масла или парафиновое масло. Эти композиции могут содержать другие, отличные от разбавителей, вещества, например смачивающие, подслащивающие,загущающие, ароматизирующие или стабилизирующие продукты. Композициями для ректального применения являются суппозитории или ректальные капсулы, которые кроме активного продукта содержат эксципиенты, такие как масло какао,полусинтетические глицериды или полиэтиленгликоли. Композиции для местного применения могут, например, представлять собой кремы, лосьоны, глазные капли, полоскания, капли для носа или аэрозоли. Дозы зависят от желаемого эффекта, от продолжительности лечения и от пути введения. Обычно они составляют от 0,5 до 10 мг/кг в сутки при подкожном применении, что соответствует суточной дозе от 3 до 60 мг для взрослого человека весом 60 кг. В общем случае врач должен определить подходящую дозу в зависимости от возраста,веса и всех остальных факторов, связанных с проходящим лечение лицом. Изобретение относится также к способу предупреждения и лечения болезней, связанных с воспалительным процессом, при котором происходит продукция цитотоксических веществ,таких как закись азота (NO). Олигосахариды формулы I могут таким образом быть использованы для предупреждения и/или лечения нейро 15 дегенеративных заболеваний, в случае которых воспаление мозга играет разрушающую роль с возможным летальным исходом, из которых можно назвать ишемии центральной нервной системы, церебральные ишемии, ишемии сетчатки и внутреннего уха, ишемии сердца (инфаркт миокарда), периферические ишемии, повреждения центральной нервной системы и, в частности, черепные, спинномозговые и черепно-спинномозговые травмы, травмы сетчатки и внутреннего уха, рассеянный склероз, невропатические боли и периферические невропатии,заболевания двигательных нейронов, в том числе боковой амиотрофический склероз, нейроСПИД, болезнь Альцгеймера, болезнь Паркинсона и хорея Гентингтона, и некоторые формы остеоартритов, в частности, локализованных в суставах. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Олигосахариды формулы в которой n является целым числом от 0 до 25;R1, R3, R4 и R5, одинаковые или разные, обозначают атом водорода или радикал SО 3 М; R2 и R6,одинаковые или разные, обозначают атом водорода или радикал SО 3 М или СОСН 3 и М обозначает натрий, кальций, магний или калий,смесь этих олигосахаридов и их диастереоизомеры. 2. Олигосахариды формулы I по п.1, у которых R4 обозначает атом водорода, смесь этих олигосахаридов и их диастереоизомеры. 3. Олигосахариды формулы I по одному из пп.1 или 2, у которых n является целым числом от 0 до 10, смесь этих олигосахаридов и их диастереоизомеры. 4. Олигосахариды формулы I по одному из пп.1 или 2, у которых n является целым числом от 0 до 6, смесь этих олигосахаридов и их диастереоизомеры. 5. Олигосахариды формулы I по одному из пп.1 или 2, у которых n является целым числом от 1 до 6, смесь этих олигосахаридов и их диастереоизомеры. 6. Способ получения олигосахаридов формулы I по п.1, отличающийся тем, что гидроксид щелочного металла или четвертичного аммония вводят во взаимодействие с олигосахаридами формулы в которой n является целым числом от 0 до 25;R1, R3, R4 и R5, одинаковые или разные, обозначают атом водорода или радикал SО 3 М; R2 и R6,одинаковые или разные, обозначают атом водорода или радикал SО 3 М или СОСН 3 и М обозначает натрий, кальций, магний или калий, или их смеси, и выделяют олигосахариды или их смеси. 7. Способ по п.6, отличающийся тем, что реакцию проводят в водной среде при температуре от 40 до 80 С и рН от 10 до 13. 8. Способ по одному из пп.6 или 7, отличающийся тем, что используют 1-5%-ный водный раствор гидроксида щелочного металла или четвертичного аммония. 9. Способ по одному из пп.6-8, отличающийся тем, что реакцию проводят при температуре от 60 до 70 С. 10. Способ по одному из пп.6-9, отличающийся тем, что рН реакционной среды составляет от 11 до 12,5. 11. Способ по пп.6-10, отличающийся тем,что гидроксидом щелочного металла или четвертичного аммония является гидроксид натрия,гидроксид калия, гидроксид лития, цезия или гидроксид тетрабутиламмония. 12. Фармацевтические композиции, содержащие в качестве активного начала по меньшей мере один олигосахарид по п.1. 13. Фармацевтические композиции, содержащие в качестве активного начала по меньшей мере один олигосахарид по одному из пп.1-5. 14. Применение олигосахаридов формулыI по одному из пп.1-5 для получения лекарственного средства, пригодного для профилактики или лечения заболеваний, связанных с воспалительным процессом, при котором происходит образование закиси азота (NO). 15. Применение олигосахаридов формулыI по п.14 для получения лекарственного средства, пригодного для профилактики и лечения церебральных, сердечных или периферических сосудистых ишемий, остеоартритов, повреждений центральной нервной системы, черепных,спинно-мозговых и черепно-спинно-мозговых травм, рассеянного склероза, невропатических болей и периферических невропатий, заболеваний двигательных нейронов, бокового амиотрофического склероза, нейро-СПИДа, болезни Альцгеймера, болезни Паркинсона и хореи Гентингтона.
МПК / Метки
МПК: C08B 37/00, A61P 25/02, C07H 19/01, A61K 31/70
Метки: олигосахариды,способ, получения, содержащие, фармацевтические, композиции
Код ссылки
<a href="https://eas.patents.su/9-4046-oligosaharidysposob-ih-polucheniya-i-soderzhashhie-ih-farmacevticheskie-kompozicii.html" rel="bookmark" title="База патентов Евразийского Союза">Олигосахариды,способ их получения и содержащие их фармацевтические композиции</a>













