Идрапаринукс для лечения и вторичной профилактики случаев венозной тромбоэмболии у пациентов с тромбозом глубоких вен
Формула / Реферат
1. Доза 2,5 мг пентасахарида метил-O-(2,3,4-три-O-метил-6-O-сульфо-a -D-глюкопиранозил)-(1R4)-O-(2,3-ди-O-метил-b-D-глюкопиранозилуроновая кислота)-(1R4)-O-(2,3,6-три-O-сульфо-a -D-глюкопиранозил)-(1R4)-O-(2,3-ди-O-метил-a -L-идопиранозилуроновая кислота)-(1R4)-2,3,6-три-O-сульфо-a -D-глюкопиранозида или его фармацевтически приемлемой соли для применения в терапии путем введения один раз в неделю.
2. Доза по п.1, где пентасахарид находится в форме его нонанатриевой соли (идрапаринукс).
3. Применение дозы 2,5 мг пентасахарида метил-O-(2,3,4-три-O-метил-6-O-сульфо-a -D-глюкопиранозил)-(1R4)-O-(2,3-ди-O-метил-b-D-глюкопиранозилуроновая кислота)-(1R4)-O-(2,3,6-три-O-сульфо-a -O-глюкопиранозил)-(1R4)-O-(2,3-ди-O-метил-a -L-идопиранозилуроновая кислота)-(1R4)-2,3,6-три-O-сульфо-a -D-глюкопиранозида или его фармацевтически приемлемой соли для приготовления лекарства, вводимого один раз в неделю, для лечения и/или вторичной профилактики случаев венозной тромбоэмболии у пациентов с тромбозом глубоких вен.
4. Применение по п.1, где пентасахарид находится в форме его нонанатриевой соли (идрапаринукс).
5. Способ лечения пациентов с тромбозом глубоких вен, страдающих от случаев венозной тромбоэмболии, и/или их вторичной профилактики, при котором указанному пациенту один раз в неделю вводят дозу 2,5 мг пентасахарида метил-O-(2,3,4-три-O-метил-6-O-сульфо-a -D-глюкопиранозил)-(1R4)-О-(2,3-ди-О-метил-b-D-глюкопиранозилуроновая кислота)-(1R4)-O-(2,3,6-три-O-сульфо-a -D-глюкопира-нозил)-(1R4)-O-(2,3-ди-O-метил-a -L-идопиранозилуроновая кислота)-(1R4)-2,3,6-три-O-сульфо-a -D-глюкопиранозида или его фармацевтически приемлемой соли.
6. Способ лечения по п.5, где пентасахарид находится в форме его нонанатриевой соли (идрапаринукс).
Текст
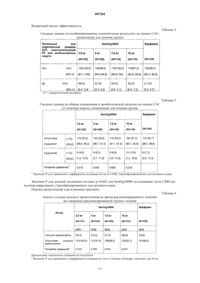
007204 Изобретение относится к специфической дозе SanOrg34006 для применения в лечении и вторичной профилактике случаев венозной тромбоэмболии (VTE, venous thromboembolic events) у пациентов с тромбозом глубоких вен (DVT, deep venous thrombosis). Рецидив VTE после лечения острого DVT является распространнным клиническим признаком после окончания острого лечения болезни с помощью антитромбозной терапии. Поэтому для снижения масштабов долговременного рецидива требуется долговременная антитромботическая терапия. Обычно для лечения VTE применяются нефракционированный гепарин (UFH), низкомолекулярный гепарин(LMWH), тромболитические агенты и варфарин. Принятый в настоящее время подход к острому лечению DVT с последующей долговременной терапией заключается в том, что гепариновую и пероральную антикоагулянтную терапию (варфарин или другой кумарин) начинают одновременно после постановки диагноза и прекращают гепариновую терапию между четвртыми и седьмыми сутками. Несколько рандомизированных испытаний на пациентах с VTE показали, что от 5 до 7 суток начальной гепариновой терапии, сопряжнной с ранним введением варфарина и лечением в течение по крайней мере 3-х месяцев является эффективным и безопасным. [Hyers, et al., ACCP 2001, CHEST 2001; 119:180S]. Для эффективного лечения, в исследованиях, выполненных как на животных, так и на людях, было показано, что уровень гепарина в плазме 0,2-0,4 МЕ/мл ингибирует увеличение количества тромбов [Hyers, et al., ACCP 2001, CHEST 2001; 119:178S]. Неожиданно и в противоречие с общей практикой в настоящее время было обнаружено, что такая низкая доза, как 2,5 мг пентасахарида метил-О-(2,3,4-три-O-метил-6-O-сульфоD-глюкопиранозил)(14)-O-(2,3-ди-O-метилD-глюкопиранозилуроновая кислота)-(14)-O-(2,3,6-три-O-сульфоDкислота)-(14)-2,3,6-три-Oглюкопиранозил)-(14)-O-(2,3-ди-O-метилL-идопиранозилуроновая сульфоD-глюкопиранозида или его фармацевтически приемлемой соли (в частности, его нонанатриевая соль SanOrg34006, см., например, US 5378829) эффективна и безопасна для лечения и вторичной профилактики VTE у пациентов с DVT при введении один раз в неделю. После введения дозы 2,5 мгVTE (см. выше). Поскольку схемы лечения и вторичной профилактики VTE у пациентов с DVT могут быть связаны с повышенным риском кровотечения, самая низкая доза антикоагулянта, являющаяся эффективной и безопасной, является наиболее предпочтительной дозой. Введение один раз в неделю низкой дозыSanOrg34006, согласно настоящему изобретению, приводит к очень низким уровням в плазме, которые неожиданно вс ещ эффективны в профилактике и лечении VTE. Схема лечения по настоящему изобретению не требует последующего мониторинга и уточнения дозы. Термин "фармацевтически приемлемая соль" означает соль с такими противоионами, как ионы щелочных или щелочно-земельных металлов, таких как натрий, кальций или магний. Дозу пентасахарида по изобретению вводят как подкожную инъекцию пациенту, подвергающемуся лечению. Предпочтительно пациент является человеком. Пентасахарид может применяться в качестве фармацевтической композиции, включающей указанный пентасахарид вместе с фармацевтически приемлемыми вспомогательными веществами и возможно с другими фармацевтическими агентами. Термин "приемлемый" означает совместимый с другими ингредиентами композиции и не вредный для реципиентов. Фармацевтическая композиция для парентерального введения дозы пентасахарида по данному изобретению может быть представлена в контейнерах на одну дозу или множество доз, в частности, инъекционными жидкостями в заранее определнных количествах, например, в запаянных флаконах и ампулах, и может также храниться в сублимационно высушенном (лиофилизированном) состоянии, требующим только добавления стерильного жидкого носителя, например воды, перед применением. Смешанный с такими фармацевтически приемлемыми вспомогательными веществами и жидкостями, например, как описано в стандартной ссылке Gennaro et al., Remington's Pharmaceutical Sciences (18thManufacture), этот пентасахарид может использоваться в виде жидкой композиции, препарата для инъекции, в форме раствора, суспензии или эмульсии. Могут быть использованы водные суспензии, изотонические физиологические растворы и стерильные инъецируемые растворы, содержащие фармацевтически приемлемые диспергирующие агенты и/или смачивающие агенты, такие как пропиленгликоль или бутиленгликоль. Предпочтительной фармацевтической композицией является изотонический физиологический раствор пентасахарида. Фармацевтическая композиция согласно изобретению может также быть представлена в форме ветеринарной композиции, такие композиции могут быть приготовлены традиционными способами. Далее изобретение проиллюстрировано следующим примером. Пример. Клинические данные, демонстрирующие как эффективность, так и безопасность (применения) дозы 2,5 мг SanOrg34006 при лечении и вторичной профилактике случаев венозной тромбоэмболии(VTE) у пациентов с тромбозом глубоких вен (DVT) по сравнению с варфарином. Общий план исследования. Исследование представляло собой двухфазное, многоцентровое, рандомизированное исследование,выполненное в пяти параллельных группах, двойное слепое для дозы SanOrg34006 и открытое слепое для эксперта для пероральной дозы варфарина (группа сравнения). План исследований проиллюстрирован на фиг. 1. Фиг. 1 План исследования После первоначального лечения всех пациентов 9-14 инъекциями (соответствует 61 суткам) эноксапарина (представляющего LMWHs) все 650 пациентов с подтвержднным симптоматическим проксимальным DVT случайным образом были определены в одну из групп лечения (2,5, 5, 7,5 или 10 мгSanOrg34006 ПК подкожно или перорально варфарин). Каждая группа лечения состояла из 130 пациентов, из которых по крайней мере 100 пациентов подходили для включения в группу назначенного лечения (ITT, Intent-To-Treat). За испытуемыми в группах лечения SanOrg34006 наблюдали в течение 4 недель после заключительных оценок. Задачи. Первичными (взаимосвязанными) задачами этого исследования было оценить взаимосвязь доза-эффект для SanOrg34006 для предотвращения рецидива и распространения VTE после периода первоначального лечения симптоматического проксимального DVT эноксапарином; определить оптимальную дозу SanOrg34006, которая будет использована в дальнейших сравнительных терапевтических исследованиях. Эту оптимальную дозу выбирали, учитывая эффективность,безопасность, маркеры коагуляции и общее исполнение. Вторичной задачей было оценить популяционную фармакокинетику SanOrg34006. Диагостика и критерии включения: симптоматический проксимальный DVT (определнный как тромбоз в подколенной вене, поверхностной бедренной вене или общей бедренной вене), подтвержднный CUS (компрессионный ультразвук/эхо) или венографией; мужчины или небеременные женщины; подписанное письменное информированное согласие. Продолжительность лечения: 9-14 инъекций эноксапарина каждому пациенту (соответствует 5-7 суткам лечения) с последующими 12 введениями SanOrg34006 один раз в неделю или 12-недельный курс варфарина. Продолжительность участия в исследовании: 61 суток лечения эноксапарином и до 12 недель 1 сутки рандомизированного лечения и для групп лечения SanOrg34006 дополнительное наблюдение в течение 4 недель. Критерии для оценки Эффективность. Первичный параметр эффективности: изменение тромботической нагрузки по оценке центрального жюри (central adjudication committee) с применением 3-точечной нормальной шкалы результатов для-2 007204 сравнения CUS и PLS (перфузионное лгочное сканирование) через 12 недель рандомизированного лечения с измерениями базового уровня (т.е. ухудшение, нормализация или отсутствие релевантных изменений), включая дополнительный анализ существенного улучшения. Вторичные параметры эффективности: изменение тромботической нагрузки с применением бинарной шкалы (т.е. ухудшение против отсутствия ухудшения); изменение CUS по 3-точечной одинарной шкале; изменение PLS по 3-точечной одинарной шкале; комбинированный клинический результат (нефатальный симптоматический PE и/или рецидив DVT, смерть из-за PE и/или DVT или необъясннная и любое значительное изменение в лечебной тактике тромботических случаев); маркеры коагуляции: плазматический D-димер (фибриновый фрагмент, освобожднный в процессе тромболиза; оценка происходящего тромбоза) и концентрации ТАТ(тромбин-антитромбиновый комплекс) во время исследуемого лечения. Безопасность. Первичные параметры безопасности: процент сильного кровотечения и снижение числа тромбоцитов. Вторичные параметры эффективности: (тяжлые) побочные реакции, лабораторные параметры (гематология, биохимия, коагуляционный статус, количество тромбоцитов) и показатели жизнедеятельности (кровяное давление, частота сердцебиения, масса тела). Фармакокинетика. Концетрации SanOrg34006 в плазме оценивали в пределах 48 ч до введения SanOrg3406 на 2-й, 4-й и 7-й неделях. Дополнительно на протяжении 7-й недели во временных рамках 0,5-2, 2-6, 6-48 и 120-168 ч после дозы. В подгруппе пациентов применяли более подробную схему анализов с предозным взятием анализа перед каждым введением и серийную схему для 7-й недели применяли также на 1-й и 12-й неделях. Параметры Смакc, Смин и AUC(0-168) (площадь под кривой концентрации) вычисляли на основании наиболее подробных данных по 7-й неделе (и по 1-й и 2-й неделям для вышеупомянутой подгруппы). Первичный анализ эффективности. Таблица 1 Сводные данные общих изменений в тромботической нагрузке по оценке CAC (3-точечная шкала); группа ITT. Данные включают необъясннные смерти, симптоматические случаи (вплоть до ухудшения),компрессионные ультрасонографические изменения в верхней части ноги (отсутствие) и сцинтиграфические изменения в лгких (отсутствие). Процентные показатели основаны на подсчтах. CAC =Central Adjudication Committee а 3 начение P для сравнения с варфарином, основаны на тесте CMH, стратифицированного для активного рака Значение P для дозовой тенденции составил р=0,388 на основании теста Cochran-Mantel-Haenszel(ненулевая корреляция) для дозовых тенденций (CMH тест), стратифицированный для активного рака.-3 007204 Вторичный анализ эффективности. Таблица 2 Сводные данные по комбинированному клиническому результату по оценке CAC; назначенная для лечения группа Таблица 3 Сводные данные по общим изменениям в тромботической нагрузке по оценке CAC(2-точечная шкала); назначенная для лечения группа Значение P для сравнения с варфарином основаны на тесте CMH, стратифицированном для активного рака Значение P для дозовой тенденции составил р=0,062 для SanOrg34006 на основании теста CMH (ненулевая корреляция), стратифицированного для активного рака. Оценки кровотечений и родственные критерии. Таблица 4 Анализ случаев сильного кровотечения во время рандомизированного лечения; все пациенты рандомизированной группы лечения Процентные показатели основаны на подсчтах.a Значение P для сравнения с варфарином основаны на тесте Cochran-Armitage, значение для 10 мг-4 007204 Значение P для дозовой тенденции составило р=0,003 для SanOrg34006 на основании теста CochranArmitage. Таблица 5 Анализ всех случаев кровотечения во время рандомизированного лечения; все пациенты рандомизированной группы лечения Процентные показатели основаны на подсчтах. а 3 начение P для сравнения с варфарином основаны на тесте Cochran-Armitage, значение для 2,5 мг Значение P для дозовой тенденции составило р=0,001 для SanOrg34006 на основании теста CochranArmitage. Выводы. Статистически значимой взаимосвязи доза-эффект для тестируемых доз SanOrg34006 не наблюдали с учтом первичной и вторичной конечных точек. Различий в эффективности между тестируемыми дозами варфарина и SanOrg34006 не наблюдали. Статистически значимо меньше случаев кровотечений происходило в группе 2,5 мг SanOrg34006 по сравнению с варфарином. Статистически значимую дозовую тенденцию наблюдали для случаев кровотечений и сильных кровотечений. Группу 10 мг SanOrg34006 преждевременно прервали, поскольку к этой дозовой группе применили правило остановки для сильных кровотечений. Все дозы SanOrg34006 и варфарина в общем хорошо переносились в отношении побочных явлений(иных, чем кровотечения), лабораторных параметров и показателей жизнедеятельности. Наблюдали пропорциональную дозе фармакокинетику, и устойчивое состояние было достигнуто на 12-й неделе при концентрации в три раза выше и значении AUC в два раза выше, чем соответствующие значения после первого введения. Масса тела и клиренс креатинина показали сильную взаимосвязь с фармакокинетикой SanOrg34006,приводящую к возрастанию экспозиции SanOrg34006 со снижением массы тела и клиренса креатинина. Случаи кровотечений (сильные и все кровотечения), совпадающие с большей экспозициейSanOrg34006, в ковариантном анализе преимущественно были связаны с возрастом и клиренсом креатинина. Все концентрации в плазме после лечения 2,5 мг SanOrg34006 оставались ниже уровней, связанных с повышенным риском кровотечения. Дополнительный анализ. Ниже на фиг. 2 показана предсказанная средняя концентрация SanOrg34006 (идрапаринукса) в плазме в зависимости от временного профиля в течение лечения пациентов с VTE дозой 2,5 мг идрапаринукса один раз в неделю на основании результатов вышеприведнного исследования. Значения, рекомендованные АССР [см. Hyers et al., ACCP 2001, CHEST 2001; 119:178S] показаны между пунктирных линий. Фиг. 2 Предсказанная средняя концентрация SanOrg34006 (идрапаринукса) в плазме в зависимости от временного профиля на протяжении лечения пациентов с VTE дозой 2,5 мг идрапаринукса (один раз в неделю) Известно, что если лечение неадекватно в течение недели, когда это лечение начали, это оказывает сильное воздействие на ход дальнейших событий [т.е. позднее по времени, даже если адекватность восстановлена (ссылка Brandjes et al., NEJM 1992;327 (21):1485-9)]. Отмечается, что испытания 'Brandjes' связаны с неадекватностью острого лечения. Между тем, неадекватное лечение ПОСЛЕ недели острого лечения приносит больший вред: неадекватность в течение следующих 12 недель (период настоящего исследования) может приводить к 25% рецидивам VTE (Cl Laagerstedt et al., Lancet 1985; Sep 7:515-8; R.Hull et al., NEJM 1979; 301(16):855-8). Первая SanOrg34006-неделя настоящего исследования в действительности является второй неделей лечения. Таким образом, если лечение SanOrg34006 было неадекватно ранее по ходу лечения, можно ожидать случаи увеличения тромботической нагрузки позже по ходу лечения. Между тем, даже если уровни в плазме 75% пациентов дозовой группы 2,5 мг были 'слишком низкими' согласно рекомендациям АССР, не наблюдали увеличения ухудшения по сравнению с популяциями более высоких доз в пределах градаций АССР. Это показано в табл. 6 ниже. Таблица 6 Доля (%; n/N) ухудшения общей тромботической нагрузки в течение 12-недельного периода лечения в разных классах наблюдаемых минимальных концентраций идрапаринукса в плазме (Смин) в течение 7-й недели, когда данные собирали от всех рандомизированных пациентов; популяция ITTc поддающейся оценке конечной точкой эффективности и подходящей оценкой PK.PK = Pharmacokinetic, фармакокинетика; подходящая оценка PK относится к Смин, которая является концентрацией непосредственно перед следующим введением, также называемая Свпадины или уровнем впадины, самый низкий уровень, определяемый для каждой вводимой последующей дозы. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Доза 2,5 мг пентасахарида метил-O-(2,3,4-три-O-метил-6-O-сульфоD-глюкопиранозил)-(14)O-(2,3-ди-O-метилD-глюкопиранозилуроновая кислота)-(14)-O-(2,3,6-три-O-сульфоDглюкопиранозил)-(14)-O-(2,3-ди-O-метилL-идопиранозилуроновая кислота)-(14)-2,3,6-три-OсульфоD-глюкопиранозида или его фармацевтически приемлемой соли для применения в терапии путем введения один раз в неделю. 2. Доза по п.1, где пентасахарид находится в форме его нонанатриевой соли (идрапаринукс). 3. Применение дозы 2,5 мг пентасахарида метил-O-(2,3,4-три-O-метил-6-O-сульфоDглюкопиранозил)-(14)-O-(2,3-ди-O-метилD-глюкопиранозилуроновая кислота)-(14)-O-(2,3,6-три-6 007204O-сульфоO-глюкопиранозил)-(14)-O-(2,3-ди-O-метилL-идопиранозилуроновая кислота)-(14)2,3,6-три-O-сульфоD-глюкопиранозида или его фармацевтически приемлемой соли для приготовления лекарства, вводимого один раз в неделю, для лечения и/или вторичной профилактики случаев венозной тромбоэмболии у пациентов с тромбозом глубоких вен. 4. Применение по п.1, где пентасахарид находится в форме его нонанатриевой соли (идрапаринукс). 5. Способ лечения пациентов с тромбозом глубоких вен, страдающих от случаев венозной тромбоэмболии, и/или их вторичной профилактики, при котором указанному пациенту один раз в неделю вводят дозу 2,5 мг пентасахарида метил-O-(2,3,4-три-O-метил-6-O-сульфоD-глюкопиранозил)-(14)-О(2,3-ди-О-метилD-глюкопиранозилуроновая кислота)-(14)-O-(2,3,6-три-O-сульфоD-глюкопиранозил)-(14)-O-(2,3-ди-O-метилL-идопиранозилуроновая кислота)-(14)-2,3,6-три-O-сульфоDглюкопиранозида или его фармацевтически приемлемой соли. 6. Способ лечения по п.5, где пентасахарид находится в форме его нонанатриевой соли (идрапаринукс).
МПК / Метки
МПК: A61P 7/02, A61K 31/70, A61K 31/7024
Метки: профилактики, тромбозом, лечения, венозной, случаев, вен, глубоких, вторичной, идрапаринукс, пациентов, тромбоэмболии
Код ссылки
<a href="https://eas.patents.su/8-7204-idraparinuks-dlya-lecheniya-i-vtorichnojj-profilaktiki-sluchaev-venoznojj-tromboembolii-u-pacientov-s-trombozom-glubokih-ven.html" rel="bookmark" title="База патентов Евразийского Союза">Идрапаринукс для лечения и вторичной профилактики случаев венозной тромбоэмболии у пациентов с тромбозом глубоких вен</a>