2-(3,5-бистрифторометилфенил)-n-метил-n-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамид
Номер патента: 4404
Опубликовано: 29.04.2004
Авторы: Хиггинз Гай Эндру, Хоффманн Торстен, Слейт Эндру, Боллард Тереса Мария, Поли Сония Мария
Формула / Реферат
1. 2-(3,5-Бистрифторметилфенил)-N-метил-N-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамид формулы I
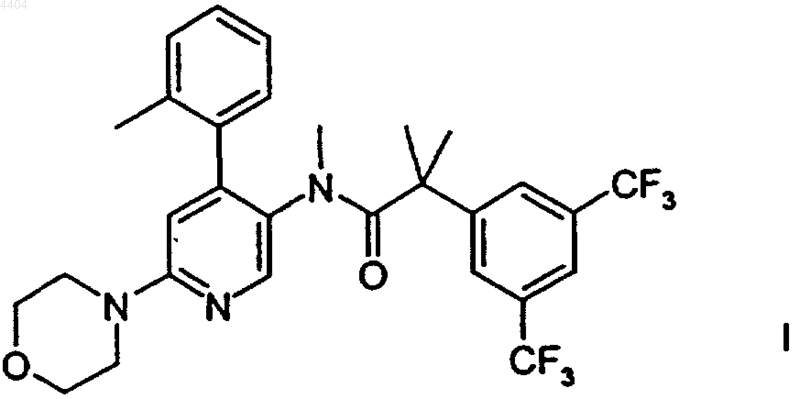
и его фармацевтически приемлемые кислотно-аддитивные соли.
2. Лекарственное средство, включающее соединение по п.1 и фармацевтически приемлемые носители.
3. Лекарственное средство по п.2, предназначенное для лечения болезней, связанных с рецептором NK-1.
4. Способ получения соединения формулы I по п.1, предусматривающий взаимодействие соединения формулы
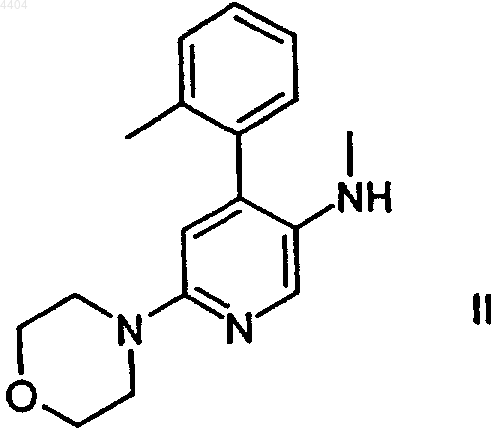
с соединением формулы
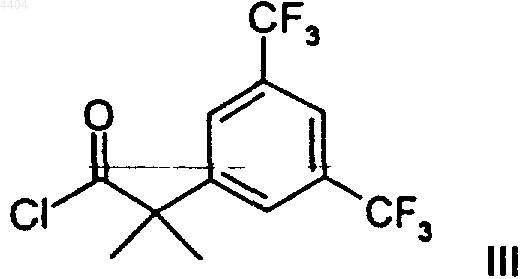
с получением соединения формулы
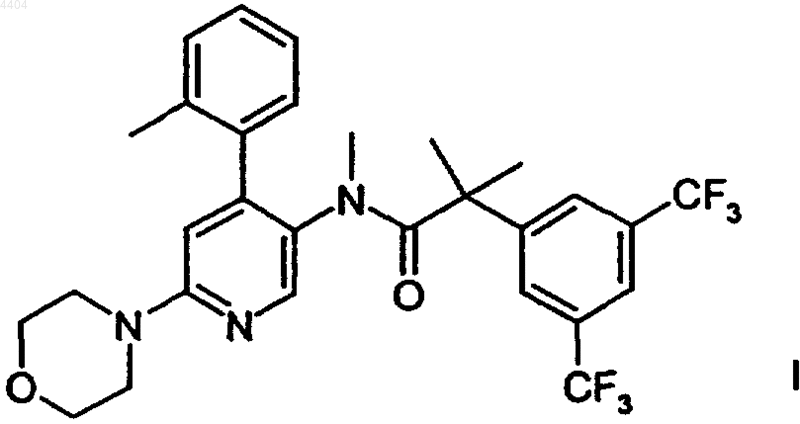
и при необходимости превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль.
5. Соединение по п.1, полученное способом, охарактеризованным в п.4.
Текст
1 Настоящее изобретение относится к соединению формулы и к его фармацевтически приемлемым кислотно-аддитивным солям. Соединение формулы I и его соли отличаются ценными терапевтическими свойствами. Было установлено, что соединение по настоящему изобретению является высоко избирательным антагонистом рецептора нейрокинина(NK-1, вещество Р). Вещество Р представляет собой встречающийся в естественных условиях ундекапептид, принадлежащий к пептидам из семейства тахикининов, последние так называются из-за быстрого сократительного действия на внесосудистую ткань гладкой мускулатуры. Рецептор вещества Р является представителем надсемейства связанных с протеином G рецепторов. Нейропептидный рецептор вещества Р(NK-1) широко распространен в нервной системе млекопитающих (особенно в головном мозге и спинальных ганглиях), кровеносной системе и периферических тканях (особенно в двенадцатиперстной кишке и тощей кишке), и он участвует в регуляции многочисленных разнообразных биологических процессов. Центральное и периферическое действие тахикинина млекопитающих, т.е. вещества Р,связывали с многочисленными воспалительными состояниям, включая мигрень, ревматоидный артрит, астму и воспалительное заболевание кишечника, а также с ролью в качестве медиатора рвотного рефлекса и модулятора нарушений центральной нервной системы (ЦНС),таких как болезнь Паркинсона (Neurosci. Res. 7,187-214, 1996), состояния тревоги (Can. J. Phys.,75, 612-621, 1997) и депрессии (Science, 281,1640-1645, 1998). Данные о возможности применения антагонистов рецептора тахикинина для лечения боли, головной боли, прежде всего мигрени,болезни Альцгеймера, рассеянного склероза,ослабления синдрома отказа от морфина, сердечно-сосудистых изменений, отека, такого как отек, вызванный термическим повреждением,хронических воспалительных заболеваний, таких как ревматоидный артрит, астма/бронхиальная гиперреактивность и другие респираторные заболевания, включая аллергический ринит, воспалительные заболевания кишечника,включая язвенный колит и болезнь Крона, повреждения глаза и глазных воспалительных заболеваний, обобщены в статье "Tachykinin Receptor and Tachykinin Receptor Antagonists" J. 2 Кроме того, антагонисты рецептора нейрокинина I разработаны с целью лечения многочисленных физиологических нарушений, связанных с избытком или с нарушением баланса тахикининов, в частности вещества Р. Примеры состояний, которые связаны с веществом Р,включают нарушения центральной нервной системы, такие как состояние тревоги, депрессия и психоз (WO 95/16679, WO 95/18124 и WO 95/23798). Антагонисты рецептора нейрокинина-1,кроме того, могут применяться для лечения состояния укачивания и индуцированной лекарственным средством рвоты. Кроме того, в журнале The New EnglandJournal of Medicine, том 34,3, 190-195, 1999 описано уменьшение индуцированной цисплатином рвоты с помощью избирательных антагонистов рецептора нейрокинина-1. Кроме того, также известны данные о возможности применения антагонистов рецептора нейрокинина-1 для лечения определенных форм недержания мочи (Neuropeptides, 32(1), 1-49,1998 и Eur. J. Pharmacol. 383(3), 297-303, 1999). В патенте US 5972938 также описан способ лечения психоиммунологического или психосоматического нарушения путем введения антагониста рецептора тахикинина, такого как рецептор NK-1. В Life Sci., 67(9), 985-1001, 2000 описано,что астроциты экспрессируют функционально активные рецепторы различных нейромедиаторов, включая вещество Р, которое является важным стимулом реактивности астроцитов при развитии ЦНС, инфекции и повреждении. При опухолях головного мозга злокачественные глиальные клетки, происходящие из астроцитов,запускаются тахикининами через рецепторыNK-1, что приводит к секреции растворимых медиаторов и повышению скорости пролиферации. Таким образом, избирательные антагонисты рецептора NK-1 могут применяться а качестве терапевтического агента для лечения злокачественных глиом в терапии рака. В Nature (London), 405 (6783), 180-193,2000 описано, что мыши с генетическим нарушением рецептора NK-1 становятся нечувствительными к наркотическим свойствам морфина. Следовательно, антагонисты рецептора NK-1 могут применяться для лечения симптомов отмены наркотиков, таких как опиаты и никотин,и уменьшения злоупотребления ими/пристрастия к ним. Объектами настоящего изобретения являются соединение формулы I и его фармацевтически приемлемые соли, получение вышеуказанного соединения, лекарственные средства,содержащие это соединение, и их изготовление,а также применение вышеуказанного соединения для лечения или профилактики болезней,прежде всего болезней и нарушений указанных 3 ранее типов, или для изготовления соответствующих лекарственных средств. Наиболее предпочтительными показаниями согласно настоящему изобретению являются показания, которые включают заболевания центральной нервной системы, например, лечение или профилактика определенных депрессивных нарушений, состояния тревоги или рвоты путем введения антагониста рецептора NK-1. Установлено, что серьезный приступ депрессии продолжается в течение по меньшей мере двух недель, во время которых в течение большей части дня и практически каждый день наблюдается подавленное настроение или потеря интереса ко всему или удовольствия от всего, или практически полная потеря активности. В контексте настоящего описания понятие"фармацевтически приемлемые кислотноаддитивные соли" включает соли с неорганическими или органическими кислотами, такими как соляная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота,муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, паратолуолсульфоновая кислота и т.п. Соединение формулы I по настоящему изобретению и его фармацевтически приемлемые соли могут быть получены методами, хорошо известными в данной области, например, с помощью описанных ниже способов, включающих взаимодействие соединения формулы 4 40 С. Требуемое соединение формулы I получают после очистки с хорошим выходом. Процесс солеобразования осуществляют при комнатной температуре согласно хорошо известным методам, которые доступны специалисту в данной области. Могут быть получены не только соли с неорганическими кислотами,но также соли с органическими кислотами. Примерами таких солей являются гидрохлориды, гидробромиды, сульфаты, нитраты, цитраты, ацетаты, малеаты, сукцинаты, метансульфонаты, паратолуолсульфонаты и т.п. На приведенных ниже схемах 1 и 2 и в примере 1 более детально описаны способы получения соединения формулы I. Исходные продукты формул III, IV и VII являются известными соединениями или могут быть получены согласно методам, известным в данной области. На схемах использовали следующие сокращения: ПивСl - пивалоилхлорид ТГФ - тетрагидофуран ТМЭДА - N,N,N',N'-тетраметилэтилендиамин ДИПЭА - N-этилдиизопропиламин Схема 1 с получением соединения формулы Схема 2 и при необходимости превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль. Согласно варианту а) осуществления способа DIPEA (N-этилдиизопропиламин) добавляют к смеси соединения формулы II и соединения формулы III в дихлорметане и смесь перемешивают при температуре в диапазоне 35 Как отмечалось ранее, соединение формулы I и его фармацевтически приемлемые кислотно-аддитивные соли обладают ценными фармакологическими свойствами. Установлено,что соединение по настоящему изобретению 5 является антагонистом рецептора нейрокинина 1 (NK-1, вещество Р). Соединение формулы I изучалось с помощью приведенных ниже тестов. Сродство соединения формулы I к NK1-рецептору оценивали с использованием человеческих NK1 рецепторов в СНО-клетках, зараженных человеческим NK1-рецептором (с использованием экспрессионной системы вируса Semliki) и в присутствии радиоактивномеченного с помощью[3 Н]-вещества Р (конечная концентрация 0,6 нМ). Опыты по связыванию проводили вHEPES-буфере (50 мМ, рН 7,4), содержащим БСА (бычий сывороточный альбумин) (0,04%),леупептин (8 мкг/мл), МnСl2 (3 мМ) и фосфорамидон (2 мкМ). В опытах по связыванию использовали 250 мкл суспензии мембран(1,25 х 105 клеток/пробирку для анализа), 0,125 мкл буфера, включающего замещающий агент,и 125 мкл [3 Н]-вещества Р. Для получения кривых замещения использовали по меньшей мере 7 концентраций соединения. Пробирки для анализа инкубировали в течение 60 мин при комнатной температуре, после чего содержимое пробирки быстро фильтровали под вакуумом через фильтры типа GF/C, которые предварительно в течение 60 мин пропитывали PEI(0,3%) с 2 промывками, для каждой из которых использовали по 2 мл HEPES-буфера (50 мМ,рН 7,4). Радиоактивность, сохранившуюся на фильтрах, оценивали с помощью сцинцилляционного счетчика. Все опыты проводили в трех повторностях по меньшей мере в 2 различных экспериментах. При изучении с использованием рекомбинантных человеческих рецепторов нейрокинина 1 (NK1), экспрессируемых в СНО-клетках, соединение формулы I проявило себя как эффективный и избирательный антагонист. Его сродство (выраженное в виде значения рKi), составляющее 9,0 для человеческого NK1-рецептора,по избирательности действия в отношении NK1 рецептора на 2 порядка превышало сродство кNK2- и NK3-peцeптopaм и по отношению к более чем 50 другим сайтам связывания, которые были исследованы. Активность in vitro оценивали по воздействию на индуцированные веществом потоки Са 2+ в СНО-клетках, экспрессирующих рекомбинантный человеческий NK1-рецептор. В этих клетках вещество Р вызывает зависящий от концентрации поток Са 2+, который может быть измерен с использованием FLIPR-методики. Повышение концентраций 2-(3,5-бистрифторметилфенил)-N-метил-N-(6-морфолин-4-ил-4 ортотолилпиридин-3-ил)изобутирамида вызывает сдвиг вправо кривой зависимости действия от концентрации вещества Р. Построение по этим данным кривой Шильда позволяет рассчитать, что антагонистическое сродство (рА 2) для этого соединения составляет 8,9 (коэффициент регрессии Шильда равен 1,1). Эти данные сви 004404 6 детельствуют о том, что 2-(3,5-бистрифторметилфенил)-N-метил-N-(6-морфолин-4-ил-4 ортотолилпиридин-3-ил) изобутирамид является конкурентным антагонистом для человеческого рекомбинантного NK1-рецептора. В опытах in vivo соединение формулы I ингибирует в результате антагонизма поведение, характеризующееся притоптыванием, у хомяков Gerbils после интрацеребровентрикулярных (i.c.v.) инъекций агониста NK1-рецептора. Рассчитанная доза этого соединения, которая вызывает 50%-ное ингибирование поведения, характеризующегося притоптыванием,при оральном введении составляла 0,2 мг/кг. Также оценивали уровни в плазме, необходимые для полного ингибирования этого поведения, и было установлено, что для полного ингибирования поведения, характеризующегося притоптыванием, необходима концентрация 10 нг/мл. Этот антагонизм сохраняется в течение нескольких часов и на этой модели функциональное время полужизни составляет 8 ч. 2-(3,5-бистрифторметилфенил)-N-метилN-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил) изобутирамид также тестировали в качестве противорвотного агента на хорьках. Рвоту у хорьков вызывали различными рвотными средствами (апоморфин, морфин, ипекакуанха, цисплатин и 011804). Предварительная обработка соединением по изобретению (0,3 мг/кг, перорально) за 2 ч до введения рвотного средства полностью блокировала рвоту, вызываемую рвотными средствами. Строили кривую зависимости реакции от полной дозы для индуцированной апоморфином рвоты и из нее было рассчитано, что значение ED50 составляет 0,1 мг/кг при пероральном введении. При моделировании состояния укачивания на землеройках Suncus murinus установлено, что значение ED50 соединения составляет 0,2 мг/кг при пероральном введении. Таким образом, можно заключить что 2(3,5-бистрифторметилфенил)-N-метил-N-(6 морфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамид представляет собой эффективный антагонист индуцированного NK1 поведения у хомяков Gerbils и блокирует рвоту у хорьков и у землероек Suncus murinus с такой же эффективностью. На крысах и собаках были изучены фармакокинетические параметры. У крыс это соединение имело конечное время полужизни 23 ч, клиренс 4 мл/мин/кг, объем распределения 8 л/кг и биологическую доступность при оральном введении 50%. У собак время полужизни молекул составляло 40 ч, клиренс - 16 мл/мин/кг, объем распределения - 8 л/кг и биологическая доступность при оральном введении - 30-40%. Соединение формулы I, а также его фармацевтически приемлемые кислотно-аддитивные соли могут применяться в качестве лекарственных средств, например, в форме фар 7 мацевтических композиций. Фармацевтические композиции могут вводиться орально, например, в форме таблеток, таблеток с покрытием,драже, желатиновых капсул с мягким или твердым покрытием, растворов, эмульсий или суспензий. Однако введение также может быть осуществлено ректально, например, в форме суппозиториев, или парентерально, например, в форме инъецируемых растворов. Соединение формулы I и его фармацевтически приемлемые кислотно-аддитивные соли могут быть подвергнуты обработке вместе с фармацевтически инертными неорганическими или органическими эксципиентами для приготовления таблеток, таблеток с покрытием, драже и желатиновых капсул с твердым покрытием. В качестве таких эксципиентов для приготовления, например таблеток, драже и желатиновых капсул с твердым покрытием, могут использоваться лактоза, кукурузный крахмал или его производные, тальк, стеариновая кислота или ее соли и т.д. Приемлемыми эксципиентами для приготовления желатиновых капсул с мягким покрытием являются, например, растительные масла,воски, жиры, полутвердые и жидкие полиолы и т.д. Приемлемыми эксципиентами для приготовления растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар,глюкоза и т.д. Приемлемыми эксципиентами для инъецируемых растворов являются, например, вода,спирты, полиолы, глицерин, растительные масла и т.д. Приемлемыми эксципиентами для суппозиториев являются, например, природные или гидрогенизированные масла, воски, жиры, полутвердые или жидкие полиолы. Кроме того, фармацевтические композиции могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты,эмульгаторы, подслащивающие вещества, красители, корригенты, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также могут содержать и другие терапевтически ценные вещества. Дозы могут варьироваться в широких пределах и, естественно, должны быть подобраны в зависимости от индивидуальных требований в каждом конкретном случае. В целом, в случае орального введения суточная доза может находиться в диапазоне от 10 до 1000 мг соединения формулы I на пациента, однако при необходимости верхний предел может быть превышен. Приведенный ниже пример 1 служит для иллюстрации настоящего изобретения, не ограничивая его объем. Все температуры даны в градусах Цельсия. Пример 1. Гидрохлорид 2-(3,5-бистрифторметилфенил)-N-метил-N-(6-морфолин-4 004404(1:1,45). а) 4-(5-Нитpо-2-пиридил)морфолин (XII). К раствору, содержащему 20 г (126 ммолей) 2-хлор-5-нитропиридина в 150 мл тетрагидрофурана, добавляли по каплям в течение 10 мин 27 мл (315 ммолей) морфолина. Реакционную смесь кипятили с обратным холодильником в течение еще 2 ч. После охлаждения до комнатной температуры растворитель удаляли под вакуумом и остаток повторно растворяли в 200 мл этилацетата. Органическую фазу промывали 200 мл 1 н. раствора бикарбоната натрия, сушили (сульфат магния) и упаривали, получая 27,3 г(количественный выход) указанного в заголовке соединения в виде твердого вещества желтого цвета. tпл 142-143 С. б) 2,2-Диметил-N-(6-морфолин-4-илпиридин-3-ил)пропионамид (V). К раствору, содержащему 27,3 г (126 ммолей) 4-(5-нитро-2-пиридил)морфолина в 600 мл метанола, добавляли 2,5 г 10%-ного палладия на активированном древесном угле. Реакционную смесь гидрировали (температура от комнатной до примерно 45 С, 1 бар) до растворения теоретического количества водорода (примерно 3 ч). Катализатор отфильтровывали и дважды промывали порциями по 100 мл метанола. Фильтрат упаривали под вакуумом, получая 22,6 г масла фиолетового цвета, которое содержало примерно до 95% требуемого аланинового производного, что подтверждено анализом с помoщью тонкослойной хроматографии. Этот неочищенный продукт растворяли в смеси, содержащей 240 мл тетрагидрофурана и 60 мл диэтилового эфира. После охлаждения до 0 С добавляли в виде одной порции 26 мл (189 ммолей) триэтиламина. При перемешивании добавляли порциями в течение 10 мин 23 г (189 ммолей) пивалоилхлорида. Ледяную баню удаляли и реакционную смесь перемешивали в течение 1 ч при комнатной температуре. Затем растворитель удаляли под вакуумом и остаток суспендировали в 200 мл 1 н. раствора бикарбоната натрия. Продукт трижды экстрагировали порциями по 200 мл дихлорметана, сушили(сульфат натрия) и упаривали. После перекристаллизации твердого остатка из смеси этилацет/гексан 1:8 получали 28,6 г (86%) указанного в заголовке соединения в виде кристаллов белого цвета; МС m/е (%) 264 (М+Н+, 100). в) N-(4-йод-6-морфолин-4-илпиридин-3 ил)-2,2-диметилпропионамид (VI). Раствор, содержащий 28,4 г (108 ммолей) 2,2-диметил-N-(6-морфолин-4-илпиридин-3-ил) пропионамида и 49 мл (324 ммоля) N,N,N',N'тетраметилэтилендиамина в 600 мл тетрагидрофурана, в атмосфере аргона охлаждали в бане с сухим льдом до -78 С. В течение 1 ч по каплям добавляли 202 мл (324 ммоля) 1,6 н. раствора нбутиллития в гексане. Реакционной смеси давали нагреться до -36 С в течение ночи. После 9 повторного охлаждения до -78 С добавляли по каплям в течение 15 мин 37 г (146 ммолей) йода, растворенного в 60 мл тетрагидрофурана. Баню с сухим льдом заменяли на ледяную баню и добавляли в течение 10 мин 90 г (363 ммоля) пентагидрата тиосульфита натрия, после чего температура реакционной смеси повышалась до 0 С. Затем добавляли 1000 мл диэтилового эфира и отделяли органический слой. Водный слой экстрагировали дважды 500 мл дихлорэтана и объединенные органические слои сушили(сульфат магния) и упаривали. После экспрессхроматографии получали 15,6 г (37%) указанного в заголовке соединения в виде масла светлокоричневого цвета, которое кристаллизовалось при выстаивании при комнатной температуре. МС m/е (%) 389 (М+, 71), 358 (25), 304 (43),57 (100). г) 2,2-Диметил-N-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)пропионамид (VIII). Смесь, содержащую 3,50 г (9,0 ммолей) N(4-йод-6-морфолин-4-илпиридин-3-ил)-2,2-диметилпропионамида, 35 мл толуола, 18 мл 2 н. раствора карбоната натрия, 312 мг (0,27 ммоля) тетракис(трифенилфосфин)палладия (0) и 1,34 г(9,9 ммоля) ортотолилбороновой кислоты, выдерживали в атмосфере аргона при 80 С в течение 12 ч. После охлаждения до комнатной температуры водную фазу отделяли и промывали дважды этилацетатом. Объединенные органические слои промывали 50 мл соляного раствора,сушили (сульфат натрия) и упаривали. После очистки экспресс-хроматографией получали 3,23 г (количественный выход) указанного в заголовке соединения в виде пены белого цвета. МС m/е (%) 354 (М+Н+, 100). д) 6-Морфолин-4-ил-4-орто-толилпиридин-3-иламин (IX). Суспензию, содержащую 2,93 г (8,28 ммоля) 2,2-диметил-N-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)пропионамида в 80 мл 3 н. раствора соляной кислоты и 5 мл 1-пропанола, нагревали до 90-95 С в течение ночи. Реакционную смесь охлаждали до комнатной температуры,промывали трижды порциями по 20 мл диэтилового эфира и фильтровали через целит. Фильтрат разбавляли 20 мл воды и доводили значение рН до 7-8, добавляя 28%-ный раствор гидроксида натрия при охлаждении на льду. Продукт экстрагировали четырьмя порциями по 100 мл дихлорметана. Объединенные органические слои промывали 50 мл соляного раствора,сушили (сульфат магния) и упаривали, получая 2,31 г (количественный выход) указанного в заголовке соединения в виде пены белого цвета. МС m/е (%) 269 (М+, 100). е) Метил-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)амин (II). Раствор, содержащий 2,24 г (8,3 ммоля) 6 морфолин-4-ил-4-ортотолилпиридин-3-иламина в 17 мл триметилортоформиата и 3 капли трифторуксусной кислоты, выдерживали в течение 2 10 ч при 130 С. Реакционную смесь упаривали и сушили под вакуумом в течение 30 мин. Оставшееся масло растворяли в 5 мл тетрагидрофурана и добавляли по каплям при охлаждении на льду к 630 мл (16,6 ммоля) алюмогидрида лития в 20 мл тетрагидрофурана. Реакционную смесь перемешивали в течение 1 ч при комнатной температуре, вновь охлаждали до 0 С и подкисляли (рН 1-2), добавляя 28%-ный раствор соляной кислоты. После перемешивания в течение 5 мин добавляли 28%-ный раствор гидроксида натрия до получения значения рН 10. Раствор фильтровали через целит, упаривали и очищали экспресс-хроматографией, получая 1,56 г (66%) указанного в заголовке соединения в виде пены белого цвета. МС m/е (%) 283 (М+, 100). ж) 2-(3,5-Бистрифторметилфенил)-N-метил-N-(6-морфолин-4-ил-4-ортотолилпиридин 3-ил)изобутирамид (I). Раствор, содержащий 1,46 г (5,15 ммоля) метил-(6-морфолин-4-ил-4-ортотолилпиридин 3-ил)амина и 1,32 мл (7,73 ммоля) N-этилдиизопропиламина в 15 мл дихлорметана, охлаждали в ледяной бане и по каплям добавляли 1,8 г(5,67 ммоля) 2-(3,5-бистрифторметилфенил)-2 метилпропионилхлорида. Реакционную смесь нагревали до 35-40 С в течение 3 ч, охлаждали вновь до комнатной температуры и перемешивали с 25 мл насыщенного раствора бикарбоната натрия. Органический слой отделяли и водную фазу экстрагировали дихлорметаном. Объединенные органические слои сушили (сульфат магния) и упаривали. Остаток очищали экспресс-хроматографией, получая 2,9 г (количественный выход) указанного в заголовке соединения в виде кристаллов белого цвета. tпл 131132 С. з) Гидрохлорид 2-(3.5-бистрифторметилфенил)-N-метил-N-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамида (1:1.45). К раствору, содержащему 2,9 г (5,13 ммоля) 2-(3,5-бистрифторметилфенил)-N-метил-N(6-морфолин-4-ил-4-ортотолилпиридин-3-ил) изобутирамида в 50 мл диэтилового эфира, добавляли при охлаждении на льду 2,8 мл 3 н. раствора соляной кислоты в диэтиловом эфире. После перемешивания в течение 15 мин при 0 С суспензию упаривали досуха, повторно суспендировали в 100 мл диэтилового эфира, фильтровали и сушили под вакуумом, получая 2,82 г(89%) указанного в заголовке соединения в виде кристаллов белого цвета. МС m/е (%) 566 (М+Н+, 100), 588 (М+Na+,11). Пример А. Таблетки следующего состава приготавливают обычным методом: мг/таблетку Действующее вещество 5 Лактоза 45 Кукурузный крахмал 15 Микрокристаллическая целлюлоза Стеарат магния Масса таблетки Пример Б. Капсулы следующего состава приготавливают обычным методом: мг/капсулу Действующее вещество 10 Лактоза 155 Кукурузный крахмал 30 Тальк 5 Масса содержимого капсулы 200 Действующее вещество, лактозу и кукурузный крахмал сначала перемешивают в миксере, а затем обрабатывают в измельчающей машине. Смесь возвращают в смеситель, добавляют тальк и тщательно перемешивают. Смесью заполняют желатиновые капсулы с твердым покрытием. Пример В. Приготавливают суппозитории следующего состава: мг/суппозиторий Действующее вещество 15 Масса наполнителя суппозитория 1285 Всего 1300 Массу наполнителя суппозитория расплавляют в стеклянном или стальном резервуаре и охлаждают до 45 С. Затем к ней добавляют тонкоизмельченное действующее вещество и перемешивают до полного диспергирования. Смесью заполняют пресс-формы для суппозиториев требуемого размера, дают остыть, затем суппозитории удаляют из пресс-форм и упаковывают по отдельности в вощеную бумагу или металлическую фольгу. ФОРМУЛА ИЗОБРЕТЕНИЯ и его фармацевтически приемлемые кислотноаддитивные соли. 2. Лекарственное средство, включающее соединение по п.1 и фармацевтически приемлемые носители. 3. Лекарственное средство по п.2, предназначенное для лечения болезней, связанных с рецептором NK-1. 4. Способ получения соединения формулыI по п.1, предусматривающий взаимодействие соединения формулы и при необходимости превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль. 5. Соединение по п.1, полученное способом, охарактеризованным в п.4.
МПК / Метки
МПК: A61K 31/5377, C07D 213/75, A61P 25/18
Метки: 2-(3,5-бистрифторометилфенил)-n-метил-n-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамид
Код ссылки
<a href="https://eas.patents.su/7-4404-2-35-bistriftorometilfenil-n-metil-n-6-morfolin-4-il-4-ortotolilpiridin-3-ilizobutiramid.html" rel="bookmark" title="База патентов Евразийского Союза">2-(3,5-бистрифторометилфенил)-n-метил-n-(6-морфолин-4-ил-4-ортотолилпиридин-3-ил)изобутирамид</a>
Предыдущий патент: Производные пиразолотриазинов, фармацевтические композиции, содержащие их, способы лечения
Следующий патент: Способ ингибирования агрегации амилоидных белков и визуализации амилоидных отложений с использованием производных изоиндолина
Случайный патент: Быстрорастворимая лекарственная форма соединения, действующего на кальциевый рецептор











