13-членные азалиды и их применение в качестве антибиотических агентов
Номер патента: 9729
Опубликовано: 28.02.2008
Авторы: Зиглер Карл Бернард, Блайз Алан Элвуд, Бертинейто Питер, Мортон Барри Джеймс, Рейган Коулман Брендан, Дерлам Джон Филип, Рафка Роберт Джон
Формула / Реферат
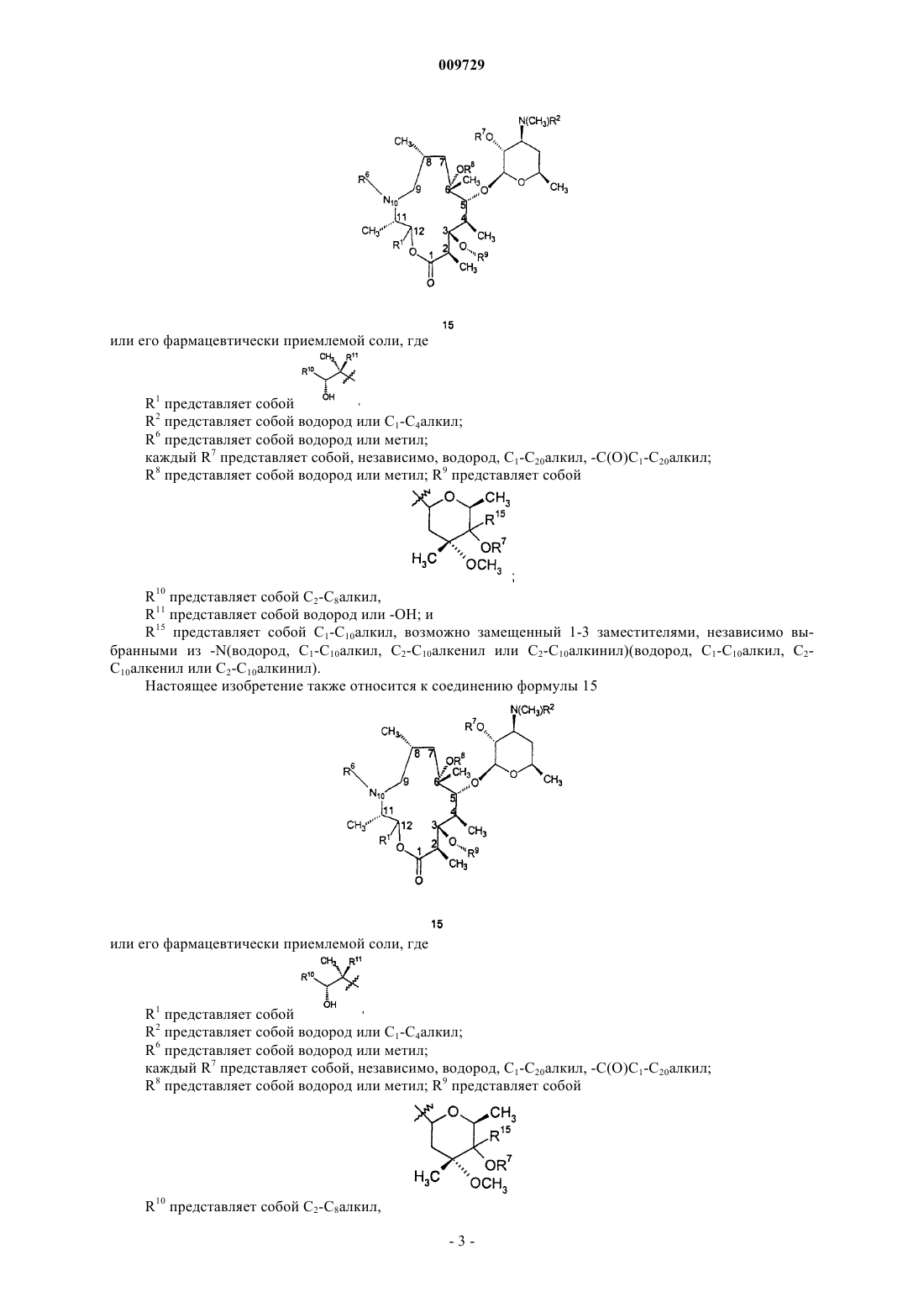
1. Соединение формулы 1
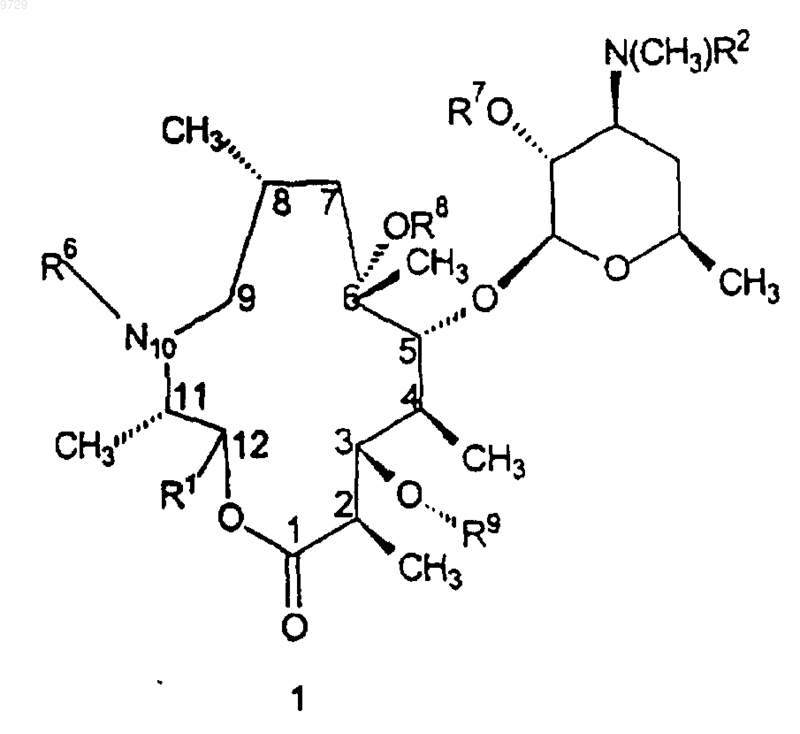
или его фармацевтически приемлемая соль,
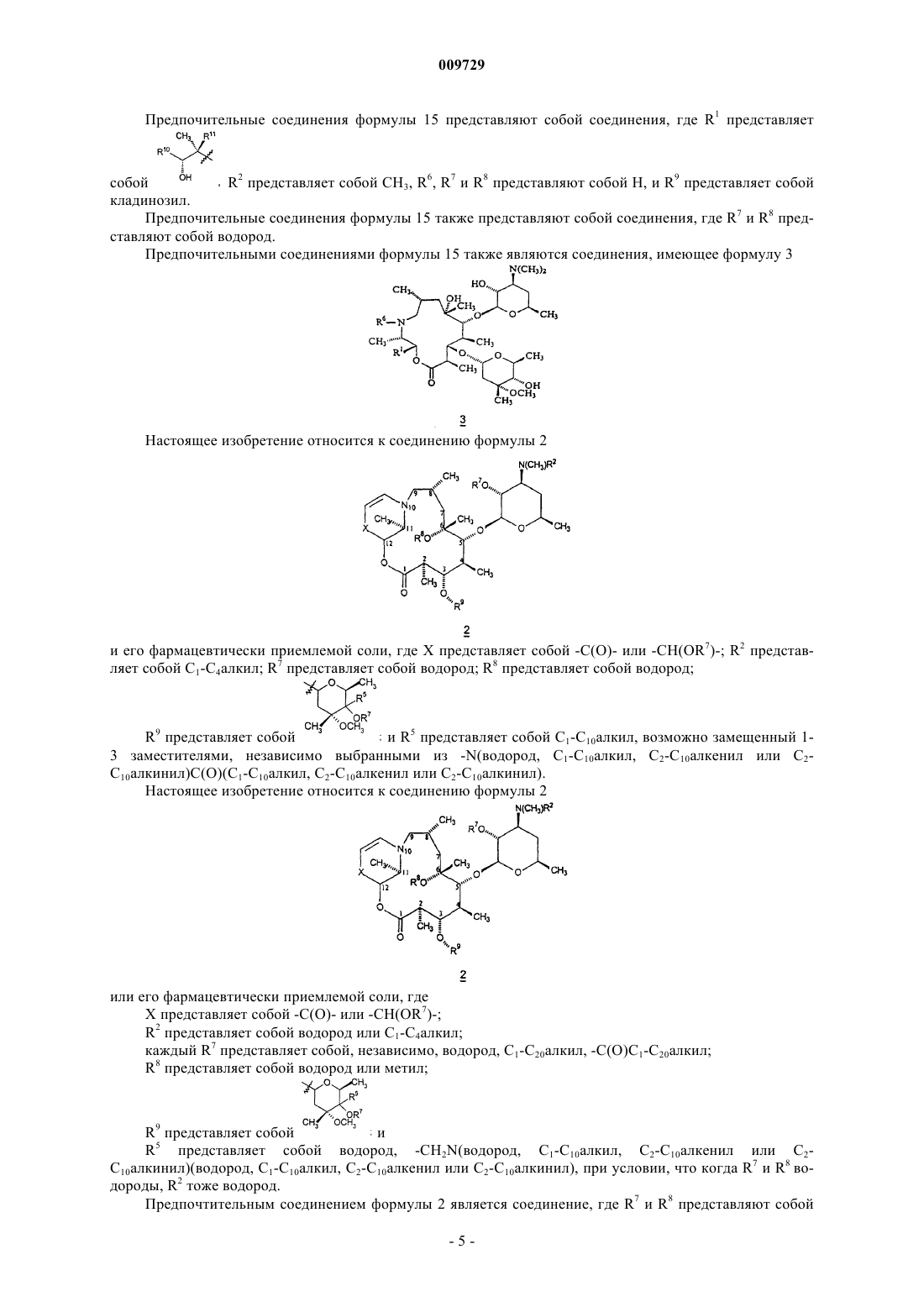
где R1 представляет собой

ацетил, 3-N,N-диметиламино-2-пропеноил,
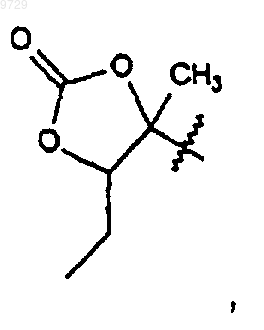
1-N-метил-5-пиразолил, 3-пиразолил, 1-метил-N-3-пиразолил, 1-N-бензил-3-пиразолил, 1-N-(3-гидроксибензил)-3-пиразолил или
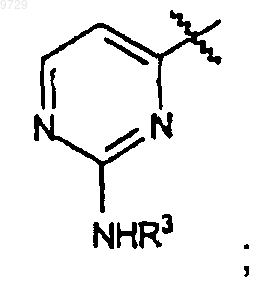
R2 представляет собой водород или С1-С4алкил;
R3 представляет собой фенил, возможно замещенный атомами галогенов,
R6 представляет собой водород или метил;
каждый R7 представляет собой, независимо, водород, С1-С20алкил, -С(O)C1-С20алкил;
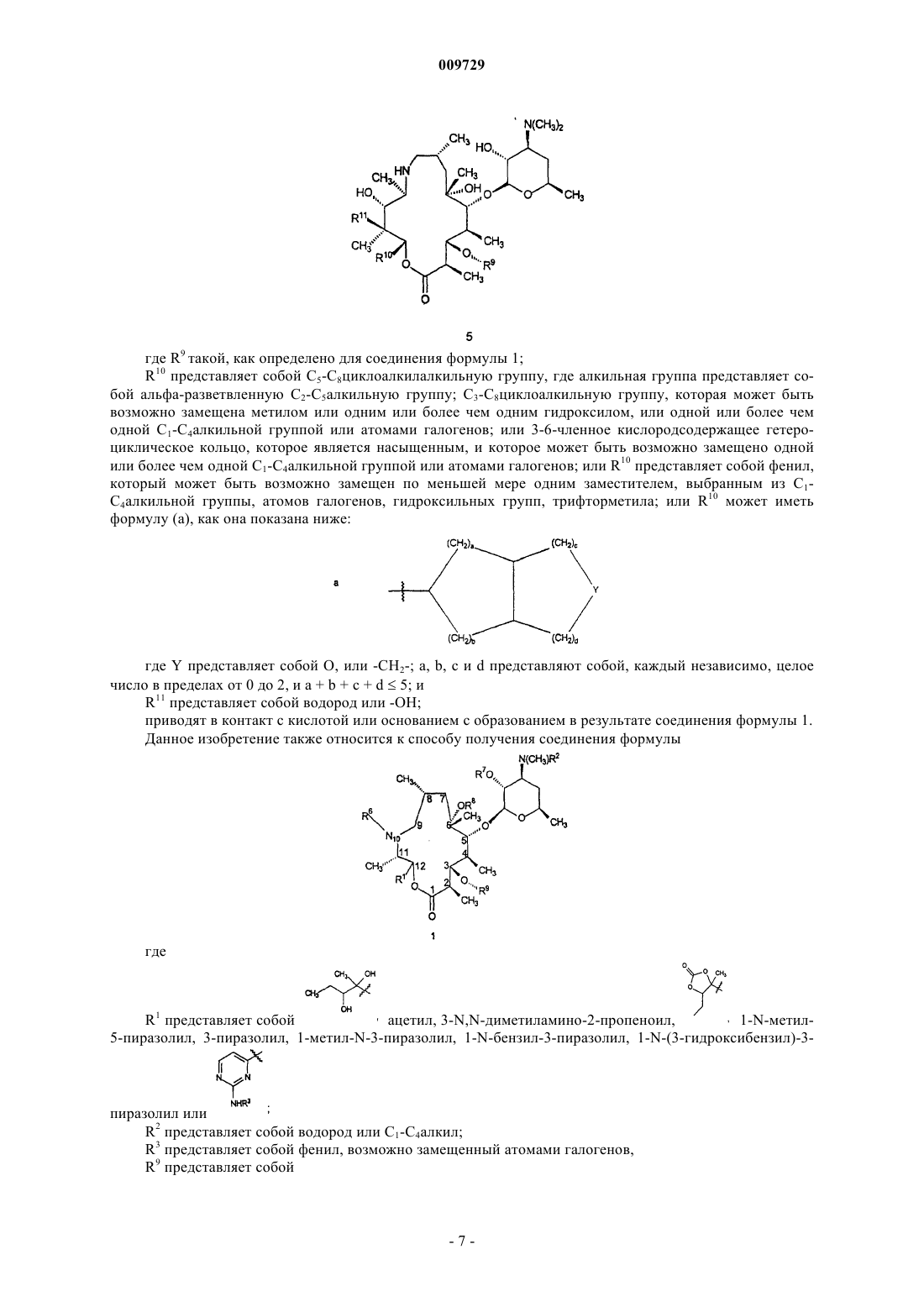
R8 представляет собой водород или метил; R9 представляет собой
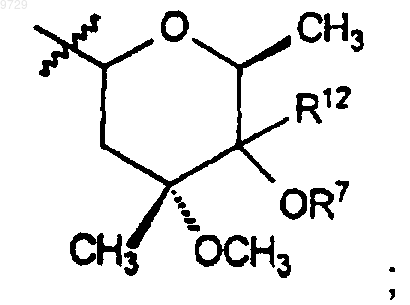
и R12 представляет собой С1-С10алкил, где алкильная группировка возможно замещена 1-3 заместителями, -N(водород, C1-С10алкил, C2-С10алкенил или С2-С10алкинил)(водород, C1-С10алкил, С2-С10алкенил или C2-С10алкинил).
2. Соединение формулы 1
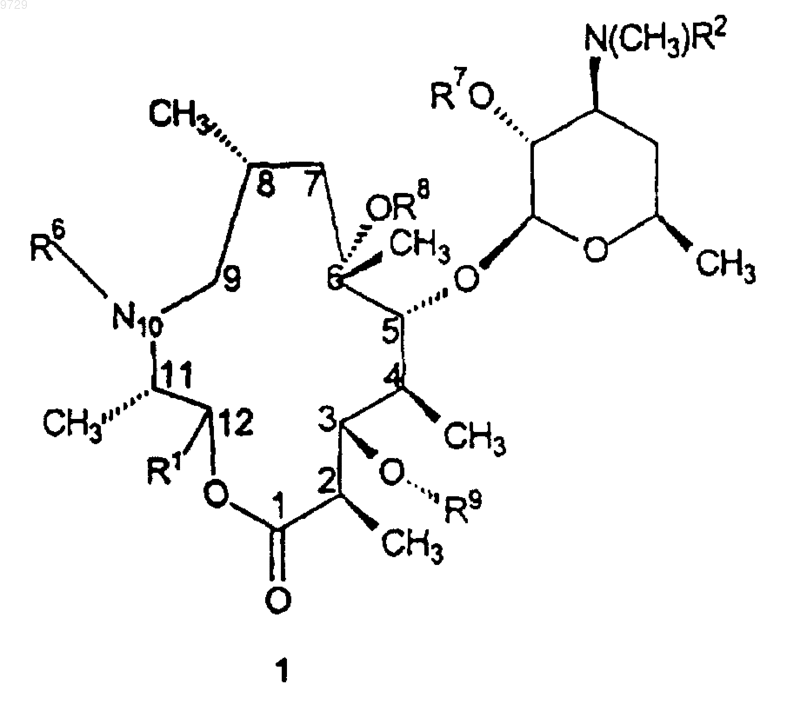
или его фармацевтически приемлемая соль,
где R1 представляет собой
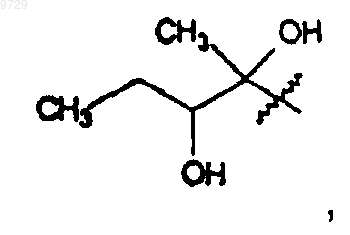
ацетил, 3-N,N-диметиламино-2-пропеноил,
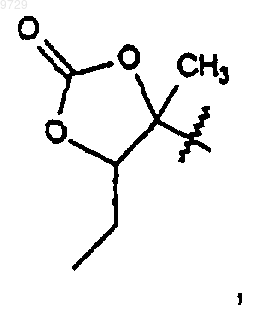
1-N-метил-5-пиразолил, 3-пиразолил, 1-метил-N-3-пиразолил, 1-N-бензил-3-пиразолил, 1-N-(3-гидроксибензил)-3-пиразолил или
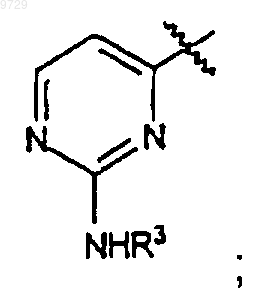
R2 представляет собой водород или С1-С4алкил;
R3 представляет собой фенил, возможно замещенный атомами галогенов,
R6 представляет собой водород или метил;
каждый R7 представляет собой, независимо, водород, C1-С20алкил;
R8 представляет собой водород или метил;
R9 представляет собой
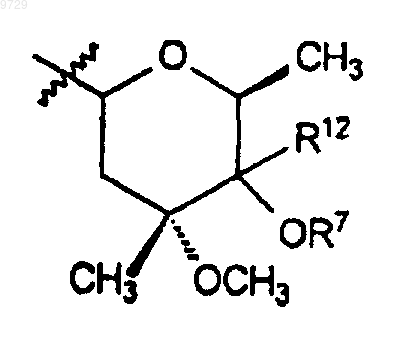
или 4"-оксокладинозил и
R12 представляет собой -CH2N(водород, С1-С10алкил, С2-С10алкенил или С2-С10алкинил)(водород, C1-С10алкил, С2-С10алкенил или С2-С10алкинил), при условии, что когда R7 и R8 водороды, R2 тоже водород.
3. Соединение по п.1 или 2, где R1 представляет собой
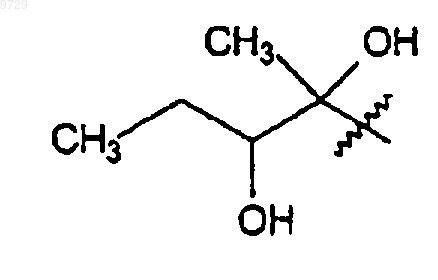 или
или 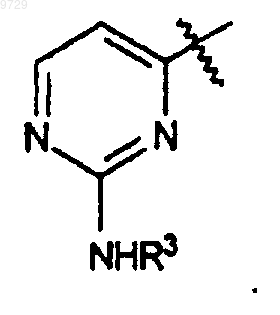
4. Соединение по любому из пп.1, 2 или 3, где R7 и R8 водород.
5. Соединение формулы 15
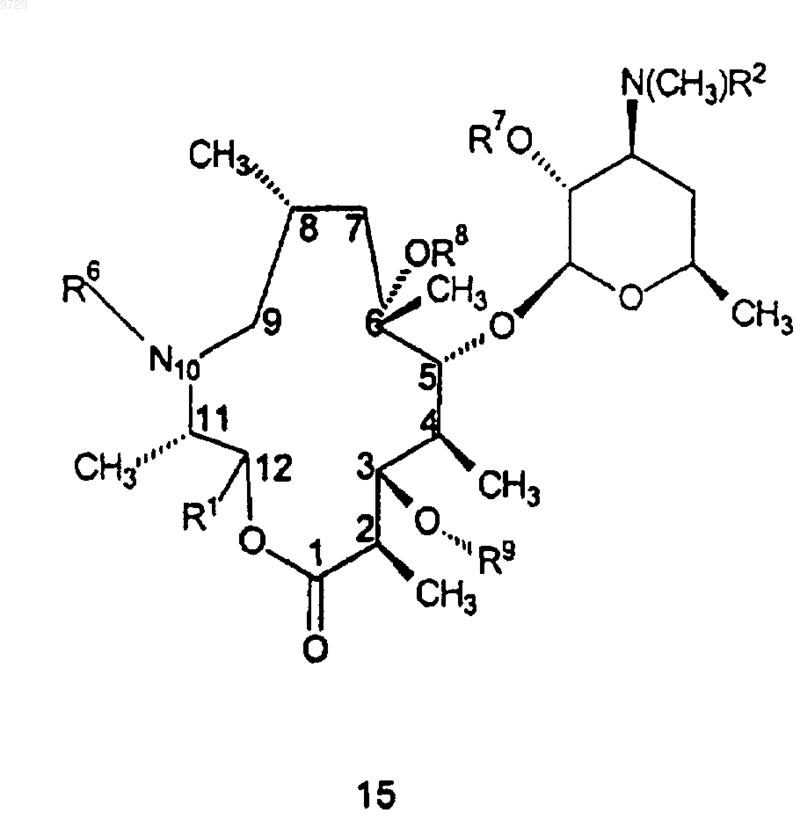
или его фармацевтически приемлемая соль,
где R1 представляет собой
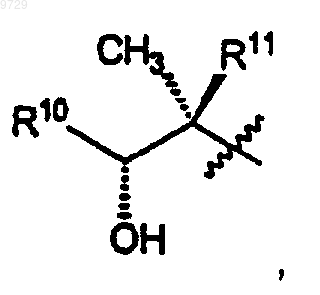
R2 представляет собой водород или С1-С4алкил;
R6 представляет собой водород или метил;
каждый R7 представляет собой, независимо, водород, C1-С20алкил, -С(O)C1-С20алкил;
R8 представляет собой водород или метил;
R9 представляет собой
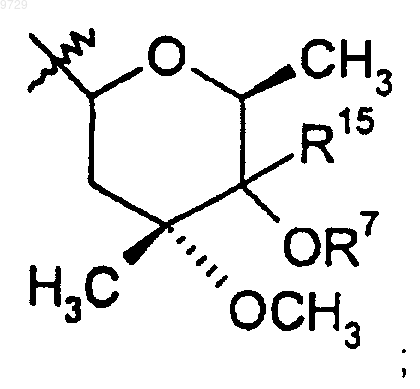
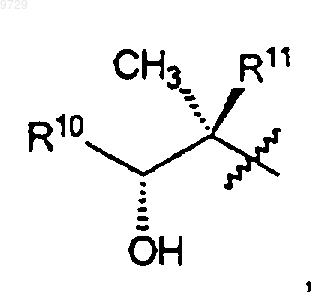
R10 представляет собой С2-С8алкил,
R11 представляет собой водород или -ОН и
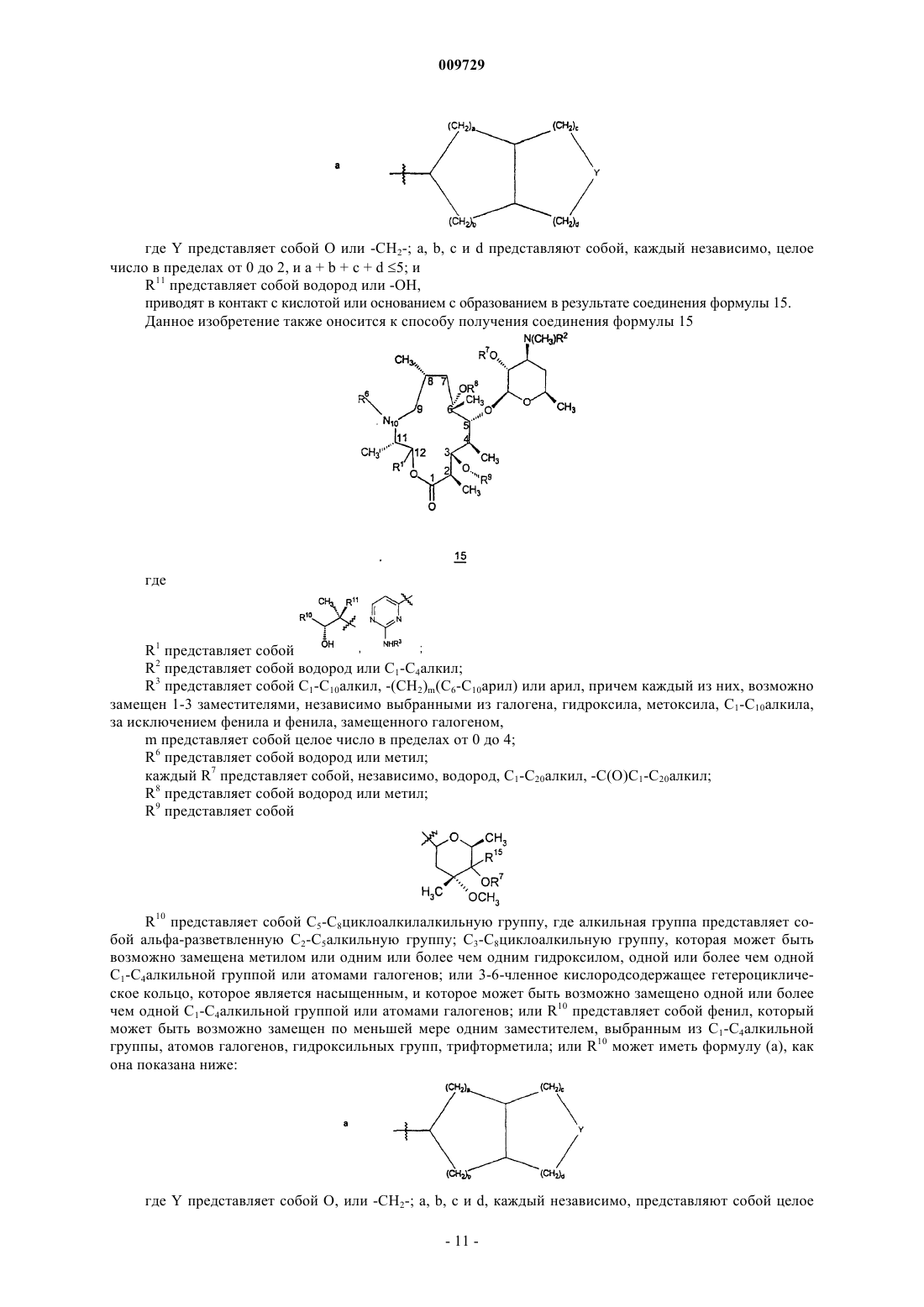
R15 представляет собой C1-С10алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, C1-С10алкил, C2-С10алкенил или С2-С10алкинил)(водород, С1-С10алкил, С2-С10алкенил или C2-С10алкинил).
6. Соединение формулы 15
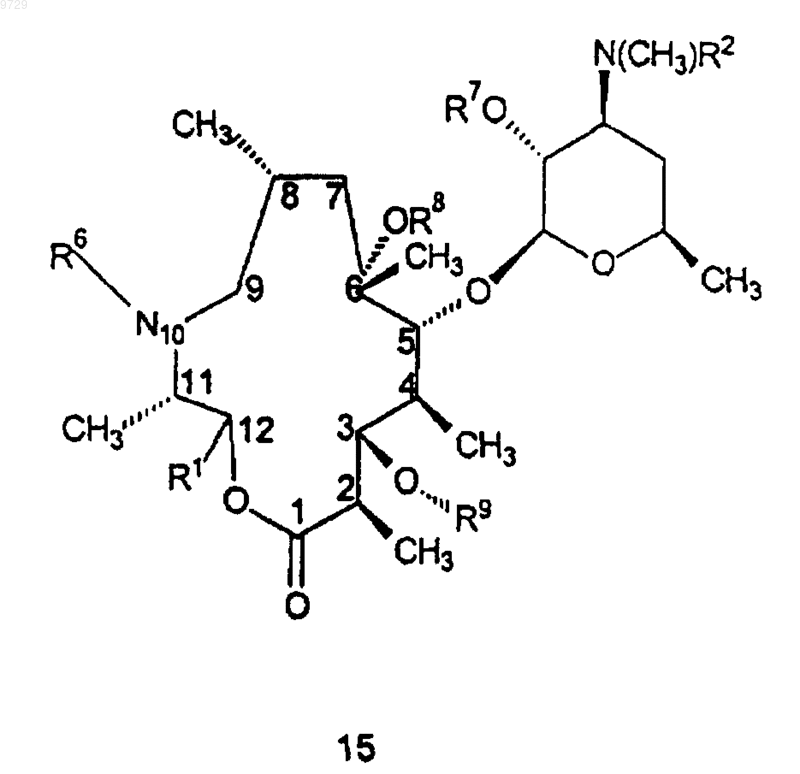
или его фармацевтически приемлемая соль,
где R1 представляет собой
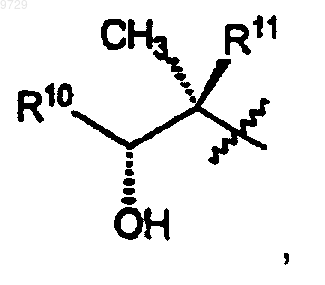
R2 представляет собой водород или С1-С4алкил;
R6 представляет собой водород или метил;
каждый R7 представляет собой, независимо, водород, C1-С20алкил, -С(O)С1-С20алкил;
R8 представляет собой водород или метил;
R9 представляет собой
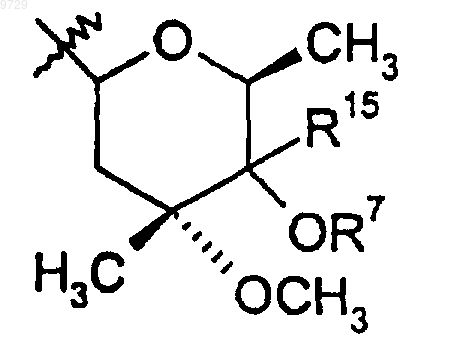
R10 представляет собой С2-С8алкил,
R11 представляет собой водород или -ОН и
R15 представляет собой H, или -CH2N(водород, C1-С10алкил, C2-С10алкенил или С2-С10алкинил) (водород, С1-С10алкил, С2-С10алкенил или С2-С10алкинил)за исключением того, что, когда R15 представляет собой H, R10 не представляет собой этил, при условии, что, когда R7 и R8 водород, R2 тоже водород.
7. Соединение формулы 15
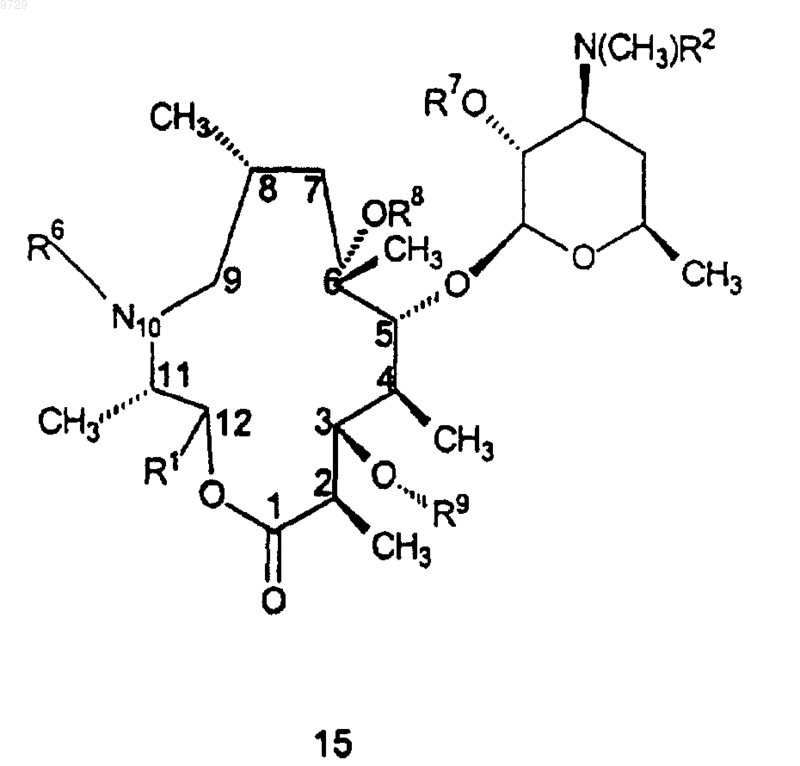
или его фармацевтически приемлемая соль,
где R1 представляет собой
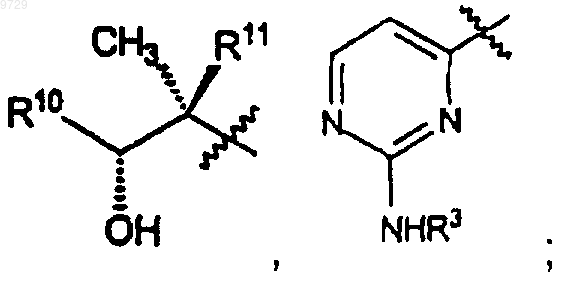
R2 представляет собой водород или С1-С4алкил;
R3 представляет собой C1-С10алкил, -(СН2)m(С6-С10арил) или арил, причем каждый из них, возможно замещен 1-3 заместителями, независимо выбранными из галогена, гидроксила, метоксила, C1-С10алкила, за исключением фенила и фенила, замещенного галогеном,
m представляет собой целое число в пределах от 0 до 4;
R6 представляет собой водород или метил;
каждый R7 представляет собой, независимо, водород, С1-С20алкил, -C(O)C1-С20алкил;
R8 представляет собой водород или метил;
R9 представляет собой
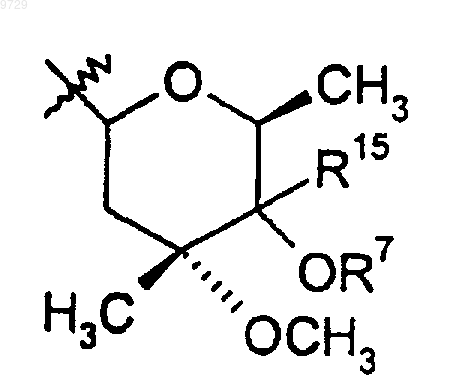
R10 представляет собой С5-С8циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С2-С5алкильную группу; С3-С8циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, одной или более чем одной С1-С4алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным и которое может быть замещено одной или более чем одной С1-С4алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть замещен по меньшей мере одним заместителем, выбранным из С1-С4алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже
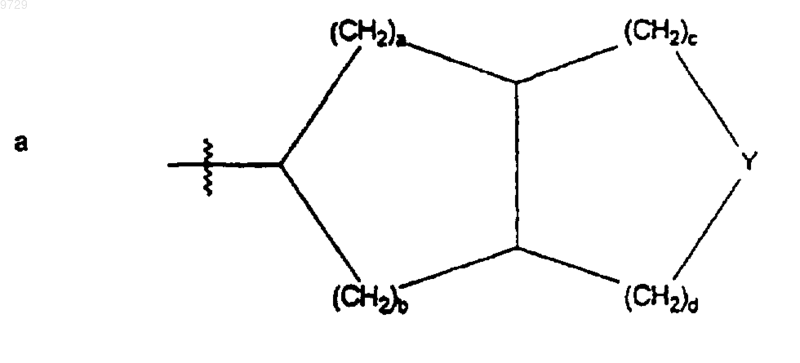
где Y представляет собой О, или -CH2-; а, b, с и d, каждый независимо, представляют собой целое число в пределах от 0 до 2, и а + b + с + d_5;
R11 представляет собой водород или -ОН и
R15 представляет собой H, С1-С10алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, С1-С10алкил, С2-С10алкенил или С2-С10алкинил)(водород, С1-С10алкил, С2-С10алкенил или С2-С10алкинил), за исключением того, что, когда R15 представляет собой H, R10 не представляет собой этил.
8. Соединение по п.7, где R1 представляет собой
R2 представляет собой CH3,
R6, R7 и R8 представляют собой H и
R9 представляет собой кладинозил.
9. Соединение по любому из пп.5-7, где R7 и R8 представляют собой водород.
10. Соединение по п.7, имеющее формулу 3
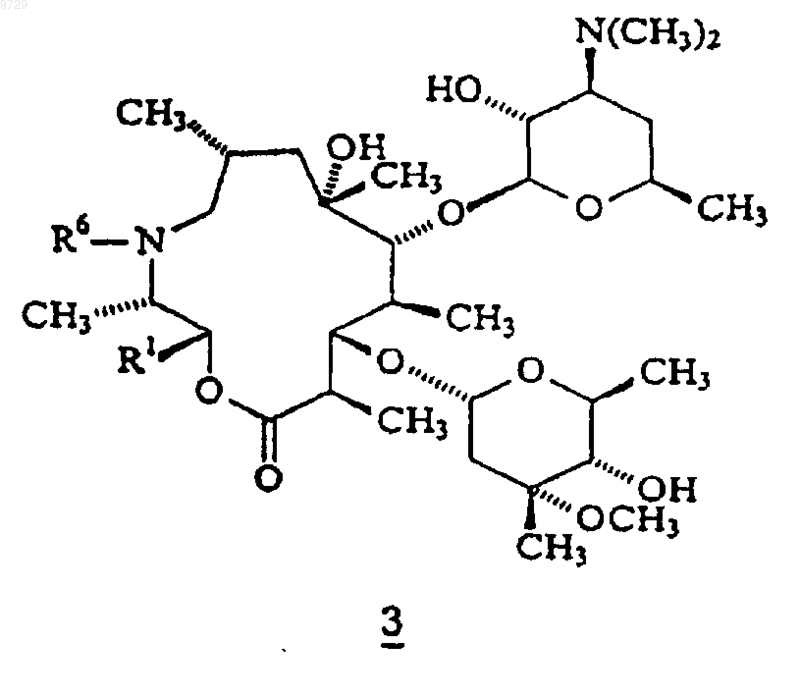
11. Соединение формулы 2

и его фармацевтически приемлемая соль,
где X представляет собой -C(O)- или -CH(OR7)-;
R2 представляет собой С1-С4алкил;
R7 представляет собой водород;
R8 представляет собой водород;
R9 представляет собой
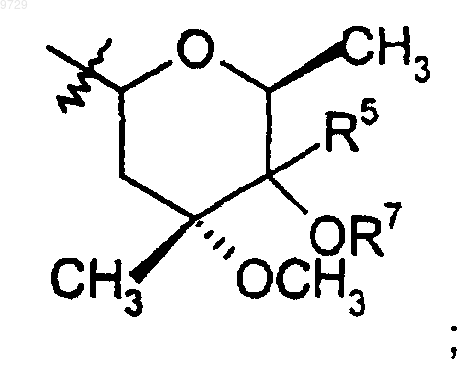
и R5 представляет собой C1-С10алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, C1-C10алкил, C2-С10алкенил или С2-С10алкинил)С(O)(С1-С10алкил, С2-С10алкенил или C2-С10алкинил).
12. Соединение формулы 2
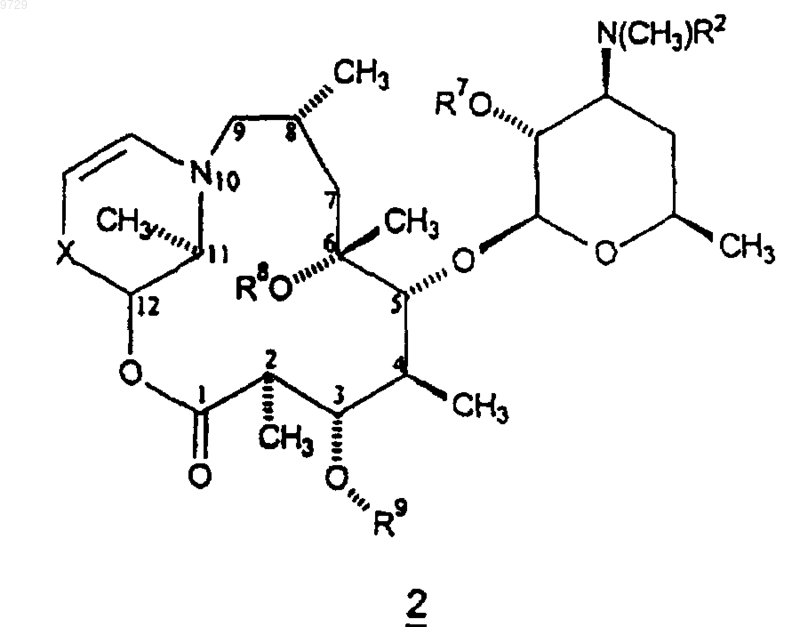
или его фармацевтически приемлемая соль,
где X представляет собой -C(O)- или -CH(OR7)-;
R2 представляет собой водород или С1-С4алкил;
каждый R7 представляет собой, независимо, водород, С1-С20алкил, -С(O)C1-С20алкил;
R8 представляет собой водород или метил;
R9 представляет собой
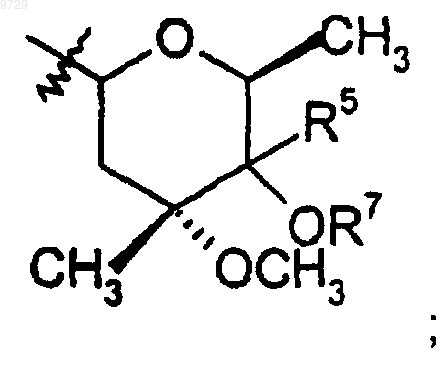
и
R5 представляет собой водород, -CH2N(водород, C1-С10алкил, С2-С10алкенил или С2-С10алкинил)(водород, C1-С10алкил, С2-С10алкенил или С2-С10алкинил), при условии, что когда R7 и R8водород, R2 тоже водород.
13. Соединение по п.12, где R7 и R8 представляют собой водород.
14. Соединение по п.12, где R9 представляет собой
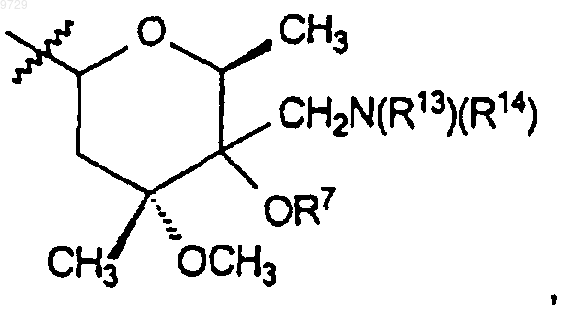
и R13 и R14 представляют собой, независимо, водород или С1-С6алкил, С2-С6алкенил или С2-С6алкинил.
15. Соединение по п.12, выбранное из группы, состоящей из соединения, где X представляет собой -C(O)-, и соединения, где X представляет собой -CH(OH)-.
16. Фармацевтическая композиция, полезная для лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, содержащая терапевтически эффективное количество соединения по пп.1-10 и фармацевтически приемлемый носитель.
17. Способ лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, при котором указанным млекопитающему, рыбе или птице вводят терапевтически эффективное количество соединения по пп.1-10.
18. Фармацевтическая композиция, полезная для лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, содержащая терапевтически эффективное количество соединения по пп.1-7 и фармацевтически приемлемый носитель.
19. Способ лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, при котором указанным млекопитающему, рыбе или птице вводят терапевтически эффективное количество соединения по пп.1, 2, 5, 6 или 7.
20. Способ получения соединения формулы
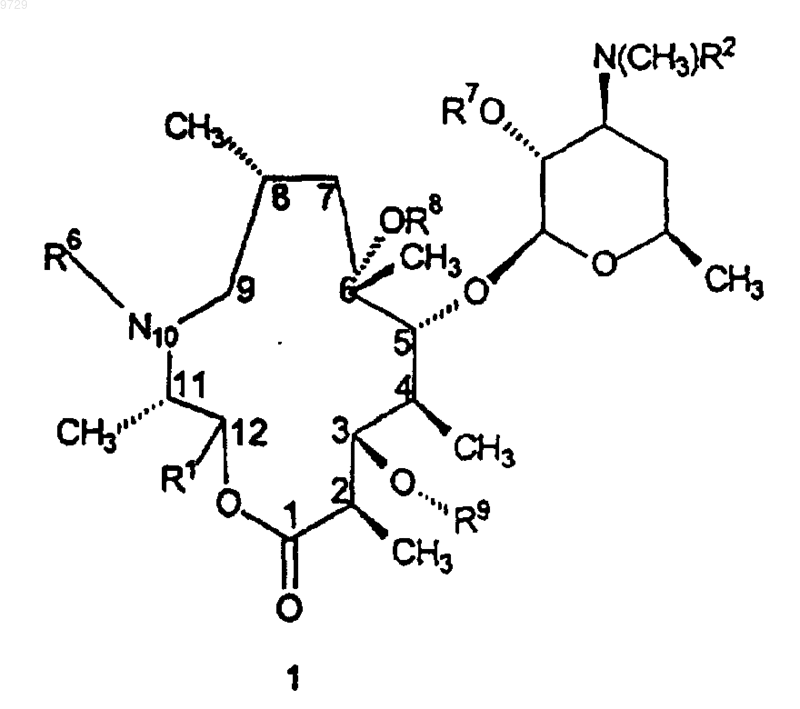
как определено в п.1,
где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,
R6, R7 и R8 представляют собой водород;
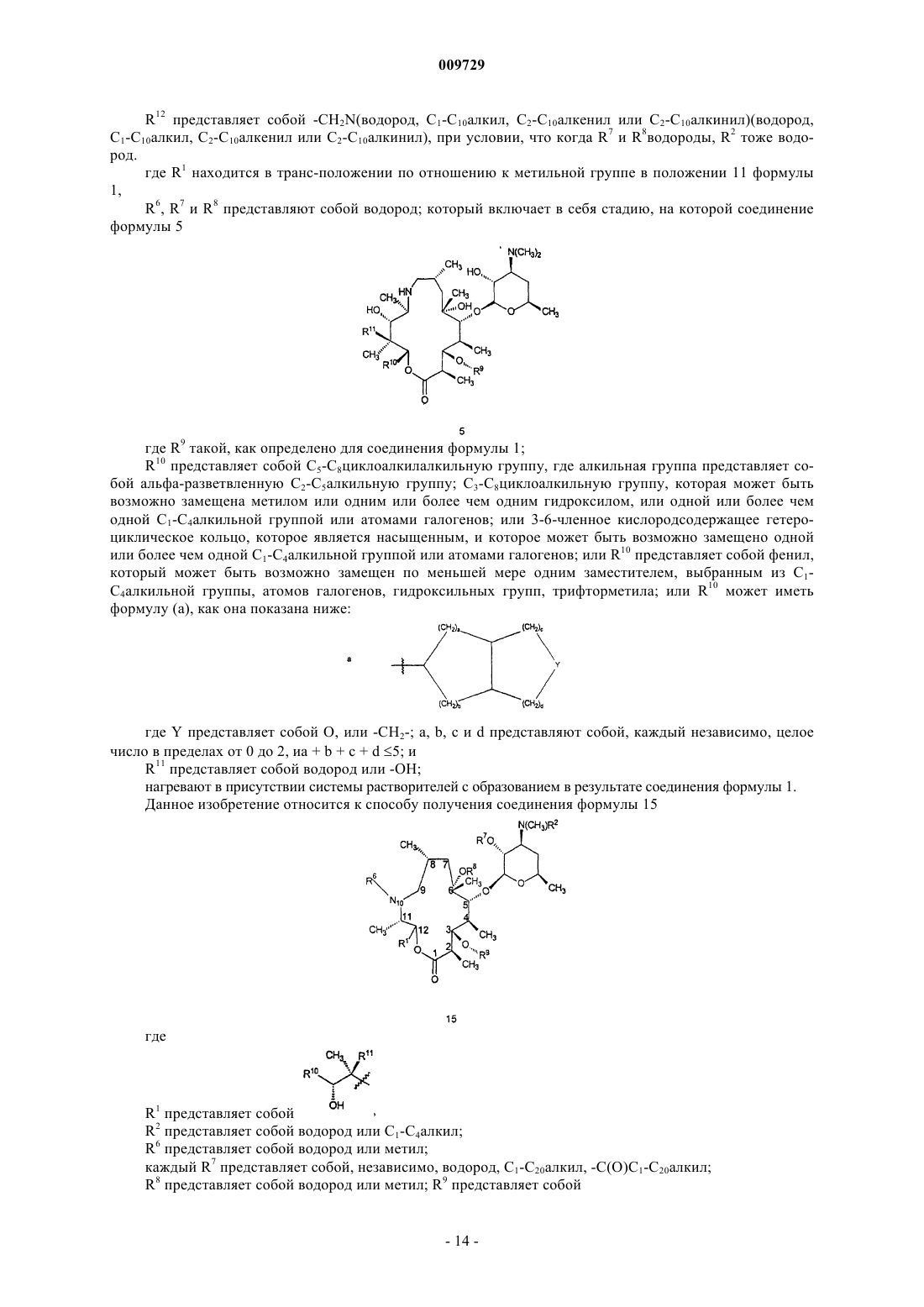
который включает в себя стадию, на которой соединение формулы 5
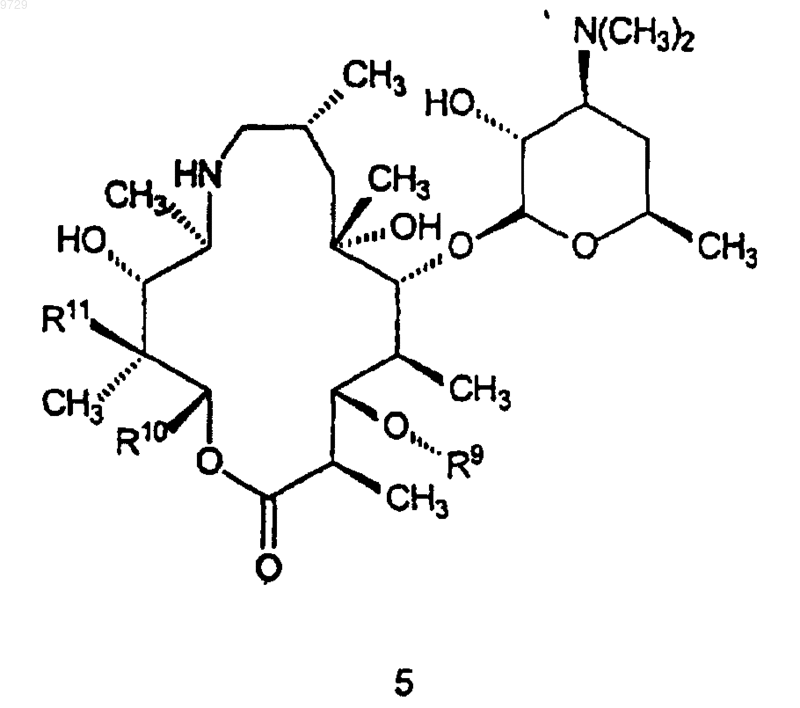
где R9 такой, как определено для соединения формулы 1;
R10 представляет собой С5-С8циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С2-С5алкильную группу; С3-С8циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, или одной или более чем одной С1-С4алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С1-С4алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С1-С4алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже
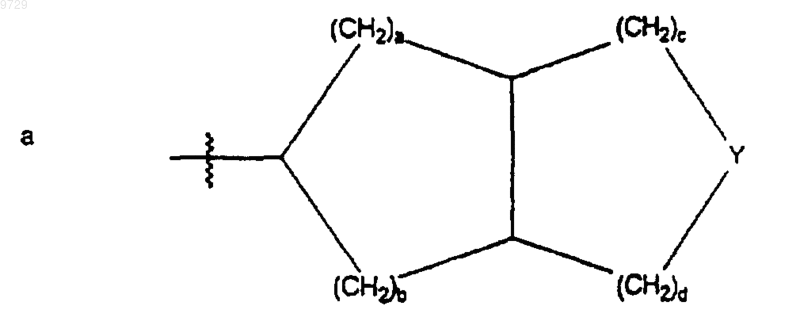
где Y представляет собой О, или -CH2-;
а, b, с и d представляют собой, каждый независимо, целое число в пределах от 0 до 2 и а + b + с + d_ 5; и
R11 представляет собой водород или -ОН;
приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 1.
21. Способ получения соединения формулы

как определено в п.2,
где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,
R6, R7 и R8 представляют собой водород;
который включает в себя стадию, на которой соединение формулы 5
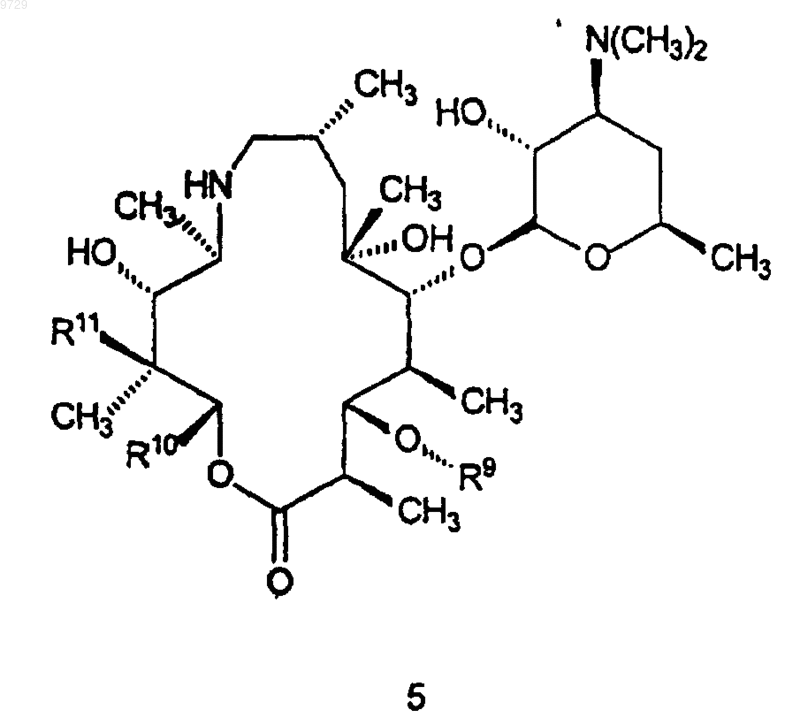
где R9 такой, как определено для соединения формулы 1,
R10 и R11 являются такими, как определено выше в п.20,
приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 1.
22. Способ получения соединения формулы 15
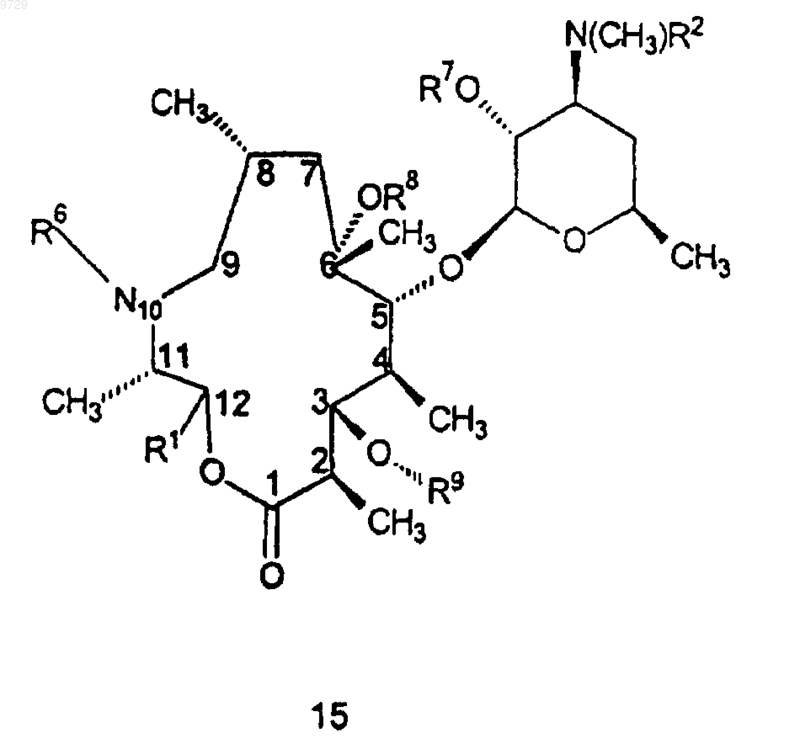
как определено в п.5, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5

где R9 такой, как определено для соединения формулы 15;
R10 представляет собой С5-С8циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С2-С5алкильную групяу; С3-С8циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С1-С4алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным и которое может быть возможно замещено одной или более чем одной С1-С4алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С1-С4алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже
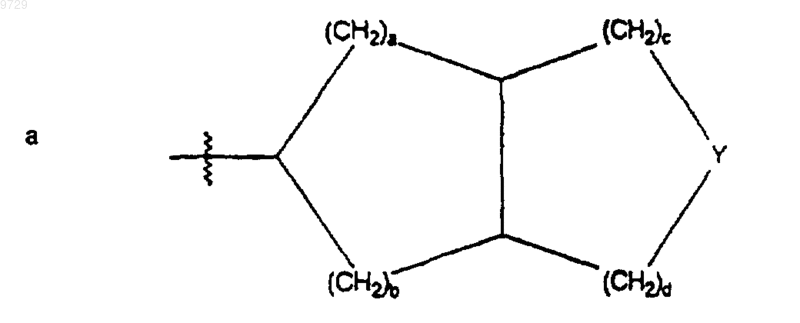
где Y представляет собой О или -CH2-;
а, b, с и d представляют собой, каждый независимо, целое число в пределах от 0 до 2, и а + b + с + d_ 5; и
R11 представляет собой водород или -ОН,
приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 15.
23. Способ получения соединения формулы 15
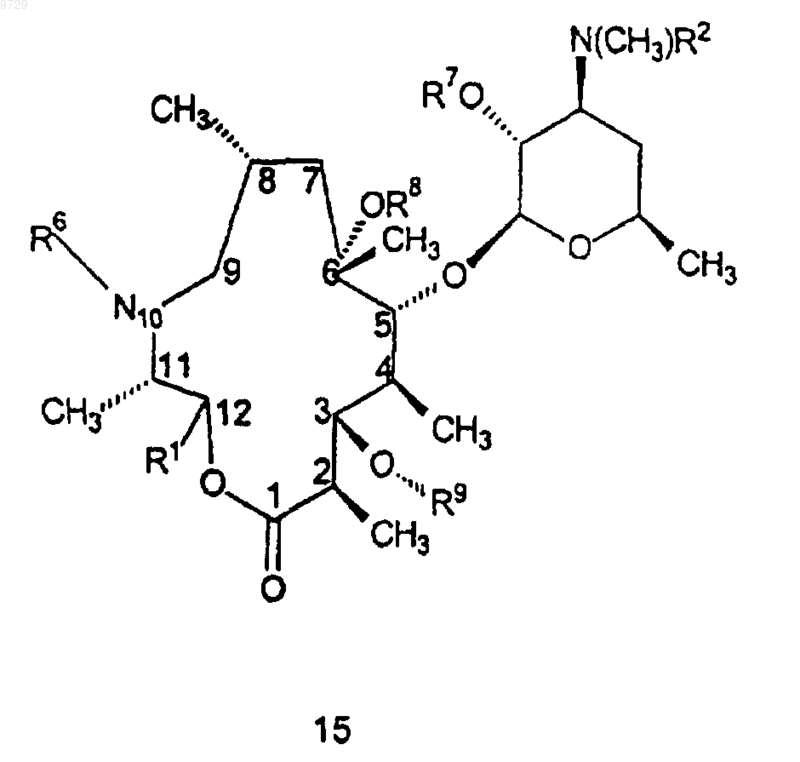
как определено в п.6, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5
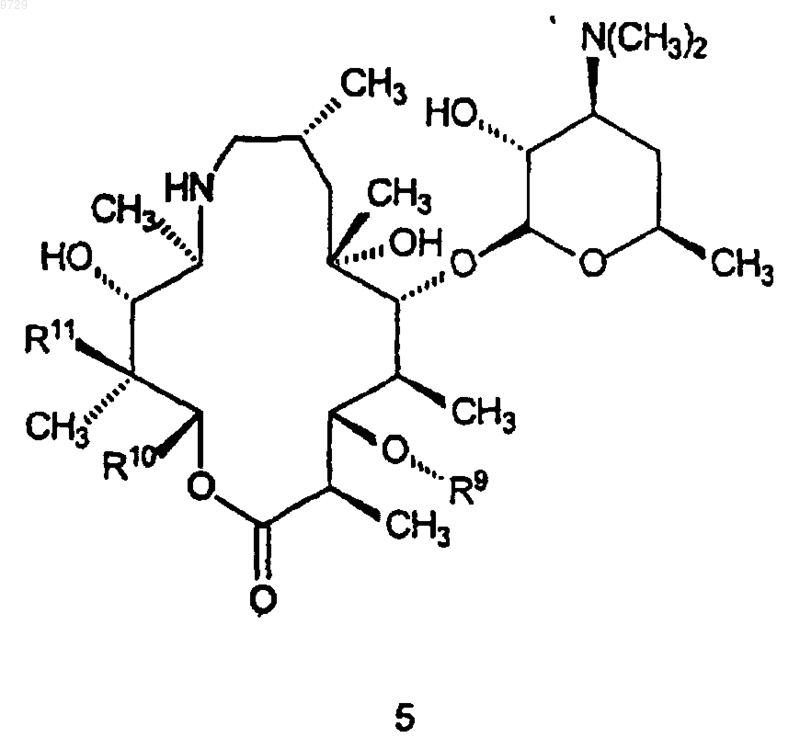
где R9 такой, как определено для соединения формулы 15,
R10 и R11 являются такими, как определено выше в п.22;
приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 15.
24. Способ получения соединения формулы 15
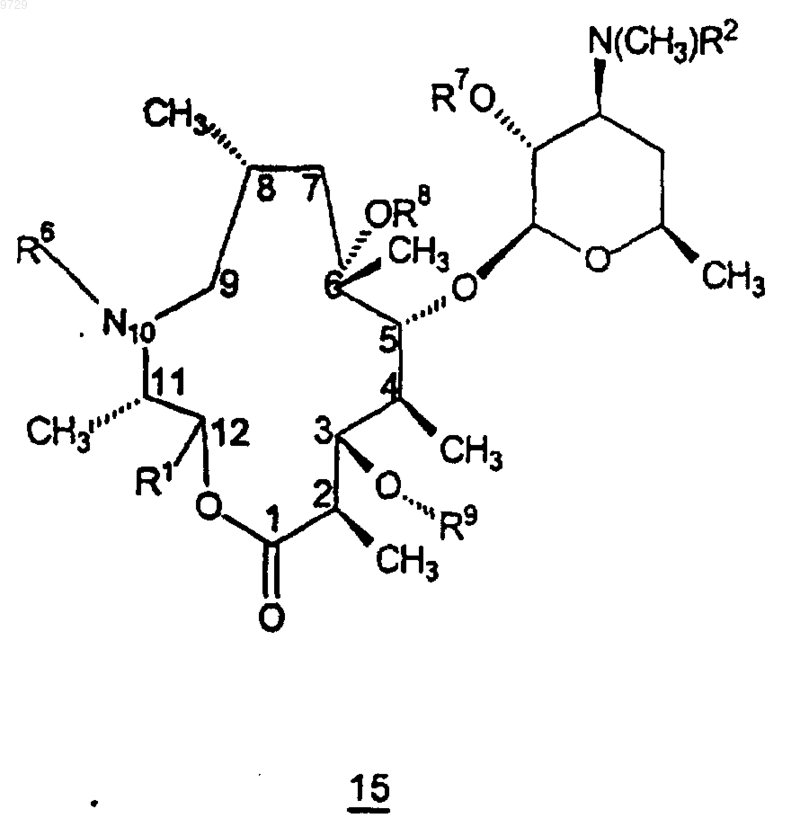
как определено в п.7, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5
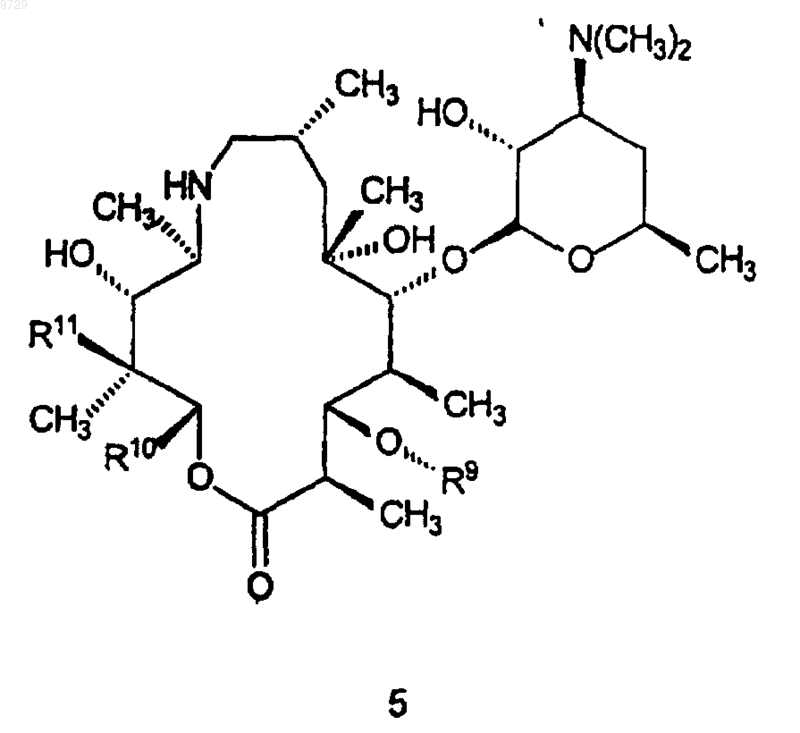
где R9 такой, как определено для соединения формулы 15,
R10 и R11 являются такими, как определено выше в п.22,
приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 15.
25. Способ получения соединения формулы 1

как определено в п.1,
где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,
R6, R7 и R8 представляют собой водород; который включает в себя стадию, на которой соединение формулы 5
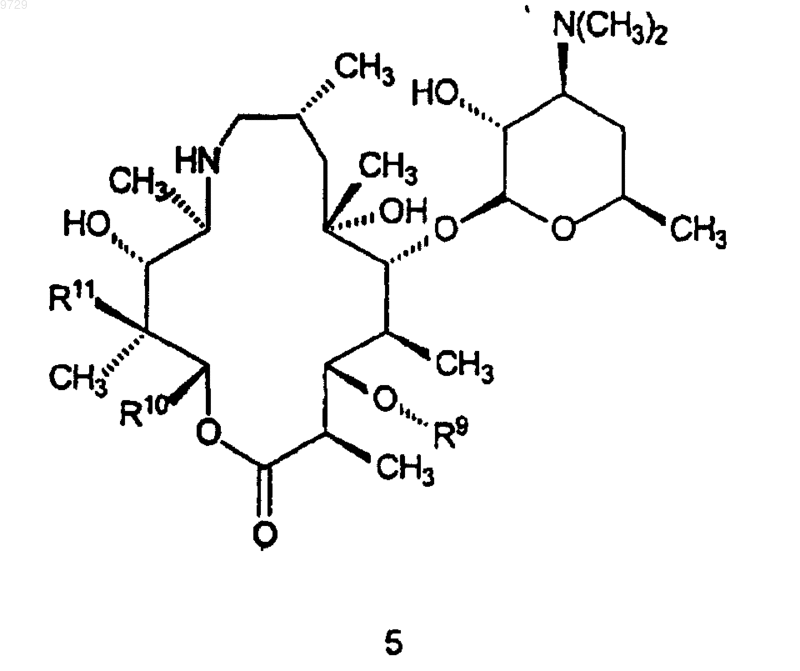
где R9 такой, как определено для соединения формулы 1,
R10 и R11 являются такими, как определено выше в п.20, нагревают в присутствии системы растворителей с образованием в результате соединения формулы 1.
26. Способ получения соединения формулы 1
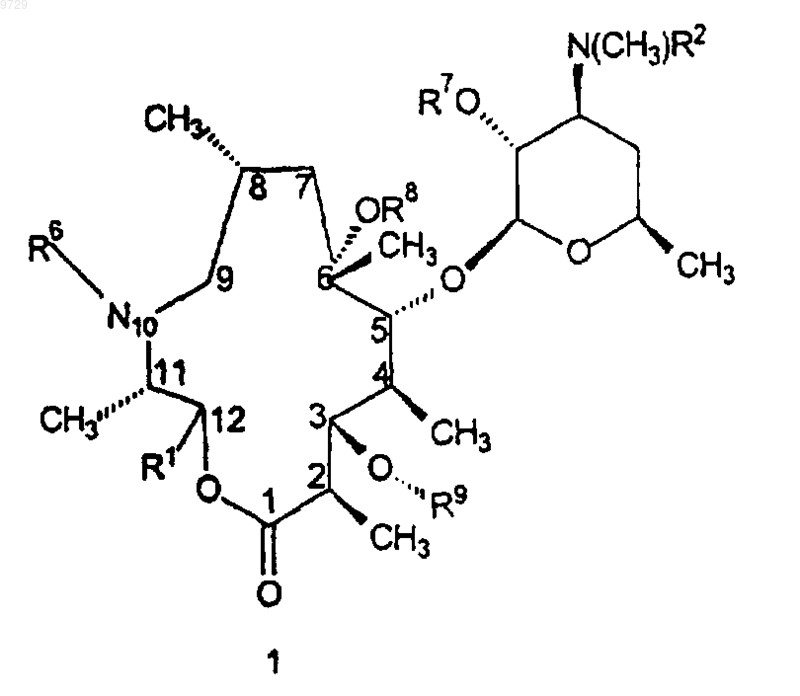
как определено в п.2,
где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,
R6, R7 и R8 представляют собой водород; который включает в себя стадию, на которой соединение формулы 5
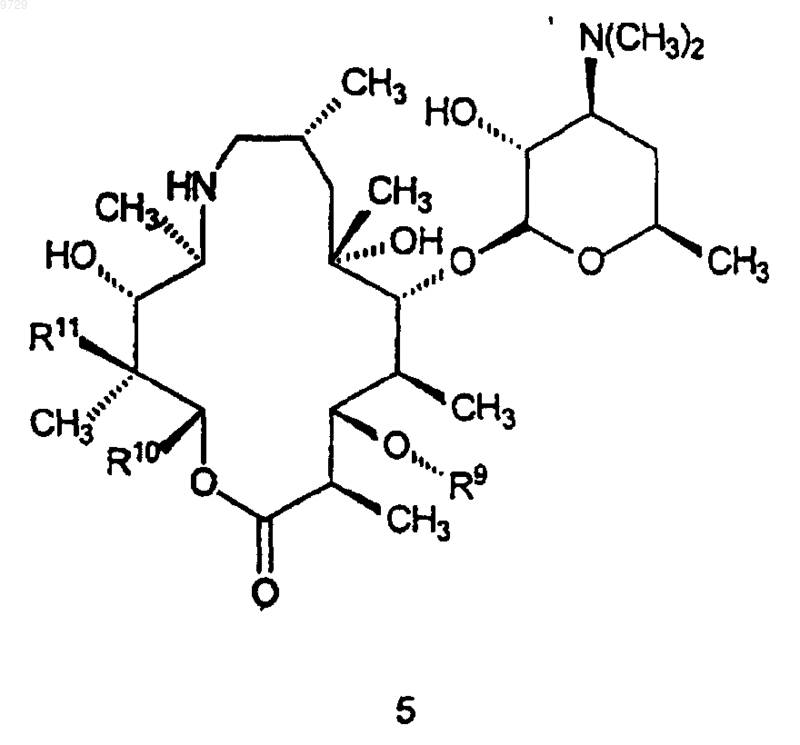
где R9 такой, как определено для соединения формулы 1,
R10 и R11 являются такими, как определено выше в п.20,
нагревают в присутствии системы растворителей с образованием в результате соединения формулы 1.
27. Способ получения соединения формулы 15
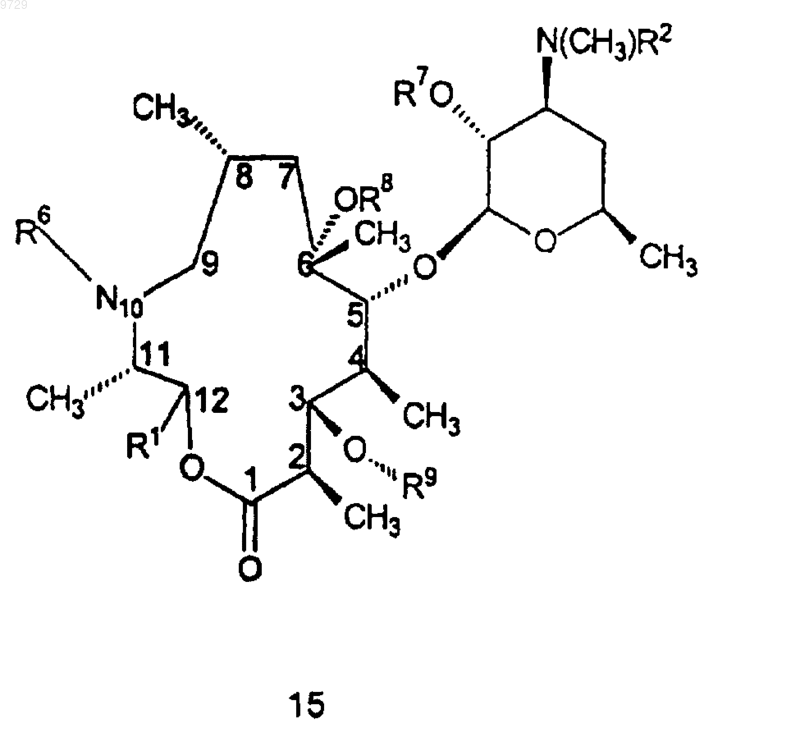
как определено в п.5, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5
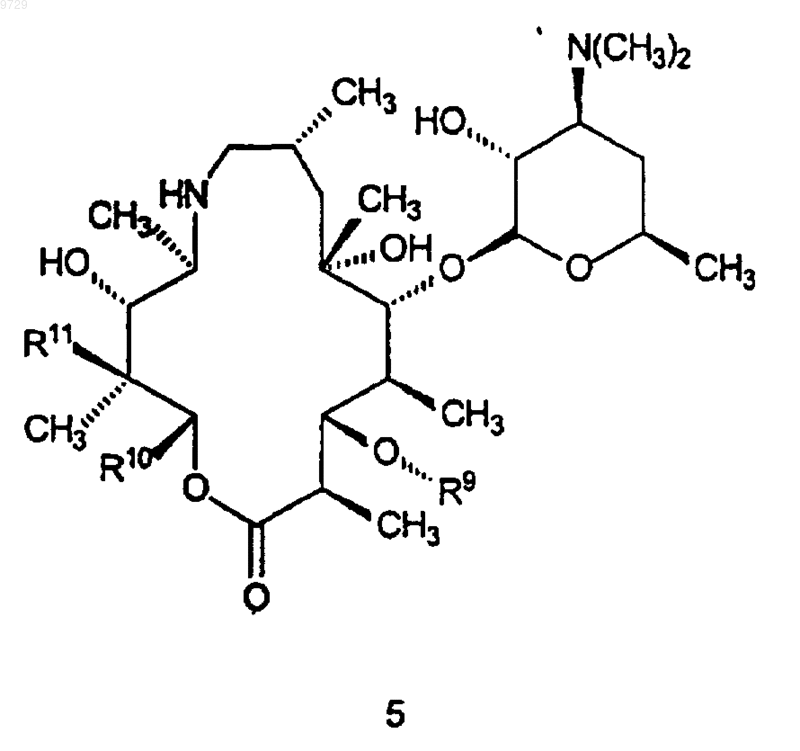
где R9 такой, как определено для соединения формулы 15,
R10 и R11 являются такими, как определено выше в п.22;
нагревают в присутствии системы растворителей с образованием в результате соединения формулы 15.
28. Способ получения соединения формулы 15
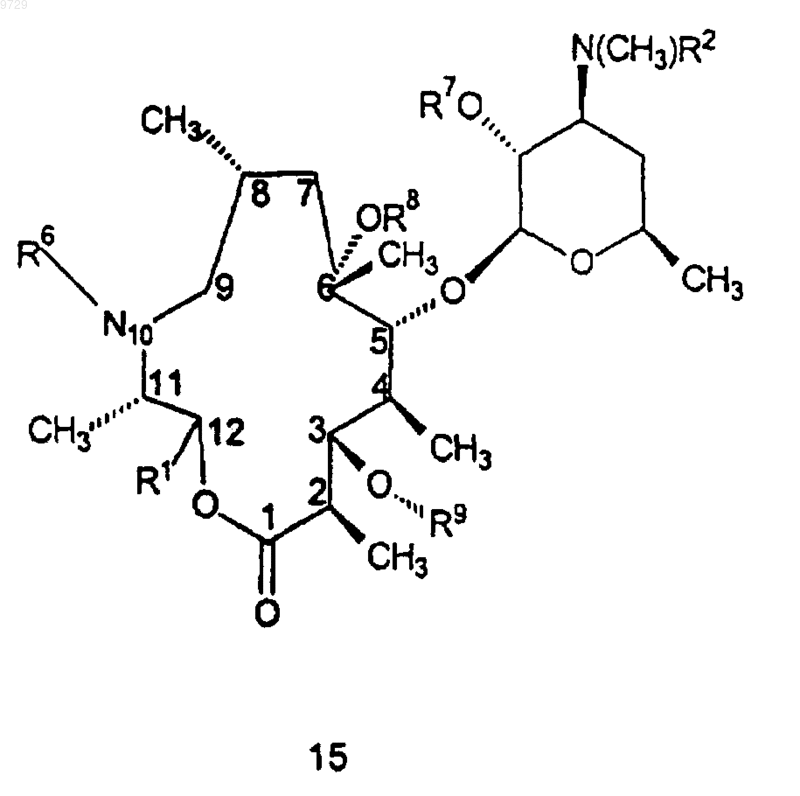
как определено в п.6, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5
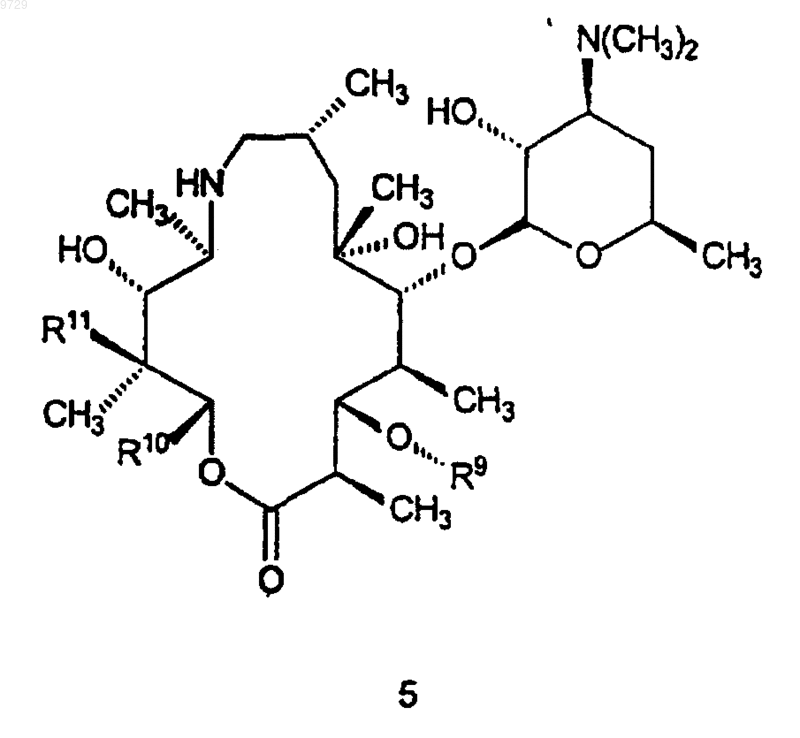
где R9 такой, как определено для соединения формулы 15,
R10 и R11 являются такими, как определено выше в п.22;
нагревают в присутствии системы растворителей с образованием в результате соединения формулы 15.
29. Способ получения соединения формулы 15
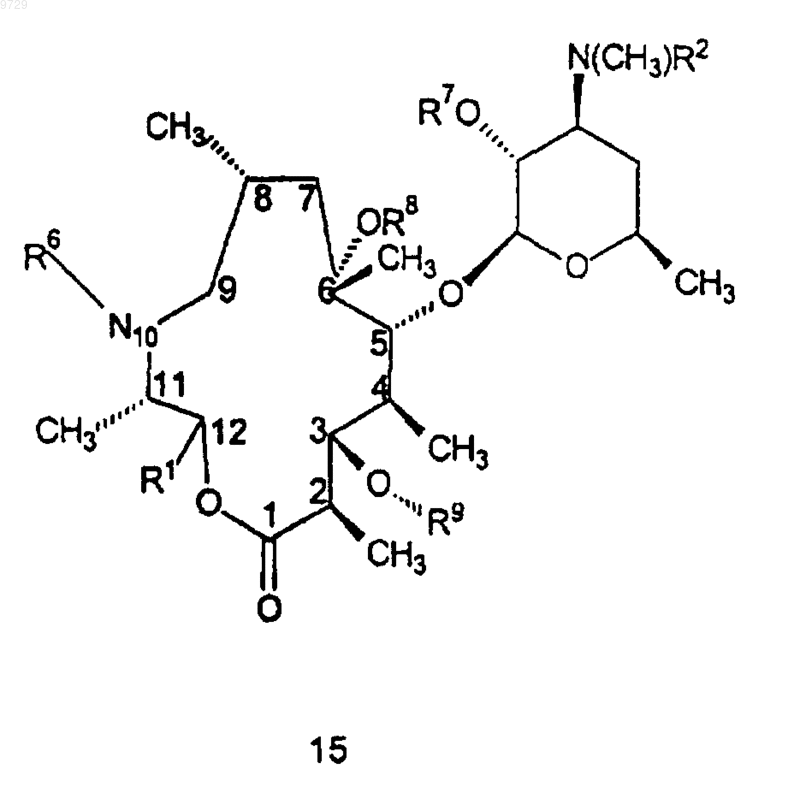
как определено в п.7, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5
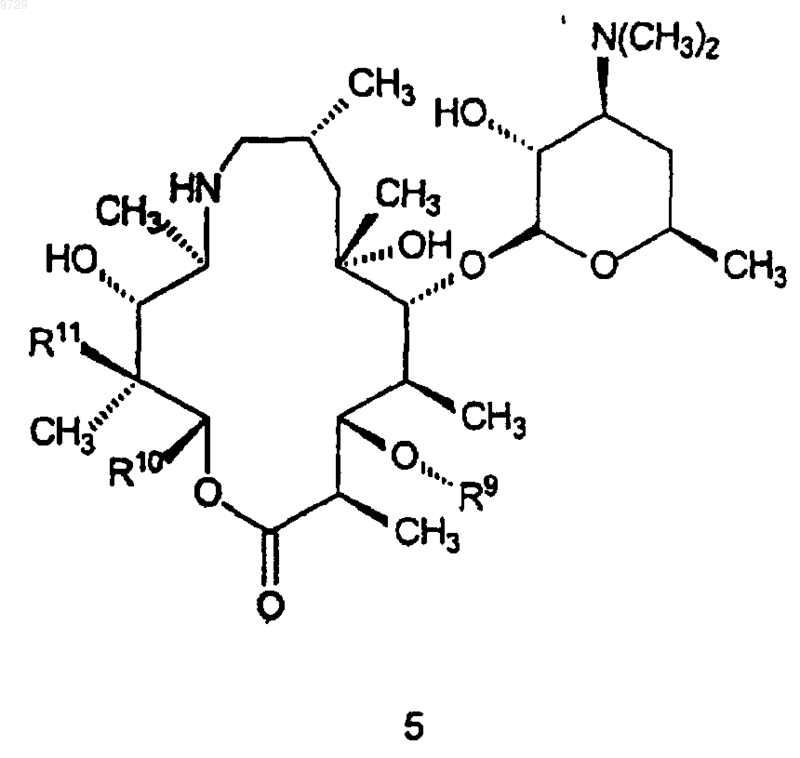
где R9 такой, как определено для соединения формулы 15,
R10 и R11 такие, как определено выше в п.22,
нагревают в присутствии системы растворителей с образованием в результате соединений формулы 15.
30. Способ по любому из пп.25-29, где система растворителей содержит растворители, выбранные из группы, состоящей из низших спиртов, диэтилового эфира, ацетона, ацетонитрила, тетрагидрофурана, этилацетата, бензола, толуола, хлороформа, метиленхлорида, диметилформамида, диметилсульфоксида, N-метилпирролидинона и их смесей.
31. Способ по любому из пп.25-29, где система растворителей дополнительно содержит протонный растворитель.
32. Способ по п.31, где протонный растворитель выбран из группы, состоящей из метанола, этанола, н-пропанола, изопропанола, н-бутанола, изобутанола, втор-бутанола, фенола, галогенофенолов, нафтолов, воды и их смесей.
Текст
009729 Предпосылки изобретения Данное изобретение относится к новым 13-членным азалидам, которые полезны в качестве антибактериальных и антипротозойных агентов для млекопитающих, включая человека, а также для рыбы и птиц. Данное изобретение также относится к фармацевтическим композициям, содержащим эти новые соединения, и к способам лечения бактериальных инфекций и протозойных инфекций у млекопитающих,рыбы и птиц, при которых новые соединения вводят млекопитающим, рыбе и птицам, которым требуется такое лечение. Известно, что макролидные антибиотики полезны при лечении широкого спектра бактериальных инфекций и протозойных инфекций у млекопитающих, рыбы и птиц. Такие антибиотики включают различные производные эритромицина А, такие как азитромицин. Азитромицин имеется в продаже и на него ссылаются в патентах США 4474768 и 4517359, которые полностью включены в данное описание изобретения посредством ссылки. Дополнительные макролиды упоминаются в заявке на патент США с серийным номером 60/063676,поданной 29 октября 1997 (Yong-Jin Wu), в заявке США с порядковым номером 60/063161, поданной 29 октября 1997 г. (Yong-Jin Wu), в заявке США с порядковым номером 60/054866, поданной 6 августа 1997 г. (Hiroko Masamune, Yong-Jin Wu, Takushi Kaneko and Paul R. McGuirk), в заявке США с порядковым номером 60/049980, поданной 11 июня 1997 г. (Brian S. Bronk, Michael A. Letavic, Takushi Kaneko andWu), заявке США с порядковым номером 60/070343, поданной 2 января 1998 г. (Dirlam) и заявке США с порядковым номером 60/097075, поданной 19 августа 1998 г. (Hengmiao Cheng, Michael A. Letavic, Carl В. Ziegler, Jason K. Dutra, Brian S. Bronk), все из которых полность включены в данное описание изобретения посредством ссылки. Поскольку вышеуказанные патенты и заявки на патенты не признаются уровнем техники в отношении настоящей заявки, остается необходимость в уровне техники в отношении легкодоступных, 13 членных азалидных антибиотических соединениях, которые обладают сильной активностью против широкого спектра бактерий и простейших. Подобно азитромицину и другим макролидным антибиотикам, новые макролидные соединения по настоящему изобретению обладают сильной активностью против различных бактериальных и протозойных инфекций, таких как описанные ниже. Краткое изложение сущности изобретения Настоящее изобретение относится к соединению формулы 1 или его фармацевтически приемлемой соли, гдеR2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой фенил, возможно замещенный атомами галогенов,R6 представляет собой водород или метил;R8 представляет собой водород или метил;R12 представляет собой C1-С 10 алкил, где алкильная группировка возможно замещена 1-3 заместителями, -N(водород, C1-С 10 алкил, C2-С 10 алкенил или С 2-С 10 алкинил)(водород, C1-С 10 алкил, С 2-С 10 алкенил или C2-С 10 алкинил). Настоящее соединение относится также к соединению формулы 1 или его фармацевтически приемлемой соли, гдеR2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой фенил, возможно замещенный атомами галогенов,R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил;R8 представляет собой водород или метил;R12 представляет собой -CH2N(водород, C1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил)(водород,С 1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил), при условии, что когда R7 и R8 водороды, R2 тоже водород. Предпочтительные соединения формулы 1 включают в себя соединения, или где R1 представляет собой Предпочтительные соединения формулы 1 также включают в себя соединения, где R7 и R8 представляют собой водород. Настоящее изобретение относится к соединению формулы 15 или его фармацевтически приемлемой соли, гдеR2 представляет собой водород или С 1-С 4 алкил;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(О)С 1-С 20 алкил;R8 представляет собой водород или метил; R9 представляет собойR10 представляет собой С 2-С 8 алкил,R11 представляет собой водород или -ОН; иR15 представляет собой C1-С 10 алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, С 1-С 10 алкил, C2-С 10 алкенил или С 2-С 10 алкинил)(водород, C1-C10 алкил, С 2 С 10 алкенил или C2-С 10 алкинил). Настоящее изобретение также относится к соединению формулы 15 или его фармацевтически приемлемой соли, гдеR2 представляет собой водород или С 1-С 4 алкил;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(O)C1-С 20 алкил;R8 представляет собой водород или метил; R9 представляет собойR11 представляет собой водород или -ОН; иR15 представляет собой H, R10 не представляет собой этил, при условии, что когда R7 и R8 водороды, R2 тоже водород. Настоящее изобретение также относится к соединению формулы 15 или его фармацевтически приемлемой соли, гдеR2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой С 1-С 10 алкил, -(СН 2)m(С 6-С 10 арил) или арил, причем каждый из них, возможно замещен 1-3 заместителями, независимо выбранными из галогена, гидроксила, метоксила, C1-С 10 алкила,за исключением фенила и фенила, замещенного галогеном,m представляет собой целое число в пределах от 0 до 4;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(О)С 1-С 20 алкил;R8 представляет собой водород или метил;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже: где Y представляет собой О, или -CH2-; а, b, с и d, каждый независимо, представляют собой целое число в пределах от 0 до 2, и а + b + с + d5;R11 представляет собой водород или -ОН; иR15 представляет собой H, C1-С 10 алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, С 1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил)(водород, C1-С 10 алкил, С 2 С 10 алкенил или С 2-С 10 алкинил), за исключением того, что, когда R15 представляет собой H, R10 не представляет собой этил.-4 009729 Предпочительные соединения формулы 15 представляют собой соединения, где R1 представляетR2 представляет собой СН 3, R6, R7 и R8 представляют собой H, и R9 представляет собой собой кладинозил. Предпочительные соединения формулы 15 также представляют собой соединения, где R7 и R8 представляют собой водород. Предпочительными соединениями формулы 15 также являются соединения, имеющее формулу 3 Настоящее изобретение относится к соединению формулы 2 и его фармацевтически приемлемой соли, где X представляет собой -C(O)- или -CH(OR7)-; R2 представляет собой С 1-С 4 алкил; R7 представляет собой водород; R8 представляет собой водород;R9 представляет собой и R5 представляет собой C1-С 10 алкил, возможно замещенный 13 заместителями, независимо выбранными из -N(водород, C1-С 10 алкил, C2-С 10 алкенил или С 2 С 10 алкинил)С(O)(С 1-С 10 алкил, С 2-С 10 алкенил или C2-С 10 алкинил). Настоящее изобретение относится к соединению формулы 2 или его фармацевтически приемлемой соли, гдеR2 представляет собой водород или С 1-С 4 алкил; каждый R7 представляет собой, независимо, водород, С 1-С 20 алкил, -С(O)C1-С 20 алкил;R8 представляет собой водород или метил;R5 представляет собой водород, -CH2N(водород, С 1-С 10 алкил, С 2-С 10 алкенил или С 2 С 10 алкинил)(водород, C1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил), при условии, что когда R7 и R8 водороды, R2 тоже водород. Предпочтительным соединением формулы 2 является соединение, где R7 и R8 представляют собой-5 009729 водород. Предпочтительным соединением формулы 2 является соединение, гдеR9 представляет собой С 1-С 6 алкил, С 2-С 6 алкенил или С 2-С 6 алкинил. Предпочтительным соединением формулы 2 является соединение, выбранное из группы, состоящей из: соединения, где X представляет собой -C(O)-, и соединения, где X представляет собой -CH(OH)-. Настоящее изобретение относится также к фармацевтической композиции, полезной для лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, содержащей терапевтически эффективное количество соединения формулы 1 или 15 и фармацевтически приемлемый носитель. Настоящее изобретение относится также к способу лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, при котором указанным млекопитающему, рыбе или птице вводят терапевтически эффективное количество соединения формулы 1 или 15. Настоящее изобретение относится также к фармацевтической композиции, полезной для лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, содержащая терапевтически эффективное количество соединения формулы 1 или 15 и фармацевтически приемлемый носитель. Настоящее изобретение относится также к способу лечения бактериальной инфекции или протозойной инфекции у млекопитающего, рыбы или птицы, при котором указанным млекопитающему, рыбе или птице вводят терапевтически эффективное количество соединения формулы 1 или 15. Данное изобретение относится также к способу получения соединения формулыR2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой фенил, возможно замещенный атомами галогенов,R9 представляет собойR12 представляет собой С 1-С 10 алкил, где алкильная группировка возможно замещена 1-3 заместителями, -N(водород, С 1-С 10 алкил, C2-С 10 алкенил или С 2-С 10 алкинил)(водород, С 1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил) и где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,R6, R7 и R8 представляют собой водород; который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 1;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, или одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил,который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1 С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН; приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 1. Данное изобретение также относится к способу получения соединения формулыR2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой фенил, возможно замещенный атомами галогенов,R9 представляет собойR1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,R6, R7 и R8 представляют собой водород; который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 1, R10 представляет собой С 5 С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2 С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, или одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1 С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН; приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 1. Данное изобретение относится также к способу получения соединения формулы 15R2 представляет собой водород или С 1-С 4 алкил;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(O)C1-С 20 алкил;R8 представляет собой водород или метил;R10 представляет собой С 2-С 8 алкил,R11 представляет собой водород или -ОН; иR15 представляет собой C1-С 10 алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, С 1-С 10 алкил, C2-С 10 алкенил или С 2-С 10 алкинил)(водород, C1-С 10 алкил, С 2 С 10 алкенил или C2-С 10 алкинил),или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 15;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН, приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 15. Данное изобретение относится также к способу получения соединения формулы 15R2 представляет собой водород или С 1-С 4 алкил; R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(O)С 1-С 20 алкил;R8 представляет собой водород или метил;R10 представляет собой С 2-С 8 алкил,R11 представляет собой водород или -ОН; иR15 представляет собой H, R10 не представляет собой этил, при условии, что когда R7 и R8 водороды, R2 тоже водород,или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 15;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН,приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 15. Данное изобретение также оносится к способу получения соединения формулы 15R2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой C1-С 10 алкил, -(СН 2)m(С 6-С 10 арил) или арил, причем каждый из них, возможно замещен 1-3 заместителями, независимо выбранными из галогена, гидроксила, метоксила, С 1-С 10 алкила,за исключением фенила и фенила, замещенного галогеном,m представляет собой целое число в пределах от 0 до 4;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(O)С 1-С 20 алкил;R8 представляет собой водород или метил;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН; иR15 представляет собой H, C1-С 10 алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, C1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил)(водород, C1-С 10 алкил, С 2 С 10 алкенил или С 2-С 10 алкинил), за исключением того, что, когда R15 представляет собой H, R10 не представляет собой этил, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 15;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН,приводят в контакт с кислотой или основанием с образованием в результате соединения формулы 15. Данное изобретение относится также к способу получения соединения формулы 1 как оно определено выше,где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,R6, R7 и R8 представляют собой водород; который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 1;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 6 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, или одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил,который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1 С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН; нагревают в присутствии системы растворителей с образованием в результате соединения формулы 1. Данное изобретение относится к способу получения соединения формулы 1R2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой фенил, возможно замещенный атомами галогенов,R9 представляет собойR12 представляет собой -CH2N(водород, С 1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил)(водород,С 1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил), при условии, что когда R7 и R8 водороды, R2 тоже водород. где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1,R6, R7 и R8 представляют собой водород; который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 1;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, или одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил,который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1 С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН; нагревают в присутствии системы растворителей с образованием в результате соединения формулы 1. Данное изобретение относится к способу получения соединения формулы 15R2 представляет собой водород или С 1-С 4 алкил;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(O)C1-С 20 алкил;R8 представляет собой водород или метил; R9 представляет собойR10 представляет собой С 2-С 8 алкил,R11 представляет собой водород или -ОН; иR15 представляет собой C1-С 10 алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, C1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил)(водород, С 1-С 10 алкил, С 2 С 10 алкенил или С 2-С 10 алкинил). или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 15;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 6 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН, нагревают в присутствии системы растворителей с образованием в результате соединения формулы 15. Данное изобретение относится к способу получения соединения формулы 15R2 представляет собой водород или С 1-С 4 алкил;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, С 1-С 20 алкил, -С(O)С 1-С 20 алкил;R8 представляет собой водород или метил;R10 представляет собой С 2-С 8 алкил,R11 представляет собой водород или -ОН; иR15 представляет собой H, R10 не представляет собой этил, при условии, что когда R7 и R8 водороды, R2 тоже водород или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 15;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 6 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или OH,нагревают в присутствии системы растворителей с образованием в результате соединения формулы 15. Данное изобретение относится к способу получения соединения формулы 15R2 представляет собой водород или С 1-С 4 алкил;R3 представляет собой C1-С 10 алкил, -(СН 2)m(С 6-С 10 арил) или арил, причем каждый из них, возможно замещен 1-3 заместителями, независимо выбранными из галогена, гидроксила, метоксила, С 1-С 10 алкила,за исключением фенила и фенила, замещенного галогеном,m представляет собой целое число в пределах от 0 до 4;R6 представляет собой водород или метил; каждый R7 представляет собой, независимо, водород, C1-С 20 алкил, -С(O)C1-С 20 алкил;R8 представляет собой водород или метил;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже: где Y представляет собой О, или -CH2-; а, b, с и d, каждый независимо, представляют собой целое число в пределах от 0 до 2, и а + b + с + d5;R11 представляет собой водород или -ОН; иR15 представляет собой H, С 1-С 10 алкил, возможно замещенный 1-3 заместителями, независимо выбранными из -N(водород, C1-С 10 алкил, С 2-С 10 алкенил или С 2-С 10 алкинил)(водород, C1-С 10 алкил, C2C10 алкенил или С 2-С 10 алкинил), за исключением того, что, когда R15 представляет собой H, R10 не представляет собой этил, или его фармацевтически приемлемой соли, который включает в себя стадию, на которой соединение формулы 5 где R9 такой, как определено для соединения формулы 15;R10 представляет собой С 5-С 8 циклоалкилалкильную группу, где алкильная группа представляет собой альфа-разветвленную С 2-С 5 алкильную группу; С 3-С 8 циклоалкильную группу, которая может быть возможно замещена метилом или одним, или более чем одним гидроксилом, одной или более чем одной С 1-С 4 алкильной группой, или атомами галогенов; или 3-6-членное кислородсодержащее гетероциклическое кольцо, которое является насыщенным, и которое может быть возможно замещено одной или более чем одной С 1-С 4 алкильной группой или атомами галогенов; или R10 представляет собой фенил, который может быть возможно замещен по меньшей мере одним заместителем, выбранным из С 1-С 4 алкильной группы, атомов галогенов, гидроксильных групп, трифторметила; или R10 может иметь формулу (а), как она показана ниже:R11 представляет собой водород или -ОН нагревают в присутствии системы растворителей с образованием в результате соединений формулы 15. В предпочтительном воплощении система растворителей, используемая в способах получения, содержит растворители, выбранные из группы, состоящей из низших спиртов, диэтилового эфира, ацетона,ацетонитрила, тетрагидрофурана, этилацетата, бензола, толуола, хлороформа, метиленхлорида, диметилформамида, диметилсульфоксида, N-метилпирролидинона и их смесей. В предпочтительном воплощении система растворителей дополнительно содержит протонный растворитель, который предпочтительно выбран из группы, состоящей из метанола, этанола, н-пропанола,изопропанола, н-бутанола, изобутанола, втор-бутанола, фенола, галогенофенолов, нафтолов, воды и их смесей. Термин "лечение" при использовании здесь, если не указано иного, включает в себя лечение или предупреждение бактериальной инфекции или протозойной инфекции, как предложено в способе по настоящему изобретению. При использовании здесь, если не указано иного, выражения "бактериальная(ые) инфекция(и)" и"протозойная(ые) инфекция(и)" включают в себя бактериальные инфекции и протозойные инфекции,которые встречаются у млекопитающих, рыбы и птиц, а также расстройства, связанные с бактериальными инфекциями или протозойными инфекциями, которые можно лечить или предупреждать путем введения таких антибиотиков, как соединения по настоящему изобретению. Такие бактериальные инфекции и протозойные инфекции и расстройства, связанные с такими инфекциями, включают в себя следующие: пневмонию, средний отит, синусит, бронхит, тонзиллит и мастоидит, связанные с инфекцией Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Staphylococcus aureus или Peptostreptococcusspp; фарингит, ревматическую атаку и гломерулонефрит, связанные с инфекцией Streptococcus pyogenes,стрептококками групп C и G, Clostridium diptheriae или Actinobacillus haemolyticum; инфекции дыхательных путей, связанные с инфекцией Mycoplasma pneumoniae, Legionella pneumophila, Streptococcus pneumoniae, Haemophilus influenzae или Chlamydia pneumoniae; неосложненные инфекции кожи и мягких тканей, абсцессы, и остеомиелит, и послеродовая лихорадка, связанные с инфекцией Staphylococcus aureus,коагулазоположительными стафилококками (то есть S. epidermidis, S. hemolyticus и так далее), Streptococcus pyogenes, Streptococcus agalactiae, стрептококковыми группами C-F (стрептококки с мелкими колониями), зеленящими стрептококками, Corynebacterium minutissimum, Clostridium spp. или Bartonellahenselae; неосложненные острые инфекции мочевых путей, связанные с инфекцией Staphylococcus saprophytics или Enterococcus spp; уретрит и цервицит; и венерические заболевания, связанные с инфекциейgonorrheae; токсинные заболевания, связанные с инфекцией S. aureus (пищевая интоксикация и токсический шок) или стрептококками групп А, В и С; язвы, связанные с инфекцией Helicobacter pylori; системные лихорадочные синдромы, связанные с инфекцией Borrelia recurrentis; болезнь Лайма, связанную с инфекцией Borrelia burgdorferi; конъюнктивит, кератит и дакриоцистит, связанные с инфекцией Chlamydia trachomatis, Neisseria gonorrhoeae, S. aureus, S. pneumoniae, S. pyogenes, H. influenzae или Listeria spp; заболевание, вызванное диссеменированным Mycobacterium avium-комплексом (MAC), связанное с инфекцией Mycobacterium avium или Mycobacterium intracellulare, гастроэнтерит, связанный с инфекциейCampylobacter jejuni; кишечных простейших, связанных с инфекцией Cryptosporidium spp; одонтогенную инфекцию, связанная с инфекцией зеленящими стрептококками; персистентный кашель, связанный с инфекцией Bordetella pertussis; газовую гангрену, связанную с инфекцией Clostridium perfringens или Bacteroides spp; и атеросклероз, связанный с инфекцией Helicobacter pylori или Chlamydia pneumoniae. Бактериальные инфекции и протозойные инфекции и расстройства, связанные с такими инфекциями, которые можно лечить или предупредить у животных, включают в себя следующие: респираторное заболевание коров, связанное с инфекцией P. haem., P. multocida, Mycoplasma bovis или Bordetella spp.; кишечное заболевание коров, связанное с инфекцией E. coli или простейшими (то есть кокцидиями, криптоспоридиями и так далее); мастит молочных коров, связанный с инфекцией Staph. aureus, Strep. uberis, Strep.hyodysinteriae; копытную гниль у коров, связанную с инфекцией Fusobacterium spp.; метрит коров, связанный с инфекцией E. coli; коровьи волосяные бородавки, связанные с инфекцией Fusobacterium necrophorum или Bacterioides nodosus; коровий инфекционный конъюнктивит, связанный с инфекцией Moraxella bovis; преждевременный выкидыш у коров, связанный с инфекцией простейшими (то есть неоспорами); инфекцию мочевых путей у собак и кошек, связанную с инфекцией E. coli; инфекции кожи и мягких тканей у собак и кошек, связанные с инфекцией Staph. epidermidis, Staph. intermedius, коагулазоотр.Staph. или P. multocida; и зубные или ротовые инфекции у собак и кошек, связанные с инфекцией Alcaligenes spp., Bacterioides spp., Clostridium spp., Enterobacter spp., Eubacterium, Peptostreptococcus, Porphyromonas или Prevotella. Другие бактериальные инфекции и протозойные инфекции и расстройства, связанные с такими инфекциями, которые можно лечить или предупреждать согласно способу по настоящему изобретению, упоминаются в J. P. Sanford et al., "The Sanford Guide To Antimicrobial Therapy", 26thEdition, (Antimicrobial Therapy, Inc., 1996). Выражение "защитная группа гидроксила" при использовании здесь, если не указано иного, включает в себя ацетил, бензилоксикарбонил, к тому же различные защитные группы гидроксила, известные специалистам в данной области техники, включают группы, упоминаемые в T. W. Greene, P. G. M. Wuts,"Protective Groups in Organic Synthesis", (J. WileySons, 1991). Термин "галогено" при использовании здесь, если не указано иного, включает в себя фторо, хлоро,бромо или йодо. Предпочтительными галогеногруппами являются фторо, хлоро и бромо. Термин "алкил" при использовании здесь, если не указано иного, включает в себя насыщенные одновалентные углеводородные радикалы, имеющие прямые, циклические или разветвленные группировки. Такие циклические группировки включают циклопропил, циклобутил или циклопентил. Алкильная группа может содержать одну или две двойные или тройные связи. Следует понимать, что там, где подразумеваются циклические группировки, должны присутствовать по меньшей мере три атома углерода в указанном алкиле, и для того, чтобы алкильная группа содержала двойную или тройную связь углеродуглерод, требуются по меньшей мере два атома углерода в алкильной группе. Там, где алкильная группировка определена как С 1-С 10 алкил, эта группа включает в себя С 6-С 10 бициклогруппы, такие как группу бицикло[3.1.1]гептилметил. Термин "алкокси" при использовании здесь, если не указано иного, включает в себя группы -Оалкил, где алкил такой, как определено выше. Термин "арил" при использовании здесь, если не указано иного, включает в себя органический радикал, полученный из ароматического углеводорода удалением одного водорода, такой как фенил или нафтил, а также бензо-конденсированные карбоциклические группировки, такие как 5,6,7,8-тетрагидронафтил. Термин "4-10-членный гетероцикл" при использовании здесь, если не указано иного, включает в себя ароматические и неароматические гетероциклические группы, содержащие один или более чем один гетероатом, каждый их которых выбран из О, S и N, причем каждая гетероциклическая группа имеет от 4 до 10 атомов в своей кольцевой системе. Неароматические гетероциклические группы включают в себя группы, имеющие только 4 атома в своей кольцевой системе, но ароматические гетероциклические группы должны иметь по меньшей мере 5 атомов в своей кольцевой системе. Гетероциклические группы включают в себя бензоконденсированные кольцевые системы и кольцевые системы, замещенные одной или двумя оксогруппировками. Примером 5-членной гетероциклической группы является тиазолил, а примером 10-членной гетероциклической группы является хинолинил. Примерами неароматических ге- 19009729 тероциклических групп являются пирролидинил, пиперидино, морфолино, тиоморфолино и пиперазинил. Неароматические гетероциклические группы включают в себя насыщенные и частично ненасыщенные кольцевые системы. Примерами ароматических гетероциклических групп являются пиридинил,имидазолил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил и тиазолил. Гетероциклические группы, имеющие конденсированое бензольное кольцо, включают в себя хроман, бензодигидрофуран и бензимидазолил. Гетероциклические группы, имеющие одну или две оксогруппировки, включают фталимид и урацил. Термин "5-10-членный гетероарил" при использовании здесь, если не указано иного, включает в себя ароматические гетероциклические группы, содержащие один или более чем один гетероатом, каждый из которых выбран из О, S и N, причем каждая гетероциклическая группа имеет от 5 до 10 атомов в своей кольцевой системе. Примеры подходящих 5-10-членных гетероарильных групп включают пиридинил,имидазолил, пиримидинил, пиразолил, (1,2,3,)- и (1,2,4)-триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, оксазолил, пирролил и тиазолил. Термин "дезозаминил" при использовании здесь, если не указано иного, относится к группе Термин "кладинозил" при использовании здесь, если не указано иного, относится к группе Термин "4"-R13)(R14)NCH2)кладинозил", при использовании здесь, если не указано иного, относится к группе Термин "4"-оксокладинозил", при использовании здесь, если не указано иного, относится к группе Выражение "выделенная или очищенная форма" при использовании здесь, если не указано иного,обозначает выделенный или очищенный из реакционной смеси, например реакционной смеси, содержащей 15-членный азалид исходный материал, который затем очищают до содержания соединения формулы 1 по меньшей мере приблизительно 95%; из бактериальной культуры или бульона; или из природного, например растительного или животного, источника, с применением традиционных методик очистки,таких как хроматография, перекристаллизация и другие, известные специалистам в данной области техники, а также методик, раскрытых в материалах заявки. Выражение "фармацевтически приемлемая(ые) соль(и)" при использовании здесь, если не указано иного, включает в себя соли кислотных или основных групп, которые могут присутствовать в соединениях по настоящему изобретению. Соединения по настоящему изобретению, основные по природе, могут образовывать большое разнообразие солей с различными неорганическими и органическими кислотами. Кислоты, которые можно использовать для получения фармацевтически приемлемых солей присоединения кислот таких основных соединений по настоящему изобретению, являются кислотами, которые образуют нетоксичные соли присоединения кислот, то есть соли, содержащие фармакологически приемлемые анионы, такие как соли гидрохлорид, гидробромид, гидроиодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, кислый цитрат, тартрат,пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкаронат, сахарат,формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, паратолуолсульфонат и памоат [то есть 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)]. Соединения по настоящему изобретению, которые содержат аминогруппировку, в дополнение к кислотам, упомянутым выше, могут образовывать фармацевтически приемлемые соли с различными аминокислотами. Предпочтительно соединения формулы 1 можно использовать в качестве антибактериальных и ан- 20009729 типротозойных агентов, когда они находятся в смеси с соединениями формулы 5. В этом случае соотношение соединения формулы 1 к соединению формулы 5 находится в пределах от приблизительно 2:98 до приблизительно 40:60. Те соединения по настоящему изобретению, которые являются кислыми по природе, могут образовывать основные соли с разными фармакологически приемлемыми катионами. Примеры таких солей включают в себя соли щелочных металлов и щелочно-земельных металлов и, в частности, соли кальциевые, магниевые, натриевые и калиевые соли соединений по настоящему изобретению. Некоторые соединения по настоящему изобретению могут иметь асимметрические центры и, следовательно, существовать в разных энантиомерных и диастереоизомерных формах. Данное изобретение относится к применению всех оптических изомеров и стереоизомеров соединений по настоящему изобретению и их смесей и ко всем фармацевтическим композициям и способам лечения, в которых они могут использоваться или содержаться. Настоящее изобретение включает соединения по настоящему изобретению и их фармацевтически приемлемые соли, в которых один или более чем один водородный, углеродный или другой атом замещен своим изотопом. Такие соединения могут быть полезны в качестве научно-исследовательских или диагностических инструментов в исследованиях фармакокинетики метаболизма и в анализах связывания. Настоящее изобретение можно понять более полно при помощи ссылки на подробное описание изобретения и иллюстративные примеры, которые предназначены для того, чтобы проиллюстрировать неограничивающие воплощения данного изобретения. Подробное описание изобретения Соединения по настоящему изобретению могут быть получены согласно нижеприведенным схемам 1 и 2 и последующему описанию. В следующих схемах, если не указано иного, заместители R1, R2, R3, R4,R5, R6, R7, R8, R9, R10, R11, R12, R13, R14 и R15 являются такими, как определено выше. Схема 1 Соединения по настоящему изобретению просто получить. Относительно вышеприведенной схемы 1,исходные соединения формулы 6 легко доступны либо через торговлю, либо посредством традиционного органического синтеза. Предпочтительным соединением формулы 6 является эритромицин A (R10 = этил; R11= -ОН). Соединения формулы 6 превращают в соединения формулы 5, где R9 = кладинозил, известными способами, такими как описанные в патенте США 4474768 и 4517350. Как правило, соединения формулы 6 обрабатывают гидроксиламином в присутствии основания, предпочтительно неорганического основания,такого как бикарбонат или карбонат щелочного металла или карбонат щелочно-земельного металла, в присутствии воды и водорастворимого органического растворителя, для того чтобы получить оксимы формулы 7. Предпочтительным соединением формулы 7 является то, в котором R10 = этил; R11 = -ОН. Предпочтительно неорганическое основание представляет собой карбонат натрия, а водорастворимый органический растворитель представляет собой метанол. Соединения формулы 7 затем обрабатывают водным основанием и реагентом, который превращает оксимную гидроксильную группу соединений формулы 7 в уходящую группу и в конечном счете дает иминоэфиры формулы 8. Реагенты, полезные в этом отношении, включают в себя галогенангидриды или ангидриды паратолуолсульфокислоты, галогенангидриды или ангидриды метансульфоновой кислоты, галогенангидриды или ангидриды трифторметансульфоновой кислоты, галогенангидриды или ангидриды парабромбензолсульфоновой кислоты и тому подобное. Предпочтительно, реагент представляет собой хлорангидрид паратолуолсульфокислоты. Предпочтительным соединением формулы 8 является то, в котором R10 = этил, и R11 = -ОН. Соединения формулы 8 затем восстанавливают традиционным водородным восстановителем, предпочтительно борогидридом натрия, для того чтобы получить соединения формулы 5, где R9 представляет собой кладинозил. В предпочтительном воплощении соединение формулы 5 представляет собой дезметилазитромицин. Соединения формулы 5 превращают в соединения формулы 1 способами, описанными в материалах заявки. Специалистам в данной области техники понятно, что соединения формулы 5 превращаются в соединения формулы 1, где R1 находится в транс-положении по отношению к метильной группе в положении 11 формулы 1 и представляет собой 009729 метил; R6, R7 и R8 = водород; и R9 = кладинозил, можно затем превратить в другие соединения формулы 1 и в соединения формулы 2 посредством традиционного органического синтеза и посредством способов,описанных в материалах данной заявки. Соединения формулы 5 превращают в соединения формулы 15 способами, описанными в материалах данной заявки. Специалистам в данной области техники понятно, что соединения формулы 5 превращаются в соединения формулы 15, где R1 находится в транс-положении по отношению к метильной, R2 = метил; R6, R7 и R8 = водород; и R9 = кладинозил, можно затем превратить в другие соединения формулы 15 и в соединения формулы 2 посредством традиционного органического синтеза и посредством способов, описанных в материалах данной заявки. Специалистам в данной области техники понятно, что в дополнение к соединениям формулы 6 другие 14-членные макролиды, склонные к расширению кольца по бекмановскому типу, такие как, например, эритромицин В, эритромицин С и кларитромицин, можно превратить в предшественников 13 членных азалидов, предусмотренных настоящим изобретением. Когда желательно, чтобы соединения формулы 1 представляли собой те, в которых R9 = 4"13R )(R14)NCH2)кладинозил, можно применять способы, обобщенные в схеме 2. Например, 2'-гидроксильную группу дезозаминильной группы соединений формулы 5 можно сначала защитить подходящей защитной группой, предпочтительно бензилоксикарбонильной ("Cbz"'(Сбензилгруппой, используя Cbz-Cl, для того чтобы получить соединения формулы 9. Такую реакцию можно провести при температуре от приблизительно -78C до приблизительно комнатной температуры,предпочтительно приблизительно при 0C. Предпочтительным соединением формулы 9 является то, в котором R10 = этил; R11 = -ОН. 4"-Гидроксильную группу кладинозильной группы соединений формулы 9 можно затем окислить, используя окислительные стандартные условия, с получением соединений формулы 10, которые несут 4"-оксокладинозильную группу. Предпочтительным соединением формулы 10 является то, в котором R10 = этил; R11 = -ОН. Такие окислительные условия можно найти, например, вJournal of Antibiotics, 1988, pages 1029-1047. Типичные условия реакции окисления включают в себя: (а) окисление по Моффетту, при котором используется N-этил-N'-(N,N-диметиламинопропил)карбодиимид и ДМСО (диметилсульфоксид) в присутствии пиридинийтрифторацетата; или (б) окисление по Сверну(Swern), при котором за оксалилхлоридом и ДМСО в CH2Cl2 следует добавление триэтиламина или, альтернативно, за трифторуксусным ангидридом и ДМСО в CH2Cl2 следует добавление триэтиламина. Предпочтительно окисление представляет собой окисление по Сверну, которое проводят в присутствии трифторуксусного ангидрида при температуре от приблизительно -78 С до приблизительно 0C. Более предпочтительно окисление по Сверну проводят при температуре приблизительно -60C. Карбонильную группу 4"-оксокладинозильной группы соединений формулы 10 затем превращают в эпоксид с получением соединений формулы 11. Предпочтительным соединением формулы 11 является то, в котором R10 = этил; R11 = -ОН. Соединения формулы 10 можно превратить в соединения формулы 11 по меньшей мере двумя способами. В одном способе (Способ А), соединение формулы 10 обрабатывают (CH3)3S(O)X2, где X2 представляет собой галогено, -BF4 или -PF6, предпочтительно иодо, в присутствии основания, такого как трет-бутилат калия, трет-бутилат натрия, этилат натрия, гидрид натрия,1,1,3,3-тетраметилгуанидин, 1,8-диазабицикло[5.4.0]ундек-7-ен, 1,5-диазабицикло[4.3.0]нон-5-ен, этилат калия или метилат натрия, предпочтительно натрий-содержащее основание, такое как гидрид натрия, в растворителе, таком как ТГФ (тетрагидрофуран), растворитель-простой эфир, диметилформамид (ДМФ) или диметилсульфоксид (ДМСО), или в смеси двух или более вышеуказанных растворителей, при температуре в пределах от приблизительно 0C до приблизительно 60C; альтернативно триметилсульфонийбромидом и сильным основанием, таким как трет-бутилат калия, в присутствии CH2Cl2/ТГФ. Во втором способе (Способ Б), соединения формулы 10 обрабатывают (CH3)3SX2, где X2 представляет собой галогено, -BF4 или -PF6, предпочтительно -BF4, в присутствии основания, такого как третбутилат калия, этилат натрия,трет-бутилат натрия, гидрид натрия, 1,1,3,3-тетраметилгуанидин, 1,8 диазабицикло[5.4.0]ундек-7-ен, 1,5-диазабицикло[4.3.0]нон-5-ен, этилат калия, гексаметилдисилазид калия (КГМДС) или метилат натрия, предпочтительно КГМДС, в растворителе, таком как ТГФ, в растворителе-простом эфире, ДМФ или ДМСО, или в смеси двух или более вышеперечисленных растворителей, при температуре в пределах от приблизительно -78 С до приблизительно 60C. Предпочтительно применяют способ Б, в котором используют триметилсульфонийбромид и третбутилат калия. Защитную, предпочтительно Cbz, группу дезозаминильной группы соединений формулы 11 под- 24009729 вергают гидрогенолизу в присутствии H2, Pd/С и любого подходящего органического растворителя,предпочтительно метил-трет-бутилового эфира ("МТБЭ"), с получением соединений формулы 12. Предпочтительным соединением формулы 12 является то, в котором R10 = этил, и R11 = -ОН. Наконец, в эпоксидной группе в положении 4" сахара кладинозы соединений формулы 12 разрывают кольцо, используяHN(R13)(R14), предпочтительно в присутствии иодида калия, с получением соединений формулы 5, в которых R9=4"-(R13)(R14)NCH2)кладинозил. Соединения формулы HN(R13)(R14) включают первичные и вторичные алкил-, алкенил- и алкиниламины и являются легко получаемыми для специалистов в данной области техники. Такая реакция предпочтительно протекает при температуре от приблизительно комнатной температуры до приблизительно 80C, предпочтительно от приблизительно 30 С до приблизительно 60C. Соединения формулы 5, где R9=4"-R13)(R14)NCH2)кладинозил, можно превратить в соединения формул 1 и 15, применяя способы, раскрытые здесь. Следует указать на то, что превращение соединений формулы 11 в соединения формулы 5, где R9 = 13 4"-(R )(R14)NCH2)кладинозил, можно осуществить в одну стадию путем обработки соединений формулы 10 HN(R13)(R14) в присутствии метанола, что удаляет защитную группу с дезозаминильной группы соединений формулы 10. Предпочтительно такую реакцию проводят в присутствии иодида калия. Для того чтобы получить соединения формулы 5, где R9 = 4"-оксокладиноза, защитную, предпочтительно Cbz, группу, которая находится на T-гидроксильной группе дезозаминильной группы соединений формулы 10, просто удаляют. Методики удаления таких защитных групп можно найти, например, вGreen et al., см. выше. К удивлению и неожиданно авторы настоящего изобретения обнаружили, что соединения формулы 5, которые представляет собой 15-членные азалиды, можно превратить в соединения формул 1 и 15, которые представляют собой 13-членные азалиды. Авторы настоящего изобретения обнаружили, что превращение соединений формулы 5 в соединения формул 1 и 15, предпочтительно где R6, R7 и R8 представляют собой водород, и предпочтительно гдеR1 находится в транс-положении по отношению к метильной группе в положении 11 формул 1 и 15, может быть осуществлено путем приведения в контакт соединения формулы 5 с кислотой или основанием. Кислоты, полезные в этой связи, включают неорганические кислоты, такие как соляная, бромистоводородная, иодисто-водородная, фтористо-водородная, серная и азотная кислоты; и органические кислоты, такие как муравьиная, уксусная, трифторуксусная, метансульфоновая, трифторметансульфоновая,бензолсульфоновая и паратолуолсульфоновая кислоты. Неорганические кислоты предпочтительно используют в форме их водных растворов; более предпочтительно, неорганические кислоты используют в форме их разбавленных, то есть 2 М, водных растворов. Органические кислоты можно использовать в форме разбавленных водных или органических растворов, где органический раствор содержит растворитель, который достаточно сольватирует как органическую кислоту, так и соединение формулы 5. Основания, подходящие в этом отношении, включают неорганические основания, такие как гидроксиды натрия, лития, калия, магния или кальция; карбонаты и бикарбонаты натрия, лития или калия; и карбонаты магния или кальция бикарбонат или карбонат. Также подходящими являются органические основания, такие как триэтиламин, этилдиизопропиламин, пиридин, 4-диметиламинопиридин, коллидин,лутидин и их смеси. Предпочтительно неорганические основания используют в форме разбавленных водных растворов. Предпочтительно органические основания используют в форме разбавленных органических растворов. Неорганические или органические основания являются предпочтительными по сравнению с неорганическими или органическими кислотами. Соединения формулы 5 можно добавлять к кислоте или основанию, или наоборот. В любом случае реакцию соединений формулы 5 с кислотой или основанием облегчают путем нагревания смеси соединения формулы 5 и кислоты или основания при температуре от приблизительно комнатной температуры до приблизительно 100C, предпочтительно при температуре от приблизительно комнатной температуры до приблизительно 60C, и более предпочтительно при температуре от приблизительно 30 до приблизительно 40 С. Такое нагревание может происходить в течение периода времени от приблизительно 20 мин до приблизительно 48 ч, предпочтительно в течение периода времени от приблизительно 1 ч до приблизительно 36 ч. Настоящее изобретение также касается способа получения соединения формул 1 и 15, или их фармацевтически приемлемой соли, включающего в себя стадию, на которой соединение формулы 5 нагревают в присутствии растворителя. Такое нагревание осуществляют при температуре от приблизительно комнатной температуры до приблизительно 100C, предпочтительно при температуре от приблизительно комнатной температуры до приблизительно 60C, и более предпочтительно при температуре от приблизительно 30C до приблизительно 40 С. Нагревание может происходить в течение периода времени от приблизительно 20 мин до приблизительно 48 ч, предпочтительно в течение периода времени от приблизительно 1 ч до приблизительно 36 ч. Подходящими растворителями являются те, которые достаточно сольватируют соединения формулы 5, и включают в себя, но не ограничены ими, низшие спирты, диэтиловый эфир, ацетон, ацетонитрил,- 25009729 тетрагидрофуран, этилацетат, бензол, толуол, хлороформ, метиленхлорид, диметилформамид, диметилсульфоксид, N-метилпирролидинон и тому подобное, и их смеси. Однако авторы настоящего изобретения обнаружили, что неожиданно и к удивлению превращение соединений формулы 5 в соединения формул 1 и 15 происходит более быстро в системе растворителей,которая содержит протонный растворитель. Пригодные протонные растворители включают в себя, но не ограничены ими, низшие спирты, такие как метанол, этанол, н-пропанол, изопропанол, н-бутанол, изобутанол и втор-бутанол; фенольные соединения, такие как фенол, галогенофенолы, нафтолы и тому подобное; воду; и их смеси. Однако следует указать на то, что протонный растворитель не представляет собой карбоновую кислоту. Когда система растворителей содержит протонный растворитель, этот протонный растворитель присутствует в количестве от приблизительно 10 до приблизительно 75% по объему, предпочтительно в количестве от приблизительно 25 до приблизительно 60% по объему. Специалистам в данной области техники понятно, что протонный растворитель является смешиваемым с растворителем, в котором нагревают соединение формулы 5, когда нагрет при температуре нагревания. Предпочтительно система растворителей содержит ацетонитрил. Более предпочтительно, система растворителей дополнительно содержит низший спирт или воду. Когда система растворителей содержит низший спирт, этот низший спирт предпочтительно представляет собой метанол. Соединения формул 1 и 15 можно выделить или очистить стандартными способами, например перекристаллизацией; хроматографией с использованием колонки, препаративной пластинки или устройства CHROMATOTRON; или другими способами, известными специалистам в данной области техники. Авторы настоящего изобретения обнаружили, что когда для выделения или очистки соединений формул 1 и 15 применяют хроматографию, элюирующая система, которая включает в себя углеводородный растворитель и органический амин, обеспечивает улучшенные результаты разделения по сравнению с другими элюирующими системами. Углеводородные растворители, пригодные в этом отношении, включают, но не ограничены ими, пентан, гексан или гексаны, гептан, петролейный эфир, бензол, толуол, ксилолы и тому подобное. Предпочтительно углеводородный растворитель представляет собой гексан или гексаны. Подходящие органические амины включают в себя, но не ограничены ими, диэтиламин, триэтиламин, этилдиизопропиламин, пиридин, 4-диметиламинопиридин, коллидин, лутидин и их смеси. Предпочтительно органический амин представляет собой диэтиламин. Преимущественно элюирующая система, которая содержит углеводородный растворитель и органический амин, дополнительно содержит полярный органический растворитель. Авторы данного изобретения обнаружили то, что добавление полярного органического растворителя к элюирующей системе обеспечивает лучшее отделение соединений формул 1 и 15 от других соединений по сравнению с элюирующей системой, которая не содержит полярный органический растворитель. Подходящие полярные растворители включают в себя низшие спирты, ацетонитрил, диметилформамид, диметилсульфоксид, Nметилпирролидинон, 1,4-диоксан, тетрагидрофуран, диэтиловый эфир, этилацетат и тому подобное, но не ограничены ими. Предпочтительно полярный органический растворитель представляет собой ацетонитрил. Более предпочтительно, элюирующая система содержит гексаны, диэтиламин и ацетонитрил. Соотношения углеводородного растворителя, органического амина и, возможно, полярного органического растворителя могут варьировать, но, как правило, соотношение углеводородного растворителя и органического амина находится в пределах от приблизительно 10:1 до приблизительно 1:1, предпочтительно от приблизительно 7:1 до приблизительно 2:1. Когда элюирующая система дополнительно содержит полярный органический растворитель, эта элюирующая система содержит от приблизительно 1 до приблизительно 15% по объему, предпочтительно от приблизительно 1,5 до приблизительно 10% по объему, полярного органического растворителя. В другом воплощении данного изобретения предпочтительными соединениями формул 1 и 15 являются те, где R1 представляет собой ацетил. Особенно предпочтительными являются соединения формулы 1, где R1 представляют собой ацетил, R6, R7 и R8 представляют собой водород; и R9 = кладинозилR9 представляет собой кладинозил ("Соединение 1 Д", табл. 1). Кроме того, что они полезны в качестве антибактериальных и антипротозойных агентов, соединения формул 1 и 15, где R1 представляет собой ацетил, полезны в качестве промежуточных соединений для получения других соединений формул 1 и 15, как описано ниже. В общем плане соединения формул 1 и 15, где R1 представляет собой ацетил, получают окислением соединений формул 1 и 15, где R1 = которые можно получить способами, обсуждаемыми в материалах заявки. Реакция окисления протекает в присутствии тетраацетата свинца, периодата натрия или любых других окислителей, которые превращают 1-метил-1,2-диолы в метилкетоны. Условия реакции, пригодные для окисления 1-метил-1,2-диола в метилкетон известны специалистам в данной области- 26009729 техники. Предпочтительно реакция окисления протекает в присутствии от приблизительно 1,0 до приблизительно 1,5 эквивалентов тетраацетата свинца на эквивалент соединения формул 1 и 15 и при температуре от приблизительно -78 С до комнатной температуры, предпочтительно от приблизительно -10C до приблизительно 10C, и в течение промежутка времени от приблизительно 10 мин до приблизительно 6 ч. Соединения формул 1 и 15, где R1 представляет собой ацетил, можно превратить в соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил. Такая реакция преимущественно происходит в присутствии избытка диметилацеталя диметилформамида. Предпочтительно эту реакцию проводят в отсутствие дополнительного растворителя. Соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил, можно превратить в соединения формул 1 и 15, где R1 = 1-N-замещеный-3-пиразолил, путем обработки соединений формулы 1, гдеR1 = 3-N,N-диметиламино-2-пропеноил, 1-замещенным гидразином или его кислой солью в количестве от приблизительно 1 до приблизительно 10 эквивалентов. Если применяют кислую соль 1-замещенного гидразина, тогда реакционная смесь, содержащая кислую соль и соединение формул 1 и 15, также содержит слабое органическое основание или щелочь для забуферивания реакционной смеси. Предпочтительные органические основания включают диизопропилэтиламин, пиридин, 4-диметиламинопиридин,лутидин, коллидин и тому подобное, и их смеси. Предпочтительно органическое основание представляет собой диизопропилэтиламин. Реакция между соединениями формул 1 и 15, где R1 = 3-N,Nдиметиламино-2-пропеноил, и 1-замещенным гидразином или его солью происходит в протонном растворителе, таком как растворитель, описанный выше, при температуре в пределах от приблизительно 50 до приблизительно 115C, в течение промежутка времени от приблизительно 1 ч до приблизительно 5 сут. Предпочтительно протонный растворитель представляет собой 2-метоксиэтанол или 2-пропанол. Соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил, можно превратить в соеди согласно методике, применяемой для получения соединений нения формул 1 и 15, где R1 = формул 1 и 15, где R1 = 1-N-замещеный-3-пиразолил, за исключением того, что R3N(H)C(=NH)NH2 используют вместо 1-замещенного гидразина. Способы получения R3N(H)C(=NH)NH2 известны специалистам в данной области техники. Соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил, можно превратить в соеди нения формул 1 и 15, где R1 = путем осуществления взаимодействия соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил, с в апротонном растворителе при температуре в пределах от приблизительно 50 до приблизительно 110C, в течение промежутка времени от известны специалиприблизительно 1 ч до приблизительно 5 сут. Способы получения стам в данной области техники. Подходящие апротонные растворители включают в себя пентан, гексаны, гептан, толуол, бензол,ксилолы, петролейный эфир, тетрагидрофуран, 1,4-диоксан и тому подобное, но не ограничены ими. Предпочтительно апротонный растворитель представляет собой толуол. Соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил, можно превратить в соединения формул 1 и 15, где R1 = 3-изоксазолил, путем осуществления взаимодействия соединения формул 1 и 15, где R1 = 3-N,N-диметил-2-пропеноил, с гидроксиламином или его кислой солью в количестве от приблизительно 1 до приблизительно 10 эквивалентов. Реакцию, используемую для получения соединений формул 1 и 15, где R1 = 3-изоксазолил, предпочтительно проводят в апротонном растворителе, таком как растворитель, описанный выше, при температуре, равной или приблизительно равной комнатной температуре в течение промежутка времени от приблизительно одного до приблизительно пяти суток. Более предпочтительно, апротонный растворитель представляет собой 1,4-диоксан. Соединения формул 1 и 15, где R1 = ацетил, можно превратить в соединения формулы 2, где X = -C(O)-,путем взаимодействия соединения формул 1 и 15, где R1 = ацетил, с избытком диметилацеталя диметилформамида с получением соединений формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил, описанных выше. Соединения формул 1 и 15, где R1 = 3-N,N-диметиламино-2-пропеноил подвергаются внутримолекулярной циклизации с образованием соединений формулы 2, где X= -C(O)-. Такая внутримолекулярная циклизация преимущественно происходит при высокой температуре, например при приблизительно 110C или выше. Соответственно, внутримолекулярную циклизацию осуществляют путем нагревания смеси высококипящего раствори- 27009729 теля и соединения формул 1 и 15, где R1 представляет собой 3-N,N-диметиламино-2-пропеноил, до температуры приблизительно 110C или выше в течение промежутка времени от приблизительно 6 до приблизительно 48 ч, предпочтительно в течение промежутка времени от приблизительно 12 до приблизительно 24 ч. Подходящие высококипящие растворители включают в себя толуол, ксилолы, хлорбензол,диметилформамид, 2-метоксиэтанол, диметилсульфоксид и тому подобное, но не ограничены ими. Предпочтительно высококипящий растворитель представляет собой 2-метоксиэтанол. Соединения формулы 2, где X = -C(O)-, превращают в соединения формулы 2, где X=-CH(OH)-, путем обработки соединений формулы 2, где X=-C(O)-, восстановителем гидридом, таким как NaBH4,LiAIH4, NaAlH4, восстановителем SELECTIDE или другим реагентом-гидридом, известным специалистам в данной области техники. Соединения по настоящему изобретению могут иметь асимметрические атомы углерода и, следовательно, существовать в разных энантиомерных и диастереомерных формах. Диастереомерные смеси можно разделить на их отдельные диастереомеры на основе их физико-химических различий способами,известными специалистам в данной области техники, например хроматографией или фракционной кристаллизацией. Энантиомеры можно разделить путем превращения энантиомерных смесей в диастереомерную смесь путем осуществления взаимодействия с соответствующим оптически активным соединением (например спиртом), разделения диастереомеров и превращения (например гидролиза) отдельных диастереомеров в соответствующие чистые энантиомеры. Применение всех таких изомеров, включая смеси диастереомеров и чистые энантиомеры, считается частью настоящего изобретения. Соединения по настоящему изобретению, являющиеся основными по природе, способны к образованию широкого ряда различных солей с различными неорганическими и органическими кислотами. Хотя такие соли должны быть фармацевтически приемлемыми для введения млекопитающим, на практике часто желательно сначала выделить соединение по настоящему изобретению из реакционной смеси в виде фармацевтически неприемлемой соли и затем просто превратить последнюю обратно в свободное основание обработкой щелочным реагентом, и затем превратить последнее свободное основание в фармацевтически приемлемую соль присоединения кислоты. Соли присоединения кислот основных соединений по изобретению легко получить путем приведения в контакт основного соединения с по существу эквивалентным количеством выбранной минеральной или органической кислоты в среде водного растворителя или в подходящем органическом растворителе, таком как метанол или этанол. Желаемую твердую соль легко получают после осторожного выпаривания растворителя. Желаемую соль также можно осадить из раствора свободного основания в органическом растворителе путем добавления к раствору подходящей минеральной или органической кислоты. Те соединения по настоящему изобретению, которые являются кислыми по природе, способны к образованию основных солей с различными катионами. Для соединений, которые нужно вводить млекопитающим, рыбе или птицам, такие соли должны быть фармацевтически приемлемыми. Когда требуется фармацевтически приемлемая соль, может быть желательно сначала выделить соединение по настоящему изобретению из реакционной смеси в виде фармацевтически неприемлемой соли и затем просто превратить последнюю в фармацевтически приемлемую соль способом, аналогичным тому, что описан выше в отношении превращения фармацевтически неприемлемых солей присоединения кислот в фармацевтически приемлемые соли. Примеры основных солей включают соли щелочных металлов или щелочно-земельных металлов, и в частности соли натрия, амина и калия. Все эти соли получают по традиционным методикам. Химические основания, которые используют в качестве реагентов для получения фармацевтически приемлемых основных солей по данному изобретению, представляют собой основания,которые образуют нетоксичные основные соли с кислыми соединениями по настоящему изобретению. Такие нетоксичные основные соли включают производные от таких фармакологически приемлемых катионов как натрий, калий, кальций, магний, различные катионы аминов и так далее. Эти соли можно легко получить путем приведения в контакт соответствующих кислотных соединений с водным раствором,содержащим желаемые фармакологически приемлемые основания с катионами, такими как натрий, калий, кальций, магний, различные катионы аминов, и так далее, и последующего выпаривания полученного в результате раствора до сухости, предпочтительно при пониженном давлении. Альтернативно, их также можно получить путем смешения вместе растворов кислотных соединений в низших спиртах и алкоголятов желаемых щелочных металлов и последующего выпаривания полученного в результате раствора до сухости тем же способом, что и ранее. В обоих случаях предпочтительно использовать стехиометрические количества реагентов, чтобы обеспечить полноту реакции и максимальные выходы желаемого конечного продукта. Антибактериальная и антипротозойная активность соединений по настоящему изобретению против бактерий- и простейших-патогенов продемонстрирована способностью соединений ингибировать рост определенных штаммов человеческих или животных патогенов. Анализ I. Анализ I, описанный ниже, использует традиционные методику и критерии интерпретации и имеет целью предложить направление химических модификаций, которые могут привести к соединениям, которые обходят определенные механизмы резистентности к макролидам. В Анализе I набор бактериаль- 28009729 ных штаммов составляют таким образом, чтобы включить ряд целевых патогенных видов, включая представителей механизмов резистентности к макролидам, которые были охарактеризованы. Использование этого набора позволяет установить связь химическая структура/активность в отношении эффективности,спектра активности и структурных элементов или модификаций, которые могут быть необходимы, чтобы устранить механизмы резистентности. Бактериальные патогены, которые составляют набор для скрининга, представлены в таблице ниже. Во многих случаях, как чувствительный к макролидам родительский штамм, так и резистентный к макролидам штамм, полученный из него, полезны для обеспечения более точной оценки способности соединений обойти механизм резистентности. Штаммы, которые содержат ген с обозначением ermА/ermВ/ermС, резистентны к антибиотикам макролидам, линкозамидам и стрептограмину В благодаря модификациям (метилированию) молекул 23S р-PHK (рибосомальная рибонуклеиновая кислота) Erm метилазой, тем самым обычно препятствуют связыванию всех трех структурных классов. Описаны два типа оттока макролидов; msrA кодирует компонент системы оттока у стафилококков, который препятствует проникновению макролидов и стрептограминов, в то время как mefA/E кодирует трансмембранный белок, который, по-видимому, выводит только макролиды. Может происходить инактивация макролидных антибиотиков, и она может быть опосредована либо фосфорилированием 2 гидроксила (mph), либо расщеплением макроциклического лактона (эстераза). Штаммы можно охарактеризовать, используя традиционную методику полимеразной цепной реакции (PCR) и/или путем секвентирования детерминанты резистентности. Использование методики PCR для этого применения описано вStandard, опубликованным по директивам Национального Комитета Клинических Лабораторных Стандартов (NCCLS); для сравнения штаммов используют минимальную ингибирующую концентрацию(MIC). Соединения первоначально растворяют в диметилсульфоксиде (ДМСО) с образованием 40 мг/мл исходных растворов. Анализ II используют для тестирования на активность против Pasteurella multocida и Анализ III ис- 29009729 пользуют для тестирования на активность против Pasteurella haemolytica. Анализ II. Анализ основан на методе разведений в жидкости в микролитровом масштабе. Единичную колониюP. multocida (штамм 59 А 067) инокулируют в 5 мл бульона с сердечно-мозговым экстрактом (BHI). Тестируемые соединения готовят, растворяя 1 мг соединения в 125 мкл диметилсульфоксида (ДМСО). Разведения испытуемого соединения готовят, используя неинокулированный BHI-бульон. Используемые концентрации испытуемого соединения варьируют от 200 мкг/мл до 0,098 мкг/мл в результате двухкратных серийных разведений. BHI, инокулированный P. multocida, разводят неинокулированным BHIбульоном с получением суспензии 104 клеток на 200 мкл. BHI-клеточные суспензии смешивают с соответствующими серийными разведениями тестируемого соединения и инкубируют при 37C в течение 18 ч. Минимальная ингибирующая концентрация (MIC) равна концентрации соединения, проявляющей 100% ингибирование роста P. multocida при определении в сравнении с неинокулированным контролем. Анализ III. Этот анализ основан на способе разведения в агаре с использованием репликатора Steers Replicator. От двух до пяти колоний, выделенных с чашки с агаром, инокулируют в BHI-бульон и инкубируют в течение ночи при 37 С при перемешивании (200 об./мин). На следующее утро 300 мкл полностью выросшей предкультуры P. haemolytica инокулируют в 3 мл свежего BHI-бульона и инкубируют при 37 С при перемешивании (200 об./мин). Соответствующие количества тестируемых соединений растворяют в этаноле и готовят серии двухкратных серийных разведений. Два мл соответствующего серийного разведения смешивают с 18 мл расплавленного BHI-агара и дают застыть. Когда инокулированная культура P.haemolytica достигает 0,5 McFarland стандарта плотности, около 5 мкл этой культуры P. haemolytica инокулируют на чашки с BHI-агаром, содержащие различные концентрации тестируемого соединения, используя Steers Replicator, и инкубируют в течение 18 ч при 37C. Исходные концентрации тестируемого соединения варьируют в пределах 100-200 мкг/мл. MIC равна концентрации тестируемого соединения,показывающей 100% ингибирование роста P. haemolytica при определении в сравнении с неинокулированным контролем. Анализ IV.In vivo активность соединений по настоящему изобретению можно определить путем традиционных исследований иммунитета животных, хорошо известных специалистам в данной области техники,обычно проводимых на мышах. Мышей по прибытии распределяют по клеткам (10 на клетку) и оставляют акклиматизироваться в течение минимум 48 ч перед использованием. Животных инокулируют 0,5 мл 3 х 103 CFU/мл (колониеобразующих единиц (КОЕ) на мл) бактериальной суспензии (P. Multocida, штамм 59 А 006) внутрибрюшинно. В каждом эксперименте имеются по меньшей мере 3 не лечимые лекарством контрольные группы, включающие одну, инфицированную 0,1 Х провокационной дозой, и две, инфицированные 1 Х провокационной дозой; группу с 10 Хпровокационной дозой также можно использовать. Как правило, всем мышам в данном исследовании можно сделать провокационную пробу в пределах 30-90 мин, особенно если для введения провокационной пробы используют автоматический шприц для непрерывного введения (такой как шприц Cornwall). Через 30 мин после начала осуществления провокационной пробы проводят первое лечение соединением. Может оказаться необходимым, чтобы второй человек начал дозирование соединения, если всем животным не была сделана провокационная проба к концу 30 мин. Путями введения являются подкожные или пероральные дозы. Подкожные дозы вводят под оттянутую кожу на задней части шеи, тогда как пероральные дозы дают при помощи иглы для кормления. В обоих случаях используют объем 0,2 мл на мышь. Соединения вводят через 30 мин, 4 и 24 ч после провокационной пробы. Контрольное соединение с известной эффективностью, вводимое тем же путем, включают в каждый тест. Животных обследуют ежедневно и записывают количество выживших в каждой группе. Мониторинг на модели с P. multocida продолжается в течение 96 ч (четырех суток) после провокационной пробы.PD50 (50% защитная доза) представляет собой рассчитанную дозу, при которой тестируемое соединение защищает 50% группы мышей от смерти вследствие бактериальной инфекции, которая была бы летальной в отсутствие лечения лекарственным средством. Соединения по настоящему изобретению показывают антибактериальную активность в одном из вышеописанных анализов, в частности в Анализе IV. Соединения по настоящему изобретению и их фармацевтически приемлемые соли (ниже: "активные соединения") можно вводить пероральным, парентеральным, местным или ректальным путями при лечении бактериальных и протозойных инфекций. Вообще, эти соединения наиболее желательно вводить в дозировках в пределах от приблизительно 0,2 мг на кг массы тела в сутки (мг/кг/сутки) до приблизительно 200 мг/кг/сутки в однократных или разделенных общих дозах (то есть от 1 до 4 доз в сутки), хотя отклонения обязательно будут иметь место в зависимости от вида, массы и состояния субъекта, которого лечат, и конкретного выбранного пути введения. Однако наиболее желательно применять уровень дозировок в пределах от приблизительно 4 до приблизительно 50 мг/кг/сутки. Тем не менее, могут иметь место отклонения в зависимости от вида млекопитающего, рыбы или птицы, которых лечат, и их индиви- 30
МПК / Метки
МПК: C07H 17/08, A61K 31/70
Метки: 13-членные, качестве, антибиотических, азалиды, применение, агентов
Код ссылки
<a href="https://eas.patents.su/30-9729-13-chlennye-azalidy-i-ih-primenenie-v-kachestve-antibioticheskih-agentov.html" rel="bookmark" title="База патентов Евразийского Союза">13-членные азалиды и их применение в качестве антибиотических агентов</a>
Предыдущий патент: Триазиновые соединения и их применение в медицине
Следующий патент: Фармацевтическая композиция для лечения сердечно-сосудистых и цереброваскулярных заболеваний
Случайный патент: Ситовая рама для вибрационного сита и способ ее изготовления