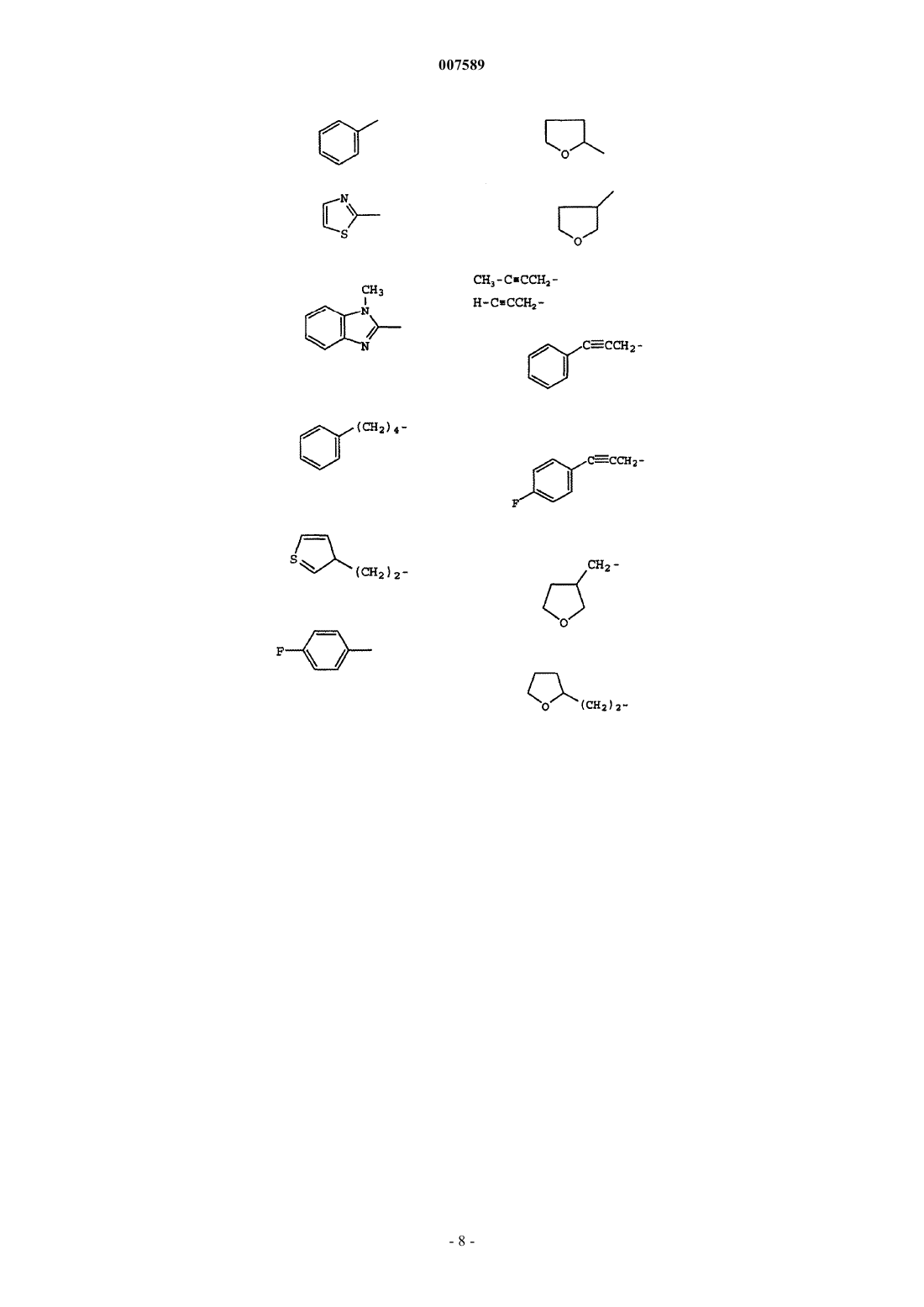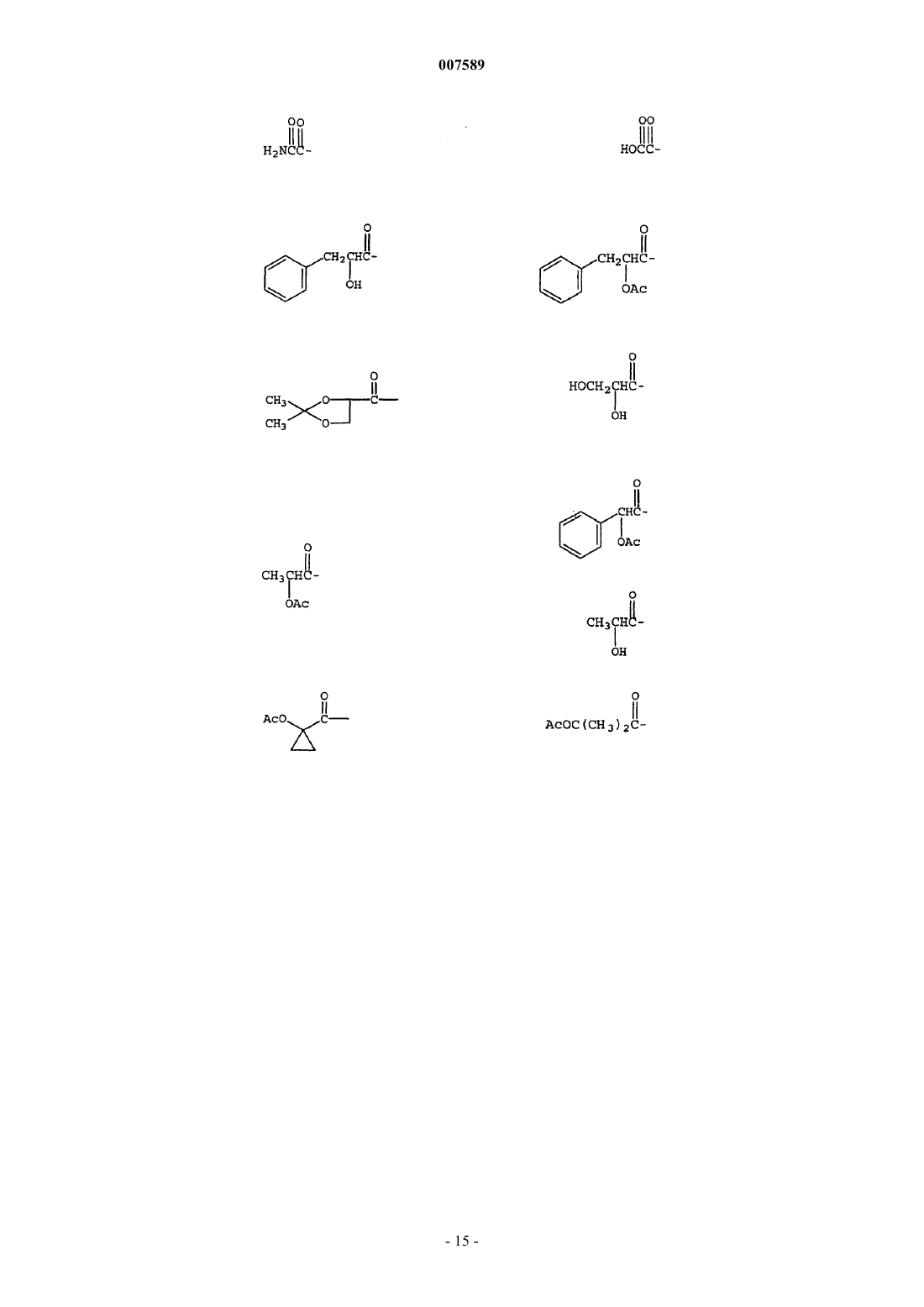Пирролидины, которые ингибируют цамф-специфичную pde
Номер патента: 7589
Опубликовано: 29.12.2006
Авторы: Бэрджесс Лоренс И., Фаулер Керри У., Шлахтер Стивен Т., Одинго Джошуа, Мартинс Тимоти Дж.
Формула / Реферат
1. Соединение, имеющее формулу
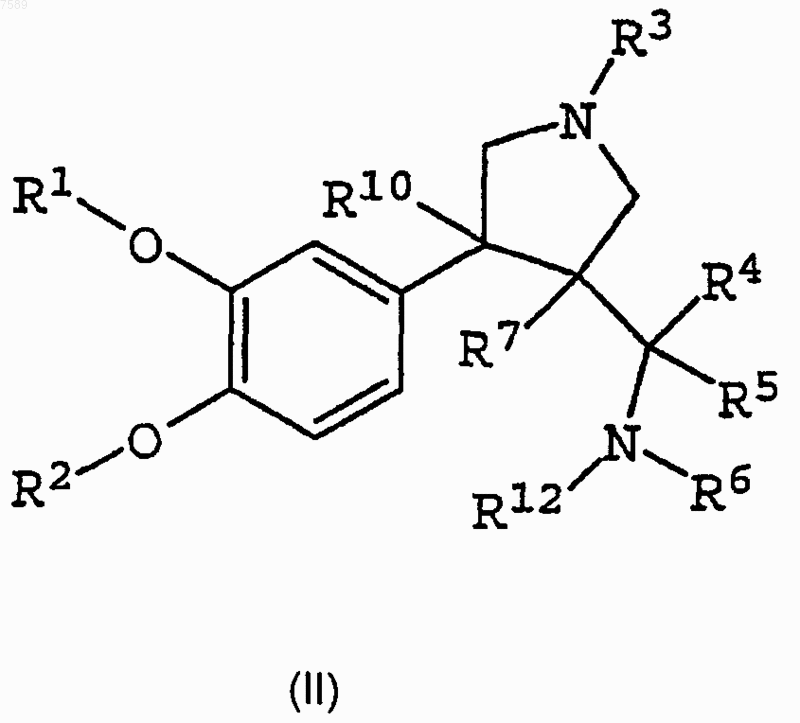
в которой
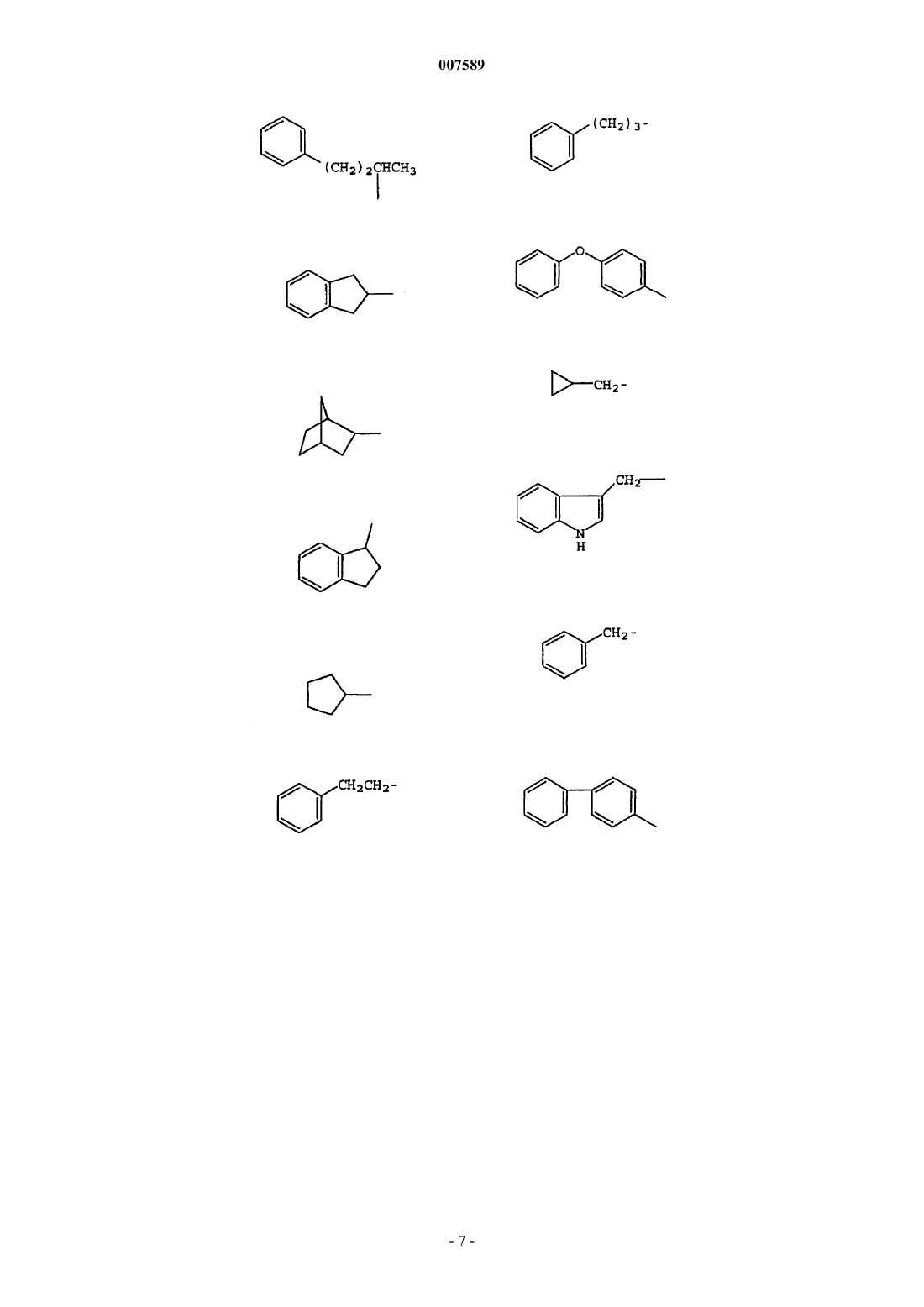
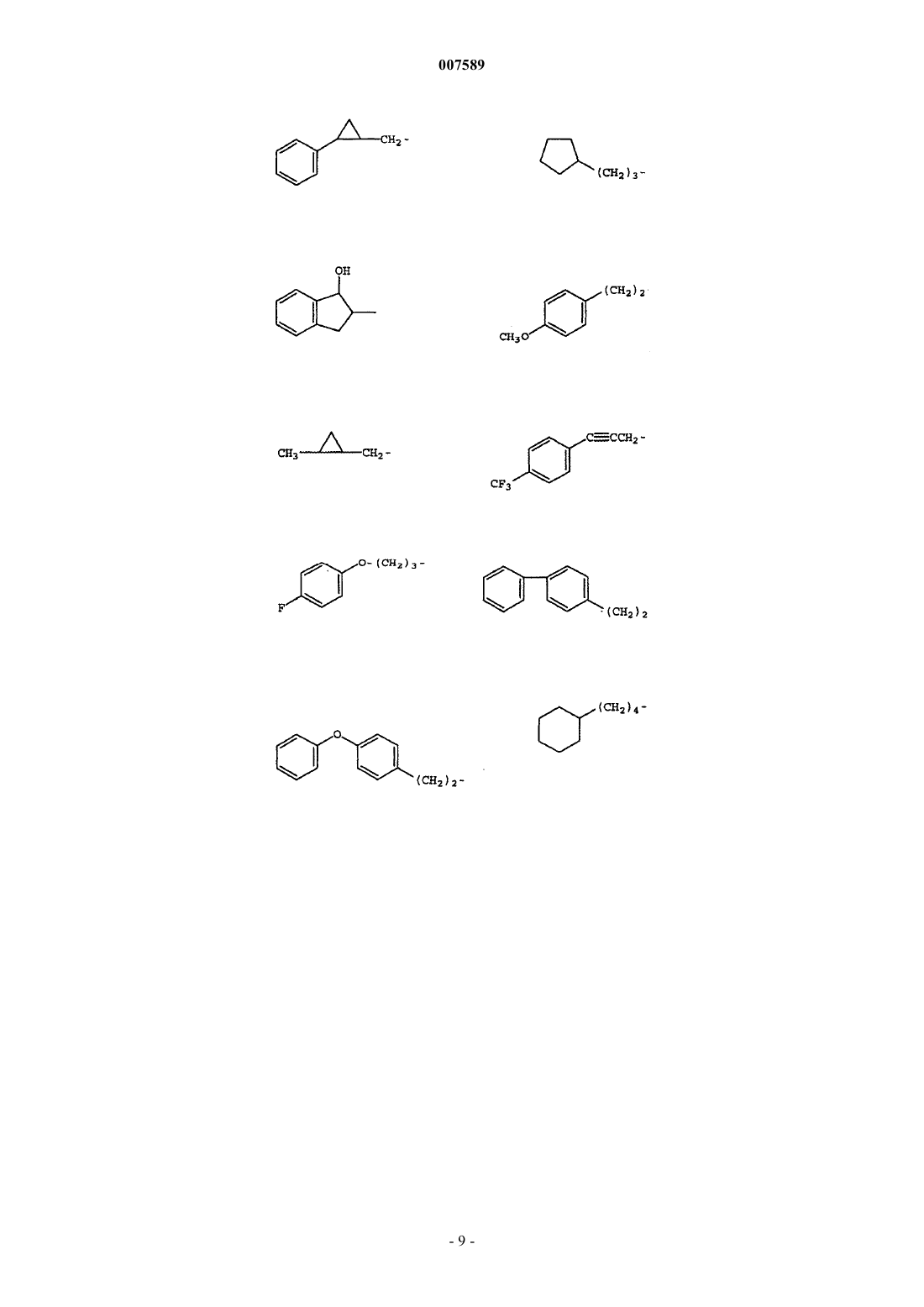
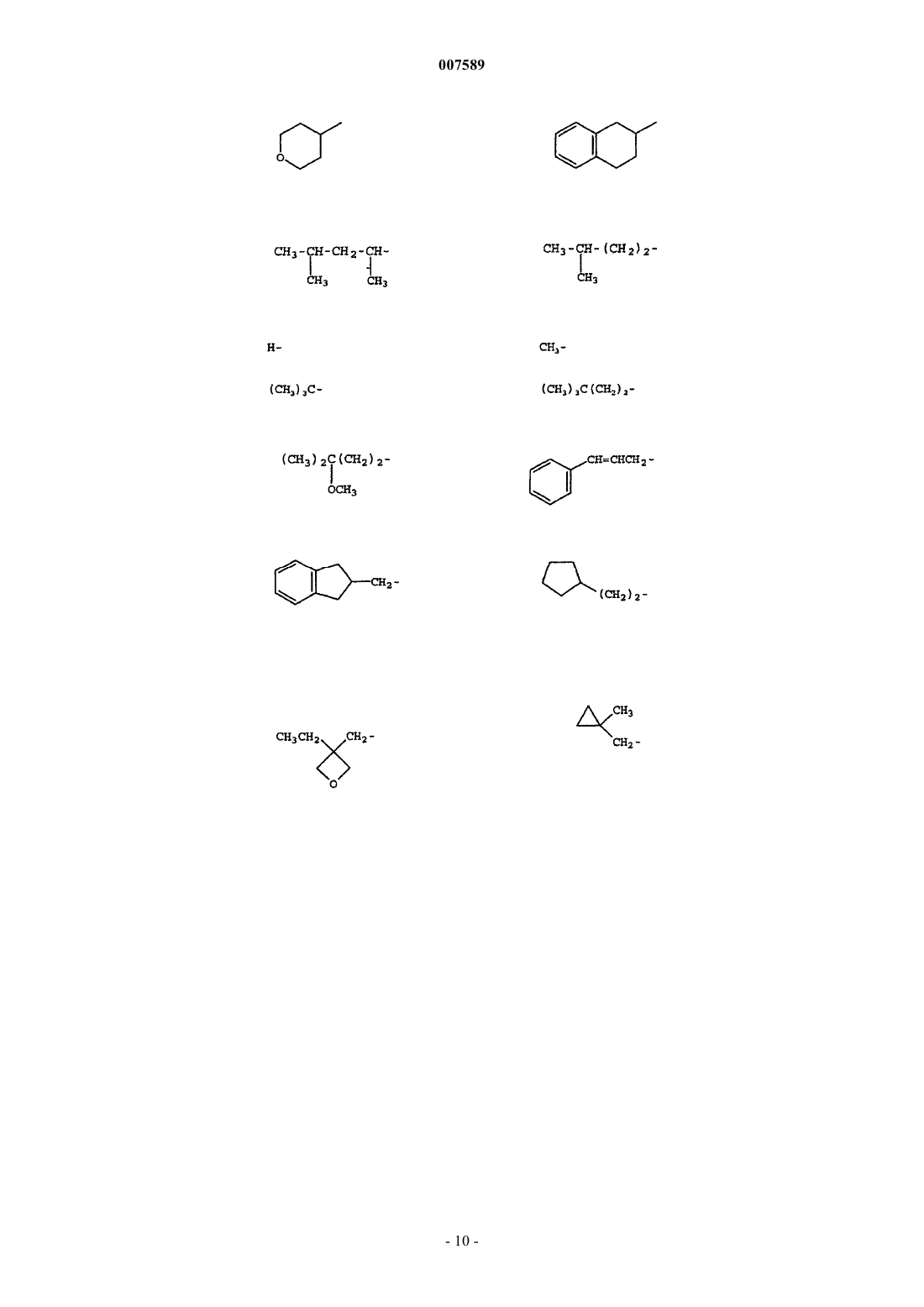
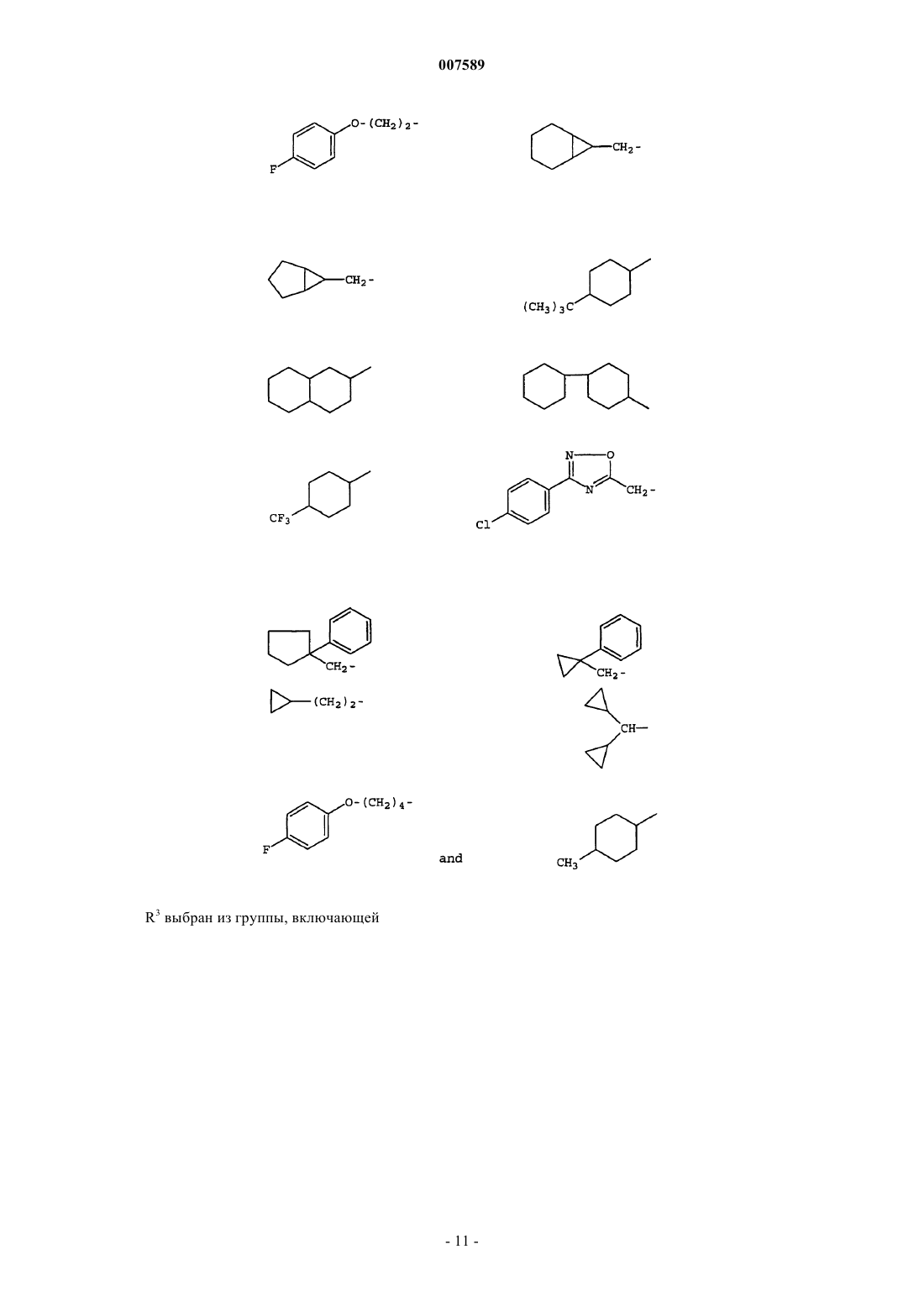
R1 представляет собой низший алкил, мостиковый алкил, арил, гетероарил, аралкил, циклоалкил, 5- или 6-членный насыщенный гетероцикл, С1-С4-алкиленарил, С1-С4-алкилен-O-арил, C1-C4-алкиленгетероарил, C1-C4-алкилен-Неt, С2-С4-алкиленарил-O-арил, C1-С4-алкилен-мостиковый алкил, C1-C3-алкиленциклоалкил, незамещенный или замещенный низшим алкилом или арилом пропаргил, незамещенный или замещенный арилом аллил или галогенциклоалкил;
R2 представляет собой водород, метил или галогензамещенный метил;
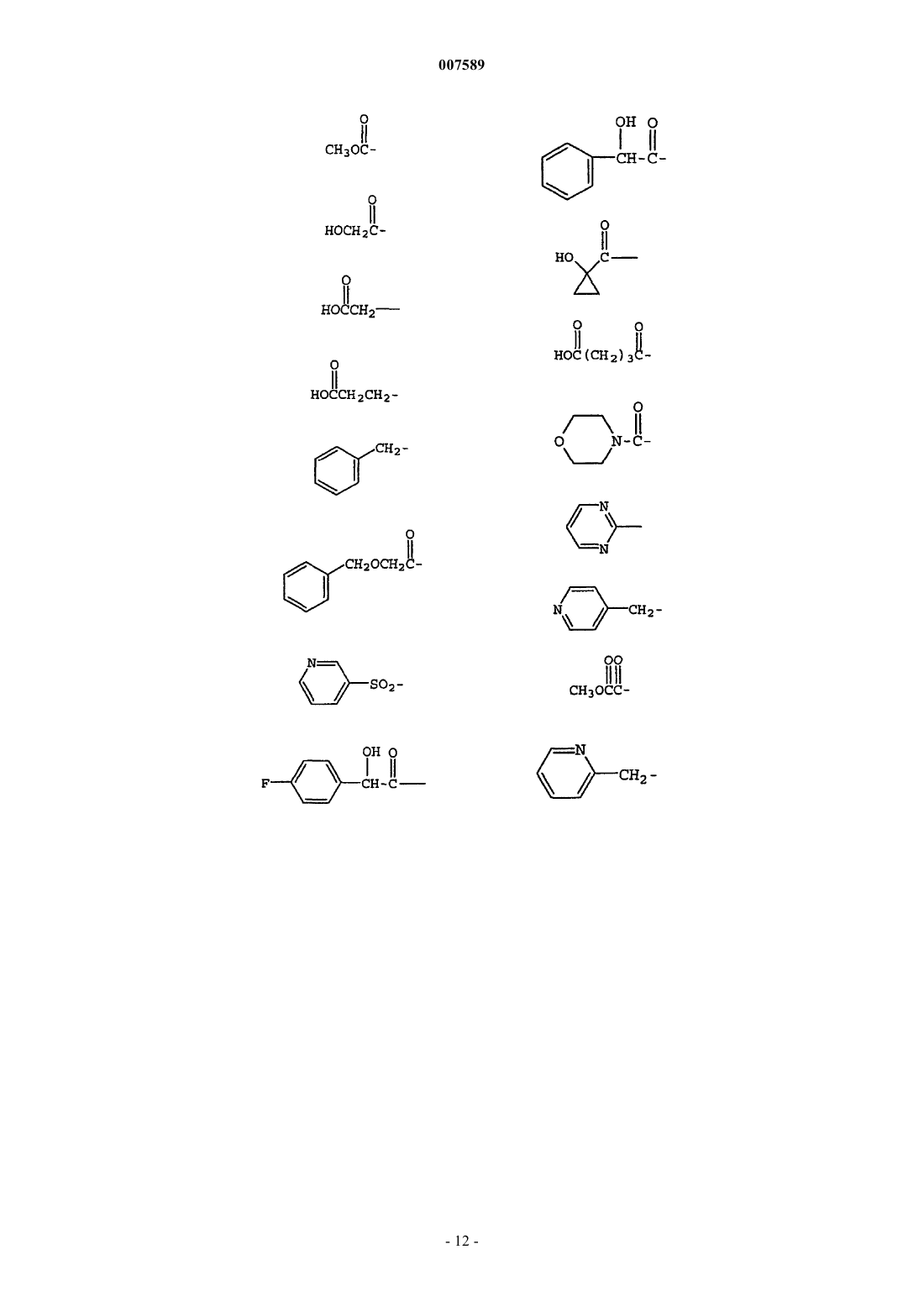
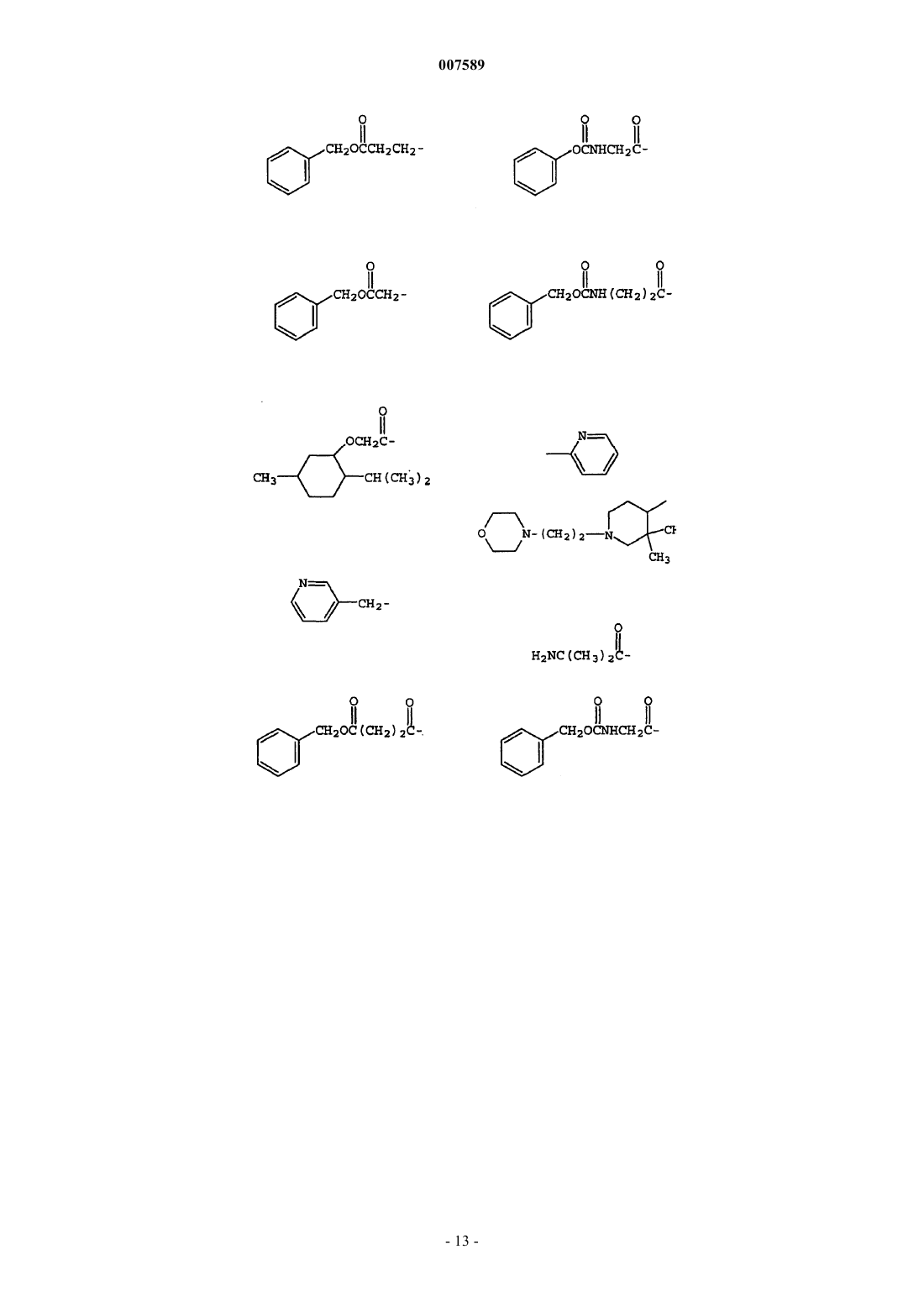
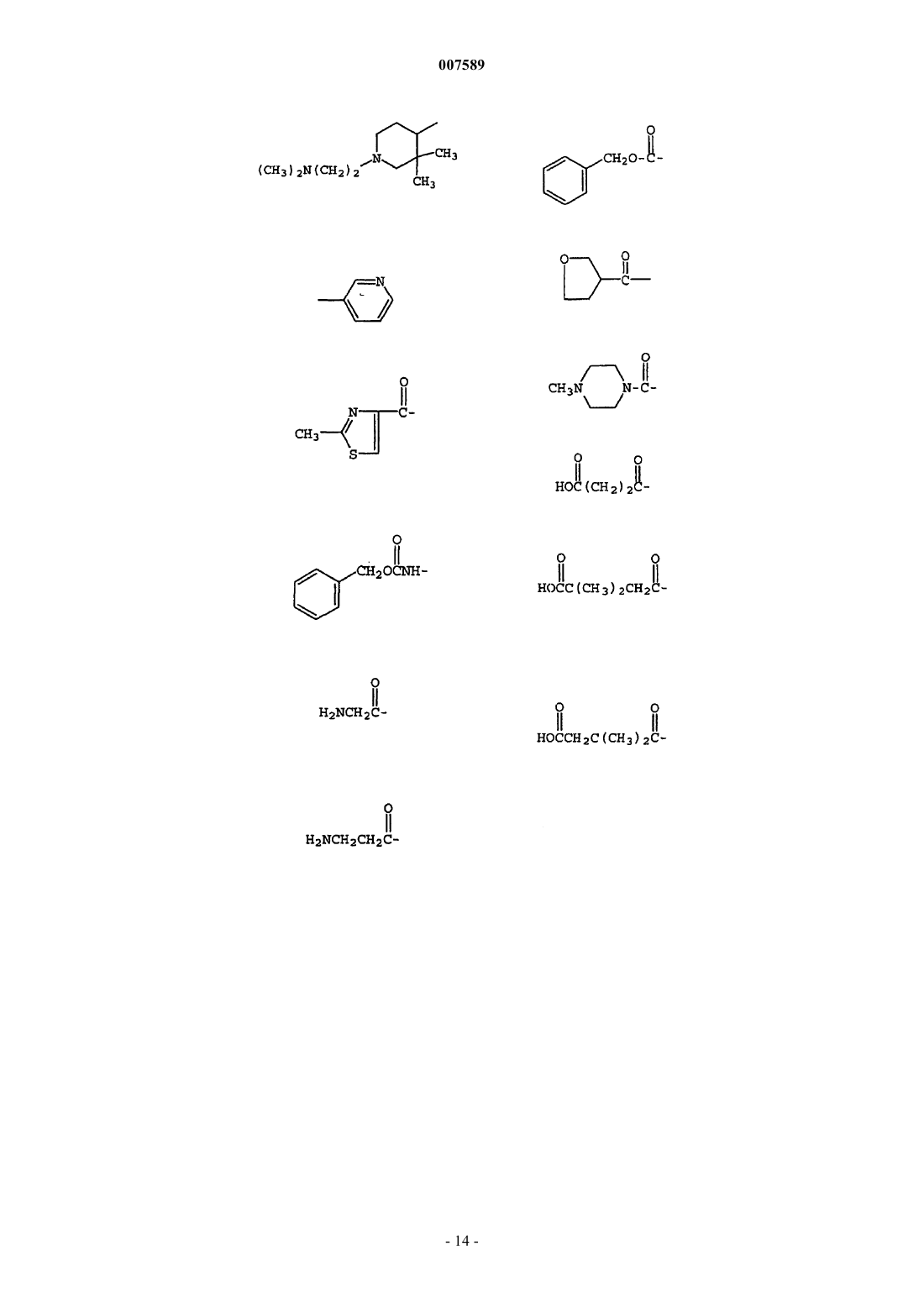
R3 выбирают из группы, состоящей из C(=O)OR7, C(=O)R7, C(=NH)NR8R9, C(=O)NR8R9, низшего алкила, мостикового алкила, циклоалкила, галогеналкила, галогенциклоалкила, C1-C3-алкиленциклоалкила, 5- или 6-членного насыщенного гетероцикла, арила, гетероарила, С1-С3-алкилен-С(=O)R7, C(=O)C(=O)NR8R9, C1-C4-алкилен-OR7, C1-C3-алкиленарила, SO2-гетероарила, Het, аралкила, алкарила, гетероаралкила, гетероалкарила, С1-С3-алкилен-С(=O)ОR7, С(=O)-С1-С3-алкилен-C(=O)OR7, C1-C3-алкиленгетероарил, C(=O)C(=O)OR7, С(=O)-С1-С3-алкилен-С(=O)OR7, C(=O)-C1-C3-алкилен-NH(C=O)OR7, С(=O)-С1-С3-алкилен-NН2 и NHC(=O)OR7;
R4 представляет собой водород, низший алкил, галогеналкил, циклоалкил или арил;
R5 представляет собой водород, низший алкил, алкинил, галогеналкил, циклоалкил или арил;
R6 и R12 представляют собой, независимо, водород, низший алкил, аралкил, SO2R11 или C(=O)R7;
R7 выбирают из группы, состоящей из разветвленного или неразветвленного низшего алкила, гетероарила, гетероцикла, аралкила и арила, и R7 может быть незамещенным или замещенным одним или несколькими OR8, NR8R9 или SR8;
R8 и R9, одинаковые или разные, выбирают из группы, состоящей из водорода, низшего алкила, циклоалкила, арила, гетероарила, алкарила, гетероаралкила, гетероалкарила и аралкила, или R8 и R9 могут вместе образовывать кольцо от 4-членного до 7-членного;
R10 представляет собой водород;
R11 представляет собой алкил, циклоалкил, трифторметил, арил, аралкил или NR8R9;
его соли и сольваты,
где низший алкил означает алкильную группу, имеющую от одного до шести атомов углерода;
мостиковый алкил означает бициклическую или полициклическую С6-С16-углеводородную группу;
арил означает моноциклическую или полициклическую ароматическую группу, предпочтительно моноциклическую или бициклическую ароматическую группу, которая может быть незамещенной или замещенной одним или более заместителями, выбираемыми из группы, состоящей из галогена, алкила, фенила, гидрокси, гидроксиалкила, алкокси, алкоксиалкила, галогеналкила, нитро, амино, алкиламино, ациламино, алкилтио, алкилсульфинила и алкилсульфонила;
аралкил означает алкильную группу, в которой один из водородных атомов замещен арильной группой;
циклоалкил означает циклическую С3-С7-углеводородную группу, возможно конденсированную с ароматической группой;
гетероарил выбирают из группы, включающей тиенил, фурил, пиридил, оксазолил, хинолил, изохинолил, индолил, триазолил, изотиазолил, изоксазолил, имидизолил, бензотиазолил, пиразинил, пиримидинил, тиазолил и тиадиазолил;
гетероцикл выбирают из группы, включающей тетрагидрофуран, пиперидин, пиперазин, сульфолан, морфолин, тетрагидропиран и диоксан.
2. Соединение по п.1, имеющее структуру
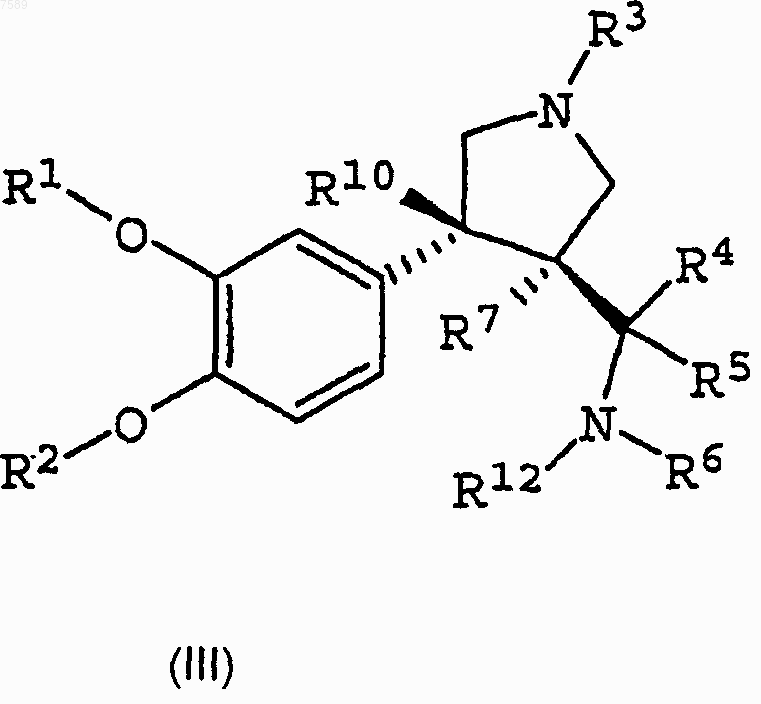
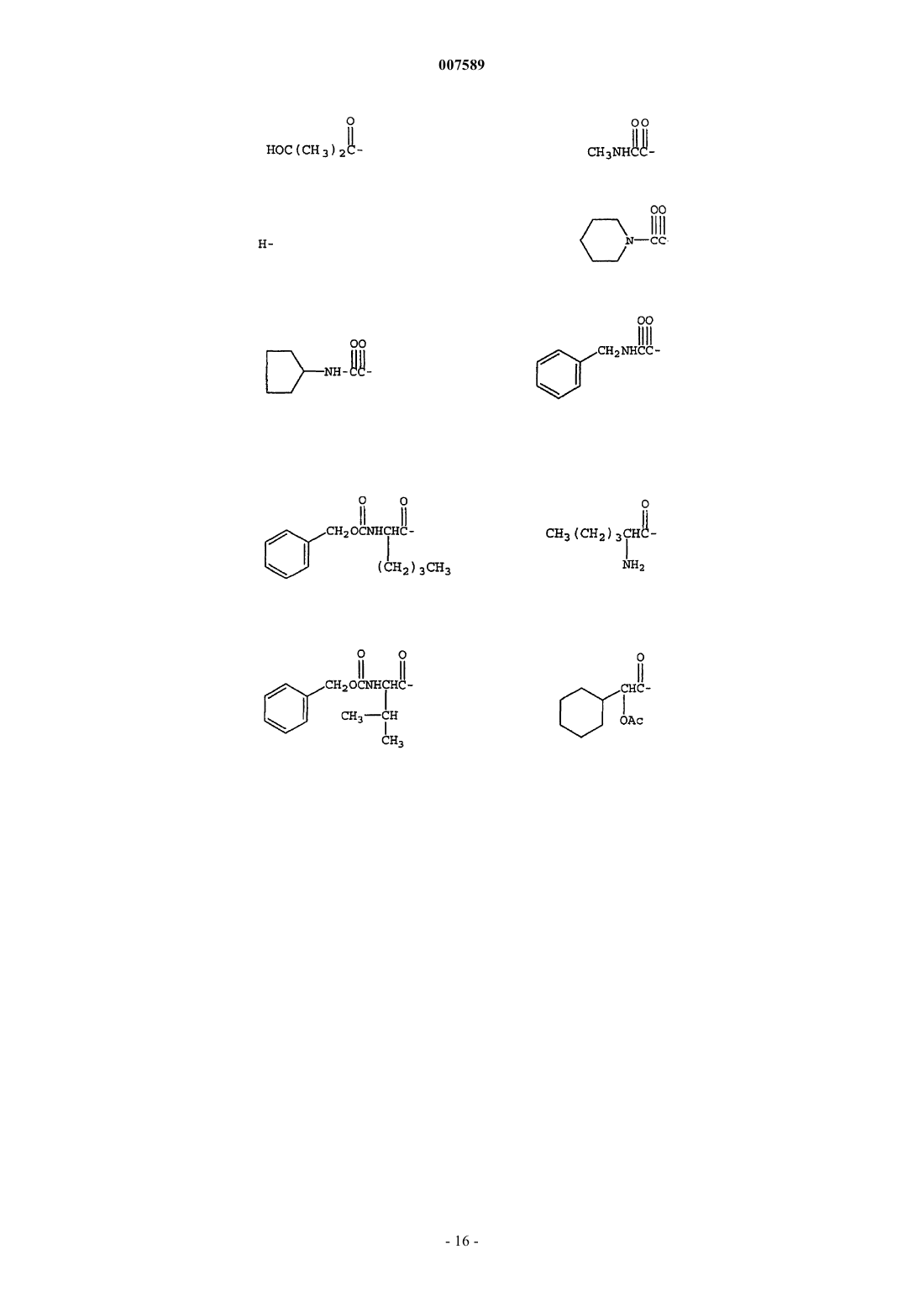
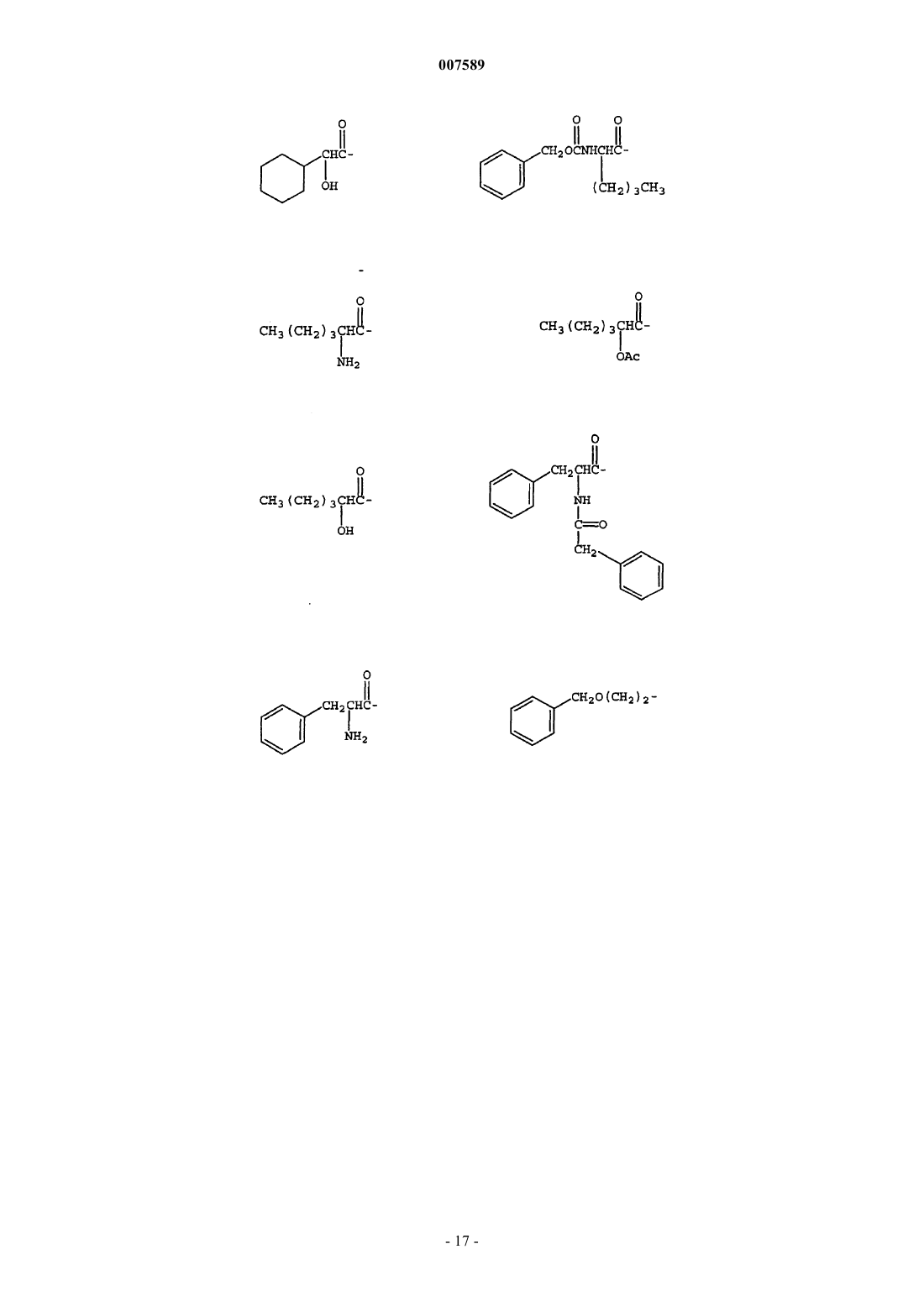
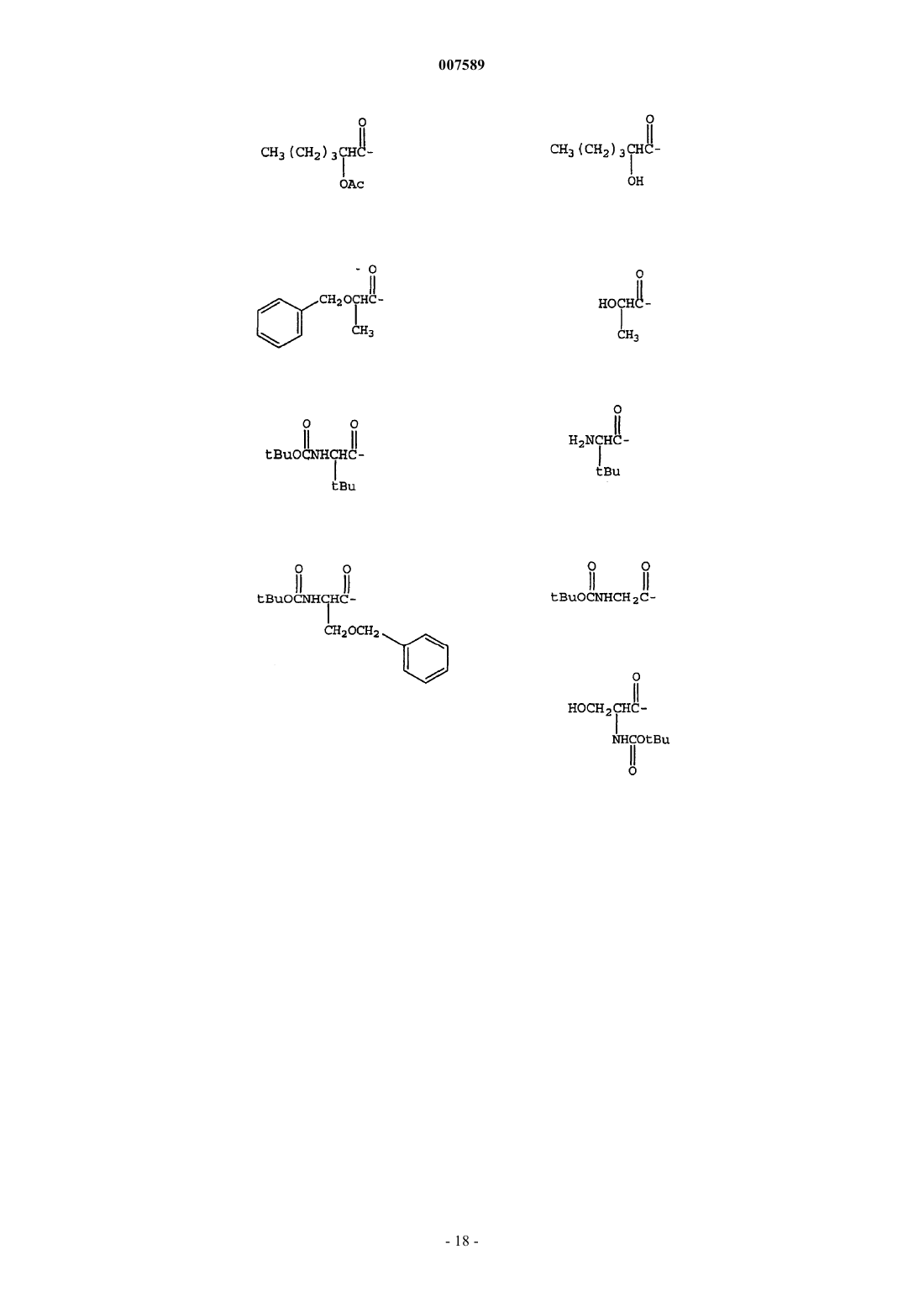
3. Соединение по п.1, где R1 выбран из группы, включающей
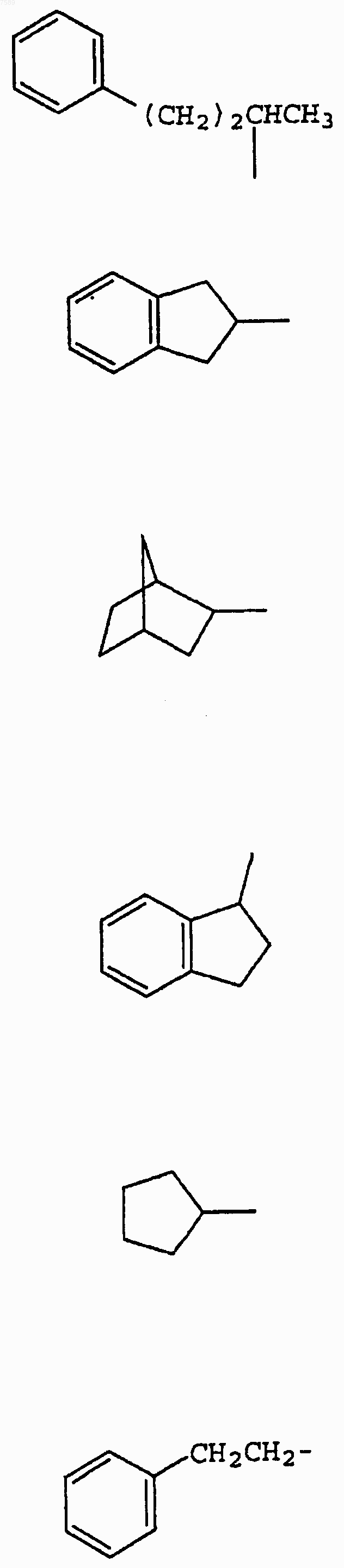
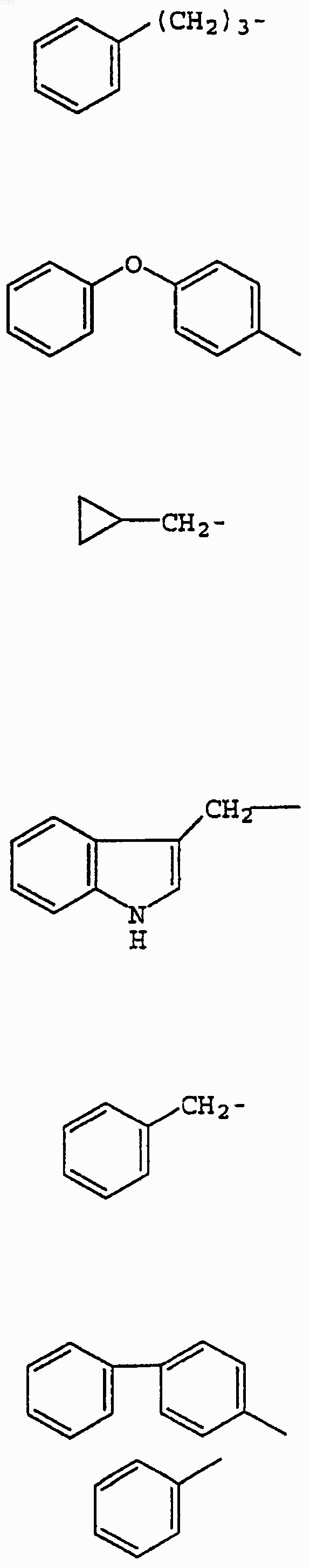
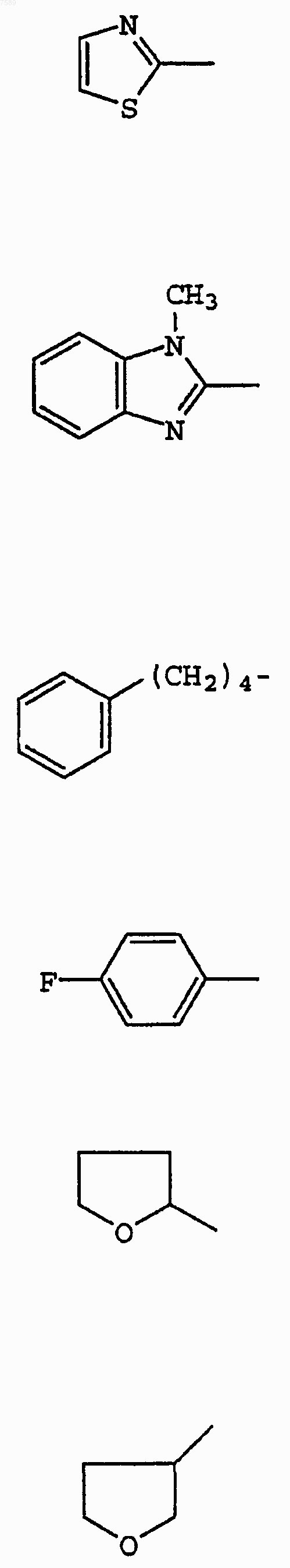
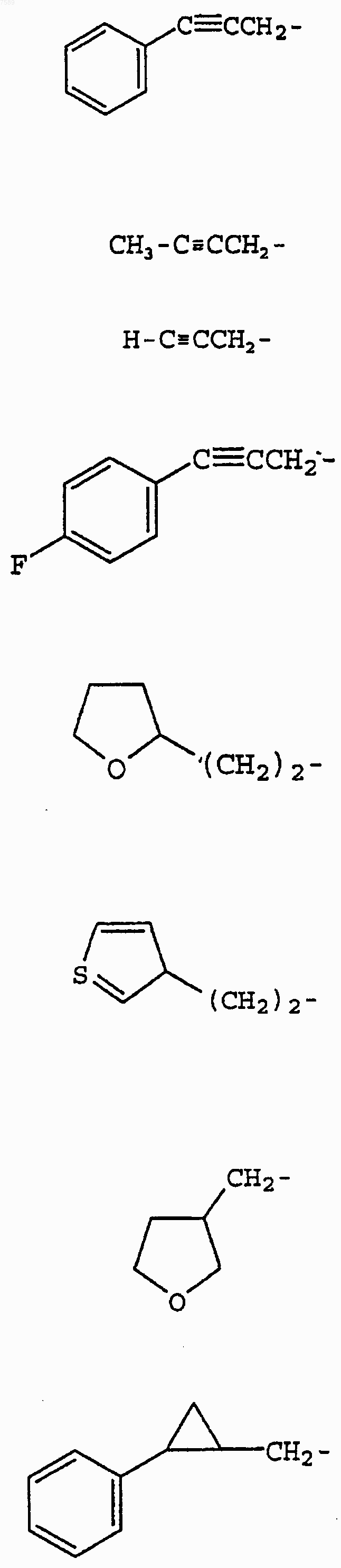
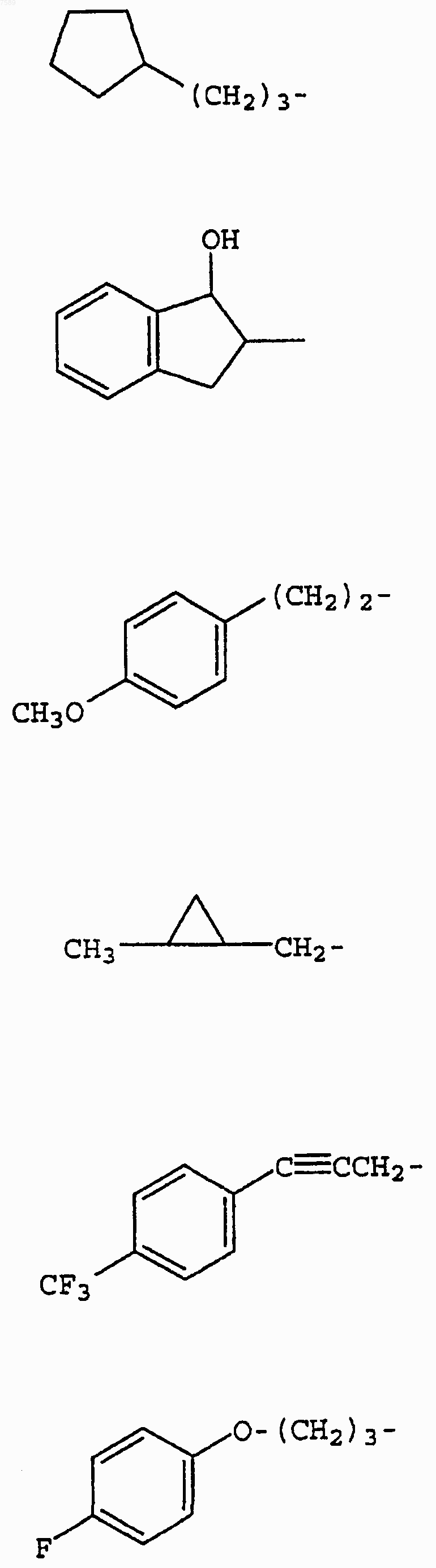
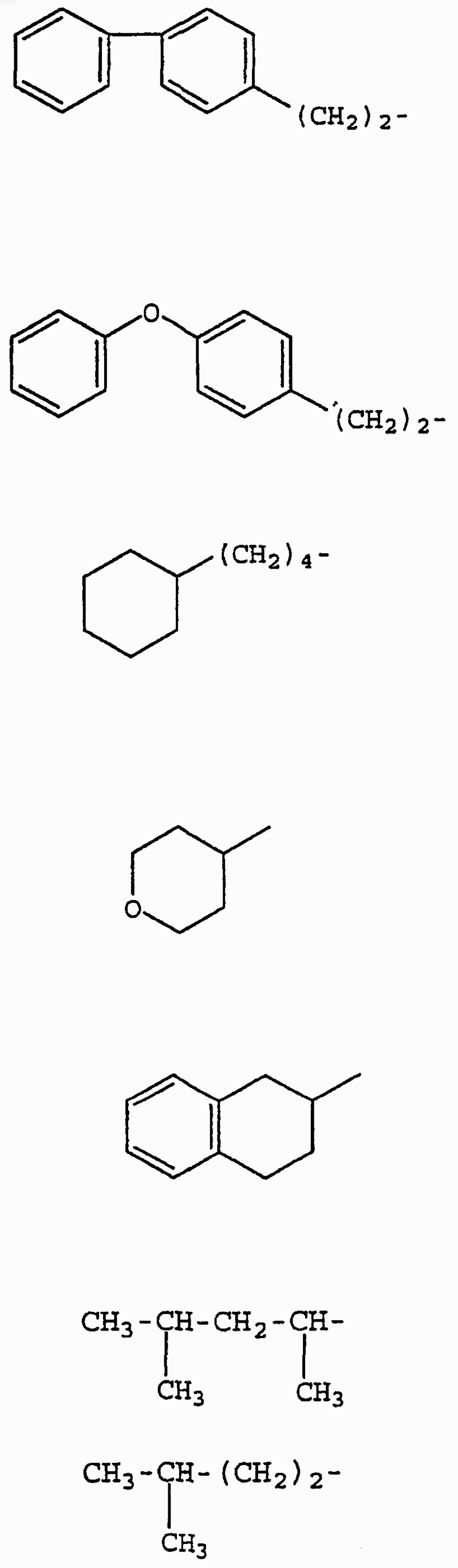
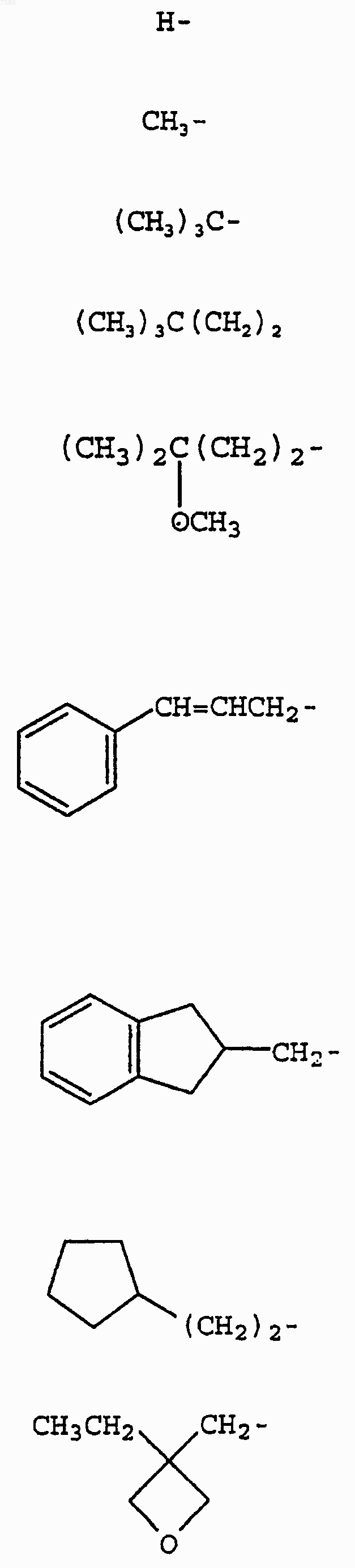
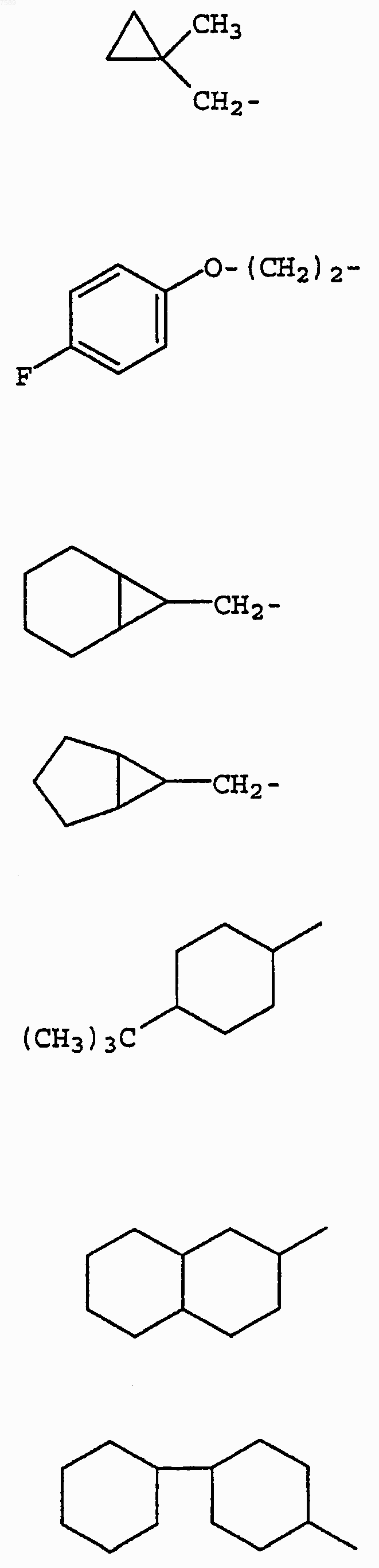
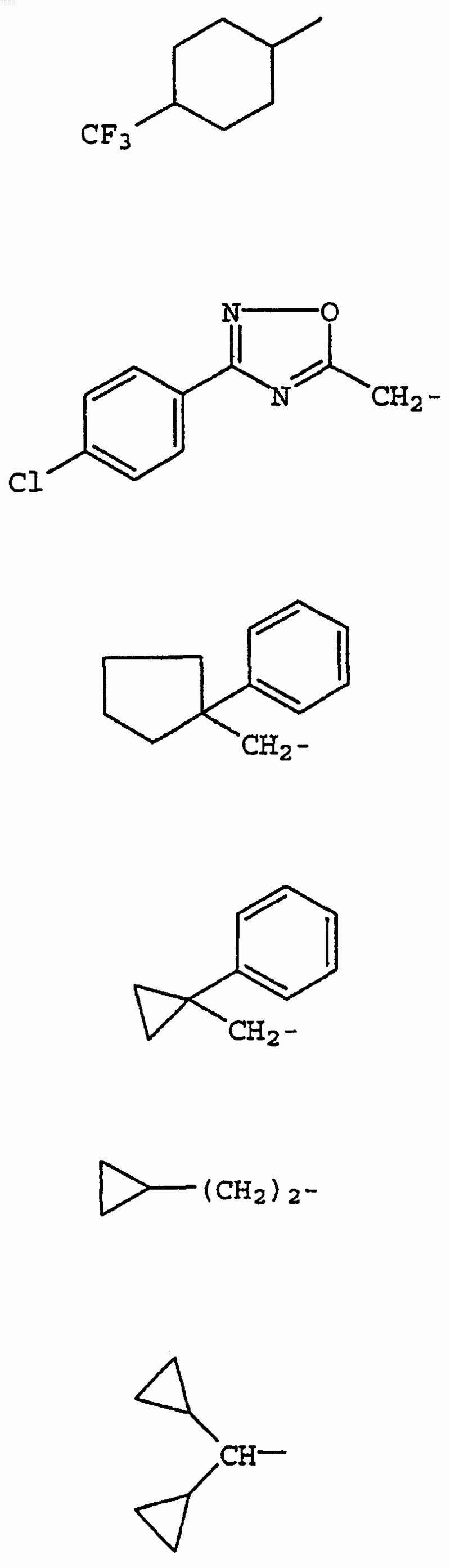
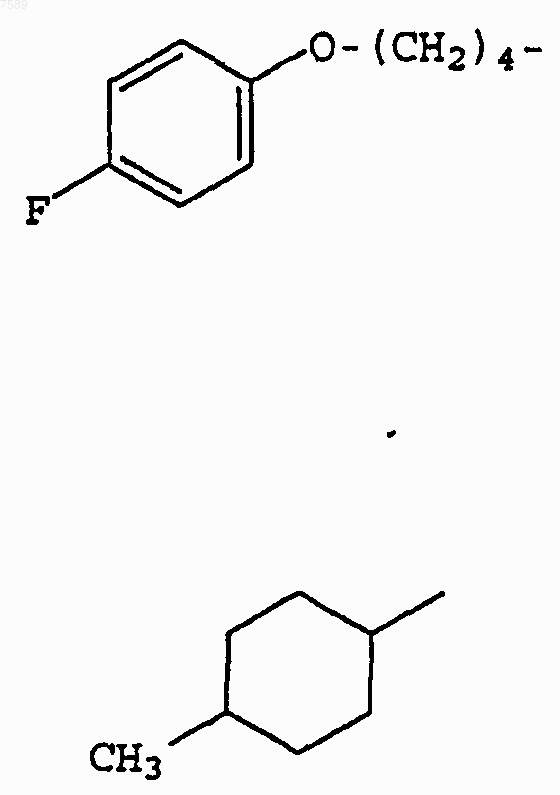
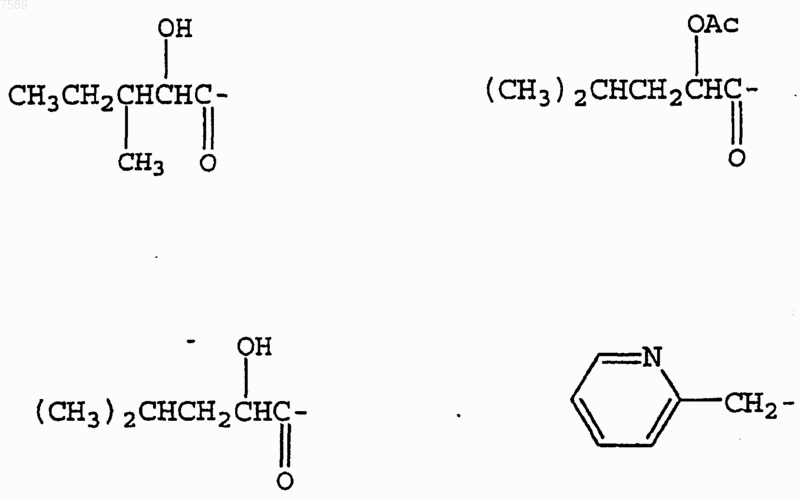
4. Соединение по п.1, где R3 выбран из группы, включающей
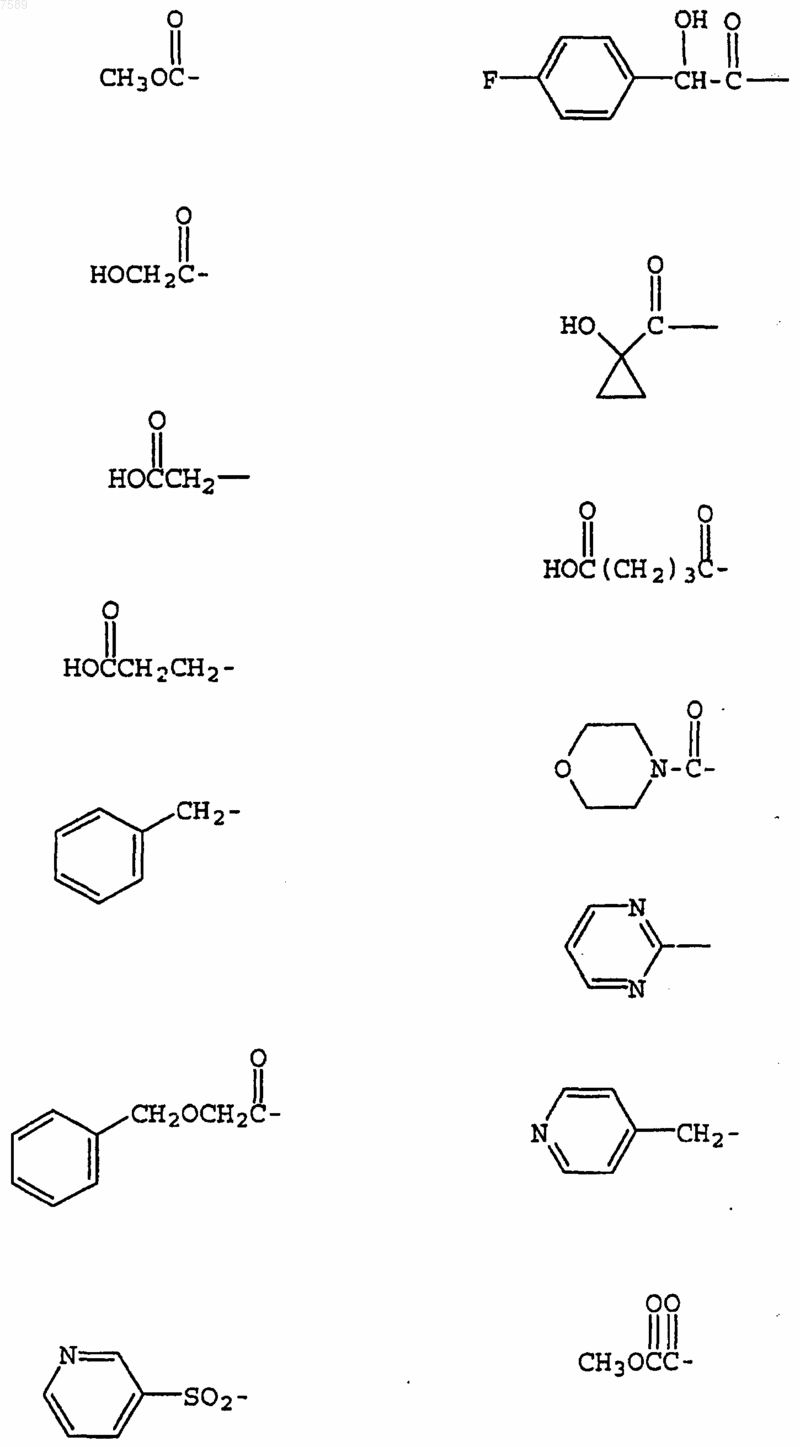
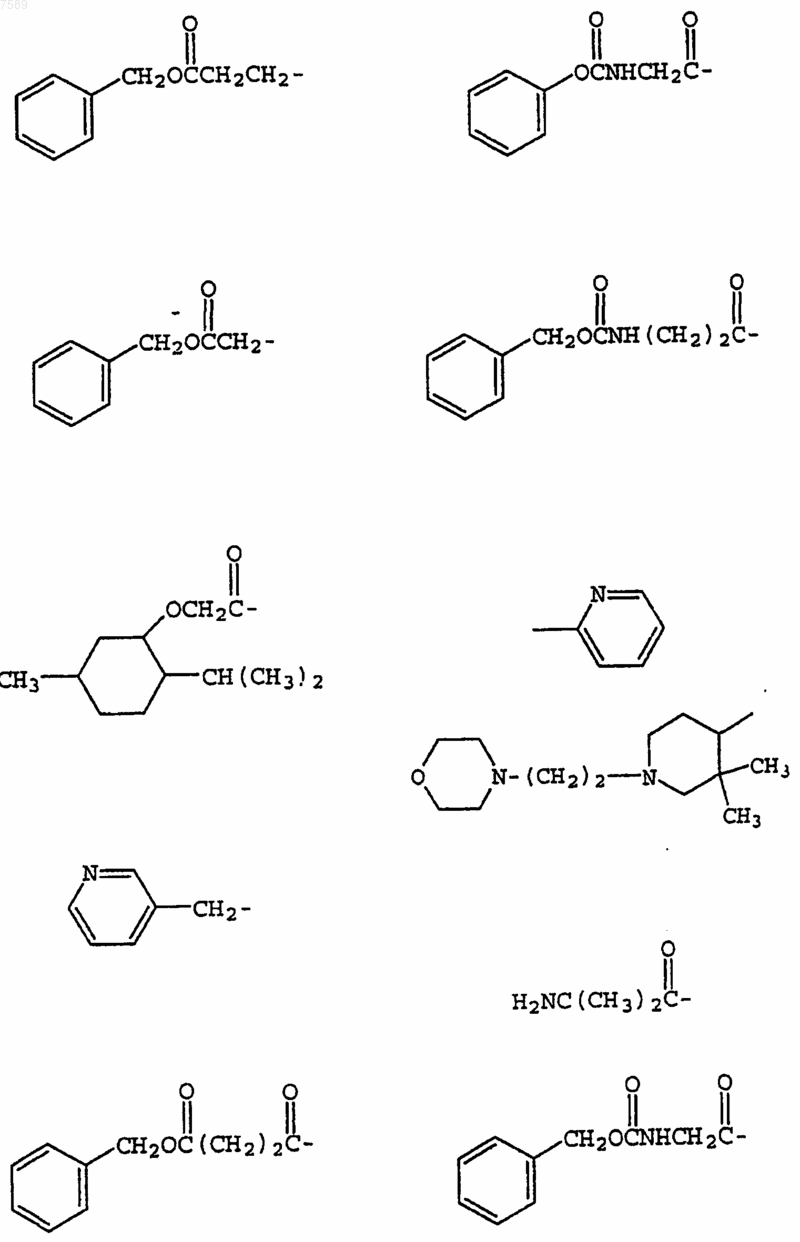
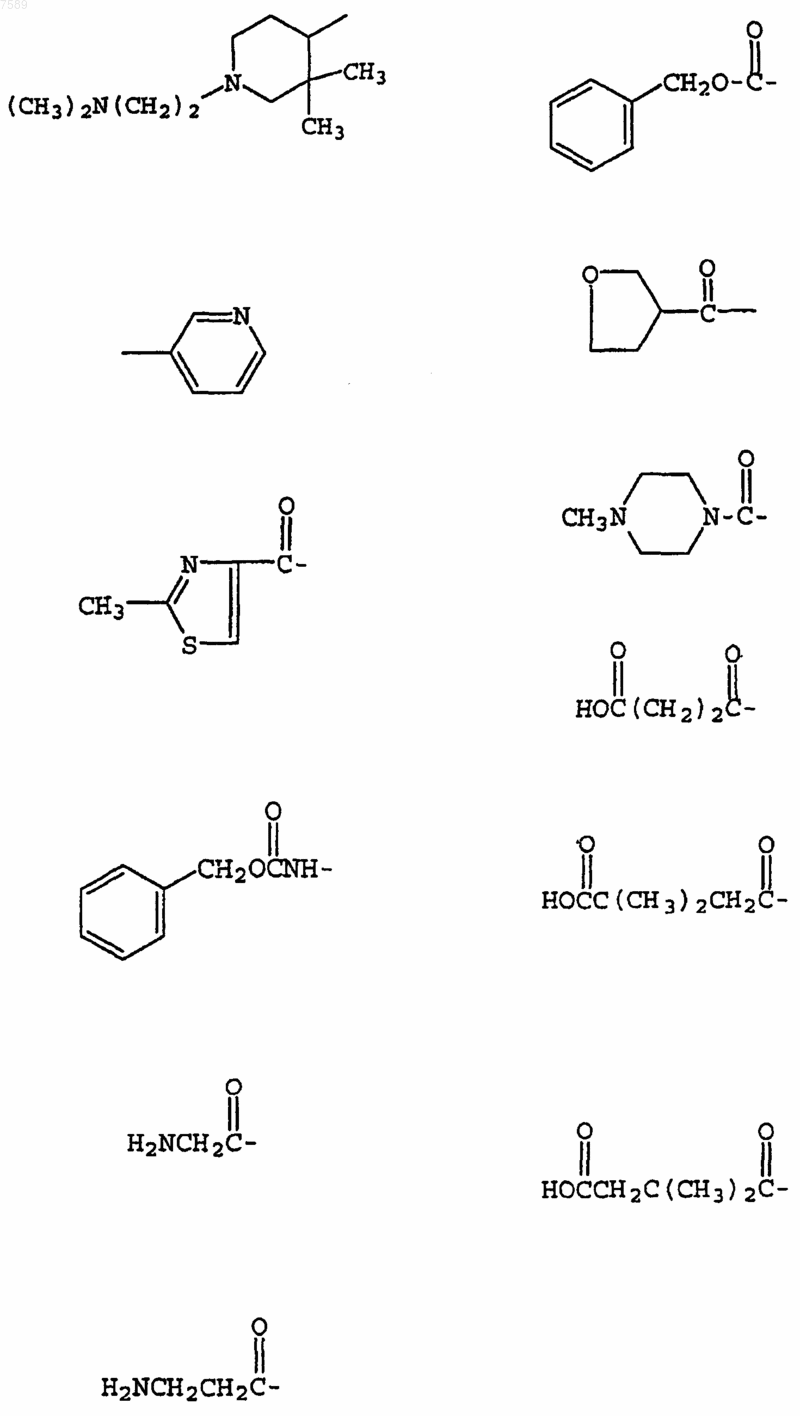
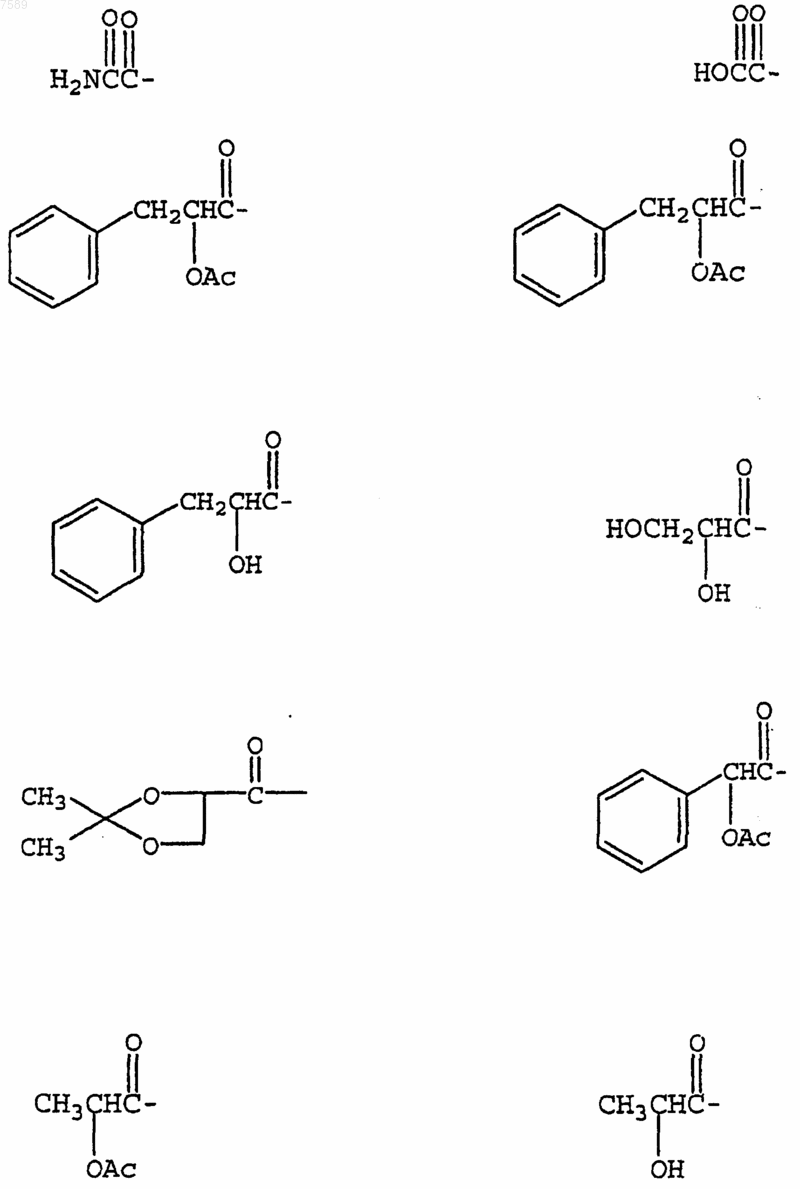
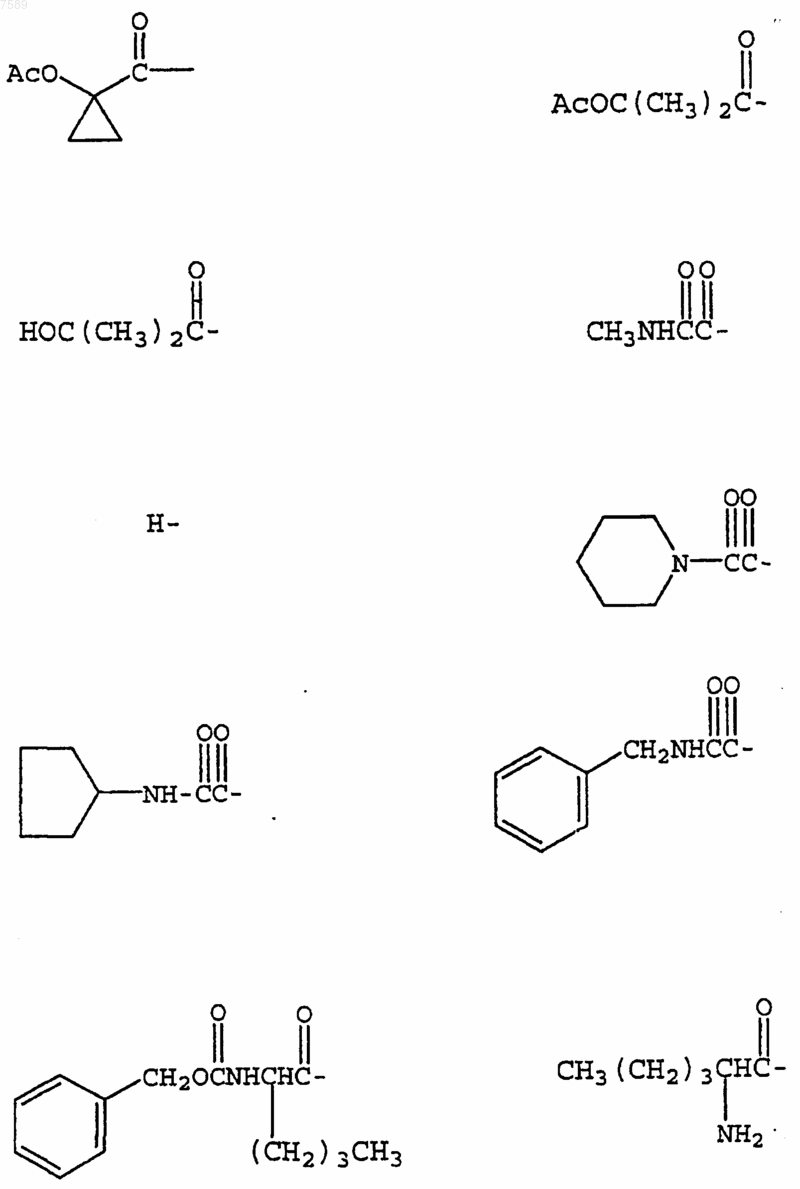
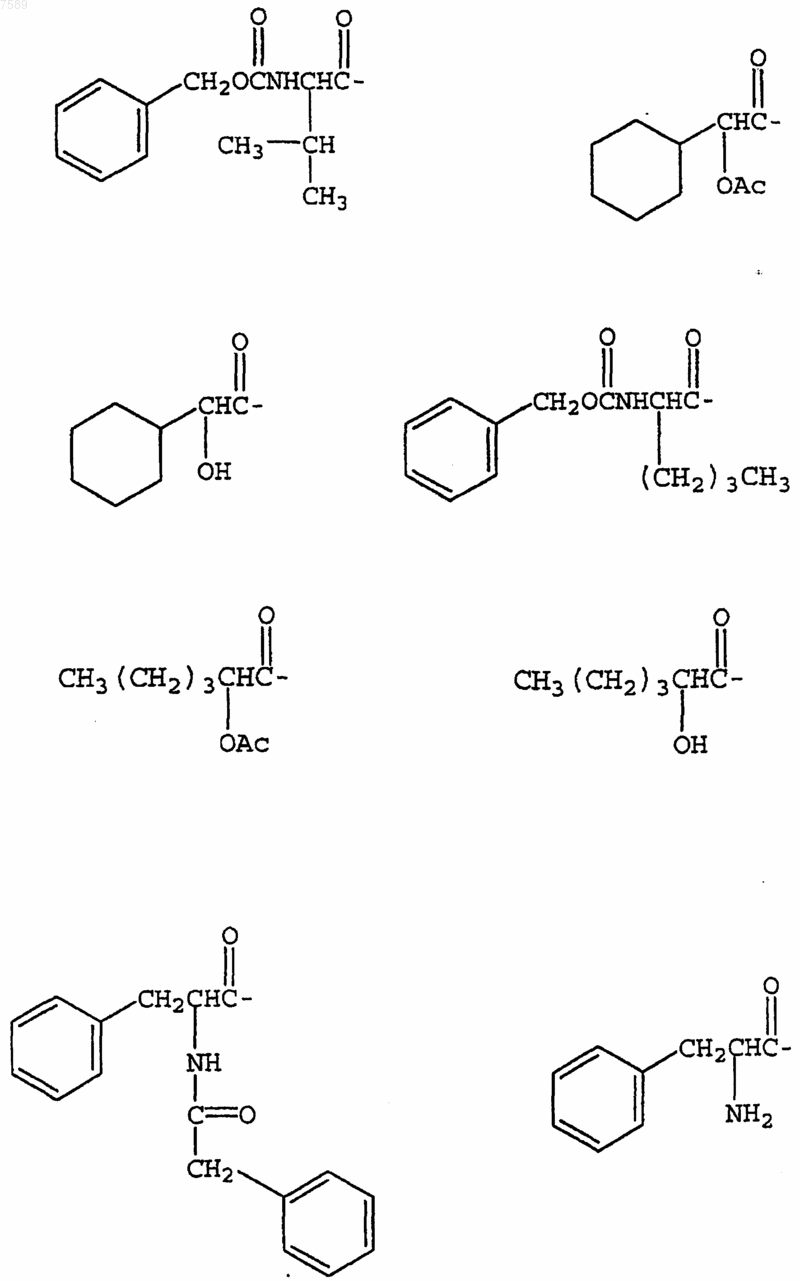
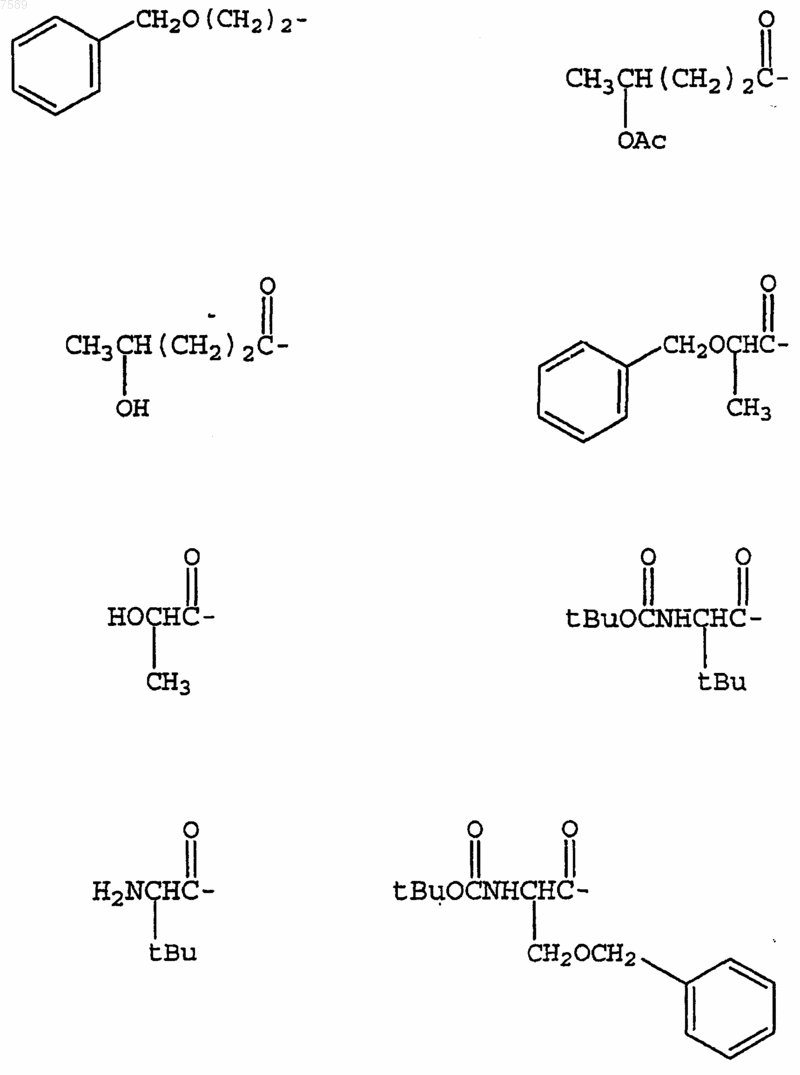
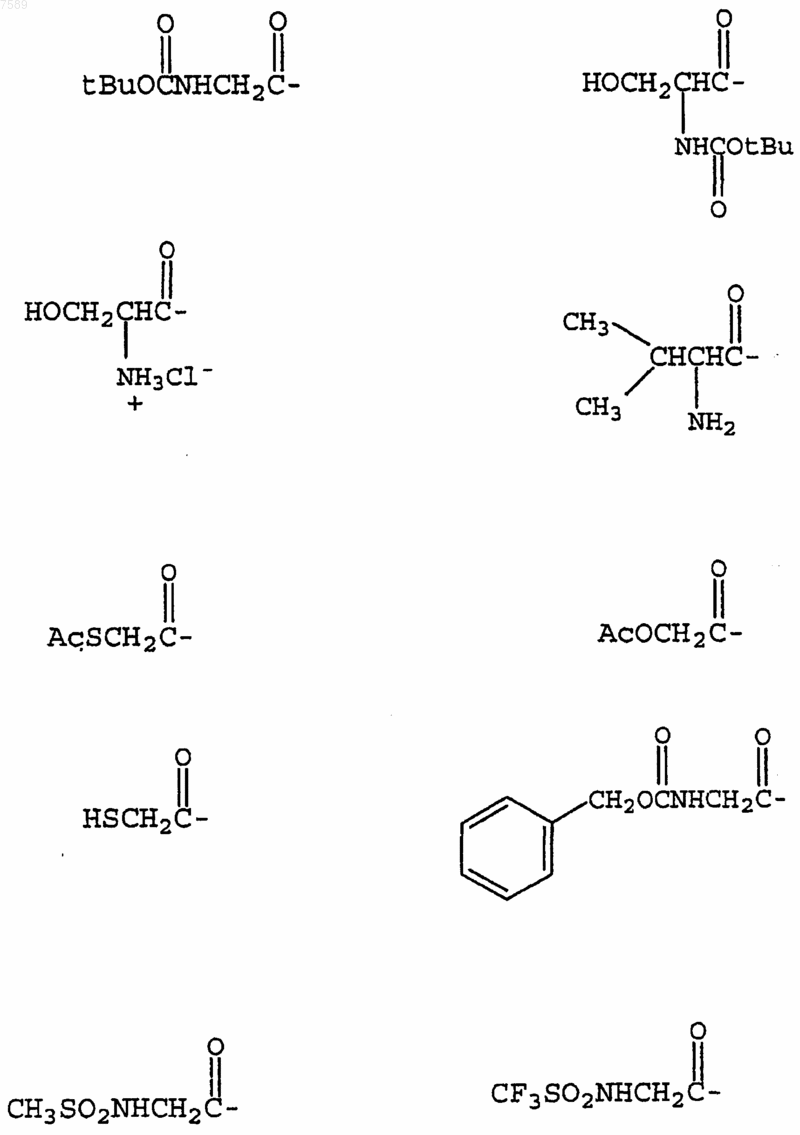
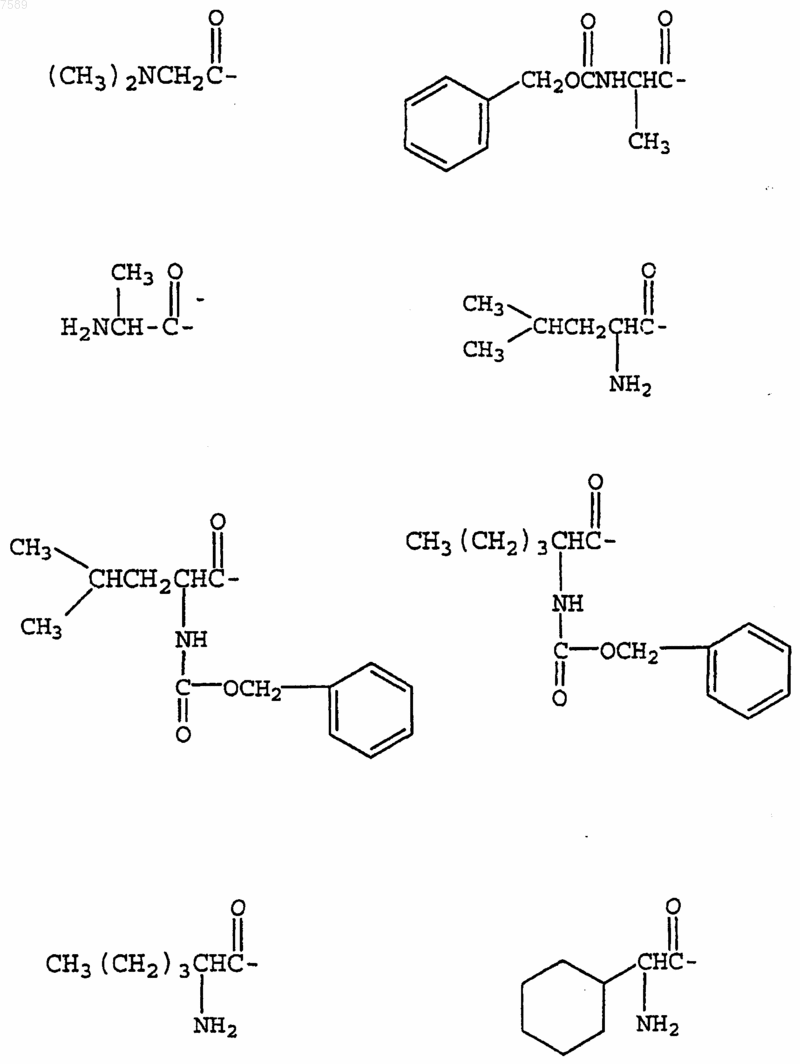
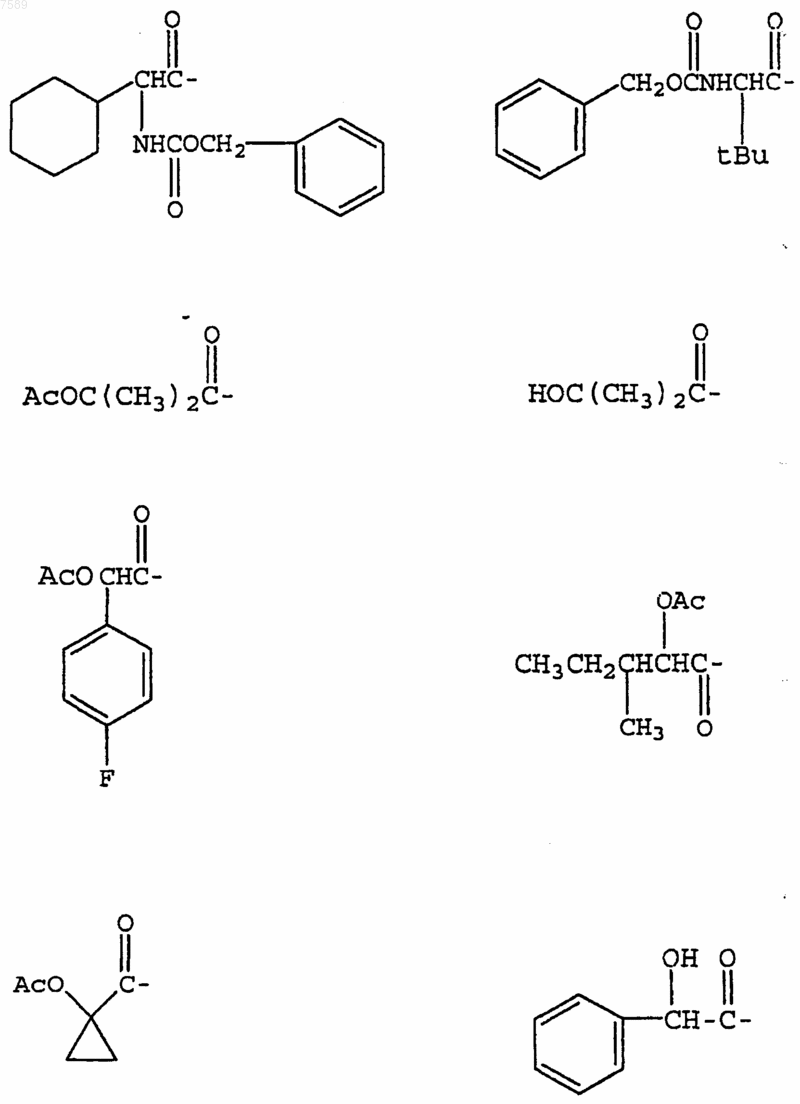
5. Соединение по п.1, где R4 выбран из группы, включающей водород, метил, трифторметил, циклопропил, этинил и фенил.
6. Соединение по п.1, где R5 означает водород или низший алкил.
7. Соединение по п.1, где R6 выбран из группы, включающей водород, C(=O)R7, С(=O)OR7этил, бензил, SO2CH3 и SO2C6H5.
8. Соединение по п.1, где R7 означает низший алкил.
9. Соединение по п.1, где R8 и R9 независимо означают водород или низший алкил или вместе образуют 5-членное или 6-членное кольцо.
10. Соединение по п.1, где R12 выбран из группы, включающей водород и низший алкил.
11. Соединение по п.1, где R1 выбран из группы, включающей циклопентил, циклопропилметил, тетрагидрофурил, инданил, норборнил, фенитил и фенилбутил; R2 выбран из группы, включающей метил и дифторметил; R3 выбран из группы, включающей бензил, СO2СН3, С(=O)СН2ОН, С(=O)СН(СН3)ОН, С(=O)С(СН3)2ОН и
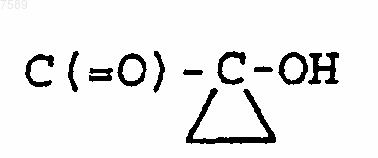
R4 означает водород; R5 означает водород или метил; R6 выбран из группы, включающей водород, метил, этил, бензоил, SO2CH3, SO2С6Н5, бензил, С(=O)С(СН3)3 и ацетил; R12 означает водород или метил; R7 означает метил; и R10 означает водород.
12. Соединение по п.1, выбранное из группы, включающей
метил(4S,3R)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-3-{[бензиламино]метил}пирролидинкарбоксилат;
метил(4S,3R)-3-(аминометил)-4-(3-циклопентилокси-4-метоксифенил)-3-метилпирролидинкарбоксилат;
метил(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-3-{[(метилсульфонил)амино]метил}пирролидинкарбоксилат;
метил(4S,3R)-3-[(ацетиламино)метил]-4-(3-циклопентилокси-4-метоксифенил)-3-метилпирролидин-карбоксилат;
метил(4S,3R)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-3-[(фенилкарбониламино)метил]пирролидинкарбоксилат;
метил(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-3-{[(фенилсульфонил)амино]метил}пирролидинкарбоксилат;
бис{[(4S,3R)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1-карбоксиметилпирролидин-3-ил]метил}амин;
1-[(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1-бензилпирролидин-3-ил]этиламин;
N-{1-[(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1-бензилпирролидин-3-ил]этил}бензамид;
N-{1-[(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1-бензилпирролидин-3-ил]этил}ацетамид;
метиловый эфир 3-(S)-(1-ацетиламиноэтил)-4-(S)-(3-циклопентилокси-4-метоксифенил)-3-метил-пирролидин-1-карбоновой кислоты;
{1-[(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1-бензилпирролидин-3-ил]этил}(фенилсульфонил)амин;
{1-[(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1-бензилпирролидин-3-ил]этил}(метилсульфонил)амин; и
метил(3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-3-(метиламино)этилпирролидин-карбоксилат.
13. Соединение по п.1, выбранное из группы, включающей
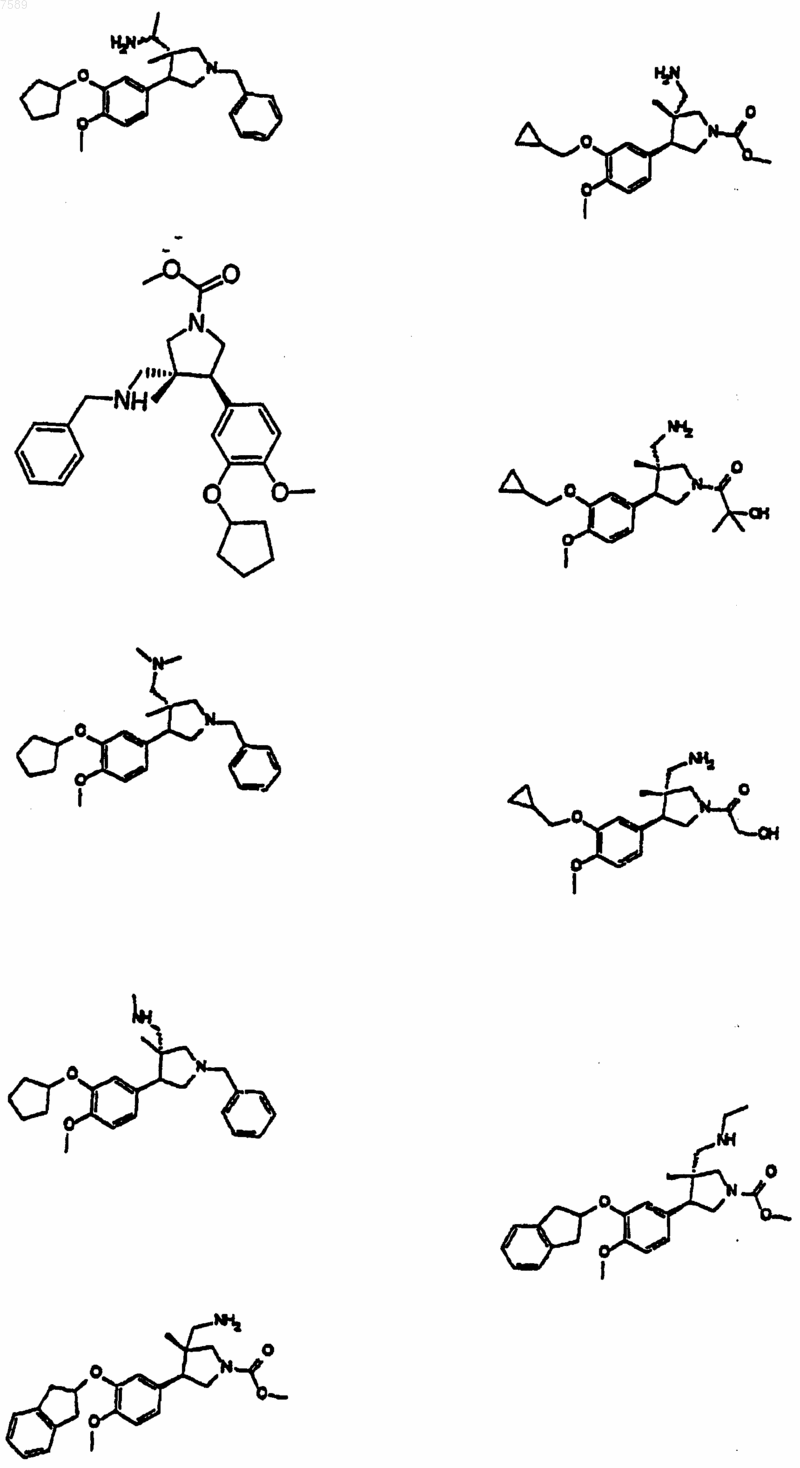
14. Соединение по п.1, имеющее IC50 относительно рекомбинантной PDE4 человека приблизительно от 1 нМ до приблизительно 25 мкМ.
15. Соединение по п.1, имеющее ЕС50 PBL/TNFa приблизительно от 10 нМ до приблизительно 20 мкМ.
16. Соединение по п.1, имеющее IC50 относительно рекомбинантной PDE4 человека приблизительно от 1 нМ до приблизительно 25 мкМ и ЕС50 PBL/TNFa приблизительно от 10 нМ до приблизительно 25 мкМ.
17. Соединение по п.1, имеющее IC50 относительно рекомбинантной PDE4 человека приблизительно от 100_10-6 М или менее.
18. Соединение по п.1, имеющее IC50 относительно рекомбинантной PDE4 человека приблизительно от 50_10-6 М или менее.
19. Соединение по п.1, имеющее ЕС50 PBL/TNFa приблизительно от 5 мкМ или менее.
20.Соединение по п.1, имеющее ЕС50 PBL/TNFa приблизительно от 2 мкМ или менее.
21. Соединение по п.1, имеющее IC50 относительно рекомбинантной PDE4 человека приблизительно от 100_10-6 или менее и ЕС50 PBL/TNFa приблизительно от 5 мкМ или менее.
22. Соединение по п.1, имеющее IC50 относительно рекомбинантной PDE4 человека приблизительно от 50_10-6 или менее и ЕС50 PBL/TNFa приблизительно от 2 мкМ или менее.
23. Фармацевтическая композиция, содержащая соединение по п.1, фармацевтически приемлемый носитель и, возможно, второй противовоспалительный терапевтический агент.
24. Композиция по п.23, отличающаяся тем, что мишенью для второго противовоспалительного терапевтического агента является TNFa.
25. Способ лечения млекопитающего в состоянии, когда ингибирование цАМФ-специфичной PDE является терапевтически полезным, предусматривающий введение указанному млекопитающему терапевтически эффективного количества соединения по п.1.
26. Способ модулирования уровней цАМФ у млекопитающего, предусматривающий введение указанному млекопитающему эффективного количества соединения по п.1.
27. Способ лечения млекопитающего в состоянии, когда ингибирование цАМФ-специфичной PDE является терапевтически полезным, предусматривающий введение млекопитающему эффективного количества фармацевтической композиции, содержащей соединение по п.1 и фармацевтически приемлемый носитель.
28. Способ по п.27, отличающийся тем, что состояние млекопитающего означает аллергическое заболевание, аутоиммунное заболевание, воспалительное заболевание, воспалительное заболевание или дерматит.
29. Способ по п.27, отличающийся тем, что состояние означает ревматоидный артрит, остеоартрит, подагрический артрит или спондилит.
30. Способ по п.27, отличающийся тем, что состояние млекопитающего означает тироид-ассоциированную офтальмопатию, болезнь Бехчета, сепсис, септический шок, эндотоксиновый бактериально-токсический шок, грамотрицательный сепсис, грамположительный сепсис, синдром токсического шока, аллергический конъюнктивит, весенний конъюнктивит или эозинофильную гранулему.
31. Способ по п.27, отличающийся тем, что состояние млекопитающего означает астму, хронический бронхит, аллергический ринит, респираторный дистресс-синдром взрослых, хроническое легочное воспалительное заболевание, хроническое закупоривающее легочное заболевание, силикоз или легочный саркоидоз.
32. Способ по п.27, отличающийся тем, что состояние млекопитающего означает реперфузионное повреждение миокарда, головного мозга или конечностей, например, повреждение головного или спинного мозга из-за травмы.
33. Способ по п.27, отличающийся тем, что состояние млекопитающего означает фиброз, келоидное образование или образование тканевого рубца.
34. Способ по п.27, отличающийся тем, что состояние млекопитающего означает системную красную волчанку, нарушение, являющееся отторжением трансплантата, гомологичную болезнь или отторжение аллотрансплантата.
35. Способ по п.27, отличающийся тем, что состояние млекопитающего означает хронический гломерулонефрит, воспалительное заболевание кишечника, болезнь Крона или язвенный колит.
36. Способ по п.27, отличающийся тем, что состояние млекопитающего означает пролиферативное лейкоцитарное заболевание или лейкоз.
37. Способ по п.27, отличающийся тем, что состояние млекопитающего означает воспалительный дерматоз, атопический дерматит, псориаз или крапивницу.
38. Способ по п.27, отличающийся тем, что состояние млекопитающего означает кардиомиопатию, застойную сердечную недостаточность, атеросклероз, гипертермию, кахексию, кахексию, вторичную к инфекции или злокачественности, кахексию, вторичную к синдрому приобретенного иммунного дефицита, ARC (спид-ассоциированный комплекс), церебральную малярию, остеопороз, заболевания типа резорбции костей, лихорадку и миалгию вследствие инфекции, эректильную дисфункцию, несахарный диабет, нарушение центральной нервной системы, депрессию, полиинфарктную деменцию, состояние страха и ответную реакцию на стресс, церебральную ишемию, позднюю дискинезию, болезнь Паркинсона или пременструальный синдром.
39. Способ по п.27, отличающийся тем, что млекопитающее показывает минимальную ответную рвотную реакцию.
40. Способ по п.27, отличающийся тем, что млекопитающее не показывает ответную рвотную реакцию.
41. Способ по п.27, отличающийся тем, что млекопитающее показывает минимальные неблагоприятные побочные воздействия на центральную нервную систему.
42. Способ по п.27, отличающийся тем, что млекопитающее не показывает неблагоприятные побочные воздействия на центральную нервную систему.
43. Способ уменьшения уровней TNF у млекопитающего, предусматривающий введение указанному млекопитающему терапевтически эффективного количества соединения по п.1.
44. Способ подавления активации воспалительной клетки млекопитающего, предусматривающий введение указанному млекопитающему терапевтически эффективного количества соединения по п.1.
45. Способ ингибирования функции PDE4 у млекопитающего, предусматривающий введение указанному млекопитающему терапевтически эффективного количества соединения по п.1.
Текст
007589 Перекрестная ссылка к родственной заявке Данная заявка подтверждает эффект предварительной заявки 60/172023, поданной 23 декабря 1999 г. Область изобретения Настоящее изобретение относится к группе соединений, которые являются сильнодействующими и селективными ингибиторами фосфодиэстеразы, специфичной к циклическому аденозин-3', 5'монофосфату (цАМФ-специфичная PDE). В частности, настоящее изобретение относится к группе новых соединений, которые полезны для ингибирования функции цАМФ-специфичной PDE, в частности PDE4,а также к способам получения соединений, фармацевтическим композициям, содержащим соединения, и использованию их как терапевтических агентов, например, при лечении воспалительных заболеваний и других заболеваний, связанных с повышенными уровнями цитокинов и провоспалительных медиаторов. Предпосылки к созданию изобретения Хронический воспалительный процесс является многофакторным осложнением заболевания, отличающимся активацией воспалительных клеток различных типов, особенно клеток лимфоидного происхождения (в том числе Т-лимфоцитов) и миелоидного происхождения (в том числе гранулоцитов, макрофагов и моноцитов). Провоспалительные медиаторы, в том числе цитокины, такие как фактор некроза опухоли (TNF) и интерлейкин-1 (IL-1), продуцируются этими активированными клетками. В соответствии с этим агент, который подавляет активацию этих клеток или их продуцирование провоспалительных цитокинов, может быть полезным для терапевтического лечения воспалительных заболеваний и других заболеваний, связанных с повышенными уровнями цитокинов. Циклический аденозинмонофосфат (цАМФ) является вторым мессенджером, который опосредует биологические ответные реакции клеток на широкий диапазон внеклеточных стимулов. Когда подходящий агонист связывается со специфическими рецепторами поверхности клетки, активируется аденилатциклаза, чтобы превратить аденозинтрифосфат (АТФ) в цАМФ. Теоретически считается, что индуцируемые агонистом воздействия цАМФ в клетке опосредуются преимущественно действием цАМФзависимых протеинкиназ. Внутриклеточные воздействия цАМФ завершаются или транспортом нуклеотида за пределы клетки, или ферментативным расщеплением фосфодиэстеразами (PDEs) циклических нуклеотидов, которые гидролизуют 3'-фосфодиэфирную связь с образованием 5'-аденозинмонофосфата(5'-АМФ). 5'-АМФ представляет собой неактивный метаболит. Структуры цАМФ и 5'-АМФ иллюстрируются ниже. Повышенные уровни цАМФ в человеческих клетках миелоидного и лимфоидного происхождения связаны с подавлением активации клеток. Семейство внутриклеточных ферментов PDEs, следовательно,регулирует уровень цАМФ в клетках. PDE4 представляет собой преобладающий изотип PDE в этих-1 007589 клетках и является основным участником деградации цАМФ. В соответствии с этим, ингибирование функции PDE может предотвратить превращение цАМФ в неактивный метаболит 5'-АМФ и, следовательно, поддерживать высокие уровни цАМФ и, таким образом, подавлять активацию клеток (см. BeavoTNF и частично ингибирует высвобождение IL-1 моноцитами (см. Semmler et al., Int. J. Immunopharmacol., 15, pp. 409-413 (1993); Molnar-Kimber et al., Mediators of Inflammation, 1, pp. 411-417 (1992. Также показано, что ингибиторы PDE4 ингибируют продуцирование супероксидных радикалов из полиморфонуклеарных лейкоцитов человека (см. Verghese et al., J. Mol. Cell. Cardiol., 21 (Suppl. 2), S61 (1989);Nielson et. al., J. Allergy Immunol., 86, pp. 801-808 (1990; ингибируют высвобождение вазоактивных аминов и простаноидов из базофилов человека (см. Peachell et al., J. Immunol., 148, pp. 2503-2510 (1992; ингибируют респираторные "вспышки" в эозинофилах (см. Dent et al., J. Pharmacol., 103, pp. 1339-1346(1991; и ингибируют активацию Т-лимфоцитов человека (см. Robicsek et al., Biochem. Pharmacol., 42,pp. 869-877 (1991. Активация воспалительных клеток и избыточное или нерегулируемое продуцирование цитокина(например, TNF и IL-1) вовлекаются в аллергические, аутоиммунные и воспалительные заболевания и нарушения, такие как ревматоидный артрит, остеоартрит, подагрический артрит, спондилит, тироидассоциированная офтальмопатия, болезнь Бехчета, сепсис, септический шок, эндотоксиновый бактериально-токсический шок, грамотрицательный сепсис, грамположительный сепсис, синдром токсического шока, астма, хронический бронхит, респираторный дистресс-синдром взрослых, хроническое легочное воспалительное заболевание, такое как хроническое закупоривающее легочное заболевание, силикоз,легочный саркоидоз, реперфузионное повреждение миокарда, головного мозга и конечностей, фиброз,муковисцитоз, келоидное образование, образование рубца, атеросклероз, нарушения, являющиеся отторжением трансплантата, такие как гомологичная болезнь и отторжение аллотрансплантата, хронический гломерулонефрит, волчанка, воспалительные заболевания кишечника, такие как болезнь Крона и неспецифический язвенный колит, пролиферативные лимфоцитарные заболевания, такие как лейкоз, и воспалительные дерматозы, такие как атопический дерматит, псориаз или крапивница. Другими состояниями, отличающимися повышенными уровнями цитокина, являются повреждения головного мозга вследствие умеренной травмы (см. Dhillon et al., J. Neurotrauma, 12, pp. 1035-1043 (1995);Suttorp et al., J. Clin. Invest., 91. pp. 1421-1428 (1993, кардиомиопатия, такая как застойная сердечная недостаточность (см. Bristow et al., Circulation, 97, pp. 1340-1341 (1998, кахексия, кахексия, вторичная к инфекции или злокачественности, кахексия, вторичная к синдрому приобретенного иммунного дефицита(СПИД), ARC (СПИД-ассоциированный комплекс), лихорадочная миалгия как следствие инфекции, церебральная малярия, остеопороз и заболевания типа резорбции костей, келоидное образование, образование тканевого рубца и гипертермия. В частности, TNF идентифицируется как играющий роль в отношении синдрома приобретенного иммунного дефицита (СПИД). СПИД возникает в результате инфицирования Т-лимфоцитов вирусом иммунодефицита человека (ВИЧ). Хотя ВИЧ также инфицирует клетки миелоидного происхождения и сохраняется в них, показано, что TNF положительно регулирует ВИЧ-инфекцию в Т-лимфоцитных и моноцитных клетках (см. Poli et al., Proc. Natl. Acad. Sci. USA, 87, pp. 782-785 (1990. Некоторые свойства TNF, такие как стимуляция коллагеназы, стимуляция развития кровеносных сосудов in vivo, стимуляция костной резорбции и способность увеличивать сцепление опухолевых клеток с эндотелием, согласуются с ролью TNF в развитии и метастатическом распространении рака у хозяина. В последнее время указывается, что TNF непосредственно причастен к активированию роста и метастазу опухолевых клеток (см. Orosz et al., J. Exp. Med., 177, pp. 1391-1398 (1993.PDE4 имеет широкое распространение в тканях. Существуют по меньшей мере четыре гена дляPDE4, множественные транскрипты которого из любого данного гена могут дать несколько различных белков, имеющих общие идентичные каталитические сайты. Аминокислотная идентичность между четырьмя возможными каталитическими сайтами составляет более 85%. Их общая чувствительность к ингибиторам и кинетическое подобие отражают функциональный аспект данного уровня аминокислотной идентичности. Теоретически считается, что роль этих альтернативно экспрессированных белков PDE4 состоит в создании механизма, по которому клетка может дифференцированно локализовать эти ферменты внутриклеточно и/или регулировать каталитическую эффективность путем посттрансляционной модификации. Любой данный тип клетки, который экспрессирует фермент PDE4, обычно экспрессирует более одного из четырех возможных генов, кодирующих эти белки. Исследователи проявляют значительный интерес к использованию ингибиторов PDE4 в качестве противовоспалительных агентов. Ранние данные указывают на то, что ингибирование PDE4 оказывает полезное действие на разнообразные воспалительные клетки, такие как моноциты, макрофаги, Т-клеткиTh-1- происхождения и гранулоциты. Синтез и/или высвобождение многих провоспалительных медиато-2 007589 ров, таких как цитокины, липидные медиаторы, супероксид и биогенные амины, такие как гистамин, ослабляется в этих клетках действием ингибиторов PDE4. Ингибиторы PDE4 также влияют на другие клеточные функции, в том числе пролиферацию Т-клеток, трансмиграцию гранулоцита в ответ на хемотоксичные вещества и целостность соединений эндотелиальных клеток в сосудистой сети. О разработке, синтезе и отборе различных ингибиторов PDE4 уже сообщалось. Метилксантины, такие как кофеин и теофилин, признаны в качестве первых описанных ингибиторов PDE4, но эти соединения не являются селективными, что касается ингибирования PDE. Лекарственное средство ролипрам,антидепрессант, был одним из первых описанных специфических ингибиторов PDE4. Ролипрам ниже приведенной структурной формулы имеет 50% ингибирующую концентрацию (IC50) приблизительно 200 нМ (наномоль), что касается ингибирования рекомбинантной PDE4 человека. Исследователи продолжают поиски ингибиторов PDE4, которые более селективны относительно ингибирования PDE4, имеют более низкую IС 50, чем ролипрам, и которые позволяют избежать нежелательных побочных действий на центральную нервную систему (ЦНС), таких как позыв на рвоту, рвота и седативный эффект, связанных с введением ролипрама. Один класс соединений приведен в патенте США 5665754, Feldman et al. Приведенными соединениями являются замещенные пирролидины,структура которых подобна структуре ролипрама. Одно конкретное соединение со структурной формулой (I) имеет IС 50 приблизительно 2 нМ относительно рекомбинантной PDE4 человека. Принимая во внимание, что наблюдалось благоприятное разделение рвотного побочного действия и эффективности,тем не менее эти соединения не проявляли уменьшения нежелательных побочных действий на ЦНС. Кроме того, некоторые компании сейчас проводят клинические исследования других ингибиторовPDE4. Однако проблемы, связанные с эффективностью и неблагоприятными побочными действиями,такими как рвота и расстройства центральной нервной системы, остаются не решенными. В соответствии с этим, соединения, которые селективно ингибируют PDE4 и которые уменьшают или исключают неблагоприятные побочные действия на ЦНС, связанные с предшествующими ингибиторами PDE4, могут быть полезны при лечении аллергических и воспалительных заболеваний и других заболеваний, связанных с избыточным или нерегулируемым продуцированием цитокинов, таких какTNF. Дополнительно, селективные ингибиторы PDE4 могут использоваться при лечении заболеваний,ассоциированных с повышенными уровнями цАМФ или функцией PDE4 в конкретной ткани-мишени. Краткое изложение сущности изобретения Настоящее изобретение относится к сильнодействующим и селективным ингибиторам PDE4, полезным при лечении заболеваний и состояний, когда ингибирование активности PDE4 рассматривается как благоприятное действие. Представленные ингибиторы PDE4 неожиданно уменьшают или исключают неблагоприятные побочные действия на ЦНС, связанные с предшествующими ингибиторами PDE4. В особенности настоящее изобретение относится к соединениям, имеющим структурную формулуR1 представляет собой низший алкил, мостиковый алкил, арил, гетероарил, аралкил, циклоалкил, 5 или 6-членный насыщенный гетероцикл, С 1-С 4-алкиленарил, С 1-С 4-алкилен-O-арил, C1-С 4-алкиленгетероарил, С 1-С 4-алкилен-Het, С 2-С 4-алкиленарил-O-арил, C1-С 4-алкилен-мостиковый алкил, С 1-С 3 алкиленциклоалкил, незамещенный или замещенный низшим алкилом или арилом, пропаргил, незамещенный или замещенный арилом, аллил или галогенциклоалкил;R2 представляет собой водород, метил или галогензамещенный метил;R7 выбирают из группы, состоящей из разветвленного или неразветвленного низшего алкила, гетероарила, гетероцикла, аралкила и арила, и R7 может быть незамещенным или замещенным одним или несколькими OR8, NR8R9 или SR8;R8 и R9, одинаковые или разные, выбирают из группы, состоящей из водорода, низшего алкила,циклоалкила, арила, гетероарила, алкарила, гетероаралкила, гетероалкарила и аралкила, или R8 и R9 могут вместе образовывать кольцо от 4-членного до 7-членного;R11 представляет собой алкил, циклоалкил, трифторметил, арил, аралкил или NR8R9; его соли и сольваты,где низший алкил означает алкильную группу, имеющую от одного до шести атомов углерода; мостиковый алкил означает бициклическую или полициклическую С 6-С 16-углеводородную группу; арил означает моноциклическую или полициклическую ароматическую группу, предпочтительно моноциклическую или бициклическую ароматическую группу, которая может быть незамещенной или замещенной одним или более заместителями, выбираемыми из группы, состоящей из галогена, алкила,фенила, гидрокси, гидроксиалкила, алкокси, алкоксиалкила, галогеналкила, нитро, амино, алкиламино,ациламино, алкилтио, алкилсульфинила и алкилсульфонила; аралкил означает алкильную группу, в которой один из водородных атомов замещен арильной группой; циклоалкил означает циклическую С 3-С 7-углеводородную группу, возможно конденсированную с ароматической группой; гетероарил выбирают из группы, включающей тиенил, фурил, пиридил, оксазолил, хинолил, изохинолил, индолил, триазолил, изотиазолил, изоксазолил, имидизолил, бензотиазолил, пиразинил, пиримидинил, тиазолил и тиадиазолил; гетероцикл выбирают из группы, включающей тетрагидрофуран, пиперидин, пиперазин, сульфолан,морфолин, тетрагидропиран и диоксан. Предпочтительные примеры соединений настоящего изобретения включают соединения, заявленные в пп.2-22 формулы изобретения. Настоящее изобретение также относится к фармацевтическим композициям, содержащим соединение структурной формулы (II), фармацевтически приемлемый носитель и, возможно, второй противовоспалительный терапевтический агент. Например, вторым противовоспалительным терапевтическим агентом может быть терапевтический агент, мишенью для которого является TNF. Настоящее изобретение также относится к способам лечения млекопитающего в состоянии, когда ингибирование цАМФ-специфичной PDE4 является терапевтически полезным, предусматривающим введение млекопитающему терапевтически эффективного количества соединения структурной формулы(II) или композиции, содержащей соединение структурной формулы (II) и фармацевтически приемлемый носитель. Примеры состояний и заболеваний, для лечения которых соединения настоящего изобретения являются полезными, перечислены в пп.28-38 формулы изобретения. В предпочтительных вариантах осуществления при лечении млекопитающего в соответствии со способом настоящего изобретения оно показывает минимальную ответную рвотную реакцию или не показывает такую реакцию. В еще одном предпочтительном варианте при лечении млекопитающего в соответствии со способом настоящего изобретения оно показывает минимальные неблагоприятные побочные воздействия на центральную нервную систему или не показывает таких воздействий. Настоящее изобретение также относится к способам модулирования уровней цАМФ у млекопитающего, уменьшения уровней TNF у млекопитающего, функцию PDE4 у млекопитающего введением терапевтически эффективных количеств соединения структурной формулы (II). Подробное описание предпочтительных примеров осуществления Настоящее изобретение относится к соединениям, имеющим структурную формулу (II)R1 представляет собой низший алкил, мостиковый алкил, арил, гетероарил, аралкил, циклоалкил, 5 или 6-членный насыщенный гетероцикл, C1-С 4-алкиленарил, C1-C4-алкилен-О-арил, C1-C4-алкиленгетероарил, C1-С 4-алкилен-Het, С 2-С 4-алкиленарил-O-арил, C1-C4-алкилен-мостиковый алкил, С 1-С 3 алкиленциклоалкил, незамещенный или замещенный низшим алкилом или арилом пропаргил, незамещенный или замещенный арилом аллил или галогенциклоалкил;R2 представляет собой водород, метил или галогензамещенный метил;R6 и R12 представляют собой независимо водород, низший алкил, аралкил, SO2R11 или C(=O)R7;R7 выбирают из группы, состоящей из разветвленного или неразветвленного низшего алкила, гетероарила, гетероцикла, аралкила и арила, и R7 может быть незамещенным или замещенным одним или несколькими OR8, NR8R9 или SR8;R8 и R9, одинаковые или разные, выбирают из группы, состоящей из водорода, низшего алкила,циклоалкила, арила, гетероарила, алкарила, гетероаралкила, гетероалкарила и аралкила, или R8 и R9 могут вместе образовывать кольцо от 4-членного до 7-членного;R11 представляет собой алкил, циклоалкил, трифторметил, арил, аралкил или NR8R9; его соли и сольваты,Как здесь используется, термин "алкил", сам по себе или в комбинации, охватывает насыщенные углеводородные группы с неразветвленной или разветвленной цепью, содержащей от одного до 16 атомов углерода. Термин "низший алкил" определен здесь как алкильная группа, имеющая от одного до шести атомов углерода (C1-C6). Примеры низших алкильных групп включают в себя, но не ограничиваются перечисленным, метил, этил, н-пропил, изопропил, изобутил, н-бутил, неопентил, н-гексил и тому подобное. Термин "алкинил" относится к ненасыщенной алкильной группе, которая имеет углеродуглеродную тройную связь. Термин "мостиковый алкил" определен здесь как бициклическая или полициклическая С 6-С 16 углеводородная группа, например норборнил, адамантил, бицикло[2.2.2]октил, бицикло[2.2.1]гептил,бицикло[3.2.1]октил или декагидронафтил. Термин "циклоалкил" означает циклическую С 3-С 7-углеводородную группу, возможно конденсированную с ароматической группой. Примеры циклоалкильных групп включают в себя, но не ограничива-5 007589 ются перечисленным, циклопропил, циклобутил, циклогексил, циклопентил, инданил и тетрагидронафтил. Термин "алкилен" относится к алкильной группе, имеющей заместитель. Например, термин "С 1-С 3 алкиленциклоалкил" относится к алкильной группе, имеющей от одного до трех атомов углерода и замещенной циклоалкильной группой. Термин "галогеналкил" определен здесь как алкильная группа, замещенная одним или несколькими галогенными заместителями или фтором, хлором, бромом, иодом или их комбинациями. Аналогично этому, "галогенциклоалкил" определен здесь как циклоалкильная группа, имеющая один или несколько галогенных заместителей. Термин "арил", сам по себе или в комбинации, определен здесь как моноциклическая или полициклическая ароматическая группа, предпочтительно моноциклическая или бициклическая ароматическая группа, например фенил или нафтил, которая может быть незамещенной или замещенной, например,одним или несколькими, в частности, одним-тремя заместителями, выбранными из группы, включающей галоген, алкил, фенил, гидрокси, гидроксиалкил, алкокси, алкоксиалкил, галогеналкил, нитро, амино,алкиламино, ациламино, алкилтио, алкилсульфинил и алкилсульфонил. Примеры арильных групп включают в себя фенил, нафтил, тетрагидронафтил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-метилфенил,4-метоксифенил, 3-трифторметилфенил, 4-нитрофенил и тому подобное. Гетероарил выбирают из группы, включающей тиенил, фурил, пиридил, оксазолил, хинолил, изохинолил, индолил, триазолил, изотиазолил, изоксазолил, имидизолил, бензотиазолил, пиразинил, пиримидинил, тиазолил и тиадиазолил. Термин "аралкил" определен здесь, как определенная ранее алкильная группа, в которой один из водородных атомов замещен арильной группой, как здесь определяется, например, фенильной группой,возможно имеющей один или несколько заместителей, например галоген, алкил, алкокси и тому подобное. Примером аралкильной группы является бензильная группа. Термин "алкарил" определен здесь, как определенная ранее арильная группа, в которой один из атомов водорода замещен алкильной, циклоалкильной, галогеналкильной или галогенциклоалкильной группой. Термины "гетероаралкил" и "гетероалкарил" определены подобно термину "аралкил" и "алкарил",однако, арильная группа замещена гетероарильной группой, как определено ранее. Гетероцикл выбирают из группы, включающей тетрагидрофуран, пиперидин, пиперазин, сульфолан, морфолин, тетрагидропиран и диоксан. Термин "галоген" определен здесь, как включающий в себя фтор, хлор, бром и иод. Термины "алкокси", "арилокси и "аралкокси" определены здесь как -OR, где R означает алкил,арил и аралкил соответственно. Термин "алкоксиалкил" определен как алкоксигруппа, присоединенная к алкильной группе. Термины "арилоксиалкил" и "аралкоксиалкил" подобно определены как арилокси- или аралкоксигруппа, присоединенная к алкильной группе. Термин "гидрокси" определен как -ОН. Термин "гидроксиалкил" определен как гидроксигруппа, присоединенная к алкильной группе. Термин "амино" определен как -NH2. Термин "алкиламино" определен как -NR2, где по меньшей мере один R означает алкил и второй R означает алкил или водород. Термин "ациламино" определен как RC(=O)N, где R означает алкил или арил. Термин "нитро" определен как -NO2. Термин "алкилтио" определен здесь как -SR, где R означает алкил. Термин "алкилсульфинил" определен как R-SO2, где R означает алкил. Термин "алкилсульфонил" определен как R-SO3, где R означает алкил. В предпочтительных примерах реализации R4 выбирается из группы, состоящей из водорода, метила, трифторметила, циклопропила, этинила и фенила. R5 является водородом или нижним алкилом, R6 выбирается из группы, состоящей из водорода, C(=O)R7, C(=O)OR7, этила, бензила, SO2CH и SO2C6H5 иR7 - это нижний алкил. В более предпочтительных примерах осуществления R5 означает водород или метил, R7 означает метил, R2 означает метил или дифторметил, R4 выбран из группы, включающей водород, низший алкил,бензил и фенил, R12 означает водород или метил и R6 выбран из группы, включающей водород, метил,этил, C(=O)OR7, бензил, SO2CH3 и SO2C6H5. R1 выбран из группы, включающей где Ас означает СН 3 С(=O) и tBu означает С(СН 3)3. В большинстве предпочтительных примеров осуществления R1 выбран из группы, включающей циклопентил, циклопропилметил, тетрагидрофурил, инданил, норборнил, фенетил и фенилбутил; R2 выбран из группы, включающей метил и дифторметил; R3 выбран из группы, включающей бензил, СO2 СН 3,С(=O)СН 2 ОН, С(=O)СН(СН 3)ОН, С(=O)С(СН 3)2 ОН, иR4 означает водород; R5 означает водород или метил; R6 означает водород, метил, этил, бензил,SO2CH3, SO2C6H5, бензоил, С(=O)С(СН 3)3 или ацетил; R12 означает водород или метил; и R10 означает водород. Настоящее изобретение включает в себя все возможные стереоизомеры и геометрические изомеры соединений структурной формулы (II) и включает в себя не только рацемические соединения, но также,кроме того, оптически активные изомеры. Когда соединение структурной формулы (II) желательно иметь в виде индивидуального энантиомера, его можно получить или расщеплением конечного продукта, или стереоспецифическим синтезом из любого изомерно чистого исходного материала, или с использованием хирального вспомогательного вещества, например, см. Z. Ma et al., Tetrahedron: Asymmetry, 8 (6),pages 883-888 (1997). Расщепление конечного продукта, промежуточного продукта или исходного материала можно осуществить любым подходящим способом, известным в данной области техники. Помимо этого, в случаях, где возможны таутомеры соединений структурной формулы (II), настоящее изобретение предполагает включить в себя все таутомерные формы соединений. Как показано далее, определенные стереоизомеры проявляют исключительную способность ингибировать PDE4 без проявления неблагоприятных побочных действий на ЦНС, обычно связанных с ингибиторами PDE4. Общепринято, в частности, что биологические системы могут проявлять высокую чувствительную активность относительно абсолютной стереохимической природы соединений. (См. Е. J. Ariens, Medicinal Research Reviews, 6:451-466 (1986); E.J. Ariens, Medicinal Research Reviews, 7:367-387 (1987); K.W.(1989); и S.C. Stinson; Chemical and Engineering News, 75:38-70 (1997. Например, ролипрам представляет собой стереоспецифичный ингибитор PDE4, который имеет один хиральный центр. (-)-Энантиомер ролипрама имеет более высокую фармакологическую активность,чем (+)-энантиомер, что может быть связано с его потенциальным антидепрессивным действием. Schultzet al., Naunyn-Schmiedeberg's Arch Pharmacol, 333:23-30 (1986). Кроме того, метаболизм ролипрама представляется стереоспецифичным с (+)-энантиомером, проявляющим большую скорость клиренса, чем (-)энантиомер. Krause et al., Xenobiotica, 18:561-571(1988). И, наконец, недавнее наблюдение указывает, что(-)-энантиомер ролипрама (R-ролипрам) приблизительно в десять раз сильнее вызывает рвоту, чем (+)энантиомер (S-ролипрам). A. Robichaud et al., Neuropharmacology, 38:289-297 (1999). Это наблюдение не просто согласовать с различием в предрасположении испытуемого животного к изомерам ролипрама и способностью ролипрама ингибировать фермент PDE4. Соединения настоящего изобретения могут иметь три или более хиральных центров. Как показано ниже, соединения специфической стереохимиче- 21007589 ской ориентации проявляют одинаковую ингибирующую активность к PDE4 и фармакологическую активность, но отличающиеся токсичность для ЦНС и рвотный потенциал. В соответствии с этим предпочтительные соединения настоящего изобретения имеют структурную формулу (III) Соединения структурной формулы (III) являются сильнодействующими и селективными ингибиторами PDE4 и не проявляют неблагоприятного побочного действия на ЦНС и рвотного потенциала, демонстрируемого стереоизомерами соединения структурной формулы (III). Соединения структурной формулы (II), которые содержат кислотные группы, могут образовывать фармацевтически приемлемые соли с подходящими катионами. Подходящими фармацевтически приемлемыми катионами являются катионы щелочного металла (например, натрия или калия) и щелочноземельного металла (например, кальция или магния). Фармацевтически приемлемые соли соединений структурной формулы (II), которые содержат основный центр, представляют собой кислотно-аддитивные соли, полученные с использованием фармацевтически приемлемых кислот. Примерами являются гидрохлорид, гидробромид, сульфат или бисульфат, фосфат или гидрофосфат, ацетат, бензоат, сукцинат, фумарат, малеат, лактат, цитрат, тартрат, глюконат, метансульфонат, бензолсульфонат и птолуолсульфонат. В свете вышеизложенного любая ссылка на соединения настоящего изобретения, появляющаяся здесь, предполагает включение соединений структурной формулы (II), а также их фармацевтически приемлемых солей и сольватов. Соединения настоящего изобретения можно использовать для терапевтического введения в виде неразбавленного химического соединения, но предпочтительнее вводить соединения структурной формулы (II) в форме фармацевтической композиции или готовой препаративной формы. В соответствии с этим, настоящее изобретение дополнительно предлагает фармацевтические готовые препаративные формы, содержащие соединение структурной формулы (II) вместе с одним или несколькими фармацевтически приемлемыми носителями и, возможно, другими терапевтическими и/или профилактическими ингредиентами. Носители называются "приемлемыми" в смысле совместимости с другими ингредиентами готовой препаративной формы и отсутствия вредного воздействия на реципиента. В частности, селективный ингибитор PDE4 настоящего изобретения полезен как таковой или в комбинации со вторым противовоспалительным терапевтическим агентом, например терапевтическим агентом, мишенью для которого является TNF, такой как ENBREL или REMICADE, который полезен при лечении ревматоидного артрита. Подобным образом также показана терапевтическая полезность антагонизма IL-1 на животных моделях для лечения ревматоидного артрита. Таким образом, представляется, что антагонизм IL-1 в комбинации с ингибированием PDE4, что ослабляет TNF, может быть эффективным. Представленные ингибиторы PDE4 полезны при лечении различных аллергических, аутоиммунных и воспалительных заболеваний. Термин "лечение" охватывает предотвращение, уменьшение, прекращение или изменение направления развития тяжести подвергаемого лечению состояния или симптомов. Как таковой, термин "лечение" включает в себя медицинское терапевтическое и/или профилактическое введение, как уместно. В частности, воспаление означает локализованную защитную ответную реакцию, вызванную поражением или разрушением тканей, которая служит, чтобы разрушить, ослабить или оградить (например,изолировать) как повреждающий агент, так поврежденную ткань. Термин "воспалительное заболевание",как здесь используется, означает любое заболевание, при котором избыточная или нерегулируемая воспалительная ответная реакция приводит к избыточным воспалительным симптомам, поражению ткани хозяина или потере функции ткани. Дополнительно термин "аутоиммунное заболевание", как используется здесь, означает любую группу нарушений, при которых поражение ткани ассоциируется с гуморальными или опосредованными клетками ответными реакциями на собственные компоненты организма. Термин "аллергическое заболевание", как используется здесь, означает любые симптомы, поражение ткани или потерю функции ткани, являющиеся результатом аллергии. Термин "артритное заболевание", как используется здесь, означает любое из большого семейства заболеваний, которые характеризуются воспалительными поражениями суставов, приписываемыми различным причинам. Термин "дерматит", как используется здесь, означает любое из большого семейства заболеваний кожи, которые характеризуются воспалением кожи, приписываемым различным причинам. Термин "отторжение трансплантата", как используется здесь, означает любую иммунную реакцию, направленную против транспланти- 22007589 рованной ткани, в том числе органа и клетки (например, костного мозга), характеризующуюся потерей функции трансплантированной и окружающей тканей, болью, отеком, лейкоцитозом или тромбоцитопенией. Настоящее изобретение также предлагает способ модулирования уровней цАМФ у млекопитающего, а также способ лечения заболеваний, характеризующихся повышенными уровнями цитокинов. Термин "цитокин", как используется здесь, означает любой секретированный полипептид, влияющий на фукции других клеток и модулирующий взаимодействие между клетками в иммунной или воспалительной ответной реакции. Цитокины включают в себя, но не ограничены перечисленным, монокины,лимфокины и хемокины независимо от того, какие клетки их продуцируют. Например, монокин в основном обозначается как продуцированный и секретированный моноцитом, однако, многие другие клетки продуцируют монокины, такие как природные клетки-киллеры, фибробласты, базофилы, нейтрофилы,эндотелиальные клетки, астроциты головного мозга, клетки стромы костного мозга, эпидермальные кератиноциты и В-лимфоциты. Лимфокины в основном обозначаются как продуцированные лимфоцитными клетками. Примерами цитокинов являются, но не ограничены перечисленным, интерлейкин-1 (IL-1),интерлейкин-6 (IL-6), альфа-фактор некроза опухоли (TNF) и бета-фактор некроза опухоли (TNF). Настоящее изобретение дополнительно предлагает способ снижения уровней TNF у млекопитающего, предусматривающий введение эффективного количества соединения структурной формулы (II) млекопитающему. Термин "снижение уровней TNF", как используется здесь, означает илиa) уменьшение избыточных in vivo уровней TNF у млекопитающего до нормальных уровней или ниже нормальных уровней ингибированием in vivo высвобождения TNF всеми клетками, в том числе, но не ограничены ими, моноцитами или макрофагами; илиb) индуцирование негативной регуляции на трансляционном или транскрипционном уровне избыточных in vivo уровней TNF у млекопитающего до нормальных уровней или ниже нормальных уровней; илиc) индуцирование негативной регуляции ингибированием прямого синтеза TNF как посттранслянционного события. Кроме того, соединения настоящего изобретения полезны для подавления активации воспалительной клетки. Термин "активация воспалительной клетки", как используется здесь, означает индуцирование стимулами (в том числе, но не ограничены ими, цитокинами, антигенами или аутоантителами) пролиферативной клеточной ответной реакции, продуцирование растворимых медиаторов (в том числе, но не ограничены ими, цитокинов, кислородных радикалов, ферментов, простаноидов или вазоактивных аминов), поверхностную клеточную экспрессию новых медиаторов или повышенного количества медиаторов (в том числе, но не ограничены ими, основных антигенов гистосовместимости или молекул клеточной адгезии) в воспалительных клетках (в том числе, но не ограничены ими, моноцитах, макрофагах,Т-лимфоцитах, В-лимфоцитах, гранулоцитах, полиморфонуклеарных лейкоцитах, тучных клетках, базофилах, эозинофилах, дендритных клетках и эндотелиальных клетках). Специалистам в этой области техники понятно, что активация одного фенотипа или комбинаций этих фенотипов в этих клетках содействует стимулированию, сохранению или обострению воспалительного состояния. Соединения настоящего изобретения также полезны для индуцирования релаксации гладких мышц дыхательных путей, увеличения просвета бронхов и предотвращения бронхостеноза. Соединения настоящего изобретения, следовательно, полезны при лечении таких заболеваний, как артритные заболевания (такие как ревматоидный артрит), остеоартрит, подагрический артрит, спондилит, тироид-ассоциированная офтальмопатия, болезнь Бехчета, сепсис, септический шок, эндотоксиновый бактериально-токсический шок, грамотрицательный сепсис, грамположительный сепсис, синдром токсического шока, астма, хронический бронхит, аллергический ринит, аллергический конъюнктивит,весенний конъюнктивит, эозинофильная гранулема, (острый) респираторный дистресс-синдром взрослых (ARDS), хроническое легочное воспалительное заболевание (такое как хроническое закупоривающее легочное заболевание), силикоз, легочный саркоидоз, реперфузионное повреждение миокарда, головного мозга и конечностей, повреждение головного или спинного мозга из-за незначительной травмы,фиброз, в том числе муковисцитоз, келоидное образование, образование тканевых рубцов, атеросклероз,аутоиммунные заболевания, такие как системная красная волчанка (SLE) и нарушения, являющиеся отторжением трансплантата (например, гомологичная болезнь (GvH) и отторжение аллотрансплантата),хронический гломерулонефрит, воспалительные заболевания кишечника, такие как болезнь Крона и неспецифический язвенный колит, пролиферативные лимфоцитарные заболевания, такие как лейкоз (например, хронический лейкоцитарный лейкоз; CLL) (см. Mentz et al., Blood 88, pp. 2172-2182 (1996, и воспалительные дерматозы, такие как атопический дерматит, псориаз или крапивница. Другими примерами таких заболеваний или родственных состояний являются кардиомиопатия, такая как застойная сердечная недостаточность, гипертермия, кахексия, кахексия, вторичная к инфекции или злокачественности, кахексия, вторичная к синдрому приобретенного иммунного дефицита СПИД,ARC (СПИД-ассоциированный комплекс), церебральная малярия, остеопороз и заболевание типа резорбции костей, лихорадка и миалгия как следствие инфекции. Кроме того, соединения настоящего изо- 23007589 бретения полезны при лечении несахарного диабета и нарушений центральной нервной системы, таких как депрессия и полиинфарктная деменция. Соединения настоящего изобретения также полезны для использования вне тех применений, которые обычно называются терапевтическими. Например, представленные соединения могут функционировать как консерванты органа-трансплантата (см. Pinsky et al., J. Clin. Invest., 92, pp. 2994-3002 (1993. Селективные ингибиторы PDE4 также можно использовать при лечении эректильной дисфункции,особенно васкулогеннной импотенции (Doherty, Jr et al., патент США 6127363), несахарного диабета(Kidney Int., 37, p. 362 (1990); Kidney Int., 35, p. 494 (1989 и нарушений центральной нервной системы,таких как полиинфарктная деменция (Nicholson, Psychopharmacology, 101, p. 147 (1990, депрессия(Eckman et al., Curr. Ther. Res., 43, p. 291 (1988, состояния страха и ответных реакций на стресс (Neuropharmacology, 38, р. 1831 (1991, церебральной ишемии (Eur. J. Pharmacol., 272, p. 107 (1995, поздней дискинезии (J. Clin. Pharmacol., 16, p. 304 (1976, болезни Паркинсона (см. Neurology, 25, p. 722 (1975);Clin. Exp. Pharmacol, Physiol, 26, p. 421 (1999 и пременструального синдрома. Что касается депрессии,селективные ингибиторы PDE4 проявляют эффективность на различных животных моделях депрессии,таких как "поведенческое отчаяние или испытания Porsolt (Eur. J. Pharmacol., 47, p. 379 (1978); Eur. J.Pharmacol, 57, p. 431 (1979); Antidepressants: neurochemical, behavioral and clinical prospectives, Enna, Malick, and Richelson, eds., Raven Press, p. 121 (1981, и "испытание с подвешиванием за хвост" (Psychopharmacology, 85, р. 367 (1985. Данные последних исследований показывают, что продолжительное лечение in vivo различными антидепрессантами увеличивает происходящую из головного мозга экспрессию PDE4 (J. Neuroscience, 19, р. 610 (1999. Следовательно, селективный ингибитор PDE4 можно использовать как таковой, так и совместно со вторым терапевтическим агентом при лечении четырьмя главными классами антидепрессантов: электросудорожные процедуры, ингибиторы моноаминоксидазы и селективные ингибиторы повторного поглощения серотонина или норэпинефрина. Селективные ингибиторы PDE4 можно также использовать для применений, которые модулируют бронхорасширяющую активность через прямое воздействие на клетки бронхиальных гладких мышц при лечении астмы. Соединения и фармацевтические композиции, подходящие для использования в настоящем изобретении, включают в себя те, в которых активный ингредиент вводится млекопитающему в эффективном количестве для достижения предполагаемой цели. Более конкретно, "терапевтически эффективное количество" означает количество, эффективное для предотвращения развития или для ослабления существующих симптомов у подвергаемого лечению субъекта. Определение эффективных количеств вполне в возможностях специалистов, работающих в этой области техники, особенно в свете подробного описания, приведенного здесь. Термин " млекопитающее", как используется здесь, включает в себя особи мужского и женского пола и охватывает людей, домашних животных (например, кошек, собак), домашний скот (например,крупный рогатый скот, лошадей, свиней) и диких животных (например, приматов, животных семейства крупных кошачьих, животных зоопарков)."Терапевтически эффективная доза" относится к количеству соединения, которое приводит к достижению желаемого эффекта. Токсичность и терапевтическую эффективность таких соединений можно определить стандартными фармацевтическими процедурами в клеточных культурах или с помощью экспериментальных животных, например, для определения LD50 (доза, смертельная для 50% популяции) иED50 (доза, терапевтически эффективная для 50% популяции). Соотношение доз между токсичным и терапевтическим действиями представляет собой терапевтический индекс, который выражен как соотношение между LD50 и ED50. Предпочтительнее соединения с более высокими терапевтическими индексами. Данные, полученные из таких результатов, можно использовать для составления диапазона дозы для лечения людей. Доза таких соединений предпочтительно лежит в диапазоне находящихся в обращении концентраций, которые включают в себя ED50 с небольшой токсичностью или с отсутствием токсичности. Доза может изменяться в этом диапазоне в зависимости от применяемой лекарственной формы и используемого способа введения. Точную готовую препаративную форму, способ введения и дозировку может выбрать врач в зависимости от состояния пациента. Дозированное количество и интервалы введения можно регулировать индивидуально, чтобы создать в плазме уровни активного компонента, которые достаточны, чтобы поддержать терапевтические действия. Как понятно специалистам в этой области, сделанные здесь ссылки на лечение распространяются как на профилактику, так и на лечение установленных заболеваний и симптомов. Понятно также, что количество соединения изобретения, требуемое для использования при лечении, изменяется с природой подвергаемого лечению состояния и с возрастом и состоянием пациента, и, в конечном счете, определяется штатным врачом больницы или ветеринаром. В основном, однако, применяемые дозы для лечения совершеннолетнего человека обычно составляют от 0,001 приблизительно до 100 мг/кг в день. Желаемая доза может быть для удобства введена в виде одинарной дозы или в виде многочисленных доз с подходящими интервалами, например, в виде двух, трех, четырех или более поддоз в день. На практике врач определяет реальную схему приема лекарственного средства, которая наиболее подходит для отдельного пациента, и доза изменяется с возрастом, массой и восприимчивостью пациента. Приведенные выше до- 24007589 зы представляют собой пример усредненного случая, однако, в отдельных случаях необходимы более высокая или более низкая дозы и такие случаи входят в объем настоящего изобретения. Для введения готовых препаративных форм настоящего изобретения может быть использован стандартный способ при лечении указанных заболеваний, такой как пероральный, парентеральный, через слизистую оболочку (например, путем сублингвального или трансбуккального введения), местное применение, чрескожный, ректальный, посредством ингаляции (например, назальной) или глубокой легочной ингаляции. Парентеральное введение включает в себя, но не ограничено перечисленным, внутривенное, внутриартериальное, внутрибрюшинное, подкожное, внутримышечное, внутриоболочечное и внутрисуставное. Парентеральное введение можно осуществить с использованием способа высокого давления, подобного POWDERJET. Для трансбуккального введения композиция может быть в форме таблеток или лепешек, приготовленных обычным способом. Например, таблетки и капсулы для перорального введения могут содержать обычные эксципиенты, такие как связующие вещества (например, сироп, камедь акации, желатин, сорбит, трагакант, клейстеризованный крахмал или поливинилпирролидон), наполнители (например, лактозу, сахар, микрокристаллическую целлюлозу, маисовый крахмал, фосфат кальция или сорбит), смазки(например, стеарат магния, стеариновую кислоту, тальк, полиэтиленгликоль или диоксид кремния), дезинтегрирующие вещества (например, картофельный крахмал или натриевую соль гликоллята крахмала) или смачивающие вещества (например, лаурилсульфат натрия). Таблетки могут быть покрыты в соответствии со способами, известными специалистам в этой области. В соответствии с другим вариантом соединения настоящего изобретения можно ввести в пероральные жидкие препараты, такие как водные или масляные суспензии, растворы, эмульсии, сиропы или эликсиры например. Кроме того, готовые препаративные формы, содержащие эти соединения, могут быть в виде сухого продукта для составления с водой или другим подходящим наполнителем перед использованием. Такие жидкие препараты могут содержать обычные добавки, такие как суспендирующие вещества, например сироп сорбита, метилцеллюлоза, сироп глюкозы/сахара, желатин, гидроксиэтилцеллюлоза, гидрксипропилметилцеллюлоза, карбоксиметилцеллюлоза, гель стеарата алюминия и гидрированные пищевые жиры; эмульгаторы, такие как лецитин, моноолеат сорбитана или камедь акации; неводные наполнители (которые могут включать в себя пищевые масла), такие как миндальное масло,фракционированное кокосовое масло, маслянистые сложные эфиры, пропиленгликоль и этиловый спирт; и консерванты, такие как метил- или пропил-п-гидроксибензоат и сорбиновая кислота. Такие препараты также могут быть приготовлены в форме суппозиториев, например, содержащих обычную основу для суппозиториев, такую как какао-масло или другие глицериды. Композиции для ингаляции обычно могут быть в форме раствора, суспензии или эмульсии, вводимых в виде сухого порошка или аэрозоля с использованием обычного пропеллента, такого как дихлордифторметан или трихлорфторметан. Типичные готовые препаративные формы для местного и чрескожного применения содержат обычные водные или неводные наполнители, такие как глазные капли, кремы, мази, лосьоны и пасты,или могут быть в форме содержащего лекарственное средство пластыря, повязки или мембраны. Дополнительно композиции настоящего изобретения могут быть приготовлены для парентерального введения инъекцией или непрерывной инфузией. Готовые препаративные формы для инъекций могут быть в форме суспензий, растворов или эмульсий в масляных или водных наполнителях и могут содержать такие вещества, как суспендирующие, стабилизирующие и/или диспергирующие вещества, для облегчения приготовления препаративной формы. В соответствии с другим вариантом, активные ингредиенты могут быть в форме порошка для составления с подходящим наполнителем (например, стерильной не содержащей пирогенов водой) перед использованием. Композиция по настоящему изобретению может быть также приготовлена в виде препарата-депо. Такие длительное время действующие готовые препаративные формы можно вводить имплантированием(например, подкожно или внутримышечно) или внутримышечной инъекцией. В соответствии с этим,соединения изобретения можно приготовить с подходящими полимерными или гидрофобными материалами (например, эмульсией в приемлемом масле), ионообменными смолами или слаборастворимыми производными (например, слаборастворимой солью). Для ветеринарного использования соединение формулы (II) или его нетоксичные соли вводят как подходящую готовую препаративную форму в соответствии с обычной ветеринарной практикой. Ветеринарный врач может легко определит схему приема лекарственного средства и способ введения средства, который наиболее подходит для конкретного животного. Таким образом, изобретение создает в дополнительном аспекте фармацевтическую композицию,содержащую соединение формулы (II) вместе с фармацевтически приемлемым разбавителем или носителем. Дополнительно настоящее изобретение предлагает способ получения фармацевтической композиции, содержащей соединения структурной формулы (II), предусматривающий смешивание соединения формулы (II) с фармацевтически приемлемым разбавителем или носителем для соединения. Определенные не ограничительные примеры соединений структурной формулы (II) приведены ниже, причем синтез соединений осуществляют по способу, приведенному ниже.- 25007589 Вообще соединения структурной формулы (II) можно получать в соответствии со следующими схемами синтеза. Специалистам в этой области понятно, что в каждой схеме, описанной ниже, применяют защитные группы, когда это необходимо, в соответствии с основными принципами химического синтеза. Защитные группы удаляют на конечных стадиях синтеза при кислотных, основных или гидрогенолитических условиях, которые очевидны для специалистов в этой области. Используя соответствующую обработку и защиту любых химических функциональных групп, синтез соединений структурной формулы (II), в частности не предлагаемых здесь, можно выполнить способами, аналогичными приведенным ниже схемам. Если не оговорено особо, все исходные материалы получали от промышленных поставщиков и использовали без дополнительной очистки. Все продукты реакции и хроматографические фракции анализировали тонкослойной хроматографией на 250 мм силикагелевых пластинках, визуализированных ультрафиолетовым (УФ) излучением при нанесении пятна I2 (иода). Продукты и промежуточные продукты очищали флэш-хроматографией или ВЭЖХ с обращенной фазой. Соединения общей структурной формулы (II) можно получить, например, как предложено в следующей схеме синтеза. Другие способы синтеза также известны специалистам в этой области. Следующая схема реакции дает соединение структурной формулы (II), где R1 и R2, например, СН 3 и циклопентил, определяются исходными материалами. Подходящий выбор других исходных материалов или осуществление реакций превращения на промежуточных продуктах и примерах, позволяет получить соединения общей структурной формулы (II), имеющие другие перечисленные заместители от R1 до R11. Промежуточный продукт 1 получают по приведенной ниже последовательности синтеза.- 26007589 Следующее ниже поясняет синтез различных промежуточных продуктов и соединений структурной формулы (II). Следующие примеры приведены для пояснения и не должны рассматриваться как ограничительные. Промежуточный продукт А. Получение (Е)-3-(3-циклопентилокси-4-метоксифенил)-2-метилакриловой кислоты. Сначала получают этиловый эфир (Е)-3-(3-циклопентилокси-4-метоксифенил)-2-метилакриловой кислоты следующим образом. В охлажденный (0 С) перемешиваемый раствор триэтилфосфонопропионата (50,6 мл; 236 ммоль; 1,05 экв.) в сухом тетрагидрофуране (500 мл) добавляют раствор гексаметилдисилиламида лития в тетрагидрофуране (247 мл 1,0 М раствора, 1,1 экв.) шприцем в атмосфере азота. Полученный желтый раствор оставляют для перемешивания при 0 С в течение 1,5 ч, затем добавляют по каплям через дополнительную воронку раствор 3-циклопентокси-4-метоксибензальдегида (49,4 г; 225 ммоль) в сухом тетрагидрофуране на протяжении 0,5 ч. Полученный оранжевый раствор оставляют для перемешивания при 0 С в течение 2 ч, затем нагревают до температуры окружающей среды и перемешивают на протяжении ночи. Реакционную смесь затем гасят добавлением воды (400 мл) и экстрагируют эфиром (2300 мл). Объединенные органические слои промывают 1 н. водной хлористо-водородной кислотой (250 мл), насыщенным водным раствором бикарбоната (250 мл) и насыщенным раствором соли (250 мл), затем сушат надMgSO4, фильтруют и концентрируют в вакууме, чтобы получить ненасыщенный сложный эфир в виде коричневой жидкости (68,4 г; 100%). 1 Н ЯМР (CDCl3, 400 МГц)7,64 (с, 1 Н), 7,01-6,96 (сл., 2 Н), 6,87 (м, 1 Н), 4,77 (м, 1 Н), 4,26 (кв, 2 Н). Масс-спектрометрия низкого разрешения (LRMS)(Электрораспыление, положительные ионы): Da/e 305,3 (m+1). Примечание: здесь и далее в данных ЯМР "сл." означает сложный сигнал, что соответствует английскому "с" complex signal. Суспензию этилового эфира (Е)-3-(3-циклопентилокси-4-метоксифенил)-2-метилакриловой кислоты (30 г, 98,6 ммоль) и LiOHH2O (гидрат гидроксида лития) (5,0 г, 119,2 ммоль, 1,2 экв.) в смеси метанола и воды (4:1, 100 мл) и перемешивают при температуре окружающей среды в течение 24 ч. Метанол удаляют при пониженном давлении и полученный остаток растворяют в воде (100 мл), промывают тремя порциями по 100 мл этилацетата, нейтрализуют 1,0 н. HCl (хлористо-водородная кислота) (100 мл) и экстрагируют двумя порциями по 150 мл этилацетата. Экстракт промывают насыщенным раствором соли,сушат над безводным Na2SO4 (сульфат натрия) и концентрируют при пониженном давлении с получением желаемого продукта в виде светло-желтого порошка (18,2 г, выход 66%). 1 Н ЯМР (300 МГц, CDCl3)(м.д.): 12,4 (шир. с, 1 Н, СООН), 7,56 (с, 1 Н, олефиновый), 7,04 (м, 3 Н,ароматический), 4,81 (м, 1 Н), 3,78 (с, 3 Н, ОСН 3), 2,06 (с, 3 Н, СН 3), 1,91-1,57 (м, 8 Н, циклопентил). Промежуточный продукт А получают альтернативным способом следующим образом. В перемешиваемый раствор этилового эфира (68,4 г; 225 ммоль) в диоксане (400 мл) добавляют раствор моногидрата гидроксида лития (14,0 г; 332 ммоль; 1,5 экв.) в воде (200 мл) при температуре окружающей среды в атмосфере азота. Наблюдали незначительно выделение тепла. Полученный мутножелтый раствор нагревают до 80 С (масляная ванна) в течение 1,5 ч. Через 0,5 ч после нагревания реакционная смесь становится прзрачной, но требуется еще дополнительно 1,5 ч для завершения реакции, как оценено тонкослойной хроматографией (TLC). Полученный раствор оставляют для охлаждения до температуры окружающей среды, разбавляют эфиром (500 мл), затем промывают 1 М водной фосфорной кислотой (Н 3 РO4). Водный слой затем экстрагируют этилацетатом (2200 мл) и объединенные слои этилацетата и эфира промывают насыщенным раствором соли (250 мл), сушат над MgSO4, затем фильтруют и концентрируют в вакууме с получением промежуточного продукта А в виде оранжевого твердого вещества (55 г; 88%). 1 Н ЯМР (CDCl3, 400 МГц):7,76 (с, 1 Н), 7,06-7,00 (сл, 2 Н), 6,89 (м, 1 Н), 4,78 (м, 1 Н), 3,88 (с, 3H),2,17 (с, 3H), 1,97-1,83 (сл, 6 Н), 1,64-1,61 (сл, 2 Н). Масс-спектрометрия низкого разрешения (LRMS) В охлажденную (0 С) перемешиваемую суспензию промежуточного продукта А (55 г; 199 ммоль) в безводном дихлорметане (400 мл) добавляют шприцем раствор оксалилхлорида в дихлорметане (109 мл 2,0 М раствора; 218 ммоль; 1,1 экв.) в осушенной хлоридом кальция атмосфере на протяжении 10 мин. Наблюдали энергичное выделение пузырьков. Полученный темный раствор оставляют для перемешивания при 0 С в течение 15 мин, затем добавляют шприцем каталитическое количество диметилформамида(0,3 мл). Полученный раствор оставляют для перемешивания при 0 С в течение 0,5 ч между тем, как прекращается выделение пузырьков, и затем оставляют для нагревания до комнатной температуры и перемешивают на протяжении ночи (17 ч). Реакционную смесь разбавляют этилацетатом (500 мл) и осторожно гасят водой (250 мл). После энергичного перемешивания смеси в течение 1 ч слои разделяют, и органический слой промывают дополнительной водой (400 мл) и насыщенным раствором соли (400 мл), затем сушат над MgSO4, фильтруют и концентрируют в вакууме с получением хлорангидрида в виде коричневого твердого вещества (57,5 г; 98%). 1 Н ЯМР (CDCl3, 400 МГц):7,98 (с, 1 Н), 7,11-7,02 (сл, 2 Н), 6,92 (м, 1 Н), 4,79 (м, 1 Н), 3,90 (с, 3H),2,22 (с, 3H), 2,01-1,82 (сл, 6 Н), 1,68-1,62 (сл, 2 Н). В охлажденный (-78 С) механически перемешиваемый раствор R-фенилоксазолидинона (10,0 г,61,3 ммоль) в сухом тетрагидрофуране (400 мл) добавляют шприцем раствор н-бутиллития в гексане (27 мл 2,5 М раствора; 1,1 экв.) в атмосфере азота. Полученный раствор оставляют для перемешивания при-78 С в течение 0,8 ч, затем добавляют канюлей раствор хлорангидрида (19,9 г; 67,4 ммоль; 1,1 экв.) в тетрагидрофуране (100 мл). После перемешивания при -78 С в течение 15 мин реакционную смесь оставляют для медленного нагревания до 0 С на протяжении 40 мин, за это время реакционная смесь превращается в густую суспензию. После перемешивания при 0 С в течение 2,5 ч реакционную смесь гасят насыщенным водным раствором хлорида аммония (300 мл) и объем тетрагидрофурана удаляют при пониженном давлении. Остаток экстрагируют хлороформом (3700 мл) и объединенные органические слои промывают водой (300 мл) и насыщенным раствором соли (300 мл), затем сушат над MgSO4, фильтруют и концентрируют в вакууме с получением 33 г светло-оранжевого твердого вещества. Этот материал суспендируют в 10% растворе этилацетата в гексане (1,2 л) и энергично перемешивают на протяжении ночи. Полученное твердое вещество в виде тонкодисперсного порошка собирают на воронке Бюхнера с отсасыванием и сушат в вакууме с получением промежуточного продукта В в виде желтоватокоричневого порошка (21,8 г; 88%). 1 Н ЯМР (CDCl3, 400 МГц):7,41-7,37 (сл, 5 Н), 7,06 (с, 1 Н), 7,01-6,97 (сл, 2 Н), 6,86 (м, 1 Н), 5,54 (т,1 Н), 4,77-4,73 (сл, 2 Н), 4,29 (т, 1 Н), 3,87 (с, 3H), 2,17 (с, 3H), 1,97-1,82 (сл, 6 Н), 1,62-1,56 (сл, 2 Н). Подобным образом может быть получен энантиомер промежуточного продукта В с использованием В охлажденную (-4 С) перемешиваемую суспензию промежуточного продукта В (9,30 г; 22,8 ммоль) и N-(метоксиметил)-N-(триметилсилилметил)бензиламина (11,7 мл; 45,6 ммоль; 2 экв.) в хлороформе (65 мл) добавляют шприцем раствор трифторуксусной кислоты в хлороформе (4,6 мл 1,0 М раствора; 4,6 ммоль; 0,2 экв.) в атмосфере азота. Полученную суспензию оставляют для перемешивания приблизительно при 0 С в течение 4 ч и затем приблизительно при 15 С на протяжении ночи (водяная баня). Полученный мутный раствор затем повторно охлаждают до -4 С и обрабатывают дополнительным количеством N-(метоксиметил)-N-(триметилсилилметил)бензиламина (5,9 мл; 22,8 моль; 1 экв.) с помо- 28007589 щью шприца и оставляют для перемешивания в течение 5 ч, за это время реакционная смесь становится гомогенной. Тонкослойная хроматография (TLC) (5% Et2O в CH2Cl2) показывает, что реакция завершена. Объем хлороформа удаляют при пониженном давлении и остаток разбавляют этилацетатом (250 мл),затем промывают последовательно 1 н. водной хлористо-водородной кислотой (250 мл), 1 н. водным гироксидом натрия (50 мл) и насыщенным раствором соли (50 мл). Органический слой затем сушат надMgSO4, фильтруют и концентрируют в вакууме с получением оранжевого полутвердого вещества (13,9 г). Очистка флэш-хроматографией на силикагеле (2% эфир в дихлорметане) приводит к получению в качестве главного компонента диастереомерного пирролидина в виде белой пены (8,25 г; 65%). Диастереомерная селективность приблизительно 10:1 (ВЭЖХ). 1 Н ЯМР (CDCl3, 400 МГц):7,427,21 (сл, 10 Н), 6,95 (с, 1 Н), 6,81 (с, 2 Н), 5,55 (дд, 1 Н), 4,74 (т, 1 Н), 4,68 (м, 1 Н), 4,10 (дд, 1 Н), 3,93 (т, 1 Н),3,70 (д, 1 Н), 3,68 (с, 3H), 3,56 (д, 1 Н), 3,42 (д, 1 Н), 2,72 (м, 2 Н), 2,64 (д, 1 Н), 2,48 (м, 1 Н), 1,85-1,78 (сл,2 Н), 1,75-1,61 (сл, 4 Н), 1,57-1,53 (сл, 2 Н), 0,96 (с, 3H). Масс-спектрометрия низкого разрешения(Электрораспыление, положительные ионы): Da/e 555,2 (m+1). Промежуточный продукт D. Получение (3S,4S)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-1 бензилпирролидин-3-карбальдегида. Процедура восстановления/окисления. В охлажденный (-78 С) перемешиваемый раствор промежуточного продукта С (15,09 г; 27,2 ммоль) в толуоле (250 мл) добавляют шприцем раствор гидрида литияалюминия в тетрагидрофуране (16,3 мл; 1,0 М; 16,3 ммоль; 0,6 экв.) в атмосфере азота. Наблюдают энергичное выделение пузырьков. Полученный раствор оставляют для перемешивания при -78 С в течение 2 ч, затем охлаждающую ванну удаляют и гасят раствор последовательным добавлением воды (0,62 мл),15% водного гидроксида натрия (0,62 мл) и дополнительной водой (1,9 мл). Полученную смесь оставляют для нагревания до комнатной температуры, перемешивают в течение 30 мин и затем разбавляют эфиром (500 мл) и сушат над MgSO4. Фильтрование и концентрирование в вакууме позволяет получить спирт (с некоторым присутствием альдегида) в виде полутвердого вещества (14,8 г). Этот материал используют сразу без дополнительной очистки. В охлажденный (-78 С) перемешиваемый раствор оксалилхлорида в дихлорметане (10,9 мл; 2,0 М; 21,8 ммоль; 0,8 экв.) в дополнительном количестве дихлорметана (75 мл) добавляют шприцем диметилсульфоксид (3,1 мл; 43,5 ммоль; 1,6 экв.) в атмосфере азота. Наблюдали энергичное выделение пузырьков. После перемешивания при -78 С в течение 20 мин добавляют с помощью канюли раствор неочищенного спирта в дихлорметане (75 мл). Полученный желтый раствор оставляют для перемешивания при-78 С в течение 20 мин, затем добавляют шприцем триэтиламин (15,2 мл; 109 ммоль; 4 экв.). Реакционную смесь оставляют для перемешивания при -78 С в течение 20 мин, затем нагревают до комнатной температуры и перемешивают дополнительно в течение 1 ч. Реакционную смесь гасят дополнительным насыщенным раствором соли (150 мл), затем экстрагируют дихлорметаном (2100 мл). Объединенные органические фракции сушат над MgSO4, фильтруют, затем концентрируют в вакууме с получением неочищенного альдегида. Очистка флэш-хроматографией на силикагеле (25% этилацетат в гексане) позволяет получить промежуточный продукт D в виде прозрачного бесцветного масла (9,8 г; 92%). 1 Н ЯМР (CDCl3, 400 МГц):9,64 (с, 1 Н), 7,37-7,26 (сл, 5 Н), 6,78-6,76 (сл, 2 Н), 6,70 (м, 1 Н), 4,74 (м,1 Н), 3,82 (с, 3H), 3,70 (м, 1 Н), 3,64-3,62 (сл, 2 Н), 3,18-3,13 (сп, 2 Н), 2,84 (т, 1 Н), 2,41 (д, 1 Н), 1,94-1,83 (сл,6 Н), 1,63-1,59 (сл, 2 Н), 0,74 (с, 3H). Масс-спектрометрия низкого разрешения(Электрораспыление, положительные ионы): Da/e 394,3 (m+1). Промежуточный продукт 1. Получение метилового эфира 4-(S)-(циклопентилокси-4-метоксифенил)-3-(S)-формил-3-метилпирролидин-1-карбоновой кислоты. Промежуточный продукт D растворяют в ацетонитриле (4,8 мл) и обрабатывают метилхлорформиатом (176 мкл, 2,3 ммоль). Полученный раствор нагревают для кипячения с обратным холодильником в течение 4 ч, тонкослойная хроматография указывает на полное расходование промежуточного продуктаD. Реакционную смесь затем концентрируют в вакууме и очищают непосредственно колоночной хроматографией на SiO2 с использованием смеси гексан/этилацетат (3:1) в качестве элюента. Промежуточный продукт 1 извлекают в виде светло-желтого масла (110 мг).(шир. с, 1 Н), 3,94-3,64 (м, 3H), 3,83 (с, 3H), 3,76 (с, 3H), 3,62-3,55 (м, 1 Н), 3,38-3,28 (дд, 1 Н), 1,95-1,75 (м,6 Н), 1,66-1,57 (м, 2 Н), 0,91 (с, 3H). Следующее ниже иллюстрирует синтез различных промежуточных продуктов и соединений структурной формулы (II). Следующие ниже примеры предназначены для пояснения и не должны рассматриваться как ограничительные. В примерах использованы следующие аббревиатуры: NaOH (гидроксид натрия), CH2Cl2 (дихлорметан), Na2SO4 (сульфат натрия), EtOAc (этилацетат), Ph (фенил), МеОН (метанол), К 2 СO3 (карбонат калия), mmol (микромоль), atm (атмосфера), MgSO4 (сульфат магния), LiOH (гидроксид лития), N (нормальный), mmol (миллимоль), mL (миллилитр) и Н 3 РO4 (фосфорная кислота). Следующие ниже процедуры использованы для осуществления примеров 1-28. Процедура восстановительного аминирования. В перемешиваемый раствор альдегида (0,24 ммоль) в дихлорэтане (1 мл) добавляют бензиламин(0,24 ммоль) с последующим добавлением триацетоксиборгидрида натрия (0,34 ммоль) при комнатной температуре в атмосфере азота. После перемешивания в течение 5 ч реакционную смесь разбавляют 1 н. водным раствором NaOH (0,3 мл) и CH2Cl2 (10 мл). Слои разделяют и экстрагируют водный слой дополнительным количеством 5 мл CH2Cl2. Объединенные органические слои затем промывают водой и насыщенным раствором соли, сушат (Na2SO4), фильтруют и концентрируют в вакууме. Остаток очищают флэш-хроматографией (3:2 EtOAc:гексан на силикагеле) с получением продукта. Процедура гидрирования. Перемешиваемый раствор исходного материала (75 мкмоль) в 95% этаноле (1 мл) обрабатывают катализатором Pearlman (гидроксид палладия на угле, 10 мг), затем помещают в атмосферу водорода (1 атм). После перемешивания при комнатной температуре в течение 24 ч реакционную смесь фильтруют через фильтровальную бумагу GF/F с отсасыванием на воронке Бюхнера и промывают 20 мл 95% этанола. Концентрирование фильтрата позволяет получить продукт. Процедура сульфонилирования. В перемешиваемый раствор исходного материала (0,1 ммоль) в 1,4-диоксане (0,3 мл) добавляют последовательно водный К 2 СO3 (0,6 мл 0,65 М раствора; 4 экв.) и раствор сульфонилхлорида (0,12 ммоль) в 1,4-диоксане (0,3 мл) при комнатной температуре. Полученный раствор оставляют для перемешивания при комнатной температуре в течение 2 ч. Реакционную смесь разбавляют смесью 1:1 гексан:EtOAc (30 мл) и промывают последовательно водой (20 мл) и насыщенным раствором соли (20 мл), затем сушат(MgSO4), фильтруют и концентрируют в вакууме с получением сульфонамида. Процедура ацилирования с основания Хюнига. В перемешиваемый раствор исходного материала (0,14 ммоль) и основания Хюнига (0,20 ммоль) в сухом CH2Cl2 (1 мл) добавляют шприцем хлорангидрид (0,14 ммоль) при комнатной температуре в атмосфере азота. После перемешивания в течение 1 ч реакционную смесь разбавляют CH2Cl2 (30 мл) и промывают последовательно 1 н. водным раствором HCl (210 мл) и насыщенным раствором соли (10 мл),затем сушат (Na2SO4), фильтруют и концентрируют в вакууме. Остаток очищают радиальной хроматографией (пластинка 1 мм хроматотрона с 3% МеОН в CH2Cl2) с получением амида. Пример 1.R=CH2Ph Метил(4S,3R)-4-(3-циклопентилокси-4-метоксифенил)-3-метил-3-[бензиламино]метилпирролидинкарбоксилат. Получают процедурой восстановительного аминирования. 1 Н ЯМР (CDCl3, 400 МГц; смесь ротомеров) : 7,34-7,28 (м, 5 Н), 6,77 (д, 1 Н), 6,67-6,64 (м, 2 Н), 4,70
МПК / Метки
МПК: A61P 37/00, A61P 25/00, C07D 207/09, A61P 35/00, A61K 31/40, C07D 207/16
Метки: цамф-специфичную, пирролидины, ингибируют, которые
Код ссылки
<a href="https://eas.patents.su/30-7589-pirrolidiny-kotorye-ingibiruyut-camf-specifichnuyu-pde.html" rel="bookmark" title="База патентов Евразийского Союза">Пирролидины, которые ингибируют цамф-специфичную pde</a>
Предыдущий патент: Способ очистки пестицидов
Следующий патент: Производные тропана в качестве модуляторов ссr5
Случайный патент: Система и способ управления основным блоком и множеством вспомогательных блоков