Замещенные тиоацетамиды
Номер патента: 6135
Опубликовано: 27.10.2005
Авторы: Чаттерджи Санкар, Вот Джеффри Л., Миллер Мэттью С., Данн Дерек, Бэйкон Эдвард Р., Малламо Джон П.
Формула / Реферат
1. Соединение формулы (I-A)
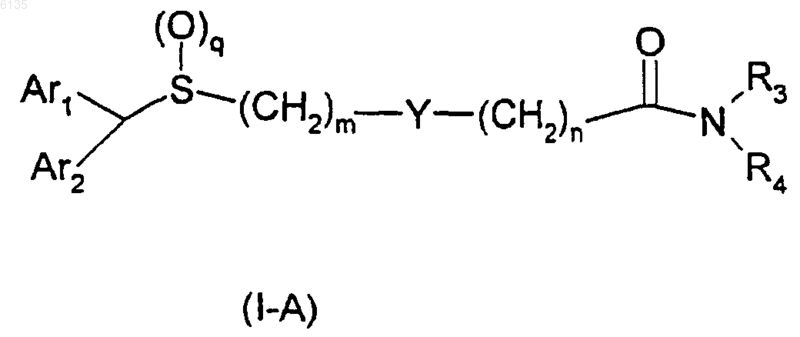
где Ar1 и Ar2, каждый независимо, выбраны из группы, включающей фенил, тиенил, изотиазолил, оксазолил, изоксазолил и тиазолил;
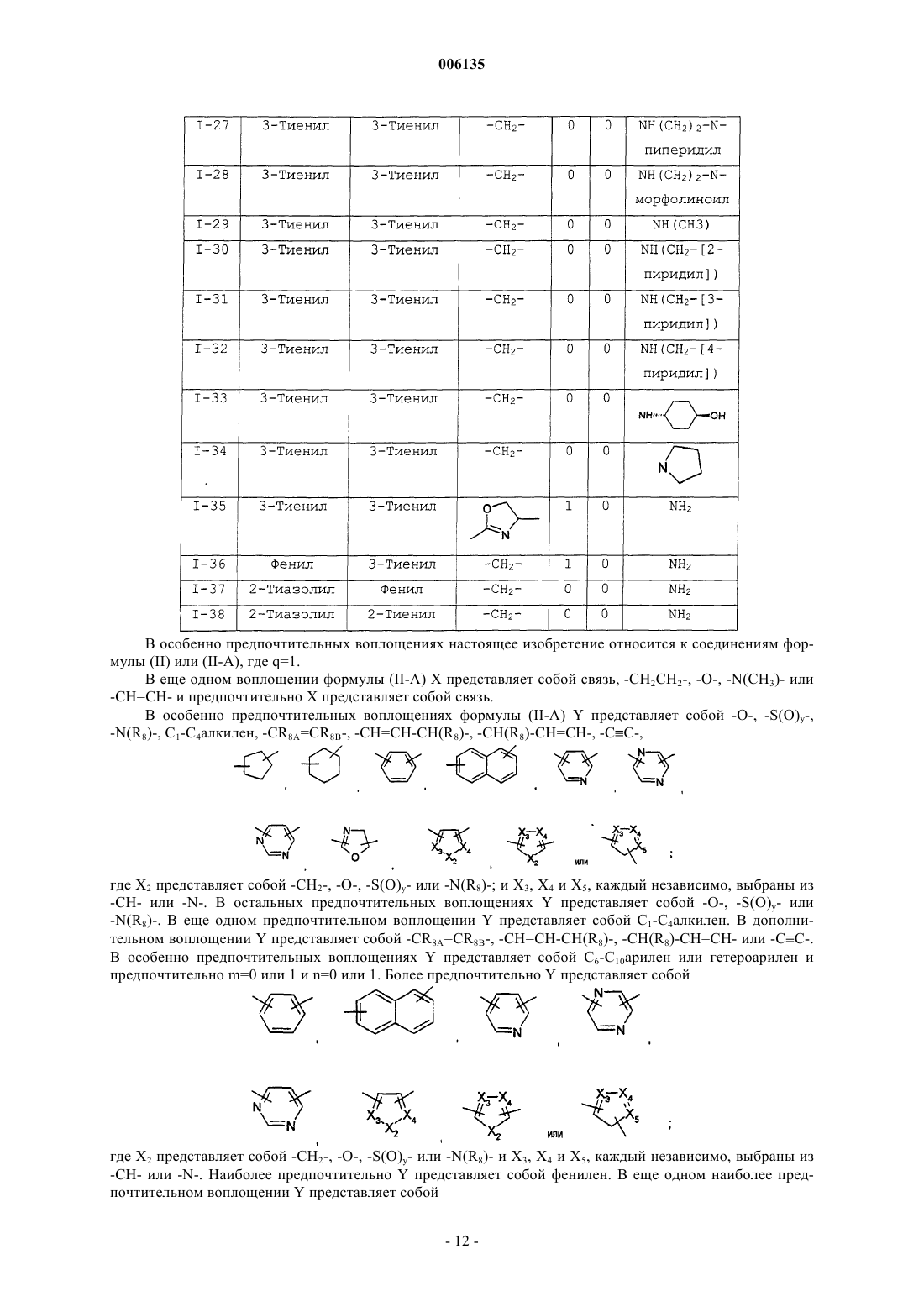
Y выбран из C1-C4 алкилена, -C(R1)(R2)-, фенилена и оксазолилена, где R1 и R2, каждый независимо, представляют собой H или C1-C6 алкил;
R3 и R4 являются одинаковыми или различными и каждый выбраны из группы, включающей H, C1-C6 алкил, где указанный алкил необязательно замещен OH или гетероциклильным кольцом, выбранным из пиперидинила, морфолинила и пиридила; или R3 и R4 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное морфолинильное или пирролидильное кольцо;
m равно 0, 1 или 2;
n равно 0, 1 или 2;
q равно 1;
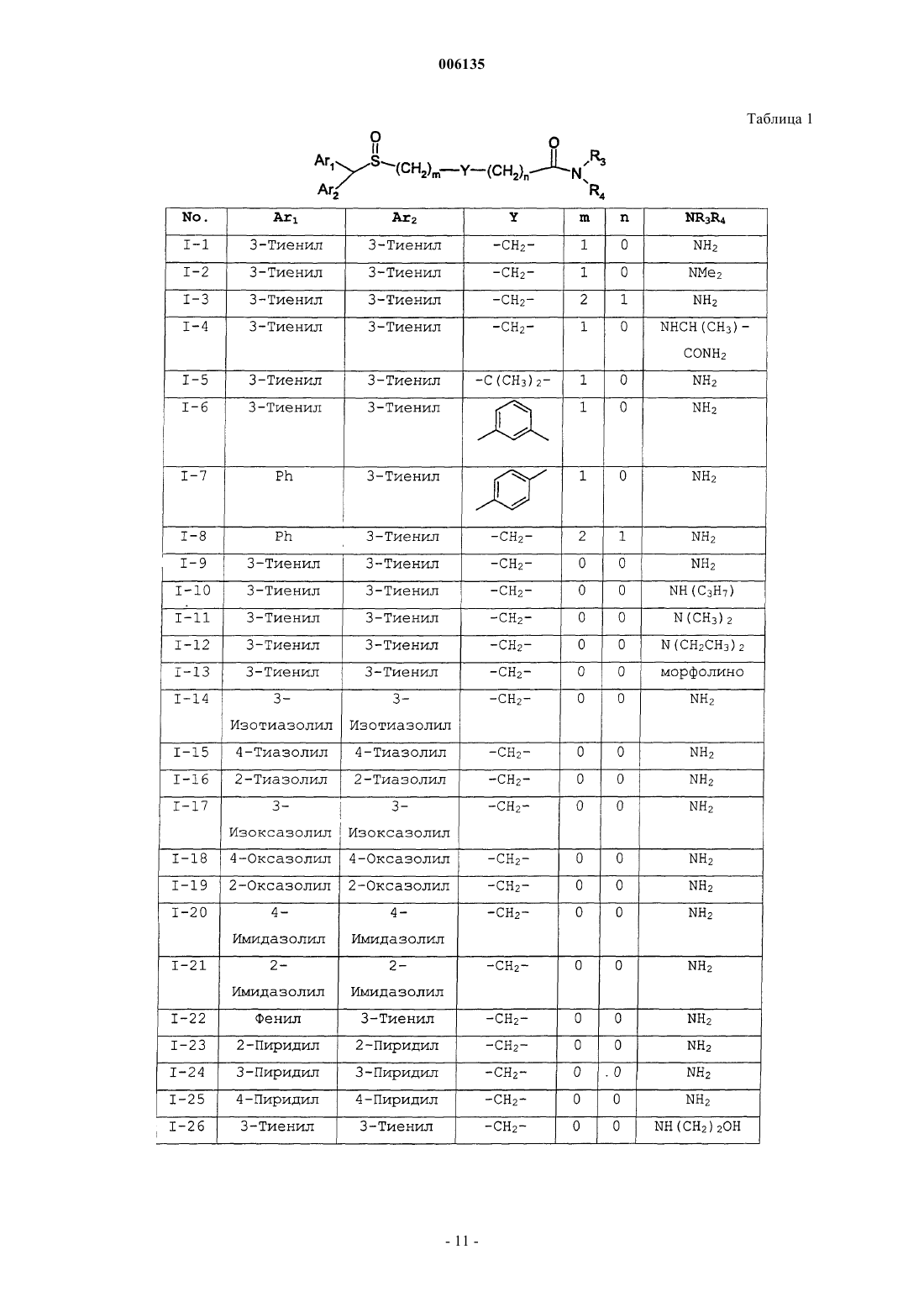
при условии, что когда Ar1 и Ar2 оба представляют собой фенил, тогда Y не может быть C1-C4 алкиленом;
и его стереоизомерные формы, смеси стереоизомерных форм или фармацевтически приемлемая соль и сложный эфир.
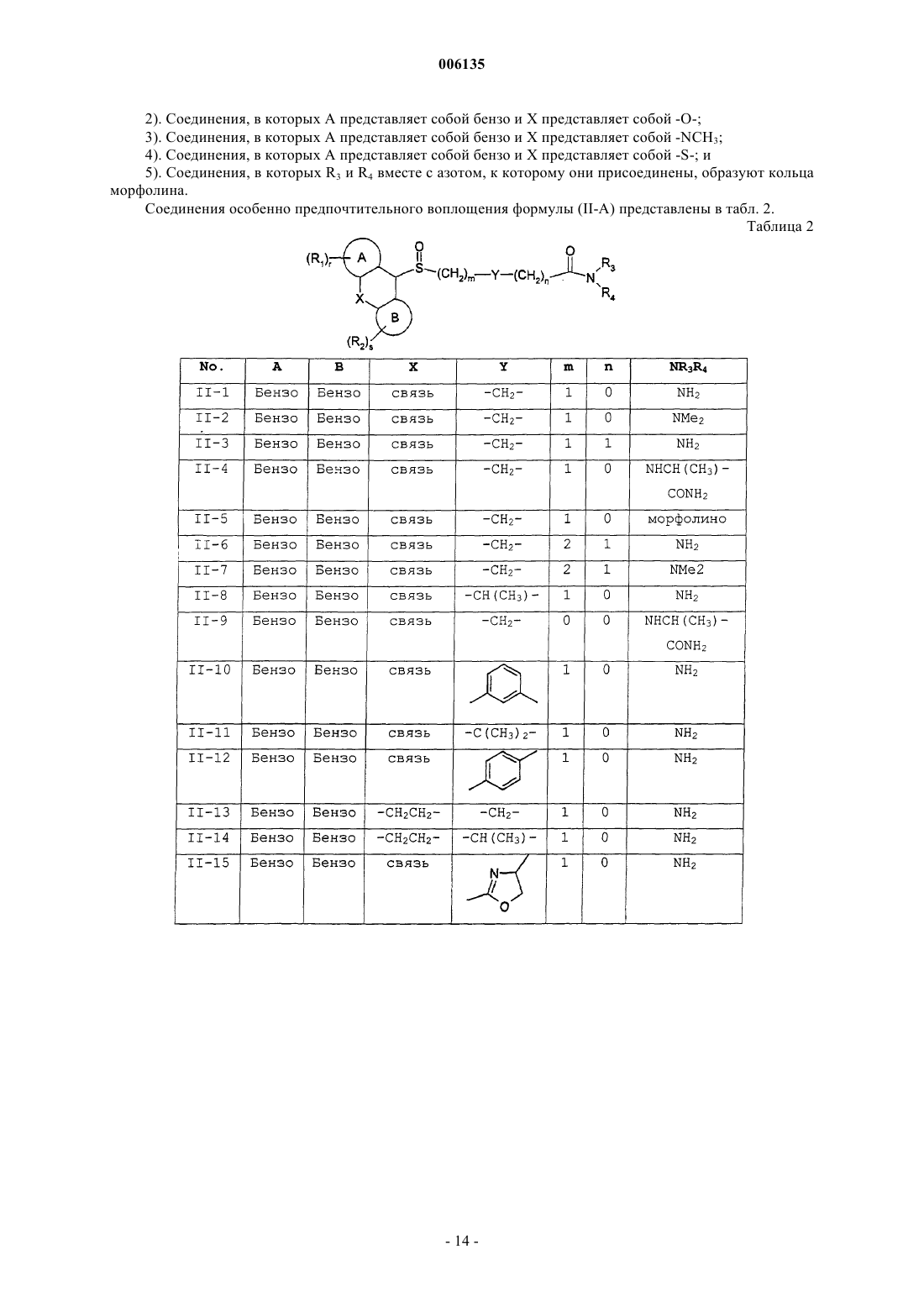
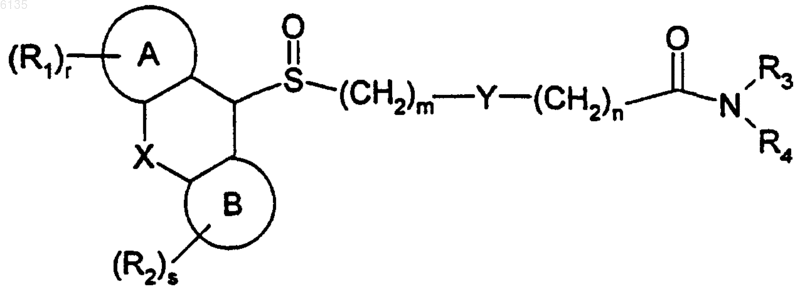
2. Соединение формулы (II-A)
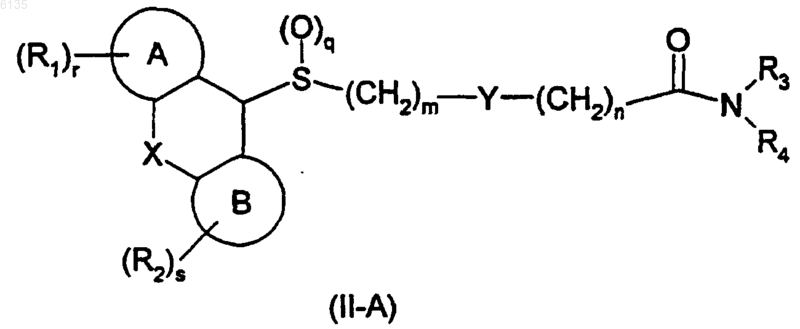
где X представляет собой связь, -CH2CH2-, -O-, -N(R8)- или -CH=CH-;
кольца A и B вместе с атомами углерода, к которым они присоединены, каждый независимо, выбраны из группы, включающей
a) фенилен и
b) 5-членное ароматическое карбоциклическое кольцо, в котором два атома углерода заменены двумя атомами азота;
R1 и R2, каждый независимо, выбраны из H и фенильного кольца, необязательно замещенного 0-2 метоксигруппами;
R3 и R4 являются одинаковыми или различными и каждый выбран из группы, включающей H, C1-C6 алкил и -CH(R6)-CONR8AR8B, где указанный алкил необязательно замещен OH или гетероциклильным кольцом, выбранным из пиперидинила, морфолинила и пиридила; или R3 и R4 вместе с атомом азота, к которому они присоединены, образуют необязательно замещенное морфолинильное или пирролидильное кольцо;
R6 представляет собой H или C1-C4 алкил;
R8, R8A и R8B, каждый независимо, представляют собой H, C1-C4 алкил или C6-C10 арил;
Y выбран из C1-C4 алкилена, -CH=CH-, фенилена, оксазолилена, фурилена, тиазолилена и -C(R14)(R15), где R14 и R15, каждый независимо, представляют собой H или C1-C6 алкил;
m равно 0, 1 или 2;
n равно 0, 1 или 2;
q равно 1;
r равно 0, 1 или 2 и
s равно 0, 1 или 2;
и его стереоизомерные формы, смеси стереоизомерных форм или фармацевтически приемлемая соль и сложный эфир.
3. Соединение по п.1, где Ar1 и Ar2, каждый независимо, выбраны из тиенила, изотиазолила, оксазолила, изоксазолила и тиазолила.
4. Соединение по п.3, где Ar1 и Ar2 представляют собой 3-тиенил.
5. Соединение по п.1, где Ar1 представляет собой фенил и Ar2 выбран из тиенила, изотиазолила, оксазолила, изоксазолила и тиазолила.
6. Соединение по п.1, где Ar1 и Ar2 представляют собой фенил.
7. Соединение по п.1, где Y представляет собой фенилен или тиазолилен.
8. Соединение по п.7, где Y представляет собой фенилен.
9. Соединение по п.1, где Y представляет собой C1-C4 алкилен.
10. Соединение по п.1, где Y представляет собой C(R1)(R2), где R1 и R2, каждый независимо, представляют собой H или C1-C6 алкил; и m и n=0.
11. Соединение по п.1, где Ar1 и Ar2, каждый независимо, выбраны из группы, включающей фенил и 3-тиенил.
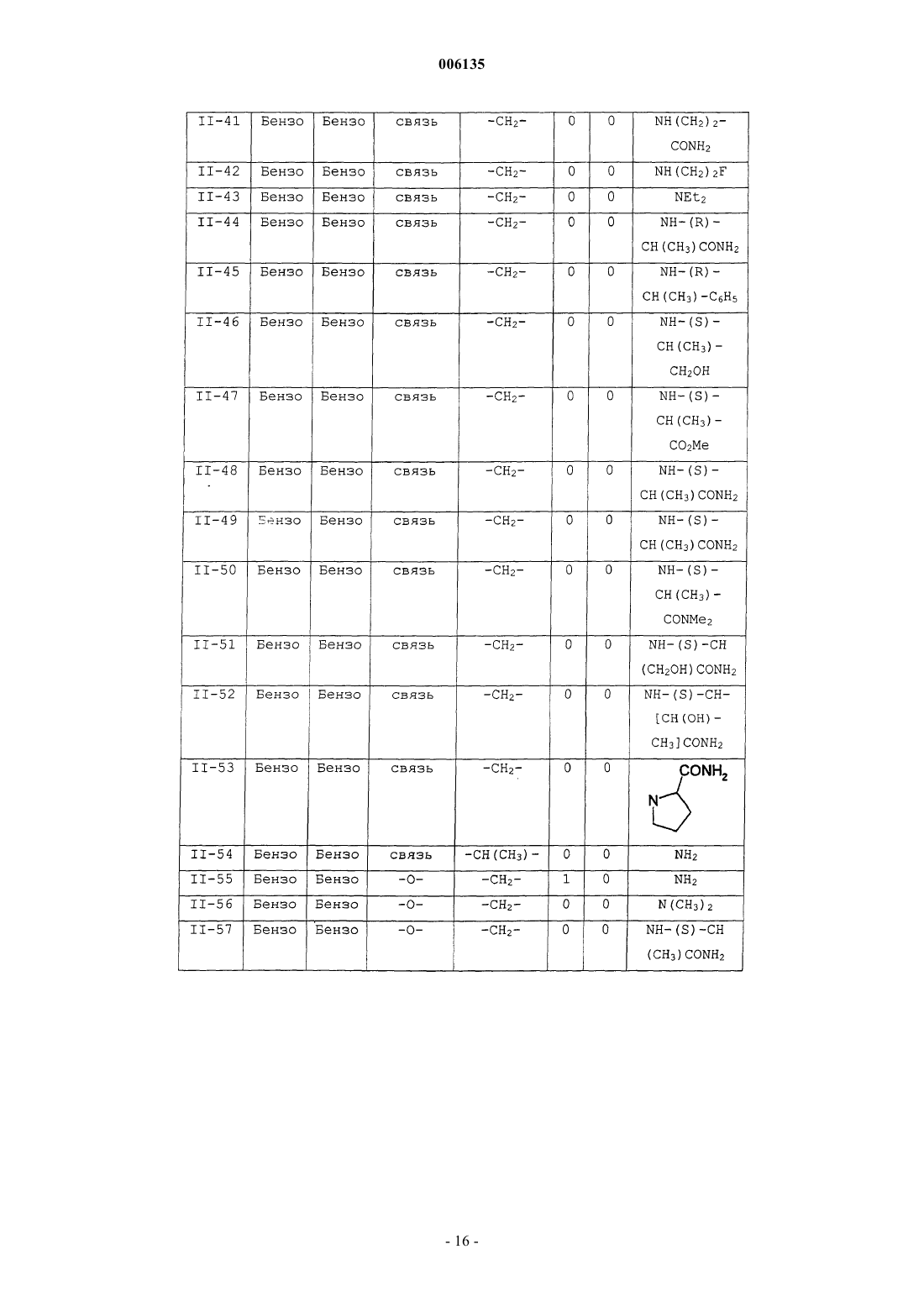
12. Соединение по п.1, где соединения выбраны в соответствии со следующей таблицей:
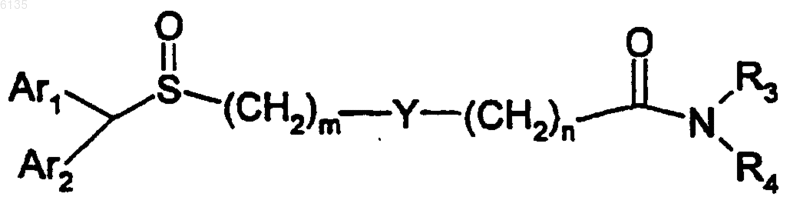
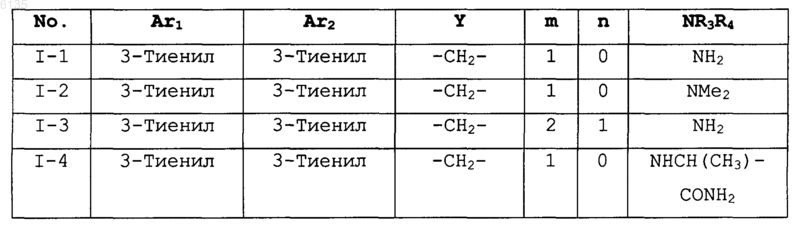
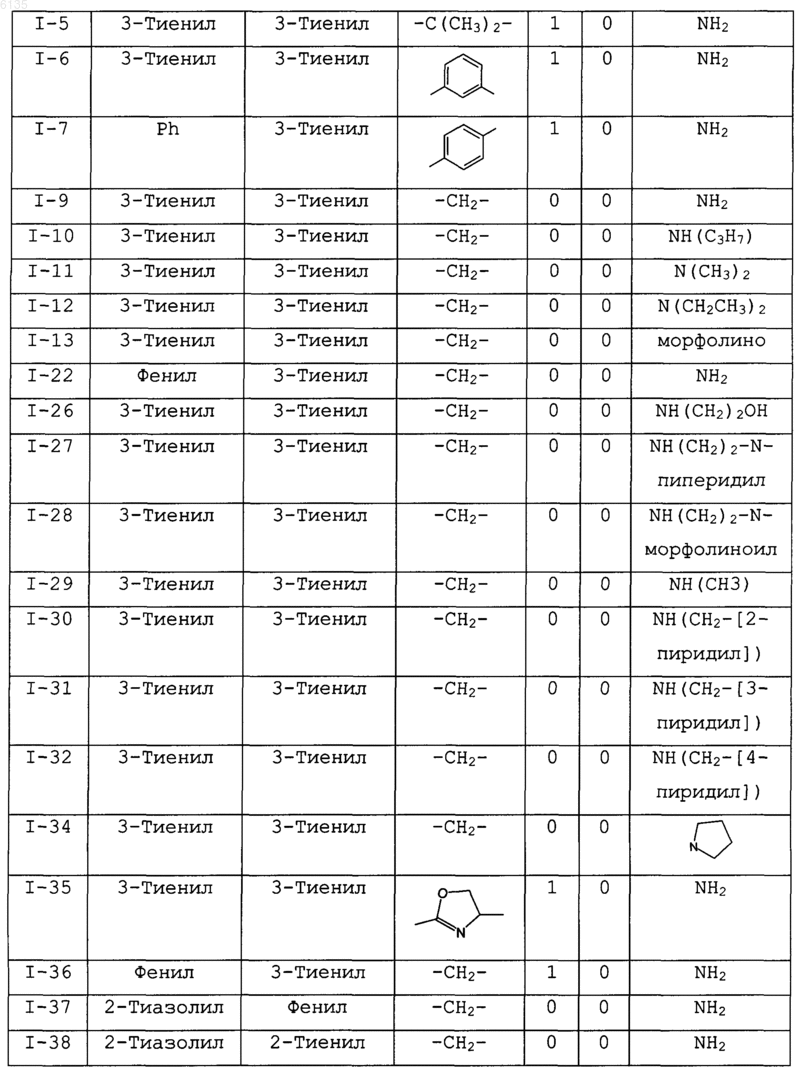
13. Соединение по п.2, где кольцо A представляет собой фенилен.
14. Соединение по п.13, где кольцо B представляет собой фенилен.
15. Соединение по п.2, где Y представляет собой фенилен.
16. Соединение по п.2, где Y представляет собой C1-C4 алкилен.
17. Соединение по п.2, где Y представляет собой C(R14)(R15), где R14 и R15, каждый независимо, представляют собой H или C1-C6 алкил; и m и n=0.
18. Соединение по п.17, где X представляет собой связь и Y представляет собой -CH2-.
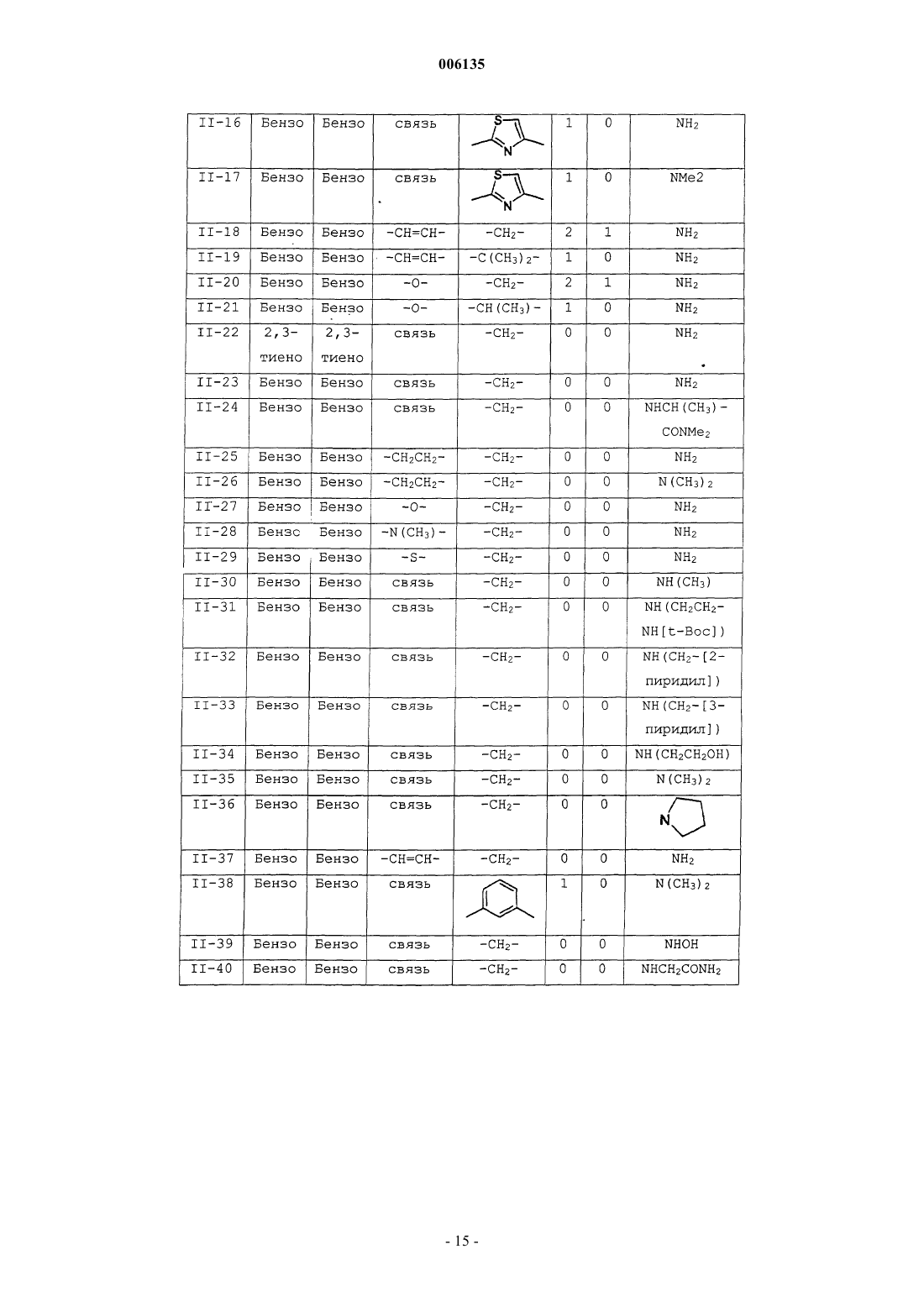
19. Соединение по п.2, где соединения выбраны в соответствии со следующей таблицей:
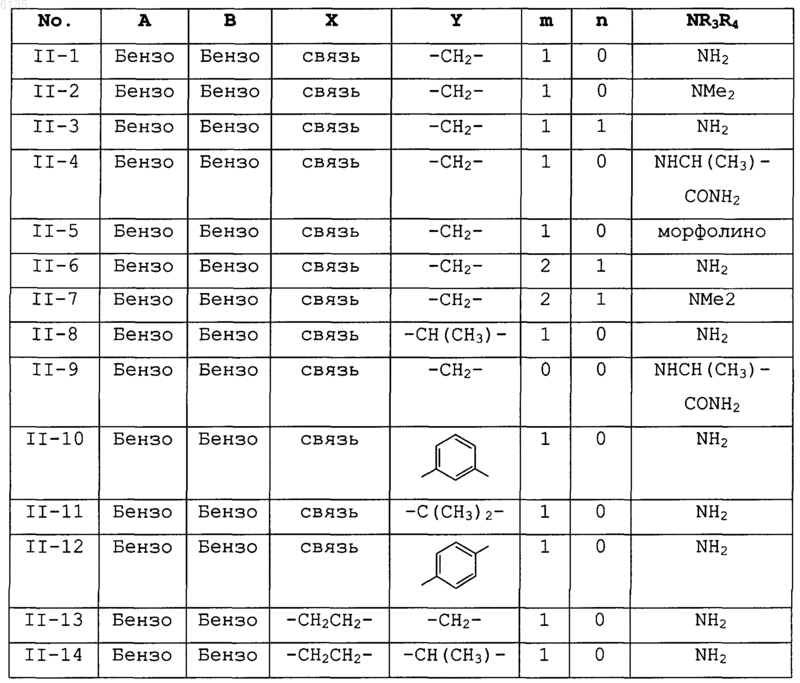
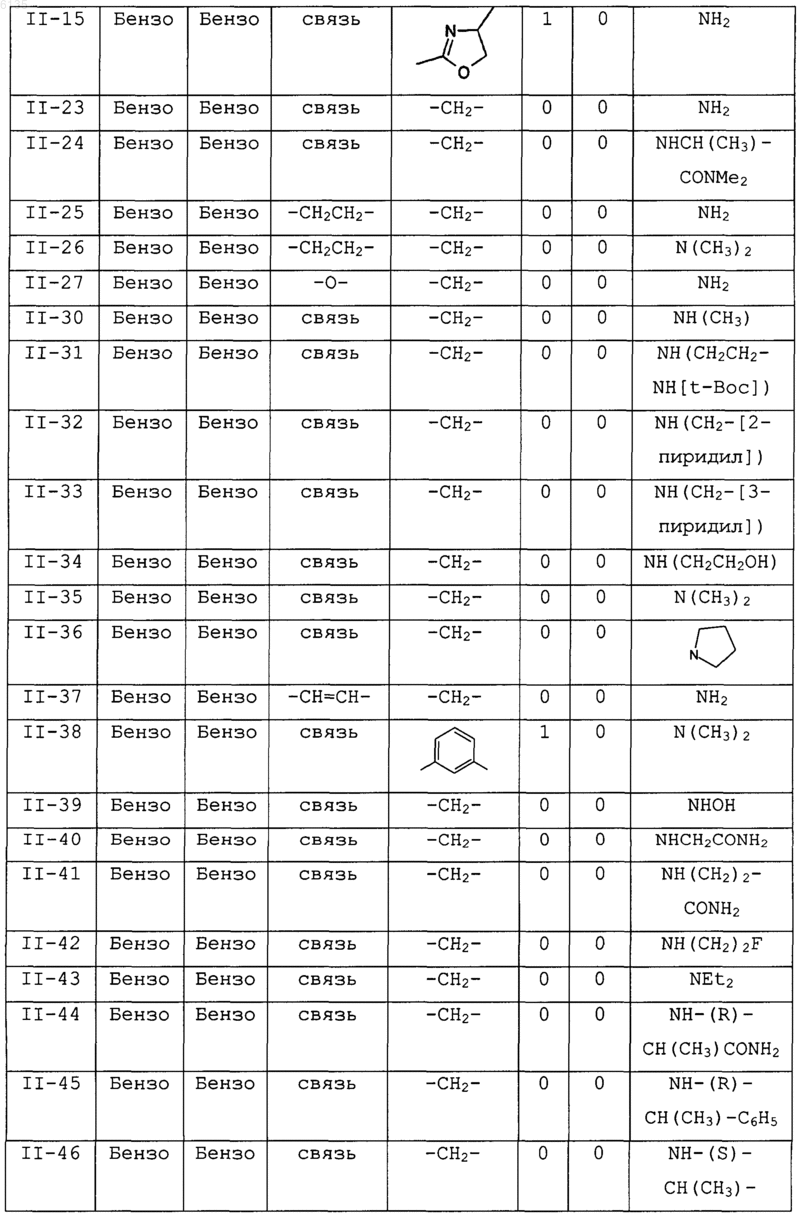
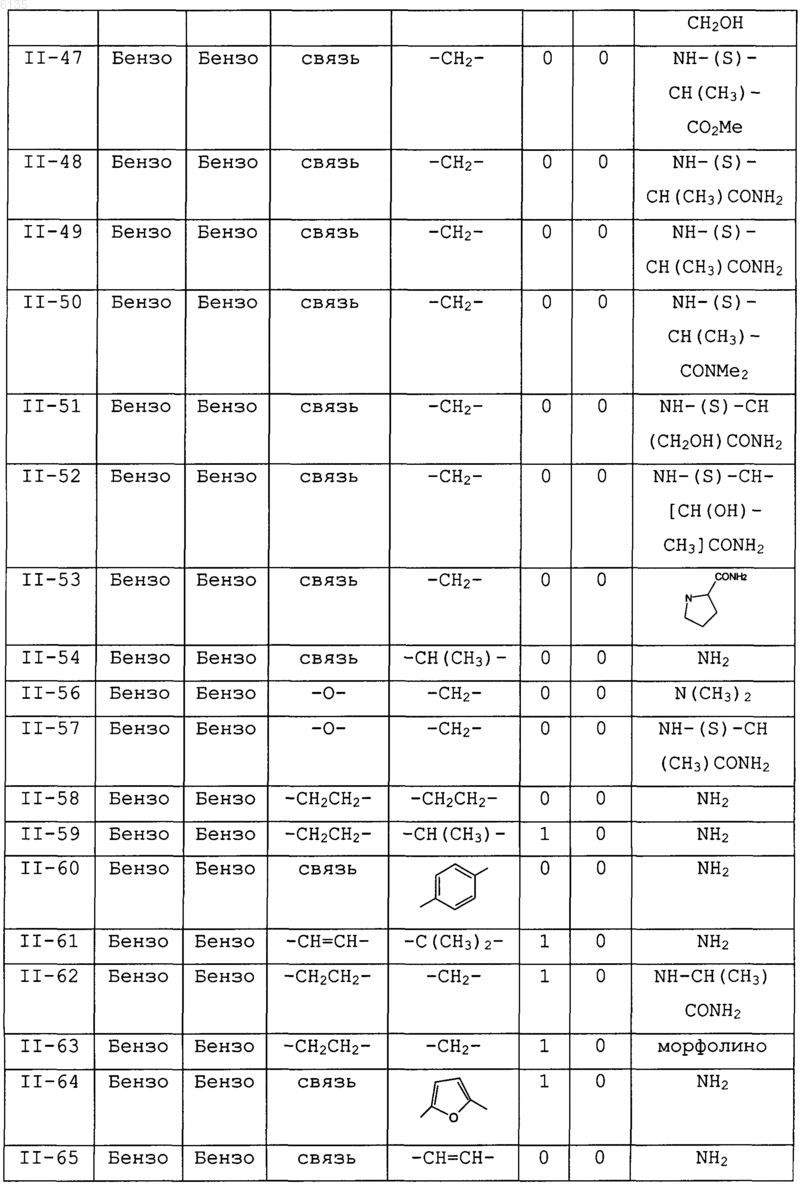
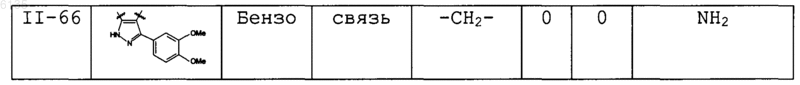
20. Соединение по п.2, где кольцо A выбрано из фенила и имидазола.
21. Соединение по любому из пп.1-19 для применения в фармации.
22. Применение соединения по любому из пп.1-19 при получении лекарственного средства для
a) лечения бессонницы, слабости, болезни Паркинсона, церебральной ишемии, удара, остановки дыхания во сне, пищевых нарушений, синдрома гиперактивности-дефицита внимания, нарушения познавательной способности, усталости, депрессии, шизофрении, синдрома хронической усталости или заболеваний, ассоциированных с гипофункциональностью коры головного мозга;
b) поддержания бодрствования или
c) стимуляции аппетита или повышения веса.
23. Фармацевтическая композиция, содержащая соединение по любому из пп.1-19 в смеси с одним или несколькими фармацевтически приемлемыми эксципиентами.
Текст
006135 Область изобретения Настоящее изобретение относится к химическим композициям, способам их получения и к применению этих композиций. В частности, настоящее изобретение относится к композициям, включающим замещенные тиоацетамиды, и их применению при лечении заболеваний, в том числе при лечении сонливости, при стимулировании бодрствования, при лечении болезни Паркинсона, мозговой ишемии, инсульта, апноэ во время сна, нарушения питания, при стимуляции аппетита и увеличения веса, при лечении синдрома гиперактивности-дефицита внимания (ADHD), при усилении функции при расстройствах,связанных с гипофункцией коры головного мозга, включая, но ими не ограничиваясь, депрессию, шизофрению, усталость, в частности усталость, ассоциированную с неврологическим заболеванием, таким как рассеянный склероз, синдром хронической усталости, и при улучшении познавательной функции при ее нарушении. Предпосылки настоящего изобретения Соединения, описанные здесь, относятся к биологическим и химическим аналогам модафинила. Модафинил, C15H15NO2S, также известный как 2-(бензгидрилсульфинил)ацетамид или 2[(дифенилметил)сульфинил]ацетамид, является синтетическим производным ацетамида со способностью стимулировать бодрствование, структура которого описана в патенте Франции 7805510 и в патенте США 4177290 (290) и который был одобрен управлением по контролю за продуктами и лекарствами США для применения при лечении повышенной дневной сонливости, связанной с нарколепсией. Как описано в указанных патентах, модафинил был испытан для возможности лечения нескольких поведенческих состояний в комбинации с различными агентами, в том числе апоморфином, амфетамином, резерпином, оксотреморином, гипнотиками, йохимбином, 5-гидрокситриптофаном и ингибиторами моноаминоксидазы. Способ получения рацемической смеси описан в патенте '290, и способ получения левовращающего изомера описан в патенте США 4927855 (оба приведены здесь в качестве ссылки). Сообщалось, что левовращающий изомер может быть использован для лечения гиперсомнии, депрессии,болезни Альцгеймера и что он обладает активностью в отношении симптомов деменции и потери памяти, особенно у пожилых людей. Основная фармакологическая активность модафинила заключается в стимулировании бодрствования. Модафинил стимулирует бодрствование у крыс (Touret et al., 1995; Edgar и Seidel, 1997), котов (Linet al., 1992), собак (Shelton et al., 1995) и млекопитающих, за исключением человека (Hernant et al, 1991),а также на моделях, воспроизводящих клинические ситуации, таких как апноэ во время сна (модель нарушения дыхания во время сна у английского бульдога) (Panckeri et al., 1996) и нарколепсия (на собаках с нарколепсией) (Shelton et al., 1995). Модафинил также был описан как средство, обладающее активностью по отношению к центральной нервной системе, и как средство, которое может быть использовано при лечении болезни Паркинсона (патент США 5180745); для защиты ткани мозга от ишемии (патент США 5391576); при лечении недержания мочи и кала (патент США 5401776); для предотвращения апноэ во время сна и для лечения расстройств, связанных с центральной нервной системой (патент США 5612379). В патенте США 5618845 описаны лекарственные препараты модафинила с частицами определенного размера менее 200 мкм. Кроме того, модафинил может быть использован для лечения расстройств питания, для увеличения веса или для стимуляции аппетита у людей и животных (предварительная заявка на патент США 60/150171 или опубликованная 1.03.2001 WO 01/13906 А 2, приведена здесь в качестве ссылки), при лечении синдрома гиперактивности-дефицита внимания (ADHD) или усталости, особенно усталости,ассоциированной с рассеянным склерозом (патент США 6346548, подан 15.08.2000, приведен здесь в качестве ссылки). В нескольких опубликованных патентных заявках описаны производные формы модафинила и применение производных модафинила при лечении различных расстройств. Например, в публикации РСТ WO 99/25329 описаны аналоги модафинила, в которых фенильные группы замещены F, Сl, Вr, СF3,NO2, NH2, C1-C4 алкилом, C1-C4 алкокси или метилендиокси и в которых амид замещен ОН, C1-C4 алкилом,C1-C4 гидроксиалкилом или C1-C4 углеводородным радикалом. Эти композиции описаны для применения при лечении сонливости, вызванной приемом лекарств, особенно сонливости, связанной с введением морфина больным раком. Аналогично, в патенте США 4066686 описаны производные бензгидрилсульфинила, в том числе производные модафинила с алкильной связью между сульфонильной и карбонильной группами, и в которых NR3R4 представляет собой NHOH. Эти соединения описаны для использования при лечении нарушений центральной нервной системы. В публикации РСТ WO 95/01333 описаны производные модафинила, которые применяются для изменения режима питания. Описанные модификации модафинила включают группу хлор в 3 положении одной из фенильных групп и заместитель пиридил во втором фениле, замену одной или двух метильных групп водородом по 2 атому углерода одной или двумя метильными группами, водороды амида могут быть замещены одной или двумя группами, выбранными из Н, пиридилметильной или этильной групп,и, кроме того, атом серы может быть неокислен.-1 006135 В публикации РСТ WO 95/01171 также описаны модифицированные соединения модафинила, которые, как утверждается, могут быть использованы для изменения режима питания. Описанные соединения содержат 4-фтор-, 3-фтор- и 4-хлор-заместители в первой фенильной группе и 4-фтор- или 3-фторзаместители во втором фениле. Также были описаны заместители, в которых амид содержит заместители с ОН или с изопропильной группой.Terauchi, Н., et al. описали производные никотинамида, которые могут использоваться в качестве ингибиторов АТФ-азы (Terauchi, Н., et al., J. Med. Chem., 1997, 40, 313-321). В частности, было описано несколько N-алкилзамещенных 2-(бензгидрилсульфинил)никотиамидов. В патентах США 4980372 и 4935240 описаны производные бензоиламинофеноксибутановой кислоты. В частности, были описаны сульфидные производные модафинила, содержащие фенильный и замещенный фенильный линкер между сульфидом и карбонилом, и замещенный арил в концевом амидном положении. Был описаны другие производные модафинила, в которых концевые фенильные группы заторможены мостиковой группой. Например, в патенте США 5563169 описаны некоторые производные ксантенила и тиаксантенила, имеющие замещенный арил в концевом амидном положении. Другие производные ксантенила и тиаксантенила описаны Annis, I.; Barany, G. Pept. Proc. Am. Pept.Ellman, используемого в качестве реагента в пептидном синтезе); Han, Y.; Barany, G. J. Org. Chem., 1997,62, 3841-3848 (получение S-ксантенила, защищенного цистеиновыми производными, используемыми в качестве реагента в пептидном синтезе); и El-Sakka, I.A., et al. Arch. Pharm. (Weinheim), 1994, 327, 133135 (тиаксантеноловые производные тиогликолевой кислоты). Таким образом, существует необходимость в новых классах соединений, которые обладают полезными свойствами. Было обнаружено, что класс соединений, называемых здесь замещенными тиоацетамидами, может использоваться в качестве агентов для лечения и профилактики заболеваний или расстройств, в том числе для лечения сонливости, для стимулирования бодрствования, для лечения болезни Паркинсона, мозговой ишемии, инсульта, для предотвращения апноэ во время сна, для лечения нарушения питания, для стимуляции аппетита и увеличения веса, для лечения синдрома гиперактивностидефицита внимания, для усиления функции при расстройствах, связанных с гипофункцией коры головного мозга, включая, но ими не ограничиваясь, депрессию, шизофрению, усталость, в частности усталость, ассоциированную с неврологическим заболеванием, таким как рассеянный склероз, синдром хронической усталости, и для улучшения познавательной функции при ее нарушении. Настоящее изобретение направлено на эти, а также другие важные цели. Краткое описание изобретения В первом аспекте настоящее изобретение относится, в частности, к различным новым замещенным тиоацетамидам. В других аспектах настоящее изобретение также включает их фармацевтические композиции, способы их получения и применение этих соединений для лечения заболеваний. В одном аспекте настоящее изобретение относится к соединениям формулы (I-A) Признаки и предпочтительные воплощения подробно описаны далее. В другом аспекте настоящее изобретение относится к соединению формулы (I) Признаки и предпочтительные воплощения подробно описаны далее. В другом аспекте настоящее изобретение относится к соединению формулы (II-А)-2 006135 Признаки и предпочтительные воплощения подробно описаны далее. В дополнительном аспекте настоящее изобретение относится к соединению формулы (II) Признаки и предпочтительные воплощения подробно описаны далее. Другим объектом настоящего изобретения являются способы лечения или предотвращения заболеваний или расстройств, в том числе лечения сонливости, стимулирования бодрствования, лечения болезни Паркинсона, мозговой ишемии, инсульта, предотвращения апноэ во время сна, лечения нарушения питания, стимуляции аппетита и увеличения веса, лечения синдрома гиперактивности-дефицита внимания, усиления функции при расстройствах, связанных с гипофункцией коры головного мозга, включая,но ими не ограничиваясь, депрессию, шизофрению, усталость, в частности усталость, ассоциированную с неврологическим заболеванием, таким как рассеянный склероз, синдром хронической усталости, и улучшения познавательной функции при ее нарушении. Другим объектом настоящего изобретения являются фармацевтические композиции, содержащие в своем составе соединения по настоящему изобретению, где композиции содержат один или несколько фармацевтически приемлемых эксципиентов и терапевтически эффективное количество по крайней мере одного из соединений по настоящему изобретению, или его фармацевтически приемлемую соль, или сложный эфир. Эти и другие объекты, возможности и преимущества замещенных тиоацетамидов будут описаны далее в подробном описании изобретения. Краткое описание чертежей На фиг. 1 графически представлены данные, показывающие бодрствование, связанное с EEG, у крыс, которым вводили соединение I-9 (100 мг/кг, внутрибрюшинно; сплошная линия) или метилцеллюлозного носителя (пунктирная линия). Бодрствование определяли в 5-минутные bins. N=13 крыс/группа. р 0,05 по сравнению с животными, которым вводили носитель. На фиг. 2 графически представлены данные, показывающие бодрствование, связанное с EEG, у крыс, которым вводили соединения II-23 (100 мг/кг, внутрибрюшинно; зарисованные треугольники) или метилцеллюлозного носителя (незарисованные треугольники). Каждая точка представляет собой средний процент времени бодрствования в течение последующих 30 мин. р 0,05 по сравнению с животными,которым вводили носитель. Подробное описание изобретения В первом воплощении настоящее изобретение относится к новым соединениям формулы (I-A) где Ar1 и Аr2, каждый независимо, выбраны из C6-С 10 арила или гетероарила; где каждый Ar1 или Аr2 может быть независимо необязательно замещен 1-3 заместителями, независимо выбранными изe) C1-C8 алкила, C2-C8 алкенила или С 2-С 8 алкинила, где 1) каждая группа алкила, алкенила или алкинила незамещена; или 2) каждая группа алкила, алкенила или алкинила независимо замещена 1-3 группами, независимо выбранными из С 6-С 10 арила, гетероарила, F, Сl, Вr, I, СF3, -CN, -NO2, -ОН, -OR7, -CH2OR8, -NR9R10, -O-3 006135(CH2)p-OH, -S-(CH2)p-OH, -X1(CH2)pOR7, X1(CH2)pNR9R10, -X1(CH2)pC(=O)NR9R10, -X1(CH2)pC(=S)NR9R10,-X1(CH2)pОС(=O)NR9R10, -X1(CH2)pCO2R8, X1(CH2)pS(O)yR7, -X1(CH2)pNR8C(=O)NR9R10, -C(=O)R13,-CO2R12, -OC(=O)R7, -C(=O)NR9R10, -ОС(=O)NR12R12A, O-тетрагидропиранила, -С(=S)NR9R10,-CH=NNR12R12A, -CH=NOR12, -CH=NR7, -CH=NNHCH(N=NH)NH2, -NR8CO2R7, -NR8C(=O)NR9R10,-NR8C(=S)NR9R10, -NHC(=NH)NH2, -NR8C(=O)R7, -NR8C(=S)R7, -NR8S(=O)2R7, -S(O)yR7, -S(=O)2NR12R12A,-P(=O)(OR8)2, -OR11 и C5-C7 моносахарида, где каждая гидроксильная группа моносахарида независимо либо незамещена, либо заменена Н, C1-C4 алкилом, C1-C4 алкокси или -O-C(=O)R7;Y представляет собой -О-, -N(R8)- или -S(O)y, m и n не могут быть равны 0;R3 и R4 одинаковые или различные, и каждый выбран из Н, C1-С 6 алкила, -ОН и -СН(R6)CONR8AR8B, при условии, что R3 и R4 одновременно не могут быть ОН; или R3 и R4 вместе с азотом, к которому они присоединены, образуют 3-7-членное гетероциклическое кольцо;R6 представляет собой Н, C1-C4 алкил или боковую цепь -аминокислоты;R9 и R10 независимо выбраны из Н, C1-C4 алкила и С 6-С 10 арила или R9 и R10 вместе с азотом, к которому они присоединены, образуют 3-7-членное гетероциклическое кольцо;R11 представляет собой остаток аминокислоты после удаления гидроксильной группы из карбоксильной группы;t равно 2, 3, или 4; у равно 0, 1 или 2; при условии, что, когда Ar1 представляет собой фенил и Аr2 представляет собой фенил или пиридил, тогда Y не может быть C1-C4 алкиленом; еще при условии, что, когда Ar1 и Аr2 представляют собой фенил, q=1, m и n=0, Y представляет собой и R3 представляет собой Н, тогда R4 не является C1-C6 алкилом; и к их стереоизомерным формам, смесям их стереоизомерных форм или к их фармацевтически приемлемым солям и сложным эфирам. В дополнительном воплощении настоящее изобретение относится к соединениям формулы (I) где Ar1 и Аr2 являются одинаковыми или различными и каждый выбран из тиофена, изотиазола, фенила,пиридила, оксазола, изокасазола, тиазола, имидазола и других пяти- или шестичленных гетероциклов,содержащих 1-3 атома -N-, -О- или -S-, при условии, что Ar1 и Аr2 одновременно не могут быть фенилом,и когда Ar1 представляет собой фенил, Аr2 не является пиридилом; R1-R4 являются одинаковыми или различными, и каждый выбран из Н, низшего алкила, -ОН, -СН(R6)-CONR6AR6B, или любые R1-R4 могут совместно образовывать 3-7-членное карбоциклическое или гетероциклическое кольцо, при условии, чтоR3 и R4 одновременно не могут быть ОН; R6A и R6B независимо представляют собой Н или низший алкил; и n равно 0, 1 или 2; и кроме того, каждый Ar1 или Аr2 может быть независимо необязательно замещен одним или несколькими заместителями, независимо выбранными изb) -CH2OR11, где R11 представляет собой остаток аминокислоты после удаления гидроксильной группы из карбоксильной группы;c) -NR8C(=O)NR9R10, -NR8C(=S)NR9R10, -CO2R12, -C(=O)R12, -С(=O)NR9R10, -C(=S)NR9R10,-CH=NOR12, -CH=NR7, -(CH2)pNR9R10, -(CH2)pNHR11 или -CH=NNR12R12A, где R12 и R12A являются одинаковыми или различными, и каждый независимо выбран из Н, алкила, состоящего из 1-4 углеродов, -ОН,алкокси, состоящего из 1-4 углеродов, -OC(=O)R7, -ОС(=O)NR9R10, -ОС(=S)NR9R10, -О(СН 2)pNR9R10,-O(CH2)pOR8, замещенного или незамещенного арилалкила, состоящего из 6-10 углеродов и замещенного или незамещенного гетероциклилалкила;e) алкила, состоящего из 1-8 углеродов, алкенила, состоящего из 2-8 углеродов, или алкинила, состоящего из 2-8 углеродов, где 1) каждая группа алкила, алкенила или алкинила незамещена; или 2) каждая группа алкила, алкенила или алкинила замещена 1-3 группами, выбранными из арила, состоящего из 6-10 углеродов, гетероциклила, арилалкокси, гетероциклоалкокси, гидроксилалкокси, алкилокси-алкокси, гидроксиалкилтио, алкокси-алкилтио, F, Cl, Br, I, -CN, -NO2, -ОН, -OR7, -Х 2(CH2)pNR9R10,-Х 2(СН 2)pС(=O)NR9R10, -Х 2(СН 2)pС(=S)NR9R10, -X2(СН 2)pОС(=O)NR9R10, -Х 2(СН 2)pCO2R7, -X2(CH2)pS(О)yR7,-X2(СН 2)pNR8C(=O)NR9R10, -ОС(=O)R7, -ОС(=O)NHR12, O-тетрагидропиранила, -NR9R10, -NR8CO2R7,-NR8C(=O)NR9R10, -NR8C(=S)NR9R10, -NHC(=NH)NH2, -NR8C(=O)R7, -NR8C(=S)R7, -NR8S(=O)2R7,-S(O)yR7, -CO2R12, -C(=O)NR9R10, -С(=S)NR9R10, -C(=O)R12, -CH2OR8, -CH=NNR12R12A, -CH=NOR12,-CH=NR7, -CH=NNHCH(N=NH)NH2, -S(=O)2NR12R12A, -P(=O)(OR8)2, -ОR11 и моносахарида, состоящего из 5-7 углеродов, где каждая гидроксильная группа моносахарида независимо либо незамещена, либо заменена Н, алкилом из 1-4 углеродов, алкилкарбонилокси, состоящего из 2-5 углеродов, или алкокси,состоящего из 1-4 углеродов, где X2 представляет собой О, S, или NR8; гдеR7 представляет собой замещенный или незамещенный алкил, замещенный или незамещенный арил или замещенный или незамещенный гетероциклил;R8 представляет собой Н или алкил, состоящий из 1-4 углеродов; р равно от 1 до 4; и где либо 1) R9 и R10, каждый независимо, представляет собой Н, незамещенный алкил, состоящий из 1-4 углеродов, или замещенный алкил; либо 2) R9 и R10 вместе образую мостиковую группу формулы -(CH2)2-X1-(CH2)2-, где X1 выбран из -О-,-S- и -СН 2-; и к их стереоизомерным формам, смесям их стереоизомерных форм или к их фармацевтически приемлемым солям и сложным эфирам. В предпочтительном воплощении изобретение относится к соединениям формулы (I), где Ar1 и Ar2 являются одинаковыми или различными и каждый выбран из тиофена, изотиазола, фенила, оксазола,изоксазола, тиазола, имидазола или других пяти- или шестичленных гетероциклов, содержащих 1-3 атома -N-, -О- или -S-, при условии, что Ar1 и Аr2 одновременно не могут быть фенилом; R1-R4 являются одинаковыми или различными, и каждый выбран из Н, низшего алкила, -ОН, -СН(R6)-CONR6AR6B или любые из R1-R4 могут совместно образовывать 3-7-членное карбоциклическое или гетероциклическое кольцо, при условии, что R3 и R4 одновременно не могут быть ОН; R6A и R6B независимо представляют собой Н или низший алкил; и n равно 0, 1, или 2; и, кроме того,каждый Ar1 или Аr2 может быть независимо необязательно замещен одним или несколькими заместителями, независимо выбранными изb) -CH2OR11, где R11 представляет собой остаток аминокислоты после удаления гидроксильной группы из карбоксильной группы;c) -NR8C(=O)NR9R10, -NR8C(=S)NR9R10, -CO2R12, -C(=O)R12, -C(=O)NR9R10, -C(=S)NR9R10,-CH=NOR12, -CH=NR7, -(CH2)pNR9R10, -(CH2)pNHR11 или -CH=NNR12R12A, где R12 и R12A являются одинаковыми или различными и каждый независимо выбран из Н, алкила, состоящего из 1-4 углеродов, -ОН,алкокси, состоящего из 1-4 углеродов, -OC(=O)R7, -ОС(=O)NR9R10, -ОС(=S)NR9R10, -О(CH2)pNR9R10,-O(CH2)pOR8, замещенного или незамещенного арилалкила, состоящего из 6-10 углеродов, и замещенного или незамещенного гетероциклилалкила;e) алкила, состоящего из 1-8 углеродов, алкенила, состоящего из 2-8 углеродов, или алкинила, состоящего из 2-8 углеродов, где 1) каждая группа алкила, алкенила или алкинила незамещена; или 2) каждая группа алкила, алкенила или алкинила замещена 1-3 группами, выбранными из арила, состоящего из 6-10 углеродов, гетероциклила, арилалкокси, гетероциклоалкокси, гидроксилалкокси, алкилокси-алкокси, гидроксиалкилтио, алкокси-алкилтио, F, Cl, Br, I, -CN, -NO2, -ОН, -OR7, -X2(CH2)pNR9R10,-X2(CH2)pC(=O)NR9R10, -X2(CH2)pC(=S)NR9R10, -X2(СН 2)pОС(=O)NR9R10, -X2(CH2)pCO2R7, -X2(CH2)pS(O)yR7,-X2(CH2)pNR8C(=O)NR9R10, -OC(=O)R7, -ОС(=O)NHR12, O-тетрагидропиранила, -NR9R10, -NR8CO2R7,-NR8C(=O)NR9R10, -NR8C(=S)NR9R10, -NHC(-NH)NH2, -NR8C(=O)R7, -NR8C(=S)R7, -NR8S(=O)2R7,-S(O)yR7, -CO2R12, -C(=O)NR9R10, -C(=S)NR9R10, -C(=O)R12, -CH2OR8, -CH=NNR12R12A, -CH=NOR12,-5 006135-CH=NR7, -CH=NNHCH(N=NH)NH2, -S(=O)2NR12R12A, -P(=O)(OR8)2, -OR11 и моносахарида, состоящего из 5-7 углеродов, где каждая гидроксильная группа моносахарида независимо либо незамещена, либо заменена Н, алкилом из 1-4 углеродов, алкилкарбонилокси, состоящим из 2-5 углеродов, или алкокси,состоящим из 1-4 углеродов, где X2 представляет собой О, S или NR8; гдеR7 представляет собой замещенный или незамещенный алкил, замещенный или незамещенный арил, или замещенный или незамещенный гетероциклил;R8 представляет собой Н или алкил, состоящий из 1-4 углеродов; р равно от 1 до 4; и где либо 1) R9 и R10, каждый независимо, представляет собой Н, незамещенный алкил, состоящий из 1-4 углеродов, или замещенный алкил; либо 2) R9 и R10 вместе образуют мостиковую группу формулы -(CH2)2-X1-(СН 2)2-, где X1 выбран из -О-,-S-, и -СН 2-; и к их стереоизомерным формам, смесям их стереоизомерных форм или к их фармацевтически приемлемым солям и сложным эфирам. В другом воплощении настоящее изобретение относится к новым соединениям формулы (II-А)a) 6-членного ароматического карбоциклического кольца, в котором 1-3 углеродных атома могут быть заменены гетероатомами, выбранными из кислорода, азота и серы; иi) один атом углерода может быть заменен атомом кислорода, азота или серы;ii) два атома углерода могут быть заменены атомом серы и азота, атомом кислорода и азота или двумя атомами азота; илиiii) три атома углерода могут быть заменены тремя атомами азота, одним атомом кислорода и двумя атомами азота или одним атомом серы и двумя атомами азота;e) C1-C8 алкила, C2-C8 алкенила или С 2-С 8 алкинила, где 1) каждая группа алкила, алкенила или алкинила незамещена; или 2) каждая группа алкила, алкенила или алкинила замещена 1-3 группами, независимо выбранными из C6-С 10 арила, гетероарила, F, Сl, Вr, I, СF3, -CN, -NO2, -ОН, -OR7, -CH2OR8, -NR9R10, -O-(CH2)p-ОН, -S(CH2)p-OH,-X1(CH2)pOR7,X1(CH2)pNR9R10,-X1(CH2)pС(=O)NR9R10,-X1(CH2)pC(=S)NR9R10,-X1(CH2)pOC(=O)NR9R10, -X1(CH2)pCO2R8, -X1(CH2)pS(O)yR7, -X1(CH2)pNR8C(=O)NR9R10, -C(=O)R13,-CO2R12, -OC(=O)R7, -C(=O)NR9R10, -ОС(=O)NR12R12A, O-тетрагидропиранила, -C(=S)NR9R10,-CH=NNR12R12A, -CH=NOR12, -CH=NR7, -CH=NNHCH(N=NH)NH2, -NR8CO2R7, -NR8C(=O)NR9R10,-NR8C(=S)NR9R10, -NHC(=NH)NH2, -NR8C(=O)R7, -NR8C(=S)R7, -NR8S(=O)2R7, -S(O)yR7, -S(=O)2NR12R12A,-P(=O)(OR8)2, -OR11 и С 5-С 7 моносахарида, где каждая гидроксильная группа моносахарида независимо либо незамещена, либо заменена Н, C1-C4 алкилом, C1-C4 алкокси или -O-C(=O)R7;R3 и R4 одинаковые или различные, и каждый выбран из Н, C1-C6 алкила, -ОН и -СН(R6)CONR8AR8B, при условии, что R3 и R4 одновременно не могут быть ОН; или R3 и R4 вместе с азотом, к которому они присоединены, образуют 3-7-членное гетероциклическое кольцо;R6 представляет собой Н, C1-C4 алкил или боковую цепь -аминокислоты;R9 и R10 независимо выбраны из Н, C1-C4 алкила и C6-С 10 арила или R9 и R10 вместе с азотом, к которому они присоединены, образуют 3-7-членное гетероциклическое кольцо;R11 представляет собой остаток аминокислоты после удаления гидроксильной группы из карбоксильной группы;Y выбран из C1-C4 алкилена, C6-С 10 арилена, гетероарилена, С 3-C8 циклоалкилена, гетероциклилена,-О-, -N(R8)-, -S(O)y, -CR8A=CR8B-, -CH=CH-CH(R8)-, -CH(R8)-CH=CH- или -ОС-; при условии, что когда Y представляет собой -О-, -N(R8)- или -S(O)y, m и n не могут быть равны 0;t равно 2, 3 или 4; у равно 0, 1 или 2; и к их стереоизомерным формам, смесям их стереоизомерных форм или к их фармацевтически приемлемым солям и сложным эфирам. В дополнительном воплощении настоящее изобретение относится к соединениям формулы (II) где Х представляет собой (СН 2)m-, -О-, -S(O)n-, -N(R5)-, -СН=СН- или -CH2-СН=СН-; m равно 0, 1, 2 или 3; n равно 0, 1 или 2; R1-R4 одинаковые или различные, и каждый выбран из Н, низшего алкила, -ОН,-СН(R6)-CONR7R8 или любые R1-R4 могут совместно образовывать 3-7-членное карбоциклическое или гетероциклическое кольцо; R5 представляет собой Н, низший алкил или -ОН; R6, R7 и R8 представляет собой Н или низший алкил; и кольцо А, вместе с углеродными атомами, к которому оно присоединено,выбрано изa) 6-членного карбоциклического кольца, в котором 1-3 углерода могут быть заменены гетероатомами, выбранными из кислорода, азота и серы; иi) один атом углерода может быть заменен атомом кислорода, азота или серы;ii) два атома углерода могут быть заменены атомом серы и азота, атомом кислорода и азота или двумя атомами азота; илиiii) три атома углерода могут быть заменены тремя атомами азота, одним атомом кислорода и двумя атомами азота или одним атомом серы и двумя атомами азота; и к их стереоизомерным формам, смесям их стереоизомерных форм или к их фармацевтически приемлемым солям и сложным эфирам. Что касается любой группы структурно близких соединений, обладающих полезным свойством, то некоторые группы и конфигурации являются предпочтительными для соединений по настоящему изобретению в их конечном применении. В некоторых воплощениях формулы (I-A) или (II-A), Y=-С(R1)(R2), где R1 и R2, каждый независимо,выбраны из Н или C1-C6 алкила; и необязательно, либо R1, либо R2 могут быть объединены либо с R3, либо с R4 с образованием 5-7-членного гетероциклического кольца. Предпочтительно либо R1 в сочетании с соответственно. В некоторых воплощениях формулы (I-A) Ar1 и Аr2, каждый независимо, выбраны из пяти- или шестичленного гетероарила, содержащего 1-3 атома -N-, -О- или -S-. Предпочтительно q=1. В предпочтительных воплощениях Ar1 и Аr2, каждый независимо, выбраны из тиенила, изотиазолила, пиридила, оксазолила, изоксазолила, тиазолила и имидазолила и более предпочтительно Ar1 и Аr2 представляют собой тиенил и особенно предпочтительно Ar1 и Аr2 представляют собой 3-тиенил. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y- или -N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -CR8A=CR8B-, -CH=CH-CH(R8)-, -СН(R8)-CH=CH- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочительно m=0 или 1 и-СН- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В другом более предпочтительном воплощении Y представляет собой В еще одном воплощении Y представляет собой фуранилен. В другом предпочтительном воплощении Y представляет собой С 3-C8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой В других воплощениях формулы (I-A) Ar1 представляет собой фенил и Аr2 представляет собой пяти- или шестичленный гетероарил, содержащий 1-3 атома -N-, -О- или -S-. Предпочтительно q=1. В остальных предпочтительных воплощениях Ar1 и Аr2, каждый независимо, представляют собой фенил,тиенил, изотиазолил, пиридил, оксазолил, изоксазолил, тиазолил и имидазолил. В дополнительных предпочтительных воплощениях Ar1 представляет собой фенил и Аr2 представляет собой тиенил, изотиазолил, пиридил, оксазолил, изоксазолил, тиазолил и имидазолил и более предпочтительно Ar1 представляет собой фенил и Аr2 представляет собой тиенил и особенно предпочтительно Аr2 представляет собой 3 тиенил. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y-или -N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -CR8A=CR9B-, -CH=CH-CH(R8)-, -CH(R8)-CH=CH- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочтительно m=0 или 1 и n=0 или 1. Более предпочтительно Y представляет собой-CH- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В еще одном наиболее предпочтительном воплощении Y представляет собой В еще одном воплощении Y представляет собой фуранилен. В дополнительных предпочтительных воплощениях Y представляет собой С 3-C8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой В еще одном воплощении формулы (I-A) Ar1 и Аr2 представляют собой фенил. Предпочтительноq=1. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y- или -N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -СR8A=СR8B-, -CH=CH-CH(R8)-, -СН(R8)-СН=СН- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочтительно m=0 или 1 и n=0 или 1. Более предпочтительно Y представляет собой-СН- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В еще одном наиболее предпочтительном воплощении Y представляет собой В еще одном воплощении Y представляет собой фуранилен. В дополнительных предпочтительных воплощениях Y представляет собой С 3-С 8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой В дополнительном воплощении формулы (I-A) Y представляет собой -О-, -S(O)y-, -N(R8)-, C1-C4 алкилен, -CR8A=CR8B-, -CH=CH-СН(R8)-, -CH(R8)-CH=CH-, -CC-, где Х 2 представляет собой -CH2-, -О-, -S(O)y- или -N(R8)- и Х 3, Х 4 и Х 5, каждый независимо, выбраны из-СН- или -N-. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y- или-N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -CR8A=CR9B-, -СН=СН-СН(R8)-, -СН(R8)-CH=CH- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочтительно m=0 или 1 и n=0 или 1. Более предпочтительно Y представляет собой-СН- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В еще одном наиболее предпочтительном воплощении Y представляет собой В еще одном воплощении Y представляет собой фуранилен. В дополнительных предпочтительных воплощениях Y представляет собой С 3-C8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой В еще одном воплощении формулы (I-A) q=1. В дополнительном воплощении формулы (I-A) Ar1 и Ar2, каждый независимо, выбраны из фенила и тиенила и q=1. Предпочтительно Ar1 и Аr2, каждый независимо, выбраны из фенила и 3-тиенила и q=1. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y- или -N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -CR8ACR8B-, -CH=CH-CH(R8)-, -СН(R8)-CH=CH- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочтительно m=0 или 1 и n=0 или 1. Более предпочтительно Y представляет собой-СН- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В еще одном наиболее предпочтительном воплощении Y представляет собой В еще одном воплощении Y представляет собой фуранилен. В дополнительных предпочтительных воплощениях Y представляет собой С 3-С 8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой Предпочтительными воплощениями формулы (I-A) являются соединения, где Ar1 и Аr2 являются одинаковыми или различными и каждый выбран из тиофена, изотиазола, фенила, пиридила, оксазола,изоксазола, тиазола, имидазола, при условии, что Ar1 и Аr2 одновременно не могут быть фенилом, и когда Ar1 представляет собой фенил, тогда Аr2 не является пиридилом. Предпочтительными воплощениями формулы (I) является соединения, где Ar1 и Аr2 являются одинаковыми или различными и каждый выбран из тиофена, изотиазола, фенила, оксазола, изоксазола, тиазола, имидазола, при условии, что Ar1 и Аr2 одновременно не могут быть фенилом. Другими предпочтительными воплощениями являются такие воплощения, где Ar1 и Ar2, каждый независимо, замещен. Дополнительные предпочтительные воплощения формулы (I) определены далее. 1). Соединения, в которых Ar1, Ar2 или оба являются тиофеном; 2). Соединения, в которых Ar1, Ar2 или оба являются изотиазолом; 3). Соединения, в которых Ar1, Ar2 или оба являются пиридилом; 4). Соединения, в которых Ar1, Ar2 или оба являются оксазолом; 5). Соединения, в которых Ar1, Ar2 или оба являются изоксазолом; 6). Соединения, в которых Ar1, Аr3 или оба являются тиазолом; 7). Соединения, в которых Ar1, Ar2 или оба являются имидазолом,8). Соединения, в которых Ar1 представляет собой фенил и Ar2 представляет собой тиофен. Соединения предпочтительного воплощения формулы (I-A) представлены в табл. 1. В особенно предпочтительных воплощениях настоящее изобретение относится к соединениям формулы (II) или (II-A), где q=1. В еще одном воплощении формулы (II-A) X представляет собой связь, -CH2CH2-, -О-, -N(СН 3)- или-СН=СН- и предпочтительно Х представляет собой связь. В особенно предпочтительных воплощениях формулы (II-A) Y представляет собой -О-, -S(O)y-,-N(R8)-, C1-C4 алкилен, -CR8A=CR8B-, -CH=CH-CH(R8)-, -CH(R8)-CH=CH-, -CC-, где Х 2 представляет собой -СН 2-, -О-, -S(O)y- или -N(R8)-; и Х 3, Х 4 и X5, каждый независимо, выбраны из-СН- или -N-. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y- или-N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -CR8A=CR8B-, -СН=СН-СН(R8)-, -СН(R8)-CH=CH- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочтительно m=0 или 1 и n=0 или 1. Более предпочтительно Y представляет собой-СН- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В еще одном наиболее предпочтительном воплощении Y представляет собой В дополнительных предпочтительных воплощениях Y представляет собой С 3-С 8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой В дополнительных воплощениях формулы (II-A) кольца А и В вместе с атомами углерода, к которым они присоединены, каждый независимо, выбраны из фенилена, тиенилена, изотиазолилена, пиридилена, оксазолилена, изоксазолилена, тиазолилена, имидазолилена. В предпочтительном воплощении кольцо А представляет собой фенилен и более предпочтительно кольца А и В представляют собой фенилен. В еще одном предпочтительном воплощении кольца А и В представляют собой тиенилен и более предпочтительно кольца А и В представляют собой 2,3-тиенилен. В предпочтительных воплощенияхq=1. В дополнительных предпочтительных воплощениях кольцо А представляет собой фенилен и кольцо В представляет собой 2,3-тиенилен. В остальных предпочтительных воплощениях Х представляет собой связь, -CH2CH2-, -О-, -N(СН 3)- или -СН=СН-. В более предпочтительном воплощении Y представляет собой -О-, -S(O)y-, -N(R8)-, C1-C4 алкилен, -CR8A=CR8B-, -СН=СН-СН(R8)-, -СН(R8)-CH=CH-, -CC-, где Х 2 представляет собой -CH2-, -О-, -S(O)y- или -N(R8)- и Х 3, Х 4 и Х 5, каждый независимо, выбраны из-СН- или -N-. В остальных предпочтительных воплощениях Y представляет собой -О-, -S(O)y- или-N(R8)-. В еще одном предпочтительном воплощении Y представляет собой C1-C4 алкилен. В дополнительном воплощении Y представляет собой -CR8A=CR8B-, -CH=CH-CH(R8)-, -СН(R8)-CH=CH- или -СС-. В особенно предпочтительных воплощениях Y представляет собой C6-С 10 арилен или гетероарилен и предпочтительно m=0 или 1 и n=0 или 1. Более предпочтительно Y представляет собой-СН- или -N-. Наиболее предпочтительно Y представляет собой фенилен. В еще одном наиболее предпочтительном воплощении Y представляет собой В дополнительных предпочтительных воплощениях Y представляет собой С 3-С 8 циклоалкилен или гетероциклилен. Предпочтительно Y представляет собой В особенно предпочтительном воплощении Х представляет собой связь и Y представляет собой-СН 2- и n=0. Предпочтительными воплощениями формулы (II) являются соединения, где кольцо А выбрано из тиофена, изотиазола, фенила, оксазола, изоксазола, тиазола и имидазола. Остальными предпочтительными воплощениями являются такие воплощения, в которых бензокольцо и кольцо А, каждое независимо,замещено. Остальные предпочтительные воплощения формулы (II) приведены далее. 1). Соединения, в которых А представляет собой бензо и Х представляет собой связь, т.е. -(CH2)m-,где m=0;- 13006135 2). Соединения, в которых А представляет собой бензо и Х представляет собой -О-; 3). Соединения, в которых А представляет собой бензо и Х представляет собой -NСН 3; 4). Соединения, в которых А представляет собой бензо и Х представляет собой -S-; и 5). Соединения, в которых R3 и R4 вместе с азотом, к которому они присоединены, образуют кольца морфолина. Соединения особенно предпочтительного воплощения формулы (II-A) представлены в табл. 2. Таблица 2 Определения. Как используется здесь, термин алкил относится к замещенной или незамещенной, разветвленной или прямой углеводородной цепи, содержащей от 1 до 8 атомов углерода, которая образуется при удалении одного атома водорода. В особенно предпочтительном воплощении алкильная группа состоит из 1-6 атомов углерода. В остальных предпочтительных воплощениях алкильная группа содержит от 1 до 4 атомов углерода. Обозначение, такое как C1-C4 алкил, относится к алкильному радикалу, содержащему от 1 до 4 атомов углерода. Примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил,втор-бутил, трет-бутил, пентил, 2-метилпентил, гексил, 2-метилгексил, 2,3-диметилгексил, гептил, октил и тому подобное. Как используется здесь, термин низший алкил относится к C1-C6 насыщенному с прямой или разветвленной цепью или циклическому углеводороду, который необязательно замещен. Низшие алкильные группы включают, но ими не ограничиваются, метил, этил, н-пропил, изопропил, н-бутил, изобутил,трет-бутил, н-пентил, циклопентил, изопентил, неопентил, н-гексил, изогексил, циклогексил, 3 метилпентил, 2,2-диметилбутил, 2,3-диметилбутил и тому подобное. Как используется здесь, термин алкенил относится к замещенной или незамещенной, прямой или разветвленной углеводородной цепи, содержащей от 2 до 8 атомов углерода, имеющей одну или несколько двойных углерод-углеродных связей, которые могут быть в любой стабильной точке цепи, и которая образуется удалением одного атома водорода. Обозначение С 2-С 8 алкенил относится к алкенильному радикалу, содержащему от 2 до 8 атомов углерода. Примеры включают этенил, пропенил, изопропенил, 2,4-пентадиенил и тому подобное. Как используется здесь, термин алкинил относится к замещенному или незамещенному, прямому или разветвленному углеводородному радикалу, содержащему от 2 до 8 атомов углерода, имеющему одну или несколько тройных углерод-углеродных связей, которые могут находиться в любой стабильной точке цепи, и который образуется удалением одного атома водорода. Обозначение С 2-С 8 алкинил отно- 17006135 сится к алкинильному радикалу, содержащему от 2 до 8 атомов углерода. Примеры включают этинил,пропинил, изопропинил, 3,5-гексадиинил и тому подобное. Как используется здесь, термин карбоцикл или карбоциклический относится к замещенному или незамещенному, стабильному моноциклическому или бициклическому углеводородному кольцу,которое является насыщенным или ненасыщенным и содержит от 3 до 10 атомов углерода. Соответственно, углеводородная группа может быть ароматической или неароматической. Связи, соединяющие эндоциклические атомы углерода карбоциклической группы, могут быть одинарными, двойными, тройными или частью конденсированной ароматической группы. Под карбоциклами подразумевают описанные здесь циклоалкильные и арильные соединения. Как используется здесь, термин циклоалкил относится к замещенному или незамещенному углеводородному кольцу, содержащему от 3 до 7 атомов углерода, образованному удалением одного атома водорода. Обозначение, такое как С 5-С 7 циклоалкил, относится к циклоалкильному радикалу, содержащему от 5 до 7 атомов углерода. Примеры включают циклопропил, циклопентил, циклогексил, циклогептил и тому подобное. Как используется здесь, термины гетероцикл или гетероциклическое относятся к замещенному или незамещенному, насыщенному, частично ненасыщенному или ненасыщенному, стабильному 3-10 членному моноциклическому или бициклическому кольцу, где по крайней мере один член кольца является гетероатомом. Соответственно, гетероциклическая группа может быть ароматической или неароматической. Обычно, гетероатомы включают, но этим не ограничиваются, атомы кислорода, азота, серы,селена и фосфора. Предпочтительными гетероатомами являются кислород, азот и сера. В неароматическом кольце гетероатомы азота и серы могут быть необязательно окислены, и азот может быть необязательно замещен. Связи, соединяющие эндоциклические атомы гетероциклической группы, могут быть одинарными, двойными, тройными или частью конденсированной ароматической группы. Под гетероциклами подразумевают описанные здесь гетерциклические и гетероарильные соединения. Как используется здесь, термин гетероциклил относится к замещенному или незамещенному, насыщенному или частично ненасыщенному, стабильному 3-7-членному гетероциклическому кольцу, которое образуется при удалении одного атома водорода. Примеры включают эпоксиэтил, пирролидил, пиразолидинил, пиперидил, пиранил, оксазолинил,морфолино, морофлинил, пиперазинил и тому подобное. Примеры гетероциклов включают, но ими не ограничиваются, 2-пирролидинил, 2 Н-пирролил, 4 пиперидинил, 6 Н-1,2,5-тиадиазинил, 2 Н,6 Н-1,5,2-дитиазинил, фуранил, фуразанил, имидазолидинил,имидазолинил, имидазолил, изоксазолил, морфолинил, оксадиазолил, 1,2,3-оксадиазолил, 1,2,4 оксадиазолил, 1,2,5-оксадиазолил, 1,3,4-оксадиазолил, оксазолидинил, оксазолил, пиперазинил, пиперидинил, птеридинил, пиперидонил, 4-пиперидинил, пуринил, пиранил, пиразинил, пиразолидинил, пиразолинил, пиразолил, пиридазинил, пиридинил, пиридил, пиримидинил, пирролидинил, пирролинил, пирролил, тетрагидрофуранил, 6 Н-1,2,5-тиадиазинил, 1,2,3-тиадиазолил, 1,2,4-тиадиазолил, 1,2,5 тиадиазолил, 1,3,4-тиадиазолил, тиазолил, тиенил, тиенотиазолил, тиенооксазолил, тиеноимидазолил,триазинил, 1,2,3-триазолил, 1,2,4-триазолил, 1,2,5-триазолил, 1,3,4-триазолил и тетразол. Подходящие гетероциклы также описаны в The Handbook of Chemistry and Physics, 76-e издание, CRC Press, Inc., 19951996, стр. 2-25 и 2-26 и приведены здесь в качестве ссылки. Предпочтительное гетероциклические группы, образованные с атомом азота, включают, но ими не ограничиваются, группы пирролидинила, пиперидинила, пиперидино, морфолинила, морфолино, тиоморфолино, N-метилпиперазинила, индолила, изоиндолила, имидазола, имидазолина, оксазолина, оксазола, триазола, тиазолина, тиазола, изотиазола, тиадиазолов, триазинов, изоксазола, оксиндола, индоксила, пиразола, пиразолона, пиримидина, пиразина, хинолина, изохинолина и тетразола. Предпочтительными гетероциклическими группами, образованными с атомом кислорода, являются,но ими не ограничиваются, группы фурана, тетрагидрофурана, пирана, бензофурана, изобензофурана и тетрагидропирана. Предпочтительными гетероциклическими группами, образованными с атомом серы,являются, но ими не ограничиваются, тиофен, тианафтен, терагидротиофен, тетрагидротиапиран и бензотиофены. Предпочтительными ароматическими гетероциклическими группами являются, но ими не ограничиваются, группы пиридила, пиримидила, пирролила, фурила, тиенила, имидазолила, тиазолила, тетразолила, хинолила, изохинолила, бензоимидазолила, тиазолила, пиразолила и бензотиазолила. Как используется здесь, термин замещенный относится к замене одного или нескольких атомов водорода указанной группы выбранной группой, обозначенной здесь как заместитель, при условии,что валентность замещенного атома не превышается и что полученное замещенное соединение является стабильным. Замещаемая группа имеет от 1 до 5, предпочтительно от 1 до 3 и более предпочтительно 1,независимо выбранный(ых) заместитель(ей). Предпочтительные заместители включают, но ими не ограничиваются, F, Cl, Вr, I, ОН, OR, NH2, NR2, NHOH, NO2, CN, СF3, СF2 СF3, C1-С 6 алкил, С 2-C6 алкенил, С 2C6 алкинил, C1-C6 алкокси, С 3-С 7 циклоалкил, гетероциклил, С 6-С 10 арил, гетероарил, арилалкил, C(=O)R,COOH, CO2R, O-C(=O)R, C(=O)NRR', NRC(=O)R', NRCO2R', OC(=O)NRR', -NRC(=O)NRR',- 18006135C6-С 10 арил. Как используется здесь, термин арил относится к замещенному или незамещенному, ароматическому карбоциклическому кольцу, содержащему от 6 до 10 атомов углерода, которое образуется при удалении одного атома водорода. Примеры включают фенил, нафтинил, инденил и тому подобное. Как используется здесь, термин гетероарил относится к замещенному или незамещенному 5-10 членному ароматическому гетероциклическому кольцу, которое образуется при удалении одного водородного атома. Примеры включают пирролил, пиридил, пиримидинил, пиразинил, тетразолил, индолил,хинолинил, пуринил, имидазолил, тиенил, тиазолил, бензотиазолил, фуранил, бензофуранил, 1,2,4 тиадизолил, изотиазолил, триазоил, тетразолил, изохинолил, бензотиенил, изобензофуранил, пиразолил,карбозолил, бензимидазолил, изоксазолил и тому подобно. Как используется здесь, термин алкилен относится к замещенной или незамещенной, разветвленной или прямой цепи углеводорода, состоящей из от 1 до 8 атомов углерода, которая образуется при удалении двух атомов водорода. Обозначение, такое как C1-C4 алкилен, относится к алкиленовому радикалу, содержащему от 1 до 4 углеродных атома. Примеры включают метилен (-CH2-), пропилиден(СН 3CH2 СН=), 1,2-этандиил (-CH2CH2-) и тому подобное. Как используется здесь, термин циклоалкилен относится к замещенному или незамещенному карбоциклическому кольцу, содержащему от 3 до 8 атомов углерода, которое образуется при удалении двух атомов водорода. Обозначение, такое как С 3-С 8 циклоалкилен, относится к циклоалкиленовому радикалу, содержащему от 3 до 8 атомов углерода. Примеры включают циклопропилен (-С 3 Н 4-), циклопентилен (-С 5 Н 8-), циклогексилен (-C6 Н 10-) и тому подобное. Как используется здесь, термин гетероциклилен относится к замещенному или незамещенному,насыщенному или частично ненасыщенному, стабильному 3-7-членному гетероциклическому кольцу,которое образуется при удалении двух атомов водорода. Примеры включают эпоксиэтилен, пирролидилен, пирролидилиден, пиразолидинилен, пиперидилен, пиранилен, морфолинилиден и тому подобное. Как используется здесь, термин арилен относится к замещенному или незамещенному ароматическому карбоциклическому кольцу, содержащему от 6 до 10 атомов углерода, которое образуется при удалении двух атомов водорода. Примеры включают фенилен (-C6 Н 4-), нафтилен (-С 10 Н 6-) и тому подобное. Фениленовая группа имеет следующую структуру: Как используется здесь, термин гетероарилен относится к замещенному или незамещенному 510-членному ароматическому гетероциклическому кольцу, которое образуется при удалении двух атомов водорода. Примеры включают гетероариленовые группы, которые относятся к соответствующим гетероарильным соединениям, описанным выше, и, в частности, включают тиенилен (-С 4H2S-), пиридилен(-C5H3N-), пиримидинилен (-С 3H2N2-), хинолинилен (-С 9 Н 5N-), тиазолилен (-С 3 НNS-) и тому подобное. Группа тиенилен имеет следующую структуру: Группа пиридилен имеет следующую структуру: Как используется здесь, термин алкокси относится к кислородному радикалу, замещенному алкильной группой. Предпочтительно алкоксигруппа содержит от 1 до 6 атомов углерода. Обозначение,такое как C1-C4 алкокси, относится к алкоксигруппе, содержащей от 1 до 4 атомов углерода. Примеры включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси и тому подобное. Как используется здесь, термин арилалкил относится к арилзамещенной алкильной группе и включает в себя бензил, бромбензил, дифенилметил, трифенилметил, фенилэтил, дифенилэтил и тому подобное. Как используется здесь, термин С 5-С 7 моносахарид относится к простым сахарам формулы(CH2O)n, где n=5-7. Моносахариды могут быть с прямой цепью или иметь разветвленную кольцевую систему и могут содержать сахарозное звено формулы -СН(ОН)-С(=O)-. Примеры включают эритрозу, треозу, рибозу, арабинозу, ксилозу, ликсозу, аллозу, альтрозу, глюкозу, маннозу, гилозу, идозу, галактозу,талозу, эритулозу, рибулозу, ксиулозу, псикозу, фруктозу, сорбозу, тагатозу, эритропентулозу, треопентулозу, глицеротетрулозу, гликопиранозу, фруктофуранозу и тому подобное.- 19006135 Как используется здесь, термин аминокислота относится к молекуле, содержащей как аминогруппу, так и карбоксильную группу. Варианты аминокислот включают -амино, -амино и -аминокислоты. -Аминокислоты представлены общей формулой НООС-СН(боковая цепь)-NН 2. Аминокислоты могут быть в виде их D, L или рацемических конфигураций. Аминокислоты включают встречающиеся и не встречающиеся в природе группы. Природные аминокислоты включают обычные 20 аминокислот, находящихся в белках, такие как глицин, серин, тирозин, пролин, гистидин, глутамин и тому подобное. Природные аминокислоты могут также включать не -аминокислоты (такие как аланин, -аминомасляная кислота, гомоцистеин и тому подобное), редко встречающиеся аминокислоты(такие как 4-гидроксипролин, 5-гидроксилизин, 3-метилгистидин и тому подобное) и небелковые аминокислоты (такие как цитруллин, омитин, канаванин и тому подобное). Аминокислоты, не встречающиеся в природе, хорошо известны в данной области и включают аналоги природных аминокислот. См.Lehninger, A.L. Biochemistry, 2-е издание; Worth Publishers: New York, 1975; 71-77, приведенные здесь в качестве ссылки. Аминокислоты, не встречающиеся в природе, также включают -аминокислоты, где указанные цепи заменены синтетическими производными. Типичные представители боковых цепей природных и не встречающихся в природе -аминокислот представлены ниже в табл. А. Таблица А Как используется здесь, термин объект относится к теплокровному животному, такому как млекопитающее, предпочтительно человек или ребенок, которые страдают или имеют предрасположенность к одному или нескольким представленным здесь заболеваниям и состояниям. Как используется здесь, терапевтически эффективное количество относится к количеству соединения по настоящему изобретению, которое эффективно снижает, устраняет, лечит или подавляет симптомы представленных здесь заболеваний или состояний. Под термином подавляет понимают все процессы, при которых происходит снижение, прерывание, задержка или остановка развития представленных здесь заболеваний и состояний, но не обязательно, окончательное исчезновение всех симптомов заболеваний и состояний, и подразумевает профилактическое лечение. Как используется здесь, термин фармацевтически приемлемые относится к таким соединениям,веществам, композициям и/или дозированным формам, которые с медицинской точки зрения являются подходящими для взаимодействия с тканями человека и животных, не обладают излишней токсично- 20006135 стью, не повреждают ткани и не вызывают аллергические реакции или другие неблагоприятные осложнения, соизмеримые с подходящим отношением выгода/риск. Как используется здесь, фармацевтически приемлемые соли относятся к описанным соединениям, в которых основное соединение модифицировано путем перевода его в кислотные или основные соли. Фармацевтически приемлемые соли включают обычные нетоксичные соли или соли четвертичного аммония основного соединения, полученные, например, из нетоксичных неорганических или органических кислот. Например, такие обычные нетоксичные соли включают соли, полученные из неорганических кислот, таких как хлористо-водородная, серная, сульфаминовая, фосфорная, азотная и тому подобное; и соли, полученные из органических кислот, таких как уксусная, пропионовая, янтарная, винная,лимонная, глутаминовая, бензойная, салициловая, толуолсульфоновая, щавелевая и тому подобное. Фармацевтически приемлемые соли по настоящему изобретению могут быть синтезированы из основного соединения, которые содержат основную или кислотную группу, путем обычных химических способов. Обычно такие соли могут быть получены взаимодействием форм свободной кислоты или основания этих соединений со стехиометрическим количеством соответствующего основания или кислоты в воде или в органическом растворителе или в их смеси. Обычно предпочтительной является неводная среда, такая как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечень подходящих солей можно найти в Remington's Pharmaceutical Sciences, 17-e издание. Mack Publishing Company, Easton, Pa.,1985, стр. 1418, описание которого включено здесь в качестве ссылки. Как используется здесь, под пролекарством подразумевают любые ковалентно-связанные носители, которые высвобождают активное основное лекарственное средство, соответствующее соединениям по настоящему изобретению in vivo при введении такого пролекарства млекопитающему. Так как пролекарства, как известно, улучшают большое число желательных свойств фармацевтических препаратов(например, растворимость, биодоступность, способы получения и тому подобное), соединения по настоящему изобретению могут быть доставлены в виде пролекарств. Таким образом, настоящее изобретение охватывает пролекарства заявленных соединений, композиции, содержащие заявленные соединения,и способы доставки этих соединений. Пролекарства по настоящему изобретению могут быть получены путем модификации функциональных групп, присутствующих в соединении, таким образом, что модифицированные соединения расщепляются, либо стандартными способами, либо in vivo, до основного соединения. Соответственно, пролекарства включают, например, соединения по настоящему изобретению, в которых гидрокси, амино или карбоксигруппа связана с любой группой таким образом, что при введении пролекарства млекопитающему они расщепляются с образованием свободного гидроксила,свободной амино или карбоновой кислоты соответственно. Примеры включают, но этим не ограничиваются, ацетатные, формиатные и бензоатные производные спирта и функциональные группы амина; и алкильные, циклоалкильные, арильные, и алкиларильные сложные эфиры, такие как метиловый, этиловый, циклопропиловый, фениловый, бензиловый и фенэтиловый сложные эфиры и тому подобное. Настоящее изобретение относится к способу лечения заболеваний и состояний объекта при необходимости такого лечения, которое заключается во введении указанному объекту терапевтически эффективного количества соединения формулы (I), (I-A), (II) или (II-A). Например, соединения формулы (I), (IA), (II) или (II-A) могут использоваться при лечении сонливости, предпочтительно сонливости, связанной с нарколепсией, для стимулирования бодрствования, для лечения болезни Паркинсона, мозговой ишемии, инсульта, для предотвращения апноэ во время сна, для лечения нарушения питания, предпочтительно нарушений питания, связанных с заболеваниями, в частности, при анорексии на нервной почве,для стимуляции аппетита и увеличения веса, для лечения синдрома гиперактивности-дефицита внимания, для усиления функции при расстройствах, связанных с гипофункцией коры головного мозга, включая, но ими не ограничиваясь, депрессию, шизофрению, усталость, в частности усталость, ассоциированную с неврологическим заболеванием, таким как рассеянный склероз, синдром хронической усталости, и улучшение когнитивной дисфункции и для улучшения познавательной функции при ее нарушении. Установление объектов, нуждающихся в лечении описанных выше заболеваний и состояний, с легкостью может осуществляться специалистом в данной области. Специалист в данной области может легко определить с помощью клинических исследований, медицинского осмотра и истории болезни/семейных заболеваний, объект, нуждающийся в таком лечении. Терапевтически эффективное количество может быть легко определено лечащим врачом, являющимся специалистом в данной области, используя обычные методы и результаты наблюдений, полученных при аналогичных случаях заболеваний. При определении терапевтически эффективного количества лечащим врачом рассматривается множество факторов, включая, но этим не ограничиваясь, вид объекта; его размер, возраст и общее состояние здоровья; другие заболевания; степень заболевания или серьезность заболевания; ответную реакцию отдельного объекта; конкретные вводимые соединения; способ введения; характеристики биодоступности вводимого препарата; режим введения; применение сопутствующего лечения и другие подобные обстоятельства. Количество соединений формулы (I), (I-A), (II) или (II-A), которые необходимы для достижения желаемого биологического эффекта, будут зависеть от ряда факторов, включая дозу вводимого препарата, химические характеристики (например, гидрофобность) используемых соединений, активность со- 21006135 единения, тип заболевания, степень заболевания больного и путь введения. Обычно при парентеральном введении соединения по данному изобретению могут вводиться в водном физиологическом буферном растворе, содержащем около 0,1-10% мас./об. соединения. Обычно доза находится в области от около 1 мкг/кг до около 1 г/кг массы тела в день; предпочтительно доза находится в области от около 0,01 до 100 мг/кг массы тела в день. Предпочтительно дневная доза для взрослого включает около 25, 50, 100 и 200 мг и эквивалентную дозу для ребенка. Предпочтительная доза вводимого препарата, вероятно, зависит от таких переменных, как вид и степень заболевания, общее состояние здоровья, относительная биологическая эффективность выбранного соединения и состава носителя для соединения, его пути введения. Соединения по настоящему изобретению могут вводиться в виде стандартной лекарственной формы, где термин стандартная лекарственная форма означает единичную дозу, которую необходимо ввести пациенту и которая может быть легко составлена и упакована, оставаясь физически и химически стабильной лекарственной формой, включающей либо только активное соединение, либо фармацевтически приемлемую композицию, описанную здесь и далее. По существу, обычно дневная доза составляет около 0,1-100 мг/кг массы тела. В соответствии с общими правилами стандартные дозы изменяются от около 0,1 до около 1000 мг в день. Предпочтительно стандартная доза, вводимая от одного до четырех раз в день, составляет от приблизительно 1 до приблизительно 500 мг и даже более предпочтительно от приблизительно 10 до приблизительно 300 мг два раза в день. В альтернативном способе описания эффективной дозы предпочтительной пероральной стандартной дозой является та, которая необходима для достижения уровня в сыворотке крови приблизительно от 0,05 до 20 мкг/мл и более предпочтительно приблизительно 1 до приблизительно 20 мкг/мл на объект. Описанные здесь соединения могут быть введены в состав фармацевтических композиций путем смешивания с одним или несколькими фармацевтически приемлемыми инертными наполнителями. Такие композиции могут быть получены для применения путем перорального введения, в частности, в виде таблеток или капсул; или путем парентерального введения, в частности, в виде жидких растворов, суспензий или эмульсий; или интраназально, в частности, в виде порошков, капель или аэрозолей для носа; или кожно, например, местно или через транскожные пластыри. Композиции могут быть удобно введены в виде стандартной лекарственной формы и могут быть приготовлены любыми из способов, известных в фармацевтической области, например, как описано вRemington: The Science and Practice of Pharmacy, 20th ed.; Gennaro, A. R., Ed.; Lippincott WilliamsWilkins: Philadelphia, PA, 2000. Фармацевтически совместимые связующие агенты и/или вспомогательные вещества могут быть включены как часть композиции. Пероральная композиция будет обычно включать инертный разбавляющий носитель или пищевой носитель. Таблетки, пилюли, порошки, капсулы, драже и тому подобное могут содержать один или несколько из любых следующих ингредиентов или соединений сходной природы: связующий компонент, такой как микрокристаллическая целлюлоза или смола трагаканта; разбавитель, такой как крахмал или лактоза; разрыхляющие вещества, такие как крахмал и производные целлюлозы; смягчающее вещество, такое как стеарат магния; агент скольжения, такой как коллоидный диоксид кремния; подслащивающий агент, такой как сахар или сахарин; или вкусовая добавка, такая как мята или метилсалицилат. Капсулы могут быть в форме твердой капсулы или мягкой капсулы, которые обычно получают из смесей желатина, необязательно смешанных с мягчителями, а также крахмальной капсулы. Кроме того, лекарственные формы могут содержать различные другие вещества, которые модифицируют физическую форму лекарственной формы, например покрытия из сахара, шеллака или энтеросолюбилизирующих агентов. Другие пероральные лекарственные формы в виде сиропа или эликсира могут содержать агенты подслащивания,консерванты, красители, красящие агенты и ароматизаторы. Кроме того, активные соединения могут быть включены в быстро растворяющиеся составы модифицированного высвобождения или длительного высвобождения, и где такие композиции длительного высвобождения являются предпочтительно бимодальными. Предпочтительные композиции включают фармацевтические композиции, в которых соединение по настоящему изобретению входит в состав для перорального или парентерального введения, или более предпочтительно в которых соединение по настоящему изобретению входит в состав таблетки. Предпочтительные таблетки включают лактозу, кукурузный крахмал, силикат магния, кроскармеллозу натрия,повидон, стеарат магния или тальк в любом сочетании. Также аспектом настоящего описания является то, что соединение по настоящему изобретению может быть включено в пищевой продукт или жидкость. Жидкие препараты для введения включают стерильные водные или неводные растворы, суспензии и эмульсии. Жидкие композиции могут также включать связующие компоненты, буферы, консерванты,желирующие агенты, подслащивающие, ароматизирующие и окрашивающие агенты и тому подобное. Неводные растворители включают спирты, пропиленгликоль, полиэтиленгликоль, растительные масла,такие как оливковое масло и органические сложные эфиры, такие как этилолеат. Водные носители включают смеси спиртов и воды, буферированную среду и соль. В частности, биологически совместимый биоразлагаемый полимер лактида, сополимер лактида/гликолида или сополимеры полиоксиэтиленаполиоксипропилена могут быть полезными инертными наполнителями для контроля за высвобождением активного соединения. Внутривенные носители могут включать жидкие и питательные наполнители,- 22006135 электролитные наполнители, такие как основанные на декстрозе Рингера (Ringer) и т.п. Другие потенциально полезные перентеральные системы доставки для этих активных соединений включают сополимерные частицы этилен-винилацетата, осмотические насосы, имплантируемые системы инфузии и липосомы. Альтернативные способы введения включают композиции для ингаляции, которые включают такие средства, как сухой порошок, аэрозоль или капли. Они могут содержаться в водных растворах, например эфир полиоксиэтилен-9-лаурила, гликохолят и деоксихолят или масляные растворы для введения в виде капель для носа или в виде геля, который будет применяться интраназально. Препараты для буккального введения включают, например, таблетки или пастилки и могут также включать ароматизирующую основу, такую как сахар или гуммиарабик, и другие инертные наполнители, такие как гликохолят. Препараты,подходящие для ректального введения, предпочтительно представлены в виде стандартной лекарственной формы суппозиториев с твердым основным носителем, таким как масло какао, и могут включать салицилат. Препараты для местного применения на коже предпочтительно имеют вид мази, крема, лосьона, пасты, геля, спрея, аэрозоля или масла. Носители, которые могут использоваться, включают вазелин,ланолин, полиэтиленгликоли, спирты или их сочетания. Препараты, подходящие для чрезкожного введения, могут быть представлены в виде дискретных пластырей и могут быть липофильными эмульсиями или буферированными водными растворами, растворенными и/или диспергировэнными в полимере или адгезиве. Соединения по настоящему изобретению могут использоваться как единственный активный ингредиент в фармацевтической композиции. Альтернативно, они могут использоваться в сочетании или объединены с другими фармацевтическими агентами, связанными с другими болезненными состояниями. В частности, соединения формул (I), (I-A), (II) или (II-A) могут быть объединены с агентами, которые являются полезными для лечения ослабленного когнитивного восприятия, связанного с различными болезненными состояниями, включающими, но не ограничивающимися этим, возраст, травма, стресс или кратковременный ослабление вследствие химического дисбаланса или токсичности, гиперсомию, депрессию, болезнь Альцгеймера, деменцию, не связанную с болезнью Альцгеймера, включая деменциию тела Леви, сосудистую деменцию и деменцию Бинсвангера, шизофрению и тому подобное. Настоящее изобретение может включать, следовательно, комбинации соединений по настоящему изобретению с аналогами эбурнана, гетероциклические индукторы тирозингидроксилазы, 3,4-дифенилхроманы, метаболиты такрина, азациклические соединения, соединения полиамина или тиамин; неантихолинергические антидепрессанты, такие как бензодиазепины; алифатические фентиазины, такие как хлорпромазин; пиперидины, такие как тиоридазин; пиперазины, такие как трифторперазин, флюфеназин и перфеназин; дибензоксазепины, такие как локсапин; дигидроиндолоны, такие как молиндон; тиоксантены, такие как тиотиксен; бутирофеноны, такие как галоперидол; дифенилбутил-пиперидины, такие как пимозид; дибензодиазепин, такие как хлозапин; бензисоксазол, такой как рисперидон; тиенобензодиазепин, такой как оланзапин; дибензотиазепин, такой как кветиапин; имидазолидинон, такой как сертиндол, бензисотиазолил-пиперазин, такой как зипразидон и т.п. Синтез. Соединения по настоящему изобретению могут быть получены способами, известными специалистам в данной области. Соединения могут быть синтезированы, например, способами, описанными ниже,или их вариациями, которые принимаются специалистами в данной области. Соответствующие модификации и изменения очевидны и хорошо известны или легко доступны в научной литературе для специалиста в данной области. Следует учесть, что соединения по настоящему изобретению могут содержать один или несколько асимметрично замещенных атомов углерода и могут быть выделены в виде оптически активных или рацемических форм. Таким образом, предполагаются все хиральные, диастереометрические, рацемические формы и все геометрические изомерные формы структуры, если конкретная стереохимическая или изомерная форма конкретно не определена. В данной области хорошо известно, как получать и выделять такие оптически активные формы. Например, смеси стереоизомеров могут быть выделены стандартными методами, включая, но этим не ограничиваясь, разделение рацемических форм, нормальную с обращенной фазой и хиральную хроматографию, преимущественное образование солей, перекристаллизацию и тому подобное, или хиральным синтезом либо из хиральных исходных веществ или конкретным синтезом целевых хиральных центров. Как легко понять, функциональные группы, имеющиеся в соединениях по настоящему изобретению, могут содержать защитную группу в процессе синтеза. Например, заместители боковой цепи аминокислоты соединений формул (I), (I-A), (II) или (II-A) могут быть замещены защитными группами, такими как трет-бутоксикарбонильная или бензилоксикарбонильная группы. Защитные группы сами по себе известны как химические функциональные группы, которые могут быть избирательно присоединены и удалены из функциональных групп, таких как гидроксильные группы и карбоксильные группы. Эти группы имеются в химическом соединении для того, чтобы делать такую функциональную группу инертной к условиям химической реакции, которой соединение подвергается. Любая из разнообразных защитных групп может использоваться в настоящем изобретении. Предпочтительные защитные группы- 23006135 включают бензилоксикарбонильную ("Cbz") группу, трет-бутилоксикарбонильную ("Воc") группу и тозильную (п-толуолсульфонильную, "tos") группу. Другие предпочтительные защитные группы по изобретению можно найти у Greene, Т.W. and Wuts, P.G.M., Protective Groups in Organic Synthesis 2d. Ed.,WileySons, 1991. Соединения по настоящему изобретению могут быть получены в соответствии с представленными следующими схемами. Реагенты и исходные вещества коммерчески доступны или легко синтезируются известными способами любым специалистом в данной области. Все заместители, если иное не указано,определены выше. Общий способ синтеза показан на схеме А для получения соединений формулы (I) [где Y=C(R1)(R2) и m, n=0] или (I-A). Схема А Схема А, стадия 1. Синтез соединения общей структуры с. На стадии 1a соответствующий арилгалогенид а подвергают реакции обмена металла с металлоорганическим соединением с получением соответствующего металлоарилсоединения. Например, подходящее галогенароматическое или галогенгетероароматическое соединение (соединение а) подвергают взаимодействию с соответствующим производным алкиллития в апротонном растворителе при температуре -78 С. Соответствующее галогенароматическое или галогенгетероароматическое соединение является соединением, где Ar1 имеет значения, указанные для целевого продукта. Соответствующее производное алкиллития представляет собой соединение, которое может участвовать в реакции обмена металл-галоген. На стадии 1b соответствующий арилальдегид b добавляют к предварительно полученному металлоарильному производному с получением желаемого диарилспирта с. Например, соответствующий ароматический альдегид или гетероароматический альдегид (соединение b) в апротонном растворителе добавляют к реакционному продукту со стадии 1 а. Соответствующий гетероароматический альдегид представляет собой гетероароматический альдегид, где Ar2 имеет значения, указанные для целевого продукта. После завершения взаимодействия реакционную смесь гасят соответствующим гасящим агентом и продукт, соединение с, выделяют обычными способами, обычно используемыми специалистами в данной области. Например, охлажденный (от -70 до -78 С) раствор соответствующего галогенароматического или галогенгетероароматического производного (соединение а) подвергают взаимодействию с н-бутиллитием (1,1 экв.) в сухом эфире. После перемешивания в течение периода времени, достаточного для завершения реакции обмена галоген-металл, в реакционный сосуд медленно добавляют следующий реа- 24006135 гент, соответствующий гетероароматический альдегид (соединение b), в эфире. Перемешивание продолжают еще 2-3 ч при пониженной температуре. Охлаждающую баню отставляют и реакционной смеси дают медленно нагреться до комнатной температуры, затем реакцию гасят предпочтительно насыщенным раствором NH4Cl. Смесь экстрагируют органическим растворителем (эфиром или этилацетатом). Органический слой промывают насыщенным солевым раствором, сушат (МgSO4 или Na2SO4) и концентрируют с получением сырого продукта. Очистку производят с использованием известных способов очистки (предпочтительно методом хроматографии на колонке и/или перекристаллизацией) с получением чистого соединения с. Этот способ является адаптацией известного способа, описанного ранее Gronowitz,S.; Eriksson, B. Arkiv Kemi 1963, 335, включено здесь в качестве ссылки в полном объеме. Альтернативно, данный класс соединений, где Ar1 такой, как Ar2, может быть получен обработкой двух эквивалентов соответствующего галогенгетероароматического производного с двумя эквивалентами н-бутиллития и затем одним эквивалентом этилформиата, как описано Nenajdenko, V.G.; Baraznenok, I.L.; Balenkova, E.S.J. Org. Chem. 1998, 6132, включено здесь в качестве ссылки в полном объеме. Схема А, стадия 2. Синтез соединения общей структуры d. На стадии 2 а спиртовую группу соединения с преобразуют в соответствующий тиол. Тиол на стадии 2b подвергают реакции замещения с соответствующим галогензамещенной алкилкарбоновой кислотой структуры Br-(CH2)m-Y-(СН 2)n-СООН с получением соединения d. Например, диарилспирт с подвергают взаимодействию с тиомочевиной в присутствии кислоты для преобразования тиоурониевой группы,которую затем гидролизуют в присутствии щелочного основания и подвергают взаимодействию с соответствующей галогензамещенной алкилкарбоновой кислотой с получением соединения d (стадия 2b). Соответствующее производное кислоты представляет собой производное кислоты, в котором m, n, Y такие, как определено для целевого продукта. Например, на стадии 2 а соответствующее количество тиомочевины обрабатывают 48%-ной НВr и водой. Смесь нагревают (предпочтительно до 60-70 С). Затем прибавляют соединение с. Температуру реакционной смеси повышают (предпочтительно до 90-95 С) и перемешивание продолжают еще некоторое время для завершения реакции. Реакционную смесь охлаждают до комнатной температуры (в некоторых случаях может потребоваться ледяная баня) и выпавший твердый продукт следует отфильтровать и тщательно промыть водой. На стадии 2b к влажному твердому продукту с предыдущей стадии добавляют еще воду и обрабатывают водным основанием, предпочтительно раствором гидроксида натрия. Смесь нагревают (предпочтительно до 70-80 С, но в некоторых случаях может потребоваться и более высокая температура) и к ней добавляют подходящее количество производного галогензамещенной алкилкарбоновой кислоты в воде(или в некоторых случаях в спиртовом растворителе). Реакционную смесь выдерживают при повышенной температуре (предпочтительно 100-110 С) в течение соответствующего периода времени, охлаждают, добавляют воду и промывают органическим растворителем (предпочтительно эфиром). Щелочной водный слой подкисляют раствором неорганической кислоты (например, водным раствором НСl). Водный (кислый) раствор затем несколько раз экстрагируют органическим растворителем (например, эфиром или этилацетатом). Объединенный органический слой промывают насыщенным солевым раствором,сушат (MgSO4 или Na2SO4) и концентрируют с получением сырого продукта, который непосредственно может быть использован на следующей стадии. Однако можно произвести очистку с использованием известных способов очистки (например, перекристаллизацией) с получением чистого соединения d. Этот способ является адаптацией известного способа, описанного ранее в патенте US 4177290,включено здесь в качестве ссылки в полном объеме. Схема А, стадия 3. Синтез соединения общей структуры е. На стадии 3 а карбоновую кислоту преобразуют в соответствующее производное кислоты, которое затем подвергают взаимодействию с соответствующим амином с получением соединения е. Например,на стадии 3 а соединение d может быть преобразовано в соответствующий хлорангидрид кислоты или в соответствующий активированный сложный эфир. Хлорангидрид кислоты может быть получен путем взаимодействия соединения d с тионилхлоридом в ароматическом углеводородном растворителе в условиях кипячения с обратным холодильником. Альтернативно, активированный сложный эфир может быть получен с помощью различных агентов, известных в данной области, таких как тетрафторборат 2-(1 Нбензотриазол-1-ил)-1,1,3,3-тетраметилурония (TBTU), N-метилфорфолин (NMM) и диметилформамид (ДМФ). На стадии 3b продукт со стадии 3 а подвергают взаимодействию с соответствующим амином структуры NHR3R4 с получением желаемого соединения е. Соответствующий амин представляет собой амин, в котором R3 и R4 соответствуют указанным для целевого продукта. Например, раствор соответствующей карбоновой кислоты (соединение d) либо в бензоле, либо в толуоле нагревают до кипения с обратным холодильником и к нему медленно добавляют подходящее количество тионилхлорида. Смесь кипятят с обратным холодильником до расходования исходного продукта (что подтверждается аналитическими методами), охлаждают и удаляют растворитель. Полученный осадок обрабатывают соответствующим органическим растворителем (предпочтительно тетрагидрофураном или метиленхлоридом) и обрабатывают газообразным аммиаком (или 28%-ным водным раствором гидроксида аммония) или соответствующим амином. Реакционную смесь затем распределяют в воде и- 25006135 органическом растворителе (предпочтительно этилацетате). Отделенный органический слой промывают водой, разбавленной кислотой, разбавленным основанием и насыщенным раствором соли, сушат над осушающим агентом (например, МgSO4 или Na2SO4) и концентрируют с получением сырого продукта,который может быть очищен с помощью колоночной хроматографии и/или перекристаллизацией соединения е. Схема А, необязательная стадия 4. Синтез соединения общей структуры f. Соединения структуры е необязательно может быть окислено с получением соединения структурыf. Таким образом, соединение f получают путем взаимодействия соединения е в подходящем растворителе с соответствующим окислителем. Соответствующий окислительный агент является окислительным агентом, который окисляет сульфидную группу соединения е. Соответствующий продукт выделяют и очищают способом, хорошо известным в данной области. Например, к охлажденному (от -15 до -25 С) раствору соединения е в органическом растворителе(предпочтительно метиленхлориде или хлороформе) медленно прибавляют подходящий окислительный агент (например, м-хлорпероксибензойную кислоту [m-СРВА], 1 экв.) в том же растворителе. Перемешивание продолжают при низкой температуре до расходования исходного продукта, как показывают различные аналитические методы. Реакционную смесь затем тщательно промывают насыщенным раствором бикарбоната натрия, водой и насыщенным солевым раствором, соответственно, сушат над осушителем (например, MgSO4 или Na2SO4) и концентрируют. Желаемый продукт (соединение f) очищают, если необходимо, с помощью известных методов очистки (предпочтительно с помощью хроматографии на колонке и/или перекристаллизацией). В некоторых случаях окисление осуществляют,используя 50%-ную Н 2O2 в растворителе ледяной уксусной кислоте. Общий способ синтеза представлен на схеме В для получения соединения формулы (II) [где кольцо А представляет собой фенилен; Y=C(R1)(R2) и m, n, r, s=0] и (II-A). Схема В Схема В, стадии 1, 2 и 3. Синтез соединений общей структуры dd, ее и ff. Стадии синтеза по схеме В включают тот же многостадийный общий способ, который представлен на схеме А, где схема В, стадии 1-3, соответствуют схеме А, стадии 2-4 соответственно. Общий метод синтеза представлен на схеме С для получения соединений формулы (I-A), где n=0 и Схема С, стадии 1 и 2. Синтез соединений общей структуры ddd и еее. Стадии синтеза по схеме С, стадии 1 и 2 включают тот же многостадийный общий способ, который представлен на схеме А, стадии 2-3 соответственно, с получением соединений структуры еее. Схема С, стадия 3. Синтез соединений общей структуры fff. Амидную группу соединения еее преобразуют в соответствующую тиоамидную группу fff с помощью соответствующего реагента переносчика серы. Например, смесь соединения еее и реагента Лавессона (Lawesson) (1,05 экв.) в подходящем растворителе (диметоксиэтане или тетрагидрофуране) нагревают до кипения с обратным холодильником до расходования исходного продукта. После охлаждения желаемый продукт (соединение fff) получают путем использования известных методов очистки (предпочтительно с помощью хроматографии на колонке и/или перекристаллизацией). Схема С, стадия 4. Синтез соединений общей структуры ggg. Тиоамидную группу соединения fff циклизуют до соответствующей тиазольной группы. Например,смесь соединения fff и соответствующего бромметилкетона (1,1 экв.) в подходящем растворителе (например, этаноле) нагревают до кипения с обратным холодильником до расходования исходного продукта. После охлаждения желаемый продукт (соединение ggg) получают путем использования известных методов очистки (предпочтительно с помощью хроматографии на колонке и/или перекристаллизацией). Схема С, стадии 5-6. Синтез соединений общей структуры hhh и iii. Стадии синтеза по схеме С, стадии 5 и 6 включают тот же многостадийный общий способ, который представлен на схеме А, стадии 3 и 4 соответственно, с получением соединений структуры hhh и iii.- 27006135 Общий метод синтеза представлен на схеме D для получения соединений формулы (II-A), где n=0 и Схема D, стадии 1-6. Синтез соединений общей структуры hhhh и iiii. Стадии синтеза по схеме D включают тот же многостадийный общий способ, который представлен на схеме С с получением соединений структуры hhhh и, необязательно, iiii. Общий метод синтеза представлен на схеме Е для получения соединения формулы (I) или (I-A), гдеR1 или R2 могут вместе с либо R3, либо R4 образовывать 3-7-членное гетероциклическое кольцо. Соответствующим образом образованное кольцо представлено на схеме Е как G. В настоящей схеме R1 вместе R3 образует гетероциклическое кольцо G. Понятно, что R1 также может вместе с R4 образовывать кольцо G, или R2 также может вместе с R3 образовывать кольцо G, или R2 также может вместе сR4 образовывать кольцо G. Реагенты и исходные продукты являются коммерчески доступными или могут быть легко синтезированы хорошо известными способами обычным средним специалистом в данной области. На реакционной схеме Е все заместители, если не указано специально, такие, как определено выше. Схема Е, стадии 1 и 2. Синтез соединений общей структуры 60, содержащей соединения формулы(I), где или R1, или R2 вместе с или R3, или R4 образуют 3-7-членное гетероциклическое кольцо G. На первой стадии соответствующий меркаптолактам 59 подвергают взаимодействию с соответствующим диарилметанолом, соединением 27, в присутствии слабой кислоты с целью осуществления нуклеофильного замещения по метанольному углероду с образованием соответствующего тиоэфира. Соответствующий меркаптолактам 59 и соответствующий диарил- или дигетероарилметанол 27 представляют собой соединения, где Ar1, Ar2, R2 и R4 такие, как определено выше для целевого продукта. На второй стадии тиоэфир, полученный на первой стадии, необязательно подвергают окислению подходящим окислительным агентом с получением соединения 60. Подходящий окислительный агент представляет собой окислительный агент, который окисляет тиоэфир до его соответствующего сульфоксида или сульфона. Метод синтеза представлен на реакционной схеме Е для получения соединения формулы (II-A), гдеR1 или R2 могут вместе с либо R3, либо R4 образовывать 3-7-членное гетероциклическое кольцо. Подобный способ может использоваться для получения соответствующего соединения формулы (II-A). Соответствующим образом образованное кольцо представлено на схеме Е как G. На настоящей схеме R1 вместе с R3 образует гетероциклическое кольцо G. Понятно, что R1 также может вместе с R4 образовывать кольцо G, или R2 также может вместе с R3 образовывать кольцо G, или R2 также может вместе сR4 образовывать кольцо G. Реагенты и исходные продукты являются коммерчески доступными или могут быть легко синтезированы хорошо известными способами обычным средним специалистом в данной области. На реакционной схеме Е все заместители, если не указано специально, такие, как определено выше. Схема F Схема F, стадии 1 и 2. Синтез соединений общей структуры 62, содержащей соединения формулы(II-A), где или R1, или R2 вместе с или R3, или R4 образуют 3-7-членное гетероциклическое кольцо G. На первой стадии соответствующий меркаптолактам 59 подвергают взаимодействию с соответствующим диарил- или дигетероарилметанолом, соединением 27 а, в присутствии слабой кислоты с целью осуществления нуклеофильного замещения по метанольному углероду с образованием соответствующего тиоэфира. Соответствующий меркаптолактам 61 и соответствующий диарил- или дигетероарилметанол 27 а представляют собой соединения, где А, X, R2 и R4 такие, как определено выше для целевого продукта. На второй стадии тиоэфир, полученный на первой стадии, необязательно подвергают окислению подходящим окислительным агентом с получением соединения 62. Подходящий окислительный агент представляет собой окислительный агент, который окисляет тиоэфир до его соответствующего сульфоксида или сульфона. Примеры Другие признаки изобретения ясны из следующего описания экспериментальных воплощений изобретения. Эти примеры представлены для иллюстрации изобретения, и не предназначены для его ограничения. Следующие примеры 1-6 были синтезированы в соответствии со схемой 1. Получение соединения С. К энергично перемешиваемой смеси тиомочевины (соединение В, 5 г, 0,066 моль), 48% НВr (30 мл) и воды (5 мл) при 70-75 С добавляют 9-гидроксифлуорен (соединение А, 9,28 г, 0,051 моль) небольшими порциями, затем дополнительное количество воды (30 мл). Реакционную смесь затем нагревают до 100105 С (температура бани), выдерживают в течение еще 30 мин и охлаждают до комнатной температуры. Выпавший осадок фильтруют, промывают водой и эфиром последовательно и сушат в вакууме с получением 14 г соответствующей соли тиоурония, которую используют на следующей стадии без дополнительной очистки. К энергично перемешиваемой смеси вышеуказанной соли тиоурония (10,47 г) в 10 н. NaOH (10,26 мл) и воде (25 мл) при 60-65 С медленно добавляют 3-бромпропионовую кислоту (5,24 г, 0,034 моль) в воде (20 мл). Реакционную смесь затем нагревают до 105-110 С (температура бани), выдерживают в течение еще 30 мин, охлаждают до комнатной температуры, разбавляют водой (25 мл) и промывают эфиром (350 мл). Водный щелочной слой подкисляют (рН 2-3) конц. НСl и экстрагируют этилацетатом (3100 мл). Объединенный органический слой сушат (MgSO4) и концентрируют с получением 7,80 г соединения С, которое используют на следующей стадии без дополнительной очистки; 1H-ЯМР (СDCl3)7,80(м, 4 Н), 7,30 (м, 4 Н), 4,90 (с, 1 Н), 2,10 (м, 4 Н). Получение соединения D. Это соединение получают из соединения А, используя тот же способ, что описан выше для синтеза соединения D, за исключением того, что на стадии алкилирования вместо 3-бромпропионовой кислоты используют 4-бромбутановую кислоту; 1H-ЯМР (СDCl3)7,70 (м, 4 Н), 7,40 (м, 4 Н), 4,80 (с, 1 Н), 2,20 (т,2 Н), 2,00 (т, 2 Н), 1,40 (м, 2 Н). Получение соединения Е. К кипящему раствору соединения С (7,8 г, 0,029 моль) в бензоле (40 мл) медленно добавляют тионилхлорид (5,3 мл). Смесь кипятят еще 2 ч, охлаждают, фильтруют и концентрируют при пониженном давлении с получением 8 г соединения Е, которое сразу используют на следующей стадии без дополнительной очистки. Получение соединения F. Это соединение получают из соединения D, используя тот же способ, что описан выше для синтеза соединения Е из соединения С. Пример 1. Синтез соединения G. Соединение Е (8 г) с предыдущей стадии растворяют в метиленхлориде (20 мл) и добавляют к энергично перемешиваемому охлажденному (0 С) 28%-ному раствору NH4OH (50 мл). Ледяную баню отставляют и перемешивание продолжают еще час. Реакционную смесь разбавляют водой (30 мл) и экстрагируют метиленхлоридом (230 мл). Объединенный органический слой промывают водой (220 мл),3%-ным раствором NаНСО 3 (230 мл), насыщенным солевым раствором (130 мл), сушат (Na2SO4) и концентрируют с получением остатка, который растирают в эфире эфиром с получением 6,30 г соединения G; 1H-ЯМР (ДМСО-d6)7,90 (д, 2 Н), 7,70 (д, 2 Н), 7,40 (м, 4 Н), 7,30 (широкий, 1 Н), 6,80 (широкий,1 Н), 5,20 (с, 1 Н), 2,30 (т, 2 Н), 2,10 (т, 2 Н). Пример 2. Синтез соединения Н. Это соединение получают из соединения Е, используя тот же способ, что описан выше для синтеза соединения G, за исключением того, что вместо 28%-ного NH4OH на стадии аминирования используют
МПК / Метки
МПК: C07C 323/60, C07D 333/18, A61P 1/14, A61K 31/165
Метки: тиоацетамиды, замещенные
Код ссылки
<a href="https://eas.patents.su/30-6135-zameshhennye-tioacetamidy.html" rel="bookmark" title="База патентов Евразийского Союза">Замещенные тиоацетамиды</a>
Предыдущий патент: Фторзамещенные циклоалканоиндолы, композиции, содержащие такие соединения, и способы лечения
Следующий патент: Способ получения вируса или вирусного белка для получения вакцины
Случайный патент: Способ повышения выхода ароматических углеводородов из алифатических углеводородов с2-с4