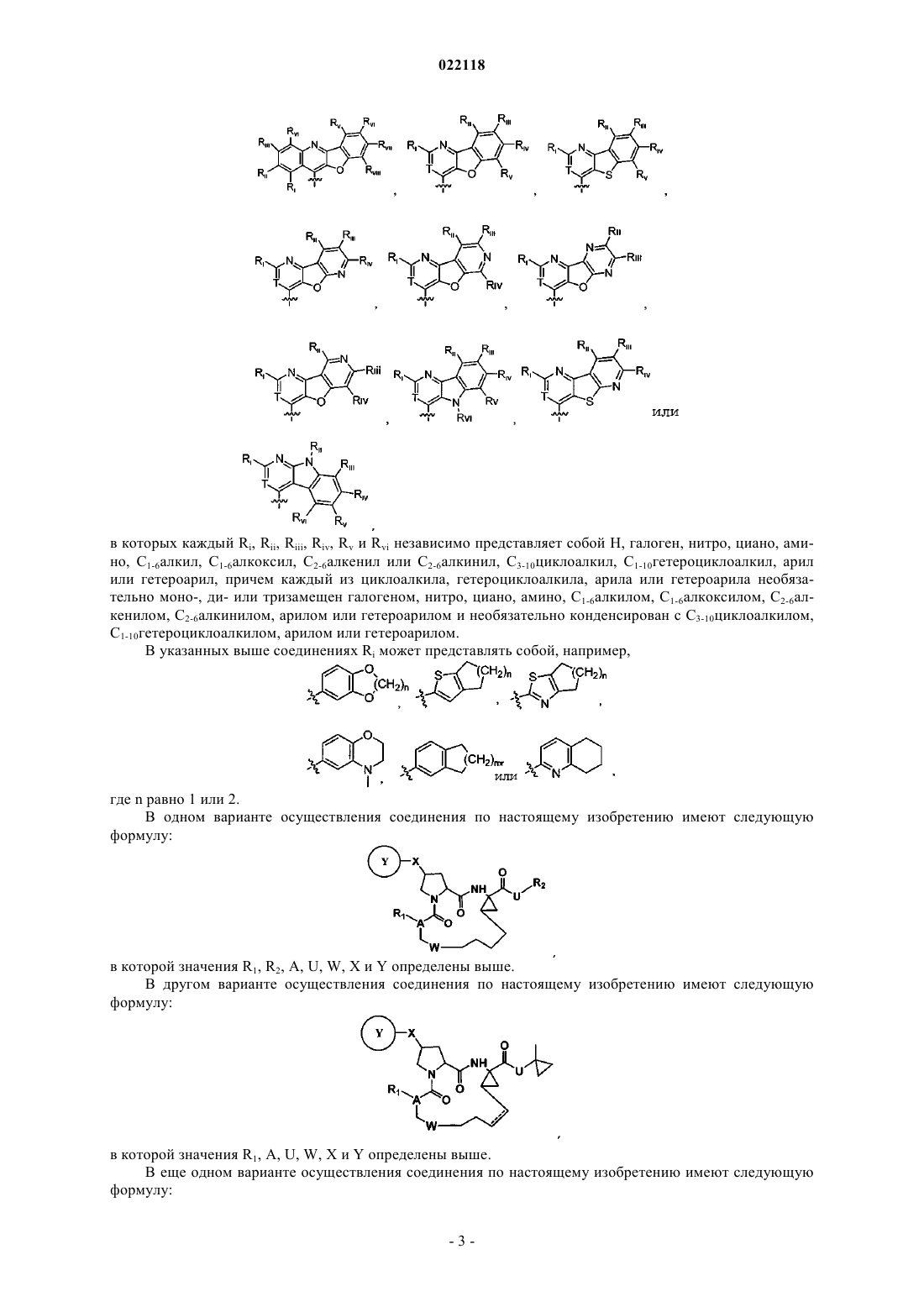
Ингибиторы протеазы hcv
Номер патента: 22118
Опубликовано: 30.11.2015
Авторы: Чэнь Чих-Мин, Линь Чу-Чун, Тсэн Ко-Фэн, Ло Пинь, Кинг Чи-Син Ричард, Ли Куан-Юань, Чэн Пэй-Чинь, Лю Йо-Чин, Лю Чэнь-Фу
Формула / Реферат
1. Соединение следующей формулы
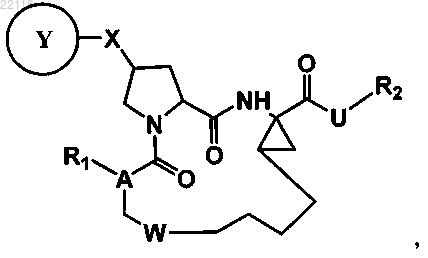
в которой
R1 представляет собой -Н или -NH-Z-R; где R представляет собой Н или представляет собой фрагмент, выбранный из C1-6алкила, С3-10циклоалкила, 3-10-членного гетероциклоалкила, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы, 6-10-членного арила и 5-10-членного гетероарила, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, каждый из которых необязательно моно-, ди- или тризамещен С1-6алкоксилом, С2-6алкенилом или С2-6алкинилом; и Z представляет собой -С(О)-, -С(О)О-, -С(О)С(О)О- или -C(O)NR'-, причем R' представляет собой Н или С1-6алкил;
R2 представляет собой Н или С3-10циклоалкил, необязательно моно-, ди- или тризамещенный С1-6алкилом;
А представляет собой N или СН;
U представляет собой -NHSO2-;
W представляет собой -(СН2)m-, причем m равно 1 или 2;
X представляет собой -О и
Y представляет собой
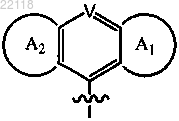
или

где V представляет собой N;
Т представляет собой -СН- или -N-;
каждый из A1 и А2 независимо представляет собой фрагмент, выбранный из 3-10-членного гетероциклоалкила, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы, 6-10-членного арила и 5-10-членного гетероарила, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, каждый из которых необязательно моно-, ди- или тризамещен галогеном, С1-6алкилом или С1-6 алкоксилом или необязательно конденсирован с 6-10-членным арилом; и
Ri представляет собой С1-6алкил, С3-10циклоалкил, 6-10-членный арил или 5-10-членный гетероарил, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, причем С1-6алкил необязательно моно-, ди- или тризамещен галогеном, и причем каждый из С3-10циклоалкила, 6-10-членного арила и 5-10-членного гетероарила необязательно моно-, ди- или тризамещен галогеном, амино, С1-6алкилом или С1-6алкоксилом или необязательно конденсирован с 3-10-членным гетероциклоалкилом, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы.
2. Соединение по п.1, в котором А представляет собой СН и W представляет собой -СН2СН2-.
3. Соединение по любому из пп.1 или 2, в котором Y представляет собой
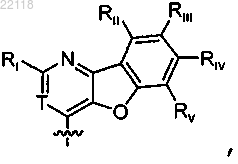
где Т представляет собой СН или N;
Ri представляет собой С1-6алкил, С3-10циклоалкил, 6-10-членный арил, 5-10-членный гетероарил, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы, причем С1-6алкил, необязательно моно-, ди- или тризамещен галогеном, и причем каждый из С3-10 циклоалкила, 6-10-членного арила и 5-10-членного гетероарила необязательно моно-, ди- или тризамещен галогеном, амино, C1-6алкилом, С1-6алкоксилом или необязательно конденсирован с 3-10-членным гетероциклоалкилом, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы;
и каждый из Rii, Riii, Riv и Rv независимо представляет собой Н, галоген, С1-6алкил или С1-6алкоксил, причем каждый из C1-6алкила и С1-6алкоксила необязательно моно-, ди- или тризамещен галогеном.
4. Соединение следующей формулы
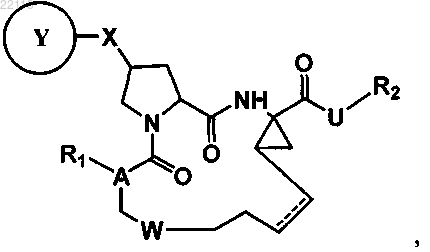
в которой
Ri представляет собой -Н или -Z-R; где R представляет собой Н или представляет собой фрагмент, выбранный из С1-6алкила, С3-10циклоалкила, 3-10-членного гетероциклоалкила, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы, 6-10-членного арила и 5-10-членного гетероарила, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, каждый из которых необязательно моно-, ди- или тризамещен галогеном, С1-6алкоксилом, С2-6алкенилом или С2-6алкинилом или 6-10-членным арилом; и Z представляет собой -С(О)-, -С(О)О-, -С(О)С(О)О- или -C(O)NR'-, причем R' представляет собой Н или С1-6алкил;
R2 представляет собой Н, С3-10циклоалкил, необязательно моно-, ди- или тризамещенный С1-6 алкилом;
А представляет собой N или СН;
U представляет собой -NHSO2-;
W представляет собой -(СН2)m-, причем m равно 1 или 2;
X представляет собой -О-;
Y представляет собой

или
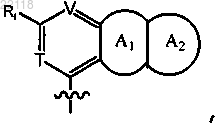
где V представляет собой N;
Т представляет собой -СН- или -N-;
каждый из А1 и А2 независимо представляет собой фрагмент, выбранный из C1-10гетероциклоалкила, 6-10-членного арила и 5-10-членного гетероарила, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, каждый из которых необязательно моно-, ди- или тризамещен галогеном, С1-6алкилом или С1-6алкоксилом или необязательно конденсирован с 6-10-членным арилом; и
Ri представляет собой С3-10циклоалкил, 6-10-членный арил или 5-10-членный гетероарил, где один, или два, или три, или четыре атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы, причем С1-6алкил необязательно моно-, ди- или тризамещен галогеном, и причем каждый из С3-10циклоалкила, 6-10-членного арила и 5-10-членного гетероарила необязательно моно-, ди- или тризамещен галогеном, амино, С1-6алкилом или С1-6алкоксилом или необязательно конденсирован с 3-10-членным гетероциклоалкилом, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы; и
--- представляет собой одинарную связь или двойную связь.
5. Соединение по п.4, в котором W представляет собой -СН2СН2- и --- представляет собой двойную связь.
6. Соединение по любому из пп.4 или 5, в котором Y представляет собой

где Т представляет собой СН или N;
Ri представляет собой С1-6алкил, С3-10циклоалкил, 6-10-членный арил, 5-10-членный гетероарил, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, причем С1-6алкил, необязательно моно-, ди- или тризамещен галогеном, и причем каждый из С3-10циклоалкила, 6-10-членного арила и 5-10-членного гетероарила необязательно моно-, ди- или тризамещен галогеном, амино, С1-6алкилом, С1-6алкоксилом или необязательно конденсирован с 3-10-членным гетероциклоалкилом, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы;
и каждый из Rii, Riii, Riv и Rv независимо представляет собой Н, галоген, С1-6алкил или С1-6алкоксил, причем каждый из С1-6алкила и С1-6алкоксила необязательно моно-, ди- или тризамещен галогеном.
7. Соединение следующей формулы:
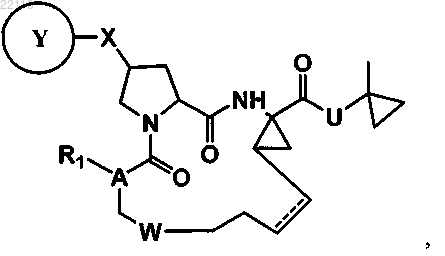
в которой
Ri представляет собой -Н, -Z-R или -NH-Z-R-; где R представляет собой Н или представляет собой фрагмент, выбранный из С1-6алкила, С3-10циклоалкила, 3-10-членного гетероциклоалкила, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы, 6-10-членного арила и 5-10-членного гетероарила, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, каждый из которых необязательно моно-, ди- или тризамещен галогеном, С1-6алкоксилом, С2-6алкенилом или С2-6алкинилом; и Z представляет собой -С(О)-, -С(О)О-, -С(О)С(О)О- или -C(O)NR'-, причем R' представляет собой Н или С1-6алкил;
А представляет собой N или СН;
U представляет собой -NHSO2-;
W представляет собой -(СН2)m-, причем m равно 1 или 2;
X представляет собой -О-;
Y представляет собой
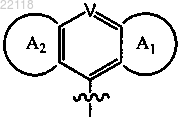
или
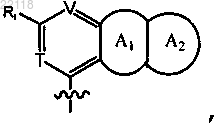
где V представляет собой N и
Т представляет собой -СН- или -N-;
каждый из А1 и А2 независимо представляет собой фрагмент, выбранный из C1-10гетероциклоалкила, арила и гетероарила, каждый из которых необязательно моно-, ди- или тризамещен галогеном, С1-6алкилом или С1-6алкоксилом или необязательно конденсирован с 6-10-членным арилом; и
Ri представляет собой С1-6алкил, С3-10циклоалкил, 6-10-членный арил, 5-10-членный гетероарил, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, причем каждый из С1-6алкила необязательно моно-, ди- или тризамещен галогеном, и причем каждый из С3-10циклоалкила, 6-10-членного арила и 5-10-членного гетероарила необязательно моно-, ди- или тризамещен галогеном, амино, С1-6алкилом или С1-6алкоксилом или необязательно конденсирован с 3-10-членным гетероциклоалкилом, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы; и
--- представляет собой одинарную связь или двойную связь.
8. Соединение по п.7, в котором А представляет собой СН; W представляет собой -СН2СН2- и --- представляет собой двойную связь.
9. Соединение по любому из пп.7 или 8, в котором Y представляет собой
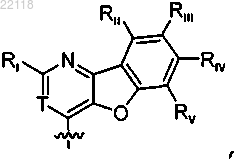
где Т представляет собой СН или N;
Ri представляет собой С1-6алкил, С3-10циклоалкил, 6-10-членный арил, 5-10-членный гетероарил, где один, или два, или три, или четыре атома гетероарильного кольца независимо выбраны из группы, состоящей из азота, кислорода и серы, причем каждый из С1-6алкила необязательно моно-, ди- или тризамещен галогеном, и причем каждый из С3-10циклоалкила, 6-10-членного арила и 5-10-членного гетероарила необязательно моно-, ди- или тризамещен галогеном, амино, С1-6алкилом или С1-6алкоксилом или необязательно конденсирован с 3-10-членным гетероциклоалкилом, где один, или два, или три атома гетероцикла независимо выбраны из группы, состоящей из азота, кислорода и серы;
и каждый из Rii, Riii, Riv и Rv независимо представляет собой Н, галоген, С1-6алкил или С1-6алкоксил, причем каждый из C1-6алкила и С1-6алкоксила необязательно моно-, ди- или тризамещен галогеном.
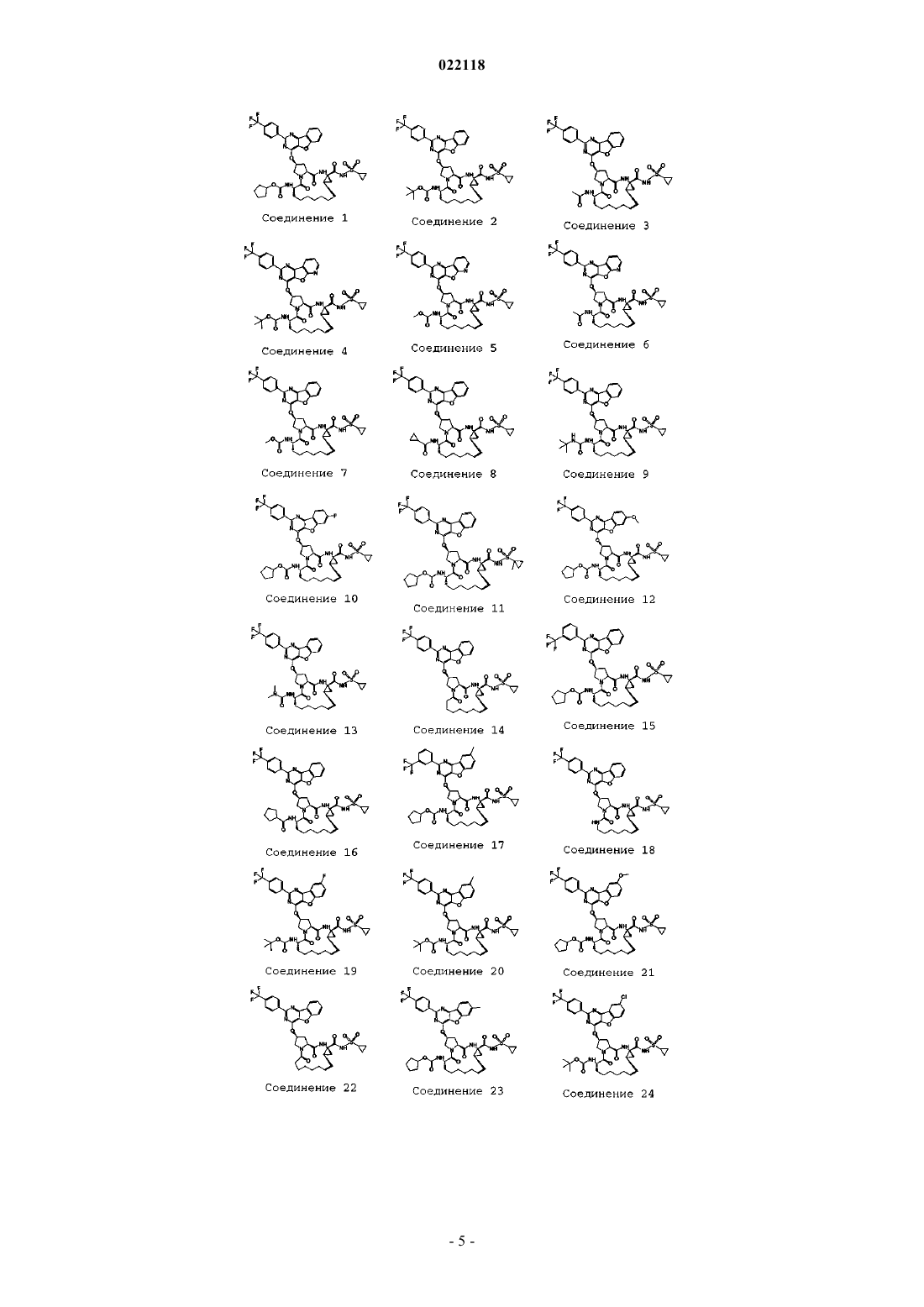
10. Соединение, которое представляет собой одно из следующих соединений:
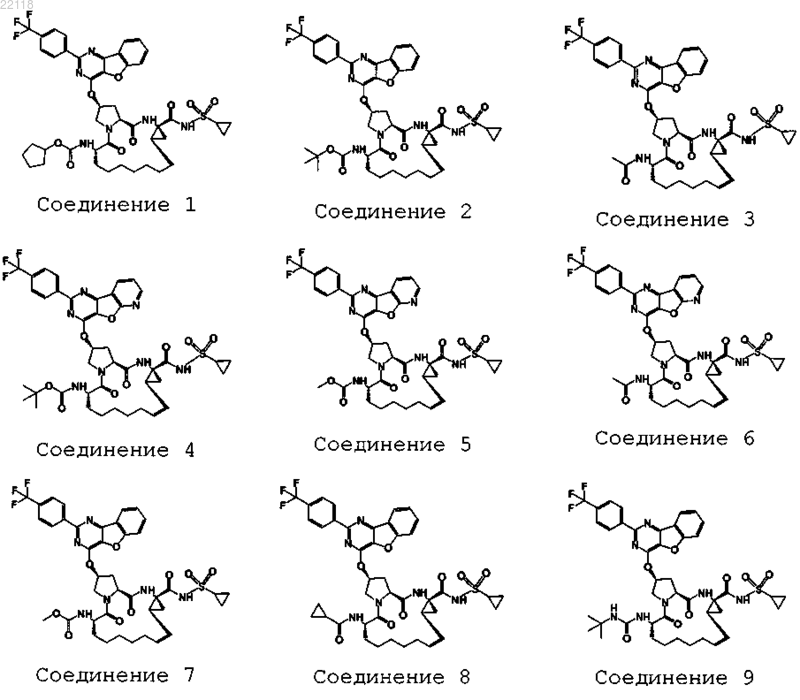
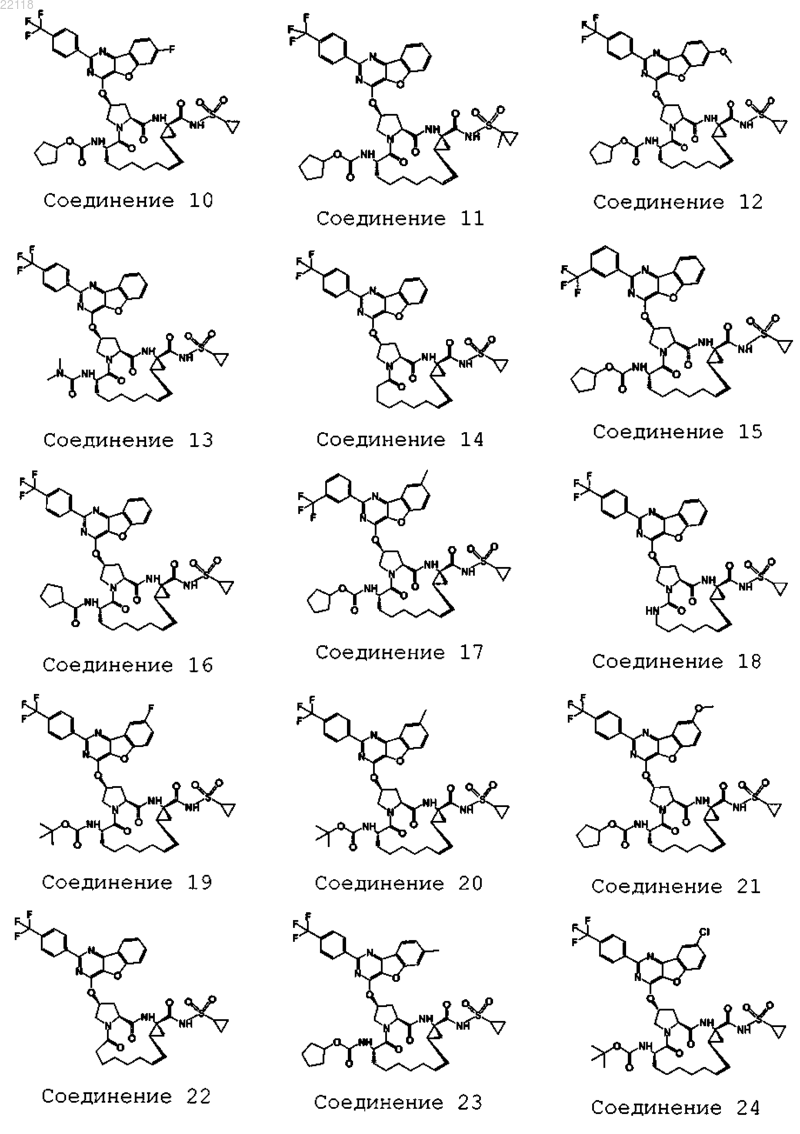
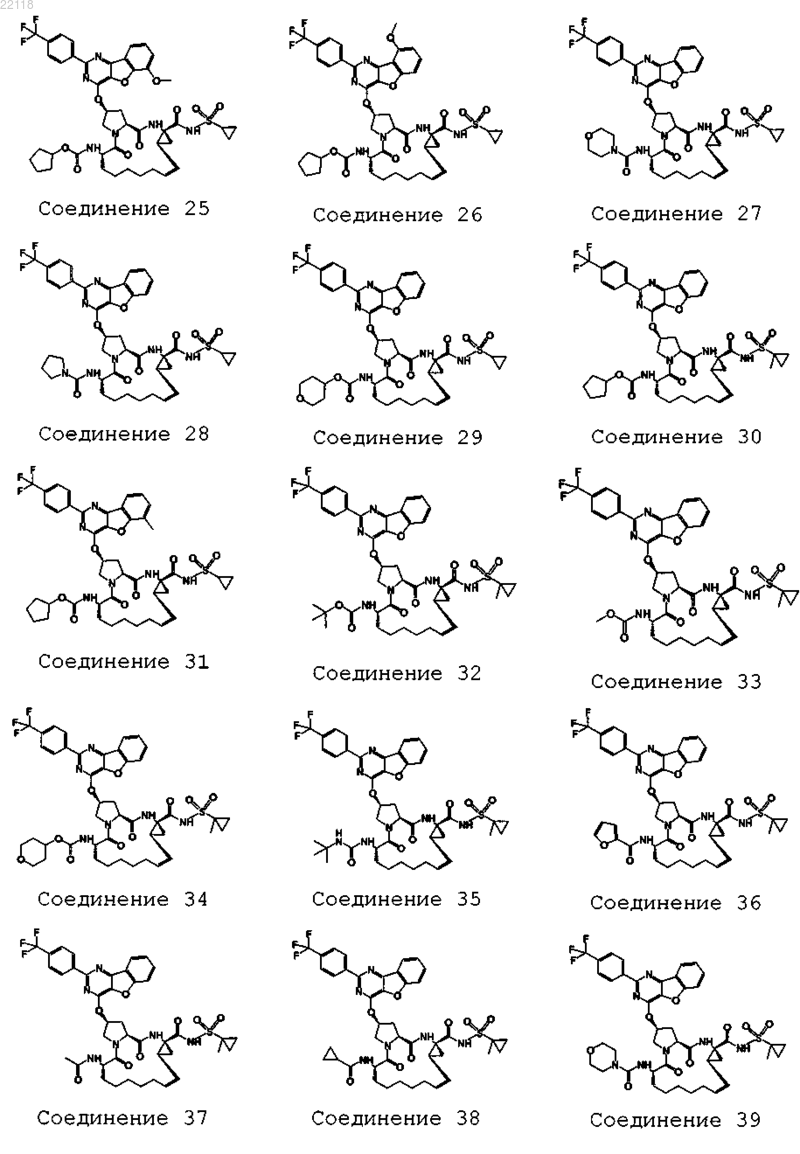
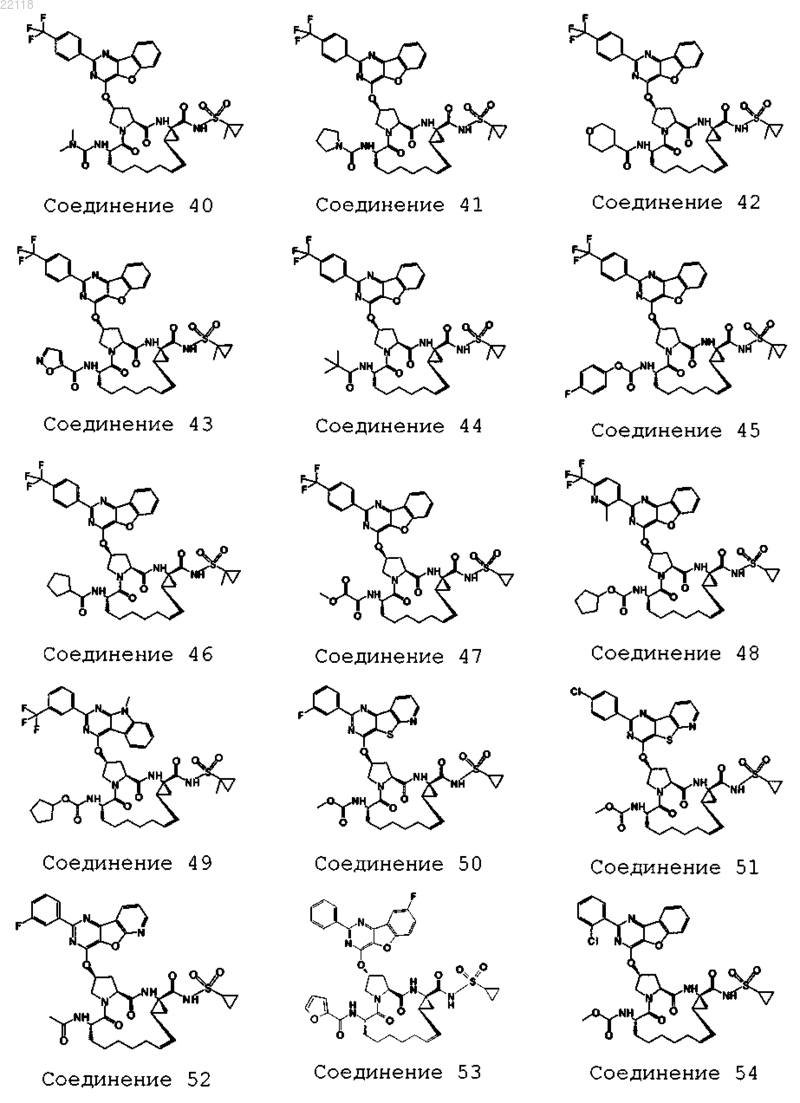
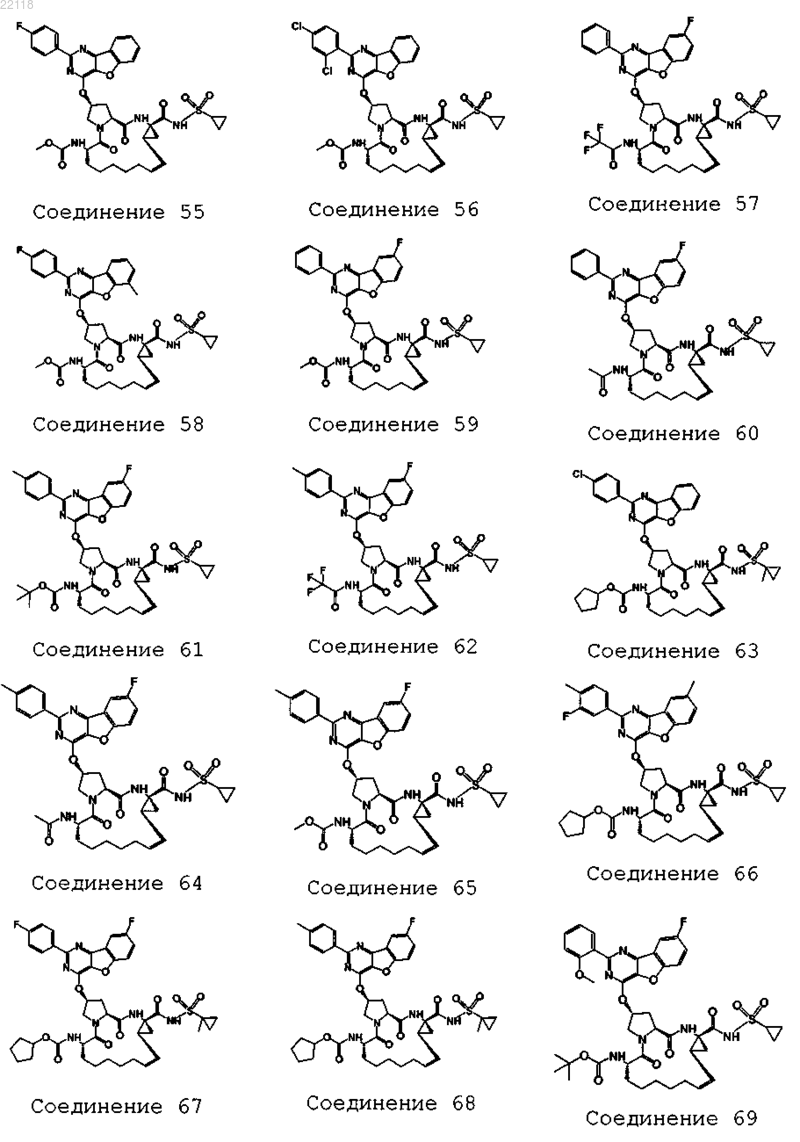


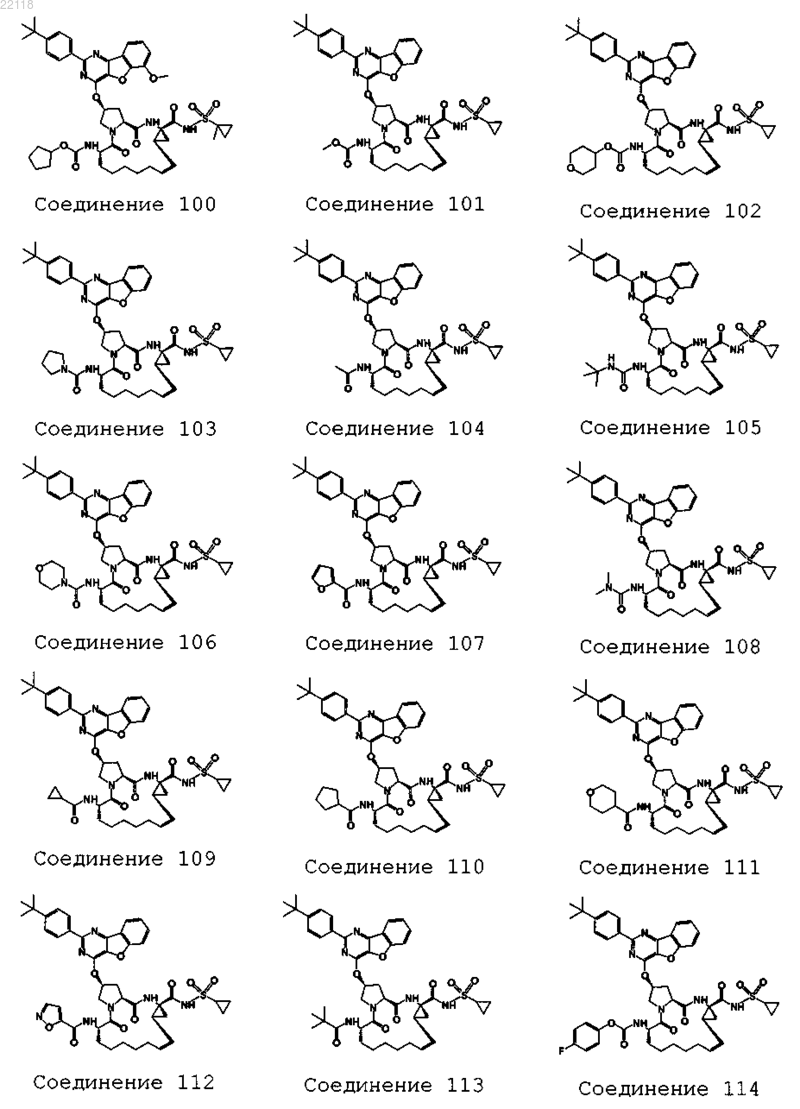
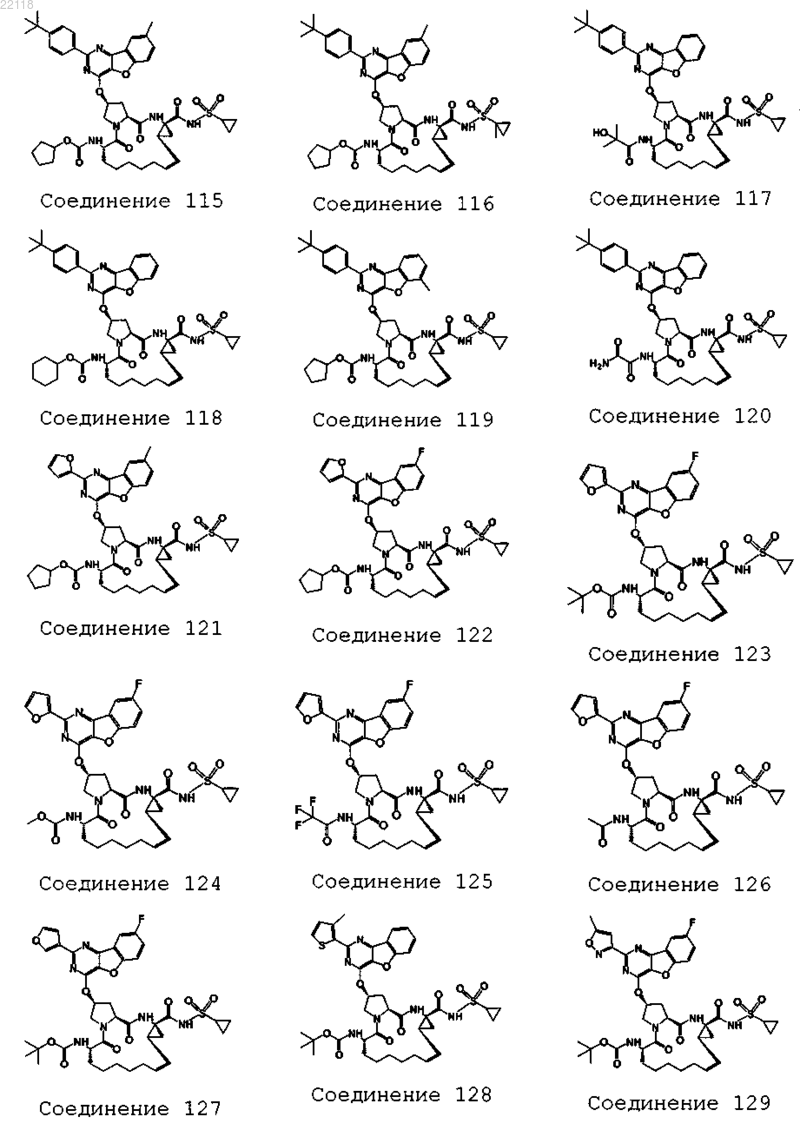
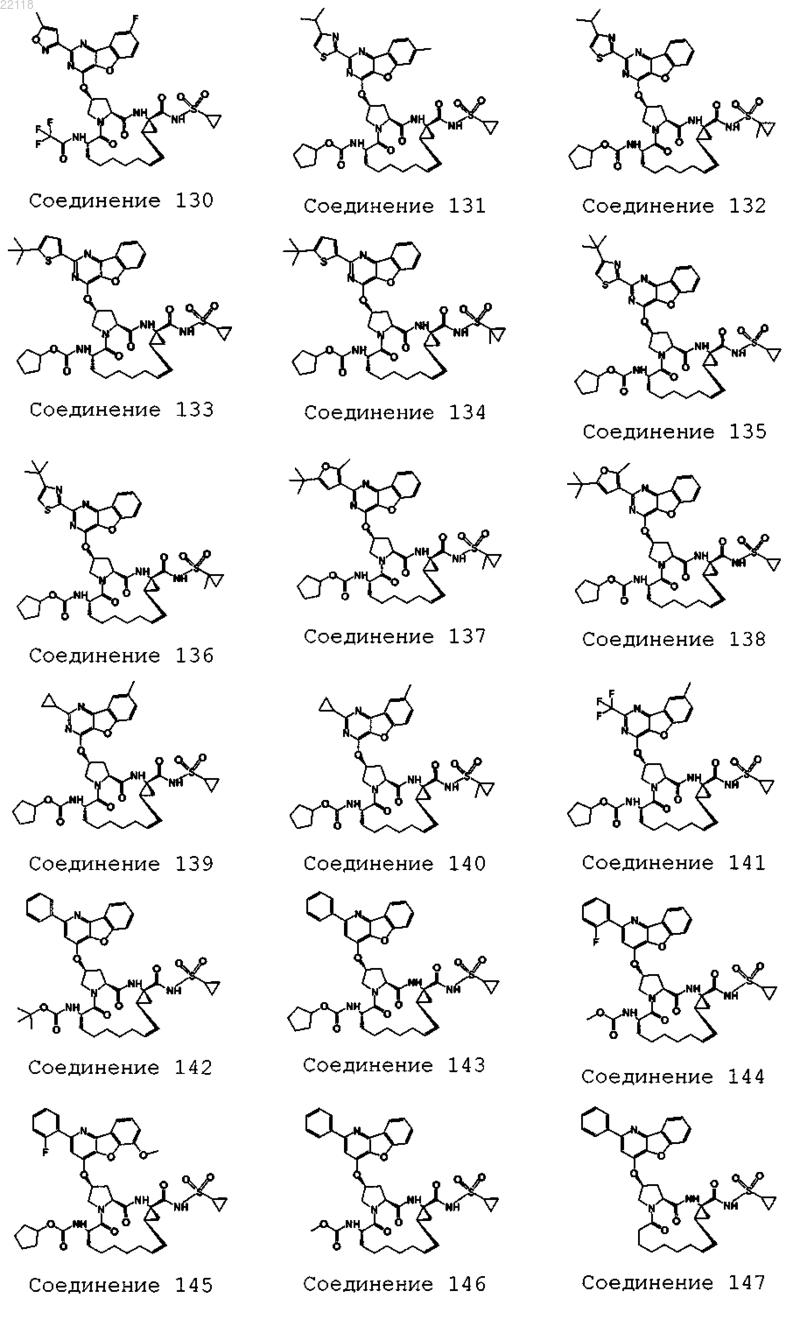
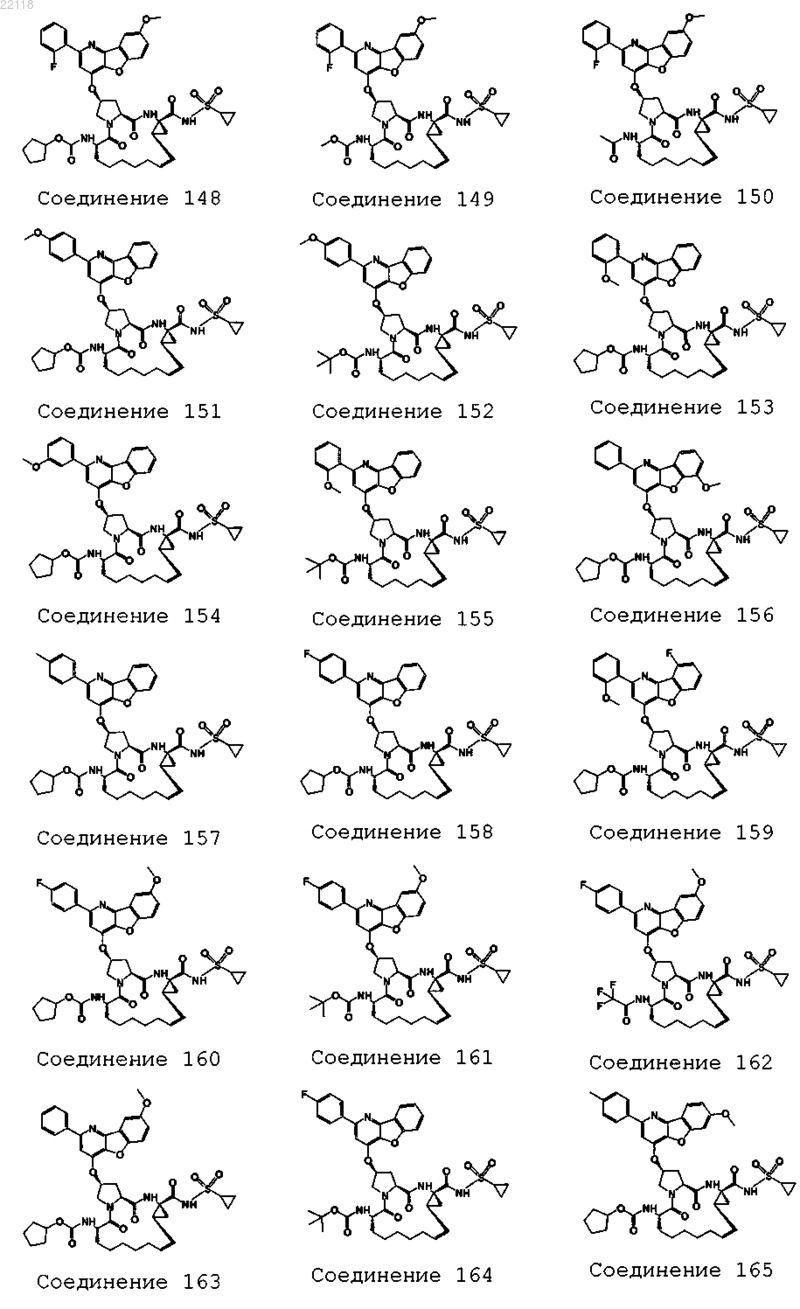
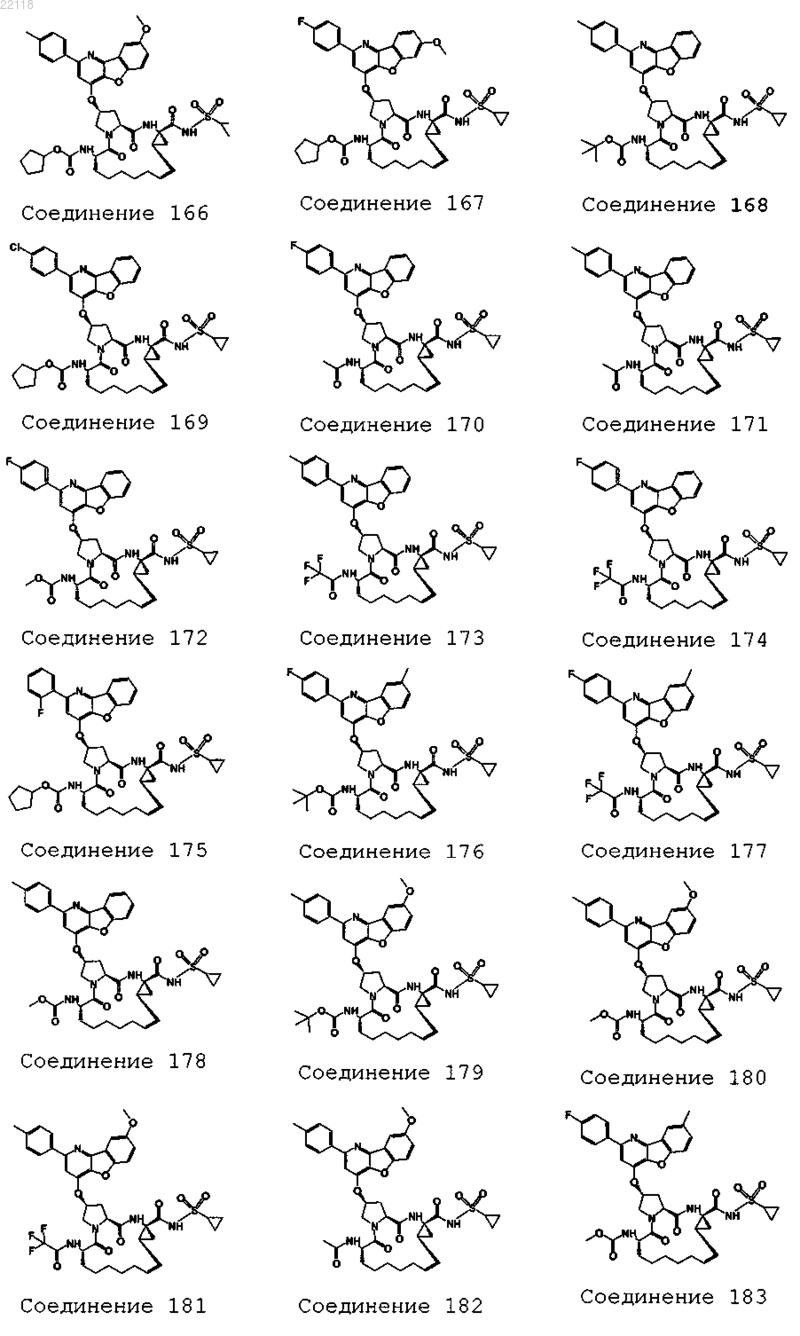
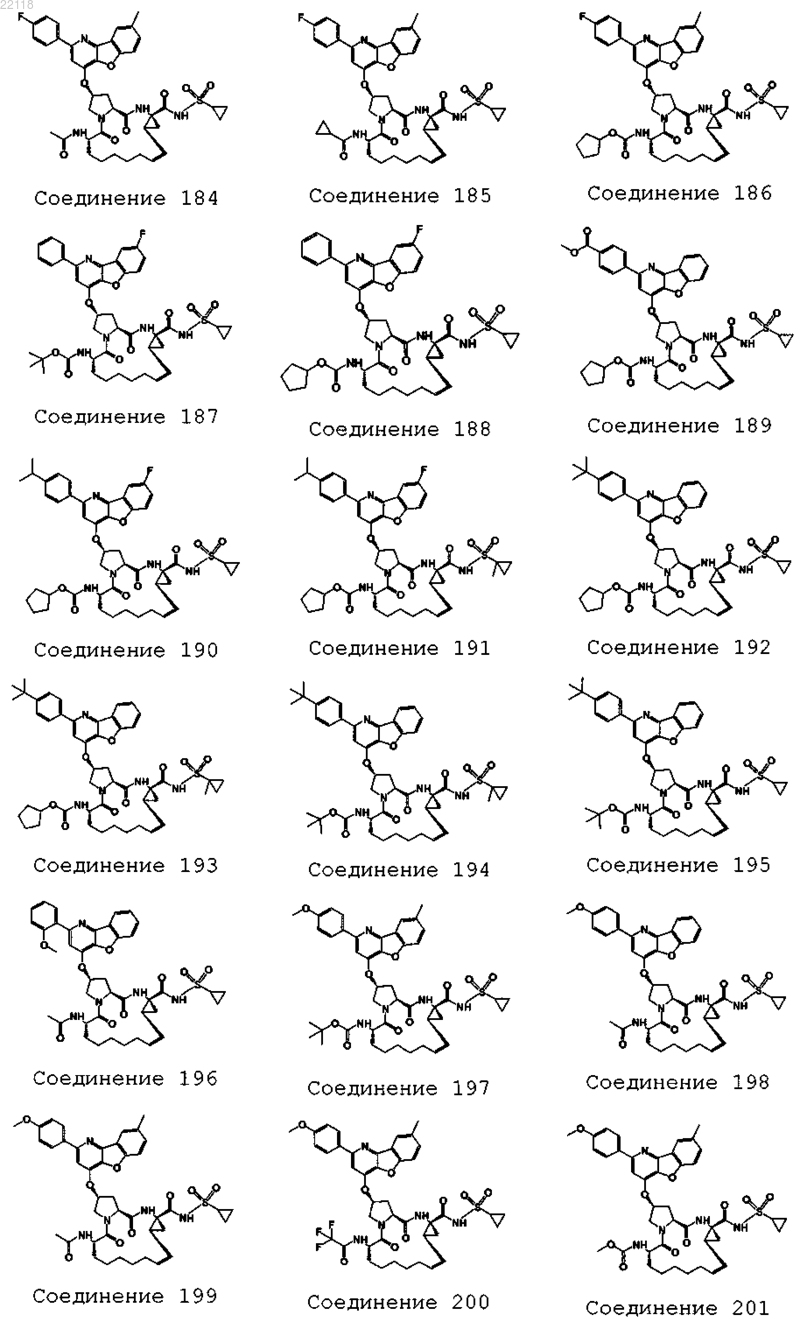
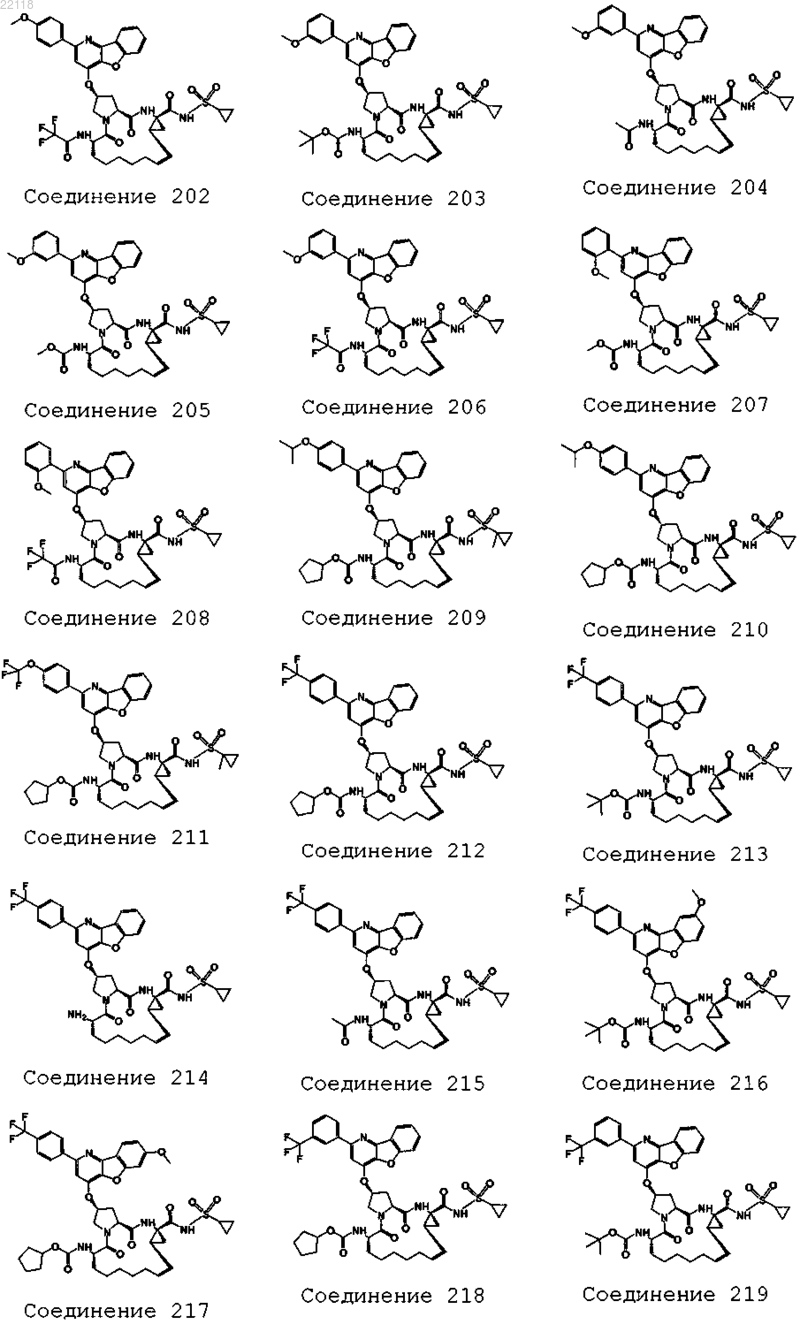
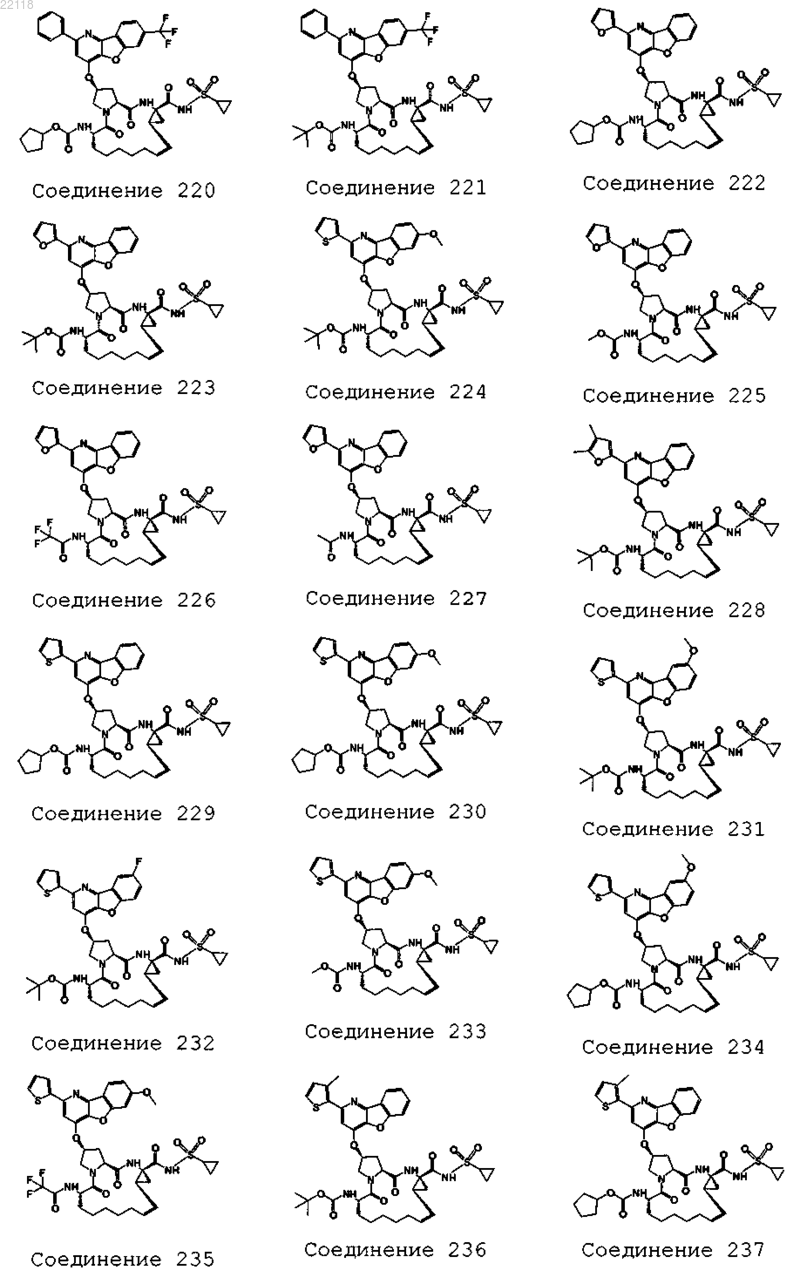
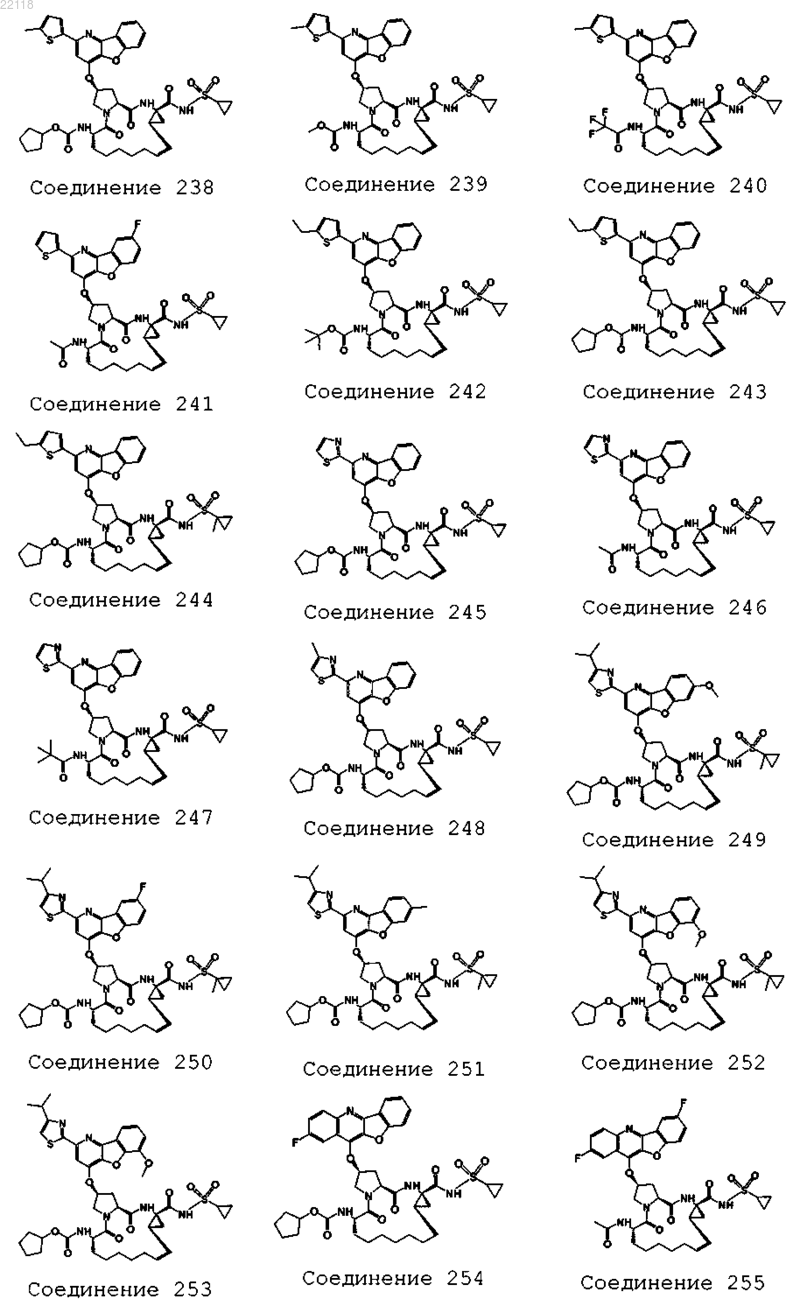
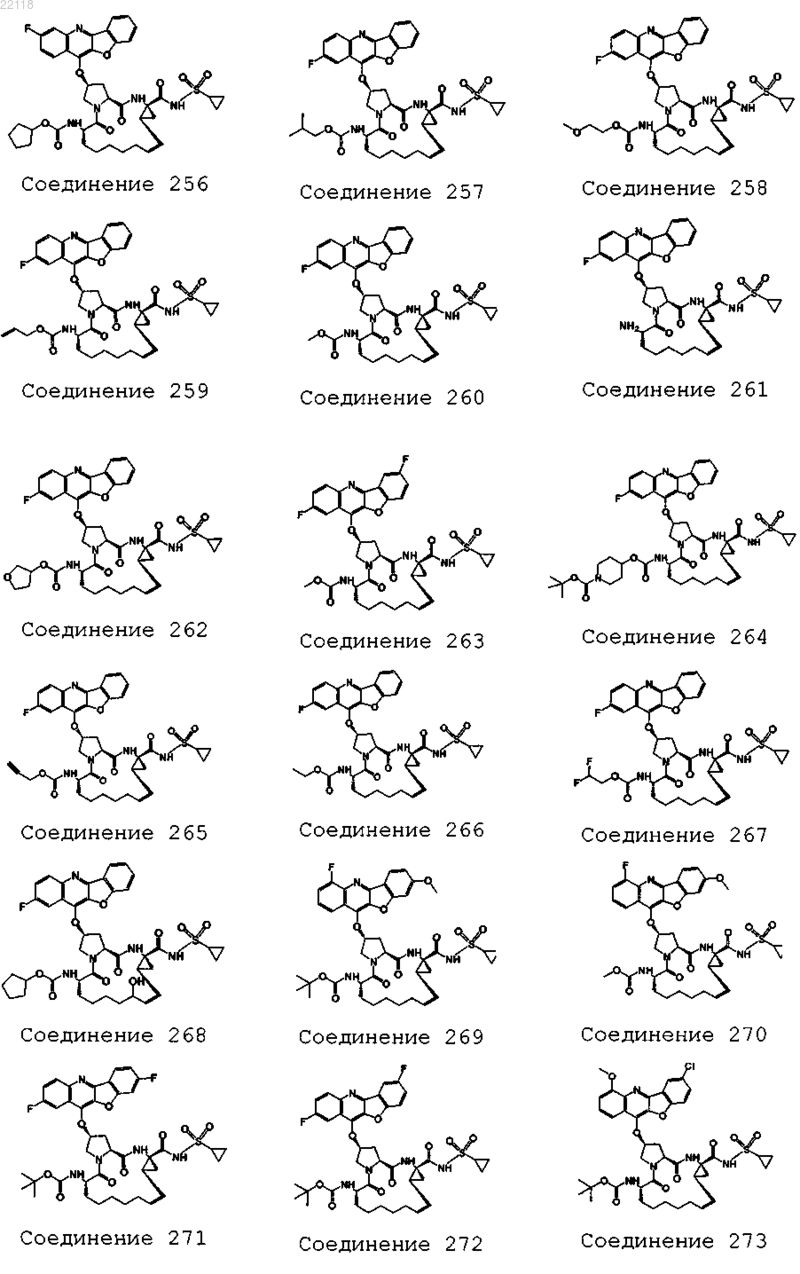

11. Соединение по п.10, выбранное из соединений 1, 16, 23, 26, 28, 30, 35, 36, 80, 81, 82, 84, 85, 86, 90, 95, 97, 100, 116 и 209.
12. Фармацевтическая композиция для применения при лечении инфекции вирусом гепатита С, содержащая соединение по любому из пп.1-11 и фармацевтически приемлемый носитель.
13. Применение соединения по любому из пп.1-11 для лечения инфекции вирусом гепатита С.
14. Применение по п.13, где соединение перорально вводят субъекту, нуждающемуся в таком лечении.
15. Применение по любому из пп.13 или 14, где соединение вводят один раз в сутки.
16. Применение соединения по любому из пп.1-11 для производства лекарственного средства для лечения инфекции вирусом гепатита С.
Текст
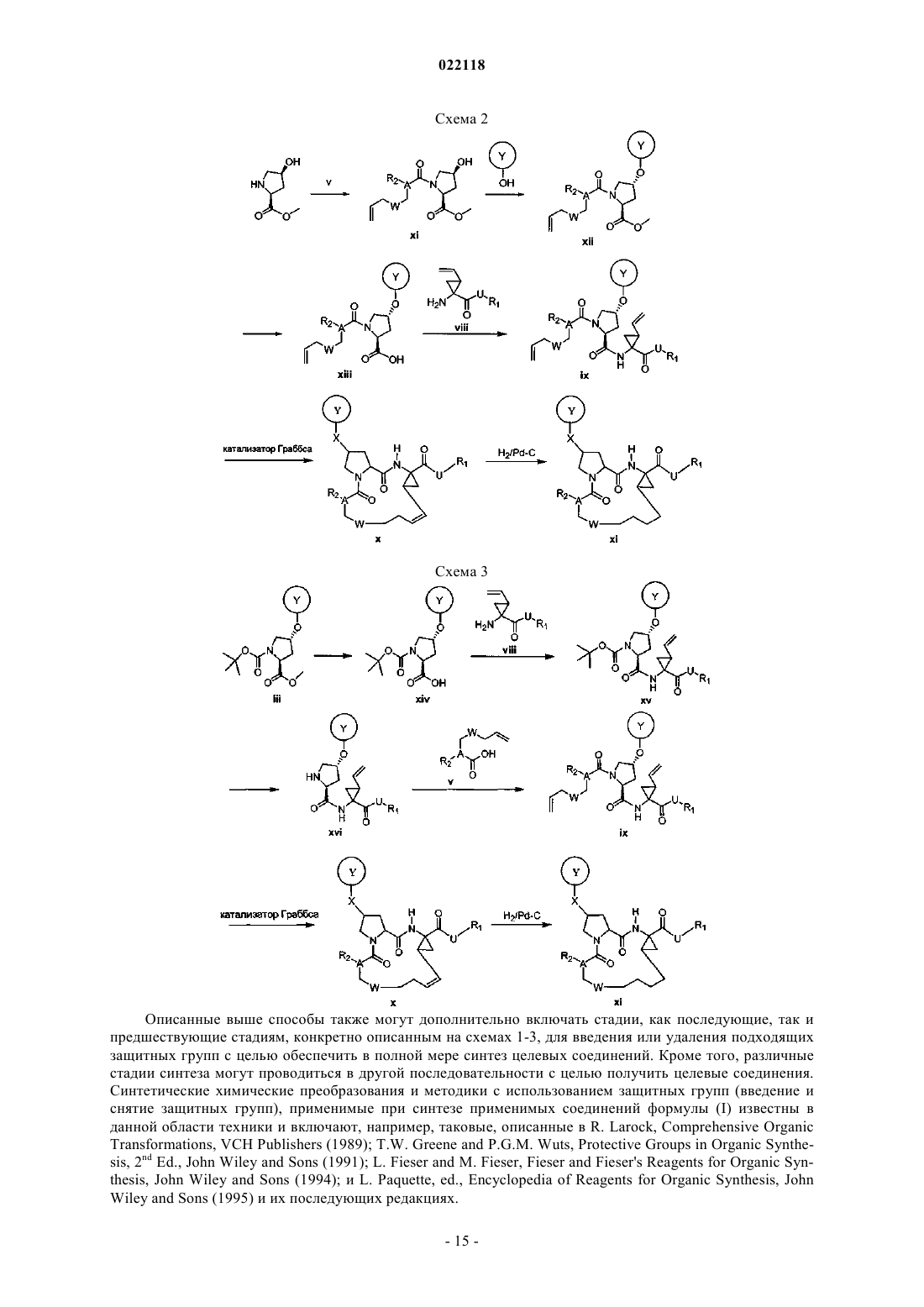
Настоящее изобретение относится к макроциклическим соединениям, представленным в описании. Указанные соединения могут быть использованы для лечения инфекции вирусом гепатита С. Предпосылки создания изобретения Вирус гепатита С (HCV), содержащий (+)-смысловую однонитевую РНК, представляет собой основной этиологический фактор для большинства случаев не-А, не-В гепатита. HCV-инфекция представляет собой очевидную проблему здоровья людей (см., например, WO 05/007681; WO 89/04669; ЕР 381216; Alberti et al., J. Hepatology, 31 (Suppl. 1), 17-24 (1999); Alter, J. Hepatology, 31 (Suppl. 1), 88-91(1999) и Lavanchy, J. Viral Hepatitis, 6, 35-47 (1999. Гепатит, вызванный HCV-инфекцией, с трудом поддается лечению, поскольку вирус может легко мутировать и избегать врожденного иммунного ответа. Немногими существующими на данный момент видами терапии HCV являются интерферон-, сочетание интерферон-/рибавирин и пегилированный интерферон-. Однако было обнаружено, что уровень устойчивого ответа для интерферона- или сочетания интерферон-/рибавирин составляет 50%, и пациенты существенно страдают от побочных эффектов указанных терапевтических средств (см., например, Walker, DDT, 4, 518-529 (1999); Weiland,FEMS Microbial. Rev., 14, 279-288 (1994) и WO 02/18369). Таким образом, остается потребность в разработке более эффективных и лучше переносимых терапевтических лекарств. Протеаза HCV, необходимая для репликации вируса, содержит приблизительно 3000 аминокислот. Она включает белок нуклеокапсида (С), белки оболочки (Е 1 и Е 2) и несколько неструктурных белков(NS2, NS3, NS4a, NS5a и NS5b). Белок NS3 обладает активностью сериновой протеазы и считается необходимым для репликации и инфективности вируса. Необходимость NS3 протеазы логически вытекает из того факта, что мутацииNS3 протеазы вируса желтой лихорадки снижали инфективность вируса (см., например, Chamber et al.,Proc. Natl. Acad. Sci. USA 87, 8898-8902 (1990). Также было показано, что мутации в активном центреNS3 протеазы HCV полностью ингибировали HCV-инфекцию в модели на шимпанзе (см., например,Rice et al., J. Virol. 74 (4) 2046-51 (2000. Кроме того, было обнаружено, что NS3 протеаза HCV способствует протеолизу на сочленениях NS3/NS4a, NS4a/NS4b, NS4b/NS5a, NS5a/NS5b, а потому отвечает за образование четырех вирусных белков в процессе репликации вируса (см., например, US 2003/0207861). Следовательно, NS3 протеаза HCV представляет собой важную цель при лечении HCV-инфекции. Потенциальные ингибиторы NS3 протеазы HCV могут быть обнаружены в WO 02/18369, WO 00/09558, WO 00/09543, WO 99/64442, WO 99/07733, WO 99/07734, WO 99/50230, WO 98/46630, WO 98/17679, WO 97/43310, US 5990276, Dunsdon et al., Biorg. Med. Chem. Lett. 10, 1571-1579 (2000); Llinas-Brunet et al.,Biorg. Med. Chem. Lett. 10, 2267-2270 (2000) и S. LaPlante et al., Biorg. Med. Chem. Lett. 10, 2271-2274(2000). Краткое описание сущности изобретения Настоящее изобретение основано на неожиданных открытиях, что конкретные макроциклические соединения блокируют активность NS3-4A протеаз, снижают содержание РНК HCV, ингибируют мутантные HCV протеазы, устойчивые к другим ингибиторам, и демонстрируют пролонгированный период полувыведения из кровеносной системы. В одном аспекте настоящее изобретение относится к соединениям формулы (I) в которой R1 представляет собой -Н, -ОН, C1-6 алкил, C1-6 алкоксил, С 3-10 циклоалкил, C1-10 гетероциклоалкил, арил, гетероарил, -Z-R или -NH-Z-R; где R представляет собой Н или представляет собой фрагмент, выбранный из C1-6 алкила, С 3-10 циклоалкила, С 1-10 гетероциклоалкила, арила и гетероарила, каждый из которых необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, С 2-6 алкенилом, С 2-6 алкинилом, арилом или гетероарилом; и Z представляет собой-С(O)-, -С(O)O-, -С(О)С(О)О-, -C(O)C(O)NH-, -C(O)NR'-, -OC(S)-, -C(S)NR'- или -C(NH)O-, причем R' представляет собой Н, C1-6 алкил, С 3-10 циклоалкил, C1-10 гетероциклоалкил, арил или гетероарил; R2 представляет собой Н или представляет собой фрагмент, выбранный из C1-6 алкила, С 3-10 циклоалкила, С 1-10 гетероциклоалкила, арила и гетероарила, каждый из которых необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, С 2-6 алкинилом, арилом или гетероарилом; А представляет собой N или СН; U представляет собой -O-, -NH-, -NH(CO)-, -NHS(O)- или где каждый из V и Т независимо представляет собой -СН- или -N-; каждый из A1 и А 2 независимо представляет собой фрагмент, выбранный из С 4-10 циклоалкила, C1-10 гетероциклоалкила, арила и гетероарила,каждый из которых необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, С 2-6 алкинилом, арилом или гетероарилом или необязательно конденсирован с С 3-10 циклоалкилом, C1-10 гетероциклоалкилом, арилом или гетероарилом; и Ri представляет собой Н, галоген, нитро, циано или амино или представляет собой фрагмент, выбранный из C1-6 алкила,C1-6 алкоксила, C2-6 алкенила, С 2-6 алкинила, С 3-10 циклоалкила, C1-10 гетероциклоалкила, арила или гетероарила,причем каждый из C1-6 алкила, C1-6 алкоксила, C2-6 алкенила и С 2-6 алкинила необязательно моно-, диили тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, C2-6 алкинилом, С 3-10 циклоалкилом, C1-10 гетероциклоалкилом, арилом или гетероарилом, причем каждый из С 3-10 циклоалкила, C1-10 гетероциклоалкила, арила и гетероарила необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, C2-6 алкинилом, С 3-10 циклоалкилом, C1-10 гетероциклоалкилом, арилом или гетероарилом или необязательно конденсирован с С 3-10 циклоалкилом, C1-10 гетероциклоалкилом, арилом или гетероарилом; и представляет собой одинарную связь или двойную связь. Группы, обозначенные переменными U, W, X и Z, являются двухвалентными. Каждая из групп представлена выше в той же ориентации, как и те, в которых переменная представлена в формуле. Возьмем, например, группу -NHSO-, обозначенную переменной U, которая, как показано в формуле, располагается между С=O и R2. Атом азота в указанной -NHS(O)-группе связан с С=O, и атом серы связан с R2. В качестве другого примера группа -С(O)O-, обозначенная переменной Z, располагается между NH и R (то есть -NH-Z-R). Атом углерода в -С(O)O- связан с NH, и атом кислорода связан с R. В отношении формулы (I) подгруппа соединений отличается тем, что R1 представляет собой -NH-ZR, в которой Z представляет собой -С(O)-, -С(O)O-, -С(О)С(О)О- или -С(О)С(O)NH-; R2 представляет собой-SOCH2-; U представляет собой -NHSO2-; представляет собой двойную связь; или Y представляет собой в которой Т представляет собой СН или N; Ri представляет собой фенил или тиазолил, необязательно замещенный галогеном, амино, C1-6 алкилом или C1-6 алкоксилом; и каждый из Rii, Riii, Riv и Rv независимо представляет собой Н, галоген, нитро, циано, амино, C1-6 алкил, C1-6 алкоксил, C2-6 алкенил или C2-6 алкинил или представляет собой фрагмент, выбранный из С 3-10 циклоалкила, C1-10 гетероциклоалкила, арила и гетероарила, каждый из которых необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, C2-6 алкинилом, арилом или гетероарилом или необязательно конденсирован с С 3-10 циклоалкилом, C1-10 гетероциклоалкилом, арилом или гетероарилом. Примеры R1 представляют собой -NH-C(О)O-t-Bu, -NH-C(O)O-циклопентил и -NH-C(О)-фурил. Другая подгруппа соединений отличается тем, что Y представляет собой в которых каждый Ri, Rii, Riii, Riv, Rv и Rvi независимо представляет собой Н, галоген, нитро, циано, амино, C1-6 алкил, C1-6 алкоксил, C2-6 алкенил или C2-6 алкинил, С 3-10 циклоалкил, C1-10 гетероциклоалкил, арил или гетероарил, причем каждый из циклоалкила, гетероциклоалкила, арила или гетероарила необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, С 2-6 алкинилом, арилом или гетероарилом и необязательно конденсирован с С 3-10 циклоалкилом,C1-10 гетероциклоалкилом, арилом или гетероарилом. В указанных выше соединениях Ri может представлять собой, например, где n равно 1 или 2. В одном варианте осуществления соединения по настоящему изобретению имеют следующую формулу: в которой значения R1, R2, A, U, W, X и Y определены выше. В другом варианте осуществления соединения по настоящему изобретению имеют следующую формулу: в которой значения R1, A, U, W, X и Y определены выше. В еще одном варианте осуществления соединения по настоящему изобретению имеют следующую формулу: в которой R1 представляет собой -Н, -ОН, C1-6 алкил, C1-6 алкоксил, С 3-10 циклоалкил, C1-10 гетероциклоалкил, арил, гетероарил или -Z-R; где R представляет собой Н или представляет собой фрагмент,выбранный из C1-6 алкила, С 3-10 циклоалкила, C1-10 гетероциклоалкила, арила и гетероарила, каждый из которых необязательно моно-, ди- или тризамещен галогеном, нитро, циано, амино, C1-6 алкилом, C1-6 алкоксилом, C2-6 алкенилом, C2-6 алкинилом, арилом или гетероарилом; и Z представляет собой -С(О)-,-С(O)O-, -С(О)С(О)О-, -C(O)C(O)NH-, -C(O)NR'-, -OC(S)-, - C(S)NR'- или -C(NH)O-, причем R' представляет собой Н, C1-6 алкил, С 3-10 циклоалкил, C1-10 гетероциклоалкил, арил или гетероарил; и значения R2, A,U, W, X и Y определены выше. Термин "алкил" относится к насыщенному неразветвленному или разветвленному углеводородному фрагменту, такому как СН 3 или -СН(СН 3)2. Термин "алкокси" относится к радикалу -О-(C1-6 алкил). Термин "алкенил" относится к неразветвленному или разветвленному углеводородному фрагменту, который содержит по меньшей мере одну двойную связь, такому как -СН=СН-СН 3. Термин "алкинил" относится к неразветвленному или разветвленному углеводородному фрагменту, который содержит по меньшей мере одну тройную связь, такому как -СС-СН 3. Термин "циклоалкил" относится к насыщенному циклическому углеводородному фрагменту, такому как циклогексил. Термин "циклоалкенил" относится к неароматическому циклическому углеводородному фрагменту, который содержит по меньшей мере одну двойную связь, такому как циклогексенил. Термин "гетероциклоалкил" относится к насыщенному циклическому фрагменту, содержащему в кольце по меньшей мере один гетероатом (например, N, О или S),такому как 4-тетрагидропиранил. Термин "гетероциклоалкенил" относится к неароматическому циклическому фрагменту, содержащему в кольце по меньшей мере один гетероатом (например, N, О или S) и по меньшей мере одну двойную связь, такому как пиранил. Термин "арил" относится к углеводородному фрагменту, содержащему одно или несколько ароматических колец. Примеры арильных фрагментов включают фенил (Ph), фенилен, нафтил, нафтилен, пиренил, антрил и фенантрил. Термин "гетероарил" относится к фрагменту, содержащему одно или несколько ароматических колец, которые содержат по меньшей мере один гетероатом (например, N, О или S). Примеры гетероарильных фрагментов включают фурил, фурилен, флуоренил, пирролил, тиенил, оксазолил, имидазолил, тиазолил, пиридил, пиримидинил, хиназолинил, хинолил, изохинолил и индолил. Термин "амино" относится к радикалу -NH2, -NH-(C1-6 алкил) или -N(C1-6 алкил)2. Если иное не указано особо, то упомянутые в этом документе алкил, алкенил, алкинил, циклоалкил,циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил и гетероарил включают как замещенные,так и незамещенные фрагменты. Возможные заместители для циклоалкила, циклоалкенила, гетероциклоалкила, гетероциклоалкенила, арила и гетероарила включают без ограничения C1-С 10 алкил, C2 С 10 алкенил, С 2-С 10 алкинил, С 3-С 20 циклоалкил, С 3-С 20 циклоалкенил, C1-С 20 гетероциклоалкил, С 1 С 20 гетероциклоалкенил, C1-С 10 алкокси, арил, арилокси, гетероарил, гетероарилокси, амино, C1 С 10 алкиламино, C1-С 20 диалкиламино, ариламино, диариламино, C1-С 10 алкилсульфонамино, арилсульфонамино, C1-С 10 алкилимино, арилимино, C1-С 10 алкилсульфонимино, арилсульфонимино, гидроксил, галоген, тио, C1-С 10 алкилтио, арилтио, C1-С 10 алкилсульфонил, арилсульфонил, ациламино, аминоацил, аминотиоацил, амидино, гуанидин, уреидо, циано, нитро, нитрозо, азидо, ацил, тиоацил, ацилокси, карбоксил и сложный эфир карбоновой кислоты. С другой стороны, возможные заместители для алкила, алкенила или алкинила включают все вышеприведенные заместители кроме C1-С 10 алкила. Циклоалкил, циклоалкенил, гетероциклоалкил, гетероциклоалкенил, арил и гетероарил также могут быть конденсированы друг с другом. Ниже представлено 281 типичное соединение по настоящему изобретению. В другом аспекте настоящее изобретение относится к способу лечения инфекции вирусом гепатита С. Указанный способ включает введение нуждающемуся в этом субъекту эффективного количества соединения формулы (I), представленной выше. В еще одном аспекте настоящее изобретение относится к фармацевтической композиции для применения при лечении HCV-инфекции. Указанная композиция содержит эффективное количество по меньшей мере одного из соединений формулы (I) и фармацевтически приемлемый носитель. Она может включать ингибитор некоторой цели, отличной от NS3 протеазы HCV, в жизненном цикле HCV, например, NS5B полимеразы, NS5A, NS4B или р 7. Примеры таких средств включают без ограничения N-[3-(l-циклобутилметил-4-гидрокси-2-оксо 1,2-дигидрохинолин-3-ил)-1,1-диоксо-1,4-дигидро-1,6-бензо[1,2,4]тиадиазин-7-ил]метансульфонамид(WO 04041818), транс-1,2-ди-4-[(фенилацетилпирролидин-2-(S)-карбонил)амино]фенилэтилен (WO 0401413) и 1-аминоадамантан (Amentadine, Griffin, 2004, J. Gen. Virol. 85: p. 451). Фармацевтическая композиция может также содержать иммуномодулирующее средство или второе противовирусное средство. Иммуномодулирующее средство относится к активному агенту, который опосредует иммунный ответ. Примеры иммуномодулирующих средств включают без ограничения Nov-205 (Novelos Therapeu- 13022118tics Inc., WO 02076490) и IMO-2125 (Idera Pharmaceuticals Inc., WO 05001055). Противовирусное средство относится к активному агенту, который убивает вирус или подавляет его репликацию. Примеры противовирусных средств включают без ограничения рибавирин, рибамидин, интерферон-, пегилированный интерферон и ингибиторы протеазы HCV, такие как 2-(2-2-циклогексил-2-[(пиразин-2-карбонил)амино] ацетиламино-3,3-диметилбутирил)окстагидроциклопента[с]пиррол-1-карбоновой кислоты (1-циклопропиламинооксалилбутил)амид (Телапревир, Vertex Pharmaceuticals Inc., WO 02018369), 3-[2-(3-третбутилуреидо)-3,3-диметилбутирил]-6,6-диметил-3-азабицикло[3.1.0]гексан-2-карбоновой кислоты (2 карбамоил-1-циклобутилметил-2-оксоэтил)амид (Боцепревир, Schering-Plough Research Institute, WO 03062265) и сложный 14-трет-бутоксикарбониламино-4-циклопропансульфониламинокарбонил-2,15 диоксо-3,16-диазатрицикло[14.3.0.04,6]нонадек-7-ен-18-иловый эфир 4-фтор-1,3-дигидроизоиндол-2 карбоновой кислоты (ITMN-191, InterMune Inc., US 2005/0267018). Под объем настоящего изобретения также подпадают использование такой композиции для леченияHCV-инфекции или для производства лекарственного средства для лечения. Детали одного или нескольких вариантов осуществления настоящего изобретения представлены в приведенном ниже описании. Другие характерные черты, цели и преимущества настоящего изобретения станут очевидны из описания и формулы изобретения. Подробное описание изобретения Соединения по настоящему изобретению могут быть синтезированы из коммерчески доступных исходных веществ способами, хорошо известными в данной области техники. Например, кто-либо может получить соединения по настоящему изобретению путем синтеза, представленным ниже в схеме 1. Схема 1 Как представлено в схеме 1, сначала проводят сочетание полициклического соединения (i) с N(трет-бутоксикарбонил)-L-пролином (ii) с последующим метилированием с получением промежуточного продукта (iii). С промежуточного продукта (iii) снимают защиту для удаления N-бутоксикарбонильной группы с получением соединения, не замещенного по N (iv), и проводят его сочетание с карбоновой кислотой (v) с получением промежуточного продукта (vi). Промежуточный продукт (vi) подвергают гидролизу с получением кислоты (vii) и проводят ее сочетание с амином (viii) с получением пирролидинового соединения (ix), содержащего две концевые алкенильные группы. Промежуточный продукт (ix) претерпевает реакцию олефинового метатезиса в присутствии катализатора Граббса с получением целевого макроциклического соединения (х). Двойная связь макроциклического аналога (xi) может быть в дальнейшем гидрирована в присутствии Pd-C с получением насыщенного макроциклического соединения(xi). На схемах 2 и 3 представлены два альтернативных пути синтеза соединений по настоящему изобретению. Описанные выше способы также могут дополнительно включать стадии, как последующие, так и предшествующие стадиям, конкретно описанным на схемах 1-3, для введения или удаления подходящих защитных групп с целью обеспечить в полной мере синтез целевых соединений. Кроме того, различные стадии синтеза могут проводиться в другой последовательности с целью получить целевые соединения. Синтетические химические преобразования и методики с использованием защитных групп (введение и снятие защитных групп), применимые при синтезе применимых соединений формулы (I) известны в данной области техники и включают, например, таковые, описанные в R. Larock, Comprehensive Organic Представленные ниже примеры 1-281 обеспечивают подробное описание того, как фактически могут быть получены соединения 1-281. Соединения, упомянутые в этом документе, содержат неароматическую двойную связь и центры асимметрии. Таким образом, они могут существовать в виде рацематов и рацемических смесей, отдельных энантиомеров, отдельных диастереоизомеров, диастереоизомерных смесей, таутомеров и цис- или транс-изомерных форм. Все подобные изомерные формы рассматриваются настоящим изобретением. Например, представленные выше соединения формул (I) могут иметь следующие стереохимические конфигурации (II): Описанные выше соединения включают сами соединения, а также их соли, пролекарства и сольваты, если это относится к данному случаю. Соль, например, может быть образована анионом и положительно заряженной группой (например, аминогруппа) соединения формулы (I). Подходящие анионы включают хлорид, бромид, иодид, сульфат, нитрат, фосфат, цитрат, метансульфонат, трифторацетат, ацетат, малат, тозилат, тартрат, фумурат, глутамат, глюкуронат, лактат, глутарат и малеат. По аналогии,соль может быть также образована катионом и отрицательно заряженной группой (например, карбоксилат) соединения формулы (I). Подходящие катионы включают ион натрия, ион калия, ион магния, ион кальция и катион аммония, такой как ион тетраметиламмония. Соединения формулы (I) также включают такие соли, которые содержат атомы четвертичного азота. Примеры пролекарств включают сложные эфиры и другие фармацевтически приемлемые производные, которые после введения субъекту способны обеспечить наличие активных соединений формулы (I). Сольват относится к комплексу, образованному активным соединением формулы (I) и фармацевтически приемлемым растворителем. Примеры фармацевтически приемлемых растворителей включают воду, этанол, изопропанол, этилацетат, уксусную кислоту и этаноламин. Под объем настоящего изобретения также подпадает способ лечения HCV-инфекции путем введения пациенту эффективного количества одного или нескольких соединений формулы (I). Термин "проведение лечения" или "лечение" относится к введению соединений субъекту, у которого присутствуетHCV-инфекция, ее симптом или предрасположенность к ней, с целью обеспечить терапевтический эффект, например излечить, ослабить, преобразовать, повлиять, улучшить или предупредить HCVинфекцию, ее симптом или предрасположенность к ней. Термин "эффективное количество" относится к количеству активного соединения по настоящему изобретению, которое требуется для обеспечения терапевтического эффекта у подвергнутого лечению субъекта. Эффективные дозы будут варьировать, что очевидно специалисту в данной области техники, в зависимости от типов подвергающихся лечению заболеваний, пути введения, использования наполнителя и возможности совместного применения с другим терапевтическим лечением. Соединения по настоящему изобретению могут оставаться в кровеносной системе на эффективном уровне в течение длительного времени. Таким образом, для обеспечения терапевтического эффекта указанные соединения могут быть введены в эффективном количестве один раз в сутки. Для применения на практике способа по настоящему изобретению композиция, содержащая одно или несколько соединений по настоящему изобретению, может быть введена парентерально, перорально,назально, ректально, местно или буккально. Используемый в этом документе термин "парентерально" относится к подкожной, внутрикожной, внутривенной, внутримышечной, внутрисуставной, внутриартериальной, интрасиновиальной, интрастернальной, интратекальной, внутриочаговой или интракраниальной инъекции, а также к любой подходящей инфузионной методике. Стерильная инъекционная композиция может представлять собой раствор или суспензию в нетоксическом парентерально приемлемом разбавителе или растворителе, таком как раствор в 1,3-бутандиоле. Среди приемлемых основ и растворителей, которые могут быть использованы, присутствуют маннит,вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или среды для суспендирования традиционно применяются жирные масла (например, синтетические моно- и диглицериды). Жирная кислота, такая как олеиновая кислота и ее глицеридные производные, применимы в приготовлении инъекционных препаратов, так как они представляют собой натуральные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных вариантах. Указанные масляные растворы или суспензии также могут содержать длинноцепочечный спиртовой разбавитель или диспергирующее средство, карбоксиметилцеллюлозу или сходные диспергирующие средства. Для приготовления составов также могут быть использованы другие широко используемые поверхностно-активные вещества, такие как Tweens или Spans, или другие аналогичные эмульгаторы или усилители биодоступности, которые традиционно используются в производстве фармацевтически приемлемых твердых, жидких или других лекарственных форм. Композиция для перорального введения может находиться в любой перорально приемлемой лекарственной форме, включая капсулы, таблетки, эмульсии и водные суспензии, дисперсии и растворы. В случае таблеток традиционно применяемые носители включают лактозу и кукурузный крахмал. Также обычно добавляют смазки, такие как стеарат магния. Для перорального введения в форме капсул применимые разбавители включают лактозу и высушенный кукурузный крахмал. Если водные суспензии или эмульсии вводят перорально, то активный ингредиент может быть суспендирован или растворен в масляной фазе в сочетании с эмульгатором или средством, способствующим суспендированию. При желании могут быть добавлены определенные подсластители, вкусоароматизаторы или красители. Назальный аэрозоль или ингаляционная композиция могут быть приготовлены в соответствии с методиками, хорошо известными специалисту в области приготовления фармацевтических составов. Например, такая композиция может быть приготовлена в виде раствора в солевом растворе, с использованием бензилового спирта или других подходящих консервантов, усилителей всасывания для усиления биодоступности, фторуглеродов и/или других солюбилизаторов или способствующих диспергированию средств, известных специалисту в данной области техники. Композиция, содержащая один или несколько активных соединений по настоящему изобретению,также может быть введена в форме суппозиториев для ректального введения. Носитель в фармацевтической композиции должен быть "приемлемым" в том смысле, что он должен быть совместимым с активным ингредиентом композиции (и предпочтительно способным стабилизировать активный ингредиент) и безвредным для субъекта, подлежащего лечению. Один или несколько солюбилизаторов могут быть использованы в качестве фармацевтических наполнителей для доставки активного соединения по настоящему изобретению. Примеры других носителей включают коллоидный оксид кремния, стеарат магния, целлюлозу, лаурилсульфат натрия и DC Yellow 10. Соединение по настоящему изобретению может быть использовано для лечения HCV совместно со вторым средством против HCV, таким как ингибитор цели, отличной от NS3 протеазы HCV, в жизненном цикле HCV, иммуномодулирующее средство и другое противовирусное средство. Соединение по настоящему изобретению и второе средство против HCV могут быть введены одновременно или в разное время. Для одновременного введения они могут быть предварительно смешаны с формированием одной пилюли или приготовлены в виде отдельных пилюль. Каждое из указанных двух средств может быть использовано в таком количестве, что их общее количество определяется специалистом в данной области техники как эффективное для проведения лечения HCV. Соединения по настоящему изобретению, описанные выше, могут быть предварительно отобраны по их эффективности в лечении HCV-инфекции путем проведения анализа in vitro (см. примеры 282 и 283), а затем подтверждены посредством экспериментов на животных и клинических исследований. Другие способы также будут очевидны для специалиста в данной области техники. Представленные ниже конкретные примеры должны истолковываться лишь как иллюстративные, а не ограничивающие оставшуюся часть описания каким бы то ни было образом. Без дополнительного уточнения полагается, что специалист в данной области техники может использовать настоящее изобретение в его максимальной полноте, основываясь на представленном в этом документе описании. Все публикации, процитированные в этом документе, включены во всей своей полноте в этот документ посредством ссылки. Пример 1. Синтез сложного циклопентилового эфира 4-циклопропансульфониламинокарбонил 2,15-диоксо-18-[2-(4-трифторметилфенил)бензо[4,5]фуро[3,2-d]пиримидин-4-илокси]-3,16-диазатрицикло[14.3.0.04,6]нонадец-14-илкарбаминовой кислоты (соединение 1). Сначала получали соединение I-3 из коммерчески доступного сложного этилового эфира 1-третбутоксикарбониламино-2-винилциклопропанкарбоновой кислоты путем синтеза, представленным ниже. К раствору сложного этилового эфира 1-трет-бутоксикарбониламино-2-винилциклопропанкарбоновой кислоты (0,34 г, 1,3 ммоль) в THF (5 мл) и метаноле (5 мл) добавляли суспензию LiOH (0,13 г, 5,3 ммоль) в воде (1,4 мл). После перемешивания в течение ночи при комнатной температуре реакционную смесь гасили добавлением 10% HCl (2 мл) и удаляли растворитель в условиях вакуума. Получен- 17022118 ный твердый порошок промывали водой (10 мл) с получением соединения I-1 (0,27 г, 90%). МС m/z 249,9 (М 23); 1H ЯМР (CDCl3)10,35 (ушир.с, 1 Н), 5,84-5,71 (м, 1 Н), 5,29 (д, J=17,4 Гц, 1 Н), 5,12 (д, J=10,2 Гц,1 Н), 2,23-2,14 (м, 1 Н), 1,87-1,65 (м, 1 Н), 1,58-1,41 (м, 1 Н), 1,43 (с, 9 Н). Раствор соединения I-1 (0,52 г, 2,3 ммоль), 2-(1 Н-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфата метанаминия (HATU, 1,74 г, 4,6 ммоль) и 4-диметиламинопиридина (1,39 г, 11,6 ммоль) в CH2Cl2 (40 мл) перемешивали при комнатной температуре в течение 1 ч, а затем медленно в течение 15 мин добавляли циклопропансульфонамид (0,57 г, 4,7 ммоль), диизопропилэтиламин (1,81 мл,14,0 ммоль) и 1,8-диазабицикло[5,4,0]ундец-7-ен (1,80 г, 11,7 ммоль). После перемешивания реакционной смеси при комнатной температуре в течение ночи растворитель удаляли в условиях вакуума. Остаток очищали по методу колоночной хроматографии на силикагеле с получением соединения I-2 (0,51 г,66%). МС m/z 353,1 (М 23); 1H ЯМР (CDCl3)9,75 (ушир.с, 1 Н), 5,64-5,51 (м, 1 Н), 5,30 (д, J=17,4 Н), 5,16 (д, J=10,2 Гц, 1 Н),2,95-2,89 (м, 1 Н), 2,19-2,10 (м, 1 Н), 1,93-1,88 (м, 1 Н), 1,47 (с, 9 Н), 1,46-1,38 (м, 1 Н), 1,32-1,23 (м, 2 Н),1,15-1,00 (м, 2 Н). К раствору соединения I-2 (0,50 г, 1,5 ммоль) в МеОН (8 мл) при комнатной температуре добавлялиSOCl2 (0,26 г, 2,2 ммоль). После кипячения реакционной смеси с обратным холодильником в течение 1 ч МеОН и SOCl2 удаляли в условиях вакуума. Остаток растирали с пентаном и фильтровали с получением промежуточного продукта I-3 в виде не совсем белого твердого вещества (0,32 г, 91%). МС m/z (M1); 1 добавляли 4-трифторметилбензоилхлорид (1,48 г, 7,1 ммоль). Затем температуру повышали до комнатной температуры и перемешивали смесь в течение 12 ч. После удаления растворителя в условиях пониженного давления полученное твердое вещество собирали, промывали водой и сушили на воздухе с получением I-4 (1,92 г, 96,0%). МС m/z 349,0 (М 1). Суспензию I-4 (1,92 г, 5,5 ммоль) и 2 н. NaOH (13 мл) в EtOH (25 мл) нагревали при 85 С в течение 12 ч. После охлаждения смесь подкисляли, а затем удаляли EtOH. Полученное твердое вещество собирали, фильтровали, промывали водой и сушили с получением I-5 (1,71 г, 95,0%). МС m/z 331 (М 1). Раствор I-5 (1,71 г, 5,2 ммоль) и избыток оксихлорида фосфора (POCl3) кипятили с обратным холодильником в течение 2 ч. После охлаждения и тщательного выпаривания смесь экстрагировали хлористым метиленом и 10% гидроксидом натрия. Органический слой сушили над MgSO4, концентрировали и выкристаллизовывали из CH2Cl2 и н-гексана с получением соединения I-6 (1,49 г, 82%). МС m/z 348,8, 350,9 (М 1); 1H ЯМР (CDCl3)8,70 (д, 2 Н), 8,34 (д, 1 Н), 7,82-7,75 (м, 4 Н), 7,57 (ддд, 1 Н). К суспензии boc-транс-4-гидрокси-L-пролина (0,53 г, 2,3 ммоль) в DMSO (25 мл) при 0 С добавляли t-BuOK (0,82 г, 5,1 ммоль). После того как смесь оставляли нагреваться до комнатной температуры и перемешиваться в течение 1 ч при 10 С медленно добавляли соединение I-6 (0,81 г, 2,3 ммоль). Перемешивание продолжали в течение ночи. Добавляли иодметан (1,02 г, 6,9 ммоль) и перемешивали реакционную смесь при комнатной температуре еще в течение 30 мин. Реакционную смесь нейтрализовали до рН 6-7 добавлением 10% водного раствора HCl и экстрагировали хлористым метиленом. Органический слой сушили над MgSO4, упаривали в условиях вакуума и очищали по методу колоночной хроматографии на силикагеле с получением соединения I-7 (1,12 г, 86%). МС m/z 557,8 (М 1); 1H ЯМР (CDCl3)8,63 (д, 2 Н), 8,28 (д, 1 Н), 7,80-7,74 (м, 2 Н), 7,70 (д, 2 Н), 7,51 (ддд, 1 Н). К раствору соединения I-7 (1,13 г, 2,0 ммоль) в МеОН (20 мл) при комнатной температуре добавляли SOCl2 (1,21 г, 9,8 ммоль). Реакционную смесь кипятили с обратным холодильником в течение 1 ч и удаляли МеОН и SOCl2. Остаток растирали в пентане. Суспензию фильтровали с получением соединенияI-8 в виде не совсем белого твердого вещества (0,87 г, 95%). МС m/z 458,1 (М 1). К раствору HATU (1,12 г, 3,0 ммоль), 1-гидроксибензотриазола (НОВТ, 0,41 г, 3,0 ммоль), I-8 (0,86 г, 1,9 ммоль) и 2-трет-бутоксикарбониламинонон-8-еновой кислоты (1,21 г, 1,9 ммоль) в CH2Cl2 (40 мл) при комнатной температуре добавляли N-метилморфолин (NMM, 1,02 г, 9,9 ммоль). После перемешивания в течение ночи смесь концентрировали в условиях вакуума. Остаток очищали по методу колоночной хроматографии на силикагеле с получением соединения I-9 (1,03 г, 73%). МС m/z 711,3 (М 1). К раствору соединения I-9 (1,01 г, 1,4 ммоль) в THF (20 мл) при комнатной температуре добавляли 0,5 М LiOH (5,7 мл, 2,9 ммоль). После перемешивания в течение ночи реакционную смесь нейтрализовали до рН 7 добавлением 10% HCl и концентрировали в условиях вакуума. Полученный остаток фильтровали и промывали водой с получением соединения I-10 (0,91 г, 92%). МС m/z 697,3 (М 1). К раствору соединения I-3 (0,28 г, 0,4 ммоль), HATU (0,31 г, 0,8 ммоль), НОВТ (0,08 г, 0,6 ммоль) и соединения I-10 (0,09 г, 0,4 ммоль) в CH2Cl2 (10 мл) при комнатной температуре добавляли NMM (0,12 г,1,2 ммоль). После перемешивания в течение ночи реакционную смесь концентрировали в условиях вакуума. Остаток очищали по методу колоночной хроматографии на силикагеле с получением соединенияH ЯМР (CDCl3)10,24 (с, 1 Н), 8,61 (д, 2 Н), 8,26 (д, 1 Н), 7,77 (д, 2 Н), 7,73-7,64 (м, 2 Н), 7,54-7,47 (м,1 Н), 7,11 (с, 1 Н), 6,19 (д, 1 Н), 5,88-5,70 (м, 2 Н), 5,38-5,25 (м, 2 Н), 5,16 (д, 1 Н), 5,00-4,90 (м, 2 Н), 4,60 (дд,1 Н), 4,88-4,34 (м, 2 Н), 4,18-4,10 (м, 1 Н), 2,98-2,89 (м, 1 Н), 2,68 (дд, 2 Н), 2,18-1,96 (м, 6 Н), 1,50-1,32 (м,7 Н), 1,28 (с, 9 Н), 1,09-1,25 (м, 2 Н). К раствору соединения I-11 (0,10 г, 0,11 ммоль) в CH2Cl2 (10 мл) при комнатной температуре в атмосфере азота N2 добавляли катализатор Ховейды-Граббса 2-го поколения (35 мг, 0,056 ммоль). Затем реакционную смесь перемешивали при 40 С в течение 24 ч для проведения метатезисной циклизации. Реакционную смесь гасили и очищали реакционную смесь по методу колоночной хроматографии с получением соединения I-12 (30 мг, 31%). МС: m/z 893,3 (М 1); 1H ЯМР (CDCl3)10,39 (с, 1 Н), 8,59 (д, 2 Н), 8,21 (д, 1 Н), 7,77 (д, 2 Н), 7,69-7,57 (м, 2 Н), 7,46 (дд,1 Н), 7,20 (с, 1 Н), 6,12 (с, 1 Н), 5,69 (кв, 1 Н), 5,12 (д, 1 Н), 4,97 (дд, 1 Н), 4,81-4,68 (м, 2 Н), 4,28-4,07 (м, 2 Н),2,96-2,49 (м, 3 Н), 2,30 (кв, 1 Н), 1,96-1,12 (м, 14 Н), 1,08 (с, 9 Н), 0,96-0,82 (м, 2 Н). К раствору соединения I-12 (30 мг, 0,034 ммоль) в МеОН (10 мл) при комнатной температуре в ат- 19022118 мосфере N2 добавляли 5% Pd-C (5 мг). Затем реакционную смесь перемешивали в атмосфере водорода при комнатной температуре и давлении 60 фунт/кв.дюйм (414 кПа) в течение 4 ч. Реакционную смесь фильтровали и очищали по методу колоночной хроматографии с получением соединения 1 (16,5 мг,55%). МС: m/z 895,3 (М 1); 1(с, 1 Н), 6,11 (с, 1 Н), 5,29 (д, 1 Н), 4,72 (м, 2 Н), 4,38 (м, 2 Н), 4,12 (м, 1 Н), 3,02-2,58 (м, 3 Н), 1,98-0,86 (м,29 Н). Примеры 2-141. Синтез соединений 2-141. Каждое из соединений 2-141 получали способом, сходным с описанным в примере 1.
МПК / Метки
МПК: A61K 31/4355, A61P 31/12, C07D 401/12, C07D 403/12
Метки: ингибиторы, протеазы
Код ссылки
<a href="https://eas.patents.su/30-22118-ingibitory-proteazy-hcv.html" rel="bookmark" title="База патентов Евразийского Союза">Ингибиторы протеазы hcv</a>
Предыдущий патент: Устройство для изготовления композитных тел непрерывных листовидных элементов
Следующий патент: Комбинированная терапия раковых заболеваний с помощью соединений – ингибиторов hsp90
Случайный патент: Экранирующее устройство