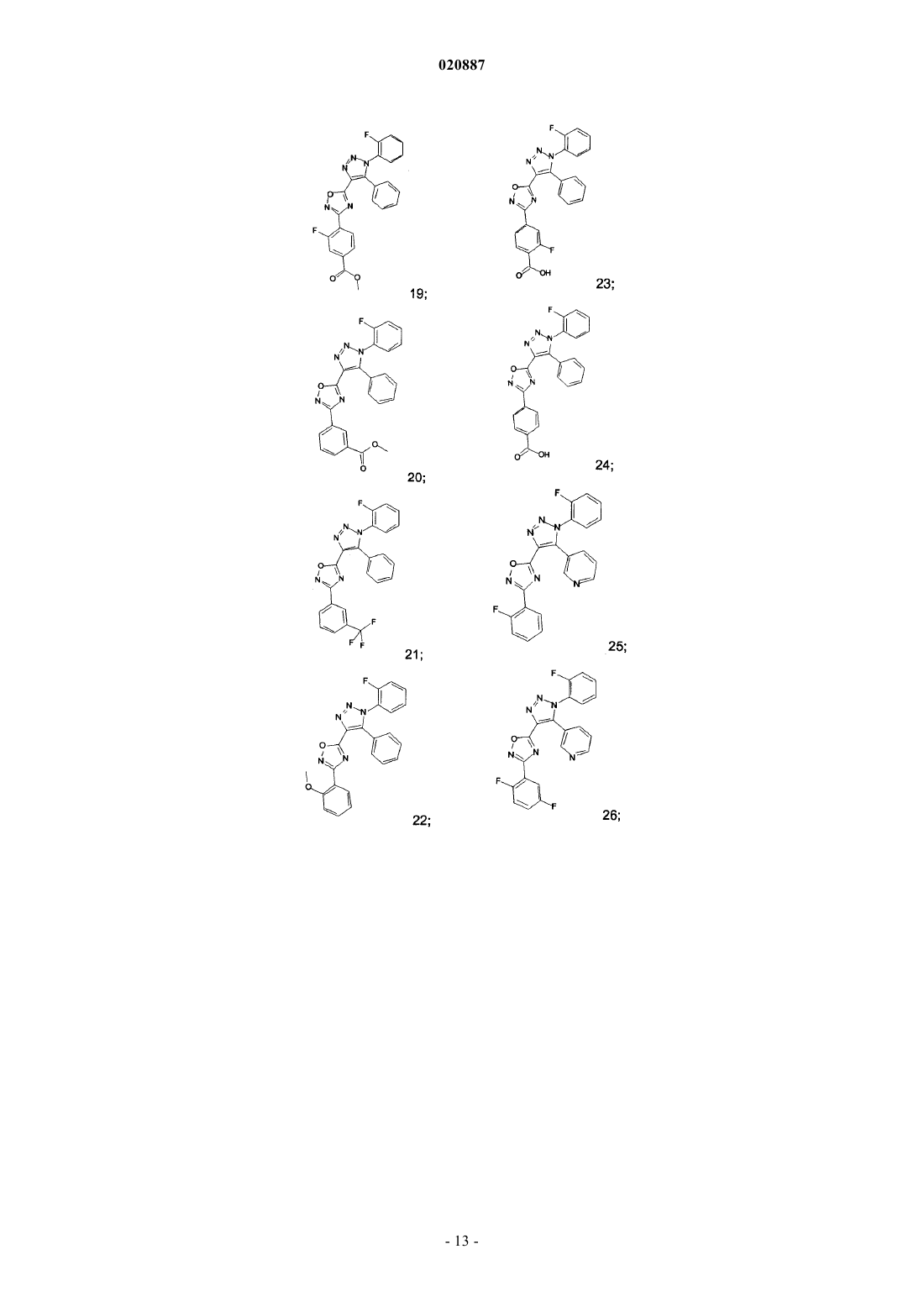Триазолсодержащие производные оксадиазола
Номер патента: 20887
Опубликовано: 27.02.2015
Авторы: Бейкер-Гленн Чарльз, Найт Крис, Бомбрэн Аньес, Клева Кристоф, Шварц Маттиас, Себий Эрик, Блэкеби Уэсли, Марэн Дельфин, Кваттропани Анна, Рауз Крейг
Формула / Реферат
1. Соединение формулы I
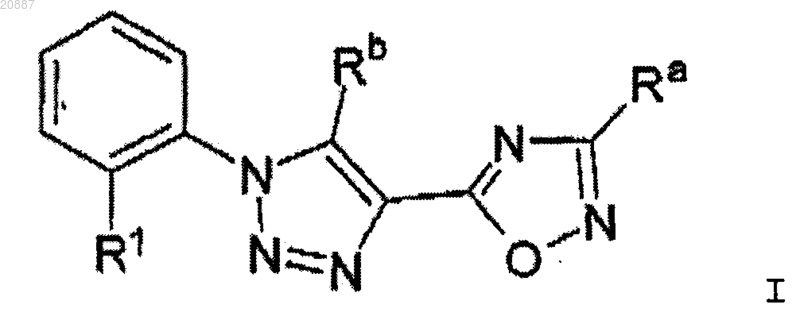
где R1 означает Hal;
Ra означает Ar или Het; при условии, что Ra не является бензо[1,3]диоксолильной группой или фенильной группой, незамещенной или замещенной по меньшей мере одним метилом, F, Cl, ОМе и/или OEt, если Rb является метильной группой;
Rb означает A, Ar, Het, Ar-алкил или Het-алкил;
Hal означает F, Cl, Br или I;
А означает разветвленный или линейный алкил, содержащий от 1 до 12 С-атомов, где один или более атомов могут быть заменены Hal, OR3, CN, CO2R3, циклоалкилом, содержащим от 3 до 7 атомов углерода в кольце, или N(R3)2, и где одна или более несмежных СН2-групп могут быть заменены О, NR3 или S и/или-СО-, -NR3CO-, -CONR3-, NR3CO2-, -NR3CONR3-, -CH=CH-, -СºС-группами или
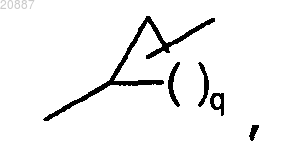 или означает циклоалкил или циклоалкилалкилен, содержащий 3-7 кольцевых С-атомов;
или означает циклоалкил или циклоалкилалкилен, содержащий 3-7 кольцевых С-атомов;q равно 1, 2, 3 или 4;
Ar означает моноциклическое или бициклическое ароматическое карбоциклическое кольцо, имеющее от 6 до 14 атомов углерода, которые могут быть незамещенными или монозамещенными, дизамещенными или тризамещенными заместителем, выбранным из R4;
Ar-алкил означает арильную группу, связанную с остальной частью молекулы через C1-C12 алкиленовую цепь;
Het означает моноциклическое или бициклическое, насыщенное, ненасыщенное или ароматическое гетероциклическое кольцо, содержащее от 1 до 4 атомов N, О и/или S, которые могут быть незамещенными или монозамещенными, дизамещенными или тризамещенными заместителем, выбранным из R4, и где одна или более СН2- группы могут быть заменены -СО-;
Het-алкил означает группу Het, связанную с остальной частью молекулы через C1-C12 алкиленовую цепь;
R4 выбирают из A, Hal, гидрокси, алкокси, карбокси, карбоксиалкила, перфторалкила, перфторалкокси, ацила, алкилсульфонила, сульфонила, -SO2R3, циано, нитро, амино, амидо, алкила, необязательно замещенного карбокси, -N(R3)2, -CO(NR3)2, -OR3, (NR3)COR3, -CO2R3, -COR3, или Ar-алкила или Het-алкила, оба необязательно замещены A, Hal, ацилом, акилсульфонилом, карбокси, -N(R3)2, -CON(R3)2, -OR3, (NR3)COR3, -CO2R3, -COR3, -SO2N(R3)2, SO2 алкилом, NR3SO2 алкилом,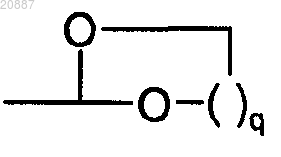 или C1-С6алкилом;
или C1-С6алкилом;R3 является Н или C1-C6 алкилом;
алкил означает углеродную цепь, содержащую от 1 до 12 атомов углерода;
алкокси означает группу -О-(СН2)n-СН3, где n равно 0, 1, 2, 3 или 4 ;
ацил означает группу -C(O)R, где R может быть A, Ar, Het, как определено выше;
и его фармацевтически приемлемые производные, сольваты, таутомеры, соли и стереоизомеры, включая их смеси во всех отношениях.
2. Соединения формулы IA, IB, IC, ID, IE, IF и IG

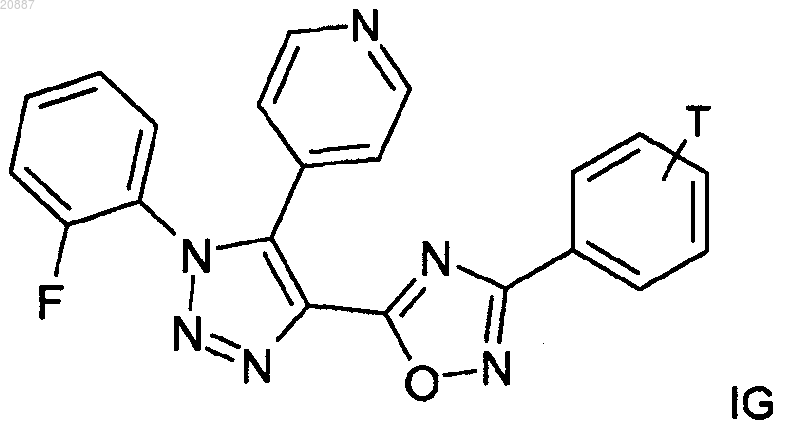
где Т означает Het-алкил, A, SO2Me, R4 и где Ra, Rb, R1, R4 являются такими, как определено в п.1,
и их фармацевтически приемлемые производные, сольваты, таутомеры, соли и стереоизомеры, включая их смеси во всех отношениях.
3. Соединения формулы I по п.1 или 2, где Het выбирают из следующих групп:

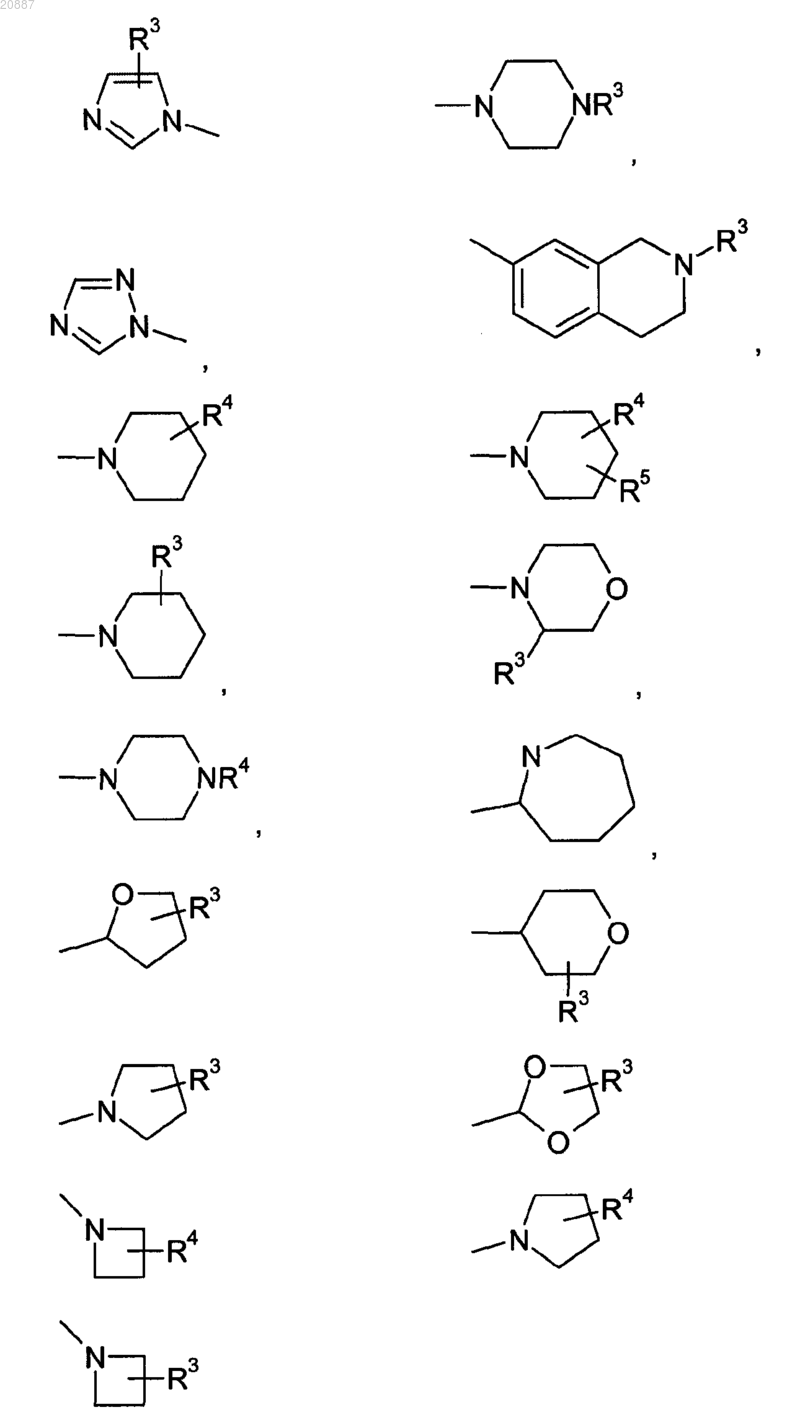
где R3, R4 являются такими, как определено выше.
4. Соединения по п.1 или 2, где R4 выбирают из следующих групп:
Hal, С1-С6алкил, -CF3, -(CH2)nOR3, -(СН2)nCOOR3, -SO2Me, -SO2N(R3)2, -COR3, -CO(NR3)2, -(CH2)nCOOtBu,
-(CH2)nN(R3)2, -(CH2)nOH, -(CH2)nN(R3)(CH2)pOR3, -(CH2)nN(R3)(CH2)pCOOR3,
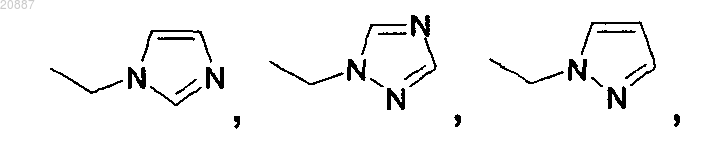
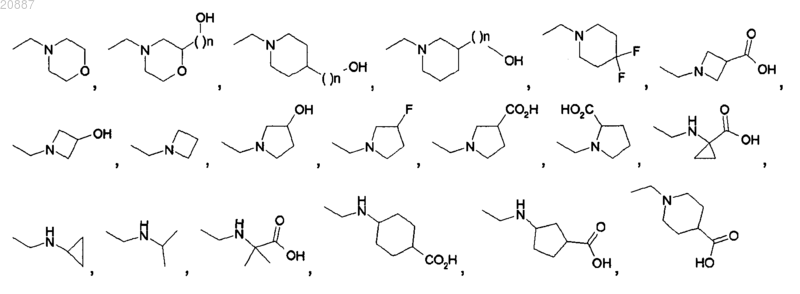
где n и p независимо выбирают из любого одного 0, 1, 2, 3 или 4 и группа R3 является такой, как определено в п.1.
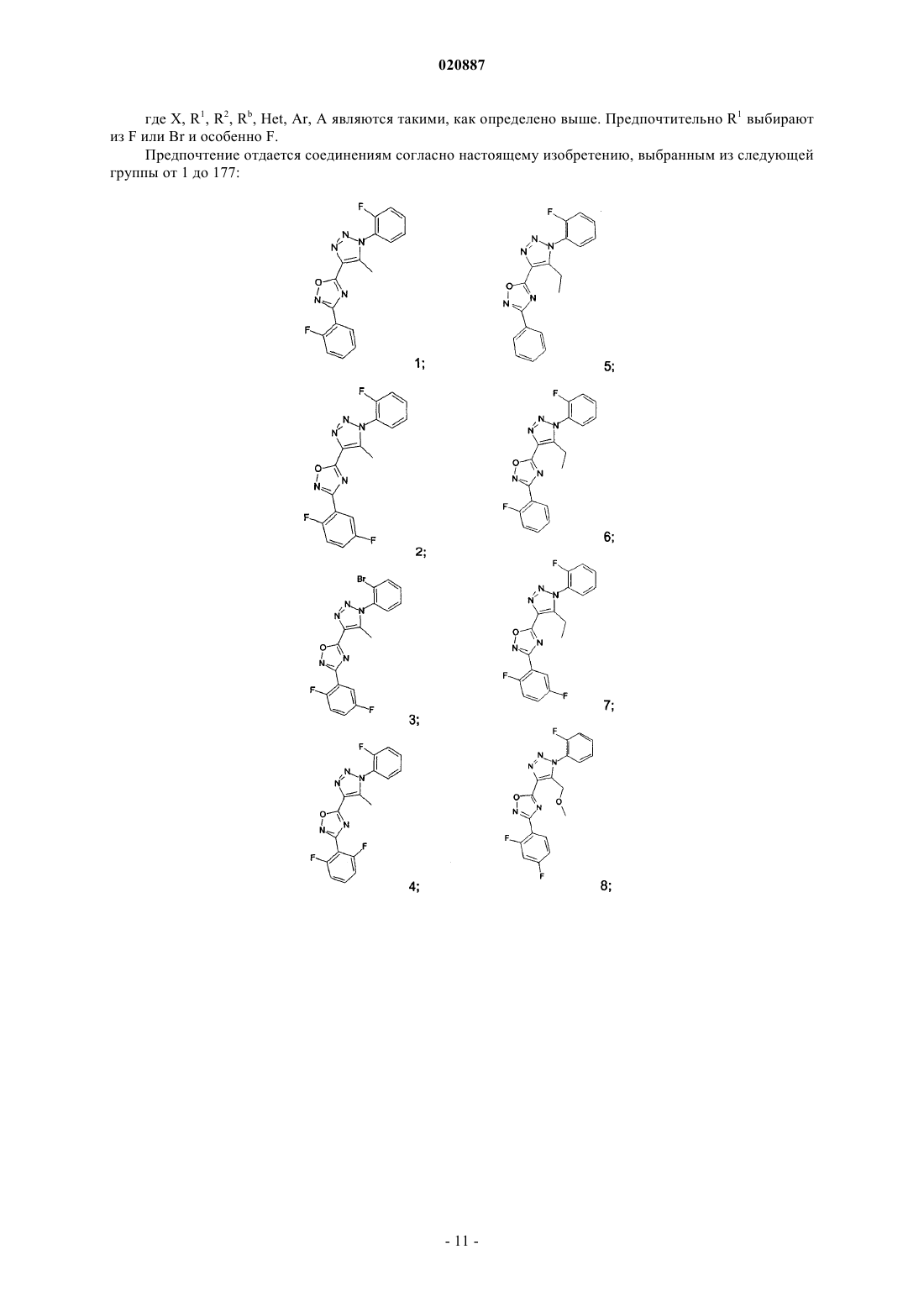
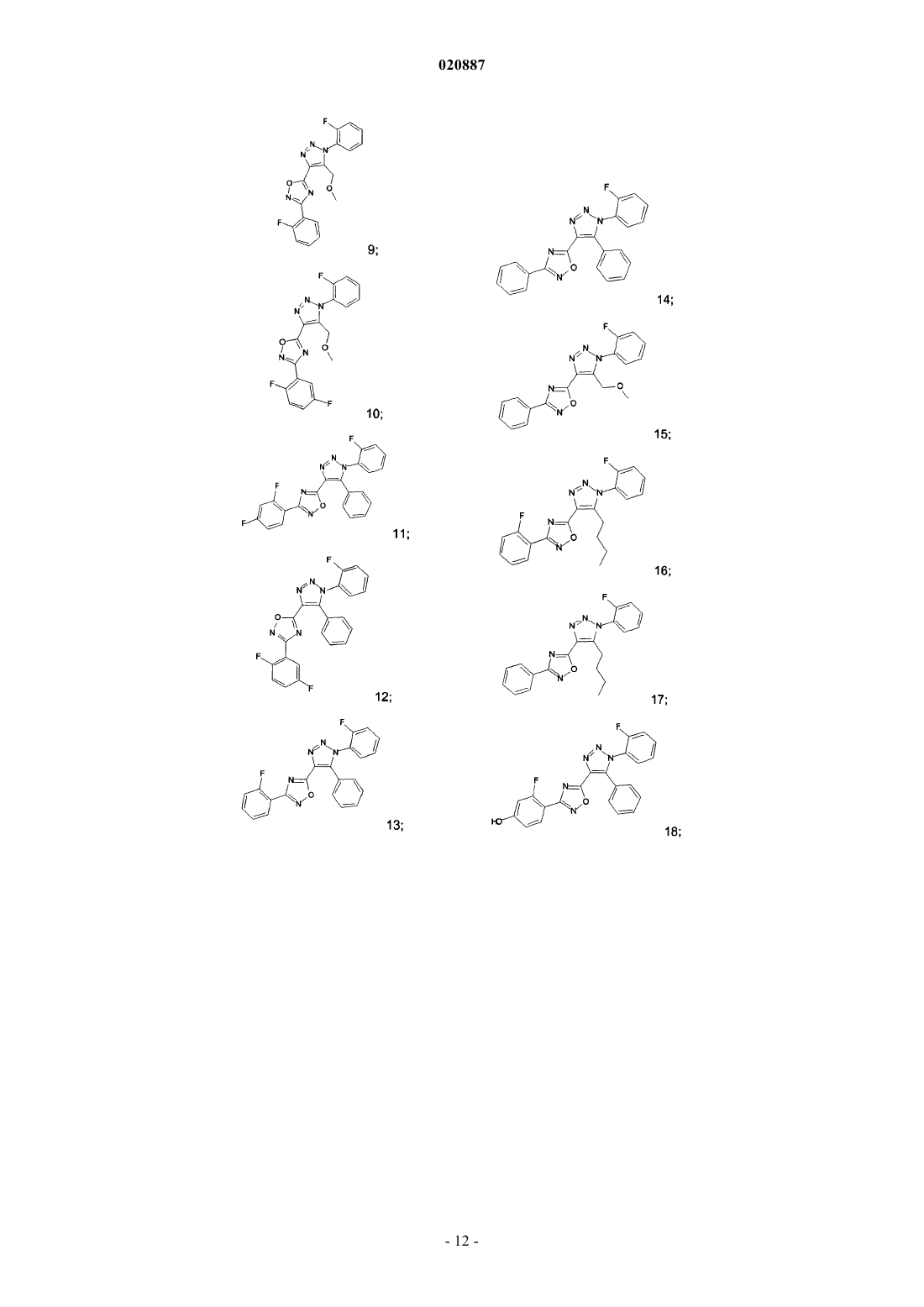
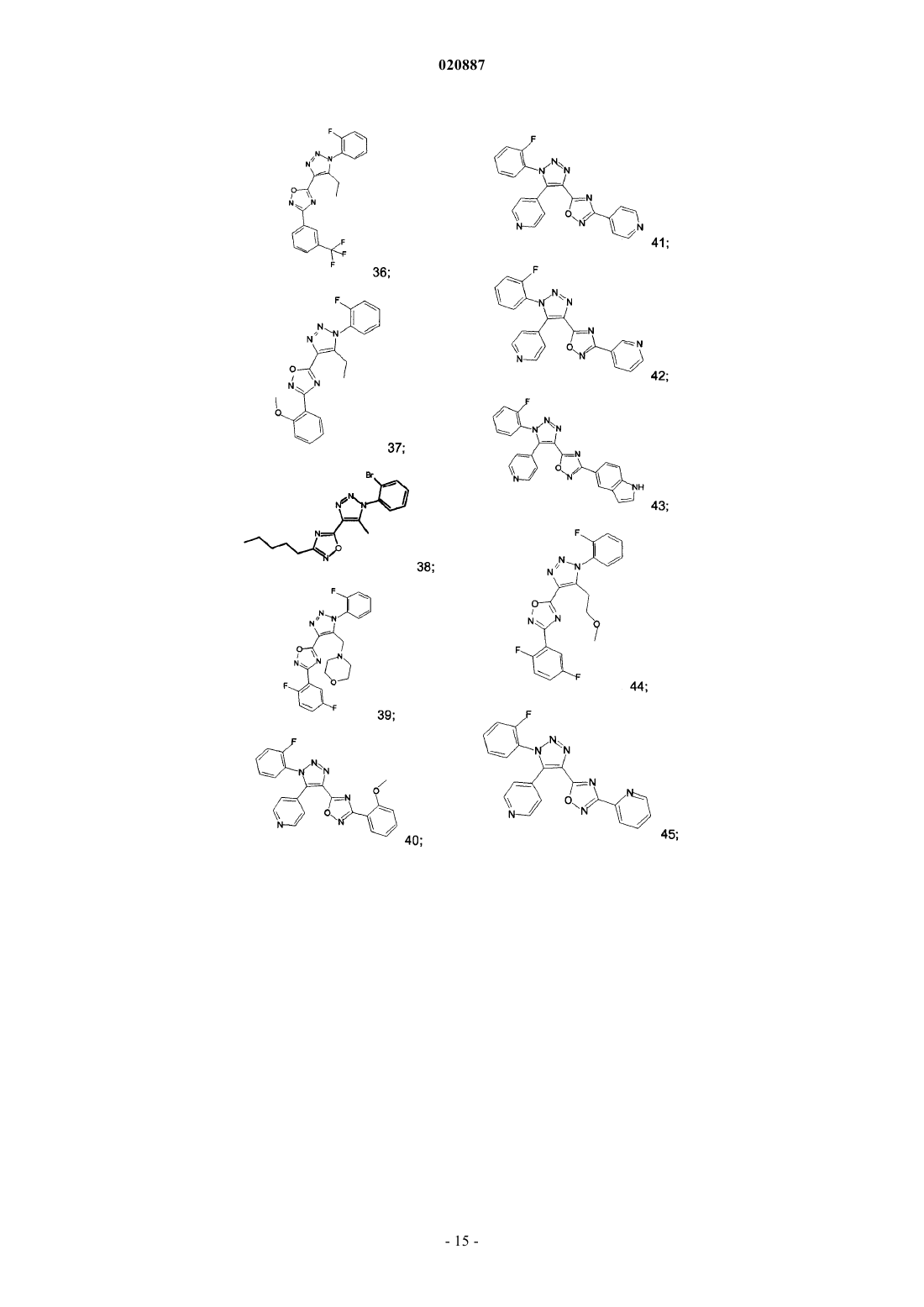
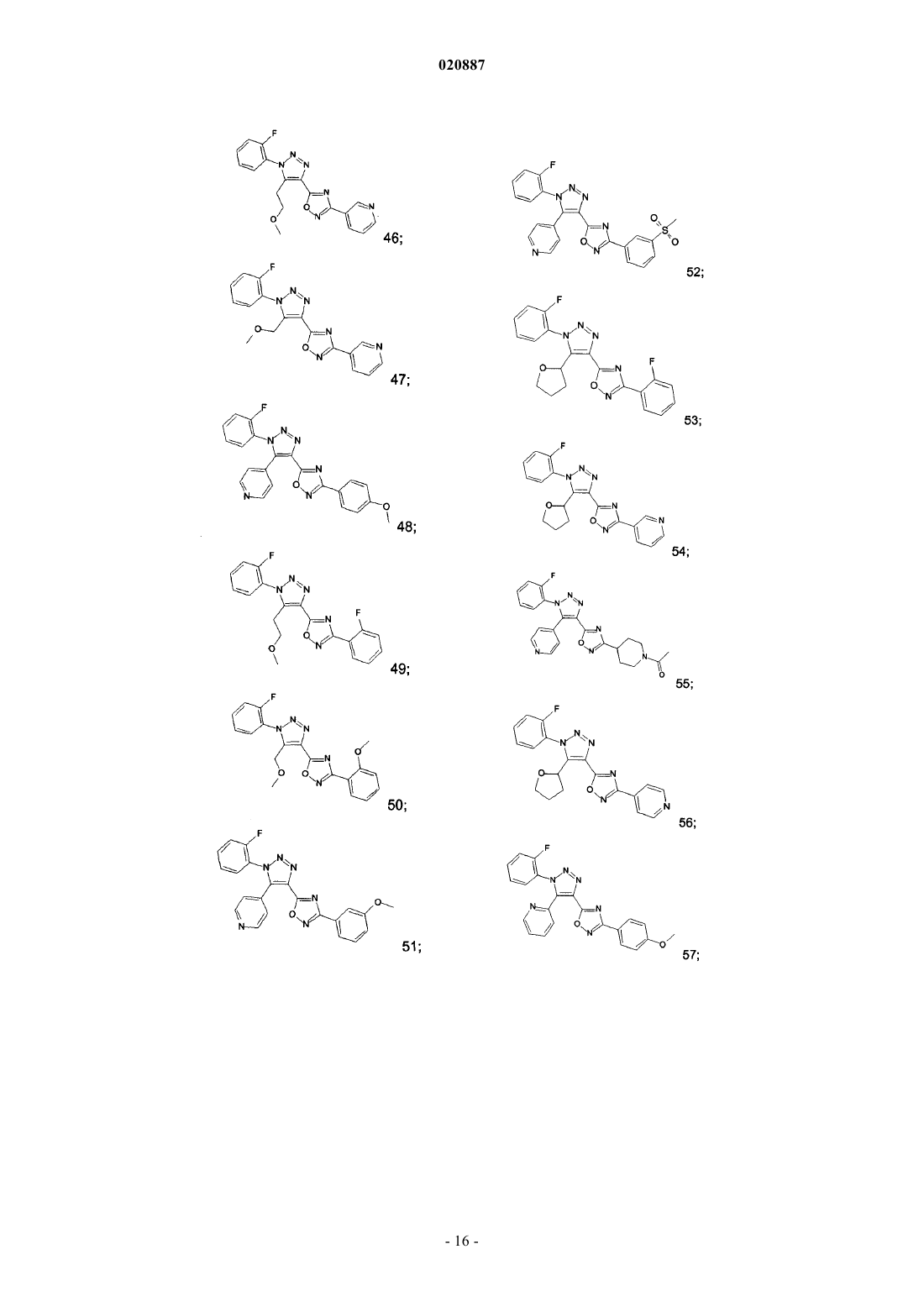
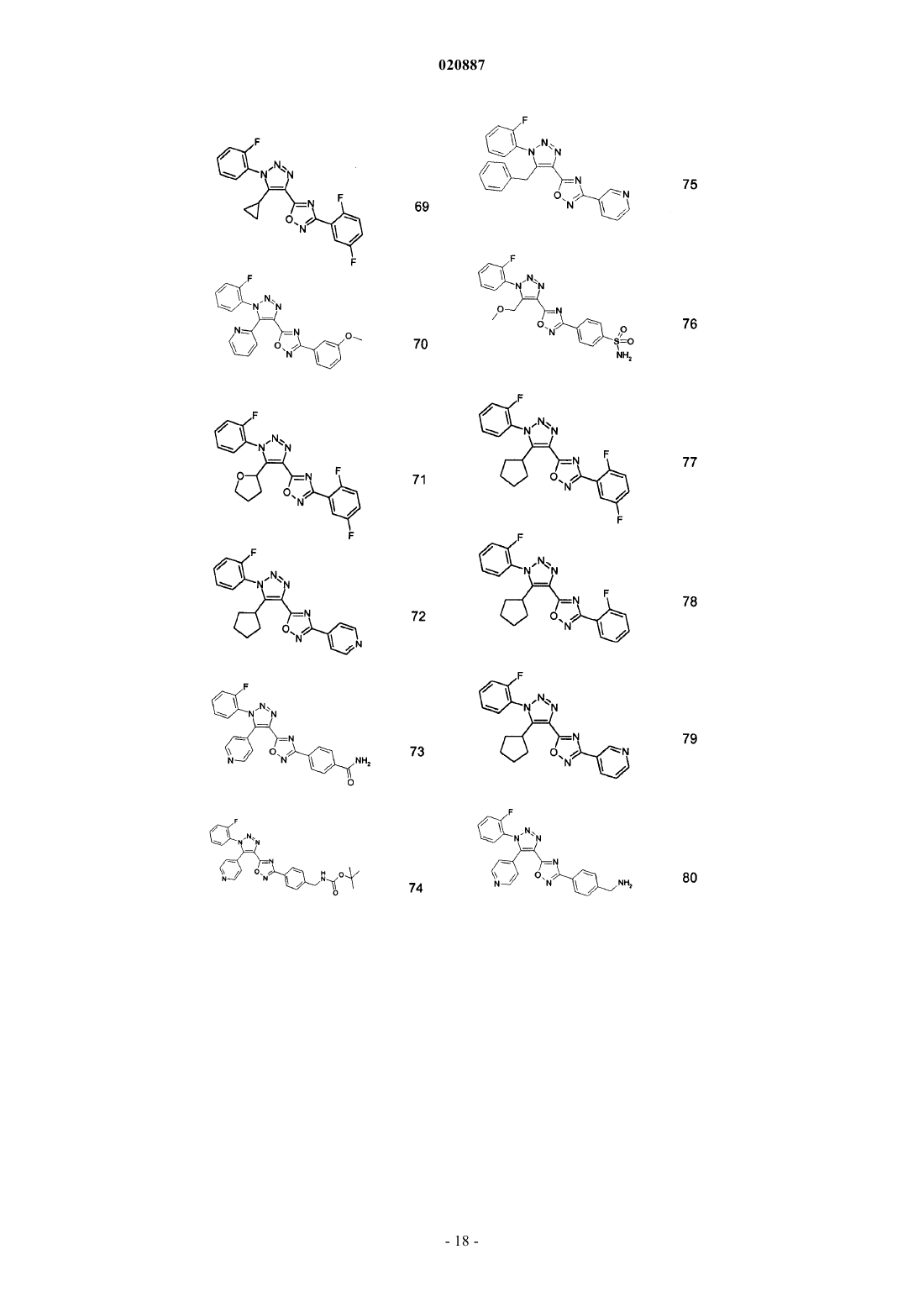
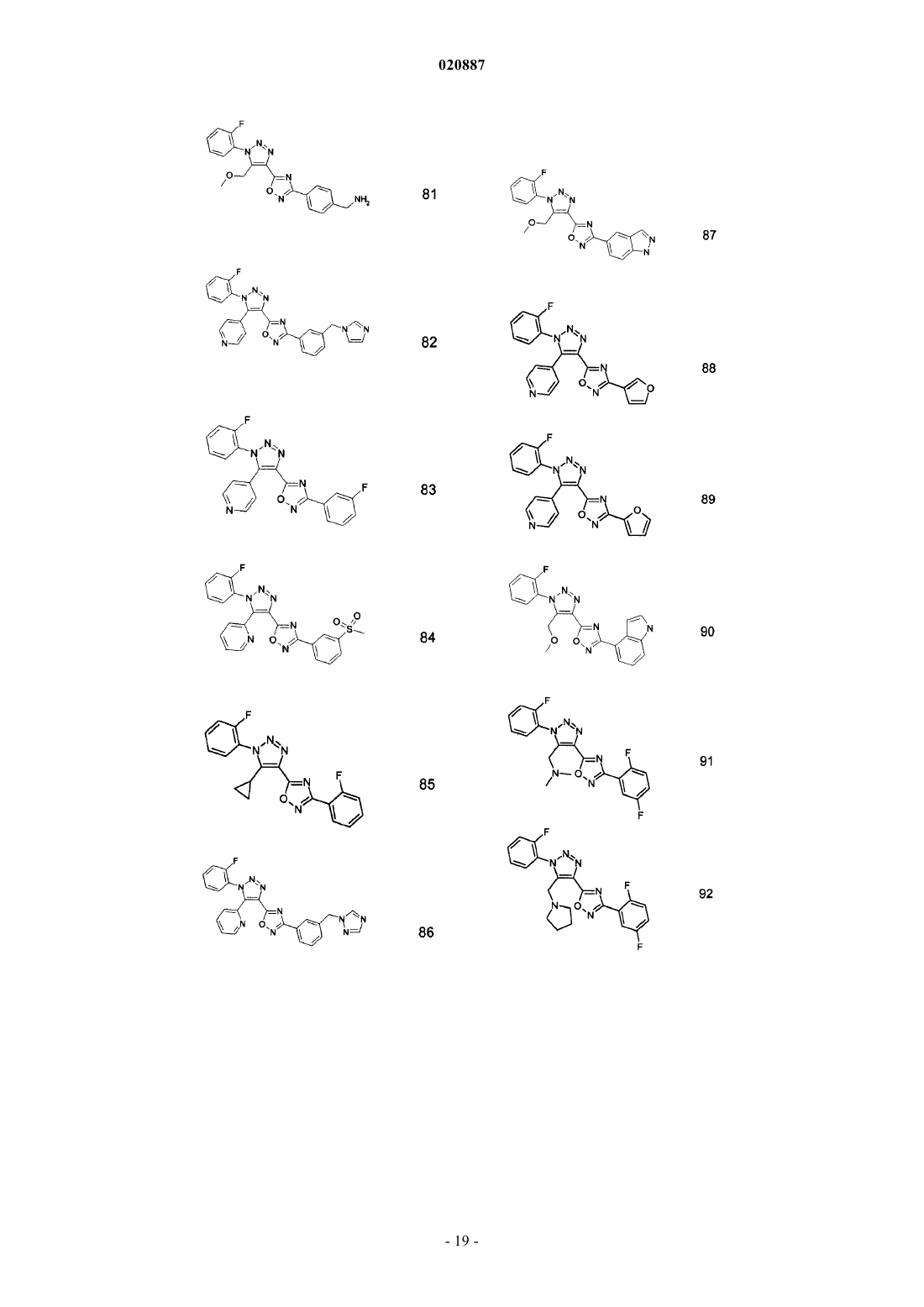
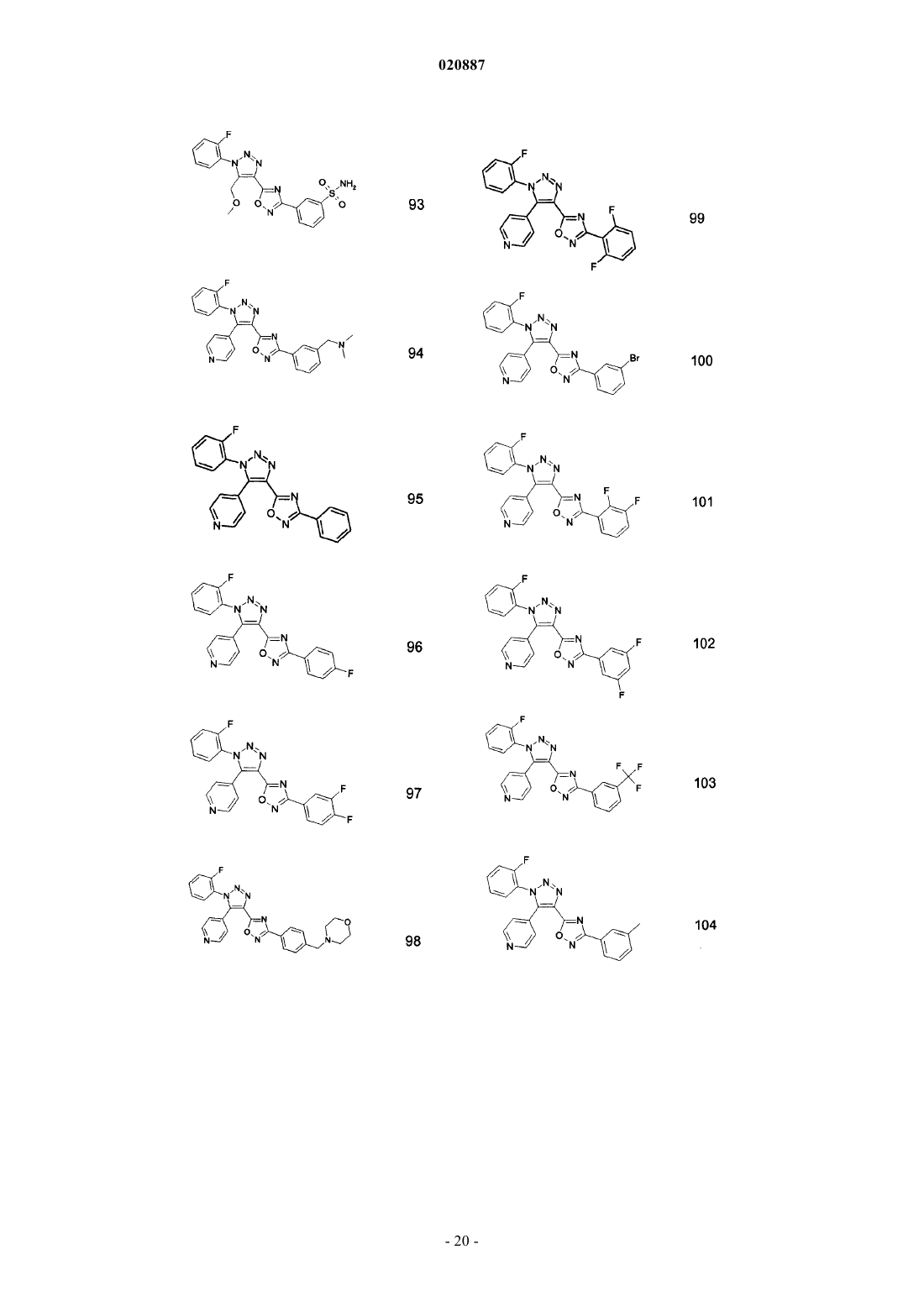
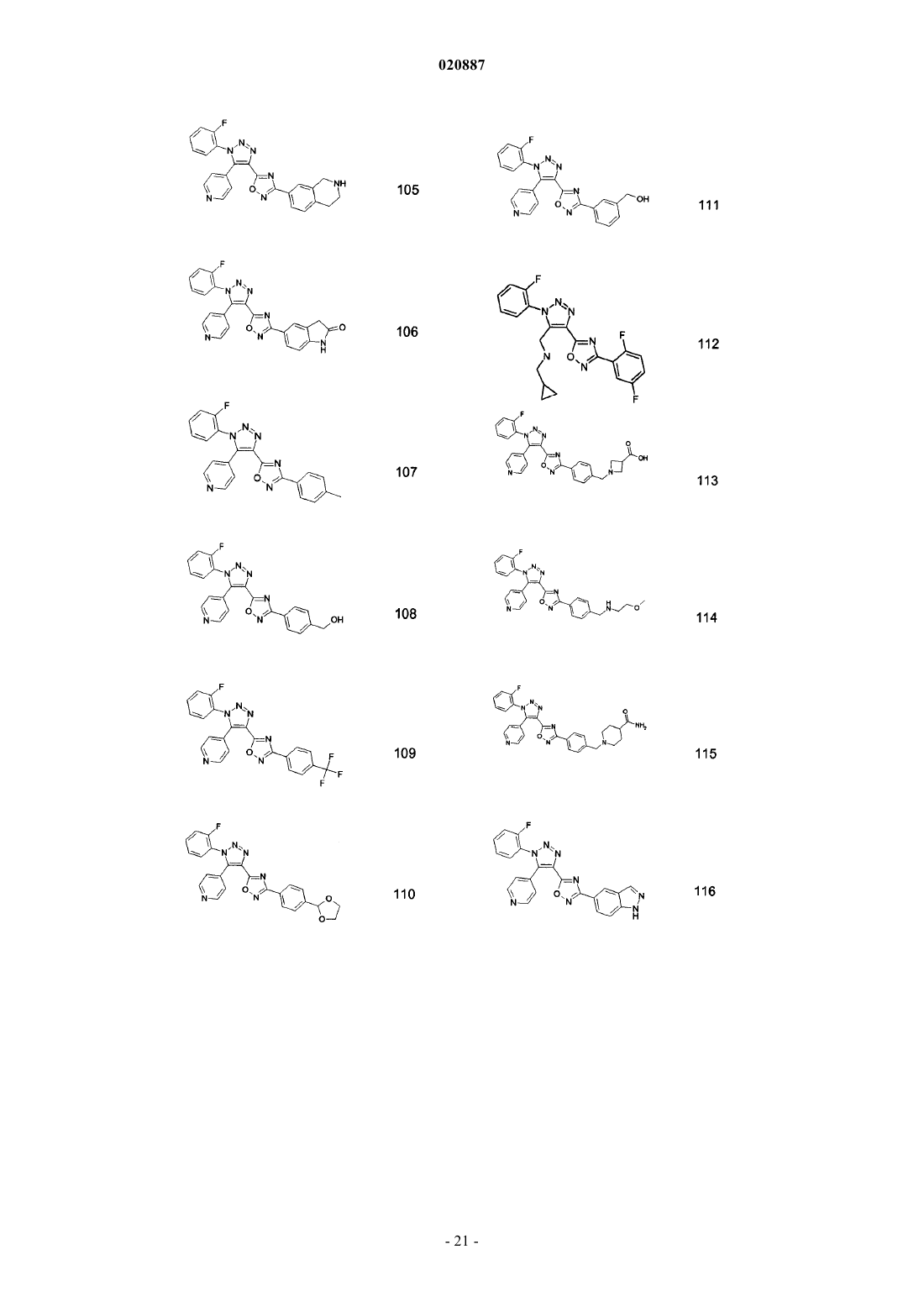
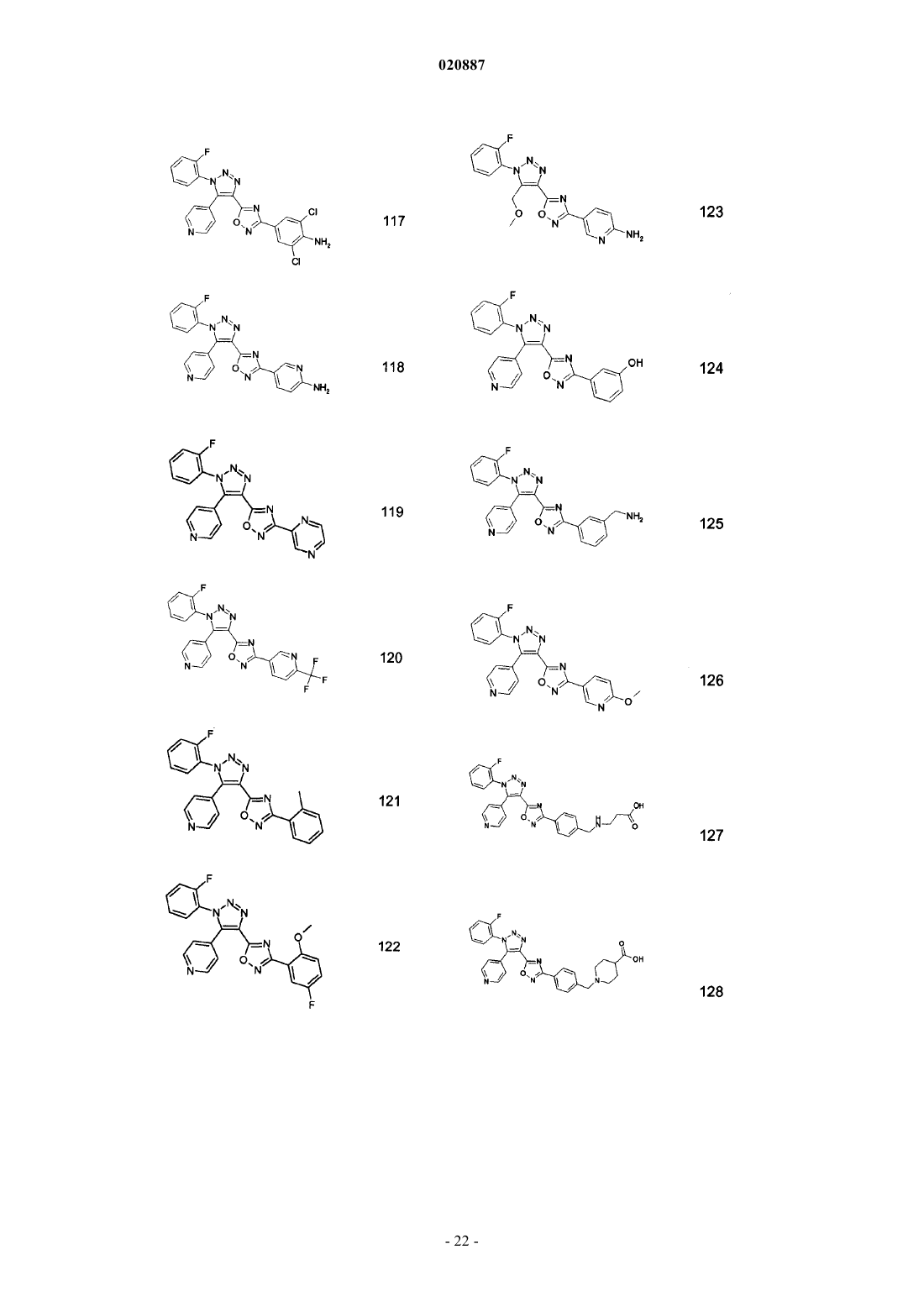
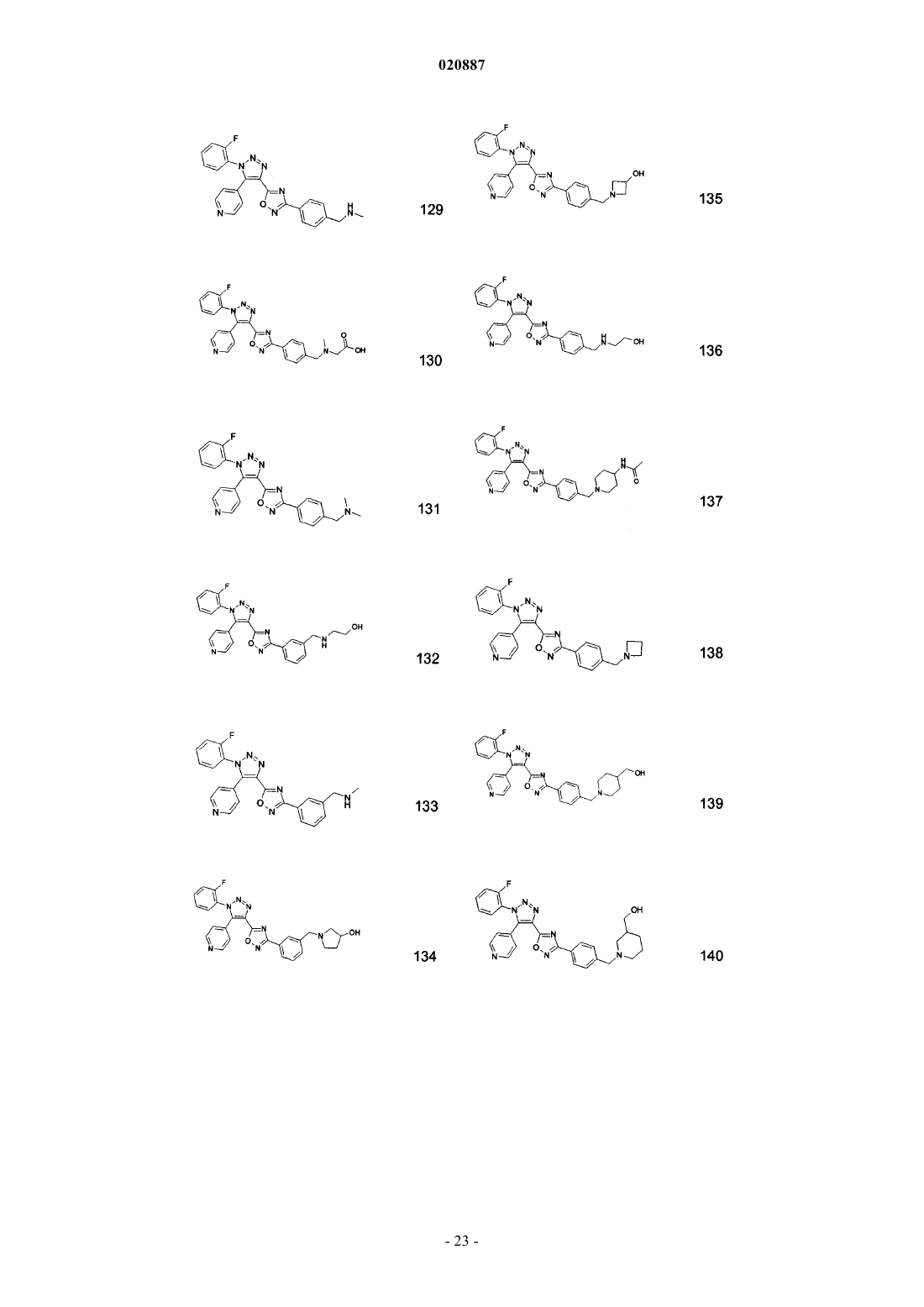
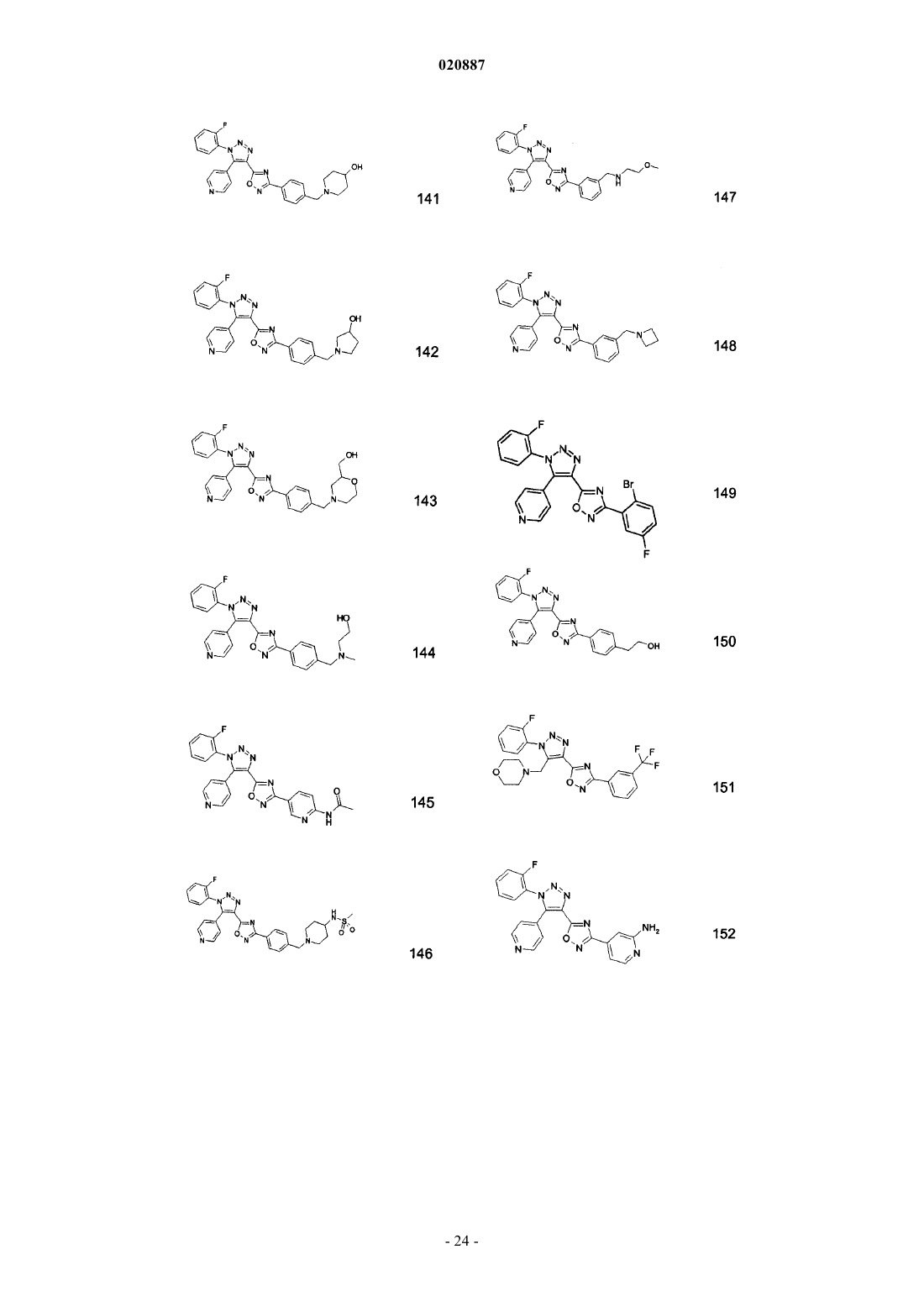
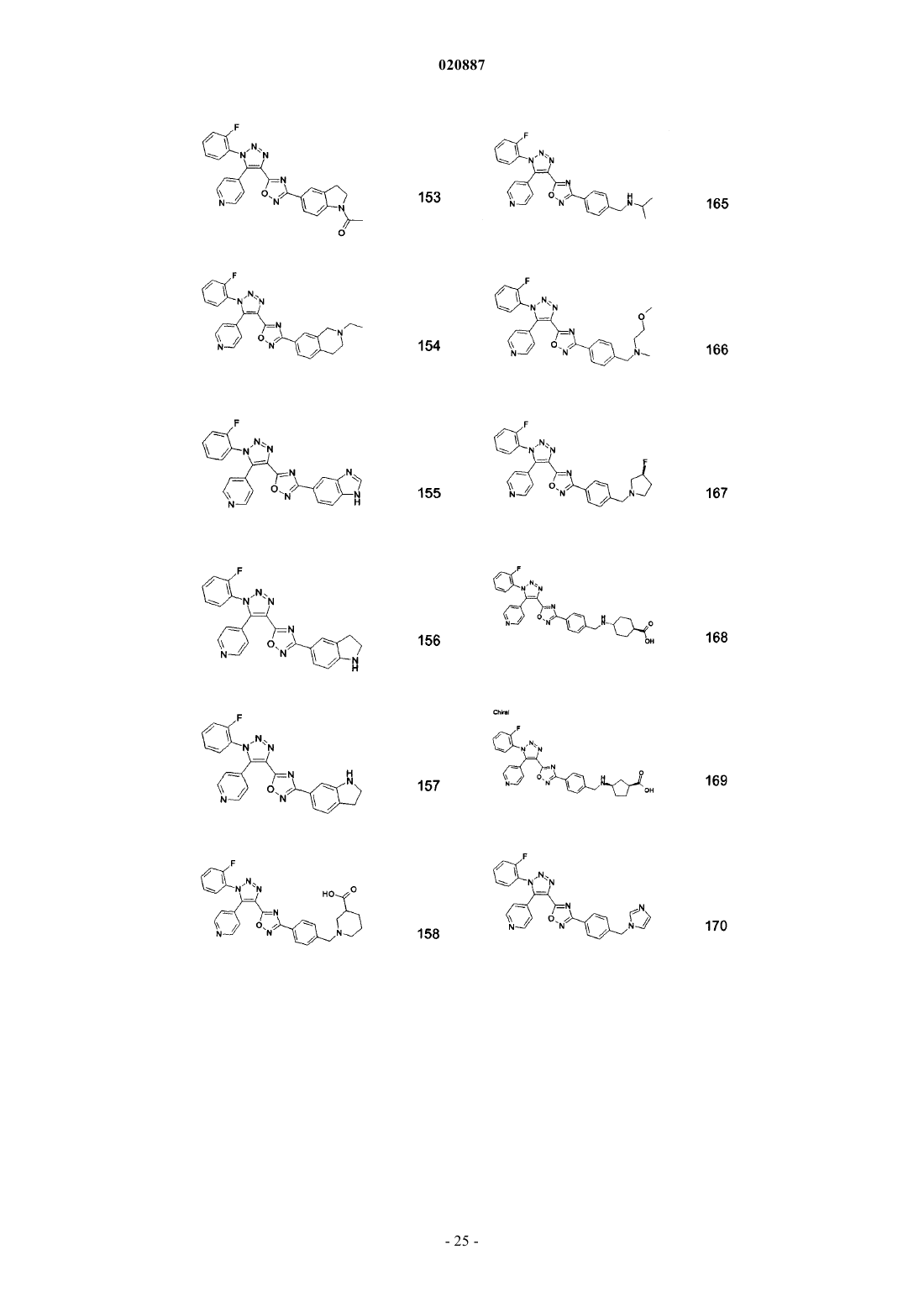
5. Соединения по любому одному из пп.1 или 2, выбранные из следующей группы:
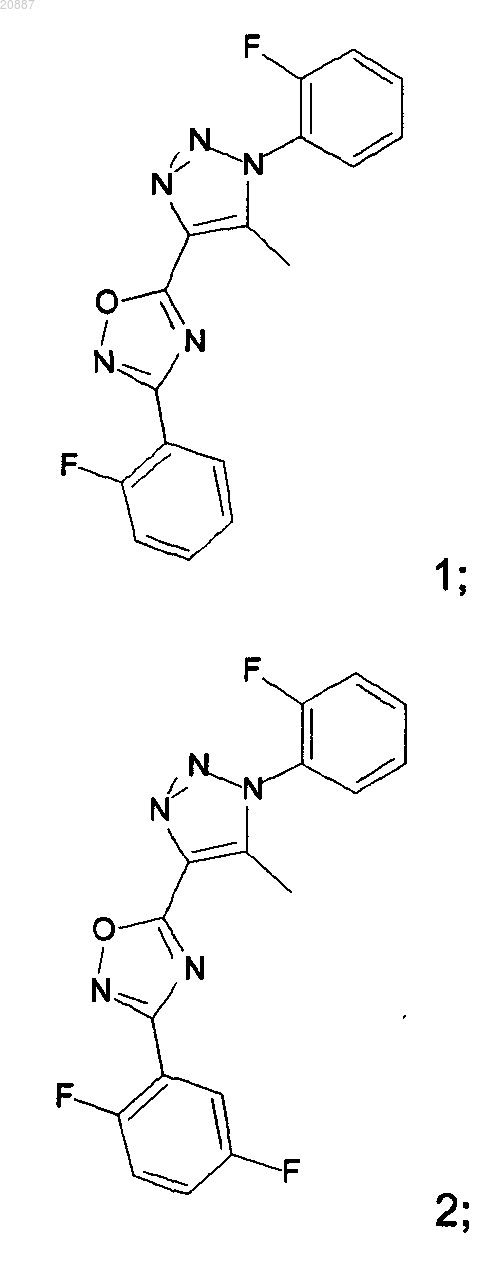
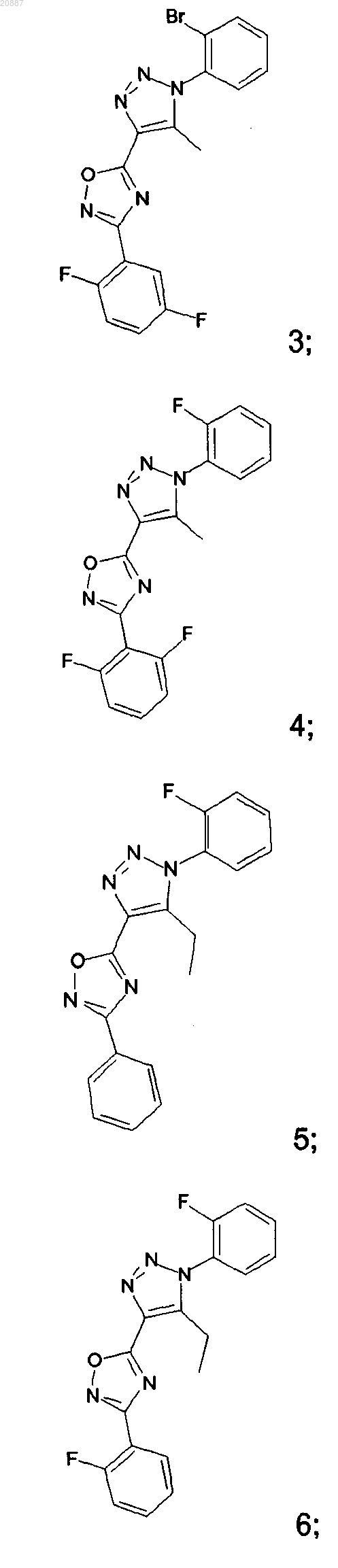
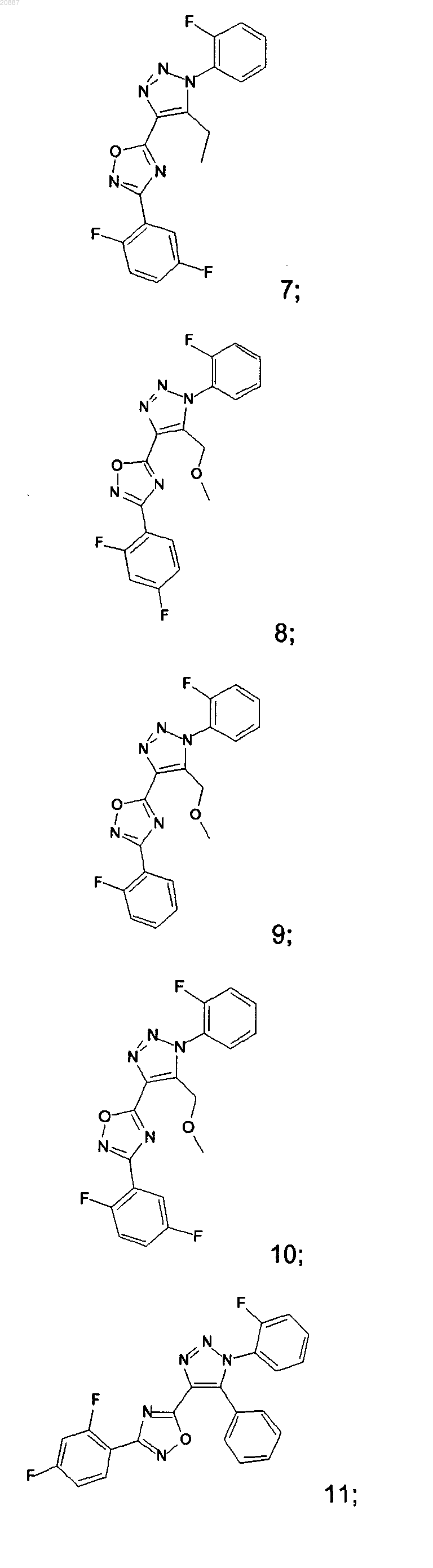
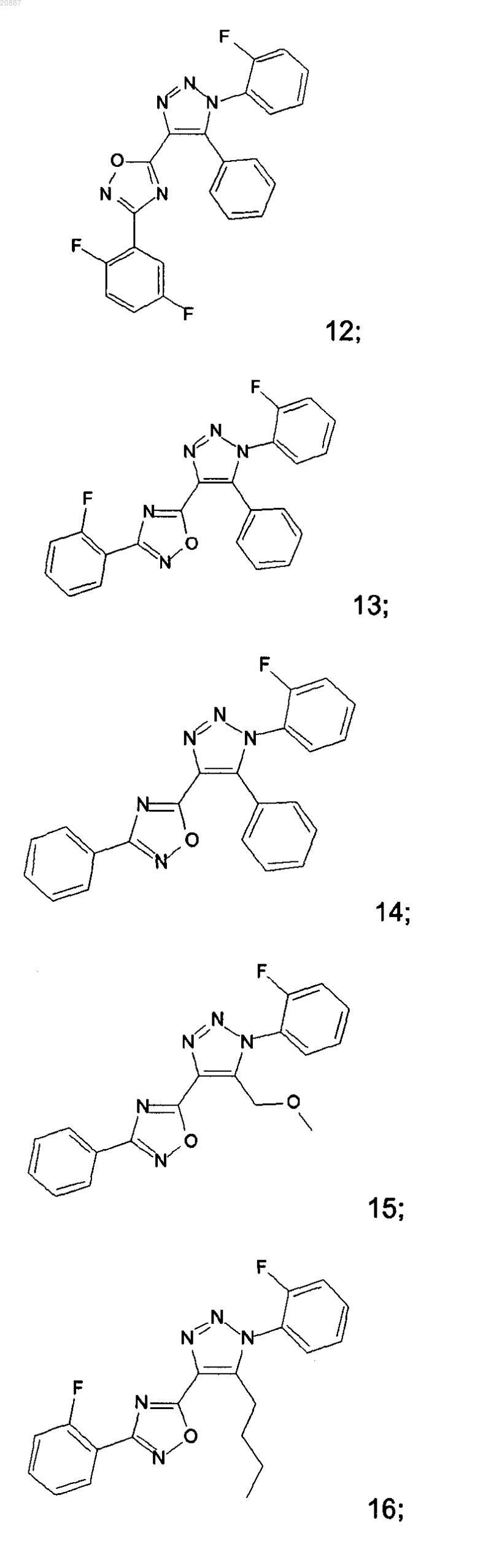
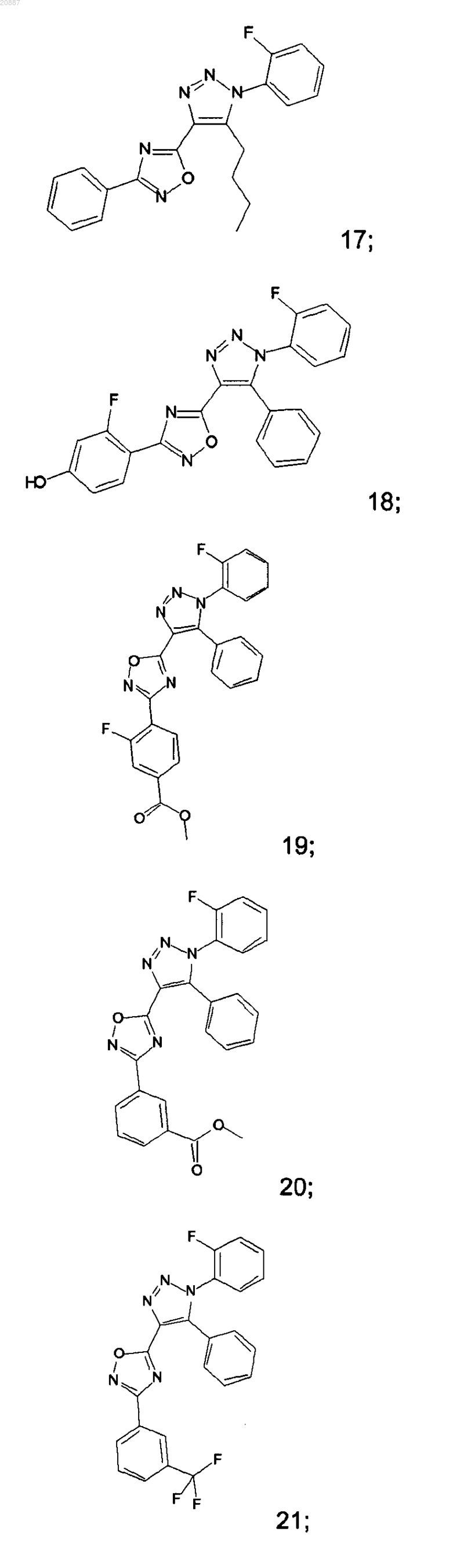
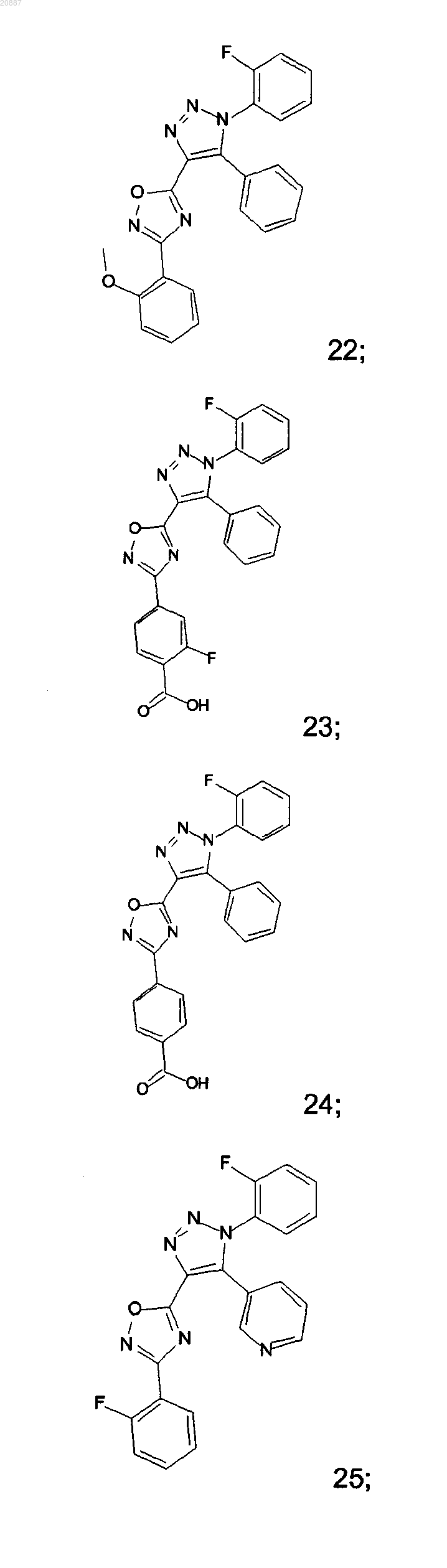
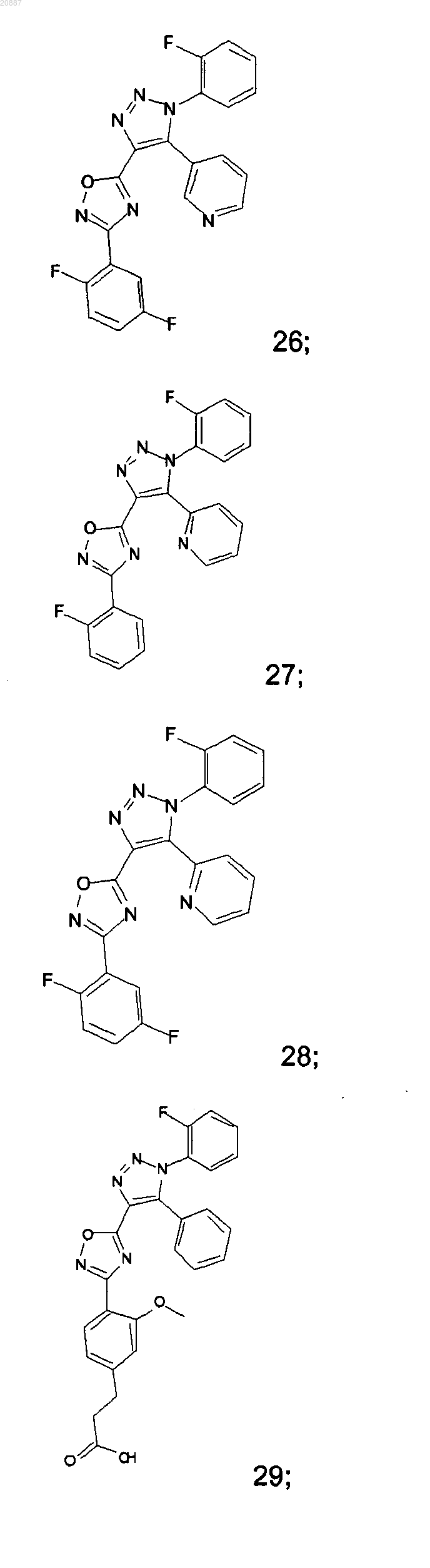
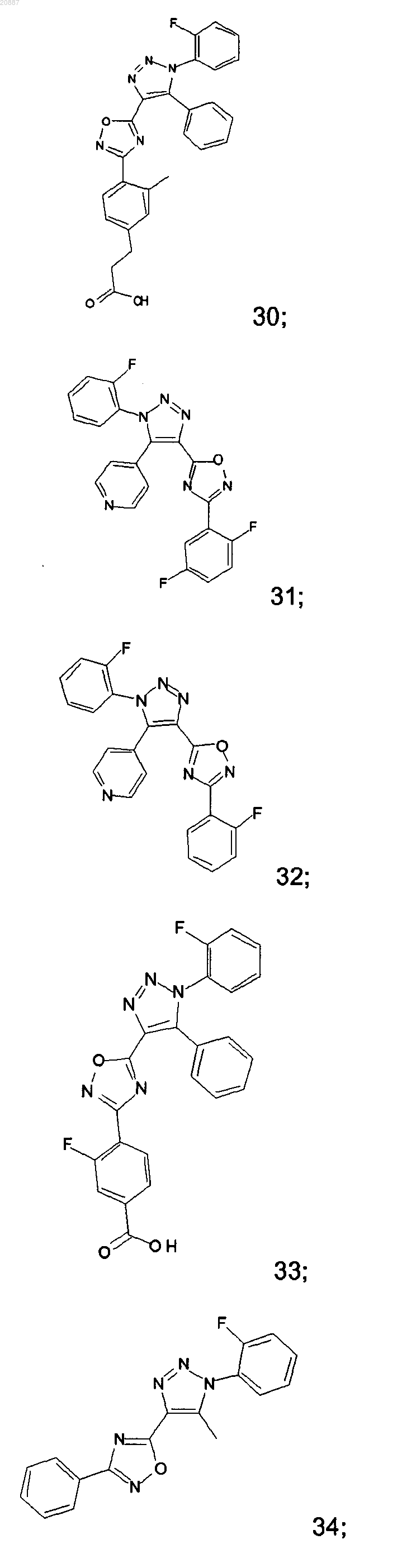
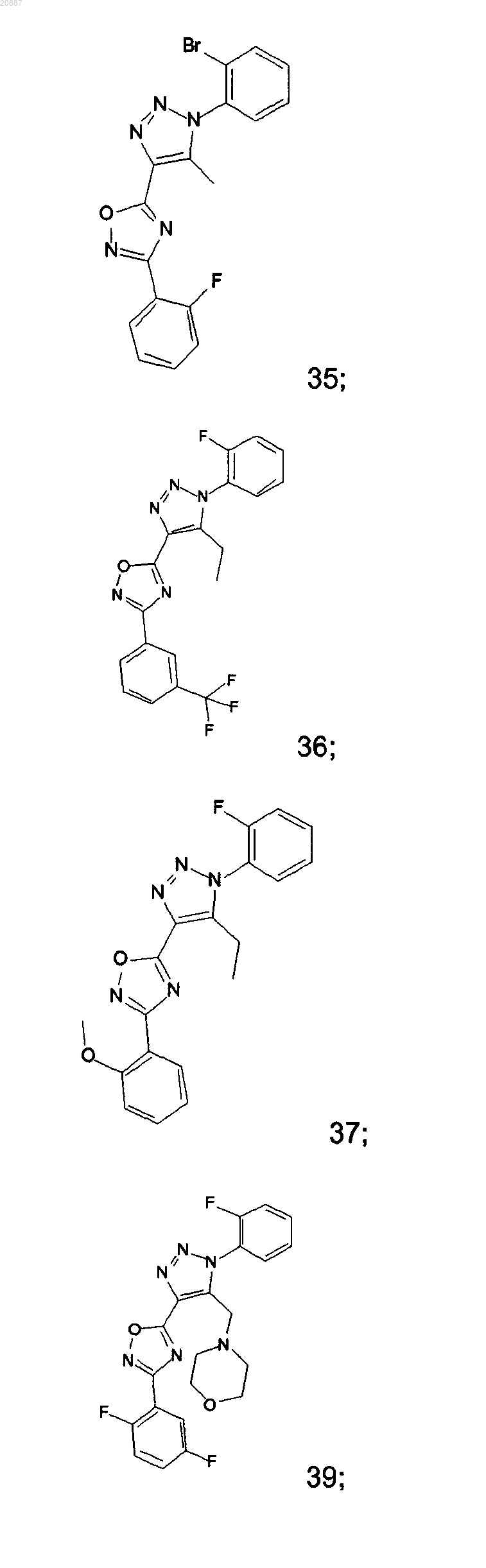
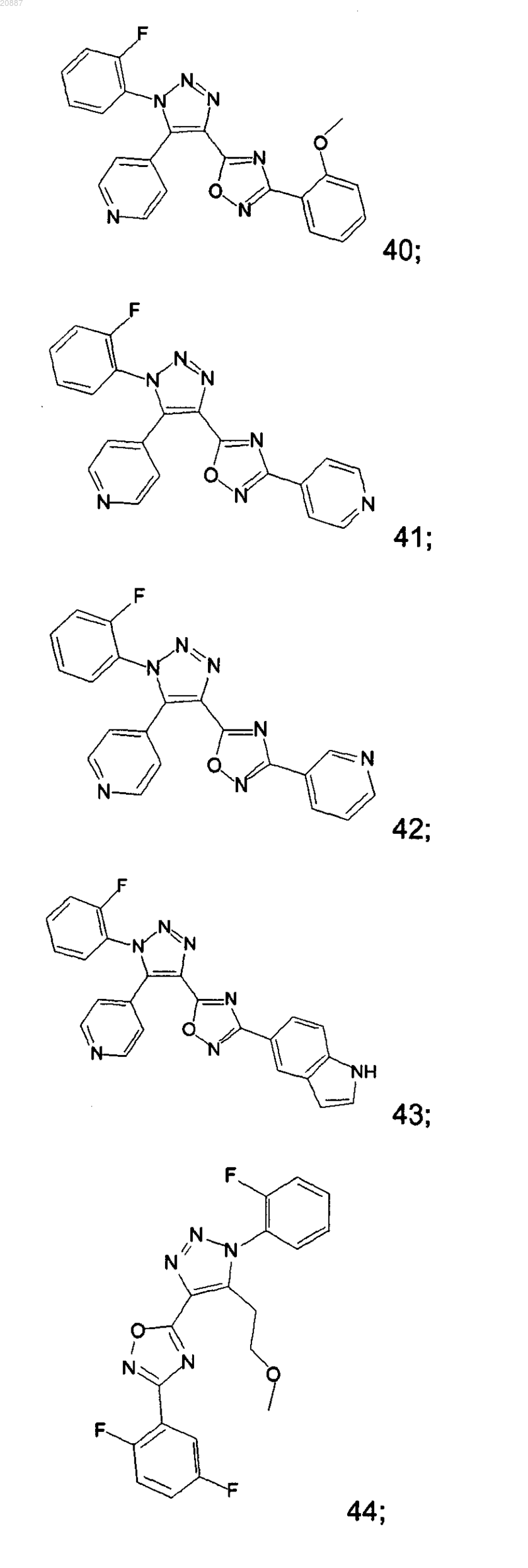
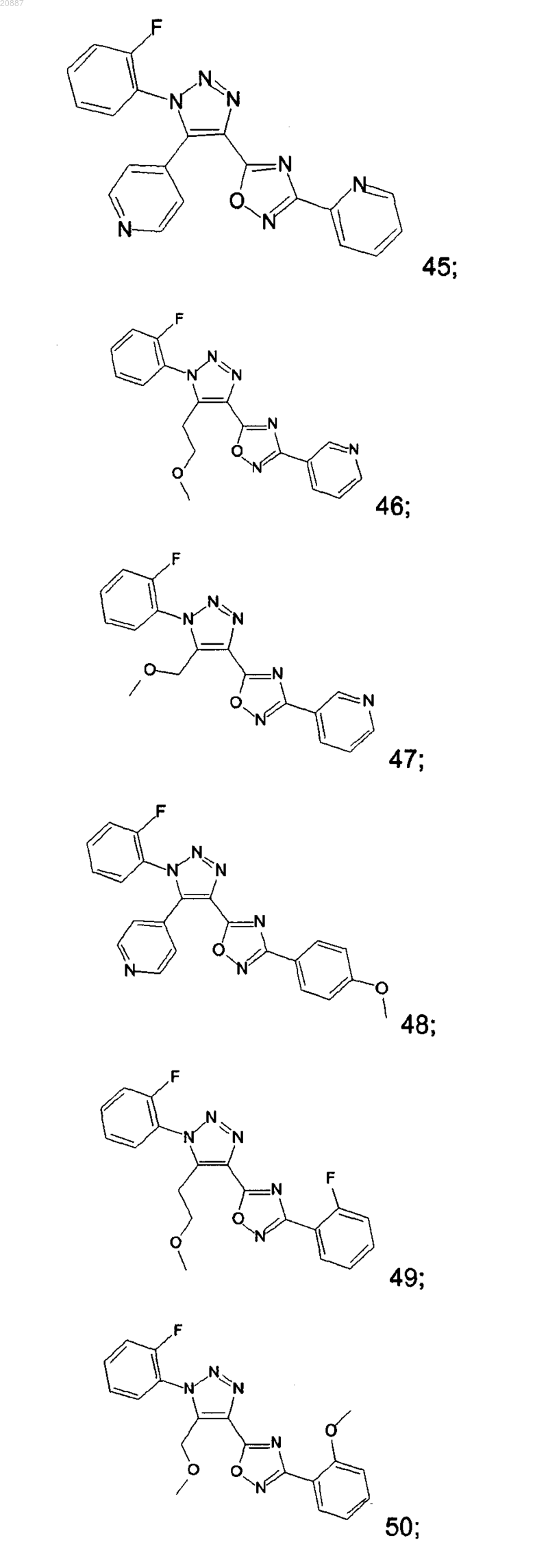
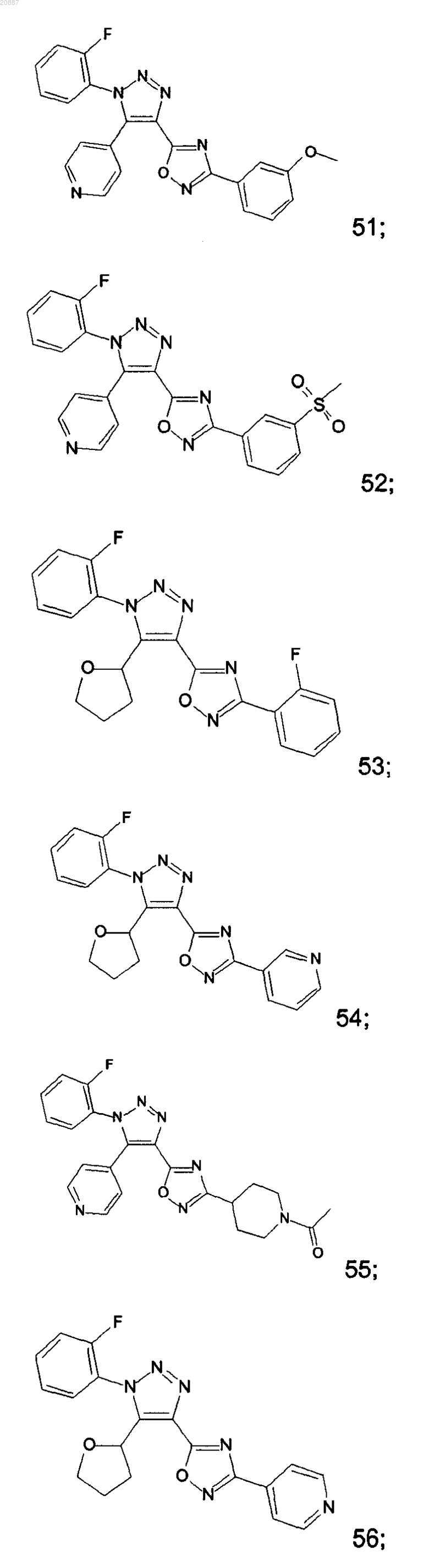

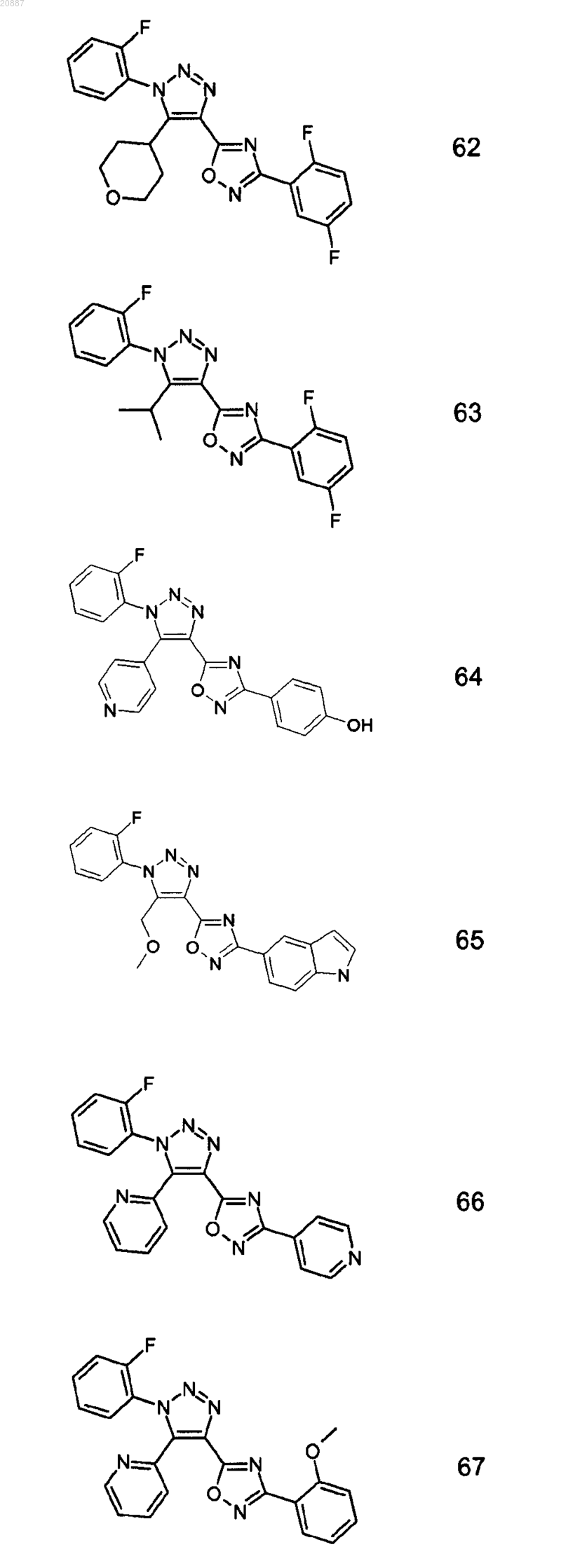
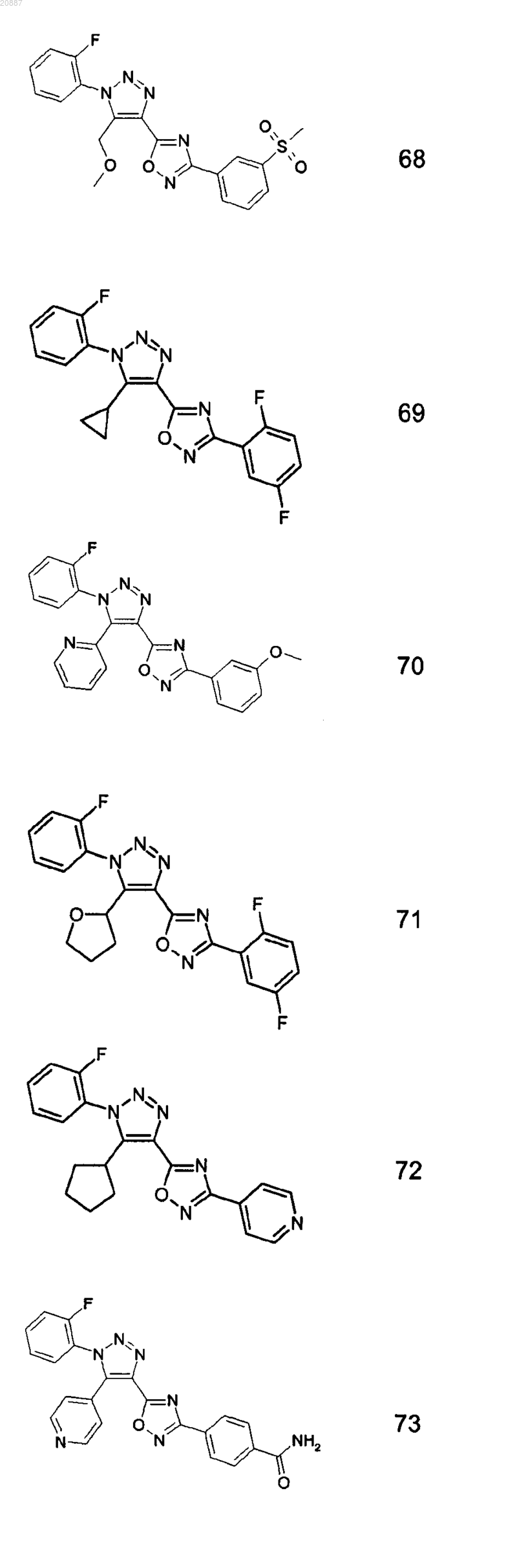
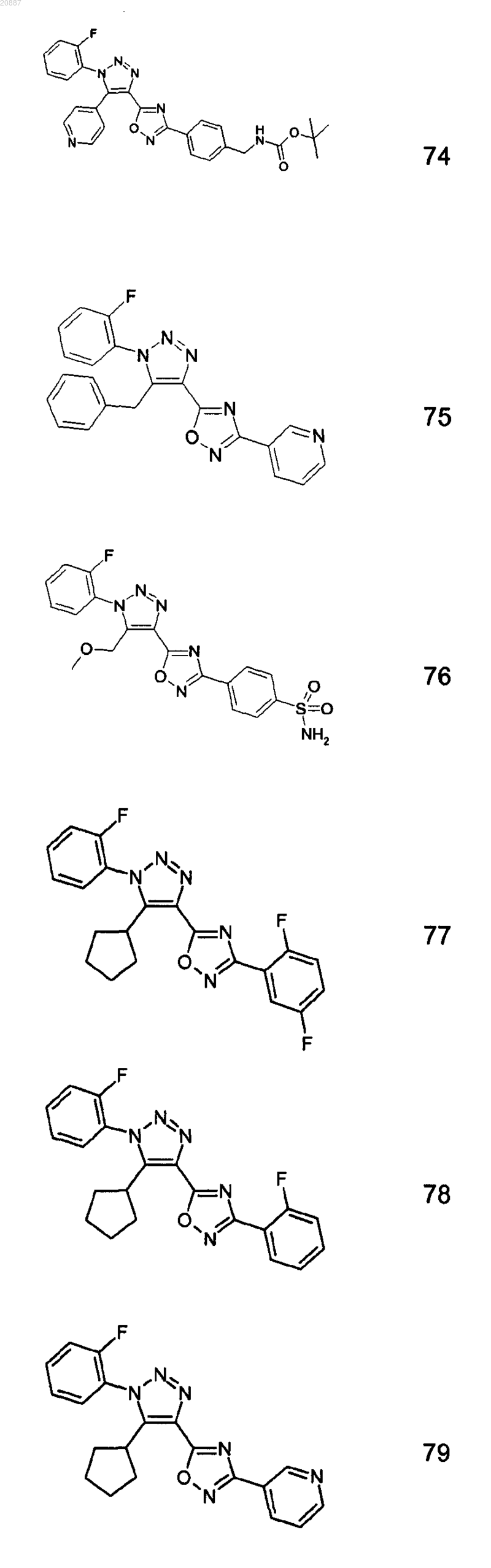
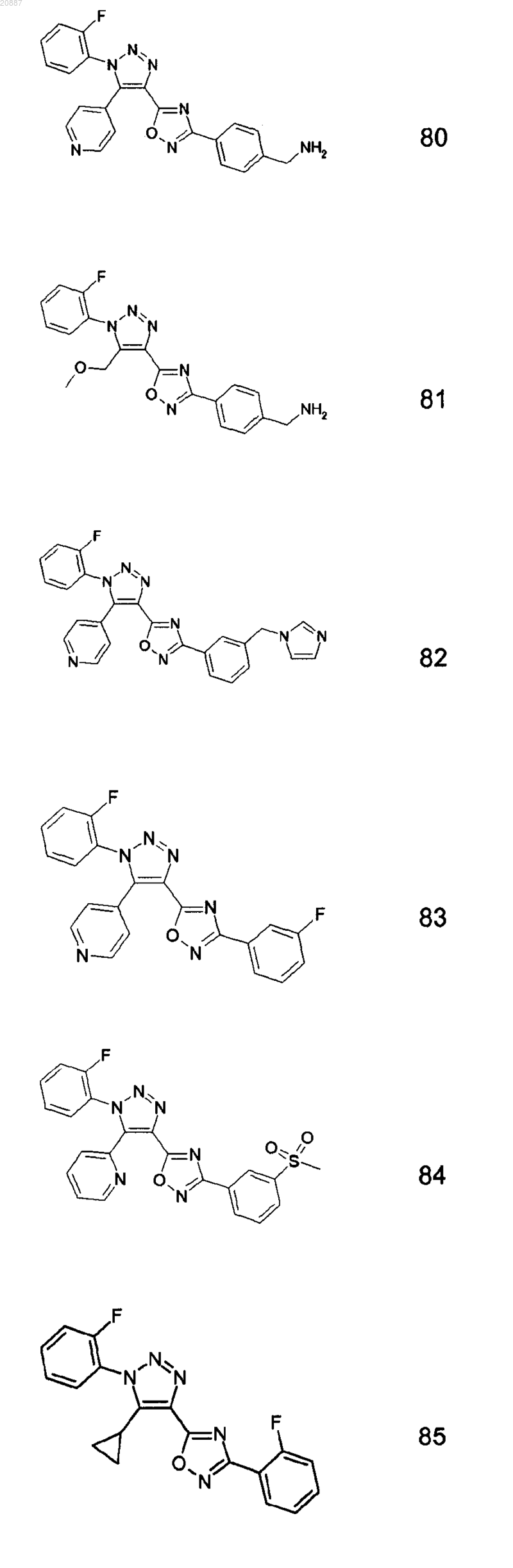
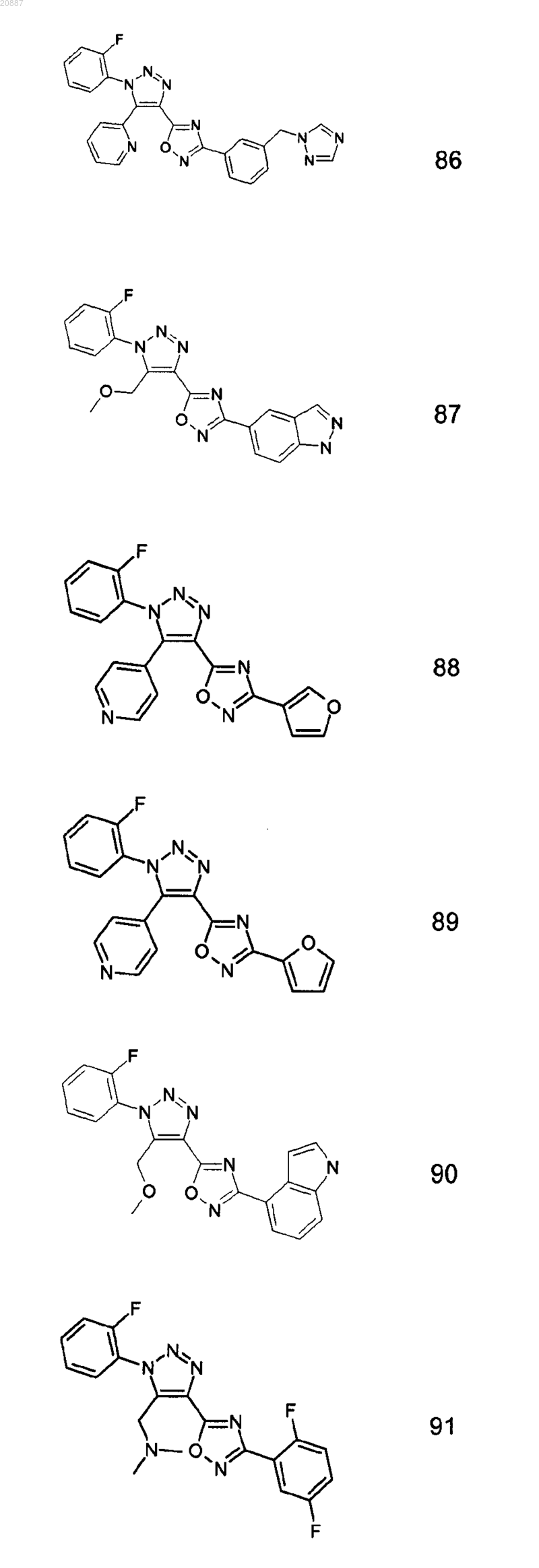
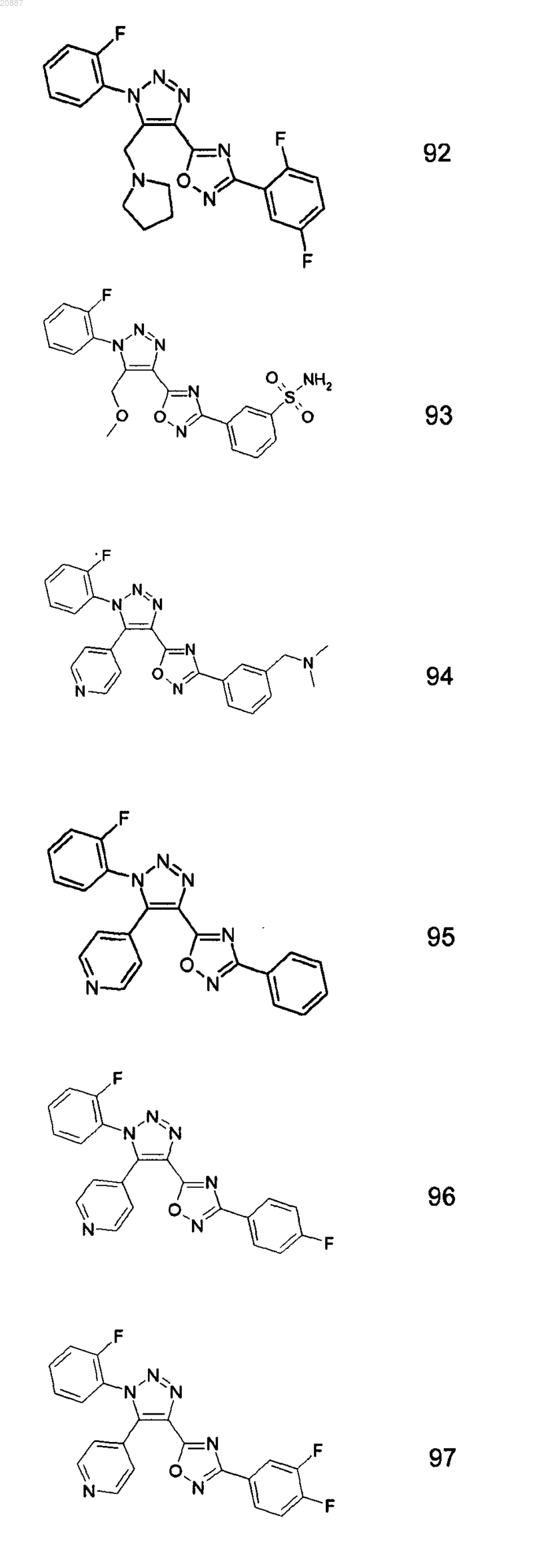
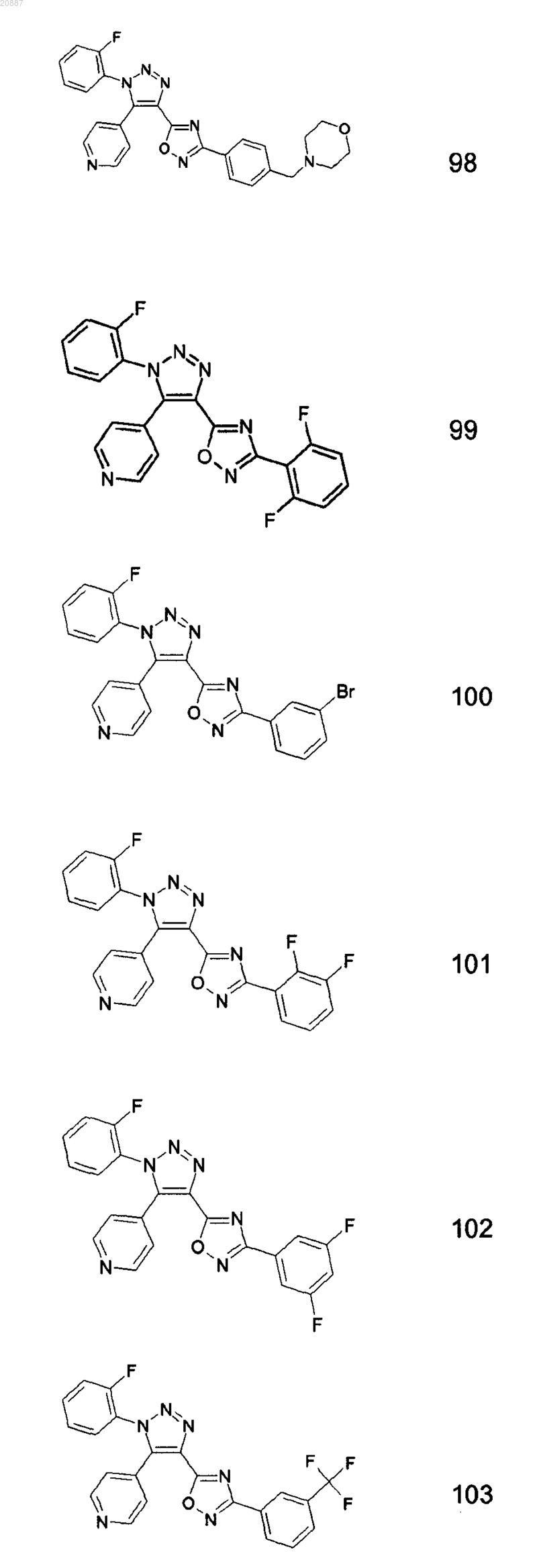
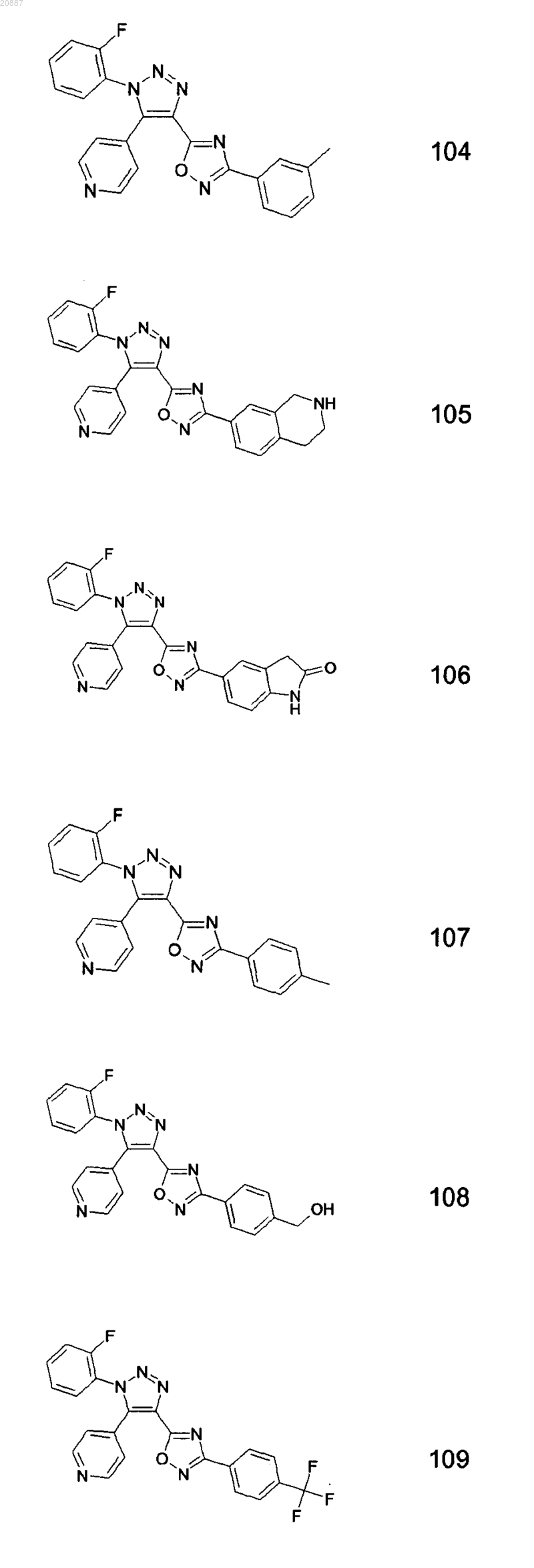
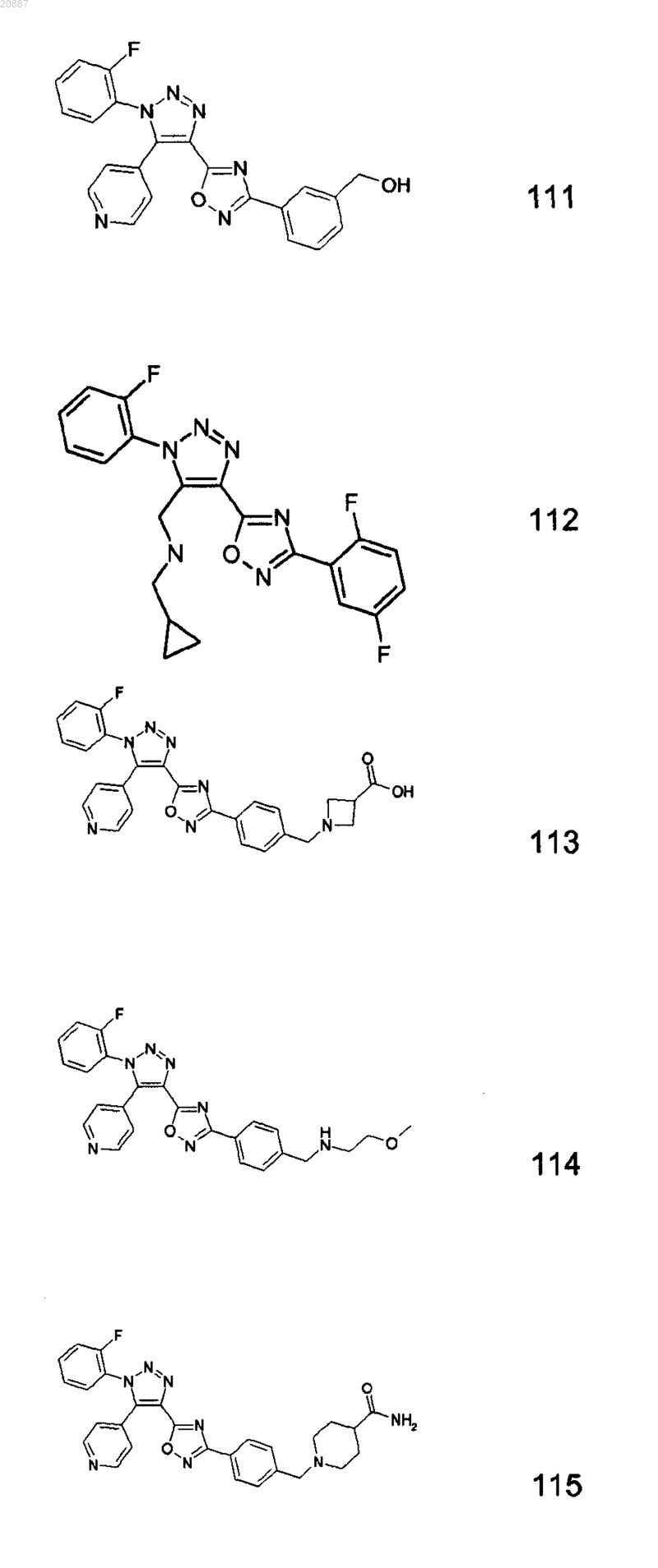
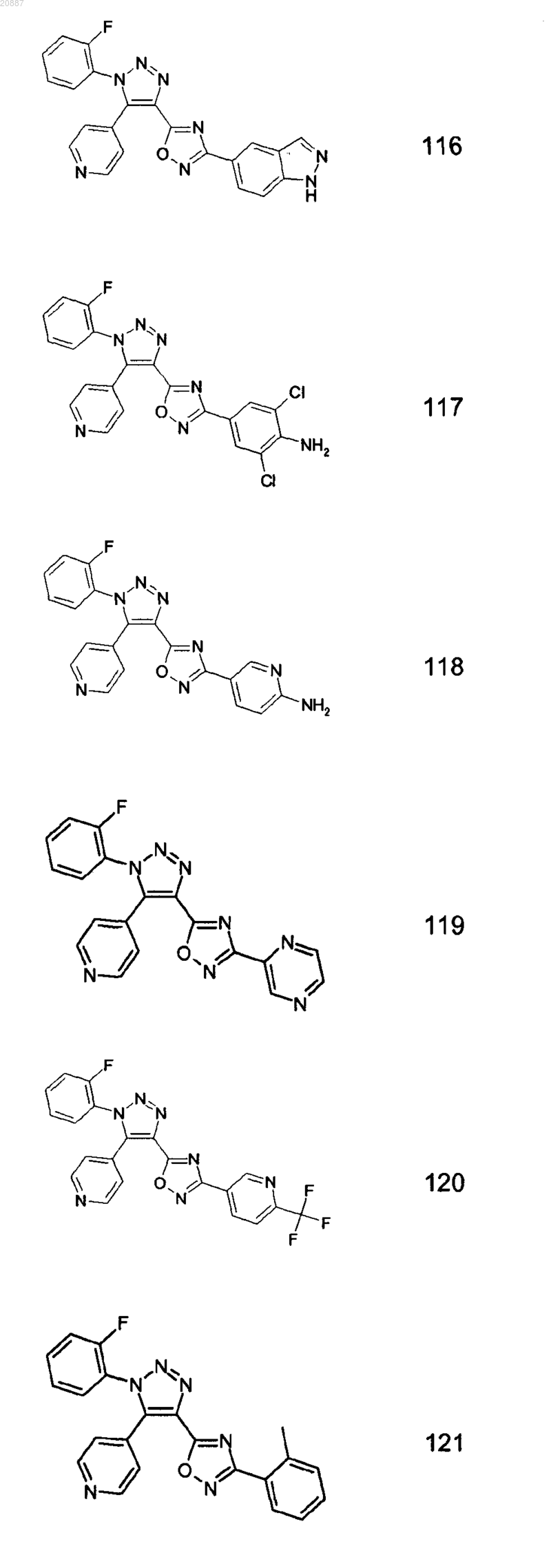
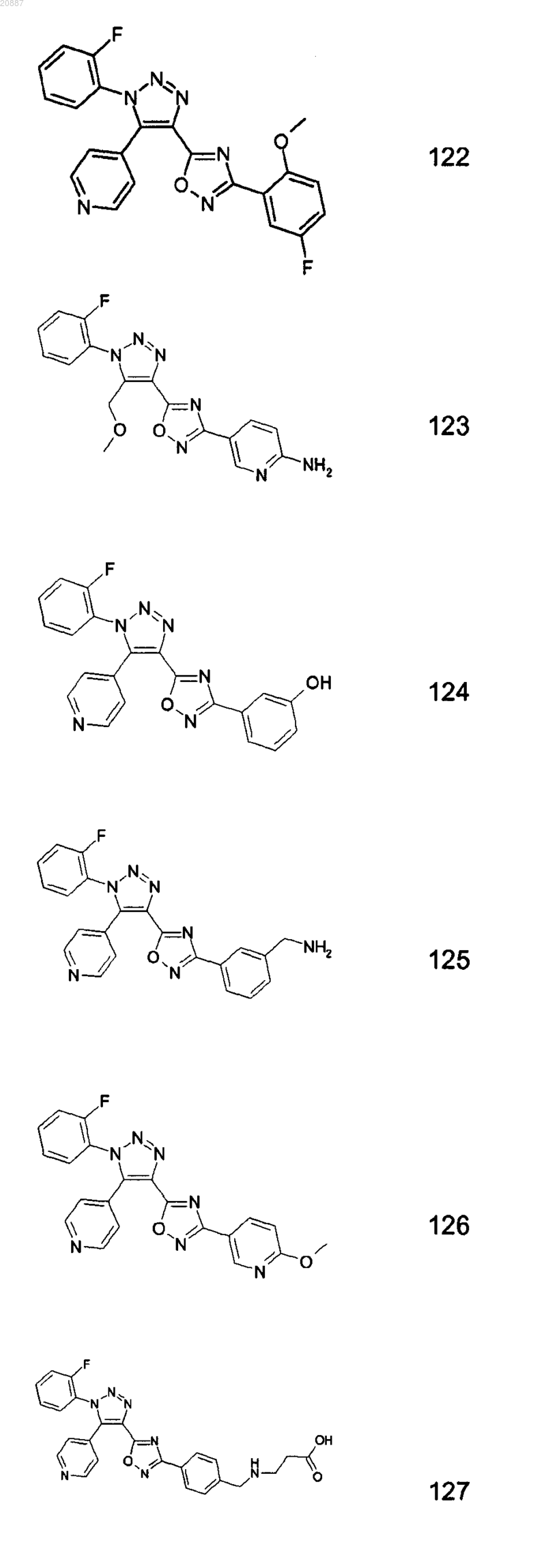
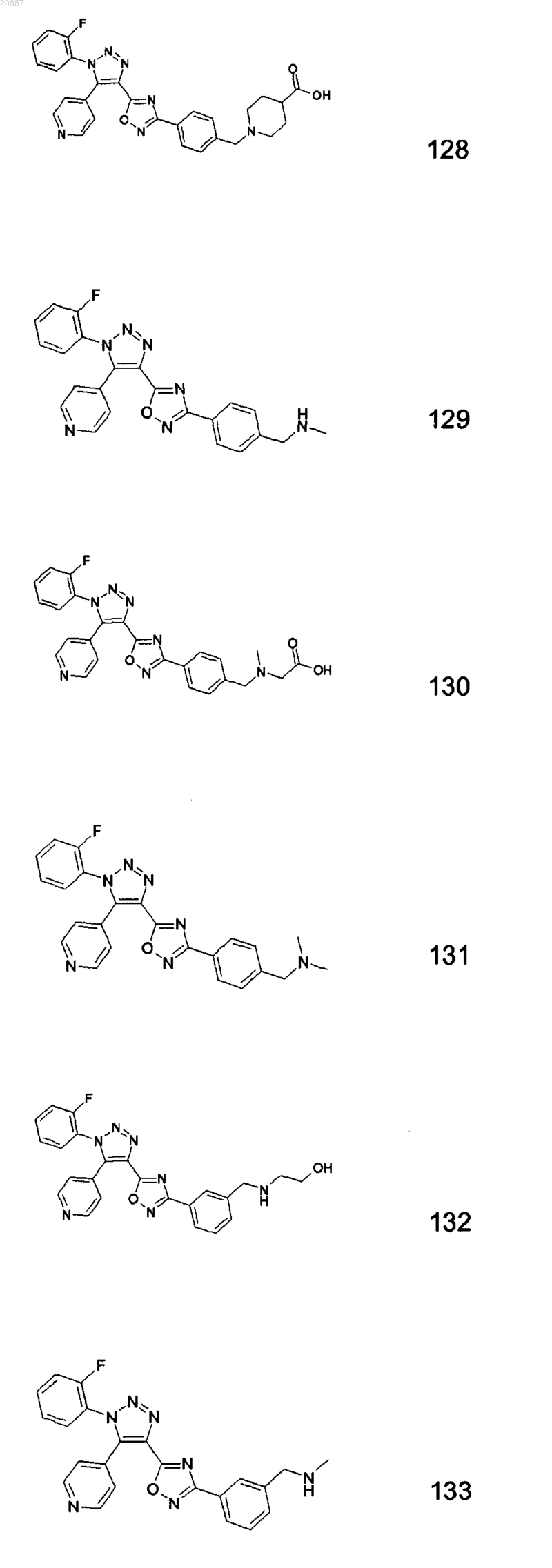
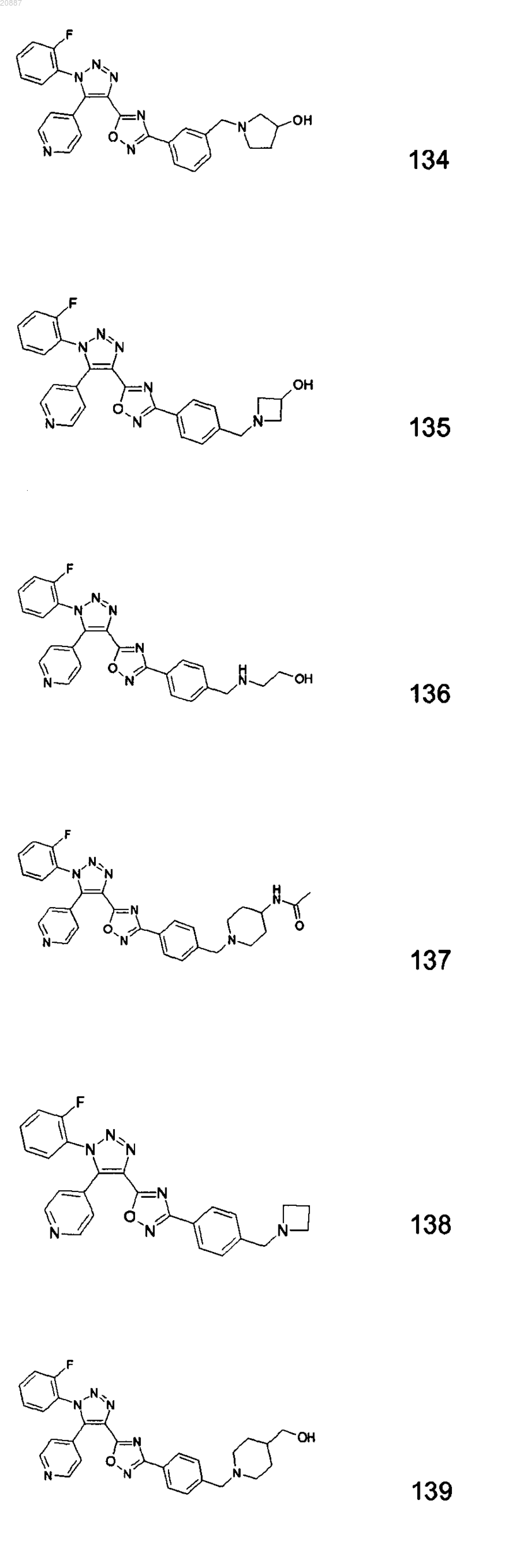
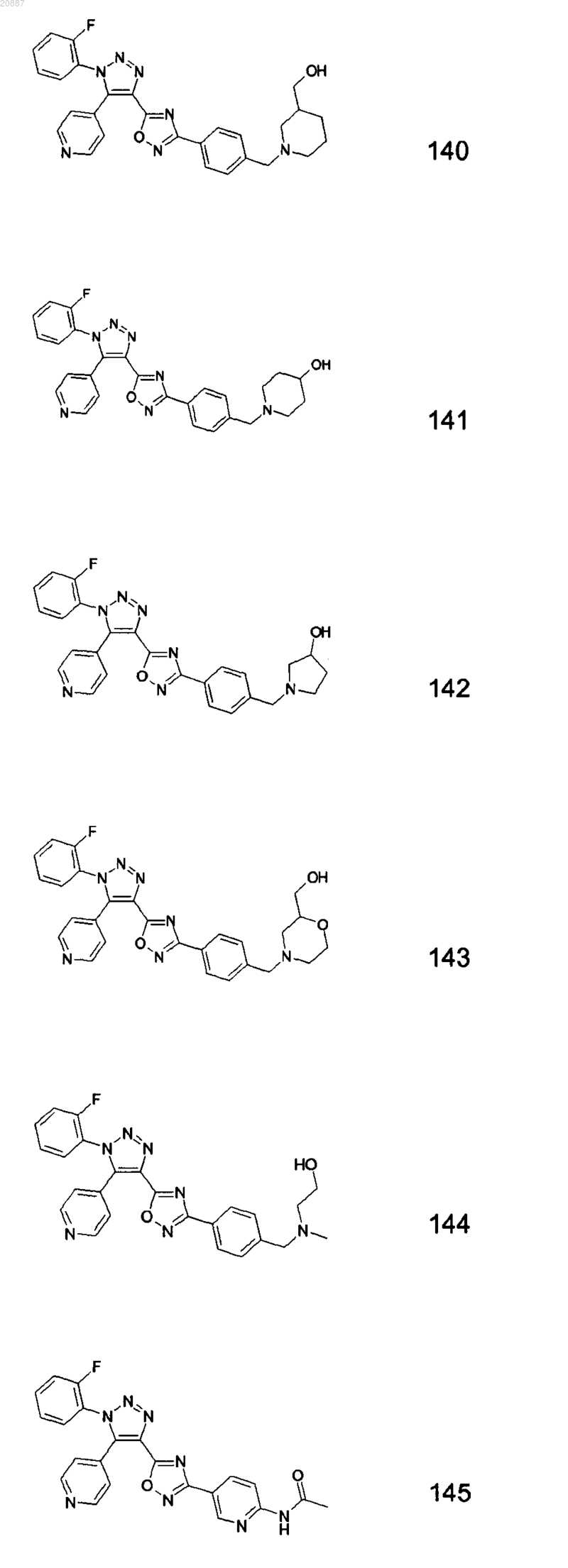
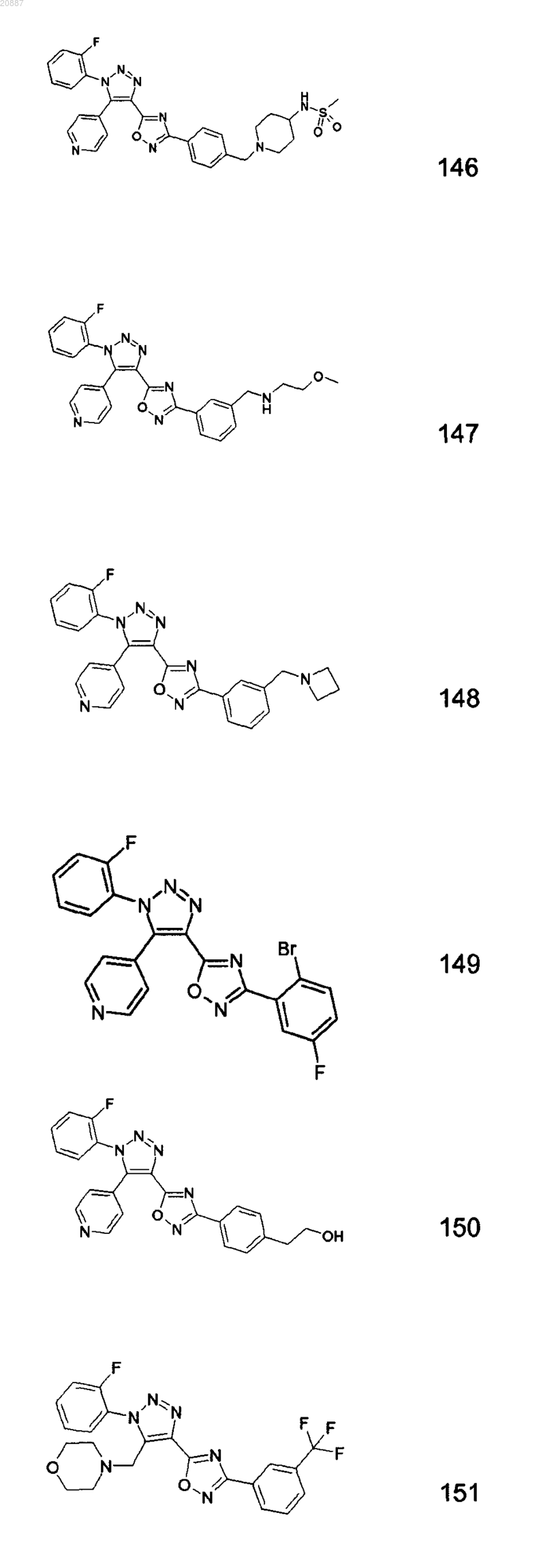
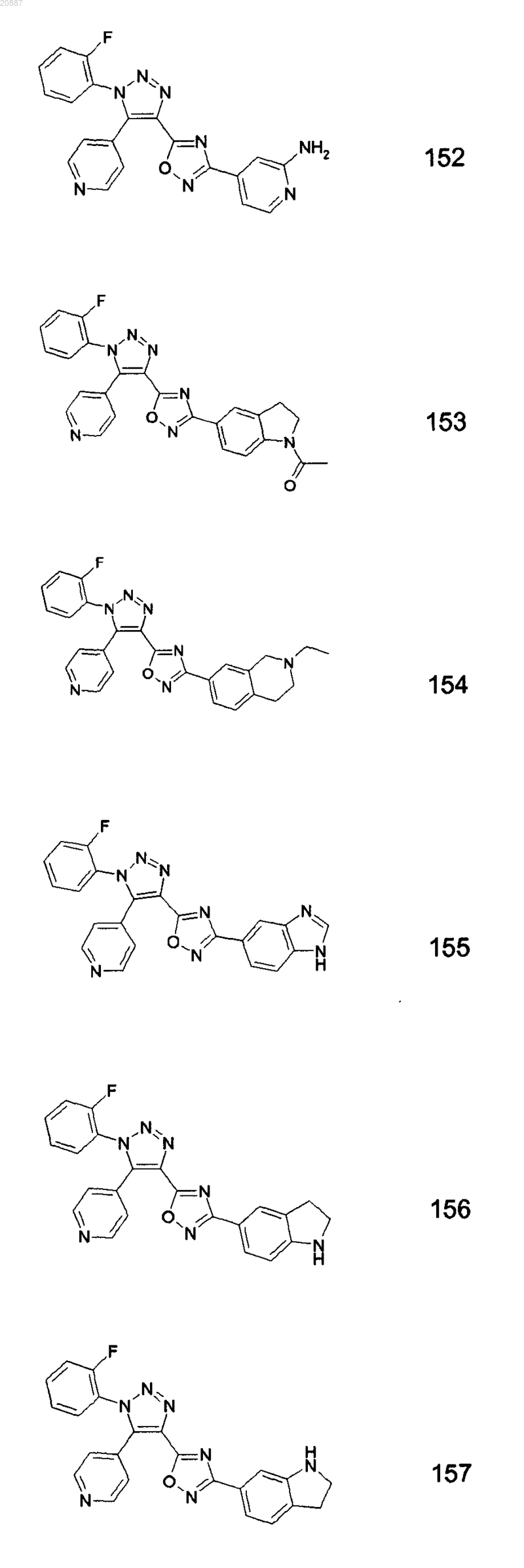
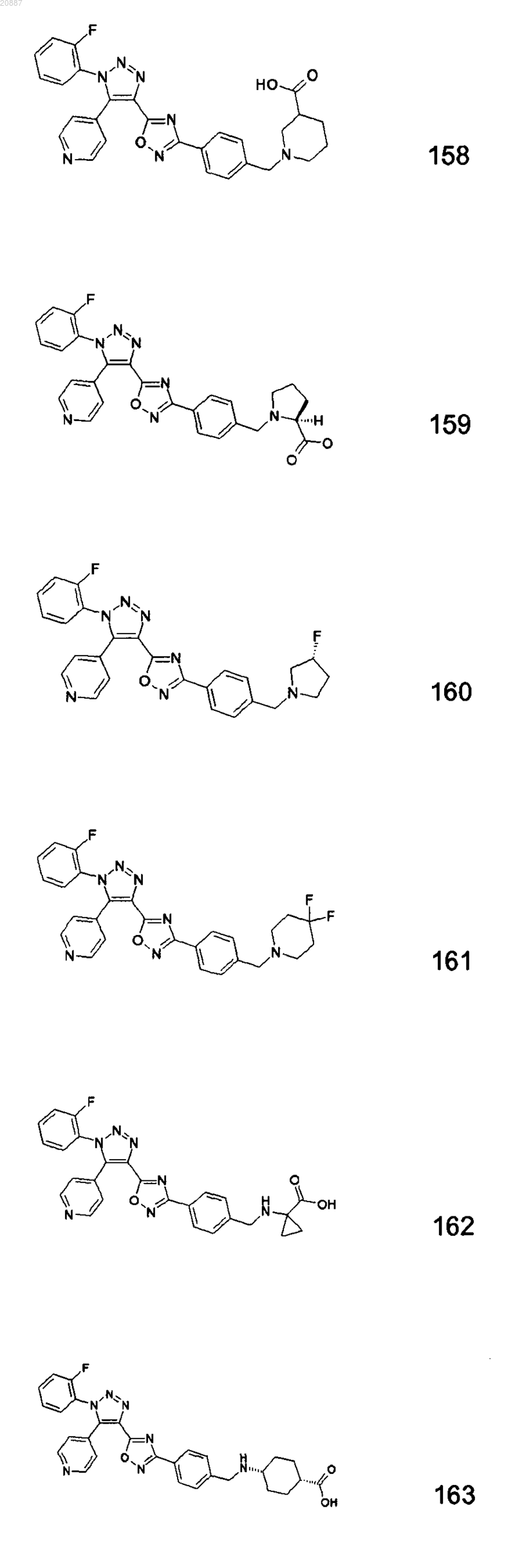
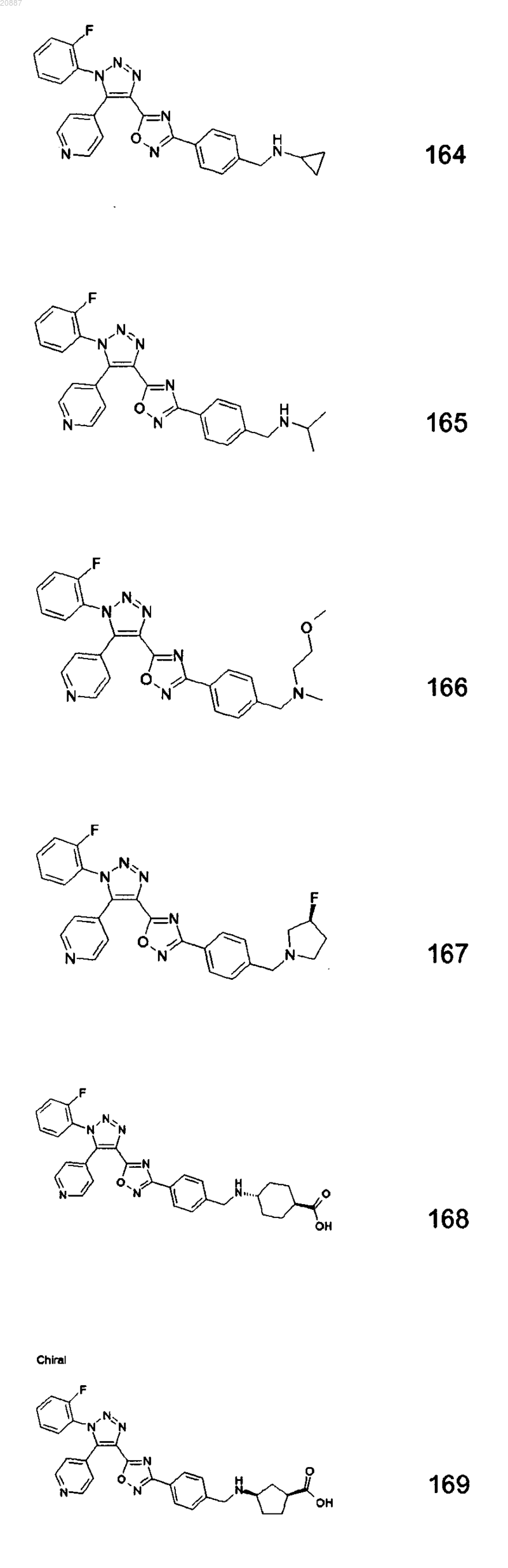
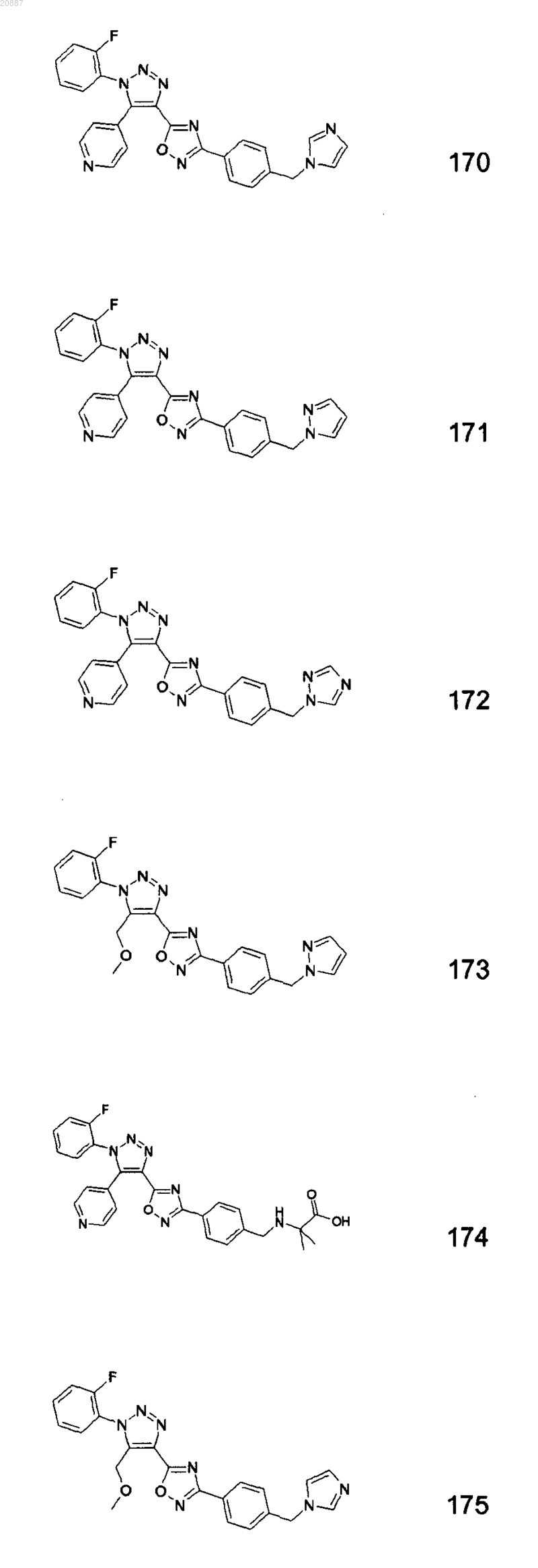
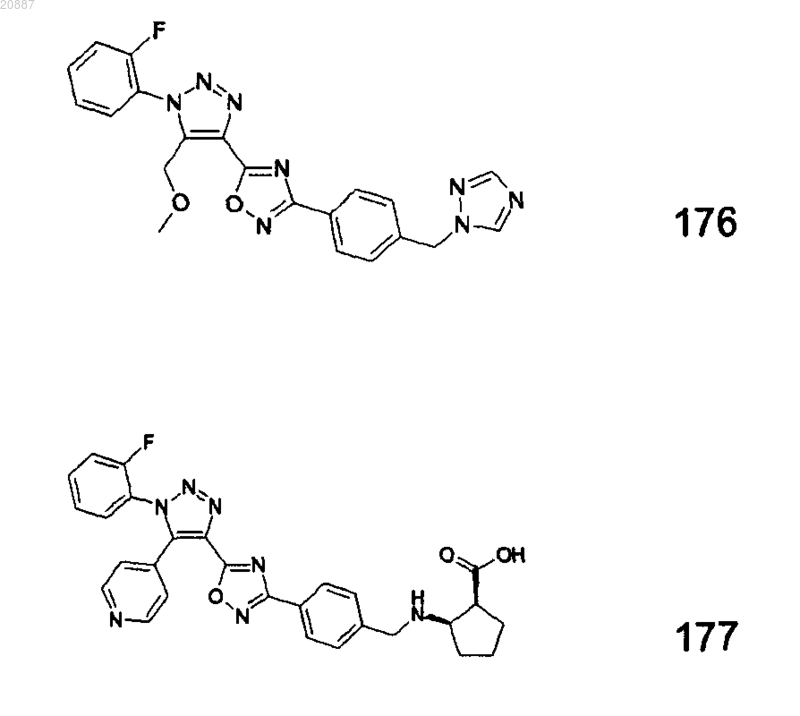
и их фармацевтически приемлемые производные, сольваты, таутомеры, соли и стереоизомеры, включая их смеси во всех отношениях.
6. Фармацевтическая композиция, содержащая по меньшей мере одно соединение по любому из пп.1-5 и/или его фармацевтически пригодные производные, таутомеры, соли, сольваты и стереоизомеры, включая их смеси во всех отношениях, и наполнители и/или адъюванты.
7. Применение соединений формулы I по любому из пп.1-5 и их фармацевтически приемлемых производных, таутомеров, солей, сольватов и стереоизомеров, включая их смеси во всех отношениях, в качестве лекарственного средства для лечения и/или профилактики нарушения, ассоциированного с сфингозин-1-фосфатом.
8. Применение соединений формулы I по любому из пп.1-5 и их фармацевтически пригодных производных, таутомеров, солей, сольватов и стереоизомеров, включая их смеси во всех отношениях, для получения лекарственного средства для лечения и/или профилактики нарушения, ассоциированного с сфингозин-1-фосфатом.
9. Применение соединений формулы I по любому из пп.1-5 и их фармацевтически пригодных производных, солей, таутомеров, сольватов и стереоизомеров, включая их смеси во всех отношениях, для получения лекарственного средства для лечения и/или профилактики иммунорегуляторного нарушения.
10. Применение по п.9, где иммунорегуляторным нарушением является аутоиммунное или хроническое заболевание, выбранное из группы, состоящей из системной красной волчанки, хронического ревматоидного артрита, сахарного диабета типа I, воспалительного заболевания кишечника, цирроза печени, увеита, рассеянного склероза, бокового амиотрофического склероза (ALS), болезни Крона, язвенного колита, буллезного пемфигоида, саркоидоза, псориаза, аутоиммунного миозита, гранулематоза Вегенера, ихтиоза, офтальмопатии Грейвса, астмы, отторжения трансплантата костного мозга или органа или реакции трансплантат против хозяина.
11. Способ получения соединений формулы I по любому из пп.1-5, включающий взаимодействие соединений формулы II
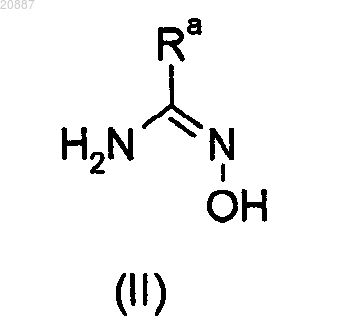
где Ra является таким, как определено в п.1, с соединениями формулы III или формулы V
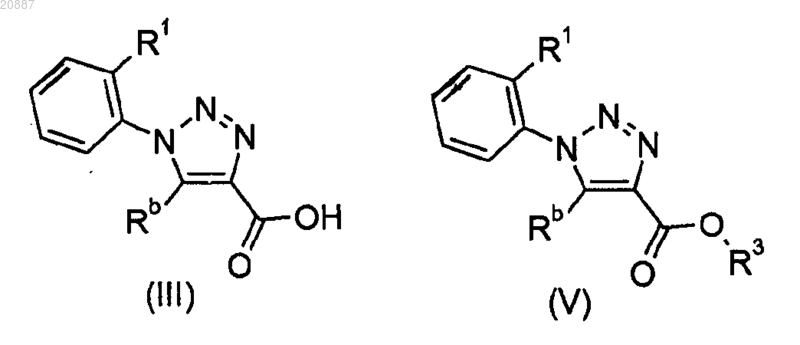
где Rb, R1, R3 являются такими, как определено в п.1, в присутствии или отсутствие основания и связывающего агента, в подходящем растворителе, при повышенной температуре с возможным использованием микроволнового излучения, с получением соединения формулы I
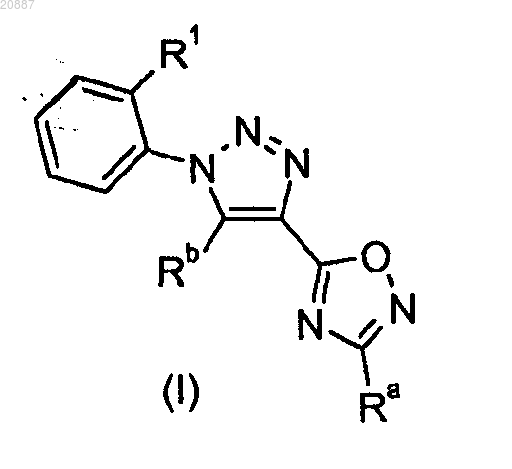
где Ra, Rb, R1 являются такими, как определено в п.1.
12. Способ по п.11, где растворитель выбирают из полярного или неполярного растворителя, выбранного из ацетонитрила, ТГФ, ДМФ, дихлорметана, толуола или их смеси.
13. Соединения формулы I по любому из пп.1-5, проявляющие величину ЕС50 в анализе связывания GTP S с рецептором S1P1, составляющую менее чем приблизительно 5 мкМ.
Текст
где R1, Ra, Rb имеют значения, данные в п.1 формулы изобретения. Соединения являются пригодными, например, в лечении аутоиммунных нарушений, таких как рассеянный склероз. Изобретение относится к триазолсодержащим производным оксадиазола, к их применению в качестве лекарственного средства и к их применению для лечения рассеянного склероза и других заболеваний. В частности, изобретение относится к применению соединений формулы IRa означает Ar или Het; при условии, что Ra не является бензо[1,3]диоксолильной группой или фенильной группой, незамещенной или замещенной по меньшей мере одним метилом, F, Cl, ОМе и/илиHal означает F, Cl, Br или I; А означает разветвленный или линейный алкил, содержащий от 1 до 12 С-атомов, где один или более атомов могут быть заменены Hal, OR3, CN, CO2R3, циклоалкилом, содержащим от 3 до 7 атомов углерода в кольце, или N(R3)2, и где одна или более несмежных СН 2-групп могут быть заменены О, NR3 или S и/или -СО-, -NR3CO-, -CONR3-, NR3CO2-, -NR3CONR3-, -CH=CH-, -СС-группами или или означает циклоалкил или циклоалкилалкилен, содержащий 3-7 кольцевых С-атомов;Ar означает моноциклическое или бициклическое ароматическое карбоциклическое кольцо, имеющее от 6 до 14 атомов углерода, которые могут быть незамещенными или монозамещенными, дизамещенными или тризамещенными заместителем, выбранным из R4;Ar-алкил означает арильную группу, связанную с остальной частью молекулы через C1-C12 алкиленовую цепь;Het означает моноциклическое или бициклическое, насыщенное, ненасыщенное или ароматическое гетероциклическое кольцо, содержащее от 1 до 4 атомов N, О и/или S, которые могут быть незамещенными или монозамещенными, дизамещенными или тризамещенными заместителем, выбранным из R4; и где одна или более СН 2-группы могут быть заменены -СО-;Het-алкил означает группу Het, связанную с остальной частью молекулы через C1-C12 алкиленовую цепь;R4 выбирают из A, Hal, гидрокси, алкокси, карбокси, карбоксиалкила, перфторалкила, перфторалкокси, ацила, алкилсульфонила, сульфонила, -SO2R3, циано, нитро, амино, амидо, алкила, необязательно замещенного карбокси, -N(R3)2, -CO(NR3)2, -OR3, (NR3)COR3, -CO2R3, -COR3, или Ar-алкила или Hetалкила, оба необязательно замещены A, Hal, ацилом, алкилсульфонилом, карбокси, -N(R3)2, -CON(R3)2,-OR3, (NR3)COR3, -CO2R3, -COR3, -SO2N(R3)2, -SO2 алкилом, NR3SO2 алкилом,или C1-С 6 алкилом;R3 является Н или C1-C6 алкилом; и их фармацевтически приемлемых производных, сольватов, таутомеров, солей и стереоизомеров,включая их смеси во всех отношениях, в качестве лекарственного средства, особенно для лечения рассеянного склероза и других заболеваний. В частности, изобретение относится к соединениям формулы IRa означает Ar или Het; при условии, что Ra не является бензо[1,3]диоксолильной группой или фенильной группой, незамещенной или замещенной по меньшей мере одним метилом, F, Cl, ОМе и/илиOEt, если Rb является метильной группой; и их фармацевтически приемлемым производным, сольватам, таутомерам, солям и стереоизомерам,включая их смеси во всех отношениях, и к их применению для лечения рассеянного склероза и других заболеваний. Соединения формулы I и родственных формул предпочтительно связываются с рецепторами сфингозин-1-фосфата (S1P). S1P является биоактивным метаболитом сфинголипидов, который секретируется гематопоэтическими клетками и хранится в активированных тромбоцитах и высвобождается из них. Он действует как агонист семейства рецепторов, сопряженных с G-белком (GPCR). Пять рецепторов сфингозин-1-фосфата было идентифицировано (S1P1, S1P2, S1P3, S1P4 и S1P5, также известные как гены дифференциации эндотелия, которыми являются Edg1, Edg5, Edg3, Edg6 и Edg8, соответственно), которые имеют широкое распространение в клетках и тканях и являются достаточно консервативными у человека и грызунов. Рецептор S1P принимает участие в ряде клеточных функций, таких как выживание, пролиферация и иммунологические реакции. Соединения согласно настоящему изобретению предпочтительно действуют как агонисты рецепторов S1P1/Edg1 и, таким образом, оказывают иммуносупрессивное действие путем модуляции транспорта лейкоцитов, объединения лимфоцитов во вторичных лимфоидных тканях и препятствуя межклеточным взаимодействиям, требуемым для эффективного иммунного ответа. Изобретение также относится к фармацевтическим композициям, содержащим такие соединения, и способам лечения или профилактики. Препарат FTY720 или финголимод, неселективный агонист рецептора S1P1, проявляет иммуносупрессивную активность и демонстрирует терапевтические эффекты в лечении рецидивирующеремитирующего рассеянного склероза. Многочисленные работы уже были опубликованы с использованием данного соединения: Cyster JG Annu Rev. Immunol. 23:127-59, 2005, Rosen H. Nat. Rev. Immunol. 5:560-570, 2005, Rosen H. Trends Immunol. 28:102-107, 2007, Yopp AC Clin. Transplant 20:788-795, 2006,Kappos L. N. Engl. J. Med. 355:1 124-1 140, 2006, Massberg S. N. Engl. J. Med. 355:1088-1089, 2006. Патентные заявки WO 2006/131336 и WO 2004/091502 описывают другие соединения, активные против иммунологических заболеваний и ревматоидного артрита. Иммуносупрессивные средства также используют в широком ряде аутоиммунных и хронических воспалительных заболеваний, включающих системную красную волчанку, хронический ревматоидный артрит, сахарный диабет типа I, воспалительные кишечные заболевания, цирроз печени, увеит и другие расстройства, такие как болезнь Крона, язвенный колит, буллезный пемфигоид, саркоидоз, псориаз, аутоиммунный миозит, гранулематоз Вегенера, ихтиоз, офтальмопатия Грейвса, атонический дерматит и астма. Они также используются как часть химиотерапевтических схем лечения опухолей, лимфом и лейкозов. Было обнаружено, что соединения согласно настоящему изобретению являются селективными агонистами рецептора S1P1 с улучшенными фармакологическими и/или другими свойствами. Таким образом, настоящее изобретение предпочтительно относится к соединениям, которые являются агонистами рецептора S1P1/Edg1, особенно избирательными по сравнению с рецептором S1P3/Edg3. Действие селективного агониста рецепторов S1P1/Edg1 имеет преимущества над современными терапиями и расширяет терапевтическое окно средств, изолирующих лимфоциты, позволяя лучше переносить более высокую дозу и, таким образом, повышая эффективность. Изобретение также относится к получению лекарственного средства для улучшения сосудистой функции, используемого самого по себе или в комбинации с другими активными соединениями или терапиями. Изобретение также относится к применению соединений формулы I в комбинации с иммуномодулирующими средствами, например, финголимодом; циклоспоринами, рапамицинами или аскомицинами или их иммуносупрессивными аналогами, например, циклоспорином А, циклоспорином G, FK-506, ABT281, ASM981, рапамицином, 40-О-(2-гидрокси)этилрапамицином и т.д.; кортикостероидами; циклофосфамидом; азатиопреном; метотрексатом; лефлуномидом; мизорибином; микофенолокислотой; мофетила микофенолатом; 15-дезоксиспергуалином; валератом дифлукортолона; дифлупреднатом; дипропионатом алклометазона; амцинонидом; амсакрином; аспарагиназой; азатиоприном; базиликсимабом; дипропионатом беклометазона; бетаметазоном; ацетатом бетаметазона; дипропионатом бетаметазона; натрийфосфатом бетаметазона; валератом бетаметазона; будесонидом; каптоприлом; хлоргидратом хлорметина; кладрибином; пропионатом клобетазола; ацетатом кортизона; кортивазолом; циклофосфамидом; цитарабином; даклизумабом; дактиномицином; дезонидом; дезоксиметазоном; дексаметазоном; ацетатом дексаметазона; изоникотинатом дексаметазона; натрий-метасульфобензоатом дексаметазона; фосфатом дексаметазона; тебутатом дексаметазона; ацетатом дихлоризона; хлоргидратом доксорубицина; хлоргидратом эпирубицина; ацетонидом флуклоролона; ацетатом флудрокортизона; флудроксикортидом; пивалатом флуметазона; флунизолидом; ацетонидом флуоцинолона; флуоцинонидом; флуокортолоном; гексаноатом флуокортолона; пивалатом флуокортолона; флуорометолоном; ацетатом флупреднидена; пропионатом флутиказона; хлоргидратом гемцитабина; халцинонидом; гидрокортизоном; ацетатом гидрокортизона; бутиратом гидрокортизона, гемисукцинатом гидрокортизона; мелфаланом; мепреднизоном; меркаптопурином; метилпреднизолоном; ацетатом метилпреднизолона; гемисукцинатом метилпреднизолона; мизопростолом; муромонабом-cd3; ацетатом параметазона; преднизолином, преднизолоном; ацетатом преднизолона; капроатом преднизолона; натрийметасульфобензоатом преднизолона; натрийфосфатом преднизолона; преднизоном; преднилиденом; рифампицином; натрия рифампицином; такролимусом; талидомидом; тиотепой; пивалатом тиксокортола; триамцинолоном; гемисукцинатом триамцинолона ацетонида; бенетонидом триамцинолона; диацетатом триамцинолона; гексацетонидом триам-2 020887CD58 или их лигандам; или другими иммуномодулирующими соединениями, например, CTLA41g, или другими ингибиторами адгезионных молекул, например, mAbs или низкомолекулярными ингибиторами,включающими антагонисты селектина и антагонисты VLA-4. Предпочтительной композицией является композиция с циклоспорином A, FK506, рапамицином или 40-(2-гидрокси)этилрапамицином и финголимодом. Триазолсодержащие производные оксадиазола формулы I и родственных формул могут быть получены из легкодоступных исходных материалов, используя следующие общие способы и процедуры. Следует отметить, что где типичные или предпочтительные экспериментальные условия (т.е., температуры реакций, время, моли реагентов, растворители и т.д.) представлены, другие экспериментальные условия также могут быть использованы, если не указано иное. Оптимальные условия реакций могут изменяться в зависимости от отдельных веществ, участвующих в реакциях, и используемых растворителей, но такие условия могут быть установлены специалистом в данной области с использованием обычных способов оптимизации. Следующие сокращения соответственно относятся к представленным ниже определениям:(этилацетат), Et2O (диэтиловый эфир), EtOH (этанол), FMOC (фторенилметилоксикарбонил), HATU (диметиламино-([1,2,3]триазоло[4,5-b]пиридин-3-илокси)метилен]диметиламмония гексафторфосфат),HPLC (высокоэффективная жидкостная хроматография, ВЭЖХ), i-PrOH (2-пропанол), K2CO3 (карбонат калия), LC (жидкостная хроматография, ЖХ), MeCN (ацетонитрил), МеОН (метанол), MgSO4 (сульфат магния), MS (масс-спектрометрия, МС), МТВЕ (метил трет-бутиловый эфир), Mtr (4-метокси-2,3,6 триметилбензолсульфонил), MW (микроволновое излучение), NaHCO3 (бикарбонат натрия), NaBH4 (борогидрид натрия), NMM (N-метилморфолин), NMR (ядерный магнитный резонанс, ЯМР), РОА (феноксиацетат), РуВОР (бензотриазол-1-илокситриспирролидинофосфония гексафторфосфат), RT (комнатная температура, кт), Rt (время удерживания), SPE (твердофазная экстракция), TBTU (2-(1-Нбензотриазол-1-ил)-1,1,3,3-тетраметилурония тетрафторборат), TEA (триэтиламин), TFA (трифторуксусная кислота, ТФУ), THF (тетрагидрофуран, ТГФ), TLC (тонкослойная хроматография, ТСХ), UV (ультрафиолет, УФ). Сокращения, употребляемые в спектрах ЯМР: quint, quintet - квинтет; sext - секстет; minus - минус. Соединения согласно изобретению названы согласно стандартам, используемым в программе"ACD/Name Batch" из Advanced Chemistry Development Inc., ACD/Labs (7.00 Release). Версия программного изделия: 7.10, полная сборка программы: 15 сентября 2003. В зависимости от природы X, Ra, Rb, R1 и R2, различные стратегии синтеза могут быть выбраны для получения соединений формулы I и родственных формул. В способе, иллюстрированном на следующих схемах, Ra, Rb, R1 и R2 являются такими, как определено выше в описании. Соединения формулы I, где группа X определена как О или S, могут быть получены аналогичным способом. В целом, производные оксадиазола, содержащие триазол, формулы I и родственных формул согласно настоящему изобретению могут быть получены из легкодоступных исходных материалов. Если таковые исходные материалы не являются коммерчески доступными, они могут быть получены стандартными способами синтеза. Следующие способы и процедуры, приведенные в описании ниже в примерах, могут быть использованы для получения соединений формулы I и родственных формул. Способ получения соединений формулы I и родственных формул, где X, Ra, Rb, R1 и R2 являются такими, как определено выше и как обозначено на схеме 1, является целью изобретения. Схема 1 Более предпочтительно, соединения формулы I и родственных формул могут быть получены 2 стадийным способом, как указано на схеме 1 а: Первая стадия заключается в сочетании амидоксима формулы (II) с карбоновой кислотой формулы(III), где Rb, R1 и R2 являются такими, как определено выше. Общие протоколы для таких реакций сочетания даны ниже в примерах с использованием условий и способов, хорошо известных специалистам в данной области для получения О-замещенных амидоксимов (IV). Стандартные связующие вещества, такие как, но не ограниченные ими, EDC, HATU, TBTU, могут быть использованы, или конденсирующие средства могут быть использованы, в присутствии или отсутствие оснований, таких как пиридин, TEA,DIEA, NMM, в подходящем растворителе, таком как DCM, ACN, ТГФ или ДМФ, при температуре, варьирующей от 20 до 50 С, предпочтительно при комнатной температуре, в течение нескольких часов, например от одного часа до 24 ч. Альтернативно производное карбоновой кислоты (например, ацилхлоридIIIa) можно соединить с амидоксимом (II), используя условия и способы, хорошо известные специалистам в данной области, в присутствии оснований, таких TEA, DIEA, NMM, в подходящем растворителе, таком какMeCN, DCM, ТГФ или ДМФ, при температуре, варьирующей от 20 до 50 С, предпочтительно при комнатной температуре, в течение нескольких часов, например, от одного часа до 24 ч (схема 2). Схема 2 Соответствующая соль (IIIb), такая как, но не ограниченная ею, литиевая, натриевая или калиевая соль карбоновой кислоты (III), может быть альтернативно использована для получения О-замещенных амидоксимов (IV). Соли могут быть активированы изобутилхлорформиатом при низкой температуре,обычно при -40 С, и затем подвергнуты взаимодействию с амидоксимом (II) с получением Озамещенных амидоксимов (IV) (схема 3). Схема 3 Затем, вторая стадия заключается в циклизации и дегидратации О-замещенных амидоксимов (IV) с образованием производных оксадиазола, содержащих триазол, формулы I и родственных формул. Протоколы представлены ниже в примерах, использованы условия и способы, хорошо известные специалистам в данной области для получения оксадиазола, такие как термолиз при температуре, колеблющейся от кт до 150 С, обычно 150 С, с использованием по возможности аппарата для микроволнового нагрева в течение времени, составляющем между 15 мин и 24 ч, предпочтительно в течение 30 мин, в подходящем растворителе, таком как ACN, ТГФ, пиридин, ДМФ или смеси из двух растворителей, такой как пиридин/ACN, в присутствии или отсутствие основания, такого как DIEA, TEA или тетрабутиламмонийфторид. Альтернативно, сложный эфир формулы (V), где Rb, R1, R2 и R3 являются такими, как определено выше в описании, могут быть прямо превращены в соединение формулы I или родственных формул термолизом при температуре, колеблющейся от комнатной температуры до 180 С, обычно 180 С, с использованием по возможности аппарата для микроволнового нагрева в течение времени, составляющем между 15 мин и 24 ч, предпочтительно в течение 30 мин в аппарате для микроволнового нагрева, в подходящем растворителе, таком как ACN, ТГФ, толуол, пиридин, ДМФ или смеси из двух растворителей, такой как пиридин/ACN, в присутствии основания, такого как, но не ограниченного ими, K2CO3 или NaH (схема 4). Схема 4-4 020887 Соединения формулы I и родственных формул, где X, Ra, Rb, R1 и R2 являются такими, как определено выше, могут быть превращены в альтернативные соединения формулы I и родственных формул, гдеX, Ra, Rb, R1 и R2 являются такими, как определено выше, при использовании подходящих способов взаимопревращения, хорошо известных специалисту в данной области. Обычно, когда Ra является бензиловым спиртом, соединение формулы (Ia) может быть также превращено в соединение формулы (Ib), когда Ra является бензиламином, как показано на схеме 5. Оно может быть сначала превращено в соответствующее соединение с мезильными или тозильными группами(Ic), которое затем взаимодействует с амином HN(R3)2 с получением соединений формулы (Ib), где X, Ra,Rb, R1, R2 и R3 являются такими, как определено выше (схема 5). Спирт (Ia) может быть окислен до соответствующего альдегида (Id) при использовании условий, хорошо известных специалистам в данной области, таких как, но не ограниченных ими, условия окисления по Сверну, или при использовании MnO2 в качестве окислительного средства, как показано на схеме 5. Затем, восстановительное аминирование соединений формулы (Id) подходящим амином HN(R3)2 приводит к соединениям формулы (Ib), где Ra является бензиламином, и где X, Rb, R1, R2 и R3 являются такими, как определено выше. Схема 5 Соединения формулы (II), где группа Ra является такой, как определено выше, являются либо коммерчески доступными, либо могут быть получены стандартными способами синтеза, хорошо известными специалистам в данной области. Обычно они могут быть получены по схеме 6 путем добавления гидроксиламина в раствор соответствующего замещенного бензонитрила формулы (VI) в растворителе или смеси растворителей, таком как EtOH, вода, при температуре, колеблющейся от 20 до 50 С, предпочтительно при комнатной температуре в течение нескольких часов, например от одного часа до 24 ч. Схема 6 Способ получения соединений формулы (II), выбранных ниже: метил 4-[амино(гидроксиимино)метил]-2-фторбензоата; метил 4-[амино(гидроксиимино)метил]-3-фторбензоата; метил 3-[амино(гидроксиимино)метил]бензоата; 2-фтор-N-гидроксибензолкарбоксимидамида; 2,6-дифтор-N-гидроксибензолкарбоксимидамида; 2-фтор-N,4-дигидроксибензолкарбоксимидамида; трет-бутил 3-4-[амино(гидроксиимино)метил]-3-метоксифенилпропаноата; трет-бутил 3-4-[амино(гидроксиимино)метил]-3-метилфенилпропаноата;N'-гидрокси-1 Н-бензимидазол-5-карбоксимидамида; трет-бутил 4-[(гидроксиамино)(имино)метил]-1-пиперидинкарбоксилата; трет-бутил 3-[амино(гидроксиимино)метил]бензилкарбамата; более подробно описан в примерах. Соединения формулы (VI), где группа Ra является такой, как определено выше, являются либо коммерчески доступными, либо они могут быть получены стандартными способами синтеза, хорошо известными специалистам в данной области. Соединения формулы (III), где Rb, R1 и R2 являются такими, как определено выше, являются либо коммерчески доступными, либо они могут быть получены стандартными способами синтеза, хорошо известными специалистам в данной области. Обработка производного азида формулы (VII), где R1 и R2 являются такими, как определено выше, замещенным алкилацетоацетатом (VIII), где Rb и R3 являются такими, как определено выше, дает возможность функционализировать [1,2,3]-триазол формулы (V). Указанное превращение происходит в присутствии основания, такого как, но неограниченного им, DBU,TEA, K2CO3, EtONa или MeONa, в подходящем растворителе, таком как ДМФ, ТГФ, метанол или этанол,при температуре, колеблющейся от 0 до 100 С, предпочтительно при 70 С, в течение нескольких часов,например от одного часа до 24 ч (схема 7). Схема 7 Способ получения соединений формулы (V), выбранных ниже: этил 1-(2-фторфенил)-5-пиридин-4 ил-1 Н-1,2,3-триазол-4-карбоксилата, более подробно описан в примерах.[1,2,3]-Триазол формулы (V) можно подвергать омылению с образованием карбоновой кислоты формулы (III) при использовании условий, хорошо известных специалистам в данной области, таких как,но не ограниченных ими, использование гидроксида металла, например, гидроксида лития, гидроксида натрия или гидроксида калия, в подходящем растворителе, таком как ТГФ, метанол, этанол или вода или в их смесях, при температуре, колеблющейся от 20 до 50 С, предпочтительно при комнатной температуре в течение нескольких часов, например от одного часа до 24 ч. Способ получения соединений формулы (III), выбранных ниже: 1-(2-фторфенил)-5-метил-1 Н-1,2,3-триазол-4-карбоновой кислоты; 5-этил-1-(2-фторфенил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-(метоксиметил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 5-бутил-1-(2-фторфенил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 5-фенил-1-(2-фторфенил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-пиридин-3-ил-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-пиридин-2-ил-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-пиридин-4-ил-1 Н-1,2,3-триазол-4-карбоновой кислоты; этил 1-(2-фторфенил)-5-пиридин-4-ил-1 Н-1,2,3-триазол-4-карбоксилата; 1-(2-фторфенил)-5-(2-метоксиэтил)-1 Н-1, 2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-(морфолин-4-илметил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 5-циклопентил-1-(2-фторфенил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 5-циклопропил-1-(2-фторфенил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-(тетрагидрофуран-2-ил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 5-бензил-1-(2-фторфенил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-(тетрагидро-2 Н-пиран-4-ил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; 1-(2-фторфенил)-5-изопропил-1 Н-1,2,3-триазол-4-карбоновой кислоты; этил 1-(2-фторфенил)-5-(морфолинометил)-1 Н-1,2,3-триазол-4-карбоксилата; этил 1-(2-фторфенил)-5-пиридин-2-ил-1 Н-1,2,3-триазол-4-карбоксилата; более подробно описан в примерах. Соединения формулы (VIII), где R3 и Rb являются такими, как определено выше, являются либо коммерчески доступными, либо могут быть получены стандартными способами синтеза, хорошо известными специалистам в данной области. Соединения формулы (V), где Rb, R1, R2 и R3 являются такими, как определено выше, могут быть превращены в альтернативные соединения формулы (V), где Rb, R1, R2 и R3 являются такими, как определено выше, при использовании подходящих способов взаимопревращения, хорошо известных специалисту в данной области. Например, [1,2,3]-триазол формулы (Va), где Rb означает Me, может быть подвергнут галогенированию с образованием [1,2,3]-триазола формулы (Vb), где группа Hal является такой, как определено выше, который может быть также превращен путем добавления аминов или спиртов в[1,2,3]-триазол формулы (Vc) или (Vd), соответственно, где группа А является такой, как определено выше, как указано на схеме 8, следуя протоколу, L'Abbe, G. et al Tetrahedron 1988, 44, 461. Схема 8 Альтернативно, [1,2,3]-триазол формулы (Vc) и (Vd) может быть прямо получен путем обработки азида (VII) галогенированным ацетоацетатом (VIII), таким как метил 4-хлорацетацетат, в присутствии амина или спирта. Реакцию можно осуществлять в растворителе, таком как ДМФ или ACN, или в выбранном амине или спирте, A2NH или АОН, соответственно, при температуре, колеблющейся от кт до 100 С, предпочтительно при 50 С, в течение нескольких часов, например, от одного часа до 24 ч (схема 9). [1,2,3]-Триазол формулы (Vc) или (Vd) может быть подвергнут омылению с образованием карбоновой кислоты формулы (IIIa) или (IIIb) при использовании условий, хорошо известных специалистам в данной области, таких как, но не ограниченных, одним условием, описанным в примерах ниже. Схема 9 Способ получения соединения формулы (IIIa), выбранного ниже: 1-(2-фторфенил)-5-(морфолин-4-илметил)-1 Н-1,2,3-триазол-4-карбоновой кислоты; этил 1-(2-фторфенил)-5-(морфолинометил)-1 Н-1,2,3-триазол-4-карбоксилата; более подробно описан в примерах. Альтернативно, [1,2,3]-триазол формулы (Ve), где R1, R2 и R3 являются такими, как определено выше, и Rb означает Н, может быть превращен в [1,2,3]-триазол формулы (Vf), где Rb означает ароматический Ar или ароматический Het, как определено выше, и внесен посредством прямого Pdкатализируемого С-5 арилирования, как представлено на схеме 10 и описано в публикации Gevorgyan, V.et al. Org. Lett. 2007, 9, 2333. Различные палладиевые катализаторы могут быть использованы, такие как,но не ограниченные ими, Pd(PPh3)2Cl2, Pd(OAc)2 или Pd2(dba)3CHCl3. Схема 10-7 020887 Азиды формулы (VII), где R1 и R2 являются такими, как определено выше, являются либо коммерчески доступными, либо могут быть получены стандартными способами синтеза, хорошо известными специалистам в данной области. Обычно, амин формулы (IX), где R1 и R2 являются такими, как определено выше, взаимодействует с нитритом натрия в водном растворе HCl при 0 С. Затем, водный раствор азида натрия добавляют, поддерживая температуру при 0 С с получением азидов формулы (VII) (схема 11). Схема 11 Амины формулы (IX), где R1 и R2 являются такими, как определено выше, являются либо коммерчески доступными, либо могут быть получены стандартными способами синтеза, хорошо известными специалистам в данной области. Если описанные выше общие способы синтеза не применимы для получения соединений формулы I и родственных формул, подходящие способы получения, известные специалисту в данной области,должны быть использованы. Фармацевтически приемлемые катионные соли соединений согласно настоящему изобретению легко получают путем взаимодействия кислотной формы с соответствующим основанием, обычно одним эквивалентом, в сорастворителе. Типичными основаниями являются гидроксид натрия, метилат натрия,этилат натрия, гидрид натрия, гидроксид калия, метилат калия, гидроксид магния, гидроксид кальция,бензатин, холин, диэтаноламин, этилендиамин, меглумин, бенэтамин, диэтиламин, пиперазин и трометамин. Соль выделяют концентрированием досуха или путем добавления осадителя. В некоторых случаях,соли могут быть получены при смешивании раствора кислоты с раствором катиона (этилгексаноат натрия, олеат магния), используя растворитель, в котором желаемая катионная соль осаждается, или могут быть иначе выделены путем концентрирования и добавления осадителя. Согласно другому общему способу, соединения формулы I и родственных формул (II), (III) и (V) могут быть превращены в альтернативные соединения формулы I и родственных формул (II), (III) и (V) при использовании подходящих способов взаимопревращения, хорошо известных специалисту в данной области. В целом пути синтеза любого отдельного соединения формулы I и родственных формул будет зависеть от специфических заместителей каждой молекулы и от степени доступности необходимых промежуточных соединений; в свою очередь, такие факторы смогут определить специалисты в данной области. Относительно всех способов защиты и снятия защиты, смотреть публикации Philip J. Kocienski, inM. Wuts in "Protective Groups in Organic Synthesis", Wiley Interscience, 3rd Edition 1999. Соединения согласно настоящему изобретению могут быть выделены в ассоциации с молекулами растворителя путем кристаллизации при упаривании соответствующего растворителя. Фармацевтически приемлемые аддитивные соли кислоты соединений формулы I и родственных формул, содержащие основный центр, могут быть получены обычным способом. Например, раствор свободного основания может быть обработан подходящей кислотой, либо неразведенной, либо в подходящем растворе, и образовавшуюся соль выделяют или фильтрацией, или упариванием в вакууме растворителя, используемого в реакции. Фармацевтически приемлемые аддитивные соли основания могут быть получены аналогичным способом путем обработки раствора соединения формулы (I), содержащего кислотный центр, подходящим основанием. Оба типа солей могут быть образованы или превращены способами с использованием ионообменной смолы. В зависимости от используемых условий, время реакции обычно составляет между несколькими минутами и 14 днями, и температура реакции составляет приблизительно между -30 и 140 С, обычно между -10 и 90 С, в частности, приблизительно между 0 и 70 С. Соединения формулы I и родственных формул также могут быть получены путем выделения в свободном состоянии соединений формулы I из одного из их функциональных производных обработкой средствами, способствующими сольволизу или гидрогенолизу. Предпочтительными исходными материалами для сольволиза или гидрогенолиза являются средства, которые подходят к формуле I и родственным формулам, но содержат соответствующие защищенные амино и/или гидроксильные группы вместо одной или более свободных амино и/или гидроксильных групп, предпочтительно такие, которые несут аминозащитную группу вместо Н-атома, связанного с Nатомом, в частности, такие, которые несут R'-N-группу, в которой R' означает аминозащитную группу вместо HN-группы, и/или такие, которые несут гидроксилзащитные группы вместо Н-атома гидроксильной группы, например, такие, которые подходят формуле I, но несут -COOR-группу, в которой R означает гидроксилзащитную группу вместо -СООН-группы. Также, для множества идентичных или различных защищенных амино и/или гидроксильных групп,-8 020887 возможно, их присутствие в молекуле исходного материала. Если присутствующие защитные группы отличаются друг от друга, во многих случаях они могут быть избирательно удалены. Термин "аминозащитная группа" известен в общих терминах и относится к группам, которые подходят для защиты (блокировки) аминогруппы от химических реакций, но которые легко удалить после того, как желаемая химическая реакция была осуществлена где-либо еще в молекуле. Типичными такими группами являются, в частности, незамещенные или замещенные ацильные, арильные, аралкоксиметильные или аралкильные группы. Поскольку, аминозащитные группы удаляются после желаемой реакции(или последовательности реакций), их тип и размер не являются критическими; однако, предпочтение оказывается группам, имеющим 1-20, в частности, 1-8 атомов углерода. Термин "ацильная группа" следует понимать в широком смысле в связи с настоящим способом. Он включает ацильные группы, произведенные из алифатических, аралифатических, ароматических или гетероциклических карбоновых кислот или сульфокислот и, в частности, алкоксикарбонильных, арилоксикарбонильных и особенно аралкоксикарбонильных групп. Примерами таких ацильных групп являются алканоил, такой как ацетил, пропионил и бутирил; аралканоил, такой как фенилацетил; ароил, такой как бензоил и толил; арилоксиалканоил, такой как РОА; алкоксикарбонил, такой как метоксикарбонил, этоксикарбонил, 2,2,2-трихлорэтоксикарбонил, ВОС (трет-бутоксикарбонил) и 2-йодэтоксикарбонил; аралкоксикарбонил, такой какCBZ ("карбобензокси"), 4-метоксибензилоксикарбонил и FMOC; и арилсульфонил, такой как Mtr. Предпочтительными аминозащитными группами являются ВОС и Mtr, кроме того, CBZ, Fmoc, бензил и ацетил. Термин "гидроксилзащитная группа" также известен в общих терминах и относится к группам, которые являются подходящими для защиты гидроксильных групп от химических реакций, но которые легко удалить после того, как желаемая химическая реакция была осуществлена где-либо еще в молекуле. Типичными такими группами являются упомянутые выше незамещенные или замещенные арильные,аралкильные или ацильные группы, а также алкильные группы. Природа и размер гидроксилзащитных групп не являются критическими, поскольку они удаляются также после желаемой химической реакции или последовательности реакций; предпочтение отдается группам, имеющим 1-20, в частности, 1-10 атомов углерода. Примерами гидроксилзащитных групп являются, в числе других, бензил, 4-метоксибензил,р-нитробензоил, р-толуолсульфонил, трет-бутил и ацетил, где бензил и трет-бутил являются наиболее предпочтительными. Соединения формулы I и родственных формул высвобождаются в свободном состоянии из их функциональных производных в зависимости от используемой защитной группы, например, при использовании сильных кислот, преимущественно используя ТФУ или хлорную кислоту, но также при использовании других сильных неорганических кислот, таких как хлористо-водородная кислота или серная кислота, сильных органических карбоновых кислот, таких как трихлоруксусная кислота или сульфокислота, такие как бензол- или р-толуолсульфокислота. Присутствие дополнительного инертного растворителя является возможным, но не всегда необходимым. Подходящими инертными растворителями являются предпочтительно органические, например, карбоновые кислоты, такие как уксусная кислота, простые эфиры, такие как тетрагидрофуран или диоксан, амиды, такие как ДМФ, галоидированные углеводороды, такие как дихлорметан, а также спирты, такие как метанол, этанол или изопропанол, и вода. Смеси указанных выше растворителей также являются подходящими. ТФУ предпочтительно используют в избытке без добавления другого растворителя, и хлорную кислоту предпочтительно используют в виде смеси уксусной кислоты и 70% хлорной кислоты в отношении 9:1. Температуры реакции расщепления преимущественно составляют приблизительно между 0 и 50 С, предпочтительно между 15 и 30 С (комнатная температура). Группы ВОС, OBut и Mtr могут, например, предпочтительно отщепляться при использовании ТФУ в дихлорметане или при использовании приблизительно от 3 до 5 н. HCl в диоксане при 15-30 С, и группаFMOC может быть отщеплена при использовании приблизительно от 5 до 50% раствора диметиламина,диэтиламина или пиперидина в ДМФ при 15-30 С. Защитные группы, которые могут быть удалены гидрогенолизом (например, CBZ, бензил или высвобождение амидиногруппы из производного оксадиазола), могут быть отщеплены, например, путем обработки водородом в присутствии катализатора (например, благородного металла, такого как палладий, преимущественно на подложке, такой как уголь). Подходящими растворителями в данном случае являются такие, которые указаны выше, в частности, например, спирты, такие как метанол или этанол, или амиды, такие как ДМФ. Обычно, гидрогенолиз осуществляют при температурах приблизительно между 0 и 100 С и давлениях приблизительно между 1 и 200 бар, предпочтительно при 20-30 С и 1-10 бар. Гидрогенолиз CBZгруппы протекает хорошо, например, при 5-10% Pd/C в метаноле или при использовании формиата аммония (вместо водорода) на Pd/C в смеси метанол/ДМФ при 20-30 С. Примерами подходящих инертных растворителей являются углеводороды, такие как гексан, петролейный эфир, бензол, толуол или ксилол; хлорированные углеводороды, такие как трихлорэтилен, 1,2 дихлорэтан, тетрахлорметан, трифторметилбензол, хлороформ или дихлорметан; спирты, такие как метанол, этанол, изопропанол, н-пропанол, н-бутанол или трет-бутанол; простые эфиры, такие как диэти-9 020887 ловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; простые эфиры этиленгликоля, такие как монометиловый или моноэтиловый эфир этиленгликоля или диметиловый эфир этиленгликоля (диглим); кетоны, такие как ацетон или бутанон; амиды, такие как ацетамид, диметилацетамид, Nметилпирролидон (NMP) или диметилформамид (ДМФ); нитрилы, такие как ацетонитрил; сульфоксиды,такие как диметилсульфоксид (ДМСО); сероуглерод; карбоновые кислоты, такие как муравьиная кислота или уксусная кислота; нитросоединения, такие как нитрометан или нитробензол; сложные эфиры, такие как этилацетат, или смеси указанных выше растворителей. Сложные эфиры могут быть подвергнуты омылению, например, при использовании уксусной кислоты или при использовании LiOH, NaOH или KOH в воде, смеси вода/ТГФ, вода/ТГФ/этанол или вода/диоксан, при температурах между 0 и 100 С. Кроме того, свободные аминогруппы могут быть ацилированы обычным способом при использовании хлорангидрида кислоты или ангидрида кислоты или алкилированы при использовании незамещенных или замещенных галоидалкила или могут взаимодействовать с СН 3-С(=NH)-OEt, предпочтительно в инертном растворителе, таком как дихлорметан или ТГФ, и/или в присутствии основания, такого как триэтиламин или пиридин, при температурах между -60 и +30 С. По всему описанию термин "удаляемая группа" предпочтительно означает Cl, Br, I или реакционноспособную модифицированную OН-группу, такую как, например, активированный сложный эфир,имидазолид или алкилсульфонилокси, имеющий 1-6 атомов углерода (предпочтительно метилсульфонилокси или трифторметилсульфонилокси), или арилсульфонилокси, имеющий 6-10 атомов углерода(предпочтительно фенил- или р-толилсульфонилокси). Радикалы такого типа для активации карбоксильной группы в обычных реакциях ацилирования описаны в литературе (например, в стандартных работах, таких как Houben-Weyl, Methoden der organischen Chemie [Methods of Organic Chemistry] , Georg-Thieme-Verlag, Stuttgart). Активированные сложные эфиры предпочтительно образуются in situ, например, посредством добавления HOBt или N-гидроксисукцинимида. Формула I и родственные формулы также охватывают оптически активные формы (стереоизомеры),энантиомеры, рацематы, диастереомеры и гидраты и сольваты указанных соединений. Термин "сольваты соединений" предназначен означать аддукты молекул инертного растворителя с соединениями, которые образуются благодаря их взаимным силам притяжения. Сольватами являются, например, моно- или дигидраты или алкоголяты. Термин "фармацевтически пригодные производные" предназначен означать, например, соли соединений формулы I и так называемых пролекарств соединений. Термин "производные пролекарств" предназначен означать соединения формулы I, которые были модифицированы, например, алкильными или ацильными группами, сахарами или олигопептидами и которые быстро расщеплялись в организме с образованием активных соединений. Они включают биодеградируемые полимерные производные соединений согласно изобретению,как описано, например, в публикации Int. J. Pharm. 115, 61-67 (1995). Формула I и родственные формулы охватывают смеси соединений формулы I, например, смеси диастереомеров, например, в отношении 1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 или 1:1000. Указанные смеси являются наиболее предпочтительными смесями стереоизомерных соединений. В частности, предпочтительными вариантами формулы I являются соединения формулы IA, IB, IС,ID, IE:- 10020887 где X, R1, R2, Rb, Het, Ar, А являются такими, как определено выше. Предпочтительно R1 выбирают из F или Br и особенно F. Предпочтение отдается соединениям согласно настоящему изобретению, выбранным из следующей группы от 1 до 177: и их фармацевтически пригодным производным, сольватам, солям и их стереоизомерам, включающим их смеси во всех отношениям. Все представленные выше и ниже радикалы, такие как X, R1, R2, R3, R4, R5, Ra, Rb, A, Het, Ar, имеют значение, указанное под формулой I, если не указано иное. В целом соединения формулы I являются тем более предпочтительными, чем более предпочтительные заместители они несут.Rb более предпочтительно означает A, Het или Het-алкил.Rb наиболее предпочтительно означает А, где А является линейным или разветвленным алкилом,содержащим от 1 до 12 С-атомов, где один или более, предпочтительно от 1 до 7 Н-атомов могут быть замещены OR3;Rb наиболее предпочтительно означает Het, где Het является пиридинилом;Rb наиболее предпочтительно означает Het-алкил, где Het является пиперидинилом, морфолино или пиперазинилом. Алкил означает углеродную цепь, содержащую от 1 до 12 атомов углерода, предпочтительно от 1 до 8 атомов углерода и наиболее предпочтительно от 1 до 6 атомов углерода. Алкил наиболее предпочтительно означает метил, также этил, пропил, изопропил, бутил, изобутил, сек-бутил или трет-бутил,кроме того, пентил, 1-, 2- или 3-метилбутил, 1,1-, 1,2- или 2,2-диметилпропил, 1-этилпропил, гексил, 1-,2-, 3- или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2-этилбутил, 1-этил-1 метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил.N(R3)2 также может означать Het. А предпочтительно означает метил, также этил, пропил, изопропил, бутил, изобутил, сек-бутил или трет-бутил, кроме того, пентил, 1-, 2- или 3-метилбутил, 1,1-, 1,2- или 2,2-диметилпропил, 1-этилпропил,гексил, 1-, 2-, 3- или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2-этилбутил, 1 этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил, также предпочтительно,например, трифторметил. А наиболее предпочтительно означает алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов углерода, предпочтительно метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил,трифторметил, пентафторэтил или 1,1,1-трифторэтил. А также означает (СН 2)nO (CH2)nCH3, (СН 2)nO(СН 2)nOR3, (CH2)nNR3(CH2)2N(R3)2, особенно, СН 2-ОСН 3, (СН 2)n-ОСН 3, (CH2)2O(CH2)2OR3, (CH2)nN(R3)2 или (СН 2) 2NH (CH2) 2N (R3)2, где n равно 1, 2, 3 или 4. Циклоалкил предпочтительно означает циклопропил, циклобутил, циклопентил, циклогексил или циклогептил. Циклоалкилалкилен предпочтительно означает циклопропилметилен, циклобутилметилен, циклопентилметилен, циклогексилметилен или циклогептилметилен. Алкилен предпочтительно означает метилен, этилен, пропилен, бутилен, пентилен или гексилен,также разветвленный алкилен. Перфторалкил предпочтительно означает CF3. Перфторалкокси предпочтительно означает OCF3.Hal означает Cl, Br, I, F и предпочтительно F, Br или Cl. Алкокси означает группу -О-(СН 2)n-СН 3, где n равно 0, 1, 2, 3 или 4, предпочтительно метокси или этокси. Карбокси означает группу -СООН. Карбоксиалкил означает сложноэфирную группу, предпочтительно СООМе или COOEt. Алкилсульфонил означает группу -S(О)2-алкил, предпочтительно метилсульфонил или этилсульфонил. Ацил означает группу -C(O)R, где R может быть A, Ar, Het, как определено выше, предпочтительно ацил означает группу ацетил-С(О)СН 3. Амино означает группу -NRR"', где каждая группа R, R"' независимо означает водород или алкил или Ar или Het или А или Het-алкил или Ar-алкил, и где R и R"', вместе с атомом азота, с которым они связаны, могут необязательно образовывать 3-8-членное Het-кольцо. Амидо означает группу -C(O)NRR"', где каждая группа R, R"' независимо означает водород или алкил или Ar или Het или А или Het-алкил или Ar-алкил, и где R и R'", вместе с атомом азота, с которым они связаны, могут необязательно образовывать 3-8-членное Het-кольцо.Ar, дополнительно к указанному выше значению, также может означать насыщенное карбоциклическое кольцо, содержащее от 6 до 14 атомов углерода, которые могут быть незамещенными или монозамещенными, дизамещенными или тризамещенными заместителем, выбранным из R4 и/или R5.Ar предпочтительно означает фенил, который может быть незамещенным или монозамещенным,дизамещенным или тризамещенным заместителем, выбранным из R4 и/или R5.Ar наиболее предпочтительно означает одну из следующих групп: где R4 и R5 являются такими, как определено выше. Более предпочтительно Ar является одной из следующих групп: где R4, R5 являются такими, как определено выше и предпочтительно, где R4 означает Hal, и R5 является Hal или Н. Кроме того, Ar предпочтительно означает незамещенный илиHet предпочтительно означает моноциклическое или бициклическое, насыщенное, ненасыщенное или ароматическое гетероциклическое кольцо, содержащее от 1 до 3 N-атомов, которые могут быть незамещенными или монозамещенными, дизамещенными или тризамещенными заместителем, выбранным из R4 и/или R5; или бициклическим, насыщенным, ненасыщенным или ароматическим гетероциклическим кольцом, содержащим 1 атом кислорода, который может быть незамещенным или монозамещенным, дизамещенным или тризамещенным заместителем, выбранным из R4 и/или R5.Het является предпочтительно 6-14-членной кольцевой системой и означает, не противопоставляя другим заместителям, например, 2- или 3-фурил, 2- или 3-тиенил, 1-, 2- или 3-пирролил, 1-, 2-, 4- или 5 имидазолил, 1-, 3-, 4- или 5-пиразолил, 2-, 4- или 5-оксазолил, 3-, 4- или 5-изоксазолил, 2-, 4- или 5 тиазолил, 3-, 4- или 5-изотиазолил, 2-, 3- или 4-пиридил, 2-, 4-, 5- или 6-пиримидинил, также предпочтительно 1,2,3-триазол-1-, -4- или -5-ил, 1,2,4-триазол-1-, -3- или -5-ил, 1- или 5-тетразолил, 1,2,3 оксадиазол-4- или -5-ил, 1,2,4-оксадиазол-3- или -5-ил, 1,3,4-тиадиазол-2- или -5-ил, 1,2,4-тиадиазол-3 или -5-ил, 1,2,3-тиадиазол-4- или -5-ил, 3- или 4-пиридазинил, пиразинил, 1-, 2-, 3-, 4-, 5-, 6- или 7 индолил, индазолил, 4- или 5-изоиндолил, 1-, 2-, 4- или 5-бензимидазолил, 1-, 3-, 4-, 5-, 6- или 7 бензопиразолил, 2-, 4-, 5-, 6- или 7-бензоксазолил, 3-, 4-, 5-, 6- или 7-бензизоксазолил, 2-, 4-, 5-, 6- или 7 бензотиазолил, 2-, 4-, 5-, 6- или 7-бензизотиазолил, 4-, 5-, 6- или 7-бенз-2,1,3-оксадиазолил, 2-, 3-, 4-, 5-,6-, 7- или 8-хинолил, 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолил, 3-, 4-, 5-, 6-, 7- или 8-циннолинил, 2-, 4-, 5-, 6-,7- или 8-хиназолинил, 5- или 6-хиноксалинил, 2-, 3-, 5-, 6-, 7- или 8-2 Н-бензо-1,4-оксазинил, также предпочтительно 1,3-бензодиоксол-5-ил, 1,4-бензодиоксан-6-ил, 2,1,3-бензотиадиазол-4- или -5-ил или 2,1,3 бензоксадиазол-5-ил. Гетероциклические радикалы также могут быть частично или полностью гидрогенизованными. Таким образом, Het также может означать, например, 2,3-дигидро-2-, -3-, -4- или -5-фурил, 2,5 дигидро-2-, -3-, -4- или -5-фурил, тетрагидро-2- или -3-фурил, 1,3-диоксолан-4-ил, тетрагидро-2- или -3 тиенил, 2,3-дигидро-1-, -2-, -3-, -4- или -5-пирролил, 2,5-дигидро-1-, -2-, -3-, -4- или -5-пирролил, 1-, 2 или 3-пирролидинил, тетрагидро-1-, -2- или -4-имидазолил, 2,3-дигидро-1-, -2-, -3-, -4- или -5-пиразолил,тетрагидро-1-, -3- или -4-пиразолил, 1,4-дигидро-1 -, -2-, -3- или -4-пиридил, 1,2,3,4-тетрагидро-1-, -2-, -3, -4-, -5- или -6-пиридил, 1-, 2-, 3- или 4-пиперидинил, 2-, 3- или 4-морфолинил, тетрагидро-2-, -3- или -4 пиранил, 1,4-диоксанил, 1,3-диоксан-2-, -4- или -5-ил, гексагидро-1-, -3- или -4- пиридазинил, гексагидро-1-, -2-, -4- или -5-пиримидинил, 1-, 2- или 3-пиперазинил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7 или -8-хинолил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или -8-изохинолил, 2-, 3-, 5-, 6-, 7- или 83,4-дигидро-2 Н-бензо-1,4-оксазинил, кроме того, предпочтительно 2,3-метилендиоксифенил, 3,4 метилендиоксифенил, 2,3-этилендиоксифенил, 3,4-этилендиоксифенил, 3,4-(дифторметилендиокси)фенил, 2,3-дигидробензофуран-5- или -6-ил, 2,3-(2-оксометилендиокси)фенил или также 3,4-дигидро-2 Н 1,5-бензодиоксепин-6- или -7-ил, также предпочтительно 2,3-дигидробензофуранил или 2,3-дигидро-2 оксофуранил.Het особенно означает одну из следующих групп: где R3, R4 и R5 являются такими, как определено выше. Предпочтительно группы R4 и R5 каждую независимо выбирают из A, Hal, гидрокси, алкокси, карбокси, карбоксиалкила, перфторалкила, перфторалкокси, ацила, алкилсульфонила, сульфонила,-SO2(R3)2, циано, нитро, амино, амидо, алкила, необязательно замещенного карбокси, -N(R3)2, -CO(NR3)2,-OR3, (NR3)COR3, -CO2R3, -COR3 или Het-алкила, необязательно замещенного A, Hal, ацилом, алкилсульфонилом, карбокси, -N(R3)2, -CON(R3)2, -OR3, (NR3)COR3, -CO2R3, -COR3, -SO2N(R3)2, -SO2 (C1-C6)
МПК / Метки
МПК: A61K 31/4245, C07D 413/14, A61P 37/00, C07D 413/04
Метки: триазолсодержащие, производные, оксадиазола
Код ссылки
<a href="https://eas.patents.su/30-20887-triazolsoderzhashhie-proizvodnye-oksadiazola.html" rel="bookmark" title="База патентов Евразийского Союза">Триазолсодержащие производные оксадиазола</a>
Предыдущий патент: Гуманизированные антитела против tl1a
Следующий патент: Пигментная композиция, способ ее получения и применение
Случайный патент: Замещенные феноксиаминотиазолоны в качестве модуляторов родственного эстрогеновому рецептору рецептора-α