Производные пурина или деазапурина для применения при лечении вирусных инфекций и других заболеваний
Формула / Реферат
1. Соединение формулы I
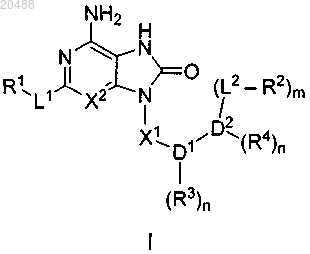
или его фармацевтически приемлемая соль, где
L1 представляет собой -О-;
R1 представляет собой Н, С1-6 алкил, C1-6 гетероалкил или С4-20 гетероциклилалкил, причем каждая гетероалкильная группа содержит 1 или 2 гетероатома, выбранных из О, N, S, и каждая гетероциклоалкильная группа содержит от 1 до 6 гетероатомов, выбранных из О, N, S;
X2 представляет собой N или C-R5;
R5 представляет собой Н, галоген или С1-6 алкил;
X1 представляет собой C1-6 алкилен;
D1 представляет собой фенил, пиридинил или тиазолил;
D2 представляет собой фенил, пиридинил или тиазолил;
каждый L2 независимо представляет собой С1-6 алкилен;
каждый R2 независимо представляет собой -NR6R7;
m равно 1;
каждый R3 и R4 независимо представляет собой галоген, C1-6 галогеналкил, -OR8 или -CN;
каждый n независимо представляет собой 0, 1, 2, 3 или 4 в зависимости от размера изображенного кольца D1 и D2 так, чтобы соответствующие точки присоединения присутствовали для каждого R3 и R4;
каждый из R6 и R7 независимо представляет собой Н или C1-6 алкил; или
R6 и R7, взятые вместе с азотом, к которому они оба присоединены, образуют замещенный или незамещенный 3-8-членный гетероцикл, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р, причем незамещенный гетероцикл замещен С1-6 алкилом; или
R7, взятый вместе с L2, и N, к которому они оба присоединены, образует замещенный или незамещенный 3-8-членный гетероцикл, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р, причем незамещенный гетероцикл замещен С1-6 алкилом; или
R7, взятый вместе с D2, L2, и N, к которому оба R7 и L2 присоединены, образует замещенный или незамещенный 5-15-членный гетероцикл или гетероарил, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р, причем незамещенный гетероцикл замещен C1-6 алкилом; и
R8 представляет собой Н или C1-6 алкил.
2. Соединение по п.1 или его фармацевтически приемлемая соль, где n равно 0, 1 или 2.
3. Соединение по п.1 или его фармацевтически приемлемая соль, где
R6 и R7, вместе с атомом азота, к которому они присоединены, образуют замещенный или незамещенный 3-8-членный гетероциклил, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р, причем незамещенный гетероцикл замещен С1-6 алкилом.
4. Соединение по п.1 или его фармацевтически приемлемая соль,
где R6 представляет собой Н или C1-6 алкил; и
R7 взят вместе с D2, L2, и N, к которому присоединены оба R7 и L2, образуют замещенный или незамещенный 5-15-членный гетероцикл или гетероарил, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р, причем незамещенный гетероцикл замещен С1-6 алкилом.
5. Соединение по любому одному из пп.1-4, где X2 представляет собой N.
6. Соединение по любому одному из пп.1-4, где X2 представляет собой C-R5.
7. Соединение по любому одному из пп.1-6, где X1 представляет собой С1-6 алкилен.
8. Соединение по любому одному из пп.1-7, где D1 представляет собой фенил.
9. Соединение по любому одному из пп.1-8, где D2 представляет собой фенил.
10. Соединение, выбранное из группы, состоящей из
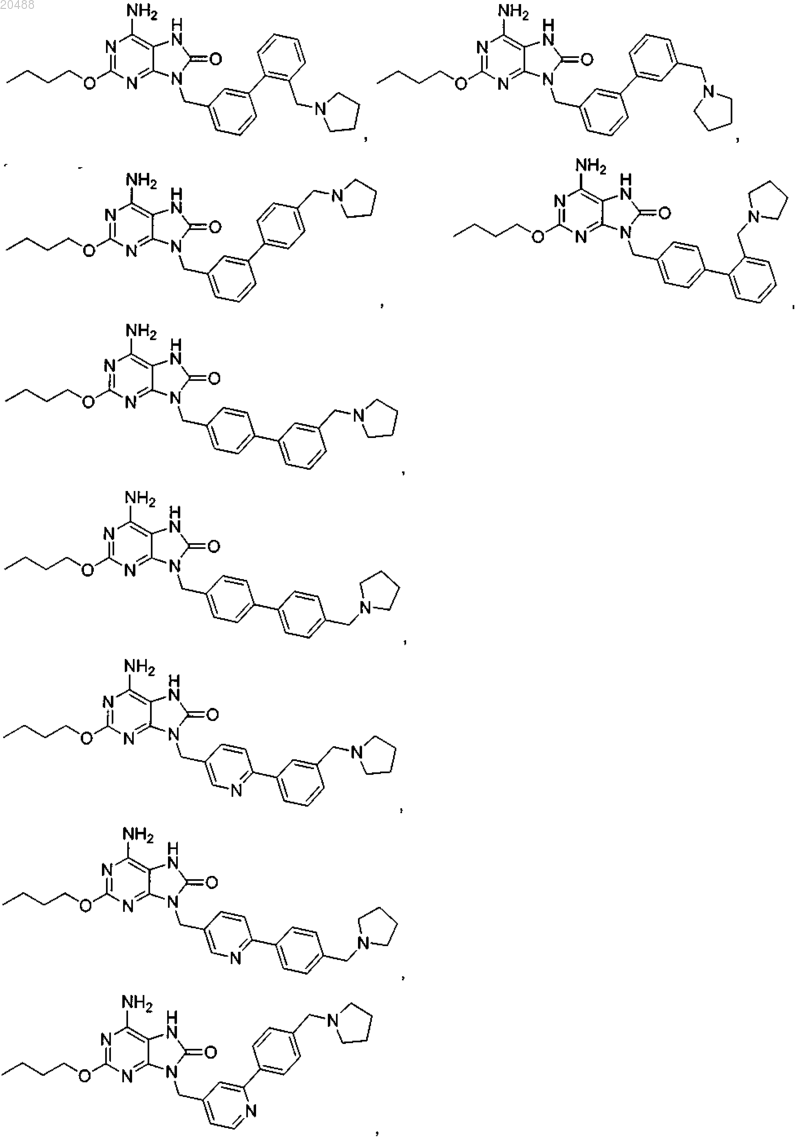

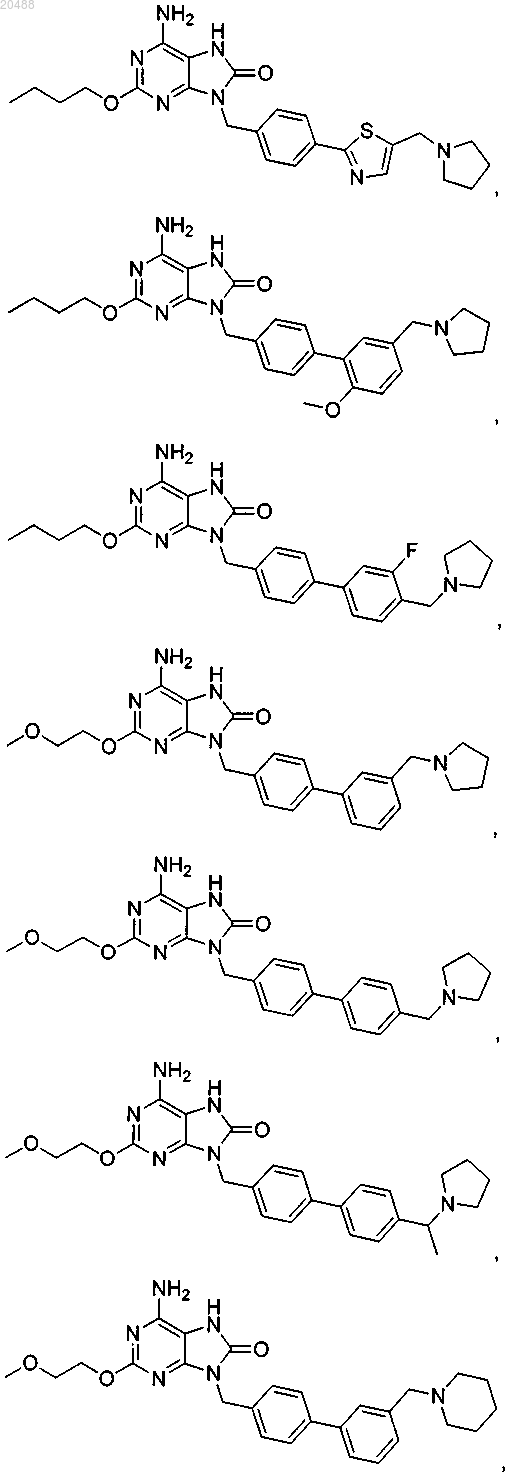
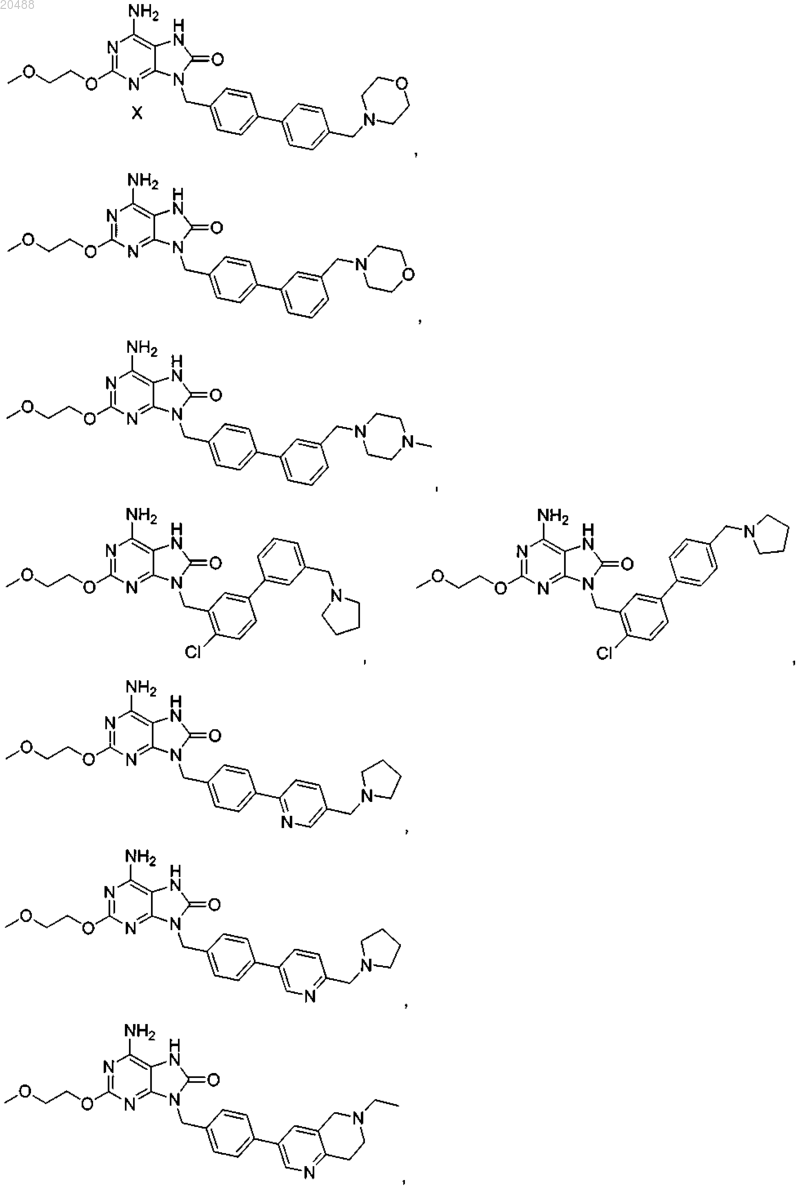
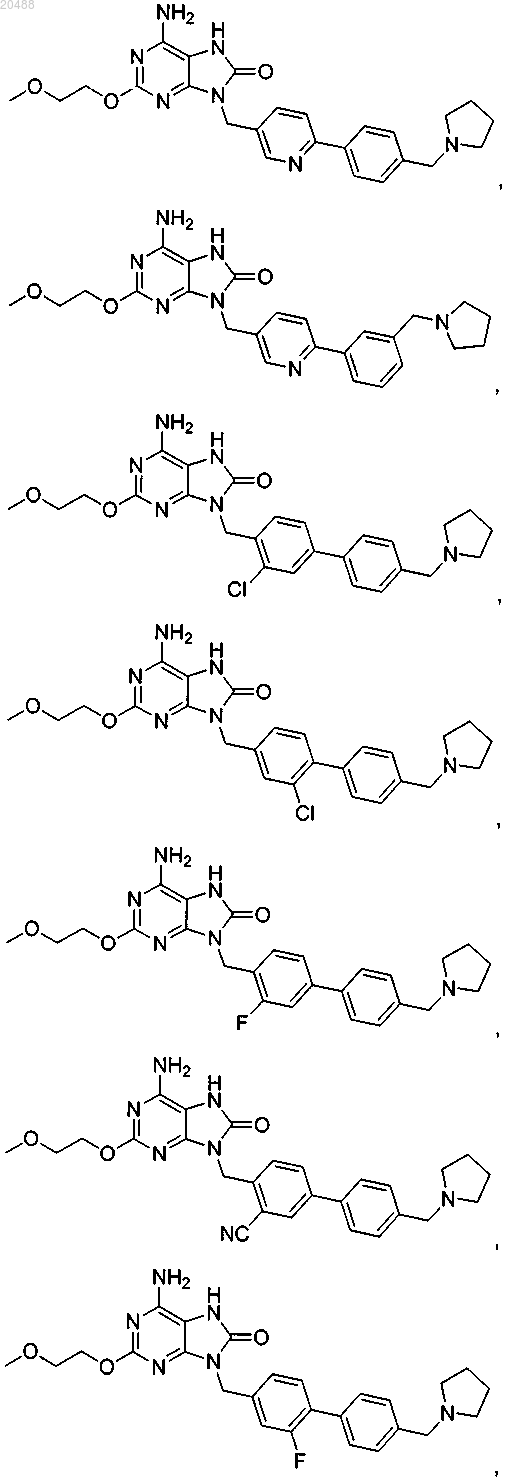
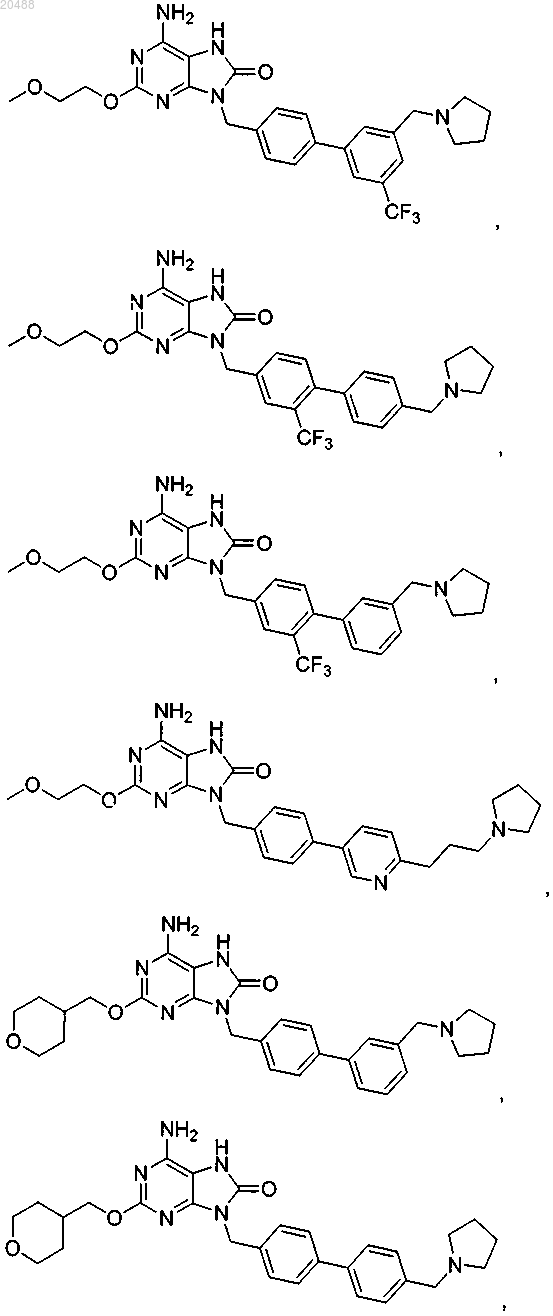
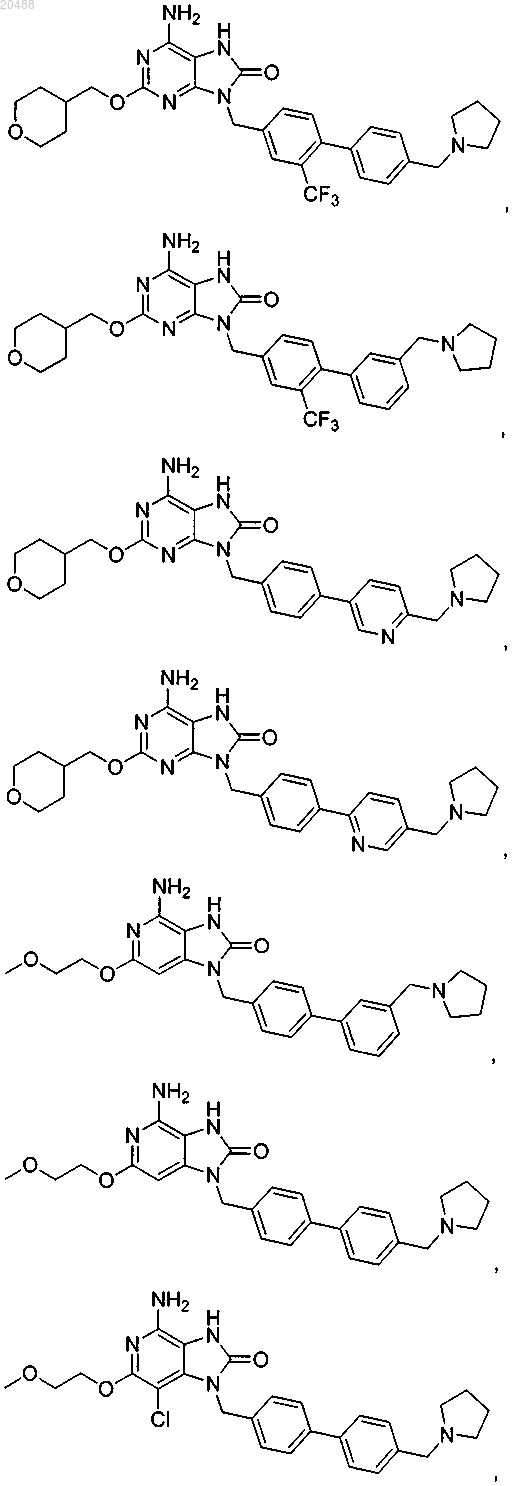
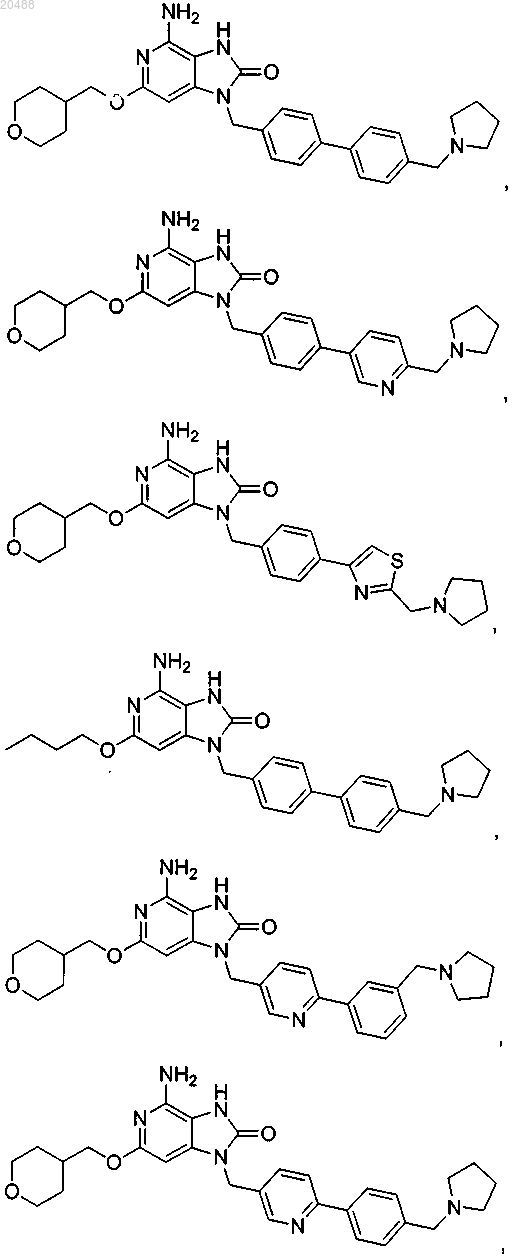
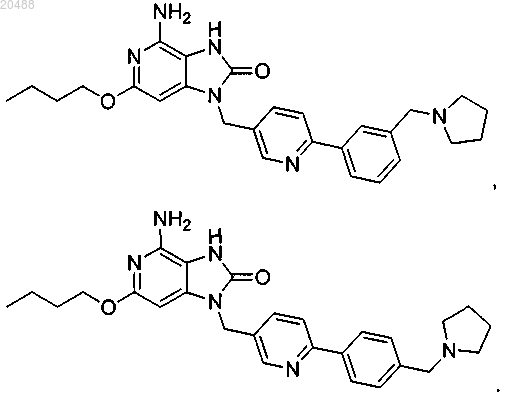
11. Соединение по п.1, имеющее следующую формулу
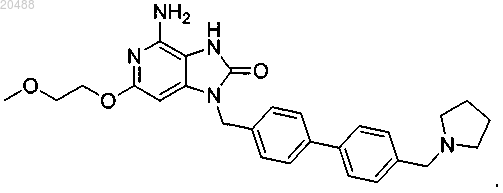
12. Фармацевтическая композиция для лечения вирусных инфекций, содержащая соединение по пп.1-11 и один или несколько фармацевтически приемлемых носителей или наполнителей.
Текст
ПРОИЗВОДНЫЕ ПУРИНА ИЛИ ДЕАЗАПУРИНА ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ВИРУСНЫХ ИНФЕКЦИЙ И ДРУГИХ ЗАБОЛЕВАНИЙ Настоящее изобретение включает новые модуляторы TLR, композиции, содержащие такие соединения, терапевтические способы, которые включают введение таких соединений. Область техники Настоящая заявка относится в основном к биарильному пурину и производным 3-деазапурина и фармацевтическим композициям, которые селективно модулируют toll-подобные рецепторы (такие какTLR-7), и способам получения и применения таких соединений. Уровень техники Врожденная иммунная система обеспечивает организм первой линией защиты от инвазивных патогенов. При врожденном иммунном ответе инвазивный патоген распознается рецептором, кодированным зародышевой линией, активация которого вызывает сигнальный каскад, который приводит к индукции экспрессии цитокина. Рецепторы врожденной иммунной системы характеризуются широкой специфичностью, распознавая молекулярные структуры, которые являются высококонсервативными среди разных патогенов. Одна группа таких рецепторов известна как toll-подобные рецепторы (TLR) из-за их гомологии с рецепторами, которые были первыми определены и названы у Drosophila и присутствуют в клетках,таких как макрофаги, дендритные клетки и эпителиальные клетки. У млекопитающих существует по меньшей мере десять различных TLR. Лиганды и соответствующие сигнальные каскады были идентифицированы для некоторых из этих рецепторов. Например, TLR-2 активируется липопротеином бактерий (например, Е. coli), TLR-3 активируется двунитевой РНК, TLR-4 активируется липополисахаридом (т.е. LPS или эндотоксином) грамотрицательных бактерий (например,Salmonella и Е. coli О 157:Н 7), TLR-5 активируется флагеллином мигрирующих бактерий (например, Listeria), TLR-7 распознает и реагирует на имиквимод (и ssRNA), и TLR-9 активируется неметилированными последовательностями CpG ДНК патогена. Стимуляция каждого из этих рецепторов приводит к активации фактора транскрипции NF-В и других сигнальных молекул, которые вовлечены в регуляцию экспрессии генов цитокина, включая те, которые кодируют фактор некроза опухоли-альфа (TNF-), интерлейкин-1 (IL-1) и определенные хемокины. Агонисты TLR-7 являются иммуностимуляторами и вызывают продуцирование эндогенного интерферона- in vivo. Существует ряд заболеваний, расстройств и состояний, связанных с TLR, в связи с чем терапии с применением агониста TLR считаются обещающими в лечении заболеваний, которые включают, но не ограничиваются ими, следующие: меланому, немелкоклеточную карциному легких, злокачественную гепатому, базальноклеточную карциному, почечноклеточный рак, миелому, аллергический ринит, астму,COPD, неспецифический язвенный колит, фиброз печени и вирусные инфекции, такие как HBV, HCV,HPV, RSV, SARS, HIV или грипп. Краткое описание изобретения В соответствии с вышеупомянутым в одном аспекте настоящее изобретение относится к соединениям формулы I или их фармацевтически приемлемым солям, гдеR1 представляет собой Н, алкил, замещенный алкил, галогеналкил, алкенил, замещенный алкенил,алкинил, замещенный алкинил, гетероалкил, замещенный гетероалкил, карбоциклил, замещенный карбоциклил, карбоциклилалкил, замещенный карбоциклилалкил, гетероциклил, замещенный гетероциклил,гетероциклилалкил, замещенный гетероциклилалкил, арил, замещенный арил, гетероарил, замещенный гетероарил, арилалкил, замещенный арилалкил, гетероарилалкил, замещенный гетероарилалкил, карбоциклилалкенил, замещенный карбоциклилалкенил, карбоциклилалкинил, замещенный карбоциклилалкинил, гетероциклилалкенил, замещенный гетероциклилалкенил, гетероциклилалкинил, замещенный гетероциклоалкинил, арилалкенил, замещенный арилалкенил, арилалкинил, замещенный арилалкинил,гетероарилалкенил, замещенный гетероарилалкенил, гетероарилалкинил, замещенный гетероарилалкинил, карбоциклилгетероалкил, замещенный карбоциклилгетероалкил, гетероциклилгетероалкил, замещенный гетероциклилгетероалкил, арилгетероалкил, замещенный арилгетероалкил, гетероарилгетероалкил или замещенный гетероарилгетероалкил; мещенный арил, гетероарил, замещенный гетероарил, гетероциклилалкил, замещенный гетероциклилалкил, арилалкил, замещенный арилалкил, гетероарилалкил, замещенный гетероарилалкил, карбоциклилгетероалкил, замещенный карбоциклилгетероалкил, гетероциклилгетероалкил, замещенный гетероциклилгетероалкил, арилгетероалкил, замещенный арилгетероалкил, гетероарилгетероалкил или замещенный гетероарилгетероалкил, циано, азидо, -С(О)Н, -C(O)R8, -S(O)R8, -S(O)2R8, -S(O)2NR8R9, -C(O)OR8 или -C(O)NR9R10; каждый не являющийся водородом R5 может быть необязательно соединен с X1 с образованием дополнительного 5-8-членного карбоциклического или гетероциклического кольца; каждый не являющийся водородом R5 может быть необязательно соединен с D1 с образованием дополнительного 5-8-членного карбоциклического или гетероциклического кольца;D1 представляет собой арил или гетероарил;D2 представляет собой арил или гетероарил; каждый L2 независимо представляет собой алкилен, замещенный алкилен, гетероалкилен, замещенный гетероалкилен или ковалентную связь; каждый R2 независимо представляет собой -NR6R7;m равно 1 или 2; каждый R3 и R4 независимо представляет собой алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, галоген, галогеналкил, галогеналкокси, гетероалкил, замещенный гетероалкил, =O, -OR8, -SR8, -NR9R10, =NR8, =NOR8, =NNR8R9, -CN, -OCN, -SCN, -N=C=O, -NCS,-NO, -NO2, =N2, -N3, -NR8C(=O)R9, -NR8C(=O)OR9, -NR8C(=O)NR9R10, -C(=O)NR9R10, -C(=O)OR8,-OC(=O)NR9R10, -OC(=O)OR8, -C(=O)R8, -S(=O)2OR8, -S(=O)2R8, -OS(=O)2OR8, -S(=O)2NR9R10, -S(=O)R8,-NR8S(=O)2R9, -NR8S(=O)2NR9R10, -NR8S(=O)2OR9, -OS(O)2NR9R10, -OP(=O)(OR8)2, -P(=O)(OR8)2,-P(O)(OR8)(R9), -P(O)R9R10, -OP(=O)R9R10, -C(=S)R8, -C(=S)OR8, -C(=O)SR8, -C(=S)SR8, -C(=S)NR9R10,-C(=NR8)NR9R10 или -NR8C(=NR8)NR9R10; каждый n независимо представляет собой 0, 1, 2, 3, 4 или 5 в зависимости от размера изображенного кольца D1 и D2 так, чтобы соответствующие точки присоединения присутствовали для каждого R3 иR4; каждый из R6 и R7 независимо представляет собой Н, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, галогеналкил, гетероалкил, замещенный гетероалкил, карбоциклил, замещенный карбоциклил, карбоциклилалкил, замещенный карбоциклилалкил, гетероциклил,замещенный гетероциклил, арил, замещенный арил, гетероарил, замещенный гетероарил, гетероциклилалкил, замещенный гетероциклилалкил, арилалкил, замещенный арилалкил, гетероарилалкил, замещенный гетероарилалкил, карбоциклилалкенил, замещенный карбоциклилалкенил, карбоциклилалкинил,замещенный карбоциклилалкинил, гетероциклилалкенил, замещенный гетероциклилалкенил, гетероциклилалкинил, замещенный гетероалкинил, арилалкенил, замещенный арилалкенил, арилалкинил, замещенный арилалкинил, гетероарилалкенил, замещенный гетероарилалкенил, гетероарилалкинил, замещенный гетероарилалкинил, карбоциклилгетероалкил, замещенный карбоциклилгетероалкил, гетероциклилгетероалкил, замещенный гетероциклилгетероалкил, арилгетероалкил, замещенный арилгетероалкил, гетероарилгетероалкил или замещенный гетероарилгетероалкил, -С(О)Н, -C(O)R8, -S(O)R8,-S(O)2R8, -C(O)OR8 или -C(O)NR9R10, S(O)2NR9R10; илиR6 и R7, взятые вместе с азотом, к которому они оба присоединены, образуют замещенный или незамещенный 3-8-членный гетероцикл, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р; илиR7, взятый вместе с L2, и N, к которому они оба присоединены, образует замещенный или незамещенный 3-8-членный гетероцикл, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р; илиR7, взят вместе с D2, L2, и N, к которому присоединены оба, R7 и L2, образует замещенный или незамещенный 5-15-членный гетероцикл или гетероарил, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р; карбоциклилгетероалкил, замещенный карбоциклилгетероалкил, гетероциклилгетероалкил, замещенный гетероциклилгетероалкил, арилгетероалкил, замещенный арилгетероалкил, гетероарилгетероалкил или замещенный гетероарилгетероалкил; и каждый из R9 и R10 независимо представляет собой Н, алкил, замещенный алкил, алкенил, замещенный алкенил, алкинил, замещенный алкинил, галогеналкил, гетероалкил, замещенный гетероалкил,карбоциклил, замещенный карбоциклил, карбоциклилалкил, замещенный карбоциклилалкил, гетероциклил, замещенный гетероциклил, гетероциклилалкил, арил, замещенный арил, гетероарил, замещенный гетероарил, замещенный гетероциклилалкил, арилалкил, замещенный арилалкил, гетероарилалкил, замещенный гетероарилалкил, карбоциклилалкенил, замещенный карбоциклилалкенил, карбоциклилалкинил, замещенный карбоциклилалкинил, гетероциклилалкенил, замещенный гетероциклилалкенил, гетероциклилалкинил, замещенный гетероциклилалкинил, арилалкенил, замещенный арилалкенил, арилалкинил, замещенный арилалкинил, гетероарилалкенил, замещенный гетероарилалкенил, гетероарилалкинил, замещенный гетероарилалкинил, карбоциклилгетероалкил, замещенный карбоциклилгетероалкил,гетероциклилгетероалкил, замещенный гетероциклилгетероалкил, арилгетероалкил, замещенный арилгетероалкил, гетероарилгетероалкил или замещенный гетероарилгетероалкил; илиR9 и R10, взятые вместе с атомом, к которому они оба присоединены, образуют замещенный или незамещенный 3-8-членный гетероцикл, который может содержать один или несколько дополнительных гетероатомов, выбранных из N, О, S или Р. В другом аспекте настоящее изобретение включает соединение по настоящему изобретению и один или несколько фармацевтически приемлемых носителей или наполнителей. В еще одном варианте осуществления композиция дополнительно содержит один или несколько дополнительных терапевтических средств. В другом аспекте настоящее изобретение включает соединение по настоящему изобретению в способе лечения вирусной инфекции. В одном варианте осуществления лечение приводит к одному или нескольким из уменьшения вирусной нагрузки или элиминирования вирусной РНК. В другом аспекте настоящее изобретение включает соединение по настоящему изобретению для применения при производстве лекарственного препарата для лечения вирусной инфекции. В другом аспекте настоящее изобретение включает соединение по настоящему изобретению для применения при лечении вирусной инфекции. В одном варианте осуществления или такое применение, или соединение для лечения приводит к одному или нескольким из уменьшения вирусной нагрузки или элиминирования вирусной РНК. В другом аспекте настоящее изобретение включает соединение по настоящему изобретению в способе для лечения или предупреждения меланомы, немелкоклеточной карциномы легких, злокачественной гепатомы, базальноклеточной карциномы, почечноклеточного рака, миеломы, аллергического ринита, астмы, COPD, язвенного колита, фиброза печени, HBV, HCV, HPV, RSV, SARS, ВИЧ или гриппа. В другом аспекте настоящее изобретение включает соединение по настоящему изобретению для применения в производстве лекарственного препарата для лечения или предупреждения меланомы, немелкоклеточной карциномы легких, злокачественной гепатомы, базальноклеточной карциномы, почечноклеточного рака, миеломы, аллергического ринита, астмы, COPD, язвенного колита, фиброза печени,HBV, HCV, HPV, RSV, SARS, ВИЧ или гриппа. Не желая ограничиваться конкретной теорией, в настоящее время изобретатели полагают, что соединения формулы I являются агонистами TLR-7 и также могут быть агонистами других TLR. Таким образом, соединения по настоящему изобретению могут использоваться для лечения или предупреждения заболеваний, на которые модуляторы TLR и, в частности, TLR-7 оказывают терапевтический эффект. Например, такие заболевания включают меланому, немелкоклеточную карциному легких, злокачественную гепатому, базальноклеточную карциному, почечноклеточный рак, миелому, аллергический ринит,астму, COPD, язвенный колит, фиброз печени, HBV, HCV, HPV, RSV, SARS, ВИЧ или грипп. Как отмечено, согласно одному аспекту, настоящее изобретение включает фармацевтическую композицию, содержащую соединение по настоящему изобретению и один или несколько фармацевтически приемлемых носителей или наполнителей. Фармацевтическая композиция настоящего изобретения может дополнительно содержать один или несколько дополнительных терапевтических средств. Одно или несколько дополнительных терапевтических средств могут без ограничения быть выбраны из интерферонов, рибавирина или их аналогов, ингибиторов протеазы HCV NS3, ингибиторов -глюкозидазы 1,гепатопротекторов, нуклеозидных или нуклеотидных ингибиторов HCV NS5B полимеразы, не нуклеозидных ингибиторов HCV NS5B полимеразы, ингибиторов HCV NS5A, ингибиторов HCV NS4A, ингибиторов HCV NS4B, TLR-7 агонистов, циклофилиновых ингибиторов, ингибиторов HCV IRES, фармакокинетических усилителей и других лекарственных средств для лечения HCV или их смесей. Как отмечено в одном аспекте, настоящее изобретение включает способ лечения вирусной инфекции, включающий введение соединения по настоящему изобретению. Соединение вводят субъекту, нуждающемуся в этом, например человеку, инфицированному вирусом семейства Flaviviridae, таким как вирус гепатита С. В одном варианте осуществления вирусная инфекция представляют собой острую или хроническую инфекцию HCV. В одном варианте осуществления лечение приводит к одному или не-3 020488 скольким из уменьшения вирусной нагрузки или элиминирования вирусной РНК. Как отмечено выше,существует ряд заболеваний, расстройств и состояний, связанных с TLR так, что терапии с применением агониста TLR считаются обнадеживающими, включая без ограничения меланому, немелкоклеточную карциному легких, злокачественную гепатому, базальноклеточную карциному, почечноклеточный рак,миелому, аллергический ринит, астму, COPD, язвенный колит, фиброз печени, HBV, HCV, HPV, RSV,SARS, ВИЧ или грипп. Как отмечено в одном аспекте, настоящее изобретение включает применение соединения по данному изобретению для производства лекарственного препарата для лечения вирусной инфекции. Другой аспект настоящего изобретения включает соединение по данному изобретению для применения при лечении вирусной инфекции. В одном варианте осуществления вирусная инфекция представляет собой острую или хроническую инфекцию HCV. В одном варианте осуществления лечение приводит к одному или нескольким из уменьшения вирусной нагрузки или элиминирования вирусной РНК. В одном варианте осуществления вирусная инфекция представляет собой острую или хроническую инфекцию HBV. В одном варианте осуществления лечение приводит к одному или нескольким из уменьшения вирусной нагрузки или элиминирования вирусной РНК. Настоящее изобретение охватывает также комбинации аспектов и вариантов осуществления, а также предпочтений, как описано в данном описании. Подробное описание изобретения Будут более подробно сделаны ссылки на определенные пункты формулы настоящего изобретения,примеры которых проиллюстрированы в сопровождающих структурах и формулах. Хотя настоящее изобретение будет описано в отношении приведенной формулы изобретения, следует понимать, что формула изобретения не предназначена для ограничения настоящего изобретения. Напротив, предполагается,что настоящее изобретение охватывает все альтернативы, модификации и эквиваленты, которые могут быть включены в объем настоящего изобретения, как определено в формуле изобретения. Все цитируемые здесь документы включены по ссылке в их полноте для всех целей. Определения. Если не заявлено иное, подразумевается, что следующие используемые в настоящем документе выражения и фразы характеризуются следующими значениями. Тот факт, что конкретное выражение или фраза не являются конкретно определенными, не должен сопоставляться с неопределенной или неудовлетворительной четкостью, и скорее выражения используются здесь в пределах своих обычных значений. Когда здесь используют торговые наименования, заявители подразумевают независимое включение торгового наименования продукта и активного(ых) фармацевтического(ых) ингредиента(ов) продукта с торговым наименованием. При применении в контексте лечения заболевания выражение "лечение" и его грамматические эквиваленты означают замедление или остановку развития заболевания или улучшение по меньшей мере одного симптома заболевания, более предпочтительно улучшение более чем одного симптома заболевания. Например, лечение инфекции вируса гепатита С может включать ослабление вирусной нагрузкиHCV у инфицированного HCV человека и/или ослабление тяжести желтухи, присутствующей у инфицированного HCV человека. Как используется в данном документе, "соединение по настоящему изобретению" или "соединение формулы I" означает соединение формулы I, включая его альтернативные формы, такие как сольватированные формы, гидратированные формы, эстерифицированные формы или их физиологически функциональные производные. Соединения по настоящему изобретению также включают их таутомерные формы, например таутомерные "енолы", как описано в данном документе. Подобным образом, что касается способных к выделению промежуточных соединений, фраза "соединение формулы (номер)" означает соединение этой формулы и его альтернативные формы."Алкил" представляет собой углеводород, содержащий нормальные, вторичные, третичные или циклические атомы углерода. Например, алкильная группа может содержать 1-20 атомов углерода (т.е. С 1-С 20 алкил), 1-10 атомов углерода (т.е. C1-С 10 алкил) или 1-6 атомов углерода (т.е. C1-С 6 алкил). Примеры подходящих алкильных групп включают без ограничения метил (Me, -CH3), этил (Et, -СН 2 СН 3), 1-пропил"Алкокси" обозначает группу, содержащую формулу -О-алкил, в которой определенная выше алкильная группа присоединена к исходной молекуле через атом кислорода. Алкильная часть алкокси-4 020488 группы может содержать 1-20 атомов углерода (т.е. C1-С 20 алкокси), 1-12 атомов углерода (т.е. С 1 С 12 алкокси) или 1-6 атомов углерода (т.е. C1-С 6 алкокси). Примеры подходящих алкоксигрупп включают без ограничения метокси (-О-СН 3 или -ОМе), этокси (-ОСН 2 СН 3 или -OEt), трет-бутокси (-О-С(СН 3)3 или"Галогеналкил" представляет собой определенную выше алкильную группу, в которой один или несколько атомов водорода алкильной группы замещены атомом галогена. Алкильная часть галогеналкильной группы может содержать 1-20 атомов углерода (т.е. С 1-С 20 галогеналкил), 1-12 атомов углерода(т.е. С 1-С 12 галогеналкил) или 1-6 атомов углерода (т.е. С 1-С 6 алкил). Примеры подходящих галогеналкильных групп включают без ограничения -CF3, -CHF2, -CFH2, -CH2CF3 и т.п."Алкенил" представляет собой углеводород, содержащий нормальные, вторичные, третичные или цикличные атомы углерода по меньшей мере с одним участком ненасыщения, т.е. углерод-углерод, sp2 двойная связь. Например, алкенильная группа может содержать 2-20 атомов углерода (т.е. С 2 С 20 алкенил), 2-12 атомов углерода (т.е. С 2-С 12 алкенил) или 2-6 атомов углерода (т.е. С 2-С 6 алкенил). Примеры подходящих алкенильных групп включают без ограничения винил (-СН=СН 2), аллил (СН 2 СН=СН 2), циклопентенил (-С 5 Н 7) и 5-гексенил (-СН 2 СН 2 СН 2 СН 2 СН=СН 2). Алкинил представляет собой углеводород, содержащий нормальные, вторичные, третичные или цикличные атомы углерода с по меньшей мере одним участком ненасыщения, т.е. углерод-углерод, sp тройная связь. Например, алкинильная группа может содержать 2-20 атомов углерода (т.е. С 2 С 20 алкинил), 2-12 атомов углерода (т.е. С 2-С 12 алкин) или 2-6 атомов углерода (т.е. С 2-С 6 алкинил). Примеры подходящих алкинильных групп включают без ограничения ацетиленовую (-ССН), пропаргильную (-CH2CCH) и т.п."Алкилен" относится к углеводородному радикалу с насыщенной, разветвленной или неразветвленной цепью или циклическому, включающему два одновалентных радикальных центра, полученных путем удаления двух атомов водорода от одинаковых или двух различных атомов углерода исходного алкана. Например, алкиленовая группа может содержать 1-20 атомов углерода, 1-10 атомов углерода или 16 атомов углерода. Типичные алкиленовые радикалы включают без ограничения метилен (-СН 2-), 1,1 этилен (-СН(СН 3)-), 1,2-этилен (-СН 2 СН 2-), 1,1-пропилен (-СН(СН 2 СН 3)-), 1,2-пропилен (-СН 2 СН(СН 3)-),1,3-пропилен (-СН 2 СН 2 СН 2-), 1,4-бутилен (-СН 2 СН 2 СН 2 СН 2-) и т.п."Алкенилен" относится к углеводородному радикалу с насыщенной, разветвленной или неразветвленной цепью или циклическому, включающему два одновалентных радикальных центра, полученных путем удаления двух атомов водорода от одинаковых или двух различных атомов углерода исходного алкена. Например, алкениленовая группа может содержать 2-20 атомов углерода, 2-10 атомов углерода или 2-6 атомов углерода. Типичные алкениленовые радикалы включают без ограничения 1,2-этилен"Алкинилен" относится к углеводородному радикалу с насыщенной, разветвленной или неразветвленной цепью или циклическому, включающему два одновалентных радикальных центра, полученных путем удаления двух атомов водорода от одинаковых или двух различных атомов углерода исходного алкина. Например, алкиниленовая группа может содержать 2-20 атомов углерода, 2-10 атомов углерода или 2-6 атомов углерода. Типичные алкиниленовые радикалы включают без ограничения ацетилен"Аминоалкил" относится к ациклическому алкильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично конечным или sp3 углеродным атомом, замещен аминорадикалом."Амидоалкил" относится к ациклическому алкильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично конечным или sp3 углеродным атомом, замещен группой-NRaCORb, в которой Ra представляет собой атом водорода или алкил, и Rb представляет собой алкил,замещенный алкил, арил или замещенный арил, как определено здесь, например -(CH2)2-NHC(O)CH3,-(CH2)3-NH-C(O)-СН 3 и т.п."Арил" означает одновалентный ароматический углеводородный радикал, полученный путем удаления одного атома водорода от одного атома углерода исходной ароматической кольцевой системы. Например, арильная группа может содержать 6-20 атомов углерода, 6-14 атомов углерода или 6-12 атомов углерода. Типичные арильные группы включают без ограничения радикалы, полученные из бензола"Арилен" относится к определенному выше арилу, содержащему два моновалентных радикальных центра, полученных путем удаления двух атомов водорода от одинаковых или двух различных атомов углерода исходного арила. Типичные ариленовые радикалы включают без ограничения фенилен."Арилалкил" относится к алкильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично с конечным или sp3 атомом углерода, замещен арильным радикалом. Типичные арилалкильные группы включают без ограничения бензил, 2-фенилэтан-1-ил, нафтилметил, 2 нафтилэтан-1-ил, нафтобензил, 2-нафтофенилэтан-1-ил и т.п. Арилалкильная группа может содержать 620 атомов углерода, например алкильный фрагмент содержит 1-6 атомов углерода, и арильный фрагмент"Арилалкенил" относится к ациклическому алкенильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично, с конечным или sp3 атомом углерода, а также sp2 атомом углерода, замещен арильным радикалом. Арильная часть арилалкенила может включать, например любую из раскрытых здесь арильных групп, и алкенильная часть арилалкенила может включать, например,любую из раскрытых здесь алкенильных групп. Арилалкенильная группа может содержать 8-20 атомов углерода, например алкенильный фрагмент включает 2-6 атомов углерода, и арильный фрагмент включает 6-14 атомов углерода."Арилалкинил" относится к ациклическому алкинильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично конечным или sp3 атомом углерода, а также sp атомом углерода, замещен арильным радикалом. Арильная часть арилалкинила может включать, например, любую из арильных групп, раскрытых здесь, и алкинильная часть арилалкинила может включать, например,любую из раскрытых здесь алкинильных групп. Арилалкинильная группа может содержать 8-20 атомов углерода, например алкинильный фрагмент содержит 2-6 атомов углерода и арильный фрагмент содержит 6-14 атомов углерода.R представляет собой галогеналкильную группу, как определено здесь. В качестве неограничивающих примеров галогеналкоксигруппы включают -O(CH2)F, -O(CH)F2 и -OCF3."Гетероалкил" относится к алкильной группе, где один или несколько атомов углерода были замещены гетероатомом, таким как О, N или S. Например, если атом углерода алкильной группы, который присоединен к исходной молекуле, замещен гетероатомом (например, О, N, Р или S), полученные гетероалкильные группы представляют собой, соответственно, алкоксигруппу (например, -ОСН 3 и т.д.), амин(например, -NHCH3, -N(CH3)2 и т.п.) или тиоалкильную группу (например, -SCH3). Если не конечный атом углерода алкильной группы, который не является присоединенным к исходной молекуле, замещен гетероатомом (например, О, N, Р или S), и полученные гетероалкильные группы, соответственно, являются алкильным эфиром (например, -СН 2 СН 2-О-СН 3 и т.д.), алкильным амином (например, -CH2NHCH3,-CH2N(CH3)2 и т.п.) или тиоалкильным эфиром (например,-СН 2-S-СН 3). Если конечный атом углерода алкильной группы замещен гетероатомом (например, О, N или S), полученные гетероалкильные группы,соответственно, представляют собой гидроксиалкильные группы (например, -СН 2 СН 2-ОН), аминоалкильные группы (например, -CH2NH2) или алкильную тиольную группу (например, -СН 2 СН 2-SH). Гетероалкильная группа может содержать, например, 1-20 атомов углерода, 1-10 атомов углерода или 1-6 атомов углерода. C1-С 6 гетероалкильная группа означает гетероалкильную группу, содержащую 1-6 атомов углерода."Гетероцикл" или "гетероциклил" относится к насыщенной или частично насыщенной циклической группе, содержащей 1-14 атомов углерода и 1-6 гетероатомов, выбранных из N, S, Р или О, и включает однокольцевые и многокольцевые системы, включающие конденсированные, с мостиковыми связями и спиро-кольцевые системы. "Гетероцикл" или "гетероциклил", как используется в данном документе,включает в качестве примера и не ограничивается такими гетероциклами, описанными с Paquette, Leo A.;Principles of Modern Heterocvclic Chemistry (W.A. Benjamin, New York, 1968), в частности главы 1, 3, 4, 6,7 и 9; The Chemistry of Heterocvclic Compounds, A Series of Monographs (John WileySons, New York,1950 to present), в частности тома 13, 14, 16, 19 и 28; и J. Am. Chem. Soc. (1960) 82:5566. В одном варианте осуществления атом(ы) углерода, азота, фосфора или серы гетероциклической группы могут быть окислены с получением фрагментов С(=О), N-оксида, фосфинаноксида, сульфинила или сульфонила. В одном примере замещенные гетероциклилы включают, например, гетероциклические кольца, замещенные любыми заместителями, раскрытыми здесь, включая оксо-группы. Неограничивающий пример гетероциклила, замещенного карбонилом, представляет собой Примеры гетероциклов включают в качестве примера и без ограничения дигидропиридил, тетрагидропиридил (пиперидил), тетрагидротиофенил, окисленный серой тетрагидротиофенил, пиперидинил,4-пиперидонил, пирролидинил, азетидинил, 2-пирролидинил, тетрагидрофуранил, декагидрохинолинил,октагидроизохинолинил, пиранил, морфолинил и бис-тетрагидрофуранил"Гетероциклилен" относится к гетероциклилу, как определено здесь, полученному путем замещения атома водорода на атом углерода или гетероатом гетероциклила с открытой валентностью. Подобным образом, "гетероарилен" относится к ароматическому гетероциклилену."Гетероциклилалкил" относится к ациклическому алкильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично конечным или sp3 атомом углерода, замещен гетероциклильным радикалом (т.е. фрагмент гетероциклилалкилен). Типичные гетероциклилалкильные группы включают без ограничения гетероциклил-СН 2-, 2-(гетероциклил)этан-1-ил и т.п., где фрагмент "гетероциклила" включает любую из гетероциклильных групп, описанных выше, включая описанные в Principles of Modern Heterocvclic Chemistry. Специалист в данной области также будет понимать, что гетероциклильная группа может присоединяться к алкильной части гетероциклильного алкила посредством углерод-углеродной связи или углерод-гетероатомной связи при условии, что полученная группа химически стойкая. Гетероциклилалкильная группа содержит 2-20 атомов углерода и 1-6 гетероатомов, например алкильная часть гетероциклилалкильной группы содержит 1-6 атомов углерода, и гетероциклильный фрагмент содержит 1-14 атомов углерода. Примеры гетероциклилалкилов включают в качестве примера и без ограничения 5-членные содержащие серу, кислород, фосфор и/или азот гетероциклы, такие как пирролидилметил, 2-тетрагидрофуранилилэтан-1-ил и т.п., 6-членные содержащие серу, кислород и/или азот гетероциклы, такие как пиперидинилметил, морфолинилметил, пиперидинилэтил, тетрагидропиранилэтил и т.п."Гетероциклилалкенил" относится к ациклическому алкенильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично конечным или sp3 атомом углерода, а также сsp2 атомом углерода, замещен гетероциклильным радикалом (т.е. гетероциклил-алкениленовый фрагмент). Часть гетероциклила гетероциклильной алкенильной группы включает любую из гетероциклильных групп, описанных в данном документе, включая описанные в Principles of Modern Heterocvclic Chemistry, и алкенильная часть гетероциклильной алкенильной группы включает любую из алкенильных групп, раскрытых здесь. Специалист в данной области также будет понимать, что гетероциклильная группа может быть присоединена к алкенильной части гетероциклильного алкенила посредством углерод-углеродной связи или углерод-гетероатомной связи при условии, что полученная группа является химически стойкой. Гетероциклильная алкенильная группа содержит 2-20 атомов углерода, например,алкенильная часть гетероциклилалкенильной группы содержит 2-6 атомов углерода, и гетероциклильный фрагмент содержит 1-14 атомов углерода."Гетероциклилалкинил" относится к ациклическому алкинильному радикалу, в котором один из атомов водорода, связанный с атомом углерода, типично конечным или sp3 атомом углерода, а также sp атомом углерода, замещен гетероциклильным радикалом (т.е. гетероциклил-алкиниленовым фрагментом). Гетероциклильный фрагмент гетероциклильной алкинильной группы включает любую из гетероциклильных групп, описанных в данном документе, включая описанные в Principles of Modern Heterocvclic Chemistry, и алкинильный фрагмент гетероциклильной алкинильной группы включает любую из алкинильных групп, раскрытых здесь. Специалист в данной области также будет понимать, что гетероциклильная группа может быть присоединена к алкинильной части гетероциклилалкинила посредством углерод-углеродной связи или углерод-гетероатомной связи при условии, что полученная группа является химически стойкой. Гетероциклилалкинильная группа содержит 3-20 атомов углерода, например алкинильная часть гетероциклилалкинильной группы содержит 2-6 атомов углерода и гетероциклильный фрагмент содержит 1-14 атомов углерода."Гетероарил" относится к моновалентному ароматическому гетероциклилу, содержащему по меньшей мере один гетероатом в кольце. Таким образом, "гетероарил" относится к ароматической группе из от 1 до 14 атомов углерода и 1-6 гетероатомов, выбранных из кислорода, азота, серы или фосфора. Для многокольцевых систем в качестве примера выражение "гетероарил" включает конденсированные, с мостиковыми связями и спирокольцевые системы, содержащие ароматические и неароматические кольца. В одном варианте осуществления кольцевые атом(ы) углерода, азота, серы или фосфора гетероарильной группы могут быть окислены с получением фрагментов С(=О), N-оксида, сульфинила или сульфонила. Примеры гетероарилов включают в качестве примера и без ограничения пиридил, тиазолил, пиримидинил, фуранил, тиенил, пирролил, пиразолил, имидазолил, тетразолил, бензофуранил, тианафталенил, индолил, хинолинил, изохинолинил, бензимидазолил, тетрагидрохинолинил, тетрагидроизохинолинил, 6 Н-1,2,5-тиадиазинил, 2 Н,6 Н-1,5,2-дитиазинил, тиенил, тиантренил, изобензофуранил, хроменил,ксантенил, феноксатинил, 2 Н-пирролил, изотиазолил, изоксазолил, пиразинил, пиридазинил, индолизинил, изоиндолил, 3 Н-индолил, 1 Н-индазолил, пуринил, 4 Н-хинолизинил, нафтиридинил, хиноксалинил,-7 020488"Карбоцикл" или "карбоциклил" относится к насыщенному, частично ненасыщенному или ароматическому кольцу, содержащему 3-7 атомов углерода как моноцикл, 7-12 атомов углерода как бицикл и до приблизительно 20 атомов углерода как полицикл. Моноциклические карбоциклы содержат 3-6 кольцевых атомов, еще более типично 5 или 6 кольцевых атомов. Бициклические карбоциклы содержат 7-12 кольцевых атомов, например, расположенных как бицикло (4,5), (5,5), (5,6) или (6,6) система, или 9 или 10 кольцевых атомов, расположенных как бицикло (5,6) или (6,6) система. Карбоциклы включают неароматические моно-, би- и полициклические кольца, некоторые из которых конденсированные, с мостиковыми связями или спиро. Неограничивающие примеры моноциклических карбоциклов включают циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил,1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил и т.п."Карбоциклилен" относится к карбоциклилу или карбоциклу, как определено выше, содержащему два моновалентных радикальных центра, полученных путем удаления двух атомов водорода из него же или два различных атома углерода исходного карбоциклила. Типичные карбоциклиленовые радикалы включают без ограничения фенилен."Арилгетероалкил" относится к гетероалкилу, как определено здесь, в котором атом водорода, который может быть присоединен или к атому углерода, или к гетероатому, был замещен арильной группой, как определено здесь. Арильные группы могут быть связаны с атомом углерода гетероалкильной группы или с гетероатомом гетероалкильной группы при условии, что полученная арилгетероалкильная группа дает химически стойкий фрагмент. Например, арилгетероалкильная группа может характеризоваться общими формулами -алкилен-О-арил, -алкилен-О-алкилен-арил, -алкилен-NH-арил, -алкилен-NHалкилен-арил, -алкилен-S-арил, -алкилен-S-алкилен-арил и т.п. К тому же любой из алкиленовых фрагментов общей вышеуказанной формулы может быть дополнительно замещен любыми заместителями,определенными или являющимися здесь примерами."Гетероарилалкил" относится к определенной здесь алкильной группе, в которой атом водорода был замещен определенной здесь гетероарильной группой. Неограничивающие примеры гетероарилалкила включают -СН 2-пиридинил, -СН 2-пирролил, -СН 2-оксазолил, -СН 2-индолил, -СН 2-изоиндолил,-СН 2-пуринил, -СН 2-фуранил, -CH2-тиенил, -СН 2-бензофуранил, -СН 2-бензотиофенил, -СН 2-карбазолил,-СН 2-имидазолил, -СН 2-тиазолил, -СН 2-изоксазолил, -СН 2-пиразолил, -СН 2-изотиазолил, -CH2-хинолил,-СН 2-изохинолил, -СН 2-пиридазил, -СН 2-пиримидил, -СН 2-пиразил, -СН(СН 3)-пиридинил, -СН(CH3)пирролил, -СН(СН 3)-оксазолил, -СН(СН 3)-индолил, -СН(СН 3)-изоиндолил, -СН(СН 3)-пуринил,-СН(СН 3)-фуранил, -СН(СН 3)-тиенил, -СН(СН 3)-бензофуранил, -СН(СН 3)-бензотиофенил, -СН(СН 3)карбазолил, -СН(СН 3)-имидазолил, -СН(СН 3)-тиазолил, -СН(СН 3)-изоксазолил, -СН(СН 3)-пиразолил,-СН(СН 3)-изотиазолил, -СН(СН 3)-хинолил, -СН(СН 3)-изохинолил, -СН(СН 3)-пиридазил, -СН(СН 3)пиримидил, -СН(СН 3)-пиразил и т.п. Выражение "необязательно замещенный" в ссылке на конкретный фрагмент соединения формулы по настоящему изобретению, например необязательно замещенная арильная группа, относится к фрагменту, содержащему 0, 1 или более заместителей. Выражение "замещенный" в ссылке на алкил, арил, арилалкил, карбоциклил, гетероциклил и другие используемые здесь группы, например "замещенный алкил", "замещенный арил", "замещенный арилалкил", "замещенный гетероциклил" и "замещенный карбоциклил", означает группу, алкил, алкилен, арил,арилалкил, гетероциклил, карбоциклил, соответственно, в которой каждый один или несколько атомов водорода независимо замещены неводородным заместителем. Типичные заместители включают без ограничения -X, -R, -О-, =O, -OR, -SR, -S-, -NR2, -N(+)R3, =NR, =NOR, =NNR2, -CX3, -CRX2, -CR2X,-CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, =N2, -N3, -NRC(=O)R, -NRC(=O)OR, -NRC(=O)NRR,-C(=O)NRR, -C(=O)OR, -OC(=O)NRR, -OC(=O)OR, -C(=O)R, -S(=O)2OR, -S(=O)2R, -OS(=O)2OR,-S(=O)2NRR, -S(=O)R, -NRS(=O)2R, -NRS(=O)2NRR, -NRS(=O)2OR, -OP(=O)(OR)2, -P(=O)(OR)2,-P(O)(OR)(R), -OP(=O)R2, -P(=O)R2, -C(=S)R, -C(=S)OR, -C(=O)SR, -C(=S)SR, -C(=S)NRR, -C(=NR)NRR,-NRC(=NR)NRR, где каждый X независимо представляет собой галоген: F, Cl, Br или I; и каждый R независимо представляет собой Н, алкил, арил, арилалкил, гетероцикл или защитную группу или фрагмент пролекарства. Двухвалентные группы также могут быть подобно замещены. Специалисты в данной области техники признают, что если фрагменты, такие как "алкил", "арил","гетероциклил" и т.д., замещены одним или несколькими заместителями, они могут альтернативно называться "алкиленовыми", "ариленовыми", "гетероциклиленовыми" и т.д. фрагментами (т.е. указывать на то, что по меньшей мере один из атомов водорода исходных "алкильных", "арильных", "гетероциклильных" фрагментов замещен указанным(и) заместителем(ями. Если фрагменты, такие как "алкил", "арил","гетероциклил" и т.д., называются здесь "замещенными" или показаны в виде диаграммы как замещенные (или необязательно замещенный, например, если число заместителей находится в диапазоне от нуля до положительного целого числа), тогда выражения "алкил", "арил", "гетероциклил" и т.д. понимают как взаимозаменяемые с "алкиленом", "ариленом", "гетероциклиленом" и т.д. Кроме того, специалисты в данной области техники признают, что, если определенные здесь выражения используют в комбинации, полученное объединенное выражение используют согласно определению. Например, хотя выражение, такое как "карбоциклилгетероалкил" может не нести конкретного определения здесь, это не должно приравниваться к недостатку ясности. Предпочтительно такое выражение используют без принятого значения в данном уровне техники для описания карбоциклильной группы, связанной через гетероалкильную группу. Другие такие выражения используют последовательно. Как будет отмечено специалистами в данной области техники, соединения по настоящему изобретению способны существовать в сольватированной или гидратированной форме. Объем настоящего изобретения включает такие формы. Более того, как будет отмечено специалистами в данной области техники, соединения могут быть способны к эстерификации. Объем настоящего изобретения включает сложные эфиры и другие физиологически функциональные производные. Объем настоящего изобретения также включает таутомерные формы, а именно описанные здесь таутомерные "енолы". К тому же объем настоящего изобретения включает формы пролекарства описанного здесь соединения. Выражение "пролекарство", как используется в данном документе, относится к любому соединению, которое при введении в биологическую систему образует лекарственное вещество, т.е. активный ингредиент, в результате самопроизвольной(ых) химической(их) реакция(ий), катализированной(ых) ферментом химической(их) реакции(ий), фотолиза и/или метаболической(их) химической(их) реакции(ий). Пролекарство, таким образом, представляет собой ковалентно модифицированный аналог или скрытую форму терапевтически активного соединения. Специалист в данной области признает, что заместители и другие фрагменты соединений формулыI должны быть выбраны для получения соединения, которое достаточно стабильно для получения фармацевтически применимого соединения, которое может быть сформулировано в приемлемо стабильную фармацевтическую композицию. Соединения формулы I, характеризующиеся такой стабильностью, рассматриваются как попадающие в объем настоящего изобретения. Как будет отмечено специалистами в данной области техники, соединения по настоящему изобретению могут содержать один или несколько хиральных центров. Объем настоящего изобретения включает такие формы. Более того, как будет отмечено специалистами в данной области техники, соединение способно к эстерификации или гидролизу. Объем настоящего изобретения включает сложные эфиры и другие физиологически функциональные производные. Объем настоящего изобретения также включает таутомерные формы, а именно раскрытые здесь таутомерные "енолы". К тому же, объем настоящего изобретения включает формы пролекарства описанного здесь соединения. Соединения по настоящему изобретению могут кристаллизироваться в более чем одну форму, характеристика, известная как полиморфизм, и такие полиморфные формы ("полиморфы") находятся в пределах объема настоящего изобретения. Обычно полиморфизм может возникать как ответ на изменения температуры, давления или и того, и другого. Полиморфизм также может возникать из вариаций в процессе кристаллизации. Полиморфы могут отличаться различными физическими характеристиками,известными в данном уровне техники, такими как дифракционные рентгенограммы, растворимость и точка плавления. Определенные соединения, описанные в данном документе, содержат один или несколько хиральных центров, или в ином случае могут быть способны к существованию в виде множества стереоизомеров. Объем настоящего изобретения включает смеси стереоизомеров, а также очищенные энантиомеры или энантиомерно/диастереомерно обогащенные смеси. Также включены в объем настоящего изобретения отдельные изомеры соединений, представленных формулой настоящего изобретения, а также их любые полностью или частично равновесные смеси. Настоящее изобретение также включает отдельные изомеры соединений, представленных вышеуказанной формулой, как смеси с их изомерами, в которых преобразованы один или несколько хиральных центров. Выражение "хиральный" относится к молекулам, которые характеризуются свойством несверхналожения зеркального отражения, в то время как выражение "ахиральный" относится к молекулам, которые являются наложимыми со своим зеркальным отражением. Выражение "стереоизомеры" относится к соединениям, которые характеризуются идентичным химическим строением, но отличаются в части группировки атомов или групп в пространстве."Диастереомер" относится к стереоизомеру с двумя или более центрами хиральности, молекулы которого не являются зеркальными изображениями друг друга. Диастереомеры характеризуются различными физическими свойствами, например точками плавления, точками кипения, спектральными свойствами и реакционными способностями. Смеси диастереомеров могут быть разделены аналитическими методиками с высоким разрешением, такими как электрофорез и хроматография."Энантиомеры" относятся к двум стереоизомерам соединения, которые являются неналожимыми зеркальными изображениями друг друга. Используемые здесь стереохимические определения и преобразования в общем вытекают из S.P.Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds (1994) John WileySons, Inc., New York. Много органических соединений существуют в оптически активных формах, т.е. они характеризуются способностью вращать плоскость плоско-поляризованного света. В описании оптически активного соединения префиксы D и L или R и S используют для обозначения абсолютной конфигурации молекулы вокруг их хирального(ых) центра(ов). Префиксы d и I или (+) и (-) используют для обозначения признака вращения плоско-поляризованного света соединением, с (-) или I означающим, что соединение является левовращающимся. Соединение с префиксом (+) или d является правовращающимся. Для данной химической структуры эти стереоизомеры идентичны, за исключением того, что они являются зеркальными изображениями друг друга. Конкретный стереоизомер может называться энантиомером, и смесь таких изомеров часто называют энантиомерной смесью. Смесь 50:50 энантиомеров называют рацемической смесью или рацематом, который может возникать там, где не было стереоселекции или стереоспецифичности в химической реакции или процессе. Выражения "рацемическая смесь" и "рацемат" относятся к эквимолярной смеси двух энантиомерных образцов, лишенных оптической активности. Настоящее изобретение включает соль или сольват описанных здесь соединений, включая их комбинации, такие как сольват соли. Соединения по настоящему изобретению могут существовать в сольватированных, например гидратированных, а также несольватированных формах, и настоящее изобретение охватывает все такие формы. Типично, но не полностью, соли по настоящему изобретению представляют собой фармацевтически приемлемые соли. Соли, охватываемые выражением "фармацевтически приемлемые соли", относятся к нетоксическим солям соединений этого изобретения. Примеры подходящих фармацевтически приемлемых солей включают неорганические кислотноаддитивные соли, такие как хлорид, бромид, сульфат, фосфат и нитрат; органические кислотноаддитивные соли, такие как ацетат, галактарат, пропионат, сукцинат, лактат, гликолят, малат, тартрат,цитрат, малеат, фумарат, метансульфонат, п-толуолсульфонат и аскорбат; соли с кислой аминокислотой,такие как аспартат и глутамат; соли щелочных металлов, такие как соль натрия и соль калия; соли щелочно-земельных металлов, такие как соль магния и соль кальция; аммонийная соль; соли органических оснований, такие как соль триметиламина, соль триэтиламина, пиридиновая соль, пиколиновая соль, дициклогексиламиновая соль и N,N'-дибензилэтилендиаминовая соль; и соли с основной аминокислотой,такие как соль лизина и соль аргинина. Соли могут быть в некоторых случаях гидратами или сольватами этанола. Защитные группы. В контексте настоящего изобретения защитные группы включают фрагменты пролекарства и химические защитные группы. Защитные группы доступны, общеизвестны и используются, и необязательно используются для предупреждения побочных реакций с защитной группой во время методик синтеза, т.е. путей или способов получения соединений по настоящему изобретению. По большей части решение относительно того,какую из групп защищать, когда это сделать и природы химической защитной группы "PG", будет зависеть от химии реакции, от которой защищают (например, кислые, основные, окислительные, восстановительные или другие условия), и предназначенного направления синтеза. PG группы не должны быть и обычно не являются одинаковыми, если соединение замещено множеством PG. В основном, PG будет использоваться для защиты функциональных групп, таких как карбоксильная, гидроксильная, тио или аминогруппы и таким образом предупреждать побочные реакции или, в ином случае, облегчать эффективность синтеза. Порядок снятия защиты с получением свободных групп без защиты зависит от предполагаемого направления синтеза и встречающихся реакционных условий и могут происходить в любом порядке, определенном специалистом. Могут быть защищены различные функциональные группы соединений по настоящему изобретению. Например, защитные группы для ОН-групп (или гидроксил, карбоновая кислота, фосфоновая кислота или другие функциональные группы) включают "группы, образующие эфир или сложный эфир". Группы, образующие эфир или сложный эфир, способны функционировать как химические защитные группы в схемах синтеза, излагаемых в данном документе. Однако некоторые гидроксильные и тиозащитные группы не являются группами, образующими ни эфир, ни сложный эфир, как будет понятно специалистам в данной области техники, и включены с амидами, как обсуждалось ниже. Очень большое количество гидроксилзащитных групп и амидобразующих групп и соответствующих реакций химического расщепления описаны в Protective Groups in Organic Synthesis, Theodora W.Greene and Peter G.M. Wuts (John WileySons, Inc., New York, 1999, ISBN 0-471-16019-9) ("Greene"). См. также Kocienski, Philip J.; Protecting Groups (Georg Thieme Verlag Stuttgart, New York, 1994), который включен ссылкой во всей его полноте. В частности Chapter 1, Protecting Groups: An Overview, pages 1-20,Chapter 2, Hydroxyl Protecting Groups, pages 21-94, Chapter 3, Diol Protecting Groups, pages 95-117, Chapter 4, Carboxyl Protecting Groups, pages 118-154, Chapter 5, Carbonyl Protecting Groups, pages 155-184. Для защитных групп для карбоновой кислоты, фосфорной кислоты, фосфоната, сульфоновой кислоты и других защитных групп для кислот см. Greene, как изложено ниже. Такие группы включают в качестве примера и без ограничения сложные эфиры, амиды, гидразиды и т.п. Защитные группы, образующие эфир и сложный эфир. Защитные группы, образующие сложный эфир, включают: (1) фосфонатные группы, образующие сложный эфир, такой как сложные эфиры фосфонамидата, фосфоротиоатные сложные эфиры, фосфонатные сложные эфиры и фосфон-бис-амидаты; (2) карбоксильные группы, образующие сложный эфир, и(3) серные группы, образующие сложный эфир, такие как сульфонат, сульфат и сульфинат. Метаболиты соединений по настоящему изобретению. Также в объем этого изобретения попадают in vivo метаболические продукты соединений, описанных в данном документе. Такие продукты могут возникать, например, из окисления, восстановления,гидролиза, амидирования, эстерификации и т.п. введенного соединения, преимущественно вследствие ферментативного процесса. Соответственно, настоящее изобретение включает соединения, полученные способом, включающим контакт соединения этого изобретения с млекопитающим за период времени,достаточный для получения его метаболического продукта. Такие продукты типично устанавливаются путем получения меченного радиоактивным изотопом (например, С 14 или Н 3) соединения по настоящему изобретению, вводимого парентерально в определяемой дозе (например, более чем приблизительно 0,5 мг/кг) животному, такому как крыса, мышь, морская свинка, обезьяна, или человеку, обеспечивая достаточное время для возникновения метаболизма (типично от приблизительно 30 с до 30 ч), и выделяют продукты его преобразования из мочи, крови или других биологических образцов. Эти продукты легко выделяются, поскольку они мечены (другие выделяются путем применения антител, способных связывать эпитопы, сохранившиеся в метаболите). Структуры метаболита определяли традиционным способом, например путем анализа MS или ЯМР. В основном, анализ метаболитов выполняют таким же образом, что и традиционные изучения метаболизма лекарственного средства, хорошо известные специалистам данной области техники. Продукты преобразования, поскольку они иным образом не обнаруженыin vivo, применимы в диагностических анализах для терапевтического дозирования соединений настоящего изобретения, даже если они сами не обладают противоинфекционной активностью. Соединения формулы I. Определения и заместители для различного класса и подкласса настоящих соединений описаны и проиллюстрированы здесь. Специалист в данной области должен понимать, что любая комбинация определений и заместителей, описанных выше, не должна приводить к недействующим образцам или соединению. "Недействующие образцы или соединения" означают структуры соединения, которые нарушают соответствующие научные принципы (такие как, например, атом углерода, соединенный более чем четырьмя ковалентными связями), или соединения, слишком нестабильные для позволения выделения и формулирования в фармацевтически приемлемые лекарственные формы. Фармацевтические составы. Соединения этого изобретения сформулированы с традиционными носителями и наполнителями,которые будут выбраны в соответствии с обычной практикой. Таблетки будут содержать наполнители,глиданты, наполнители, связующие и т.п. Водные составы получали в стерильной форме, и если они предназначены для доставки отличным от перорального введением, обычно они будут изотоничными. Все составы необязательно будут содержать наполнители, такие как изложены в Handbook of Pharmaceutical Excipients (1986), здесь включены ссылкой во всей полноте. Наполнители включают аскорбиновую кислоту и другие антиоксиданты, хелатирующие средства, такие как EDTA, углеводы, такие как декстрин, гидроксиалкилцеллюлоза, гидроксиалкилметилцеллюлоза, стеариновая кислота и т.п., рН составов находится в диапазоне от 2 до приблизительно 11, но обычно приблизительно 7-10. Так как это возможно для активных ингредиентов вводиться отдельно, может быть предпочтительным их присутствие в виде фармацевтических составов. Составы по настоящему изобретению как для ветеринарного, так и для человеческого применения, содержат по меньшей мере один активный ингредиент, вместе с одним или несколькими приемлемыми носителями и необязательно другие терапевтические ингредиенты. Носитель(и) должен быть "приемлемым" в смысле его совместимости с другими ингредиентами состава и физиологически безопасным для получающего его пациента. Составы включают такие, которые подходят для вышеупомянутых путей введения. Составы условно могут находиться в стандартной лекарственной форме и могут быть получены любыми способами,хорошо известными в данном уровне техники фармацевтики. Техники и составы, в общем, обнаружены вRemington's Pharmaceutical Sciences (Mack Publishing Co., Easton, Pa.), включенный в настоящий документ ссылкой в своей полноте. Такие способы включают стадию введения активного ингредиента с носителем, который состоит из одного или нескольких вспомогательных ингредиентов. В основном составы приготовлены равномерно и тесно связаны с активным ингредиентом в жидких носителях или мелкодисперсных твердых носителях или обоих, и затем при необходимости придавали форму продукту. Составы настоящего изобретения, подходящие для перорального введения, могут быть представлены в виде дискретных компонентов, таких как капсулы, крахмальные капсулы или таблетки, каждый содержащий предварительно определенное количество активного ингредиента; в виде порошка или гранул; в виде раствора или суспензии в водной или неводной жидкости; или в виде жидкой эмульсии масло-вводе или жидкой эмульсии вода-в-масле. Активный ингредиент также может быть введен в виде болюса,электуария или пасты. Таблетку готовят при помощи сжатия или формовки, необязательно с одним или несколькими вспомогательными ингредиентами. Сжатые таблетки могут быть получены путем сжатия в подходящем устройстве активного ингредиента в свободно-сыпучей форме, такой как порошок или гранулы, необязательно смешанными со связующим, смазочным средством, инертным разбавителем, консервантом, поверхностно-активным или диспергирующим средством. Формованные таблетки могут быть образованы формованием в подходящем устройстве смеси порошкообразного активного ингредиента, увлажненного инертным жидким разбавителем. Таблетки необязательно могут быть покрыты или с желобками и необязательно сформулированы для обеспечения медленного или контролируемого высвобождения активного ингредиента. Для введения в глаз или другие наружные ткани, например рот и кожа, составы предпочтительно наносят в виде мази или крема местного действия, содержащих активный(е) ингредиент(ы) в количестве,например, 0,075-20% вес./вес. (включая активный(е) ингредиент(ы) в диапазоне от 0,1 до 20% с увеличением 0,1% вес./вес., таким как 0,6% вес./вес., 0,7% вес./вес. и т.д.), предпочтительно от 0,2 до 15% вес./вес. и наиболее предпочтительно от 0,5 до 10% вес./вес. Когда они сформулированы в виде мази,активные ингредиенты могут быть использованы или с парафинистой, или со смешиваемой с водой мазевой основой. Альтернативно, активные ингредиенты могут быть сформулированы в виде крема с кремовой основой масло-в-воде. При необходимости, водная фаза кремового основания может включать, например, по меньшей мере 30% вес./вес. многоатомного спирта, т.е. спирта, включающего две или несколько гидроксильных групп, таких как пропиленгликоль, бутан-1,3-диол, маннит, сорбит, глицерин и полиэтиленгликоль(включая PEG 400) и их смеси. Составы местного действия желательно включают соединение, которое усиливает поглощение или проникание активного ингредиента через кожу или другие пораженные зоны. Примеры таких усилителей кожного проникновения включают диметилсульфоксид и связанные аналоги. Масляная фаза эмульсий этого изобретения может составляться из известных ингредиентов известным способом. Поскольку фаза может содержать только эмульгатор (в ином случае известный как эмульгирующее вещество), она желательно содержит смесь по меньшей мере одного эмульгатора с жиром или маслом или и с жиром, и маслом. Предпочтительно гидрофильный эмульгатор включен вместе с липофильным эмульгатором, который действует как стабилизатор. Он также предпочтительно включает и масло, и жир. Вместе эмульгатор(ы) с или без стабилизатора(ов) образуют так называемый эмульгирующий воск, и воск вместе с маслом и жиром образуют так называемую эмульгирующую мазевую основу, которая образует масляную дисперсную фазу кремовых составов. Эмульгирующие вещества и стабилизаторы эмульсии, подходящие для применения в составе настоящего изобретения, включают Tween 60, Span 80, цетостеариловый спирт, бензиловый спирт, миристиловый спирт, глицерилмоностеарат и натрия лаурилсульфат. Выбор подходящих масел или жиров для состава лежит в основе достижения желаемых косметических свойств. Крем должен быть предпочтительно нежирным, непачкающим и смываемым продуктом подходящей консистенции для избегания протекания из трубок или других контейнеров. Могут быть использованы моно- или двухосновные алкильные сложные эфиры с неразветвленной или разветвленной цепью, такие как диизоадипат, изоцетилстеарат, пропиленгликолевый диэфир кокосовых жирных кислот,изопропилмиристат, децилолеат, изопропилпальмитат, бутилстеарат, 2-этилгексилпальмитат или смесь сложных эфиров с разветвленной цепью, известных как Crodamol CAP, последние три являлись предпочтительными сложными эфирами. Они могут использоваться отдельно или в комбинации в зависимости от требуемых свойств. Альтернативно, используются липиды с высокой точкой плавления, такие как белый мягкий парафин и/или жидкий парафин или другие минеральные масла. Фармацевтические составы по данному изобретению содержат одно или несколько соединений настоящего изобретения вместе с одним или несколькими фармацевтически приемлемыми носителями или наполнителями и необязательно другими терапевтическими средствами. Фармацевтические составы,содержащие активный ингредиент, могут быть в любой форме, подходящей для предполагаемого способа введения. Для перорального применения, например, могут быть получены таблетки, пастилки, лепешки, водные или масляные суспензии, диспергируемые порошки или гранулы, эмульсии, жесткие или мягкие капсулы, сиропы или эликсиры. Композиции для перорального применения могут быть получены согласно любому способу, известному в технике для изготовления фармацевтических композиций, и такие композиции могут содержать одно или несколько средств, включая подсластители, ароматизирующие средства, красящие вещества и консерванты, для обеспечения приятного на вкус препарата. Таблетки, содержащие активный ингредиент в смеси с нетоксическим фармацевтически приемлемым наполнителем, который подходит для изготовления таблеток, являются приемлемыми. Этими наполнителями могут быть, например, инертные разбавители, такие как карбонат кальция или натрия, лактоза, моногидрат лактозы, кроскармелоза натрия, повидон, фосфат кальция или натрия; средства для гранулирования и дезинтегрирования, такие как маисовый крахмал или альгиновая кислота; связующие средства, такие как целлюлоза, микрокристаллическая целлюлоза, крахмал, желатин или камедь; и смазывающие средства,такие как стеарат магния, стеариновая кислота или тальк. Таблетки могут быть непокрытыми или могут быть покрытыми известными методиками, включая микроинкапсулирование для замедленной дезинте- 12020488 грации и поглощения в желудочно-кишечном тракте, и таким образом обеспечивается пролонгированное действие за более длительный период. Например, может применяться материал с временной задержкой,такой как глицерилмоностеарат или глицерилдистеарат отдельно или с воском. Составы для перорального применения также могут быть представлены в качестве жестких желатиновых капсул, где активный ингредиент смешан с инертным жидким разбавителем, например фосфатом кальция или каолином, или в качестве мягких желатиновых капсул, где активный ингредиент смешан с водой или масляной средой, такой как арахисовое масло, жидкий парафин или оливковое масло. Водные суспензии настоящего изобретения содержат активные материалы в смеси с наполнителями, подходящими для изготовления водных суспензий. Такие наполнители включают суспендирующее средство, такое как натрийкарбоксиметилцеллюлоза, метилцеллюлоза, гидроксипропилметилцеллюлоза,натрия альгинат, поливинилпирролидон, трагакантовая камедь и гуммиарабик, и диспергирующие или смачивающие средства, такие как встречающийся в природе фосфатид (например, лецитин), продукт конденсации алкиленоксида с жирной кислотой (например, полиоксиэтиленстеарат), продукт конденсации этиленоксида с длинноцепочечным алифатическим спиртом (например, гептадекаэтиленоксицетанол), продукт конденсации этиленоксида с неполным сложным эфиром, полученным из жирной кислоты и гекситангидрида (например, полиоксиэтиленсорбитанмоноолеат). Водная суспензия также может содержать один или несколько консервантов, таких как этил или н-пропил п-гидроксибензоат, одно или несколько красящих веществ, одно или несколько ароматизирующих средств и один или несколько подсластителей, таких как сахароза или сахарин. Масляные суспензии могут быть составлены путем суспендирования активного ингредиента в растительном масле, таком как арахисовое масло, оливковое масло, кунжутное масло или кокосовое масло,или в минеральном масле, таком как жидкий парафин. Пероральные суспензии могут содержать загуститель, такой как пчелиный воск, твердый парафин или цетиловый спирт. Изложенные здесь подсластители и ароматизирующие средства могут быть добавлены с обеспечением приятного на вкус перорального препарата. Эти композиции могут быть защищены путем добавления антиоксиданта, такого как аскорбиновая кислота. Диспергируемые порошки и гранулы настоящего изобретения, подходящие для получения водной суспензии путем добавления воды, обеспечивают активный ингредиент в смеси с диспергирующим или смачивающим средством, суспендирующим средством и одним или несколькими консервантами. Подходящие диспергирующие или смачивающие средства и суспендирующие средства представлены в примерах выше. Могут быть представлены дополнительные наполнители, например, подсластители, ароматизирующие и красящие вещества. Фармацевтические композиции настоящего изобретения также могут быть в форме эмульсий масло-в-воде. Масляной фазой может быть растительное масло, такое как оливковое масло или арахисовое масло, минеральное масло, такое как жидкий парафин, или их смесь. Подходящие эмульгирующие средства включают камеди природного происхождения, такие как гуммиарабик и трагакантовая камедь,встречающиеся в природе фосфатиды, такие как соевый лецитин, сложные эфиры или неполные сложные эфиры, полученные из жирных кислот и ангидридов гекситола, такой как сорбитанамоноолеат, и продукты конденсации этих неполных сложных эфиров с этиленоксидом, такие как полиоксиэтилена сорбинана моноолеат. Эмульсия может также содержать подсластители и ароматизирующие средства. Сиропы и эликсиры могут быть сформулированы с подсластителями, такими как глицерин, сорбит или сахароза. Такие составы также могут содержать смягчители, консервант, ароматизатор или красящее вещество. Фармацевтические композиции настоящего изобретения могут находиться в форме стерильного впрыскиваемого препарата, такого как стерильная впрыскиваемая водная или маслосодержащая суспензия. Эта суспензия может быть сформулирована согласно известному уровню техники с применением подходящих диспергирующих или смачивающих средств и суспендирующих средств, упомянутых здесь. Стерильный впрыскиваемый препарат также может быть стерильным впрыскиваемым раствором или суспензией в нетоксическом парентерально приемлемом разбавителе или растворителе, таком как раствор в 1,3-бутандиоле, или полученный в качестве лиофилизированного порошка. Среди возможных применяемых приемлемых носителей и растворителей присутствует вода, раствор Рингера и изотонический раствор хлорида натрия. К тому же, стерильные жирные масла обычно могут использоваться в качестве растворителя или суспендирующей среды. С этой целью может использоваться любая смесь стерильного масла, включая синтетические моно- или диглицериды. К тому же жирные кислоты, такие как олеиновая кислота, могут аналогичным образом использоваться при получении впрыскиваемых препаратов. Количество активного ингредиента, которое может быть объединено с материалом-носителем с получением одной лекарственной формы, будет изменяться в зависимости от хозяина, которого лечат, и конкретного пути введения. Например, состав замедленного высвобождения, предназначенный для перорального введения людям, может содержать приблизительно 1-1000 мг активного материала, смешанного с подходящим и пригодным количеством материала-носителя, которое может изменяться от приблизительно 5 до приблизительно 95% всего веса композиции (вес./вес.). Фармацевтическая композиция может быть получена для обеспечения более легкоизмеряемых количеств для введения. Например, водный раствор, предназначенный для внутривенного введения, может содержать от приблизительно 3 до 500 мкг активного ингредиента на 1 мл раствора для того, чтобы могло возникать вливание подходящего объема при скорости от приблизительно 30 мл/ч. Составы, подходящие для введения в глаз, включают глазные капли, где активный ингредиент растворен или суспендирован в подходящем носителе, особенно в водном растворителе для активного ингредиента. Активный ингредиент предпочтительно присутствует в таких составах в концентрации 0,520%, преимущественно 0,5-10%, в частности приблизительно 1,5% вес./вес. Составы, подходящие для местного введения в рот, включают лепешки, содержащие активный ингредиент в ароматизированной основе, обычно сахароза и камедь или трагакант; пастилки, содержащие активный ингредиент в инертном основании, таком как желатин и глицерин или сахароза и камедь; и ополаскиватели, содержащие активный ингредиент в подходящем жидком носителе. Составы для ректального введения могут присутствовать в суппозитории с подходящим основанием, содержащим, например, масло какао или салицилат. Составы, подходящие для внутрилегочного или назального введения, характеризовались размером частиц, например, в диапазоне от 0,1 до 500 мкм (включая размеры частиц в диапазоне от 0,1 до 500 мкм с шагом, таким как 0,5, 1, 30, 35 мкм и т.д.), которые вводились быстрой ингаляцией через носовой канал или путем ингаляции через рот так, чтобы достичь альвеолярных мешочков. Подходящие составы включают водные или масляные растворы активного ингредиента. Составы, подходящие для аэрозольного введения, или в виде сухого порошка могут быть получены общепринятыми способами и могут быть доставлены с другими терапевтическими средствами, такими как соединения, прежде используемые при лечении или профилактике инфекций, как описано в данном документе. Составы, подходящие для вагинального введения, могут присутствовать в виде составов пессариев,тампонов, кремов, гелей, паст, пен или спреев, содержащих вдобавок к активному ингредиенту такие подходящие носители, которые известны в данном уровне техники. Составы, подходящие для парентерального введения, включают водные и неводные стерильные инъекционные растворы, которые могут содержать антиоксиданты, буферы, бактериостатические факторы и растворы, которые делают состав изотоническим с кровью предполагаемого реципиента; и водные,и неводные стерильные суспензии, которые могут включать суспендирующие средства и загустители. Составы представлены в контейнерах с однократной дозой или множественными дозами, например запаянные ампулы и пробирки, и могут храниться при условиях сушки сублимацией (лиофилизированный), при которых требуется добавление стерильного жидкого носителя, например воды для инъекции,сразу перед применением. Неподготовленные растворы и суспензии для инъекций получали из стерильных порошков, гранул и таблеток ранее описанного вида. Предпочтительные стандартные лекарственные составы содержат ежедневную дозу или единичную ежедневную субдозу, как было сказано выше, или их соответствующую фракцию активного ингредиента. Нужно понимать, что вдобавок к конкретно вышеупомянутым ингредиентам составы по настоящему изобретению могут включать другие средства, обычно применяемые в данном уровне техники, относящиеся к типу рассматриваемого состава, например подходящие для перорального введения, могут включать ароматизирующие средства. Соединения по настоящему изобретению также могут быть составлены для обеспечения контролируемого высвобождения активного ингредиента, чтобы позволить менее частое дозирование или чтобы улучшить фармакокинетический профиль или профиль токсичности активного ингредиента. Соответственно, настоящее изобретение также обеспечивает композиции, содержащие одно или несколько соединений по настоящему изобретению, составленные для длительного или контролируемого высвобождения. Эффективная доза активного ингредиента зависит, по меньшей мере, от природы состояния, которое лечат, токсичности, будет ли соединение использоваться профилактически (более низкие дозы) или против активного заболевания или состояния, способа его доставки и фармацевтического состава, и будет определяться врачом с применением обычных изучений увеличения дозы. Ожидаемая эффективная доза может быть от приблизительно 0,0001 до приблизительно 1000 мг/кг веса тела в день. Например,ежедневная возможная доза для взрослого человека, у которого вес тела приблизительно 70 кг, будет приблизительно в диапазоне от 0,05 до приблизительно 100 мг, или от приблизительно от 0,1 до приблизительно 25 мг, или от приблизительно 0,4 до приблизительно 4 мг и может принимать форму одной или множественных доз. В еще одном варианте осуществления настоящая заявка раскрывает фармацевтические композиции,содержащие соединение формулы I или его фармацевтически приемлемую соль, и фармацевтически приемлемый носитель или наполнитель. Пути введения. Одно или несколько соединений по настоящему изобретению (здесь называются активными ингредиентами) вводят таким путем, который подходит для состояния, которое лечат. Подходящие пути включают пероральный, ректальный, назальный, местный (включая буккальный и сублингвальный), ва- 14020488 гинальный и парентеральный (включая подкожный, внутримышечный, внутривенный, внутрикожный,интратекальный и эпидуральный) и т.п. Будет отмечено, что предпочтительный путь может изменяться,например, с состоянием реципиента. Преимущество соединений настоящего изобретения в том, что они перорально биологически доступные и могут дозироваться перорально. Комбинированная терапия. В одном варианте осуществления соединения по настоящему изобретению применяют в комбинации с дополнительными активными терапевтическим ингредиентом или средством. В одном варианте осуществления комбинации соединений Формулы I и дополнительных активных средств могут быть выбраны для лечения пациентов с вирусной инфекцией, например, HBV, HCV илиHIV инфекцией. Применимые активные терапевтические средства для HBV включают ингибиторы обратной транскриптазы, такие как ламивудин (Epivir), адефовир (Hepsera), тенофовир (Viread), телбивудин(Tyzeka), энтекавир (Baraclude) и Clevudine. Другие применимые активные терапевтические средства включают иммуномодуляторы, такие как интерферон -2b (Intron А), пегилированный интерферон-2 а (Pegasys), интерферон -2 а (Roferon), интерферон -N1, преднизон, преднизолон, Thymalfasin,агонисты рецепторов ретиноевой кислоты, 4-метилумбеллиферон, Alamifovir, Metacavir, Albuferon,агонисты TLR (например, TLR-7 агонисты) и цитокины. Что касается лечения HCV, неограничивающие примеры подходящих комбинаций включают комбинации одного или нескольких соединений по настоящему изобретению с одним или несколькими интерферонами, рибавирином или его аналогами, ингибиторами HCV NS3 протеазы, ингибиторами глюкозидазы 1, гепатопротекторами, нуклеозидными или нуклеотидными ингибиторами HCV NS5B полимеразы, ненуклеозидными ингибиторами HCV NS5B полимеразы, ингибиторами HCV NS5A, TLR-7 агонистами, ингибиторами циклофилина, ингибиторами IRES HCV, фармакокинетическими энхансерами и другими лекарственными средствами для лечения HCV. Более конкретно, одно или несколько соединений по настоящему изобретению могут объединяться с одним или несколькими соединениями, выбранными из группы, включающей: 1) интерфероны, например пегилированный rIFN2b (PEG-Intron), пегилированный rIFN- -2 аMitoQ,6) нуклеозидные или нуклеотидные ингибиторы HCV NS5B полимеразы, например, R1626, R7128(R4048), IDX184, IDX-102, PSI-7851, ВСХ-4678, валопицитабин (НМ-283) и MK-0608,7) ненуклеозидные ингибиторы HCV NS5B полимеразы, например филибувир (PF-868554), АВТ 333, АВТ-072, BI-207127, VCH-759, VCH-916, JTK-652, MK-3281, VBY-708, VCH-222, A848837, ANA598, GL60667, GL59728, А-63890, А-48773, А-48547, ВС-2329, VCH-796 (несбувир), GSK625433, BILN1941, XTL-2125 и GS-9190,8) ингибиторы NS5A HCV, например AZD-2836 (A-831), AZD-7295 (А-689) и BMS-790052,9) TLR-7 агонисты, например имиквимод, 852 А, GS-9524, ANA-773, ANA-975, AZD-8848 (DSP3025), PF-04878691 и SM-360320,10) ингибиторы циклофилина, например DEBIO-025, SCY-635 и NIM811,11) ингибиторы IRES HCV, например MCI-067,12) фармакокинетические энхансеры, например BAS-100, SPI-452, PF-4194477, ТМС-41629, GS9350, GS-9585 и рокситромицин,13) другие лекарственные средства для лечения HCV, например тимозин -1 (Zadaxin), нитазоксанид (Alinea, NTZ), BIVN-401 (виростат), PYN-17 (алтирекс), KPE02003002, актилон (CPG-10101), GS9525, KRN-7000, цивацир, GI-5005, XTL-6865, BIT225, РТХ-111, ITX2865, TT-033i, ANA 971, NOV-205,тарвацин, ЕНС-18, VGX-410C, EMZ-702, AVI 4065, BMS-650032, BMS-791325, бавитуксимаб, MDX1106 (ONO-4538), оглуфанид, FK-788 и VX-497 (меримеподиб). К тому же соединения по настоящему изобретению могут применяться в комбинации с другими терапевтическими средствами для лечения или профилактики HIV или AIDS и/или одного или нескольких других заболеваний, которые присутствуют у субъекта, страдающего от HIV или AIDS (например, бак- 15020488 териальные и/или грибковые инфекции, другие вирусные инфекции, такие как гепатит В или гепатит С,или рак, такой как саркома Капоши). Дополнительное(ые) терапевтическое(ие) средство(а) может быть скомбинировано с одной или несколькими солями по настоящему изобретению (например, скомбинированы в таблетке). В одном варианте осуществления неограничивающие примеры подходящих комбинаций включают комбинации одного или нескольких соединений по настоящему изобретению с одним или несколькими ингибиторами HIV протеазы, HIV ненуклеозидными ингибиторами обратной транскриптазы, HIV нуклеозидными ингибиторами обратной транскриптазы, HIV нуклеотидными ингибиторами обратной транскриптазы, HIV интегразными ингибиторами, gp41 ингибиторами, CXCR4 ингибиторами, ингибиторами входа, gp120 ингибиторами, G6PD и NADH-оксидазными ингибиторами, CCR5 ингибиторами, CCR8 ингибиторами, RNазы H ингибиторами, ингибиторами созревания, фармакокинетическими энхансерами и другими лекарственными средствами для лечения HIV. Более конкретно, одно или несколько соединений по настоящему изобретению могут объединяться с одним или несколькими соединениями, выбранными из группы, включающей: 1) ингибиторы HIV протеазы, например ампренавир (Agenerase), атазанавир (Reyataz), фосампренавир (Lexiva), индинавир (Crixivan), лопинавир, ритонавир (norvir), нелфинавир (Viracept), саквинавир(PPL-100), DG35, и AG 1859, SPI-256, ТМС 52390, PL-337, SM-322377, SM-309515, GRL-02031, CRS-074,CRS-075, KB-98 и А-790742,2) HIV ненуклеозидные ингибиторы обратной транскриптазы, например каправирин, эмивирин, делавиридин (Rescriptor), эфавиренз (Sustiva), невирапин (Viramune), (+)-каланолид А, каланолид В, этравирин (Intelence), GW5634, DPC-083, DPC-961, DPC-963, MIV-150, MIV-160, MIV-170, дапивирин (ТМС 120), рилпивирин (ТМС-278), BILR 355 BS, VRX 840773, UK-453061, и RDEA806, RDEA 427, RDEA 640,IDX 899, ANX-201 (Thiovir), R-1206, LOC-dd, IQP-0410 (SJ-3366), YM-215389, YM-228855, CMX-052 иCMX-182,3) нуклеозидные ингибиторы обратной транскриптазы HIV, например зидовудин (Retrovir), эмтрицитабин (Emtriva), диданозин (Videx), ставудин (Zerit), залцитабин (Hivid), ламивудин (Epivir), абакавирFTC, PSI-5004), D-d4FC, фосфазид, фозивудин тидоксил, априцитибин (AVX754, SPD-754), GS-7340, KP1461, AVX756, ОВР-601, диоксолантимин, ТМС-254072, INK-20, PPI-801, PPI-802, MIV-410, 4'-Ed4T, B108 и фозалвудинтидоксил (HDP 99.0003),4) нуклеотидные ингибиторы обратной транскриптазы HIV, например тенофовир дизопроксил фумарат (Viread) и адефовир дипивоксил,5) HIV интегразные ингибиторы, например куркумин, производные куркумина, цикориевая кислота, производные цикориевой кислоты, 3,5-дикаффеолихиновая кислота, производные 3,5 дикаффеолихиновой кислоты, ауринтрикарбоновая кислота, производные ауринтрикарбоновой кислоты,фенэтиловый сложный эфир кофеиновой кислоты, производные фенэтилового сложного эфира кофеиновой кислоты, тирфорстин, производные тирфорстина, кверцетин, производные кверцетина, S-1360, зинтевир (AR-177), L-870812 и L-870810, ралтегравир (Isentress, MK-0518), элвитегравир (GS-9137), BMS538158, GSK364735C, BMS-707035, MK-2048, GSK-349572 (S-349572), GSK-265744 (S-265744), GSK247303 (S-247303), S-1360 (GW810871), 1,5-DCQA, INH-001, INT-349, V-165, RIN-25, BFX-1001, BFX1002, BFX-1003, RSC-1838, ВСН-33040 и ВА 011,6) gp41 ингибиторы, например энфувиртид (Fuzeon), сифувертид, MPI-451936, FB006M, А-329029 иCCR5mAb004,12) CCR8 ингибиторы, например ZK-756326,13) РНазы Н ингибиторы, например ODN-93 и ODN-112,14) ингибиторы созревания, например бевиримат (РА-457), РА-040, МРС-9055 (vicecon, MPI49839), АСН-100703, АСН-100706,15) фармакокинетические энхансеры, например BAS-100, SPI-452, PF-4194477, ТМС-41629, GS9350, GS-9585 и рокситромицин,16) другие лекарственные средства для лечения HIV, например REP 9, SP-01A, TNX-355, DES6,- 16020488ODN-93, ODN-112, VGV-1, амплиген, HRG214, цитолин, VGX-410, VGX-820, KD-247, AMZ 0026, CYT 99007, А-221 HIV, HPH-116, DEBIO-025, BAY 50-4798, MDX010 (ипилимумаб), PBS 119, BIT-225, UBT8147, ITI-367, AFX-400, BL-1050, GRN-139951, GRN-140665, АХ-38679, RGB-340638, PPI-367 и ALG 889. Если нарушением является рак, рассматривается комбинация по меньшей мере с одной противораковой терапией. В частности, при антираковой терапии рассматривается комбинация с другим противоопухолевым средством (включая химиотерапевтические, гормональные средства или средства на основе антител), а также комбинация с хирургической терапией и лучевой терапией. Комбинационные терапии по данному изобретению, таким образом, включают введение по меньшей мере одного соединения формулы (I) или его соли или сольвата и применение по меньшей мере одного другого способа лечения рака. Предпочтительно комбинационные терапии по данному изобретению включают введение по меньшей мере одного соединения формулы (I) или его соли или сольвата и по меньшей мере одного другого фармацевтически активного средства, предпочтительно противоопухолевого средства. Соединение(я) формулы (I и другое(ие) фармацевтически активное(ые) средство(а) могут быть введены вместе или отдельно и, при введении отдельно, они могут проходить одновременно или последовательно в любом порядке (включая введение в разные дни согласно режиму терапии) и любым подходящим путем. Количества соединения(й) формулы (I) и другого(их) фармацевтически активного(ых) средства(в) и относительные сроки введения будут выбраны для достижения желаемого эффекта комбинированной терапии. В одном варианте осуществления дополнительная противораковая терапия включает по меньшей мере одно дополнительное противоопухолевое средство. Любое противоопухолевое средство, характеризующееся активностью против допускаемой лечимой опухоли, можно использовать в комбинации. Типичные применимые противоопухолевые средства включают без ограничения средства антимикроканальцев, такие как дитерпеноиды и алкалоид барвинка; платиновые координационные комплексы; алкилирующие средства, такие как азотистые иприты, оксазафосфолины, алкилсульфонаты, нитрозомочевины и триазены; антибиотические средства, такие как антрациклины, актиномицины и блеомицины; ингибиторы топоизомеразы II, такие как эпидофиллотоксины; антиметаболиты, такие как аналоги пурина и пиримидина, и антифолатные соединения; ингибиторы топоизомеразы I, такие как камптотецины; гормоны и гормональные аналоги; ингибиторы пути сигнальной трансдукции; ингибиторы ангиогенеза нерецепторной тирозинкиназы; иммунотерапевтические средства; проапоптозные средства; и ингибиторы сигналинга клеточного цикла. Антимикроканальцевые или антимитотические средства являются фазоспецифическими средствами, активными против микроканальцев опухолевых клеток во время фазы М или деления клеток при клеточном цикле. Примеры антимикроканальцевых средств включают без ограничения дитерпеноиды и алкалоиды барвинка. Дитерпеноиды, полученные из природных источников, являются фазоспецифическими противораковыми средствами, которые действуют при G2/M фазах клеточного цикла. Полагали, что дитерпеноиды стабилизируют подгруппу -тубулина микроканальцев, путем связывания с этим белком. Распад белка,как оказывается, ингибирован митозом, который подавлен, и последующей гибелью клеток. Примеры дитерпеноидов включают без ограничения паклитаксел и его аналог доцетаксел. Паклитаксел, 5,20-эпокси-1,2,4,7,10,13-гексагидрокситакс-11-ен-9-он 4,10-диацетат 2-бензоат 13-сложный эфир с (2R,3S)-N-бензоил-3-фенилизосерином; является природным продуктом дитерпена,выделенного из тиса тихого Taxus brevifolia и является коммерчески доступным в виде инъецируемого раствора TAXOL. Он является членом таксанового семейства терпенов. Паклитаксел был одобрен для клинического применения при лечении рефракторного рака яичника в США (Markman et al., Yale Journalof Biology and Medicine, 64:583, 1991; McGuire et al., Ann. Intern, Med., 11 1:273, 1989) и для лечения рака молочной железы (Holmes et al., J. Nat. Cancer Inst., 83:1797,1991.) Он является перспективным кандидатом для лечения опухолей на коже (Einzig et. al., Proc. Am. Soc. Clin. Oncol., 20:46) и карцином головы и шеи (Forastire et al., Sem. Oncol., 20:56, 1990). Соединение также показывает возможность лечения поликистозного заболевания почки (Woo et al., Nature, 368:750. 1994), рака легких и малярии. Лечение пациентов паклитакселом приводит к подавлению деятельности костного мозга (множественная последовательность клеточных поколений, Ignoff, R.J. et al, Cancer Chemotherapy Pocket GuideA 1998), связанному с длительностью дозирования выше пороговой концентрации (50 нМ) (Kearns, C.M. et al., Seminars in Oncology, 3(6) p. 16-23, 1995). Доцетаксел, (2R,3S)-N-карбокси-3-фенилизосерин,N-te/f-бутиловый сложный эфир, 13-сложный эфир с 5-20-эпокси-1,2,4,7,10,13-гексагидрокситакс-11-ен-9-он 4-ацетат 2-бензоат, тригидрат; является коммерчески доступным в виде инъецируемого раствора TAXOTERE. Доцетаксел предназначен для лечения рака молочной железы. Доцетаксел является полусинтетическим производным паклитаксела, см. полученный с применением природного предшественника, 10-деацетилбаккатина III, экстрагированного из иголки дерева тиса европейского. Алкалоиды барвинка являются фазоспецифическими противоопухолевыми средствами, полученными из растения барвинка. Алкалоиды барвинка действуют при фазе М (митозе) клеточного цикла пу- 17020488 тем связывания, в частности, с тубулином. Следовательно, молекула связанного тубулина не способна полимеризироваться в микроканальцах. Полагали, что митоз был ингибирован в метафазе после гибели клеток. Примеры алкалоидов барвинка включают без ограничения винбластин, винкристин и винорелбин. Винбластин, винкалейкобластин сульфат, является коммерчески доступным как VELBAN в виде инъецируемого раствора. Хотя его можно обозначить как вторую линию терапии различных солидных опухолей, в первую очередь, он обозначен для лечения рака яичка и различных лимфом, включая болезнь Ходжкина; и лимфоцитарных и гистиоцитарных лимфом. Миелосупрессия представляет собой дозолимитирующий побочный эффект винбластина. Винкристин, винкалейкобластин, 22-оксо-, сульфат,является коммерчески доступным как ONCOVIN в виде инъецируемого раствора. Винкристин обозначен для лечения острых лейкемий и также применяют в схемах, схема лечения ходжкиновских и неходжкиновских злокачественных лимфом. Облысение и неврологические эффекты являются самыми распространенными побочными эффектами винкристина, и в меньшей степени возникают эффекты миелосупрессия и мукозит желудочно-кишечного тракта. Винорелбин, 3',4'-дидегидро-4'-дезокси-С'-норвинкалейкобластин [R-(R,R)-2,3-дигидроксибутандиоат (1:2)(соль)], коммерчески доступный в виде инъецируемого раствора винорелбина тартрата (NAVELBINE), является полусинтетическим алкалоидом барвинка. Винорелбин указан в виде единственного средства или в комбинации с другими химиотерапевтическими средствами, такими как цисплатин,при лечении разных солидных опухолей, особенно немелкоклеточного рака легкого, запущенного рака молочной железы и гормон-рефрактерного рака предстательной железы. Миелосупрессия является наиболее распространенным дозоограничивающим побочным эффектом винорелбина. Платиновые координационные комплексы представляют собой нефазоспецифические противораковые средства, которые взаимодействуют с ДНК. Платиновые комплексы вводят в опухолевые клетки,подвергают гидратации, и образуются внутренние и поперечные сшивания в ДНК с вызовом неблагоприятных биологических эффектов на опухоли. Примеры платиновых координационных комплексов включают без ограничения оксалиплатин, цисплатин и карбоплатин. Цисплатин, цисдиаминдихлорплатина, коммерчески доступный как PLATINOL в виде инъекционного раствора. Цисплатин прежде всего предназначен для лечения метастатического семенникового рака, рака яичника и запущенного рака мочевого пузыря. Карбоплатин, платина, диамин [1,1-цикл обутан-дикарбоксилат(2-)О,О'], является коммерчески доступным как PARAPLATIN в виде инъекционного раствора. Карбоплатин прежде всего указан в первой и второй линии лечения запущенного рака мочевого пузыря. Алкилирующие средства являются нефазоспецифическими противораковыми средствами и сильными электрофилами. Типично, путем алкилирования алкилирующие средства образуют ковалентные сцепления с ДНК через нуклеофильные фрагменты молекулы ДНК, такие как фосфат, амино, сульфогидрил, гидроксил, карбоксил и имидазольные группы. Такое алкилирование разрушает функцию нуклеиновой кислоты, приводя к гибели клеток. Примеры алкилирующих средств включают без ограничения азотистые иприты, такие как циклофосфамид, мелфалан и хлорамбуцил; алкилсульфонаты, такие как бусульфан; нитрозомочевины, такие как кармустин; и триазены, такие как дакарбазин. Циклофосфамид, 2[бис(2-хлорэтил)амино]тетрагидро-2 Н-1,3,2-оксазафосфорин 2-оксидмоногидрат, коммерчески доступный в виде инъекционного раствора или таблеток как CYTOXAN. Циклофосфамид представлен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами при лечении злокачественных лимфом, множественной миеломы и лейкемий. Мелфалан, 4-[бис(2-хлорэтил)амино]-Lфенилаланин, является коммерчески доступным в виде инъекционного раствора или таблеток, как ALKERAN. Мелфалан представлен для паллиативного лечения множественной миеломы и нерезектабельной эпителиальной карциномы яичника. Подавление деятельности костного мозга является самым распространенным дозолимитирующим побочным эффектом мелфалана. Хлорамбуцил, 4-[бис(2 хлорэтил)амино]бензолбутановая кислота, коммерчески доступный в виде таблеток LEUKERAN. Хлорамбуцил предназначен для паллиативного лечения хронического лимфолейкоза и злокачественных лимфом, таких как лимфосаркома, гигантофолликулярная лимфома и болезнь Ходжкина. Бусульфан, 1,4 бутандиолдиметансульфонат, коммерчески доступен как таблетки MYLERAN. Бусульфан предназначен для паллиативного лечения хронической миелогенной лейкемии. Кармустин, 1,3-[бис(2-хлорэтил)]-1-нитрозомочевина, коммерчески доступен в виде одной ампулы с лиофилизированным материалом, как BiCNU. Кармустин предназначен для паллиативного лечения в виде единственного средства или в комбинации с другими средствами для опухолей мозга, множественной миеломы, болезни Ходжкина и неходжкинских лимфом. Дакарбазин, 5-(3,3-диметил-1-триазено)имидазол-4-карбоксамид, коммерчески доступен в виде одной ампулы с материалом DTIC-Dome. Дакарбазин предназначен для лечения метастатической злокачественной меланомы и в комбинации с другими средствами для второй линии лечения болезни Ходжкина. Противоопухолевые антибиотики представляют собой нефазоспецифические средства, которые связываются или внедряются в ДНК. Типично, такое действие приводит к стабильным комплексам ДНК или разрыву нити, что разрушает обычную функцию нуклеиновых кислот, приводя к гибели клеток. Примеры антибиотических противоопухолевых средств включают без ограничения актиномицины, такие как дактиномицин, антроциклины, такие как даунорубицин и доксорубицин; и блеомицины. Дактиномицин, также известный как актиномицин D, коммерчески доступен в инъецируемой форме как COSMEGEN. Дактиномицин предназначен для лечения опухоли Вилма и рабдомиосаркомы. Даунорубицин,(8S-цис-)-8-ацетил-10-[(3-амино-2,3,6-тридеоксиL-ликсогексопиранозил)окси]-7,8,9,10 тетрагидро-6,8,11-тригидрокси-1-метокси-5,12-нафтацендион гидрохлорид, коммерчески доступен в липосомальной инъецируемой форме как DAUNOXOME или в инъецируемой как CERUBIDINE. Даунорубицин предназначен для индукции ремиссии при лечении острого нелимфоидного лейкоза и запущенной саркомы Капоши, связанной с HIV. Доксорубицин, (8S,10S)-10-[(3-амино-2,3,6-тридеоксиLликсогексопиранозил)окси]-8-гликолоил,7,8,9,10-тетрагидро-6,8,11-тригидрокси-1-метокси-5,12 нафтацендион гидрохлорид, коммерчески доступен в инъецируемой форме как RUBEX или ADRIAMYCINRDF. Доксорубицин преимущественно предназначен для лечения острой лимфобластной лейкемии и острой миелобластной лейкемии, а также он является применимым компонентом при лечении некоторых солидных опухолей и лимфом. Блеомицин, смесь цитотоксических гликопептидных антибиотиков, выделенных из штамма Streptomyces verticillus, коммерчески доступен как BLENOXANЕ. Блеомицин предназначен для паллиативного лечения в виде единственного средства или в комбинации с другими средствами плоскоклеточной карциномы, лимфом и семенниковых карцином. Ингибиторы топоизомеразы II включают без ограничения эпидофиллотоксины. Эпидофиллотоксины являются фазоспецифическими противоопухолевыми средствами, полученными из растения мандрагоры. Эпидофиллотоксины типично воздействуют на клетки в фазах S и G2 клеточного цикла образованием тройного комплекса с топоизомеразой II и ДНК, вызывая разрыв нити ДНК. Разрывы нити нарастают, и затем клетки гибнут. Примеры эпидофиллотоксинов включают без ограничения этопозид и тенипозид. Этопозид, 4'-диметилэпиподофиллотоксин 9[4,6-0-(R)-этилиденD-глюкопиранозид], коммерчески доступен в виде инъекционного раствора или капсул как VePESID и общеизвестный как VP-16. Этопозид предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения семенникового и немелкоклеточного легочного рака. Тенипозид, 4'деметилэпиподофиллотоксин 9[4,6-0-(R)-тенилиденD-глкжопиранозид], коммерчески доступен в виде инъекционного раствора как VUMON и общеизвестный как VM-26. Тенипозид предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения острой лейкемии у детей. Антиметаболитические опухолевые средства являются фазоспецифическими противоопухолевыми средствами, которые действуют в S-фазе (ДНК синтез) клеточного цикла путем ингибирования ДНК синтеза или путем ингибирования синтеза на основе пурина или пиримидина и, таким образом, ограничивают ДНК синтез. Следовательно, S-фаза не проходит, и следует гибель клеток. Примеры антиметаболитических противоопухолевых средств включают без ограничения фторурацил, метотрексат, цитарабин, меркаптопурин, тиогуанин и гемцитабин. 5-фторурацил, 5-фтор-2,4-(1 Н,3H)пиримидиндион, коммерчески доступен как фторурацил. Введение 5-фторурацила приводит к ингибированию синтеза тимидилата и также включено и в РНК и в ДНК. Типичным результатом является гибель клеток. 5 Фторурацил предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения карциномы молочной железы, кишечника, прямой кишки, желудка и поджелудочной железы. Другие фторпиримидиновые аналоги включают 5-фтордеоксиуридин (флоксуридин) и 5-фтордеоксиуридина монофосфат. Цитарабин, 4-амино-1D-арабинофуранозил-2(1 Н)-пиримидинон, коммерчески доступен как CYTOSAR-U и общеизвестный как Ara-С. Полагали, что цитарабин проявляет клеточную фазовую специфичность при S-фазе путем ингибирования удлинения цепи ДНК путем конечного включения цитарабина в растущую цепь ДНК. Цитарабин предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения острой лейкемии. Другие аналоги цитидина включают 5-азацитидин и 2',2'-дифтордеоксицитидин (гемцитабин). Меркаптопурин, 1,7-дигидро-6 Нпурин-6-тион моногидрат, коммерчески доступный как PURINETHOL. Меркаптопурин проявляет клеточную фазовую специфичность при S-фазе путем ингибирования синтеза ДНК путем еще одного точно не определенного механизма. Меркаптопурин предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения острой лейкемии. Применимым аналогом меркаптопурина является азатиопурин. Тиогуанин, 2-амино-1,7-дигидро-6 Н-пурин-6-тион, коммерчески доступный как TABLOID. Тиогуанин проявляет клеточную фазовую специфичность при Sфазе путем ингибирования синтеза ДНК путем еще одного точно не определенного механизма. Тиогуанин предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения острой лейкемии. Другие аналоги пурина включают пентостатин, эритрогидроксинониладенин, флударабин фосфат и кладрибин. Гемцитабин, 2'-деокси-2',2'-дифторцитидин моногидрохлорид (-изомер), коммерчески доступный как GEMZAR. Гемцитабин проявляет клеточную фазовую специфичность при S-фазе и путем блокирования прогрессирования клеток через G1/S границу. Гемцитабин предназначен в виде комбинации с цисплатином для лечения местнораспространенного немелкоклеточного рака легкого и когда один при лечении местнораспространенного рака поджелудочной железы. Метотрексат, N-[4(2,4-диамино-6-птеридинил)метил]метиламино]бензоил]-L-глутаминовая кислота, коммерчески доступен как метотрексат натрия. Метотрексат проявляет клеточнофазовые эффекты, в частности при S-фазе, путем ингибирования синтеза ДНК, восстановления и/или репликация путем ингибирования редуктазы дигидрофолиевой кислоты, которая требуется для синтеза пуриновых нуклеотидов и тимидилата. Метотрексат предназначен в виде единственного средства или в комбинации с другими химиотерапевтическими средствами для лечения хориокарциномы, менингеального лейкоза,неходжкинской лимфомы и карцином молочной железы, головы, шеи, яичника и мочевого пузыря. Камптотецины, включая камптотецин и производные камптотецина, доступны или разрабатываются как ингибиторы топоизомеразы I. Цитотоксическая активность камптотецинов предполагается как связанная с ее ингибиторной активностью топоизомеразы I. Примеры камптотецинов включают, но не ограничиваясь, иринотекан, топотекан и различные оптические формы 7-(4-метилпиперазинометилен)10,11-этилендиокси-20-камптотецина, описанные ниже. Иринотекан HCl, (4S)-4,11-диэтил-4-гидрокси-9[(4-пиперидинопиперидино)карбонилокси]-1 Н-пирано[3',4',6,7]индолизино[1,2-b]хинолин-3,14(4 Н,12 Н)диона гидрохлорид, коммерчески доступный как инъецируемый раствор CAMPTOSAR. Иринотекан представляет собой производное камптотецина, которое связано, вместе с его активным метаболитомSN-38, с комплексом топоизомераза I - ДНК. Считается, что цитотоксичность возникает в результате необратимых разрывов двойных нитей, вызванных взаимодействием тройного комплекса топоизомеразаI:ДНК:иринтекан или SN-38 с ферментами репликации. Иринотекан назначают для лечения метастатического рака толстой кишки или прямой кишки. Топотекан HCl, (S)-10-[(диметиламино)метил]-4-этил-4,9 дигидрокси-1 Н-пирано[3',4',6,7]индолизино[1,2-b]хинолин-3,14-(4 Н,12 Н)-диона моногидрохлорид, коммерчески доступный как инъецируемый раствор HYCAMTI N. Топотекан представляет собой производное камптотецина, которое связывается с комплексом топоизомераза I - ДНК и предотвращает повторное лигирование однонитевых разрывов, вызванных топоизомеразой I в ответ на деформацию кручения молекулы ДНК. Топотекан назначают для второй линии лечения метастатической карциномы яичников и мелкоклеточного рака легких. Гормоны и гормоны-аналоги являются пригодными соединениями для лечения рака, в котором существует взаимосвязь между гормоном(ами) и ростом и/или отсутствием роста раковой опухоли. Примеры гормонов и гормонов-аналогов, пригодных в лечении рака, включают без ограничения адренокортикостероиды, такие как преднизон и преднизолон, которые пригодны в лечении злокачественной лимфомы и острой лейкемии у детей; аминоглутетимид и другие ингибиторы ароматазы, такие как анастрозол,летразол, воразол и экземестан, пригодны в лечении адренокортикальной карциномы и гормонозависимой карциномы молочной железы, содержащей эстрогеновые рецепторы; прогестрины, такие как мегестролацетат, пригодные в лечении гормонозависимого рака молочной железы и эндометриальной карциномы; эстрогены, андрогены и антиандрогены, такие как флутамид, нилутамид, бикалутамид, ципротерон ацетат, и 5-редуктазы, такие как финастерид и дутастерид, пригодные в лечении рака предстательной железы и доброкачественной гипертрофии предстательной железы; антиэстрогены, такие как тамоксифен, торемифен, ралоксифен, дролоксифен, йодоксифен, а также селективные модуляторы эстрогеновых рецепторов (SERM), так описанные в патентах США 5681835, 5877219 и 6207716, пригодные в лечении гормонозависимой карциномы молочной железы и других восприимчивых раковых опухолей; и гонадотропинвысвобождающий гормон (GnRH) и его аналоги, которые стимулируют высвобождение лютеинизирующего гормона (LH) и/или фолликулостимулирующего гормона (FSH) для лечения рака предстательной железы, например LHRH агонисты и антагонисты, такие как гозерелина ацетат и леупролид. Ингибиторы пути сигнальной трансдукции являются такими ингибиторами, которые блокируют или ингибируют химический процесс, который вызывает внутриклеточное изменение. Как используется в данном документе, это изменение является клеточной пролиферацией или дифференциацией. Ингибиторы сигнальной трансдукции, пригодные в настоящем изобретении, включают ингибиторы рецепторных тирозинкиназ, нерецепторных тирозинкиназ, блокаторы SH2/SH3 домена, серин/треонинкиназы,фосфотидилинозит-3 киназы, миоинозитоловый путь передачи сигнала и Ras онкогены. Некоторые белковые тирозинкиназы катализируют фосфорилирование конкретных тирозильных остатков в различных белках, вовлеченных в регулирование клеточного роста. Такие белковые тирозинкиназы можно в широком смысле классифицировать как рецепторные или нерецепторные киназы. Рецепторные тирозинкиназы являются трансмембранными белками, имеющими внеклеточный лигандсвязывающий домен, трансмембранный домен и домен тирозинкиназы. Рецепторные тирозинкиназы вовлечены в регулирование клеточного роста и обычно называются рецепторами фактора роста. Неподходящая или неконтролируемая активация многих таких киназ, т.е. аберрантная активность рецептора фактора роста киназы, например, посредством сверхэкспрессии или мутации, была показана как такая,которая влечет за собой неконтролируемый клеточный рост. Соответственно, аберрантная активность таких киназ связана с ростом болезнетворных тканей. Следовательно, ингибиторы таких киназ будут обеспечивать способы лечения рака. Рецепторы фактора роста включают, например, рецептор эпидермального фактора роста (EGFr), рецептор фактора роста, связанный с тромбоцитами, (PDGFr), erbB2,erbB4, ret, рецептор васкулярного эндотелиального фактора роста (VEGFr), домены гомологии тирозин- 20020488 киназы с иммуноглобулинподобным и эпидермическим фактором роста (TIE-2), рецептор инсулиноподобного фактора роста -I (IGFI), фактор, стимулирующий колонии макрофагов, (cfms), BTK, ckit, cmet,рецепторы фактора роста фибробласта (FGF), Trk рецепторы (TrkA, TrkB и TrkC), ephrin (eph) рецепторы и RET протоонкоген. Некоторые ингибиторы рецепторов роста разрабатываются и включают антагонисты лигандов, антитела, ингибиторы тирозинкиназы и антисмысловые олигонуклеотиды. Рецепторы фактора роста и средства, которые ингибируют функцию рецептора фактора роста, описаны, например, вKath, John С., Exp. Opin. Ther. Patents (2000) 10(6):803-818; Shawver et al., DDT Vol. 2, No. 2 February 1997; и Lofts, F.J. et al., "Growth factor receptors as targets", New Molecular Targets for Cancer Chemotherapy,ed. Workman, Paul и Kerr, David, CRC press 1994, London. Тирозинкиназы, которые не являются киназами рецептора фактора роста, называются нерецепторными тирозинкиназами. Нерецепторные тирозинкиназы, пригодные в настоящем изобретении, которые являются мишенями или потенциальными мишенями противораковых лекарственных средств, включаютcSrc, Lck, Fyn, Yes, Jak, cAbl, FAK (киназа фокальной адгезии), тирозинкиназу Брутона и Bcr-Abl. Такие нерецепторные киназы и средства, которые ингибируют функцию нерецепторных тирозинкиназ, описаны в Sinh, S. and Corey, S.J., (1999) Journal of Hematotherapy and Stem Cell Research 8 (5): 465-80; and Bolen, J.В., Brugge, J.S., (1997) Annual review of Immunology. 15: 371-404. Блокаторы SH2/SH3 домена представляют собой средства, которые разрушают связь домена SH2 или SH3 в разнообразии ферментов или адапторных белков, включая PI3-K р 85 субъединицу, Src семейство киназ, адапторные молекулы (She,Crk, Nek, Grb2) и Ras-ГЭП. SH2/SH3 домены как мишени для противораковых лекарственных средств обсуждаются в Smithgall, Т.Е. (1995), Journal of Pharmacological and Toxicological Methods. 34(3) 125-32. Ингибиторы серин/треонинкиназ включают блокаторы МАР-киназного каскада, которые включают блокаторы Raf киназ (rafk), киназы, регулируемой митогеном или внеклеточным сигналом (MEK), и киназы, регулируемые внеклеточным сигналом, (ERK); и блокаторы членов семейства протеинкиназы С,включая блокаторы PKC (альфа, бета, гамма, эпсилон, мю, лямбда, йота, зета). Семейства IkB киназ(IKKa, IKKb), семейства PKB киназ, члены akt семейства киназ и киназ рецептора TGF-. Такие серин/треонинкиназы и их ингибиторы описаны в Yamamoto, Т., Taya, S., Kaibuchi, K., (1999), Journal of(1995), Cancer Treatment and Research. 78: 3-27, Lackey, K. et al., Bioorganic and Medicinal Chemistry Letters, (10), 2000, 223-226; патенте США 6268391 и Martinez- lacaci, L., et al., Int. J. Cancer (2000), 88(1),44-52. Ингибиторы членов семейства фосфотидил-инозитол-3-киназы, включая блокаторы PI3-киназы,ATM, ДНК-РК и Ku, также применимы в настоящем изобретении. Такие киназы обсуждаются в Abraham, RT. (1996), Current Opinion in Immunology. 8(3) 412-8; Canman, C.E., Lim, D.S. (1998), Oncogene 17Zhong, H. et al., Cancer res, (2000) 60(6), 1541-1545. Также применимыми в настоящем изобретении являются ингибиторы миоинозитольного пути передачи сигнала, такие как блокаторы фосфолипазы С и аналоги миоинозитола. Такие ингибиторы сигнала описаны в Powis, G., and Kozikowski A., (1994) New Molecular Targets for Cancer Chemotherapy ed., PaulWorkman and David Kerr, CRC press 1994, London. Другая группа ингибиторов пути сигнальной трансдукции представляет собой ингибиторы Ras онкогена. Такие ингибиторы включают ингибиторы фарнезилтрансферазы, геранил-геранил трансферазы и СААХ протеазы, а также антисмысловые олигонуклеотиды, рибозимы и иммунотерапию. Такие ингибиторы показаны как блокирующие ras активацию в клетках, содержащих дикий тип мутантной ras, таким образом действуя как антипролиферативные средства. Ингибирование Ras онкогена обсуждается в Scharovsky,О.G., Rozados, V.R., Gervasoni, S.I. Matar, P. (2000), Journal of Biomedical Science. 7(4) 292-8; Ashby, M.N.(1998), Current Opinion in Lipidology. 9 (2) 99-102 и BioChim. Biophys. Acta, (19899) 1423(3): 19-30. Как указано выше, антагонисты антител к связыванию рецепторной киназы и лиганда могут также служить в качестве ингибиторов сигнальной трансдукции. Эта группа ингибиторов пути сигнальной трансдукции включает применение гуманизированых антител к внеклеточному домену связывания лиганда рецепторных тирозинкиназ. Например, Imclone C225 EGFR специфическое антитело (см. Green,M.С. et al., Monoclonal Antibody Therapy for Solid Tumors, Cancer Treat. Rev., (2000), 26(4), 269-286); Herceptin erbB2 антитело (см. Tyrosine Kinase Signalling in Breast cancer erbB Family Receptor Tyrosine Kinases, Breast cancer Res., 2000, 2(3), 176-183) и 2 СВ VEGFR2 специфическое антитело (см. Brekken, R.A.mice, Cancer Res. (2000) 60, 5117-5124). Антиангиогенные средства, включая ингибиторы ангиогенеза на основе нерецепторных киназ, также могут быть применимыми. Антиангиогенные средства, такие как те, которые ингибируют эффекты васкулярного эндотелиального фактора роста (например, антитело антиваскулярного эндотелиального фактора роста клеток бевацизумаб [Avastin], и соединения, которые работают посредством других механизмов (например, линомид, ингибиторы функции интегрина avb3, эндостатин и ангиостатин). Средства, применимые для иммунотерапевтических режимов, могут также быть применимыми в комбинации с соединениями формулы (I). Иммунотерапевтические подходы включают, например, exvivo и in-vivo подходы для увеличения иммуногенности опухолевых клеток пациента, такие как трансфекция цитокинами, такими как интерлейкин 2, интерлейкин 4 или фактор, стимулирующий колонии гранулоцитов-макрофагов, подходы для уменьшения анергии Т-клеток, подходы с применением трансфецированных иммуноцитов, таких как трансфецированные цитокином дендритные клетки, подходы с применением трансфецированных цитокином опухолевых клеточных линий и подходы с применением антиидиотипических антител. Средства, применимые для проапоптотических режимов (например, bcl-2 антисмысловые олигонуклеотиды), можно также применять в комбинации настоящего изобретения. Ингибиторы сигналинга клеточного цикла ингибируют молекулы, вовлеченные в контроль клеточного цикла. Семейство протеинкиназ, называемых циклинзависимые киназы (CDK), и их взаимодействие с семейством белков, называемых циклины, контролирует продвижение через эукариотический клеточный цикл. Координатная активация и инактивация различных циклин/CDK комплексов необходима для нормального продвижения через клеточный цикл. Некоторые ингибиторы сигналинга клеточного цикла разрабатываются. Например, примеры циклинзависимых киназ, включая CDK2, CDK4 и CDK6, и ингибиторы для них описаны, например, в Rosania et al., Exp. Opin. Ther. Patents (2000) 10(2):215-230. Для лечения или профилактики легочных расстройств, антихолинергические средства возможного применения для лечения астмы, COPD, бронхита и т.п. и, следовательно, пригодные в качестве дополнительного терапевтического средства, включают антагонисты мускаринового рецептора (особенно М 3 подтипа), которые показали терапевтическую эффективность у человека для контроля холинергического характера в COPD (Witek, 1999); 1-4-гидрокси-1-[3,3,3-трис-(4-фторфенил)пропионил]пирролидин-2 карбонилпирролидин-2-карбоновой кислоты (1-метилпиперидин-4-илметил)амид; 3-[3-(2-диэтиламиноацетокси)-2-фенилпропионилокси]-8-изопропил-8-метил-8-азониабицикло[3.2.1]октан (ипратропий-N,Nдиэтилглицинат); 1-циклогексил-3,4-дигидро-1 Н-изохинолин-2-карбоновой кислоты 1-аза-бицикло(бузепид); 7-[3-(2-диэтиламиноацетокси)-2-фенилпропионилокси]-9-этил-9-метил-3-окса-9-азониатрицикло[3.3.1.02,4]нонан (окситропий-N,N-диэтилглицинат); 7-[2-(2-диэтиламиноацетокси)-2,2-дитиофен-2-ил-ацетокси]-9,9-диметил-3-окса-9-азониатрицикло[3.3.1.02,4]нонан (тиотропий-N,N-диэтилглицинат); диметиламиноуксусной кислоты 2-(3-диизопропиламино-1-фенилпропил)-4-метилфенил сложный эфир (толтеродин-N,N-диметилглицинат); 3-[4,4-бис-(4-фторфенил)-2-оксоимидазолидин-1 ил]-1-метил-1-(2-оксо-2-пиридин-2-ил-этил)пирролидиний; 1-[1-(3-фторбензил)пиперидин-4-ил]-4,4-бис(4-фторфенил)имидазолидин-2-он; 1-циклооктил-3-(3-метокси-1-аза-бицикло[2.2.2]окт-3-ил)-1-фенилпроп-2-ин-1-ол; 3-[2-(2-диэтиламиноацетокси)-2,2-дитиофен-2-ил-ацетокси]-1-(3-феноксипропил)-1 азониабицикло[2.2.2]октан (аклидиний-N,N-диэтилглицинат) или (2-диэтиламиноацетокси)-дитиофен-2 ил-уксусной кислоты 1-метил-1-(2-феноксиэтил)пиперидин-4-ил сложный эфир; -2 агонист, применяемый для лечения бронхоконстрикции при астме, COPD и бронхита, включает салметерол и альбутерол; противовоспалительные модуляторы сигнальной трансдукции для астмы. Относительно легочных условий при астме специалисты в данной области техники оценят, что астма представляет собой хроническое воспалительное заболевание дыхательных путей, обусловленное проникновением провоспалительных клеток, главным образом эозинофилов и активированных Тлимфоцитов, в слизистую и подслизистый слой бронхов. Секреция мощных химических медиаторов,включая цитокины, этими провоспалительными клетками изменяет проницаемость слизистой, выделение слизи и вызывает сокращение гладких мышц. Все эти факторы приводят к увеличенной реакционности дыхательных путей и к широкому разнообразию раздражающих факторов (Kaliner, 1988). Целевые пути сигнальной трансдукции представляют собой приемлемый подход для лечения воспалительных заболеваний, поскольку эти же пути обычно вовлечены в некоторые клеточные типы и регулируют некоторые согласованные воспалительные процессы, следовательно, модуляторы имеют перспективу широкого спектра благоприятных эффектов. Множество воспалительных сигналов активируют разнообразие рецепторов на поверхности клеток, которые активируют ограниченное количество путей сигнальной трансдукции, большинство из которых включает каскады киназ. Эти киназы, в свою очередь, могут активировать факторы транскрипции, которые регулируют множество воспалительных генов. Применение "модуляторов противовоспалительной сигнальной трансдукции" (названные в данном тексте AISTM), подобных ингибиторам фосфодиэстеразы (например, PDE-4, PDE-5 или PDE-7 специфичная), ингибиторам фактора транскрипции (например, блокирование NFB посредством ингибирования IKK) или ингибиторам киназы (например, блокирующим Р 38 MAP, JNK, PI3K, EGFR или Syk), является логическим подходом для угнетения воспаления, т.к. эти маленькие молекулы достигают ограниченного количества общих внутриклеточных путей - тех путей сигнальной трансдукции, которые являются критическими точками для противовоспалительного терапевтического воздействия (см. обзор P.J. Barnes, 2006). Дополнительные терапевтические средства включают 5-(2,4-дифторфенокси)-1-изобутил-1 Н- 22020488RWJ-67657); 4-циано-4-(3-циклопентилокси-4-метоксифенил)циклогексанкарбоновой кислоты 2-диэтиламиноэтиловый сложный эфир (2-диэтилэтилового сложного эфира пролекарство циломиласта, PDE-4 ингибитор); (3-хлор-4-фторфенил)-[7-метокси-6-(3-морфолин-4-ил-пропокси)хиназолин-4-ил]амин (гефитиниб, ингибитор EGFR) и 4-(4-метилпиперазин-1-илметил)-N-[4-метил-3-(4-пиридин-3-илпиримидин-2-иламино)фенил]бензамид (иматиниб, ингибитор EGFR). Более того, астма представляет собой хроническое воспалительное заболевание дыхательных путей,вызываемое проникновением противоспалительных клеток, главным образом эозинофилов и активированных Т-лимфоцитов (Poston, Am. Rev. Respir. Dis., 145 (4 Pt 1), 918-921, 1992; Walker, J. Allergy Clin.Immunol., 88 (6), 935-42, 1991) в слизистую и подслизистую основу бронхов. Секреция мощных химических медиаторов, включая цитокины, этими провоспалительными клетками изменяет проницаемость слизистой, выделение слизи и вызывает сокращение гладких мышц. Все эти факторы приводят к увеличенной реакционности дыхательных путей к широкому разнообразию раздражающих факторов (Kaliner,"Bronchial asthma, Immunologic diseases" E.M. Samter, Boston, Little, Brown и Company: 117-118. 1988). Глюкокортикоиды, которые были впервые введены в качестве терапии астмы в 1950 (Carryer, Journal of Allergy, 21, 282-287, 1950), остаются наиболее мощной и соответственно эффективной терапией для этого заболевания, хотя их механизм действия до сих пор полностью не понятен (Morris, J. AllergyClin. Immunol., 75 (1 Pt) 1-13, 1985). К сожалению, пероральные методы лечения глюкокортикоидами связаны с сильными нежелательными побочными эффектами, такими как ожирение, гипертензия, глаукома, непереносимость глюкозы, ускорение развития катаракты, потеря минералов костей и психологические эффекты, все из которых ограничивают их применение в качестве пролонгированных терапевтических средств (Goodman и Gilman, 10th edition, 2001). Решение для системных побочных эффектов заключается в доставке стероидных лекарственных средств непосредственно к месту воспаления. Ингаляторные кортикостероиды (ICS) были разработаны для уменьшения тяжелых вредных воздействий пероральных стероидов. Хотя ICS очень эффективны при контроле воспаления при астме, они тоже не доставляются точно в оптимальное место действия в легких и вызывают нежелательные побочные эффекты во рту и глотке (кандидоз, фарингит, дисфония). Комбинации ингаляторных бронходилататоров агониста 2-адренорецептора, такие как формотерол или салметерол с ICS, также применимы для лечения как бронхоконстрикции, так и воспаления, связанного с астмой и COPD (Symbicort и Advair соответственно). Однако эти комбинации имеют побочные эффекты как ICS, так и агониста 2-адренорецептора из-за системной абсорбции (тахикардия, вентрикулярная аритмия, гипокалиемия), главным образом из-за того, что средство не доставляется в оптимальное место действия в легких. Вследствие всех проблем и неблагоприятных состояний, связанных с нежелательным профилем побочных эффектов ICS и 2 агонистов, будет весьма полезно обеспечивать общее пролекарство стероид-2-агонист для защиты фармакологических свойств как стероидов, так и 2-агонистов, пока такое пролекарство не достигнет легких, таким образом уменьшая ротоглоточные побочные эффекты ICS и побочные эффекты на сердечнососудистую систему 2-агонистов. В одном аспекте такое общее пролекарство стероид-2-агонист будет эффективно доставляться в эндобронхиальное пространство и преобразовываться в активные лекарственные средства вследствие действия легочных ферментов, таким образом доставляя в место воспаления и бронхоконстрикции терапевтическое количество обоих лекарственных средств. Противовоспалительное средство для комбинированной терапии включает дексаметазон, дексаметазона натрия фосфат,фторметолон, фторметолона ацетат, лотепреднол, лотепреднола этабонат, гидрокортизон, преднизолон,флудрокортизоны, триамцинолон, триамцинолон ацетонид, бетаметазон, беклометазон дипропионат,метилпреднизолон, флуоцинолон, флуоцинолонацетонид, флунизолид, флуокортин-21-бутилат, флуметазон, флуметазонпивалат, будесонид, галобетазола пропионат, мометазонфуроат, флутиказонпропионат,циклесонид или их фармацевтически приемлемую соль. В еще одном варианте осуществления данная заявка раскрывает фармацевтические композиции,содержащие соединение по настоящему изобретению или его фармацевтически приемлемую соль в комбинации по меньшей мере с одним дополнительным активным средством и фармацевтически приемлемым носителем или наполнителем. В еще одном варианте осуществления данная заявка обеспечивает комбинацию фармацевтического средства с двумя или более терапевтическими средствами в единичной лекарственной форме. Таким образом, также возможно скомбинировать любое соединение по настоящему изобретению с одним или несколькими другими активными средствами в единичной лекарственной форме. Комбинированную терапию можно вводить в одновременном или последовательном режиме. При последовательном введении комбинацию можно вводить в двух или нескольких введениях. Совместное введение соединения по настоящему изобретению с одним или несколькими другими активными средствами обычно относится к одновременному или последовательному введению соединения по настоящему изобретению и одного или нескольких других активных средств так, чтобы терапевтически эффективные количества соединения по настоящему изобретению и одного или нескольких других активных средств присутствовали оба в теле пациента. Совместное введение включает введение единичных доз соединения настоящего изобретения перед или после введения единичных доз одного или нескольких других активных средств, например введение соединения настоящего изобретения в течение секунд, минут или часов введения одного или нескольких других активных средств. Например, стандартная доза соединения по настоящему изобретению может вводиться первой, с последующим введением в течение секунд или минут стандартной дозы одного или нескольких других активных средств. Альтернативно, стандартная доза одного или нескольких других активных средств может вводиться первой, с последующим введением стандартной дозы соединения по настоящему изобретению в течение секунд или минут. В некоторых случаях может быть желательным вводить стандартную дозу соединения по настоящему изобретению первой, с последующим, через период в часы (например, 1-12 ч), введением стандартной дозы одного или нескольких других активных средств. В других случаях может быть желательным вводить стандартную дозу одного или нескольких других активных средств вначале с последующим, через период в часы (например, 1-12 ч), введением стандартной дозы соединения по настоящему изобретению. Комбинированная терапия может обеспечивать "синергизм" и "синергический эффект", т.е. достигаемый эффект, когда активные ингредиенты применяют вместе, больше, чем сумма эффектов, которая получается при применении соединений отдельно. Синергический эффект можно получить, когда активные ингредиенты: (1) совместно составлены и вводятся или доставляются одновременно в комбинированном составе; (2) доставляются попеременно или параллельно в качестве отдельных составов или (3) посредством любого другого режима. Когда доставляется при попеременной терапии, синергический эффект можно получить, если соединения вводят или доставляют последовательно, например, в отдельных таблетках, пилюлях или капсулах или путем различных инъекций в отдельных шприцах. В основном во время поочередной терапии эффективная дозировка каждого активного ингредиента вводится последовательно, т.е. периодически, поскольку в комбинированной терапии эффективные дозировки двух или нескольких активных ингредиентов вводят совместно. Способы лечения. Как используется в данном документе, "агонист" представляет собой вещество, которое стимулирует его участника связывания, типично рецептор. Стимуляция определяется в рамках конкретного анализа или может быть очевидной в литературе из обсуждения в данном документе, которое делает сравнение с фактором или веществом, которое принято в качестве "агониста" или "антагониста" конкретного участника связывания при, по существу, аналогичных условиях, как оценивается специалистами в данной области. Стимуляция может быть определена по отношению к увеличению конкретного эффекта или функции, которая вызывается взаимодействием агониста или частичного агониста с участником связывания и может включать аллостерические эффекты. Как используется в данном документе, "антагонист" представляет собой вещество, которое ингибирует его участника связывания, типично рецептор. Ингибирование определено в рамках конкретного анализа или может быть очевидным в литературе из обсуждения в данном документе, которое делает сравнение с фактором или веществом, которое принято в качестве "агониста" или "антагониста" конкретного участника связывания при, по существу, аналогичных условиях, как оценивается специалистами в данной области. Ингибирование может быть определено по отношению к уменьшению конкретного эффекта или функции, которое индуцируется взаимодействием антагониста с участником связывания, и может включать аллостерические эффекты. Как используется в данном документе, "частичный агонист" или "частичный антагонист" представляет собой вещество, которое обеспечивает уровень стимуляции или ингибирования, соответственно, с его участником связывания, который представляет собой неполный или полный агонист или антагонист соответственно. Признают, что стимуляция и, следовательно, ингибирование определяется в основном для любого вещества или категории веществ, определенных как агонисты, антагонисты или частичные агонисты. Как используется в данном документе, "внутренняя активность" или "эффективность" относится к некоторой мере биологической эффективности комплекса участника связывания. Относительно фармакологии рецептора, ситуация, в которой внутренняя активность или эффективность будет определена,будет зависеть от ситуации комплекса участника связывания (например, рецептор/лиганд) и рассмотрения активности, соответствующей конкретному биологическому результату. Например, в некоторых случаях внутренняя активность может варьировать в зависимости от конкретной рассматриваемой системы вторичных мессенджеров. Где такие контекстуально конкретные оценки являются актуальными, и как они могут быть уместны в контексте настоящего изобретения, будет очевидно специалисту в данной области. Как используется в данном документе, модуляция рецептора включает агонизм, частичный агонизм, антагонизм, частичный антагонизм или обратный агонизм рецептора. Как будет понятно специалистам в данной области техники, при лечении вирусной инфекции, такой как HCV, HBV или HIV, такое лечение может характеризоваться разнообразием путей и измеряться разнообразием предельных значений. Объем настоящего изобретения призван охватывать все такие параметры. В одном варианте осуществления способ может использоваться для индуцирования иммунного ответа против различных эпитопов вирусной инфекции у человека. Индукцию иммунного ответа против вирусной инфекции можно оценить с применением любой техники, которая известна специалистам в данной области для определения, будет ли возникать иммунный ответ. Подходящие способы обнаружения иммунного ответа для настоящего изобретения включают, среди прочих, обнаружение уменьшения вирусной нагрузки или антигена в сыворотке субъекта, обнаружение IFNсекретирующих пептидных специфических Т-клеток и обнаружение повышенных уровней одного или нескольких ферментов печени, таких как аланинтрансфераза (ALT) и аспартаттрансфераза (AST). В одном варианте осуществления обнаружение IFNсекретирующих пептидных специфических Т-клеток выполняется с применениемELISPOT анализа. Другой вариант осуществления включает уменьшение вирусной нагрузки, связанной сHBV инфекцией, включая снижение, как измерено ПЦР тестом. Дополнительно соединения данного изобретения применимы в лечении рака или опухолей (включая дисплазии, такие как маточная дисплазия). Они включают гематологические злокачественные опухоли, внутриротовые карциномы (например, губ, языка или глотки), органов пищеварения (например, пищевод, желудок, тонкая кишка, толстая кишка, толстый кишечник или прямая кишка), печени и желчных протоков, поджелудочной железы, дыхательной системы, такой как гортань или легкое (мелкоклеточные и немелкоклеточные), кости, соединительной ткани, кожи (например, меланома), молочной железы, органов размножения (матка, шейка матки, семенник, яичник или простата), мочевых путей (например,мочевой пузырь или почка), мозга и эндокринных желез, таких как щитовидная железа. В кратком описании соединения данного изобретения применяют для лечения любого новообразования, включая не только гематологические злокачественные опухоли, а также солидные опухоли всех видов. Гематологические злокачественные опухоли в широком смысле определены как пролиферативные расстройства клеток крови и/или их предшественников, в которых эти клетки разрастаются неконтролируемым образом. Анатомически гематологические злокачественные опухоли подразделены на две основные группы: лимфомы - злокачественные массы лимфоцитов, первично, но не исключительно, в лимфатических узлах и лейкозы - новообразования, полученные типично из лимфоидных или миелоидных клеток и в первую очередь поражающие костный мозг и периферическую кровь. Лимфомы можно подразделить на заболевание Ходжкина и неходжкинскую лимфому (NHL). Последняя группа содержит несколько отдельных категорий, которые могут отличаться клинически (например, агрессивная лимфома, вялотекущая лимфома), гистологически (например, фолликулярная лимфома, лимфома клеток мантийной ткани) или на основе происхождения злокачественной клетки (например, В лимфоцит, Т лимфоцит). Лейкемия и связанные злокачественные опухоли включают острую миелогенный лейкоз (AML),хронический миелолейкоз (CML), острый лимфобластный лейкоз (ALL) и хронический лимфолейкоз(CLL). Другие гематологические злокачественные опухоли включают плазмаклеточную дегенерацию,включая множественную миелому и миелодиспластический синдром. Примеры синтеза. К раствору хлорпурина 1 (2,54 г, 10,0 ммоль) в DMF (20 мл) добавляли раствор бутоксида натрия(1M в nBUOH, 20 мл, 20 ммоль). Реакционную смесь перемешивали при 100 С в течение 6 ч. Реакционную смесь выливали в насыщенный раствор NH4Cl (100 мл) и EtOAc (80 мл). Слои разделяли и водный слой экстрагировали EtOAc (50 мл). Объединенные органические слои промывали рассолом (75 мл). Органический слой сушили, отфильтровывали и концентрировали in vacuo. Сырой продукт перенесли на следующую стадию без дополнительной очистки. 2: 1 Н-ЯМР: 300 МГц, (CDCl3) : 7,87 (s, 1H), 5,58-5,68 (m, 3H), 4,33 (t, 2H, J=7 Гц), 4,15 (m, 1 Н), 3,77 К раствору алкоксипурина 2 (2,9 г, 10,0 ммоль) в ацетонитриле (25 мл) порциями добавляли Nбромсукцинимид (2,6 г). Реакцию перемешивали при кт в течение 2 ч и затем выливали в 20% раствор сульфата натрия (50 мл) и EtOAc (50 мл). Слои разделяли. Органический слой промывали насыщенным раствором NaHCO3 (25 мл), затем сушили, отфильтровывали и концентрировали in vacuo. Сырой материал очищали путем колоночной флеш-хроматографии (EtOAc/гексаны). 3: 1 Н-ЯМР: 300 МГц, (CDCl3) : 5,60 (m, 3H), 4,31 (m, 2H), 4,17 (m, 1H), 3,73 (m, 1H), 3,08 (m, 1H),2,13 (m, 1H), 1,47-1,80 (m, 8H), 0,98 (t, 3H, J=7 Гц). К раствору бромида 3 (1,85 г, 5,00 ммоль) в МеОН (25 мл) добавляли раствор метоксида натрия (1M в МеОН, 10 мл). Реакционную смесь перемешивали при 60 С в течение 6 ч. Смесь концентрировали invacuo, затем добавляли воду (20 мл). Смесь экстрагировали EtOAc (25 мл). Органический слой сушили,отфильтровывали и концентрировали in vacuo. Сырой материал очищали путем колоночной флешхроматографии (EtOAc/гексаны). 4: 1 Н-ЯМР: 300 МГц, (CDCl3) : 5,51 (m, 1H), 5,29 (br s, 2H), 4,29 (t, 2H, J=7 Гц), 4,12 (m, 4 Н), 3,71 К раствору метилимидата 4 (1,2 г) в МеОН (15 мл) добавляли трифторуксусную кислоту (1,5 мл). Реакционную смесь перемешивали при кт в течение 4 суток и концентрировали in vacuo. Твердое вещество отфильтровывали и промывали МеОН/EtOAc. 5: 1 Н-ЯМР: 300 МГц, (CD3OD) : 4,48 (t, 2H, J=7 Гц), 4,14 (s, 3H), 1,79 (m, 2H), 1,50 (m, 2H), 0,98 (t,3H, J=7 Гц). К раствору пуриновой соли 5 (1,76 г, 5,00 ммоль) в DMF (25 мл) добавляли Mg(Ot-Bu)2 (2,13 г, 12,5 ммоль) и 3-йодбензилбромид (6) (1,63 г, 5,50 ммоль). Реакционную смесь перемешивали при 60 С в течение 3 ч. Реакционную смесь выливали в насыщенный раствор NH4Cl (50 мл) и EtOAc (50 мл). Слои разделяли и органический слой промывали рассолом (25 мл). Органический раствор сушили над Na2SO4,отфильтровывали и концентрировали in vacuo. Сырой материал очищали путем колоночной флешхроматографии (CH2Cl2 и EtOAc, содержащие 2% МеОН). добавляли карбонат калия (K2CO3) (41 мг, 0,29 ммоль) и [1,1-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (2,1 мг, 0,0029 ммоль). Реакционную смесь перемешивали при 80 С в течение 2 ч. Реакционную смесь затем разбавляли водой (1 мл) и EtOAc (1 мл). Слои разделяли и органический слой концентрировали in vacuo. Сырой материал очищали путем колоночной флеш-хроматографии К раствору метилимидата 9 (28 мг, 0,057 ммоль) в THF (1 мл) добавляли 1 М раствор HCl (120 мкл). Реакцию перемешивали при 55 С в течение 3 ч. THF удаляли in vacuo. Оставшееся масло разбавляли водой (2 мл), замораживали и оставляли в лиофилизаторе на всю ночь. Синтезировали из соединения 7 по методике для соединения 9 с применением 1-(3-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидина. 10: 1 Н-ЯМР: 300 МГц, (CDCl3) : 7,27-7,61 (m, 8H), 5,31 (br s, 2H), 5,16 (s, 2H), 4,31 (t, 2H, J=7 Гц),4,10 (s, 3H), 3,68 (s, 2 Н), 2,55 (br s, 4H), 1,71-1,81 (m, 6H), 1,44 (m, 2H), 0,95 (t, 3H, J=7 Гц). Синтезировали из соединения 10 по методике для соединения А. В: 1 Н-ЯМР: 300 МГц, (CD3OD) : 7,89 (s, 1 Н), 7,78 (s, 1 Н), 7,42-7,67 (m, 6 Н), 5,11 (s, 2H), 4,50 (m,4 Н), 3,52 (br m, 2 Н), 3,22 (br m, 2 Н), 2,19 (br m, 2 Н), 2,04 (br m, 2 Н), 1,76 (m, 2 Н), 1,45 (m, 2 Н), 0,94 (t, 3H,J=7 Гц). Синтезировали из соединения 7 по методике для соединения 9 с применением 1-(4-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидина. 11: 1 Н-ЯМР: 300 МГц, (CDCl3) : 7,60 (s, 1H), 7,27-7,51 (m, 7H), 5,30 (br s, 2H), 5,16 (s, 2H), 4,31 (t,2H, J=7 Гц), 4,10 (s, 3H), 3,67 (s, 2H), 2,55 (br s, 4H), 1,72-1,81 (m, 6H), 1,48 (m, 2H), 0,95 (t, 3H, J=7 Гц,). Синтезировали из соединения 11 по методике для соединения А. С: 1 Н-ЯМР: 300 МГц, (CD3OD) : 7,44-7,74 (m, 8 Н), 5,11 (br s, 2 Н), 4,52 (br s, 2H), 4,45 (s, 2H), 3,54 Синтезировали из соединения 5 по методике для соединения 7 с применением 4-йодбензилбромида. 12: 1 Н-ЯМР: 300 МГц, (CDCl3) : 7,64 (d, 2H, J=8 Гц), 7,07 (d, 2H, J=8 Гц), 5,34 (br s, 2H), 5,04 (s,2H), 4,31 (t, 2H, J=7 Гц), 4,09 (s, 3H), 1,78 (m, 2H), 1,50 (m, 2 Н), 0,97 (t, J=7 Гц). Синтезировали из соединения 12 по методике для соединения 9 с применением 1-(2-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидина. 13: 1 Н-ЯМР: 300 МГц, (CDCl3) : 7,56 (d, 1 Н, J=8 Гц), 7,19-7,36 (m, 7H), 5,27 (br s, 2H), 5,15 (s, 2H),4,33 (t, 2H, J=7 Гц), 4,13 (s, 3H), 3,53 (s, 2H), 2,43 (m, 4H), 1,72-1,81 (m, 6H), 1,49 (m, 2H), 0,97 (t, 3H, J=7 Гц). Синтезировали из соединения 13 по методике для соединения А. Синтезировали из соединения 12 по методике для соединения 9 с применением 1-(3-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидина. 14: 1 Н-ЯМР: 300 МГц, (CDCl3) : 7,26-7,56 (m, 8H), 5,28 (br s, 2H), 5,14 (s, 2H), 4,32 (t, 2H, J=7 Гц),4,11 (s, 3H), 3,67 (s, 2 Н), 2,54 (br s, 4H), 1,74-1,83 (m, 6H), 1,51 (m, 2H), 0,97 (t, 3H, J=7 Гц). Синтезировали из соединения 14 по методике для соединения А. Е: 1 Н-ЯМР: 300 МГц, (CD3OD) : 7,88 (br s, 1 Н), 7,70 (br m, 3H), 7,53 (br m, 4H), 5,09 (s, 2H), 4,55 (br Синтезировали из соединения 12 по методике для соединения 9 с применением 1-(4-(4,4,5,5 тетраметил-1,3,2-диоксаборолан-2-ил)бензил)пирролидина. 15:1 Н-ЯМР: 300 МГц, (CDCl3) : 7,51 (m, 4H), 7,38 (m, 4H), 5,42 (br s, 2H), 5,13 (s, 2H), 4,32 (t, 2 Н, J= 7 Гц), 4,10 (s, 3H), 3,65 (s, 2 Н), 2,54 (br s, 4H), 1,78 (m, 6H), 1,50 (m, 2H), 0,97 (t, 3H, J=7 Гц). Синтезировали из соединения 15 по методике для соединения А. Синтезировали из соединения 5 по методике для соединения 7 с применением 2-бром-5(бромметил)пиридина. 16: 1 Н-ЯМР: 300 МГц, (CDCl3) : 8,44 (d, 1H, J=2 Гц), 7,58 (dd, 1H, J=8, 2 Гц), 7,43 (d, 1H, J=8 Гц),5,26 (br s, 2H), 5,07 (s, 2H), 4,30 (t, 2H, J=7 Гц), 4,11 (s, 3H), 1,78 (m, 2H), 1,50 (m, 2 Н), 0,98 (t, 3H, J=7 Гц).
МПК / Метки
МПК: A61K 31/522, C07D 473/24, A61P 31/12, C07D 473/34, C07D 473/18, C07D 473/16
Метки: производные, инфекций, других, применения, пурина, вирусных, лечении, заболеваний, деазапурина
Код ссылки
<a href="https://eas.patents.su/30-20488-proizvodnye-purina-ili-deazapurina-dlya-primeneniya-pri-lechenii-virusnyh-infekcijj-i-drugih-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Производные пурина или деазапурина для применения при лечении вирусных инфекций и других заболеваний</a>
Предыдущий патент: Новые вторичные производные 8-оксихинолин-7-карбоксамида
Следующий патент: Модуляторы фармакокинетических свойств лекарственных средств
Случайный патент: Самобуферирующиеся композиции белков












