Производные бензимидазола в качестве противовоспалительных средств
Номер патента: 20282
Опубликовано: 30.10.2014
Авторы: Додс Хенри, Арндт Кирстен, Припке Хеннинг, Мак Юрген, Кюльцер Раймунд, Суна Эдгарс, Лубрикс Димитрийс, Рённ Роберт, Штенкамп Дирк, Пелькман Беньямин, Клиндер Клаус, Пфау Роланд
Формула / Реферат
1. Соединение общей формулы Id

в которой
R1 обозначает галоген, -OH, -CN; C1-C3-алкил, C2-C6-алкинил или -OC1-C3-алкил, где последние 3 группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -CN, =O, -OH, -OCH3 и -OCF3;
R2, R3 и R4 независимо обозначают водород, фтор, хлор- или -CH3, необязательно замещенный 1 или большим количеством атомов фтора;
Ra и Rb независимо обозначают водород или C1-C3-алкил или оба вместе с атомом углерода, к которому они присоединены, образуют C3-С7-циклоалкиленовое кольцо или 4-6-членное гетероциклоалкиленовое кольцо;
Rc обозначает водород или C1-C3-алкил;
W обозначает -C(O)-, -S(O)-, -S(O)2- или -C(O)O-, где эти группы присоединены к атому азота фрагмента
-NRc- через атом углерода или атом серы;
M обозначает C1-C7-алкил или C3-С7-циклоалкил, обе эти группы необязательно содержат в качестве заместителей 1 или большее количество групп, выбранных из группы, включающей фтор, -OH, -CN, -NH2,
-OC1-C3-алкил, -SC1-C3-алкил, C6-C10-арил (где последняя арильная группа может содержать 1 или большее количество заместителей, выбранных из группы, включающей галоген, -OH, -CN, C1-C3-алкил и -OC1-C3-алкил (где последние 2 алкильные группы необязательно замещены 1 или большим количеством атомов фтора)), C1-С7-алкил, C3-С7-циклоалкил-C0-C2-алкил (где последние алкильные и циклоалкильные группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -CN, =O, -NH2, -NH(C1-C3-алкил), -N(С1-С3-алкил)2, -OH и -OC1-C3-алкил); или C6-C10-арил, гетероарил или 4-7-членный гетероциклоалкил, где все эти группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей галоген, -CN, -OC1-C3-алкил, C1-С7-алкил и С3-С7-циклоалкил (где последние алкильные и циклоалкильные группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -CN и -OC1-C3-алкил);
R6 обозначает водород; C1-C3-алкил или C3-C5-циклоалкил-C0-C1-алкил, где последние 2 группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -OCH3, -NH(C1-C3-алкил) и -N(C1-C3-алкил)2;
каждый R7 обозначает водород, галоген, C1-C5-алкил-O-, C3-C5-циклоалкил-C0-C2-алкил-O- или 4-5-членный гетероциклоалкил-C0-C2-алкил-O- (где в последних 3 группах алкильные, циклоалкильные или гетероциклоалкильные фрагменты необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор и -OC1-C3-алкил, или содержат в качестве заместителей 1 или большее количество C1-C3-алкильных групп, которые могут быть необязательно замещены 1 или большим количеством атомов фтора);
L обозначает -C(O)NH- или -S(O)2NH-, где эти группы связаны с 9-членным конденсированным гетероароматическим ядром через атом углерода или атом серы, соответственно;
A обозначает водород, C1-C6-алкил, C3-C6-алкинил, фенил, 5-6-членный гетероарил, C3-C6-циклоалкил-C0-C2-алкил-, 4-6-членный гетероциклоалкил-C0-C2-алкил, фенил-C1-C3-алкил- или 5-6-членный гетероарил-C1-C3-алкил, где в этих группах алкильные, алкинильные, циклоалкильные и гетероциклоалкильные фрагменты необязательно содержат 1 или 2 заместителя, выбранных из числа R9a, и фенильные и гетероарильные фрагменты необязательно содержат 1 или 2 заместителя, выбранных из числа R9b;
каждый R9a независимо обозначает фтор, фенил, C1-C2-алкил или -OC1-C4-алкил, где последние 2 группы необязательно замещены 1-3 атомами фтора;
каждый R9b независимо обозначает фтор, хлор, бром, C1-C2-алкил или -OC1-C2-алкил, где последние 2 группы необязательно замещены 1 или большим количеством атомов фтора;
где термин "гетероциклоалкил" означает стабильные 4-, 5-, 6- или 7-членные моноциклические гетероциклические кольцевые системы, которые могут быть и насыщенными, и мононенасыщенными, и где 1 или 2 кольцевых атомов углерода могут быть независимо заменены на гетероатомы, которые выбраны из группы, включающей кислород, азот и серу, последние 2 из этих гетероатомов могут быть необязательно окислены; и
термин "гетероарил" означает 5- или 6-членные гетероциклические ароматические группы, которые могут содержать 1, 2, 3 или 4 гетероатома, выбранных из группы, включающей кислород, серу и азот;
его фармацевтически приемлемые соли с органическими или неорганическими кислотами или основаниями.
2. Соединение по п.1, в котором
M обозначает C1-C6-алкил, C3-C6-циклоалкил или 4-6-членный гетероциклоалкил, где все эти группы необязательно замещены 1 или большим количеством групп, выбранных из группы, включающей фтор,
-OH, -CN, -NH2, фенил, -CF3, C1-C2-алкил и C3-С5-циклоалкил-C0-C1-алкил; или фенил или 5-6-членный гетероарил, где обе эти группы необязательно содержат 1 или большее количество заместителей, независимо выбранных из группы, включающей фтор, хлор, метил, -CF3 и -OCH3;
его фармацевтически приемлемые соли с органическими или неорганическими кислотами или основаниями.
3. Соединение формулы Ie по п.1 или 2
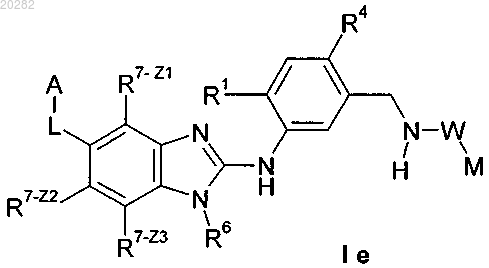
в которой
A обозначает водород, C1-C6-алкил, фенилпропаргил, фенил, C3-C6-циклоалкил-C0-C2-алкил-, тетрагидрофуранил-C0-C2-алкил, пирролидинил-C0-C2-алкил, пиперидин-C0-C2-алкил или пиридил-С1-C2-алкил-, где в этих группах алкильные, алкинильные, циклоалкильные и гетероциклоалкильные фрагменты необязательно содержат 1 или большее количество заместителей, выбранных из числа R9a, и фенильные и пиридильные фрагменты необязательно содержат 1 или большее количество заместителей, выбранных из числа R9b;
каждый R9a независимо обозначает фтор, С1-C2-алкил или -OC1-C4-алкил, где в последних 2 группах алкильные фрагменты необязательно замещены 1 или большим количеством атомов фтора;
каждый R9b независимо обозначает фтор, хлор или бром;
L обозначает -C(O)NH- или -S(O)2NH-, где эти группы связаны с 9-членным конденсированным гетероароматическим ядром через атом углерода или атом серы, соответственно;
W обозначает -C(O)- или -S(O)2-;
M обозначает С1-С4-алкил или C3-C6-циклоалкил, где последние 2 группы необязательно замещены 1 или большим количеством групп, выбранных из группы, включающей фтор, -OH, -CN, -NH2, фенил, CF3, C1-C2-алкил и циклопропилметил; или обозначает оксетанил или тетрагидрофуранил, где обе эти группы необязательно замещены группой CH3; или фенил или тиенил, где обе эти группы необязательно содержат 1 или 2 заместителя, независимо выбранных из группы, включающей фтор или хлор;
R1 обозначает фтор, хлор, бром, CH3, CH2F, CHF2, CF3 или -OCH3;
R4 обозначает водород или фтор;
R6 обозначает водород, С1-C3-алкил или C3-С5-циклоалкил-C0-С1-алкил, где последние 2 группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -OCH3, -NH(С1-C3-алкил) и -N(С1-C3-алкил)2;
R7-Z2 обозначает водород, галоген или -OC1-C5-алкил, где в последней группе алкил необязательно замещен 1 или большим количеством атомов фтора;
R7-Z1 и R7-z3 независимо обозначают водород или фтор;
его фармацевтически приемлемые соли с органическими или неорганическими кислотами или основаниями.
4. Соединение по любому из пп.1-3, выбранное из
Пример Структура
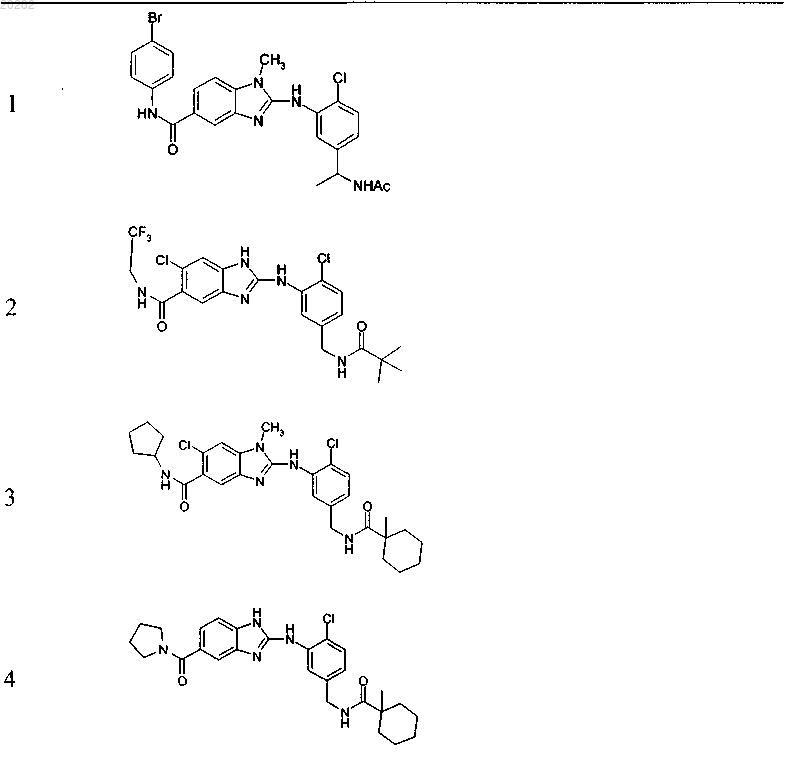
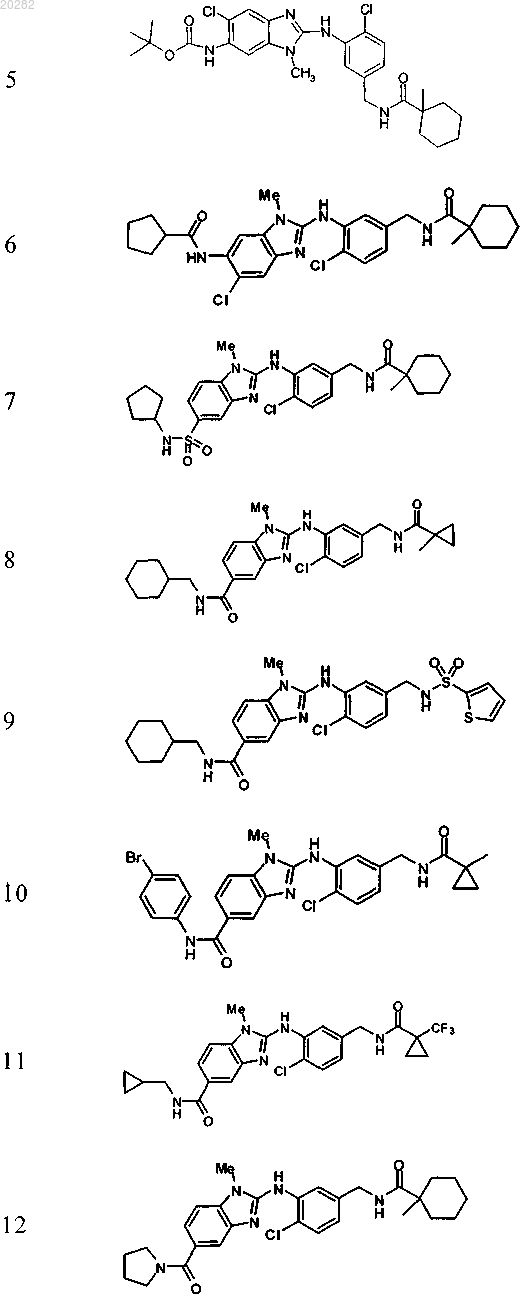
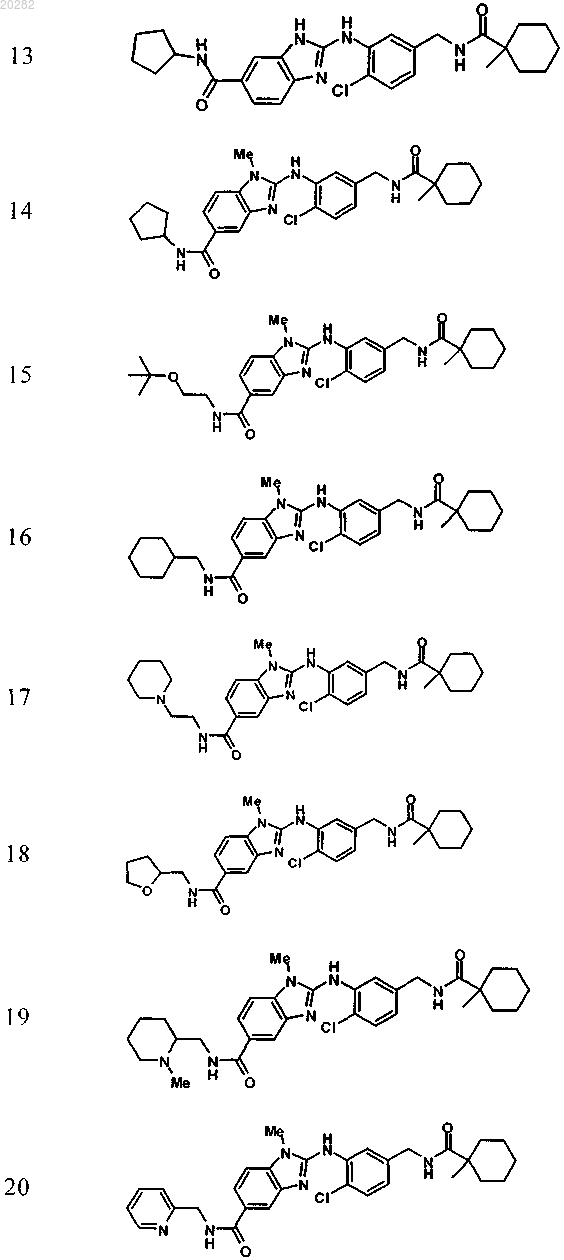
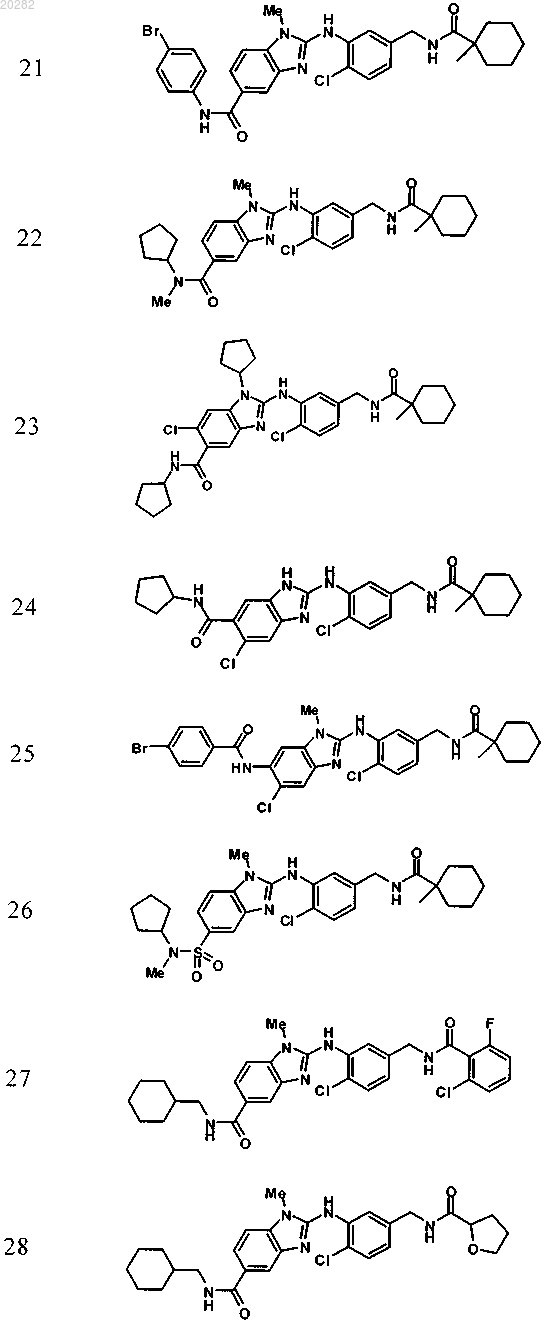

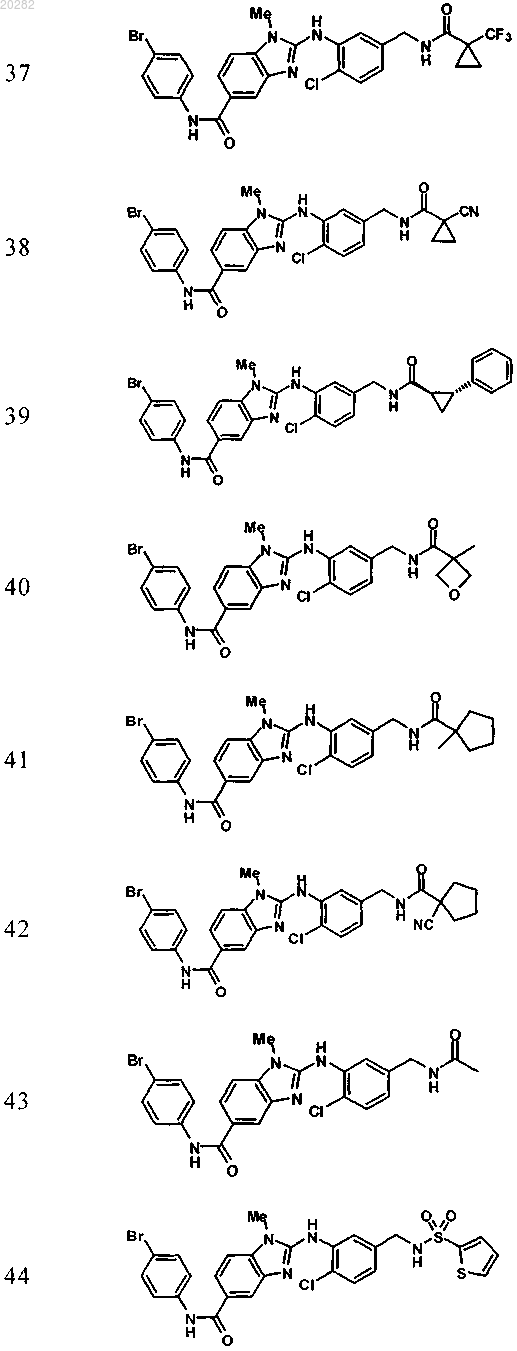
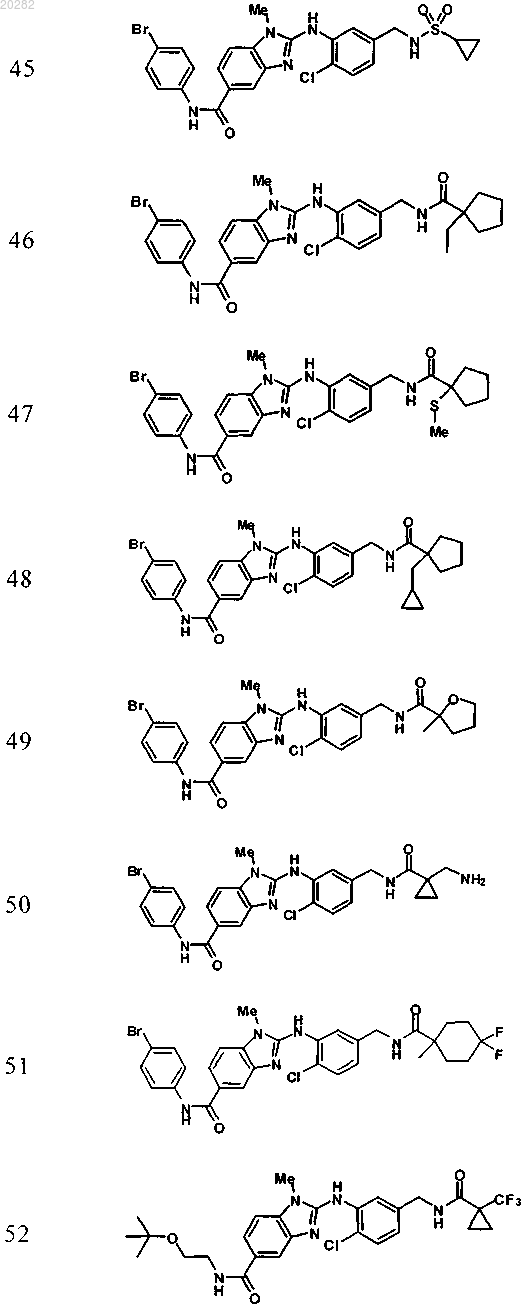
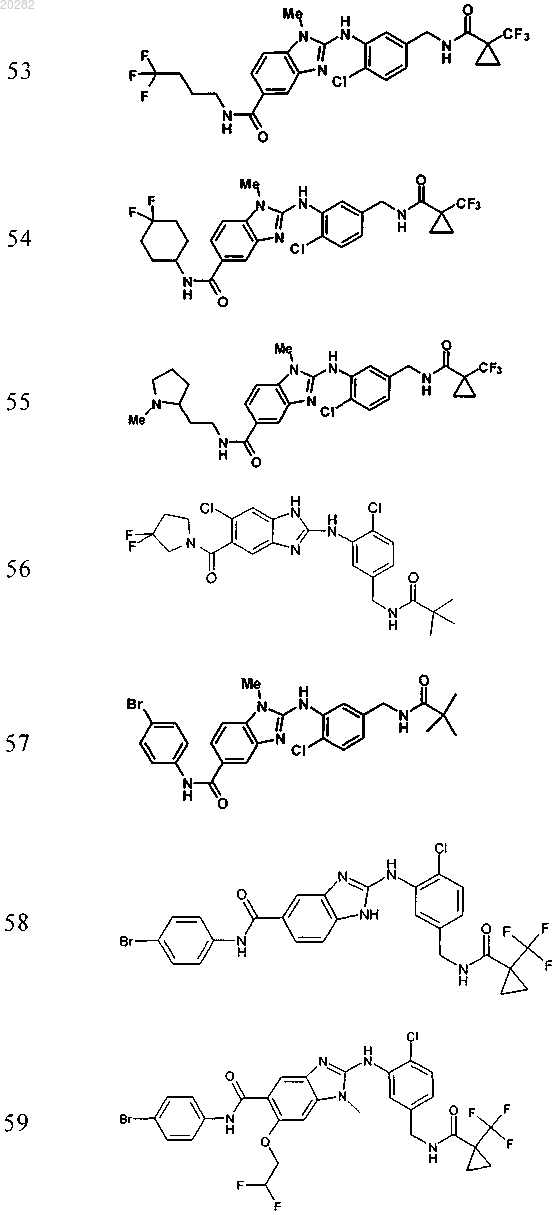
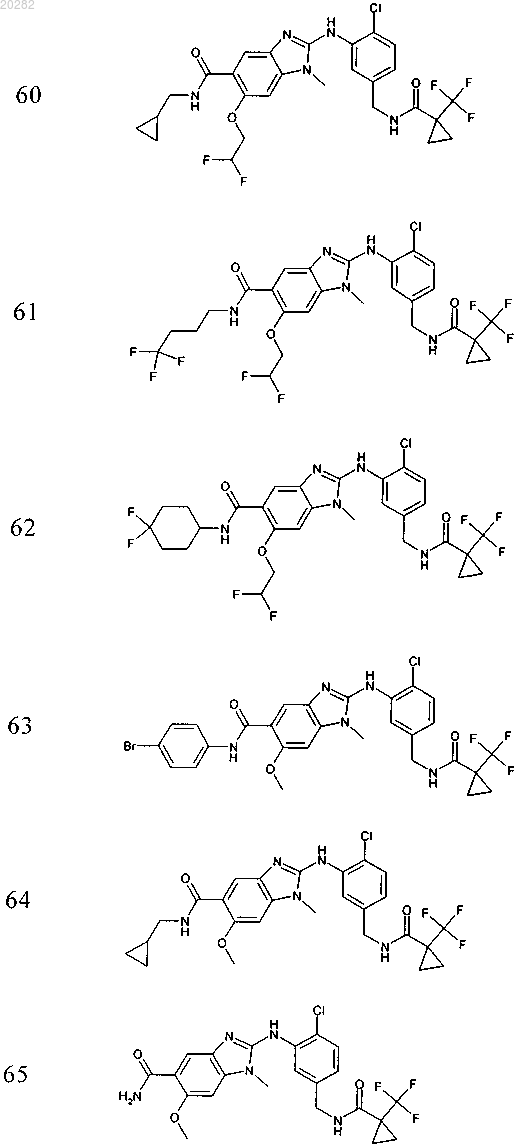
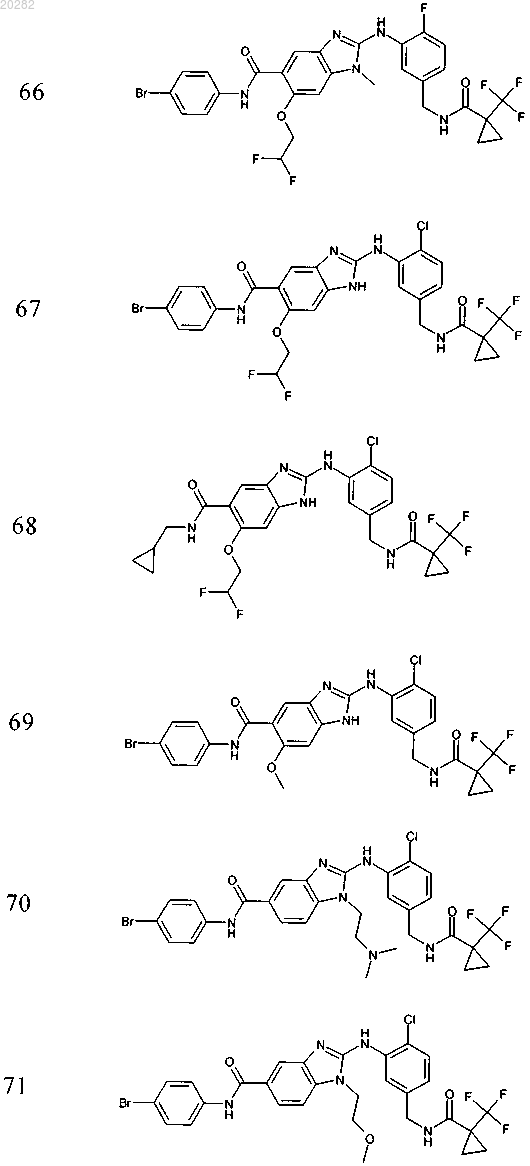
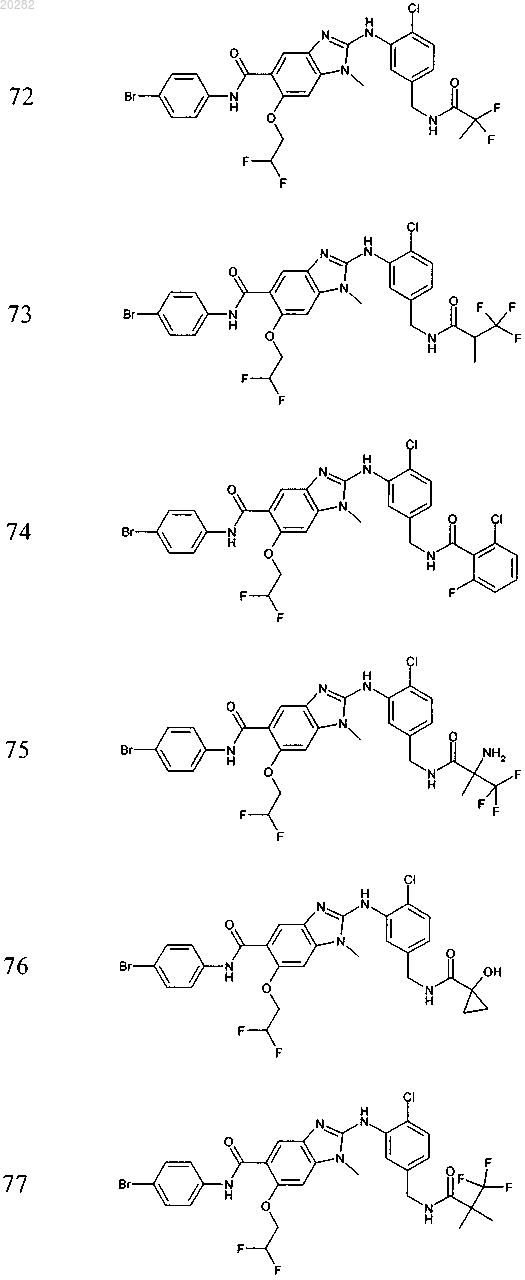
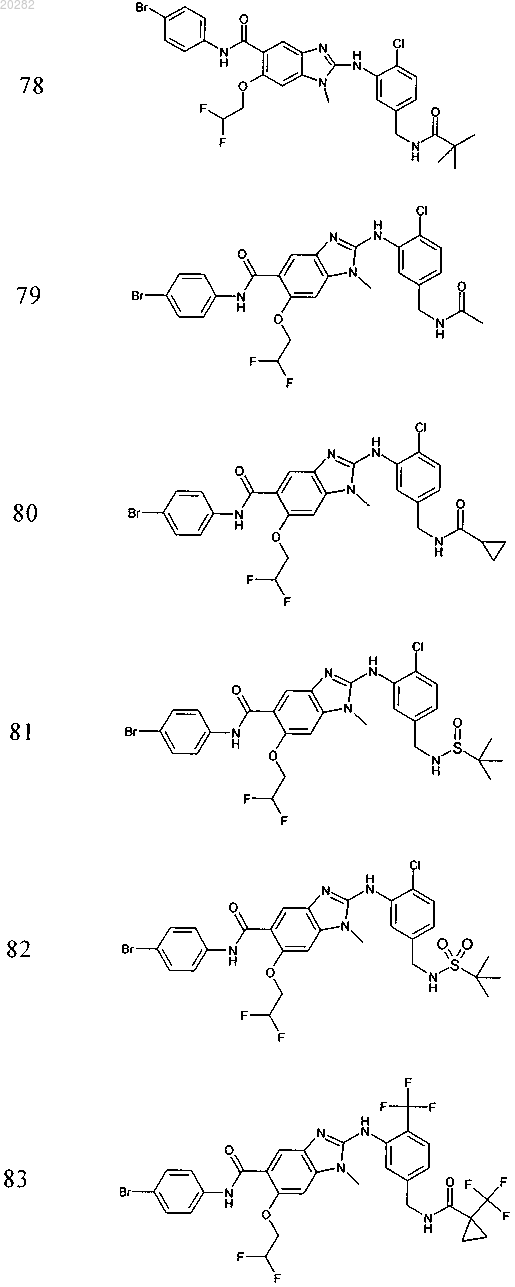
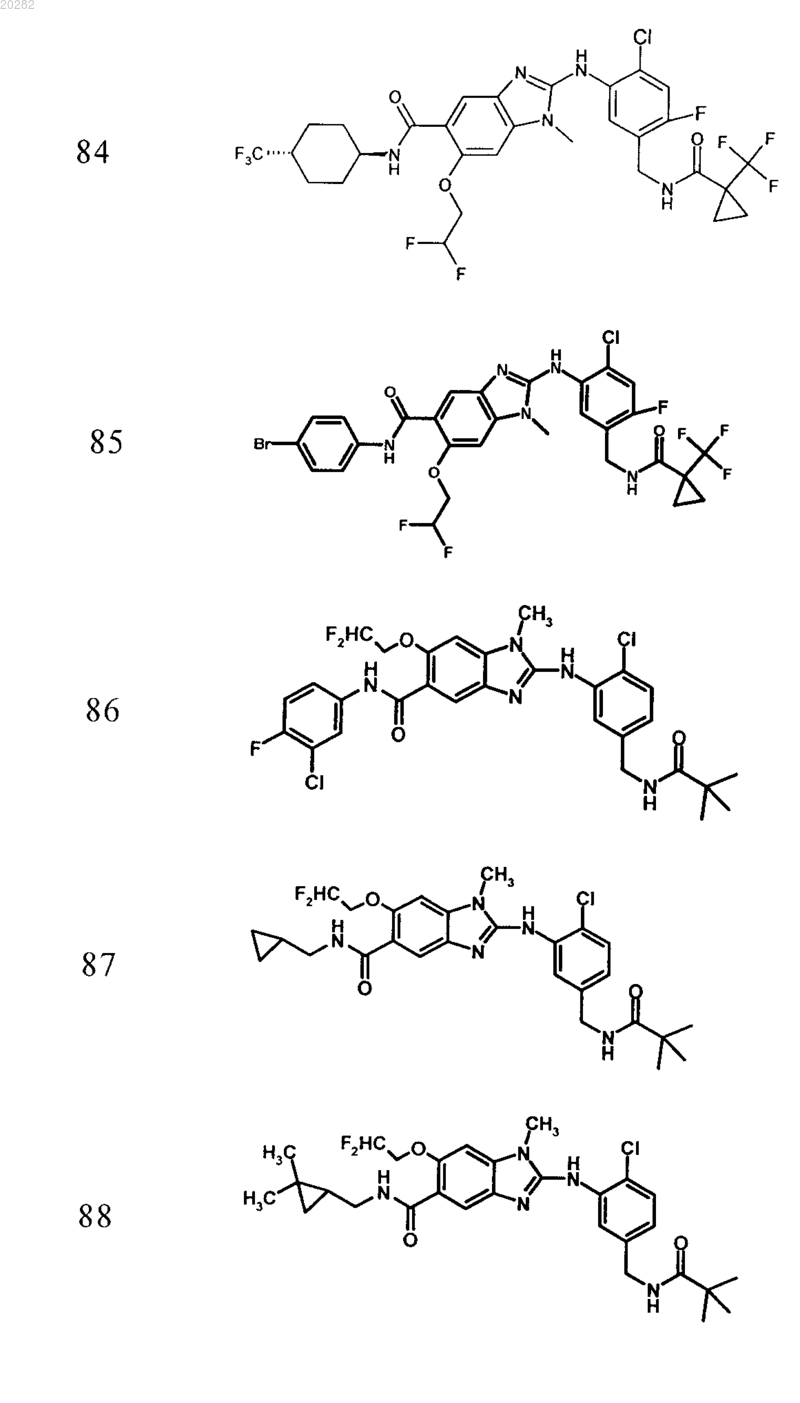
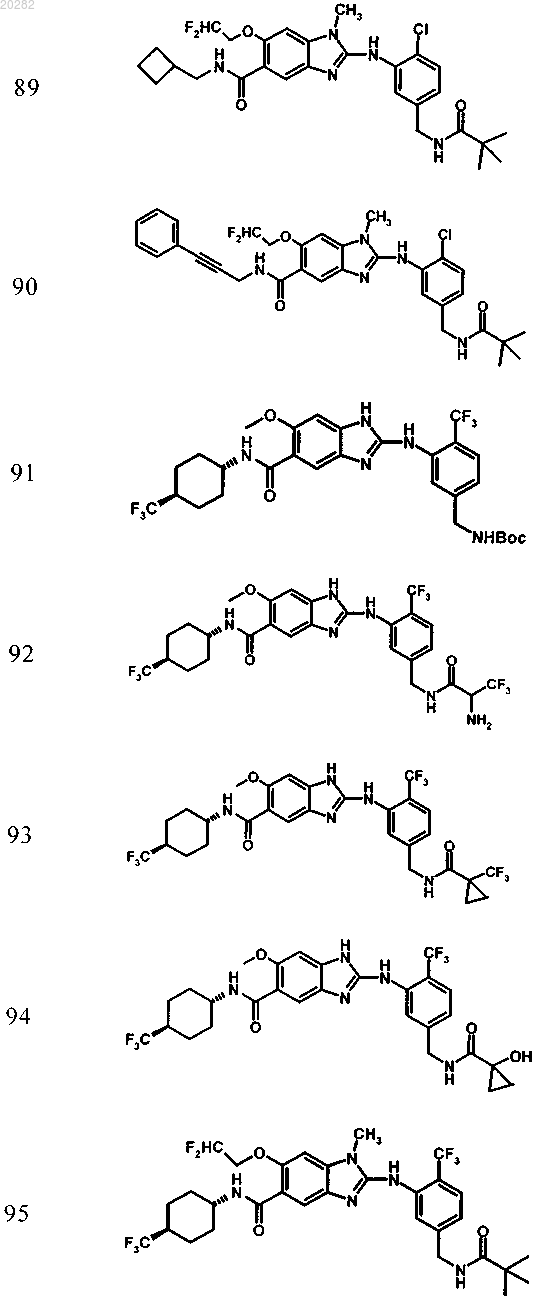
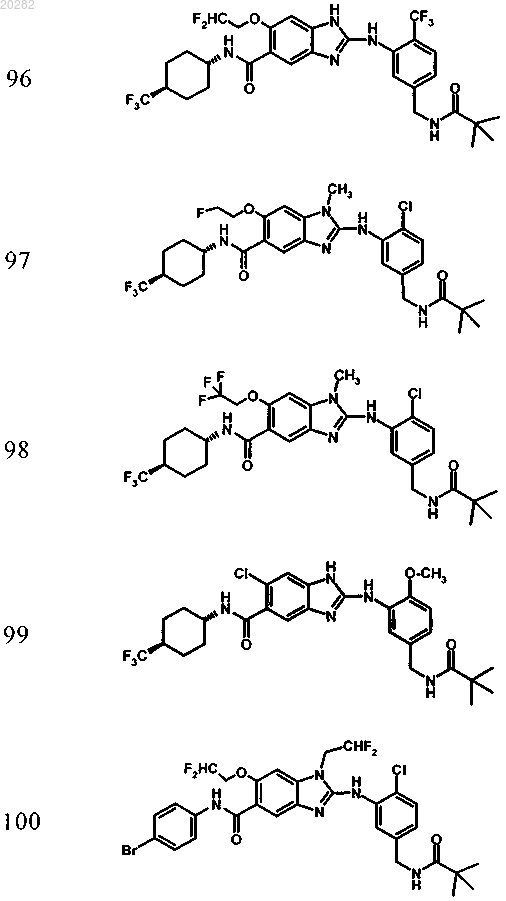
или его фармацевтически приемлемая соль с органической или неорганической кислотой или основанием.
5. Применение соединения по любому из пп.1-4 в качестве фармацевтического средства, обладающего ингибирующей активностью в отношении микросомной простагландин-E2-синтазы-1 (mPGES-1).
6. Фармацевтическая композиция, включающая по меньшей мере одно соединение по любому из пп.1-4 в смеси с фармацевтически приемлемым вспомогательным веществом, разбавителем или носителем.
7. Применение соединения по любому из пп.1-4 для предупреждения и/или лечения воспалительных заболеваний или родственных патологических состояний, включающих воспалительный компонент.
8. Применение по п.7, где патологическим состоянием, которое необходимо лечить и/или предупреждать, является боль.
Текст
ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ СРЕДСТВ Белоусов Ю.В., Куликов А.В.,Кузнецова Е.В. (RU) В изобретении описаны соединения общей формулы Id Веселицкая И.А., Кузенкова Н.В.,Веселицкий М.Б., Каксис Р.А., в которой A, L, M, R1, R2, R3, R4, R6, R7, Ra, Rb, Rc, W определены в описании, их соли,предпочтительно их фармацевтически приемлемые соли. Соединения могут быть применимы для лечения и/или предупреждения воспалительных заболеваний и родственных патологических состояний, в частности для лечения и/или предупреждения боли. Также описаны применение таких соединений в качестве фармацевтических средств и фармацевтические композиции, содержащие такие соединения.(71)(73) Заявитель и патентовладелец: БРИНГЕР ИНГЕЛЬХАЙМ ИНТЕРНАЦИОНАЛЬ ГМБХ (DE) Область техники, к которой относится изобретение Настоящее изобретение относится к новым соединениям, которые являются ингибиторами микросомной простагландин-E2-синтазы-1 (mPGES-1), к фармацевтическим композициям, содержащим эти соединения, и к применению таких соединений в качестве лекарственных средств, предназначенных для лечения и/или предупреждения воспалительных заболеваний и родственных патологических состояний. Уровень техники Существует много острых и хронических заболеваний/нарушений, которые являются воспалительными по своей природе, включая, но не ограничиваясь только ими, ревматоидные заболевания, например ревматоидный артрит, остеоартрит, заболевания внутренних органов, например воспалительную болезнь кишечника, аутоиммунные заболевания, например красную волчанку, заболевания легких, такие как астма и ХОЗЛ (хроническое обструктивное заболевание легких). Существующие способы лечения нестероидными противовоспалительными лекарственными средствами (НСПВС) и ингибиторами циклооксигеназы(COX)-2 являются эффективными, но при этом часто проявляются побочные эффекты со стороны желудочно-кишечного тракта и сердечно-сосудистой системы. Настоятельно необходимы новые средства лечения, которые обладают такой же эффективностью и улучшенным профилем побочных эффектов. Ингибиторы НСПВС и COX-2 уменьшают воспаление и боль посредством ингибирования обеих изоформ ферментов COX. Фермент циклооксигеназа (COX) существует в двух формах, одна из которых конститутивно экспрессируется во многих клетках и тканях (COX-1) и другая индуцируется в большинстве клеток и тканей провоспалительными факторами, такими как цитокины, во время воспалительного ответа (COX-2). В ходе метаболизма COX превращают арахидоновую кислоту в нестабильный промежуточный продукт, простагландин-H2 (PGH2). Затем PGH2 подвергается метаболизму с образованием других простагландинов, включая PGE2, PGF2, PGD2, простациклин и тромбоксан A2. Известно, что эти метаболиты арахидоновой кислоты обладают выраженной физиологической и патофизиологической активностью, включая провоспалительные эффекты. В частности, известно, что PGE2 является сильным провоспалительным медиатором, и также известно, что он может являться причиной лихорадки, воспаления и боли. Поэтому было разработано много лекарственных средств, действие которых направлено на ингибирование образования PGE2, включая "НСПВС" (нестероидные противовоспалительные лекарственные средства) и "коксибы" (селективные ингибиторы COX-2). Действие таких лекарственных средств преимущественно основано на ингибировании COX-1 и/или COX-2, вследствие которого уменьшается образование PGE2. Однако ингибирование COX обладает тем недостатком, что оно приводит к уменьшению образования всех метаболитов PGH2 в прямом направлении, а для некоторых из них известно, что они обладают полезными характеристиками. Ввиду этого, известно/предполагается, что лекарственные средства, действие которых основано на ингибировании COX, являются причиной неблагоприятных биологических эффектов. Например, неселективное ингибирование COX с помощью НСПВС может являться причиной побочных эффектов со стороны желудочно-кишечного тракта и влиять на тромбоциты и работу почек. Полагают, что, хотя при селективном ингибировании COX-2 коксибами ослабляются такие побочные эффекты со стороны желудочно-кишечного тракта, все же происходят нарушения сердечно-сосудистой системы. Таким образом, несомненно полезным для клинической практики было бы альтернативное средство лечения воспалительных заболеваний, которое не приводит к указанным выше побочным эффектам. В частности, можно ожидать, что, лекарственное средство, которое предпочтительно селективно ингибирует превращение PGH2 в провоспалительный медиатор PGE2, будет уменьшать воспалительный ответ при отсутствии соответствующего уменьшения образования других полезных метаболитов арахидоновой кислоты. Соответственно, можно ожидать, что такое ингибирование будет облегчать указанные выше нежелательные побочные эффекты.PGH2 можно превратить в PGE2 с помощью простагландин-E-синтазы (PGES). Описаны две микросомные простагландин-E-синтазы (mPGES-1 и mPGES-2) и одна цитозольная простагландин-E-синтаза(cPGES). Лейкотриены (LT) образуются из арахидоновой кислоты под действием ряда ферментов, отличающихся от тех, которые относятся к пути COX/PGES. Известно, что лейкотриен B4 является сильным провоспалительным медиатором, в то время как цистейнилсодержащие лейкотриены, С 4, D4 и Е 4 (CysLT), в основном, являются весьма активными бронхосуживающими средствами и поэтому участвуют в патологии астмы. Биологические воздействия CysLT опосредуются двумя рецепторами, обозначаемыми как CysLT1 иCysLT2. Антагонисты лейкотриенового рецептора (LTRa) были разработаны в качестве альтернативы стероидам для лечения астмы. Эти лекарственные средства можно вводить перорально, но они не обеспечивают удовлетворительную борьбу с воспалением. Применяющиеся в настоящее время LTRa являются высокоселективными по отношению к CysLT1. Можно предположить, что более эффективная борьба с астмой и, возможно, также с ХОЗЛ может быть обеспечена, если будет возможным уменьшение активности обоих рецепторов CysLT. Это можно осуществить путем разработки неселективных LTRa, а также путем ингибирования активности белков, например ферментов, участвующих в синтезе CysLT. Из числа таких белков можно отметить 5-липоксигеназу, активирующий 5-липоксигеназу белок (FLAP) и лейкотриен-C4-синтазу. Ингибитор FLAP также может уменьшать количество образующегося провоспалительного LTB4.mPGES-1, FLAP и лейкотриен-C4-синтаза относятся к семейству связанных с мембраной белков,участвующих в метаболизме эйкозаноида и глутатиона (MAPEG). Другие представители этого семейства включают микросомные глутатион-S-трансферазы (MGST1, MGST2 и MGST3). Обзор приведен в публикации P.-J. Jacobsson et al. in Am. J. Respir. Crit. Care Med. 161, S20 (2000). Хорошо известно, что соединения, полученные в качестве антагонистов одного из MAPEG, также могут проявлять ингибирующую активность по отношению к другим представителям семейства, см. публикации J.H. Hutchinson et al.in J. Med. Chem. 38, 4538 (1995) и D. Claveau et al. in J. Immunol. 170, 4738 (2003). В первой публикации также указано, что такие соединения также могут проявлять значительную перекрестную реакционную способность с белками каскада арахидоновой кислоты, которые не принадлежат к семейству MAPEG,например с 5-липоксигеназой. Таким образом, средства, способные ингибировать действие mPGES-1 и, следовательно, уменьшающие количество образующегося конкретного метаболита арахидоновой кислоты, PGE2, вероятно,будут полезны для лечения воспаления. Кроме того, средства, способные ингибировать действие белков,участвующих в синтезе лейкотриенов, вероятно, также будут полезны для лечения астмы и ХОЗЛ. Известно, что в дополнение к их противовоспалительному воздействию ингибиторы mPGES-1 также можно применять для лечения или предупреждения новообразований, например, как это описано в заявке на международный патент WO 2007/124589. Рациональным объяснением этому может являться тот факт, что, как полагают, продуцирование PGE2 стимулирует образование, рост и/или метастазирование новообразований. Поскольку mPGES-1 часто экспрессируется вместе с COX-2 в доброкачественных и злокачественных новообразованиях, ингибирование mPGES-1 (а не COX-2) может являться причиной уменьшения количества PGE2 и поэтому ингибиторы mPGES-1 могут быть применимы для лечения доброкачественных и злокачественных новообразований. Упоминание или обсуждение в настоящем описании очевидно опубликованного ранее документа не следует обязательно рассматривать в качестве подтверждения того, что документ соответствует части известного уровня техники или соответствует известному уровню техники. Подробное описание изобретения Первым вариантом осуществления являются соединения общей формулы IdR1 обозначает галоген, -OH, -CN; C1-C3-алкил, C2-C6-алкинил, -OC1-C3-алкил, где последние 3 группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -CN, =O, -OH, -OCH3, -OCF3;R2, R3 и R4 независимо обозначают водород, фтор, хлор или -CH3, необязательно замещенный 1 или большим количеством атомов фтора;Ra, Rb независимо обозначают водород, C1-C3-алкил или оба вместе с атомом углерода, к которому они присоединены, образуют C3-C7-циклоалкиленовое кольцо или 4-6-членное гетероциклоалкиленовое кольцо;Rc обозначает водород или C1-C3-алкил;W обозначает -C(O)-, -S(O)-, -S(O)2- или -C(O)O-, где эти группы присоединены к атому азота фрагмента -NRc- через атом углерода или атом серы;M обозначает C1-C7-алкил, C3-C7-циклоалкил, обе эти группы необязательно содержат в качестве заместителей 1 или большее количество групп, выбранных из группы, включающей: фтор, -OH, -CN,-NH2, -OC1-C3-алкил, -SC1-C3-алкил, C6-C10-арил (где последняя арильная группа может содержать 1 или большее количество заместителей, выбранных из группы, включающей галоген, -OH, -CN, C1-C3-алкил,-OC1-C3-алкил (где последние 2 алкильные группы необязательно замещены 1 или большим количеством атомов фтора, С 1-С 7-алкил, C3-С 7-циклоалкил-С 0-С 2-алкил (где последние алкильные и циклоалкильные группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -CN, =O, -NH2, -NH(C1-C3-алкил), -N(С 1-C3-алкил)2, -ОН, -OC1-C3-алкил); или C6-C10-арил,гетероарил, 4-7-членный гетероциклоалкил, все эти группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей галоген, -CN, -OC1-C3-алкил, C1-C7-алкил,С 3-С 7-циклоалкил (где последние алкильные и циклоалкильные группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -CN, -ОС 1-C3-алкил);R6 обозначает водород; C1-C5-алкил, C3-С 5-циклоалкил-С 0-С 1-алкил, где последние 2 группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор,-ОСН 3, -NH(C1-C3-алкил), -N(С 1-C3-алкил)2; каждый R7 обозначает водород, галоген, C1-C5-алкил-О-, C3-С 5-циклоалкил-С 0-С 2-алкил-О-, 4-5-2 020282 членный гетероциклоалкил-С 0-С 2-алкил-О- (где в последних 3 группах алкильные, циклоалкильные или гетероциклоалкильные фрагменты необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор, -OC1-C3-алкил, или содержат в качестве заместителей 1 или большее количество C1-C3-алкильных групп, которые могут быть необязательно замещены 1 или большим количеством атомов фтора);L обозначает -C(O)NH- или -S(O)2NH-, где эти группы связаны с 9-членным конденсированным гетероароматическим ядром через атом углерода или атом серы, соответственно;A обозначает водород, C1-С 6-алкил, C3-C6-алкинил, фенил, 5-6-членный гетероарил, C3-C6-циклоалкил-C0-C2-алкил-, 4-6-членный гетероциклоалкил-C0-C2-алкил, фенил-C1-C3-алкил-, 5-6-членный гетероарил-С 1-C3-алкил, где в этих группах алкильные, алкинильные, циклоалкильные и гетероциклоалкильные фрагменты необязательно содержат 1 или 2 заместителя, выбранных из числа R9a, и фенильные, тиенильные и пиридильные фрагменты необязательно содержат 1 или 2 заместителя, выбранных из числа R9b; каждый R9a независимо обозначает фтор, фенил, С 1-С 2-алкил,-ОС 1-С 4-алкил, где последние 2 группы необязательно замещены 1-3 атомами фтора; каждый R9b независимо обозначает фтор, хлор, бром, C1-C2-алкил, -ОС 1-С 2-алкил, где последние 2 группы необязательно замещены 1 или большим количеством атомов фтора; где термин "гетероциклоалкил" означает стабильные 4-, 5-, 6- или 7-членные моноциклические гетероциклические кольцевые системы, которые могут быть и насыщенными, и мононенасыщенными, и где 1 или 2 кольцевых атома углерода могут быть независимо заменены на гетороатомы, которые выбраны из группы, включающей кислород, азот и серу, последние 2 из этих гетероатомов могут быть необязательно окислены; и термин "гетероарил" означает 5- или 6-членные гетероциклические ароматические группы, которые могут содержать 1, 2, 3 или 4 гетероатома, выбранных из группы, включающей кислород, серу и азот; их фармацевтически приемлемые соли с органическими или неорганическими кислотами или основаниями. Другим вариантом осуществления являются соединения общей формулы Id, в которой группы A, L,R1, R2, R3, R4, R6, R7, Ra, Rb, Rc, W обладают такими же значениями, как определенные в предыдущем варианте осуществления, и M обозначает C1-C6-алкил, C3-C6-циклоалкил, 4-6-членный гетероциклоалкил, где все эти группы необязательно замещены 1 или большим количеством групп, выбранных из группы, включающей фтор, -OH, -CN, -NH2, фенил, -CF3, C1-C2-алкил, C3-C5-циклоалкил-C0-С 1-алкил; или фенил, 5-6-членный гетероарил, где обе эти группы необязательно содержат 1 или большее количество заместителей, независимо выбранных из группы, включающей фтор, хлор, метил, -CF3, -OCH3; их фармацевтически приемлемые соли с органическими или неорганическими кислотами или основаниями. В другом варианте осуществления настоящее изобретение относится к соединениям формулы Id, а именно к соединениям формулы Ie в которой А обозначает водород, C1-C6-алкил, фенилпропаргил, фенил, C3-C6-циклоалкил-C0-C2-алкил-, тетрагидрофуранил-C0-C2-алкил, пирролидинил-C0-C2-алкил, пиперидин-C0-C2-алкил, пиридил-С 1-C2-алкил-,где в этих группах алкильные, алкинильные, циклоалкильные и гетероциклоалкильные фрагменты необязательно содержат 1 или большее количество заместителей, выбранных из числа R9a, и фенильные и пиридильные фрагменты необязательно содержат 1 или большее количество заместителей, выбранных из числа R9b; каждый R9a независимо обозначает фтор, С 1-C2-алкил, -ОС 1-С 4-алкил, где в последних 2 группах алкильные фрагменты необязательно замещены 1 или большим количеством атомов фтора; каждый R9b независимо обозначает фтор, хлор, бром;L обозначает -C(O)NH- или -S(O)2NH-, где эти группы связаны с 9-членным конденсированным гетероароматическим ядром через атом углерода или атом серы, соответственно;M обозначает С 1-С 4-алкил, C3-C6-циклоалкил, где последние 2 группы необязательно замещены 1 или большим количеством групп, выбранных из группы, включающей фтор, -OH, -CN, -NH2, фенил, CF3,С 1-C2-алкил, циклопропилметил; или обозначает оксетанил или тетрагидрофуранил, где обе эти группы необязательно замещены группой CH3; или фенил, тиенил, где обе эти группы необязательно содержат 1 или 2 заместителя, независимо выбранных из группы, включающей фтор или хлор;R4 обозначает водород или фтор;R6 обозначает водород, C1-C3-алкил, C3-C5-циклоалкил-C0-С 1-алкил, где последние 2 группы необязательно содержат 1 или большее количество заместителей, выбранных из группы, включающей фтор,-OCH3, -NH(C1-C3-алкил), -N(С 1-C3-алкил)2;R7-Z2 обозначает водород, галоген, -OC1-C5-алкил, где в последней группе алкил необязательно замещен 1 или большим количеством атомов фтора;R7-Z1 и R7-Z3 независимо обозначают водород или фтор; к их фармацевтически приемлемым солям с органическими или неорганическими кислотами или основаниями. Использующиеся термины и определения Выражение "фармацевтически приемлемое" используется в настоящем изобретении для указания таких соединений, материалов, композиций и/или дозированных форм, которые в соответствии с основными положениями медицины являются подходящими для использования при соприкосновении с тканями людей и животных без проявления чрезмерной токсичности, раздражающего воздействия, аллергической реакции или других затруднений или осложнений при разумном соотношении польза/риск. При использовании в настоящем изобретении "фармацевтически приемлемые соли" означают производные раскрытых соединений, в которых исходное соединение изменено путем образования его солей с кислотой или основанием. Примеры фармацевтически приемлемых солей включают, но не ограничиваются только ими, соли неорганических или органических кислот с основными остатками, такими как аминогруппы; соли щелочных металлов или органических соединений с кислотными остатками, такими как карбоксигруппы и т.п. Фармацевтически приемлемые соли включают обычные нетоксичные соли или четвертичные аммониевые соли исходного соединения, образованные, например, из нетоксичных неорганических или органических кислот. Фармацевтически приемлемые соли, предлагаемые в настоящем изобретении, можно синтезировать из исходного соединения, которое содержит основной или кислотный фрагмент, по обычным химическим методикам. Обычно такие соли можно получить по реакции этих соединений в форме свободной кислоты или основания со стехиометрическим количеством соответствующего основания или кислоты в воде, или органическом растворителе, или в их смеси; обычно являются предпочтительными неводные среды, такие как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечни подходящих солей приведены в публикации Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton,Pa., 1985, p. 1418, описание которой включено в настоящее изобретение в качестве ссылки. Примеры фармацевтически активных солей каждого их соединений, которые являются объектами настоящего изобретения, включают, но не ограничиваются только ими, соли, которые получают из фармацевтически приемлемых кислот или оснований, включая органические и неорганические кислоты и основания. Если предпочтительное соединение является основанием, то соли можно получить из фармацевтически приемлемых кислот. При выборе наиболее предпочтительной соли или при принятии решения о том, следует ли использовать соль или нейтральное соединение, принимают во внимание, в частности, такие характеристики, как биологическая доступность, простота приготовления, способность подвергаться обработке и устойчивость при хранении. Подходящие фармацевтически приемлемые кислоты включают уксусную кислоту, бензолсульфоновую кислоту (безилат), бензойную кислоту, п-бромфенилсульфоновую кислоту, камфорсульфоновую кислоту, угольную кислоту, лимонную кислоту, этансульфоновую кислоту, фумаровую кислоту, глюконовую кислоту, глутаминовую кислоту, бромисто-водородную кислоту, хлористо-водородную кислоту,йодисто-водородную кислоту, изетионовую кислоту, молочную кислоту, малеиновую кислоту, яблочную кислоту, миндальную кислоту, метансульфоновую кислоту (мезилат), слизевую кислоту, азотную кислоту,щавелевую кислоту, памоевую кислоту, пантотеновую кислоту, фосфорную кислоту, янтарную кислоту,серную кислоту, винную кислоту, п-толуолсульфоновую кислоту и т.п. Примеры фармацевтически приемлемых солей включают, но не ограничиваются только ими, ацетат, бензоат, гидроксибутират, бисульфат,бисульфит, бромид, бутин-1,4-диоат, капроат, хлорид, хлорбензоат, цитрат, дигидрофосфат, динитробензоат,фумарат, глутаминат, гликолят, гептаноат, гексин-1,6-дикарбонат, гидроксибензоат, йодид, лактат, малеат,малонат, манделат, метафосфат, метансульфонат, метоксибензоат, метилбензоат, моногидрофосфат, нафталин-1-сульфонат, нафталин-2-сульфонат, оксалат, фенилбутират, фенилпропионат, фосфат, фталат,фенилацетат, пропансульфонат, пропиолат, пропионат, пироглутаминат, пирофосфат, пиросульфат, себацинат, суберат, сукцинат, сульфат, сульфит, сульфонат, тартрат, трифторацетат, ксилолсульфонат и т.п."Изомеры". Следует понимать, что соединения, предлагаемые в настоящем изобретении, могут содержать 1 или большее количество асимметрически замещенных атомов углерода и поэтому их можно выделить в виде рацемической формы или оптически активной формы (т.е. в форме их соответствующих энантиомеров или диастереоизомеров). В некоторых случаях энантиомер или диастереоизомер соединения формулы Id может обладать большей активностью, чем другой изомер. При необходимости диастереоизомеры можно выделить путем разделения диастереоизомерной смеси соединений по обычным методикам, например с помощью фракционной кристаллизации или ВЭЖХ (высокоэффективная жидкостная хроматография). Искомые энантиомеры можно получить по методикам, хорошо известным специалисту в данной области техники,т.е. по реакции соответствующих оптически активных исходных веществ при условиях, которые не приводят к рацемизации или эпимеризации (т.е. по методике "хирального пула"), по реакции соответствующего исходного вещества с "хиральным вспомогательным соединением", которое затем можно удалить на подходящей стадии, путем получения производных (т.е. разделение, включая динамическое разделение), например, с гомохиральной кислотой с последующим разделением диастереоизомерных производных по обычным методикам, таким как хроматография (см., например, Thomas J. Tucker, et al., J. Med.Chem. 1994, 37, 2437-2444), или по реакции с соответствующим хиральным реагентом или хиральным катализатором при условиях, известных специалисту в данной области техники (например, Mark A.Huffman, et al., J. Org. Chem. 1995, 60, 1590-1594). Соединения, предлагаемые в настоящем изобретении, могут содержать двойные связи и таким образом существовать в виде геометрических изомеров, обладающих E- (заместители расположены с разных сторон от двойной связи) и Z- (заместители расположены с одной стороны от двойной связи) конфигурацией, различающихся расположением заместителей вокруг каждой отдельной двойной связи. Все такие изомеры и их смеси входят в объем настоящего изобретения. Соединения, предлагаемые в настоящем изобретении, также могут обладать таутомерией. Все таутомерные формы и их смеси входят в объем настоящего изобретения. Например, соединение, содержащее фрагмент "1H-бензимидазол", можно рассматривать как идентичное соответствующему соединению, содержащему фрагмент "3H-бензимидазол". Если специально не указана конкретная стереохимическая конфигурация или изомерная форма, то все хиральные, энантиомерные, диастереоизомерные, рацемические формы, таутомерные формы и все геометрические изомерные формы структуры входят в объем настоящего изобретения. Очевидно, что предпочтительным является изомер, который наиболее фармакологически эффективен и приводит к наименьшему количеству побочных эффектов. Объектом настоящего изобретения также являются дейтерированные соединения общей формулыId, т.е. такие, в которых 1 или большее количество атомов водорода, например 1, 2, 3, 4 или 5 атомов водорода, заменены на изотоп водорода, дейтерий. Термин "C1-C3-алкил" (включая являющиеся частями других групп) означает алкильные группы,содержащие от 1 до 3 атомов углерода, термин "С 1-С 4-алкил" означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 4 атомов углерода, термин "C1-C6-алкил" означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 6 атомов углерода, и термин "С 1-С 8-алкил" соответственно означает разветвленные и неразветвленные алкильные группы, содержащие от 1 до 8 атомов углерода. Примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил,н-пентил, изопентил, неопентил, гексил, н-гептил и н-октил. Для указанных выше групп также необязательно могут использоваться аббревиатуры Me, Et, n-Pr, i-Pr, n-Bu, i-Bu, t-Bu и т.п. Если не указано иное, то определения пропила и бутила включают все возможные изомерные формы указанных групп. Так, например, пропил включает н-пропил и изопропил, бутил включает изобутил, втор-бутил и трет-бутил. Термин"алкил" также включает алкильные группы, в которых от 1 до 3 атомов водорода заменены атомами фтора. Термин "C1-Cn-алкилен", где n обозначает целое число, равное от 1 до n, по отдельности или в комбинации с другим радикалом, означает ациклический, обладающий линейной или разветвленной цепью двухвалентный алкильный радикал, содержащий от 1 до n атомов углерода. Например, термин "C1-C4 алкилен" включает -(CH2)-, -(CH2-CH2)-, -(CH(CH3-, -(CH2-CH2-CH2)-, -(C(CH3)2)-, -(CH(CH2CH3-,-(CH(CH3)-CH2)-, -(CH2-CH(CH3-, -(CH2-CH2-CH2-CH2)-, -(CH2-CH2-CH(CH3-, -(CH(CH3)-CH2-CH2)-,-(CH2-CH(CH3)-CH2)-, -(CH2-C(CH3)2)-, -(C(CH3)2-CH2)-, -(CH(CH3)-CH(CH3-, -(CH2-CH(CH2CH3-,-(CH(CH2CH3)-CH2)-, -(CH(CH2CH2CH3-, -(CHCH(CH3)2)- и -C(CH3)(CH2CH3)-. Термин "C3-С 8-циклоалкил" (включая являющиеся частями других групп) означает циклические алкильные группы, содержащие от 3 до 8 атомов углерода, и термин "C3-C6-циклоалкил" означает циклические алкильные группы, содержащие от 3 до 6 атомов углерода. Примеры включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил или циклооктил, а также включают следующие структуры: Если не указано иное, то циклические алкильные группы могут быть замещены 1 или большим количеством групп, выбранных из группы, включающей метил, этил, изопропил, трет-бутил, гидроксигруппу, фтор, хлор, бром и йод. Эти циклоалкилы могут быть дополнительно аннелированы (т.е. скон-5 020282 денсированы) с бензольным кольцом таким образом, что образуются 9-12-членные бициклические гетероциклы. Термин "C2-C6-алкенил" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкенильные группы, содержащие от 2 до 6 атомов углерода, при условии, что они содержат по меньшей мере 1 двойную связь. Алкенильные группы, содержащие от 2 до 4 атомов углерода,являются предпочтительными. Примеры включают этенил или винил, пропенил, бутенил, пентенил или гексенил. Если не указано иное, то определения пропенил, бутенил, пентенил и гексенил включают все возможные изомерные формы указанных групп. Так, например, пропенил включает 1-пропенил и 2 пропенил, бутенил включает 1-бутенил, 2-бутенил и 3-бутенил, 1-метил-1-пропенил, 1-метил-2-пропенил и т.п. Термин "С 2-С 7-алкинил" (включая являющиеся частями других групп) означает разветвленные и неразветвленные алкинильные группы, содержащие от 2 до 7 атомов углерода, при условии, что они содержат по меньшей мере 1 тройную связь. Алкинильные группы, содержащие от 2 до 4 атомов углерода,являются предпочтительными. Примеры включают этинил, пропинил, бутинил, пентинил или гексинил. Если не указано иное, то определения пропинил, бутинил, пентинил и гексинил включают все возможные изомерные формы указанных групп. Так, например, пропинил включает 1-пропинил и 2-пропинил,бутинил включает 1-бутинил, 2-бутинил и 3-бутинил, 1-метил-1-пропинил, 1-метил-2-пропинил и т.п. Термин "галоген" при использовании в настоящем изобретении включает фтор, хлор, бром и йод. Если не указано иное, то предпочтительными галогенами считаются фтор, хлор и бром. Термин "4-7-членный гетероциклоалкил" означает стабильные 4-, 5-, 6- или 7-членные моноциклические гетероциклические кольцевые системы, которые могут быть и насыщенными, и мононенасыщенными. 1 или 2 кольцевых атомов углерода могут быть независимо заменены на гетороатомы, которые выбраны из группы, включающей кислород, азот и серу, последние два из этих гетероатомов могут быть необязательно окислены (таким образом образуя N-оксид, сульфоксид или сульфон). Вышеуказанные гетероциклы могут быть связаны с остальной частью молекулы через атом углерода или атом азота. Примеры 4-, 5-, 6- или 7-членных гетероциклических кольцевых систем включают Эти гетероциклоалкилы могут быть дополнительно аннелированы (т.е. сконденсированы) с бензольным кольцом таким образом, что образуются 8-11-членные бициклические гетероциклы. Термин "арил" (включая являющиеся частями других групп) означает ароматические кольцевые системы, содержащие от 6 до 14 атомов углерода (например, C6-C10-арил). Такие группы могут быть моноциклическими, бициклическими или трициклическими и содержать от 6 до 14 кольцевых атомов углерода. Примеры включают фенил, 1-нафтил или 2-нафтил, предпочтительной арильной группой является фенил. Если не указано иное, то ароматические группы могут быть замещены 1 или большим количеством групп, выбранных из группы, включающей метил, этил, н-пропил, изопропил, трет-бутил, гидроксигруппу, метоксигруппу, трифторметоксигруппу, фтор, хлор, бром и йод, кроме того, группы могут быть одинаковые или разные. Термин "гетероарил" означает 5- или 6-членные гетероциклические ароматические группы, которые могут содержать 1, 2, 3 или 4 гетероатома, выбранных из группы, включающей кислород, серу и азот, и которые дополнительно содержат количество сопряженных двойных связей, достаточное для образования ароматической системы. Эти гетероарилы могут быть дополнительно аннелированы (т.е. сконденсированы) с бензольным кольцом таким образом, что образуются 9-10-членные бициклические гетероарилы. Примеры 5- или 6-членных гетероциклических ароматических групп включают Примеры 9- или 10-членных гетероциклических ароматических групп включают Если не указано иное, вышеуказанные гетероарилы могут быть замещены 1 или большим количеством групп, выбранных из группы, включающей метил, этил, н-пропил, изопропил, трет-бутил, гидроксигруппу, метоксигруппу, трифторметоксигруппу, фтор, хлор, бром и йод, кроме того группы могут быть одинаковые или разные. Кроме того, атом азота, содержащийся в гетероарильной группе, может быть окислен, таким образом образуя N-оксид. Для исключения сомнений отметим, что типы 2 или большего количества заместителей в соединении формулы I могут быть одинаковыми, фактические типы соответствующих заместителей не всегда зависят друг от друга. Например, в случае, если оба Z1 и Z2 обозначают =C(R7)-, то соответствующие рассматриваемые =C(R7)-группы могут быть одинаковыми или разными. Аналогично, если группы содержат 1 или большее количество заместителей, определенных в настоящем изобретении, то типы этих отдельных заместителей не следует считать зависящими друг от друга. Например, если группа A обозначает C1-C8-алкил, замещенный двумя группами R9a, где в обоих случаях R9a обозначает -N(C1-C3-алкил)2,то типы двух групп -N(C1-C3-алкил)2 не следует считать зависящими друг от друга, т.е. два фрагмента-N(C1-C3-алкил)2 могут быть одинаковыми или разными. Аналогично, C1-C3-алкильные группы, входящие в состав одной определенной группы -N(C1-C3-алкил)2 не зависят друг от друга, т.е. они могут быть одинаковыми или отличаться друг от друга. Для исключения сомнений отметим, что, если в настоящем изобретении указаны предпочтительные характеристики, то такие характеристики можно рассматривать независимо от других предпочтительных характеристик или совместно с другими предпочтительными характеристиками. Специалист в данной области техники должен понимать, что соединения формулы Id, которые являются объектом настоящего изобретения, включают такие, которые являются стабильными. Т.е. соединения, предлагаемые в настоящем изобретении, включают такие, которые являются достаточно прочными для их выделения, например, из реакционной смеси в достаточно чистом виде. Методики получения Соединения, предлагаемые в настоящем изобретении, можно получить в соответствии с методиками, которые хорошо известны специалистам в данной области техники, например так, как это описано ниже в настоящем изобретении и в экспериментальном разделе. Другим объектом настоящего изобретения является способ получения соединения формулы Id, который можно осуществить в соответствии с приведенными ниже схемами A-E.(R5=H, все другие переменные группы являются такими, как определено в п.1 формулы изобретения) Защитная группа PG, которую вводят на стадии а), представляет собой стандартную защитную группу атома азота, хорошо известную специалистам в данной области техники, например защитную группу атома азота, описанную в публикации "Protective Groups in Organic Synthesis", 3rd edition,T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999), например трет-бутоксикарбонильную, бензилоксикарбонильную, этоксикарбонильную, метоксикарбонильную, аллилоксикарбонильную или трифторметилкарбонильную группу. Стадию а) можно провести в соответствии с методиками, описанными в литературе, как это описано в публикации "Protective Groups in Organic Synthesis", 3rd edition, T.W. GreeneP.G.M. Wutz, WileyInterscience (1999), например с использованием таких реагентов, как 2-(трет-бутоксикарбонилоксиимино)-2-фенилацетонитрил (BOC-ON), ди-трет-бутилдикарбонат (BOC2O), диметилдикарбонат, диэтилдикарбонат, этилхлорформиат, метилхлорформиат, аллилхлорформиат, бензилхлорформиат или хлорангидрид трифторуксусной кислоты, при условиях, которые хорошо известны из литературы, предпочтительно в присутствии основания, например гидроксида натрия, триэтиламина, диизопропилэтиламина, 4-диметиламинопиридина. Подходящим растворителем для проведения этой стадии является,-8 020282 например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадию b) можно провести с использованием H2/никель Ренея, H2/палладий на угле, порошкообразное Fe/водный раствор NH4Cl, Fe/HCl, Zn/HCl, Na2S2O4, SnCl2/HCl, Zn/HCl или NaBH4/CuCl или в соответствии с методиками, описанными в литературе, например в публикации R. Larock, ComprehensiveOrganic Transformations, VCH Verlagsgemeinschaft, Weinheim (1989). Подходящим растворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон, этанол, метанол, изопропанол или смеси указанных выше растворителей. Стадию с) можно провести в соответствии со стандартными методиками, описанными в литературе,например с использованием таких реагентов, как 1,1'-тиокарбонилди-2-пиридон или 1,1'-тиокарбонилдиимидазол, или с использованием тиофосгена в растворителе, таком как, например, дихлорметан или диметилформамид, и необязательно с добавлением основания, такого как 4-диметиламинопиридин или триэтиламин. Стадию d) можно провести при стандартных условиях, известных специалистам в данной области техники, в присутствии подходящего растворителя, такого как диэтиловый эфир, диметилформамид, дихлорметан, ацетонитрил и/или тетрагидрофуран. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований. Стадию е) предпочтительно проводят в присутствии подходящего "реагента сочетания". В качестве"реагента сочетания" можно использовать, например, соединение на основе карбодиимида, такое как дициклогексилкарбодиимид (ДЦК), 1-этил-3-(3-диметиламинопропил)карбодиимид (или его соль, например гидрохлорид) или N,N-диизопропилкарбодиимид (ДИК). Реакцию можно проводить при любой подходящей температуре (например, при температуре от примерно 0 до примерно 200C) и ее также можно провести в присутствии добавки (такой, как 2,2,2-трифтор-N,O-бис-(триметилсилил)ацетамид). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадии d) и е) можно провести последовательно с выделением промежуточного продукта XV или без выделения XV. Стадия f): защитные группы можно удалить в соответствии с методиками, которые хорошо известны специалистам в данной области техники, и так, как это описано ниже в настоящем изобретении. Например, описанные в настоящем изобретении соединения/промежуточные продукты, содержащие защитные группы, можно химически превратить в не содержащие защитные группы соединения с использованием растворов HCl или H2SO4, трифторуксусной кислоты, KOH; Ba(OH)2, Pd на угле, триметилсилилйодида или при других условиях, как это описано в публикации "Protective Groups in Organic Synthesis",3rd edition, T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадия g): реакцию сочетания амина XVII с кислотой XXa можно провести с использованием дополнительного in-situ активирующего реагента, такого как циклический ангидрид 1-пропилфосфоновой кислоты, O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат или гексафторфосфат, N,N'дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид, карбонилдиимидазол, оксалилхлорид, или других активирующих реагентов, известных в данной области техники. Реакцию сочетания предпочтительно проводить в присутствии основания, такого как NaOH, KOH,NaHCO3, триэтиламин, N-этилдиизопропиламин, N,N-диметиламинопиридин, или других подходящих оснований, известных в данной области техники и описанных, например, в публикации Houben-Weyl,"Methods in Organic Synthesis", Vol. E22a, p 425ff. Альтернативно, реакцию сочетания амина XVII можно провести с использованием активированного производного кислоты XXb, где отщепляющейся группой LG может являться, например, анион фтора,хлора, брома, азидный анион или анион изопропилокси-C(O)-O. Реакцию сочетания предпочтительно проводить в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований при условиях, описанных,например, в публикации Houben-Weyl, "Methods in Organic Synthesis", Vol. E22a, p 425ff. Если стадию g) проводят в присутствии триметилалюминия или триэтилалюминия, то отщепляющейся группой в соединении XXb также может являться метоксигруппа или этоксигруппа. Описанные выше реакции сочетания проводят в подходящем растворителе, таком как, например,дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, Nметилпирролидон, или в смеси указанных выше растворителей.(R5=алкильные цепи, соответствующие приведенным выше определениям,другие переменные группы являются такими, как определено в п.1 формулы изобретения) Стадия h): восстановительное аминирование проводят в соответствии с известными методиками,например с использованием триацетоксиборогидрида натрия, борогидрида натрия или цианоборогидрида натрия в подходящем растворителе, таком как тетрагидрофуран или дихлорметан, с добавлением уксусной кислоты или трифторуксусной кислоты, если это является подходящим, или с использованием палладияна-древесном угле в атмосфере водорода в тетрагидрофуране, или этаноле, или метаноле, или изопропаноле,или диметилформамиде, предпочтительно в присутствии уксусной кислоты или трифторуксусной кислоты. Стадию i) можно провести в соответствии со стандартными методиками, описанными в литературе,например с использованием таких реагентов, как тиофосген в подходящем растворителе, таком как, например, дихлорметан или диметилформамид, необязательно с добавлением основания, такого как 4-диметиламинопиридин или триэтиламин. Стадию j) можно провести при стандартных условиях, известных специалистам в данной области техники, в присутствии подходящего растворителя, такого как диэтиловый эфир, диметилформамид, дихлорметан, ацетонитрил и/или тетрагидрофуран. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований. Стадию k) предпочтительно проводят в присутствии подходящего реагента сочетания, такого как,например, соединение на основе карбодиимида, такое как дициклогексилкарбодиимид (ДЦК), 1-этил-3(3-диметиламинопропил)карбодиимид (или его соль, например гидрохлорид) или N,N-диизопропилкарбодиимид (ДИК). Реакцию можно проводить при любой подходящей температуре (например, при температуре от примерно 0 до примерно 200C) и ее также можно провести в присутствии добавки (та- 10020282 кой, как 2,2,2-трифтор-N,O-бис-(триметилсилил)ацетамид). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран, ацетонитрил, диметилформамид,диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадии j) и k) можно провести последовательно с выделением промежуточного продукта XXI или без выделения XXI. Стадия l): защитные группы можно удалить в соответствии с методиками, которые хорошо известны специалистам в данной области техники, и так, как это описано ниже в настоящем изобретении. Например, описанные в настоящем изобретении соединения/промежуточные продукты, содержащие защитные группы, можно химически превратить в не содержащие защитные группы соединения с использованием растворов HCl или H2SO4, трифторуксусной кислоты, KOH; Ba(OH)2, Pd на угле, триметилсилилйодида или при других условиях, как это описано в публикации "Protective Groups in Organic Synthesis",3rd edition, T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран, ацетонитрил, диметилформамид, диметилацетамид, N-метилпирролидон, метанол, этанол или смеси указанных выше растворителей. Стадия m): реакцию сочетания амина XXIII с кислотой XXa можно провести с использованием дополнительного in-situ активирующего реагента, такого как циклический ангидрид 1-пропилфосфоновой кислоты, O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат или гексафторфосфат, N,N'дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид, карбонилдиимидазол, оксалилхлорид, или других активирующих реагентов, известных в данной области техники. Реакцию сочетания предпочтительно проводить в присутствии основания, такого как NaOH, KOH,NaHCO3, триэтиламин, N-этилдиизопропиламин, N,N-диметиламинопиридин, или других подходящих оснований, известных в данной области техники и описанных, например, в публикации Houben-Weyl,"Methods in Organic Synthesis", Vol. E22a, p 425ff. Альтернативно, реакцию сочетания амина XXIII можно провести с использованием активированного производного кислоты XXb, где отщепляющейся группой LG может являться, например, анион фтора,хлора, брома, азидный анион или анион изопропилокси-C(O)-O. Реакцию сочетания предпочтительно проводить в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований при условиях, описанных,например, в публикации Houben-Weyl, "Methods in Organic Synthesis", Vol. E22a, p 425ff. Если стадию m) проводят в присутствии триметилалюминия или триэтилалюминия, то отщепляющейся группой всоединении XXb также может являться метоксигруппа или этоксигруппа. Описанные выше реакции сочетания проводят в подходящем растворителе, таком как, например,дихлорметан, тетрагидрофуран, ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон, или в смеси указанных выше растворителей. Схема C(R5 и все переменные группы являются такими, как определено в п.1 формулы изобретения) Стадию n) можно провести в соответствии со стандартными методиками, описанными в литературе,например с использованием таких реагентов, как 1,1'-тиокарбонилди-2-пиридон или 1,1'-тиокарбонилдиими- 11020282 дазол, или с использованием тиофосгена в растворителе, таком как, например, дихлорметан или диметилформамид, и необязательно с добавлением основания, такого как 4-диметиламинопиридин или триэтиламин. Стадию o) можно провести при стандартных условиях, известных специалистам в данной области техники, в присутствии подходящего растворителя, такого как диэтиловый эфир, диметилформамид, дихлорметан, ацетонитрил и/или тетрагидрофуран. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований. Стадию p) предпочтительно проводят в присутствии подходящего "реагента сочетания". В качестве"реагента сочетания" можно использовать, например, соединение на основе карбодиимида, такое как дициклогексилкарбодиимид (ДЦК), 1-этил-3-(3-диметиламинопропил)карбодиимид (или его соль, например гидрохлорид) или N,N-диизопропилкарбодиимид (ДИК). Реакцию можно проводить при любой подходящей температуре (например, при температуре от примерно 0 до примерно 200C) и ее также можно провести в присутствии добавки (такой, как 2,2,2-трифтор-N,O-бис-(триметилсилил)ацетамид). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил,диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадии o) и p) можно провести последовательно с выделением промежуточного продукта XXV или без выделения XXV. Структурные фрагменты XXIX-а или XXIX-b также можно использовать в качестве предшественников в соответствии со схемой D (PG1=защитная группа).(все переменные группы, за исключением группы L, являются такими, как определено в п.1 формулы изобретения)- 12020282 Защитная группа PG1 представляет собой стандартную защитную группу атома азота, хорошо известную специалистам в данной области техники, например защитную группу атома азота, описанную в публикации "Protective Groups in Organic Synthesis", 3rd edition, T.W. GreeneP.G.M. Wutz, WileyInterscience (1999), например трет-бутоксикарбонильную, бензилоксикарбонильную, этоксикарбонильную, метоксикарбонильную, аллилоксикарбонильную или трифторметилкарбонильную группу. Стадию q) можно провести при стандартных условиях, известных специалистам в данной области техники, в присутствии подходящего растворителя, такого как диэтиловый эфир, диметилформамид, дихлорметан, ацетонитрил и/или тетрагидрофуран. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований. Стадию r) предпочтительно проводят в присутствии подходящего "реагента сочетания". В качестве"реагента сочетания" можно использовать, например, соединение на основе карбодиимида, такое как дициклогексилкарбодиимид (ДЦК), 1-этил-3-(3-диметиламинопропил)карбодиимид (или его соль, например гидрохлорид) или N,N-диизопропилкарбодиимид (ДИК). Реакцию можно проводить при любой подходящей температуре (например, при температуре от примерно 0 до примерно 200C) и ее также можно провести в присутствии добавки (такой, как 2,2,2-трифтор-N,O-бис-(триметилсилил)ацетамид). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадии q) и r) можно провести последовательно с выделением промежуточного продукта XXVII или без выделения XXVII. Стадия s): защитную группу PG1 можно удалить в соответствии с методиками, которые хорошо известны специалистам в данной области техники, и так, как это описано ниже в настоящем изобретении. Например, описанные в настоящем изобретении соединения/промежуточные продукты, содержащие защитные группы, можно химически превратить в не содержащие защитные группы соединения с использованием растворов HCl или H2SO4, трифторуксусной кислоты, KOH; Ba(OH)2, Pd на угле, триметилсилилйодида или при других условиях, как это описано в публикации "Protective Groups in Organic Synthesis",3rd edition, T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон, метанол, этанол или смеси указанных выше растворителей. Стадия t): реакцию сочетания амина XXVIII с кислотой A-COOH можно провести с использованием дополнительного in-situ активирующего реагента, такого как циклический ангидрид 1-пропилфосфоновой кислоты, O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат или гексафторфосфат, N,N'-дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид, карбонилдиимидазол, оксалилхлорид, или других активирующих реагентов, известных в данной области техники. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH,NaHCO3, триэтиламин, N-этилдиизопропиламин, N,N-диметиламинопиридин, или других подходящих оснований, известных в данной области техники и описанных, например, в публикации Houben-Weyl,"Methods in Organic Synthesis", Vol. E22a, p 425ff. Альтернативно, реакцию сочетания амина XXVIII можно провести с использованием активированного производного кислоты A-C(O)-LG, где отщепляющейся группой LG может являться, например,анион фтора, хлора, брома, азидный анион или анион изопропилокси-C(O)-O, или с использованием ASO2-Cl. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH,NaHCO3, триэтиламин, N-этилдиизопропиламин, N, N-диметиламинопиридин, или других подходящих оснований при условиях, описанных, например, в публикации Houben-Weyl, "Methods in Organic Synthesis",Vol. E22a, p 425ff. Описанные выше реакции сочетания проводят в подходящем растворителе, таком как, например,дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, Nметилпирролидон, или в смеси указанных выше растворителей. Структурные фрагменты XXX-a или XXX-b также можно использовать в качестве предшественников в соответствии со схемой E.(все переменные группы, за исключением группы L, являются такими, как определено в п.1 формулы изобретения) Стадию u) можно провести при стандартных условиях, известных специалистам в данной области техники, в присутствии подходящего растворителя, такого как диэтиловый эфир, диметилформамид, дихлорметан, ацетонитрил и/или тетрагидрофуран. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH, NaHCO3, триэтиламин, N-этилдиизопропиламин, 4-диметиламинопиридин, или других подходящих оснований. Стадию v) предпочтительно проводят в присутствии подходящего "реагента сочетания". В качестве"реагента сочетания" можно использовать, например, соединение на основе карбодиимида, такое как дициклогексилкарбодиимид (ДЦК), 1-этил-3-(3-диметиламинопропил)карбодиимид (или его соль, например гидрохлорид) или N,N-диизопропилкарбодиимид (ДИК). Реакцию можно проводить при любой подходящей температуре (например, при температуре от примерно 0 до примерно 200C) и ее также можно провести в присутствии добавки (такой, как 2,2,2-трифтор-N,O-бис-(триметилсилил)ацетамид). Подходящим сорастворителем для проведения этой стадии является, например, дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, N-метилпирролидон или смеси указанных выше растворителей. Стадии u) и v) можно провести последовательно с выделением промежуточного продукта XXXI или без выделения XXXI. Стадию w) можно провести по известным методикам проведения реакций омыления, например с использованием водного раствора NaOH или KOH в этаноле, метаноле или диоксане. Стадия x): реакцию сочетания амина XXXIV с кислотой XXXIII можно провести с использованием дополнительного in-situ активирующего реагента, такого как циклический ангидрид 1-пропилфосфоновой кислоты, O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат или гексафторфосфат, N,N'-дициклогексилкарбодиимид, 1-(3-диметиламинопропил)-3-этилкарбодиимид, карбонилдиимидазол, оксалилхлорид, или других активирующих реагентов, известных в данной области техники. Реакцию сочетания предпочтительно проводят в присутствии основания, такого как NaOH, KOH,- 14020282NaHCO3, триэтиламин, N-этилдиизопропиламин, N,N-диметиламинопиридин, или других подходящих оснований, известных в данной области техники и описанных, например, в публикации Houben-Weyl,"Methods in Organic Synthesis", Vol. E22a, p 425ff. Описанные выше реакции сочетания проводят в подходящем растворителе, таком как, например,дихлорметан, тетрагидрофуран (ТГФ), ацетонитрил, диметилформамид (ДМФ), диметилацетамид, Nметилпирролидон, или в смеси указанных выше растворителей. Специалисты в данной области техники должны понимать, что в реакциях, описанных выше и ниже в настоящем изобретении, функциональные группы промежуточных продуктов может быть необходимо защитить защитными группами. Введение и удаление защитных групп функциональных групп можно проводить до или после проведения реакций, приведенных на описанных выше схемах. Защитные группы можно удалить в соответствии с методиками, которые хорошо известны специалистам в данной области техники, и так, как это описано ниже в настоящем изобретении. Например, описанные в настоящем изобретении соединения/промежуточные продукты, содержащие защитные группы,можно химически превратить в не содержащие защитные группы соединения по обычным методикам удаления защитных групп. От типа проводимого химического превращения будут зависеть необходимость введения и тип защитных групп, а также последовательность проведения синтеза. Применение защитных групп подробно описано в публикациях "Protective Groups in Organicedition, T.W. GreeneP.G.M. Wutz, Wiley-Interscience (1999). Условия проведения отдельных стадий, приведенных на описанных выше схемах, например стадий введения/удаления защитных групп, восстановительного аминирования, образования амида и других,хорошо известны специалистам и описаны в стандартной литературе, такой как публикация HoubenWeyl: Methoden der organischen Chemie, Georg-Thieme-Verlag, Stuttgart, и более подробно описаны в качестве примеров в экспериментальном разделе. Соединения формулы Id (включая соединения I-1 - I-4) можно выделить из реакционных смесей по обычным методикам. Биологическое исследование Основой использующего исследования является измерение ингибирования различными соединениями зависимого от микросомной простагландин-E2-синтазы-1 (mPGES-1) образования простагландинаE2 (PGE2) из PGH2. Таким образом, образование PGE2 используют в качестве сигнала и снижение интенсивности этого сигнала можно рассматривать как ингибирование mPGES-1. Аналогичные исследования для измерения ингибирования mPGES-1 описаны ранее в литературе (1, 2). Список использующихся реагентов: Глутатион (Sigma, G-4251) Замороженная культура бактерии E.coli экспрессирующего штамма Rosetta Лизогенный бульон (ЛБ), среда для выращивания с ампициллином (Amp), конечная концентрация в культуре 50 мкг/мл Исходный раствор хлорамфеникола 34 мг/мл, конечная концентрация в культуре 34 мкг/мл Стерильные колбы для выращивания культур объемом 500 мл-1 л 0,1 М KPi буфер (калий-фосфатный буфер), pH 7,4 9,25% HClPGH2 (0,25 мкМ) Тетрагидрат Fe(II)Cl2, 99% (Sigma, 220229) 384-луночный планшет с соединениями 96-луночный полипропиленовый планшет (Thermo Fast 96 Skirted, VWR) 384-луночный полипропиленовый планшет для проведения ПЦР (полимеразная цепная реакция)(Greiner 785201) 384-луночный полипропиленовый планшет, Greiner (In vitro, cat. no. 781280) Липкая герметизирующая пленка для 96-луночных планшетов (Sigma-Aldrich) Алюминиевая фольга (фольга для проведения ПЦР, 310-0030-127-471, выпускаемая фирмой Labora) ЗФФ (забуференный фосфатом физиологический раствор) (GIBCO 14040) Набор для исследования простагландина E2 (Cisbio, cat. no. 62P2APEC) Робот Biomek FX (Beckman Coulter) Робот Biomek NX (Beckman Coulter) Дозирующее устройство Multidrop; микродозирующее или комбинированное (ThermoLabsystems) Устройство для считывания планшетов: Safire2 (Tecan) Микросомы бактерии E.coli штамма Rosetta, экспрессирующей рекомбинантный mPGES-1 человека, можно получить так, как описано ниже: 5 мл ЛБ, содержащего Amp и хлорамфеникол, инокулируют бактериями замороженной культуры. Инкубируют при 200 об/мин при 37C в течение ночи. Затем 500800 мл LB, содержащего Amp и хлорамфеникол, инокулируют с помощью 5 мл культуры и выращивают до OD640, составляющего 0,6-0,8. Перед индуцированием культуру охлаждают до +4C. Культуру индуцируют с помощью IPTG (изопропилтиогалактозид) при конечной концентрации, равной 400 мкМ. Белок экспрессируют при встряхивании при 200 об/мин при комнатной температуре, 18-23C, в течение ночи. На следующий день можно провести следующие стадии. 1. Клетки осаждают в колбах для центрифугирования объемом 250 мл при 7000 об/мин в течение 15 мин. 2. Таблетки, полученные из 250 мл культуры, растворяют в 12,5 мл буфера для гомогенизации. 3. Клетки диспергируют с помощью обработки ультразвуком при амплитуде, составляющей 35%, в течение 410 с. 4. Добавляют 2,5 мл MgCl2 (100 мМ) и 12,5 мкл (0,8 мг/мл) DNase (дезоксирибонуклеаза) и инкубируют на льду в течение 30 мин. 5. Остатки бактерий осаждают при 7000 об/мин в течение 15 мин и собирают надосадочную жидкость. 6. Мембраны, содержащие белок, отделяют от надосадочной жидкости с помощью ультрацентрифугирования при 45000g в течение 1 ч. 7. Надосадочную жидкость отбрасывают, и таблетки растворяют в 20 мМ KPi буфере, и фермент делят на аликвоты и хранят при -80C. Перед проведением каждого эксперимента размораживают аликвоту фермента и затем разводят в 0,1 М KPi буфере со значением pH, равным 7,4, содержащем 2,5 мкМ GSH (глутатион). Затем в 384 луночный планшет при комнатной температуре помещают 50 мкл этого фермента. 0,5 мкл ингибитора растворяют в ДМСО и затем добавляют в каждую лунку и инкубируют при комнатной температуре в течение 25 мин. Затем в каждую лунку добавляют 2 мкл PGH2, растворенного в подходящем растворителе, и через 1 мин при комнатной температуре добавляют подкисленный останавливающий раствор, содержащий FeCl2. 4 мкл полученного раствора переносят в отдельный планшет и разводят в 750 раз в две отдельные стадии, затем определяют количество PGE2. Для определения количества образовавшегося PGE2 проводят детектирование PGE2 с помощью однородной флуоресценции с разрешением по времени (HTRF) с использованием имеющегося в продаже набора, выпускающегося фирмой CisBio, в основном, в соответствии с инструкциями изготовителя. Вкратце, методика заключается в следующем: 10 мкл разведенного образца переносят в белый 384 луночный планшет и последовательно проводят приведенные ниже стадии при комнатной температуре или так, как это указано. В лунки, содержащие отрицательный контроль (ОК), добавляют 5 мкл восстанавливающего буфера,полученного от изготовителя. Планшет закрывают липкой герметизирующей пленкой. Планшет центрифугируют при 1200 об/мин в течение 1 мин. Образцы ОК закрывают герметизирующей пленкой. 250 мкл меченного с помощью d2 PGE2 (d2-PGE2) разводят в 4750 мкл восстанавливающего буфера,полученного от изготовителя. 250 мкл криптата Eu3+ разводят в 4750 мкл восстанавливающего буфера, полученного от изготовителя. В лунки в рядах 1-24 с помощью Multidrop добавляют 5 мкл d2-PGE2. Затем с лунок, содержащих ОК, удаляют герметизирующую пленку. В лунки в рядах 1-24 с помощью Multidrop добавляют 5 мкл меченого с помощью криптата Eu3+ анти-PGE2. Планшет закрывают герметизирующей пленкой. Планшет центрифугируют при 1200 об/мин в течение 1 мин и выдерживают при 4C в течение ночи. После инкубирования в течение ночи флуоресценцию исследуют с использованием соответствующего устройства считывания микропланшетов. Интенсивность флуоресценции криптата Eu3+ и d2-PGE2 измеряют при следующих длинах волн возбуждения и испускания: криптат европия: maxex=307 нм,maxem=620 нм и d2: maxex=620 нм, maxem=665 нм, соответственно. Конкретные значения HTRF (резонансный перенос энергии флуоресценции) определяют как отношение интенсивности испускания при длине волны, равной 665 нм, к интенсивности испускания при длине волны, равной 620 нм. Для определения количества PGE2 в неизвестных образцах используют стандартную зависимость, полученную для синтетического PGE2. Степень ингибирования можно рассчитать как выраженное в процентах ингибирование, равное отношению количества PGE2, образующегося в неизвестных образцах, к количеству PGE2,образующегося в контрольных образцах. Литература 1. Riendeau, D., R. Aspiotis, D. Ethier, Y. Gareau, E. Grimm, J. Guay, S. Guiral, H. Juteau, J. Mancini,N. Methot, J. Rubin, and R. Friesen, Inhibitors of the inducible microsomal prostaglandin E2 synthase (mPGES-1) Результаты исследования В табл. 1 приведены значения ингибирующего воздействия на mPGES-1 (выраженное в % ингибирование), измеренные для некоторых образцов при концентрации, равной 10 мкМ (если не указано иное),по данным исследования с помощью HTRF, описанного выше. Примеры показывают, что соединения при концентрации, равной 10 мкМ, ингибируют продуцирование PGE2 до указанной степени. Эти результаты свидетельствуют об успешном ингибировании mPGES-1 данными соединениями. Таблица 1 Ингибирующее воздействие на mPGES-1 (выраженное в % ингибирование) соединений, предлагаемых в настоящем изобретении, при концентрации, равной 10 мкМ, по данным исследования с помощью HTRF В табл. 2 приведены значения ингибирующего воздействия на mPGES-1 (IC50), измеренные для некоторых образцов по данным исследования с помощью HTRF, описанного выше. Эти результаты свидетельствуют об успешном ингибировании mPGES-1 данными соединениями. Таблица 2 Ингибирующее воздействие на mPGES-1 (значения IC50, выраженные в нМ) соединений,предлагаемых в настоящем изобретении, по данным исследования с помощью HTRF Способ лечения Настоящее изобретение относится к соединениям формулы Id, которые применимы для предупреждения и/или лечения заболевания и/или патологического состояния, в котором ингибирование простагландин-E-синтаз, в частности микросомной простагландин-E2-синтазы-1 (mPGES-1), оказывает благоприятное терапевтическое воздействие, включая, но не ограничиваясь только ими, лечение и/или предупреждение воспалительных заболеваний и/или родственных патологических состояний. Термин "воспаление" следует понимать как включающий любое воспалительное заболевание, нарушение или патологическое состояние само по себе, любое патологическое состояние, которое включает связанный с ним воспалительный компонент, и/или любое патологическое состояние, характеризующееся воспалением в качестве симптома, включая, в частности, острое, хроническое, язвенное, специфическое, аллергическое и некротическое воспаление, и другие формы воспаления, известные специалистам в данной области техники. Таким образом, для задач настоящего изобретения этот термин также включает воспалительную боль, боль в целом и/или лихорадку. В случае, если патологическое состояние включает связанный с ним воспалительный компонент или патологическое состояние характеризуется воспалением в качестве симптома, специалист в данной области техники должен понимать, что соединения, предлагаемые в настоящем изобретении, можно применять для устранения симптомов воспаления и/или лечения воспаления, связанного с патологическим состоянием. Соединения, предлагаемые в настоящем изобретении, также могут влиять на проявления, не связанные с воспалением, например уменьшать потерю костной массы у субъекта. Такие патологические состояния включают остеопороз, остеоартрит, болезнь Педжета и/или периодонтальные заболевания. Другим объектом настоящего изобретения является применение соединения формулы Id в качестве лекарственного средства. Другим объектом настоящего изобретения является применение соединений формулы Id для лечения и/или предупреждения заболевания и/или патологического состояния, в котором ингибированиеmPGES-1 оказывает благоприятное терапевтическое воздействие. Другим объектом настоящего изобретения является применение соединения формулы Id для лечения и/или предупреждения воспалительных заболеваний и/или родственных патологических состояний. Настоящее изобретение также относится к применению соединений формулы Id для лечения и/или предупреждения следующих заболеваний и патологических состояний: 1. ревматические заболевания, или аутоиммунные заболевания, или скелетно-мышечные заболевания: все формы ревматических заболеваний, включая, например, ревматизм мягких тканей, ревматоидный артрит, ревматическую полимиалгию; реактивный артрит, теносиновит, подагра или обменный артрит, бурсит, тендинит, хронический полиартрит у детей, спондилоартропатия, такая как, например,спондилит, анкилозирующий спондилоартрит, псориатическая артропатия; саркоидоз, фибромиалгия,миозит, полимиозит, остеоартрит, травматический артрит, коллагенозы любой этиологии, например системная красная волчанка, склеродерма, дерматомиозит, болезнь Стилла, синдром Шегрена, синдром Фелти; ревматический полиартрит и ревматическая болезнь сердца, заболевания кровеносных сосудов,такие как васкулит, нодозный полиартрит, синдром Бехчета, гигантоклеточный артрит, гранулематоз Вегенера, пурпура Шенлейна-Геноха; псориатический артрит, грибковый артрит, в частности, включая боль, связанную с любым из вышеуказанных патологических состояний; 2. головная боль, такая как мигрень с аурой и без нее, головная боль напряжения, сильная присту- 18020282 пообразная головная боль с периодическими рецидивами и головная боль различной этиологии; 3. симпатически поддерживаемая боль, такая как комплексный региональный болевой синдром типа I и II; 4. невропатическая боль, такая как боль в нижней части спины, боль в бедре, боль в ноге, негерпетическая невралгия, постгерпетическая невралгия, диабетическая невропатия, боль, вызванная поражением нерва, невропатическая боль, связанная с синдромом приобретенного иммунодефицита (СПИД),травма головы, поражения нервов, вызванные токсином и химиотерапией, фантомные боли в ампутированных конечностях, рассеянный склероз, травматический вывих зуба, болезненная травматическая мононевропатия, болезненная полиневропатия, синдром таламической боли, боль после удара, поражение центральной нервной системы, послеоперационная боль, запястный синдром, тригеминальная невралгия,постмастэктомический синдром, постторакотомический синдром, боль в культе, повторяющаяся боль при движении, невропатическая боль, связанная с гипералгезией и аллодинией, боль, обусловленная алкоголизмом, и другая обусловленная действием лекарственных средств боль; 5. боль, вызванная раком или связанная с опухолями, такими как опухоли костей, лимфолейкоз; болезнь Ходжкина, злокачественная лимфома; лимфогранулематоз; лимфосаркома; солидные злокачественные опухоли; обширные метастазы; 6. нарушения внутренних органов, такие как хроническая тазовая боль, панкреатит, пептическая язва, интерстициальный цистит, цистит, почечная колика, ангина, дисменорея, менструация, гинекологическая боль, синдромом раздраженной толстой кишки (СРК), воспалительная болезнь кишечника, болезнь Крона и язвенный колит, нефрит, простатит, вульводиния, неязвенная диспепсия, экстракардиальная боль в груди, боль, ишемия миокарда; 7. связанные с воспалением заболевания уха, носа, рта и горла, такие как грипп, и вирусные/бактериальные инфекции, такие как простуда, аллергический ринит (сезонный и круглогодичный), фарингит,тонзиллит, гингивит, ларингит, синусит и вазомоторный ринит, лихорадка, сенная лихорадка, тиреоидит,отит, патологические состояния зубов, такие как зубная боль, периоперационные и постоперационные патологические состояния, тригеминальная невралгия, увеит; ирит, аллергический кератит, конъюнктивит, блефарит, неврит зрительного нерва, хориоидит, глаукома и симпатическая офтальмия, а также боль, связанная с этими заболеваниями; 8. неврологические заболевания, такие как отек головного мозга и ангионевротический отек, деменция головного мозга, такая как, например, болезнь Паркинсона и болезнь Альцгеймера, старческое слабоумие; рассеянный склероз, удар, злокачественная миастения, инфекции мозга и мозговой оболочки,такие как энцефаломиелит, менингит, включая ВИЧ (вирус иммунодефицита человека), а также шизофрения, бредовые нарушения, аутизм, аффективные расстройства и связанные с тиком нарушения; 9. профессиональные заболевания, такие как пневмокониоз, включая алюминоз, антракоз, асбестоз,халикоз, птилоз, сидероз, силикоз, табакоз и биссиноз; 10. заболевания легких, такие как астма, включая аллергическую астму (атопическую и неатопическую), а также бронхостеноз напряжения, профессиональную астму, вирусное или бактериальное обострение астмы, другие неаллергические типы астмы и "бронхит младенцев", хроническое обструктивное заболевание легких (ХОЗЛ), включая эмфизему, респираторный дистресс-синдром у взрослых, бронхит,пневмонию, респираторный дистресс-синдром у взрослых (РДСВ), болезнь голубятников, аллергический альвеолит у сельскохозяйственных рабочих; 11. заболевания кожи, такие как псориаз и экзема, дерматит, солнечный ожог, ожоги, а также растяжения связок и сухожилий и травмы тканей; 12. сосудистые или сердечные заболевания, которые связаны с воспалением, такие как артериосклероз, включая атеросклероз, связанный с трансплантами сердца, нодозный панартериит, нодозный периартериит, преходящий артериит, гранулематоз Вегенера, гигантоклеточный артрит, реперфузионное поражение и нодозная эритема, тромбоз (например, тромбоз глубоких вен, тромбоз почечной, печеночной, воротной вены); заболевание коронарной артерии, аневризма, отторжение трансплантата сосудов,инфаркт миокарда, эмболия, удар, тромбоз, включая венозный тромбоз, стенокардия, включая нестабильную стенокардию, воспаление, связанное с коронарными бляшками, вызванное бактериями воспаление, включая воспаление, вызванное хламидиями, вызванное вирусами воспаление и воспаление, связанное с хирургическими операциями, такими как операция по установке трансплантата сосудов, включая операцию аортокоронарного шунтирования, операции по замене кровеносных сосудов, включая ангиопластику, установку стента, эндартерэктомию, или другие инвазивные процедуры, в которые вовлечены артерии, вены и капилляры, рестеноз артерии; 13. симптомы, связанные с диабетом, такие как диабетическая васкулопатия, диабетическая невропатия, диабетическая ретинопатия, последующая резистентность капилляров, или симптомы диабета,связанные с инсулином (например, гипергликемия, диурез, протеинурия и повышенное выведение нитритов и калликреина с мочой); 14. доброкачественные и злокачественные опухоли и неоплазия, включая рак, такой как колоректальный рак, рак мозга, рак кости, эпителиальную образовавшуюся в клетках неоплазию (эпителиальная карцинома), такую как базальноклеточная карцинома, аденокарцинома, желудочно-кишечный рак, такой как рак губы, рак полости рта, рак пищевода, рак тонкой кишки, рак желудка, колоректальный рак, рак печени, рак мочевого пузыря, рак поджелудочной железы, рак яичников, рак шейки матки, рак легких,рак молочной железы, рак кожи, такой как плоскоклеточный и базальноклеточный рак, рак предстательной железы, почечно-клеточная карцинома, и другие известные типы рака, влияющие на эпителиальные клетки всего организма; неоплазии, такие как желудочно-кишечный рак, язва пищевода Баррета, рак печени, рак мочевого пузыря, рак поджелудочной железы, рак яичников, рак предстательной железы, рак шейки матки, рак легких, рак молочной железы и рак кожи; аденоматозный полипоз, включая наследственный аденоматозный полипоз (НАП), а также предупреждение образования полипов у пациентов с риском заболевания НАП; 15. другие заболевания и патологические состояния, такие как эпилепсия, септический шок, например, при котором применяют антигиповолемические и/или антигипотензивные средства, сепсис, остеопороз, доброкачественная гиперплазия предстательной железы и гиперактивность мочевого пузыря,нефрит, прурит, витилиго, нарушения висцеральной подвижности в респираторной, мочеполовой, желудочно-кишечной или сосудистой системах, раны, аллергические реакции кожи, смешанные васкулярные и аваскулярные синдромы, септический шок, связанный с бактериальными инфекциями или с травмой,поражение центральной нервной системы, повреждения тканей и послеоперационная лихорадка, синдромы, сопровождающиеся зудом. В контексте настоящего изобретения предпочтительным является применение соединения формулыId для лечения и/или предупреждения боли; в частности боли, связанной с любым из приведенных выше заболеваний или патологических состояний. Соединения по изобретению могут использоваться в способе лечения и/или предупреждения описанных выше заболеваний и патологических состояний, который включает введение человеку соединения формулы Id в эффективном количестве. Соединения, предлагаемые в настоящем изобретении, также могут обладать тем преимуществом,что они могут являться более эффективными, менее токсичными, более длительно действующими, более активными, приводящими к меньшему количеству побочных эффектов, легче всасывающимися и/или обладать улучшенным фармакокинетическим профилем (например, лучшая пероральная биологическая доступность и/или меньшее значение клиренса), чем соединения предшествующего уровня техники, или обладающими другими полезными фармакологическими, физическими или химическими характеристиками, отсутствующими у соединений предшествующего уровня техники, при их использовании при любом из указанных выше показаний или в других случаях. Дозировка Термин "эффективное количество" означает количество соединения, которое обеспечивает терапевтический эффект подвергающегося лечению пациента. Этот эффект может быть объективным (т.е. измеряемым с помощью каких-либо исследований или маркеров) или субъективным (т.е. субъект сообщает об эффекте или ощущает его). Соединения, предлагаемые в настоящем изобретении, можно вводить в разных дозах. Значения доз для перорального введения, введения в легкие и местного введения находятся в диапазоне от примерно 0,01 мг/(кг массы тела пациента) в сутки (мг/кг/сутки) до примерно 100 мг/кг/сутки, предпочтительно от примерно 0,01 до примерно 100 мг/кг/сутки и более предпочтительно от примерно 0,1 до примерно 25 мг/кг/сутки. Например, композиция для перорального введения обычно содержит от примерно 0,01 до примерно 5000 мг и предпочтительно от примерно 1 до примерно 2000 мг активного ингредиента. Предпочтительное значение дозы для внутривенного введения находится в диапазоне от примерно 0,001 до примерно 10 мг/кг/ч при постоянной скорости вливания. Соединения предпочтительно можно вводить в виде 1 суточной дозы или полную суточную дозу можно вводить в виде разделенных доз 2, 3 или 4 раза в сутки. В любом случае врач или специалист в данной области техники сможет определить фактическую дозировку, которая является наиболее подходящей для конкретного пациента и которая обычно меняется в зависимости от пути введения, типа и серьезности подвергающегося лечению патологического состояния, а также вида, возраста, массы тела, пола, почечной функции, функции печени и реакции конкретного пациента, подвергающегося лечению. Указанные выше дозы являются типичными для среднего случая; разумеется, могут быть отдельные случаи, когда следует использовать более широкие или более узкие диапазоны доз, и они включены в объем настоящего изобретения. Фармацевтические препараты Подходящие препараты для введения соединений формулы Id известны специалистам с общей подготовкой в данной области техники, и они включают, например, таблетки, пилюли, капсулы, суппозитории, пастилки, лепешки, растворы, сиропы, эликсиры, облатки, средства для инъекции, средства для ингаляции, порошки и т.п. Такие препараты можно приготовить в соответствии со стандартной и/или общепринятой фармацевтической практикой. В зависимости, например, от эффективности и физических характеристик соединения, предлагаемого в настоящем изобретении (т.е. активного ингредиента), содержание фармацевтически активного соединения (соединений) должно находится в диапазоне от 1 до 99 мас.%, предпочтительно от 10 до 90 мас.%, более предпочтительно от 20 до 70 мас.% от массы композиции в целом. Подходящие таблетки можно изготовить, например, путем смешивания одного или большего количества соединений формулы Id с известными инертными наполнителями, например инертными разбавителями, носителями, разрыхлителями, вспомогательными веществами, поверхностно-активными веществами, связующими и/или смазывающими веществами. Таблетки также могут содержать несколько слоев. Соединения по изобретению могут использоваться в фармацевтическом препарате, включающем соединение формулы Id в смеси фармацевтически приемлемым вспомогательным веществом, разбавителем или носителем. Комбинированная терапия Соединения, предлагаемые в настоящем изобретении, можно использовать в комбинации с другими известными средствами лечения, использующимися в даннойобласти техники в связи с лечением любого из патологических состояний, лечение которого является задачей настоящего изобретения. В число таких средств лечения, которые считаются подходящими для комбинации со способом лечения, предлагаемым в настоящем изобретении, входят нестероидные противовоспалительные лекарственные средства (НСПВС), включая ингибиторыCOX-2; антагонисты опиатного рецептора; антагонисты каннабиноидного рецептора; блокаторы натриевых каналов; блокаторы кальциевых каналов N-типа; серотонинергические и норадренергические модуляторы; кортикостероиды; антагонисты гистаминового рецептора H1; антагонисты гистаминового рецептора H2; ингибиторы протонного насоса; антагонисты лейкотриена и ингибиторы 5-липоксигеназы; местные анестетики; агонисты и антагонисты VR1; агонисты никотинового ацетилхолинового рецептора; антагонисты рецептора Р 2 Х 3; агонисты и антагонисты NGF; антагонисты NK1 и NK2; антагонисты NMDA; модуляторы калиевых каналов; модуляторы GABA; серотонинергические и норадренергические модуляторы; средства для борьбы с мигренью. Указанный список не считается ограничивающим. Ниже приведены типичные примеры таких средств лечения. Нестероидные противовоспалительные лекарственные средства (НСПВС), включая ингибиторыCOX-2: производные пропионовой кислоты (алминопрофен, беноксапрофен, буклоксиновая кислота,карпрофен, фенбуфен, фенопрофен, флурбипрофен, ибупрофен, индопрофен, кетопрофен, миропрофен,напроксен, оксапрозин, пирпрофен, пранопрофен, супрофен, тиопрофеновая кислота и тиоксапрофен),производные уксусной кислоты (индометацин, ацеметацин, алклофенак, клиданак, диклофенак, фенклофенак, фенклозиновая кислота, фентиазак, фурофенак, ибуфенак, изоксепак, окспинак, сулиндак, тиопинак, толметин, зидометацин и зомепирак), производные фенамовой кислоты (меклофенамовая кислота,мефенамовая кислота и толфенамовая кислота), производные бифенилкарбоновой кислоты, оксикамы(изоксикам, мелоксикам, пироксикам, судоксикам и теноксикам), салицилаты (ацетилсалициловая кислота, сульфасалазин) и пиразолоны (апазон, безпиперилон, фепразон, мофебутазон, оксифенбутазон, фенилбутазон), коксибы (целекоксиб, валекоксиб, рофекоксиб и эторикоксиб) и т.п. Противовирусные лекарственные средства, такие как ацикловир, теновир, плеконарил, перамивир,докозанол и т.п. Антибиотики, такие как гентамицин, стрептомицин, гелданамицин, дорипенем, цефалексин, цефаклор, цефтазихин, цефепим, эритромицин, ванкомицин, азтреонам, амоксициллин, бацитрацин, эноксацин, мафенид, доксициклин, хлорамфеникол и т.п. Антагонисты опиатного рецептора: морфин, пропоксифен (дарвон), трамадол, бупренорфин и т.п. Глюкокортикостероиды, такие как бетаметазон, будезонид, дексаметазон, гидрокортизон, метилпреднизолон, преднизолон, преднизон, триамцинолон и дефлазакорт. Иммунодепрессивные, иммуномодулирующие или цитостатические лекарственные средства, включая, но не ограничиваясь только ими, гидроксихлорохин, D-пеницилламин, сульфазалицин, ауранофин,препараты золота, меркаптопурин, такролимус, сиролимус, микофенолят мотефил, циклоспорин, лефлуномид, метотрексат, азатиоприн, циклофосфамид и глатирамер ацетат и новантрон, финголимод(FTY720), миноциклин, талидомид и т.п. Антитела к TNF или антагонисты рецептора TNF, такие как, но не ограничивающиеся только ими,этанерцепт, инфликсимаб, адалимумаб (D2E7), CDP 571 и Ro 45-2081 (ленерцепт), или биологические средства, действие которых направлено на мишени, такие как, но не ограничиваясь только ими, CD-4,CTLA-4, LFA-1, IL-6, ICAM-1, C5, и натализумаб и т.п. Антагонисты рецептора IL-1, такие как, но не ограничиваясь только им, кинерет. Блокаторы натриевых каналов: карбамазепин, мексилетин, ламотригин, тектин, лакозамид и т.п. Блокаторы кальциевых каналов N-типа: зиконотид и т.п. Серотонинергические и норадренергические модуляторы: пароксетин, дулоксетин, клонидин, амитриптилин, циталопрам. Антагонисты гистаминового рецептора H1: бромфенирамин, хлорфенирамин, дексхлорфенирамин,трипролидин, клемастин, дифенгидрамин, дифенилпиралин, трипеленнамин, гидроксизин, метдиазин,прометазин, тримепразин, азатидин, ципрогептадин, антазолин, фенирамин пириламин, астемизол, терфенадин, лоратадин, цетиризин, деслоратадин, фексофенадин, левоцетиридин и т.п. Антагонисты гистаминового рецептора H2: циметидин, фамотидин, ранитидин и т.п. Ингибиторы протонного насоса: омепразол, пантопразол, эзомепразол и т.п. Антагонисты лейкотриена и ингибиторы 5-липоксигеназы: зафирлукаст, монтелукаст, пранлукаст,зилеутон и т.п. Местные анестетики, такие как амброксол, лидокаин и т.п. Модуляторы калиевых каналов: такие как ретигабин. Модуляторы GABA: лакозамид, прегабалин, габапентин и т.п. Средства для борьбы с мигренью: суматриптан, золмитрипан, наратриптан, элетриптан, телкагепант и т.п. Антитела NGF, такие как RI-724 и т.п. Комбинированная терапия также возможна в новых подходах к лечению боли, например, с помощью антагонистов Р 2 Х 3, антагонистов VR1, антагонистов NK1 и NK2, антагонистов NMDA, антагонистов mGluR и т.п. Комбинация соединений предпочтительно является синергетической комбинацией. Синергизм, как описано, например, в публикации Chou and Talalay, Adv. Enzyme Regul. 22:27-55 (1984), возникает в случае, если воздействие соединений при их введении в комбинации является более сильным, чем суммарное воздействие соединений при их введении по отдельности в виде отдельных средств. Обычно синергетический эффект наиболее четко проявляется при использовании соединений в субоптимальных концентрациях. Синергизм может проявляться в более низкой цитотоксичности, усиленном фармакологическом действии или каком-либо другом более благоприятном свойстве комбинации, по сравнению с отдельными компонентами. Экспериментальный раздел Примеры получения соединений общей формулы Id. Если не указано иное, то одну или большее количество таутомерных форм соединений, приведенных в примерах, описанных ниже в настоящем изобретении, можно получить in situ и/или выделить. Все таутомерные формы соединений, приведенных в примерах, описанных ниже в настоящем изобретении,следует рассматривать как раскрытые. Настоящее изобретение проиллюстрировано приведенными ниже примерами, в которых могут быть использованы следующие аббревиатуры. АббревиатурыAcOH - уксусная кислота БСТФА - (N,O-бис-(триметилсилил)трифторацетамидMeOH - метанол МС - масс-спектрометрия МТБЭ - метил-трет-бутиловый эфир ЯМР - ядерный магнитный резонанс ПЭ - петролейный эфирPPA - циклический ангидрид 1-пропилфосфоновой кислоты ОФ - обращенная фаза КТ - комнатная температураTBTU - О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийтетрафторборат ТКДИ - тиокарбонилдиимидазол ТЭА - триэтиламин ТГФ - тетрагидрофуран ТФК - трифторуксусная кислота ТСХ - тонкослойная хроматография Аналитические методики Данные ТСХ получали с использованием приведенных ниже пластин для ТСХa) пластины с силикагелем 60 F254 Merck No. 1.05714.0001, в экспериментальной части обозначены как "силикагель";b) пластины для хроматографии с обращенной фазой: RP-8 F 254s Merck No. 1.15684.0001, в экспериментальной части обозначены как "RP-8";c) пластины с оксидом алюминия 60 F254 Merck No. 1.05713.0001, в экспериментальной части обозначены как "Alox". Приведенные значения Rf определяли без насыщения атмосферы камеры. Данные ВЭЖХ/МС, когда они приведены, были получены при следующих параметрах.Agilent 1100 с насосом для подачи четырех компонентов, автоматический пробоотборник GilsonG215, детектор на диодной матрице HP. Детектирование с помощью диодной матрицы проводили в диапазоне длин волн 210-550 нм. Диапазон масс-спектрометрического детектирования: от m/z 120 до m/z 1000. Использовали следующие методики. Методика А. Подвижная фаза: В качестве неподвижной фазы использовали следующую колонку (температура колонки: постоянная, 25C): Zorbax Stable Bond C18, 1,8 мкм, 3,030 мм. Методика В. Подвижная фаза: В качестве неподвижной фазы использовали следующую колонку (температура колонки: постоянная, 25C): Zorbax StableBond C18, 3,5 мкм, 4,675 мм. Для приведенных ниже соединений представлены структурные формулы. Специалист в данной области техники должен понимать, что должны соблюдаться правила валентности и поэтому каждый атом должен образовывать определенное количество связей, которые не обязательно изображены на чертежах. Например, в случае, если гетероатом, которым является азот, изображен только с одной или двумя свя- 23020282 зями, то специалист в данной области техники должен понимать, что он должен образовывать еще одну или две связи (всего три), при этом такие связи (одна или две) обычно заканчиваются атомами водорода(таким образом образуя фрагмент -NH2 или -N(H)-). Пример 1. 2-[5-(1-Ацетамидоэтил)-2-хлорфениламино]-N-(4-бромфенил)-1-метилбензимидазол-5 карбоксамид.(a) 4-Хлорметил-3-нитробензиламин. Ацетат аммония (3,86 г, 50 ммолей), NaBH3CN (0,22 г, 3,5 ммоля) и 3 молекулярные сита (25 г) при КТ добавляли к смеси 4-хлор-3-нитроацетофенона (1,00 г, 5 ммолей) и MeOH (15 мл). Смесь перемешивали при КТ в течение 20 ч и добавляли NaHCO3 (насыщенный водный раствор) и EtOAc. Смесь фильтровали и водный слой промывали с помощью EtOAc. Объединенные органические фазы сушили над Na2SO4 и концентрировали и получали искомое промежуточное соединение. Выход: 0,27 г (27%).(b) N-[1-(4-Хлор-3-нитрофенил)этил]ацетамид. ТЭА (0,28 мл, 2,0 ммоля), затем ацетилхлорид (96 мкл, 1,3 ммоля) при КТ добавляли к 4-хлор-метил-3-нитробензиламину (0,27 г, 1,3 ммоля) в ТГФ (5 мл). Смесь перемешивали при КТ в течение 3,5 ч и добавляли дополнительное количество ацетилхлорида (20 мкл, 0,27 ммоля). Через 1 ч при КТ добавлялиNaHCO3 (водный раствор, 5%) и смесь экстрагировали с помощью EtOAc. Объединенные экстракты сушили над Na2SO4 и концентрировали и получали искомое промежуточное соединение. Выход: 0,30 г (92%).(c) N-[1-(3-Амино-4-хлорфенил)этил]ацетамид. Раствор дитионита натрия (1,08 г, 6,1 ммоля) в H2O (4 мл) при энергичном перемешивании при 55C добавляли к смеси N-[1-(4-хлор-3-нитрофенил)этил]ацетамида (0,30 г, 1,2 ммоля) и EtOH (20 мл). Через 4 ч при 55C добавляли дополнительное количество дитионита натрия (0,20 г, 1,1 ммоля) и перемешивание продолжали при 55C в течение 1,5 ч. Смеси давали охладиться и добавляли NaHCO3 (насыщенный водный раствор). Смесь экстрагировали с помощью EtOAc, и объединенные экстракты сушили над Na2SO4 и концентрировали, и получали искомое промежуточное соединение. Выход: 90 мг (34%).N-[1-(3-Амино-4-хлорфенил)этил]ацетамид (90 мг, 0,2 ммоля) при КТ добавляли к смеси 1,1'-тиокарбонилди-2-пиридона (69 мг, 0,2 ммоля), ДМАП (7 мг, 0,05 ммоля) и ДХМ (2 мл). Смесь концентрировали и использовали на следующей стадии без дополнительной очистки.(e) 3-Нитро-N-(4-бромфенил)-4-метиламинобензамид. Смесь 3-нитро-4-метиламинобензойной кислоты (196 мг, 1,00 ммоля), 20 мл ДХМ, 0,15 мл пиридина и 160 мг 1-хлор-N,N,2-триметилпроп-1-ениламина перемешивали до получения прозрачного раствора. Добавляли 4-броманилин (172 мг, 1,0 ммоля) и смесь перемешивали в течение 16 ч. Смесь фильтровали через слой ALOX B и концентрировали. Добавляли 5 мл ДМФ и 20 мл H2O и осадок собирали и сушили. Выход: 240 мг (68%).MeOH и 30 мг 5% Pd на угле перемешивали в атмосфере водорода (3,5 бар) в течение 4 ч. Катализатор удаляли фильтрованием и смесь концентрировали и использовали на следующей стадии без дополнительной очистки.N-[1-(4-Хлор-3-изотиоцианатофенил)этил]ацетамид в ДМФ (2 мл) при КТ добавляли к смеси 3-амино-N-(4-бромфенил)-4-метиламинобензамида (87 мг, 0,2 ммоля, неочищенное вещество, полученное на предыдущей стадии) в ДМФ (2 мл). Смесь перемешивали при КТ в течение ночи и концентрировали. Оста- 24020282 ток очищали с помощью хроматографии и получали искомое промежуточное соединение. Выход: 130 мг.N,N-Диизопропилкарбодиимид (46 мкл, 0,2 ммоля) при КТ добавляли к 3-3-[5-(1-ацетамидоэтил)2-хлорфенил]тиоуреидо-N-(4-бромфенил)-4-(метиламино)бензамиду (130 мг, 0,2 ммоля) в ДМФ (2 мл). Смесь перемешивали при 80 С в течение 2 ч, охлаждали и концентрировали. Остаток очищали с помощью хроматографии и получали искомое соединение. Выход: 30 мг (24%). МС m/z: 540 [M+H]+. Методика ВЭЖХ A: Rt=1,60 мин. Пример 2. 2-[5-(трет-Бутилкарбониламинометил)-2-хлорфениламино]-6-хлор-N-(2,2,2-трифторэтил) бензимидазол-5-карбоксамид.(а) трет-Бутил-4-хлор-3-нитробензилкарбамат. Ди-трет-бутилдикарбонат (21,05 г, 96,5 ммоля) в ДХМ (30 мл) добавляли к охлажденной льдом смеси 4-хлор-3-нитробензиламина (15 г, 80,4 ммоля), ДМАП (0,49 г, 4 ммоля) и ДХМ (100 мл). Смесь перемешивали при КТ в течение 12 ч, выливали в аммиак и экстрагировали с помощью ДХМ. Объединенные экстракты промывали рассолом и концентрировали. Остаток промывали с помощью Et2O и получали искомое промежуточное соединение, которое непосредственно использовали на следующей стадии без какой-либо дополнительной очистки.(100 мл) нагревали при 90C в течение 4 ч и смеси давали охладиться. Значение pH доводили до 10 и смесь фильтровали через целит. Твердые вещества промывали с помощью EtOAc и EtOH и объединенные фильтраты концентрировали для удаления органических растворителей. Остаток добавляли к аммиаку и смесь экстрагировали с помощью ДХМ. Объединенные экстракты промывали рассолом, сушили над Na2SO4 и концентрировали. Кристаллизация из смеси EtOAc/петролейный эфир давала искомое промежуточное соединение. Выход: 15,5 г (75% в пересчете на 4-хлор-3-нитробензиламин).(c) трет-Бутил-4-хлор-3-изотиоцианатобензилкарбамат. Искомое промежуточное соединение получали из трет-бутил-3-амино-4-хлорбензилкарбамата в соответствии с примером 1, стадия (d).(d) Этил-2-[5-(трет-бутоксикарбониламинометил)-2-хлорфениламино]-6-хлорбензимидазол-5-карбоксилат. Искомое промежуточное соединение получали за две стадии из трет-бутил-4-хлор-3-изотиоцианатобензилкарбамата и этил-2-хлор-4,5-диаминобензойной кислоты в соответствии с примером 1,стадия (g), с добавлением ТЭА, и в соответствии с примером 1, стадия (h).(e) Этил-2-[5-(аминометил)-2-хлорфениламино]-6-хлорбензимидазол-5-карбоксилат. Смесь 1,15 г (2,4 ммоля) этил-2-[5-(трет-бутилкарбониламинометил)-2-хлорфениламино]бензимидазол-5-карбоксилата и 10 мл 4 М раствора HCl в диоксане перемешивали в течение ночи. Реакционную смесь концентрировали при пониженном давлении и получали искомое промежуточное соединение. Выход: 1,0 г (100%).(f) Этил-2-[5-(трет-бутилкарбониламинометил)-2-хлорфениламино]-6-хлорбензимидазол-5-карбоксилат. Смесь этил-2-[5-(аминометил)-2-хлорфениламино]-6-хлорбензимидазол-5-карбоксилата (1,00 г,2,4 ммоля), пивалоилхлорида (0,296 мл, 2,4 ммоля), 1,5 мл ТЭА и 50 мл ТГФ перемешивали при КТ в течение 18 ч. Смесь концентрировали, разбавляли с помощью EtOAc, дважды промывали с помощьюH2O, сушили над Na2SO4 и концентрировали. Остаток очищали с помощью хроматографии и получали искомое промежуточное соединение. Выход: 0,92 г (83%).(g) 2-[5-(трет-Бутилкарбониламинометил)-2-хлорфениламино]-6-хлорбензимидазол-5-карбоновая кислота. Смесь этил-2-[5-(трет-бутилкарбониламинометил)-2-хлорфениламино]-6-хлорбензимидазол-5-карбоксилата (0,91 г, 1,9 ммоля) и 20 мл EtOH обрабатывали 1 н. раствором NaOH (3,9 мл+0,98 мл+0,98 мл) при КТ в течение 4 ч, при 50C в течение 5 ч и при КТ в течение 3 дней. Смесь концентрировали, разбавляли с помощью H2O, подкисляли 1 н. раствором HCl и охлаждали в бане со льдом. Осадок отфильтровывали,промывали водой со льдом и сушили и получали искомое промежуточное соединение. Выход: 0,81 г (95%).(a) 2-Хлор-N-циклопентил-4-фтор-5-нитробензамид и 2-хлор-N-циклопентил-4-циклопентиламино 5-нитробензамид. 2-Хлор-4-фтор-5-нитробензоилхлорид (1,5 г, 6,30 ммоля) при -20C добавляли к смеси циклопентиламина (430 мкл, 12,6 ммоля), ТЭА (1,76 мл, 12,6 ммоля) и ДХМ (30 мл). Через 12 ч при КТ смесь разбавляли с помощью ДХМ и промывали с помощью NH4OH (насыщенный водный раствор). Органический слой промывали с помощью H2O и рассолом, сушили над Na2SO4, концентрировали и очищали с помощью ВЭЖХ и получали 510 мг (28%) 2-хлор-N-циклопентил-4-фтор-5-нитробензамида и 300 мгN-Метиламин в MeOH (2 М раствор, 2,0 мл, 4,0 ммоля) добавляли к 2-хлор-N-циклопентил-4-фтор 5-нитробензамиду (230 мг, 0,79 ммоля) в EtOH. Смесь нагревали в герметичном сосуде при 50C в течение 12 ч, охлаждали и концентрировали. Остаток очищали с помощью хроматографии и получали искомое промежуточное соединение. Выход: 150 мг (64%).(c) 5-Амино-2-хлор-N-циклопентил-4-метиламинобензамид. Искомое промежуточное соединение получали из 2-хлор-N-циклопентил-4-метиламино-5-нитро- 26020282(d) 3-Амино-4-хлорбензиламин. Смесь 3-амино-4-хлорбензонитрила (1,32 г, 8,33 ммоля), никеля Ренея (0,25 г) и 80 мл NH3 в MeOH перемешивали в атмосфере H2 (3 бар) при КТ в течение 4 ч. Смесь фильтровали и концентрировали и искомое промежуточное соединение использовали без дополнительной очистки.(0,59 г, 4,17 ммоля), 1,47 г TBTU, 1,45 мл ТЭА и 30 мл ТГФ перемешивали при КТ в течение 6 ч. Смесь концентрировали, разбавляли с помощью EtOAc, дважды промывали 2 М раствором NaOH и 1 раз рассолом, сушили над Na2SO4, фильтровали и концентрировали и получали искомое промежуточное соединение. Выход: 1,17 г (100%).(f) N-(4-Хлор-3-изотиоцианатобензил)-1-метилциклогексиламид. Искомое промежуточное соединение получали из N-(4-хлор-3-аминобензил)-1-метилциклогексиламида по аналогии с примером 1, стадия (d), но с использованием 1,1'-тиокарбонилдиимидазола вместо 1,1'-тиокарбонилди-2-пиридона.(g) 6-Хлор-2-2-хлор-5-[(1-метилциклогексиламидо)метил]фениламино-N-циклопентил-1-метилбензимидазол-5-карбоксамид. Искомое соединение получали из N-(4-хлор-3-изотиоцианатобензил)-1-метилциклогексиламида и 5-амино-2-хлор-N-циклопентил-4-метиламинобензамида по аналогии с примером 1, стадии (g и h), но без выделения тиоуреидного производного и с использованием в качестве реагента сочетания ЭДХ вместо(910 мг, 2,0 ммоля), NaOH (2 М водный раствор, 3,0 мл, 6,0 ммоля) и диоксана (15 мл) нагревали при 90C в течение 12 ч и концентрировали. Остаток подвергали распределению между NaOH (2 М водный раствор) и МТБЭ. Водную фазу подкисляли до pH 4-5 с помощью HCl (4 М водный раствор). Осадок собирали, промывали с помощью H2O и сушили и получали искомое промежуточное соединение. Выход: 873 мг (99%).(3 мл). Через 10 мин при КТ добавляли пирролидин (37 мкл, 0,45 ммоля) в ДМФ (1 мл). Через 12 ч при КТ смесь концентрировали и остаток подвергали распределению между водой и ДХМ. Водный слой экстрагировали с помощью ДХМ и объединенные экстракты промывали рассолом, сушили над Na2SO4 и концентрировали. Остаток очищали с помощью хроматографии и получали искомое соединение. Выход: 127 мг (57%). 400 МГц 1H-ЯМР (ДМСО-d6, ч./млн)11,22-11,08 (1 Н, m), 8,83-8,69 (1 Н, m), 8,55 (1 Н, s), 8,12 (1 Н, t,J=5,8 Гц), 7,58-7,44 (1H, m), 7,41-7,28 (2 Н, m), 7,26-7,18 (1 Н, m), 6,89-6,82 (1H, m), 4,28 (2H, d, J=5,8 Гц),3,50-3,41 (4H, m), 2,01-1,91 (2H, m), 1,89-1,75 (4H, m), 1,47-1,16 (8H, m), 1,12 (3H, s).(a) Ди-трет-бутил-2,5-дихлор-4-нитрофенилимидодикарбонат. Ди-трет-бутилдикарбонат (4,58 г, 21,0 ммоля) порциями добавляли к смеси 2,5-дихлор-4-нитроанилина (2,07 г, 10,0 ммоля), ДМАП (61,1 мг, 0,5 ммоля) и ТГФ (15 мл). Через 12 ч при КТ смесь концентрировали и остаток подвергали распределению между EtOAc и лимонной кислотой (1 М водный раствор). Органический слой промывали рассолом, сушили над Na2SO4 и концентрировали. Остаток промывали петролейным эфиром и получали искомое промежуточное соединение. Выход: 3,67 г (91%).(b) трет-Бутил-2-хлор-5-(метиламино)-4-нитрофенилкарбамат. Искомое промежуточное соединение получали из ди-трет-бутил-2,5-дихлор-4-нитрофенилимидодикарбоната в соответствии с примером 3, стадия (b).(c) трет-Бутил-4-амино-2-хлор-5-(метиламино)фенилкарбамат). Искомое промежуточное соединение получали из трет-бутил-2-хлор-5-(метиламино)-4-нитрофенилкарбамата в соответствии с примером 2, стадия (b).(d) трет-Бутил-5-хлор-2-2-хлор-5-[(1-метилциклогексиламидо)метил]фениламино-1-метил-6-бензимидазолилкарбамат. Искомое соединение получали из N-(4-хлор-3-изотиоцианатобензил)-1-метилциклогексиламида и третбутил-4-амино-2-хлор-5-(метиламино)фенилкарбамата в соответствии с описанными выше методиками. 200 МГц 1 Н-ЯМР (ДМСО-d6, ч./млн)8,55 (1 Н, s), 8,40 (1 Н, s), 8,12 (1H, t, J=5,2 Гц), 7,80-7,74 (1 Н,m), 7,48-7,29 (3H, m), 7,01-6,89 (1 Н, m), 4,26 (2H,d, J=6,0 Гц), 3,66 (3H, s), 2,00-1,85 (2 Н, m), 1,46 (9 Н, s),1,42-1,10 (8 Н, m), 1,06 (3H, s). МС m/z: 560 [M+H]+. Пример 6. N-4-Хлор-3-[5-хлор-6-(циклопентиламидо)-1-метил-2-бензимидазолиламино]бензил-1 метилциклогексиламид.(a) N-[4-Хлор-3-(6-амино-5-хлор-1-метил-2-бензимидазолиламино)бензил]-1-метилциклогексиламид. Смесь трет-бутил-5-хлор-2-2-хлор-5-[(1-метилциклогексиламидо)метил]фениламино-1-метил-6 бензимидазолилкарбамата (400 мг, 0,71 ммоля), ТФК (0,5 мл; 6,7 ммоля) и ДХМ (10 мл) нагревали в герметизированной пробирке при 80C в течение 3 ч. Смесь охлаждали, разбавляли с помощью ДХМ и промывали с помощью NaHCO3 (насыщенный водный раствор; осторожно: выделение газа) и сушили надNa2SO4. Концентрирование давало искомое промежуточное соединение. Выход: 320 мг (98%).(b) N-4-Хлор-3-[5-хлор-6-(циклопентиламидо)-1-метил-2-бензимидазолиламино]бензил-1-метилциклогексиламид. Искомое соединение получали из N-[4-хлор-3-(6-амино-5-хлор-1-метил-2-бензимидазолиламино)бензил]1-метилциклогексиламида, циклопентилкарбоновой кислоты и HBTU в соответствии с примером 4, стадия (b). 200 МГц 1 Н-ЯМР (ДМСО-d6, ч./млн)9,37 (1 Н, s), 8,42 (1H, s), 8,12 (1 Н, t, J=5,8 Гц), 7,84-7,72 (1 Н,m), 7,51 (1 Н, s), 7,43 (1H, d, J=8,2 Гц), 7,36 (1 Н, s), 6,96 (1 Н, dd, J=8,2, 1,2 Гц), 4,27 (2H, d, J=5,8 Гц), 3,67 му льдом раствору 4-хлор-3-нитробензилсульфонилхлорида (2,0 г, 7,8 ммоля) в MeCN (20 мл). Через 1 ч при КТ смесь выливали в смесь воды со льдом и экстрагировали с помощью EtOAc. Объединенные экстракты промывали рассолом, сушили над Na2SO4 и концентрировали и получали искомое промежуточное соединение. Выход: 2,2 г (92%).(b) N-Циклопентил-4-метиламино-3-нитробензолсульфонамид. Искомое промежуточное соединение получали из 4-хлор-N-циклопентил-3-нитробензолсульфонамида и метиламина в соответствии с примером 3, стадия (b).(c) 3-Амино-N-циклопентил-4-метиламинобензолсульфонамид. Искомое промежуточное соединение получали из N-циклопентил-4-метиламино-3-нитробензолсульфонамида в соответствии с примером 2, стадия (b).(d) N-4-Хлор-3-[5-(N-циклопентилсульфамоил)-1-метил-2-бензимидазолиламино]бензил-1-метилциклогексиламид. Искомое соединение получали из N-(4-хлор-3-изотиоцианатобензил)-1-метилциклогексиламида и 3-амино-N-циклопентил-4-метиламинобензолсульфонамида в соответствии с примером 3, стадия (g). 200 МГц 1H-ЯМР (ДМСО-d6, ч./млн)8,51 (1 Н, s), 8,13 (1H, t, J=6,0 Гц), 7,87-7,81 (1 Н, m), 7,58-7,39(500 мг, 1,19 ммоля, получали по экспериментальным методикам, аналогичным описанным выше) иEtOH (20 мл) насыщали аммиаком. Добавляли свежеприготовленный никель Ренея (7 мг, 0,12 ммоля) и смесь гидрировали (КТ, 70 атм) в течение 48 ч. Смесь фильтровали через целит и осадок на фильтре промывали с помощью EtOAc. Объединенные фильтраты концентрировали, и остаток обрабатывали смесью петролейного эфира и диэтилового эфира, и получали искомое промежуточное соединение. Выход: 500 мг (98%).(b) 2-2-Хлор-5-[(1-метилциклопропиламидо)метил]фениламино-N-циклогексилметил-1-метилбензимидазол-5-карбоксамид. Искомое соединение получали из 2-(5-аминометил-2-хлорфениламино)-N-циклогексилметил-1 метилбензимидазол-5-карбоксамида, 1-метилциклопропилкарбоновой кислоты и HBTU в соответствии с примером 4, стадия (b). 200 МГц 1 Н-ЯМР (ДМСО-d6, ч./млн)8,38 (1H, s), 8,33-8,22 (1 Н, m), 8,19-8,08 (1H, m), 7,91-7,80 Тиофен-2-сульфонилхлорид (64 мг, 0,35 ммоля) в MeCN (1 мл) добавляли к смеси 2-(5-аминометил 2-хлорфениламино)-N-циклогексилметил-1-метилбензимидазол-5-карбоксамида (150 мг, 0,35 ммоля),ТЭА (150 мкл, 1,1 ммоля) и MeCN (2 мл). Через 12 ч при КТ смесь разбавляли с помощью ДХМ и промывали с помощью NH3 (насыщенный водный раствор) и рассолом, сушили над Na2SO4 и концентрировали. Остаток очищали с помощью хроматографии и получали искомое соединение. Выход: 36 мг (18%). 200 МГц 1 Н-ЯМР (ДМСО-d6, ч./млн)8,50-8,36 (2 Н, m), 8,35-8,22 (1 Н, m), 7,94-7,82 (3H, m), 7,697,57 (2 Н, m), 7,42 (1 Н, d, J=8,2 Гц), 7,37 (1 Н, d, J=8,2 Гц), 7,18-7,11 (1H, m), 7,04-6,95 (1H, m), 4,09-3,96
МПК / Метки
МПК: A61K 31/4188, A61P 11/00, C07D 471/04, A61P 29/00
Метки: производные, качестве, средств, бензимидазола, противовоспалительных
Код ссылки
<a href="https://eas.patents.su/30-20282-proizvodnye-benzimidazola-v-kachestve-protivovospalitelnyh-sredstv.html" rel="bookmark" title="База патентов Евразийского Союза">Производные бензимидазола в качестве противовоспалительных средств</a>
Предыдущий патент: Пестицидные смеси
Следующий патент: Средство для профилактики и лечения высокопатогенных инфекционных заболеваний
Случайный патент: Применение пираклостробина в качестве сафенера для тритиконазола при борьбе с вредными грибами












