Низкомолекулярные миристатные ингибиторы тирозинкиназы bcr-abl и способы их применения
Номер патента: 19869
Опубликовано: 30.06.2014
Авторы: Чжан Цзяньминг, Войцеховская Эми, Денг Сяньминг, Чанг Джевон, Грей Натанаэл С., Окрам Барун
Формула / Реферат
1. Соединение формулы (I) или его фармацевтически приемлемая соль
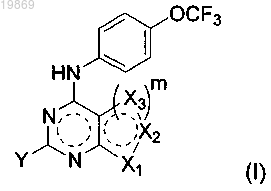
где каждый из X1, Х2 или Х3 независимо представляет собой NR1, CR1, С(О), О или S;
каждый R1 независимо выбран из Н; С1-6-алкила, возможно замещенного от одного до двух заместителями, выбранными из OR2, NR2R2, CF3 или CN; С3-8-циклоалкила; (CH2)nC3-8-гетероциклоалкила, содержащего от одного до двух гетероатомов, независимо выбранных из N или О, и возможно замещенного от одного до трех заместителями, независимо выбранными из ОН, NR2R2 или С1-2-алкила, замещенного одной ОН; (CH2)nC6-10-арила, возможно замещенного от одного до двух заместителями, независимо выбранными из С1-6-алкила, галогена, OR2, CF3 или SO2NRxRx; (CH2)nC3-12-гетероарила, содержащего один гетероатом, представляющий собой N, и возможно замещенного от одной до двух =O или одной CF3; -C(O)Rx; (CH2)nC(O)ORx; (CH2)nC(O)NRxRx; S(O)2Rx; C(O)NR2S(O)2Rx или отсутствует;
каждый Rx, для каждого случая, независимо представляет собой Н; С1-6-алкил, возможно замещенный OR2 или NR2R2; (CH2)nC3-12-гетероциклоалкил, содержащий от одного до трех гетероатомов, независимо выбранных из N, О или S, и возможно замещенный от одного до двух заместителями, независимо выбранными из галогена, 3-трифторметилфенила, бензила, фуран-3-илкарбонила, 1-пирролидинила, =O, (CH2)nOR2, (CH2)nC(O)OR2, C(O)NH2, NR2R2, фенила или R2; С6-8-арил, возможно замещенный от одного до двух заместителями, независимо выбранными из С1-6-алкила, CF3 или 3-трифторметилбензоиламино; (CH2)nC3-8-гетероарил, содержащий от одного до двух гетероатомов, независимо выбранных из N или S, и возможно замещенный одной (CH2)nC(O)OR2; NHR2 или C(NH)NH2;
R2 представляет собой Н или C1-6-алкил, возможно замещенный одной ОН;
Y представляет собой Н, ОН, NH2 или СН3;
m равен 1 или 2; и
каждый n независимо равен 0, 1 или 2,
при условии, что указанное соединение не представляет собой соединение, выбранное из группы, состоящей из
[1-(2,4-диметилфенил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амина,
5-фенил-N-(4-(трифторметокси)фенил)тиено[2,3-d]пиримидин-4-амина,
N-[4-(трифторметокси)фенил]-4-хиназолинамина,
6-метил-N-[4-(трифторметокси)фенил]-4-хиназолинамина,
6-этил-N-[4-(трифторметокси)фенил]-4-хиназолинамина,
3-метил-N-[4-(трифторметокси)фенил]-3Н-1,2,3-триазоло[4,5-d]пиримидин-7-амина,
3-этил-N-[4-(трифторметокси)фенил]-3Н-1,2,3-триазоло[4,5-d]пиримидин-7-амина,
1-метил-N-[4-(трифторметокси)фенил]-1Н-пиразоло[3,4-d]пиримидин-4-амина,
N-[4-(трифторметокси)фенил]-9Н-пурин-6-амина.
2. Соединение по п.1, выбранное из соединений формул (II), (III) или (VIII)
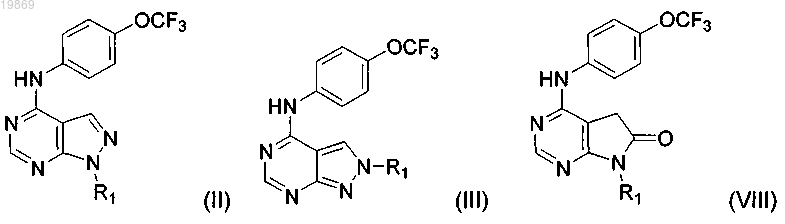
где R1 выбран из Н; C1-6-алкила, возможно замещенного от одного до двух заместителями, выбранными из ОН, NR2R2, CF3 или CN; (CH2)nC3-8-циклоалкила; (CH2)nC3-8-гетероциклоалкила, содержащего один гетероатом, представляющий собой О; (CH2)nC6-10-арила, возможно замещенного от одного до двух заместителями, независимо выбранными из С1-6-алкила, галогена, ОН, CF3 или SO2NRxRx; (CH2)nC3-2-гетероарила, содержащего один гетероатом, представляющий собой N, и возможно замещенного одной или двумя =O или одной CF3; (CH2)nC(O)NRxRx или -S(O)2Rx;
Rx для каждого случая независимо представляет собой Н или С1-6-алкил;
R2 представляет собой Н или C1-6-алкил, возможно замещенный одной ОН; и
каждый n независимо равен 0, 1 или 2.
3. Соединение по п.2, отличающееся тем, что:
а) соединение является соединением формулы (II) и выбрано из следующих:
2-(4-(4-(трифторметокси)фениламино)-1Н-пиразоло[3,4-d]пиримидин-1-ил)этанол;
(1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-этил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-этансульфонил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-циклогексил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
2-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-1-ил]ацетамид;
3-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-1-ил]пропионамид;
[1-(тетрагидрофуран-3-илметил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
3-диметиламин-2-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-1-ил]пропионитрил;
(1-бутил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-трет-бутил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[1-(2,2,2-трифторэтил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(1-бензил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-фенетил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[1-(3-фтор-4-трифторметилбензил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[1-(3-бромбензил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
3-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-1-илметил]фенол;
(1-пиридин-3-илметил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-пиридин-2-илметил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(1-пиридин-4-илметил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
2-{2-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-1-ил]этил}изоиндол-1,3-дион;
[1-(2-аминоэтил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(4-трифторметоксифенил)-[1-(4-трифторметилпиридин-2-ил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]амин,
[1-(2,3-диметилфенил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[1-(2-фторфенил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[1-(2,4-дихлорфенил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[1-(2-этилфенил)-1Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(1-пиридин-2-ил-1Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
3-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-1-ил]бензолсульфонамид; или
b) соединение является соединением формулы (III) и выбрано из следующих:
2-(4-(4-(трифторметокси)фениламино)-2Н-пиразоло[3,4-d]пиримидин-2-ил)этанол;
(2-этил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(2-циклогексил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
2-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-2-ил]ацетамид;
[2-(тетрагидрофуран-3-илметил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(2-бутил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[2-(2,2,2-трифторэтил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(2-бензил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(2-фенетил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[2-(3-фтор-4-трифторметилбензил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[2-(3-бромбензил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
3-[4-(4-трифторметоксифениламино)пиразоло[3,4-d]пиримидин-2-илметил]фенол;
(2-пиридин-3-илметил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(4-трифторметоксифенил)-[2-(4-трифторметилпиридин-2-ил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]амин;
[2-(2,3-диметилфенил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[2-(2-фторфенил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[2-(2,4-дихлорфенил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[2-(2-этилфенил)-2Н-пиразоло[3,4-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(2-пиридин-2-ил-2Н-пиразоло[3,4-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин; или
с) соединение является соединением формулы (VIII) и выбрано из следующих:
4-(4-трифторметоксифениламино)-5,7-дигидропирроло[2,3-d]пиримидин-6-он;
7-метил-4-(4-трифторметоксифениламино)-5,7-дигидропирроло[2,3-d]пиримидин-6-он.
4. Соединение по п.1 формулы (IV)
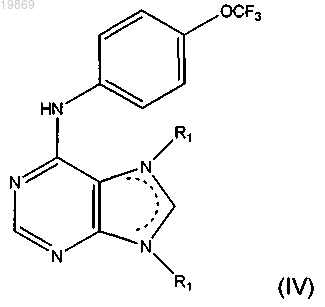
где каждый R1 независимо выбран из Н; С1-6-алкила; (CH2)nC3-8-гетероциклоалкила, содержащего от одного до двух гетероатомов, независимо выбранных из N или О, и возможно замещенного от одного до трех заместителями, независимо выбранными из ОН или С1-2алкила, замещенного одной ОН; или отсутствует; и
каждый n независимо равен 0, 1 или 2.
5. Соединение по п.4, выбранное из следующих:
(9-метил-9Н-пурин-6-ил)-(4-трифторметоксифенил)амин;
(7-метил-7Н-пурин-6-ил)-(4-трифторметоксифенил)амин;
2-гидроксиметил-5-[6-(4-трифторметоксифениламино)пурин-9-ил]тетрагидрофуран-3,4-диол;
[9-(2-морфолин-4-ил-этил)-9Н-пурин-6-ил]-(4-трифторметоксифенил)амин.
6. Соединение по п.1, выбранное из соединений формул (V), (VI) или (VII)
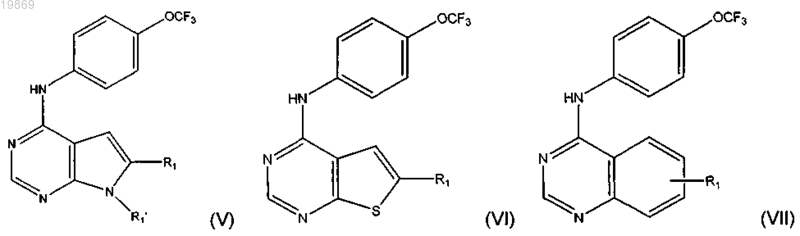
где R1 независимо выбран из Н; С1-6-алкила, возможно замещенного одним заместителем, выбранным из ОН или NR2R2; (CH2)nC3-8-гетероциклоалкила, содержащего от одного до двух гетероатомов, независимо выбранных из N или О, и возможно замещенного от одного до трех заместителями, независимо выбранными из (CH2)nOH или NR2R2; -C(O)Rx, (CH2)nC(O)ORx, -C(O)NR2S(O)2Rx или (CH2)nC(O)NRxRx;
Rx для каждого случая независимо представляет собой Н; С1-6-алкил, возможно замещенный одной OR2 или NR2R2, (CH2)nC3-12-гетероциклоалкил, содержащий от одного до трех гетероатомов, независимо выбранных из N, О или S, и возможно замещенный от одного до двух заместителями, независимо выбранными из галогена, 3-трифторметилфенила, бензила, фуран-3-илкарбонила, 1-пирролидинила, =O, (CH2)nOR2, (CH2)nC(O)OR2, C(O)NH2, NR2R2, фенила или R2; С6-8-арил, возможно замещенный от одного до двух заместителями, независимо выбранными из С1-6-алкила, CF3 или 3-трифторметилбензоиламино; (CH2)nC3-8-гетероарил, содержащий от одного до двух гетероатомов, независимо выбранных из N или S, и возможно замещенный одной (CH2)nC(O)OR2; NHR2 или C(NH)NH2;
R1' выбран из Н; С1-6алкила, возможно замещенного одной ОН; (CH2)nC3-8-гетероциклоалкила, содержащего от одного до двух гетероатомов, независимо выбранных из N или О, и возможно замещенного от одного до трех заместителями, независимо выбранными из ОН или R2; (CH2)nC6-8-арила, возможно замещенного OR2; или (CH2)nC(O)NRyRy;
Ry для каждого случая независимо представляет собой Н; С1-6-алкил, возможно замещенный OR2, (CH2)nC3-8-гетероциклоалкил, содержащий от одного до двух гетероатомов, независимо выбранных из N или О;
R2 представляет собой Н или C1-4-алкил, возможно замещенный одним ОН; и
каждый n независимо равен 0, 1 или 2.
7. Соединение по п.6, отличающееся тем, что R1 независимо выбран из Н; C1-6-алкила, возможно замещенного одним заместителем, выбранным из ОН или NR2R2; (CH2)nC3-8-гетероциклоалкила, содержащего один гетероатом, представляющий собой N, и возможно замещенного NR2R2; -C(O)Rx; (CH2)nC(O)ORx; -C(O)NR2S(O)2Rx или (CH2)nC(O)NRxRx;
Rx для каждого случая независимо представляет собой Н; С1-6-алкил, возможно замещенный одной OR2 или NR2R2; (CH2)nC3-12-гетероциклоалкил, содержащий от одного до трех гетероатомов, независимо выбранных из N, О или S, и возможно замещенный от одного до двух заместителями, независимо выбранными из галогена, 3-трифторметилфенила, фуран-3-илкарбонила, 1-пирролидинила, =O, (CH2)nOR2, (CH2)nC(O)OR2, C(O)NH2, NR2R2 или R2; С6-8-арил, возможно замещенный от одного до двух заместителями, независимо выбранными из С1-6-алкила или 3-трифторметилбензоиламино; NHR2 или C(NH)NH2; и
R2 представляет собой Н или C1-4-алкил, возможно замещенный одной ОН.
8. Соединение по п.6 или 7, отличающееся тем, что R1' выбран из Н; С1-6-алкила, возможно замещенного одной ОН; (CH2)nC3-8-гетероциклоалкила, содержащего от одного до двух гетероатомов, независимо выбранных из N или О, и возможно замещенного от одного до трех заместителями, независимо выбранными из ОН или R2; (CH2)nC6-8-арила, возможно замещенного OR2; или (CH2)nC(O)NRyRy;
Ry для каждого случая независимо представляет собой Н; С1-6-алкил, возможно замещенный OR2; (CH2)nC3-8-гетероциклоалкил, содержащий от одного до двух гетероатомов, независимо выбранных из N или О.
9. Соединение по любому из пп.6-8, отличающееся тем, что указанное соединение выбрано из следующих:
а) соединений формулы (V):
N-(2-морфолин-4-ил-этил)-3-[4-(4-трифторметоксифениламино)пирроло[2,3-d]-пиримидин-7-ил]пропионамид;
2-гидроксиметил-5-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]тетрагидрофуран-3,4-диол;
(7Н-пирроло[2,3-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(7-метил-7Н-пирроло[2,3-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
2-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]этанол;
[7-(2-морфолин-4-ил-этил)-7Н-пирроло[2,3-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[7-(4-метоксибензил)-7Н-пирроло[2,3-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
3-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]пропионамид;
N-этил-3-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]пропионамид;
N-(3-метоксипропил)-3-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]пропионамид;
N-(2-морфолин-4-ил-этил)-3-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]пропионамид;
этиловый эфир 7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбоновой кислоты;
(4-бромпиперидин-1-ил)-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло-[2,3-d]пиримидин-6-ил]метанон;
амид 1-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбонил]пиперидин-4-карбоновой кислоты;
амид 1-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбонил]пиперидин-3-карбоновой кислоты;
этиловый эфир 1-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбонил]пиперидин-3-карбоновой кислоты;
(3-гидроксиметилпиперидин-1-ил)-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-ил]метанон;
8-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбонил]-1-фенил-1,3,8-триаза-спиро[4.5]декан-4-он;
[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-ил]метанол;
(2-метоксиметилпирролидин-1-ил)-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-ил]метанон;
амид 7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбоновой кислоты;
этиламид 7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбоновой кислоты;
(1-этилпирролидин-2-ил)амид 7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбоновой кислоты;
N-[7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбонил]гуанидин;
(4-диэтиламино-1-метилбутил)амид 7-метил-4-(4-трифторметоксифениламино)-7Н-пирроло[2,3-d]пиримидин-6-карбоновой кислоты;
N-(1-гидрокси-4-метилпент-3-ил)-3-[4-(4-трифторметоксифениламино)пирроло[2,3-d]пиримидин-7-ил]пропионамид; или
b) соединений формулы (VI):
N-(2-гидроксиэтил)-4-(4-(трифторметокси)фениламино)тиено[2,3-d]пиримидин-6-карбоксамид;
тиено[2,3-d]пиримидин-4-ил-(4-трифторметоксифенил)амин;
(6-метилтиено[2,3-d]пиримидин-4-ил)-(4-трифторметоксифенил)амин;
метиловый эфир 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты;
4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновая кислота;
(2-морфолин-4-ил-этил)амид 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты;
[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанол;
этиламид 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты;
(2-гидроксиэтил)амид 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты;
[6-(3-диметиламинопирролидин-1-илметил)тиено[2,3-d]пиримидин-4-ил]-(4-трифторметоксифенил)амин;
(3-диметиламинопирролидин-1-ил)-[4-(4-трифторметоксифениламино)тиено[2,3-d]-пиримидин-6-ил]метанон;
(1-бензилпирролидин-3-ил)амид 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты;
(2-гидроксиметилпирролидин-1-ил)-[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанон;
пиперазин-1-ил-[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанон;
(4-пирролидин-1-ил-пиперазин-1-ил)-[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанон;
[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]-[4-(3-трифторметилфенил)пиперазин-1-ил]метанон;
(2-морфолин-4-ил-этил)амид 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты;
(4-метилпиперазин-1-ил)-[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанон;
(4-гидроксипиперидин-1-ил)-[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанон;
(4-метоксипиперидин-1-ил)-[4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-ил]метанон;
[2-метил-5-(3-трифторметилбензоиламино)фенил]амид 4-(4-трифторметоксифениламино)тиено[2,3-d]пиримидин-6-карбоновой кислоты; или
с) соединений формулы (VII):
4-(4-(трифторметокси)фениламино)-N-(2-гидроксиэтил)хиназолин-7-карбоксамид;
метиловый эфир 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанол;
(7-диэтиламинометилхиназолин-4-ил)-(4-трифторметоксифенил)амин;
диэтиламид 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
[4-(фуран-3-карбонил)пиперазин-1-ил]-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(3-трифторметилфенил)амид 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
(3-метоксипропил)амид 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
N'-этилгидразид 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
этиловый эфир (2-{[4-(4-трифторметоксифениламино)хиназолин-7-карбонил]амино}тиазол-5-ил)уксусной кислоты;
(4-метоксипиперидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(3-гидроксипирролидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(2-гидроксиметилпирролидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(3-диметиламинпирролидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(2-гидроксиэтил)метиламид 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
метил-(1-метилпиперидин-4-ил)амид 4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты;
4-метил-N-[4-(4-трифторметоксифениламино)хиназолин-7-карбонил]бензолсульфонамид;
2-метилпропан-2-сульфоновой кислоты [4-(4-трифторметоксифениламино)хиназолин-7-карбонил]амид;
(4-метил-[1,4]диазепан-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(3,5-диметилпиперазин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
(4-гидроксипиперидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты метил-(2-метиламиноэтил)амид;
4-(4-трифторметоксифениламино)хиназолин-7-карбоновой кислоты (2-гидроксиэтил)амид;
1-фенил-8-[4-(4-трифторметоксифениламино)хиназолин-7-карбонил]-1,3,8-триаза-спиро[4.5]декан-4-он;
(4-бромпиперидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон;
амид 1-[4-(4-трифторметоксифениламино)хиназолин-7-карбонил]пиперидин-4-карбоновой кислоты;
амид 1-[4-(4-трифторметоксифениламино)хиназолин-7-карбонил]пиперидин-3-карбоновой кислоты;
этиловый эфир 1-[4-(4-трифторметоксифениламино)хиназолин-7-карбонил]пиперидин-3-карбоновой кислоты;
(3-гидроксиметилпиперидин-1-ил)-[4-(4-трифторметоксифениламино)хиназолин-7-ил]метанон.
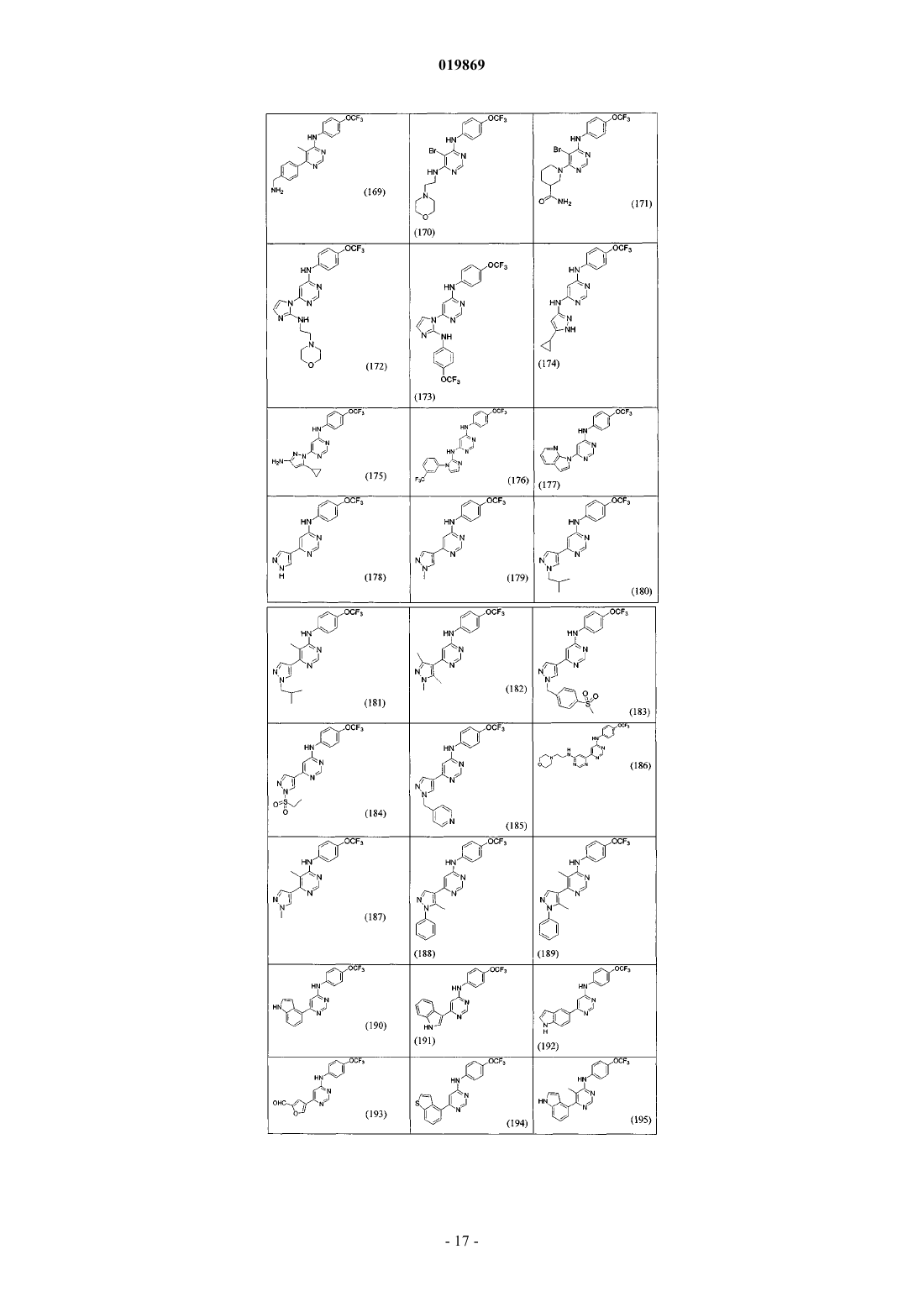
10. Соединение, выбранное из следующих:
4-(6-(4-(трифторметокси)фениламино)-5-метилпиримидин-4-ил)-N-(2-морфолиноэтил)бензамид;
6-(1Н-пирроло[2,3-b]пиридин-1-ил)-N-(4-(трифторметокси)фенил)пиримидин-4-амин;
N-(4-(трифторметокси)фенил)-6-(1,3,5-триметил-1Н-пиразол-4-ил)пиримидин-4-амин;
4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензолсульфонамид;
N-метил-4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензолсульфонамид;
N-этил-4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]бензолсульфонамид;
N-(2-гидроксиэтил)-4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]бензолсульфонамид;
[6-(4-метансульфонилфенил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(4-метансульфонилфенил)-5-метилпиримидин-4-ил]-(4-трифторметоксифенил)амин;
{6-[4-(пропан-2-сульфонил)фенил]пиримидин-4-ил}-(4-трифторметоксифенил)амин;
{5-метил-6-[4-(пропан-2-сульфонил)фенил]пиримидин-4-ил}-(4-трифторметоксифенил)амин;
N,N-диэтил-4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]бензолсульфонамид;
N,N-диэтил-4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензолсульфонамид;
{6-[4-(пиперидин-1-сульфонил)фенил]пиримидин-4-ил}-(4-трифторметоксифенил)амин;
4-метил-N-{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}бензолсульфонамид;
4-метил-N-{4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}бензолсульфонамид;
N-{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}метансульфонамид;
{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}амид этансульфоновой кислоты;
{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}амид бутан-1-сульфоновой кислоты;
{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}амид пропан-2-сульфоновой кислоты;
{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}амид пентан-2-сульфоновой кислоты;
N-(2-гидроксиэтил)-4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензамид;
4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]-N-(2-морфолин-4-ил-этил)бензамид;
N-(3-метоксипропил)-4-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензамид;
N-{3-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}ацетамид;
3-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензамид;
3-[5-метил-6-(4-трифторметоксифениламино)пиримидин-4-ил]бензойная кислота;
(6-бифенил-4-ил-пиримидин-4-ил)-(4-трифторметоксифенил)амин;
(6-бифенил-4-ил-5-метилпиримидин-4-ил)-(4-трифторметоксифенил)амин;
[6-(5-метоксинафталин-2-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(5-метоксинафталин-2-ил)-5-метилпиримидин-4-ил]-(4-трифторметоксифенил)амин;
{3-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}ацетонитрил;
[6-(3-нитрофенил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
4-метокси-N-{4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фенил}бензамид;
[6-(4-аминометилфенил)-5-метилпиримидин-4-ил]-(4-трифторметоксифенил)амин;
5-бром-N-(2-морфолин-4-ил-этил)-N'-(4-трифторметоксифенил)пиримидин-4,6-диамин;
амид 1-[5-бром-6-(4-трифторметоксифениламино)пиримидин-4-ил]пиперидин-3-карбоновой кислоты;
{6-[2-(2-морфолин-4-ил-этиламино)имидазол-1-ил]пиримидин-4-ил}-(4-трифторметоксифенил)амин;
(4-трифторметоксифенил)-{6-[2-(4-трифторметоксифениламино)имидазол-1-ил]пиримидин-4-ил}амин;
N-(5-циклопропил-1Н-пиразол-3-ил)-N'-(4-трифторметоксифенил)пиримидин-4,6-диамин,
[6-(3-амино-5-циклопропилпиразол-1-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
N-(4-трифторметоксифенил)-N'-[1-(3-трифторметилфенил)-1Н-имидазол-2-ил]пиримидин-4,6-диамин;
(6-пирроло[2,3-b]пиридин-1-ил-пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[6-(1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1-метил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин,
[6-(1-изобутил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1-изобутил-1Н-пиразол-4-ил)-5-метилпиримидин-4-ил]-(4-трифторметоксифенил)амин,
(4-трифторметоксифенил)-[6-(1,3,5-триметил-1Н-пиразол-4-ил)пиримидин-4-ил]амин;
{6-[1-(4-метансульфонилбензил)-1Н-пиразол-4-ил]пиримидин-4-ил}-(4-трифторметоксифенил)амин;
[6-(1-этансульфонил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1-пиридин-4-илметил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
N6-(2-морфолин-4-ил-этил)-N6'-(4-трифторметоксифенил)-[4,4']бипиримидинил-6,6'-диамин;
[5-метил-6-(1-метил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(5-метил-1-фенил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[5-метил-6-(5-метил-1-фенил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин,
[6-(1Н-индол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1Н-индол-3-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1Н-индол-5-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]фуран-2-карбальдегид;
(6-бензо[b]тиофен-4-ил-пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[6-(1Н-индол-4-ил)-5-метилпиримидин-4-ил]-(4-трифторметоксифенил)амин;
(6-дибензофуран-4-ил-пиримидин-4-ил)-(4-трифторметоксифенил)амин;
[6-(1-бензил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1-бензил-1Н-пиразол-4-ил)-5-метилпиримидин-4-ил]-(4-трифторметоксифенил)амин;
N6,N6'-бис-(4-трифторметоксифенил)-[4,4']бипиримидинил-6,6'-диамин;
N6-(2-морфолин-4-ил-этил)-N6'-(4-трифторметоксифенил)-[4,4']бипиримидинил-6,6'-диамин;
N-(4-метил-3-{1-[6-(4-трифторметоксифениламино)пиримидин-4-ил]-1Н-имидазол-2-иламино}фенил)бензамид;
N-(4-метил-3-{1-[6-(4-трифторметоксифениламино)пиримидин-4-ил]-1H-имидазол-2-иламино}фенил)-4-морфолин-4-илметил-3-трифторметилбензамид;
[6-(1-пиридин-3-илметил-1Н-пиразол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
[6-(1Н-пирроло[2,3-b]пиридин-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
4-[6-(4-трифторметоксифениламино)пиримидин-4-ил]-1Н-пиридин-2-он;
[6-(2-метилтиазол-4-ил)пиримидин-4-ил]-(4-трифторметоксифенил)амин;
2-фтор-5-[6-(4-трифторметоксифениламино)пиримидин-4-ил]бензальдегид;
{6-[2-(4-метилпиперазин-1-ил)пиридин-4-ил]пиримидин-4-ил}-(4-трифторметоксифенил)амин.
11. Соединение формулы (X) или его фармацевтически приемлемая соль
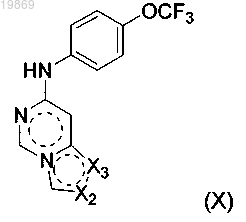
где каждый из Х2 или Х3 независимо представляет собой NR1, CR1, C(O), О или S; каждый R1 независимо выбран из Н; С6-8-арила, возможно замещенного от одного до двух заместителями, независимо выбранными из NO2, OR2 или C(O)NR2; или (CH2)nC3-8-гетероциклоалкила, содержащего два гетероатома, представляющих собой О и N; или отсутствует; R2 представляет собой Н или С1-6-алкил и каждый n независимо равен 0, 1 или 2.
12. Соединение по п.11, формулы (XI)
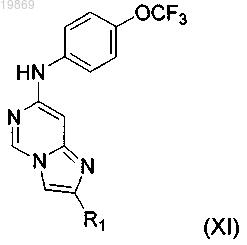
где R1 независимо выбран из Н; С6-8-арила, возможно замещенного от одного до двух заместителями, независимо выбранными из NO2, OR2 или C(O)NR2; R2 представляет собой Н или С1-6-алкил.
13. Соединение по п.12, выбранное из следующих:
2-(3-нитрофенил)-N-(4-(трифторметокси)фенил)имидазо[1,2-с]пиримидин-7-амин;
2-гидрокси-3-[7-(4-трифторметоксифениламино)имидазо[1,2-с]пиримидин-2-ил]бензамид.
14. Фармацевтическая композиция, содержащая соединение по любому из пп.1-13 или его фармацевтически приемлемую соль и фармацевтически приемлемый наполнитель.
15. Композиция по п.14, дополнительно содержащая дополнительный терапевтический агент, представляющий собой ингибитор сайта связывания АТФ.
16. Способ ингибирования киназной активности у субъекта, включающий этап введения указанному субъекту соединения по любому из пп.1-13 или его фармацевтически приемлемой соли, или композиции по любому из пп.14 и 15.
17. Способ лечения расстройства, связанного с киназной активностью, у субъекта, включающий введение указанному субъекту, нуждающемуся в таком лечении, эффективного количества соединения или его фармацевтически приемлемой соли по любому из пп.1-13 или композиции по любому из пп.14 и 15.
18. Способ по любому из пп.16 и 17, отличающийся тем, что соединение является ингибитором киназы.
19. Способ по любому из пп.16-18, отличающийся тем, что соединение взаимодействует с Bcr-abl.
20. Способ по п.19, отличающийся тем, что мишенью указанного соединения является сайт связывания на Bcr-abl.
21. Способ по п.18, отличающийся тем, что указанный субъект идентифицируют как нуждающийся в ингибировании киназы и соединение вводят идентифицированному субъекту.
22. Способ по любому из пп.16 и 17, дополнительно включающий этап идентификации субъекта, нуждающегося в таком лечении расстройства, связанного с киназной активностью, и введение указанного соединения идентифицированному субъекту.
23. Способ по любому из пп.16 и 17, отличающийся тем, что расстройство, связанное с киназной активностью, представляет собой расстройство клеточной пролиферации или заболевание, выбранное из группы, включающей рак, такой как диссеминированный рак; лейкемию, включая хроническую миелоидную лейкемию, множественную миелому или лимфому; опухоль, такую как солидная опухоль; неоплазму, неоваскуляризацию, васкуляризацию, сердечно-сосудистое заболевание, метастаз, инфекцию, тромбоз, атеросклероз, меланому, кожное заболевание, ревматоидный артрит, диабетическую ретинопатию, отек желтого пятна или дегенерацию желтого пятна, воспалительное и артритное заболевание или остеосаркому.
24. Способ по любому из пп.16-21, дополнительно включающий введение дополнительного терапевтического агента, представляющего собой ингибитор сайта связывания АТР.
25. Способ по п.24, отличающийся тем, что ингибитор сайта связывания АТР выбран из следующих: иматиниб, Нилотиниб, Дазатиниб, АР234464, AZD0530 и SKI-606.
26. Способ по любому из пп.16-25, отличающийся тем, что субъект представляет собой млекопитающее, такое как примат или человек.
27. Способ по любому из пп.16-26, отличающийся тем, что этап введения соединения включает введение соединения перорально, парентерально, внутривенно, внутримышечно или местное применение соединения.
28. Способ по любому из пп.16-27, отличающийся тем, что этап введения соединения включает введение соединения в дозе от приблизительно 0,01 мкг/кг/сутки до 100 мг/кг/сутки.
Текст
НИЗКОМОЛЕКУЛЯРНЫЕ МИРИСТАТНЫЕ ИНГИБИТОРЫ ТИРОЗИНКИНАЗЫ BCRABL И СПОСОБЫ ИХ ПРИМЕНЕНИЯ Согласно настоящему изобретению предложены новые гетероарильные соединения, которые связаны с арильной группой через аминогруппу. В частности, предложены соединения общих формул (I), (IX) и (X): где Х 1, Х 2, Х 3, Y, L, A, R3 и m такие, как определено в настоящем описании. Такие соединения применимы для лечения раковых заболеваний.(71)(73) Заявитель и патентовладелец: ДАНА ФАРБЕР КАНСЕР ИНСТИТЬЮТ, ИНК. (US) Заявка испрашивает приоритет на основании предварительной заявки на патент США 61/004462,поданной 28 ноября 2007 года. Полный текст указанной заявки включен в настоящую заявку посредством ссылки. Уровень техники Протеинкиназы представляют собой большое семейство белков, которые играют ключевую роль при регуляции широкого спектра процессов в клетках и поддержании контроля клеточных функций. К таким киназам относятся рецепторные тирозинкиназы, такие как рецепторная киназа тромбоцитарного фактора роста (PDGF-R, ФРТР), рецепторная киназа фактора стволовых клеток, c-Kit и нерецепторные тирозинкиназы, такие как гибридная тирозинкиназа Bcr-abl. Хроническая миелоидная лейкемия (ХМЛ) относится к интенсивно изучаемому раковому заболеванию человека, которое возникает в результате реципрокной транслокации, приводящей к слиянию протоонкогена Abl на 9 хромосоме с геном Bcr на хромосоме 22. Формирующийся в результате гибридный белок Bcr-abl способствует трансформации В-клеток, увеличивая их митогенную активность, снижая чувствительность к апоптотическим факторам и изменяя адгезию и хоуминг клеток-предшественников ХМЛ. STI-571 (Гливек) является ингибитором онкогенной Bcr-abl-тирозинкиназы и используется для лечения хронической миелоидной лейкемии (ХМЛ). Однако некоторые пациенты на стадии бластного криза ХМЛ устойчивы к STI-571 из-за мутаций киназы Bcr-abl. Новые соединения согласно настоящему изобретению ингибируют одну или более киназ, в частности дикий тип и одну или более мутантных форм Bcr-abl, и поэтому могут использоваться для лечения заболеваний, связанных с нарушением киназной активности, в особенности связанных с активностью киназы Bcr-abl. Краткое описание изобретения Согласно одному из аспектов настоящего изобретения предложено соединение формулы I или его фармацевтически приемлемая соль, сольват или гидрат: где каждый из Х 1, Х 2 или Х 3 независимо представляет собой NR1, CR1, C(O), О или S; каждый R1 независимо выбран из Н, возможно замещенного C1-6-алкила, возможно замещенного С 3-12-циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12-арила,возможно замещенного С 3-12-гетероарила, возможно замещенного C1-6-аралкила, возможно замещенногоC1-6-гетероаралкила, возможно замещенного C1-6-галогеналкила, возможно замещенного (CH2)nC3-12 гетероциклоалкила, возможно замещенного (CH2)nC3-12-арила, возможно замещенного (CH2)nC3-12 гетероарила, возможно замещенного (CH2)nC3-12-циклоалкила, C1-6-галогеналкила, С 1-6-аминоалкила, галогена, (CH2)nC(O)Rx, (CH2)nC(O)ORx, (CH2)nC(O)NRxRx, -(CH2)nC(O)NRxRxS(O)2Rx; -C(O)Rx, -C(S)Rx,-C(NR)Rx, -SRx, -S(O)Rx, -S(O)2Rx, -ORx, -NRxRx, нитро, циано или отсутствует; каждый Rx, для каждого случая, независимо представляет собой Н, возможно замещенный C1-6 алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, С 1-6-галогеналкил; NHNHR2 илиm равен 1 или 2; и каждый n независимо равен 0, 1 или 2. Согласно одному варианту реализации настоящего изобретения предложено соединение формулыII или его фармацевтически приемлемая соль, сольват или гидрат:Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, воз-1 019869 можно замещенный С 3-12 циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или C1-6-галогеналкил; и каждый n независимо равен 0, 1 или 2. Согласно другому варианту реализации настоящего изобретения предложено соединение формулыIII или его фармацевтически приемлемая соль, сольват или гидрат:Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или C1-6-галогеналкил; и каждый n независимо равен 0, 1 или 2. Согласно некоторым вариантам реализации настоящего изобретения предложено соединение формулы IV или его фармацевтически приемлемая соль, сольват или гидрат: где каждый R1 независимо выбран из Н, возможно замещенного C1-6-алкила, возможно замещенного С 3-12 циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12 арила, возможно замещенного С 3-12-гетероарила, возможно замещенного C1-6-аралкила, возможно замещенного С 1-6-гетероаралкила, возможно замещенного C1-6-галогеналкила, возможно замещенногоRx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или C1-6-галогеналкил; и каждый n независимо равен 0, 1 или 2. Согласно другому варианту реализации настоящего изобретения предложено соединение формулыV или его фармацевтически приемлемая соль, сольват или гидрат: где R1 независимо выбран из Н, возможно замещенного C1-6-алкила, возможно замещенного С 3-12 циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12-арила, возможно замещенного С 3-12-гетероарила, возможно замещенного (CH2)nC3-12-гетероциклоалкила, -C(O)Rx, ORx, -SRx, -NRxRx, нитро, циано, С 1-6-галогеналкила, С 1-6-аминоалкила, (CH2)nC(O)Rx, (CH2)nC(O)ORx,(CH2)nC(O)NRxRx или -(CH2)nC(O)NRxRxS(O)2Rx;Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, NHNHR2 или C(NH)NH2;Ry для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или C1-6-галогеналкил; каждый n независимо равен 0, 1 или 2; иR2 представляет собой Н или С 1-4-алкил. В другом варианте реализации R1 независимо выбран из Н, возможно замещенного C1-6-алкила,возможно замещенного С 3-12-циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12-арила, возможно замещенного С 3-12-гетероарила, возможно замещенного (CH2)nC3-12 гетероциклоалкила, -C(O)Rx, -ORx, -SRx, -NRxRx, нитро, циано, С 1-6-галогеналкила, C1-6-аминоалкила,(CH2)nC(O)Rx, (CH2)nC(O)ORx, (CH2)nC(O)NRxRx или -(CH2)nC(O)NRxRxS(O)2Rx;Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, NHNHR2 или C(NH)NH2; иR2 представляет собой Н или С 1-4-алкил. В другом дополнительном варианте реализации R1' выбран из Н, возможно замещенного C1-6 алкила, возможно замещенного С 3-12-циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12-арила, возможно замещенного С 3-12-гетероарила, возможно замещенного C1-6 аралкила, возможно замещенного C1-6-гетероаралкила, возможно замещенного C1-6-галогеналкила, возможно замещенного (CH2)nC3-12-гетероциклоалкила, возможно замещенного (CH2)nC3-12-арила, возможно замещенного (CH2)nC3-12-гетероарила, возможно замещенного (CH2)nC3-12-циклоалкила, (CH2)nC(O)Ry,(CH2)nC(O)ORy, (CH2)nC(O)NRyRy, -C(O)Ry, -C(S)Ry, -C(NR)Ry, галогена, С 1-6-галогеналкила, -S(O)Ry илиRy для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или C1-6-галогеналкил; Согласно другим вариантам реализации настоящего изобретения предложено соединение формулыVI или его фармацевтически приемлемая соль, сольват или гидрат: где R1 независимо выбран из Н, возможно замещенного C1-6-алкила, возможно замещенного С 3-12 циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12-арила, возможно замещенного С 3-12-гетероарила, возможно замещенного (CH2)nC3-12-гетероциклоалкила, -C(O)Rx, ORx, -SRx, -NRxRx, нитро, циано, C1-6-галогеналкила, C1-6-аминоалкила, (CH2)nC(O)Rx, (CH2)nC(O)ORx,(CH2)nC(O)NRxRx или -(CH2)nC(O)NRxRxS(O)2Rx;Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12 циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, NHNHR2, C(NH)NH2;R2 представляет собой Н или С 1-4-алкил; и каждый n независимо равен 0, 1 или 2. Согласно другому варианту реализации настоящего изобретения предложено соединение формулыVII или его фармацевтически приемлемая соль, сольват или гидрат:Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, NHNHR2 или C(NH)NH2;m равен 1 или 2; и каждый n независимо равен 0, 1 или 2. Согласно другому варианту реализации настоящего изобретения предложено соединение формулыVIII или его фармацевтически приемлемая соль, сольват или гидрат:Rx независимо для каждого случая представляет собой Н, возможно замещенный C1-6-алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или C1-6-галогеналкил; и каждый n независимо равен 0, 1 или 2. Согласно другому аспекту настоящего изобретения предложено соединение формулы IX или его фармацевтически приемлемая соль, сольват или гидрат:L представляет собой NR3, О, S, S(O), S(O)2, C(O), C(S), C(NR), C(NRx)NRx, C(O)NRx, C(O)NRxNRx,C(O)ONRx, C(O)NRxO, C(O)O, OC(O), OC(O)O или связь; каждый Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6 алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, C1-6-галогеналкил; NHNHR2 илиC(NH)NH2; А представляет собой возможно замещенный C1-6-алкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, возможно замещенный С 3-12-циклоалкил или возможно замещенный С 312-гетероциклоалкил. В одном из вариантов реализации А представляет собой возможно замещенный С 1-6-алкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил или возможно замещенный С 3-12 гетероциклоалкил. В другом варианте реализации настоящего изобретения А представляет собой возможно замещенное фенильное кольцо, возможно замещенное нафтильное кольцо, возможно замещенное пиперидиновое кольцо, возможно замещенное имидазольное кольцо, возможно замещенное пиразольное кольцо, возможно замещенное 1 Н-пиразольное кольцо, возможно замещенное 1 Н-пирроло[2,3-b]пиридиновое кольцо, возможно замещенное пиримидиновое кольцо, возможно замещенное пиразиновое кольцо, возможно замещенное пиридиновое кольцо, возможно замещенное индольное кольцо, возможно замещенное 1 Ниндольное кольцо, возможно замещенное фурановое кольцо, возможно замещенное бензо[b]тиофеновое кольцо, возможно замещенное дибензофурановое кольцо, возможно замещенное 1 Н-пиридин-2-оновое кольцо, возможно замещенное тиазольное кольцо или этильную группу. В другом варианте реализации настоящего изобретения А возможно замещен C1-6-алкилом, C2-6 алкенилом, С 2-6-алкинилом, С 3-12-циклоалкилом, С 3-12-гетероциклоалкилом, С 3-14-аралкилом, С 3-14 гетероаралкилом, С 3-12-арилом, (СН 2)рС 3-12-арилом, С 3-12-гетероарилом, (СН 2)рС 3-12-гетероарилом, галогеном, галогеналкилом, циано, (CH2)pCN, нитро, C1-6-алкокси, С 3-12-арилокси, С 1-С 4-галогеноалкокси, C1 С 6-галогеналкилом, гидроксилом, C1-6-гидроксилалкилом, C1-6-карбоксилом, СНО, амино, аминоалкилом,диалкиламино, OR15, SR15, NR17R17C(O)OR15, C(O)NR15R16, OC(O)NRI5R16, NR15C(O)NR15R16,NR17S(O)2R15, NR17(CH2)nR17, C(O)R17, C(O)NR17R17, NR15C(O)R17, S(O)R17, S(O)2R17 или S(O)2NR17R17; каждый R15 независимо представляет собой водород, С 3-14-аралкил, C1-6-алкил, С 3-12-циклоалкил, С 312-арил, С 3-12-гетероциклоалкил или С 3-12-гетероарил; каждый R16 независимо представляет собой водород, С 3-14-аралкил или C1-6-алкил; каждый R17 независимо представляет собой Н, C1-6-алкил, C1-6-гидроксиалкил, С 1-6-алкокси, С 3-12 циклоалкил, С 3-12-арил, С 3-12-гетероарил, С 3-12-гетероциклоалкил, гидроксил, или каждый R17 может образовывать гетероциклоалкильное кольцо с другим R17; где каждый A, R15, R16 и R17 может быть дополнительно возможно замещен C1-6-алкилом, C1-6 алкокси, C1-6-галогеноалкокси, С 3-12-гетероциклоалкилом, амино, галогеном, C1-6-галогеналкилом, SO2 алкилом или NHC(O)-арилом; и каждый р независимо равен от 0 до 6. Согласно другому аспекту настоящего изобретения предложено соединение формулы X или его фармацевтически приемлемая соль, сольват или гидрат: где каждый из Х 2 или Х 3 независимо представляет собой NR1, CR1, C(O), О или S; каждый R1 независимо выбран из Н, возможно замещенного C1-6-алкила, возможно замещенного С 312-циклоалкила, возможно замещенного С 3-12-гетероциклоалкила, возможно замещенного С 3-12-арила,возможно замещенного С 3-12-гетероарила, возможно замещенного C2-6-аралкила, возможно замещенного С 2-12-гетероаралкила, возможно замещенного C1-6-галогеналкила, возможно замещенного (CH2)nC3-12 арила, возможно замещенного (CH2)nC3-12-гетероарила, возможно замещенного (CH2)nC3-12-циклоалкила,возможно замещенного (CH2)nC3-12-гетероциклоалкила, C1-6-галогеналкила, С 1-6-аминоалкила, галогена,(CH2)nC(O)Rx, (CH2)nC(O)ORx, (CH2)nC(O)NRxRx, -(CH2)nC(O)NRxRxS(O)2Rx; -C(O)Rx, -C(S)Rx, -C(NR)Rx,-SRx, -S(O)Rx, -S(O)2Rx, -ORx, -NRxRx, нитро, циано или отсутствует; каждый Rx для каждого случая независимо представляет собой Н, возможно замещенный C1-6 алкил, возможно замещенный С 3-12-циклоалкил, возможно замещенный С 3-12-гетероциклоалкил, возможно замещенный С 3-12-арил, возможно замещенный С 3-12-гетероарил, C1-6-галогеналкил; NHNHR2 илиR2 представляет собой Н или C1-6-алкил; и каждый n независимо равен 0, 1 или 2. Согласно одному из вариантов реализации настоящего изобретения предложено соединение формулы XI или его фармацевтически приемлемая соль, сольват или гидрат: где R1 независимо выбран из Н, возможно замещенного C1-6-алкила, возможно замещенного С 3-12 арила или возможно замещенного С 3-12-гетероарила. Согласно некоторым аспектам настоящего изобретения предложен способ лечения заболевания субъекта, при котором ингибирование киназной активности, в особенности активности Bcr-abl, может способствовать предотвращению, устранению или облегчению патологического течения и/или симптомов определенных расстройств и/или заболеваний, при этом указанный способ лечения заключается во введении субъекту терапевтически эффективного количества соединения согласно изобретению или его фармацевтически приемлемой соли, сольвата или гидрата. Согласно одному из аспектов настоящего изобретения предложен способ лечения расстройств субъекта, связанных с киназной активностью, включающий введение нуждающемуся субъекту эффективного количества любого соединения или фармацевтически приемлемой соли, сольвата или гидрата из соединений, описанных в данной заявке. В некоторых вариантах реализации настоящего изобретения указанное соединение является ингибитором киназы. В другом варианте реализации соединение взаимодействует с Bcr-abl. В другом дополнительном варианте реализации мишенью для соединения является сайт связывания на Bcr-abl. В другом варианте реализации указанный субьект идентифицируют как нуждающийся в ингибировании киназной активности и вводят указанное соединение согласно настоящему изобретению указанному идентифицированному субъекту. Согласно еще одному варианту реализации настоящего изобретения предложен способ, дополнительно включающий этап идентификации субъекта, нуждающегося в подобном лечении расстройства,связанного с киназной активностью, и введения соединения указанному идентифицированному субъекту. Согласно другим вариантам реализации настоящего изобретения предложен способ лечения субъекта, страдающего от расстройства клеточной пролиферации или заболевания, связанного с клеточной пролиферацией. В другом варианте реализации настоящего изобретения заболевание представляет собой рак, опухоль, неоплазму, неоваскуляризацию, васкуляризацию, сердечно-сосудистое заболевание, метастаз, инфекцию, тромбоз, атеросклероз, меланома, кожное заболевание, ревматоидный артрит, диабетическую ретинопатию, отек желтого пятна или дегенерацию желтого пятна, воспалительное заболевание или заболевание, связанное с артритом, или остеосаркому. Еще в одном варианте субъект страдает от солидной опухоли или диссеминированного рака. В другом дополнительном варианте реализации рак представляет собой лейкемию, множественную миелому или лимфому. В некоторых вариантах лейкемия представляет собой хроническую миелоидную лейкемию. Согласно другому аспекту настоящего изобретения предложен способ лечения рака у субъекта,включающий введение указанному субъекту эффективного количества любого соединения или его фармацевтически приемлемой соли, сольвата или гидрата, из соединений, описанных в данной заявке. Согласно одному из вариантов реализации настоящего изобретения предложен способ, описанный выше, дополнительно включающий введение дополнительного терапевтического агента. В другом варианте реализации изобретения дополнительный терапевтический агент представляет собой ингибитор сайта связывания АТФ. В другом дополнительном варианте реализации ингибитор сайта связывания АТФ выбран из следующих: Иматиниб (STI571), Нилотиниб (AMN107), Дазатиниб (BMS-354825),АР 234464 (Ariad Pharmaceuticals), AZD0530 (Astrazeneca) и SKI-606 (Wyeth). В другом варианте реализации настоящего изобретения указанный субъект представляет собой млекопитающее. В другом варианте реализации субъект представляет собой примата или человека. Согласно одному из вариантов реализации настоящего изобретения предложен способ, в котором этап введения соединения включает введение соединения перорально, местно, парентерально, внутривенно или внутримышечно. В другом варианте реализации способ согласно настоящему изобретению включает этап введения эффективного количества композиции, содержащей соединение согласно изобретению и фармацевтически приемлемый наполнитель. В некоторых вариантах реализации этап введения соединения включает введение соединения согласно настоящему изобретению в дозе примерно от 0,01 мкг/кг в день до 100 мг/кгв день. Согласно другому аспекту настоящего изобретения предложен способ ингибирования киназной активности у субъекта, включающий этап введения субъекту любого соединения или его фармацевтически приемлемой соли, сольвата или гидрата из описанных в данной заявке соединений. Согласно другим аспектам настоящего изобретения предлагожено применение описанных в данной заявке соединений для производства лекарственного состава, предназначенного для лечения заболевания субъекта, патологическое течение и/или симптомы которого связаны с киназной активностью, в особенности активностью Bcr-abl. Согласно другиме аспектам настоящего изобретения предложена фармацевтическая композиция,содержащая любое из описанных в данной заявке соединений или его фармацевтически приемлемую соль, сольват или гидрат. Согласно одному из вариантов реализации настоящего изобретения предложена композиция, дополнительно содержащая дополнительный терапевтический агент. В другом варианте реализации указанный дополнительный терапевтический агент представляет собой ингибитор сайта связывания АТФ. Еще в одном варианте реализации ингибитор сайта связывания АТФ выбран из следующих: Иматиниб (STI571), Нилотиниб (AMN107), Дазатиниб (BMS-354825), АР 234464 (Ariad Pharmaceuticals), AZD0530 (Astrazeneca) и SKI-606 (Wyeth). Согласно некоторым аспектам настоящего изобретения предложен набор, содержащий эффективное количество описанного в данной заявке соединения, или его фармацевтически приемлемой соли,сольвата или гидрата, в дозированной форме, наряду с инструкциями для введения указанного соединения субъекту, страдающему нарушением клеточной пролиферации или имеющему предрасположенность к указанному нарушению. Согласно некоторым аспектам настоящего изобретения предложен способ ингибирования активности Bcr-abl, включающий взаимодействие Bcr-abl с соединением согласно изобретению, которое связывается с сайтом (карманом) связывания остатка миристиновой кислоты на Bcr-abl. Согласно одному из аспектов настоящего изобретения предложен способ идентификации соединения, которое модулирует киназную активность Bcr-abl, включающий: а) взаимодействие Bcr-abl с соединением в условиях, подходящих для модуляции киназной активности Bcr-abl; иb) определение способности соединения модулировать киназную активность Bcr-abl; при этом указанное соединение способно взаимодействовать с сайтом связывания остатка миристновой кислоты на Bcr-abl. В одном варианте реализации изобретения настоящего изобретения взаимодействие соединения с сайтом связывания остатка миристиновой кислоты на Bcr-abl является связывающим взаимодействием. В другом варианте реализации связывающее взаимодействие представляет собой ионное, ковалентное или непрямое взаимодействие. Еще в одном варианте реализации соединение согласно изобретению имеет связывающее взаимодействие с Ala452, Tyr454, Glu481, Pro484, Val487, Phe516, Ile521 или Val525(нумерация основана на кристаллической структуре с кодом банка данных о белках: 1OPL, источник:Nagar, В., Hantschel, О., Young, M.A., Scheffzek, K., Veach, D., Bornmann, W., Clarkson, В., Superti-Furga,G., Kuriyan, J. Structural basis for the autoinhibition of c-Abl tyrosine kinase Cell (Cambridge, Mass.), v112,pp. 859-871, 2003. В других вариантах реализации способность соединения согласно изобретению модулировать киназную активность определяется прямым связыванием соединения с сайтом связывания остатка миристиновой кислоты на Bcr-abl. В другом варианте реализации соединение согласно изобретению создают de novo. В других вариантах реализации соединение согласно изобретению создается на основе известного лиганда сайта связывания остатка миристиновой кислоты на Bcr-abl. Подробное описание изобретения Соединения согласно сзобретению Примеры соединений согласно настоящему изобретению включают следующие соединения, структуры которых представлены в табл. 1-9. 2-(4-(4-(Трифторметокси)фениламино)-1 Н-пиразоло[3,4-d]пиримидин-1-ил)этанол (1); Синтез соединений согласно изобретению Соединения формул II и III получали в результате двухстадийной реакции. Сначала проводили реакцию сочетания хлорсодержащего гетероарильного соединения с замещенным галогеналкоксипроизводным анилина в основных условиях. Получившееся в результате соединение затем обрабатывали производным гидразина для получения смеси соединений формул II и III, которые разделяли с помощью метода хроматографии (схема 1). Альтернативно, добавляли гидразин с последующим добавлением электрофильного соединения в основных условиях, получая соединения формул II и III. Схема 1 Соединения формул IV и V получали посредством реакции галогенированного конденсированного бициклического гетероарильного соединения с возможно замещенной хлорсодержащей алкильной группой при основных условиях. Полученный в результате замещенный амин вводили в реакцию сочетания по положению хлора гетероарила с производным анилина с получением соединений формул IV или V(схема 2). Схема 2 также предполагает модификацию функциональной группы боковой цепи замещенного амина для получения разнообразно замещенных соединений согласно изобретению. Схема 2 Согласно схеме 3 предложен синтетический способ получения соединений формул V и VI. Гетероарильное соединение со смежными заместителями: хлором и альдегидной группой, вводили в реакцию с производным замещенного тиола или производным вторичного амина для получения конденсированного бициклического каркаса соединений формул V и VI. Дополнительные модификации функциональных групп проводили для получения соединений согласно изобретению. Схема 3 Соединения формулы VII получали путем сочетания галогенированного конденсированного бициклического гетероарильного соединения с замещенным производным анилина. Дополнительные модификации функциональной группы боковой цепи проводили для получения соединений формулы VII (схема 4). Схема 4 Соединения формулы IX синтезировали путем сочетания на первом этапе дигалогенированного гетероарильного соединения с производным анилина и последующего сочетания в условиях реакции Митцуноби для получения соединений формулы IX. Альтернативно, на втором этапе вторая группа галогена гетероарильного кольца замещалась нуклеофильной группой при основных условиях для получения соединения формулы IX (схема 5). Схема 5 В добавление к схеме 5, соединения формулы IX также получали в результате реакций, представленных на схеме 6, при этом продукт сочетания на первом этапе дополнительно подвергали реакции сочетания в условиях Митсуноби с гетероарильной группой, которую далее подвергали модификации функциональной группы. Схема 6 Арилзамещенные конденсированные бициклические соединения формулы X синтезировали в соответствии со схемой 7. Гетероарильное соединение, замещенное галогеном и аминогруппой, вводили в реакцию с альфа-галогенкарбонильным соединением, что позволило получить бициклическое гетероарильное соединение. Последующее сочетание с производным анилина позволило получить соединение формулы X. Схема 7 Кислоты и основания, используемые при реализации способов согласно изобретению, известны в данной области. Кислотные катализаторы представляют собой любой кислые реагенты, который может иметь как неорганическую природу (например, соляная, серная, азотная кислоты, треххлористый алюминий), так и органическую (например, камфорсульфоновая кислота, п-толуолсульфоновая кислота, уксусная кислота, трифлат иттербия). Кислоты используются либо в каталитических, либо в стехиометрических количествах для ускорения химических реакций. Основания представляют собой любой основной реагент, который может иметь как неорганическую природу (например, бикарбонат натрия, гидроксид калия), так и органическую (например, триэтиламин, пиридин). Основания используются либо в каталитических, либо в стехиометрических количествах для ускорения химических реакций. Соединения согласно изобретению определяются в данной заявке согласно их химическим структурам и/или химическим названиям. В случае несоответствия между химической структурой и химическим названием соединения (при наличии в заявке и того, и другого) химическая структура является определяющей для идентификации соединения. Изобретение предусматривает только те комбинации заместителей и переменных, которые приводят к образованию стабильных соединений. Термин "стабильный" при использовании в данной заявке относится к соединениям, которые обладают достаточной стабильностью для возможности их производства и поддерживают свою целостность в течение периода времени, достаточного для применения указанных соединений в целях, предусмотренных настоящим изобретением (например, включения в состав терапевтических составов, использования в качестве промежуточных продуктов при производстве терапевтических соединений, изолируемых или не изолируемых промежуточных продуктов, лечения или предотвращения расстройств, описанных в данной заявке). Соединения, полученные способами согласно изобретению, могут быть включены в композиции, такие как растворы, капсулы, кремы или мази для их применения субъектом (например, человеком, животным). Такие композиции (например, фармацевтические составы) применяются субъектом для достижения желаемого уровня здоровья или другого благоприятного физиологического эффекта, связанного с подобными соединениями. Нуклеофильные агенты, известные в данной области, описаны в книгах и статьях по химии, включенных в данную заявку посредством ссылок. Химические реагенты, используемые в вышеуказанных способах, могут включать, например, растворители, реагенты, катализаторы, реагенты, содержащие защитные группы и открывающие группы и т.д. Способы, описанные выше, могут также дополнительно включать этапы, либо предшествующие, либо последующие стадиям, детально описанным в данной заявке, и заключающиеся в добавлении или удалении подходящих защитных групп для того, чтобы в итоге обеспечить синтез соединений в соответствии с формулами, описанными в данной заявке. Способы, описанные в данной заявке, предусматривают превращение соединений одной формулы в соединения дру- 20019869 гой формулы. Способ превращения относится к одной или более химическим трансформациям, которые могут быть проведены in situ или путем выделения промежуточных соединений. Такие трансформации могут включать реакцию исходных соединений или промежуточных продуктов с дополнительными реагентами при использовании технологий и методов, известных в данной области, описанных в том числе в ссылках, включенных в данную заявку. Промежуточные продукты могут быть применены после их очистки (например, фильтрации, дистилляции, кристаллизации, хроматографии) или без нее. Другие варианты относятся к промежуточным соединениям, рассмотренным в данной заявке, и их применению в способах (например, лечения, синтеза), описанных в данной заявке. Способы лечения Соединения согласно настоящему изобретению в свободной форме или форме фармацевтически приемлемой соли проявляют важные фармакологические свойства, как показано, например, в результате исследований in vitro, описанных далее в разделе "Анализы", и поэтому показаны для лечения заболеваний и расстройств, связанных с активностью Bcr-abl. Для Bcr-abl соединения согласно настоящему изобретению предпочтительно имеют IC50 в пределах от 110-10 до 110-5 M, предпочтительно менее чем 1 мкМ для дикого типа Bcr-abl и по меньшей мере двух других мутантов Bcr-abl (мутантов, выбранных изG250E, E255V, T315I, F317L и М 351 Т). Согласно настоящему изобретению также предложен способ предотвращения или лечения заболеваний или состояний, сопровождающихся нарушениями роста клеток у субъекта, включая человека,причем указанный способ включает введение субъекту соединения согласно настоящему изобретению в количестве, эффективном для подавления активности ФРТР, c-Kit и/или Bcr-abl. ФРТ (фактор роста тромбоцитов, PDGF) является распространенным фактором роста, который играет важную роль как при нормальном росте клеток, так и при такой патологической пролиферации клеток, которая наблюдается при канцерогенезе и заболеваниях гладкомышечных клеток кровеносных сосудов, например, при атеросклерозе и тромбозе. Соединения согласно изобретению могут подавлять ФРТР и поэтому также подходят для лечения опухолевых заболеваний, описанных далее. Соединения согласно настоящему изобретению также подавляют клеточные процессы с участием фактора стволовых клеток (ФСК, также известного как лиганд c-kit или фактор steel), такие как автофосфорилирование рецептора ФСК (kit) и активацию киназы МАПК (митоген-активируемой протеинкиназы), которая стимулируется ФСК. Соединения согласно настоящему изобретению, таким образом, ингибируют также автофосфорилирование рецептора ФСК (и протоонкогена c-kit). Линия клеток М 07 е представляет собой клетки мегакариобластного лейкоза человека, пролиферация которых зависит от ФСК. Соединения согласно настоящему изобретению подавляют автофосфорилирование ФСКР в микромолярных концентрациях. Активность киназы abl, особенно киназы v-abl, также ингибируют соединения согласно настоящему изобретению. Аналогично, соединения согласно настоящему изобретению также ингибируют киназуBcr-abl и, таким образом, подходят для лечения Bcr-abl-положительных раковых и опухолевых заболеваний, таких как лейкемии (особенно хроническая миелоидная лейкемия и острая лимфобластная лейкемия, при которых особо задействованы апоптотические механизмы), а также оказывают влияние на подгруппу лейкемических стволовых клеток, что предполагает также возможность очистки стволовых клеток in vitro от названных клеток (например, при удалении костного мозга) и реимплантации стволовых клеток, очищенных от раковых (например, реимплантация очищенных клеток костного мозга). Кроме того, согласно настоящему изобретению предложен способ подавления активности Bcr-abl,заключающийся во взаимодействии Bcr-abl с соединением согласно изобретению, которое связывается с сайтом связывания остатка миристиновой кислоты на Bcr-abl. Кроме того, соединения согласно настоящему изобретению могут использоваться в комбинации с другими противоопухолевыми агентами. Лечение заболеваний Термин "опухоль" используется для описания ненормального клеточного роста в ткани, вызванного ускоренной клеточной пролиферацией по сравнению с нормальной тканью и продолжающимся ростом после подавления ростовых факторов. Для опухоли в целом характерно частичное или полное отсутствие структурной организации и функциональной координации с нормальной тканью и, как правило, формирование обособленной массы ткани, которая может быть доброкачественной (доброкачественная опухоль) или злокачественной (карцинома). Опухоли обычно обильно снабжаются кровеносными сосудами. Термин "рак" используется в данной заявке как общий термин для описания злокачественных опухолей или карцином. Такие злокачественные опухоли могут внедряться в окружающие ткани, могут метастазировать к некоторым участкам тела, имеют способность рецидивировать после попытки их удаления и вызывают смерть пациента, несмотря на проведение адекватного лечения. При использовании в данной заявке термины карцинома и рак объединены термином опухоль. Заболевания или расстройства, которые можно вылечить, облегчить или предотвратить с помощью настоящего изобретения, включают: саркомы, неоплазию, злокачественные заболевания внутренних органов, такие как рак глаза, рак прямой кишки, рак толстой кишки, рак шейки матки, рак простаты, рак груди и рак мочевого пузыря, доброкачественные и злокачественные опухоли, включающие различные раковые заболевания, такие как рак анального канала или полости рта, желудка, прямой кишки, печени,поджелудочной железы, легких, шейки матки, тела матки, яичников, предстательной железы, яичек, почек, ротовой полости/глотки, пищевода, гортани, почек, мозга/ЦНС (например, глиомы), головы и шеи,горла, кожную меланому, острый лимфолейкоз, острый миелоидный лейкоз, саркому Юинга, саркому Капоши, карциному базальных клеток и эпидермоидную карциному, мелкоклеточный рак легких, хориокарциному, рабдомиосаркому, ангиосаркому, гемангиоэндотелиому, опухоль Вильмса, нейробластому,лимфому, нейрофиброматоз, туберозный склероз (каждое из которых вызывает доброкачественные опухоли кожи), гемангиомы, лимфангиогенез, рабдомиосаркомы, ретинобластомы, остеосаркомы, акустическую невриному, нейрофиброму, трахому, пиогенные гранулемы, раковые заболевания крови, такие как лейкемии, любые из различных острых или хронических неопластических заболеваний костного мозга,при которых происходит неограниченная пролиферация белых кровяных телец, обычно сопровождающаяся анемией, нарушением свертываемости крови и увеличением лимфатических узлов, печени и селезенки, псориаз, акнэ, розацеа, бородавки, экзему, нейрофиброматоз, синдром Стерджа-Вебера, венозные язвы кожи, туберозный склероз, хронические воспалительные заболевания, артриты, волчанку, склеродерму, диабетическую ретинопатию, ретролентальную фиброплазию, отторжение трансплантанта роговицы, неоваскулярную глаукому и ретролентальную фиброплазию, эпидемический кератоконъюнктивит,дефицит витамина А, расстройства, связанные с неправильным ношением контактных линз, атопический кератит, кератит верхних конечностей, птеригиум, сухой кератит, синдром Шергена, фликтенулезный конъюнктивит, сифилис, микобактериальные инфекции, деградацию липидов, химические ожоги, бактериальные поражения, грибковые поражения, инфекцию простого герпеса, вирус опоясывающего герпеса,инфекцию простейшими, разъедающую язву роговицы Мурена, краевую дегенерацию Терриена, краевой кератолизис, травму, ревматоидный артрит, системную волчанку, множественный артериит, саркоидоз Вегенера, склерит, болезнь Стивенса-Джонсона, пемфигоит, радиальную кератотомию, отторжение трансплантанта роговицы, диабетическую ретинопатию, макулярную эдему, дегенерацию желтого пятна,серповидноклеточную анемию, саркоид, эластичную псевдоксантому, болезнь Педжета, закупорку вен,артериальную закупорку, обструктивное заболевание сонной артерии, хронический увеит/витреит, болезнь Лайма, системную красную волчанку, болезнь Илза, болезнь Бехчета, инфекции, вызывающие ретинит или хороидит, синдром предполагаемого гистоплазмоза глаз, болезнь Беста, миопию, ямку диска зрительного нерва, болезнь Штадгарта, периферический увеит, хроническую отслойку сетчатки, синдромы повышенной вязкости крови, токсоплазмоз, травму, осложнения после лазерной терапии, покраснение радужки (неоваскуляризация радужки), заболевания, вызванные аномальной пролиферацией клеток сосудисто-волокнистой или волокнистой соединительной ткани, включающие все формы пролиферативной витреоретинопатии, ассоциированной или неассоциированной с диабетом, неоваскулярные заболевания, паннус, диабетический отек желтого пятна, сосудистую ретинопатию, дегенерацию сетчатки, воспалительные заболевания сетчатки, пролиферативную витреоретинопатию, заболевания, связанные с покраснением радужки (неоваскуляризацией радужки), заболевания, вызванные аномальной пролиферацией сосудисто-волокнистой или волокнистой соединительной ткани, включающие все формы пролиферативной витреоретинопатии, болезнь Крона и неспецифический язвенный колит, саркоидоз, остеоартрит, воспалительные заболевания пищеварительного тракта, кожные повреждения, болезнь РандюВебера-Ослера, или наследственную геморрагическую телеангиэктазию, остеоартрит, саркоидоз, кожные повреждения, синдром приобретенного иммунодефицита и непроходимость тонкой кишки. В частном варианте реализации настоящего изобретения подавление киназной активности Bcr-abl является важным аспектом настоящего изобретения. Более конкретно, настоящее изобретение относится к способам лечения раковых заболеваний, в том числе хронической миелоидной лейкемии, включающим воздействие на раковые клетки ингибующим или терапевтически эффективным количеством или концентрацией по меньшей мере одного из описанных соединений. Указанный способ может использоваться в терапевтических целях для сравнительных анализов, таких как определение связывающей активности аналогов и определение чувствительности рака пациентов к одному или более соединениям согласно настоящему изобретению. Соединения согласно настоящему изобретению, подавляющие киназную активность, применяют для лечения, облегчения или предотвращения, среди других заболеваний, доброкачественных и злокачественных опухолей, включая различные раковые заболевания, такие как хроническая миелоидная лейкемия, рак шейки, анального отверстия и ротовой полости, желудка, толстой кишки, мочевого пузыря,прямой кишки, печени, поджелудочной железы, легкого, груди, шейки матки, тела матки, яичников,предстательной железы, яичек, почек, мозга/ЦНС (например, глиомы), головы и шеи, глаза, горла, кожная меланома, острый лимфолейкоз, острая миелогенная лейкемия, саркома Юинга, саркома Капоши,карцинома базальных клеток и эпидермоидная карцинома, мелкоклеточный рак легких, хориокарцинома,рабдомиосаркома, ангиосаркома, гемангиоэндотелиома, опухоль Вильмса, нейробластома, рак ротовой полости/глотки, пищевода, гортани, почек и лимфома. Кроме того, такие патологические состояния, как нейрофиброматоз, туберозный склероз (каждое из которых вызывает доброкачественные опухоли кожи),гемангиомы, лимфоангиогенез и другие, можно эффективно лечить с помощью соединений согласно настоящему изобретению. Соединения согласно настоящему изобретению могут быть применены для лечения незлокачественных пролиферативных расстройств, таких как атеросклероз, тромбоз, псориаз, склеродермия и фиброз, а также для защиты стволовых клеток, например от гемотоксического эффекта химиотерапевтических агентов, таких как 5-флуороурацил, и при астме. Соединения согласно настоящему изобретению могут быть особенно пригодны для лечения заболеваний, которые реагируют на подавление ФРТР киназы. Способы лечения, облегчения или предотвращения кожных заболеваний, таких как псориаз, акне,розацеа, бородавки, экзема, гемангиомы, нейрофиброматоз, синдром Стерджа-Вебера, венозные язвы кожи, туберозный склероз, хроническое воспалительное заболевание и артрит, наряду с такими воспалительными заболеваниями, как хроническое воспалительное заболевание, включая артриты, волчанку и слеродермию, также рассматриваются в настоящем изобретении, такие способы включают введение терапевтически эффективного количества одного или более из описанных соединений субъекту, нуждающемуся в таком лечении. Заболевания, связанные с неоваскуляризацией, включают неоваскуляризацию диска зрительного нерва, неоваскуляризацию радужной оболочки, неоваскуляризацию сетчатки, неоваскуляризацию хороидеи, неоваскуляризацию роговицы и неоваскуляризацию стекловидного тела. Заболевания, связанные с неоваскуляризацией роговицы и неоваскуляризацией сетчатки/хороидеи,которые можно вылечить, облегчить или предотвратить согласно настоящему изобретению, включают,но не ограничиваются перечисленными: диабетическую ретинопатию, ретинопатию недоношенных, отторжение трансплантанта роговицы, неоваскулярную глаукому и ретролентальную фиброплазию, эпидемический кератоконъюнктивит, дефицит витамина А, расстройства, связанные с неправильным ношением контактных линз, атопический кератит, кератит верхних конечностей, сухой кератоконъюнктивит,синдром Шегрена, розацеа, фликтенулезный конъюнктивит, сифилис, микобактериальную инфекцию,деградацию липидов, химические ожоги, бактериальные поражения, грибковые поражения, инфекцию простого герпеса, вирус опоясывающего герпеса, инфекцию, вызванную простейшими, саркому Капоши,разъедающую язву Морена, краевую дегенерацию Терриена, краевой кератолизис, травму, ревматоидный артрит, системную волчанку, полиартериит, гранулематоз Вегенера, склерит, болезнь СтивенсаДжонсона, пемфигоид, радиальную кератотомию, отек желтого пятна, дегенерацию желтого пятна, серповидноклеточную анемию, саркоид, сифилис, эластическую псевдосаркому, болезнь Педжета, закупорку вен, артериальную закупорку, обструктивное поражение сонных артерий, хронический увеит/витриит,микобактериальную инфекцию, болезнь Лайма, системную красную волчанку, ретинопатию недоношенных, болезнь Илза, болезнь Бехчета, инфекции, вызывающие ретинит или хореоидит, синдром предполагаемого гистоплазмоза глаз, врожднную дегенерацию желтого пятна, миопию ямки зрительного нерва,дегенерацию жлтого пятна Штаргардта, промежуточный увеит, хроническую отслойку сетчатки, синдром повышенной вязкости крови, токсоплазмоз, травму и остожнения после лазерной терапии. Другие заболевания включают, но не ограничиваются, заболеваниями, связанными с покраснением радужки (неоваскуляризацией радужки), заболеваниями, вызванными ненормальнымми пролиферацией клеток сосудисто-волокнистой и волокнистой соединительной ткани, включающими все формы пролиферативной витреоретинопатии, связанной или нет с диабетом, и отторжение трансплантанта роговицы. Заболевания, связанные с хроническим воспалением и артритом, можно лечить, смягчать или предотвращать с помощью составов и способов согласно настоящему изобретению. Заболевания и симптомы хронического воспаления включают воспалительные заболевания пищеварительного тракта, такие как болезнь Крона и неспецифический язвенный колит, псориаз, саркоидоз, ревматоидный артрит, остеоартрит, волчанка и скеродермия. Кроме того, соединения согласно настоящему изобретению оказывают благоприятное действие при лечении расстройств, возникающих в результате трансплантации, например, аллогенной трансплантации,в особенности отторжения ткани, в частности облитерирующего бронхиолита (ОБ), т.е. хронического отторжения аллогенных легочных трансплантатов. В отличие от пациентов без ОБ, у пациентов с ОБ часто выявляется завышенная концентрация ФРТ в бронхоальвеолярной жидкости. Возможны синергические эффекты с другими иммуномодулирующими или противовоспалительными веществами, например при использовании в комбинации с циклоспорином, рапамицином или аскомицином, или их иммуносупрессорными аналогами, например, циклоспорином A (CsA), циклоспорином G, FK-506, рапамицином или подобными соединениями, кортикостероидами, циклофосфамидом, азатиоприном, метотрексатом, бреквинаром, лефлуномитом, мизорибиномом, микофенольной кислотой, мофетила микофенолатом, 15-дезоксиспергуалином, иммуносупрессорными антителами, особенно моноклональными антителами к рецепторам лейкоцитов, например, МНС, CD2, CD3, CD4, CD7, CD25, CD28, В 7, CD45, CD58 или их лигандам, или другими иммуномодулирующими соединениями, такими как CTLA41g. Соединения согласно настоящему изобретению также эффективны для лечения заболеваний, связанных с миграцией и пролиферацией гладкомышечных клеток сосудов (при которых ФРТ и ФРТР часто также играют роль), таких как рестеноз и атеросклероз. Фармацевтические композиции Фармацевтические композиции и формы дозирования согласно настоящему изобретению содержат один или более активных ингредиентов, описанных в данной заявке. Фармацевтические композиции и формы дозирования согласно изобретению, как правило, также включают один или более фармацевтически приемлемых наполнителей или разбавителей. Термин "фармацевтически приемлемый" при использовании в данной заявке относится к компоненту, который согласно обоснованному медицинскому заключению подходит для использования при контакте с тканями человека и других млекопитающих и не проявляет неспецифической токсичности, не вызывает раздражения, аллергической реакции и т.д., его применение имеет благоприятное соотношение пользы/риска. Термин "фармацевтически приемлемая соль" обозначает любую нетоксичную соль, которая при введении реципиенту способна образовывать, напрямую или не напрямую, соединение или пролекарство соединения согласно настоящему изобретению. "Фармацевтически приемлемый противоион" представляет собой ионную часть соли, которая не является токсичной при высвобождении ее из соли после введения реципиенту. Согласно настоящему изобретению также предложены композиции, содержащие эффективное количество соединения согласно настоящему изобретению и приемлемый носитель. Предпочтительно рецептура композиции согласно изобретению разработана для фармацевтического применения ("фармацевтическая композиция") с фармацевтически приемлемым носителем. Носитель (носители) должен быть "приемлемым" с точки зрения его совместимости с другими компонентами состава и, в случае фармацевтически приемлемого носителя, безвредным для реципиента в количествах, обычно используемых в лекарственных препаратах. Фармацевтически приемлемые носители, адъюванты и наполнители, которые могут быть пригодными для фармацевтических композиций согласно настоящему изобретению, включают ионообменники,оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как человеческий сывороточный альбумин, буферные основы, такие как фосфаты, глицин, сорбиновую кислоту, сорбат калия, частично глицеридные смеси насыщенных растительных жирных кислот, воду, соли или электролиты, такие как протаминсульфат, гидрофосфат натрия, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный оксид кремния, трисиликат магния, поливинилпирролидон, соединения на основе целлюлозы, полиэтиленгликоль, карбоксиметилцеллюлозу натрия, полиакрилаты, воски, полиэтилен-полиоксипропиленблок-полимеры, полиэтиленгликоль и ланолин, но не ограничиваются перечисленными. Как правило, фармацевтические композиции и формы дозирования содержат один или более наполнителей. Подходящие наполнители хорошо известны специалистам в области фармацевтики, и неорганичивающие примеры подходящих вспомогательных веществ приведены в данной заявке. Является ли наполнитель подходящим для его включения в фармацевтическую композицию или форму дозирования,зависит от ряда факторов, хорошо известных в данной области, включающих способ введения формы дозирования пациенту, но не ограничиваясь им. Наполнители могут иметь разнообразные формы в зависимости от необходимой формы препарата для введения субъекту. Например, наполнители, подходящие для использования в жидкой или аэрозольной форме дозирования для перорального введения, включают воду, гликоли, масла, спирты, ароматизаторы, консерванты и красители, но не ограничиваются ими. Примеры наполнителей для применения в твердой форме дозирования для перорального введения (например, форме порошка, таблеток, капсул и каплетов) включают крахмал, сахара, микрокристаллическую целлюлозу, растворители, гранулирующие компоненты, смазки, связывающие вещества и дезинтегрирующие компоненты, но не ограничиваются ими. Такие способы приготовления включают стадию связывания молекулы для введения с такими компонентами, как носитель, который представляет собой один или более вспомогательных ингредиентов. Как правило, композиции готовят путем равномерного и интенсивного перемешивания активных ингредиентов с жидкими носителями, липосомами или мелко раздробленными твердыми носителями, или и теми, и другими, с последующей формовкой продукта, при необходимости. Фармацевтические композиции согласно настоящему изобретению представляют собой композиции, подходящие для энтерального введения, такого как пероральное или ректальное, трансдермального введения, местного применения и парентерального введения млекопитающим, включая людей, в целях подавления активности Bcr-abl и лечения связанных с активностью Bcr-abl расстройств, и включают эффективное количество фармакологически активного соединения согласно настоящему изобретению, отдельно или в комбинации с одним или более фармацевтически приемлемыми носителями. В частности,фармацевтические композиции включают эффективное для ингибирования Bcr-abl количество соединения согласно настоящему изобретению. Дозированная форма для однократного введения согласно изобретению является подходящей для перорального, мукозального введения пациенту (например, назального, сублингвального, вагинального, трансбуккального или ректального), парентерального введения(например, подкожного, внутривенного, болюсной инъекции, внутримышечного, внутриартериального,подкожного, интраартикулярного, интрасиновиального, интрастернального, интратекального, введения внутрь пораженных тканей и внутричерепной инъекции или инфузии), для ингаляции спреем, местного применения, ректального, назального, трансбуккального, вагинального введения, введения с помощью имплантированного резервуара или трансдермального введения пациенту. Примеры форм дозирования включают, но не ограничиваются перечисленными: таблетки; каплеты; капсулы, такие как мягкие эластичные желатиновые капсулы, крахмальные капсулы; пастилки; таблетки для рассасывания; дисперсные составы; суппозитории; мази; припарки; пасты; порошки; повязки; кремы; пластыри; растворы; пэтчи; аэрозоли (например, назальные спреи и ингаляторы); гели; жидкие формы дозирования, подходящие для перорального или мукозального введения пациенту, включая суспензии(например, водные или неводные жидкие суспензии, эмульсии типа "масло в воде" или жидкие эмульсии типа "вода в масле"), растворы и эликсиры; жидкие формы дозирования, подходящие для парентерального введения пациенту; и стерильные сухие остатки (например, кристаллические или аморфные сухие остатки), которые могут быть разбавлены для получения жидкой формы дозирования, подходящей для парентерального введения пациенту. Композиции, их внешний вид и форма дозирования согласно изобретению обычно различаются в зависимости от их применения. Например, форма дозирования для экстренного лечения расстройства может содержать большее количество одного или более входящих в состав активных ингредиентов, чем форма дозирования для продолжительного лечения такого же заболевания. Подобным образом, парентеральная форма дозы может содержать меньшие количества одного или более содержащихся в ней активных ингредиентов, чем пероральная форма дозы для лечения того же заболевания или расстройства. Эти и другие отличия конкретных форм дозирования согласно настоящему изобретению очевидны для специалистов в данной области. См., например, Remington's Pharmaceutical Sciences, 18th ed., Mack Publishing, Easton Pa. (1990). Композиция для перорального введения может быть представлена любой приемлемой формой дозирования, включая, капсулы, таблетки, эмульсии и водные суспензии, дисперсные составы и растворы,но не ограничиваясь перечисленными. В случае таблеток для перорального применения наиболее часто применяемые носители включают лактозу и зерновой крахмал. Как правило, также добавляют смазывающие агенты, такие как стеарат магния. Разбавители, используемые в капсулах для перорального введения, включают лактозу и сухой зерновой крахмал. В случае водных суспензий или эмульсий для перорального введения активный ингредиент может быть суспендирован или растворен в масляной фазе,смешанной с эмульгирующими или суспендирующими агентами. При необходимости могут быть добавлены некоторые вкусовые добавки, ароматизаторы или красители. Композиции для аэрозоля или ингалятора для назального применения могут быть приготовлены в соответствии с рецептурами, известными в области фармацевтики, и могут представлять собой соляные растворы, содержащие бензиловый спирт или другие подходящие консерванты, стимуляторы абсорбции для усиления биодоступности, фторуглероды и/или другие растворяющие или диспергирующие агенты, известные в данной области. Гетероциклические соединения согласно настоящему изобретению также могут использоваться в форме суппозиториев для ректального введения. При необходимости таблетки могут быть покрыты согласно стандартным водным или неводным технологиям покрытия. Такие формы дозирования могут быть получены в соответствии с любым из способов, применяемых в фармацевтике. В целом, фармацевтические композиции и формы дозирования готовят путем равномерного и интенсивного перемешивания активных ингредиентов с жидкими носителями, мелко раздробленными твердыми носителями или и теми и другими, с последующим приданием продукту желаемой формы при необходимости. Предпочтительными являются таблетки и желатиновые капсулы, содержащие активный компонент,наряду с а) разбавителями, например, лактозой, декстрозой, сахарозой, маннитом, сорбитолом, целлюлозой и/или глицином; b) смазывающими веществами, например, диоксидом кремния, тальком, стеариновой кислотой, магниевой или кальциевой солью стеариновой кислоты и/или полиэтиленгликолем; для таблеток также с) связывающими веществами, например, алюмосиликатом магния, крахмальной пастой,желатином, трагантом, метилцеллюлозой, карбоксиметилцеллюлозой натрия и/или поливинилпирролидоном; при необходимости d) разрыхлителями, например, углеводами, агаром, альгиновой кислотой или ее натриевой солью или шипучими смесями; и/или е) абсорбентами, красителями, ароматизаторами и вкусовыми добавками. Таблетки могут быть покрыты либо пленочной оболочкой, либо энтеросолюбильной оболочкой в соответствии с методами, известными в данной области. Например, таблетка может быть приготовлена путем прессования или формовки. Прессованные таблетки готовят в специальном аппарате при прессовании активных ингредиентов в сыпучем состоянии,типа порошка или гранул, возможно смешанных с наполнителем. Формованные таблетки готовят путем формовки в специальном аппарате смеси порошкообразного соединения с инертным жидким разбавителем. Композиции для инъекций предпочтительно представляют собой водные изотонические растворы или суспензии, а суппозитории предпочтительно готовят из масляных эмульсий или суспензий. Композиции могут быть стерилизованы и/или содержать адъюванты, такие как консерванты, стабилизаторы,увлажняющие компоненты или эмульгаторы, катализаторы растворения, соли для регуляции осмотического давления и/или буферы. Кроме того, они могут также содержать другие терапевтически ценные вещества. Указанные композиции готовят согласно стандартным методам смешивания, гранулирования или нанесения покрытия, соответственно, и содержат примерно от 0,1 до 75%, предпочтительно примерно от 1 до 50% активного ингредиента. Стерильные композиции для инъекций, например, стерильные водные или масляные суспензии для инъекций, могут быть приготовлены в соответствии с технологиями, известными в данной области, с использованием подходящих диспергирующих или увлажняющих компонентов (таких как, например, Твин 80) и суспендирующих компонентов. Стерильный состав для инъекций также может представлять собой стерильный раствор или суспензию для инъекций в нетоксичным разбавителе или растворителе, приемлемом для парентерального введения. Среди приемлемых наполнителей и растворителей могут применяться маннит, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, жирные масла обычно используются в качестве растворителя или суспендирующей среды (например, синтетические моно- и диглицериды). Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, применяют для приготовления составов для инъекций,также как и природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в полиоксиэтилированной форме. Данные масляные растворы или суспензии также могут содержать разбавители, включающие длинноцепочечные спирты, или диспергирующие компоненты,или карбоксиметилцеллюлозу, или подобные диспергирующие агенты. Для приготовления лекарственных средств, как правило, применяются также поверхностно-активные вещества, такие как твины или спаны, или другие подобные эмульгаторы или усилители биодоступности, обычно используемые в производстве фармацевтически приемлемых твердых, жидких или других форм дозирования. Подходящие составы для трансдермального применения включают эффективное количество соединения согласно настоящему изобретению с носителем. Предпочтительно носители включают абсорбируемые фармакологически приемлемые растворители для обеспечения прохождения соединения через кожу пациента. Например, устройства для трансдермального применения могут быть в форме бандажа,включающего основной каркас, резервуар, содержащий соединение, возможно с носителями; возможно контролирующий скорость барьер для доставки соединения к коже пациента с контролируемой и предопределенной скоростью в течение пролонгированного периода времени и элементы удержания устройства на коже. Матриксные трансдермальные составы также могут использоваться. Подходящие составы для местного применения, например, на коже или для глаз, предпочтительно представляют собой водные растворы, мази, кремы или гели, хорошо известные в данной области. Они могут содержать растворители, стабилизаторы, поддерживающие тонус кожи агенты, буферы и консерванты. Фармацевтические составы содержат эффективное количество для ингибирования Bcr-abl соединения согласно настоящему изобретению, как описано выше, либо отдельно, либо в комбинации с другим терапевтическим агентом. В комбинации с другим активным ингредиентом соединение согласно настоящему изобретению можно вводить либо одновременно с другим активным ингредиентом, до или после его введения, либо отдельно таким же или другим способом введения, либо вместе с ним в одном фармацевтическом составе. Носитель или фармацевтический состав должен быть "приемлемым" с точки зрения совместимости с активным ингредиентом состава (и предпочтительно способности его стабилизировать) и безвредным для субъекта, которому проводят лечение. Например, солюбилизирующие компоненты, такие как циклодекстрины, которые образуют специфические более растворимые комплексы с соединениями согласно данному изобретению или одним или более солюбилизирующими компонентами, могут применяться в качестве фармацевтических наполнителей для доставки соединений согласно изобретению. Примеры других носителей включают коллоидный диоксид кремния, стеарат магния, целлюлозу, лауреат сульфат натрия и DC Yellow 10. При использовании в данной заявке термины "животное", "субъект" и "пациент" включают коров,обезьян, лошадей, овец, свиней, куриц, индюков, куропаток, кошек, собак, мышей, крыс, кроликов, морских свинок и человека (предпочтительно человека), но не ограничиваются перечисленными. Фармакологически активные соединения согласно настоящему изобретению можно использовать при производстве фармацевтических композиций, содержащих их эффективное количество в связанном состоянии или в виде смеси с наполнителями или носителями, подходящими либо для энтерального, парентерального, перорального, мукозального введения, либо для местного применения. Соотношения дозировок для животных и людей (в миллиграммах на квадратный метр поверхности тела) описаны в источнике: Freireich et al., (1966) Cancer Chemother Rep 50: 219. Площадь поверхности тела можно приблизительно оценить на основании роста и веса пациента. См., например, Scientific tables,Geigy Pharmaceuticals, Ardley, N.Y., 1970, 537. Эффективное количество соединения настоящего изобретения может находиться в пределах примерно от 0,001 мг/кг примерно до 1000 мг/кг, предпочтительно от 0,01 мг/кг примерно до 100 мг/кг, предпочтительно от 0,1 мг/кг примерно до 10 мг/кг; или в любых пределах с любым значением нижней границы от 0,001 до 900 мг/кг и верхней границы от 0,1 до 1000 мг/кг(например, 0,005 и 200 мг/кг, 0,5 и 20 мг/кг). Для специалистов в данной области очевидно, что эффективные дозы также будут различаться в зависимости от конкретного заболевания, способа введения, использования вспомогательных веществ и совместного проведения других терапевтических процедур,таких как использование других агентов. Доза вводимого активного соединения зависит от вида теплокровного животного (млекопитающего), веса тела, возраста и индивидуального состояния и от формы введения. Единица дозирования для перорального введения млекопитающим весом примерно 50-70 кг может содержать примерно от 5 до 500 мг активного ингредиента. Соединение согласно изобретению можно, например, вводить в дозе в пределах от примерно 0,5 до примерно 100 мг/кг массы тела, альтернативные дозы составляют 1 мг до 1000 мг/доза каждые 4-120 ч,или согласно требованиям, предъявляемым к определенному лекарству. Способы согласно изобретению предусматривают введение эффективного количества соединения или композиции соединения с достижением желаемого или заданного эффекта. Как правило, фармацевтические композиции согласно настоящему изобретению необходимо вводить примерно от 1 примерно до 6 раз в день или, альтернативно,путем непрерывной инфузии. Такое введение может использоваться как в качестве длительной терапии,так и экстренной терапии. Количество активного ингредиента, который может быть связан с носителем с образованием дозированной формы для однократного введения, будет меняться в зависимости от субъекта, которому проводят лечение, и конкретного способа введения. Типовой состав содержит примерно от 5 примерно до 95% активного соединения (мас./мас.). Альтернативно такие составы содержат примерно от 20% примерно до 80% активного соединения. Могут требоваться более низкие или более высокие дозы, чем указанные выше. Определенная дозировка и схема лечения для каждого отдельного пациента будет зависеть от набора факторов, включающих активность специфических используемых соединений, возраста пациента, массы тела, общего состояния здоровья, пола, питания, времени введения, скорости выведения, комбинации лекарств, тяжести и течения заболевания, патологического состояния или симптомов, предрасположенности пациента к заболеванию, патологическому состоянию или возникновению симптомов и заключения лечащего врача. Определения При использовании в данной заявке термин "алкил" относится к линейной или разветвленной углеводородной цепи, содержащей от 1 до 12 атомов углерода. Термин "низший алкил" относится к С 1-С 6 углеводородным цепям алкила. Примеры алкильных групп включают метил, этил, н-пропил, изопропил,трет-бутия и н-пентил. Алкильные группы могут быть возможно замещенными одним или более заместителями. Термин "алкенил" относится к ненасыщенной линейной или разветвленной углеводородной цепи,содержащей 2-12 атомов углерода и по меньшей мере одну углерод-углеродную двойную связь. Алкенильные группы могут быть возможно замещенными одним или более заместителями. Термин "алкинил" относится к ненасыщенной линейной или разветвленной углеводородной цепи,содержащей 2-12 атомов углерода и по меньшей мере одну углерод-углеродную тройную связь. Алкинильные группы могут быть возможно замещенными одним или более заместителями.Sp2 или sp атомы углерода алкенильной группы и алкинильной группы, соответственно, возможно являются точкой присоединения алкенильной или алкинильной группы. Термин "алкокси" относится к -О-алкильному радикалу. Термин "амид" относится к -C(O)NH2, и "N-алкилзамещенный амид" имеет формулу C(O)NHR; где указанная дивалентная "амидная" группа представляет собой -C(O)N- или -NC(O)-. При использовании в данной заявке термин "галоген" относится к -F, -Cl, -Br или -I. При использовании в данной заявке термин "галогеноалкил" относится к алкильной группе, в которой один или более водородных радикалов (включая все) замещены галогеновой группой, где каждая галогеновая группа независимо выбрана из -F, -Сl, -Br и -I. Термин "галогенметил" относится к метилу, у которого от одного до трех водородных радикалов замещены галогеновой группой. Примеры галогеналкильных групп включают трифторметил, бромметил, 1,2-дихлорэтил, 4-йодбутил, 2-фторпентил и т.д. Термин "циклоалкил" относится к углеводородной 3-8-членной моноциклической или 7-14-членной бициклической системе колец, которая имеет по меньшей мере одно насыщенное кольцо, или углеводородной 3-8-членной моноциклической или 7-14-членной бициклической системе колец, имеющей по меньшей мере одно неароматическое кольцо, при этом неароматическое кольцо имеет некоторую степень ненасыщенности. Циклоалкильные группы могут быть возможно замещенными одним или более заместителями. В одном варианте реализации 0, 1, 2, 3 или 4 атома каждого кольца циклоалкильной группы могут быть замещены. Типичные примеры циклоалкильных групп включают циклопропил, циклопентил, циклогексил, циклобутил, циклогептил, циклооктил, циклононил, циклодецил, циклогексенил,бицикло[2.2.1]гепт-2-енил, дигидронафталинил, бензоциклопентил, циклопентенил, циклопентадиенил,циклогексенил, циклогексадиенил, циклогептенил, циклогептадиенил, циклогептатриенил, циклооктенил, циклооктадиенил, циклооктатриенил, циклооктатетраенил, циклононенил, циклононадиенил, циклодеценил, циклодецадиенил и т.д. Термин "арил" относится к углеводородной моноциклической, бициклической или трициклической системе ароматических колец. Арильные группы могут быть возможно замещенными одним или более заместителями. В одном варианте реализации 0, 1, 2, 3, 4, 5 или 6 атомов каждого кольца арильной группы могут быть замещенными. Примеры арильных групп включают фенил, нафтил, антраценил, флуоренил, инденил, азуленил и т.д. При использовании в данной заявке термин "аралкил" обозначает арильную группу, которая соединена с другой группой посредством (С 1-С 6)алкиленовой группы. Аралкильные группы могут быть возможно замещенными, либо в арильной части аралкилыюй группы, либо в алкиленовой части аралкильной группы, одним или более заместителями. Типичные аралкильные группы включают бензил, 2 фенил-этил, нафто-3-ил-метил и т.д. При использовании в данной заявке термин "алкилен" относится к алкильной группе, которая имеет две точки соединения. Термин "(С 1-С 6)алкилен" относится к алкиленовой группе, которая имеет от 1 до 6 атомов углерода. Неограничивающие примеры алкиленовых групп включают метилен (-СН 2-), этилен(-СН 2 СН 2-), н-пропилен (-CH2CH2CH2-), изопропилен (-СН 2 СН(СН 3)-) и т.д. Термин "арилалкокси" относится к алкоксигруппе, замещенной арилом. Термин "гетероарил" относится к 5-8-членной моноциклической, 8-12-членной бициклической или 11-14-членной трициклической системе колец, имеющей в кольце 1-4 гетероатома в случае моноциклической системы, 1-6 гетероатомов в случае бициклической или 1-9 гетероатомов в случае трициклической системы, где указанные гетероатомы выбраны из О, N или S, и остальные атома кольца представлены углеродом (с соответствующими атомами водорода, если иное не указано), при этом по меньшей мере одно кольцо в системе колец является ароматическим. Гетероарильные группы могут быть возможно замещенными одним или более заместителями. В одном варианте реализации 0, 1, 2, 3 или 4 атома каждого кольца гетероарильной группы могут быть замещенными. Примеры гетероарильных групп включают пиридил, 1-оксо-пиридил, фуранил, бензо[1,3]диоксилил, бензо[1,4]диоксинил, тиенил, пирролил,оксазолил, оксадиазолил, имидазолил, тиазолил, изоксазолил, хинолинил, пиразолил, изотиазолил, пиридазинил, пиримидинил, пиразинил, триазинил, триазолил, тиадизолил, изохинолинил, индазолил, бензоксазолил, бензофурил, индолизинил, имидазопиридил, тетразолил, бензимидазолил, бензотиазолил,бензотиадиазолил, бензоксадиазолил, индолил, тетрагидроиндолил, азаиндолил, имидазопиридил, хиназолинил, пуринил, пирроло[2,3]пиримидинил, пиразоло[3,4]пиримидинил и бензо(b)тиенил, 3 Нтиазоло[2,3-с][1,2,4]тиадиазолил, имидазо[1,2-d]-1,2,4-тиадиазолил, имидазо[2,1-b]-1,3,4-тиадиазолил,1 Н,2 Н-фуро[3,4-d]-1,2,3-тиадиазолил,1 Н-пиразоло[5,1-с]-1,2,4-триазолил,пирроло[3,4-d]-1,2,3 триазолил, циклопентатриазолил, 3 Н-пирроло[3,4-с]изоксазолил, 1 Н,3 Н-пирроло[1,2-с]оксазолил, пирроло[2,1b]оксазолил и т.д. При использовании в данной заявке термин "гетероаралкил" или "гетероарилалкил" обозначает гетероарильную группу, которая соединена с другой группой через (С 1-С 6)алкилен. Гетероаралкильные группы могут быть возможно замещенными, либо в гетероарильной части гетероаралкильной группы,либо в алкиленовой части гетероаралкилыюй группы, одним или более заместителями. Примеры гетероаралкильных групп включают 2-(пиридин-4-ил)-пропил, 2-(тиен-3-ил)этил, имидазол-4-ил-метил и т.д. Термин "гетероциклоалкил" относится к неароматической 3-8-членной моноциклической, 7-12 членной бициклической или 10-14-членной трициклической системе колец, включающей 1-3 гетероатома в случае моноциклической системы, 1-6 гетероатомов в случае бициклической или 1-9 гетероатомов в случае трициклической, где указанные гетероатомы выбраны из О, N, S, В, Р и Si, предпочтительно О, N и S, при этом неароматическая система является полностью насыщенной. Термин "гетероциклоалкил" также относится к неароматической 5-8-членной моноциклической, 7-12-членной бициклической или 1014-членной трициклической системе колец, включающей 1-3 гетероатома в случае моноциклической, 1 6 гетероатома в случае бициклической или 1-9 гетероатомов в случае трициклической системы, где указанные гетероатомы выбраны из О, N, S, В, Р или Si, при этом неароматическая система колец имеет некоторую степень ненасыщенности. Бициклические и трициклические системы колец могут представлять собой системы конденсированных колец или системы спиро-колец. Гетероциклоалкильные группы могут быть возможно замещенными одним или более заместителями. В одном варианте реализации 0, 1, 2,3 или 4 атома каждого кольца гетероциклоалкильной группы могут быть замещенными. Примеры гетероциклоалкильных групп включают пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 4-пиперидонил, тетрагидропиранил, тетрагидротиопиранил, тетрагидротиопиранил сульфон, морфолинил, тиоморфолинил, тиоморфолинил сульфоксид, тиоморфолинил сульфон, 1,3-диоксолан, 1,4-диокса-8-аза-спиро[4.5]дец-8-ил, тетрагидрофуранил, тетрагидротиенил, тиирен,тииренил, тиадиазиринил, диоксазолил, 1,3-оксатиолил, 1,3-диоксолил, 1,3-дитиолил, оксатиазинил, диоксазинил, дитиазинил, оксадиазинил, тиадиазинил, оксазинил, тиазинил, 1,4-оксатиин,1,4-диоксин, 1,4 дитиин, 1 Н-пиранил, оксатиепинил, 5 Н-1,4-диоксепинил, 5 Н-1,4-дитиепинил, 6 Н-изоксазоло[2,3-d]-1,2,4 оксадиазолил, 7 аН-оксазоло[3,2-d]-1,2,4-оксадиазолил и т.д. Термин "алкиламино" относится к аминному заместителю, который дополнительно замещен одной или двумя алкильными группами. Термин "аминоалкил" относится к алкильному заместителю, который также замещен одной или более аминными группами. Термин "эффективное количество" используется в данной заявке для описания концентрации или количества соединения согласно настоящему изобретению, которое может быть использовано для благоприятного изменения течения заболевания или состояния, подлежащего лечению, независимо от того,является ли это изменение ремиссией, уменьшением скорости роста или размера раковых, опухолевых или других клеток, благоприятного физиологического результата, включающего нормализацию кожи или ткани и т.д. в зависимости от заболевания или состояния, подлежащего лечению. При использовании в данной заявке термины "предотвратить", "предотвращающий", "предотвращение" и т.д. относятся к снижению вероятности развития расстройства или патологического состояния у субъекта, который не страдает от расстройства или патологического состояния, но находится в группе риска или имеет предрасположенность к развитию расстройства или патологического состояния. Термин "субъект" используется в настоящей заявке в отношении животного, предпочтительно человека, которому проводят лечение, включая профилактическое лечение, с применением соединений согласно настоящему изобретению. В случае лечения таких инфекций, патологических состояний или заболеваний, которые специфичны для определенного животного, например, для человека, термин пациент относится к этому определенному животному. В большинстве случаев термин пациент относится к человеку. При использовании в данной заявке термины "лечить", "подверженный лечению", "лечение" и т.д. относятся к снижению выраженности или облегчению расстройства и/или симптомов, связанных с указанным расстройством. Необходимо понимать, что лечение расстройства или патологического состояния не требует, хотя и не исключает, полного устранения расстройства, патологического состояния или связанных с ним симптомов. Термин "IC50" обозначает концентрацию соединения, которая приводит к ингибированию активности пептида, белка, фермента или биологического процесса на 50%."Сайт связывания остатка миристиновой кислоты" в области Bcr-abl представляет собой сайт, с которым может связываться остаток миристиновой кислоты при нахождении белка BCR-Abl в подходящей конформации для связывания остатка миристиновой кислоты. Сайт связывания остатка миристиновой кислоты описан, например, в источнике Hantschel et al.,"A Myristoyl/Phosphotyrosine Switch Regulates cAbl" Cell (2003), Vol. 112, 845-857 и Bhushan et al.,"Structural Basis for the Autoinlaibition of c-Abl TyrosineKinase" Cell (2003), Vol. 112, 859-871. Гибридный белок Bcr-Abl является результатом реципрокной транслокации, которая приводит к слиянию протоонкогена Abl с геном Bcr. Bcr-abl становится способным трансформировать В-клетки путем увеличения митогенной активности. Такое увеличение приводит к снижению чувствительности к апоптозу, наряду с изменением адгезии и хоуминга клеток-предшественников ХМЛ. Согласно настоящему изобретению предложены соединения, составы и способы лечения связанных с киназной активностью заболеваний, в особенности связанных с активностью ФРТР, c-Kit и киназы Bcr-abl заболеваний. При использовании в данной заявке термин "заместитель" или "замещенный" означает, что водородный радикал соединения или группы (такой как, например, алкильной, алкенильной, алкинильной,алкиленовой, арильной, аралкильной, гетероарильной, гетероаралкильной, циклоалкильной или гетероциклоалкильной группы) замещен или возможно замещен любой желаемой группой, которая не оказывает существенного неблагоприятного влияния на стабильность соединения. В одном варианте реализации предпочтительными являются заместители, которые не оказывают неблагоприятного влияния на свойства соединения. Термин "замещенный" относится к одному или более заместителям (которые могут быть одинаковыми или разными), каждый из которых замещает атом водорода. Примеры заместителей включают, но не ограничиваются перечисленными: галогены (F, Cl, Br или I), гидроксил, амино, алкиламино,ариламино, диалкиламино, диариламино, алкилариламино, циано, нитро, меркапто, тио, имино, формил,карбамидо, карбамил, карбоксил, тиоуреид, тиоцианат, сульфамидо, сульфонилалкил, сульфониларил,алкил, алкенил, алкокси, меркаптоалкокси, арил, гетероарил, циклоалкил, гетероциклоалкил, причем алкил, алкенил, алкокси, алкоксиалкил, арил, гетероарил, циклоалкил и гетероциклоалкил возможно замещены алкилом, арилом, гетероарилом, галогеном, гидроксилом, амином, меркапто, циано, нитро, оксо(=O), тиоксо- (=S), имино (=NR), C(=N-NRk)Rk или C(=N-ORk)Rk. В других вариантах реализации заместители при любой группе (такой как, например, алкильной,алкенильной, алкинильной, арильной, аралкильной, гетероарильной, гетероаралкильной, циклоалкильной и гетероциклоалкильной) могут находиться при любом атоме этих групп, при этом любая группа,которая может быть замещена (такая как, например, алкильная, алкенильная, алкинильная, арильная,аралкильная, гетероарильная, гетероаралкильная, циклоалкильная, гетероциклоалкильная), может быть возможно замещенной одним или более заместителями (которые могут быть одинаковыми или разными),каждый из которых замещает атом водорода. Примеры подходящих заместителей включают, но не ограничиваются перечисленными: алкил, алкенил, алкинил, циклоалкил, гетероциклоалкил, аралкил, гетероаралкил, арил, гетероарил, галоген, галогеналкило, циано, нитро, алкокси, арилокси, гидроксил, гидроксилалкил, окс (т.е., карбонил), карбоксил, формил, алкилкарбонил, алкилкарбонилалкил, алкоксикарбонил, алкилкарбонилокси, арилоксикарбонил, гетероарилокси, гетероарилоксикарбонил, тио, меркапто,меркаптоалкил, арилсульфонил, амино, аминоалкил, диалкиламино, алкилкарбониламино, алкиламинкарбонил или алкоксикарбониламино; алкиламино, ариламино, диариламино, алкилкарбонил или ариламин-замещенный арил; арилалкиламином, аралкиламинкарбонил, амидо, алкиламинсульфонил, ариламинсульфонил, диалкиламинсульфонил, алкилсульфониламино, арилсульфониламино, имино, карбамидо, карбамил, тиоуреидо, тиоцианато, сульфамидо, сульфонилалкил, сульфониларил или меркаптоалкокси.
МПК / Метки
МПК: A01N 43/04
Метки: миристатные, применения, способы, низкомолекулярные, bcr-abl, тирозинкиназы, ингибиторы
Код ссылки
<a href="https://eas.patents.su/30-19869-nizkomolekulyarnye-miristatnye-ingibitory-tirozinkinazy-bcr-abl-i-sposoby-ih-primeneniya.html" rel="bookmark" title="База патентов Евразийского Союза">Низкомолекулярные миристатные ингибиторы тирозинкиназы bcr-abl и способы их применения</a>
Предыдущий патент: Способ закрывания системы запирания цилиндрического прохода
Следующий патент: Способ и устройство для нанесения внутреннего покрытия в трубопроводе
Случайный патент: Способ селективного гидрирования и катализатор