Соединения, модулирующие активность toll-подобных рецепторов
Номер патента: 19768
Опубликовано: 30.06.2014
Авторы: Карсон Деннис А., Коттэм Ховард Б., Чэнь Майкл, Хайяши Томоко
Формула / Реферат
1. Соединение, имеющее структуру согласно формуле I
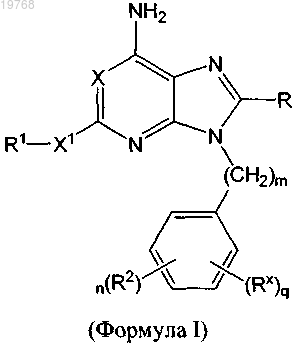
или его фармацевтически приемлемая соль, включая его гидрат,
где X представляет собой N или CR2;
R представляет собой -OR1, -SR1 или -NRaRb,
X1 представляет собой связь или -О-, -S- или -NRc-;
Rc представляет собой водород, C1-C10-алкил или замещенный C1-C10-алкил или Rc и R1 вместе с атомом азота могут образовывать гетероциклическое кольцо или замещенное гетероциклическое кольцо;
каждый R1 независимо представляет собой водород, C1-C10-алкил, замещенный C1-C10-алкил, C1-C10-алкокси, замещенный C1-C10-алкокси, C1-C10-алкил-C1-C10-алкокси, замещенный C1-C10-алкил-C1-C10-алкокси, C5-C10-арил, замещенный C5-C10-арил, C5-C9-гетероциклил, замещенный C5-C9-гетероциклил, C3-С9-карбоциклил или замещенный C3-С9-карбоциклил;
каждый R2 независимо представляет собой водород, -ОН, C1-C6-алкил, замещенный C1-C6-алкил, C1-C6-алкокси, замещенный C1-C6-алкокси, -С(О)-C1-C6-алкил (алканоил), замещенный -С(О)-C1-C6-алкил, -С(О)-C6-C10-арил (ароил), замещенный -С(О)-C6-C10-арил, -С(О)ОН (карбоксил), -С(О)О-C1-C6-алкил (алкоксикарбонил), замещенный -С(О)О-C1-C6-алкил, -NRaRb, -C(O)NRaRb (карбамоил), замещенный C(O)NRaRb, гало, нитро или циано;
заместители на алкильных, алкокси, арильных или гетероциклических группах представляют собой гидрокси, C1-C6-алкил, гидрокси-C1-C6-алкилен, карбокси-C1-C6-алкилен, C1-C6-алкокси, C3-С6-циклоалкил, C1-C6-алкокси-C1-C6-алкилен, амино, циано, галоген или арил;
каждый Ra и Rb независимо представляет собой водород, С1-С20-алкил, C3-C8-циклоалкил, C1-C6-алкокси, гало-C1-C6-алкил, C3-C8-циклоалкил-C1-C6-алкил, C1-C6-алканоил, гидрокси-C1-C6-алкил, арил, арил-C1-C6-алкил, Het, Het-C1-C6-алкил или C1-C6-алкоксикарбонил;
Rx представляет собой -X2-((R3)r-(R4)s)p;
каждый X2 независимо представляет собой амидосвязующую группу, алкиламидосвязующую группу, замещенное 5-6-членное кольцо или кислородсодержащий фрагмент;
каждый R3 независимо представляет собой полиэтиленгликолевый (PEG) фрагмент, который представляет собой -О-СН2-СН2- или -СН2-СН2-О-;
каждый R4 независимо представляет собой Н, -C1-C6-алкил, -C1-C6-алкокси, -NRaRb, -N3, -ОН, -CN, -СООН,
-COOR1, -C1-C6-алкил-NRaRb, C1-C6-алкил-ОН, C1-C6-алкил-CN, C1-C6-алкил-СООН, C1-C6-алкил-COOR1, 5-6-членное кольцо, замещенное 5-6-членное кольцо, -C1-C6-алкил-5-6-членное кольцо, -C1-C6-алкилзамещенное 5-6-членное кольцо, C2-C9-гетероциклил или замещенный C2-C9-гетероциклил;
m представляет собой 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10;
n представляет собой 0, 1, 2, 3 или 4;
р представляет собой от 1 до 100;
q представляет собой 1, 2, 3, 4 или 5;
r представляет собой от примерно 5 до примерно 100;
s представляет собой от 1 до 1000;
сумма n и q равна 5.
2. Соединение по п.1, в котором X1 представляет собой кислород.
3. Соединение по п.1 или 2, в котором R1 представляет собой замещенный C1-C6-алкил или C1-C10-алкил-C1-C10-алкокси-фрагмент, предпочтительно R1 представляет собой -СН2СН2ОСН3.
4. Соединение по любому из пп.1-3, в котором X2 представляет собой -C(O)NH-, -NH(O)C-, -C1-C6-алкил-С(О)NH-, -C1-C6-алкил-NH(О)С-, -C(O)NH-C1-C6-алкил-, -NH(O)C-C1-C6-алкил-, -C1-C6-алкил-NH(O)С-C1-C6-алкил-, -C1-C6-алкил-С(О)NH-C1-C6-алкил или -C(O)NH-(CH2)t-, где t равно 1, 2, 3 или 4.
5. Соединение по любому из пп.1-4, в котором n равно 4 и R2 представляет собой водород в каждом случае.
6. Соединение по любому из пп.1-5, в котором каждое PEG звено представляет собой -О-СН2-СН2- или СН2-СН2-О-.
7. Соединение по любому из пп.1-6, в котором r равно от примерно 5 до примерно 50, предпочтительно от примерно 5 до примерно 25, более предпочтительно от примерно 5 до примерно 15 и наиболее предпочтительно r равно примерно 10.
8. Соединение по любому из пп.1-7, в котором s равно от примерно 5 до примерно 100, предпочтительно от примерно 5 до примерно 50, более предпочтительно от примерно 5 до примерно 25, еще более предпочтительно от примерно 5 до примерно 15, наиболее предпочтительно s равно примерно 10.
9. Соединение по любому из пп.1-8, в котором один или более PEG фрагментов являются линейными или в котором один или более PEG фрагментов являются разветвленными.
10. Соединение по любому из пп.1-9, в котором каждый заместитель R4 независимо представляет собой Н, С1-С2-алкил, -С1-С2-алкокси (например, -ОСН3), -NRaRb, -ОН, -CN, -СООН, -COOR1, -С1-С2-алкил-NRaRb, С1-С2-алкил-ОН, С1-С2-алкил-CN, С1-С2-алкил-СООН или С1-С2-алкил-COOR1.
11. Соединение по любому из пп.1-10, в котором m равно 1.
12. Соединение по п.11, в котором R2 представляет собой водород, n равно 4, q равно 1, р равно 1, r равно примерно 10 и s равно 1.
13. Фармацевтическая композиция для применения в медицинской терапии аутоиммунного нарушения или заболевания или воспалительного нарушения или заболевания, включающая фармацевтически приемлемую соль соединения по любому из пп.1-12.
14. Фармацевтическая композиция по п.13, в которой фармацевтически приемлемая соль является приготовленной с использованием кислоты, выбранной из группы, состоящей из соляной, бромисто-водородной, серной, сульфаминовой, фосфорной, азотной кислоты, уксусной, пропионовой, янтарной, гликолевой, стеариновой, молочной, яблочной, винной, лимонной, аскорбиновой, памовой, малеиновой, гидроксималеиновой, фенилуксусной, глутаминовой, бензойной, салициловой, сульфаниловой, 2-ацетоксибензойной, фумаровой, толуолсульфоновой, метансульфоновой, этандисульфоновой, щавелевой и изэтионовой кислоты.
15. Фармацевтическая композиция по п.13, в которой фармацевтически приемлемая соль является приготовленной с использованием основания, выбранного из группы, состоящей из гидроксида калия, гидроксида натрия, гидроксида аммония, кофеина и амина.
16. Применение соединения по любому из пп.1-12 или фармацевтической композиции по любому из пп. 13-15 в эффективном количестве для профилактики, ингибирования или лечения аутоиммунного состояния у млекопитающего, предпочтительно человека.
17. Применение соединения по любому из пп.1-12 или фармацевтической композиции по любому из пп.13-15 в эффективном количестве для профилактики, ингибирования или лечения воспалительного состояния у млекопитающего, предпочтительно человека.
18. Применение соединения по любому из пп.1-12 для изготовления лекарственного средства для профилактики, ингибирования или лечения аутоиммунного нарушения или заболевания или воспалительного нарушения или заболевания.
19. Соединение по п.1, в котором замещенное 5-6-членное кольцо представляет собой арильное кольцо или гетероарильное кольцо.
20. Соединение по п.19, в котором гетероарильное кольцо представляет собой тетразол, пиридил, 2,5-пирролидиндион или замещенный 2,5-пирролидиндион.
21. Соединение по п.1, в котором замещенное 5-6-членное кольцо представляет собой карбоциклическое кольцо или гетероциклическое кольцо.
22. Соединение по п.1, в котором кислородсодержащий фрагмент представляет собой -О- или -C1-C6-алкокси.
Текст
Изобретение относится к низкомолекулярным конъюгатам, которые являются агонистами или антагонистами одного или более Toll-подобных рецепторов.(71)(73) Заявитель и патентовладелец: ДЗЕ РЕГЕНТС ОФ ДЗЕ ЮНИВЕРСИТИ ОФ КАЛИФОРНИЯ Заявка претендует на преимущество даты подачи заявки США под серийным номером 61/151737 от 11 февраля 2009 г., полностью включенной здесь путем отсылки. Описанное здесь изобретение было сделано при поддержке правительства по грантам с номерамиAI056453 и AI077989-01, присужденным Национальными институтами здравоохранения. Правительство США обладает определенными правами на изобретение. Область техники, к которой относится изобретение Технология частично относится к молекулам, которые модулируют функцию Toll-подобного рецептора, и способам лечения заболеваний путем введения таких молекул субъекту, нуждающемуся в этом. Сведения о предшествующем уровне техникиToll-подобные рецепторы (TLR) представляют собой паттерн-распознающие рецепторы, представленные на клетках разного типа, которые распознают определенные молекулярные структуры, присутствующие в микробах, таких как бактерии, вирусы или грибы (1). TLR распознают липопротеин (TLR2),двухцепочечную РНК (TLR3), липополисахарид (LPS, TLR4), флагеллин (TLR5), одноцепочечную РНК(TLR7/8) и бактериальные или вирусные неметилированные CpG ДНК (TLR9). Все TLR, за исключениемTLR3, передают сигнал через адаптерный белок, называемый MyD88, приводя к активации NF-kappaB и генов, кодирующих синтез цитокинов (2).TLR7 и 8, локализованные внутри клеток в эндосомальных компартментах, распознают одноцепочечные молекулы РНК и определенный синтетический гуанозиновый аналог клеток хозяина (3, 4). Богатая гуанином и уридином одноцепочечная РНК была идентифицирована как природный лиганд дляTLR7 (5). К тому же было идентифицировано несколько низкомолекулярных активаторов TLR7, включающих имидазохинолины и пурин-подобные молекулы (3, 6, 7). Из последних, 9-бензил-8-гидрокси-2(2-метоксиэтокси)аденин ("SM") был идентифицирован как сильный и специфический агонист TLR7 (8). Производные SM синтезировали путем введения альдегидной функциональной группы на бензильный фрагмент и промежуточного связывания с разными вспомогательными химическими соединениями посредством бифункциональной линкерной молекулы, содержащей гидразин и N-гидроксисукцинимид(9). Конъюгация с белком мышиным сывороточным альбумином (MSA) повышала силу от 10 до 100 раз и улучшала фармакодинамику in vivo по сравнению с лекарственным веществом, не связанным с белками плазмы крови. Конъюгат MSA может доставляться в дыхательную систему путем интраназального или внутритрахеального введения. Доставка лекарственного средства интраназально доказала свою эффективность в двух мышиных моделях инфекционного заболевания, бактериальной инфекции и вирусной инфекции (9). Промежуточное соединение SM также было конъюгировано с липидом, диолеоилфосфатидилэтаноламином (DOPE), и было определено, что конъюгат проявлял усиленную активность агониста TLR7 (например, WO 2008/115319, опубликованный 25 сентября 2008 г. на основе Международной патентной заявки PCT/US2008/001631, зарегистрированной 7 февраля 2008 г.). Сущность изобретения Обеспечены низкомолекулярные конъюгаты, которые могут модулировать активность одного ли более Toll-подобных рецепторов (например, конъюгаты являются агонистами, антагонистами или обоими). Термин "Toll-подобный рецептор" (TLR) относится к члену семейства рецепторов, которые связываются с патоген-ассоциированными молекулярными паттернами (РАМР) и способствуют иммунному ответу у млекопитающих. Известно 10 TLR у млекопитающих, например TLR1-10. Термин "агонист Tollподобного рецептора" (агонист TLR) относится к молекуле, которая взаимодействует с TLR и стимулирует активность рецептора. Синтетические агонисты TLR представляют собой химические соединения,которые разработаны для взаимодействия с TLR и стимулирования активности рецептора. Примеры агонистов TLR включают агонист TLR7, агонист TLR3 или агонист TLR9. Термин "антагонист Tollподобного рецептора" (антагонист TLR) относится к молекуле, которая взаимодействует с TLR и ингибирует или нейтрализует сигнальную активность рецептора. Синтетические антагонисты TLR представляют собой химические соединения, разработанные для взаимодействия с TLR и препятствования активности рецептора. Примеры антагонистов TLR включают антагонист TLR7, антагонист TLR3 или антагонист TLR9. Таким образом, в одном варианте обеспечено соединение, имеющее структуру согласно формуле I или его фармацевтически приемлемая соль, включая его гидрат,-1 019768 где X представляет собой N или CR2;X1 представляет собой связь или -О-, -S- или -NRc-;Rc представляет собой водород, C1-C10-алкил или замещенный C1-C10-алкил или Rc и R1 вместе с атомом азота могут образовывать гетероциклическое кольцо или замещенное гетероциклическое кольцо;R1 представляет собой водород, C1-C10-алкил, замещенный C1-C10-алкил, C1-C10-алкокси, замещенный C1-C10-алкокси, C1-C10-алкил-C1-C10-алкокси, замещенный C1-C10-алкил-C1-C10-алкокси, C5-C10-арил,замещенный C5-C10-арил, C5-C9-гетероциклил, замещенный C5-C9-гетероциклил, C3-C9-карбоцикл или замещенный C3-C9-карбоцикл; каждый R2 независимо представляет собой водород, -ОН, C1-C6-алкил, замещенный C1-C6-алкил,C1-C6-алкокси, замещенный C1-C6-алкокси, -С(О)-C1-C6-алкил (алканоил), замещенный -С(О)-C1-C6 алкил, -С(О)-C6-C10-арил (ароил), замещенный -С(О)-C6-C10-арил, -С(О)ОН (карбоксил), -С(О)О-C1-C6 алкил (алкоксикарбонил), замещенный -С(О)О-C1-C6-алкил, -NRaRb, -C(O)NRaRb (карбамоил), замещенный -C(O)NRaRb, гало, нитро или циано; заместители на алкильных, арильных или гетероциклических группах представляют собой гидрокси, C1-C6-алкил, гидрокси-C1-C6-алкилен, C1-C6-алкокси, C3-С 6-циклоалкил, C1-C6-алкокси-C1-C6 алкилен, амино, циано, галоген или арил; каждый Ra и Rb независимо представляет собой водород, C1-C6-алкил, C3-C8-циклоалкил, C1-C6 алкокси, гало-C1-C6-алкил, C3-C8-циклоалкил-C1-C6-алкил, C1-C6-алканоил, гидрокси-C1-C6-алкил, арил,арил-C1-C6-алкил, Het, Het-C1-C6-алкил или C1-C6-алкоксикарбонил; каждый Rx независимо представляет собой -X2-R3)r-(R4)s)p, -C(O)NRaRb или -CH2NH-биотин; каждый X2 независимо представляет собой связь или связующую группу; каждый R3 независимо представляет собой полиэтиленгликолевый (PEG) фрагмент; каждый R4 независимо представляет собой Н, -C1-C6-алкил, -C1-C6-алкокси, -NRaRb, -N3, -ОН, -CN,-СООН, -COOR1, -C1-C6-алкил-NRaRb, -C1-C6-алкил-ОН, -C1-C6-алкил-CN, -C1-C6-алкил-СООН, -C1-C6 алкил-COOR1, 5-6-членное кольцо, замещенное 5-6-членное кольцо, -C1-C6-алкил 5-6-членное кольцо,-C1-C6-алкилзамещенное 5-6-членное кольцо, C2-C9-гетероциклил или замещенный C2-C9-гетероциклил;n представляет собой 0, 1, 2, 3 или 4; р представляет собой от 1 до 100;r представляет собой от 1 до 1,000;s представляет собой от 1 до 1,000; сумма n и q равна 5. В определенных вариантах также обеспечено соединение, имеющее структуру согласно формуле II или его фармацевтически приемлемая соль либо его гидрат,где X, X1, X2, R, R1, R2, R3, R4, m, n, р, q, r и s варианты описаны выше для формулы I. В некоторых вариантах обеспечено соединение, имеющее структуру согласно формуле III или его фармацевтически приемлемая соль либо его гидрат,где X, X1, R, R1 и R2 варианты описаны выше для формулы I;R3, R4, m, n, р, q, r и s варианты описаны выше для формулы I; каждый X3 независимо является связью или связующей группой; каждый X независимо представляет собой макромолекулу;u равно от 1 до 1,000. В некоторых вариантах X представляет собой N. В определенных вариантах X1 представляет собой кислород и в некоторых вариантах R1 представляет собой замещенный C1-C10-алкил, а именно C1-C10 алкил-C1-C10-алкокси-фрагмент (например, -СН 2 СН 2 ОСН 3). В некоторых вариантах R1 состоит из шести или менее неводородных атомов. В некоторых вариантах n равно 4 и R2 представляет собой водород в каждом случае. В определенных вариантах X2 и/или X3 независимо представляют собой амидосвязующую группу(например, -C(O)NH или -NH(O)C-); алкиламидосвязующую группу (например, -C1-C6-алкил-С(О)NH-,-C1-C6-алкил-NH(О)С-, -C(O)NH-C1-C6-алкил-, NH(O)C-C1-C6-алкил-, -C1-C6-алкил-NH(О)С-C1-C6-алкил-,-C1-C6-алкил-C(O)NH-C1-C6-алкил- или -C(O)NH-(CH2)t-, где t равно 1, 2, 3 или 4); замещенное 5-6 членное кольцо (например, арильное кольцо, гетероарильное кольцо (например, тетразол, пиридил, 2,5 пирролидиндион (например, 2,5-пирролидиндион, замещенный замещенной фенильной группой, карбоциклическое кольцо или гетероциклическое кольцо) или кислородсодержащий фрагмент (например,-О-, -C1-C6-алкокси). Фрагмент PEG может включать одно или более PEG звеньев. Фрагмент PEG может включать примерно от 1 до 1,000 PEG звеньев, включая, без ограничения, примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13,14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800 или 900 звеньев в некоторых вариантах. В определенных вариантах фрагмент PEG может содержать примерно от 5 до 25 PEG звеньев, примерно от 10 до 50 PEG звеньев, примерно от 50 до 150 PEG звеньев, примерно от 120 до 350 PEG звеньев, примерно от 250 до 550 PEG звеньев или примерно от 650 до 950 PEG звеньев. В определенных вариантах PEG звено представляет собой -О-СН 2-СН 2- или -СН 2-СН 2 О-. В некоторых вариантах r равно примерно от 5 до 100, иногда r равно примерно от 5 до 50 или примерно от 5 до 25. В определенных вариантах r равно примерно от 5 до 15 и иногда r равно примерно 10. В некоторых вариантах R3 представляет собой PEG звено и r равно примерно от 2 до 10 (например, r равно примерно от 2 до 4). В определенном варианте R3 представляет собой -О-СН 2-СН 2- или -СН 2-СН 2-О-. В некоторых вариантах R3 представляет собой -О-СН 2-СН 2- или -СН 2-СН 2-О- и r равно примерно от 1 до 1000 (например, примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24,25, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800, 900 или 1000). В определенных родственных вариантах r равно примерно от 5 до 25, примерно от 10 до 50, примерно от 50 до 150, примерно от 120 до 350, примерно от 250 до 550 или примерно от 650 до 950. В некоторых вариантах s равно примерно от 5 до 100, иногда s равно примерно от 5 до 50 или примерно от 5 до 25. В определенных вариантах s равно примерно от 5 до 15, иногда s равно примерно 10. В некоторых вариантах s равно примерно 5 или меньше (например, s равно 1). В некоторых вариантах (R3)r заместитель является линейным, и в определенных вариантах (R3)r заместитель является разветвленным. Для линейных фрагментов s иногда меньше, чем r (например, когда R3 представляет собой-О-СН 2-СН 2- или -СН 2-СН 2-О-) и иногда s равно 1. В некоторых вариантах R3 представляет собой линейный PEG фрагмент (например, содержащий примерно от 1 до 1000 PEG звеньев), s равно 1 и r равно 1. Для разветвленных фрагментов s иногда меньше, больше или равно r (например, когда R3 представляет собой -О-СН 2-СН 2- или -СН 2-СН 2-О-), иногда r равно 1, s равно 1 и р равно примерно от 1 до 1000 (например, р равно примерно 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25,30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800, 900 или 1000). В некоторых вариантах t равно примерно от 5 до 100, иногда t равно примерно от 5 до 50 или примерно от 5 до 25. В определенных вариантах t равно примерно от 5 до 15, иногда t равно примерно 10. В некоторых вариантах t равно примерно 5 или меньше (например, t равно 1). В определенных вариантах u равно примерно от 5 до 100, иногда u равно примерно от 5 до 50 или примерно от 5 до 25. В некоторых вариантах u равно примерно от 5 до 15, иногда u равно примерно 10. В определенных вариантах u равно примерно 5 или меньше (например, u равно 1). В определенных вариантах R4 заместитель независимо представляет собой Н, С 1-С 2-алкил, -С 1-С 2 алкокси (например, -ОСН 3), -NRaRb, -ОН, -CN, -СООН, -COOR1, -С 1-С 2-алкил-NRaRb, С 1-С 2-алкил-ОН,С 1-С 2-алкил-CN, С 1-С 2-алкил-СООН или С 1-С 2-алкил-COOR1. В некоторых вариантах R4 является фа-3 019768 культативно замещенным 5-6-членным кольцом (например, арильным кольцом, гетероарильным кольцом, карбоциклическим кольцом, гетероциклическим кольцом). В определенных вариантах R4 не является водородом и иногда R4 не является гидроксилом. В некоторых вариантах, относящихся к соединению, имеющему структуру согласно формуле I, m равно примерно 1, R2 представляет собой водород и n равно 4, q равно 1, r равно примерно 10 и s равно 1. Каждый X4 может быть одинаковой или различной макромолекулой. В определенных вариантах макромолекула выбрана из группы, состоящей из антитела, фрагмента антитела, антигена, патогенного антигена (например, антиген S. aureus), белка (например, человеческий сывороточный альбумин или его фрагмент), глицерина, липида, фосфолипида (например, DOPE), сфинголипида и т.п. В некоторых вариантах макромолекулой является DOPE. В одном варианте изобретение обеспечивает способ профилактики, ингибирования или лечения воспалительного или аутоиммунного состояния (нарушения или заболевания) (например, ревматоидного артрита) у субъекта, включающий введение соединения, имеющего следующую структуру: или его фармацевтически приемлемой соли либо его гидрата человеческому субъекту, нуждающемуся в этом, в количестве, эффективном для профилактики, ингибирования или лечения ревматоидного артрита. Также обеспечена фармацевтическая композиция, включающая фармацевтически приемлемую соль соединения, имеющего структуру согласно формулам I, II или III. Также здесь обеспечен способ профилактики, ингибирования или лечения воспалительного состояния у субъекта, который включает введение соединения, имеющего структуру согласно формулам I, II или III, субъекту, нуждающемуся в этом, в количестве, эффективном для профилактики, ингибирования или лечения состояния, например аутоиммунного нарушения или его симптомов. Также здесь обеспечен способ профилактики, ингибирования и лечения аутоиммунного состояния у субъекта, который включает введение соединения, имеющего структуру согласно формулам I, II или III, субъекту, нуждающемуся в этом, в количестве, эффективном для профилактики, ингибирования или лечения состояния или его симптомов, например воспаления. Таким образом, изобретение обеспечивает соединения для применения в медицинской терапии, а именно агенты, которые предупреждают, ингибируют или лечат воспалительные нарушения или заболевания, например ревматоидный артрит или рак, факультативно в сочетании с другими соединениями. Соответственно, соединения изобретения являются эффективными для профилактики, ингибирования или лечения аутоиммунного нарушения или заболевания, воспалительного нарушения или заболевания,или рака. Также здесь обеспечено применение соединений для производства медицинских препаратов для профилактики, ингибирования или лечения воспалительных и/или аутоиммунных нарушений или заболеваний, или рака. В одном варианте изобретение обеспечивает способы профилактики, ингибирования или лечения рака у субъекта, который включает введение соединения, имеющего структуру согласно формулам I, II или III, субъекту, нуждающемуся в этом, в количестве, эффективном для профилактики,ингибирования или лечения рака. В одном варианте соединение изобретения вводится субъекту с раковым заболеванием, таким как лимфома Ходжкина, неходжскинская лимфома, лейкемия, множественная миелома или опухоль мозга, при котором показаны кортикостероиды, например дексаметазон, преднизилон, метилпреднизолон или гидрокортизон. В одном варианте соединение изобретения вводится субъекту, имеющему риск ракового заболевания, развитие которого связано с воспалением, например рак кишечника. Таким образом, изобретение обеспечивает соединения, предназначенные для применения в медицинской терапии, а именно агенты, которые предупреждают, ингибируют или лечат раковые заболевания, факультативно в сочетании с другими соединениями. Таким образом, соединения технологии являются эффективными для профилактики, ингибирования или лечения разных аутоиммунных нарушений/заболеваний, воспалительных нарушений/заболевании и злокачественных новообразований. Перечень фигур Чертежи иллюстрируют варианты изобретения и не являются ограничением. Следует отметить, что для ясности и простоты иллюстрации данные чертежи не сделаны в масштабе и что в некоторых случаях разные варианты изобретения могут показаться увеличенными или укрупненными для облегчения понимания конкретных вариантов. В данном документе используются следующие сокращения. Toll-подобный рецептор (TLR), липополисахарид (LPS), белок первичного ответа миелоидной дифференциации (88) (MyD88), мононуклеарные клетки костного мозга (BMDM), мононуклеарные клетки периферической крови (РВМС), полиэтиленгликоль (PEG), этанол (EtOH), тетрагидрофуран (THF), 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин(pDC), овальбумин (OVA), мышиный сывороточный альбумин (MSA), человеческий сывороточный альбумин (HSA) и иммуноглобулин (Ig). Фиг. 1 иллюстрирует схему, которую использовали для синтеза липид- (6), PEG- (8) или липид-PEG(9) TLR7 конъюгатов. (6), (8) и (9) относятся к обозначениям соединений. Фиг. 2A-2D отражают результаты иммунологической характеристики in vitro конъюгатов TLR7 в мышиных макрофагах. Фиг. 2 Е отражает результаты оценки контаминации эндотоксином с использованием не отвечающих на LPS макрофагов мутантного и дикого типов. Фиг. 3 А, 3 В отражают результаты иммунологической характеристики in vitro конъюгатов TLR7 в человеческих РВМС. Фиг. 4 А, 4 В иллюстрируют кинетику индукции провоспалительных цитокинов конъюгатами TLR7in vivo. Фиг. 5 А-5 С иллюстрируют адъювантные свойства (например, способность инициировать иммунный ответ) конъюгатов TLR7 in vivo. Фиг. 6 А-6 С отражают результаты оценки возможных побочных эффектов конъюгатов TLR7. Фиг. 7 А, 7 В иллюстрируют снижение перитонеальной инфильтрации нейтрофилами путем обработки с помощью 1V136 (свободный фармакофор) и 1V282 (соединение 8). Фиг. 8 иллюстрирует эффект обработки 1V282 (соединение (8 на индуцированный экспериментальный аутоиммунный энцефаломиелит (ЕАЕ). Фиг. 9 А-9 Е показывает in vitro активность конъюгатов агониста TLR7 при изменении длин цепей на клетки NFkBbla RAW 264.7 и макрофаги костного мозга (BMDM). Фиг. 10 А-10 С отражает in vivo фармакодинамику конъюгатов агонист TLR7-PEG, введенных мышам. Фиг. 11 А, 11 В иллюстрируют противовоспалительные эффекты 1V282, вводимого ежедневно через зонд (А) или подкожной инъекцией (В), в модели артрита, инициированного переносом сыворотки. Фиг. 12 А, 12 В показывают противовоспалительный эффект конъюгатов агонист TLR7-PEG в модели артрита, индуцированного тиогликолятом. Сведения, подтверждающие возможность осуществления изобретения Обеспечены низкомолекулярные конъюгаты, которые являются агонистами или антагонистами одного или более Toll-подобных рецепторов. Такие конъюгаты могут быть использованы различными способами, включающими, но без ограничения, лечение состояний, таких как, например, аутоиммунные,воспалительные и клеточные пролиферативные нарушения или заболевания. Соединения. Известны низкомолекулярные модуляторы TLR. Примеры низкомолекулярных соединений описаны в Американском патенте 6329381, выданном 11 декабря 2001 г., вытекающем из заявки на патент 09/555292, поданной 26 мая 2000 г., и в PCT/US2006/032371, поданной 21 августа 2006 г. (опубликованной как WO 2007/024707 1 марта 2007 г.); PCT/US2008/001631, поданной 7 февраля 2008 г. (опубликована как WO 2008/115319 25 сентября 2008 г.); PCT/US07/009840, поданной 23 апреля 2007 г. (опубликована как WO 2007/142755 13 декабря 2007 г.); и Американской предварительной заявки 61/026999, поданной 7 февраля 2008 г. Установлено, что определенные низкомолекулярные агонисты TLR (например, называемые здесь как "низкомолекулярная мишень") могут быть конъюгированы с одним или более фрагментами PEG, и полученный конъюгат может проявлять активность антагониста TLR. Существует несколько известных способов конъюгации низкомолекулярной мишени с одним или более фрагментами PEG. Например, несколько PEG реактантов являются коммерчески доступными и пригодными для конъюгации с разными реакционноспособными группами на низкомолекулярных соединениях (например, NOF Corporation,Япония (World Wide Web URL peg-drag.com/pegproduct/activatedpeg.html. Использующийся здесь термин "PEG реактант" относится к молекуле, которая соединена с низкомолекулярной мишенью в условиях, которые генерируют продукт конъюгации PEG-низкомолекулярная мишень. Например, определенные PEG реактанты, имеющие следующую структуру, могут взаимодействовать с разными целевыми группами на низкомолекулярном соединении: СН 3 О(СН 2 СН 2 О)n-X, где X представляет собой реакционноспособную группу согласно табл. 1.NHS представляет собой N-сукцинимидил. В некоторых вариантах PEG реактант имеет структуру СН 3 О(СН 2 СН 2 О)n-Х-NHS, где X может быть -СОСН 2 СН 2 СОО-, -СОСН 2 СН 2 СН 2 СОО-, -СН 2 СОО- и -(CH2)5COO-. В определенных вариантах В некоторых вариантах определенные PEG реактанты являются бифункциональными. Примеры бифункциональных PEG реактантов имеют структуру X-(ОСН 2 СН 2)n-X, где X представляет собой (Nсукцинимидилоксикарбонил)метил (CH2COO-NHS), сукцинимидилглутарат (-COCH2CH2CH2COO-NHS),(N-сукцинимидилоксикарбонил)пентил(-(CH2)5COO-NHS),3-(N-малеимидил)пропанамидо,(-NHCOCH2CH2-MAL), аминопропил (-CH2CH2CH2NH2) или 2-сульфанилэтил (-CH2CH2SH), в некоторых вариантах. В определенных вариантах некоторые PEG реактанты являются гетерофункциональными. Примеры гетерофункциональных PEG реактантов имеют структуры где X может представлять собой (N-сукцинимидилоксикарбонил)метил (CH2COO-NHS), сукцини-6 019768 мидилглутарат (-COCH2CH2CH2COO-NHS), (N-сукцинимидилоксикарбонил)пентил (-(CH2)5COO-NHS),3-(N-малеимидил)пропанамидо, (-NHCOCH2CH2-MAL), 3-аминопропил (-CH2CH2CH2NH2), 2 сульфанилэтил (-CH2CH2SH), 5-(N-сукцинимидилоксикарбонил)пентил (-(СН 2)5 СОО-NHS) или рнитрофенилоксикарбонил, (-CO2-p-C6H4NO2), в некоторых вариантах. Также могут использоваться определенные разветвленные PEG реактанты, а именно такие, которые имеют структуру где X представляет собой спейсер и Y представляет собой функциональную группу, включающую,но без ограничения, малеимид, амин, глутарил-NHS, карбонат-NHS или карбонат-р-нитрофенол, в некоторых вариантах. Преимуществом PEG реактантов с разветвленной цепью является получение продуктов конъюгации, обладающих свойствами замедленного высвобождения. Также PEG реактант в определенных вариантах может быть гетерофункциональным реактантом,таким как В некоторых вариантах могут использоваться Вос-защищенный-амино-PEG-карбоксил-NHS или малеимид-PEG-карбоксил-NHS реактанты. В определенных вариантах в качестве PEG реактанта может быть использован гребенчатый полимер для введения некоторого количества PEG звеньев в конъюгат. Пример гребенчатого полимера показан ниже. В контексте PEG реактантов, специально показанных в данном разделе под названием "Соединения", заместитель "n" или "m", показанный только в PEG реактантах, равен "r", определенному выше для формулы I, II или III, в некоторых вариантах. PEG реактант и/или продукт конъюгации PEG, может иметь молекулярную массу, изменяющуюся примерно от 5 до 100,000 грамм на моль. В некоторых вариантах PEG реактант и/или продукт конъюгации PEG имеет среднюю или номинальную молекулярную массу, примерно, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 2000,3000, 4000, 5000, 6000, 7000, 8000, 9000, 10000, 20000, 30000, 40000, 50000, 60000, 70000, 80000 или 90000 г на 1 моль. В некоторых вариантах PEG фрагмент в указанном здесь соединении является гомогенным и молекулярная масса PEG фрагмента является одинаковой для каждой молекулы конкретной партии соединения (например, R3 представляет собой одно из PEG звеньев и r равно от 2 до 10). В определенных вариантах один или более R4 заместителей заканчивают PEG фрагмент (например,формула I; линейный или разветвленный PEG фрагмент). Каждый R4 заместитель может быть одинаковым или разным, и в некоторых вариантах независимо может быть выбран из группы, состоящей из-CH2-CH2-NH2, -СН 2-СН 2-ОН, -СН 2-СН 2-СООН, -CH2-CH2-COOR1. Линкером может быть любой пригодный линкер, включая линкер, описанный здесь. Пригодный линкер может быть использован для образования конъюгатов (например, X2, X3), и известно множество линкеров. Неограничивающие примеры линкеров, которые могут использоваться,включают следующие: Использующиеся здесь термины "алкил", "алкенил" и "алкинил" включают моновалентные углеводородные радикалы с прямой цепью, разветвленной цепью и циклические, и их комбинации, которые содержат только С и Н, когда они являются незамещенными. Примеры включают метил, этил, изобутил,циклогексил, циклопентилэтил, 2-пропенил, 3-бутинил и подобные. Общее число атомов углерода в каждой такой группе в некоторых случаях описано здесь, например, когда группа может содержать до десяти атомов углерода, это может быть представлено как 1-10 С или С 1-С 10 или С 1-10. В случаях, когда допускается замена гетероатомами (как правило, N, О и S) атомов углерода, как, например, в гетероалкильных группах, описывающие группу числа, несмотря на написание в виде, например, C1-C6, являются суммой числа атомов углерода в группе плюс число таких гетероатомов, которые включены в качестве заменителей атомов углерода в остове описываемого кольца или цепи. Как правило, алкильные, алкенильные и алкинильные заместители изобретения содержат один 10 С(алкил) или два 10 С (алкенил или алкинил). Предпочтительно, чтобы они содержали один 8 С (алкил) или два 8 С (алкенил или алкинил). В некоторых случаях они содержат один 4 С (алкил) или два 4 С (алкенил или алкинил). Одна группа может включать более одного типа кратной связи или более одной кратной связи; такие группы включены в определение термина "алкенил", когда они содержат по меньшей мере одну двойную связь углерод-углерод, и включены в определение термина "алкинил", когда они содержат по меньшей мере одну тройную связь углерод-углерод. Алкильные, алкенильные и алкинильные группы часто являются факультативно замещенными, при условии, что такое замещение химически целесообразно. Типичные заместители включают, но не ограничиваются, гало, =O, =N-CN, =N-OR, =NR, OR, NR2, SR, SO2R, SO2NR2, NRSO2R, NRCONR2, NRCOOR,NRCOR, CN, COOR, CONR2, OOCR, COR и NO2, где каждый R независимо представляет собой Н, С 1-С 8 алкил, С 2-С 8-гетероалкил, С 1-С 8-ацил, С 2-С 8-гетероацил, С 2-С 8-алкенил, С 2-С 8-гетероалкенил, С 2-С 8 алкинил, С 2-С 8-гетероалкинил, C6-C10-арил или С 5-С 10-гетероарил, каждый R является факультативно замещенным гало, =О, =N-CN, =N-OR', =NR', OR', NR'2, SR', SO2R', SO2NR'2, NR'SO2R', NR'CONR'2,NR'COOR', NR'COR', CN, COOR', CONR'2, OOCR', COR' и NO2, где каждый R' независимо представляет собой Н, С 1-С 8-алкил, С 2-С 8-гетероалкил, С 1-С 8-ацил, С 2-С 8-гетероацил, C6-C10-арил или С 5-С 10 гетероарил. Алкильные, алкенильные и алкинильные группы также могут быть замещенными С 1-С 8 ацилом, С 2-С 8-гетероацилом, C6-C10-арилом или С 5-С 10-гетероарилом, каждый из которых может быть замещенным заместителями, которые пригодны для конкретной группы."Ацетиленовые" заместители представляют собой C2-C10-алкинильные группы, которые являются факультативно замещенными и имеют формулу -CC-Ri, где Ri представляет собой Н или С 1-С 8-алкил,С 2-С 8-гетероалкил, С 2-С 8-алкенил, С 2-С 8-гетероалкенил, С 2-С 8-алкинил, С 2-С 8-гетероалкинил, С 1-С 8-ацил,С 2-С 8-гетероацил, C6-C10-арил, С 5-С 10-гетероарил, С 7-С 12-арилалкил или С 6-С 12-гетероарилалкил, и каждая Ri группа является факультативно замещенной одним или более заместителей, выбранных из гало,=О, =N-CN, =N-OR', =NR', OR', NR'2, SR', SO2R', SO2NR'2, NR'SO2R', NR'CONR'2, NR'COOR', NR'COR',CN, COOR', CONR'2, OOCR', COR' и NO2, в которых каждый R' независимо представляет собой Н, C1-C6 алкил, С 2-С 6-гетероалкил, C1-C6-ацил, С 2-С 6-гетероацил, C6-C10-арил, С 5-С 10-гетероарил, С 7-C12 арилалкил или С 6-12 гетероарилалкил, каждый из которых является факультативно замещенным одной или более группами, выбранными из гало, С 1-С 4-алкила, С 1-С 4-гетероалкила, C1-C6-ацила, C1-C6 гетероацила, гидрокси, амино и =О; и в которых два R' могут быть связаны для формирования 3-7 членного кольца, факультативно содержащего до трех гетероатомов, выбранных из N, О и S. В некоторых вариантах Ri в -CC-Ri представляет собой Н или Me."Гетероалкил", "гетероалкенил" и "гетероалкинил" и т.п. определены аналогично соответствующим гидрокарбильным (алкильным, алкенильным и алкинильным) группам, но "настоящие" термины относятся к группам, которые содержат от одного до трех О, S или N гетероатомов или их комбинацию в остатке остова; таким образом, по меньшей мере один атом углерода соответствующей алкильной, алке-8 019768 нильной или алкинильной группы заменен одним из указанных гетероатомов для образования гетероалкильной, гетероалкенильной или гетероалкинильной групп. Типичные и предпочтительные размеры гетероатомов алкильной, алкенильной и алкинильной групп в целом являются такими же, как для соответствующих гидрокарбильных групп, и заместители, которые могут присутствовать на гетероформах, являются такими, которые описаны выше для гидрокарбильных групп. Из соображений химической стабильности должно быть понятно, что если не указано иное, такие группы не включают более двух смежных гетероатомов, за исключением, когда оксо группа присутствует на N или S, как в нитро или сульфонильной группе. Несмотря на то что использующийся здесь термин "алкил" включает циклоалкильную и циклоалкилалкильную группы, термин "циклоалкил" может использоваться здесь для описания карбоциклической неароматической группы, которая соединена посредством кольцевого атома углерода, и "циклоалкилалкил" может использоваться для описания карбоциклической неароматической группы, которая соединена с молекулой через алкильный линкер. Аналогично, "гетероциклил" может использоваться для описания неароматической циклической группы, которая содержит по меньшей мере один гетероатом в качестве члена кольца, и которая соединена с молекулой посредством кольцевого атома, которым может являться С или N; и "гетероциклилалкил" может использоваться для описания такой группы, которая соединена с другой молекулой с помощью линкера. Размеры и заместители, которые являются пригодными для циклоалкильной, циклоалкилалкильной, гетероциклильной и гетероциклилалкильной групп являются такими же, которые описаны выше для алкильных групп. Использующиеся здесь данные термины также включают кольца, которые содержат двойную связь или две, при условии, что кольцо не является ароматическим. Использующийся здесь термин "ацил" охватывает группы, включающие алкильный, алкенильный,алкинильный, арильный или арилалкильный радикал, присоединенный к одному или двум положениям со свободными валентностями карбонильного атома углерода, и гетероацил относится к соответствующим группам, в которых по меньшей мере один атом углерода, отличный от карбонильного углерода,заменен гетероатомом, выбранным из N, О и S. Таким образом, гетероацил включает, например,-C(=O)OR и -C(=O)NR2, а также -С(=О)-гетероарил. Ацильные и гетероацильные группы присоединены к любой группе или молекуле, к которой они присоединены посредством открытой валентности карбонильного атома углерода. Как правило, они представляют собой С 1-С 8-ацильные группы, которые включают формил, ацетил, пивалоил и бензоил, и С 2-С 8-гетероацильные группы, которые включают метоксиацетил, этоксикарбонил и 4-пиридиноил. Гидрокарбильные группы, арильные группы и гетероформы таких групп, которые включают ацильную или гетероацильную группу, могут быть замещенными заместителями, описанными здесь как в целом пригодные заместители для каждого из соответствующих компонентов ацильной или гетероацильной группы."Ароматический" фрагмент или "арильный" фрагмент относится к моноциклическому или конденсированному бициклическому фрагменту, имеющему хорошо известные характеристики ароматичности; примеры включают фенил и нафтил. Аналогично, "гетероароматический" и "гетероарильный" относятся к таким моноциклическим или конденсированным бициклическим кольцевым системам, которые содержат в качестве членов кольца один или более гетероатомов, выбранных из О, S и N. Включение гетероатома обеспечивает ароматичность в 5-членных кольцах, а также 6-членных кольцах. Типичные гетероароматические системы включают моноциклические С 5-С 6-ароматические группы, такие как пиридил,пиримидил, пиразинил, тиенил, фуранил, пирролил, пиразолил, тиазолил, оксазолил и имидазолил, и конденсированные бициклические фрагменты, образованные слиянием одной из этих моноциклических групп с фенильным кольцом или с любой из гетероароматических моноциклических групп с образованием С 8-С 10-бициклической группы, такой как индонил, бензимидазолил, индазолил, бензотриазолил, изохинолил, хинолил, бензотиазолил, бензофуранил, пиразолопиридил, хиназолинил, хиноксалинил, циннолинил и т.п. Любая моноциклическая или конденсированная кольцевая бициклическая система, которая имеет характеристики ароматичности на основании распределения электронов по кольцевой системе,является включенной в данное определение. Термин также включает бициклические группы, в которых,по меньшей мере, кольцо, которое напрямую присоединено к остатку молекулы, имеет характеристики ароматичности. Как правило, кольцевые системы содержат 5-12 атомов в гетероцикле. Предпочтительно,чтобы моноциклические гетероарилы содержали 5-6 атомов в гетероцикле и бициклические гетероарилы содержали 8-10 атомов в гетероцикле. Арильные и гетероарильные фрагменты могут быть замещенными разными заместителями, включающими С 1-С 8-алкил, С 2-С 8-алкенил, С 2-С 8-алкинил, С 5-С 12-арил, С 1-С 8-ацил и их гетероатомы, каждый из которых может быть, кроме того, замещенным; другие заместители для арильных и гетероарильных фрагментов включают гало, OR, NR2, SR, SO2R, SO2NR2, NRSO2R, NRCONR2, NRCOOR, NRCOR, CN,COOR, CONR2, COCR, COR и NO2, где каждый R независимо представляет собой Н, С 1-С 8-алкил, С 2-С 8 гетероалкил, С 2-С 8-алкенил, С 2-С 8-гетероалкенил, С 2-С 8-алкинил, С 2-С 8-гетероалкинил, C6-C10-арил, С 5 С 10-гетероарил, С 7-С 12-арилалкил или С 6-С 12-гетероарилалкил, и каждый R является факультативно замещенным, как описано выше для алкильных групп. Группы заместителей на арильной или гетероариль-9 019768 ной группе, как известно, могут быть к тому же замещенным группами, описанными здесь, пригодными для каждого типа таких заместителей или для каждого компонента заместителя. Таким образом, например, арилалкильный заместитель может быть замещенным на арильную часть заместителями, описанными здесь, что характерно для арильных групп, и может быть к тому же замещенным на алкильную часть заместителями, описанными здесь, что характерно или приемлемо для алкильных групп. Аналогично, "арилалкил" и "гетероарилалкил" относятся к ароматическим и гетероароматическим кольцевым системам, которые присоединены к их месту присоединения посредством связующей группы,такой как алкилен, включая замещенные или незамещенные, насыщенные или ненасыщенные, циклические или ациклические линкеры. Как правило, линкером является С 1-С 8-алкил или его гетероформа. Данные линкеры могут также включать карбонильную группу, делая их, таким образом, способными обеспечить заместители, как ацильный или гетероацильный фрагмент. Арильное или гетероарильное кольцо в арилалкильной или гетероарилалкильной группе может быть замещенным такими же заместителями, которые описаны выше для арильных групп. Предпочтительно, чтобы арилалкильная группа включала фенильное кольцо, факультативно замещенное группами, определенными выше для арильных групп, и С 1-С 4-алкилен, который является незамещенным или замещенным одной или двумя С 1-С 4 алкильными группами или гетероалкильными группами, в которых алкильные или гетероалкильные группы могут быть факультативно циклизированы с образованием кольца, такого как циклопропан, диоксолан или оксациклопентан. Аналогично, гетероарилалкильная группа предпочтительно включает С 5 С 6-моноциклическую гетероарильную группу, которая является факультативно замещенной группами,описанными выше в качестве заместителей, как правило, на арильных группах, и С 1-С 4-алкилен, который является незамещенным или замещенным одной или двумя С 1-С 4-алкильными группами или гетероалкильными группами, или включает факультативно замещенное фенильное кольцо или С 5-С 6 моноциклический гетероарил и С 1-С 4-гетероалкилен, который является незамещенным или замещенным одной или двумя С 1-С 4-алкильными или гетероалкильными группами, где алкильные или гетероалкильные группы могут факультативно циклизироваться с образованием кольца, такого как циклопропан, диоксолан или оксациклопентан. В случае, когда арилалкильная или гетероарилалкильная группа описана как факультативно замещенная, заместители могут быть на алкильной или гетероалкильной части, или на арильной или гетероарильной части группы. Заместители, факультативно присутствующие на алкильной или гетероалкильной части, являются такими, которые в целом описаны выше для алкильных групп; заместители, факультативно присутствующие на арильной или гетероарильной части, являются такими, которые в целом описаны выше для арильных групп. Использующиеся здесь "арилалкильные" группы являются гидрокарбильными группами, если они незамещенные, и описаны общим числом атомов углерода в кольце и алкилене или аналогичном линкере. Таким образом, бензильная группа представляет собой С 7-арилалкильную группу и фенилэтил представляет собой С 8-арилалкил. Описанный выше "гетероарилалкил" относится к фрагменту, включающему арильную группу, которая присоединена посредством линкерной группы, и отличается от "арилалкила" тем, что по меньшей мере один атом кольца арильного фрагмента или один атом в линкерной группе является гетероатомом,выбранным из N, О и S. Гетероарилалкильные группы описаны здесь в соответствии с общим числом атомов в кольце и линкере, и включают арильные группы, связанные посредством гетероалкильного линкера; гетероарильные группы, связанные посредством гидрокарбильного линкера, такого как алкилен; и гетероарильные группы, связанные посредством гетероалкильного линкера. Таким образом, например, С 7-гетероарилалкил будет включать пиридилметил, фенокси и N-пирролилметокси. Использующийся здесь "алкилен" относится к бивалентной гидрокарбильной группе; так как он является бивалентным, он может связывать вместе две другие группы. Как правило, он относится к-(СН 2)n-, где n равно 1-8 и предпочтительно n равно 1-4, но если специально оговорено, алкилен может быть также замещенным другими группами и иметь другую длину, и не требуется открытых валентностей на противоположных концах цепи. Таким образом, -СН(Ме)- и -С(Ме)2- могут также называться алкиленами, также как циклическая группа, такая как циклопропан-1,1-диил. В случаях, когда алкиленовая группа является замещенной, заместители включают такие, которые обычно присутствуют на алкильных группах, как описано здесь. В целом, любая алкильная, алкенильная, алкинильная, ацильная, или арильная, или арилалкильная группа, или любая гетероформа одной из этих групп, которая содержится в заместителе, может сама по себе быть факультативно замещенной дополнительными заместителями. Природа данных заместителей аналогична заместителям, которые перечислены в отношении самих первичных заместителей, если заместители не описаны иначе. Таким образом, в случаях, когда вариантом, например, R2 является алкил,данный алкил может быть факультативно замещенным оставшимися заместителями, приведенными в качестве вариантов для R2, если это имеет химический смысл и не нарушает предельный размер, предусмотренный для самого алкила; например, алкил, замещенный алкилом или алкенилом, будет только расширять верхний предел числа атомов углерода для этих вариантов, и не является включенным. Однако, алкил, замещенный арилом, амино, алкокси, =О и подобными, будет включен в объем изобретения, и атомы этих групп заместителей не учитывают в числе, которое используется для описания алкила, алкенила и других описанных групп. Если не указано число заместителей, то каждая такая алкильная, алкенильная, алкинильная, ацильная или арильная группа может быть замещенной числом заместителей согласно ее свободными валентностями; в частности, любая из этих групп может быть замещенной, например, атомами фтора в любой или во всех ее свободных валентностях. Использующийся здесь термин "гетероформа" относится к производному группы, такой как алкил,арил или ацил, в которой по меньшей мере один атом углерода указанной карбоциклической группы заменен гетероатомом, выбранным из N, О или S. Таким образом, гетероформами алкила, алкенила, алкинила, ацила, арила и арилалкила являются соответственно гетероалкил, гетероалкенил, гетероалкинил,гетероацил, гетероарил и гетероарилалкил. Следует понимать, что, как правило, не более чем два атомаN, О или S соединены последовательно, за исключением тех случаев, когда оксо группа присоединена кN или S с образованием нитро или сульфонильной группы. Гетероформный фрагмент в отдельных случаях называется здесь как "Het". Использующийся здесь термин "гало" или "галоген" включает фтор, хлор, бром и йод. Чаще всего предпочтительными являются фтор и хлор. Использующийся здесь "амино" относится к NH2, но в случаях, когда амино описан как "замещенный" или "факультативно замещенный", термин включает NR'R",где каждый R' и R" независимо представляет собой Н или является алкильной, алкенильной, алкинильной, ацильной, арильной или арилалкильной группой, или гетероформой одной из этих групп, и каждая из алкильной, алкенильной, алкинильной, ацильной, арильной или арилалкильной групп, или гетероформа одной из этих групп является факультативно замещенной заместителями, описанными здесь как пригодные для соответствующей группы. Термин также включает формы, в которых R' и R" связаны вместе с образованием 3-8-членного кольца, которое может быть насыщенным, ненасыщенным или ароматическим, и которое содержит 1-3 гетероатомов, независимо выбранных из N, О и S в качестве членов кольца, и которое является факультативно замещенным заместителями, описанными как пригодные для алкильных групп или, если NR'R" является ароматической группой, то эта группа является факультативно замещенной заместителями, описанными как типичные для гетероарильных групп. Использующийся здесь термин "карбоцикл" относится к циклическому соединению, содержащему только атомы углерода в кольце, в то время как "гетероцикл" относится к циклическому соединению,содержащему гетероатом. Карбоциклические и гетероциклические структуры охватывают соединения,имеющие моноциклические, бициклические или множественные кольцевые системы. Использующийся здесь термин "гетероатом" относится к любому атому, который не является углеродом или водородом,такому как азот, кислород или сера. Иллюстративные примеры гетероциклов включают, но без ограничения, тетрагидрофуран, 1,3-диоксолан, 2,3-дигидрофуран, пиран, тетрагидропиран, бензофуран, изобензофуран, 1,3-дигидроизобензофуран, изоксазол, 4,5-дигидроизоксазол, пиперидин, пирролидин, пирролидин-2-она, пиррол, пиридин, пиримидин, октагидропирроло[3,4-b]пиридин, пиперазин, пиразин, морфолин, тиоморфолин, имидазол, имидазолидин-2,4-диона, 1,3-дигидробензимидазол-2-она, индол, тиазол, бензотиазол, тиадиазол, тиофен, тетрагидротиофен-1,1-диоксид, диазепин, триазол, гуанидин, диазабицикло[2.2.1]гептан, 2,5-диазабицикло[2.2.1]гептан, 2,3,4,4 а,9,9 а-гексагидро-1 Н-бета-карболин, оксиран, оксетан, татрагидропиран, диоксан, лактоны, азиридин, азетидин, пиперидин, лактамы и может также охватывать гетероарилы. Другие иллюстративные примеры гетероарилов включают, но без ограничения, фуран, пиррол, пиридин, пиримидин, имидазол, бензимидазол и триазол. В некоторых случаях описанные здесь соединения содержат один или более хиральных центров. Изобретение включает каждую из изолированных стереоизомерических форм, а также смеси стереоизомеров с изменяющейся степенью хиральной чистоты, включая рацемические смеси. Также охваченными являются разные диастереомеры и таутомеры, которые могут быть образованы. Соединения изобретения могут также существовать в одной или более таутомерных формах. Например, когда R представляет собой -ОН, описанное здесь соединение может существовать в одной или более таутомерных формах. Использующийся здесь термин "факультативно замещенный" указывает, что конкретная группа или группы, описанные здесь, могут не содержать неводородные заместители, или группа или группы могут содержать один или более неводородных заместителей. Если не указано иначе, общее число таких заместителей, которые могут присутствовать, равно количеству атомов Н, присутствующих на незамещенной форме описываемой группы. В случаях, когда факультативный заместитель присоединен посредством двойной связи, такой как карбонильный кислород (=O), группа захватывает две свободные валентности,таким образом, общее число заместителей, которое может быть включено, является уменьшенным в соответствии с числом свободных валентностей. Фармацевтические композиции и составы. Описанное здесь соединение может быть приготовлено в виде фармацевтически приемлемой соли. Использующийся здесь термин "фармацевтически приемлемая соль" относится к производному раскрытых соединений, в которых родительское соединение модифицировано путем приготовления их солей с кислотами и основаниями. Примеры фармацевтически приемлемых солей включают, но без ограничения,соли минеральных или органических кислот по основным остаткам, таким как амины; соли щелочных металлов или органические соли по кислым остаткам, таким как карбоновые кислоты и т.п. Фармацевти- 11019768 чески приемлемые соли включают обычно используемые нетоксичные соли или четвертичные аммониевые соли родительского соединения, образованные, например, из нетоксичных неорганических или органических кислот. Например, обычно используемые нетоксичные соли включают такие, которые получены из неогранических кислот, таких как соляная, бромисто-водородная, серная, сульфаминовая, фосфорная, азотная и подобных; и соли, приготовленные из органических кислот, такие как уксусная, пропионовая, янтарная,гликолевая, стеариновая, молочная, яблочная, винная, лимонная, аскорбиновая, памовая, малеиновая,гидроксималеиновая, фенилуксусная, глутаминовая, бензойная, салициловая, сульфаниловая, 2 ацетоксибензойная, фумаровая, толуолсульфоновая, метансульфоновая, этандисульфоновая, щавелевая,изэтионовая и подобные. В других примерах типичные нетоксичные соли включают такие соли, которые получены из оснований, таких как гидроксид калия, гидроксид натрия, гидроксид аммония, кофеин, разные амины и подобные. Фармацевтически приемлемые соли могут быть синтезированы традиционными химическими способами из родительского соединения, которое содержит основную или кислую группу. В целом, такие соли могут быть приготовлены путем взаимодействия свободных кислых или основных форм этих соединений со стехиометрическим количеством соответствующего основания или кислоты в воде, или в органическом растворителе, или в смеси их обоих; в целом, предпочтительной является неводная среда, такая как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Перечень пригодных солей содержится в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, PA, p. 1418 (1985), раскрытие которого представлено здесь посредством отсылки. Использующийся здесь термин "фармацевтически приемлемый" относится к соединениям, материалам, композициям и/или лекарственным формам, которые являются, в пределах объема тщательной медицинской оценки, пригодными для использования в контакте с тканями человека и животных без избыточной токсичности, раздражения, аллергической реакции или других проблем или жалоб, соизмеримых с приемлемым соотношением польза/риск. Термины "стабильное соединение" и "стабильная структура" указывают на соединение, которое является достаточно устойчивым для того, чтобы выдержать выделение до приемлемой степени чистоты из реакционной смеси, и составления в эффективный терапевтический агент. Стабильные соединения предусмотрены здесь для применения в описанных способах терапии. Описанное здесь соединение может быть составлено в комбинации с одним или более других агентов. Один или более других агентов могут включать, без ограничения, другое описанное здесь соединение, агент против клеточной пролиферации (например, химиотерапевтический), противовоспалительный агент и антиген. Описанное здесь соединение может быть составлено в виде фармацевтической композиции и вводиться хозяину-млекопитающему, такому как пациент - человек или животное, в разных формах, приспособленных для выбранного режима введения, например орального или парентерального, внутривенного, внутримышечного, местного или подкожного режимов. В определенных вариантах композиция вводится местно, например внутрипузырно. Композиция часто включает разбавитель, а также, в некоторых случаях, адъювант, буфер, консервант и т.п. Соединение может также вводиться в виде липосомальной композиции или, в определенных вариантах, в виде микроэмульсии. Также разработаны разные системы с замедленным высвобождением лекарственных средств, которые могут применяться к описанному здесь соединению. См., например, патент США 5624677, способы которого включены здесь посредством отсылки. Таким образом, соединения могут вводиться системно, например орально, в комбинации с фармацевтически приемлемым носителем, таким как инертный разбавитель или усваиваемый пищевой носитель. Описанные здесь соединения могут быть заключены в желатиновые капсулы с твердой или мягкой оболочкой, могут быть прессованы в таблетки или введены напрямую с пищей диеты пациента. Для орального терапевтического введения активное соединение может быть объединено с одним или более вспомогательных веществ и применяться в форме таблеток для проглатывания, таблеток для медленного растворения в щечном кармане, пастилок, капсул, эликсиров, суспензий, сиропов, облаток и подобных. Такие композиции и составы должны содержать по меньшей мере 0,1% активного соединения. Процент композиций и составов может, безусловно, изменяться и, как правило, составляет примерно от 2 до 60% массы заданной стандартной лекарственной формы. Количество активного соединения в таких терапевтически эффективных композициях является таким, которое обеспечивает получение эффективного уровня дозы. Таблетки, пастилки, драже, капсулы и подобные могут также содержать следующее: связующие,такие как трагант, камедь, кукурузный крахмал или желатин; вспомогательные вещества, такие как дикальция фосфат; дезинтеграторы, такие как кукурузный крахмал, картофельный крахмал, альгиновую кислоту и подобные; лубрикант, такой как стеарат магния; и может быть добавлен подсластитель, такой как сахароза, фруктоза, лактоза или аспартам, или ароматизатор, такой как мята перечная, масло грушанки или вишневый ароматизатор. В случае, когда стандартная лекарственная форма представляет собой капсулу, она может содержать, дополнительно к материалам указанного выше типа, жидкий носитель,- 12019768 такой как растительное масло или полиэтиленгликоль. Другие различные материалы могут присутствовать в качестве покрытий или для изменения физической формы твердой стандартной лекарственной формы. Например, таблетки, драже или капсулы могут быть покрыты желатином, воском, шеллаком или сахаром и подобными. Сироп или эликсир может содержать активное соединение, сахарозу или фруктозу в качестве подсластителя, метил и пропилпарабены в качестве консервантов, краситель и ароматизатор,такой как вишневый или апельсиновый ароматизатор. Конечно, любой материал, который используется для приготовления любой стандартной лекарственной формы, должен быть фармацевтически приемлемым и главным образом нетоксичным в применяемых количествах. К тому же, активное соединение может быть внедрено в составы и устройства с замедленным высвобождением. Активное соединение может вводиться путем инфузии или инъекции. Растворы активного соединения или его фармацевтически приемлемой соли могут быть приготовлены в воде, факультативно смешанной с нетоксичным поверхностно-активным веществом. Дисперсии также могут быть приготовлены в глицерине, жидких полиэтиленгликолях, триацетине и их смесях, а также в маслах. В обычных условиях хранения и применения данные составы содержат консервант для предотвращения роста микроорганизмов. Фармацевтическая лекарственная форма может включать стерильный водный раствор или дисперсию, или стерильный порошок, включающий активный компонент, который адаптирован для экстемпорального приготовления стерильных растворов или дисперсий, и факультативно инкапсулирован в липосомы. Готовая лекарственная форма иногда представляет собой стерильную жидкость и является стабильной в условиях производства и хранения. Жидкий носитель или наполнитель может являться растворителем или жидкой дисперсионной средой, включающей, например, воду, этанол, полиол (например,глицерин, пропиленгликоль, жидкие полиэтиленгликоли и подобные), растительные масла, нетоксичные эфиры глицерина и их пригодные смеси. Собственная текучесть может поддерживаться, например, с помощью образования липосом, путем сохранения требуемого размера частиц в случае дисперсий или с помощью использования поверхностно-активных веществ. Предотвращение действия микроорганизмов может быть осуществлено с помощью разных антибактериальных и противогрибковых агентов, например парабенов, хлорбутанола, фенола, сорбиновой кислоты, тимеросала и т.п. Изотонический агент, например сахар, буфер или хлорид натрия, является включенным в некоторые варианты. Пролонгированную абсорбцию инъецируемой композиции можно осуществить путем использования в композиции задерживающих абсорбцию агентов, например моностеарата алюминия и желатина. Стерильные растворы часто готовят путем внедрения активного соединения в требуемом количестве в соответствующий растворитель, иногда с одним или более других ингредиентов, перечисленных выше, с последующей стерилизацией путем фильтрации. В случае стерильных порошков для приготовления стерильных инъецируемых растворов, иногда использующимися способами приготовления являются методы вакуумной сушки и лиофилизации, которые позволяют получить порошок активного ингредиента дополнительно к любому дополнительно необходимому ингредиенту, присутствующему в предварительно стерильно отфильтрованных растворах. Для местноговведения соединение данного изобретения может применяться в чистой форме, например, когда находится в жидкой форме. Однако, в целом, желательно вводить соединение в виде композиции или состава в комбинации с приемлемым носителем, который может быть твердым веществом или жидкостью. Эффективные твердые носители включают высокодисперсные твердые вещества, такие как тальк, глину, микрокристаллическую целлюлозу, кремнезем, глинозем и т.п. Эффективные жидкие носители включают воду, спирты, или гликоли, или водно-спиртовые/гликольные смеси,в которых соединения настоящего изобретения могут растворяться или диспергироваться на эффективных уровнях, факультативно с добавлением нетоксичных поверхностно-активных веществ. Адъюванты,такие как ароматизаторы и дополнительные антимикробные агенты, могут быть добавлены для оптимизации свойств для заданного применения. Полученные жидкие композиции могут наноситься на гигроскопические прокладки, которые используются для пропитки повязок и других перевязочных материалов, или распыляться на пораженную область с помощью дозирующих или аэрозольных распылителей. Сгустители, такие как синтетические полимеры, жирные кислоты, соли жирных кислот и эфиров,жирные спирты, модифицированные целлюлозы или модифицированные минеральные материалы также могут использоваться с жидкими носителями для образования легко намазывающихся паст, гелей, мазей,мыла и подобных, для непосредственного нанесения на кожу потребителя. Эффективные дозировки соединений могут быть установлены путем сравнения их in vitro и in vivo активности в животных моделях. Способы экстраполяции эффективных дозировок у мышей и других животных на человека известны в данной области; например, см. патент США 4938949. Способность соединения настоящего изобретения действовать в качестве агониста TLR или антагониста TLR может быть определена с помощью известных фармакологических моделей, включая методики, раскрытые Lee et al., PNAS, 100:6646 (2003). Как правило, концентрация соединения(й) в жидкой композиции будет составлять примерно 0,1-25 мас.%,предпочтительно примерно 0,5-10 мас.%. Концентрация в полутвердой или твердой композиции, такой как гель или порошок, будет составлять примерно 0,1-5 мас.%, предпочтительно примерно 0,5-2,5 мас.%. Количество соединения или его активной соли или производного, требуемое для применения в лечении, будет изменяться не только в зависимости от выбранной конкретной соли, но также от режима введения, природы заболевания, подлежащего лечению, возраста и состояния пациента, и будет в конечном итоге находиться на рассмотрении лечащего терапевта или клинициста. Как правило, пригодная доза находится в диапазоне примерно от 0,5 до 100 мг/кг, например от 10 до 75 мг/кг массы тела в день, такая как от 3 до 50 мг на 1 кг массы тела реципиента в день, и часто находится в диапазоне от 6 до 90 мг/кг/день или примерно от 15 до 60 мг/кг/день. Соединение может удобно вводиться в виде стандартной лекарственной формы и содержит, например, от 5 до 1000 мг, или от 10 до 750 мг, или от 50 до 500 мг активного ингредиента на стандартную лекарственную форму. Активный ингредиент может вводиться для достижения пика концентрации в плазме активного соединения, составляющей примерно от 0,01 до 100 пМ, примерно от 0,5 до 75 пМ, примерно от 1 до 50 пМ или примерно от 2 до 30 пМ. Такие концентрации могут быть достигнуты, например, путем внутривенной инъекции от 0,05 до 5% раствора активного ингредиента, факультативно в солевом растворе, или орального введения в виде болюса, содержащего примерно 1-100 мг активного ингредиента. Желательные уровни содержания в крови могут поддерживаться непрерывной инфузией для обеспечения примерно 0,01-5,0 мг/кг/ч или периодическими инфузиями, содержащими примерно 0,4-15 мг/кг активного ингредиента(ов). Требуемая доза может удобно присутствовать в виде однократной дозы или в виде разделенных общих доз, вводимых с соответствующими интервалами, например две, три, четыре или более доз в день. Субдоза может к тому же быть разделена, например, на ряд отдельных введений с небольшими промежутками; такие как множественные ингаляции из инсуффлятора или путем нанесения множества капель в глаза. Лечение. Использующиеся здесь термины "лечить" и "лечение" относятся к (i) профилактике патологического состояния от возникновения (например, профилактике); (ii) ингибированию патологического состояния или прекращению его развития; (iii) обезболиванию патологического состояния; и/или (iv) улучшению, облегчению, уменьшению и удалению симптомов состояния. Кандидатная молекула или соединение, описанное здесь, может входить в состав или лекарственный препарат в терапевтически эффективном количестве, которое является таким количеством, которое может привести к биологическому эффекту (например, ингибированию воспаления), или привести к улучшению, облегчению, уменьшению и затуханию симптомов состояния, например заболевания. Термины также могут относиться к снижению или остановке скорости пролиферации клеток (т.е. замедлению или остановке роста опухоли) или уменьшению числа пролиферирующих злокачественных клеток (т.е. удаление части или всей опухоли). Данные термины также применимы к снижению титра микроорганизма в системе (т.е. клетки, ткани или субъект), пораженной микроорганизмом, снижению скорости размножения микробов, уменьшению количества симптомов или действию симптома, связанного с микробной инфекцией, и/или удалению заметного количества микробов из системы. Примеры микроорганизмов включают, но без ограничения,вирус, бактерию и грибок. Использующийся здесь термин "терапевтически эффективное количество" относится к количеству соединения, обеспеченного здесь, или количеству комбинации соединений, обеспеченных здесь, для лечения или профилактики заболевания или нарушения, или для лечения симптома заболевания или нарушения у субъекта. Использующиеся здесь термины "субъект" и "пациент" относятся к индивидууму, который будет получать или получал лечение (т.е. введение соединения, описанного здесь) согласно описанному здесь способу. Описанное здесь соединение может вводить субъекту, нуждающемуся в этом, для возможной профилактики, ингибирования или лечения одного или более воспалительных нарушений. Использующиеся здесь термины "лечение", "терапия" и "терапевтический эффект" могут относиться к уменьшению, ингибированию или остановке (предупреждению) реакции на воспаление (т.е. замедлению или перебоям выработки антитела или количества антител на специфический антиген), снижению количества воспаленной ткани и смягчению, полному или частичному, воспалительного состояния. Условия воспаления включают, без ограничения, аллергию, астму, аутоиммунное нарушение, хроническое воспаление, хроническое воспаление предстательной железы, гломерулонефрит, гиперчувствительность, воспалительные заболевания кишечника, миопатию (т.е. в комбинации с системным склерозом, болезнью Вагнера и/или миозит с тельцами включения), воспаление тазовых органов, реперфузионное повреждение, ревматоидный артрит, отторжение трансплантата, васкулит и нарушения лейкоцитов (т.е. синдром ЧедиакаХигаси, хронический гранулематоз). Определенные аутоиммунные нарушения также являются воспалительными нарушениями (например, ревматоидный артрит). В некоторых вариантах воспалительное нарушение является выбранным из группы, состоящей из хронического воспаления, хронического воспаления предстательной железы, гломерулонефрита, гиперчувствительности, миопатии, воспаления тазовых органов, реперфузионного повреждения, отторжения трансплантата, васкулита и нарушения лейкоцитов. В определенных вариантах воспалительные состояния включают, но без ограничения, бронхоэктаз, бронхиолит, муковисцидоз, острое повреждение легких, синдром острой дыхательной недостаточности (ARDS), атеросклероз и септический шок (например, септицемия с множественным поражением органов). В некоторых вариантах воспалительное состояние не является состоянием, выбранным из группы, состоящей из аллергии, астмы, ARDS и аутоиммунного нарушения. В определенных вариантах воспалительное состояние не является состоянием, выбранным из группы, состоящей из воспаления желу- 14019768 дочно-кишечного тракта, воспаления мозга, воспаления кожи и воспаления суставов. В определенных вариантах воспалительное состояние представляет собой нарушение, опосредованное нейтрофилами. Описанное здесь соединение может вводиться субъекту, нуждающемуся в этом, для возможного лечения одного или более аутоиммунных нарушений. В таких терапиях термины "лечение", "терапия" и"терапевтический эффект" могут относиться к снижению, ингибированию или прекращению аутоиммунной реакции (например, замедлению или прерыванию выработки антитела или ряда антител к специфическому антигену), снижению количества воспаленной ткани и облегчению, полному или частичному,аутоиммунного нарушения. Аутоиммунные нарушения включают, но без ограничения, аутоиммунный энцефаломиелит, колит, аутоиммунный инсулинозависимый сахарный диабет (IDDM) и гранулематоз Вегенера и синдром Такаясу. Модели для тестируемых соединений для таких заболеваний включают, без ограничения, (a) (i) C5BL/6, индуцированные пептидом миелинового гликопротеина олигодендроцитов(MOG), (ii) мыши SJL PLP139-151 или 178-191 ЕАЕ, и (iii) модель ЕАЕ с адоптивным переносом, индуцированная MOG или PLP пептидами для аутоиммунного энцефаломиелита; (b) экспериментальная модель аутоиммунного диабета (NOD) мышей для аутоиммунного IDDM; (с) модель колита, индуцированная декстрана натрия сульфатом (DSS) и модель колита, индуцированная тринитробензолсульфоновой кислотой (TNBS), для колита; и (d) системное поражение мелких кровеносных сосудов в качестве модели для гранулематоза Вегенера и болезни Такаясу. Описанное здесь соединение может вводиться субъекту для возможного лечения одного или более из следующих нарушений: острый рассеянный энцефаломиелит (ADEM); болезнь Аддисона; очаговая алопеция; анкилозирующий спондилоартрит; антифосфолипидный синдром (APS); аутоиммунная гемолитическая анемия; аутоиммунный гепатит; аутоиммунное заболевание внутреннего уха; буллзный пемфигоид; целиакия; болезнь Чагаса; хроническая обструктивная болезнь легких; болезнь Крона (один или два типа идиопатического воспалительного заболевания кишечника "IBD"); болезнь Вагнера; инсулинозависимый сахарный диабет; эндометриоз; синдром Гудпасчера; базедова болезнь; острый первичный идиопатический полирадикулоневрит (GBS); зоб Хасимото; гнойный гидраденит; идиопатическая тромбоцитопеническая пурпура; интерстициальный цистит; красная волчанка; синдром Шарпа; очаговая склеродермия, множественный склероз (MS); миастения гравис; нарколепсия; нейромиотония; обыкновенная пузырчатка; злокачественная анемия; полимиозит; билиарный первичный цирроз печени; ревматоидный артрит; шизофрения; склеродермия; ксеродерматоз; височный артериит (также известный как "синдром Хортона-Магата-Брауна"); неспецифический язвенный колит (один из двух типов идиопатического воспалительного заболевания кишечника"IBD"); васкулит; витилиго и некротический неинфекционный гранулематоз. В некоторых вариантах аутоиммунное нарушение или заболевание не является нарушением или заболеванием, выбранным из группы, состоящей из болезни Крона (или заболевания Крона), ревматоидного артрита, волчанки и множественного склероза. Описанное здесь соединение может вводиться субъекту, нуждающемуся в этом, для индуцирования иммунного ответа у субъекта. В определенных вариантах иммунный ответ может быть генерирован автоматически субъектом против чужеродного антигена (например, патогенная инфекция). В некоторых вариантах антиген вводится совместно с описанным здесь соединением, при этом иммунный ответ возникает у субъекта против антигена. Антиген может быть специфическим для конкретных условий клеточной пролиферации (например, специфический раковый антиген) или конкретного патогена (например, антиген грамположительной бактерии; антиген S. aureus), в определенных вариантах. Описанные здесь соединения могут вводиться субъекту, нуждающемуся в этом, для потенциального лечения одного или более нарушений клеточной пролиферации. В таких терапиях термины "терапия","лечение" и "терапевтический эффект" могут относиться к снижению или остановке клеточной пролиферации (например, замедление или прерывание роста опухоли), снижению числа пролиферирующих раковых клеток (например, удаляемая часть или всей опухоли) и уменьшению, полному или частичному, состояния клеточной пролиферации. Состояния клеточной пролиферации включают, но без ограничения,рак ободочной и прямой кишки, молочной железы, легких, печени, предстательной железы, лимфоузлов,толстой кишки, мозга, головы и шеи, кожи, печени, почек и сердца. Примеры рака включают гематопоэтические неопластические нарушения, которые являются заболеваниями, в которые вовлечены гиперпластические/неопластические клетки гематопоэтического происхождения (например, происходящие из миелоидной, лимфоидной или эритроидной клеточных линий или их клеточные предшественники). Заболевания могут возникать из слабо дифференцированной острой лейкемии, например эритробластной лейкемии и острой мегакариобластной лейкемии. Дополнительные миелоидные нарушения включают,но без ограничения, острую промиелоидную лейкемию (APML), острый миелогенный лейкоз (AML) и хроническую миелогенную лейкемию (CML) (рассмотрены в Vaickus, Crit. Rev. in Oncol./Hemotol. 11:267-297 (1991; лимфолейкоз включает, но без ограничения, острый лимфобластный лейкоз (ALL),который включает В-клеточную линию ALL и Т-клеточную линию ALL, хронический лимфолейкоз(CLL), пролимфоцитарный лейкоз (PLL), волосатоклеточный лейкоз (HLL) и макроглобулинемию Вальденстрма (WM). Дополнительные формы злокачественной лимфомы включают, но без ограничения,неходжскинскую лимфому и ее разновидности, периферическую Т-клеточную лимфому, Т-клеточную лейкоз/лимфому взрослых (ATL), кожную Т-клеточную лимфому (CTCL), лейкоз больших гранулярных лейкоцитов (LGF), болезнь Ходжкина и болезнь Рид-Штернберга. В конкретном варианте клеточное пролиферативное нарушение представляет собой неэндокринную опухоль или эндокринные опухоли. Иллюстративные примеры неэндокринных опухолей включают, но без ограничения, аденокарциному,карциному ацинарных клеток, желзисто-плоскоклеточный рак, гигантоклеточные опухоли, внутрипротоковые папиллярные слизистые опухоли, муцинозную цистаденокарциному, панкреатобластому, серозную цистаденому, твердые и псевдопапиллярные опухоли. Эндокринная опухоль может представлять собой инсулиному. Состояния клеточной пролиферации также включают воспалительные состояния, такие как воспалительные состояния кожи, включающие, например, экзему, дискоидную красную волчанку, лишай Вильсона, склеротический лишай, фунгоидный микоз, фотодерматоз, розовый лишай, псориаз. Также включенными являются клеточные пролиферативные состояния, относящиеся к ожирению, такие как,например, пролиферация адипоцитов. Состояния клеточной пролиферации также включают вирусные заболевания, включающие, например, синдром приобретенного иммунного дефицита, аденовирусные инфекции, альфавирусные инфекции, арбовирусные инфекции, болезнь Борна, буньявирусные инфекции, калицивирусные инфекции,ветряную оспу, коронавирусные инфекции, инфекции вирусом Коксаки, цитомегаловирусные инфекции,тропическую лихорадку, ДНК-вирусную инфекцию, эктиму, контагиозные, энцефалитные, арбовирусные инфекции, вирус Эпштейна-Барра, инфекционную эритему, хантавирусные инфекции, геморрагическую лихорадку, вирусный гепатит, вирус простого герпеса, опоясывающий герпес, синдром Ханта, инфекцииHerpesviridae, мононуклеарные инфекции, грипп, например, у птиц или человека, геморрагическую лихорадку Ласса, корь, контагиозный моллюск, свинку, парамиксовирусные инфекции, флеботомную лихорадку, полиомавирусные инфекции, гидрофобию, респираторно-синцитиальные вирусные инфекции,лихорадку долины Рифт, РНК вирусные инфекции, краснуху, медленные вирусные заболевания, оспу,лейкоэнцефалит Ван-Богарта, онкогенный вирус, бородавки, лихорадку Западного Нила, вирусные заболевания и желтую лихорадку. Например, большой Т-антиген трансформирующего вируса SV40 действует на UBF, активирует его и захватывает другие вирусные белки в Pol I комплекс, и тем самым стимулирует клеточную пролиферацию для обеспечения размножения вирусов. Состояния клеточной пролиферации также включают состояния, которые относятся к ангиогенезису (например, раковым заболеваниям) и ожирению, вызванному пролиферацией адипоцитов и других жировых клеток. Клеточные пролиферативные состояния также включают сердечные состояния, возникающие в результате сердечного стресса, такого как повышенное кровяное давление, баллонная ангиопластика, порок сердца и инфаркт миокарда. Например, кардиомиоциты являются дифференцированными мышечными клетками в сердце, которые составляют большую часть стенки желудочка, и клетками гладкой мускулатуры, выстилающими кровеносные сосуды. Несмотря на то что оба типа относятся к мышечным клеткам, кардиомиоциты и клетки гладкой мускулатуры отличаются по их механизмам сокращения, роста и дифференциации. Кардиомиоциты становятся терминально дифференцированными сразу после формирования сердца и, таким образом, теряют способность к делению, в то время как клетки гладкой мускулатуры сосудов непрерывно подвергаются изменению от сократительного до пролиферативного фенотипа. Под воздействием разных патофизиологических стрессов, таких как, например, повышенное кровяное давление, баллонная ангиопластика, клапанный порок и инфаркт миокарда, сердце и сосуды подвергаются морфологическим изменениям, связанным с ростом, которые могут снижать сердечную функцию и в итоге проявляться в сердечной недостаточности. Таким образом, здесь обеспечены способы лечения сердечных клеточных пролиферативных состояний путем введения описанного здесь соединения в эффективном количестве для лечения сердечного состояния. Соединение может вводиться до или после возникновения, или обнаружения сердечного стресса, и соединение или нуклеиновую кислоту можно вводить после возникновения или обнаружения, например, повышенного давления, баллонной ангиопластики, порока клапанов или инфаркта миокарда. Введение такого соединения может уменьшать пролиферацию васкулярных мышечных клеток и/или клеток гладкой мускулатуры. Также определенные варианты направлены на лечение симптомов старения и/или лечения состояний, относящихся к старению клеток, путем введения кандидатной молекулы или нуклеиновой кислоты,описанной здесь. Например, преждевременное старение при синдроме Вернера происходит в результате мутаций в гене синдрома Вернера, который кодирует ДНК-геликазу. Без привязки к теории известно, что данный белок локализуется в ядрышко и специфически связывается с G-квадруплексами, и мутации в гене WRN, кодирующем ДНК-геликазы, приводят к старению. Примеры Представленные ниже примеры иллюстрируют и не ограничивают изобретение. Молекулы TLR могут воздействовать на локализацию рецептора, клеточную активацию и продукцию цитокинов. В случае TLR4 и 9, локализация TLR реагирует на значительный профиль индукции цитокинов (10-12). Конъюгация лекарственного средства с липидами может способствовать проникновению лекарственного средства внутрь клеток с помощью полярного липидного носителя, достигая тем самым эффективной внутриклеточной концентрации лекарственного средства более эффективно и с большей специфичностью, чем традиционные системы доставки. Конъюгация лекарственных средств с липидом, разработанная с медицинской мазью или кремом, может обеспечить проникновение через кожу для лечения кожных заболеваний. Пегилирование может продлевать циркуляцию в крови лекарственных средств путем увеличения стабильности in vivo, которая, в свою очередь, приводит к понижению токсичности (13). В данном случае, липид и полиэтиленгликоль конъюгировали с агонистом TLR7 (SM), и тестировали иммунную активность конъюгатов. Отдельно взятые конъюгаты агониста TLR7 показали разные профили иммуностимуляции in vivo и in vitro. Конъюгация агонистов TLR7 с липидом улучшала способность к стимуляции врожденного иммунитета по сравнению с неконъюгированными агонистамиTLR7 (SM). Конъюгаты липид-агонист TLR7 показали быстрое начало и продолжительное адъювантное действие in vivo. Эти данные предполагают, что конъюгаты липид-агонист TLR7 могут найти применение в качестве адъювантов для терапевтической вакцинации. Конъюгирование агониста TLR7 с PEG,однако, изменяло свойства SM фармакофора, и конъюгат, наоборот, ингибировал активность антагонистаTLR7. Пример 1. Синтез и характеристика конъюгатов. Материалы. 1,2-Диолеоил-sn-глицеро-3-фосфоэтаноламин (DOPE) получали от компании Avanti Polar Lipids(Alabaster, AL). Все другие реагенты, имеющие степень очистки, по меньшей мере, "химически чистые",получали от компании Sigma-Aldrich (St. Louis МО) и использовали без дальнейшей очистки. Растворители получали от компании Fischer Scientific (Pittsburgh, PA) и использовали в том виде, в котором были приобретены, или повторно перегоняли с соответствующим высушивающим агентом. Овальбумин(OVA, марки V) получали от компании Sigma-Aldrich. Уровни эндотоксина в реагентах и конъюгатах для исследований иммунологических активностей измеряли с использованием набора QCL1000 Endopoint chromogenic LAL assay, полученного от компании BioWhittaker (Walkerville, Maryland, США). Реагенты, которые содержали менее чем 1 пикограмм(пг) эндотоксина на микрограмм (мкг) белка или лекарственного средства, использовали на протяжении всех экспериментов. Поскольку DOPE дал ложноположительные результаты в LAL-тесте, мононуклеарные клетки костного мозга (BMDM), полученные от не отвечающих на липосахариды мутантных мышей(С 3 Н/HeJ), использовали для проверки контаминирования эндотоксином (см. фиг. 1 В). Уровни продукции цитокина BMDM, полученным от мышей С 3 Н/HeJ, были аналогичны уровням в клетках, полученных от дикого типа линии С 3 Н/HeOuJ, что указывало на то, что контаминация эндотоксином была незначительной (см. фиг. 2 В). Все конъюгаты хранили при -80 С в форме сухого порошка. Конъюгаты растворяли в DMSO при 100 мМ и далее разбавляли перед иммунологическими анализами. Аналитическую TLC выполняли с использованием предварительно покрытых алюминиевых пластинок TLC silica Gel 60 F254, полученных от компании EMD (Gibbstown, NJ), и визуализировали с помощью УФ-света. Флэш-хроматографию проводили на EMD силикагеле 60 (40-63 мкм) с использованием описанной системы растворителей. Хроматографию и масс-спектры (ESI) для соединений без липидов записывали на хромато-масс-спектрометре 1100 LC/MSD (Agilent Technologies, Inc., Santa Clara CA) на колонке Supelco Discovery C18 HS (Sigma-Aldrich) с чистотой выше 98% относительной площади. Масс-спектр (ESI) соединений, содержащих липид, записывали на приборе Finnigan LCQDECA (ThermoFisher Scientific Inc. Waltham, MA). 1H ЯМР спектр получали на приборе Varian Mercury Plus 400 (Varian,Inc., Palo Alto CA). Химические сдвиги выражали в частях на миллион (ppm) с использованием пригодных дейтерированных растворителей для ЯМР относительно TMS при 0 ppm. Мышей C57BL/6 (В 6) получали от компании Charles River Laboratories (Wilmington, MA). Мышей С 3 Н/HeJ и С 3 Н/HeOuJ получали от компании Jackson Laboratories (Bar Harbor, ME). TLR7-дефицитные мыши (C57BL/6 генетический фон) были подарком от Dr. S. Akira (Osaka University, Osaka, Япония) и были переведены на генетическую основу C57BL/6 путем десяти возвратных скрещиваний. Животные были скрещены и содержались в UCSD в комнатах при 220,5 С при 12:12-часовом цикле света-темноты с 7 часов утра до 7 часов вечера. Все процедуры и протоколы были утверждены Комитетом Института по содержанию и использованию животных. Химический синтез. Описанные здесь схемы химического синтеза используют числа в скобках при ссылке на соединение на фиг. 1, и буквы в скобках при ссылке на стадию реакции (например, добавленное химическое вещество(а) и/или условия реакции). Например, (а) относится к стадии реакции, которая включает добавление реактанта, которое может привести к образованию соединения (2), при соединении и взаимодействии с соединением (1). Условия реакции и добавленные соединения для каждой стадии реакции являются следующими: (а) литий N,N'-метилэтилендиаминоалюминий гидриды (Cha, J. et al. (2002), Selective conversion of aromatic nitriles to aldehydes by lithium N,N'-dimethylethylenediaminoaluminum hedride, Bull. Korean Chem. Soc. 23, 1697-1698), THF, 0C; (b) Nal, хлортриметилсилан, CH3CN, комн.темп.; (с) PBS,комн.темп.; (d) NaOH:EtOH 1:1, дефлегмация; (e) DOPE, HATU, триэтиламин, DMF/DCM 1:1,комн.темп.; (f) O-(2-аминоэтил)-O'-(2-азидоэтил)нонаэтиленгликоль, HATU, триэтиламин, DMF,комн.темп.; (g) 4-пентиноевая кислота, аскорбат натрия, Cu(OAc)2, t-BuOH/H2O/THF 2:2:1, комн.темп.; и Синтез 4-6-амино-2-(2-метоксиэтокси)-8-оксо-7 Н-пурин-9(8 Н)-ил)метил)бензойной кислоты (см. фиг. 1, соединение 5). 20 мл смеси 1:1 этанол:вода добавляли в 0,10 г (0,28 ммоль) 4-6-амино-8-метокси-2-(2 метоксиэтокси)-9 Н-пурин-9-ил)метил)бензонитрила (см. фиг. 1, соединение 1), и комбинацию нагревали с обратным холодильником в течение 8 ч. Реакционную смесь оставляли охлаждаться и подкисляли до рН 2 концентрированной HCl. Водный раствор затем экстрагировали DCM (320 мл), высушивали надMgSO4 и выпаривали в вакууме для получения смеси 8-оксо-9-бензойной кислоты (соединение 5), 8 метокси-9-бензойной кислоты и 8-оксо-9-этилбензоата. После сушки продукты растворяли в CH3CN (25 мл) и добавляли Nal (0,14 г, 0,96 ммоль) (фиг. 1, стадия реакции (b. В полученный раствор добавляли 12 мкл (0,96 ммоль) хлортриметилсилана по каплям при перемешивании. Реакционную смесь нагревали при 40 С в течение 4 ч, затем охлаждали, фильтровали и промывали водой (20 мл), и затем диэтиловым эфиром (20 мл) для получения белого твердого вещества с выходом 85%. Анализ методом ядерного магнитного резонанса (ЯМР) выполняли на конечном продукте со следующими результатами. 1 Н ЯМР (400 МГц, DMSO-d6)(ppm): 10.33 (s, 1H), 7.89 (d, J=8 Гц, 2H), 7.37 (d, J=8 Гц, 2H), 6.65 (s,2H), 4.92 (s, 2H), 4.24 (t, J=4 Гц, 2 Н), 3.56 (t, J=4 Гц, 2H), 3.25 (s, 3 Н). Время удерживания (Rt) на ВЭЖХ=14.3 мин.ESI-MS (режим определения положительных ионов): расчетное для C16H17N5O5 m/z [M+1] 360.34; обнаруженное 360.24. Синтез 2-(4-6-амино-2-(2-метоксиэтокси)-8-оксо-7 Н-пурин-9(8 Н)-ил)метил)бензамидо)этил-2,3 бис-(олеоилокси)пропил фосфата (см. фиг. 1, соединение 6). В раствор, содержащий 0,022 г (0,06 ммоль) соединения 5 в 1 мл безводного N,Nдиметилметанамида (DMF), добавляли О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат (HATU) (0,026 г, 0,067 ммоль) и безводный триэтиламин (TEA) (17.0 мкл, 0,12 ммоль). Готовили раствор 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина (0,05 г, 0,067 ммоль) в безводной смеси 1:1 дихлорметан (DCM):DMF (1 мл) и медленно добавляли в реакционную смесь (фиг. 1 стадия реакции (е. Реакционную смесь перемешивали при комнатной температуре до полного завершения и затем выпаривали в вакууме. Продукт очищали флэш-хроматографией с использованием 15% метанола (МеОН) вDCM для получения 0,038 г белого твердого вещества с выходом 58%. Анализ ЯМР выполняли на конечном продукте со следующими результатами. 1ESI-MS (режим определения отрицательных ионов): расчетное для C57H92N6O12P m/z [M-1] 1083.35; обнаруженное 1083.75. Синтез 4-6-амино-8-гидрокси-2-(2-метоксиэтокси)-9 Н-пурин-9-ил)метил)-N-(32-азидо 3,6,9,12,15,18,21,24,27,30-декаоксадотриаконтил)бензамида (см. фиг. 1, соединение 7). В раствор соединения 5 (0,100 г, 0,278 ммоль) в безводном DMF (5 мл) добавляли HATU (0,117 г,0,306 ммоль) и безводный TEA (77.014 мкл, 0,556 ммоль) (см. фиг. 1, стадия реакции (f. Готовили раствор О-(2-аминоэтил)-О'-(2-азидоэтил)нонаэтиленгликоль (0,150 г, 0,306 ммоль) в безводном DMF (1 мл) и медленно добавляли в реакционную смесь. Реакционную смесь перемешивали при комнатной температуре до завершения и затем выпаривали в вакууме. Продукт очищали флэш-хроматографией с использованием 5% МеОН в DCM для получения 0,224 г непрозрачного масла с выходом 93%. Время удерживания на ВЭЖХ=12 мин. ЯМР анализ выполняли на конечном продукте со следующими результатами. 1 Н ЯМР (400 МГц, DMSO-d6)(ppm): 10.01 (s, 1H), 8.45 (t, J=5.6 Гц, 1 Н), 7.78 (d, J=8.3 Гц, 2H), 7.35ESI-MS (режим определения положительных ионов): расчетное для C38H61N9O14 m/z [M+1] 868.94; обнаруженное 868.59. Синтез 3-(1-(1-(4-6-амино-8-гидрокси-2-(2-метоксиэтокси)-9 Н-пурин-9-ил)метил)фенил)-1-оксо 5,8,11,14,17,20,23,26,29,32-декаокса-2-азатетратриаконтан-34-ил)-1 Н-1,2,3-триазол-4-ил)пропановой кислоты (см. фиг. 1, соединение 8). Соединение 7 (0,218 г, 0,251 ммоль) и 4-пентиноевую кислоту (0,074 г, 0,753 ммоль) растворяли 1:1 в смеси t-бутанол:H2O (3 мл) (см. фиг. 1, стадия реакции (g. В реакционную смесь медленно добавляли аскорбат натрия (0,02 г, 100 ммоль) и Cu(ОАс)2 (0,009 г, 50 ммоль) в смеси 1:1 t-бутанол:H2O (1 мл), и перемешивали при комнатной температуре до тех пор, пока соединение 7 полностью не прореагирует по данным TLC. Продукт экстрагировали DCM (10 мл) и H2O (10 мл), и органический слой высушивали надMgSO4 для получения 0,230 г непрозрачного масла с выходом 95%. Время удерживания на ВЭЖХ=11.5 мин. ЯМР анализ выполняли на конечном продукте со следующими результатами. 1 Н ЯМР (400 МГц, DMSO-d6)(ppm): 13.48 (s, 1 Н), 7.76 (d, J=8.29 Гц, 2H), 7.75 (s, 1H), 7.23 (d,J=8.29, 2H), 4.88 (s, 2H), 4.41 (t, J=5.12 Гц, 2 Н), 4.23 (t, J=4 Гц, 2 Н), 3.74 (t, J=5.12 Гц, 2 Н), 3.57 (t, J=4 Гц,2 Н), 3.51 (m, 8H), 3.42 (m, 36H), 3.26 (s, 3H), 2.79 (t, J=7.56 Гц, 2 Н), 2.24 (t, J=7.56 Гц, 2 Н).ESI-MS (режим определения положительных ионов): расчетное для C43H67N9O16 m/z [M+1] 966.04; обнаруженное 966.67. Синтез 2-(3-(1-(1-(4-6-амино-8-гидрокси-2-(2-метоксиэтокси)-9 Н-пурин-9-ил)метил)фенил)-1 оксо-5,8,11,14,17,20,23,26,29,32-декаокса-2-азатетратриаконтан-34-ил)-1 Н-1,2,3-триазол-4 ил)пропанамидо)этил-2,3-бис-(олеоилокси)пропил фосфата (см. фиг. 1, соединение 9). В раствор соединения 8 (96 мг, 0,1 ммоль), HATU (42 мг, 0,11 ммоль) в безводном DMF (1 мл) добавляли безводный TEA (2,7 мкл, 0,2 ммоль). В реакционную смесь по каплям добавляли раствор DOPE(81,4 мг, 0,11 ммоль) в 1:1 DCM:DMF (1 мл) и перемешивали при комнатной температуре до завершения реакции (см. фиг. 1, стадия реакции (h. После завершения реакции продукт изолировали путем выпаривания в вакууме с последующей флэш-хроматографией с использованием 15% МеОН в DCM для получения 155 мг непрозрачного масла с выходом 92%. ЯМР анализ выполняли на конечном продукте со следующими результатами. 1ESI-MS (режим определения положительных ионов): расчетное для C84H142N10O23P m/z [M+1] 1691.05; обнаруженное 1692.82. Другие соединения синтезировали с использованием аналогичных методик (например, соединения,показанные в табл. 2). Например, 4-6-амино-8-гидрокси-2-(2-метоксиэтокси)-9 Н-пурин-9-ил)метил)-Nгексадецилбензамин (соединение 1Z7) и 4-6-амино-8-гидрокси-2-(2-метоксиэтокси)-9 Н-пурин-9 ил)метил)-N,N-дигексадецилбензамин (соединение 1Z9) готовили и очищали, как описано выше для приготовления соединения 6 на фиг. 1, за исключением того, что соответствующие моно- и дизамещенные гексадециламины использовали вместо 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламина. Массу, равную 583.7, наблюдали для соединения 1Z7 с помощью ESI-MS (режим определения положительных ионов; расчетная масса для C32H50N6O4 m/z [M+1] составила 582.78). Массу, равную 808.2, наблюдали для 1Z9 с помощью ESI-MS (режим определения положительных ионов; расчетная масса для C48H82N5O4 m/z [M+1] составила 807.20). Биотинилированное производное(соединение 1Z18) готовили из аминометильного производного (1V184) и конъюгировали с биотином с использованием такой же методики, которая описана выше. Массу, равную 571.5, наблюдали с помощью ESI-MS(режим определения положительных ионов; расчетная масса для C26H34N8O5S m/z [M+1] составила 570.66). Экспериментальные методы.In vitro методы. Измерения in vitro индукции цитокинов выполняли с использованием моноцитарной макрофагальной линии клеток лейкоза мышей RAW 264.7. Мыши RAW 264.7 были получены от компании AmericanModified Eagle Medium (Irvine Scientific, Irvine, CA), дополненной 10% термоинактивированной фетальной телячьей сыворотки, 2 мМ L-глутамина и 100 ед./мл пенициллина/100 мкг/мл стрептомицина].BMDM готовили из TLR7-дефицитных мышей линии C57BL/6, как описано в Wu, C.C. et al. (2007), "Immunotherapeutic activity of a conjugate of Toll-like receptor 7 ligand", Proc Natl Acad Sci USA 104, 3990-5. В целом, клетки RAW264.7 или BMDM инкубировали с разными концентрациями конъюгатов в течение 18 ч при 37 С, 5% CO2 и собирали супернатанты культур. Уровни цитокинов (IL-6, IL-12 или TNF) в супернатантах определяли с помощью ELISA (BD Biosciences Pharmingen, La Jolla, CA) (Cho, H.J. etal., "Immunostimulatory DNA-based vaccines induce cytotoxic lymphocyte activity by a T-helper cellindependent mechanism" [см. примечание], Nat Biotechnol 18, 509-14 (2000, и результаты представлены на фиг. 2A-2D. Данные представлены как среднее значениестанд.откл.средн. с трехкратным повторением и являются иллюстрацией трех независимых экспериментов. Минимальные детектируемые уровни данных цитокинов составили 15 пг/мл. Уровни TNF измеряли (см. фиг. 2 А) путем инкубирования приблизительно 1106/мл клеток RAW 264.7 с разными конъюгатами или контролями, как описано выше. Уровни IL-6 и IL-12 измеряли (см. фиг. 2B-2D) путем инкубирования 0,5106/мл BMDM с разными конъюгатами или контролями, как описано выше. Конъюгаты готовили в виде базовых растворов (10 мкм для SM и соединений (6), (8) и (9),0,1 мкм для соединения (4 а, из которых готовили серийные разведения (1:5).BMDM также использовали для оценки уровня контаминации эндотоксином конъюгатов TLR7,синтезированных с помощью описанных здесь схем синтеза. 0,5106/мл BMDM, полученных от мышей С 3 Н/HeJ (не отвечающий на LPS мутант) или С 3 Н/HeOuJ (дикий тип), инкубировали с конъюгатамиTLR7 (10 мкМ SM, 0,1 мкМ соединения 4 а, 10 мкМ соединения 6, 10 мкМ соединения 8 или 10 мкМ соединения 9) в течение 18 ч. Уровни IL-6 или IL-12 в супернатантах культур измеряли с помощью ELISA,- 19019768 и результаты представлены на фиг. 2 В. Каждый из конъюгатов TLR7 индуцировал аналогичные уровниIL-6 в TLR4 мутантных и дикого типа мышах, что указывало на то, что контаминация LPS данных конъюгатов является минимальной. Мононуклеарные клетки периферической крови человека (РВМС) были изолированы из человеческих лейкоцитарных плнок, полученных от компании The San Diego Blood Bank (San Diego, CA), как описано в Hayashi, T. et al., "Enhancement of innate immunity against Mycobacterium avium infection by immunostimulatory DNA is mediated by indoleamine-2,3-dioxygenase", Infect Immun 69:6156-64 (2001). PBMC(1106/мл) инкубировали с разными концентрациями конъюгатов TLR7 в течение 18 ч при 37 С, 5% CO2 и собирали супернатанты культур. Уровни цитокинов (IL-6, TNF- или EFN1) в супернатантах определяли с помощью анализов на основе микросфер Luminex (Invitrogen, Carisbad, CA), и результаты представлены на фиг. 3 А, 3 В. Данные представлены как среднеестанд.откл.средн. трехкратного повторения и являются иллюстрацией трех независимых экспериментов. Минимальные детектируемые уровни IL-6,TNF- и IFN1 составили 6, 10 и 15 пг/мл соответственно. Методы in vivo. Фармакокинетику индукции провоспалительных цитокинов конъюгатами TLR7 исследовали с помощью 6-8-недельных мышей C57BL/6. Мышам внутривенно инъецировали агонисты TLR7 и их конъюгаты (40 нмоль соединения (4 а) или 200 нмоль SM и соединения (6), (8) или (9) на мышь). Образцы крови собирали через 2, 4, 6, 24 и 48 ч после инъекций. Сыворотку отделяли и хранили при -20 С до использования. Уровни цитокинов (например, IL-6 и TNF-) в сыворотке измеряли с помощью микроанализа на основе микросфер Luminex и результаты представлены на фиг. 4 А, 4 В. Данные представлены как среднеестанд.откл.средн. пяти мышей и являются иллюстрацией двух независимых экспериментов. Минимальные детектируемые уровни IL-6 и TNF- составили 5 и 10 пг/мл соответственно. Также исследовали инициацию иммунной реакции (например, адъювантность) конъюгатами TLR7. Группы (n=5) из мышей C57BL/6 иммунизировали подкожно 20 мкг овальбумина (OVA), смешанного примерно с 10 нмоль разных конъюгатов TLR7, на 0 и 7 день, при этом 10 нмоль является дозой, заданной для TLR7 части конъюгата, и фактическое количество зависит от фактической химической формулы каждого конъюгата. TLR9-активирующую иммуностимулирующую олигонуклеотидную последовательность (ISS-ODN; 1018) использовали в качестве положительного контроля адъюванта, индуцирующегоTh1 (Roman, M. et al., Immunostimulatory DNA sequences function as T helper-1-promoting adjuvants (1997),Nat Med 3:849-54). Сыворотку собирали на 0, 7, 14, 21, 28, 42 и 56 день. Мыши, иммунизированные солевым раствором или OVA, смешанным с носителем, служили в качестве контролей. Мышей умерщвляли на 56 день и извлекали селезенки для приготовления спленоцитов и гистологических срезов. Приблизительно 200 мкл 2.5106/мл исходных клеток селезенки аликвотировали в титрационные микропланшеты с круглым дном для тканевой культуры в трех экземплярах в общем объеме 200 мкл RPMI 1640 полной среды [RPMI1640 (Irvine Scientific, Irvine, CA), с добавлением 10% термоинактивированной FCS, 2 мМ Lглутамина и 100 ед./мл пенициллина/100 мкг/мл стрептомицина] и рестимулировали 100 мкг/мл OVA или только средой. В некоторых экспериментах место инъекции исследовали через 24 ч после иммунизации на признаки воспаления или местной реакции. Наблюдали за активностью мышей как показателем возможного "болезненного" отклика на иммунизацию и затем взвешивали каждую неделю. Дополнительно к извлечению селезенки на 56 день также собирали легкие, печень, сердце и почки, фиксировали в 10% забуференном формалине (Fisher Scientific, Pittsburgh, PA) и заливали в парафин. Срезы толщиной 5 мкм окрашивали гематоксилином и эозином (НЕ) и оценивали под микроскопом. Анти-OVA антитела подклассов IgG (и в некоторых вариантах конкретно IgG1 и IgG2) измеряли с помощью ELISA, как описано в Cho, H.J. et al., "Immunostimulatory DNA-based vaccines induce cytotoxic(2000), и результаты представлены на фиг. 5 А и 5 В. Каждый планшет ELISA содержал титр предварительно рассчитанной сыворотки для создания стандартной кривой. Титр этого стандарта был рассчитан как наибольшее разведение сыворотки, при котором значение оптической плотности составляло двойной фон. Разные образцы сыворотки тестировали с разведением 1:100. Результаты выражены в единицах на мл, рассчитаны на основе единицы/мл стандартной сыворотки и представлены как среднеестанд.откл.средн. пяти животных в каждой группе.и Т обозначают Р 0,05 и Р 0,01 с помощью однофакторного дисперсионного анализа ANOVA по сравнению с мышами, иммунизированными OVA,смешанным с носителем соответственно. Спленоциты готовили из извлеченных селезенок. Культуры спленоцитов (рестимулированные 100 мкг/мл OVA или только средой) затем инкубировали при 37 С, 5% СО 2 и супернатанты собирали через 72 ч. Уровни IFN в супернатантах культур измеряли с помощью ELISA (BD Bioscience PharMingen) согласно инструкциям производителя (Kobayashi, H. et al., Prepriming: a novel approach to DNA-based vaccination and immunomodulation", Springer Semin Immunopathol 22:85-96 (2000), и результаты показаны на фиг. 5 С. Среднее количество всех клеток селезенки в каждой группе рассчитывали и сравнивали с PBSиммунизированными группами для контроля пролиферации клеток в селезенке. Данные представлены как среднеестанд.откл.средн. пяти мышей и являются иллюстрацией трех независимых экспериментов. Оценку возможного вредного воздействия конъюгатов TLR7 выполняли с помощью трехступенчатого анализа (подсчет общего количества спленоцитов, гистологическое исследование и визуальное наблюдение области инъекции, а также общего состояния здоровья и поведения обработанных мышей). Мышей C57BL/6 иммунизировали 20 мкг OVA, смешанного с конъюгатами TLR7, носителем или контрольным агонистом (олигонуклеотидная последовательность ISS-ODN). На 56 день мышей умерщвляли и подсчитывали общее количество спленоцитов, результаты представлены на фиг. 6 А. Селезенки собирали и подвергали гистологическому анализу, как показано на фиг. 6 В (кратность увеличения=100). Кожу в местах инъекции проверяли через 24 ч после инъекции, как показано на фиг. 6 С. Существенное различие в количестве спленоцитов, подсчитанных у мышей, иммунизированных OVA плюс конъюгатыTLR7, и мышей, иммунизированных только OVA (см. фиг. 6 А), отсутствует. Гистологическое исследование селезенок мышей, иммунизированных OVA, смешанным с конъюгатами TLR7, не показало повреждения белой пульпы селезенки или повышенной насыщенности клетками в красной пульпе (см. фиг. 6 В). Кожа в местах инъекций не имела видимого покраснения или глаукоматозной реакции (см. фиг. 6 С). Эффективность терапии соединением (8) оценивали измерением снижения количества нейтрофилов, инвазирующих перитонеальную область обработанных мышей, а также воздействием на индуцированный экспериментальный аутоиммунный энцефаломиелит (ЕАЕ). Снижение перитонеальной нейтрофильной инфильтрации измеряли путем обработки мышей C57BL/6 внутривенными инъекциями (i.v.) 50 нмолей свободного фармакофора (1V136) или соединения (8) в течение 3 дней. 2 мл 3% тиогликолята(TG) инъецировали внутрибрюшинно (i.p.) через 18 ч после инъекции последнего соединения для индуцирования рекрутинга нейтрофилов. Перитонеальные клетки отбирали через 4 ч после инъекции TG. Подсчитывали общее количество клеток с использованием гемацитометра и морфологически идентифицировали нейтрофилы. Результаты представлены на фиг. 7 А и 7 В. Действие соединения (8) на экспериментальный аутоиммунный энцефаломиелит (ЕАЕ) определяли с использованием мышей C57BL/6, обработанных миелин-олигодендроцитарным гликопротеином(MOG). MOG представляет собой мембранный белок, который экспрессируется на клеточной поверхности олигодендроцита и наружной поверхности миелиновой оболочки. MOG представляет собой аутоантигенный белок, который при разрушении может привести к заболеванию, характеризующемуся демиелинизацией нейронов, аналогично симптомам, ассоциированным, например, с множественным склерозом. Было показано, что MOG является высокоэнцефалитогенным и может индуцировать сильные Т и В клеточные ответы у грызунов. ЕАЕ представляет собой воспалительное демиелинизирующее заболевание центральной нервной системы (CNS) и широко изучено как животная модель человеческих демиелинизирующих заболеваний CNS, включающих множественный склероз и острый диссеминированный энцефаломиелит (ADEM), а также является эффективным для изучения воспаления мозга. Обработка MOG (или пептидами MOG) может применяться для индуцирования ЕАЕ. Мышей обрабатывали белком MOG в течение 6 дней. На 6 день и в последующие дни (см. фиг. 8) ежедневно инъецировали внутривенно (i.v.) 50 нмоль соединения (8) или PBS. Клинические показатели ЕАЕ были использованы в качестве клинической метрики для демиелинизации и были определены визуально. Статистически значимые клинические показатели наблюдали на 11-17 день обработки соединением (8), как указано на фиг. 8 (см. данные, помеченные ). В некоторых экспериментах статистическую оценку выполняли для определения статистической значимости наблюдаемых результатов. Статистическое программное обеспечение (Prism 4.0, GraphPad,San Diego CA) использовали для статистического анализа, включая регрессионный анализ. Данные наносили на график и описывали нелинейной регрессией, исходя из распределения Гаусса с нормированными стандартными отклонениями между группами. В экспериментах на адъювантность статистическое различие между группами анализировали с помощью двухфакторного дисперсионного анализа ANOVA с послеэкспериментальными исследованиями методом Бонферрони для сравнения контрольных мышей с мышами, которые были иммунизированы OVA. Величина Р 0,05 считалась статистически значимой. Результаты и обсуждение. Химический синтез. Синтез соединения (4) из соединения (1) позволял достичь устойчивого соотношения конъюгации 5:1 UC1V150 с белком MSA (Wu, C.C. et al., "Immunotherapeutic activity of a conjugate of a Toll-like receptor 7 ligand", Proc Natl Acad Sci USA 104, 3990-5 (2007. Щелочной гидролиз (фиг. 1, стадия реакции (d 9-бензилнитрила соединения (1) обеспечивал функциональную группу бензойной кислоты широкого назначения (соединение (5 и сборку конъюгатов (6), (8) и (9). Бензойная кислота связывалась с DOPE путем активирования HATU в присутствии TEA в безводном DMF (фиг. 1, стадия реакции (е для получения соединения 6 с выходом 58%. Из-за трудности в растворении соединения (6) в пригодных растворителях для тестирования, PEG спейсер был присоединен для улучшения растворимости. Легкодоступные амин/азид бифункциональныеPEG присоединяли к бензойной кислоте путем активации при помощи HATU в присутствии TEA в безводном DMF (см. фиг. 1, стадия реакции (f), что приводило к получению соединения (7. Образование 1,2,3-триазола с помощью медь (I)-катализируемого циклоприсоединения азидов/алкинов с 4 пентаноевой кислотой (фиг. 1, стадия реакции (g позволило получить соединение (8) с выходом 95%. В заключение, соединение (9) готовили путем активированного HATU образования амида с DOPE (фиг. 1,стадия реакции (h и соединением (8). Измерения in vitro индукции цитокинов конъюгированными с липидами агонистами TLR7. Соединение агониста TLR7 (4 а) при ковалентном связывании с мышиным сывороточным альбумином проявляет активность 10 или выше в индукции цитокинов in vitro и in vivo, по сравнению с неконъюгированным лекарственным средством (SM) (Wu, C.C. et al., "Immunotherapeutic activity of a conjugate ofa Toll-like receptor 7 ligand", Proc Natl Acad Sci USA 104, 3990-5 (2007. С помощью аналогичного анализа сравнивали активность in vitro конъюгатов липид-агонист TLR (фиг. 1, соединение 6), конъюгатовPEG-агонист TLR7 (фиг. 1, соединение 8) и конъюгатов PEG-липид (фиг. 1, соединение 9) с использованием мышиной макрофагальной клеточной линии RAW264 и первичных макрофагов костного мозга(BMDM). Соответствующие клетки стимулировали в течение 18 ч серийно разведенными конъюгатамиTLR7 и уровни высвобождаемых в среду цитокинов измеряли с помощью ELISA, и сравнивали с неконъюгированным агонистом TLR7 (SM) (см. фиг. 2 А, ряд A-D). Ранее было показано, что соединение (4 а) (например, конъюгат TLR7-MSA) является в 100 раз сильнее в качестве индуктора цитокинов по сравнению с неконъюгированным агонистом, в то время как конъюгат липид-TLR7 был в 10 раз сильнее при нормализации до молярной доли неконъюгированного агониста. Несмотря на то что конъюгаты PEG-TLR7 (соединение 8) показали меньшую активность по сравнению с неконъюгированным TLR7 (SM), конъюгация липида с конъюгатами PEG-TLR7 (липидPEG-TLRT) (соединение 9) восстанавливала их активность до аналогичного уровня неконъюгированныхTLR7 (SM). Главным образом аналогичные концентрации MSA, липида или PEG без TLR7 конъюгации,при самых высоких уровнях в конъюгированной форме, использовали в качестве негативного контроля и индуцировали минимальные уровни цитокина или их отсутствие в клетках RAW264.7 и BMDM соответственно (данные не показаны). Для оценки способности одних лишь конъюгированных форм агонистов TLR7 индуцировать стимуляцию макрофагов, в отличие от стимуляции макрофагов без TLR7, BMDM, полученные от мышей дикого типа и TLR7-дефицитных мышей (TLR7-KO или нокаутных мышей), обрабатывали соединениями (4 а), (6), (8), (9) и SM. Соединения (4 а), (6), (8), (9) и SM не индуцировали или индуцировали незначительное количество IL-12 и IL-6, в то время как данные конъюгаты были активными у дикого типаDMDM, что указывало на то, что агонистическая активность присутствовала благодаря активности TLR7 данных конъюгатов (см. фиг. 2C-2D). Оценка эндотоксина (фиг. 2 В и описанная выше), кроме того, подтверждала вывод о том, что активность агониста была благодаря TLR7 активности данных конъюгатов(например, отсутствие значительной статистической разницы в уровнях продукции IL-6). Для дополнительного исследования иммунологических активностей в человеческих клетках человеческие РВМС от трех доноров обрабатывали конъюгатами TLR7 и определяли уровни IL-6 и IFNa1 с помощью анализа Luminex (фиг. 3 А, 3 В). В данном эксперименте человеческий сывороточный альбумин(HSA), конъюгированный с TLR7 (4b), использовали вместо MSA-конъюгатов (4 а). Порядок активности конъюгатов TLR7 был аналогичен порядку, наблюдаемому в мышиных макрофагах 4a)(6)(9)/=SM(8 (фиг. 3 А). Устойчивую тенденцию активности соединений наблюдали в РВМС от всех доноров. В отличие от соединения (4 а), соединение (4b) (например, конъюгат TLR7-HSA) индуцировал минимальные уровни IFNa1 в человеческих РВМС (наблюдаемые у трех доноров) (фиг. 3 В).In vivo кинетика индукции провоспалительных цитокинов конъюгатами TLR. Для сравнения in vivo иммунологических свойств конъюгатов TLR7 мыши C57BL/5 получали внутривенно конъюгаты агониста TLR7, и изучали кинетику провоспалительных цитокинов в сыворотке(фиг. 4 А и 4 В). На основании более раннего исследования (Wu, C.C. et al., Proc Natl Acad Sci USA 104,3990-5 (2007, соединение (4 а) использовали при более низкой концентрации (40 нмоль на животное),чем соединения SM, (6), (8) и (9) (200 нмоль на животное). Максимальную индукцию TNF и IL-6 наблюдали через 2 ч после инъекции для всех конъюгатов TLR7 (фиг. 4 А, 4 В соответственно). Уровни цитокинов, индуцированных неконъюгированным TLR7 (SM), быстро уменьшались через 2 ч. Индукция цитокина соединениями (4 а), (6) и (9) продолжалась вплоть до 6 ч. Соединение (8) индуцировало только низкий уровень IL-6 (см. фиг. 4 В), и значительно не индуцировало TNF в любой момент времени после инъекции (см. фиг. 4 В). Сыворотка от контрольной мыши, которая получала солевой раствор, MSA илиDOPE, показала незначительные или не детектируемые уровни цитокина (данные не показаны). Конъюгаты липид-TLR7 способствуют быстрой и продолжительной эндокринной реакции. Эффективность адъювантных свойств оценивали путем измерения уровней и индуцированных вакциной изотипов антиген-специфических IgG, в частности IgG1 и IgG2 (Mosmann, T.R., and Coffman, R.L.,"TH1 and TH2 cells:different patterns of lymphokine secretion lead to different functional properties", AnnualReview Immunology 7:145-73 (1989. Группы мышей C57BL/6 (n=5 животных на группу) подкожно иммунизировали OVA (овальбумин), смешанным с конъюгатами TLR7. ISS-ODN использовали в качестве положительного контроля сильного Th1 адъюванта. Мышей, иммунизированных солевым раствором илиOVA-специфических IgG1 и IgG2a в сыворотке контролировали с помощью ELISA на 0, 7, 14, 21, 28, 42 и 56 день (фиг. 5 А, 5 В). Индукцию антител IG подкласса наблюдали не ранее 14 дней после иммунизации мышей OVA, смешанным с соединением (4 а) или соединением (6) (см. фиг. 5 А). Уровни анти-OVAIgG2a непрерывно повышались у мышей, иммунизированных смесями OVA/соединение (6), в то время как уровни у мышей, иммунизированных смесью OVA/соединение (4 а), последовательно снижались, как показано на фиг. 5 А. Эти данные согласуются с усиленной OVA-специфической секрецией IFN клетками селезенки у мышей, иммунизированных OVA в комбинации с соединениями (4 а) или (6) (см. фиг. 5 С). Оценка in vivo побочных эффектов. Агонисты TLR7 (SM) могут индуцировать эффекты анорексии и гипотермии у мышей (Hayashi, T.et al., "Mast cell dependent anorexia and hypothermia induced by mucosal activation of Toll like Receptor 7",Am J. Physiol Regul Integr Comp Physiol 295, R123-32 (2008, вызывая потерю веса. Таким образом, как часть экспериментального протокола, контролировали массу тела и реакцию кожи (в месте инъекции) мышей, иммунизированных конъюгатами липид-агонист TLR7. Минимальная доза неконъюгированного агониста TLR7 (SM), которая индуцировала аноректическую реакцию у мышей, составила 50 нмолей на мышь при мукозальном введении (Hayashi, Т. et al., Am J. Physiol Regul Intergr Comp Physiol 295, R123-32(2008. Дозу для экспериментов с адъювантами (10 нмолей на мышь) выбирали таким образом, чтобы избежать болезненной реакции, вызванной агонистами TLR7. Значительных различий между средней массой тела мышей, иммунизированных OVA, смешанным с соединением (6) и мышами, которых инъецировали солевым раствором, не наблюдалось (данные не показаны). Постоянный прием TLR7 может также индуцировать пролиферацию миелоидных клеток (Baenziger,S. et al., "Triggering TLR7 in mice induces immune activation and lymphoid system disruption, resemblingHIV-mediated pathology", Blood 113:377-388 (2009). Общее количество клеток селезенки были рассчитано в качестве индикатора пролиферации миелоидных клеток селезенки (см. фиг. 6 А). Не было значительной разницы в общем количестве спленоцитов между мышами, иммунизированными OVA, конъюгатами агониста TLR7 и контрольным солевым раствором (см. фиг. 6 В). Гистологическое исследование селезенок мышей, иммунизированных OVA, смешанным с агонистами TLR7, показало отсутствие структурного нарушения белой пульпы селезнки (зародышевый центр) и отсутствие увеличения насыщенности клетками в красной пульпе (см. фиг. 6 В). К тому же, не наблюдалось значительного различия в гистологическом исследовании образов печени, легких, сердца и почек, собранных от каждой группы (данные не показаны). Также не было макроскопически видимого покраснения или глаукоматозной реакции в месте инъекции или около него при введении конъюгатов липид-TLR7 (см. фиг. 6 С). Тиогликолят (TG) может быть использован как вызывающий агент для рекрутинга лейкоцитов и макрофагов в место воспаления. В ответ на инфекцию или воспаление нейтрофилы обычно являются первым гранулоцитарным типом клеток, которые поступают в место инфекции или воспаления. Таким образом, терапия тиогликолятом вызывает рекрутинг многих типов клеток с иммунным ответом, которые могут быть эффективными для определения возможных побочных эффектов, ассоциированных с введением конъюгатов TLR7. Способ, который использовали для этих исследований, состоял в предварительной обработке мышей разными соединениями конъюгатов TLR7 в течение 3 дней, с последующей инъекцией 2 мл 3% раствора триогликолята через 18 ч после последней обработки конъюгатом TLR7. Через 4 ч после инъекции TG общее количество перитонеальных клеток собирали и подсчитывали. Нейтрофилы идентифицировали морфологически и подсчитывали. Результаты представлены на фиг. 7 А, 7 В. Мышей, обработанных только солевым раствором, использовали в качестве негативного контроля и устанавливали базальный уровень общего количества перитонеальных клеток и общего количества нейтрофилов, рекрутированных для необработанных мышей. Мыши, обработанные TG (в солевом растворе),но не обработанные предварительно конъюгатом TLR7, были использованы в качестве положительного контроля для рекрутинга и показали приблизительно 5106 всех клеток, рекрутированных в перитонеальную область, из которых приблизительно 90% составляли нейтрофилы (больше чем 4106 нейтрофилов из 5106 всех клеток). Мыши, предварительно обработанные TLR7 свободным фармакофором(1V136) или конъюгатом TLR7 (1V282, соединение (8, показали снижение общего количества рекрутированных клеток и рекрутированных нейтрофилов, что указывало на то, что обработка свободным фармакофором или соединением (8) может уменьшать уровень воспалительной/инфекционной реакции, на которую реагируют лейкоциты, гранулоциты и макрофаги, но могут иметь небольшой эффект или его отсутствие на распределение рекрутированных типов клеток (например, относительные количества каждого типа клеток). Таким образом, свободный фармакофор и соединение (8) не показали дополнительного вредного воздействия (например, болезненной реакции, как описано выше) по сравнению с TG и уменьшали рекрутинг лейкоцитов, гранулоцитов и макрофагов.MOG белок также использовали для оценки возможных вредных эффектов разных конъюгатовTLR7, как описано выше. Результаты оценивали наблюдением разных симптомов, ассоциированных с Серьезность симптомов записывали как "клинический показатель" и производили сравнение между необработанными мышами (PBS) и мышами, обработанными соединением (8) после первых 6 дней MOG обработки (см. фиг. 8). Статистически значимые различия в клинических показателях указанысвыше 11-17 дней. Обработка соединением (8) значительно снижала тяжесть симптомов ЕАЕ в период между 11 и 17 днями, а также снижала начальное увеличение тяжести симптомов, как указано различием на графике двух линий, которые начинаются на 8 день и проходят через 11 день. Таким образом, можно сделать вывод о том, что соединение 8 не вызывает дополнительной побочной реакции (например, отсутствует болезненная реакция, как описано выше) и может также снижать тяжесть симптомов, ассоциированных с MOG-индуцированной ЕАЕ. Выводы. Неконъюгированный TLR7 (SM) является нерастворимым в водном растворе. Растворимость в воде может играть роль в контроле биологической доступности лекарственного средства путем увеличения диффузии лекарственного средства или стимулирования внедрения в клетки. Пегилирование может улучшать растворимость лекарственного средства и уменьшать иммунодефицит (Veronese, F.M. andMero, A., "The impact of PEGylation on biological therapies", BioDrugs 22, 315-29 (2008. Пегилирование также может увеличивать стабильность лекарственного средства, время удерживания конъюгатов в крови и может снижать протеолиз, и выведение с мочой (Veronese, F.M. and Mero, A. BioDrugs 22, 315-29(2008. В случае, когда TLR7 конъюгировано с PEG (например, соединение (8, растворимость значительно возрастает (данные не показаны). Однако, возможность индукции цитокинов является ослабленной по сравнению с немодифицированным агонистом TLR7 in vitro (фиг. 2 А, ряд А и В) и in vivo (фиг. 4 А и 4 В). Активность in vitro и in vivo может быть восстановлена дальнейшей конъюгацией с DOPE (соединение (9. Соединение (9) может индуцировать иммунную реакцию Th2 (указанную уровнями IgG1),при проявлении минимального ответа Th1 (указанного уровнями IgG2). Соединения конъюгатов агониста TLR7 (4 а) (MSA конъюгат) и (6) (липидный конъюгат) вызывали быстрое повышение титра IgG2a (фиг. 5 А). Уровни IgG2a у мышей, иммунизированных конъюгатамиMSA-TLR7 (соединение (4 а, понижались через три недели после последней иммунизации, в то время как мыши, иммунизированные OVA, смешанным с конъюгатами липид-TLR7 (соединение (6, показали устойчивые и, кроме того, возрастающие уровни антиген-специфического IgG2a (фиг. 5 А). Несмотря на то что соединение (4 а) не сохраняло уровни IgG2a, секреция OVA-специфического IFN клетками селезенки у мышей, иммунизированных OVA, смешанным с соединением (4 а), сохраняла относительно высокие уровни (фиг. 5 С). Такие же агонисты TLR7, конъюгированные с разными группами, которые дают отличающиеся иммунные профили, могут быть эффективными в разработке адъювантов для лечения разных категорий заболеваний, таких как, например, инфекция и аутоиммунное заболевание. Были синтезированы разные конъюгаты агониста TLR7, и было обнаружено отличие в их иммунологических профилях in vivo и in vitro. Различие в физических свойствах предложенных конъюгатов агониста TLR7 дает возможность более широкого применения в лечении разных заболеваний. Растворимые в воде конъюгаты могут обеспечить режим для системного введения. Содержащие липиды конъюгаты могут быть пригодными для местного введения, требующего постоянной стимуляции прилегающих иммунных клеток (например, применение адъюванта для инфекционных заболеваний). Липидный фрагмент может способствовать проникновению лекарственного средства через кожный барьер и может быть предпочтительным для лечения кожных заболеваний. Конъюгация агониста TLR7 с липидом или PEG фрагментами может быть обещающей стратегией для расширения клинического лечения инфекции, рака или аутоиммунного заболевания. На основании представленных здесь данных был сделан вывод о том, что соединение (8) обладает антагонистической активностью при определенных условиях. Фиг. 4 А-В показывает, что соединение (8) обладает незначительной или отсутствием IL-6 или TNF стимулирующей активности, и может уменьшать определенные аспекты воспаления или реакции на инфекцию, обычно ассоциированные с увеличением активности IL-6 или TNF (см. фиг. 7 А, 7 В и фиг. 8). Данные наблюдения согласуются с антагонистической активностью (например, соединение может связываться, но не стимулировать активацию рецептора). Активация Toll-подобных рецепторов (TLR) на клетках врожденной иммунной системы инициирует, усиливает и направляет антиген-специфический приобретенный иммунный ответ. Лиганды, которые стимулируют TLR, таким образом, являются потенциальными иммуностимуляторами. В данном исследовании сильный агонист TLR был конъюгирован с полиэтиленгликолем (PEG), липидом или липидPEG с помощью изменяемой функциональной группы бензойной кислоты. По сравнению с немодифицированным агонистом TLR, каждый конъюгат проявил разный иммунологический профиль in vitro и invivo. В мышиных макрофагах и мононуклеарных клетках периферической крови человека конъюгаты липид-TLR являлись по меньшей мере в 100 раз более сильными, чем свободные лиганды TLR, в то время как эффективности PEG и конъюгатов PEG-липид были аналогичными свободной форме. При введении конъюгатов системно in vivo, липидные и липид-PEG TLR7 конъюгаты обеспечивали устойчивые уровни иммуностимулирующих цитокинов в сыворотке по сравнению с немодифицированным активато- 24019768 ром TLR. При использовании конъюгатов в качестве адъювантов во время вакцинации, только конъюгаты липид-TLR7 индуцировали устойчивый Th1, а также Th2 антиген-специфические ответы. Представленные данные показали, что иммуностимулирующая активность TLR7 лиганда может распространяться и фокусироваться конъюгацией, возможно расширяя, таким образом, потенциальное терапевтическое применение данных агентов. Дополнительные соединения и их свойства. Биологические активности. Активность in vitro агониста TLR7, конъюгированного с PEG с разной длиной цепи, определяли с помощью GeneBlazerCellSensor клеточной линии NFkB-bla RAW 264.7 (Invitrogen) и первичных мышиных BMDM. Клетки инкубировали с разными концентрациями конъюгатов липид-PEG агониста TLR7. Активацию NFkB клеточной линии Cellsensor определяли согласно инструкциям производителя. BMDM инкубировали с конъюгатами в течение ночи, и уровень IL-6 в супернатанте оценивали в помощью ELISA. Примерную YC50 рассчитывали с использованием Prism. Конъюгаты с 6, 10 и 18 PEG цепями показали аналогичную активность в обеих NFkB-bla RAW клетках и BMDM (фиг. 9A-9D). В анализах с использованием клеток NFkB-bla RAW конъюгаты, содержащие более длинные PEG цепи, были менее активными для активации NFkB (фиг. 9D-9E). Напротив,конъюгаты с длинной цепью показали более высокие активности для IL-6 секреции с помощью BMDM(фиг. 9D-9 Е). Среди конъюгатов с 6 PEG цепью конъюгаты с NH2 терминальной группой показали слегка повышенную активность, чем конъюгаты с СООН или N3 терминальными группами (фиг. 9 А). Мышам C57BL/6 инъецировали 200 нмоль разных конъюгатов агониста TLR7-PEG в 100 мкл солевого раствора. Сыворотку собирали в указанное время и уровни цитокинов (TNF-альфа, EL-6, IL-12) определяли с помощью микросфер Luminex (фиг. 10 А, 10 В). Все соединения, используемые в исследовании, были визуально растворимы в 0,1-0,2% DMSO-солевых растворах. В случае, когда свободный агонист TLR7 конъюгировали с 6 PEG цепью (1Z2), активность была уменьшенной (фиг. 10 А, 10 В). Конъюгаты, содержащие более длинные цепи, такие как 1V303 (18 PEG цепь) и 1Z3 (примерно s 47 PEG цепь),индуцировали цитокины на уровне неконъюгированного агониста (1V136). 1Z5, который содержит приблизительно 271-PEG цепь, индуцировал более высокие уровни цитокинов, чем неконъюгированный агонист TLR7. Для сравнения in vivo биоактивностей между NH2 и СООН терминальными группами использовали 6 PEG цепь и 10 PEG цепь, конъюгированные с агонистами TLR7 (фиг. 10C). 1Z2 и 1V298, которые содержат NH2 терминальную группу, показали относительно высокую индукцию цитокинов, чем их соответствующие конъюгаты, содержащие СООН терминальную группу (фиг. 10C-D). Противовоспалительную эффективность конъюгатов агонист TLR7-PEG тестировали на мышиных моделях человеческих воспалительных заболеваний (артрит с переносом сыворотки, экспериментальный аллергический энцефаломиелит (ЕАЕ) (см. выше) и тиогликолят-индуцированный перитонит). Для артрита с переносом сыворотки (фиг. 11) мышей C57BL/6 вводили сыворотку K/BxN в 0 день и обрабатывали ежедневно через зонд (фиг. 11 А) или подкожной инъекцией (фиг. 11 В) 1V282. Ежедневное введение 1V282 снижало набухание лапы как при подкожной обработке, так и при обработке через зонд. Для тиогликолят-индуцированного перитонита (фиг. 12) мышам C57BL/6 внутривенно или орально вводили 1V282 в течение трех дней. Через день после последней обработки мыши получали интраперитонеально 2 мл тиогликолевой среды. Внутривенное и подкожное введение 1V136 использовали в качестве положительных контролей. Через 3 ч после введения тиогликолята оценивали инфильтрацию нейтрофилами в перитонеальной области. Системное и оральное введение 1V282 снижало клеточную инфильтрацию, в частности нейтрофильную в перитонеальную область. Диабеты 1 типа у человека характеризуются специфическим разрушением панкреатическихклеток, обычно ассоциированным с иммуноопосредованным повреждением. Химически индуцированные модели диабета используют для тестирования возможности уменьшения тяжести или начала заболевания при постоянном введении конъюгатов агонист TLR7-PEG. Использовали множественные маленькие дозы стрептозотоцина (алкилирующего агента) (например, 40 мг/кг на пять последующих дней). У восприимчивых грызунов происходит индуцирование инсулинозависимого диабета, при котором разрушение иммунитета играет некоторую роль, как в человеческом диабете 1 типа. На основании механизма действия, наблюдаемого в других родственных заболеваниях, конъюгаты TLR7-PEG будут ослаблять течение данного заболевания.a - приблизительная молекулярная масса благодаря гетерогенности PEG полимера.b - характеризуется только ЯМР. Каждый патент, патентная заявка, публикация и документ, на которые делаются здесь ссылки,включены здесь полностью посредством отсылки. Список вышеуказанных патентов, патентных заявок,публикаций и документов не является признанием того, что любой из вышеуказанных относится к предшествующему уровню техники или является признанием содержания или даты данных публикаций или документов. Изменения вышеперечисленного могут быть сделаны без отступления от основных аспектов изобретения. Хотя изобретение было описано с существенными деталями со ссылкой на один или более конкретных вариантов, специалистам среднего уровня будет понятно, что могут быть внесены изменения в варианты, специально раскрытые в данном патенте, однако эти изменения и улучшения находятся в пределах объема и сущности изобретения. Изобретение, иллюстративно описанное здесь, может быть пригодно для осуществления на практике в отсутствие любого(ых) элемента(ов), специально здесь не раскрытого. Таким образом, например, в каждом указанном здесь случае любой из терминов "включающий", "состоящий в основном из" и "состоящий из" может быть заменен любым из двух других терминов. Термины и выражения, которые были использованы, использовали как термины для описания и не ограничения, и использование таких терминов и выражений не включает каких-либо эквивалентов признаков, показанных и описанных, или их частей, и возможны разные изменения в объеме заявленного изобретения. Используемые в описании формы в единственном числе включают также ссылки на них во множественном числе, если контекст не указывает ясно иное. Использующийся здесь термин "примерно" относится к величине в пределах 10% основного параметра (т.е. 10%), и использование термина "примерно" в начале последовательности величин изменяет каждую величину (т.е. "примерно 1, 2 или 3" равно примерно 1, примерно 2 и примерно 3). Например, масса "примерно 100 г" может включать от 90 до 110 г. Таким образом, должно быть понятно,что, несмотря на то что настоящее изобретение было специально раскрыто с помощью иллюстративных вариантов и факультативных признаков, модификация и изменение раскрытых здесь понятий могут быть выбраны опытными в данной области специалистами и такие изменения и модификации рассматриваются как находящиеся в объеме данного изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение, имеющее структуру согласно формуле I или его фармацевтически приемлемая соль, включая его гидрат,где X представляет собой N или CR2;R представляет собой -OR1, -SR1 или -NRaRb,X1 представляет собой связь или -О-, -S- или -NRc-;Rc представляет собой водород, C1-C10-алкил или замещенный C1-C10-алкил или Rc и R1 вместе с атомом азота могут образовывать гетероциклическое кольцо или замещенное гетероциклическое кольцо; каждый R1 независимо представляет собой водород, C1-C10-алкил, замещенный C1-C10-алкил, C1C10-алкокси, замещенный C1-C10-алкокси, C1-C10-алкил-C1-C10-алкокси, замещенный C1-C10-алкил-C1-C10 алкокси, C5-C10-арил, замещенный C5-C10-арил, C5-C9-гетероциклил, замещенный C5-C9-гетероциклил,C3-С 9-карбоциклил или замещенный C3-С 9-карбоциклил; каждый R2 независимо представляет собой водород, -ОН, C1-C6-алкил, замещенный C1-C6-алкил,C1-C6-алкокси, замещенный C1-C6-алкокси, -С(О)-C1-C6-алкил (алканоил), замещенный -С(О)-C1-C6 алкил, -С(О)-C6-C10-арил (ароил), замещенный -С(О)-C6-C10-арил, -С(О)ОН (карбоксил), -С(О)О-C1-C6 алкил (алкоксикарбонил), замещенный -С(О)О-C1-C6-алкил, -NRaRb, -C(O)NRaRb (карбамоил), замещенный C(O)NRaRb, гало, нитро или циано; заместители на алкильных, алкокси, арильных или гетероциклических группах представляют собой гидрокси, C1-C6-алкил, гидрокси-C1-C6-алкилен, карбокси-C1-C6-алкилен, C1-C6-алкокси, C3-С 6 циклоалкил, C1-C6-алкокси-C1-C6-алкилен, амино, циано, галоген или арил; каждый Ra и Rb независимо представляет собой водород, С 1-С 20-алкил, C3-C8-циклоалкил, C1-C6 алкокси, гало-C1-C6-алкил, C3-C8-циклоалкил-C1-C6-алкил, C1-C6-алканоил, гидрокси-C1-C6-алкил, арил,арил-C1-C6-алкил, Het, Het-C1-C6-алкил или C1-C6-алкоксикарбонил;Rx представляет собой -X2-R3)r-(R4)s)p; каждый X2 независимо представляет собой амидосвязующую группу, алкиламидосвязующую группу, замещенное 5-6-членное кольцо или кислородсодержащий фрагмент; каждый R3 независимо представляет собой полиэтиленгликолевый (PEG) фрагмент, который представляет собой -О-СН 2-СН 2- или -СН 2-СН 2-О-; каждый R4 независимо представляет собой Н, -C1-C6-алкил, -C1-C6-алкокси, -NRaRb, -N3, -ОН, -CN,-СООН, -COOR1, -C1-C6-алкил-NRaRb, C1-C6-алкил-ОН, C1-C6-алкил-CN, C1-C6-алкил-СООН, C1-C6 алкил-COOR1, 5-6-членное кольцо, замещенное 5-6-членное кольцо, -C1-C6-алкил-5-6-членное кольцо,-C1-C6-алкилзамещенное 5-6-членное кольцо, C2-C9-гетероциклил или замещенный C2-C9-гетероциклил;n представляет собой 0, 1, 2, 3 или 4; р представляет собой от 1 до 100;r представляет собой от примерно 5 до примерно 100;s представляет собой от 1 до 1000; сумма n и q равна 5. 2. Соединение по п.1, в котором X1 представляет собой кислород. 3. Соединение по п.1 или 2, в котором R1 представляет собой замещенный C1-C6-алкил или C1-C10 алкил-C1-C10-алкокси-фрагмент, предпочтительно R1 представляет собой -СН 2 СН 2 ОСН 3. 4. Соединение по любому из пп.1-3, в котором X2 представляет собой -C(O)NH-, -NH(O)C-, -C1-C6 алкил-С(О)NH-, -C1-C6-алкил-NH(О)С-, -C(O)NH-C1-C6-алкил-, -NH(O)C-C1-C6-алкил-, -C1-C6-алкилNH(O)С-C1-C6-алкил-, -C1-C6-алкил-С(О)NH-C1-C6-алкил или -C(O)NH-(CH2)t-, где t равно 1, 2, 3 или 4. 5. Соединение по любому из пп.1-4, в котором n равно 4 и R2 представляет собой водород в каждом случае. 6. Соединение по любому из пп.1-5, в котором каждое PEG звено представляет собой -О-СН 2-СН 2 или СН 2-СН 2-О-. 7. Соединение по любому из пп.1-6, в котором r равно от примерно 5 до примерно 50, предпочти- 29
МПК / Метки
МПК: A61P 29/00, A61K 31/52, C07D 473/02
Метки: модулирующие, toll-подобных, рецепторов, активность, соединения
Код ссылки
<a href="https://eas.patents.su/30-19768-soedineniya-moduliruyushhie-aktivnost-toll-podobnyh-receptorov.html" rel="bookmark" title="База патентов Евразийского Союза">Соединения, модулирующие активность toll-подобных рецепторов</a>
Предыдущий патент: Способ транспортировки рельсов и машина для его осуществления
Следующий патент: Способ превращения гидратов, залегающих на морском дне, в товарное углеводородное соединение
Случайный патент: Применение козьей сыворотки, полученной иммунизацией козы вич, для изготовления лекарственных средств












