Производные 2-циклопропилкарбониламино-5-фенил[1,2,4]триазоло[1,5-a]пиридина для лечения дегенеративных и воспалительных заболеваний
Номер патента: 18587
Опубликовано: 30.09.2013
Авторы: Блан Хавьер, Жуанниго Нолвен, Ходжес Аластэр Джеймс, Ван Ромпай Люк Джулиан Корина, Флетчер Стефен Роберт, Мене Кристель Жанн Мари, Смитс Коэн Курт
Формула / Реферат
1. Применение соединения формулы (I)
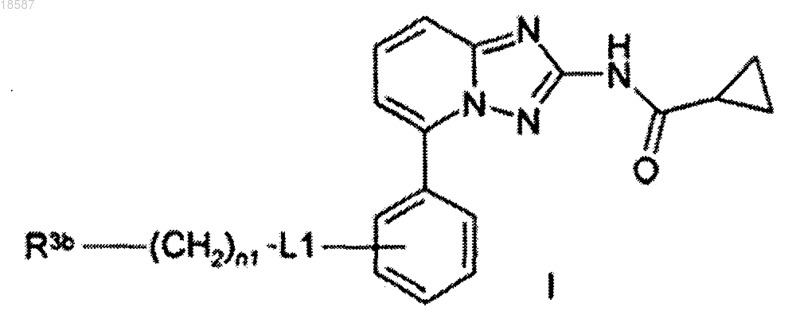
в которой
L1 выбирают из одинарной связи, -O-, -С(О)-, -С[=N(R4a)]-, -N(R4a)-, -CON(R4a)-, -SO2N(R4a)-, -S(O)2-,
-N(R4a)CO-, -CH2-N(R4a)- или -N(R4a)SO2-;
R3b независимо выбирают из
замещенного или незамещенного С6-10арила,
замещенного или незамещенного С3-С7циклоалкила,
замещенного или незамещенного 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, выбранных из N, О или S,
замещенного или незамещенного 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, О или S; или
R3b независимо выбирают из O-R3c, NH-R3c, CO-R3c и CON(R4a)-R3c; и
R3c независимо выбирают из
замещенного С1-С6алкила,
замещенного или незамещенного С6-10арила,
замещенного или незамещенного С3-С7циклоалкила,
замещенного или незамещенного 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, выбранных из N, О или S,
замещенного или незамещенного 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, О или S,;
каждый R4a независимо выбирают из Н, С1-С6алкила, замещенного С1-С6алкила, С3-С7циклоалкила, замещенного С3-С7циклоалкила;
причем заместители в определениях R3b , R3c, R4a выбирают из группы, состоящей из галогена, циано, нитро, трифторметила, трифторметокси, азидо, -NR'"SO2R", -SO2NR"R'", -C(O)R", -C(O)OR", -OC(O)R",
-NR"'C(O)R", -C(O)NR"R"', -NR"R"', -(CR"'R"')mOR"', где каждый R" независимо выбран из Н, С1-С8алкила,
-(СН2)t(С6-С10арила), -(СН2)t(5-10-членного гетероарила, включающего 1-3 гетероатома, выбранных из N, О или S), -(СН2)t(С3-С10циклоалкила) и -(СН2)t(4-10-членного гетероциклоалкила, включающего 1- 3 гетероатома, выбранных из N, О или S), где t представляет целое число 0-4; и
любая алкильная группа может быть замещена галогеном или ОН; и
любой арил, гетероарил, циклоакил или гетероциклоалкил могут быть замещены замещенным или незамещенным С1-С4алкилом, галогеном, незамещенным C1-С4алкокси, незамещенным С1-С4галогеналкилом, незамещенным С1-С4гидроксиалкилом или незамещенным С1-С4галогеналкокси или ОН;
каждый R"' независимо представляет Н или С1-С6алкил;
n1 равно 0, 1, 2, 3 или 4;
при условии, что
i) когда L1 представляет собой -O-, -N(R4a)-, -CH2-N(R4a)-, -CON(R4a)- или -SO2N(R4a)- и R3b является отличным от циклоалкила, арила или 5-10-членного гетероарила, тогда n1 равен 1, 2, 3 или 4;
ii) когда L1 представляет собой связь, n1 равен 0 и R3b представляет собой -OR3c, тогда R3c является отличным от Me или CF3;
или его фармацевтически приемлемой соли,
в лечении и/или предупреждении заболеваний, включающих деградацию хряща, деградацию кости и/или сустава; и/или состояний, включающих воспаление или иммунные реакции, таких как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей, ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния, заболевания, включающие ухудшение ремоделирования хряща, врожденные мальформации хряща, болезни Кастлемена, множественной миеломы, псориаза, саркомы Капоши и/или месангиального пролиферативного гломерунефрита и отторжение трансплантата; или пролиферативных заболеваний.
2. Применение соединения по п.1, где L1 выбирают из одинарной связи, -O-, -N(R4a)-; -С(О)-, -С[=N(R4a)]-,
-CON(R4a)-, -SO2N(R4a)-, -S(O)2-, -N(R4a)SO2- и -N(R4a)CO-; n1 имеет значение 0, 1, 2, 3 или 4; и R3b представляет собой пиперидинил, морфолинил, пиперазинил, гомопиперазинил или пирролидинил, каждый из которых может быть не замещен или замещен С1-С6алкилом, ацилом, фенилом или ОН, при условии, что
когда гетероцикл прикреплен через гетероатом и L1 представляет собой -O-, -N(R4a)-, -SO2N(R4a)- и
-CON(R4a)-; n1 не равно 0 или 1.
3. Применение соединения по п.1 или 2, где R4a представляет собой Н, замещенный или незамещенный С1-С4алкил.
4. Применение соединения по п.1 или 2, где R4a представляет собой -(CH2)n2-R6a; где n2 имеет значение 0, 1 или 2; и R6a представляет собой Н, CN, NMe2 или тетрагидрофуранил.
5. Применение соединения по п.1 или 2, где R4a представляет собой -СН(СН3)-(СН2)n2-R6a; где n2 имеет значение 0 или 1; и R6a представляет собой Н или ОМе.
6. Применение соединения по п.1 или 2, где R3b представляет собой OPh, или О-(4-F-Ph).
7. Применение соединения по п.1, где Ph-L1-(CH2)n1-R3b выбирают из
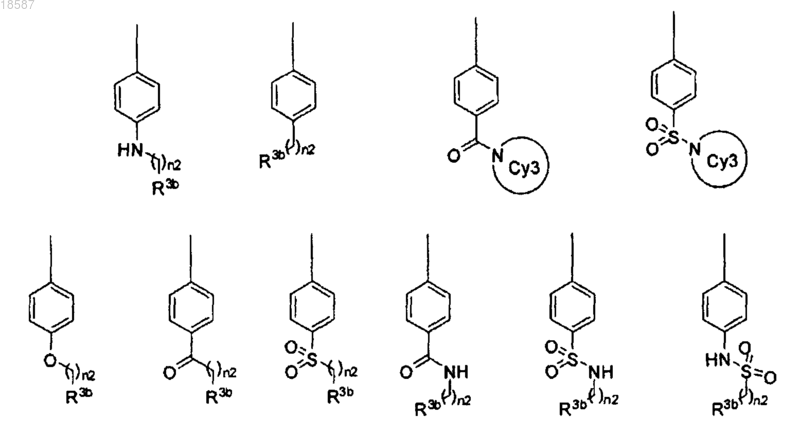
где n2 равен n1; и R3b и n1 являются такими же, как в п.1; и Су3 представляет собой замещенную или незамещенную N-содержащую 4-7-членную гетероциклоалкильную группу.
8. Применение соединения по п.7, где R3b выбирают из
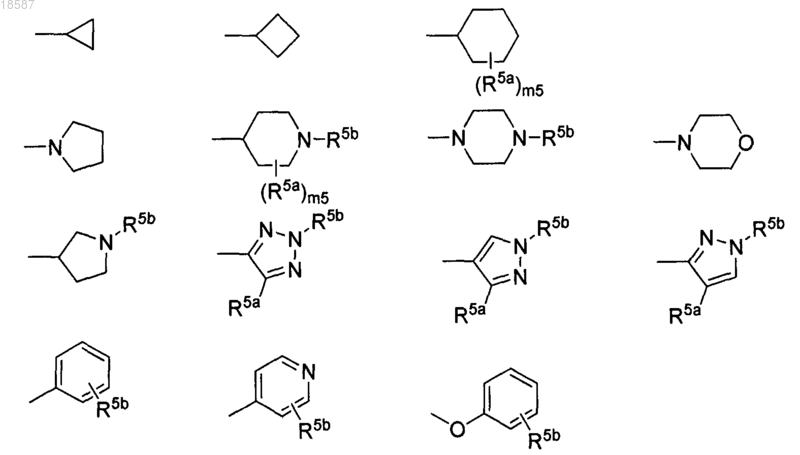
где каждый R5a независимо представляет собой С1-С4алкил, галоген, CF3 или фенил; R5b представляет Н,
С6-10арил, 5-10-членный гетероарил, включающий 1-3 гетероатома, выбранных из N, О или S, С3-С6циклоалкил или 4-7-членный гетероциклоалкил, включающий 1-3 гетероатома, выбранных из N, О или S; и m5 равен 0, 1 или 2.
9. Применение соединения по п.7, где Су3 выбирают из
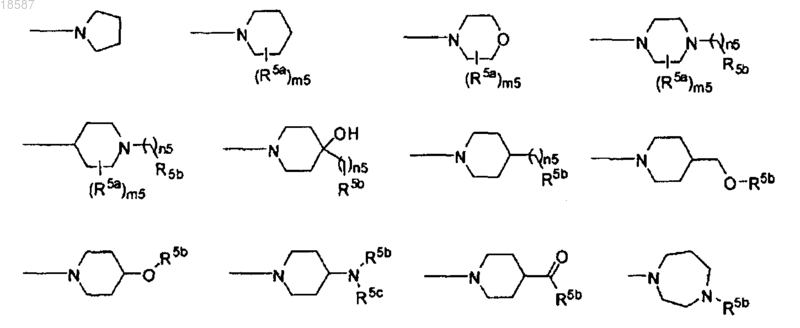
где каждый R5a независимо представляет собой С1-С4алкил, галоген, оксогруппу, CF3 или фенил; R5b представляет собой Н, С1-С4алкил, С6-С10арил, 5-10-членный гетероарил, включающий 1-3 гетероатома, выбранных N, О или S, С3-С6циклоалкил, 4-7-членный гетероциклоалкил, включающий 1-3 гетероатома, выбранных N, О или S; R5c представляет собой Н, С1-С4алкил; m5 имеет значение 0, 1 или 2; и n5 имеет значение 0, 1 или 2.
10. Применение соединения по любому из пп.1-9, где заболевание включает в себя воспаление, состояние, включающее иммунную реакцию или аутоиммунное заболевание, ухудшение ремоделирования хряща, пролиферативное заболевание, врожденную мальформацию хряща, болезнь Кастлемена, множественную миелому, псориаз, саркому Капоши и/или месангиальный пролиферативный гломерунефрит или представляет собой отторжение трансплантата.
11. Применение соединений по любому из пп.1-9, где заболевание, включающее воспаление, выбирают из ревматоидного артрита, остеоартрита, аллергии дыхательных путей и воспалительных заболеваний кишечника.
12. Применение соединений по любому из пп.1-9, где состояние, включающее иммунный ответ или аутоиммунное заболевание, выбирают из COPD, астмы, системной эриматозной волчанки, сахарного диабета типа I и воспалительного заболевания кишечника.
13. Применение соединений по любому из пп.1-9, где состояние, включающее ухудшение ремоделирования хряща, выбирают из остеоартрита, псориатического артрита, ювенильного ревматоидного артрита, подагрического артрита, септического или инфекционного артрита, реактивного артрита, симпатической рефлекторной дистрофии, альгодистрофии, синдромома Tietze или костального хондрита, фибромиалгии, остеохондрита, нейрогенного или невропатического артрита, артропатии, эндемических форм артрита, болезни Mseleni и болезни Handigodu; дегенерации, являющейся результатом фибромиалгии, системной эритематозной волчанки, склеродермы и анкилозирующего спондилита.
14. Применение соединений по любому из пп.1-9, где пролиферативное заболевание выбирают из рака, лейкемии, множественной миеломы или псориаза.
15. Применение соединений по любому из пп.1-9, где заболевание, включающее воспаление, представляет ревматоидный артрит.
16. Применение соединений по любому из пп.1-9, где заболевание является отторжением трансплантата.
Текст
ПРОИЗВОДНЫЕ 2-ЦИКЛОПРОПИЛКАРБОНИЛАМИНО-5 ФЕНИЛ[1,2,4]ТРИАЗОЛО[1,5-a]ПИРИДИНА ДЛЯ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ И ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ Раскрывают применение производных [1,2,4]триазоло[1,5-а]пиридина, а именно, производных 2-циклопропилкарбониламино-5-фенил-[1,2,4]триазоло[1,5-а]пиридина,которые имеют формулу,представленную формулой (I). Соединения могут быть использованы для приготовления фармацевтических композиций и могут быть использованы для предупреждения и лечения ряда состояний у млекопитающих,в том числе людей, включающих в качестве неограничивающего примера заболевания, включающие деградацию хряща, деградацию кости и/или сустава; и/или состояния, включающие воспаление или иммунные реакции, такие как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей, таких как астма, ринит, ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника,обусловленные действием эндотоксина болезненные состояния, такие как осложнения после шунтирования,или хронические обусловленные действием эндотоксина состояния, способствующие возникновению,например, хронической сердечной недостаточности, заболевания, включающие ухудшение ремоделирования хряща, такие как заболевания, включающие анаболическую стимуляцию хондроцитов, врожденные мальформации хряща, заболевания, связанные с гиперсекрецией IL6, и отторжение трансплантата, такие как отторжение пересаженного органа и пролиферативные заболевания. Мене Кристель Жанн Мари, Ван Ромпай Люк Джулиан Корина (BE),Флетчер Стефен Роберт (FR), Блан Хавьер (BE), Жуанниго Нолвен (FR),Ходжес Аластэр Джеймс (GB), Смитс Коэн Курт (BE) Область техники, к которой относится изобретение Настоящее изобретение относится к соединениям, которые являются ингибиторами JAK (Янускиназы), семейства тирозинкиназ, которые вовлечены в модуляцию деградации хрящей, деградации суставов и заболеваний, включающих такую деградацию и/или воспаление. Настоящее изобретение также обеспечивает способы получения этих соединений, фармацевтические композиции, содержащие эти соединения, способы предупреждения и/или лечения заболеваний, включающих деградацию хрящей, деградацию костей и/или суставов, состояний, включающих воспаление или иммунные реакции, обусловленных действием эндотоксина болезненных состояний, рака и отторжения пересаженных органов; и/или способы предупреждения и/или лечения заболеваний, включающих деградацию хрящей, деградацию суставов и/или воспаление, путем введения соединения изобретения. Янус-киназы (JAK-киназы) представляют собой цитоплазматические тирозинкиназы, которые трансдуцируют передачу сигнала цитокинов от мембранных рецепторов к факторам транскрипцииSTAT. Описаны четыре члена семейства JAK-киназ, JAK1, JAK2, JAK3 и TYK2. При связывании цитокина с его рецептором члены семейства JAK-киназ ауто- и/или трансфосфорилируют друг друга с последующим фосфорилированием STAT-киназ, которые затем мигрируют в ядра для модуляции транскрипции. Внутриклеточная сигнальная трансдукция JAK-STAT-киназ использует интерфероны, большую часть интерлейкинов, а также ряд цитокинов и эндокринные факторы, такие как ЕРО, ТРО, GH, OSM,LIF, CNTF, GM-CSF, PRL (Vainchenker W. et al. (2008. Исследование комбинаций генетических моделей и небольших молекул ингибиторов JAK-киназ открыло терапевтический потенциал нескольких JAK-киназ. JAK3-киназа признана в генетике мышей и человека в качестве мишени иммуносупрессии (О'Shea J. et al. (2004. Ингибиторы JAK3-киназы были результативно приняты в клиническую разработку, сначала в отношении отторжения пересаженных органов, но позднее также и в отношении других иммуновоспалительных показаний, таких как ревматоидный артрит (RA), псориаз и болезнь Крона (http://clinicaltrials.gov/).TYK2-киназа представляет собой потенциальную мишень для иммуновоспалительных заболеваний,которая признана в генетике человека и в исследованиях нокаутирования мышей (Levy D. и Loomis С.JAK1-киназа представляет собой новую мишень в области иммуновоспалительных заболеваний.JAK1-киназа гетеродимеризуется с другими JAK-киназами с трансдуцированием цитокинзависимой провоспалительной передачи сигнала. Таким образом, ингибирование JAK1-киназы и/или других JAKкиназ, как предполагают, имеет терапевтический эффект для ряда воспалителных состояний, а также для других заболеваний, обусловленных JAK-опосредованной сигнальной трансдукцией. Предпосылки создания изобретения Хрящ представляет собой несосудистую ткань, хондроциты которой составляют основной клеточный компонент. Хондроциты в нормальном суставном хряще занимают приблизительно 5% объема ткани, при этом внеклеточный матрикс заполняет оставшиеся 95% ткани. Хондроциты секретируют компоненты матрикса, главным образом протеогликаны и коллагены, которые в свою очередь снабжают хондроциты средой, подходящей для их выживания при воздействии механического напряжения. В хряще,тип II коллагена, вместе с типом IX белкового коллагена, скомбинирован в твердые фибриллоподобные структуры, которые придают хрящу большую механическую прочность. Протеогликаны могут поглощать воду и являются ответственными за упругие/эластичные и амортизационные свойства хряща. Одной из функциональных ролей хряща в суставе является предоставление возможности костям соединяться друг с другом безболезненно. Утрата суставного хряща, следовательно, вызывает трение костей друг о друга, что приводит к боли и к потере подвижности. Деградация хряща может иметь различные причины. В воспалительных артритах, таких как ревматоидный артрит, например, деградация хряща вызвана секрецией протеаз (например, коллагеназ) воспаленными тканями (например, воспаленный синовиальный слой). Деградация хряща также может быть результатом повреждения хряща, в результате несчастного случая, или хирургического вмешательства, или ненормально увеличенной нагрузки или"изнашивания и старения". Способность ткани хряща регенерироваться после таких повреждающих факторов ограничена. Хондроциты в поврежденном хряще часто проявляют сниженную активность синтезирования хряща (анаболическая активность) и/или повышенную активность деградирования хряща (катаболическая активность). Дегенерация хряща является признаком различных заболеваний, среди которых ревматоидный артрит и остеоартрит являются наиболее известными. Ревматоидный артрит (RA) представляет собой хроническое дегенеративное заболевание суставов, характеризующееся воспалением и деструкцией структур суставов. В том случае, когда заболевание недиагностировано, оно приводит к существенной недееспособности и боли вследствие потери функциональности суставов и даже к преждевременной смерти. Цель терапии ревматоидного артрита, следовательно, заключается не в том, чтобы замедлить развитие заболевания, но и добиться ремиссии с тем, чтобы остановить деструкцию суставов. Кроме тяжести исхода заболевания высокий уровень распространения ревматоидного артрита (0,8% взрослых во всем мире страдают от этого заболевания) означает высокие социально-экономические последствия (что касается обзоров по ревматоидному артриту, мы ссылаемся на обзор Smolen and Steiner (2003); обзор Lee andWeinblatt (2001); обзор Choy and Panayi (2001); обзор О'Dell (2004) и обзор Firestein (2003. Остеоартрит (также называемый как ОА или артрит изнашивания и старения) представляет собой наиболее обычную форму артрита и характеризуется утратой суставного хряща, часто связанной с гипертрофией кости, и болью. Заболевание в основном поражает руки и испытывающие нагрузку суставы,такие как колени, запястья и кости. Этот процесс истончает хрящ. В том случае, когда площадь поверхности исчезла вследствие истончения, достигается остеоартрит степени I; в том случае, когда площадь тангенциальной поверхности исчезла, достигается остеоартрит степени II. Существуют дополнительные уровни дегенерации и деструкции, которые поражают глубину и слои кальцинированного хряща, которые граничат с субхондральной костью. Что касается большого обзора по остеоартриту, то мы ссылаемся на обзор Wieland et al., 2005. Клинические проявления развития состояния при остеоартрите представляют собой следующее: увеличенный объем сустава, боль, крепитацию (хруст) и функциональную недееспособность, которые приводят к боли и сниженной подвижности суставов. В том случае, когда заболевание развивается дальше, то появляется боль в состоянии покоя. Если состояние сохраняется без коррекции и/или терапии, то сустав разрушается, приводя к недееспособности. Тогда требуется реконструктивная хирургия с полным протезированием. Терапевтические способы коррекции поражений суставного хряща, которые появляются в ходе остеоартритического заболевания, были разработаны, но на настоящий момент ни один из них не способен быть промежуточным звеном регенерации суставного хряща in situ и in vivo. Остеоартрит трудно лечить. В настоящее время нет доступного средства для лечения, и лечение фокусируется на обезболивании и на предотвращении наступления деформации пораженного сустава. Обычные виды лечения включают применение нестероидных противовоспалительных лекарственных средств (NSAIDs). Биологически активные добавки, такие как хондроитин-сульфат и глюкозаминсульфат, рекомендованы в качестве безопасных и эффективных методов лечения остеоартрита, последнее клиническое испытание открыло то, что оба вида лечения не снижали боль, сопутствующую остеоартриту. (Clegg et al., 2006). В своей совокупности нет доступных модифицирующих течение заболевания остеоартритических лекарственных средств. В тяжелых случаях может быть необходима замена сустава. В особенности это имеет место в отношении запястий и коленей. Если сустав является чрезвычайно болезненным и не может быть заменен, он может быть подвергнут сращиванию. Эта процедура останавливает боль, но приводит к постоянной утрате функции сустава, что делает ходьбу и сгибание затруднительными. Другое возможное лечение представляет собой трансплантацию культивированных аутологичных хондроцитов. Здесь, у пациента берут хондральный клеточный материал, посылают в лабораторию, где его выращивают. Затем материал имплантируют в поврежденные ткани с тем, чтобы закрыть дефекты ткани. Другое лечение включает внутрисуставную инстилляцию препарата Hylan G-F 20 (например, Synvisc, Hyalgan, Artz), вещества, которое улучшает временно реологические свойства синовиальной жидкости, производя почти мгновенное ощущение свободного движения и заметное снижение боли. Другие опубликованные способы включают применение сухожильных, периостальных, фасциальных, мышечных или перихондральных графтов; имплантацию фибрина или культивированных хондроцитов; имплантацию синтетических матриксов, таких как коллаген, углеродные нити; введение электромагнитных полей. Все из упомянутых способов предоставляли минимальные и недостаточные эффекты,дающие в результате ткань плохого качества, которая не может ни выдерживать утяжеленную нагрузку,ни давать возможность восстановления суставной функции с нормальным движением. Стимуляция анаболических процессов, блокирование катаболических процессов или комбинация этих двух методов могут приводить к стабилизации хряща и, возможно, даже к реверсии нарушения и,следовательно, могут предотвращать дальнейшее развитие заболевания. Различные триггеры могут стимулировать анаболическую стимуляцию хондроцитов. Инсулиноподобный фактор роста I (IGF-I) представляет собой численно преобладающий фактор роста в синовиальной жидкости и стимулирует синтез как протеогликанов, так и коллагена. Также было показано, что члены семейства костных морфогенетических белков (BMP), в особенности ВМР 2, ВМР 4, ВМР 6 и ВМР 7, и члены семейства трансформирующих факторов роста (TGF-) человека могут индуцировать анаболическую стимуляцию хондроцитов (Chubinskaya and Kuettner, 2003). Недавно было идентифицировано соединение, которое индуцирует анаболическую стимуляцию хондроцитов (US 6500854; ЕР 1391211). Однако большинство из этих соединений проявляют тяжелые побочные эффекты и, как следствие, существует сильная потребность в соединениях, которые стимулируют дифференцировку хондроцитов без этих побочных эффектов.Vandeghinste et al. (WO 2005/124342) открыли JAK1-киназу в качестве мишени, ингибирование которой могло бы иметь терапевтическую значимость для нескольких заболеваний, включающих остеоартрит. JAK1-киназы принадлежат к семейству Янус-киназ (JAK-киназы), состоящему из цитоплазматических тирозинкиназ, участвующих в опосредованной рецепторами цитокинов внутриклеточной сигналь-2 018587TYK2-киназа. JAK-киназы рекрутируются рецепторами цитокинов, при связывании цитокина, с последующей гетеродимеризацией рецептора цитокина и общей субъединицы рецептора (обычная цепь -с,gp130). Затем JAK-киназы активируются посредством ауто- и/или трансфосфорилирования с помощью другой JAK-киназы, что приводит к фосфорилированию рецепторов и к рекрутированию и фосфорилированию членов семейства (сигнальный трансдуктор и активатор транскрипции)-белков (белки STAT). Фосфорилированные белки STAT димеризуются и проникают в ядра, где они связываются с энхансерной областью цитокинотвечающих генов. Нокаутирование гена JAK1-киназы у мышей показало то, чтоJAK1-киназа играет важнейшие и неизбыточные роли во время развития: мыши с нокаутированным геном JAK1-киназы (JAK1-/-мыши) умирали в пределах 24 ч после рождения, и развитие лимфоцитов было сильнейшим образом нарушено (снижено). Кроме того, клетки с нокаутированным геном JAK1-киназы(JAK1-/-клетки) были нереакционноспособными или менее реакционноспособными по отношению к цитокинам, которые используют рецепторы цитокинов класса II, рецепторы цитокинов, которые используют субъединицу -с для передачи сигнала, и семейство рецепторов цитокинов, которые используют субъединицу gp130 для передачи сигнала (Rodig et al., 1998). Различные группы участвовали в передаче сигнала JAK-STAT-киназ в биологии хондроцитов. Li etal. (2001) показали, что онкостатин М индуцирует экспрессию генов ММР и TIMP3 в первичных хондроцитах посредством активации сигнальных путей JAK/STAT- и MAPK-киназ. Osaki et al. (2003) показали,что опосредованное интерфероном- ингибирование коллагена II в хондроцитах включает передачу сигнала JAK-STAT-киназ. IL1- индуцирует катаболизм хряща путем снижения экспрессии компонентов матрикса и путем индуцирования экспрессии коллагеназ и индуцируемой синтазы оксида азота (NOS2),которая обуславливает продуцирование оксида азота (NO). Otero et al. (2005) показали, что лептин и ILl синергистически индуцировали продуцирование NO или экспрессию мРНК синтазы NOS2 в хондроцитах и что то было подвергнуто блокаде посредством ингибитора JAK-киназ. Legendre et al. (2003) показали, что IL6/рецептор IL6 индуцировал отрицательную регуляцию генов коллагена II типа специфического матрикса хряща, центрального белка аггрекана и белка сшивок в суставных хондроцитах быка и что это было обусловлено передачей сигнала JAK-STAT-киназ. Следовательно, эти наблюдения позволяют предположить роль в отношении активности JAK-киназ в гомеостазе хряща и терапевтические возможности ингибиторов JAK-киназ. Члены семейства JAK-киназ были вовлечены в дополнительные состояния, включающие миелопролиферативные нарушения (O'Sullivan et al., 2007, Mol. Immunol. 44(10):2497-506), где были идентифицированы мутации JAK2-киназ. Это указывает на то, что ингибиторы JAK-киназ, в частности JAK2 киназ, также могут быть использованы в лечении миелопролиферативных нарушений. Кроме того, семейство JAK-киназ, в частности JAK1-киназа, JAK2-киназа и JAK3-киназа, было связано с раковыми заболеваниями, в частности с лейкемиями, например с острой миелоидной лейкемией (O'Sullivan et al.,Mol. Immunol. 44(10):2497-506; Xiang et al., 2008, "Identification of somatic JAK1 mutations in patients withacute myeloid leukemia" Blood First Edition Paper, ранее опубликованной он-лайн 26 декабря 2007; DOI 10.1182/blood-2007-05-090308) и с острой лимфобластной лейкемией (Mullighan et al., 2009) или с солидными опухолями, например с лейомиосаркомой матки (Constantinescu et al., 2007, Trends in BiochemicalSciences 33(3): 122-131), с раком предстательной железы (Tam et al., 2007, British Journal of Cancer, 97,378-383). Эти результаты указывают на то, что ингибиторы JAK-киназ, в частности JAK1-киназ и/илиJAK2-киназ, также могут иметь применение в лечении раковых заболеваний (лейкемии и солидных опухолей, например лейомиосаркомы, рака предстательной железы). Кроме того, заболевание Кастлемана, множественная миелома, мезангиальный пролиферативный гломерулонефрит, псориаз и саркома Капоши, вероятно, возникают вследствие гиперсекреции цитокинаIL-6, биологические эффекты которого обусловлены внутриклеточной передачей сигнала JAK-STATкиназ (Tetsuji Naka, Norihiro Nishimoto and Tadamitsu Kishimoto, Arthritis Res. 2002, 4 (suppl. 3):S233S242). Этот результат показывает, что ингибитор JAK-киназ также может найти применение в лечении вышеупомянутых заболеваний. Связь с аутоиммунными заболеваниями была установлена для JAK3- и TYK2-киназ. МутацииJAK3-киназ и также -с-цепи рецепторов компонентов передачи сигнала в обратном направлении и рецептора IL7 служат причиной в совокупности для 70% случаев возникновения тяжелого комбинированного иммунодефицита у человека (О'Shea et al., 2004). Следует отметить, что JAK1-киназа кооперируется с JAK3-киназой в трансдуцировании сигналов от -с-цепи рецепторов. Полиморфизмы TYK2 киназы наблюдают при системной эритематозной волчанке (SLE) (О'Sullivan et al., 2007, Mol. Immunol. 44(10):2497-506). Следовательно, направленное воздействие на семейство JAK-киназ может обеспечить терапевтическую возможность в области иммуновоспалительных заболеваний. Текущие виды терапии не являются удовлетворительными, и, следовательно, сохраняется потребность в установлении дополнительных соединений, которые могут быть полезны в лечении заболеваний,включающих деградацию хрящей, деградацию костей и/или суставов, например остеоартрита; и/или состояний, включающих воспаление или иммунные реакции, такие как болезнь Крона, ревматоидный арт-3 018587 рит, псориаз, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности), заболевания, включающие ухудшение ремоделирования хряща (например, заболевания,включающие анаболическую стимуляцию хондроцитов), врожденные мальформации хряща, заболевания, связанные с гиперсекрецией IL6, и отторжение трансплантата (например, отторжение пересаженного органа). Ингибиторы JAK-киназ также могут найти применение в лечении пролиферативных заболеваний. В частности, ингибиторы JAK-киназ находят применение в лечении раковых заболеваний, в особенности, лейкемий и солидных опухолей (например, лейомиосаркомы матки, рака предстательной железы). Настоящее изобретение, таким образом, обеспечивает соединения, способы для их изготовления и фармацевтические композиции, содержащие соединение изобретения вместе с подходящим фармацевтическим носителем. Настоящее изобретение также обеспечивает применение соединения изобретения в получении лекарственного препарата для лечения дегенеративных заболеваний суставов. Краткое изложение сущности изобретения Настоящее изобретение основано на открытии того, что ингибиторы JAK-киназы являются полезными в лечении заболеваний, включающих деградацию хряща, деградацию кости и/или сустава, например остеоартрита; и/или состояний, включающих воспаление или иммунные реакции, таких как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные воздействием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности), заболевания, включающие ухудшение ремоделирования хряща (например, заболевания, включающие анаболическую стимуляцию хондроцитов), врожденные мальформации хряща, заболевания, связанные с гиперсекрецией IL6, и отторжение трансплантата (например, отторжение пересаженного органа). Ингибиторы JAK-киназ также могут найти применение в лечении пролиферативных заболеваний. В частности, ингибиторы JAK-киназ находят применение в лечении раковых заболеваний, в особенности, лейкемий и солидных опухолей (например, лейомиосаркомы матки, рака предстательной железы). Настоящее изобретение также обеспечивает способы для получения этих соединений, фармацевтические композиции, содержащие эти соединения, и способы лечения заболеваний,включающих деградацию хряща, деградацию сустава и/или воспаление хряща, путем введения соединения изобретения. В связи с вышеизложенным в первом аспекте изобретения раскрывают применение 1,2,4 триазоло[1,5-а]пиридиновых соединений, имеющих формулу (I)L1 выбирают из одинарной связи, -O-, -С(О)-, -С[=N(R4a)]-, -N(R4a)-, -CON(R4a)-, -SO2N(R4a)-, -S(O)2-,4aR3b независимо выбирают из замещенного или незамещенного С 6-10 арила, замещенного или незамещенного С 3-С 7 циклоалкила, замещенного или незамещенного 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, выбранных из N, О или S, замещенного или незамещенного 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, О или S; илиR3b независимо выбирают из O-R3c, NH-R3c, CO-R3c и CON (R4a)-R3c;R3c независимо выбирают из замещенного С 1-С 6 алкила, замещенного или незамещенного С 6-10 арила,замещенного или незамещенного С 3-С 7 циклоалкила, замещенного или незамещенного 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, выбранных из N, О или S, замещенного или незамещенного 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, О или S; каждый R4a независимо выбирают из Н, С 1-С 6 алкила, замещенного С 1-С 6 алкила, С 3-С 7 циклоалкила; причем заместители в определениях R3b , R3c, R4a выбирают из группы, состоящей из галогена, циано, нитро, трифторметила, трифторметокси, азидо, -NR"'SO2R", -SO2NR"R"', -C(O)R", -C(O)OR",OC(O)R", -NR'"C(O)R", -C(O)NR"R'", -NR"R"', -(CR"'R'")mOR"', где каждый R" независимо выбран из Н,С 1-С 8 алкила, -(СН 2)t(С 6-С 10 арила), -(СН 2)t(5-10-членного гетероарила, включающего 1-3 гетероатома,выбранных из N, О, или S), -(СН 2)t(С 3-С 10 циклоалкила) и -(СН 2)t(4-10-членного гетероциклоалкила,включающего 1-3 гетероатома, выбранных из N, О, или S), где t представляет целое число 0-4; любая алкильная группа может быть замещена галогеном или ОН; любой арил, гетероарил, циклоакил или гетероциклоалкил могут быть замещены замещенным или незамещенным С 1-С 4 алкилом, галогеном, незамещенным C1-С 4 алкокси, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом или незамещенным C1-С 4 галогеналкокси или ОН; каждый R"' независимо представляет Н или С 1-С 6 алкил;i) когда L1 представляет собой -O-, -N(R4a)-, -CH2-N(R4a)-, -CON(R4a)- или -SO2N(R4a)- и R3b является отличным от циклоалкила, арила или 5-10-членного гетероарила, тогда n1 равен 1, 2, 3 или 4;ii) когда L1 представляет собой связь, n1 равен 0, и R3b представляет собой -OR3c, тогда R3c является отличным от Me или CF3; или его фармацевтически приемлемая соль,в лечении и/или предупреждении заболеваний, включающих деградацию хряща, деградацию кости и/или сустава; и/или состояний, включающих воспаление или иммунные реакции, таких как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей, ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния, заболевания, включающие ухудшение ремоделирования хряща, врожденные мальформации хряща, болезни Кастлемена, множественной миеломы, псориаза, саркомы Капоши и/или месангиального пролиферативного гломерунефрита и отторжение трансплантата; или пролиферативных заболеваний. В дополнительном аспекте настоящее изобретение раскрывает применение 1,2,4-триазоло[1,5 а]пиридиновых соединений формулы I, которые способны быть действенными в модулировании активности JAK-киназ in vivo. В дополнительном аспекте настоящее изобретение обеспечивает применение соединений формулыI или их фармацевтически приемлемых солей для лечения и/или предупреждения заболеваний, включающих деградацию хряща, деградацию кости и/или сустава, например остеоартрита; и/или состояний,включающих воспаление или иммунные реакции, такие как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит,воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния(например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности), заболевания, включающие ухудшение ремоделирования хряща (например, заболевания, включающие анаболическую стимуляцию хондроцитов), врожденные мальформации хряща, заболевания, связанные с гиперсекрецией IL6, и отторжение трансплантата (например, отторжение пересаженного органа) или пролиферативных заболеваний. В дополнительном аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении или в предупреждении состояния, выбранного из состояний, перечисленных в этом документе, особенно таких состояний, которые могут быть связаны с аберрантной активностью JAK-киназ,таких как заболевания, включающие деградацию хряща, деградацию кости и/или сустава, например остеоартрит; и/или состояния, включающие воспаление или иммунные реакции, такие как болезнь Крона,ревматоидный артрит, псориаз, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности), заболевания, включающие ухудшение ремоделирования хряща (например,заболевания, включающие анаболическую стимуляцию хондроцитов), врожденные мальформации хряща, заболевания, связанные с гиперсекрецией IL6, и отторжение трансплантата (например, отторжение пересаженного органа). Ингибиторы JAK-киназ также могут найти применение в лечении пролиферативных заболеваний. :В частности, ингибиторы JAK-киназ находят применение в лечении раковых заболеваний, в особенности лейкемий и солидных опухолей (например, лейомиосаркомы матки, рака предстательной железы). В конкретном варианте осуществления состояние выбирают из воспаления, такого как ревматоидный артрит, ювенильный идиопатический артрит, псориаз, аллергия дыхательных путей(например, астма, ринит), воспалительные заболевания кишечника (например, болезнь Крона, колит),обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности) и отторжение пересаженного органа; и деградации или дегенерации хряща, кости и/или сустава, такой как остеоартрит. В дополнительном аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении или в предупреждении пролиферативных нарушений, в частности ракового заболевания,(например, солидные опухоли), лейкемий, множественной миеломы или псориаза. В дополнительном аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении или в предупреждении состояния, которое причинно связано с аномальной активностьюJAK-киназ. Другие цели и преимущества изобретения станут ясны специалистам в данной области из рассмот-5 018587 рения раздела, обеспечивающего подробное описание изобретения. Подробное описание изобретения Следующие термины, как подразумевают, имеют значения, представленные сразу же ниже, и являются полезными в понимании описания и предполагаемого объема настоящего изобретения. При описании изобретения, которое может включать соединения, фармацевтические композиции,содержащие такие соединения, и способы применения таких соединений и композиций, следующие термины, если присутствуют, имеют следующие значения, если не указано иное. Также следует понимать,что описанные в этом документе любые фрагменты, определенные далее ниже, могут быть замещены разнообразными заместителями и что соответственные определения предназначены для включения таких замещенных фрагментов в пределах их объема, который изложен ниже. Если не установлено иное, термин "замещенный" должен быть определен так, как изложено ниже. Следует дополнительно понимать,что термины "группы" и "радикальные группы" могут считаться взаимозаменяемыми при использовании в этом документе. Ацил относится к радикальной группе -C(O)R20, где R20 представляет собой водород, С 1-С 8 алкил,С 3-С 10 циклоалкил, С 3-С 10 циклоалкилметил, 4-10-членный гетероциклоалкил, арил, арилалкил, 5-10 членный гетероарил или гетероарилалкил, которые определены в этом документе. Репрезентативные примеры включают формил, ацетил, циклогексилкарбонил, циклогексилметилкарбонил, бензоил и бензилкарбонил, но не ограничиваются этим. Характерными ацильными группами являются -С(O)Н, -С(O)С 1-С 8 алкил, -С(O)-(СН 2)t(С 6-С 10 арил), -С(О)-(СН 2)t(5-10-членный гетероарил), -С(O)-(СН 2)t(С 3-С 10 циклоалкил) и -С(О)-(СН 2)t(4-10-членный гетероциклоалкил), где t представляет собой целое число от 0 до 4. Замещенный ацил относится к радикальной группе -C(O)R21, где R21 независимо представляет собой С 1-С 8 алкил, замещенный галогеном или гидроксигруппой; или С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, арилалкил, 5-10-членный гетероарил или гетероарилалкил, каждый из которых замещен незамещенным С 1-С 4 алкилом, галогеном, незамещенной С 1-С 4 алкоксигруппой, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом или незамещенной С 1-С 4 галогеналкоксигруппой или гидроксигруппой. Ациламиногруппа относится к радикальной группе NR22C(O)R23, где R22 представляет собой водород, C1-C8 алкил, С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, арилалкил, 5-10 членный гетероарил или гетероарилалкил, и R23 представляет собой водород, С 1-С 8 алкил, С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, арилалкил, 5-10-членный гетероарил или гетероарилалкил, которые определены в этом документе. Характерная ациламиногруппа включает формиламиногруппу, ацетиламиногруппу, циклогексилкарбониламиногруппу, циклогексилметилкарбониламиногруппу, бензоиламиногруппу и бензилкарбониламиногруппу, но не ограничивается этим. Характерные ациламиногруппы представляют собой -NR21'C(О)-С 1-С 8 алкил, -NR21'C(O)-(CH2)t(C6 С 10 арил), -NR21'C(O)-(CH2)t (5-10-членный гетероарил), -NR21'C(O)-(CH2)t(С 3-С 10 циклоалкил) и-NR21'C(O)-(СН 2)t (4-10-членный гетероциклоалкил), где t представляет собой целое число от 0 до 4, каждый R21' независимо представляет собой Н или С 1-С 8 алкил. Замещенная ациламиногруппа относится к радикальной группе -NR24C(O)R25, гдеR24 независимо представляет собой Н, С 1-С 8 алкил, замещенный галогеном или гидроксигруппой; или С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, арилалкил, 5-10-членный гетероарил или гетероарилалкил, каждый из которых замещен незамещенным С 1-С 4 алкилом, галогеном, незамещенной С 1-С 4 алкоксигруппой, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом,или незамещенной С 1-С 4 галогеналкоксигруппой или гидроксигруппой; иR25 независимо представляет собой Н, С 1-С 8 алкил, замещенный галогеном или гидроксигруппой; или С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, арилалкил, 5-10-членный гетероарил или гетероарилалкил, каждый из которых замещен незамещенным С 1-С 4 алкилом, галогеном, незамещенной С 1-С 4 алкоксигруппой, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом,или незамещенной С 1-С 4 галогеналкоксигруппой или гидроксилом; при условии, что по меньшей мере один из заместителей: R24 или R25 является отличным от Н. Алкоксигруппа относится к группе -OR26, где R26 представляет собой С 1-С 8 алкил. Конкретные алкоксигруппы представляют собой метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, нбутоксигруппу, трет-бутоксигруппу, втор-бутоксигруппу, н-пентоксигруппу, н-гексоксигруппу и 1,2 диметилбутоксигруппу. Конкретные алкоксигруппы являются низшими алкоксигруппами, то есть имеют от 1 до 6 атомов углерода. Дополнительные конкретные алкоксигруппы имеют от 1 до 4 атомов углерода. Замещенная алкоксигруппа относится к алкоксигруппе, замещенной одной или несколькими группами из тех групп, которые перечислены в определении "замещенного" в этом документе, и в особенности относится к алкоксигруппе, имеющей 1 или более заместителей, например от 1 до 5 заместителей,особенно от 1 до 3 заместителей и в особенности 1 заместитель, выбранный из группы, состоящей из аминогруппы, замещенной аминогруппы, С 6-С 10 арила, -О-арила, карбоксила, цианогруппы, С 3-С 10 циклоалкила, 4-10-членного гетероциклоалкила, галогена, 5-10-членного гетероарила, гидроксила, нитрогруппы, тиоалкоксигруппы, тио-О-арила, тиола, алкил-S-(О)-, арил-S-(О)-, алкил-S-(О)2- и арил-S-(O)2-. Показательные замещенные алкоксигруппы представляют собой -О-(СН 2)t(С 6-С 10 арил), -О-(СН 2)t(5-10-6 018587 членный гетероарил), -О-(СН 2)t(С 3-С 10 циклоалкил) и -О-(СН 2)t(4-10-членный гетероциклоалкил), где t является целым числом от 0 до 4, и любые присутствующие арильные, гетероарильные, циклоалкильные или гетероциклоалкильные группы могут быть сами по себе замещены незамещенным С 1-С 4 алкилом,галогеном, незамещенной С 1-С 4 алкоксигруппой, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом или незамещенной С 1-С 4 галогеналкоксигруппой или гидроксилом. Конкретные показательные замещенные алкоксигруппы представляют собой OCF3, OCH2CF3, OCH2Ph, ОСН 2 циклопропил, ОСН 2 СН 2 ОН, OCH2CH2NMe2. Алкоксикарбонил относится к радикальной группе -С(О)-OR27, где R27 представляет собой С 1-С 8 акил, С 3-С 10 циклоалкил, С 3-С 10 циклоалкилалкил, 4-10-членный гетероциклоалкилалкил, арилалкил или 5-10-членный гетероарилалкил, которые определены в этом документе. Показательные алкоксикарбонильные группы представляют собой С(O)O-С 1-С 8 алкил, -С(O)О-(СН 2)t(С 6-С 10 арил), -С(О)О-(СН 2)t(5-10 членный гетероарил), -С(О)О-(СН 2)t(С 3-С 10 циклоалкил) и -С(О)О-(СН 2)t(4-10-членный гетероциклоалкил) , где t является целым числом от 0 до 4. Замещенный алкоксикарбонил относится к радикальной группе -С(О)-OR28, где R28 представляет собой С 1-С 8 акил, С 3-С 10 циклоалкил, С 3-С 10 циклоалкилалкил или 4-10-членный гетероциклоалкилалкил,каждый из которых замещен галогеном, замещенной или незамещенной аминогруппой или гидроксигруппой; или С 6-С 10 арилалкил или 5-10-членный гетероарилалкил, каждый из которых замещен незамещенным С 1-С 4 алкилом, галогеном, незамещенной С 1-С 4 алкоксигруппой, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом или незамещенной С 1-С 4 галогеналкоксигруппой или гидроксилом. Алкил означает неразветвленный или разветвленный алифатический углеводород, имеющий 1-20 атомов углерода. Особый алкил имеет 1-12 атомов углерода. Более особый представляет собой низший алкил, который имеет 1-6 атомов углерода. Дополнительная особая алкильная группа имеет 1-4 атома углерода. Показательные группы с прямой цепью включают метил, этил, н-пропил, и н-бутил. "Разветвленный" означает, что одна или более низших алкильных групп, таких как метил, этил, пропил или бутил, являются присоединенными к линейной алкильной цепи, характерные группы с разветвленной цепью включают изопропил, изобутил, трет-бутил и изоамил. Замещенный алкил относится к алкильной группе, замещенной галогеном или ОН. Арил относится к одновалентной ароматической углеводородной группе, полученной удалением одного атома водорода от одного атома углерода исходной ароматической циклической системы. В особенности, арил относится к ароматической циклической структуре, моноциклической или полициклической, которая включает от 6-10 кольцевых членов. В том случае, когда арильная группа представляет собой моноциклическую кольцевую систему, она предпочтительно содержит 6 атомов углерода. Обычные арильные группы включают группы, полученные из ацеантрилена, аценафтилена, ацефенантрилена,антрацена, азулена, бензола, хризена, коронена, флуорантена, флуорена, гексацена, гексафена, гексалена,аз-индацена, сим-индацена, индана, индена, нафталина, октацена, октафена, окталена, овалена, пента-2,4 диена, пентацена, пенталена, пентафена, перилена, феналена, фенантрена, пицена, плиадена, пирена, пирантрена, рубицена, трифенилена и тринафталина, но не ограничиваются этим. Особенно арильные группы включают фенил, нафтил, инденил и тетрагидронафтил."Замещенный арил" относится к арильной группе, замещенной одной или несколькими группами из тех групп, которые перечислены в определении "замещенного" в этом документе, и особенно относится к арильной группе, которая может быть необязательно замещена 1 или более заместителями. Конкретно,"замещенный арил" относится к арильной группе, замещенной одной или более группами, выбранными из галогена, С 1-С 8 алкила, С 1-С 8 галогеналкила, С 1-С 8 галогеналкоксигруппы, гидроксигруппы, С 1 С 8 алкоксигруппы. Примеры репрезентативных замещенных арилов включают следующее: В этих формулах один из заместителей R49 или R50 может представлять собой водород, и по меньшей мере один из заместителей R49 или R50 независимо выбирают из С 1-С 8 алкила, C1-С 8 алкоксигруппы."Циклоалкил" относится к циклическим неароматическим гидрокарбильным группам, имеющим от 3 до 10 атомов углерода. Такие циклоалкильные группы включают в качестве примера однокольцевые структуры, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил."Замещенный циклоалкил" относится к циклоалкильной группе, которая определена выше, замещенной одной или несколькими группами из тех групп, которые перечислены в определении "замещенного" в этом документе, и особенно относится к циклоалкильной группе, имеющей 1 или более заместителей, например от 1 до 5 заместителей, особенно от 1 до 3 заместителей, в особенности 1 заместитель."Галогено" или "галоген" относится к фтору (F), хлору (Cl), брому (Br) и йоду (I). Конкретные галогеногруппы представляют собой либо фтор, либо хлор."Гетеро" в том случае, когда используют для описания соединения или группы, присутствующей в соединении, означает, что один или более атомов углерода в соединении или в группе были заменены гетероатомом азота, кислорода или серы. "Гетеро" может быть применен к любым гидрокарбильным группам, описанным выше, таким как алкил, например гетероалкил, циклоалкил, например гетероциклоалкил, арил, например гетероарил, циклоалкенил, например циклогетероалкенил, и тому подобное,имеющим от 1 до 5, в особенности от 1 до 3 гетероатомов."Гетероарил" означает ароматическую циклическую структуру, моноциклическую или полициклическую, которая включает один или более гетероатомов и 5-12 кольцевых членов, более обычно 5-10 кольцевых членов. Гетероарильная группа может представлять собой, например, 5-членное или 6 членное моноциклическое кольцо или бициклическую структуру, образованную из конденсированных 5 и 6-членных колец, или из двух конденсированных 6-членных колец, или в качестве дополнительного примера из двух конденсированных 5-членных колец. Каждое кольцо может содержать вплоть до четырех гетероатомов, обычно выбранных из азота, серы и кислорода. Обычно гетероарильное кольцо будет содержать вплоть до 4 гетероатомов, более обычно вплоть до 3 гетероатомов, более обычно вплоть до 2,например 1 гетероатом. В одном варианте осуществления гетероарильное кольцо содержит по меньшей мере 1 атом азота в кольце. Атомы азота в гетероарильных кольцах могут быть основными, как в случае имидазола или пиридина, или, по существу, неосновными, как в случае азота в индоле или в пирроле. В большинстве случаев число основных атомов азота, присутствующих в гетероарильной группе, включая любые аминогруппы-заместители кольца, будет составлять менее 5. Примеры 5-членных моноциклических гетероарильных групп включают пиррольные, фурановые, тиофеновые, имидазольные, фуразановые, оксазольные, оксадиазольные, оксатриазольные, изоксазольные, тиазольные, изотиазольные, пиразольные, триазольные группы, но не ограничиваются этим. Примеры 6-членных моноциклических гетероарильных групп включают пиридин, пиразин, пиридазин, пиримидин и триазин, но не ограничиваются этим. Конкретные примеры бициклических гетероарильных групп, содержащих 5-членное кольцо, конденсированное с другим 5-членным кольцом, включают имидазотиазол и имидазоимидазол, но не ограничиваются этим. Конкретные примеры бициклических гетероарильных групп, содержащих 6-членное кольцо, конденсированное с 5-членным кольцом, включают бензофурановые, бензотиофеновые, бензимидазольные, бензоксазольные, изобензоксазольные, бензизоксазольные, бензтиазольные, бензизотиазольные, изобензофурановые, индольные, изоиндольные, изоиндолоновые, индолизиновые, индолиновые, изоиндолиновые, пуриновые (например, аденин, гуанин), индазольные, пиразолопиримидиновые,триазолопиримидиновые, бензодиоксольные и пиразолопиридиновые группы, но не ограничиваются этим. Конкретные примеры бициклических гетероарильных групп, содержащих два конденсированных 6-членных кольца, включают хинолиновые, изохинолиновые, хромановые, тиохромановые, хроменовые,изохроменовые, хромановые, изохромановые, бензодиоксановые, хинолизиновые, бензоксазиновые, бензодиазиновые, пиридопиридиновые, хиноксалиновые, хиназолиновые, циннолиновые, фталазиновые,нафтиридиновые и птеридиновые группы, но не ограничиваются этим. Конкретные гетероарильные группы представляют собой гетероарильные группы, полученные из тиофена, пиррола, бензотиофена,бензофурана, индола, пиридина, хинолина, имидазола, оксазола и пиразина. Примеры репрезентативного арила, имеющего гетероатомы, содержащий замещение, включают следующее: где каждый W выбирают из C(R54)2, NR54, О и S; и каждый Y выбирают из карбонила, NR54, О и S; и R54 представляет собой независимо водород, С 1-С 8 алкил, С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, 5-10-членный гетероарил. Примеры репрезентативных гетероарилов включают следующее: где каждый Y выбирают из карбонила, N, NR55, О и S; и R55 независимо представляет собой водород, С 1 С 8 алкил, С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил, и 5-10-членный гетероарил. Используемый в этом документе термин "гетероциклоалкил" относится к 4-10-членному, стабильному гетероциклическому неароматическому кольцу и/или включает конденсированные кольца, содержащие один или более гетероатомов, независимо выбранных из N, О и S. Конденсированная гетероциклическая кольцевая система может включать карбоциклические кольца и требует включения только одного гетероциклического кольца. Примеры гетероциклических колец включают морфолин, пиперидин(например, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил и 4-пиперидинил) , пирролидин (например,1-пирролидинил, 2-пирролидинил и 3-пирролидинил), пирролидон, пиран (2 Н-пиран или 4 Н-пиран), дигидротиофен, дигидропиран, дигидрофуран, дигидротиазол, тетрагидрофуран, тетрагидротиофен, диоксан, тетрагидропиран (например, 4-тетрагидропиранил), имидазолин, имидазолидинон, оксазолин, тиазолин, 2-пиразолин, пиразолидин, пиперазин и N-алкилпиперазины, такие как N-метилпиперазин, но не ограничиваются этим. Дополнительные примеры включают тиоморфолин и его S-оксид и S,S-диоксид (в особенности тиоморфолин). Еще дополнительные примеры включают азетидин, пиперидон, пиперазон иN-алкилпиперидины, такие как N-метилпиперидин. Конкретные примеры гетероциклоалкильных групп показаны в следующих иллюстративных примерах: где каждый Y выбирают из CR56, C(R56)2, NR56, О и S; и каждый Y выбирают из NR56, О и S; и R56 независимо представляет водород, С 1-С 8 алкил, С 3-С 10 циклоалкил, 4-10-членный гетероциклоалкил, С 6-С 10 арил,и 5-10-членный гетероарил. Эти гетероциклоалкильные кольца могут быть необязательно замещены одной или несколькими группами, выбранными из группы, состоящей из ацила, ациламиногруппы, ацилоксигруппы (-О-ацил или -OC(O)R20), алкоксигруппы, алкоксикарбонила, алкоксикарбониламиногруппы(амидогруппа или -C(O)-NR"2), аминокарбониламиногруппы (-NR-С(О)-NR2), аминокарбонилоксигруппы (-O-С(О)-NR"2), аминосульфонила, сульфониламиногруппы, арила, -О-арила, азидогруппы, карбоксила, цианогруппы, циклоалкила, галогена, гидроксигруппы, нитрогруппы, тиола, -S-алкила, -Sарила, -S(О)-алкила, -S(O)-арила, S(O)2-алкила и -S(О)2-арила. Группы-заместители включают карбонил или тиокарбонил, который обеспечивает, например, производные лактама и мочевины."Замещенный" относится к группе, в которой один или более атомов водорода, каждый независимо,заменены одинаковыми или различными заместителями. Среднему специалисту в области органического синтеза будет ясно, что максимальное число гетероатомов в стабильном, химически возможном (допустимом) гетероциклическом кольце, является ли оно ароматическим или неароматическим, определяется размером кольца, степенью ненасыщенности и валентностью гетероатомов. Как правило, гетероциклическое кольцо может иметь от одного до четырех гетероатомов, если гетероароматическое кольцо является химически возможным и стабильным."Фармацевтически приемлемый" означает разрешенный или одобренный регуляторным органом правительства страны или штата или соответствующим органом стран, отличных от Соединенных Штатов, или то, что приведено в Фармакопее США или в других общепризнанных фармакопеях для приме-9 018587 нения на животных и в большей степени на людях."Фармацевтически приемлемая соль" относится к соли соединения изобретения, которая является фармацевтически приемлемой и которая обладает желательной фармакологической активностью исходного (родоначального) соединения. В частности, такие соли являются нетоксичными и могут представлять собой соли присоединения неорганических и органических кислот и соли присоединения основания. Конкретно, такие соли включают: 1) соли присоединения кислоты, образованные с неорганическими кислотами, такими как хлористоводородная кислота, бромисто-водородная кислота, серная кислота, азотная кислота, фосфорная кислота,и тому подобное; или образованные с органическими кислотами, такими как уксусная кислота, пропионовая кислота, капроновая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4 гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота,этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфокислота, 4-метилбицикло[2.2.2]-окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 3-фенилпропионовая кислота, триметилуксусная кислота, третичная бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота,салициловая кислота, стеариновая кислота, муконовая кислота и тому подобное; или(2) соли, образованные либо при замене кислотного протона, присутствующего в исходном соединении, на ион металла, например ион щелочного металла, ион щелочно-земельного металла или ион алюминия; либо при его координации с органическим основанием, таким как этаноламин, диэтаноламин,триэтаноламин, N-метилглюкамин и тому подобное. Соли дополнительно включают только в качестве примера натрий, калий, кальций, магний, аммоний, тетраалкиламмоний и тому подобное; и в том случае,когда соединение содержит основную функциональность, соли нетоксичных органических или неорганических кислот, такие как гидрохлорид, гидробромид, тартрат, мезилат, ацетат, малеат, оксалат и тому подобное. Термин "фармацевтически приемлемый катион" относится к приемлемому катионному противоиону кислотной функциональной группы. В качестве примера таких катионов могут быть приведены натриевые, калиевые, кальциевые, магниевые, аммониевые, тетраалкиламмониевые катионы и тому подобное."Фармацевтически приемлемая среда для лекарства" относится к разбавителю, адъюванту, эксципиенту или носителю, с которым соединение изобретения вводят."Предупреждение" или "предотвращение" относится к снижению риска приобретения или развития заболевания или нарушения (то есть к фактору, способствующему тому, чтобы по меньшей мере один из клинических симптомов заболевания не развивался у субъекта, который мог быть подвергнут воздействию вызывающего заболевание вещества, или который мог быть предрасположен данному заболеванию,с опережением начала заболевания). Термин "профилактика" относят к "предупреждению" и относится к мере или к процедуре, целью которой является предупреждение, а не лечение или вылечивание заболевания. Неограничивающие примеры профилактических мер могут включать введение вакцин; введение гепарина с низкой молекулярной массой госпитализированным пациентам с риском тромбоза вследствие, например, иммобилизации; и введение противомалярийного средства, такого как хлорохин, накануне визита географической зоны,где малярия является эндемической или где риск заражения малярией является высоким."Процесс лечения" или "лечение" любого заболевания или нарушения относится в одном варианте осуществления к уменьшению интенсивности симптомов заболевания или нарушения (то есть к купированию заболевания или к снижению проявления степени или тяжести по меньшей мере одного из его клинических симптомов). В другом варианте осуществления "процесс лечения" или "лечение" относится к улучшению по меньшей мере одного физического параметра, который не может быть явным (заметным) для субъекта. В еще одном варианте осуществления "процесс лечения" и "лечение" относится к модулированию заболевания или нарушения либо физически (например, стабилизация явного симптома), физиологически, (например, стабилизация физического параметра), либо обоими методами. В дополнительном варианте осуществления "процесс лечения" и "лечение" относится к замедлению прогрессирования заболевания. Используемый в этом документе термин "состояние(я), включающее(ие) воспаление" относится к группе состояний, включающих ревматоидный артрит, остеоартрит, ювенильный идиопатический артрит, псориаз, аллергию дыхательных путей (например, астма, ринит), воспалительные заболевания кишечника (например, болезнь Крона, колит), обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению хронической сердечной недостаточности) и сопутствую- 10018587 щие заболевания, вовлекающие в патологический процесс хрящ, такие как заболевания суставов. В особенности термин относится к ревматоидному артриту, остеоартриту, аллергии дыхательных путей (например, астме) и воспалительным заболеваниям кишечника. Используемые в этом документе термины "состояние(я), вовлекающее(ие) в патологический процесс иммунную реакцию" или "аутоиммунные заболевания" используют взаимозаменяемо и используют при обращении к группе заболеваний, включающих обструктивное заболевание дыхательных путей, в том числе COPD (хроническую обструктивную болезнь легких), астму (например, наследственную (эндогенную) бронхиальную астму, приобретенную (экзогенную) бронхиальную астму, пылевую астму,детскую астму), в особенности хроническую или застарелую астму (например, поздную астму и гиперчувствительность дыхательных путей), бронхит, в том числе бронхиальную астму, системную эритематозную волчанку (SLE), множественный склероз, сахарный диабет типа I и осложнения, сопутствующие тому, атопическую экзему (атопический дерматит), контактный дерматит и дополнительные экзематозные дерматиты, воспалительное заболевание кишечника (например, болезнь Крона и неспецифический язвенный колит), атеросклероз и амиотрофический латеральный склероз. Особенно термин относится кCOPD (хроническая обструктивная болезнь легких), астме, системной эриматозной волчанке, сахарному диабету типа I и воспалительному заболеванию кишечника. Использованный в этом документе термин "отторжение трансплантата" относится к острому или хроническому отторжению алло- или ксенографтов клеток, ткани или цельных органов, например панкреатического островка, стволовых клеток, костного мозга, кожи, мышцы, роговичной ткани, нейрональной ткани, сердца, легких, объединенного аппарата сердце-легкие, почки, печени, кишечника, поджелудочной железы, трахеи или пищевода, или к заболеваниям-реакциям "трансплантат против хозяина". Использованный в этом документе термин "пролиферативное(ые) заболевание(я)" относится к состояниям, таким как раковое заболевание (например, лейомиосаркома матки или рак предстательной железы), миелопролиферативные нарушения, называемые, в частности, как активирующие мутацииJAK2-киназы (истинная полицитемия, эссенциальная тромбоцитемия и миелоидная метаплазия с миелофиброзом), лейкемия (например, острая миелоидная лейкемия и острая лимфобластная лейкемия), множественная миелома, псориаз, рестеноз, склеродермит или фиброз. В частности, термин относится к раковому заболеванию, лейкемии, множественной миеломе и псориазу. Использованный в этом документе термин "раковое заболевание" относится к злокачественному или доброкачественному росту клеток на коже или в органах тела, например и без ограничения, в молочной (грудной) железе, предстательной железе, легком, почке, поджелудочной железе, желудке или кишечнике. Раковое заболевание имеет тенденцию инфильтрировать в смежную ткань и распространяться(метастазировать) в отдаленных органах, например в кости, печени, легком или мозге. Используемый в этом документе термин "раковое заболевание" включает как типы клеток метастатической опухоли, такие как меланома, лимфома, лейкемия, фибросаркома, рабдомиосаркома и мастоцитома, но не ограниченные этим, так и типы карциномы тканей, такие как раковое заболевание прямой и ободочной кишки,рак предстательной железы, мелкоклеточный рак легкого и немелкоклеточный рак легкого, рак молочной железы, рак поджелудочной железы, рак мочевого пузыря, рак почек, рак желудка, глиобластома,первичный рак печени, рак яичников, рак предстательной железы и лейомиосаркома матки, но не ограниченные этим. Использованный в этом документе термин "лейкемия" относится к неопластическим заболеваниям крови и кроветворных органов. Такие заболевания могут вызывать дисфункцию костного мозга и иммунной системы, что делает организм "хозяина" высокочувствительным к инфекции и кровотечению. В частности, термин лейкемия относится к острой миелоидной лейкемии (AML) и к острой лимфобластной лейкемии (ALL). Использованный в этом документе термин "заболевания, включающие ухудшение ремоделирования хряща" или "заболевания, включающие анаболическую стимуляцию хондроцитов" включает состояния,такие как остеоартрит, псориатический артрит, ювенильный ревматоидный артрит, подагрический артрит, септический или инфекционный артрит, реактивный артрит, симпатическая рефлекторная дистрофия, альгодистрофия, синдром Tietze или костальный хондрит, фибромиалгия, остеохондрит, нейрогенный или невропатический артрит, артропатия, эндемические формы артрита, например деформирующий остеоартрит эндемический, болезнь Mseleni и болезнь Handigodu; дегенерация, являющаяся результатом фибромиалгии, системной эритематозной волчанки, склеродермы и анкилозирующего спондилита. Использованный в этом документе термин "врожденная(ые) мальформация(ии) хряща" включает состояния, такие как наследственный хондролиз, хондродисплазии и псевдохондродисплазии, в частности, но без ограничения, микротия, анотия, метафизарная хондродисплазия и сопутствующие тому нарушения. Использованный в этом документе термин "заболевание(я), связанное(ые) с гиперсекрецией IL6" включает состояния, такие как болезнь Кастлемана, множественная миелома, псориаз, саркома Капоши и/или мезангиальный пролиферативный гломерулонефрит. фармацевтически приемлемые соли. В том случае, когда в этом документе диапазоны относятся, например, но без ограничения, к С 1-С 8 алкилу, то упоминание диапазона следует рассматривать как представление каждого члена вышеупомянутого диапазона. Все изотопные варианты соединений, обеспеченные в этом документе, радиоактивные или нерадиоактивные, как подразумевается, попадают в пределы объема изобретения. Также следует понимать, что соединения, которые имеют одинаковую молекулярную формулу, но отличаются природой или последовательностью связывания их атомов или расположением их атомов в пространстве, называют термином "изомеры". Изомеры, которые отличаются расположением их атомов в пространстве, называют термином "стереоизомеры". Стереоизомеры, которые не являются зеркальными изображениями друг друга, называют термином"диастереомеры", и стереоизомеры, которые являются неналагающимися зеркальными изображениями друг друга, называют термином "энантиомеры". В том случае, когда соединение имеет асимметрический центр, например, он является связанным с четырьмя различными группами, возможна пара энантиомеров. Энантиомер может быть охарактеризован абсолютной конфигурацией его асимметрического центра и описан правилами R- и S-последовательности по системе Кана и Прелога или направлением, в котором молекула вращает плоскость поляризованного света, и обозначен как правовращающий или левовращающий (то есть как (+)- или (-)-изомеры соответственно). Хиральное соединение может существовать либо как индивидуальный энантиомер, либо как смесь энантиомеров. Смесь, содержащую равные пропорции энантиомеров, называют как "рацемическая смесь"."Таутомеры" относятся к соединениям, которые имеют взаимозаменяемые формы конкретной структуры соединения и которые варьируются по смещению атомов водорода и электронов. Так, две структуры могут находиться в равновесии посредством движения п-электронов и атома (обычно Н). Например, енолы и кетоны являются таутомерами, так как они быстро взаимопревращаются в результате обработки либо кислотой, либо основанием. Другой пример таутомеризма представляет собой аци- и нитроформы фенилнитрометана, которые подобным образом образуются в результате обработки кислотой или основанием. Таутомерные формы могут быть подходящими в достижении оптимальной химической реакционной способности и биологической активности соединения, представляющего интерес. Соединения этого изобретения могут обладать одним или более асимметрическими центрами; такие соединения, таким образом, могут быть получены как индивидуальные (R)- или (S)-стереоизомеры или как их смеси. Если не указано иное, описание или название конкретного соединения в описании изобретения и пункты формулы, как подразумевается, включают как индивидуальные энантиомеры, так и их смеси,рацемические или иные. Способы определения стереохимии и разделение стереоизомеров являются хорошо известными в данной области. Соединения Настоящее изобретение основано на открытии того, что JAK-киназы являются полезными в лечении заболеваний, включающих деградацию хряща, деградацию кости и/или сустава, например остеоартрита; и/или состояний, включающих воспаление или иммунные реакции, таких как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности), заболевания, включающие ухудшение ремоделирования хряща (например, заболевания, включающие анаболическую стимуляцию хондроцитов), врожденные мальформации хряща, заболевания, связанные с гиперсекрецией IL6, и отторжение трансплантата (например, отторжение пересаженного органа). Ингибиторы JAK-киназ также могут найти применение в лечении пролиферативных заболеваний. В частности, ингибиторы JAK-киназ находят применение в лечении раковых заболеваний, в особенности лейкемий и солидных опухолей (например, лейомиосаркомы матки, рака предстательной железы), особенно заболеваний, включающих деградацию хряща, деградацию кости и/или сустава и/или воспаление, путем введения соединения изобретения. Соединения настоящего изобретения могут быть ингибиторами одного или более членов семейства JAK-киназ; конкретно они могут ингибировать активность одной или более из киназ: JAK1, JAK2, JAK3 и/или TYK2. В соответствии с вышеизложенным в первом аспекте изобретения раскрывают применение 1,2,4 триазоло[1,5-а]пиридиновых соединений, имеющих формулу (I)L1 выбирают из одинарной связи, -O-, -С(О)-, -С[=N(R4a)]-, -N(R4a)-, -CON(R4a)-, -SO2N(R4a)-, -S(O)2-,4aR3b независимо выбирают из замещенного или незамещенного С 6-С 10 арила, замещенного или незамещенного С 3-С 7 циклоалкила, замещенного или незамещенного 4-7-членного гетероциклоалкила, содержащего 1-3 гетероатома, выбранных из N, О или S, замещенного или незамещенного 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, О или S; илиR3b независимо выбирают из O-R3c, NH-R3c, CO-R3c и CON(R4a)-R3c;R3c независимо выбирают из замещенного С 1-С 6 алкила, замещенного или незамещенного С 6 С 10 арила, замещенного или незамещенного С 3-С 7 циклоалкила, замещенного или незамещенного 4-7 членного гетероциклоалкила, содержащего 1-3 гетероатома, выбранных из N, О или S, замещенного или незамещенного 5-10-членного гетероарила, содержащего 1-3 гетероатома, выбранных из N, О или S; каждый R4a независимо выбирают из Н, С 1-С 6 алкила, замещенного С 1-С 6 алкила, С 3-С 7 циклоалкила; причем заместители в определениях R3b, R3c, R4a выбирают из группы, состоящей из галогена, циано, нитро, трифторметила, трифторметокси, азидо, -NR"'SO2R", -SO2NR"R"', -C(O)R", -C(O)OR",-OC(O)R", -NR"'C(O)R", -C(O)NR"R"', -NR"R"', -(CR"'R'")mOR"', где каждый R" независимо выбран из Н,С 1-С 8 алкила, -(СН 2)t(С 6-С 10 арила), -(СН 2)t(5-10-членного гетероарила, включающего 1-3 гетероатома,выбранных из N, О или S), -(СН 2)t(С 3-С 10 циклоалкила) и -(СН 2)t(4-10-членного гетероциклоалкила, включающего 1-3 гетероатома, выбранных из N, О или S), где t представляет целое число 0-4; любая алкильная группа может быть замещена галогеном или ОН; и любой арил, гетероарил, циклоакил или гетероциклоалкил могут быть замещены замещенным или незамещенным С 1-С 4 алкилом, галогеном, незамещенным C1-С 4 алкокси, незамещенным С 1-С 4 галогеналкилом, незамещенным С 1-С 4 гидроксиалкилом или незамещенным C1-С 4 галогеналкокси или ОН; каждый R"' независимо представляет Н или С 1-С 6 алкил;i) когда L1 представляет собой -O-, -N(R4a)-, -CH2-N(R4a)-, -CON(R4a)- или -SO2N(R4a)- и R3b является отличным от циклоалкила, арила или 5-10-членного гетероарила, тогда n1 равен 1, 2, 3 или 4;ii) когда L1 представляет собой связь, n1 равен 0 и R3b представляет собой -OR3c, тогда R3c является отличным от Me или CF3; или его фармацевтически приемлемая соль в лечении и/или предупреждении заболеваний, включающих деградацию хряща, деградацию кости и/или сустава; и/или состояний, включающих воспаление или иммунные реакции, таких как болезнь Крона,ревматоидный артрит, псориаз, аллергия дыхательных путей, ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния, заболевания, включающие ухудшение ремоделирования хряща, врожденные мальформации хряща, болезни Кастлемена, множественной миеломы, псориаза, саркомы Капоши и/или месангиального пролиферативного гломерунефрита и отторжение трансплантата; или пролиферативных заболеваний. В предпочтительном варианте осуществления раскрывают применение соединения в соответствии с вышеупомянутой формулой I, в которойL1 выбирают из одинарной связи, -O-, -С(О)-, -С[=N(R4a)]-, -N(R4a)-, -CON(R4a)-, -SO2N(R4a)-,-S(O)2-, -N(R4a)CO- или -N(R4a)SO2-,каждый R1 независимо выбирают из незамещенного C1-С 6 алкила, незамещенного ацила, незамещенной ациламиногруппы, незамещенной С 1-С 6 алкоксигруппы, незамещенной амидогруппы, незамещенной аминогруппы, незамещенного аминосульфонила, сульфоновой кислоты, сложного эфира сульфоновой кислоты, карбоксигруппы, цианогруппы, незамещенного С 3-С 7 циклоалкила, незамещенного 47-членного гетероциклоалкила, галогена и гидроксила; или его фармацевтически приемлемые соли. В дополнительном аспекте изобретения R4a представляет собой Н, замещенный или незамещенный С 1-С 4 алкил. В одном варианте осуществления в отношении соединений формулы I R4a представляет собой-(CH2)n2-R6a, где n2 имеет значение 0, 1, 2 и R6a представляет собой Н, CN, NMe2 или тетрагидрофуранил. В еще одном варианте осуществления в отношении соединений формулы I R4a представляет собой-СН(СН 3)(CH2)n2-R6a, где n2 имеет значение 0 или 1 и R6a представляет собой Н или ОМе. В еще одном варианте осуществления в отношении соединений формулы I R3b представляет собойOPh и O-(4-F-Ph). В одном варианте осуществления соединение соответствует формуле I и -Ph-L1-(CH2)n1-R3b представляет собой где n2 равно n1; и R3b и n1 являются такими же, как описаны для формулы I; и Су 3 представляет собой замещенную или незамещенную азотсодержащую 4-7-членную гетероциклоалкильную группу. В другом варианте осуществления группа -Ph-L1-(CH2)n1-R3b является такой же, как описана в предыдущих абзацах, и R3b представляет собой незамещенный пиридил. В еше одном варианте осуществления группа -Ph-L1-(CH2)n1-R3b является такой же, как описана в предыдущих абзацах, и R3b представляет собой пиридил, замещенный одной или более группами, выбранными из галогена, цианогруппы, нитрогруппы, трифторметила, трифторметоксигруппы, азидогруппы, -NR"'SO2R", -SO2NR"R"', C(O)R", -C(O)OR", -OC(O)R", -NR'"C(O)R", -C(O)NR"R'", -NR"R'",-(CR"'R'")mOR"', где каждый R" независимо выбирают из Н, С 1-С 8 алкила, -(СН 2)t(С 6-С 10 арила)-, -(СН 2)t(510-членного гетероарила), -(СН 2)t(С 3-С 10 циклоалкила) и -(СН 2)t(4-10-членного гетероциклоалкила), где t представляет собой целое число от 0 до 4. В еще одном варианте осуществления группа -Ph-L1-(CH2)n1-R3b является такой же, как описана в предыдущих абзацах, и R3b представляет собой пиридил, замещенный галогеном, цианогруппой, метилом или трифторметилом. В еше одном варианте осуществления группа -Ph-L1-(CH2)n1-R3b является такой же, как описана в предыдущих абзацах, и n1 или n2 имеет значение 1. В еше одном варианте осуществления группа -Ph-L1-(CH2)n1-R3b является такой же, как описана в предыдущих абзацах, и n1 или n2 имеет значение 2. В конкретном варианте осуществления раскрывают применение соединения в соответствии с формулой I, и R3b выбирают из где каждый R5a независимо представляет собой С 1-С 4 алкил, галоген, CF3 или фенил; R5b представляет собой Н, арил, 5-10-членный гетероарил, гетероарил, С 3-С 6 циклоалкил или 4-7-членный гетероциклоалкил; и m5 имеет значение 0, 1 или 2. В другом конкретном варианте осуществления соединения применение соединения, соответствующее формуле I, и Су 3 выбирают из где каждый R5a независимо представляет собой С 1-С 4 алкил, галоген, CF3 или фенил; R5b представляет собой Н, арил, 5-10-членный гетероарил, гетероарил, С 3-С 6 циклоалкил или 4-7-членный гетероциклоалкил; R5c представляет собой Н или С 1-С 4 алкил; m5 имеет значение 0, 1 или 2; n5 имеет значение 0, 1 или 2. В более особом варианте осуществления раскрывают применение соединения в соответствии с любой формулой из формул Va, Vb, Vc или Vd В более особом варианте осуществления раскрывают применение соединения в соответствии с любой формулой из формул VIa, VIc или VId В более особом варианте осуществления раскрывают применение соединения в соответствии с любой формулой из формул VIIa, VIIb, VIIc, VIId, VIIe или VIIf В другом более особом варианте осуществления раскрывают применение соединения в соответствии с любой формулой из формул VIIIa, VIIIb, VIIIc, VIIId, VIIIe, VIIIf, VIIIg, VIIIh, VIIIi, VIIIj, VIIIk или В другом более особом варианте осуществления раскрывают применение соединения в соответствии с любой формулой из формул IXa, IXb, IXc, IXd, IXe, IXf, IXg, IXh, IXi, IXj, IXk или IXl В некоторых аспектах настоящее изобретение обеспечивает соединения формулы X или XI в которой R3b представляет собой замещенный или незамещенный 4-7-членный гетероциклоалкил; при условии, что в том случае, когда соединение соответствует формуле X, гетероциклоалкильное кольцо является отличным от незамещенного морфолин-1-ила. В одном варианте осуществления соединение соответствует формуле X. В другом варианте осуществления соединение соответствует формуле XI. В одном конкретном варианте осуществления в отношении соединений в соответствии с формулойX R3b представляет собой незамещенный азетидинил, пирролидинил, пиперидинил, пиперазинил, азепинил, пирролидонил, пиранил, дигидротиофенил, дигидропиранил, дигидрофуранил, дигидротиазолил,тетрагидрофуранил, тетрагидротиофенил, диоксанил, тетрагидропиранил, имидазолинил, имидазолидинонил, оксазолинил, тиазолинил, 2-пиразолинил, пиразолидинил, тиоморфолинил-S-оксид и тиоморфолинил-S,S-диоксид пиперидонил или пиперазонил. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой незамещенный азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, тиоморфолин-1-ил-S,Sдиоксид, пиперазин-1-ил или азепин-1-ил.- 17018587 В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой незамещенный азетидин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой незамещенный пирролидин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой незамещенный пиперидин-1-ил или пиперазин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой незамещенный тиоморфолин-1-ил-S,S-диоксид. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой незамещенный азепин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, морфолин-1-ил, пиперазин-1-ил или азепин 1-ил; замещенный одной или более группами, выбранными из С 1-С 4 алкила, С 1-С 4 галогеналкила, цианогруппы, аминогруппы, диалкиламиногруппы, диалкиламинометила, гидроксигруппы, галогена, ацила,ациламиногруппы, С 1-С 4 гидроксиалкила, С 1-С 4 алкоксигруппы, карбоксамидогруппы и С 1-С 4 диалкилкарбоксамидогруппы. В одном конкретном варианте осуществления в отношении соединений формулы X R3b представляет собой азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, морфолин-1-ил, пиперазин-1-ил или азепин 1-ил; замещенный Me, CF3, F, Cl, дифтором, диметилом, гидроксигруппой, цианогруппой, диметиламиногруппой, диметиламинометилом, гидроксиметилом, карбоксамидогруппой, N,N-диметилкарбоксамидогруппой, метоксигруппой, этоксигруппой или 2,2,2-трифторэтилом. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный азетидинил, пирролидинил, пиперидинил, пиперазинил, азепинил, пирролидонил, пиранил, дигидротиофенил, дигидропиранил, дигидрофуранил, дигидротиазолил, тетрагидрофуранил, тетрагидротиофенил, диоксанил, тетрагидропиранил, имидазолинил, имидазолидинонил, оксазолинил, тиазолинил, 2-пиразолинил, пиразолидинил, морфолинил, тиоморфолинил-S-оксид и тиоморфолинил-S,S-диоксид пиперидонил или пиперазонил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, морфолинил, тиоморфолин 1-ил-S,S-диоксид, пиперазин-1-ил или азепин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный азетидин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный пирролидин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный пиперидин-1-ил или пиперазин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный тиоморфолин-1-ил-S,S-диоксид. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный морфолин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой незамещенный азепин-1-ил. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, морфолин-1-ил, пиперазин-1-ил или азепин-1-ил; замещенный одной или более группами, выбранными из С 1-С 4 алкила, С 1-С 4 галогеналкила,цианогруппы, аминогруппы, диалкиламиногруппы, диалкиламинометила, гидроксигруппы, галогена,ацила, ациламиногруппы, С 1-С 4 гидроксиалкила, С 1-С 4 алкоксигруппы, карбоксамидогруппы и С 1 С 4 диалкилкарбоксамидогруппы. В одном конкретном варианте осуществления в отношении соединений формулы XI R3b представляет собой азетидин-1-ил, пирролидин-1-ил, пиперидин-1-ил, морфолин-1-ил, пиперазин-1-ил или азепин-1-ил; замещенный Me, CF3, F, Cl, дифтором, диметилом, гидроксигруппой, цианогруппой, диметиламиногруппой, диметиламинометилом, гидроксиметилом, карбоксамидогруппой, N,N-диметилкарбоксамидогруппой, метоксигруппой, этоксигруппой или 2,2,2-трифторэтилом. В одном варианте осуществления в отношении соединений формулы I выбирают соединение из соединений, приведенных в качестве примера в табл. 1. В одном варианте осуществления соединение изобретения не является изотопным вариантом. В одном аспекте соединение изобретения в соответствии с любым вариантом осуществления из вариантов осуществления, описанных в этом документе, присутствует в форме свободного основания. В одном аспекте соединение изобретения в соответствии с любым вариантом осуществления из вариантов осуществления, описанных в этом документе, представляет собой фармацевтически приемлемую соль. Хотя точно описанные группы для каждого варианта осуществления были перечислены выше в об- 18018587 щем порядке по отдельности, соединение изобретения включает группу, в которой несколько или каждый вариант осуществления в соответствии с вышеупомянутой формулой, а также в соответствии с другими представленными в этом документе формулами, выбирают из одного или более конкретных членов или групп, обозначенных, соответственно, для каждой переменной. Таким образом, подразумевается, что изобретение включает все комбинации таких вариантов осуществления в пределах его объема. Другие производные соединений изобретения имеют активность как в их кислотных формах, так и в формах производных кислот, но форма, чувствительная к кислоте, часто дает преимущества растворимости, совместимости с тканью или отсроченного высвобождения в организме млекопитающего (см.,Bundgard, H., Design of Prodrugs, pp. 7-9, 21-24, Elseivier, Amsterdam 1985). Фармацевтические композиции При применении лекарственных препаратов соединения изобретения обычно вводят в форме фармацевтической композиции. Такие композиции могут быть приготовлены способом, хорошо известным в фармацевтической области, и содержат по меньшей мере одно активное соединение. Как правило, соединения этого изобретения вводят в фармацевтичски эффективном количестве. Количество соединения,собственно вводимое, обычно будет определяться терапевтом в свете релевантных обстоятельств, включающих состояние, которое подлежит лечению, выбранный путь введения, вводимое соединение как таковое, возраст, вес и реакция конкретного пациента, тяжесть симптомов у конкретного пациента и тому подобное. Фармацевтические композиции, включающие соединения изобретения, могут быть введены разнообразными путями, включающими пероральный, ректальный, трансдермальный, подкожный, интраартикулярный, внутривенный, внутримышечный и интраназальный пути. В зависимости от предполагаемого пути доставки соединения этого изобретения предпочтительно составляют в смеси либо в форме инъекционных или пероральных композиций, либо в форме целебных мазей, лосьонов или пластырей, все из которых для трансдермального введения. Композиции для перорального введения могут иметь форму нерасфасованных жидких растворов,или суспензий, или нерасфасованных порошков. Чаще, однако, композиции представлены в стандартных(дозированных) лекарственных формах для облегчения точного дозирования лекарства. Термин "стандартные (дозированные) лекарственные формы" относится к физически дискретным единицам, подходящим в качестве единичных дозировок для человеческих субъектов и других млекопитающих, где каждая единица содержит заданное количество активного вещества, вычисленное для получения желательного терапевтического эффекта, в сочетании с подходящим(ей) фармацевтическим(ой) эксципиентом,средой для лекарства или носителем. Обычные стандартные (дозированные) лекарственные формы включают предварительно заполненные, заранее измеренные ампулы или шприцы с жидкими композициями или пилюли, таблетки, капсулы или тому подобное в случае твердых композиций. В таких композициях соединение фурансульфокислоты представляет собой обычно второстепенный компонент (от приблизительно 0,1 до приблизительно 50 мас.% или предпочтительно от приблизительно 1 до приблизительно 40 мас.%), где остальная часть представляет собой раличные среды для лекарства или носители и технологические добавки, полезные для формования желательной дозированной формы. Жидкие формы, подходящие для перорального введения, могут включать подходящую водную или неводную среду для лекарства с буферными растворами, с добавками, способствующими суспендированию и распылению лекарства, с окрашивающими веществами, ароматизирующими добавками и тому подобным. Твердые формы могут включать, например, любые из следующих ингредиентов, или соединений аналогичной природы: связующее вещество, такое как микрокристаллическая целлюлоза, трагакантовая камедь или желатин; эксципиент, такой как крахмал или лактоза, вещество для улучшения распадаемости таблеток, такое как альгиновая кислота, Primogel или кукурузный крахмал; скользящее вещество, такое как стеарат магния; регулятор сыпучести (глидант), такой как коллоидный диоксид кремния; подслащивающее вещество, такое как сахароза или сахарин; или ароматизирующее вещество, такое как мята перечная (мятное масло), метилсалицилат или экстракт из апельсиновой корки. Инъекционные композиции обычно основаны на инъекционном стерильном солевом растворе, или забуференном фосфатом физиологическом растворе, или на других инъекционных носителях, известных в данной области. Исходя из вышесказанного, активное соединение в таких композициях обычно представляет собой второстепенный компонент, часто составляющий от приблизительно 0,05 до 10 мас.%,где остальная часть представляет собой инъекционный носитель или тому подобное. Трансдермальные композиции обычно составляют в форме местнодействующей(его) мази или крема, содержащей(его) активный(е) ингредиент(ы), как правило, в количестве, находящемся в диапазоне от приблизительно 0,01 до приблизительно 20 мас.%, предпочтительно от приблизительно 0,1 до приблизительно 20 мас.%, предпочтительно от приблизительно 0,1 до приблизительно 10 мас.% и более предпочтительно от приблизительно 0,5 до приблизительно 15 мас.%. При составлении смеси в форме мази активные ингредиенты обычно будут скомбинированы либо с парафинистой, либо с водорастворимой или смешивающейся с водой основой мази. Альтернативно, активные ингредиенты могут быть составлены в крем, например, с основой крема типа "масло в воде". Такие трансдермальные составы хорошо известны в данной области и, как правило, включают дополнительные ингредиенты для улучшения проникнове- 19018587 ния в кожу, стабильности активных ингредиентов или состава. Соединения этого изобретения также могут быть введены с помощью трансдермального приспособления. Соответственно, трансдермальное введение может быть выполнено с использованием пластыря либо резервуарного или пористомембранного типа, либо из набора твердых матриц. Вышеописанные компоненты для перорально вводимых, инъекционных или местно вводимых композиций являются лишь репрезентативными. Другие вещества, а также технологические методы и тому подобное изложены в части 8 книги Remington's Pharmaceutical Sciences, 17th edition, 1985, Mack Publishing Company, Easton, Pennsylvania, которая включена в этот документ путем ссылки. Соединения этого изобретения также могут быть введены в формах с замедленным высвобождением или из систем доставки лекарственного средства с замедленным высвобождением. Описание репрезентативных материалов с замедленным высвобождением могут быть обнаружены в книге Remington'sPharmaceutical Sciences. Следующие примеры составов иллюстрируют репрезентативные фармацевтические композиции,которые могут быть получены в соответствии с этим изобретением. Настоящее изобретение, однако, не ограничено следующими фармацевтическими композициями. Состав 1. Таблетки. Соединение изобретения может быть смешано в виде сухого порошка с сухим желатиновым связующим в приблизительном массовом соотношении 1:2. Незначительное количество стеарата магния добавляют в качестве скользящего вещества. Смесь формуют :в таблетки массой 240-270 мг (80-90 мг активного амидного соединения на таблетку) в таблеточном прессе. Состав 2. Капсулы. Соединение изобретения может быть смешано в виде сухого порошка с крахмальным разбавителем в приблизительном массовом соотношении 1:1. Смесь помещают в капсулы массой 250 мг (125 мг активного амидного соединения на капсулу). Состав 3. Жидкость. Соединение изобретения (125 мг) может быть смешано с сахарозой (1,75 г) и ксантановой камедью(4 мг), и получающаяся в результате смесь может быть размешана, пропущена через сетчатый фильтр N 10 меш, и затем смешана с заранее приготовленным раствором микрокристаллической целлюлозы и карбоксиметилцеллюлозы натрия (11:89, 50 мг) в воде. Бензоат натрия (10 мг), ароматизирующее вещество,и окрашивающее вещество разбавляют водой и добавляют при перемешивании. Затем при перемешивании может быть добавлено достаточное количество воды. Достаточное количество воды затем добавляют с получением общего объема 5 мл. Состав 4. Таблетки. Соединение изобретения может быть смешано в виде сухого порошка с сухим желатиновым связующим в приблизительном массовом соотношении 1:2. Незначительное количество стеарата магния добавляют в качестве скользящего вещества. Смесь формуют в таблетки массой 450-900 мг (150-300 мг активного амидного соединения на таблетку) в таблеточном прессе. Состав 5. Раствор для инъекций. Соединение изобретения может быть растворено или суспендировано в инъекционной водной среде на основе забуференного стерильного физиологического раствора в концентрации приблизительно 5 мг/мл. Состав 6. Местнодействующий. Стеариловый спирт (250 г) и белый вазелин (250 г) могут быть расплавлены при приблизительно 75 С и затем может быть добавлена смесь соединения изобретения (50 г), метилпарабена (0,25 г), пропилпарабена (0,15 г), лаурилсульфата натрия (10 г) и пропиленгликоля (120 г), растворенная в воде (приблизительно 370 г), получающуюся в результате смесь перемешивают до тех пор, пока она не застынет. Способы лечения Соединения настоящего изобретения используют в качестве терапевтических средств для лечения состояний у млекопитающих, которые причинно связаны или обусловлены аберрантной активностьюJAK-киназ; в особенности состояний, связанных с аберрантной активностью одной или более киназ изJAK1-, JAK2-, JAK3- и/или TYK2-киназ. В связи с вышеизложенным соединение изобретения и фармацевтические композиции, включающие соединения этого изобретения, находят применение в качестве терапевтических средств для предупреждения и/или лечения заболеваний, включающих деградацию хряща, деградацию кости и/или сустава, например остеоартрита; и/или состояний, включающих воспаление или иммунные реакции, таких как болезнь Крона, ревматоидный артрит, псориаз, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например, хронической сердечной недостаточности), заболевания, включающие ухудшение ремоделирования хряща (например, заболевания, включающие анаболическую стимуляцию хондроцитов), врожденные мальформации хряща, заболевания, связанные с гиперсекрецией также могут найти применение в лечении пролиферативных заболеваний. В частности, ингибиторы JAKкиназ находят применение в лечении раковых заболеваний, в особенности, лейкемий и солидных опухолей (например, лейомиосаркомы матки, рака предстательной железы). В особенности состояния выбирают из воспалительных состояний, состояний, связанных с деградацией хряща и/или сустава у млекопитающих, включая людей. В другом варианте осуществления соединения и фармацевтические композиции, включающие их, находят применение в качестве терапевтических средств для предупреждения и/или лечения пролиферативных нарушений у млекопитающих, включая людей. В особом варианте осуществления соединение изобретения и их фармацевтические композиции находят применение в качестве терапевтических средств для предупреждения и/или лечения ракового заболевания у млекопитающих,включая людей. В другом аспекте настоящее изобретение обеспечивает соединение изобретения для применения в лечении, предупреждении или для профилактики состояния, включающего аутоиммунную реакцию или аутоиммунное заболевание. В конкретном варианте осуществления аутоиммунное заболеваниие выбирают из хронического обструктивного заболевания легких, астмы, системной эриматозной волчанки,сахарного диабета типа I и воспалительного заболевания кишечника. В другом аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении, предупреждении или для профилактики заболеваний, включающих ухудшение ремоделирования хряща (например, состояние, сопутствующее анаболической стимуляции хондроцитов, или заболевания,вовлекающие в патологический процесс анаболическую стимуляцию хондроцитов), например остеоартрита, псориатического артрита, ювенильного ревматоидного артрита, подагрического артрита, септического или инфекционного артрита, реактивного артрита, симпатической рефлекторной дистрофии, альгодистрофии, синдрома Tietze или костального хондрита, фибромиалгии, остеохондрита, нейрогенного или невропатического артрита, артропатии, эндемических форм артрита, например деформирующего остеоартрита эндемического, болезни Mseleni и болезни Handigodu; дегенерации, являющейся результатом фибромиалгии, системной эритематозной волчанки, склеродермы и анкилозирующего спондилита. В другом аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении, предупреждении или для профилактики врожденных мальформаций хряща, включающих наследственный хондролиз, хондродисплазии и псевдохондродисплазии, в частности, но без ограничения, микротию, анотию, метафизарную хондродисплазию и сопутствующие тому нарушения. В другом аспекте это изобретение обеспечивает применение соединения изобретения в лечении,предупреждении или для профилактики состояния, включающего воспаление. В другом аспекте настоящее изобретение обеспечивает соединение изобретения для применения в лечении, предупреждении или для профилактики заболеваний или нарушений, которые опосредованы воспалением или приводят к воспалению, таких как, например, ревматоидный артрит и остеоартрит, аллергия дыхательных путей (например, астма, ринит), ювенильный идиопатический артрит, колит, воспалительные заболевания кишечника, обусловленные действием эндотоксина болезненные состояния (например, осложнения после шунтирования или хронические обусловленные действием эндотоксина состояния, способствующие возникновению, например хронической сердечной недостаточности) и сопутствующие тому заболевания, вовлекающие в патологический процесс хрящ, например заболевание суставов. В конкретном варианте осуществления состояние, включающее воспаление, выбирают из ревматоидного артрита, остеоартрита,аллергии дыхательных путей (например, астма) и воспалительных заболеваний кишечника. В другом аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении, предупреждении или для профилактики пролиферативного заболевания, в частности ракового заболевания (например, солидных опухолей, таких как лейомиосаркома матки или рак предстательной железы), лейкемий (например, AML или ALL), множественная миелома и/или псориаз. В другом аспекте настоящее изобретение обеспечивает соединение изобретения для применения в лечении, предупреждении или для профилактики ракового заболевания (например, солидных опухолей, таких как лейомиосаркома матки или рак предстательной железы) и/или лейкемий. В другом аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении, предупреждении или для профилактики заболеваний, связанных с гиперсекрецией IL6, в частности болезни Кастлемана или мезангиального пролиферативного гломерулонефрита. В другом аспекте настоящее изобретение обеспечивает применение соединения изобретения в лечении, предупреждении или для профилактики отторжения трансплантата. В конкретном варианте осуществления изобретение обеспечивает способы лечения отторжения пересаженных органов. В качестве дополнительного аспекта изобретения обеспечивают применение соединения изобретения в качестве фармацевтического препарата, главным образом, в лечении или предупреждении вышеупомянутых состояний и заболеваний. Также обеспеченным в этом документе является применение соединений настоящего изобретения в изготовлении лекарственного препарата для лечения или предупреждения одного из вышеупомянутых состояний и заболеваний. Уровни дозы инъекции колеблются в диапазоне от приблизительно 0,1 до по меньшей мере 10 мг/кг/ч, все в течение периода времени от приблизительно 1 до приблизительно 120 ч и в особенности в течение периода времени 24-96 ч. Предварительно заполняемый болюс в количестве от приблизительно 0,1 до приблизительно 10 мг/кг или более также может быть введен для достижения адекватных уровней равновесной (стабильной) концентрации. Максимальная общая доза, как ожидают, не превышает приблизительно 2 г/день для пациента-человека массой 40-80 кг. Для предупреждения и/или лечения длительных (хронических) состояний, таких как дегенеративные состояния, программа лечения растягивается на многие месяцы или годы, поэтому пероральное введение дозы является предпочтительным для удобства пациентов и для переносимости пациентами. При пероральном введении дозы одна-пять и особенно две-четыре и обычно три пероральные дозы в день представляют собой репрезентативные схемы. С использованием этих протоколов введения дозы каждая доза обеспечивает от приблизительно 0,01 до приблизительно 20 мг/кг соединения изобретения, где каждая из конкретных доз обеспечивает от приблизительно 0,1 до приблизительно 10 мг/кг и в особенности приблизительно 1-5 мг/кг. Дозы при трансдермальном введении, как правило, выбирают для обеспечения аналогичных или более низких уровней в крови, чем достигаются с использованием доз при инъекционном введении. При применении для предупреждения начала воспалительного состояния соединения этого изобретения будут вводиться пациенту с риском развития состояния, обычно по заключению или под присмотром лечащего врача, при уровнях дозировки, описанных выше. Пациенты с риском развития конкретного состояния, как правило, включают пациентов, которые имеют семейный анамнез этого состояния, или пациенты, которые были идентифицированы с помощью генетического тестирования или скрининга как особенно предрасположенные к развитию этого состояния. Соединения изобретения могут быть введены в качестве единственного активного вещества, или они могут быть введены в комбинации с другими веществами, включая другие соединения, которые проявляют аналогичную или сходную терапевтическую активность и которые, как определено, являются безопасными и эффективными для такого объединенного введения. В конкретном варианте осуществления совместное введение двух (или более) веществ предусматривает значительно более низкие дозы каждого вещества, которое должно быть применено, посредством чего снижаются видимые побочные эффекты. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения заболевания, включающего воспаление; конкретные вещества включают иммунорегуляторные средства, например азатиоприн, кортикостероиды (например,преднизолон или дексаметазон), циклофосфамид, циклоспорин А, такролимус, микофенолат-мофетил,муромонаб-CD3 (OKT3 (антигенный маркер популяции зрелых периферических Т-лимфоцитов у человека), например Orthocolone), ATG (антитимоцит-глобулин), аспирин, ацетаминофен, ибупрофен, напроксен и пироксикам, но не ограничиваются этим. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения артрита (например, ревматоидный артрит); конкретные вещества включают аналгетики, нестероидные противовоспалительные лекарственные средства(NSAIDS), стероиды, синтетические базисные препараты для лечения ревматоидного артрита (DMARDS,например, но без ограничения, метотрексат, лефлуномид, сульфазалазин, ауранофин, ауротиомалат натрия, пеницилламин, хлорокин, гидроксихлорокин, азатиоприн, и циклоспорин), и биологические базисные препараты для лечения ревматоидного артрита (DMARDS, например, но без ограничения, инфликсимаб, этанерцепт, адалимумаб, ритуксимаб и абатацепт), но не ограничиваются этим. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения пролиферативных нарушений; конкретные вещества включают метотрексат, леуковорин, адриамицин, пренизон, блеомицин, циклофосфамид, 5-фтороурацил,паклитаксел, доцетаксел, винкристин, винбластин, винорелбин, доксорубицин, таксифен, торемифен,мегестрол-ацетат, анастрозол, гозерелин, моноклональное анти-HER2-антитело (например, Герцептин),капецитабин, ралоксифен-гидрохлорид, ингибиторы рецепторов эпидермального фактора роста (EGFR,например Iressa, Tarceva, Erbitux), ингибиторы факторов роста эндотелия сосудов (VEGF, напримерAvastin), ингибиторы протеасомы (например, Velcade), Glivec или ингибиторы hsp90 (например,17-AAG), но не ограничиваются этим. Кроме того, соединение изобретения может быть введено в комбинации с другими методами лечения, включающими лучевую терапию или хирургию, но не ограниченными этим. В конкретном варианте осуществления пролиферативное нарушение выбирают из ракового заболевания, миелопролиферативного заболевания или лейкемии. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предепреждения аутоиммунных заболеваний; конкретные вещества включают глюкокортикоиды, цитостатические вещества (например, пуриновые аналоги), алкилирующие агенты (например, азотистые иприты (циклофосфамид), нитрозомочевины, соединения платины и другие), антиметаболиты (например, метотрексат. Азатиоприн и меркаптопурин), цитотоксические антибиотики (например, дактиномицин, антрациклины, митомицин С, блеомицин и митрамицин), антитела (например, моноклональные анти-CD20-, анти-CD25- или анти-CD3- (OTK3) антитела, Atgam и Thymoglobuline), циклоспорин, такролимус, рапамицин (сиролимус), интерфероны (например, IFN-), TNFсвязывающие белки (например, инфликсимаб (Remicade), этанерцепт (Enbrel), или адалимумаб (Humira,- 22018587 микофенолат, Fingolimod, Myriocin, но не ограничиваются этим. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения отторжения трансплантата; конкретные вещества включают ингибиторы кальциневрина (например, циклоспорин или такролимус (FK506, ингибиторыmTOR (например, сиролимус, эверолимус), антипролиферативные препараты (например, азатиоприн,микофенольная кислота), кортикостероиды (например, преднизолон, гидрокортизон), антитела (например, моноклональные анти-IL-2R-рецептор-антитела, базиликсимаб, даклизумаб), поликлональные анти-Т-клеточные антитела (например, антитимоцит-глобулин (ATG), антилимфоцит-глобулин (ALG, но не ограничиваются этим. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения астмы, и/или ринита, и/или COPD (хроническое обструктивное заболевание легких); конкретные вещества включают антагонисты 2-адреноцепторов (например, салбутамол, левалбутерол, тербуталин и битолтерол), эпинефрин (в виде ингаляций или в таблетках), антихолинергические вещества (например, ипратропий-бромид), глюкокортикоиды (пероральные или в виде ингаляций), длительно действующие 2-агонисты (например, салметерол, формотерол,бамбутерол и перорально вводимый албутерол замедленного высвобождения), комбинации ингалируемых стероидов и длительно действующих бронхолитических веществ (например, флутиказон/салметерол, будезонид/формотерол), антагонисты рецепторов лейкотриена и ингибиторы синтеза(например, монтелукаст, зафирлукаст и зилеутон), ингибиторы высвобождения медиаторов (например,кромогликат и кетотифен), биологические регуляторы реакции IgE (например, омализумаб), антигистаминные препараты (например, цетеризин, циннаризин, фексофенадин), вазоконстрикторные препараты(например, оксиметазолин, ксилометазолин, нафазолин и трамазолин), но не ограничиваются этим. Кроме того, соединение изобретения может быть введено в комбинации с методами неотложной терапии астмы и/или хронического обструктивного заболевания легких, где такие методы терапии включают введение кислорода или гелиево-кислородной дыхательной среды, введение распыляемого салбутамола или тербуталина (необязательно в комбинации с антихолинергическим веществом (например,ипратропий, системных стероидов (пероральные или внутривенные, например преднизон, преднизолон,метилпреднизолон, дексаметазон или гидрокортизон), внутривенного салбутамола, неспецифических агонистов, инъекционных или ингаляционных препаратов (например, эпинефрин, изоэтарин, изопротеренол, метапротеренол), антихолинергических препаратов (внутривенные или распыляемые, например,гликопирролат, атропин, ипратропий), метилксантинов (теофиллин, аминофиллин, бамифиллин), ингаляционных анестезирующих препаратов, которые имеют бронхолитический эффект (например, изофлуран, галотан, энфлуран), кетамина, внутривенного сульфата магния. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения IBD (воспалительное заболевание кишечника); конкретные вещества включают глюкокортикоиды (например, преднизон, буденозид), синтетические модифицирующие заболевания, иммуномодулирующие препараты (например, метотрексат, лефлуномид,сульфасалазин, мезалазин, азатиоприн, 6-меркаптопурин и циклоспорин) и биологические модифицирующие заболевания, иммуномодулирующие препараты (инфликсимаб, адалимумаб, ритуксимаб и абатацепт), но не ограничиваются этим. В одном варианте осуществления, соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения SLE (системная эриматозная волчанка); конкретные вещества включают базисные препараты для лечения ревматоидного артрита (DMARDs), такие как противомалярийные препараты (например, плакенил, гидроксихлорокин), иммунодепрессанты (например,метотрексат и азатиоприн), циклофосфамид и микофенольная кислота; иммунодепрессивные лекарственные средства и анальгетики, такие как нестероидные противовоспалительные лекарственные средства, опиаты (например, декстропропоксифен и кокодамол), опиоиды (например, гидрокодон, оксикодон,МС-контин или метадон) и фентаниловый трансдермальный пластырь (Дюрогезик), но не ограничиваются этим. В одном варианте осуществления соединение изобретения совместно вводят с другим терапевтическим средством для лечения и/или предупреждения псориаза; конкретные вещества включают препараты для местного лечения, такие как омывающие жидкости, увлажняющие средства, лекарственные кремы и мази, содержащие деготь, дитранол (антралин), кортикостероиды, например дезоксиметазон (Topicort),флуоцинонид, аналоги витамина D3 (например, кальципотриол), ретиноиды на основе масла арганы (этретинат, ацитретин, тазаротен), препараты для системного лечения, такие как метотрексат, циклоспорин,ретиноиды, тиогуанин, гидроксимочевина, сульфасалазин, микофенолат мофетил, азатиоприн, такролимус, сложные эфиры фумаровой кислоты, или биологические препараты, такие как Amevive, Enbrel, Humira, Remicade, Raptiva, и устекинумаб (блокаторы IL-12 и IL-23), но не ограничиваются этим. Кроме того, соединение изобретения может быть введено в комбинации с другими методами терапии, включающими фототерапию или фотохимиотерапию (например, сочетание фототерапии и ПУФА (псорален + УФ-излучение)-терапии), но не ограниченными этим. С помощью термина "совместное введение" включают любое средство доставки двух или более терапевтических средств пациенту в рамках одной и той же программы лечения, что будет очевидно для специалиста в данной области. Хотя два или более средства могут быть введены одновременно в одном составе, это не является решающим фактором. Вещества могут быть введены различными составами в разное время. Общие методы синтеза Соединения изобретения могут быть получены из легкодоступных исходных веществ с использованием следующих общих способов и методик. Будет ясно, что в том случае, когда даны обычные или предпочтительные условия процессов (то есть температуры реакций, продолжительности, мольные соотношения реагентов, растворители, параметры давления и так далее), другие условия процесса также могут быть использованы, если не указано иное. Оптимальные реакционные условия могут варьироваться в зависимости от конкретных используемых реагентов или растворителей, но такие условия могут быть определены специалистом в данной области с помощью общепринятых алгоритмов оптимизации. Кроме того, что будет ясно специалистам в данной области, для предотвращения протекания нежелательных реакций на некоторых функциональных группах могут быть необходимы обычно применяемые защитные группы. Подбор подходящей защитной группы для конкретной функциональной группы,а также подходящих условий для введения защитных групп и снятия защитных групп хорошо известен в данной области. Например, многочисленные защитные группы и их введение и удаление описаны в работе T.W. Greene and P.M. Wuts, Protecting Groups in Organic Synthesis, Second Edition, Wiley, New York,1991 и в ссылках, приведенных в этой работе. Подробно представлены следующие способы, касающиеся получения репрезентативных бициклогетероарилов, которые были приведены в этом документе выше. Соединения изобретения могут быть получены из известных или коммерчески доступных исходных веществ и реагентов специалистом в области органического синтеза. Все реагенты являются технического сорта и используются в состоянии поставки без дополнительной очистки, если не указано иное. Коммерчески доступные безводные растворители используют в реакциях, проводимых в инертной атмосфере. Растворители химически чистого сорта используют во всех случаях, если не указано иное. Колоночную хроматографию осуществляют на силикагеле 60 (35-70 мкм). Тонкослойную хроматографию выполняют с использованием пластинок, предварительно покрытых слоем силикагеля F-254 (толщина 0,25 мм). 1 Н ЯМР-спекты записывают на ЯМР-спектрометре Bruker DPX 400 (400 МГц) . Химические сдвигидля 1 Н ЯМР-спектров сообщают в миллионных долях (ppm) относительно пика тетраметилсилана ( 0,00) или соответственного остаточного растворителя, то естьCHCl3 ( 7,27), в качестве внутреннего эталона. Мультиплетности сигналов даны в виде синглета (с), дуплета (д), триплета (т), квадруплета (кв.), мультиплета (м) и широкого сигнала (ш.). Константы спинспинового взаимодействия (J) даны в Гц. Электроспрей масс-спектры получают на спектрометре Micromass с платформой для проведения анализа методами жидкостной хроматографии и масс-спектрометрии(LC/MS). Колонка, используемая для всего анализа методом LCMS: Waters: Acquity с фазой С 18 с частицами UPLC BEN размером 1,7 мкм, 2,1 мм (внутренний диаметр)50 мм (длина) (каталожный номер 186002350). Препаративный высокоэффективный жидкостной хроматограф (HPLC): Waters: XBridge Prep с фазой С 18 с частицами размером 5 мкм ODB 19 мм (внутренний диаметр)100 мм (длина) (каталожный номер 186002978). Все способы выполняют с использованием градиентов MeCN/Н 2 О. Н 2 О содержит или 0,1% TFA или 0,1% NH3. Перечень сокращений, используемых в экспериментальном разделе. Синтетическое получение соединений изобретения Соединение изобретения может быть получено в соответствии со следующей схемой. Получение основного промежуточного соединения. Схема 1 К раствору 2-амино-6-бромпиридина (1) (253,8 г, 1,467 моль) в дихлорметане (DCM) (2,5 л), охлажденному до 5 С, добавляют этоксикарбонилизотиоцианат (173,0 мл, 1,467 моль) по каплям в течение 15 мин. Реакционной смеси затем дают нагреться до комнатной температуры (20 С) и перемешивают в течение 16 ч. Выпаривание в вакууме дает твердое вещество, которое собирают фильтрацией, тщательно промывают бензином (3600 мл) и сушат на воздухе с предоставлением соединения (2). Тиомочевину используют как есть для следующей стадии без какой-либо очистки. 1 Н (400 МГц, CDCl3)12,03 (1 Н, ш.с, NH), 8,81 (1 Н, д, J=7,8 Гц, Н-3), 8,15 (1 Н, ш.с, NH), 7,60 (1 Н,т, J=8,0 Гц, Н-4), 7,32 (1 Н, дд, J=7,7 и 0,6 Гц, Н-5), 4,31 (2 Н, кв., J=7,1 Гц, СН 2), 1,35 (3 Н, т, J=,1 Гц, СН 3). 1.1.2. 5-Бром-[1,2,4]триазоло[1,5-а]пиридин-2-иламин (3) К суспензии гидроксиламингидрохлорида (101,8 г, 1,465 моль) в смеси EtOH/MeOH (1:1, 900 мл) добавляют N,N-диизопропилэтиламин (145,3 мл, 0,879 моль) и смесь перемешивают при комнатной температуре (20 С) в течение 1 ч. Затем добавляют 1-(6-бромпиридин-2-ил)-3-карбоэтокситиомочевину (2)(89,0 г, 0,293 моль) и смесь медленно нагревают для осуществления кипячения с обратным холодильником (следует отметить, что необходим скруббер-отбеливатель для поглощения выделяемого H2S). После 3 ч кипячения с обратным холодильником смеси дают остыть и фильтруют, собирая осажденное твердое вещество. Дополнительный продукт собирают выпариванием в вакууме фильтрата, добавлением Н 2 О(250 мл) и фильтрацией. Объединенное твердое вещество промывают последовательно посредством H2O(250 мл), смеси EtOH/MeOH (1:1, 250 мл) и Et2O (250 мл), затем сушат в вакууме с предоставлением триазолопиридинового производного (3) в виде твердого вещества. Соединение используют так как есть для следующей стадии без какой-либо очистки. 1 Н (400 МГц, DMSC-d6)7,43-7,34 (2 Н, 2 ароматич.-Н), 7,24 (1 Н, дд, J=6,8 и 1,8 Гц, ароматич.-Н),6,30 (2 Н, ш., NH2); m/z 213/215 (1:1, М+Н+, 100%). 1.1.3. Методика моноацилирования для получения промежуточного соединения (5-бром[1,2,4]триазоло[1,5-а]пиридин-2-ил)амида циклопропанкарбоновой кислотыEt3N (11,6 мл, 83,3 ммоль), после этого циклопропанкарбонилхлорид (83,3 ммоль). Затем реакционной смеси дают нагреться до температуры окружающей среды и перемешивают до полного израсходования исходного вещества (3). При необходимости, для гарантированного обеспечения завершения реакции добавляют дополнительно триэтиламин (Et3N) (4,64 мл, 33,3 ммоль) и хлорангидрид кислоты (33,3 ммоль). После выпаривания растворителя в вакууме получающийся в результате остаток обрабатывают посредством 7N метанольного раствора аммиака (50 мл) и перемешивают при температуре окружающей среды в течение 1 ч для гидролизирования любого бис-ацилированного продукта. Выделение продукта осуществляют удалением летучих компонентов в вакууме с последующим порошкованием с Et2O (диэтиловый эфир) (50 мл). Твердое вещество собирают фильтрацией, промывают посредством H2O (250 мл), ацетона (50 мл) и Et2O (50 мл), затем сушат в вакууме, что дает требуемое промежуточное ацильное соединение (4). Способ А. 1.1.4. Получение соединений изобретения посредством сочетания Сузуки (5) 1.1.5. Соответствующую бороновую кислоту (2 экв.) добавляют к раствору промежуточного бромсодержащего соединения в смеси 1,4-диоксан/вода (5:1). К раствору добавляют K2CO3 (2 экв.) и [1,1'бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (PdCl2dppf) (5%). Получающуюся в результате смесь затем греют в микроволновой печи при 140 С в течение 30 мин (эта реакция также может быть выполнена посредством обычного нагревания на масляной бане при 90 С в течение 16 ч под N2). Добавляют воду и раствор экстрагируют этилацетатом. Органические слои сушат над MgSO4 и выпаривают в вакууме. Конечное соединение получают после очистки флэш-хроматографией. Метод В. Две капли диметилформамида (DMF) добавляют к раствору 4-[2-(циклопропанкарбониламино)[1,2,4]триазоло[1,5-а]пиридин-5-ил]бензойной кислоты (1 экв.), полученной способом А, в дихлорметане(DCM) в атмосфере N2. Оксалилхлорид (2 экв.) добавляют по каплям к этому получающемуся в результате раствору (выделение газа). Смесь перемешивают при комнатной температуре в течение 2 ч. После завершения реакции, что подтверждено методом жидкостной хроматографии-масс-спектрометрии(LCMS), растворитель удаляют. Неочищенный хлорангидрид кислоты используют без дополнительной очистки на следующей стадии. В 2. Получение амида (общий способ) Соответствующий амин (1,1 экв.; R2b, R2c и m1 являются такими же, как описаны в этом документе) и триэтиламин (Et3N) (5 экв.) растворяют в дихлорметане (DCM) в атмосфере N2 и охлаждают при 0 С. Хлорангидрид кислоты (В 1, 1 экв.), растворенный в DCM, добавляют по каплям к этому раствору. Реакционную смесь перемешивают при комнатной температуре в течение 3 ч. По истечении этого времени реакция является завершенной. Соединение экстрагируют посредством этилацетата (EtOAc) и воды,промывают соляным раствором и сушат над MgSO4. Органические слои фильтруют и упаривают. Конечное соединение выделяют препаративной высокоэффективной жидкостной хроматографией (HPLC). Препаративный высокоэффективный жидкостной хроматограф (HPLC): фирма Waters, колонки XBridgePrep OBD 19 мм (внутренний диаметр)100 мм (длина) с фазой С 18, с частицами размером 5 мкм (каталожный номер 186002978). Все способы выполняют с использованием градиентов MeCN/H2O. H2O со- 27018587(DMF) под N2 и добавляют по каплям соответственный алкилирующий агент (1,1 экв.). Получающуюся в результате суспензию греют при 50 С в течение 16 ч. По истечении этого времени реакция является завершенной. Соединение экстрагируют посредством этилацетата (EtOAc) и воды, промывают солевым раствором и сушат над MgSO4. Органические слои фильтруют и упаривают. Конечное соединение выделяют препаративной высокоэффективной жидкостной хроматографией (HPLC). Препаративный высокоэффективный жидкостной хроматограф (HPLC): фирма Waters, колонки XBridge Prep OBD 19 мм (внутренний диаметр)100 мм (длина) с фазой С 18, с частицами размером 5 мкм (каталожный номер 186002978). Все способы выполняют с использованием градиентов MeCN/H2O. H2O содержит или 0,1% трифторуксусной кислоты (TFA) или 0,1% NH3. Способ D-С(=O)- или -SO2-. Производное анилина (1 экв.), полученное способом А, и триэтиламин (Et3N) (5 экв.) растворяют в дихлорметане (DCM) под N2 и охлаждают при 0 С. Соответственный хлорангидрид кислоты (для А) или сульфонилхлорид (для В) (1,5 экв.), растворенный в DCM, добавляют по каплям к этому раствору. Реакционную смесь перемешивают при комнатной температуре в течение 16 ч. По истечении этого времени реакция является завершенной. Соединение экстрагируют посредством EtOAc и воды, промывают соляным раствором и сушат над MgSO4. Органические слои фильтруют и упаривают. Конечное соединение выделяют препаративной высокоэффективной жидкостной хроматографией (HPLC). Препаративный высокоэффективный жидкостной хроматограф (HPLC): фирма Waters, колонки XBridge Prep OBD 19 мм(внутренний диаметр)100 мм (длина) с фазой С 18, с частицами размером 5 мкм (каталожный номер 186002978). Все способы выполняют с использованием градиентов MeCN/Н 2 О. Н 2 О содержит или 0,1% трифторуксусной кислоты (TFA), или 0,1% NH3. Способ Е Соответствующий альдегид (2 экв.), производное анилина (1 экв.), полученное способом А, и тетран-пропоксид титана (Ti(OPr)4) перемешивают при комнатной температуре в течение 3 ч. Смесь разбавляют в этаноле и добавляют Na(CN)BH3 (1 экв.). Получающийся в результате раствор перемешивают при комнатной температуре в течение 16 ч. Смесь разбавляют водой и фильтруют. Фильтрат промывают этанолом. Объединенные фазы с растворителем упаривают под вакуумом. Конечное соединение выделяют препаративной высокоэффективной жидкостной хроматографией (HPLC). Препаративный высокоэффективный жидкостной хроматограф (HPLC): фирма Waters, колонкиXBridge Prep OBD 19 мм (внутренний диаметр)100 мм (длина) с фазой С 18, с частицами размером 5 мкм (каталожный номер 186002978). Все способы выполняют с использованием градиентов MeCN/Н 2 О. Н 2 О содержит или 0,1% трифторуксусной кислоты (TFA), или 0,1% NH3. Способ F К раствору 5-бром-2-аминотриазолопиридина (1 экв.) в безводном ацетонитриле (CH3CN) при 5 С добавляют триэтиламин (Et3N) (2,5 экв.), после этого ацетилхлорид (2,5 экв.). Затем реакционной смеси дают нагреться до температуры окружающей среды и перемешивают до полного израсходования исходного вещества. При необходимости, для гарантированного обеспечения завершения реакции добавляют дополнительно Et3N (1 экв.) и хлорангидрид кислоты (1 экв.). После выпаривания растворителя в вакууме получающийся в результате остаток обрабатывают посредством 7N метанольного раствора аммиака(50 мл) и перемешивают при температуре окружающей среды (в течение 16 ч) для того, чтобы гидролизовать любой бис-ацилированный продукт. Выделение продукта осуществляют путем удаления летучих компонентов в вакууме с последующим добавлением воды и экстракцией этилацетатом. Органическую фазу затем сушат над MgSO4, упаривают в вакууме. Соединение может быть использовано без дополнительной очистки. Реакция по Сузуки (общий способ)
МПК / Метки
МПК: A61P 19/02, A61K 31/437, C07D 471/04
Метки: лечения, производные, заболеваний, 2-циклопропилкарбониламино-5-фенил[1,2,4]триазоло[1,5-a]пиридина, дегенеративных, воспалительных
Код ссылки
<a href="https://eas.patents.su/30-18587-proizvodnye-2-ciklopropilkarbonilamino-5-fenil124triazolo15-apiridina-dlya-lecheniya-degenerativnyh-i-vospalitelnyh-zabolevanijj.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 2-циклопропилкарбониламино-5-фенил[1,2,4]триазоло[1,5-a]пиридина для лечения дегенеративных и воспалительных заболеваний</a>
Предыдущий патент: Способ выплавки ферросиликоалюминия в руднотермической печи
Следующий патент: Способ пуска реактора гидрирования лигроиновой фракции
Случайный патент: Почвообрабатывающая машина и устройство, предназначенное для оснащения такой машины












