Производные этилендиамина для лечения микобактериальных инфекций
Формула / Реферат
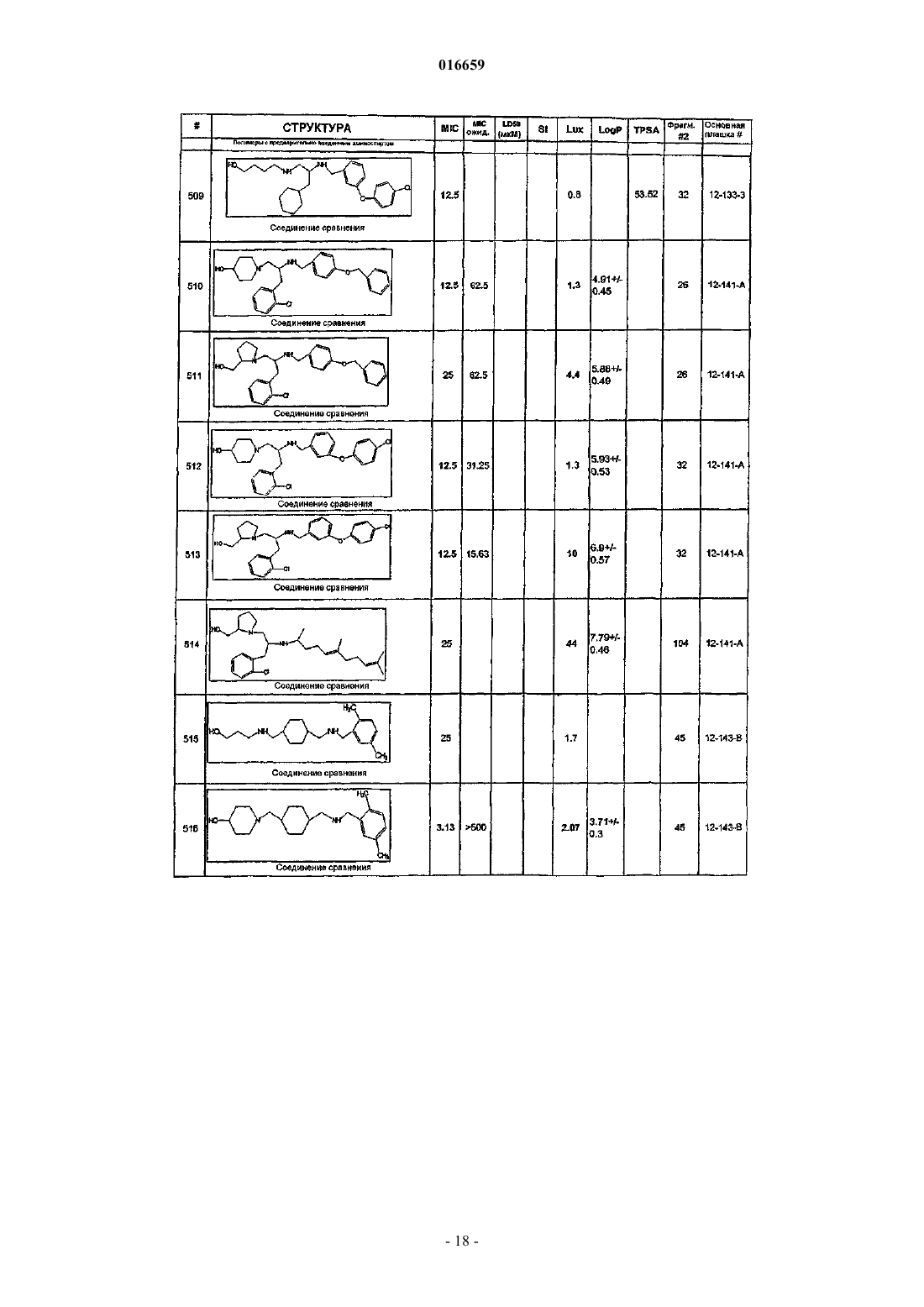
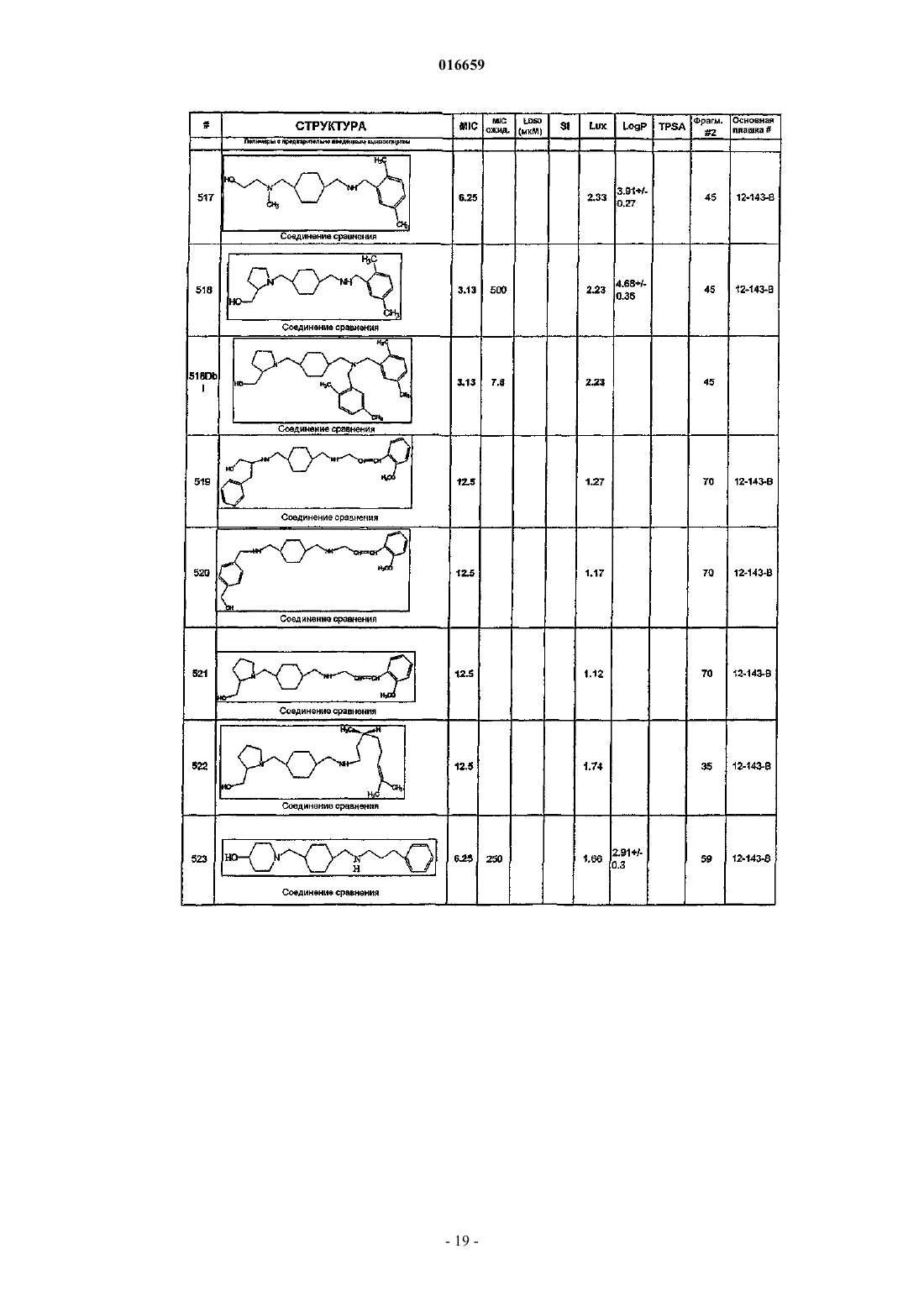
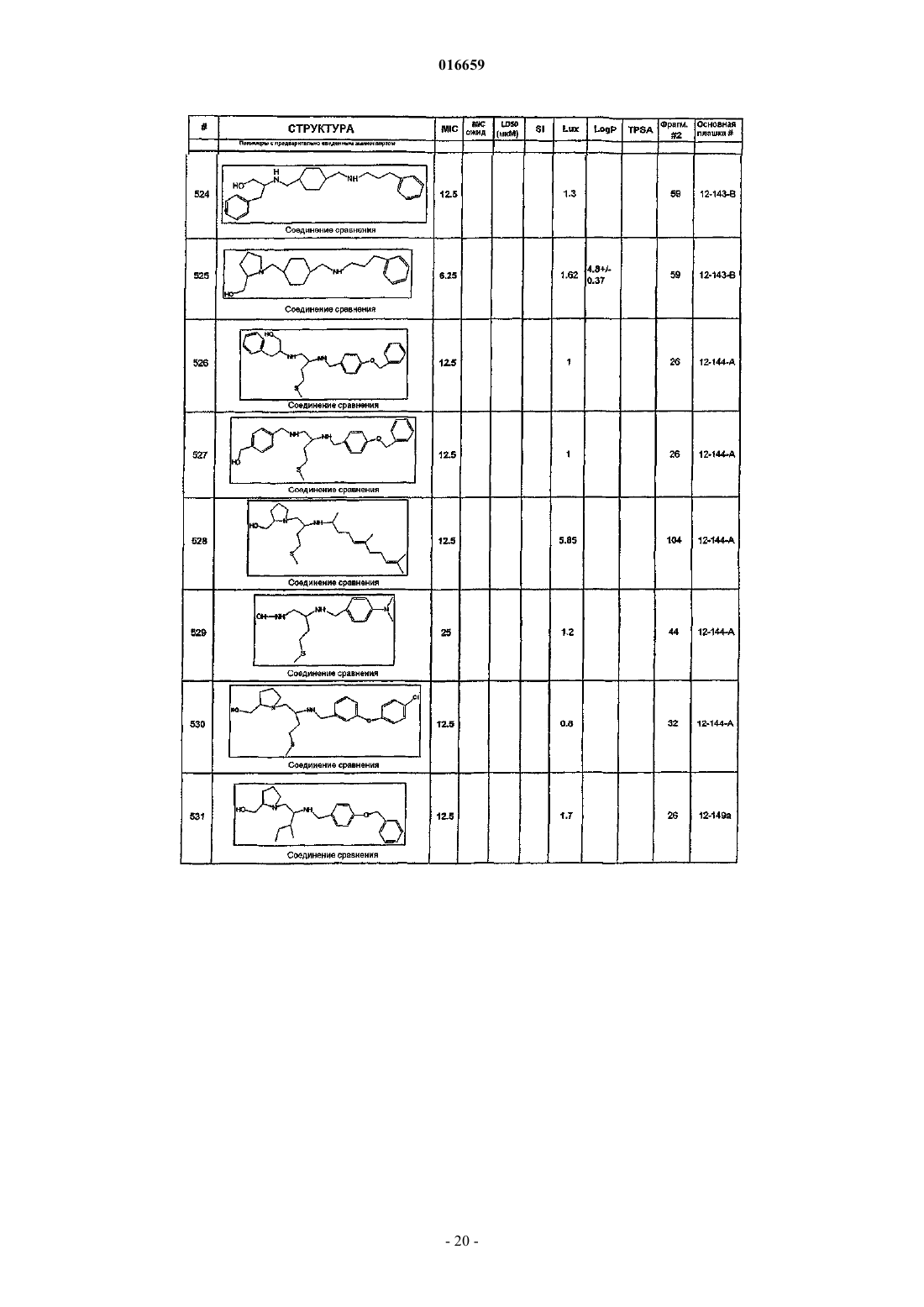
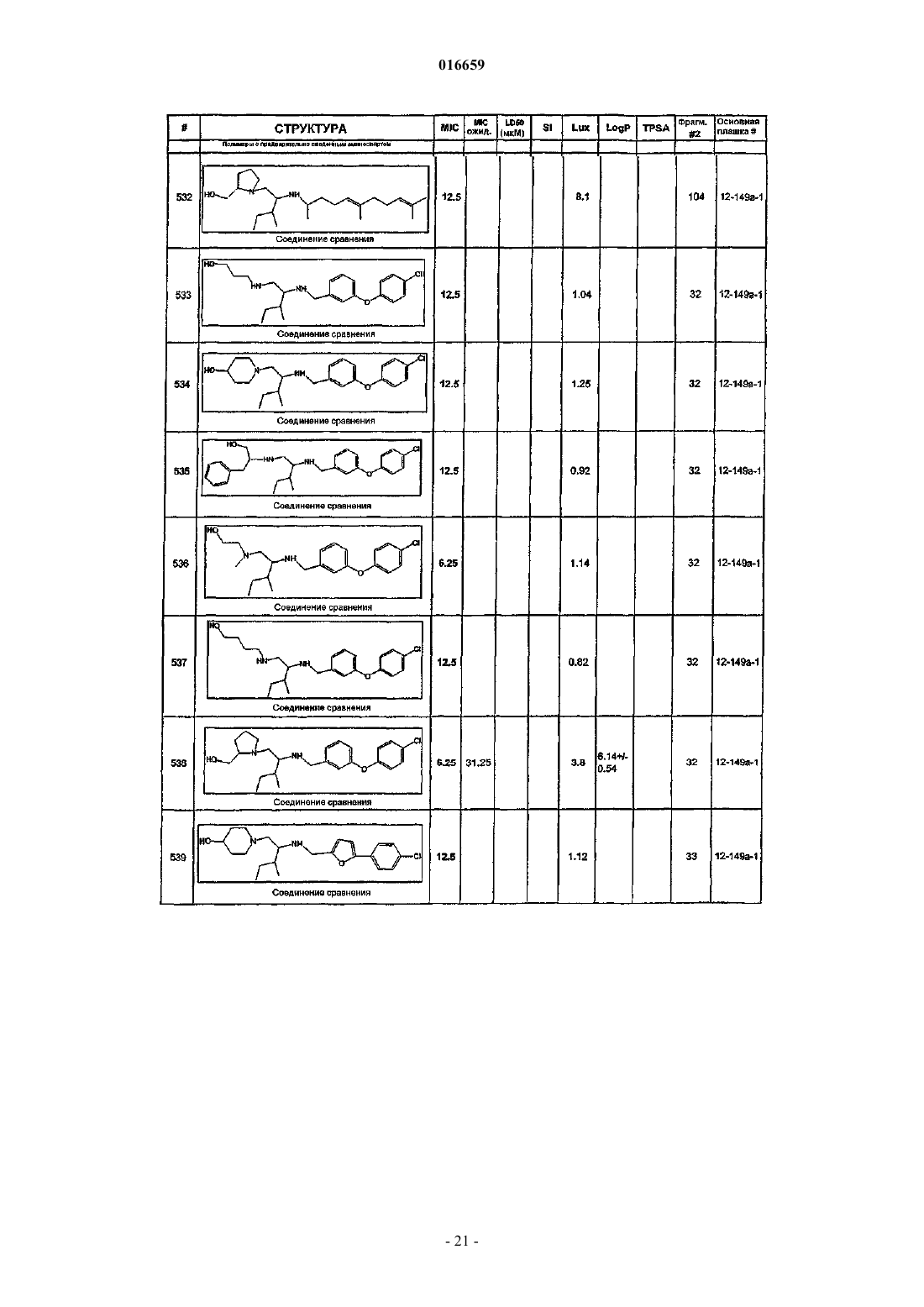
1. Замещенное этилендиаминовое соединение, выбранное из
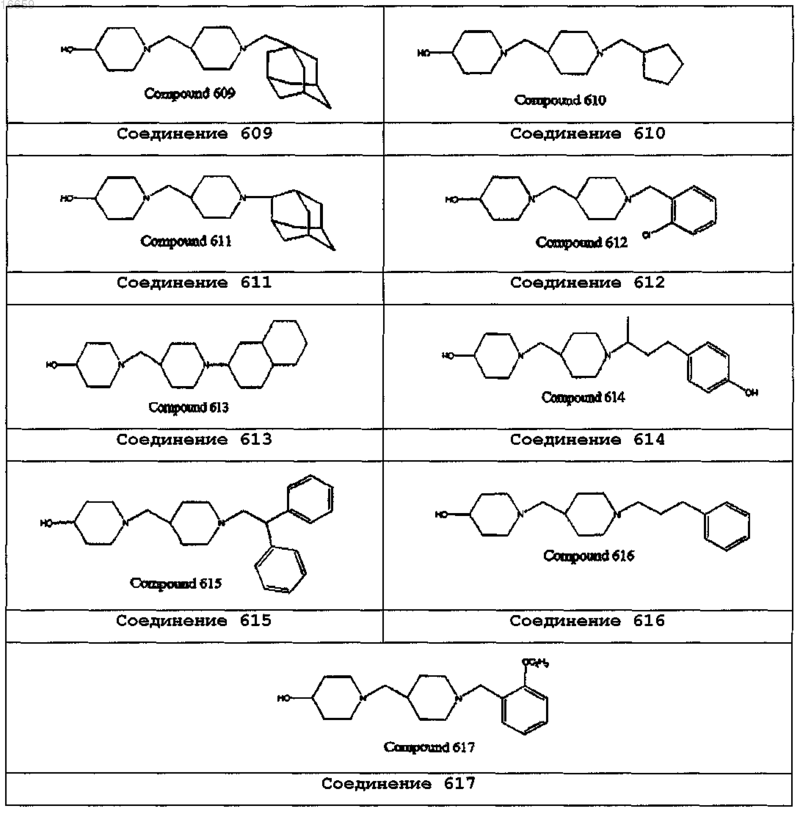
2. Фармацевтическая композиция, содержащая соединение по п.1 и фармацевтически приемлемый носитель для лечения микобактериальной инфекции у человека или животного.
3. Фармацевтическая композиция по п.2, для наружного, перорального, подкожного, внутримышечного, внутриглазного, внутриартериального, внутривенного или локального применения с использованием имплантируемой единичной дозы
4. Фармацевтическая композиция по п.2, где композиция находится в жидкой форме или в виде аэрозоля.
5. Применение соединения по п.1 для изготовления лекарственного средства для лечения микобактериальной инфекции у человека или животного.
6. Применение по п.5, где микобактериальная инфекция представляет собой М.tuberculosis (МОТТ), М.avium intracellulare, M.kansarii, M.fortuitum, M.chelonae, M.leprae, M.africanum, M.bovis, M.microti, M.avium paratuberculosis, M.intracellulare, M.scrofulaceum, M.xenopi, M.Marinum или M.ulcerans.
7. Применение соединения по п.1 для лечения микобактериальной инфекции у человека или животного.
Текст
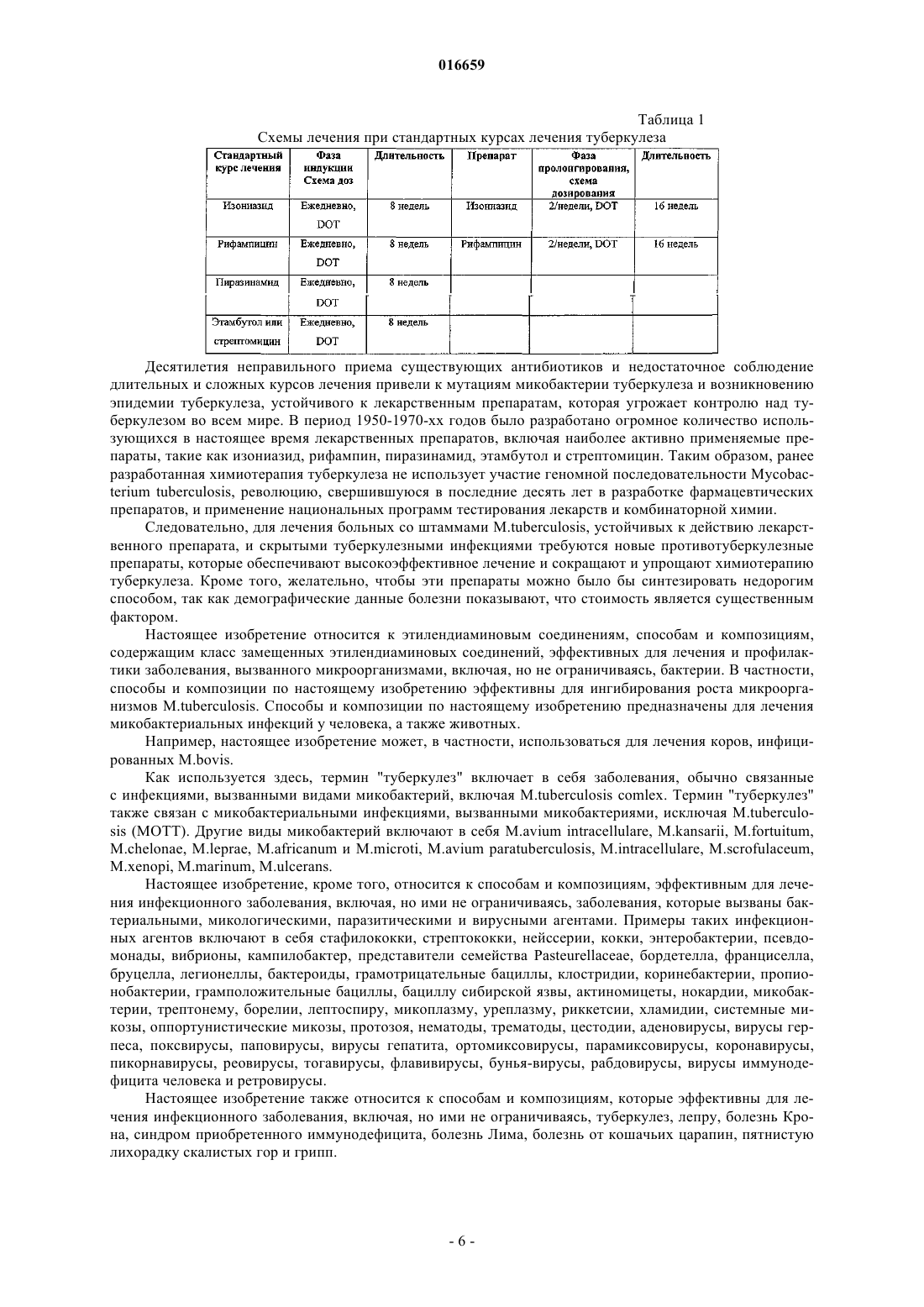
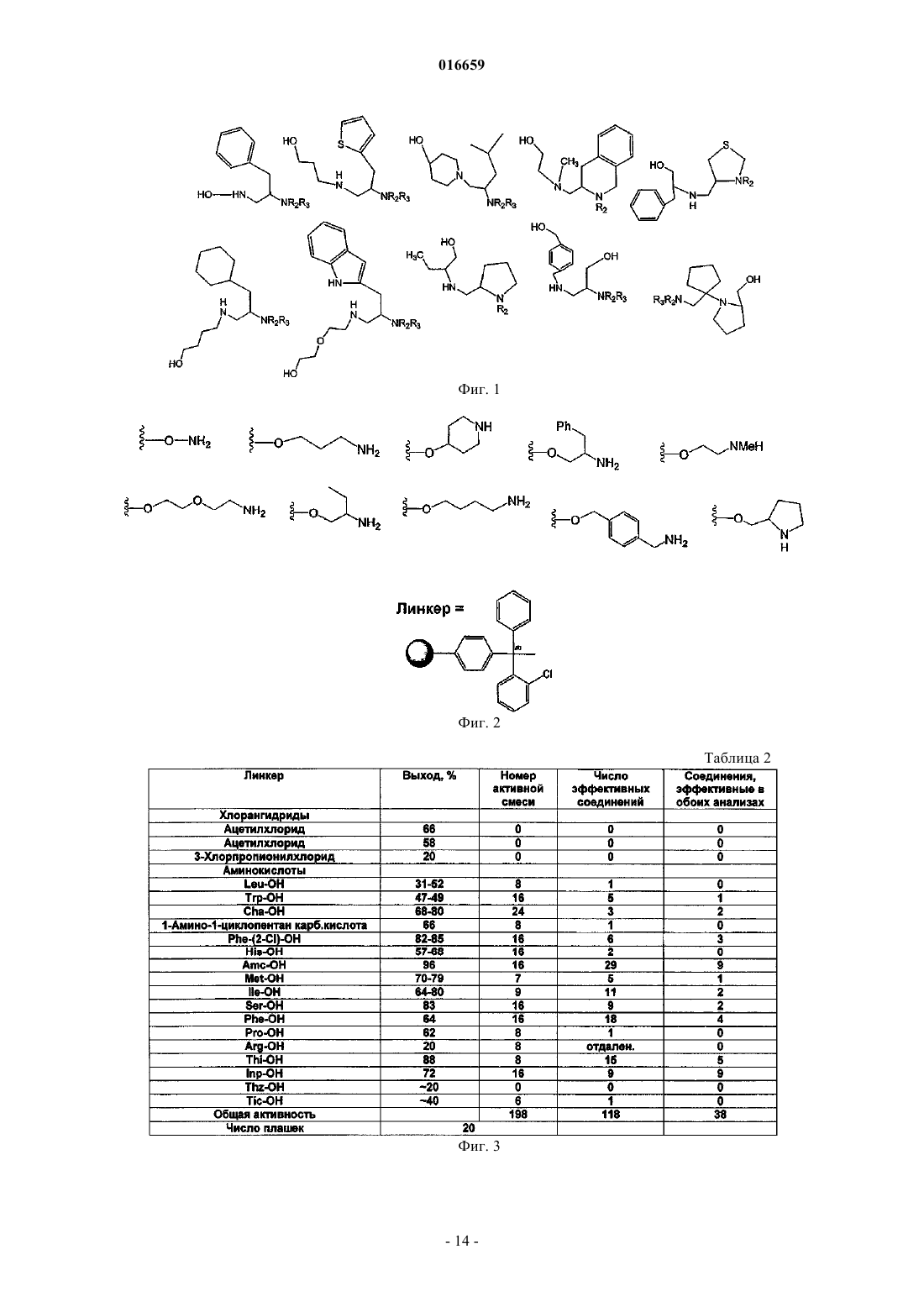
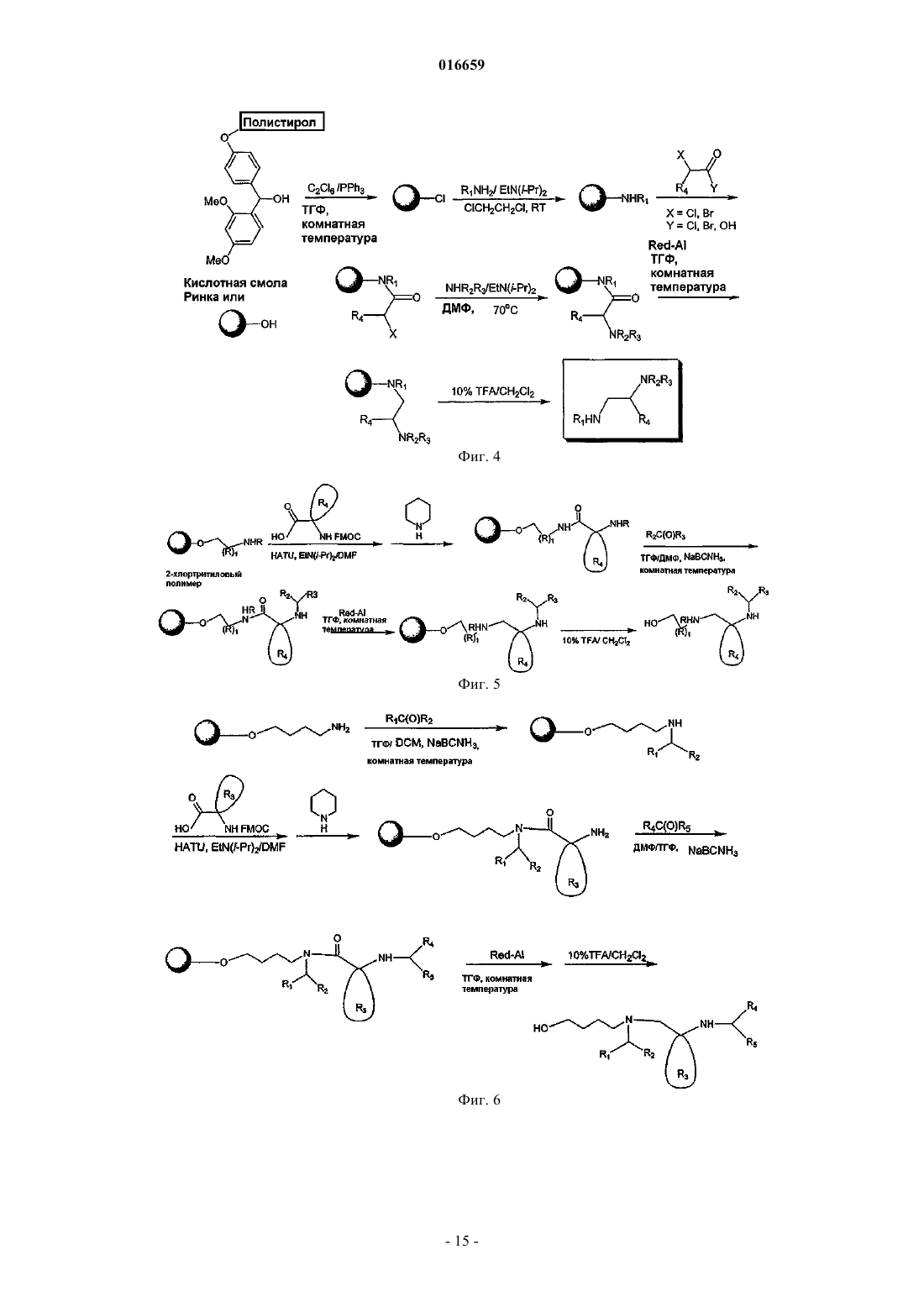
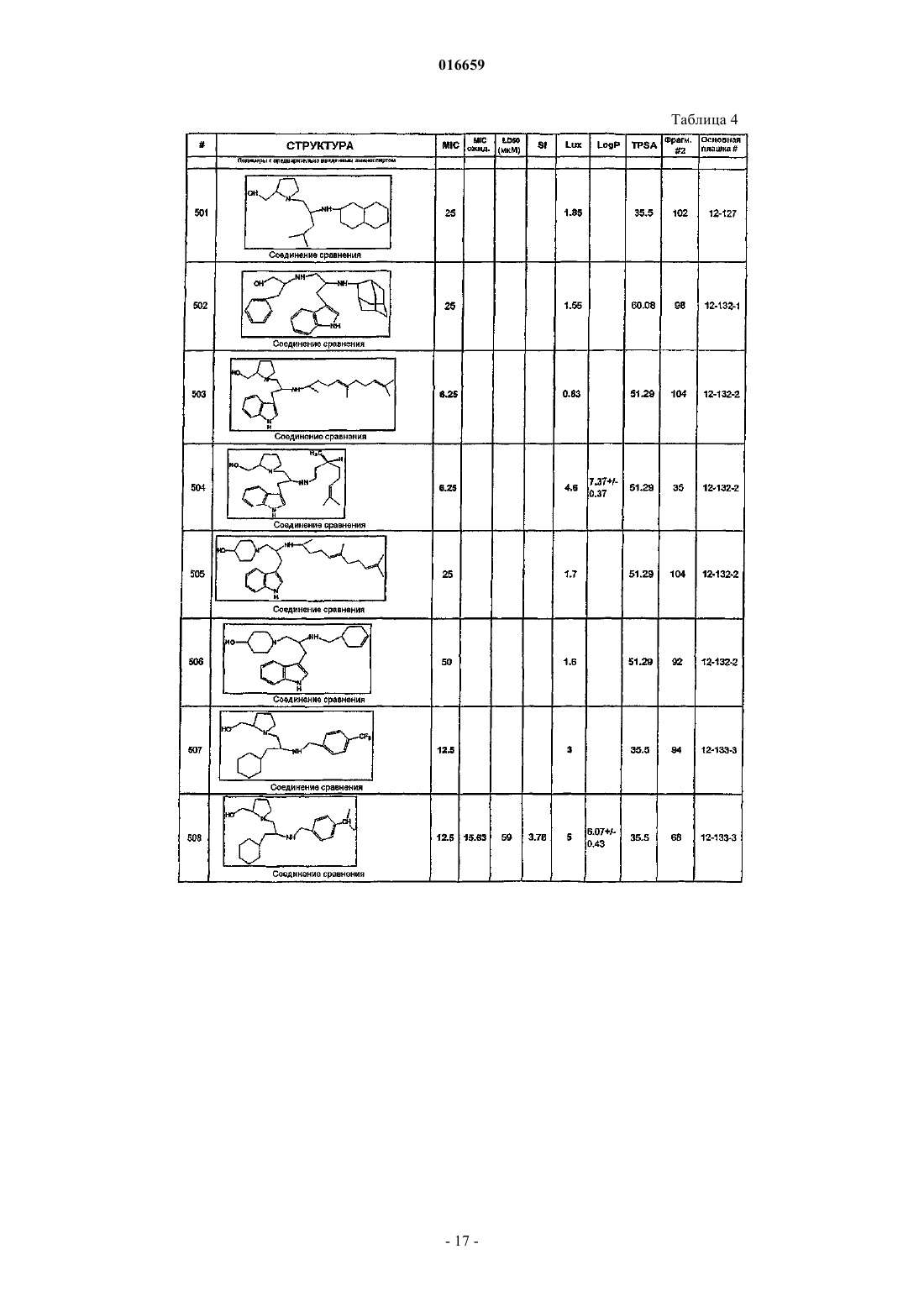
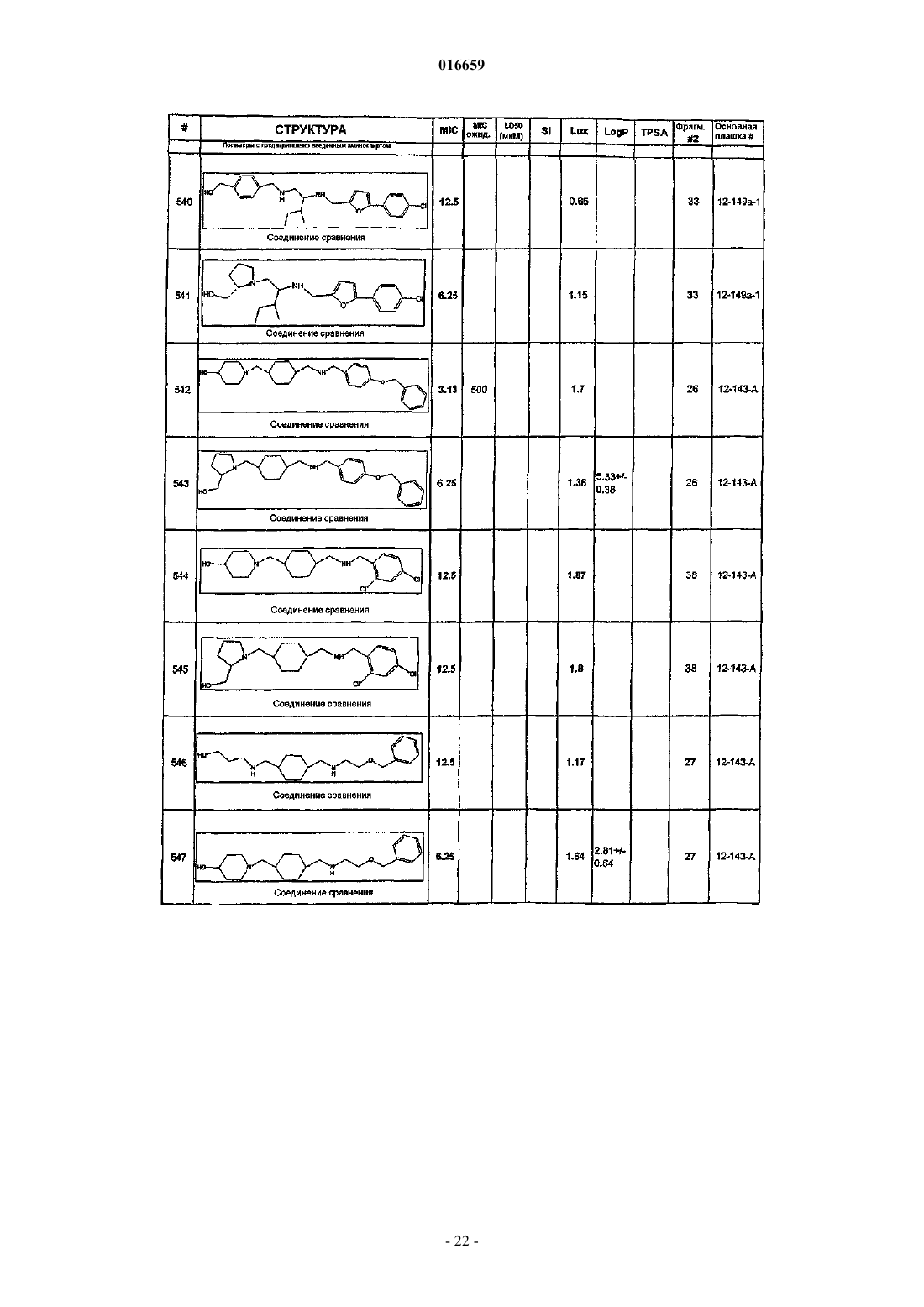
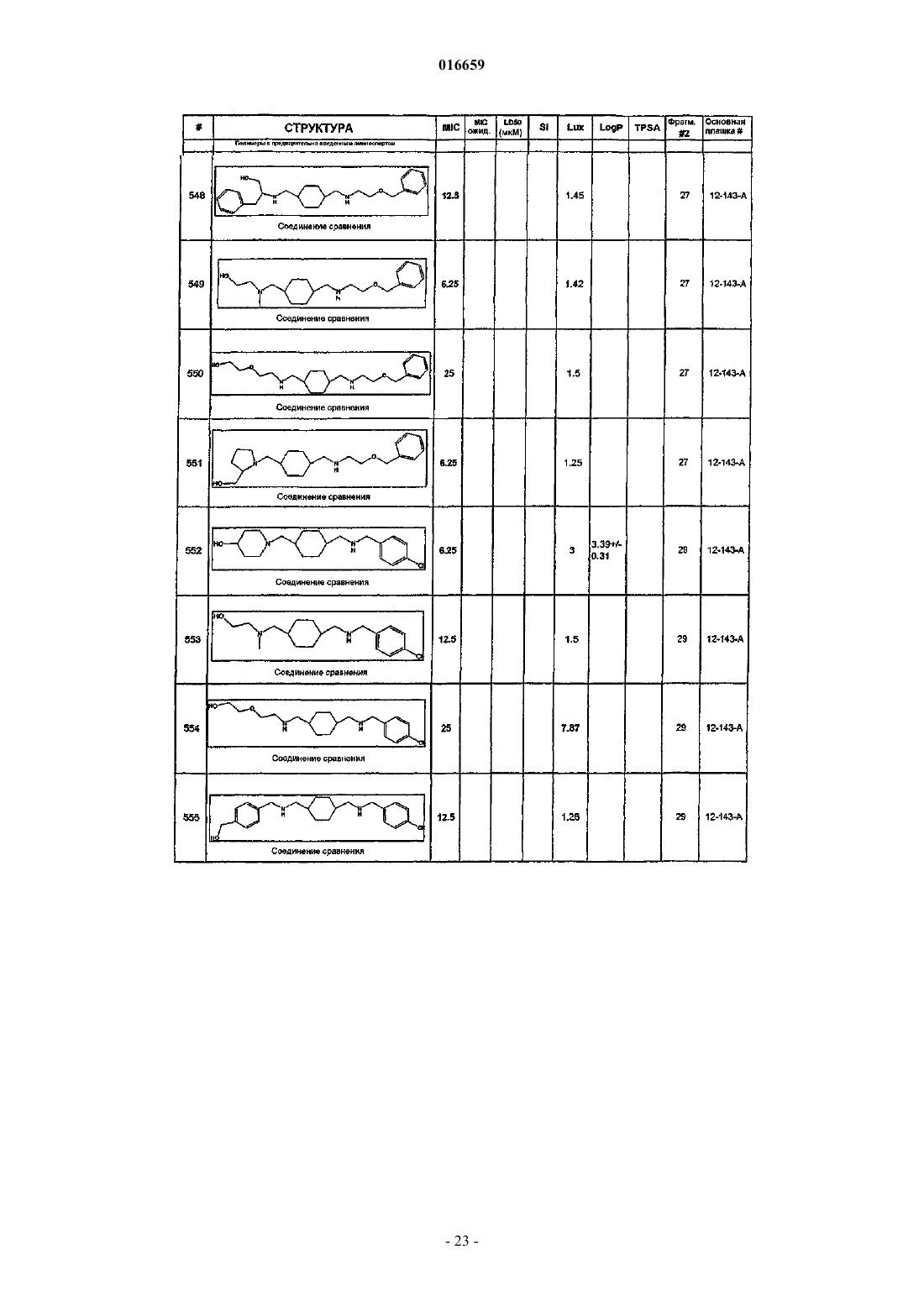
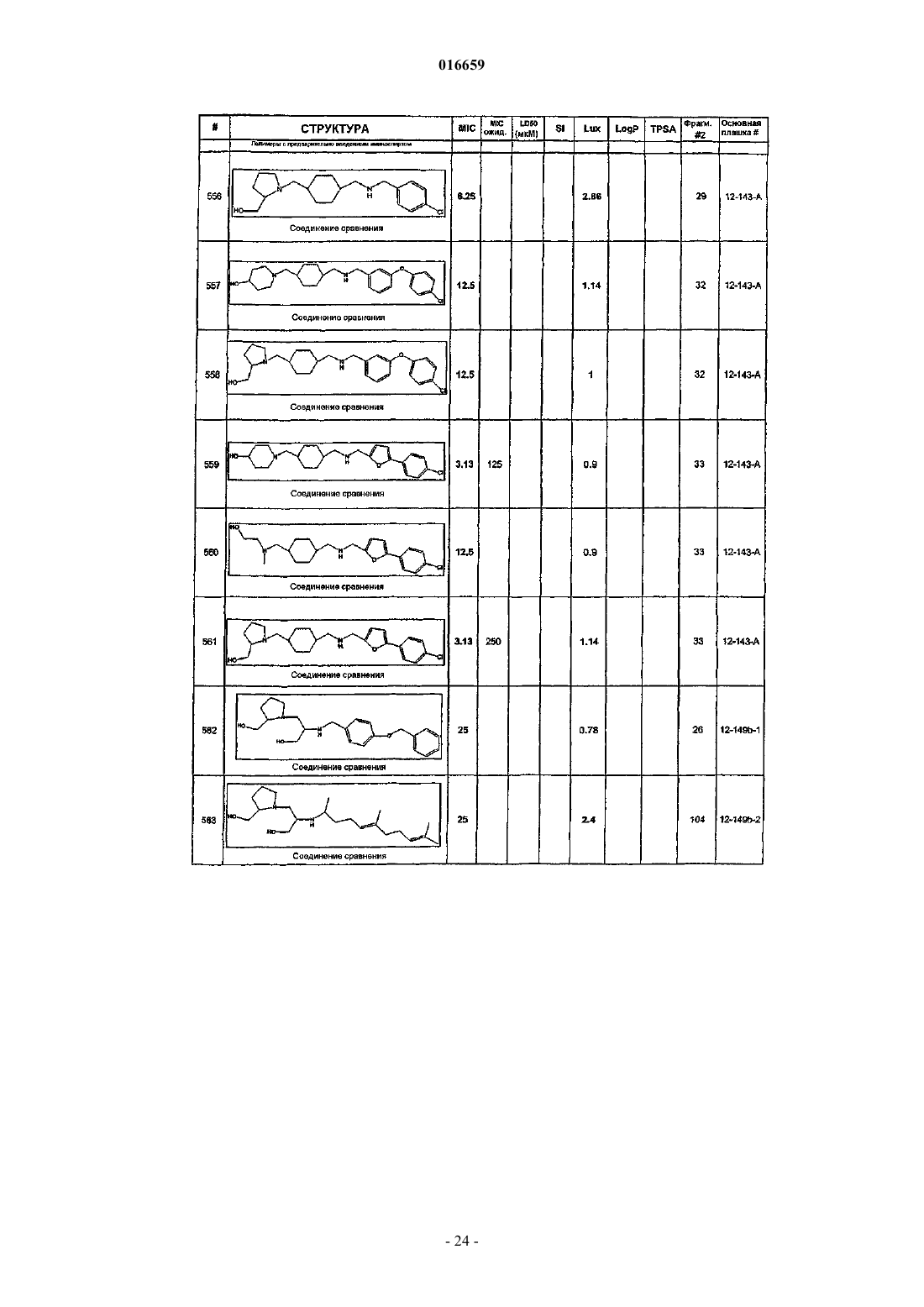
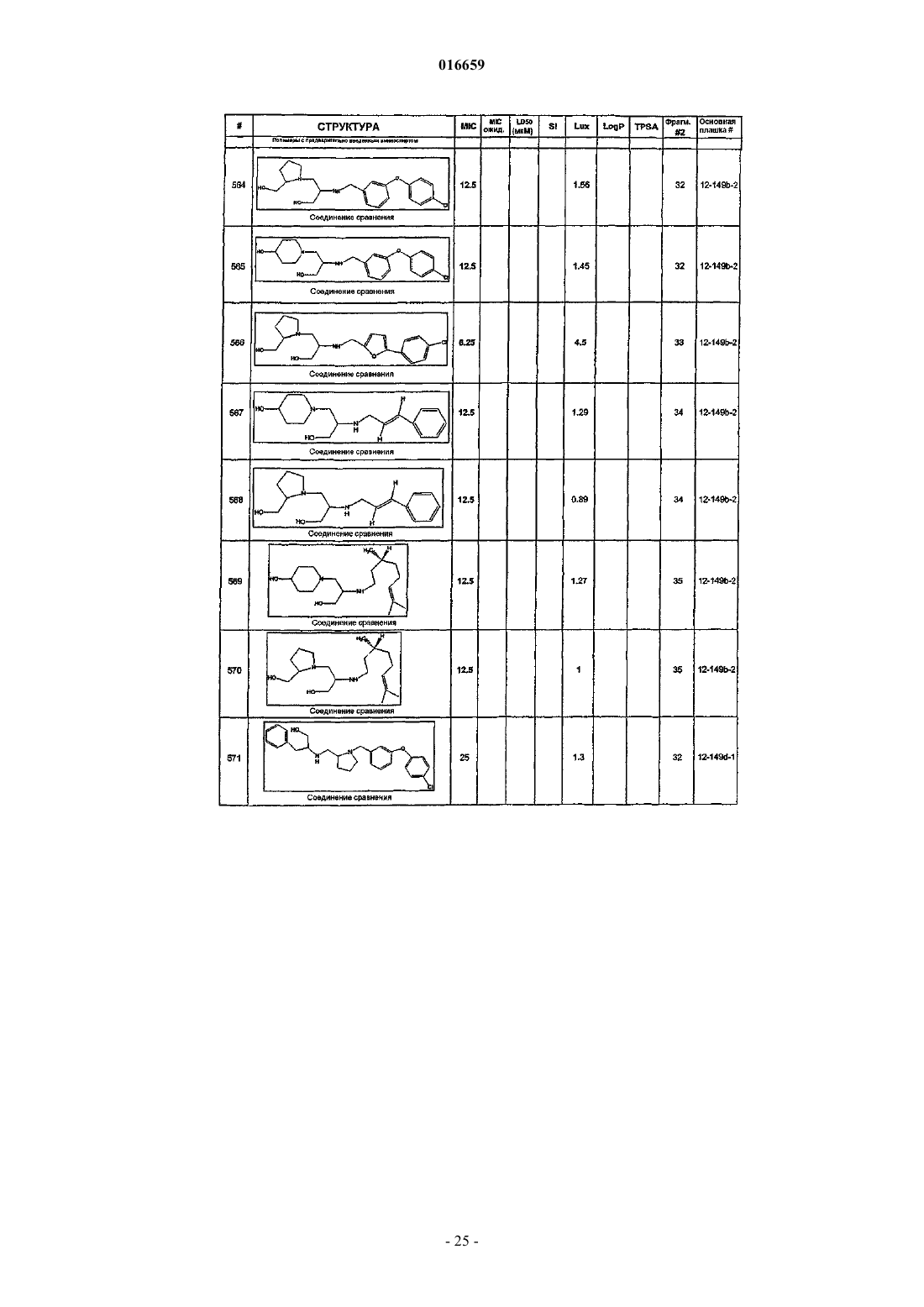
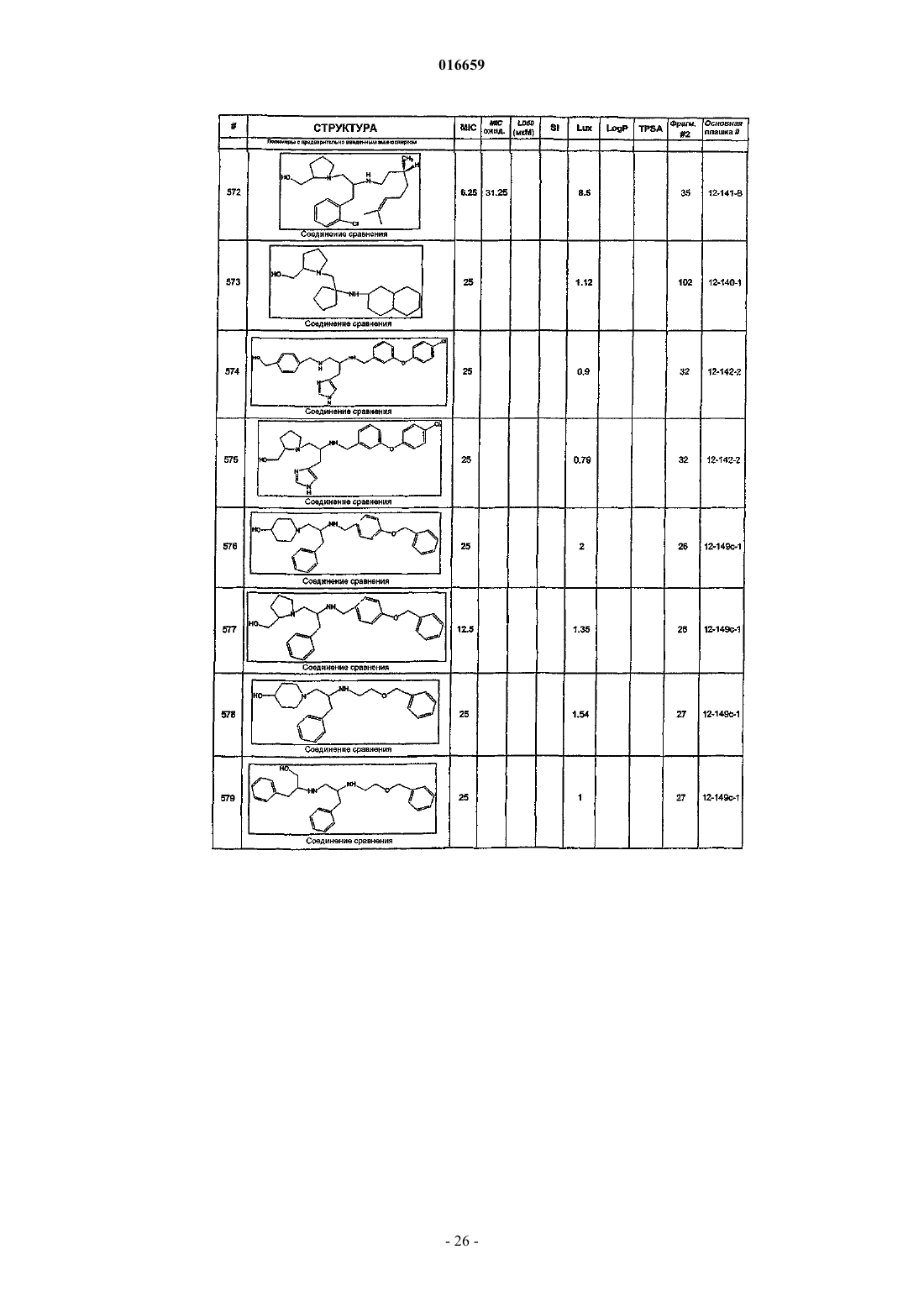
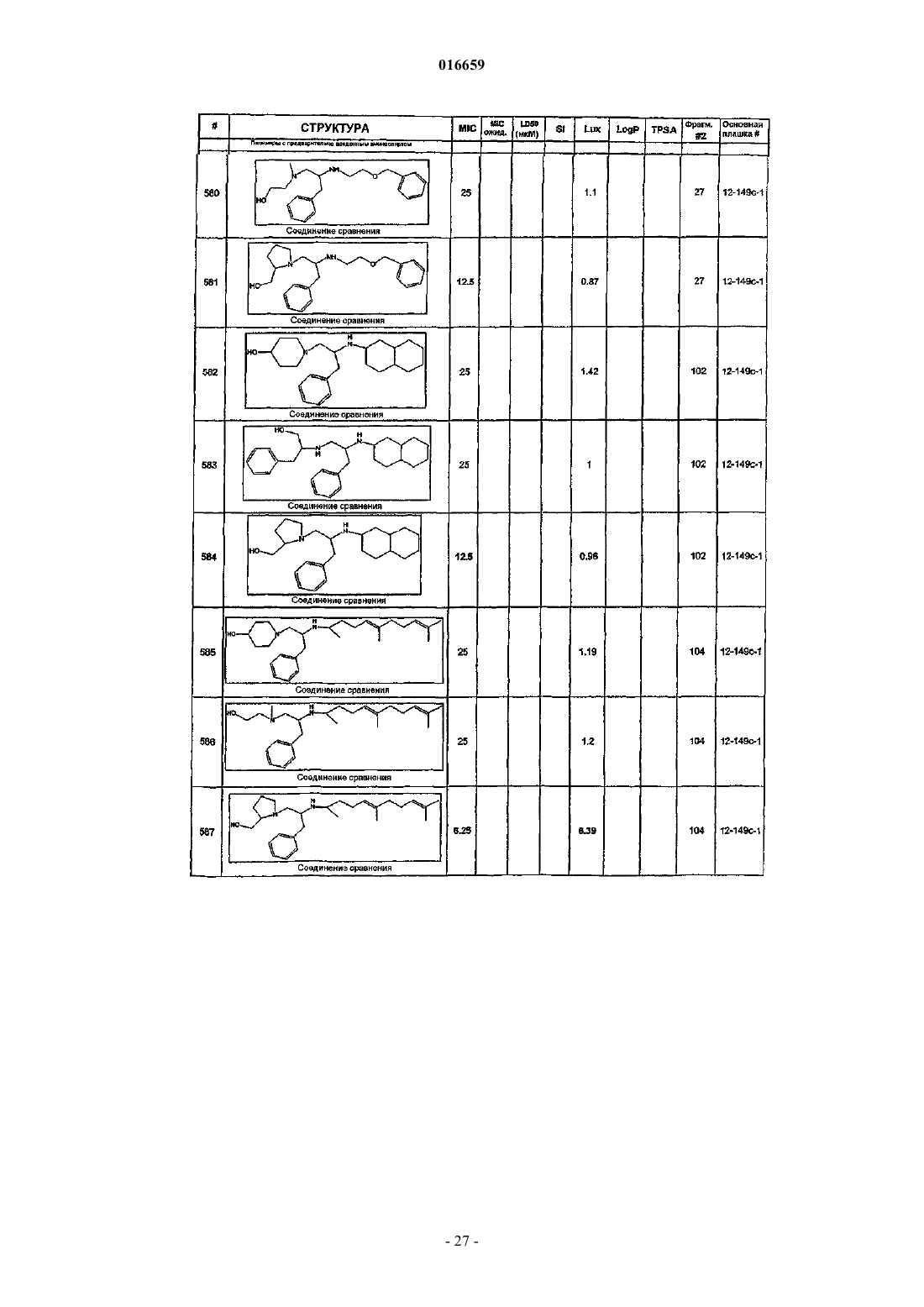
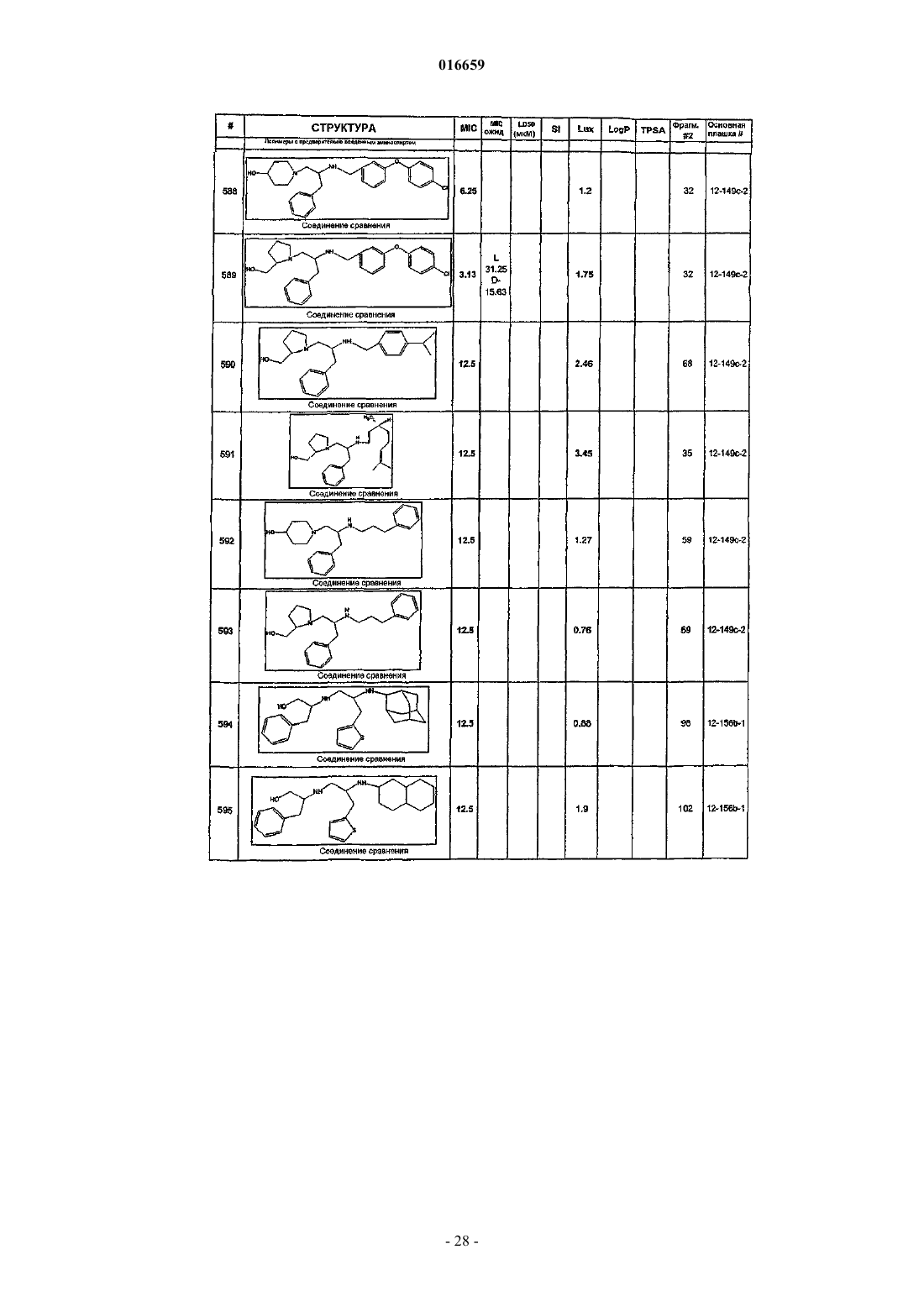
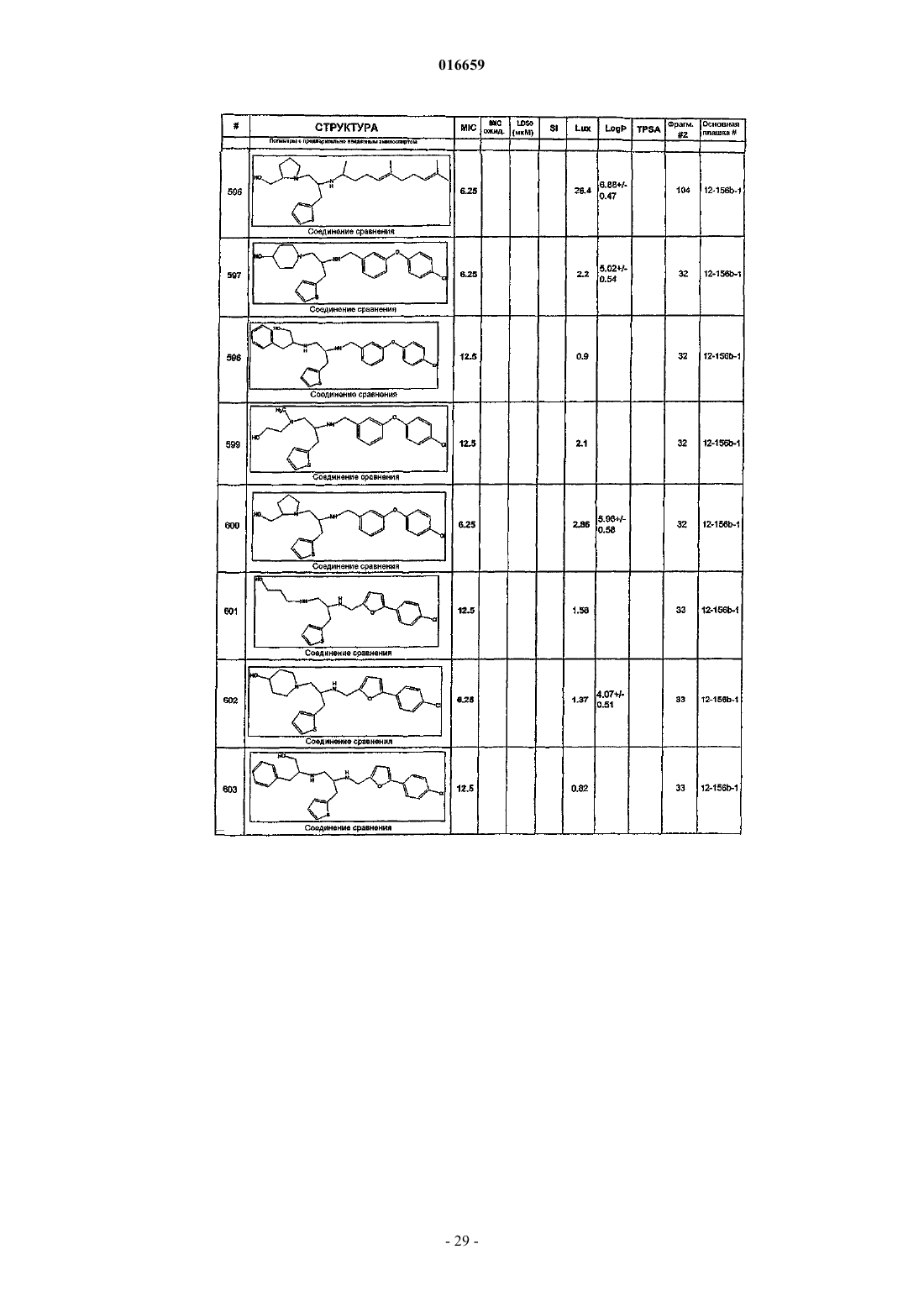
ПРОИЗВОДНЫЕ ЭТИЛЕНДИАМИНА ДЛЯ ЛЕЧЕНИЯ МИКОБАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ Изобретение относится к замещенным производным этилендиамина, которые эффективны для лечения заболевания, вызванного микроорганизмами, в частности туберкулеза. Кроме того,изобретение относится к композициям, содержащим замещенные производные этилендиамина,для лечения инфекционных заболеваний. Применение упомянутых выше соединений для лечения микобактериальной инфекции и для изготовления лекарственного средства для лечения микобактериальной инфекции также раскрыто в настоящем изобретении. 016659 Область техники Настоящее изобретение относится к соединениям этилендиамина, которые эффективны для лечения инфекционного заболевания, способам и композициям для лечения заболевания, вызванного микроорганизмами, в частности туберкулеза. Настоящее изобретение также относится к способам и композициям с улучшенной активностью в отношении микобактерий, а именно к композициям, содержащим новые производные замещенного этилендиамина. Предпосылки изобретения Микобактериальные инфекции часто проявляются как заболевания, такие как туберкулез. Инфекции человека, вызванные микобактериями, широко распространены с древних времен, и на сегодняшний день туберкулез остается главной причиной смертности. Хотя параллельно с повышением стандартов жизни начиная с середины XIX века риск заболевания снижался, микобактериальные заболевания до сих пор являются основной причиной заболеваемости и смертности в странах с ограниченными медицинскими возможностями. Кроме того, у пациентов с пораженной иммунной системой микобактериальные заболевания могут вызвать очень сильное диссеминированное заболевание. Несмотря на усилия многих всемирных организаций здравоохранения, так и не удалось ни искоренить микобактериальные заболевания, ни устранить их угрозу. Около 1/3 населения планеты инфицировано комплексом Mycobacteriumtuberculosis, обычно называемых как туберкулез (ТБ), ежегодно происходит приблизительно 8 миллионов новых случаев заражения, и каждый год от ТБ умирает от 2 до 3 миллионов людей. Туберкулез (ТБ) является наиболее частой причиной смерти людей при заражении одним этиологическим фактором (см.Dye et al., J. Am. Med. Association, 282, 677-686, (1999) и 2000 WHO/OMS Press Release). После десятилетнего снижения заболеваемости в настоящее время число инфицированных ТБ увеличивается. В Соединенных Штатах, вероятно заражено до 10 миллионов человек. В 1990 г. сообщалось о почти 28000 новых случаях, что на 9,4% больше, чем в 1989 г. Начиная с 1985 по 1990 гг. отмечен рост заболеваемости на 16%. Перенаселенность и воздушное пространство являются особенно благоприятными условиями для распространения ТБ, способствуя увеличению случаев заболевания, что наблюдается, например, среди тюремных заключенных и среди бездомных в больших городах США. Приблизительно половина пациентов с "синдромом приобретенного иммунодефицита" (СПИД) заражены микобактериальной инфекцией, при этом ТБ у таких пациентов является особенно изнуряющим осложнением. Больные СПИДом в наибольшей степени подвержены риску развития клинического ТБ, и, кажется, противо-ТБ терапия является менее эффективной, чем у пациентов, не страдающих СПИДом. Поэтому инфекция часто прогрессирует до летального диссеминированного заболевания. Микобактерии, иные, чем М.tuberculosis, все в большей степени обнаруживаются в условнопатогенных инфекциях, которые беспокоят больных СПИДом. 68% выделенных микобактерий у больных СПИДом составляют организмы группы М.avium intracellulare (MAC), в частности серотипы четыре и восемь. У больных СПИДом обнаружено огромное число MAC (до 1010 кислотоустойчивых бацилл на 1 г ткани) и, следовательно, составлен прогноз заболевания для инфицированного СПИДом пациента. Всемирная организация здравоохранения (ВОЗ) продолжает поддерживать борьбу против ТБ, рекомендуя превентивные проекты, такие как "Expanded Program on Immunization" (EPI) ("Расширенная программа иммунизации"), и терапевтические согласованные проекты, такие как "Directly ObservedTreatment Short-Course" (DOTS) "Краткосрочный курс контролируемой терапии". Для уничтожения ТБ в равной мере значимыми являются диагностика, лечение и профилактика. Быстрое определение больных с активной формой ТБ позволит проводить раннее лечение, при котором будут вылечены приблизительно 90% больных. Таким образом, ранняя диагностика является определяющим фактором для борьбы с ТБ. Кроме того, проведение полного курса лечения будет гарантировать не только уничтожение инфекции, но также снижение опасности появления штаммов с устойчивостью к лекарственным препаратам. Появление штаммов М.tuberculosis, устойчивых к лекарственным препаратам, является очень опасным явлением. Процент появления новых случаев ТБ с доказанной устойчивостью по крайней мере к одному стандартному препарату вырос от 10% в начале 1980-х до 23% в 1991 г. Соблюдение режимов лечения поэтому также является определяющим фактором в усилиях по подавлению ТБ и предупреждает появление штаммов с устойчивостью к лекарственным препаратам. В равной степени важным является разработка новых терапевтических средств, которые эффективны в качестве вакцин и в качестве лекарственных средств при заболеваниях, вызываемых штаммами микобактерий, устойчивых к лекарственным препаратам. Хотя было идентифицировано более 37 видов микобактерий, более 95% всех инфекций человека вызываются шестью видами микобактерий: М.tuberculosis, M.aviumin intracellulare, M.kansasii,M.fortuitum, M.chelonae и М.leprae. Наиболее распространенным заболеванием у человека, вызываемым микобактерией, является туберкулез (ТБ), который преимущественно вызывается штаммами микобактерий, включающих М.tuberculosis, M.bovis или М.africanum (Merck Manual. 1992). Заражение обычно возникает при вдыхании инфекционных частиц, которые способны проникнуть в легкие. После того как бациллы поглощаются альвеолярными макрофагами, они могут свободно реплицироваться с последующим разрушением фагоцитарных клеток. Происходит каскадный эффект, при котором деструкция фаго-1 016659 цитарных клеток вызывает миграцию дополнительных макрофагов и лимфоцитов к месту инфекции, что,в конечном счете, также приводит к их уничтожению. Во время начальной стадии заболевание затем диссеминируется инфицированными макрофагами, которые попадают в местные лимфоузлы, а также в поток крови и другие ткани, такие как костный мозг, селезенка, почки, кости и центральная нервная система (см. Murray et al. Medical Microbiology, The C.V. Mosby Company. 219-230 (1990. До сих пор до конца не ясны факторы, которые вносят вклад в вирулентность микобактерий. Многие исследователи полагают, что в морфологию колоний и вирулентность вносят вклад липиды клеточной стенки и поверхности бактерий. Имеющиеся данные показывают, что С-микозиды, находящиеся на поверхности некоторых микобактериальных клеток, играют важную роль в облегчении выживания организма внутри макрофагов. Другие микобактерии содержат трегалозу 6,6' димиколат, фактор жгутообразования. Взаимосвязь между морфологией колонии и вирулентностью, в частности, явно прослеживается у бацилл М.avium, M.avium по нескольким различиям в формах колоний. Бациллы, которые растут как прозрачные или шероховатые колонии на обычных лабораторных средах, способны размножаться в макрофагах в тканевой культуре, вирулентны при введении восприимчивым мышам и устойчивы к антибиотикам. Шероховатые или бесцветные колонии бацилл, которые растут на лабораторной культуральной среде, часто спонтанно принимают морфологию матовых R колоний, при этом они не способны размножаться в макрофагах, невируленты у мышей и очень чувствительны к антибиотикам. Различие в морфологии колоний бесцветных, шероховатых и матовых штаммов М.avium почти, несомненно, связано с наличием гликолипидного покрытия на поверхности бесцветных и шероховатых организмов, которые действуют как защитная капсула. Эта капсула, или покрытие, главным образом, состоит из С-микозидов,которые вероятно защищают вирулентные организмы М.avium от лизосомальных ферментов и антибиотиков. Напротив, неверулентные матовые формы М.avium имеют очень малое количество С-микозида на своей поверхности. Как резистентность к антибиотикам, так и устойчивость к уничтожению макрофагами характерны для гликолипидного барьера на поверхности М.avium. Диагностирование микобактериальной инфекции подтверждается путем выделения и идентификации патогена, хотя обычное диагностирование основывается на мазке мокроты, рентгеновском исследовании грудной клетки (CXR) и клинических симптомах. Выделение микобактерии в среде занимает от четырех до восьми недель. Идентификация вида занимает более двух недель. Существует несколько других методик определения микобактерии, такие как полимеразная цепная реакция (PCR), прямой метод определения микобактерии туберкулеза или прямой метод определения амплифицированных микобактерий туберкулеза (MTD) и определительные анализы, в которых используются радиоактивные метки. Одним из диагностических тестов, который широко используется для определения инфекционных заболеваний, вызванных M.tuberculosis, является туберкулиновая кожная проба. Хотя существует большое количество варианты этого теста, проводимого на коже, обычно используется один из двух препаратов туберкулиновых антигенов: старый туберкулин (ОТ) или очищенное производное белка (PPD). Препарат антигена либо вводят в кожу чрескожным путем, либо наносят местно и затем инвазивно транспортируют в кожу, используя многочелюстной инокулятор (инъекционная кожная проба). При проведении диагностического кожного теста сталкиваются с несколькими трудностями. Например, инъекционная кожная проба не может быть широко рекомендована, так как количество вводимого антигена в интрадермальный слой нельзя точно контролировать (см. Murray et al. Medical Microbiology, TheC.V. Mosby Company 219-230 (1990. Хотя туберкулиновые кожные пробы используются широко, для получения их результатов обычно требуется 2-3 дня, часто результаты бывают ошибочны из-за ложноположительных результатов, которые иногда наблюдают у пациентов, которые подвергались воздействию микобактериальной инфекции, но при этом здоровы. Кроме того, часто встречаются случаи ошибочного диагностирования, так как положительный результат наблюдается не только у пациентов с активной формой ТБ, но также и у людей,привитых бациллами Кальметта-Герена (BCG), и у людей, зараженных микобактериями, но у которых болезнь не развивается. Поэтому с помощью туберкулиновой пробы трудно отличить пациентов с активной формой ТБ от других, например от пациентов, контактирующих с зараженными ТБ на бытовом уровне. Кроме того, туберкулиновая проба часто дает перекрестную реакцию у тех пациентов, которые инфицированы иными микобактериями, чем М.tuberculosis (MOTT). Таким образом, доступное в настоящее время диагностирование с использованием кожных проб часто дает ошибки и неточности. Обычное лечение туберкулеза, вызванного чувствительными к лекарственному препарату бактериями, представляет собой шестимесячный курс, включающий введение четырех препаратов, назначаемых в течение 2 месяцев, а затем двух препаратов, назначаемых в течение 4 месяцев. Двумя самыми важными препаратами, назначаемыми на протяжении шестимесячного курса, являются изониазид и рифампин. Хотя курс относительно прост, его осуществление является весьма сложным. В течение первой фазы терапии часто требуется ежедневный прием восьми или девяти пилюль; пугающая и запутанная перспектива. Даже у пациентов в тяжелом состоянии после нескольких недель лечения часто исчезают симптомы, а через несколько месяцев им кажется, что они вылечились. Однако, если лечение не продолжается до полного завершения, у пациента может развиться рецидив, и вероятность рецидива у пациента,-2 016659 не прошедшего полный курс лечения, является высокой. Для того чтобы обеспечить строгое соблюдение курса лечения, используются различные виды помощи, ориентированной на пациента. Самым эффективным способом, гарантирующим лечение пациентов, является контролируемая терапия, которая заключается в том, что член медицинской бригады следит за приемом пациентом каждой дозы каждого препарата. Контролируемая терапия может осуществляться в клинике, по месту жительства пациента или в любом месте, определяемом по взаимному согласию. Почти все больные туберкулезом, вызванным бактериями, чувствительными к лекарственным препаратам, которые прошли полный курс лечения, будут вылечены и риск рецидива у них очень низкий ("Ending Neglect: The Elimination of Tuberculosis in theHealth Promotion and Disease Prevention, Institute of Medicine. Неопубликовано). Необходимы эффективные курсы лечения, которые включают в себя усовершенствованную вакцинацию и протоколы лечения. Доступные на сегодняшний день способы лечения не всегда эффективны из-за трудностей с проведением полного курса лечения, и эти трудности способствуют появлению штаммов микобактерий, устойчивых к действию лекарственных препаратов. Этамбутол (ЕМВ) представляет собой антибиотик, широко применяющийся для лечения ТБ, более 300 миллион доз которого было использовано для лечения туберкулеза в 1988 г. Этамбутол, разработанный лабораториями Lederle Laboratories в 1950-х гг., обладает низкой токсичностью и хорошими фармакокинетическими свойствами. Однако этамбутол имеет относительно высокую минимальную ингибирующую концентрацию (MIC), приблизительно 5 мкг/мл и может вызывать неврит зрительного нерва. Поэтому существует возрастающая необходимость в новых, более эффективных терапевтических композициях (см., например, патенты США 3176040, 4262122, 4006234,3931157, 3931152, Re. 29358 и Hausler et al., BioorganicMedicinal Chemistry Letters. 11 (2001), 16791681). 3a десятилетия после обнаружения лечебных эффектов этамбутола был достигнут небольшой прогресс в фармакологическом лечении ТБ. Более того, в связи с одновременным появлением штаммов, устойчивых к лекарственным препаратам, и большим распространением микобактериальной инфекции стало очевидным, что наиболее значимыми в борьбе против туберкулеза являются новые терапевтические композиции. Необходимы абсолютно эффективные курсы лечения, которые включают в себя усовершенствованную вакцинацию и протоколы лечения. Желательно получение терапевтической вакцины, которая могла бы предотвратить появление туберкулеза и, таким образом, исключить необходимость лечения. Хотя в настоящее время доступные терапевтические средства, такие как этамбутол, являются эффективными,появление штаммов, устойчивых к лекарственным препаратам требует разработки новых фармацевтических препаратов и композиций, более универсальных, чем этамбутол. В данный момент доступные терапевтические средства не всегда эффективны из-за сложностей проведения полного курса лечения, делая возможным появлением штаммов микобактерий, устойчивых к лекарственным препаратам. Необходимы новые противотуберкулезные препараты, которые обеспечат высокоэффективное лечение и сократят или упростят химиотерапию при туберкулезе. Сущность изобретения Настоящее изобретение относится к соединениям этилендиамина, способам и композициям, содержащим соединения этилендиамина, эффективные для лечения инфекционного заболевания. Настоящее изобретение также относится к способам и композициям, содержащим соединения этилендиамина, обладающего улучшенной активностью против микобактерий, включая замещенные этилендиамины, обладающие улучшенной противотуберкулезной активностью. Настоящее изобретение охватывает замещенные этилендиамины, которые могут быть производными различных аминосоединений. В настоящем изобретении замещенные этилендиамины основаны на следующей структуре. Замещенные производные этилендиамина, описанные здесь, синтезированы и подвергнуты скринингу на их активность следующим образом. Химическую библиотеку замещенных этилендиаминов получали на твердой полистирольной подложке, используя методы смешения и разделения. Этот метод-3 016659 позволяет синтезировать разнообразные замещенные этилендиамины. Эти диамины подвергают скринингу на противотуберкулезную активность, используя биологические анализы in vitro, включая технологию высокоэффективного скрининга (HTS), основанную на недавно расшифрованной геномной последовательности M.tuberculosis, и анализе минимальной ингибирующей концентрации (MIC). Способы и композиции, описанные здесь, включают замещенные этилендиамины, которые являются эффективными в отношении заболевания, вызванного инфекционными организмами, включая, но не ограничиваясь, бактерии и вирусы. Один из вариантов осуществления данного изобретения относится к способам и композициям, содержащим замещенные этилендиамины, которые являются эффективными в отношении микобактериальной инфекции. Другой вариант осуществления изобретения относится к способам и композициям, содержащим замещенные этилендиамины, для лечения микобактериального заболевания, которые имеют MIC, равную 50 мкМ или меньше. Другой вариант осуществления настоящего изобретения относится к замещенным этилендиаминам для лечения микобактериальной инфекции, имеющим MIC 25 мкМ или меньше. Еще один вариант осуществления настоящего изобретения относится к замещенным этилендиаминам для лечения микобактериальной инфекции, имеющим MIC 12,5 мкМ или меньше. Другой вариант осуществления настоящего изобретения относится к замещенным этилендиаминам для лечения микобактериальной инфекции,имеющим MIC 5 мкМ или меньше. В другом варианте осуществления настоящего изобретения способы и композиции содержат замещенные этилендиамины с активностью Luc HTS, равной 10% или больше. В еще одном варианте осуществления настоящего изобретения способы и композиции содержат замещенные этилендиамины, где одна аминогруппа является производным первичного амина, а другая аминогруппа является производным первичного или вторичного амина. Настоящее изобретение охватывает различные комплексы солей и другие замещенные производные замещенных этилендиаминов. Настоящее изобретение также охватывает энантиомеры и другие стереоизомеры замещенных этилендиаминов и их замещенных производных. Настоящее изобретение также включает в себя лечение животных, включая, но этим не ограничиваясь, людей. Соответственно, объектом настоящего изобретения являются способы и композиции для лечения и профилактики заболеваний, вызванных инфекционными агентами. Соответственно, объектом настоящего изобретения являются способы и композиции для лечения и профилактики инфекционных заболеваний. Другим объектом настоящего изобретения являются способы и композиции для лечения и профилактики микобактериальной инфекции, включая, но этим не ограничиваясь, туберкулез. Еще одним объектом настоящего изобретения являются способы и композиции для лечения и профилактики инфекционных заболеваний, использующие композиции, содержащие замещенные этилендиамины. Другим объектом настоящего изобретения являются способы и композиции для лечения и профилактики микобактериальной инфекции, использующие композиции, содержащие замещенные этилендиамины. Еще одним объектом настоящего изобретения являются способы и композиции для лечения и профилактики туберкулеза, использующие композиции, содержащие замещенные этилендиамины. Другим объектом настоящего изобретения являются способы и композиции для лечения и профилактики туберкулеза, использующие композиции, содержащие замещенные этилендиамины, где диамин имеет MIC, равную 50 мкМ или меньше. Другим объектом настоящего изобретения являются способы и композиции для лечения и профилактики туберкулеза, использующие композиции, содержащие замещенные этилендиамины, где диамин имеет MIC, равную 2 5 мкМ или меньше. Другим объектом настоящего изобретения являются способы и композиции для лечения и профилактики туберкулеза, использующие композиции, содержащие замещенные этилендиамины, где диамин имеет MIC, равную 12,5 мкМ или меньше. Другим объектом настоящего изобретения являются способы и композиции для лечения и профилактики туберкулеза, использующие композиции, содержащие замещенные этилендиамины, где диамин имеет MIC, равную 5 мкМ или меньше. Еще одним объектом настоящего изобретения являются способы и композиции для лечения и профилактики туберкулеза, использующие композиции, содержащие замещенные этилендиамины, где диамин имеет активность HTS/Luc, равную 10% или больше. Еще одним объектом настоящего изобретения являются композиции для терапевтического препарата для лечения и профилактики микобактериальной инфекции. Другим объектом настоящего изобретения являются композиции для терапевтического препарата для лечения и профилактики микобактериальной инфекции, вызванной М.tuberculosis complex,М.avium intracellulare, M.kansarii, M.fortuitum, M.chelonae, М.leprae, M.africanum, M.Microti, M.arium-4 016659 Эти и другие объекты, особенности и преимущества настоящего изобретения будут понятны после рассмотрения следующего далее подробного описания вариантов осуществления и прилагаемой формулы изобретения. Краткое описание чертежей На фиг. 1 показаны характерные примеры диаминовых продуктов, синтезированных из полимеров с предварительно введенным аминоспиртом. На фиг. 2 изображены коммерчески доступные полимеры предварительно введенным аминоспиртом. На фиг. 3 представлена табл. 2, которая показывает полученную библиотеку 21120 заданных аналогов этамбутола. На фиг. 4 представлена схема 1, на которой схематически показан синтез основных 100000 соединений библиотеки аналогов этамбутола. На фиг. 5 представлена схема 2, на которой схематически показано использование полимеров с предварительно введенным аминоспиртом и аминокислоты в качестве линкера. На фиг. 6 представлена схема 3, на которой схематически показаны дополнительные модификации линкера: применение полимеров с предварительно введенным аминоспиртом. На фиг. 7 представлена табл. 3, в которой перечислены аминокислоты, использующиеся при получении библиотеки. На фиг. 8 представлены характерные карбонильные соединения, использующиеся в качестве реагентов в синтезе. На фиг. 9 представлены характерные примеры данных MIC и Lux. На фиг. 10 показан список наиболее эффективных соединений и их структуры. На фиг. 11 показана табл. 4, в которой представлено расположение при разделении. Подробное описание изобретения Настоящее изобретение будет более понятно после рассмотрения следующего далее подробного описания приведенных здесь конкретных осуществлений. Однако, хотя настоящее изобретение описано со ссылками на конкретные детали некоторых его осуществлений, эти детали не следует рассматривать как ограничивающие объем данного изобретения. Текст указанных здесь ссылок включен в полном объеме, включая предварительную патентную заявку США 60/381224, поданную 17 мая 2002 г., и патентную заявку США 10/147587, поданную 17 мая 2002 г. Заболеваемость микобактериальными инфекциями, такими как инфекции, вызывающие туберкулез,которая, как казалось, уменьшилась, снова увеличивается и составляет серьезную угрозу для здоровья. Туберкулез (ТБ) является наиболее частой причиной смерти людей при заражении одним этилогическим агентом, ежегодно умирает от двух до трех миллионов человек, зараженных туберкулезом. В местах скопления большого числа людей или местах проживания в помещениях, не соответствующих стандартам проживания, все чаще можно обнаружить лиц, страдающих микобактериальной инфекцией. Люди с пораженной иммунной системой подвержены большему риску заражения микобактериальной инфекцией и гибели от нее. Кроме того, появление штаммов микобактерий, устойчивых к лекарственным препаратам,привело к трудностям лечения таких инфицированных людей. Много людей, зараженных микобактериями, являются бедными или проживают в областях с ограниченными медицинскими возможностями. В результате различных проблем (экономические проблемы,низкий уровень образования и т.п.), многие из этих индивидуумов неспособны соблюдать предписанный курс лечения. В конечном счете, постоянное несоблюдение этими и другими индивидуумами курса лечения привело к распространению болезни. Такое несоблюдение курса лечения часто приводит к возникновению штаммов микобактерий, устойчивых к лекарственным препаратам. Необходимы эффективные композиции и вакцины, направленные на различные штаммы микобактерий, для увеличения числа подавляемых случаев туберкулеза. Химиотерапия является обычным способом лечения туберкулеза. В настоящее время при некоторых используемых способах химиотерапии требуется сочетание трех или четырех препаратов, вводимых ежедневно в течение двух месяцев, или введение два раза в неделю в течение от четырех до двенадцати месяцев. В табл. 1 показано несколько схем лечения при стандартных курсах лечения туберкулеза.-5 016659 Таблица 1 Схемы лечения при стандартных курсах лечения туберкулеза Десятилетия неправильного приема существующих антибиотиков и недостаточное соблюдение длительных и сложных курсов лечения привели к мутациям микобактерии туберкулеза и возникновению эпидемии туберкулеза, устойчивого к лекарственным препаратам, которая угрожает контролю над туберкулезом во всем мире. В период 1950-1970-хх годов было разработано огромное количество использующихся в настоящее время лекарственных препаратов, включая наиболее активно применяемые препараты, такие как изониазид, рифампин, пиразинамид, этамбутол и стрептомицин. Таким образом, ранее разработанная химиотерапия туберкулеза не использует участие геномной последовательности Mycobacterium tuberculosis, революцию, свершившуюся в последние десять лет в разработке фармацевтических препаратов, и применение национальных программ тестирования лекарств и комбинаторной химии. Следовательно, для лечения больных со штаммами М.tuberculosis, устойчивых к действию лекарственного препарата, и скрытыми туберкулезными инфекциями требуются новые противотуберкулезные препараты, которые обеспечивают высокоэффективное лечение и сокращают и упрощают химиотерапию туберкулеза. Кроме того, желательно, чтобы эти препараты можно было бы синтезировать недорогим способом, так как демографические данные болезни показывают, что стоимость является существенным фактором. Настоящее изобретение относится к этилендиаминовым соединениям, способам и композициям,содержащим класс замещенных этилендиаминовых соединений, эффективных для лечения и профилактики заболевания, вызванного микроорганизмами, включая, но не ограничиваясь, бактерии. В частности,способы и композиции по настоящему изобретению эффективны для ингибирования роста микроорганизмов М.tuberculosis. Способы и композиции по настоящему изобретению предназначены для лечения микобактериальных инфекций у человека, а также животных. Например, настоящее изобретение может, в частности, использоваться для лечения коров, инфицированных М.bovis. Как используется здесь, термин "туберкулез" включает в себя заболевания, обычно связанные с инфекциями, вызванными видами микобактерий, включая M.tuberculosis comlex. Термин "туберкулез" также связан с микобактериальными инфекциями, вызванными микобактериями, исключая М.tuberculosis (MOTT). Другие виды микобактерий включают в себя М.avium intracellulare, M.kansarii, M.fortuitum,M.chelonae, M.leprae, M.africanum и М.microti, M.avium paratuberculosis, М.intracellulare, M.scrofulaceum,M.xenopi, M.marinum, M.ulcerans. Настоящее изобретение, кроме того, относится к способам и композициям, эффективным для лечения инфекционного заболевания, включая, но ими не ограничиваясь, заболевания, которые вызваны бактериальными, микологическими, паразитическими и вирусными агентами. Примеры таких инфекционных агентов включают в себя стафилококки, стрептококки, нейссерии, кокки, энтеробактерии, псевдомонады, вибрионы, кампилобактер, представители семейства Pasteurellaceae, бордетелла, франциселла,бруцелла, легионеллы, бактероиды, грамотрицательные бациллы, клостридии, коринебактерии, пропионобактерии, грамположительные бациллы, бациллу сибирской язвы, актиномицеты, нокардии, микобактерии, трептонему, борелии, лептоспиру, микоплазму, уреплазму, риккетсии, хламидии, системные микозы, оппортунистические микозы, протозоя, нематоды, трематоды, цестодии, аденовирусы, вирусы герпеса, поксвирусы, паповирусы, вирусы гепатита, ортомиксовирусы, парамиксовирусы, коронавирусы,пикорнавирусы, реовирусы, тогавирусы, флавивирусы, бунья-вирусы, рабдовирусы, вирусы иммунодефицита человека и ретровирусы. Настоящее изобретение также относится к способам и композициям, которые эффективны для лечения инфекционного заболевания, включая, но ими не ограничиваясь, туберкулез, лепру, болезнь Крона, синдром приобретенного иммунодефицита, болезнь Лима, болезнь от кошачьих царапин, пятнистую лихорадку скалистых гор и грипп.-6 016659 Второе поколение антибиотиков на основе этамбутола. Настоящее изобретение, в частности, относится к новой библиотеке диаминовых соединений семейства этамбутола, содержащих модифицированный этиленовый мостик, получаемой из коммерчески доступных полимеров с предварительно введенным аминоспиртом. С тем чтобы увеличить структурное разнообразие библиотеки аналогов этамбутола и оценить влияние модифицированного линкера на активность диаминов, разнообразных по своей структуре, против М.tuberculosis, схема синтеза введения аминокислоты в связывающий линкер между двумя аминокомпонентами была изменена. Используемые аминокислоты представляли интерес, так как делали возможным введение другого элемента разнообразия в линкер (такой как R4), а также изменяли хиральность. Для поставленной задачи было важно синтезировать подбиблиотеку диаминов, очень похожих на этамбутол по наличию аминоспиртовой группы в молекуле и отличающихся по наличию сложного линкера между двумя атомами амина (см. фиг. 1 характерных примеров). Кроме того, тот факт, что 2-хлортритиловые полимеры с предварительно введенными аминоспиртами являются коммерчески доступными (фиг. 2) и хорошо подходят для предложенной химической структуры, является очень привлекательным. Соединения в библиотеке получали в миллимолярном масштабе в 96-луночном формате в смеси 10 соединений в лунке (для большинства плашек). В табл. 2 (фиг. 3) суммированы данные для плашек, в которых проходит синтез. Твердофазный синтез с использованием полимеров, предварительно насыщенных аминоспиртом. Получали двадцать 96-луночных плашек. Четвертую и пятую стадии синтеза, начинающегося с коммерчески доступных полимеров с предварительно введенным аминоспиртом, сходных с теми, которые использовались для создания первой библиотеки из 100000 соединений (схема 1, фиг. 4), использовали для получения заданных диаминов (схемы 2 и 3, фиг. 5 и 6 соответственно). Этот синтез имел некоторые отличия: (1) две первые стадии схемы 1 отсутствовали в схемах 2 и 3; (2) в схеме 1 второй амин вводили в молекулу как целый синтон путем нуклеофильного замещения функциональной группы Cl линкера, тогда как в схеме 2 и 3 получение второго амина осуществляли путем модификации существующей аминогруппы с помощью карбонильных соединений. Схема 2. Ацилирование приобретенного 2-хлортритилового полимера с предварительно введенным аминоспиртом, осуществляли путем взаимодействия пептида с Fmoc-защищенными аминокислотами в присутствии HATU (гексафторфосфат О-(7-азабензотриазол-1-ил)-N,N,N,N-тетраметилурония) иEtN(изо-Pr)2 в смеси DCM/ДМФ при комнатной температуре. Взаимодействие проводили дважды для большего выхода продуктов. Список аминокислот, используемых для создания этой библиотеки, показан в табл. 3 (фиг. 7). Снятие защиты (удаление группы Fmoc) проводили реакцией с пиперидином при комнатной температуре. Преобразование аминогруппы достигалось восстановительным алкилированием с 96 различными карбонильными соединениями, такими как альдегиды, кетоны и карбоновые кислоты, в присутствииNaBCNH3 при комнатной температуре в течение 72-96 ч. Выбор карбонильных соединений осуществляли таким образом, чтобы конечные диаминовые продукты могли бы нести одинаковые или сходные типы заместителей, которые наблюдали у наиболее эффективных соединений, полученных в предыдущей библиотеке аналогов этамбутола, а также обладать структурным разнообразием (фиг. 8). Полный список использованных карбонильных соединений приведен в табл. 4. Восстановление аминоэтиленамидов до соответствующих диаминов осуществляли, используя растворимый восстановительный агент 65 + мас.% Red-Al при комнатной температуре. Отделение продуктов от полимера проводили с помощью 10% раствора трифторуксусной кислоты в дихлорметане с получением соли ТФУ диаминов.-7 016659 Для получения библиотеки стадию ацилирования в схеме синтеза осуществляли, используя синтезатор Quest 210 с массой полимера в каждой пробирке, равной 0,1-0,15 г. После взаимодействия полученные полимеры тщательно промывали, сушили и затем объединяли группы из десяти полимеров. Небольшое количество каждого полимера (0,05 г) архивировали до смешивания для облегчения повторного синтеза и разделения архивов. Удаление защитной группы Fmoc, добавление карбонильного компонента, восстановление и отделение осуществляли в 96-луночных реакционных блоках, используя систему Combiclamps от WhatmanPolyfiltronics или систему FlexChem от Robbins Scientific. Суспензию объединенных полимеров в смеси 2:1 DCM/ТТФ поровну распределяли в одну из реакционных плашек с получением приблизительно 10 мг полимера на лунку. 96 различных карбонильных соединений помещали в одну из 96-луночных плашек с образцами и добавляли одно карбонильное соединение на лунку, в каждую отдельную смесь десяти полимеров, с получением запланированных 960 диаминов на плашку. Восстановление осуществляли в том же формате, а после отделения и фильтрации в плашки для хранения проводили упаривание ТФУ перед биологическим анализом. Оценку качества полученной библиотеки диаминов проводили с помощью масс-спектрометрии с ионизацией распылением, используя два наугад выбранных ряда (16 образцов) на плашку, с общим количеством 17%. Успешное получение соединения основывалось на образовании молекулярного иона рассчитанной массы. В зависимости от использованной в синтезе аминокислоты регистрировали процент заранее вычисленных ионов и таким образом получали прогнозированные соединения с выходом в интервале от 31 до 96% (табл. 2, фиг. 3). На основании MS анализа из запланированных 15360 соединений на самом деле образовывалось 7500 диаминов. Аминокислоты, такие как аминометилциклогексилкарбоновая кислота, тиенилаланин или фенилаланин, давали желаемые соединения с хорошим выходом(88-96%). В то же время некоторые аминокислоты, такие как аргинин, тетрагидроизохинолинкарбоновая кислота и тиазолидинкарбоновая кислота, не давали соответствующих продуктов. Схема 3. Успех в получении аналогов этамбутола с модифицированным линкером способствовал попытке синтеза другой суббиблиотеки диаминов c использованием коммерчески доступных полимеров с предварительно введенным аминоспиртом (схема 3, фиг. 6). Этот путь обеспечивает выход соединений диаминов, которые сходны с соединениями, полученными по схеме 2, фиг. 5, а также обладали желаемыми заместителями на первом атоме азота. Авторами был проиллюстрирован этот способ, в котором исходными продуктами являются коммерчески доступные полимеры с предварительно введенным 1,4-аминобутанолом. Были получены пять плашек с использование пяти аминокислот Phe, Amc, Cha, Trp и Inp (табл. 2), которые давали наилучшие предварительные результаты в анализах скрининга (см. номер наиболее эффективных соединений в табл. 2). Самой первой стадией была стадия получения производных аминогруппы посредством восстановительного алкилирования с помощью 10 карбонильных соединений (циклооктанон,4-бензилоксибензальдегид, (S)-цитронеллал, миртенал, тетрагидро-4 Н-пиран-4-он, норкамфор,4-(4-гидроксифенил)-2-бутанон, геранилацетон, 2-декалон, 2-адамантанон) в присутствии NaBCNH3 при комнатной температуре. Следующие стадии осуществляли тем же способом, как описано ранее для схемы 2. Скрининг библиотеки на активность против M.tuberculosis и разделение активных смесей. Для скрининга новой библиотеки соединений аналогов этамбутола использовали высокоэффективный анализ с рекомбинантной микобактерией, содержащей комплекс промотор/люцифераза Rv0341, а также MIC, фиг. 9. Для разделения было отобрано 198 смесей соединений, обладающих противотуберкулезной активностью, табл. 2 (активность при 12,5 мкМ при HTS Luc-анализе и/или значение MIC 12,5 мкМ). Разделение всех 198 смесей соединений осуществляли путем отдельного повторного синтеза соединений диамина в 96-луночном формате, используя сохраненный архив полимеров (по их объединению) и тот же путь синтеза, как в схемах 2 и 3. Для каждой плашки, в которой проводили разделение, использовали те же способы скрининга. Несколько карбонильных соединений были идентифицированы как эффективные синтоны, способствующие противотуберкулезной активности (фиг. 5). Проведение разделения давало 118 эффективных соединений с новой структурой, которые являются противотуберкулезными соединениями (фиг. 10, табл. 4), для 38 из этих соединений активность была доказана в обоих анализах. В табл. 4 (фиг. 10) перечислены наиболее эффективные соединения и их структуры. Композиции. Терапевтические композиции, включая композиции, содержащие замещенные производные этилендиамина по настоящему изобретению, могут быть получены в физиологически приемлемых смесях,например в смеси с фармацевтически приемлемыми носителями, с использованием известных способов. Например, замещенное производное этилендиамина объединяют с фармацевтически приемлемым эксципиентом с образованием терапевтической композиции.-8 016659 Композиции по настоящему изобретению могут вводиться в твердой, жидкой форме или в виде аэрозоля. Примеры твердых композиций включают в себя пилюли, кремы, мыла и имплантируемые лекарственные формы. Пилюли могут вводиться перорально. Лечебные кремы и противомикобактериальные мыла могут наноситься местно. Имплантируемые лекарственные формы могут вводиться локально, например в легкие, или могут имплантироваться для системного действия терапевтической композиции,например подкожно. Примеры жидких композиций включают в себя препараты, подходящие для внутримышечной, подкожной, внутривенной, внутриартериальной инъекции и препараты для местного нанесения и введения в глаза. Примеры аэрозольных композиций включают в себя ингаляторные препараты для введения в легкие. Материал, обеспечивающий продолжительное высвобождение, как используется здесь, представляет собой материал, сделанный из веществ, обычно полимеров, разрушающихся под действием ферментов или кислого/основного гидролиза или растворяющихся. При введении в организм материал подвергается действию ферментов или жидкостей организма. Материал, обеспечивающий продолжительное высвобождение, по желанию, выбран из биосовместимых веществ, включая, но ими не ограничиваясь, лизосомы,полилактиды, поликликолид (полимер гликолевой кислоты), полилактид со-гликолид (сополимеры молочной кислоты и гликолевой кислоты), полиангидриды, сложные поли(орто)эфиры, полипептиды, гиалуроновую кислоту, коллаген, хондроитин сульфат, карбоновые кислоты, жирные кислоты, фосфолипиды, полисахариды, нуклеиновые кислоты, полиаминокислоты, аминокислоты, такие как фенилаланин,тирозин, изолейцин, полинуклеотиды, поливинилпропилен, поливинилпирролидон и силикон. Предпочтительным биоразлагаемым материалом является материал, который является либо полилактидом, либо поликликолидом, либо полилактид со-гликолидом. Доза композиции будет зависеть от состояния, при котором проводится лечение, конкретной используемой композиции и других клинических факторов, таких как масса и состояние пациента, и пути введения. Походящие уровни доз могут находиться в диапазоне от 100 до 0,1 мг/кг, более предпочтительно от 50 до 0,2 мг/кг, более предпочтительно от 25 до 0,5 мг/кг. Таблетки или другие формы средства могут содержать от 1 до 1000 мг замещенного этилендиамина. Могут использоваться уровни доз и схема приема, сходная с уровнями доз и схемой приема этамбутола или других противотуберкулезных препаратов. Композиция может вводиться в сочетании с другими композициями и процедурами лечения других заболеваний, существующих наряду с микобактериальной инфекцией. Например, часто туберкулез встречается как вторичное осложнение, связанное с синдромом приобретенного иммунодефицита(СПИДом). Лечение больных направлено на лечение СПИДа, которое включает в себя такие процедуры,как хирургическое вмешательство, облучение или химеотерапия, может быть более эффективным при применении терапевтических способов и композиций, описанных здесь. Следующие конкретные примеры иллюстрируют данное изобретение применительно к конкретным схемам синтеза замещенных производных этилендиамина и демонстрируют in vitro и in vivo подавление роста колоний М.tuberculosis. Кроме того, способы, описанные R. Lee et al. J. Comb. Chem. 2003, 5, 172187, приведены здесь в качестве ссылки в своем полном объеме. Специалисту в данной области будет очевидно, что существуют другие примеры, в том числе с незначительными модификациями химических процедур, и что изобретение не ограничивается этими конкретными примерами, приведенными в качестве иллюстрации. Пример 1. Получение библиотеки диамина из коммерчески доступных полимеров, предварительно насыщенных аминоспиртом. Общие способы. Все агенты были закуплены у фирмы Sigma-Aldrich. Полимеры, предварительно насыщенные аминоспиртом, были закуплены у фирмы NovaBiochem. Растворители ацетонитрил, дихлорметан, диметилформамид, этилендихлорид, метанол и тетрагидрофуран были закуплены у фирмы Aldrich и использовались в том виде, в котором были получены. Твердофазный синтез осуществляли на синтезаторе QUEST 210 (Argonaut Technologies) и с помощью оборудования комбинаторной химии (Whatman Polyfiltronicsand Robbins Scientific). Упаривание растворителей осуществляли с помощью Speed Vac AES (Savant). Данные масс-спектрометрии получали путем ионизации распылением, Perkin Elmer/Sciex, API-300,TQMS с автоматической пипеткой. Схема 2. Описание способа. Стадию ацилирования проводили в 5-миллилитровых пробирках, при этом использовался синтезатор Quest 210. Удаление Fmoc группы, реакцию восстановительного алкилирования с карбонильными соединениями, восстановление с помощью Red-Al и отделение от твердой фазы осуществляли в 96 луночных (объем каждой лунки равен 2 мл) химически устойчивых плашках.-9 016659 Стадия 1. Ацилирование полимеров, предварительно насыщенных аминоспиртом, аминокислотами. Каждую пробирку с 0,150 г соответствующего полимера (в интервале 0,3-1,0 ммоль/г) и все полимеры заранее оставляли набухать в DCM в течение 1,5 ч и фильтровали. Если использовались полимеры,защищенные группами Fmoc, полимер перемешивали с 2,5 мл 20% раствора пиперидина в ДМФ в течение 10 мин, фильтровали и промывали 2,5 мл ДМФ. Процедуру повторяли, но время перемешивания составляло 20 мин. После этого все полимеры фильтровали, промывали ДМФ (12,5 мл) и DCM (23 мл). В каждую пробирку помещали 1 мл дихлорметана. Аминокислоты, 0,38 ммоль в 1 мл ДМФ (2,5 молярный избыток для насыщения полимера), смешивали с HATU, 0,3 ммоль, 011 г в 0,5 мл ДМФ (2 молярный избыток для насыщения полимера), и оставляли на 15-20 мин. Затем в каждую пробирку добавляли 1,5 мл смеси кислота-HATU, после чего добавляли раствор 1,5 ммоль, 0,26 мл (10 молярный избыток для насыщения полимера) EtNPr2 в 0,5 мл дихлорметана. Взаимодействие осуществляли в течение 8 ч при 45 С и в течение 6-8 ч при комнатной температуре. После завершения реакции полимеры фильтровали,промывали смесь 1:1 ДМФ и дихлорметана (13 мл) дихлорметаном (13 мл) и ацилирование повторяли с теми же количествами реагентов. В конце полимеры фильтровали, промывали смесью 1:1 ДМФ и дихлорметана (13 мл) метанолом (33 мл), отсасывали жидкость досуха (на Quest) в течение 30 мин и переносили в пузырьки (один полимер на пузырек) и сушили в испарителе под вакуум в течение 1 ч. После этой стадии все полимеры подвергали качественному контролю с помощью MS спектра. Стадия 2. Алкилирование аминогруппы. Удаление защиты. 10 полимеров, полученных в первых трех стадиях, объединяли, оставляя приблизительно 0,03 г каждого в отдельных пузырьках для нужд разделения. Суспензию смеси полимеров (0,08-1,0 г) в 100 мл смеси 2:1 дихлорметана и ТГФ распределяли в две 96-луночные плашки, оснащенные фильтром, и фильтровали, используя устройство для фильтрации. Реакционные плашки переносили на держатель и для удаления защитной Fmoc группы добавляли 0,2 мл 20% раствора пиперидина в ДМФ и оставляли на 10 мин. Через 10 мин плашку фильтровали, промывали 0,2 мл ДМФ и удаление защиты повторяли, используя 0,2 мл 20% раствора пиперидина в ДМФ, и оставляли на 20 мин. После этого плашку фильтровали, промывали ДМФ (0,2 мл на лунку) и дихлорметаном (20,5 мл на лунку). Взаимодействие с карбонильными соединениями. В каждую лунку ряда А реакционной плашки помещали 0,1 мл дихлорметана, 0,08 мл 1,0 М раствора соответствующей кислоты в ДМФ из основной плашки, 0,05 мл раствора PyBrop в ДМФ (0,012 г,0,025 ммоль, 2,5 молярный избыток для насыщения полимера) и 0,05 мл EtNiPr2 в дихлорметане(0,017 мл, 0,10 ммоль, 10 молярный избыток для насыщения полимера). В каждую лунку ряда В-Н помещали 0,1 мл ТГФ, 0,160 мл 1,0 М раствора соответствующего альдегида или кетона в ДМФ из основной плашки и оставляли для взаимодействия в течение 30 мин. Через 30 мин добавляли 0,075 мл(0,075 ммоль) 1,0 М раствора NaBCNH3 в ТГФ. Реакционные плашки герметизировали и оставляли при комнатной температуре в течение 72 ч. В конце полимеры фильтровали, промывали ТГФ, DCM (11 мл),метанолом (21 мл) и сушили в испарители под вакуумом в течение 3 ч. Стадия 3. Восстановление с помощью Red-Al. Реакционные плашки помещали на держатель. Добавляли смесь 1:6 Red-Al (65 + мас.% в толуоле) и ТГФ, 0,6 мл на лунку (0,28 ммоль Red-Al на лунку) и оставляли для взаимодействия на 4 часа. После завершения взаимодействия полимеры фильтровали, промывали ТГФ (21 мл), метанолом (31 мл) и сушили в устройстве для фильтрации. Стадия 4. Отделение. Эту стадии осуществляли, используя устройство для отделения. В реакционные плашки (помещенные над плашками для сбора в этом устройстве) помещали смесь 10:88:2 ТФУ, дихлорметана и триизопропилсилана, 0,5 мл на лунку. Через 15 мин растворы фильтровали и собирали в соответствующие лунки плашки для сбора. Процедуру повторяли. Растворители упаривали на Speed vac, и образцы осадка были готовы к анализу. Схема 3. Описание способа. Стадию восстановительного алкилирования 4-аминобутан-1-ол полимера и стадию ацилирования проводили в 5-миллилитровых пробирках, используя синтезатор Quest 210. Удаление Fmoc группы, реакцию восстановительного алкилирования с карбонильными соединениями, восстановление с помощьюRed-Al и отделение от твердой фазы осуществляли в 96-луночных (объем каждой лунки равен 2 мл) химически устойчивых плашках.- 10016659 Стадия 1. Восстановительное алкилирование 4-аминобутан-1-ол полимера. Суспензию полимера (в интервале 0,3-1,0 ммоль/г), 1,0 г (до 1,0 ммоль) в 30 мл смеси 2:1 дихлорметан и ТГФ распределяли в 10 пробирок, 3 мл на пробирку, и фильтровали, затем в каждую пробирку помещали 0,10 г полимеров. Полимер заранее оставляли набухать в DCM в течение 1,5 ч и фильтровали. В каждую пробирку помещали 1,5 мл 1,2-дихлорэтана, 0,3 ммоль (3 молярный избыток) соответствующего альдегида или кетона (агент алкилирования) и оставляли для взаимодействия на 30 мин. После этого добавляли 0,3 ммоль (0,3 мл) 1 М раствора NaBCNH3 в ТГФ и взаимодействие проводили при комнатной температуре в течение 48 ч. После завершения взаимодействия все пробирки фильтровали, промывали ТГФ (23 мл), МеОН (33 мл) и жидкость досуха отсасывали (на Quest) в течение 30 мин. Стадия 2. Ацилирование аминокислотами. Все пробирки заранее дважды промывали DCM. В каждую пробирку добавляли 1 мл дихлорметана. Аминокислоты, 0,25 ммоль в 1 мл ДМФ (2,5 молярный избыток для насыщения полимера) смешивали сHATU, 0,2 ммоль, 0,076 г в 0,5 мл ДМФ (2 молярный избыток для насыщения полимеров) и оставляли на 15-20 мин. Затем в каждую пробирку добавляли 1,5 мл смеси кислота-HATU, после чего добавляли раствор 1,0 ммоль, 0,17 мл (10 молярный избыток для насыщения полимера) EtNiPr2 в 0,5 мл дихлорметана. Взаимодействие осуществляли в течение 8 ч при 45 С и в течение 6-8 ч при комнатной температуре. Через 16 ч полимеры фильтровали, промывали смесью 1:1 ДМФ и дихлорметана (13 мл), дихлорметана(13 мл) и ацилирование повторяли с тем же количеством реагентов. В конце полимеры фильтровали,промывали смесью 1:1 ДМФ и дихлорметана (13 мл), метанола (33 мл), досуха отсасывали жидкость(на Quest) в течение 30 мин и переносили в пузырьки (один полимер на пузырек) и сушили на испарителе под вакуумом в течение 1 ч. После этой стадии все полимеры подвергали качественному контролю с помощью MS спектра. Все последующие реакционные стадии, алкилирование аминогруппы (стадия 3), восстановление с помощью Red-Al (стадия 4) и расщепление (стадия 5), осуществляли таким же образом, как описано в схеме 2 данного описания. Пример 2. Разделение. Разделение активных лунок осуществляли повторным синтезом отдельных соединений из находящихся в архиве Fmoc-защищенных -аминоацетамидных полимеров (10 полимеров, 0,05-0,10 г каждый),которые оставляли в конце стадии ацилирования перед объединением. Каждому полимеру отводили отдельную колонку (1, 2, 3 и т.д.) в 96-луночной плашке, оснащенной фильтром, и разделяли между рядамиX (А, В, С и т.д.), где X представляет собой номер обнаруженных эффективных соединений в первоначальной скринированной плашке. В каждую лунку ряда добавляли выбранное карбонильное соединение(присутствует в эффективном соединении) и другие необходимые реагенты: первое выбранное карбонильное соединение добавляли к полимерам ряда "А", второе карбонильное соединение добавляли к полимерам ряда "В", третье карбонильное соединение добавляли к полимерам ряда "С" и т.д. Расположение в характерной 96-луночной плашке для разделения показано в табл. 4, фиг. 11. Реакционные плашки герметизировали и оставляли при комнатной температуре в течение 72 ч. В конце полимеры фильтровали, промывали ТГФ, DCM (11 мл), метанолом (21 мл) и сушили в испарителе под вакуумом в течение 2 ч. Восстановление и отделение осуществляли в соответствии со стадиями 5 и 6 схемы синтеза. Лунки с продуктами после отделения анализировали с помощью ESI-MS (массспектроскопия с ионизирующим распылением) для того, чтобы подтвердить выделение активных соединений, и анализировали с помощью анализа MIC. Твердофазный синтез выбранных замещенных этилендиаминов. Использование синтезатора Quest 210. Схема твердофазного синтеза, описанная выше для получения библиотеки производных диамина,использовалась для более масштабного синтеза выбранных замещенных производных этилендиамина. В данном случае все стадии реакции, начиная с ацилирования коммерчески доступных полимеров, заранее насыщенных аминоспиртом, и заканчивая отделением окончательного продукта, осуществляли только с помощью аппарата Quest, в котором одновременно можно проводить до двадцати реакций. Очищение всех сырых образцов выполняли с помощью флэш-хроматографии на CombiFlash (Isco, Inc.) с получением желаемых продуктов со степенью очистки больше 90%. В данном случае в качестве примера ниже описан синтез одного из активных соединений, 1-(2-[3-(4-хлорфенокси)бензил]амино-3 фенилпропил)пиперидин-4-ола. Характерный синтез активных соединений. Удаление защитной Fmoc группы. Коммерчески доступный полимер (N-FMOS-пиперидинил-4-окси)-(4-метоксифенил)метил полистирол, в области (линкер) 0,88 ммоль/г (0,4 г, 0,35 ммоль), помещали в одну из 10-миллилитровых пробирок синтезатора Quest 210. Добавляли раствор пиперидина (1,5 мл) в ДМФ (6 мл) и перемешивали в течение 30 мин, фильтровали, промывали ДМФ (16 мл) и снова добавляли пиперидин. Полимер промывали ДМФ (18 мл) и DCM (28 мл). Ацилирование Fmoc защищенным L-фенилаланином. Полимер еще раз промывали 5 мл DCM в течение 20 мин. Fmoc L-фенилаланин (0,0341 г,0,88 ммоль) в 1 мл ДМФ (2,5 молярный избыток для насыщения полимера) смешивали с HATU (0,33 г,0,88 ммоль) в 3 мл ДМФ и добавляли в пробирку, после чего добавляли раствор 0,6 мл EtNiPr2. Взаимодействие проводили при комнатной температуре в течение 20 ч. После завершения взаимодействия полимер фильтровали, промывали смесью 1:1 ДМФ и дихлорметана (16 мл), дихлорметаном (16 мл) и ацилирование повторяли с тем же количеством реагентов. В конце полимеры фильтровали, промывали смесью 1:1 ДМФ и дихлорметана (26 мл). Удаление защитной Fmoc группы. Раствор пиперидина (1,5 мл) в ДМФ (6 мл) добавляли к полимеру и полученную суспензию перемешивали в течение 30 мин, фильтровали, промывали ДМФ (16 мл) и еще раз добавляли пиперидин. Полимер промывали ДМФ (18 мл) и метанолом (28 мл) и жидкость досуха отсасывали в атмосфере Ar в течение 20 мин. Взаимодействие с карбонильным соединением. Полимер снова промывали ТГФ в течение 30 мин, фильтровали и помещали в 6 мл ТГФ. Добавляли 3-(4-хлорфенокси)бензальдегид (0,280 мл, 1,00 ммоль), после чего добавляли 1,0 М раствор NaBCNH3 в ТГФ (1 мл, 1 ммоль) через 30 мин. Реакционную смесь оставляли взаимодействовать при комнатной температуре в течение 72 ч. В конце полимер фильтровали, промывали ТГФ (16 мл) и МеОН (26 мл) и сушили в атмосфере Ar в течение 30 мин. Восстановление с помощью Red-Al. Полученный полимер в пробирке снова промывали безводным ТГФ (26 мл) и фильтровали. В сосуд добавляли 5 мл безводного ТГФ, после чего при перемешивании добавляли коммерчески доступныйRed-Al как 65+% в толуоле (1 мл, 3,2 ммоль). Через 4 ч полимер фильтровали, промывали ТГФ (21 мл) и МеОН (31 мл) (добавление МеОН необходимо осуществлять осторожно) и сушили в атмосфере Ar в течение 10 мин. Отделение. Для этой последней стадии синтеза в пробирку с полимерами помещали DCM (8 мл) и ТФУ (1 мл) и образовавшуюся ярко-красную суспензию оставляли перемешиваться в течение 30 мин. Полимер фильтровали и фильтрат собирали в пробирку, предназначенную для сбора фильтрата. Процедуру повторяли.DCM и избыток ТФУ упаривали на Speed vac. Сырой 1-(2-[3-(4-хлорфенокси)бензил]амино-3 фенилпропил)пиперидин-4-ол (в виде трифторацетата) очищали флэш-хроматографией на CombiFlash(600/400/10). Получали: 0,128 мг дитрифторацетата 1-(2-[3-(4-хлорфенокси)бензил]амино-3 фенилпропил)пиперидин-4-ола, выход 53%, со степенью очистки по крайней мере 95%. Масс-спектрометрия (ESI) m/z (MH)+ 451,2, 453,2. 2. Фармацевтическая композиция, содержащая соединение по п.1 и фармацевтически приемлемый носитель для лечения микобактериальной инфекции у человека или животного. 3. Фармацевтическая композиция по п.2, для наружного, перорального, подкожного, внутримышечного, внутриглазного, внутриартериального, внутривенного или локального применения с использованием имплантируемой единичной дозы 4. Фармацевтическая композиция по п.2, где композиция находится в жидкой форме или в виде аэрозоля. 5. Применение соединения по п.1 для изготовления лекарственного средства для лечения микобактериальной инфекции у человека или животного. 6. Применение по п.5, где микобактериальная инфекция представляет собой М.tuberculosis (МОТТ),М.avium intracellulare, M.kansarii, M.fortuitum, M.chelonae, M.leprae, M.africanum, M.bovis, M.microti,M.avium paratuberculosis, M.intracellulare, M.scrofulaceum, M.xenopi, M.Marinum или M.ulcerans. 7. Применение соединения по п.1 для лечения микобактериальной инфекции у человека или животного.
МПК / Метки
МПК: C07D 211/26, C07C 211/00, C07D 401/00, C07D 207/04, C07C 205/00
Метки: этилендиамина, инфекций, микобактериальных, производные, лечения
Код ссылки
<a href="https://eas.patents.su/30-16659-proizvodnye-etilendiamina-dlya-lecheniya-mikobakterialnyh-infekcijj.html" rel="bookmark" title="База патентов Евразийского Союза">Производные этилендиамина для лечения микобактериальных инфекций</a>
Предыдущий патент: Способ контроля состояния магистральных трубопроводов
Следующий патент: Способ лечения меланомы
Случайный патент: Способ и композиция для добычи углеводородов с искусственным поддержанием энергии пласта с очень высокой соленостью и высокой температурой