Замещённые гетероароилом фенилаланин-амиды
Номер патента: 11928
Опубликовано: 30.06.2009
Авторы: Мисслитц Ульф, Либл Рекс, Райнхард Роберт, Парра-Рападо Лилиана, Цагар Цирилл, Ракк Михаель, Плат Петер, Пуль Михаэль, Витшель Маттиас, Зиферних Бернд
Формула / Реферат
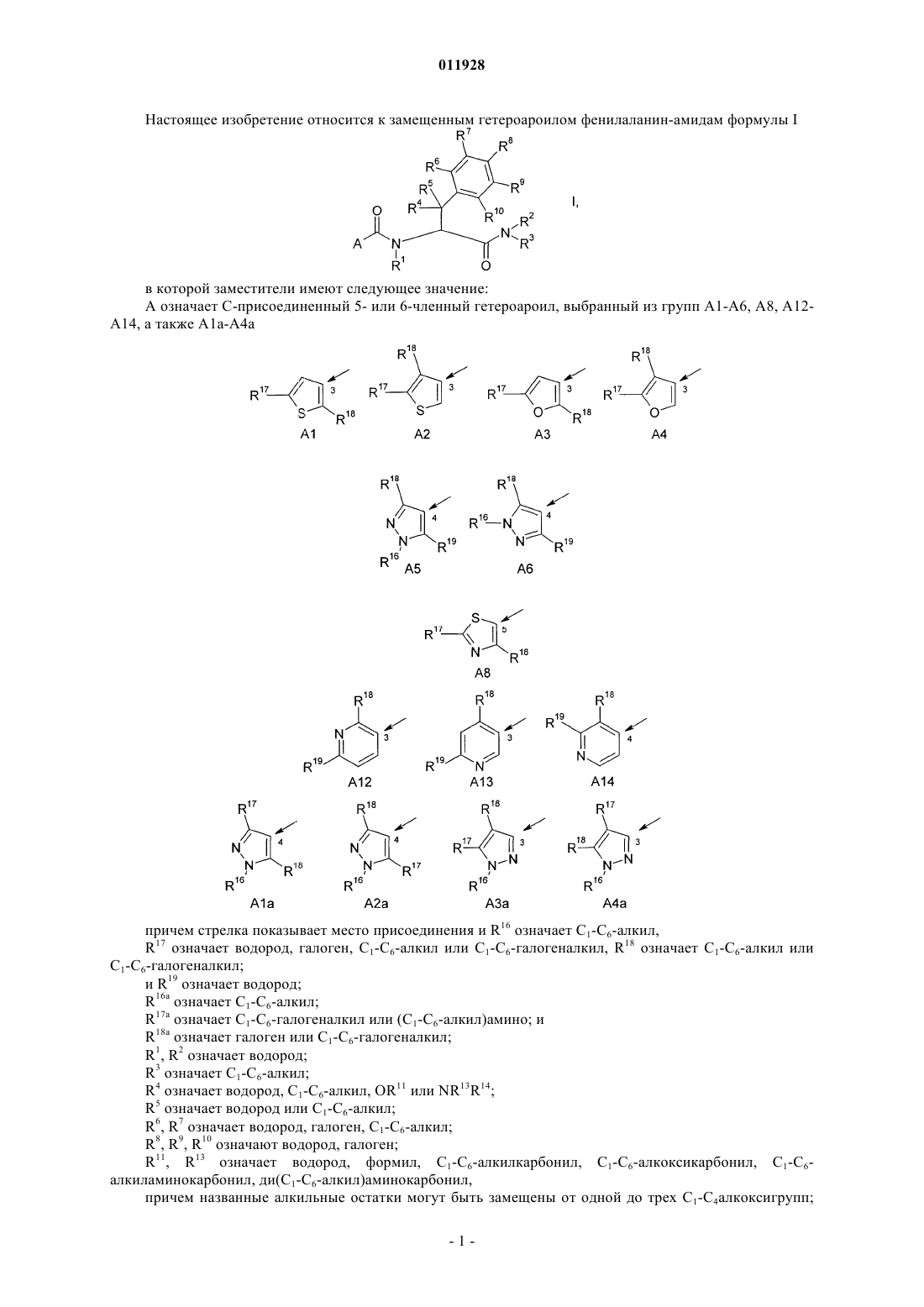
1. Замещенные гетероароилом фенилаланинамиды формулы I
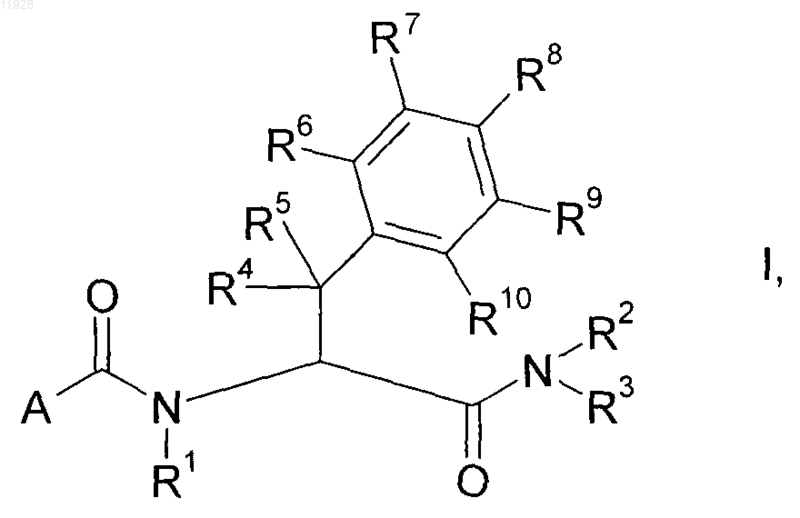
где переменные имеют следующие значения:
А означает С-присоединенный 5- или 6-членный гетероароил, выбранный из групп А1-А6, А8, А12-А14, а также А1а-А4а
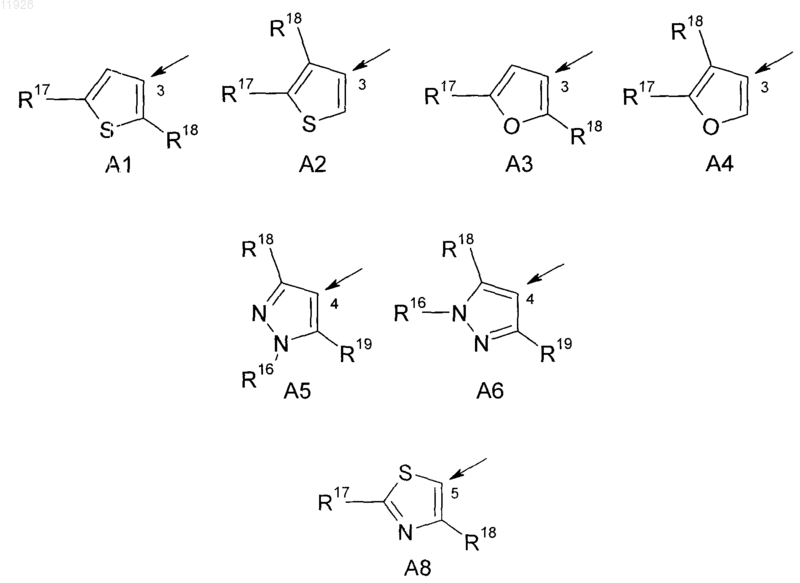
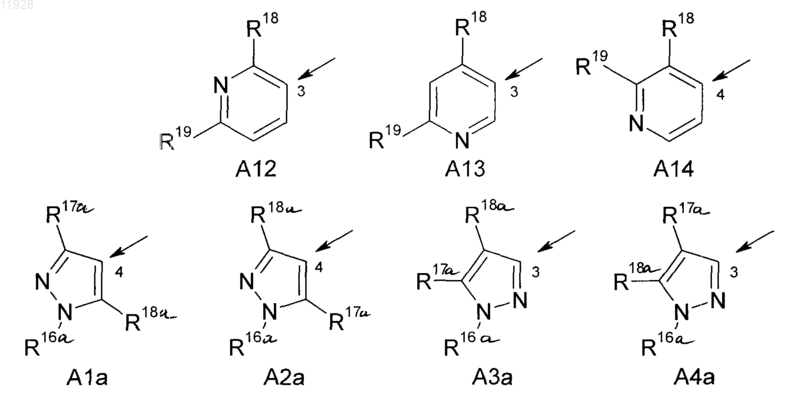
причем стрелка показывает место присоединения и
R16 означает C1-С6-алкил,
R17 означает водород, галоген, C1-С6-алкил или C1-С6-галогеналкил,
R18 означает C1-С6-алкил или C1-С6-галогеналкил; и
R19 означает водород;
R16a означает C1-С6-алкил;
R17a означает C1-С6-галогеналкил или (C1-С6-алкил)амино; и
R18a означает галоген или C1-С6-галогеналкил;
R1, R2 означает водород;
R3 означает C1-С6-алкил;
R4 означает водород, C1-С6-алкил, OR11 или NR13R14;
R5 означает водород или C1-С6-алкил;
R6, R7 означает водород, галоген, С1-С6-алкил;
R8, R9, R10 означают водород, галоген;
R11, R13 означает водород, формил, C1-С6-алкилкарбонил,
C1-С6-алкоксикарбонил, С1-С6-алкиламинокарбонил, ди(С1-С6-алкил)аминокарбонил,
причем названные алкильные остатки могут быть замещены от одной до трех С1-С4алкоксигрупп; фениламинокарбонил, фенилсульфониламинокарбонил, N-(C1-С6-алкил)-N-(фенил)аминокарбонил, морфолиниламинокарбонил,
причем фенильный остаток может быть частично или полностью галогенирован и/или может быть замещен от одной до трех цианогрупп; или SO2R15;
R14 означает фенил-С1-С6-алкил;
R15 означает C1-С6-алкил;
а также их применимые в сельском хозяйстве соли.
2. Замещенные гетероароилом фенилаланинамиды формулы I по п.1, где А означает С-присоединенный пиразолил, выбранный из групп А1а-А4а
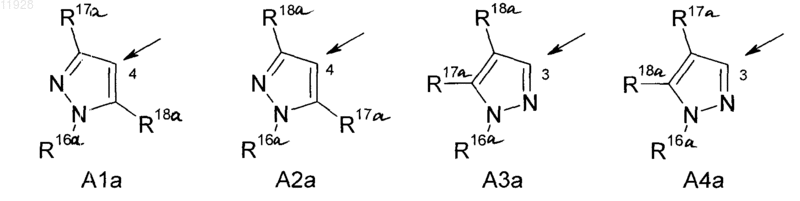
причем стрелка показывает место присоединения и R16a означает C1-С6-алкил;
R17a - C1-С6-галогеналкил или (С1-С6-алкил)амино; и
R18a означает галоген или C1-С6-галогеналкил.
3. Замещенные гетероароилом фенилаланинамиды формулы I по п.1, где А означает С-присоединенный пиразолил, выбранный из групп А1а-А2а
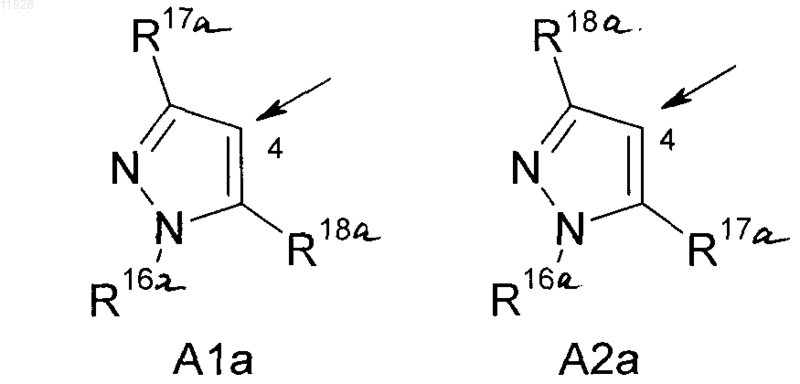
причем стрелка показывает место присоединения, и
R16a означает C1-С6-алкил;
R17a - C1-С6-галогеналкил или (С1-С6-алкил)амино; и
R18a означает галоген или C1-С6-галогеналкил.
4. Замещенные гетероароилом фенилаланинамиды формулы I по п.1
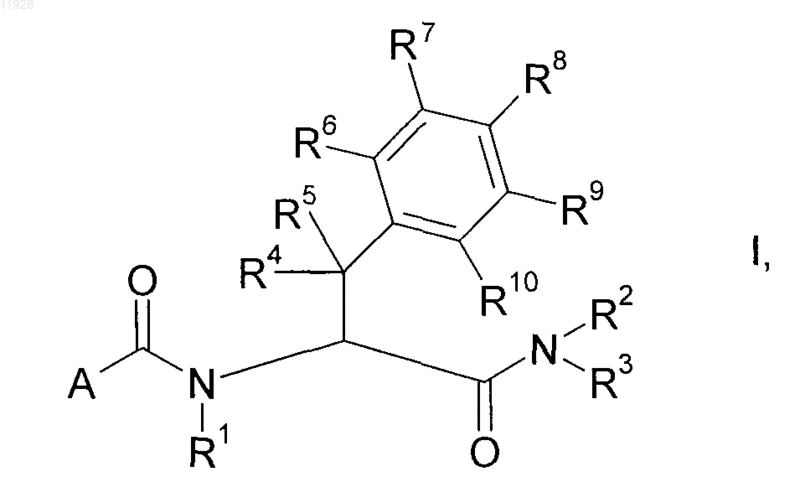
где переменные имеют следующие значения:
А означает С-присоединенный 5- или 6-членный гетероароил, выбранный из групп А1-А6, А8, А12-А14

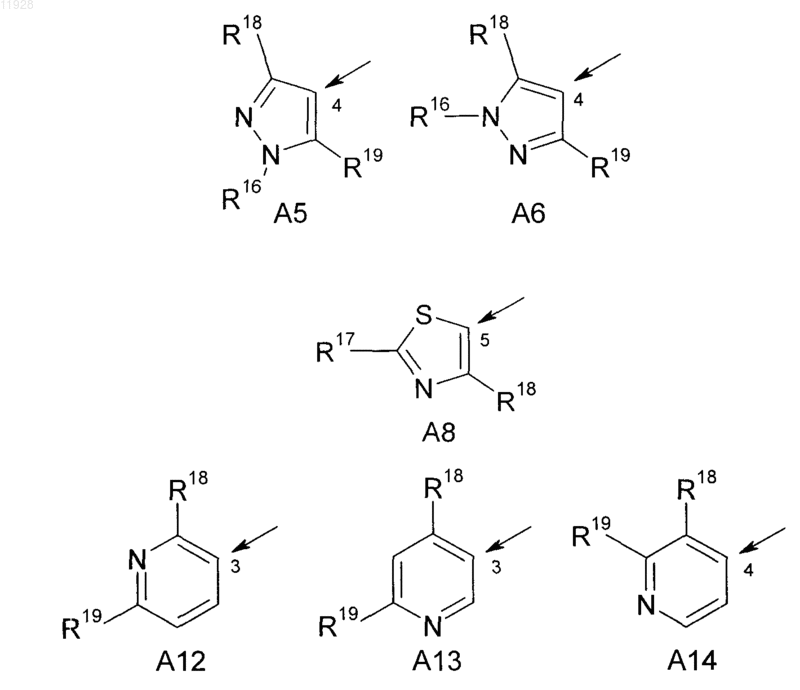
причем стрелка показывает место присоединения и
R16 означает C1-С6-алкил,
R17 означает водород, галоген, C1-С6-алкил или С1-С6-галогеналкил,
R18 означает C1-С6-алкил или C1-С6-галогеналкил;
R19 означает водород;
R1, R2 означает водород;
R3 означает C1-С6-алкил;
R4 означает водород, C1-С6-алкил, OR11 или NR13R14;
R5 означает водород или C1-С6-алкил;
R6, R7 означает водород, галоген, С1-С6-алкил;
R8, R9, R10 означают водород, галоген; водород, формил, С1-С6-алкилкарбонил, С1-С6-алкоксикарбонил, С1-С6-алкиламинокарбонил, ди-(С1-С6-алкил)аминокарбонил,
причем названные алкильные остатки могут быть замещены от одной до трех С1-С4-алкоксигрупп; фениламинокарбонил, фенилсульфониламинокарбонил, N-(C1-С6-алкил)-N-(фенил)аминокарбонил, морфолиниламинокарбонил,
причем фенильный остаток может быть частично или полностью галогенирован и/или может быть замещен от одной до трех цианогрупп; или SO2R15;
R14 означает фенил-С1-С6-алкил;
R15 означает С1-С6-алкил;
а также их применимые в сельском хозяйстве соли.
5. Замещенные гетероароилом фенилаланинамиды формулы I по пп.1-4, где R1, R2, R5, R9 и R10 означают водород.
6. Замещенные гетероароилом фенилаланинамиды формулы I по пп.1-4, где R4 означает водород, С1-С4-алкил или OR11.
7. Способ получения замещенных гетероароилом фенилаланинамидов формулы I по п.1, отличающийся тем, что фенилаланины формулы V
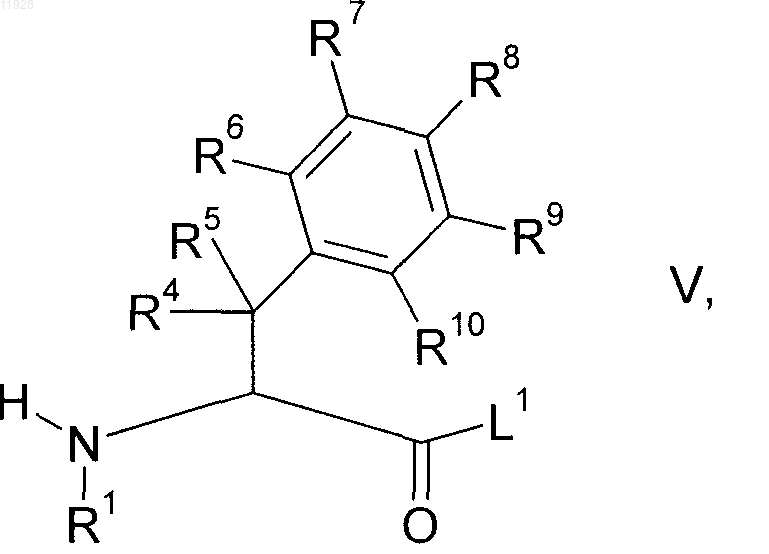
где R1 и R4-R10 имеют приведенные в п.1 значения и L1 означает нуклеофильно вытесняемую уходящую группу, подвергают взаимодействию с гетероарильной кислотой (производными) формулы IV
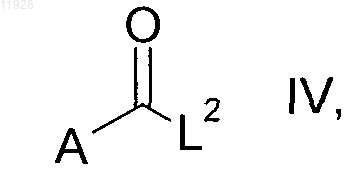
где А имеет приведенные в п.1 значения и L2 означает нуклеофильно вытесняемую уходящую группу, с получением соответствующих производных гетероароила формулы III

где A, R1 и R4-R10 имеют приведенные в п.1 значения и L1 означает нуклеофильно вытесняемую уходящую группу, и полученные производные гетероароила формулы III подвергают взаимодействию с амином формулы II

где R2 и R3 имеют приведенные в п.1 значения.
8. Способ получения замещенных гетероароилом фенилаланинамидов формулы I по п.7, где R4 означает гидрокси и R5 означает водород, отличающийся тем, что производные гетероароила формулы III, где R4 означает гидрокси и R5 означает водород, получают ацилированием кетосоединений формулы XIII

где R1, а также R6-R10 имеют приведенные в п.1 значения и L1 означает нуклеофильно вытесняемую уходящую группу, гетероарильной кислотой (производными) формулы IV в N-ацилкетосоединения формулы XII
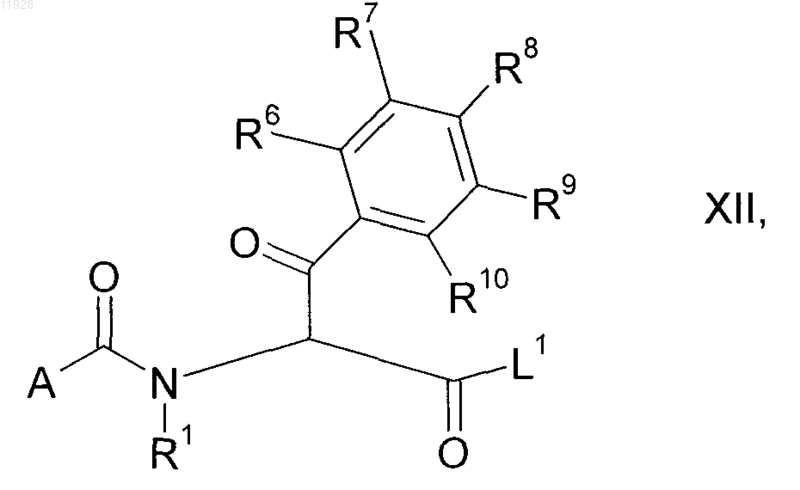
где A, R1, а также R6-R10 имеют приведенные в п.1 значения и L1 означает нуклеофильно вытесняемую уходящую группу, ё последующим восстановлением кетогруппы.
9. Производные гетероароила формулы III
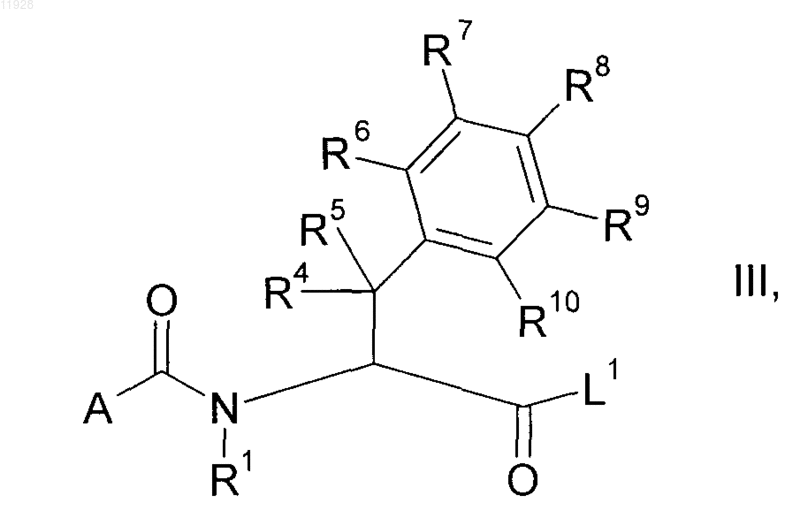
где R1 и R4-R10 имеют приведенные в п.1 значения, А означает A1, А2, A3, А4, А5, А6 или А8,
причем R16-R19 имеют значения, определенные в п.1, и L1 означает гидрокси или C1-С6-алкокси.
10. Средство, содержащее гербицидно активное количество по меньшей мере одного замещенного гетероароилом фенилаланина формулы I или применимой в сельском хозяйстве соли соединения формулы I по пп.1-6 и обычные для создания препаративной формы защиты растений вспомогательные средства.
11. Способ получения средств по п.10, отличающийся тем, что смешивают гербицидно активное количество по меньшей мере одного замещенного гетероароилом фенилаланина формулы I или применимой в сельском хозяйстве соли соединения формулы I по пп.1-6 и обычные для создания препаративной формы защиты растений вспомогательные средства.
12. Способ борьбы с нежелательным ростом растений, отличающийся тем, что гербицидно активным количеством по меньшей мере одного замещенного гетероароилом фенилаланина формулы I или применимой в сельском хозяйстве солью соединения формулы I по пп.1-6 воздействуют на растения, их пространство произрастания и/или на семена.
13. Применение замещенных гетероароилом фенилаланинамидов формулы I и применимых в сельском хозяйстве солей по пп.1-6 в качестве гербицидов.
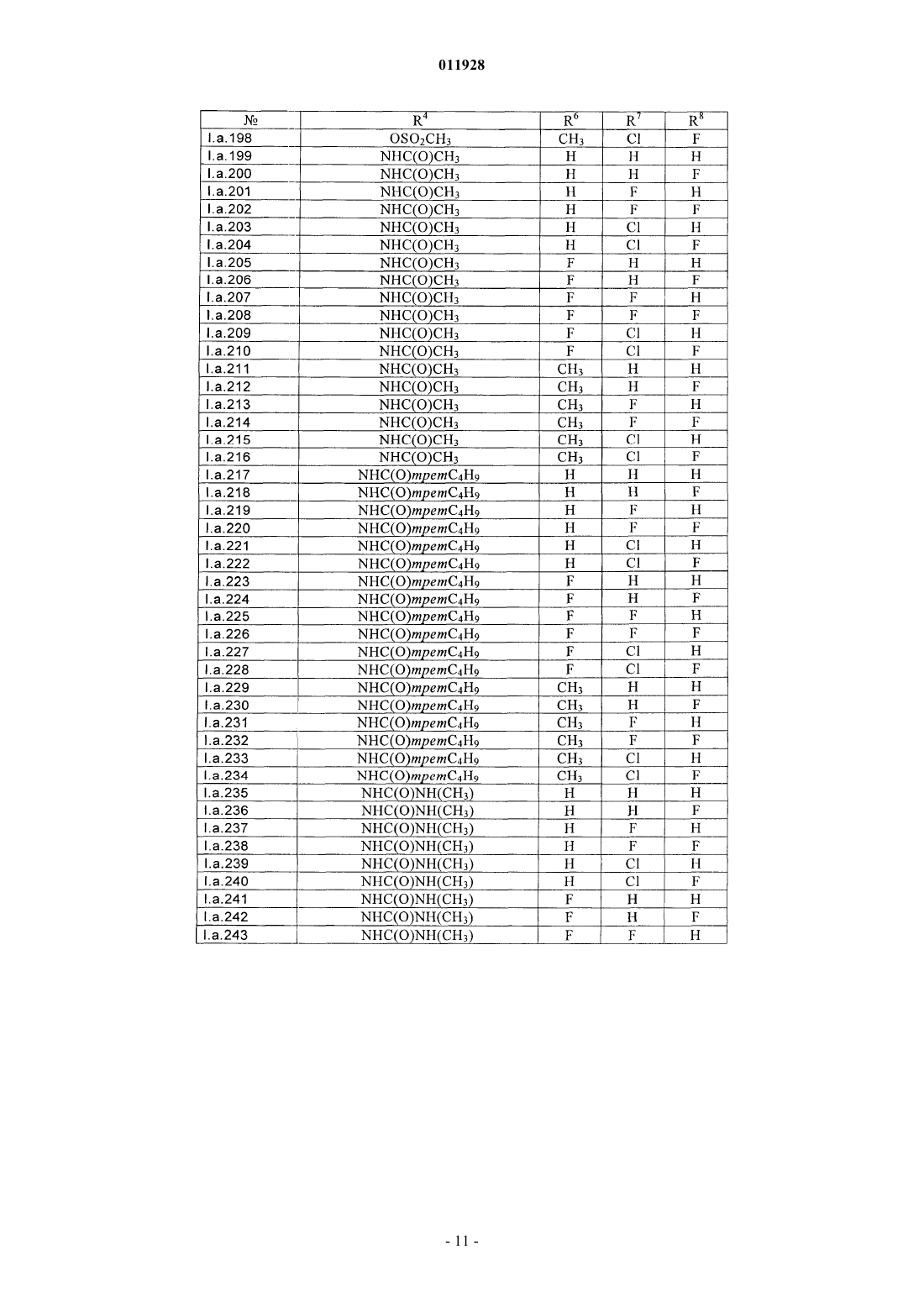
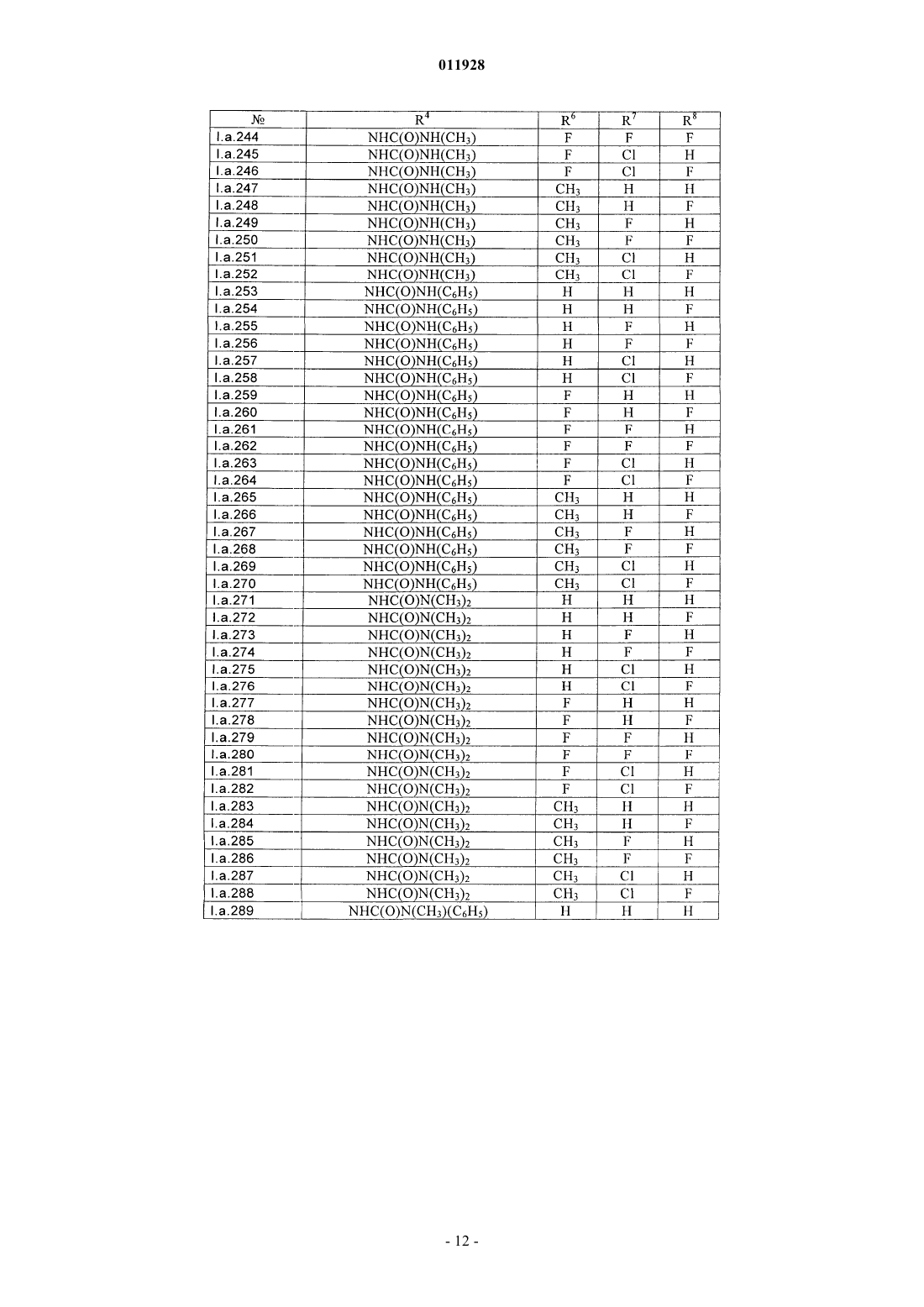
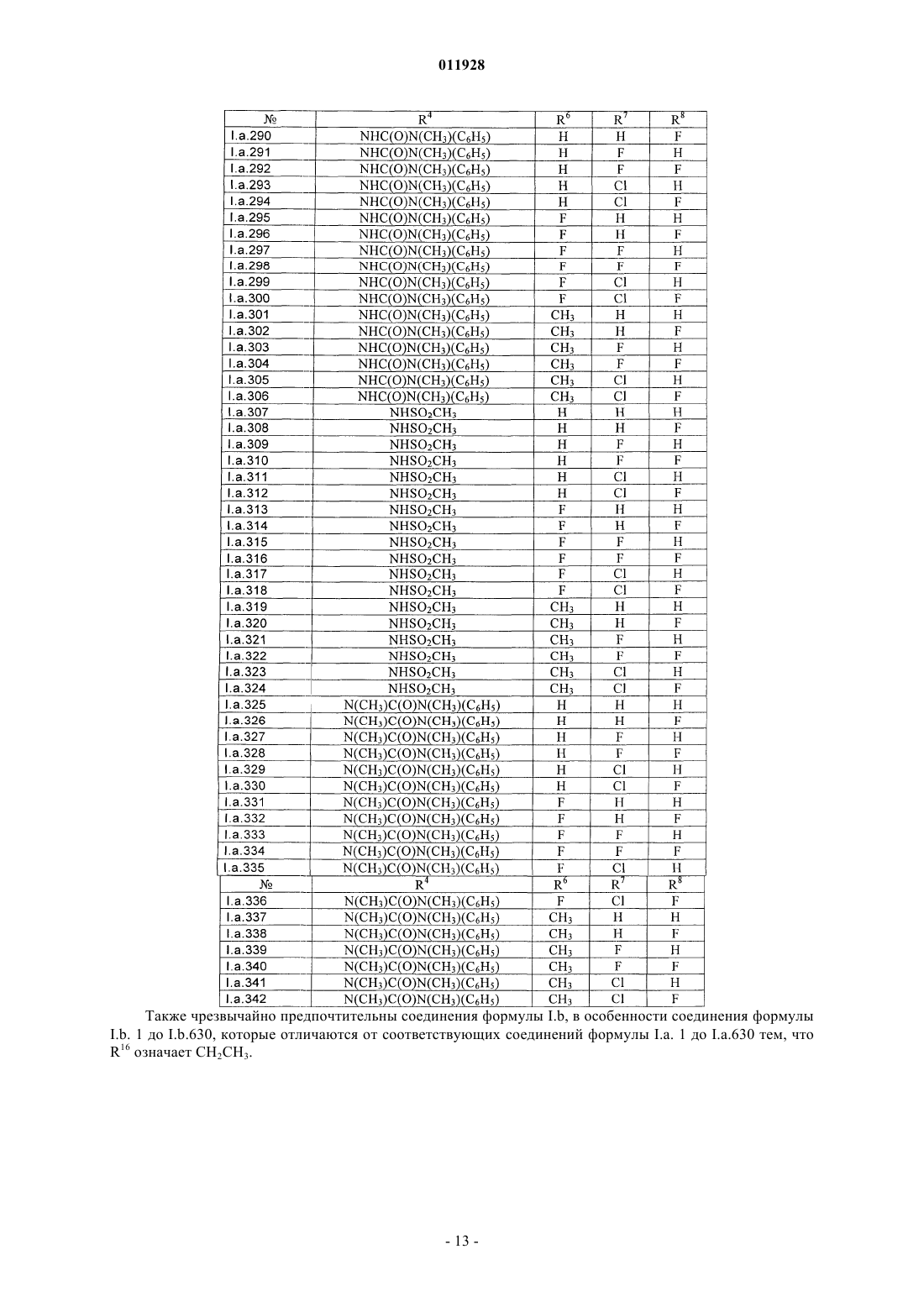
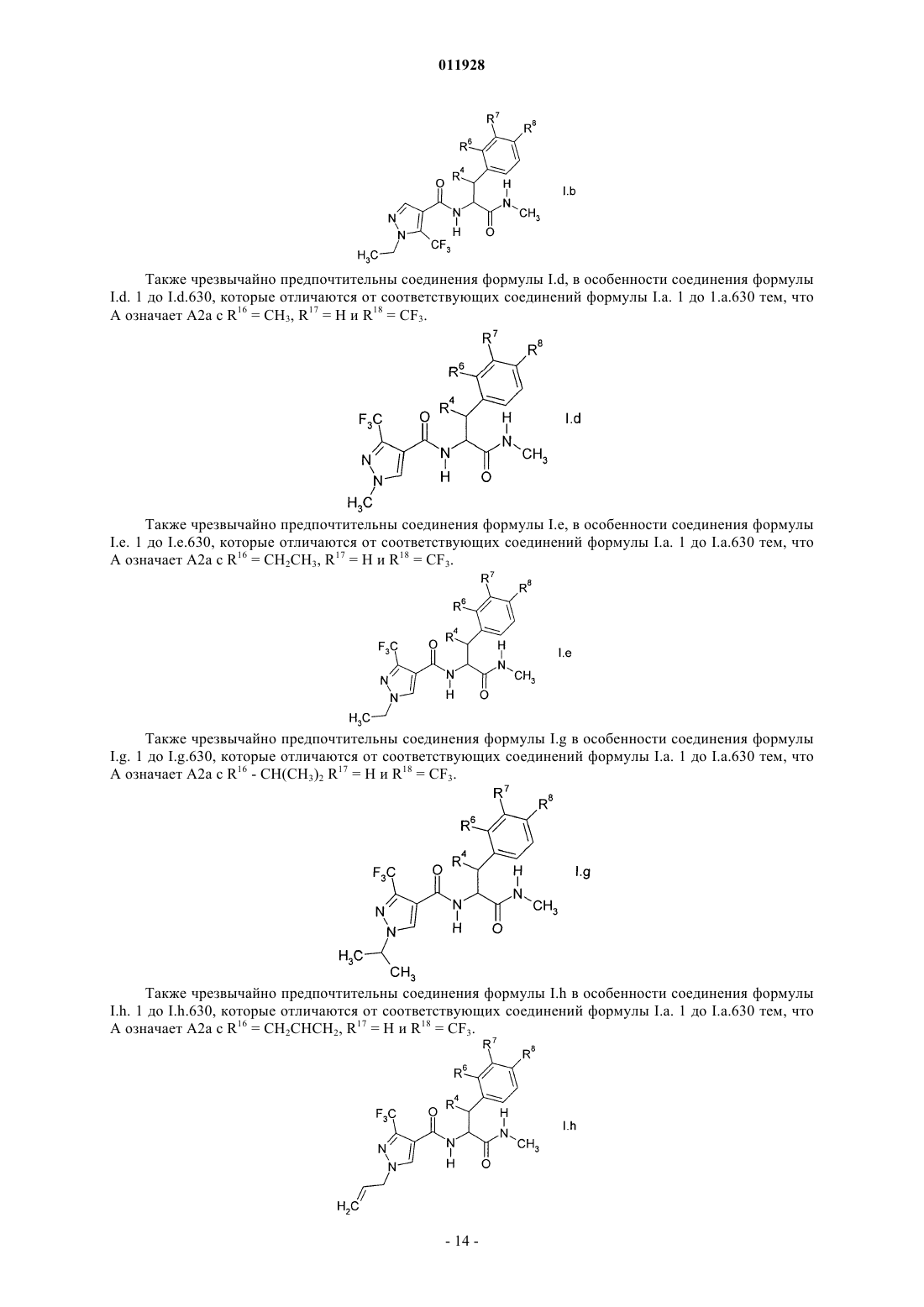
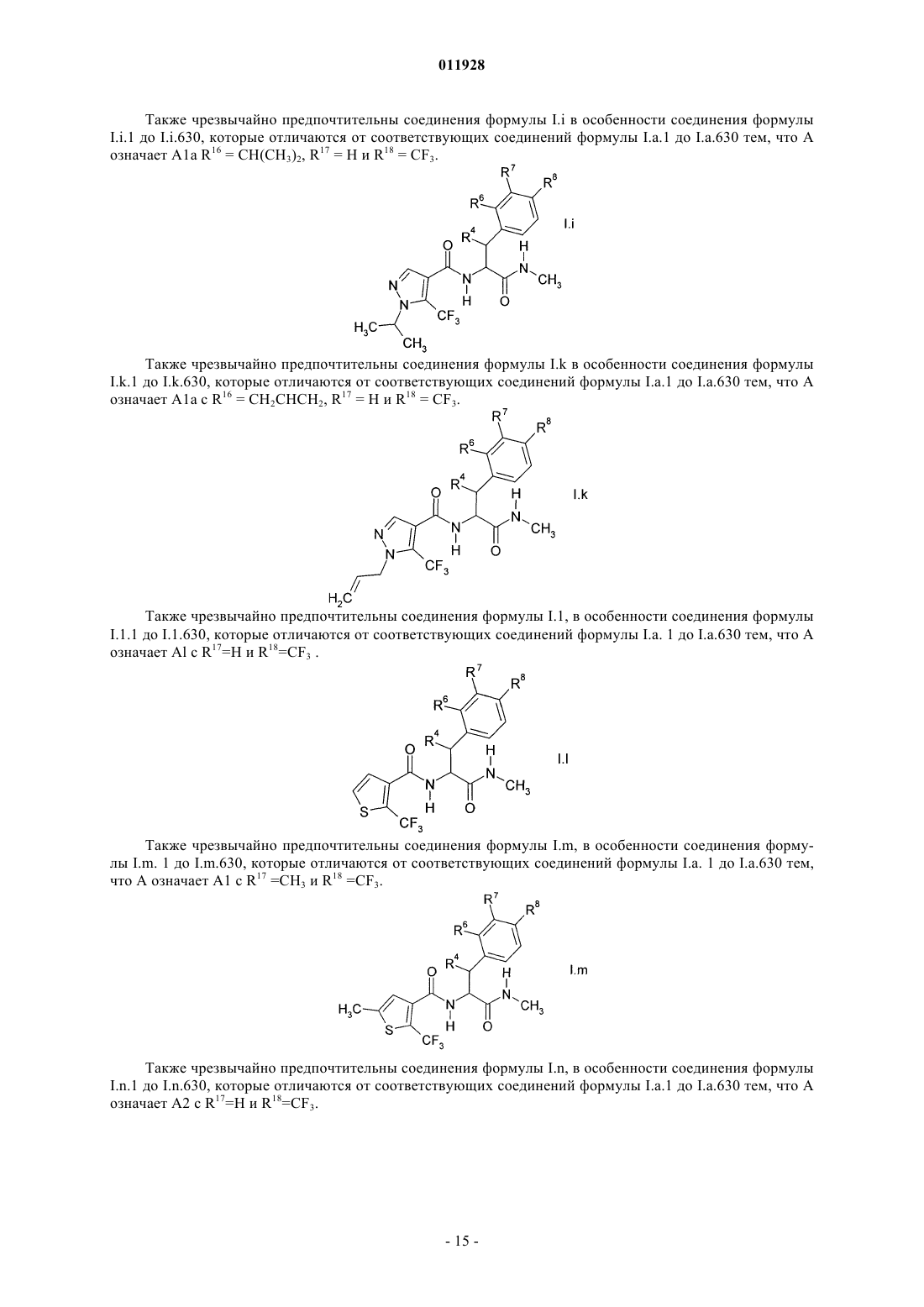
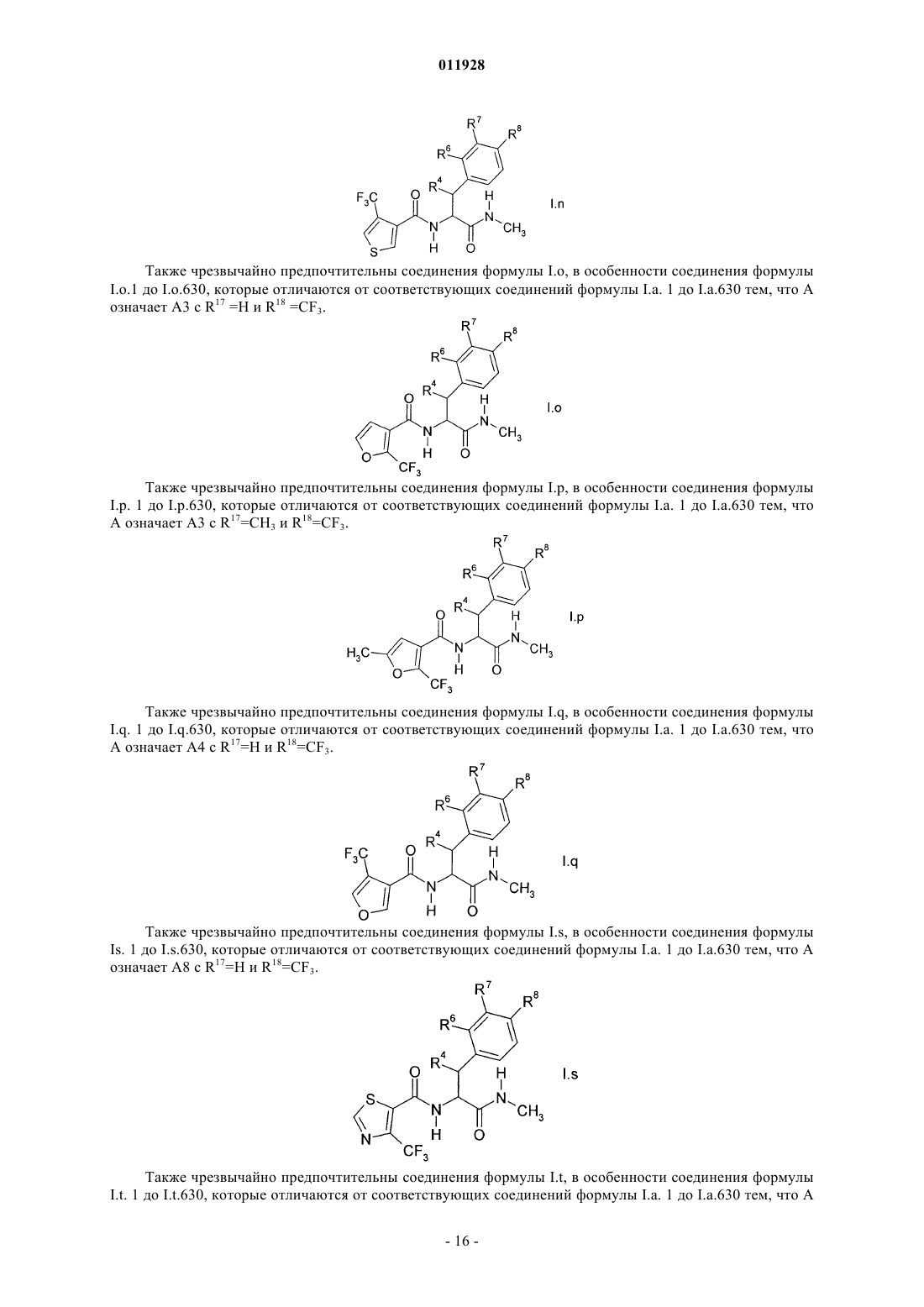
Текст
011928 Настоящее изобретение относится к замещенным гетероароилом фенилаланин-амидам формулы I в которой заместители имеют следующее значение: А означает С-присоединенный 5- или 6-членный гетероароил, выбранный из групп А 1-А 6, А 8, А 12 А 14, а также А 1 а-А 4 а причем стрелка показывает место присоединения и R16 означает C1-С 6-алкил,R17 означает водород, галоген, C1-С 6-алкил или C1-С 6-галогеналкил, R18 означает C1-С 6-алкил илиR18a означает галоген или C1-С 6-галогеналкил;R5 означает водород или C1-С 6-алкил;R11, R13 означает водород, формил, C1-С 6-алкилкарбонил, C1-С 6-алкоксикарбонил, С 1-С 6 алкиламинокарбонил, ди(С 1-С 6-алкил)аминокарбонил,причем названные алкильные остатки могут быть замещены от одной до трех С 1-С 4 алкоксигрупп;-1 011928 фениламинокарбонил, фенилсульфониламинокарбонил, N-(C1-С 6-алкил)-N-[-(фенил)аминокарбонил,морфолиниламинокарбонил,причем фенильный остаток может быть частично или полностью галогенирован и/или может быть замещен от одной до трех цианогрупп; или SO2R15;R15 означает С 1-С 6-алкил; а также к их применимым в сельском хозяйстве солям. Кроме того, изобретение относится к способу и к промежуточным продуктам для получения соединений формулы I, к средствам, содержащим эти соединения, а также к применению этих соединений и содержащих их средств для борьбы с вредоносными растениями. Из литературных источников, например, из WO 03/066576, известны фенилаланин-амиды, которые замещены бензоильным остатком. В международных заявках WO 01/55146, WO 02/06995 и WO 02/40469 описываются, среди прочего,гетероциклилкарбонил-замещенные фенилаланин-амиды с фармацевтической активностью. Гербицидные свойства известных до сих пор соединений, соответственно, переносимость культурными растениями могут удовлетворять только условно. В основу настоящего изобретения поэтому положена задача разработки новых, в особенности гербицидно активных соединений с улучшенными свойствами. В соответствие с этим были разработаны гетероароил-замещенные фенилаланин-амиды формулы I,а также их гербицидная активность. Далее были разработаны гербицидные средства, которые содержат соединения I и имеют очень хорошее гербицидное действие. Кроме того, был разработан способ получения этих средств и способ борьбы с нежелательными растениями соединениями I. Соединения формулы I содержат в зависимости от вида замещения два или несколько центров хиральности и имеются в качестве энантиомеров или смесей диастереомеров. Объектом изобретения являются как чистые энантиомеры или диастереомеры, так и их смеси. Соединения формулы I могут иметься также и в форме своих применимых в сельском хозяйстве солей, причем вид соли, как правило, не играет роли. В общем пригодны соли тех катионов или кислотноаддитивные соли тех кислот, катионы, соотвественно, анионы которых не оказывают негативного влияния на гербицидную активность соединений I. В особенности пригодны в качестве катионов ионы щелочных металлов, предпочтительно, натрия,лития и калия, щелочно-земельных металлов, предпочтительно, кальция и магния, и переходных металлов, предпочтительно, марганца, меди, цинка и железа, а также аммония, причем здесь, по желанию,один до четырех атомов водорода могут быть заменены С 1-С 4-алкилом, гидрокси-С 1-С 4-алкилом, С 1-С 4 алкокси-С 1-С 4-алкилом, гидрокси-С 1-С 4-алкокси-С 1-С 4-алкилом, фенилом или бензилом, предпочтительно, аммоний, диметиламмоний, диизопропиламмоний, тетраметиламмоний, тетрабутиламмоний, 2-(2 гидрокси-эт-1-окси)эт-1-иламмоний, ди-(2-гидрокси-эт-1-ил)амоний, триметилбензиламмоний, далее ионы фосфония, ионы сульфония, предпочтительно три-(С 1-С 4-алкил)сульфоний и ионы сульфоксония,предпочтительно три-(С 1-С 4-алкил)сульфоксоний. Анионами применимых кислотно-аддитивных солей являются, прежде всего, хлорид, бромид, фторид, гидросульфат, сульфат, дигидрофосфат, гидрофосфат, нитрат, гидрокарбонат, карбонат, гексафторосиликат, гексафторофосфат, бензоат, а также анионы С 1-С 4-алкановых кислот, предпочтительно формиат, ацетат, пропионат и бутират. Названные для заместителей R1-R19 или в качестве остатков фенильного или гетроциклильного кольца органические молекулы представляют собой сборные понятия для индивидуального перечисления отдельных членов групп. Все углеводородные цепи, т.е. все алкил-, алкенил-, алкинил-, цианоалкил-,галогеналкил-, галогеналкенил-, галогеналкинил-, алкокси-, галогеналкокси-, алкоксиалкил-, алкилкарбонил-,алкенилкарбонил-, алкинилкарбонил-, алкоксикарбонил-, алкенилоксикарбонил-, алкинилоксикарбонил-, алкиламино-, алкиламинокарбонил-, алкениламинокарбонил-, алкиниламинокарбонил-, алкилсульфониламинокарбонил-, диалкиламинокарбонил-, N-алкенил-N-алкиламинокарбонил-, N-алкинил-N-алкиламинокарбонил-, Nалкокси-N-алкиламинокарбонил-, N-алкенил-N-алкоксиаминокарбонил-, N-алкинил-N-алкоксиаминокарбонил-,диалкиламинотиокарбонил, алкилкарбонилалкил, алкоксииминоалкил, N-(алкиламино)иминоалкил, N(диалкиламино)иминоалкил, фенилалкил-, фенилкарбонилалкил-, N-алкил-N-фениламинокарбонил-, фенилалкилкарбонил, гетероциклилалкил-, гетероциклилкарбонилалкил-, N-алкил-N-гетероциклиламинокарбонил-, гетероциклилалкилкарбонил-, алкилтио-и алкилкарбонилокси-элементы могут быть неразветвленными или разветвленными. Если не указано по-другому, галогенированные заместители имеют предпочтительно один до пяти одинаковых или различных атомов галогена. Значение галоген представляет собой фтор, хлор, бром или йод. Далее имеются, например, следующие значения: С 1-С 4-алкил, а также алкильные остатки С 1-С 4-алкилкарбонилокси и C1-С 6-алкилиминоокси-С 1-С 4 алкила означают, например, метил, этил, н-пропил, 1-метилэтил, н-бутил, 1-метилпропил, 2-метилпропил-2 011928 и 1,1-диметилэтил; С 1-С 6-алкил, а также алкильные остатки С 1-С 6-алкилсульфониламинокарбонила, N-(С 3-С 6-алкенил)N-(C1-С 6-алкил)аминокарбонила, (С 3-С 6-алкинил)-N-(С 1-С 6-алкил)аминокарбонила, N-(C1-С 6-алкокси)-N(C1-С 6-алкил)аминокарбонила, C1-С 6-алкилкарбонил-C1-С 6-алкила, C1-С 6-алкоксиимино-С 1-С 6-алкила, N(С 1-С 6-алкиламино)имино-C1-С 6-алкила, N-(ди-С 1-С 6-алкиламино)имино-C1-С 6-алкила, фенил-С 1-С 6 алкила, фенилкарбонил-C1-С 6-алкила, N-(С 1-С 6-алкил)-N-фениламинокарбонила, гетероциклил-C1-С 6 алкила, гетероциклилкарбонил-С 1-С 6-алкила и N-(С 1-С 6-алкил)-N-гетероциклиламинокарбонила означают С 1-С 4-алкил, приведенный выше, а также, например, н-пентил, 1-метилбутил, 2-метилбутил, 3 метилбутил, 2,2-диметилпропил, 1-этилпропил, н-гексил, 1,1-диметилпропил, 1,2-диметилпропил, 1 метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2-диметилбутил, 1,3 ди-метилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1-этилбутил, 2-этилбутил, 1,1,2 триметилпропил,1-этил-1-метилпропил и 1-этил-3-метилпропил; С 1-С 6-алкилкарбонил означает, например, метилкарбонил, этилкарбонил, пропилкарбонил, 1 метилэтилкарбонил, бутилкарбонил, 1-метилпропилкарбонил, 2-метилпропилкарбонил или 1,1 диметилэтилкарбонил;C1-С 6-алкилкарбонил, а также алкилкарбонильные остатки С 1-С 6-алкилкарбонил-C1-С 6-алкила, фенил-С 1-С 6-алкилкарбонила и гетероциклил-C1-С 6-алкилкарбонила означают С 1-С 4-алкилкарбонил, как приведено выше, а также, например, пентилкарбонил, 1-метилбутилкарбонил, 2-метилбутилкарбонил, 3 метилбутилкарбонил, 2,2-диметилпропилкарбонил, 1-этилпропилкарбонил, метилкарбонил, 1,1 диметилпропилкарбонил,1,2-диметилпропилкарбонил,1-метилпентилкарбонил,2-метилпентилкарбонил, 3-метилпентилкарбонил, 4-метилпентилкарбонил, 1,1-диметилбутилкарбонил, 1,2 диметилбутилкарбонил,1,3-диметилбутилкарбонил,2,2-диметилбутилкарбонил,2,3 диметилбутилкарбонил, 3,3-диметилбутилкарбонил, 1-этилбутилкарбонил, 2-этилбутилкарбонил, 1,1,2 триметилпропилкарбонил, 1,2,2-триметилпропилкарбонил, 1-этил-1-метилпропилкарбонил или 1-этил-2 метил-пропилкарбонил; С 1-С 4-галогеналкил, означает С 1-С 4-алкильный остаток, приведенный выше, который замещен частично или полностью фтором, хлором, бромом и/или иродом, а именно, хлорметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлордифторметил, бромметил, йодметил, 2-фторэтил, 2-хлорэтил, 2-бромметил, 2-йодэтил, 2,2-дифторэтил, 2,2,2 трифторэтил, 2-хлор-2-фторэтил, 2-хлор-2,2-дифторэтил, 2,2-дихлор-2-фторэтил, 2,2,2-трихлорэтил, пентафторэтил, 2-фторпропил, 3-фторпропил, 2,2-дифторпропил, 2,3-дифторпропил, 2-хлорпропил, 3 хлорпропил,2,3-дихлорпропил,2-бромпропил,3-бромпропил,3,3,3-трифторпропил,3,3,3 трихлорпропил, 2,2,3,3,3-пентафторпропил, гептафторпропил, 1-(фторметил)-2-фторэтил, 1-(хлорметил)2-хлорэтил, 1-(бромметил)-2-бромметил, 4-фторбутил, 4-хлорбутил, 4-бромбутил и нонафторбутил; С 1-С 6-галогеналкил означает С 1-С 4-галогеналкил, привденный выше, а также, например 5 фторпентил, 5-хлорпентил, 5-бромпентил, 5-йодпентил, ундекафторпентил, 6-фторгексил, 6-хлогексил,6-бромгексил, 6-йодгексил и додекафторгексил; С 1-С 4-алкокси означает, например, метокси, этокси, пропокси, 1-метилэтокси, бутокси, 1 метилпропокси, 2-метилпропокси и 1,1-диметилэтокси;C1-С 6-алкокси, а также алкоксичасти N-(C1-С 6-алкокси)-N-(С 1-С 6-алкил)аминокарбонила, N-(С 3-С 6 алкенил)-N-(C1-С 6-алкокси)аминокарбонила, N-(С 3-С 6-алкинил)-N-(С 1-С 6-алкокси)аминокарбонила и C1 С 6-алкоксиимино-C1-С 6-алкила означают С 1-С 4-алкокси, приведенный выше, а также, например, пентокси, 1-метил-бутокси, 2-метилбутокси, 3-метоксибутокси, 1,1-диметилпропокси, 1,2-диметил-пропокси,2,2-диметилпропокси, 1-этилпропокси, гексокси, 1-метилпентокси, 2-метилпентокси, 3-метилпентокси,4-метилпентокси, 1,1-диметилбутокси,1,2-диметилбутокси, 1,3-диметилбутокси, 2,2-диметилбутокси,2,3-диметилбутокси, 3,3-диметилбутокси, 1-этилбутокси, 2-этилбутокси, 1,1,2-триметилпропокси, 1,2,2 триметилпропокси, 1-этил-1-метилпропокси и 1-этил-2-метилпропокси; С 1-С 4-алкоксикарбонил,а также алкоксикарбонильные части С 1-С 4-алкокси-С 1-С 4 алкоксикарбонили и ди-(С 1-С 4-алкил)амино-С 1-С 6-алкоксикарбонила означают, например, метоксикарбонил,этоксикарбонил,пропоксикарбонил,1-метилэтоксикарбонил,бутоксикарбонил,1 метилпропоксикарбонил, 2-метилпропоксикарбонил или 1,1-диметилэтоксикарбонил;(C1-С 6-алкиламино)карбонил означает (С 1-С 4-алкиламино)карбонил, приведенный выше, а также,например, пентиламинокарбонил, 1-метилбутиламинокарбонил, 2-метилбутиламинокарбонил, 3 метилбутиламинокарбонил, 2,2-диметилпропиламинокарбонил, 1-этилпропиламинокарбонил, гексиламинокарбонил, 1,1-диметилпропиламинокарбонил, 1,2-диметилпропиламинокарбонил, 1-метилпентиламинокарбонил,2-метилпентиламинокарбонил,3-метилпентиламинокарбонил,4-метилпентиламинокарбонил,1,1-диметилбутиламинокарбонил,1,2-диметилбутиламинокарбонил,1,3 диметилбутиламинокарбонил, 2,2-диметилбутиламинокарбонил, 2,3-диметилбутиламинокарбонил, 3,3 диметилбутиламинокарбонил,1-этилбутиламинокарбонил,2-этилбутиламинокарбонил,1,1,2 триметилпропиламинокарбонил,1,2,2-триметилпропиламинокарбонил,1-этил-1-метилпропиламинокарбонил или 1-этил-2-метилпропиламинокарбонил; ди(C1-С 6-алкил)аминокарбонил означает ди(С 1-С 4-алкил)аминокарбонил, приведенный выше, а также, например, N-метил-N-пентиламинокарбонил, N-метил-N-(1-метилбутил)аминокарбонил, N-метил-N(2-метилбутил)аминокарбонил,N-метил-N-(3-метилбутил)аминокарбонил,N-метил-N-(2,2 диметилпропил)аминокарбонил,N-метил-N-(1-этилпропил)аминокарбонил,N-метил-N-гексиламинокарбонил,N-метил-N-(1,1-диметилпропил)аминокарбонил,N-метил-N-(1,2-диметилпропил)аминокарбонил, N-метил-N-(1-метилпентил)аминокарбонил, N-метил-N-(2-метилпентил)аминокарбонил, Nметил-N-(3-метилпентил)аминокарбонил, N-метил-N-(4-метилпентил)аминокарбонил, N-метил-N-(1,1 диметилбутил)аминокарбонил,N-метил-N-( 1,2-диметилбутил)-аминокарбонил,N-метил-N-(1,3 диметилбутил)аминокарбонил,N-метил-N-(2,2-диметилбутил)аминокарбонил,N-метил-N-(2,3-4 011928 диметилбутил)аминокарбонил,N-метил-N-(3,3-диметилбутил)аминокарбонил,N-метил-N-(1-этилбутил)аминокарбонил, N-метил-N-(2-этилбутил)аминокарбонил, N-метил-N-(1,1,2-триметилпропил)аминокарбонил, N-метил-N-(1,2,2-триметилпропил)аминокарбонил, N-метил-N-(1-этил-1-метилпропил)аминокарбонил, N-метил-N-(1-этил-2-метилпропил)аминокарбонил, N-этил-N-пентиламинокарбонил, Nэтил-N-(1-метилбутил)аминокарбонил, N-этил-N-(2-метилбутил)аминокарбонил, N-этил-N-(3-метилбутил)аминокарбонил, N-этил-N-(2,2-диметилпропил)аминокарбонил, N-этил-N-(1-этилпропил)аминокарбонил, N-этил-N-гексиламинокарбонил, N-этил-N-(1,1-диметилпропил)-аминокарбонил, N-этил-N(1,2-диметилпропил)аминокарбонил,N-этил-N-(1-метилпентил)аминокарбонил,N-этил-N-(2 метилпентил)-аминокарбонил, N-этил-N-(3-метилпентил)-аминокарбонил, N-этил-N-(4-метилпентил)аминокарбонил,N-этил-N-(1,1-диметилбутил)-аминокарбонил,N-этил-N-(1,2-диметилбутил)аминокарбонил,N-этил-N-(1,3-диметилбутил)аминокарбонил,N-этил-N-(2,2-диметилбутил)аминокарбонил, N-этил-N-(2,3-диметилбутил)аминокарбонил, N-этил-N-(3,3-диметилбутил)аминокарбонил,N-этил-N-(1-этилбутил)аминокарбонил,N-этил-N-(2-этилбутил)аминокарбонил,N-этил-N-(1,1,2 триметилпропил)аминокарбонил, N-этил-N-(1,2,2-триметилпропил)аминокарбонил, N-этил-N-(1-этил-1 метилпропил)аминокарбонил, N-этил-N-(1-этил-2-метилпропил)аминокарбонил, N-пропил-N-пентиламинокарбонил,N-бутил-N-пентиламинокарбонил,N,N-дипентиламинокарбонил,N-пропил-Nгексиламинокарбонил, N-бутил-N-гексиламинокарбонил, N-пентил-N-гексиламинокарбонил или N,Nдигексиламинокарбонил; С-присоединенный 5- или 6-членный гетероарил с одним до четырех атомов азота или с одним до трех атомов азота и одним атомом кислорода или атомом серы, или с одним атомом кислорода или атомом серы означает, например, связанные С-атомом ароматические 5-членные гетероциклы, которые наряду с атомами углерода могут содержать один до четырех атомов азота, или один до трех атомов азота и один атом серы или кислорода, или один атом серы или кислорода в качестве членов кольца, например,2-фурил, 3-фурил, 2-тианил, 3-тиенил, 2-пирролил, 3-пирролил, 3-изоксазолил, 4-изоксазолил, 5 изоксазолил, 3-изотиазолил, 4-изотиазолил, 5-изотиазолил, 3-пиразолил, 4-пиразолил, 5-пиразолил, 2 оксазолил, 4-оксазолил, 5-оксазолил, 2-тиазолил, 4-тиазолил, 5-тиазолил, 2-имидазолил, 4-имидазолил,1,2,4-оксадиазол-3-ил, 1,2,4-оксадиазол-5-ил, 1,2,4-тиадиазол-3-ил, 1,2,4-тиадиазол-5-ил, 1,2,4-триазол-3 ил, 1,3,4-оксадиазол-2-ил, 1,3,4-тиалиазол-2-ил и 1,3,4-триазол-2-ил, например, связанные через С-атом ароматические 6-членные гетероциклы, которые наряду с атомами углерода могут содержать один до четырех, предпочтительно один до трех атомов азота в качестве членов кольца, например, 2-пиридинил,3-пиридинил, 4-пиридинил, 3-пиридазинил, 4-пиридазинил, 2-пиримидинил, 4-пиримидинил, 5 пиримидинил, 2-пиразинил, 1,3,5-триазин-2-ил и 1,2,4-тризин-3-ил; Все фенильные кольца, соответственно, все фенильные компоненты в фениламинокарбониле, фенилсульфониламинокарбониле, N-(C1-С 6-алкил)-N-фениламинокарбониле и морфолиниламинокарбониле, если не указано по-другому, являются незамещенными или имеют один до трех атомов галогена и/или цианоостаток. В особенно предпочтительной форме выполнения переменные соединения формулы I имеют нижеследующие значения, причем они представляют собой в отдельном и в комбинации друг с другом особые формы выполнения соединений формулы I. Предпочтительны замещенные гетероароилом фенилаланин-амиды формулы I, в которой А означает С-присоединенный пиразолил, выбранный из групп А 1 а-А 4 а причем стрелка показывает место присоединения и R16a означает С 1-С 6-алкил;R18a означает галоген или C1-С 6-галогеналкил. Также предпочтительны замещенные гетроароилом фенилаланин-амиды формулы I, в которой А означает С-присоединенный пиразолил, выбранный из групп A1a-А 2 а причем стрелка показывает место присоединения иR17a - С 1-С 6-галогеналкил или (C1-С 6-алкил)амино; и R18a означает галоген или C1-С 6-галогеналкил. Также предпочтительны замещенные гетроароилом фенилаланин-амиды формулы I, в которой А означает С-присоединенный 5- или 6-членный гетероароил, выбранный из групп А 1-А 6, А 8, А 12-А 14 причем стрелка показывает место присоединения иR5 означает водород или C1-С 6-алкил;R11, R13 означают водород, формил, C1-С 6-алкилкарбонил, C1-С 6-алкоксикарбонил, С 1-С 6 алкиламинокарбонил, ди-(С 1-С 6-алкил)аминокарбонил,причем названные алкильные остатки могут быть замещены от одной до трех С 1-С 4-алкоксигрупп; фениламинокарбонил, фенилсульфониламинокарбонил, N-(C1-С 6-алкил)-N-(фенил)аминокарбонил, морфолиниламинокарбонил,причем фенильный остаток может быть частично или полностью галогенирован и/или может быть замещен от одной до трех цианогрупп; или SO2R15;R15 означает C1-С 6-алкил. Также предпочтительны замещенные гетроароилом фенилаланин-амиды формулы I, в которой R1,2 5R , R , R9 и R10 означают водород. Также предпочтительны замещенные гетроароилом фенилаланин-амиды формулы I, в которой R4 означает водород, С 1-С 4-алкил или OR11. Чрезвычайно предпочтительны соединения фомулы I.a (соответствует формуле I с А = A1a, причемR16 означает СН 3, R17 означает H и R18 означает CF3; R1, R2 ,R9, R10 = H, R3 = СН 3), в частности соединения формулы I.a.1 до I.а.630 табл. 1, причем значения переменных А и R1 до R19 играют особую роль для соединений согласно изобретению не только в комбинации друг с другом, но и в отдельности Также чрезвычайно предпочтительны соединения формулы I.b, в особенности соединения формулыI.b. 1 до I.b.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что Также чрезвычайно предпочтительны соединения формулы I.d, в особенности соединения формулыI.d. 1 до I.d.630, которые отличаются от соответствующих соединений формулы I.a. 1 до 1.а.630 тем, что А означает А 2 а с R16 = CH3, R17 = H и R18 = CF3. Также чрезвычайно предпочтительны соединения формулы I.e, в особенности соединения формулыI.e. 1 до I.е.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает А 2 а с R16 = CH2CH3, R17 = H и R18 = CF3. Также чрезвычайно предпочтительны соединения формулы I.g в особенности соединения формулыI.g. 1 до I.g.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает А 2 а с R16 - CH(CH3)2 R17 = H и R18 = CF3. Также чрезвычайно предпочтительны соединения формулы I.h в особенности соединения формулыI.h. 1 до I.h.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает А 2 а с R16 = CH2CHCH2, R17 = H и R18 = CF3.- 14011928 Также чрезвычайно предпочтительны соединения формулы I.i в особенности соединения формулыI.i.1 до I.i.630, которые отличаются от соответствующих соединений формулы I.a.1 до I.а.630 тем, что А означает A1a R16 = CH(CH3)2, R17 = H и R18 = CF3. Также чрезвычайно предпочтительны соединения формулы I.k в особенности соединения формулыI.k.1 до I.k.630, которые отличаются от соответствующих соединений формулы I.a.1 до I.а.630 тем, что А означает A1a с R16 = CH2CHCH2, R17 = H и R18 = CF3. Также чрезвычайно предпочтительны соединения формулы I.1, в особенности соединения формулыI.1.1 до I.1.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает Al с R17=H и R18=CF3 . Также чрезвычайно предпочтительны соединения формулы I.m, в особенности соединения формулы I.m. 1 до I.m.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем,что А означает A1 с R17 =СН 3 и R18 =CF3. Также чрезвычайно предпочтительны соединения формулы I.n, в особенности соединения формулыI.n.1 до I.n.630, которые отличаются от соответствующих соединений формулы I.a.1 до I.а.630 тем, что А означает А 2 с R17=H и R18=CF3. Также чрезвычайно предпочтительны соединения формулы I.o, в особенности соединения формулыI.o.1 до I.о.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает A3 с R17 =Н и R18 =CF3. Также чрезвычайно предпочтительны соединения формулы I.p, в особенности соединения формулыI.p. 1 до I.р.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.a.630 тем, что А означает A3 с R17=CH3 и R18=CF3. Также чрезвычайно предпочтительны соединения формулы I.q, в особенности соединения формулыI.q. 1 до I.q.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает А 4 с R17=H и R18=CF3. Также чрезвычайно предпочтительны соединения формулы I.s, в особенности соединения формулыIs. 1 до I.s.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А означает А 8 с R17=H и R18=CF3. Также чрезвычайно предпочтительны соединения формулы I.t, в особенности соединения формулыI.t. 1 до I.t.630, которые отличаются от соответствующих соединений формулы I.a. 1 до I.а.630 тем, что А Замещенные гетероароилом фенилаланин-амиды формулы I могут быть получены различным образом, например, следующими способами: Способ А. Фенилаланин формулы V сначала превращается гетероариловой кислотой (производными) формулы IV в соответствующее производное гетероароила формулы III, который затем реагирует с амином II с получением целевого замещенного гетероароилом фенилаланин-амида формулы I:L2 означает нуклеофильно вытесняемую, уходящую группу, например гидрокси, галоген, C1-С 6 алкилкарбонил, C1-С 6-алкоксикарбонил, С 1-С 4-алкилсульфонил, фосфорил или изоуреил. Взаимодействие фенилаланинов формулы V с гетероарильной кислотой (производными) формулыIV, где L2 означает гидрокси, с получением производных гетероароила формулы III осуществляется в присутствии реагента активирования и основания обычно при температуре от 0C до точки кипения реакционной смеси, предпочтительно 0 до 110C, особенно предпочтительно при комнатной температуре в инертном органическом растворителе [ср. публикации Bergmann, E. D.; et al., J Chem Soc 1951, 2673;(10),891-894 (1991)]. Пригодными реагентами активирования являются агенты конденсации, такие, как связанный полистиролом дициклогексилкарбодиимид, диизопропилкарбодиимид, карбонилдиимидазол, сложные эфиры хлоругольной кислоты, такие как метилхлороформиат, этилхлороформиат, изопропилхлороформиат,изобутилхлороформиат, втор-бутилхлороформиат или аллилхлороформиат, пивалоилхлорид, полифосфорная кислота, ангидрид пропанфосфоновой кислоты, бис(2-оксо-3-оксазолидинил)фосфорилхлорид(BOPCl) или сульфонилхлориды, такие как метансульфонилхлорид, толуолсульфонилхлорид или безолсульфонилхлорид. Пригодными растворителями являются алифатические углеводороды, такие как пентан, гексан,- 17011928 циклогексан и смеси C5-C8-алканов, ароматические углеводороды, такие как бензол, толуол, о-, и- и пксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран (THF), нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон,метилэтилкетон, диэтилкетон и трет.-бутилметилкетон, а также диметилсульфоксид, диметилформамид(DMF), диметилацетамид (DMA) и N-метилпирролидон (NMP) или же вода, особенно предпочтительны метиленхлорид, THF и вода. Могут также применяться смеси названных растворителей. В качестве оснований пригодны в основном неорганические соединения, такие как гидроксиды щелочных и щелочноземельных металлов, такие, как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, оксиды щелочных и щелочно-земельных металлов, такие как оксид лития, оксид натрия, оксид кальция и оксид магния , гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития , гидрид натрия, гидрид калия и гидрид кальция, карбонаты щелочных и щелочноземельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, кроме того, органические основания, например третичные амины, такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин,и N-метилпиперидин, пиридин, замещенные пиридины, такие как коллидин, литидин и 4 диметиламинопиридин, также бициклические амины. Особенно предпочтительны гидроксид натрия,триэтиламин и пиримидин. Основания в общем применяются в эквимолярных количествах. Они могут также применяться в избытке или, в случае необходимости, в качестве растворителя. Исходные продукты в общем подвергаются взаимодействию друг с другом в эквимолярных количествах. Может быть благоприятным применение соединения IV в избытке в пересчете на соединение V. Реакционные смеси перерабатываются обычным образом, например, смешением с водой, разделением фаз и, в случае необходимости, хроматографической очисткой сырых продуктов. Промежуточные и конечные имеются обычно в форме вязких масел, которые освобождаются при пониженном давлении и при умеренно повышенной температуре от летучих компонентов и очищаются. Если промежуточные и конечные продукты получаются как твердые вещества, может осуществляться очистка перекристаллизацией или дигерированием. Взаимодействие фенилаланинов формулы V с гетероарильной кислотой (производными) формулыIV, где L2 означает галоген, C1-С 6-алкилкарбонил, C1-С 6-алкоксикарбонил, С 1-С 4-алкилсульфонил, фосфорил или изоуреил, с получением производных гетероароила формулы III осуществлется в присутствии основания обычно при температуре от 0C до точки кипения реакционной смеси, предпочтительно от 0C до 100C, особенно предпочтительно при комнатной температуре в инертном органическом растворителе [ср. публикации Bergmann, E. D.; et al., J. Chem. Soc. 1951, 2673; Zhdankin, V. V.; et al., Tetrahedronal., Indian J. Chem B. 41(3),593-595(2002); Clark, J. E. et al., Sythesis (10),891-894 (1991)]. Пригодными растворителями являются алифатические углеводороды, такие как пентан, гексан,циклогексан и смеси С 5-С 8-алканолы, ароматические углеводороды, такие как бензол, толуол, о-, и- и пксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран (THF), нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон,метилэтилкетон, диэтилкетон и трет-бутилметилкетон, а также диметилсульфоксид, диметилформамид(DMF), диметилацетамид (DMA) и N-метилпирролидон (NMP) или же вода, особенно предпочтительны метилепхлорид, THF и вода. Могут также применяться смеси названных растворителей. В качестве оснований пригодны в основном неорганические соединения, такие как гидроксиды щелочных и щелочно-земельных металлов, такие, как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, оксиды щелочных и щелочно-земельных металлов, такие как оксид лития, оксид натрия, оксид кальция и оксид магния, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, карбонаты щелочных и щелочноземельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, кроме того, органические основания, например третичные амины, такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин,и N-метилпиперидин, пиридин, замещенные пиридины, такие как коллидин, литидин и 4 диметиламинопиридин, также вициклические амины. Особенно предпочтительны гидроксид натрия,триэтиламин и пиримидин. Основания в общем применяются в эквимолярных количествах. Они могут также применяться в избытке или, в случае необходимости, в качестве растворителя. Исходные продукты в общем подвергаются взаимодействию друг с другом в эквимолярных количе- 18011928 ствах. Может быть благоприятным применение соединения IV в избытке в пересчете на соединение V. Переработку и выделение продуктов может осуществляться известным самим по себе образом. Естественно аналогичным образом сначала могут фенилаланины формулы V подвергаться взаимодействию с аминами формулы II с получением соответствующих аминов, которые затем подвергают реакции с гетероарильной кислотой (производными) формулы IV с получением целевых замещенных гетероарилом фенилаланин-амидов формулы I. Необходимые для получения производных гетероароила формулы III фенилаланины формулы V,где L1 означают гидрокси, известны из литературных источников, также и в форме энантиомеров и диастереомеров или могут быть получены в соответствие с цитируемыми литературными источниками:R4 = OR11: конденсацией эквивалентов глициненолата с бензальдегидами (см. Hvidt, T. et al., Tetrahedron Lett. 27 (33), 3807-3810 (1986) ; Saeed, A. et al., Tetrahedron 48 (12), 2507-2514 (1992); Kikuchi, J. et al., Chem.(12), 1479 (1986); JP 2001046076; Herbert R. B. et al., Can. J. Chem. 72(1), 114-117(1994; расщеплением 2-N-фталоил-3-гидрокси-фенилаланинов (Hutton, C. A., Org. Lett. 1 (2), 295297(1999; окислительным аминогидроксилированием и заключительным снятием защиты производных коричной кислоты (Kim, I. H. et al., Tetrahedron Lett. 42 (48), 8401-8403 (2001); расщеплением замещенных оксазолидинов (Wu S. D. et al., Sythetic Commun. 16 (12), 1479-1484(1986; расщеплением замещенных оксазолинов (Soloshonok V. A.; et al; Tetrahedron 52 (1), 245-254 (1996);(1974 расщеплением замещенных имидазолин -4-онов (Davis С et al., J. Chem. Soc. 3479 (1951R4=NR13R14: раскрытием кольца замещенных имидазолидинонов (Kavrakova I. К. et al., Org. Prep. Proced. Int. 28(3), 333-338 (1996 раскрытием кольца замещенных имидазолинов имидазолинов (Meyer R., Liebigs Ann. Chem., 1183(1977); Hayashi T. et al., Tetrahedron Lett. 37 (28), 4969-4972 (1996); Lin Y. R. et al., J. Org. Chem. 62 (6),1799-1803 (1997) ; Zhou X. T. et al., Tatrahedron Assym. 10 (5), 855-862 (1999) ) восстановлением производных 2-ацидо-3-амино-фенилаланина (Moyna, G. et al., Synthetic Commun. 27 (9), 1561-1567 (1997 гидрированием замещенных имидазолидинов (Alker D. et al., Tetrahedron Lett. 39 (5-6), 475-478(1998 Требуемые для получения производных ароила формулы III фенилаланины формулы V, где L1 означают C1-С 6-алкокси, также и в форме энантиомеров и диастереомеров, известны в литературных источниках или могут быть получены согласно цитируемым литературным источникам:R4 = OR11: конденсацией эквивалентов глициненолата с альдегидами: Nicolaou K. С. et al., J. Am. Chem. Soc. 124 (35), 10451-10455 (2002); Carrara, G. et al., Gazz. Chim. Ital. 82, 325 (1952); Fuganti, С. et al., J. Org.Chem. 51 (7), 1126-1128 (1986); Boger D. L. et al., J. Org. Chem. 62 (14), 4721-4736 (1997); Honig H. et al.,Tetrahedron (46), 3841 (1990); Kanemasa S. et al., Tetrahedron Lett. 34 (4), 677-680 (1993); US 4873359) расщеплением дигидропиразинов (Li, Y. Q. et al., Tetrahedron Lett. 40 (51), 9097-9100 (1999); Beulshausen, T. et al., Liebigs Ann. Chem. (11), 1207-1209 (1991 восстановлением производных N-аминофенилсерина (Poupardin O. et al., Tetrahedron Lett. 42 (8),1523-1526 (2001 расщеплением производных N-карбамоилфенилсерина (Park H. et al., J. Org. Chem. 66 (21), 72237226 (2001); US 6057473; Kim I. H. et al., Tetrahedron Lett. 42 (48), 8401-8403 (2001); Nicolaou K. C. et al.,Angew.N. Chem. Int. Edit. 37 (19), 2714-2716 (1998 расщеплением замещенных оксазолидинов (Zhou C. Y. et al., Sythetic Commun. 17 (11), 1377-1382(1987 восстановлением производных 2-ацидо-3-гидроксифенилпропионовой кислоты (Corey E. J. et al.,Tetrahedron Lett. 32 (25), 2857-2860 (1991 раскрытием кольца азиридинов с кислородсодержащими нуклеофилами (Davis F. A. et al., J. Org.Chem. 22, 1233 (1957 расщеплением замещенных имидазолидинонов (Davis, А. С; et al., J. Chem. Soc. 3479 (1951R4=NR13R14: восстановлением замещенных производных 2-азидо-3-аминофенилаланинов (Lee S. H., Tetrahedron 57(11),2139-2145(2001 раскрытием кольца замещенных имидазолинов (Zhou X. T. et al., Tetrahedron Asymmetr. 10 (5), 855862 (1999); Hayashi T. et al., Tetrahedron Lett. 37 (28), 4969-4972 (1996 Требуемая для получения производных гетероароила формулы III гетероарильная кислота (производные) формулы IV может быть приобретена на рынке или же могут быть получены аналогично известным из литературных источников приемам посредством реакции Гриньяра из соответствующего галогенида [например, A. Mannschuk et. Al, Angew. Chem. 100, 299 (1988)]. Реакция взаимодействия производных гетероароила формулы III, где L1 означает гидрокси, соответственно его соли, с амином формулы II с получением целевых замещенных гетероароилом фенилаланин-амидов формулы I осуществляется в присутствии реагента активирования и, в случае необходимости, в присутствии основания обычно при температуре от 0C до точки кипения реакционной смеси,предпочтительно от 0 до 100C, особенно предпочтительно при комнатной температуре в инертном органическом растворителе [ср. публикации Perich J. W., Johns R. В., J. Org. Chem. 53 (17), 4103-4105(1990); Guan et al., J. Comb. Chem. 2, 297 (2000)]. Пригодными реагентами активирования являются агенты конденсации, такие как связанный полистиролом дициклогексилкарбодиимид, диизопропилкарбодиимид, карбонилдиимидазол, сложные эфиры хлоругольной кислоты, такие как метилхлороформиат, этилхлороформиат, изопропилхлороформиат,изобутилхлороформиат, втор.-бутилхлороформиат или аллилхлороформиат, пивалоилхлорид, полифосфорная кислота, ангидрид пропанфосфоновой кислоты, бис(2-оксо-3-оксазолидинил)-фосфорилхлорид(BOPCl) или сульфонилхлориды, такие как метансульфонилхлорид, толуолсульфонилхлорид или безолсульфонилхлорид. Пригодными растворителями являются алифатические углеводороды, такие как пентан, гексан,циклогексан и смеси С 5-С 8-алканов, ароматические углеводороды, такие как бензол, толуол, о-, и- и пксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран (THF), нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон,метилэтилкетон, диэтилкетон и трет-бутилметилкетон, а также диметилсульфоксид, диметилформамид(DMF), диметилацетамид (DMA) и N-метилпирролидон (NMP) или же вода, особенно предпочтительны метиленхлорид, THF и вода. Могут также применяться смеси названных растворителей. В качестве оснований пригодны в основном неорганические соединения, такие как гидроксиды щелочных и щелочно-земельных металлов, такие, как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, оксиды щелочных и щелочно-земельных металлов, такие как оксид лития, оксид натрия, оксид кальция и оксид магния, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, карбонаты щелочных и щелочноземельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, кроме того, органические основания, например третичные амины, такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин,и N-метилпиперидин, пиридин, замещенные пиридины, такие как коллидин, литидин и 4 диметиламинопиридин, также бициклические амины. Особенно предпочтительны гидроксид натрия,триэтиламин и пиримидин. Основания в общем применяются в каталитических количествах. Они могут также применяться эк- 20011928 вимолярно, в избытке или, в случае необходимости, в качестве растворителя. Исходные продукты в общем подвергаются взаимодействию друг с другом в эквимолярных количествах. Может быть благоприятным применение соединения II в избытке в пересчете на соединение III. Переработка и выделение продуктов может осуществляться известным самим по себе образом. Реакция взаимодействия производных гетероароила формулы III, где L1 означает C1-С 6-алкокси с амином формулы II с получением целевых замещенных гетероароилом фенилаланин-амидов формулы I осуществляется обычно при температуре от 0C до точки кипения реакционной смеси, предпочтительно от 0 до 100C, особенно предпочтительно при комнатной температуре в инертном органическом растворителе, в случае необходимосати, в присутствии основания [ср. Kawahata N. H. et al., Tetrahedron Lett. 43Chem. Soc. 121 (36), 8407-8408 (1999)]. Пригодными растворителями являются алифатические углеводороды, такие как пентан, гексан,циклогексан и смеси С 5-С 8-алканов, ароматические углеводороды, такие как бензол, толуол, о-, и- и пксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран (THF), нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон,метилэтилкетон, диэтилкетон и трет-бутилметилкетон, спирты, такие как метанол, этанол, н-пропанол,изопропанол, н-бутанола и трет.-бутанол, а также диметилсульфоксид, диметилформамид (DMF), диметилацетамид (DMA) и N-метилпирролидон (NMP) или же вода, особенно предпочтительны метиленхлорид, THF, метанол, этанол и вода. Могут применяться также и смеси приведенных растворителей. Взаимодействие может осуществляться, в случае необходимости, в присутствии основания. В качестве оснований пригодны в основном неорганические соединения, такие как гидроксиды щелочных и щелочно-земельных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, оксиды щелочных и щелочно-земельных металлов, такие как оксид лития, оксид натрия,оксид кальция и оксид магния, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, карбонаты щелочных и щелочно-земельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, кроме того, органические основания, например третичные амины, такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, и Nметилпиперидин, пиридин, замещенные пиридины, такие как коллидин, литидин и 4 диметиламинопиридин, также бициклические амины. Особенно предпочтительны гидроксид натрия,триэтиламин, этилдиизопропиламин, N-метилморфолин и пиримидин. Основания в общем применяются в каталитических количествах. Они могут также применяться эквимолярно, в избытке или, в случае необходимости, в качестве растворителя. Исходные продукты применяются в общем в эквимолярных количествах друг с другом. Может быть благоприятным применение соединения II в избытке, в пересчете на соединение III. Переработка и выделение продуктов может осуществляться известным самим по себе образом. Требуемые для получения замещенных гетероароилом серин-амиды формулы II могут быть приобретены на рынке. Способ В. Производные гетероароила формулы III, где R4 означает гидрокси, могут быть получены таким образом, что ацилированные производные глицина формулы VIII, где ациловая группа может быть отщепляемой защитной группой, такой как бензилоксикарбонил (ср. соединение VIIIa с= бензил) или трет.бутилоксикарбонил (ср. соединение VIIIa с= трет-бутил), конденсируются гетероциклилкарбонильными соединениями VII до соответствующих альдольных продуктов VI. Затем отщепляется защитная группа и полученный таким образом фенилаланин формулы V, где R4 означает гидрокси, ацилируется гетероарильной кислотой (производными) формулы IV. Аналогично также и ацилированное производное глицина формулы VIII, причем ацилгруппа представляет собой замещенный гетероароильный остаток (ср. соединение VIIIb), при воздействии основания может подвергаться взаимодействию с гетероциклил-карбонильным соединением VII с получением производного гетероароила формулы III, где R4 означает гидрокси:L2 означает нуклеофильно вытесняемую, уходящую группу, например гидрокси, галоген, C1-С 6 алкилкарбонил, C1-С 6-алкоксикарбонил, С 1-С 4-алкилсульфонил, фосфорил или изоуреил. Взаимодействие производных глицина формулы VIII с гетероциклильными соединениями формулыVII с получением соответствующего альдольного продукта VI, соответственно, производного гетероароила формулы III, где R4 означает гидрокси, осуществляется обычно при температуре от -100C до точки кипения реакционной смеси, предпочтительно от -80 до 20C, в оосбенности от -80 до -20C, в инертном органическом растворителе в присутствии основания [ср. J.-F. Rousseau et al., J. Org. Chem. 63, 27312737 (1998)]. Пригодными растворителями являются алифатические углеводороды, такие, как пентан, гексан,циклогексан и смеси С 5-С 8-алканов, ароматические углеводороды, такие как бензол, толуол, о-, и- и пксилол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран, а также диметилсульфоксид, диметилформамид, диметилацетамид особенно предпочтительны диэтиловый эфир, диоксан и тетрагидрофуран. Могут применяться также и смеси названных растворителей. В качестве оснований пригодны в основном неорганические соединения, такие, как гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, азиды щелочных металлов, такие как гексаметилдизилацид лития, металлорганические соединения, в частности, алкилы щелочных металлов, такие как метиллитий, бутиллитий и фениллитий, а также алкоголяты щелочных и щелочно-земельных металлов, такие как метанолат натрия, этанолат натрия, этанолат калия, трет-бутанолат калия, трет.-пентанолат калия и диметоксимагний, кроме того, органические основания, например третичные амины, такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин и N-метилпиперидин, пиридин, замещенные пиридины, такие как коллидин, литидин и 4-диметиламинопиридин, также бициклические амины. Особенно предпочтительны гидрид натрия, триэтиламин, гексаметилдизилацид лития и диизопропилэтиламин лития. Основания применяются в общем в эквимолярных количествах, они могут также применяться в каталитических количествах, в избытке или, в случае необходимости, в качестве растворителей. Исходные продукты подвергаются взаимодействию друг с другом в эквимолярных количествах. Может быть благоприятным применение оснований и/или гетероциклилкарбонильных соединений формулы VII в избытке в пересчете на производные глицина формулы VIII. Переработка и выделение продуктов может осуществляться известным самим по себе образом. Необходимые для получения соединений I производные глицина формулы VIII могут быть приобретены на рынке и известны из литературных источников [например, из H. Pessoa-Mahana et al., Synth.Comm. 32, 1437 (2002] или могут быть получены согласно цитируемым литературным источникам. Отщепление защитной группы с получением фенилаланинов формулы V, где R4 означает гидрокси,осуществляется известными в литературных источниках методами [ср. J.-F. Rousseau et al., J. Org. Chem. 63, 2731-2737 (1998; J. M. Andres, Tetrahedron 56, 1523 (2000)]; в случае, еслиозначает бензил, посредством гидрогенолиза, предпочтительно водородом и Pd/C в метаноле; в случае, еслиозначает- 22011928 трет.-бутил, посредством кислоты, предпочтительно соляной кислоты в диоксане. Взаимодействие фенилаланинов формулы V, где R4 означает гидрокси, с гетероарильной кислотой(производными) IV с получением производных гетероароила формулы III, где R4 означает гидрокси,осуществляется обычно аналогично приведенному в А взаимодействию фенилаланинов формулы V с гетероарильной кислотой (производными) формулы III с получением производных гетероароила III. Производные гетероароила формулы III, где R4 означает гидрокси, подвергаются затем взаимодействию с аминами формулы II аналогично способу А с получением целевых замещенных гетероароилом фенилаланинамидов формулы I, где R4 означает гидрокси, которые потом могут дериватизироваться с соединениями формулы IX в замещенные гетероароилом фенилаланин-амиды формулы I, где R4 =OR11 [ср. , например, публикацииYokokawa, F. et al., Tetrahedron Lett. 42 (34), 5903-5908 (2001); Arrault, A. et al., Tetrahedron Lett. 43( 22), 40414044(2002)]. Производные гетероароила формулы III, где R4 означает гидрокси, могут сначала дериватизироваться с соединениями формулы IX в дальнейшие производные гетероароила формулы III [ср., например,Troast D. et al., Org. Lett. 4 (6), 991-994 (2002); Ewing W. et al., Tetrahedron Lett., 30 (29), 3757-3760 (1989);Paulsen H. et al., Liebigs Ann. Chem. 565 (1987)] и затем аналогично способу А подвергаться взаимодействию с аминами формулы II с получением целевых замещенных гетероароилом фенил-аланин-амиды формулы I, где R4=OR11:L1 означает нуклеофильно вытесняемую, уходящую группу, например гидрокси или C1-С 6-алкокси.L3 означает нуклеофильно вытесняемую, уходящую группу, например галоген, гидрокси, или C1-С 6 алкокси. Взаимодействие производных гетероароила формулы III, где R4 означает гидрокси, соответственно,11OR с аминами формулы II с получением замещенных гетероароилом фенилаланин-амидов формулы I,где R4 означает гидрокси, соответственно,OR11 обычно осуществляется аналогично описанной в А реакции взаимодействия производных гетероароила формулы III с аминами формулы II. Взаимодействие производных гетероароила формулы III, где R4 означает гидрокси, соответственно,замещенные гетероароилом фенилаланинамиды формулы I, где R4 означает гидрокси, с соединениями формулы IX с получением производных гетероароила формулы III, где R4=OR11, соответственно, замещенных гетероароилом фенилаланинамидов формулы I, где R4=OR11, осуществляется обычно при температуре от 0 до 100C, предпочтительно от 10 до 50C, в инертном органическом растворителе в присутствии основания [ср., например, публикации Troast, D. et al., Org. Lett. 4 (6), 991-994 (2002); Ewing W. etal., Tetrahedron Lett., 30 (29), 3757-3760 (1989); Paulsen, H. et al., Liebigs Ann. Chem. 565(1987)]. Пригодными растворителями являются алифатические углеводороды, такие как пентан, гексан,циклогексан и смеси С 5-С 8-алканов, ароматические углеводороды, такие как бензол, толуол, о-, и- и пксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет.-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран, нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон, метилэтилкетон, диэтилкетон и трет-бутилметилкетон, спирты, такие как метанол, этанол, н-пропанол, изо- 23011928 пропанол, н-бутанола и трет.-бутанол, а также диметилсульфоксид, диметилформамид, диметилацетамид, особенно предпочтительны дихлорметан, трет.-бутилметиловый эфир, диоксан и тетрагидрофуран. Могут применяться также и смеси приведенных растворителей. В качестве оснований пригодны в основном неорганические соединения, такие как гидроксиды щелочных и щелочно-земельных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, оксиды щелочных и щелочно-земельных металлов, такие как оксид лития, оксид натрия, оксид кальция и оксид магния, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития , гидрид натрия, гидрид калия и гидрид кальция, амиды щелочных металлов, такие как амид лития, амиид натрия и амид калия, карбонаты щелочных и щелочно-земельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, металлорганические соединения, в частности, алкилы щелочных металлов,такие как метиллитий, бутиллитий и фениллитий, а также алкоголяты щелочных и щелочно-земельных металлов, такие как метанолат натрия, этанолат натрия, этанолат калия, трет-бутанолат калия, трет.пентанолат калия и диметоксимагний, кроме того, органические основания, например третичные амины,такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, и N-метилпиперидин,пиридин, замещенные пиридины, такие как коллидин, литидин и 4-диметиламинопиридин, также бициклические амины. Особенно предпочтительны гидроксид натрия, гидрид натрия и триэтиламин. Основания в общем применяются в эквимолярных количествах. Они могут также применяться каталитически, в избытке или, в случае необходимости, в качестве растворителя. Исходные продукты подвергаются взаимодействию друг с другом в общем в эквимолярных количествах. Может быть благоприятным применение основания и/или соединения IX в избытке, в пересчете на соединение III, соответственно, I. Переработка и выделение продуктов может осуществляться известным самим по себе образом. Требуемые для получения соединения формулы VIII могут быть приобретены на рынке. Способ С. Производные гетероила формулы III, где R4 означает гидрокси, могут быть также получены таким образом, что соединения аминомалонила формулы XI ацилируют гетероарильной кислотой (производными) формулы IV в соответствующие соединения N-ацил-аминомалонила формулы X и затем конденсируют с гетероциклилкарбонильным соединением формулы VII при декарбоксилированииL1 означает нуклеофильно вытесняемую уходящую группу, например гидрокси или C1-С 6-алкокси.L2 означает нуклеофильно вытесняемую уходящую группу, например, гидрокси, галоген, C1-С 6 алкилкарбонил, C1-С 6-алкоксикарбонил, C1-С 6-алкилсульфонил, форсфорил или изоуреил.L4 означает нуклеофильно вытесняемую уходящую группу, например гидрокси или C1-С 6-алкокси. Алкилирование соединений аминомалонила формулы XI гетероарильной кислотой(производными) формулы V в соответствующие соединения N-ациламиномалонгила формулы X обычно осуществляется аналогично приведенной в А реакции взаимодействия фенилаланинов формулы V гетероарильной кислотой (производными) формулы IV с получением соответствующих производных гетероаролила формулы III. Взаимодействие соединений N-ацил-аминомалонила формулы X с гетероциклилкарбонильными соединениями формулы VII с получением производных гетероароила формулы III, где R4 означает гидрокси, осуществляется обычно при температуре от 0 до 100C, предпочтительно от 10 до 50C, в инертном органическом растворителе в присутствии основания [см. например, US 4904674; Hellmann, H. et al., Liebigs Ann. Chem. 631, 175-179 (1960)] В том случае, если L4 в соединениях N-ацил-аминомалонила формулы X означает C1-С 6-алкокси,благоприятно сначала переводить L4 путем омыления сложного эфира [например, согласно Hellmann, H.et al., Liebigs Ann. Chem. 631, 175-179 (1960)] в гидроксигруппу. Пригодными растворителями алифатические углеводороды, такие как пентан, гексан, циклогексан и смеси С 5-С 8-алканов, ароматические углеводороды, такие как бензол, толуол, о-, и- и п-ксилол, галогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры, такие как диэтиловый эфир, диизопропиловый эфир, трет-бутилметиловый эфир, диоксан, анизол и тетрагид- 24011928 рофуран, нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон, метилэтилкетон,диэтилкетон и трет-бутилметилкетон, спирты, такие как метанол, этанол, н-пропанол, изопропанол, нбутанол и трет.-бутанол, а также диметилсульфоксид, диметилформамид, диметилацетамид, особенно предпочтительны диэтиловый эфир, диоксан и тетрагидрофуран. Могут применяться также и смеси приведенных растворителей. В качестве оснований пригодны в основном неорганические соединения, такие как гидроксиды щелочных и щелочноземельных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид кальция, оксиды щелочных и щелочно-земельных металлов, такие как оксид лития, оксид натрия, оксид кальция и оксид магния, гидриды щелочных и щелочно-земельных металлов, такие как гидрид лития, гидрид натрия, гидрид калия и гидрид кальция, амиды щелочных металлов, такие как амид лития, амиид натрия и амид калия, карбонаты щелочных и щелочно-земельных металлов, такие как карбонат лития, карбонат калия и карбонат кальция, а также гидрокарбонаты щелочных металлов, такие как гидрокарбонат натрия, металлорганические соединения, в частности, алкилы щелочных металлов, такие как метиллитий, бутиллитий и фениллитий, а также алкоголяты щелочных и щелочно-земельных металлов, такие как метанолат натрия, этанолат натрия, этанолат калия, трет-бутанолат калия, трет.пентанолат калия и диметоксимагний, кроме того, органические основания, например третичные амины,такие как триметиламин, триэтиламин, диизопропилэтиламин, N-метилморфолин, и N-метилпиперидин,пиридин, замещенные пиридины, такие как коллидин, литидин и 4-диметиламинопиридин, также бициклические амины. Особенно предпочтительны гидроксид натрия, диизопропилэтиламин и триэтиламин. Основания в общем применяются в каталитических количествах. Они могут также применяться эквимолярно, в избытке или, в случае необходимости, в качестве растворителя. Исходные продукты подвергаются взаимодействию друг с другом в общем в эквимолярных количествах. Может быть благоприятным применение основания в избытке, в пересчете на соединение X. Переработка и выделение продуктов может осуществляться известным самим по себе образом. Полученные таким образом производные гетероароила формулы III, где R4 означает гидрокси, могут превращаться согласно способам А, соответственно, В в целевые замещенные гетероароилом фенилаланин-амиды формулы I, где R4 означает OR11. Требуемые соединения аминомалонила формулы XI могут быть приобретены на рынке, соответственно, известны из литературных источников [например, US 4904674; Hellmann, H. et al., Liebigs Ann.Chem. 631, 175-179 (1960)] или могут быть получены согласно цитируемым литературным источникам. Требуемые гетероциклические соединения формулы VII могут быть приобретены на рынке. Способ D. Производные гетероароила формулы III, где R4 означает гидрокси и R5 означает водород, могут быть получены таким образом, что кетосоединения формулы XIII сначала ацилируют гетероарильной кислотой (производными) IV в соотвествующие N-ацил-кетосоединения формулы XII и затем восстанавливают кетогруппу [Girard A, Tetrahedron Lett. 37(44),7967-7970(1996); Nojori R., J. Am. Chem. Soc. 111(25),9134-9135(1989); Schmidt U., Synthesis (12),1248-1254 (1992); Bolhofer, A.; J. Am. Chem. Soc. 75,4469 (1953)]:L1 означает нуклеофильно вытесняемую уходящую группу, например, гидрокси или C1-С 6-алкокси.L2 означает нуклеофильно вытесняемую уходящую группу, например, гидрокси, галоген, С 1-С 6 алкилкарбонил, C1-С 6-алкоксикарбонил, C1-С 6-алкилсульфонил, фосфорил или изоуреил. Ацилирование кетосоединений формулы XIII гетероарильной кислотой(производными) формулыIV в N-ацил-кетосоединения формулы XII обычно осуществляется аналогично приведенному в способе А взаимодействию фенилаланинов формулы V с гетероарильной кислотой(производными) формулы IV с получением соответствующих производных гетероароила формулы III. Требуемые для получения производных гетероароила формулы III, где R4 означает гидрокси и R5 означает водород, кетосоединения формулы XIII известны из литературных источников [WO 02/083111;al, Synthetic Communications 2 (4), 237-242 (1972)] или могут быть получены согласно цитируемым литературным источникам. Восстановление N-ацил-кетосоединений формулы XII в производные гетероароила формулы III, гдеR4 означает гидрокси и R5 означает водород, осуществляется обычно при температуре от 0 до 100C,предпочтительно от 20 до 80C, в инертном органическом растворителе в присутствии агента восстановления. Пригодными растворителями являются алифатические углеводороды, такие как пентан, гексан,циклогексан и смеси С 5-С 8-алканов, ароматические углеводороды, такие как толуол, о-, м- и п-ксилол,глогенированные углеводороды, такие как метиленхлорид, хлороформ и хлорбензол, простые эфиры,такие, как диэтиловый эфир, диизопропиловый эфир, трет.-бутилметиловый эфир, диоксан, анизол и тетрагидрофуран, нитрилы, такие как ацетонитрил и пропионитрил, кетоны, такие как ацетон , метилэтилкетон, диэтилкетон и трет.-бутилметиловый кетон, спирты, такие как метанол, этанол, н-пропанол, изопропанол, н-бутано и трет.-бутано, а также диметилсульфоксид, диметилформамид и диметилацетамид,особенно предпочтительно толуол, метиленхлорид или трет.-бутилметиловый эфир. Могут применяться смеси приведенных растворителей. В качестве агента восстановления пригодны, например, боргидрид натрия, боргидрид цинка, цианоборгидрид натрия, триэтилборгидрид лития (Superhydrid), три-втор.-бутилборгидрид лития (LSelectrid), Litiumaluminiumhydrid или Boran [vgl. z.B. WO 00/20424; Marchi, С. et al., Tetrahedron 58 (28),5699 (2002); Blank, S. et al., Liebigs Ann. Chem. (8), 889-896 (1993); Kuwano, R. et al., J. Org .Chem. 63 (10),3499-3503 (1998); Clariana, J. et al., Tetrahedron 55 (23), 7331-7344 (1999)]. Восстановление может также осуществляться в присутствии водорода и катализатора. В качестве катализатора пригодны, например [Ru(BINAP)Cl2] или Pd/C [ср. Noyori, R. et al., J. Am. Chem. Soc. 111(25), 9134-9135 (1989); Bolhofer, A. et al., J. Am. Chem. Soc. 75, 4469 (1953)]. Наряду с этим восстановление может осуществляться также и в присутствии микроорганизма. В качестве микроорганизма пригоден, например, Saccharomyces Rouxii [vgl. Soukup, M. et al., Helv. Chim.N-ацил-кетосоединения формулы XII и соответствующий агент восстановления в общем подвергаются взаимодействию друг с другом в эквимолярных количествах. Может быть благоприятным применение агента восстановления в избытке, в пересчете на соединение формулы XII. Переработка и выделение продуктов осуществляется известным образом. Полученные таким образом производные гетероароила формулы III, где R4 означает гидрокси и R5 означает водород, могут затем превращаться согласно вышеприведенному способу А и В в целевые замещенные гетероароилом фенилаланин-амиды I, где R4 =OR11. Производные гетероароила формулы III где A, R1 и R4 -R10 имеют приведенные выше значения, и L1 означает нуклеофильно вытесняемую,уходящую группу, например гидрокси или С 1-С 6-алкокси, также являются объектом настоящего изобретения. Особенно предпочтительные формы выполнения промежуточных продуктов в отношении заместителей соответствуют остаткам A, R1 и R4 до R10 формулы I. Особенно предпочтительны производные гетероароила формулы III, в которой А означает 5- или 6 членный гетероароил, выбранный из группы, включающей тиенил, ферил, пиразолил, имидазолил, тиазолил, оксазолил и пиридил; причем названные гетероароил-остатки могут быть частично или полностью галогенированы и/или могут иметь до 3 остатков, выбранных из группы, включающей C1-С 6-алкил, С 3 С 6-циклоалкил, и C1-С 6-галогеналкил;R6 водород, фтор или СН 3;R11 означает водород,С 1-С 4-алкилкарбонил,С 1-С 4-алкиламинокарбонил,ди-(С 1-С 4 алкил)аминокарбонил, фениламинокарбонил, N-(C1-С 4-алкил)-N-(фенил)аминокарбонил, SO2CH3. Особенно предпочтительны производные гетероароила формулы III, в которой А означает С- 26011928 присоединенный пиразолил, выбранный из группы, включающей A1a до А 4 а, где причем стрелка показывает место присоединения и R16 означает C1-С 6-алкил;R17 означает водород, галоген, C1-С 6-алкил или C1-С 6-галогеналкил; особенно предпочтительно водород, С 1-С 4-алкил или С 1-С 4-галогеналкил; в частности предпочтительно водород или С 1-С 4-алкил; чрезвычайно предпочтительно водород; иR18 - C1-С 6-алкил или C1-С 6-галогеналкил; особенно предпочтительно С 1-С 4-алкил или С 1-С 4 галогеналкил; в частности предпочтительно С 1-С 4-галогеналкил; чрезвычайно предпочтительно CF3; особенно предпочтительно A1a, А 2 а, или А 3 а,причем R16 до R18 имеют значения как определено выше; чрезвычайно предпочтительно A1a или А 2 а,причем R16 до R18 имеют значения, как определено выше;R6 водород, фтор или СН 3; 10,0 г (55.2 ммоль) DL-трео-3-фенилсерингидрата подают в раствор из 1.1 г (27.6 ммоль) NaOH в воде. К раствору прикапывают одновременно 3.3 г (83 ммоль) NaOH в воде и 11.7 н (55 ммоль) 1-метил 3-трифторометил-1 Н-пиразол-4-карбонилхлорида, так что раствор остается слабо щелочным и не превышает температуру 30C. Полученный раствор перемешивают при комнатной температуре 48 ч, затем при охлаждении льдом прикапывают 75 мл концентрированной соляной кислоты. Образовавшийся осадок отсасывают, промывают и сушат. Получают 15,7 г указанного в заголовке соединения в качестве бесцветных кристаллов. 1 Н-ЯМР (DMSO):= 8,50 (s, 1H); 7,95 (d, 1H); 7,1-7,5 (m, 5H); 5,25 (d, 1H); 4,70 (dd, 1H); 3,95 (s,3H). 1.2) -(2-гидрокси-1-метилкарбамоил-2-фенилэтил)амид 1-метил-3-трифторометил-1 Н-пиразол-4 карбоновой кислоты 15,7 г (43,8 ммоль) 3-гидрокси-2-[(1-метил-3-трифторометил-1 Н-пиразол-4-карбонил)амино]-3 фенилпропионовой кислоты растворяют в тетрагидрофуране. Добавляют при -20C 8,9 г (87,7 ммоль) Nметилморфолина, растворенного в тетрагидрофуране и затем 12,0 г (87,7 ммоль) сложного изобутилового эфира хлормуравьиной кислоты, растворенной в тетрагидрофуране. После дополнительного перемешивания в течение 10 мин прикапывают 34,0 г (438 ммоль) 40%-ого раствора метиламина в воде. Через 2- 27011928 ч при -20C прикапывают 100 мл 5%-го раствора NaHCO3 и перемешивают в течение 30 мин при комнатной температуре. Осадок отфильтровывают, промывают и сушат. Получают 13,1 г указанного в заголовке соединения в качестве бесцветных кристаллов. 1 Н-ЯМР (DMSO):= 8,50 (s, 1H); 7,2-7,9 (m, 7H); 6,75 (brs, 1H); 5,15 (brs, 1H); 4,55 (dd, 1H); 4,00 (s,3H); 2,60 (d, 3H). 1.3) 2-метилкарбамоил-2-[(1-метил-3-трифторометил-1 Н-пиразол-4-карбонил)амино]-1-фенилэтиловый эфир 2,2-диметилпропионовой кислоты (табл. 4,4.15) 0,5 г (1,35 ммоль) (2-гидрокси-1-метилкарбамоил-2-фенилэтил)амид 1-метил-3-трифторометил-1 Нпиразол-4-карбоновой кислоты растворяют в пиридине. Затем при комнатной температуре прикапывают 0,20 г (1,71 ммоль) хлорангидрида пивалиновой кислоты и добавляют на кончике шпателя 4 диметиламинопиридина. Через 24 ч при комнатной температуре добавляют еще раз 0,06 г пивалоилхлорида и перемешивают в течение 3 ч при комнатной температуре. К реакционной смеси добавляют лед,подкисляют 10%-ой соляной кислотой, экстрагируют метиленхлоридом. Органическую фазу промывают,сушат и концентрируют. После хроматографической чистки (силикагель, циклогексан/этилацетат) получают 183 мг указанного в заголовке соединения в качестве бесцветных кристаллов. 1 Н-ЯМР (DMSO):= 8,50 (s, 1H); 8,35 (d, 1H); 8,0 (q, 1H); 7,2-7,5 (m, 5H); 6,0 (d, 1H); 5,0 (q, 1H); 4,0[2-(бензилформиламино)-1-метилкарбамоил-2-фенилэтил]амид 1-метил-3-трифторометил-1 Нпиразол-4-карбоновой кислоты (табл. 4,4.23) 2.1) сложный этиловый эфир 1-бензил-5-фенил-4,5-дигидро-1 Н-имидазол-4-карбоновой кислоты 25,7 г (0,1305 моль) бензилиденбензиламина растворяют в этаноле и прикапывают 15,2 г (0,1305 моль) сложного этилового эфира изоцианоуксусной кислоты. Раствор нагревают с обратным холодильником в течение 16 ч. После удаления растворителя и сушки получают 40,2 г указанного в заголовке соединения в качестве басцветного масла. 1 Н-ЯМР (DMSO):=7,1-7,4 (m, HH); 4,6 (d, 1H); 4,5 (d, 1H); 4,3 (d, 1H); 4,1 (q, 2H); 3,8 (d, 1H); 1,1 (t,3H). 2.2) 2-амино-3-(бензилформиламино)-3-фенилпропионовая кислота 14,8 г (0,048 моль) сложного этилового эфира 1-бензил-5-фенил-4,5-дигидро-1 Н-имидазол-4 карбоновой кислоты нагревают с обратным холодильником в 47%-ом HBr-растворе в течение 3 ч. Растворитель удаляют, остаток смешивают с водой и фильтруют. Растворители удаляют, остаток загружают в этанол и разбавляют диэтиловым эфиром. Суспензию фильтруют и удаляют растворитель. Получают 14,0 г указанного в заголовке соединения, которое применяют на следующей стадии без очистки. 2.3) сложный метиловый эфир 2-амино-3-(бензилформиламино)-3-фенилпропионовой кислоты 13,5 г (0,04 моль) 2-амино-3-(бензилформиламино)-3-фенилпропионовой кислоты растворяют в метаноле и прикапывают 7,1 г (0,06 моль) тианилхлорида и 1 каплю митериформамида. Через 20 ч удаляют растворитель, остаток суспендируют в диэтиловом эфире и при перемешивании добавляют 5%-ый раствор NaHCO3. Органическую фазу отделяют, промывают и сушат. После удаления растворителя получают 4,0 г указанного в заголовке соединения в качестве бесцветного масла, которое применяют на следующей стадии без очистки. 2.4) сложный метиловый эфир 3-(бензилформиламино)-2-[(1-метил-3-трифторометил-1 Н-пиразол 4-карбонил)амино]-3-фенилпропионовой кислоты 2,3 г (0,0075 моль) сложного метилового эфира 2-амино-3-(бензилформиламино)-3-фенилпропионовой кислоты растворяют в метиленхлориде. К реакционной смеси добавляют 1,46 г (0,0075 моль) 1-метил-3-трифторометил-1H-пиразол-4-карбоновой кислоты, а также 1,52 г (0,015 моль) триэтиламина в тетрагидрофуране. Потом добавляют при 0-5C 1,78 г (0.0075 моль) бис(2-оксо-3 оксазолидинил)фосфорилхлорида. Через 3 ч при 0C в течение 15 ч перемешивают при комнатной температуре. Растворитель удаляют, остаток загружают в метиленхлорид, промывают и сушат. После удаления растворителя и хроматографической чистки (силикагель, циклогексан/этилацетат) получают 3,0 г указанного в заголовке соединения в качестве бесцветного масла. 1 Н-ЯМР (DMSO):= 9,10 (d, 1H); 8,51 (s, 1H); 8,38 (s, 1H); 6,8-7,4 (m, 10 Н); 5,50 (t, 1 Н);5,15 (d, 1H); 4,40 (d, 1H); 4,30 (d, 1H); 3,95 (s, 3H); 3,80 (s, 3H). 2.5) [2-(бензилформиламино)-1-метилкарбамоил-2-фенилэтил]амид 1-метил-3-трифторометил-1 Нпиразол-4-карбоновой кислоты (табл. 4,4.23) 2,4 г (0,0049 моль) сложного метилового эфира 3-(бензилформиламино)-2-[(1-метил-3 трифторометил-1 Н-пиразол-4-карбонил)амино]-3-фенилпропионовой кислоты растворяют в метаноле. При 0C в реакционный раствор вводят метиламин-газ.Через 1 ч нагревают в течение 0,5 ч до комнатной температуры. Удаляют растворитель и остаток промывают небольшим количеством метанола и нгексаном. Получают 980 мг указаного в заголовке соединения в качестве бесцветных кристаллов. 1 Н-ЯМР (DMSO):= 8,80 (d, 1H); 8,51 (s, 1H); 8,40 (s, 1H); 8,38 (m, 1H); 6,7-7,4 (т, 10 Н); 5,50 (t, 1H); 5,07 (d, 1H); 4,45 (d, 1H); 4,15 (d, 1H); 3,95 (s, 3H); 2,35 (d, 3H). Пример 3. 3-хлоро-2-трифторметилбензойная кислота 1,03 г (42,4 ммоль) обломков магния растворяют в тетрагидрофуране. К реакционной смеси добавляют 2 капли 1,2-дибромметана и реакционную смесь перемешивают после начала экзотермической ре- 29011928 акции при 32-35C при охлаждении льдом. Затем прикапывают 10,0 г (38,5 ммоль) 1-бром-3-хлор-2 трифторметилбензола в тетрагидрофуране таким образом, что температура не превышает 32 С. Реакционную смесь перемешивают 30 мин, охлаждают до 0C и в течение 2 ч вводят диокид углерода. Затем нагревают до комнатной температуры и еще в течение 2 ч СО 2. Реакционный раствор выливают на смесь из 1M соляной кислоты и льда и экстрагируют метилтрет-бутиловым эфиром. Органическую фазу потом экстрагируют посредством 1M NaOH, водную фазу подкисляют концентрированной соляной кислотой и экстрагируют метиленхлоридом. После сушки и дистиляционного удаления растворителя получают 7,7 г (84 % теории) указанного в заголовке соединения в качестве бесцветных кристаллов (Т.пл. 110C). В нижеследующих табл. 2, 3, 4 и 5 наряду с вышестоящими соединениями приведены еще другие производные III, а также замещенные гетероароилом фенилаланин-амиды I, которые получены или могут быть получены аналогично вышеописанным способам.
МПК / Метки
МПК: A01N 43/08, C07D 213/81, C07D 207/34, A01N 43/56, C07D 213/82, C07D 231/14, A01N 43/10, C07D 333/38, C07D 307/68, A01N 43/78, C07D 277/56
Метки: фенилаланин-амиды, гетероароилом, замещённые
Код ссылки
<a href="https://eas.patents.su/30-11928-zameshhyonnye-geteroaroilom-fenilalanin-amidy.html" rel="bookmark" title="База патентов Евразийского Союза">Замещённые гетероароилом фенилаланин-амиды</a>
Предыдущий патент: Способ выделения золота из тугоплавких сульфидных руд и концентратов
Следующий патент: Соединения 1-(азолин-2-ил)амино-1,2-дифенилэтана для борьбы с насекомыми, паукообразными и нематодами
Случайный патент: Полиморфные модификации телмисартана, способ их получения и их применение для изготовления лекарственного средства