Гетероциклокарбоксамидные производные
Номер патента: 10264
Опубликовано: 30.06.2008
Авторы: Вальтер Харальд, Эренфройнд Йозеф, Тоблер Ханс
Формула / Реферат
1. Соединение формулы (I)

в которой Het обозначает пирролил или пиразолил, которые замещены группами R8, R9 и R10;
X обозначает простую связь;
Y обозначает (CR12R13)(CR14R15)m(CR16R17)n;
m обозначает 0 или 1;
n обозначает 0 или 1;
R1 обозначает водород;
R2 и R3 в каждом случае независимо друг от друга обозначают водород, галоген, С1-С4алкил, С1-С4алкокси или С1-С4галоалкокси;
R4, R5, R6 и R7 в каждом случае независимо друг от друга обозначают водород, галоген, С1-С4алкил, С1-С4галоалкил, С1-С4алкокси, С1-С4галоалкокси, С1-С4алкилтио, С1-С4галоалкилтио, гидроксиметил, С1-С4алкоксиметил, С(О)СН3 или С(О)ОСН3;
R8, R9 и R10 в каждом случае независимо друг от друга обозначают водород, галоген, циано, нитро, С1-С4алкил, С1-С4галоалкил, С1-С4алкокси(С1-С4)алкилен или С1-С4галоалкокси(С1-С4)алкилен, при условии, что по меньшей мере одна из групп R8, R9 и R10 не обозначает водород;
R12 и R13 в каждом случае независимо друг от друга обозначают водород, галоген, С1-С5алкил, С1-С4алкокси, СН2ОН, С3-С6циклоалкил, СН2О-С(=О)СН3, СН2-С3-С6циклоалкил или бензил;
или R12 и R13 вместе с атомом углерода, к которому они присоединены, образуют группу С=О или 3-5-членное карбоциклическое кольцо;
или R12 и R13 вместе образуют С1-С6алкилиденовую группу или С3-С6циклоалкилиденовую группу; и
R14, R15, R16 и R17 в каждом случае независимо друг от друга обозначают водород или СН3.
2. Соединение формулы (I) по п.1, где R8, R9 и R10 в каждом случае независимо друг от друга обозначают водород, хлор, фтор, метил, CF3, CHF2 или CH2F, при условии, что по меньшей мере одна из групп R8, R9 и R10 не обозначает водород;
3. Соединение формулы (I) по п.1, где m равно 0 и n равно 0.
4. Соединение формулы (I) по п.3, где R12 и R13 в каждом случае независимо друг от друга обозначают водород, С1-С4алкил или С1-С4алкокси.
5. Соединение формулы (I) по п.1, где R2 обозначает водород, галоген или С1-С4алкил.
6. Соединение формулы (I) по п.1, где R3 обозначает водород или метил.
7. Соединение формулы (I) по п.1, где Het обозначает пиразолил.
8. (9-Изопроп-1,2,3,4-тетрагидро-1,4-метанонафтален-5-ил)амид 3-дифторметил-1-метил-1Н-пиразол-4-карбоновой кислоты
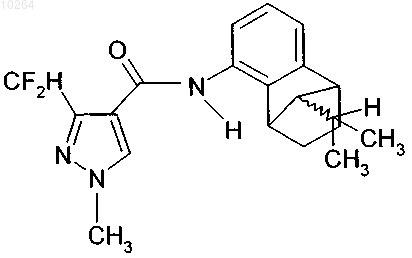
9. Соединение формулы (I) по п.1, где Het обозначает пирролил.
10. Композиция для борьбы с микроорганизмами и предупреждения их нападения и поражения ими растений, в которой действующее вещество представляет собой соединение формулы (I) по п.1 и которая содержит приемлемый носитель.
11. Способ борьбы с фитопатогенными микроорганизмами или предупреждения поражения ими культурных растений, который заключается в том, что соединения формулы (I) по п.1 наносят на листву или почву.
12. Способ борьбы с фитопатогенными микроорганизмами или предупреждения поражения ими культурных растений, который заключается в том, что соединения формулы (I) по п.1 наносят на затопленные рисовые поля.
13. Способ борьбы с фитопатогенными микроорганизмами или предупреждения поражения ими культурных растений, который заключается в том, что соединения формулы (I) по п.1 наносят на семена.
Текст
010264 Настоящее изобретение относится к новым производным трициклических аминов, которые обладают бактерицидной активностью, прежде всего фунгицидной активностью. Изобретение относится также к получению указанных соединений, к новым промежуточным продуктам, применяемым для получения таких соединений, к агрохимическим композициям, которые содержат в качестве действующего вещества по меньшей мере одно из новых соединений, к приготовлению указанных композиций и к применению действующих веществ или композиций в сельском хозяйстве или садоводстве для борьбы или предупреждения заражения растений фитопатогенными микроорганизмами, предпочтительно грибами. Настоящее изобретение относится к соединению формулы (I) в которой Het обозначает 5- или 6-членное гетероциклическое кольцо, содержащее 1-3 гетероатома, в каждом случае независимо друг от друга выбранных из кислорода, азота и серы, при условии, что кольцо не представляет собой 1,2,3-триазол, где кольцо замещено группами R8, R9 и R10; X обозначает простую или двойную связь; Y обозначает О, S, N(R11) или (CR12R13)(CR14R15)m(CR16R17)n; m обозначает 0 или 1; n обозначает 0 или 1; R1 обозначает водород, С 1-С 4 алкил, С 1-С 4 галоалкил, С 1-С 4 алкокси, С 1-С 4 галоалкокси,CH2CCR18, CH2CR19=CHR20, CH=C=CH2 или COR21; R2 и R3, в каждом случае независимо друг от друга,обозначают водород, галоген, С 1-С 4 алкил, С 1-С 4 алкокси или С 1-С 4 галоалкокси; R4, R5, R6 и R7, в каждом случае независимо друг от друга, обозначают водород, галоген, С 1-С 4 алкил, С 1-С 4 галоалкил, С 1 С 4 алкокси, С 1-С 4 галоалкокси, С 1-С 4 алкилтио, С 1-С 4 галоалкилтио, гидроксиметил, С 1-С 4 алкоксиметил,С(О)СН 3 или С(О)ОСН 3; R8, R9 и R10, в каждом случае независимо друг от друга, обозначают водород,галоген, циано, нитро, С 1-С 4 алкил, С 1-С 4 галоалкил, С 1-С 4 алкокси(С 1-С 4)алкилен или С 1 С 4 галоалкокси(С 1-С 4)алкилен, при условии, что по меньшей мере одна из групп R8, R9 и R10 не обозначает водород; R11 обозначает водород, С 1-С 4 алкил, бензил (в котором фенильная группа необязательно имеет вплоть до 3 заместителей, в каждом случае независимо друг от друга выбранных из галогена, С 1 С 4 алкила, С 1-С 4 галоалкила и С 1-С 4 алкоксигруппы), формил, С(О)С 1-С 4 алкил (необязательно замещенный галогеном или С 1-С 4 алкоксигруппой), С(=О)О-С 1-С 6 алкил (необязательно замещенный галогеном, С 1 С 4 алкокси- или цианогруппой) или С 1-С 4 алкокси(С 1-С 4)алкилен; R12, R13, R14, R15, R16 и R17 В каждом случае независимо друг от друга обозначают водород, галоген, гидрокси, С 1-С 6 алкил, С 2-С 6 алкенил [оба необязательно замещенные галогеном, гидрокси-, С 1-С 4 алкоксигруппой, =О, арилом или О-С(О)-С 1 С 4 алкилом или 3-7-членным карбоксильным кольцом (которое в свою очередь необязательно имеет в качестве заместителей вплоть до 3 метильных групп)], 3-7-членное насыщенное кольцо (которое необязательно имеет в качестве заместителей вплоть до 3 метильных групп и необязательно содержит один гетероатом, выбранный из азота и кислорода) или С 1-С 4 алкокси; или R12 и R13 вместе с атомом углерода,к которому они присоединены, образуют группу С=О или 3-5-членное карбоциклическое кольцо (которое необязательно имеет в качестве заместителей вплоть до 3 метильных групп и необязательно содержит вплоть до 2 гетероатомов, в каждом случае независимо друг от друга выбранных из О и N); или R12 иR13 вместе образуют С 1-С 6 алкилиденовую группу (которая необязательно имеет в качестве заместителей вплоть до 3 метильных групп) или С 3-С 6 циклоалкилиденовую группу (которая необязательно имеет в качестве заместителей вплоть до 3 метильных групп); R18, R19 и R20, в каждом случае независимо друг от друга, обозначают водород, галоген, С 1-С 4 алкил, С 1-С 4 галоалкил или С 1-С 4 алкокси(С 1-С 4)алкилен; и R21 обозначает водород, С 1-С 6 алкил, С 1-С 6 галоалкил, С 1-С 4 алкокси(С 1-С 4)алкилен, С 1-С 4 алкил-S-(С 1 С 4)алкилен, С 1-С 4 алкокси или арил. Галоген представляет собой фтор, хлор, бром или йод; предпочтительно фтор, хлор или бром. Каждый алкильный остаток может иметь прямую или разветвленную цепь и представляет собой,например, метил, этил, н-пропил, н-бутил, н-пентил, н-гексил, изопропил, н-бутил, втор-бутил, изобутил,трет-бутил, неопентил, н-гептил, 1,3-диметилбутил, 1,3-диметилпентил, 1-метил-3-этилбутил или 1,3,3 триметилбутил. Аналогично этому каждый алкиленовый остаток может иметь прямую или разветвленную цепь. Галоалкильные остатки или алкильные остатки, замещенные одним или несколькими одинаковыми или различными атомами галогена, представляют собой, например, CF3, CF2Cl, CHF2, CH2F, CCl3,CF3CH2, CHF2CH2, CH2FCH2, CH3CHF или CH3CF2. Алкенильные и алкинильные остатки могут иметь прямые или разветвленные цепи. Каждый алкенильный остаток, когда это возможно, может иметь либо (Е)-, либо (Z)-конфигурацию. 3-5-Членное карбоциклическое кольцо представляет собой спиро-3- или 5-членное кольцо. Арил представляет собой фенил, нафтил, антрацил, флуоренил и инданил, но предпочтительно обозначает фенил. Алкилиденовые остатки могут иметь прямые или разветвленные цепи. Алкилиден представляет со-1 010264 бой метилиден [СН 2=], этилиден [СН 3 С(Н)=], н-пропилиден, изопропилиден [(СН 3)2 С=], н-бутилиден,изобутилиден, 2-бутилиден, н-пентилиден, изопентилиден, неопентилиден, 2-пентилиден, н-гексилиден,2-гексилиден, 3-гексилиден, изогексилиден и неогексилиден. Циклоалкил представляет собой циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Циклоалкенил представляет собой циклобутенил, циклопентенил, циклогексенил и циклогептенил. Циклоалкилиден представляет собой циклопропилиден [ц(С 3 Н 4)=], циклобутилиден, циклопентилиден и циклогексилиден. В одном из объектов изобретения R11 обозначает водород, С 1-С 4 алкил, бензил (в котором фенильная группа необязательно имеет вплоть до 3 заместителей, в каждом случае независимо друг от друга выбранных из галогена, С 1-С 4 алкила, С 1-С 4 галоалкила и С 1-С 4 алкоксигруппы), формил, С(О)С 1-С 4 алкил или С 1-С 4 алкокси(С 1-С 4)алкилен. В другом объекте изобретения R12, R13, R14, R15, R16 и R17, в каждом случае независимо друг от друга, обозначают водород, С 1-С 4 алкил или С 1-С 4 алкокси.Het более предпочтительно обозначает пирролил, пиразолил, тиазолил, оксазолил, пиридинил или 2,3-дигидро[1,4]оксатиинил.Het еще более предпочтительно обозначает пирролил, пиразолил, тиазолил или пиридинил.Het наиболее предпочтительно обозначает пирролил или пиразолил. Предпочтительно X обозначает простую связь. В одном из объектов изобретения Y обозначает О, S, N(R11), СН 2, СН 2 СН 2, СН 2 СН 2 СН 2, С(СН 3)2,СН(СН 3), СН(С 2 Н 5), С(СН 3)(С 2 Н 5), СН(ОСН 3) или С(ОСН 3)2; предпочтительно N(R11), О, S, СН 2, СН 2 СН 2,СН 2 СН 2 СН 2, С(СН 3)2, СН(СН 3) или СН(С 2 Н 5); более предпочтительно N(R11), О, S, СН 2 или СН 2 СН 2 и наиболее предпочтительно О, СН 2 или N(R11). Предпочтительно Y обозначает О, N(R11) или (CR12R13)(CR14R15)m(CR16R17)n. Более предпочтительно Y обозначает О или (CR12R13)(CR14R15)m(CR16R17)n. Еще более предпочтительно Y обозначает (CR12R13)(CR14R15)m(CR16R17)n. Наиболее предпочтительно Y обозначает (CR12R13). Предпочтительно n обозначает 0. Предпочтительно m обозначает 0. Предпочтительно R1 обозначает водород, CH2CCR18, CH=C=CH2 или COR21. Более предпочтительно R1 обозначает водород, СН 2 ССН, СН=С=СН 2, С(О)Н или С(О)СН 3. Еще более предпочтительно R1 обозначает водород, CH2 ССН, СН=С=СН 2 или С(О)СН 3. Еще более предпочтительно R1 обозначает водород, СН 2 ССН или СН=С=СН 2. Наиболее предпочтительно R1 обозначает водород. Предпочтительно R2 обозначает водород, галоген или С 1-С 4 алкил. Более предпочтительно R2 обозначает водород или галоген. Наиболее предпочтительно R2 обозначает водород. Предпочтительно R3 обозначает водород или метил. Более предпочтительно R3 обозначает водород. Предпочтительно R4 обозначает водород, С 1-С 4 алкил, галоген, С 1-С 4 галоалкил, С 1-С 4 алкокси,С(О)СН 3 или С(О)ОСН 3. Более предпочтительно R4 обозначает водород, С 1-С 2 алкил, галоген, CF3, метокси, С(О)СН 3 или С(О)ОСН 3. Еще более предпочтительно R4 обозначает водород, метил, хлор, CF3 или метокси. Наиболее предпочтительно R4 обозначает водород или метил. Предпочтительно R5 обозначает водород, С 1-С 4 алкил, галоген, С 1-С 4 галоалкил, С 1-С 4 алкокси,С(О)СН 3 или С(О)ОСН 3. Более предпочтительно R5 обозначает водород, С 1-С 2 алкил, хлор, F3, метокси, С(О)СН 3 или С(О)ОСН 3. Наиболее предпочтительно R5 обозначает водород или метил. Предпочтительно R6 обозначает водород, С 1-С 4 алкил, С 1-С 4 алкокси или С(О)СН 3. Более предпочтительно R6 обозначает водород, метил, метокси или С(О)СН 3. Наиболее предпочтительно R6 обозначает водород или метил. Предпочтительно R7 обозначает водород, С 1-С 4 алкил, С 1-С 4 алкокси или С(О)СН 3. Более предпочтительно R7 обозначает водород, метил, метокси или С(О)СН 3. Наиболее предпочтительно R7 обозначает водород или метил. Предпочтительно R8 обозначает водород, галоген, С 1-С 4 алкил, С 1-С 4 галоалкил или метоксиметилен. Более предпочтительно R8 обозначает водород, хлор, фтор, бром, С 1-С 2 алкил, CF3, CF2Cl, CHF2,CH2F или метоксиметилен.-2 010264 Еще более предпочтительно R8 обозначает водород, хлор, фтор, С 1-С 2 алкил, CF3, CF2Cl, CHF2, CH2F или метоксиметилен. Наиболее предпочтительно R8 обозначает водород, хлор, фтор, метил, CF3, CHF2 или CH2F. Предпочтительно R9 обозначает водород, галоген, С 1-С 4 алкил или С 1-С 4 галоалкил или метоксиметилен. Более предпочтительно R9 обозначает водород, хлор, фтор, бром, С 1-С 2 алкил, CF3, CF2Cl, CHF2,CH2F или метоксиметилен. Еще более предпочтительно R9 обозначает водород, хлор, фтор, С 1-С 2 алкил, CF3, CF2Cl, CHF2, CH2F или метоксиметилен. Наиболее предпочтительно R9 обозначает водород, хлор, фтор, метил, CF3, CHF2 или CH2F. Предпочтительно R10 обозначает водород, галоген, С 1-С 4 алкил, С 1-С 4 галоалкил или метоксиметилен. Более предпочтительно R10 обозначает водород, хлор, фтор, бром, С 1-С 2 алкил, CF3, CF2Cl, CHF2,CH2F или метоксиметилен. Еще более предпочтительно R10 обозначает водород, хлор, фтор, С 1-С 2 алкил, CF3, CF2Cl, CHF2,CH2F или метоксиметилен. Наиболее предпочтительно R10 обозначает водород, хлор, фтор, метил, CF3, CHF2 или CH2F. В одном из объектов изобретения R11 обозначает водород, С 1-С 4 алкил, бензил, формил, С(О)СН 3 или С(О)ОС(СН 3)3; более предпочтительно водород или С 1-С 2 алкил. Предпочтительно R11 обозначает С 1-С 4 алкил, формил, С(О)СН 3 или С(О)ОС 1-С 6 алкил (необязательно замещенный галогеном, CN- или С 1-С 4 алкоксигруппой). Более предпочтительно R11 обозначает С(О)ОС 1-С 4 алкил. В одном из объектов изобретения R12, R13, R14, R15, R16 и R17, в каждом случае независимо друг от друга, обозначают водород, С 1-С 2 алкил или метокси. Предпочтительно R12 и R13, в каждом случае независимо друг от друга, обозначают водород, галоген, С 1-С 5 алкил, С 1-С 3 алкокси, СН 2 ОН, СН(О), С 3-С 6 циклоалкил, СН 2 О-С(=О)СН 3, СН 2-С 3-С 6 циклоалкил или бензил; или R12 и R13 вместе с атомом углерода, к которому они присоединены, образуют группу С=О или 3-5-членное карбоциклическое кольцо; или R12 и R13 вместе образуют С 1-С 5 алкилиден или С 3 С 6 циклоалкилиден. Более предпочтительно R12 и R13, в каждом случае независимо друг от друга, обозначают Н, СН 3,С 2 Н 5, н-С 3 Н 7, изоС 3 Н 7, н-С 4 Н 9, втор-С 4 Н 9, изоС 4 Н 9, СН(С 2 Н 5)2, СН 2-циклопропил или циклопентил; или в которой Y, R4, R5, R6 и R7 имеют значения, указанные выше для соединения формулы (I), можно применять в качестве промежуточных продуктов при получении соединений формулы (I). Некоторые соединения формулы (С) являются новыми, а другие уже описаны. Таким образом, другим объектом настоящего изобретения является соединение формулы (С), в которой Y обозначает О или S; и R4, R5, R6 и R7 каждый обозначает С(О)ОСН 3; или Y обозначает N(R11) или(CR12R13)(CR14R15)m(CR16R17)n; R4, R5, R6, R7, R14, R15, R16, R17, m и n каждый имеет значения, указанные выше для соединения формулы (I); R11 обозначает бензил (в котором фенильная группа необязательно имеет вплоть до 3 заместителей, в каждом случае независимо друг от друга выбранных из галогена, С 1 С 4 алкила, С 1-С 4 галоалкила и С 1-С 4 алкоксигруппы); и R12 и R13 вместе с атомом углерода, к которому они-3 010264 присоединены, образуют 3-5-членное карбоциклическое кольцо (которое необязательно имеет в качестве заместителей вплоть до 3 метильных групп и содержит 1 или 2 гетероатома, которые, в каждом случае независимо друг от друга, выбраны из О и N). Соединения формулы (D) в которой Y, R4, R5, R6 и R7 имеют значения, указанные выше для соединения формулы (I), можно также применять в качестве промежуточных продуктов при получении соединений формулы (I). Некоторые соединения формулы (D) являются новыми, а другие уже описаны. Таким образом, еще одним объектом настоящего изобретения является соединение формулы (D), в которой Y обозначает О или S; и R4, R5, R6 и R7 каждый обозначает С(О)ОСН 3; или Y обозначает N(R11) или (CR12R13)(CR14R15)m(CR16R17)n; R4, R5, R6, R7, R14, R15, R16, R17, m и n каждый имеет значения, указанные выше для соединения формулы (I); R11 обозначает бензил (в котором фенильная группа необязательно имеет вплоть до 3 заместителей, в каждом случае независимо друг от друга выбранных из галогена,С 1-С 4 алкила, С 1-С 4 галоалкила и С 1-С 4 алкоксигруппы); и R12 и R13 вместе с атомом углерода, к которому они присоединены, образуют 3-5-членное карбоциклическое кольцо (которое необязательно имеет в качестве заместителей вплоть до 3 метильных групп и содержит 1 или 2 гетероатома, которые в каждом случае независимо друг от друга выбраны из О и N). Соединения формул (I), (С) и (D) могут находиться в виде различных геометрических или оптических изомеров или в различных таутомерных формах. Под объем изобретения подпадают для каждой формулы все указанные изомеры и таутомеры и их смеси во всех пропорциях, а также изотопические формы, такие как дейтерированные соединения. Соединения, приведенные ниже в табл. 1-29, иллюстрируют соединения, предлагаемые в изобретении. В табл. 1 представлено 94 соединения формулы (С), в которой Y, R4, R5, R6 и R7 имеют значения,указанные в табл. 1. Таблица 1[когда Z обозначает 24], табл. 25 [когда Z обозначает 25], табл. 26 [когда Z обозначает 26], табл. 27 [когда Z обозначает 27], табл. 28 [когда Z обозначает 28] и табл. 29 [когда Z обозначает 29]. X обозначает либо простую связь (-), либо двойную связь (=). Таблица ZR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 3. В табл. 4 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 4. В табл. 5 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 5. В табл. 6 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 6. В табл. 7 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 7. В табл. 8 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 8. В табл. 9 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 9. В табл. 10 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 10. В табл. 11 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 11. В табл. 12 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 12. В табл. 13 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 13. В табл. 14 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 14. В табл. 15 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 15. В табл. 16 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 16. В табл. 17 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 17. В табл. 18 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 18. В табл. 19 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 19. В табл. 20 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 20. В табл. 21 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 21. В табл. 22 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 22. В табл. 23 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 23. В табл. 24 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 24. В табл. 25 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 25. В табл. 26 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 26. В табл. 27 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 27. В табл. 28 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 28. В табл. 29 представлено 235 соединений формулы (I), в которой Het обозначаетR2 и R3 оба обозначают водород и X, Y, R1, R4, R5, R6 и R7 имеют значения, указанные в табл. 29. В контексте настоящего описания температура дана в градусах Цельсия; ЯМР обозначает спектр ядерного магнитного резонанса; МС - масс-спектр и % обозначает мас.%, если не указано, что соответствующие концентрации даны в других единицах; син обозначает син-конфигурацию соответствующего заместителя относительно аннелированного бензольного конца; и анти относится к антиконфигурации соответствующего заместителя относительно аннелированного бензольного кольца. tnл обозначает температуру плавления; s обозначает синглет; d обозначает дублет; t обозначает триплет; m обозначает мультиплет; tкип обозначает температуру кипения; br обозначает уширенный (ушир.); dd обозначает дублет дублетов; q обозначает квартет; част./млн обозначает части на миллион. В табл. 30 представлены некоторые температуры плавления и некоторые ЯМР-спектры, все полученные с использованием CDCl3 в качестве растворителя (если не указано иное; если присутствует смесь растворителей, то она указана, например, [CDCl3/d6-ДМСО]), (не ставилась задача во всех случаях представить все характеристики) для соединений, представленных в табл. 1-29. Таблица 30 Соединения формулы (I) можно получать с помощью реакций, которые в обобщенном виде представлены ниже на схемах. Получение соединения формулы (I). Схема 1 Соединение формулы (I) [в которой R1 обозначает водород; и Het, R2, R3, R4, R5, R6, R7, X и Y имеют значения, указанные выше для соединения формулы (I)] можно синтезировать взаимодействием соединения формулы (II) [в которой Het имеет значения, указанные выше для соединения формулы (I), и R' обозначает С 1-С 5 алкил] с анилином формулы (III) [в которой R2, R3, R4, R5, R6, R7, X и Y имеют значения,указанные выше для соединения формулы (I)] в присутствии NaN(TMS)2 при температуре в интервале от-10 С до температуры окружающей среды, предпочтительно в безводном ТГФ, согласно методу, описан- 20010264 ному у J. Wang и др., Synlett, 2001, с. 1485. Схема 2 В альтернативном варианте соединение формулы (I) [в которой R1 обозначает водород; и Het, R2,R , R , R5, R6, R7, X и Y имеют значения, указанные выше для соединения формулы (I)] можно получать взаимодействием соединения формулы (II) [в которой Het имеет значения, указанные выше для соединения формулы (I)] с анилином формулы (III) [в которой R2, R3, R4, R5, R6, R7, X и Y имеют значения,указанные выше для соединения формулы (I)] в присутствии активатора [такого как ВОР-Cl] и двух эквивалентов основания [такого как триэтиламин] или взаимодействием соединения формулы (II") [в которой Het имеет значения, указанные выше для соединения формулы (I); и Q обозначает Cl, F или Br], которое получают из соединения формулы (II') обработкой галогенирующим агентом, таким как тионилхлорид, оксалилхлорид, фосген, SF4, ДАСТ (трифтористая диэтиламиносера), дезоксофтор или тионилбромид, с анилином формулы (III) [в которой R2, R3, R4, R5, R6, R7, X и Y имеют значения, указанные выше для соединения формулы (I)] в присутствии одного эквивалента основания [такого как NEt3, NaHCO3,KHCO3, Na2CO3 или K2CO3] в растворителе [таком как дихлорметан, этилацетат или ДМФ] предпочтительно при температуре в интервале от -10 до 30 С. Схема 3 3 Кроме того, соединение формулы (I) [в которой R1 обозначает водород и Het, R2-R7, X и Y имеют значения, указанные выше для соединения формулы (I)] подвергают взаимодействию с вариантами соединений формулы Z-R1 [в которой R1 имеет значения, указанные выше для соединения формулы (I), за исключением того, что не обозначает водород; и Z предпочтительно обозначает Cl, Br или I; или Z имеет такое значение, что Z-R1 представляет собой ангидрид, т.е. когда R1 обозначает COR, Z обозначает[таком как этилацетат или в двухфазной смеси [такой как смесь дихлорметан/вода] при температуре в интервале от -10 до 30 С. Исходные продукты. Гетероциклические кислоты и эфиры [т.е. соединения формулы (II') или (II)], как правило, известны из литературы или их можно синтезировать с помощью известных методов. Ортозамещенные аминобензонорбонены (включая их гомологи) формулы (С) или (D) (схема 4) можно получать посредством добавления по Дильсу-Альдеру полученного in situ бензина [например,используя в качестве исходного продукта 6-нитроантраниловую кислоту формулы (А), согласно методу,описанному у L. Paquette и др., J. Amer. Chem. Soc. 99, 1977, с. 3734, или другие приемлемые предшественники (см. Н. Pellissier и др., Tetrahedron, 59, 2003, с. 701] к 5-7-членному циклическому 1,4-диену с получением нитробензонорборнадина формулы (В) согласно методам или по аналогии с методами, которые описаны у L. Paquette и др., J. Amer. Chem. Soc. 99, 1977, с. 3734, D. Gravel и др., Can. J. Chem. 69,1991, с. 1193, J.R. Malpass и др., Tetrahedron, 48, 1992, с. 861, D.E. Lewis и др., Synthetic Communications,23, 1993, с. 993, R.N. Warrener и др., Molecules, 6, 2001, с. 353, R.N. Warrener и др., Molecules, 6, 2001, с. 194 или I. Fleming и др., J. Chem. Soc, Perkin Trans. 1, 1998, с 2645. Пригодными для осуществления этой стадии апротонными растворителями являются этилацетат, дихлорметан, ацетон, ТГФ и диметоксиэтан. Температура реакции находится в интервале от комнатной температуры до 100 С, предпочтительно в интервале 40-80 С. Для последующего осуществления избирательного восстановления нитрогруппы в соединении- 21010264 формулы (В) с получением аминобензонорборнадиена формулы (С) требуются мягкие условия [например, либо металлический цинк в присутствии хлорида аммония, либо амальгама алюминия]. Оба варианта метода осуществляют в протонных растворителях, таких как этанол, вода или их смеси. В альтернативном варианте соединение формулы (С) можно получать также из соединения формулы (В) путем каталитического гидрирования в присутствии в качестве катализатора модифицированного 5% Pt/C при повышенном давлении (10 бар) и повышенной температуре (100 С) в смеси толуол-вода. Каталитическое восстановление в стандартных условиях (например, в присутствии 5% Pd/C, или 5% Ra/Ni, или 5%Rh/C) в растворителе [таком как метанол, этанол, ТГФ или этилацетат] приводит к восстановлению обеих нитрогрупп и двойной связи и к получению бензонорборнена формулы (D). Предпочтительные реакционные условия включают температуру окружающей среды и нормальное давление. Схема 4 Некоторые из соединений формул (В), (С) и (D) описаны в литературе [см., например, , L.A.Kirby и др., J. Chem. Soc., Perkin Trans. 2, 1997, с. 1081]. Новые исходные продукты формул (С) или (D) можно синтезировать по аналогии со схемой 4 или согласно методам, приведенным в процитированных выше литературных ссылках. При создании изобретения неожиданно было установлено, что новые соединения формулы (I) можно применять на практике, они обладают очень ценным для защиты растений спектром активности в отношении болезней, которые вызываются грибами, а также бактериями и вирусами. Соединения формулы (I) можно использовать в сельскохозяйственном секторе и близких областях в качестве действующих веществ для борьбы с вредителями растений. Новые соединения обладают очень высокой активностью при низких нормах расхода, хорошо переносятся растениями и безопасны для окружающей среды. Они обладают очень ценным лечебным, профилактическим и системным действием и их можно применять для защиты многих видов культурных растений. С помощью соединений формулы(I) можно ингибировать или уничтожать вредителей, которые встречаются на различных видах культурных растений или на частях таких растений (плодах, цветках, листьях, стеблях, клубнях, корнях), при этом защита, например, от этих фитопатогенных микроорганизмов распространяется также на те части растения, которые формируются в более поздний период. Соединения формулы (I) можно использовать также в качестве протравителей, предназначенных для обработки материала для размножения растений, в частности, семян (плод, клубни, зерна) и проростков растений (например, риса) с целью защиты от заражения грибами, а также для защиты от обитающих в почве фитопатогенных грибов. Кроме того, соединения, предлагаемые в настоящем изобретении, можно применять для борьбы с грибами в родственных областях, например, для защиты технических материалов, включая древесину и технические продукты на основе древесины, при хранении продуктов и в гигиенических целях и т.д. Соединения формулы (I) обладают эффективностью, например, в отношении фитопатогенных грибов из следующих классов: несовершенные грибы (Fungi imperfecti) (например, представители p.p. Botrytis, Pyricularia, Helminthosporium, Fusarium, Septoria, Cercospora и Alternaria) и базидомицеты (Basidiomycetes) (например, представители p.p. Rhizoctonia, Hemileia, Puccinia). Кроме того, они обладают активностью также в отношении представителей класса аскомицетов (Ascomycetes) (например, p.p. Venturia иErysiphe, Podosphaera, Monilinia, Uncinula) и класса оомицетов (Oomycetes) (например, p.p. Phytophthora,Pythium, Plasmopara). Обнаружена очень высокая активность в отношении настоящей мучнистой росы(Erysiphe spp.). Кроме того, новые соединения формулы (I) обладают эффективностью в отношении фитопатогенных бактерий и вирусов (например, в отношении Xanthomonas spp, Pseudomonas spp, Erwiniaamylovora, а также в отношении вируса табачной мозаики).- 22010264 Согласно настоящему изобретению подлежащие защите целевые культурные растения включают,как правило, следующие виды растений: зерновые (пшеница, ячмень, рожь, овес, рис, кукуруза, сорго и родственные культуры); свекольные (сахарная свекла и кормовая свекла); семечковые, косточковые и ягодные культуры (яблони, груши, сливы, персики, миндаль, вишня, земляника, малина и ежевика); бобовые растения (бобы, чечевица, горох, соя); масличные культуры (рапс, горчица, мак, маслины, подсолнечниковые, кокос, клещевина, какао-бобы, арахис); огуречные растения (тыквы, огурцы, дыни); волокнистые растения (хлопчатник, лен, конопля, джут); цитрусовые культуры (апельсины, лимоны, грейпфруты, мандарины); овощные культуры (шпинат, салат, спаржа, капустные, моркови, луки, томаты, картофель, сладкий перец); лавровые культуры (авокадо, коричное дерево, камфорное дерево) или такие растения, как табак, орехи, кофе, баклажаны, сахарный тростник, чай, перец, виноград, хмель, бананы и природные каучуконосы, а также декоративные растения. Соединения формулы (I) применяют в немодифицированном виде или предпочтительно в сочетании с адъювантами, которые обычно используют для приготовления композиций. Для этой цели их принято включать с помощью известных методов в состав препаративных форм, таких как эмульгирующиеся концентраты, предназначенные для покрытия пасты, готовые к применению распыляемые растворы или разбавляемые растворы, разбавляемые эмульсии, смачивающиеся порошки, растворимые порошки,дусты, гранулы, или капсулированные, например, в полимерные вещества формы. Методы обработки,такие как опрыскивание, обработка в виде тумана, опыливание, разбрасывание, покрытие или полив,выбирают в зависимости от типа композиции, а также в соответствии с поставленными целями и конкретными условиями. Композиции могут содержать также дополнительные адъюванты, такие как стабилизаторы, противовспенивающие вещества, регуляторы вязкости, связующие вещества и прилипатели, а также удобрения или другие действующие вещества, предназначенные для достижения определенных целей. Приемлемые носители и адъюванты могут быть твердыми или жидкими и представляют собой вещества, которые можно использовать для приготовления препаративных форм, например природные или регенерированные минеральные субстанции, растворители, диспергирующие вещества, смачивающие вещества, прилипатели, загустители, связующие вещества или удобретения. Такие носители описаны,например, в WO 97/33890. Соединения формулы (I), как правило, применяют в виде композиций, и их можно применять для обработки посевной площади или растений, подлежащих обработке, одновременно или последовательно с другими действующими веществами. Эти другие действующие вещества могут представлять собой удобрения или доноры микроэлементов, или другие препараты, оказывающие влияние на рост растения. Можно применять также гербициды избирательного действия или инсектициды, фунгициды, бактерициды, нематоциды, моллюскициды или смеси, состоящие из нескольких этих препаратов, при необходимости вместе с другими носителями, поверхностно-активными веществами или другими способствующими нанесению адъювантами, которые обычно применяются для изготовления препаративных форм. Соединения формулы (I) можно смешивать с другими фунгицидами, в результате чего неожиданно может быть получено синергетическое действие. Особенно предпочтительными компонентами таких смесей являются азолы, такие как азаконазол,BAY 1412, битертанол, бромуконазол, ципроконазол, дифеноконазол, диниконазол, эпоксиконазол, фенбуконазол, флухинконазол, флусилазол, флутриафол, гексаконазол, имазалил, имибенконазол, ипконазол, метконазол, миклобутанил, перфуразоат, пенконазол, пирифенокс, прохлораз, пропиконазол, симеконазол, тебуконазол, тетраконазол, триадимефон, триадименол, трифлумизол, тритиконазол; пиримидинилкарбинолы, такие как анцимидол, фенаримол, нуаримол; 2-аминопиримидины, такие как бупримат,диметиримол, этиримол; морфолины, такие как додеморф, фенпропидин, фенпропиморф, спироксамин,тридеморф; анилинопиримидины, такие как ципродинил, мепанипирим, пириметанил; пирролы, такие как фенпиклонил, флудиоксонил; фениламиды, такие как беналаксил, фуралаксил, металаксил, Rметалаксил, офурас, оксадиксил; бензимидазолы, такие как беномил, карбендазим, дебакарб, фуберидазол, тиабендазол; дикарбоксимиды, такие как хлозолинат, дихлозолин, ипродин, миклозолин, процимидон, винклозолин; карбоксамиды, такие как карбоксин, фенфурам, флутоланил, мепронил, оксикарбоксин, тифлузамид; гуанидины, такие как гуазатин, додин, иминоктадин; стробилурины, такие как азоксистробин, крезоксим-метил, метоминостробин, SSF-129, трифлоксистробин, пикоксистробин, BAS 500F(предлагаемое название пираклостробин), BAS 520; дитиокарбаматы, такие как фербам, манкоцеб, манеб, метирам, пропинеб, тирам, цинеб, цирам; N-галометилтиотетрагидрофталимиды, такие как каптафол, каптан, дихлофлуанид, флуромид, фолпет, толифлуанид; медьсодержащие соединения, такие как бордоская жидкость, гидроксид меди, оксихлорид меди, сульфат меди, оксид меди, манкоппер, оксин меди; нитрофенольные производные, такие как динокап или нитротал-изопропил; фосфорорганические производные, такие как эдифенфос, ипробенфос, изопротиолан, фосдифен, пиразофос, токлофос-метил; другие соединения из различных классов, такие как ацибензолар-S-метил, анилазин, бентавиликарб, бластицидин-S, хинометионат, хлоронеб, хлороталонил, цифлуфенамид, цимоксанил, дихлон, дихломезин,дихлоран, диэтофенкарб, диметоморф, дитианон, SYP-LI90 (предлагаемое название: флуморф), дитианон, этабоксам, этридиазол, фамоксадон, фенамидон, феноксанил, фентин, феримзон, флуазинам, флу- 23010264 сульфамид, фенгексамид, фосэтил алюминий, гимексазол, ипроваликарб, IKF-916 (циазофамид), касугамицин, метасульфокарб, метрафенон, никобифен, пенцикурон, фталид, полиоксины, пробеназол, пропамокарб, пирохилон, хиноксифен, хинтозен, сера, триазоксид, трициклазол, трифорин, валидамицин, зоксамид (RH7281). Предпочтительным методом внесения соединения формулы (I) или агрохимической композиции,которая содержит по меньшей мере одно из таких соединений, является листовая обработка. Частота обработок и норма расхода должны зависеть от риска заражения соответствующим патогеном. Однако соединения формулы (I) могут также проникать в растение из почвы через корни (системное действие) при пропитывании места произрастания растения жидкой композицией или при внесении соединений в твердой форме в почву, например в гранулированной форме (почвенное внесение). В культуры риса-падди такие гранулы можно вносить на затопляемые рисовые поля. Соединениями формулы (I) можно обрабатывать также семена (нанесение покрытия) либо путем пропитки семян или клубней жидкой композицией фунгицида, либо путем нанесения на них покрытия из сухой композиции. Композицию [т.е. композицию, содержащую соединение формулы (I) и при необходимости твердый или жидкий адъювант] приготавливают известным методом, как правило, путем смешения до однородного состояния и/или размалывания соединения с наполнителями, например, растворителями, твердыми носителями, поверхностно-активными веществами (детергенты). Агрохимические композиции, как правило, должны содержать от 0,1 до 99 мас.%, предпочтительно от 0,1 до 95 мас.% соединения формулы (I), от 99,9 до 1 мас.%, предпочтительно от 99,8 до 5 мас.% твердого или жидкого адъюванта, от 0 до 25 мас.%, предпочтительно от 0,1 до 25 мас.% поверхностноактивного вещества. Как правило, целесообразно использовать норму внесения от 5 г до 2 кг действующего вещества(д.в.) на гектар (га), предпочтительно от 10 г до 1 кг д.в./га, наиболее предпочтительно от 20 до 600 г д.в./га. При использовании в качестве агента для пропитывания семян общепринятые дозы составляют от 10 мг до 1 г действующего вещества на 1 кг семян. В то время как концентрированные композиции являются более предпочтительными в качестве поступающих в продажу продуктов, непосредственный потребитель, как правило, применяет разбавленные композиции. Ниже изобретение более подробно проиллюстрировано на примерах, не ограничивающих его объем. Пример 1. В этом примере проиллюстрировано получение соединения 2.01. Раствор 1,4-диметил-5-нитро-1,4-дигидро-1,4-эпоксинафталина (5,49 г, 25,27 ммоль) (см. Т. Nishiyama и др., Rikagaku-hen, 28, 2000, cc. 37-43) в ТГФ (55 мл) гидрировали в присутствии RaNi (1,1 г) при температуре окружающей среды. Поглощение водорода составляло 2,23 л (97%) через 18 ч. После отфильтровывания катализатора фильтрат упаривали и растворяли в простом эфире, промывали водным раствором NaHCO3 и сушили (NaSO4) с получением 4,60 г неочищенного продукта в виде масла. После растирания в гексане со следовыми количествами простого эфира получили 4,51 г (94%) кристаллического продукта красноватого цвета. Пример 2. В этом примере проиллюстрировано получение соединения 1.01. К 1,4-диметил-5-нитро-1,4-дигидро-1,4-эпоксинафталину (4,22 г, 19,43 ммоль) (см. пример 1) в этаноле (60 мл) добавляли раствор хлорида аммония (2,08 г) в воде (5,2 мл) при 47 С. Добавляли при интенсивном перемешивании в течение 5 мин порошкообразный цинк (9,10 г, 0,14 моль) в виде одной порции. Суспензию нагревали до температуры дефлегмации в течение 5,5 ч. И затем фильтровали через устройство типа Hyflo, получая прозрачный фильтрат желтого цвета. После упаривания получали неочищенный продукт в количестве 4,57 г в виде вязкого масла. После колоночной хроматографии на силикагеле в смеси этилацетат-гексан (1:4) получили 1,24 г (34%) требуемого продукта в виде кристаллов коричневатого цвета. Пример 3. В этом примере проиллюстрировано получение соединения 2.16. Раствор 5-нитробензонорборнадиена (L.A. Paquette и др., J. Amer. Chem. Soc. 99, 1977, с. 3734) (2,52 г, 13,46 ммоль) в метаноле (100 мл) гидрировали в присутствии 5% Pd/C (0,5 г) при температуре окружающей среды. Поглощение Н 2 составляло 1,14 л (95%) через 11 мин. Раствор отфильтровывали от катализатора и упаривали, в результате получили неочищенный продукт (1,86 г, 87% ) в виде масла желтого цвета, которое отверждалось при выстаивании при комнатной температуре (tпл 63-64C). Пример 4. В этом примере проиллюстрировано получение соединения 3.023. Раствор 1-метил-4-трифторметил-1 Н-пиррол-3-карбоновой кислоты (1,02 г, 5,3 ммоль) и каталитическое количество ДМФ (3 капли) в дихлорметане (20 мл) после предварительного охлаждения на льду подвергали взаимодействию с оксалилхлоридом (0,805 г, 1,2 экв.) в течение 2 ч. Затем через 15 мин в- 24010264 реакционную смесь добавляли по каплям раствор 1,8-диметил-11-оксатрицикло[6.2.1.02,7]ундека 2,4,6-триен-3-иламина (соединение . 2.01; см. выше метод получения) (1,0 г, 5,284 ммоль) и триэтиламин (1,07 г, 10,57 ммоль) в 20 мл дихлорметана при охлаждении (3-7 С) с последующим перемешиванием при температуре окружающей среды в течение 3,25 ч. Затем реакционную смесь сливали на ледяную воду и экстрагировали дихлорметаном, получая 2,26 г неочищенного продукта. После очистки на силикагеле в смеси этилацетат-гексан (1:1) и последующего растирания с простым эфиром-гексаном получили твердый продукт (1,14 г, 59%) в виде смеси изомеров. Пример 5. В этом примере проиллюстрировано получение соединения 3.024. Суспензию NaH (0,107 г, 60%-ная масляная дисперсия, 2,7 ммоль) в ДМФ (5 мл) подвергали взаимодействию с раствором (1,8-диметил-11-оксатрицикло[6.2.1.02,7]ундека-2,4,6-триен-3-ил)амида 1 метил-4-трифторметил-1 Н-пиррол-3-карбоновой кислоты (соединение 3.023; см. выше метод получения) (0,65 г, 1,784 ммоль) в 5 мл ДМФ при 10-15 С в течение 30 мин. Добавляли 3-бром-1-пропин (0,276 г, 2,32 ммоль) и смеси давали дополнительно прореагировать в течение ночи при температуре окружающей среды. После обработки ледяной водой и этилацетатом и очистки на силикагеле получили 0,36 г(50%) требуемого продукта в виде смеси изомеров. Примеры композиций соединений формулы (I). Процессы обработки для получения композиций соединений формулы (I), таких как эмульгирующиеся концентраты, растворы, гранулы, дусты и смачивающиеся порошки, описаны в WO 97/33890. Биологические примеры: фунгицидное действие. Пример В-1. Действие против Puccinia recondita на пшенице (бурая ржавчина пшеницы). Однонедельные растения пшеницы сорта Arina обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения пшеницы инокулировали путем опрыскивания опытных растений суспензией спор (1105 уредоспор/мл). После инкубации в течение 2 дней при 20 С и 95%-ной относительной влажности растения выдерживали в теплице в течение 8 дней при 20 С и 60%-ной относительной влажности. Признаки болезни оценивали через 10 дней после инокуляции. Каждое из соединений 3.048, 14.048, 29.048, 15.048, 20.048, 3.028, 22.048, 21.048, 15.023, 15.027,15.028, 3.035, 14.035, 15.035, 15.052, 14.210, 15.210, 14.202 и 15.202 практически полностью предупреждало поражение грибом (поражение 0-5%). Пример В-2. Действие против Podosphaera leucotricha на яблоне (настоящая мучнистая роса яблонь). Пятинедельные саженцы яблонь сорта Mclntosh обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения яблонь инокулировали путем встряхивания растений, зараженных настоящей мучнистой росой яблонь,над опытными растениями. После инкубации в течение 12 дней при 22 С и 60%-ной относительной влажности и световом режиме 14/10 ч (день/ночь) оценивали признаки заболевания. Каждое из соединений 3.048, 14,048, 15.048, 22.048, 14.210, 15.210, 14.202, 15.202 и 15.023 проявило высокую эффективность (поражение 20%). Пример В-3. Действие против Venturia inaequalis на яблоне (парша яблонь). Четырехнедельные саженцы яблонь сорта Mclntosh обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения яблонь инокулировали путем опрыскивания опытных растений суспензией спор (4105 конидий/мл). После инкубации в течение 4 дней при 21 С и 95%-ной относительной влажности растения выдерживали в теплице в течение 4 дней при 21 С и 60%-ной относительной влажности. После дополнительной инкубации в течение 4 дней при 21 С и 95%-ной относительной влажности оценивали признаки заболевания. Каждое из соединений 3.048, 14.048, 14.210, 15.210, 14.202, 15.202 и 15.048 проявило высокую эффективность (поражение 20%). Пример В-4. Действие против Erysiphe graminis на ячмене (настоящая мучнистая роса ячменя). Однонедельные растения ячменя сорта Regina обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения ячменя инокулировали путем встряхивания растений, зараженных настоящей мучнистой росой, над опытными растениями. После инкубации в теплице в течение 6 дней при 20 С/18 С (день/ночь) и 60%ной относительной влажности оценивали признаки заболевания. Каждое из соединений 3.023, 14.023, 3.048, 14.048, 15.048, 3.027, 3.028, 15.023, 14.210, 15.210,14.202, 15.202 и 15.027 проявило высокую эффективность (поражение 20%). Пример В-5. Действие против Botrytis cinerea на культурном винограде (серая гниль винограда). Пятинедельные чубуки винограда сорта Gutedel обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 2 дня после обработки растения винограда инокулировали путем опрыскивания опытных растений суспензией спор (1106 конидий/мл). После инкубации в теплице в течение 4 дней при 21 С и 95%-ной относительной влажности оценивали- 25010264 признаки заболевания. Каждое из соединений 14.048, 15.048, 3.028, 14.210, 15.210, 14.202, 15.202 и 15.027 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-6. Действие против Botrytis cinerea на томатах (серая гниль томатов). Четырехнедельные растения томатов сорта Roter Gnom обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 2 дня после обработки растения томатов инокулировали путем опрыскивания опытных растений суспензией спор (1105 конидий/мл). После инкубации в вегетационной камере в течение 4 дней при 20 С и 95%-ной относительной влажности оценивали признаки заболевания. Каждое из соединений 3.048, 3.052, 14.052, 15.048, 14.210, 15.210, 14.202, 15.202 и 15.023 проявило высокую активность (поражение заболеванием 50%). Пример В-7. Действие против Septoria nodorum на пшенице (септориоз листьев пшеницы). Однонедельные растения пшеницы сорта Arina обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения пшеницы инокулировали путем опрыскивания опытных растений суспензией спор (5105 конидий/мл). После инкубации в течение 1 дня при 20 С и 95%-ной относительной влажности растения выдерживали в теплице в течение 10 дней при 20 С и 60%-ной относительной влажности. Признаки заболевания оценивали через 11 дней после инокуляции. Каждое из соединений 3.002, 3.048, 14.048, 14.210, 15.210, 14.202, 15.202 и 15.048 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-8. Действие против Helminthosporium teres на ячмене (сетчатая пятнистость ячменя). Однонедельные растения ячменя сорта Regina обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 2 дня после обработки растения ячменя инокулировали путем опрыскивания опытных растений суспензией спор (3104 конидий/мл). После инкубации в теплице в течение 4 дней при 20 С и 95%-ной относительной влажности оценивали признаки заболевания. Каждое из соединений 3.023, 14.023, 3.048, 14.048, 15.048, 3.027, 15.023, 15.027, 14.210, 15.210,14.202, 15.202 и 15.028 проявило высокую активность в этом опыте (поражение заболеванием 20%). Пример В-9. Действие против Alternaria solani на томатах (бурая пятнистость томатов). Четырехнедельные растения томатов сорта Roter Gnom обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 2 дня после обработки растения томатов инокулировали путем опрыскивания опытных растений суспензией спор (2105 конидий/мл). После инкубации в вегетационной камере в течение 3 дней при 20 С и 95%-ной относительной влажности оценивали признаки заболевания. Каждое из соединений 3.023, 14.023, 3.048, 14.048, 14.210, 15.210, 14.202, 15.202 и 15.048 проявило очень высокую активность в этом опыте (поражение заболеванием 20%). Пример В-10. Действие против Uncinula necator на культурном винограде (настоящая мучнистая роса винограда). Пятинедельные чубуки винограда сорта Gutedel обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения винограда инокулировали путем встряхивания растений, зараженных настоящей мучнистой росой, над опытными растениями. После инкубации в течение 7 дней при 26 С и 60%-ной относительной влажности и световом режиме 14/10 ч (день/ночь) оценивали признаки заболевания. Каждое из соединений 14.048, 15.048, 14.028 и 15.023 проявило очень высокую активность в этом опыте (поражение заболеванием 20%). Пример В-11. Системное действие против Erysiphe sraminis на ячмене (настоящая мучнистая роста ячменя) (опыт в мешочках). Композицию тестируемого соединения (0,002% действующего вещества) вносили в мешочек, в который предварительно помещали фильтровальную бумагу. После такой обработки в верхнюю складку фильтровальной бумаги вносили семена ячменя (сорта Express). Подготовленные таким образом мешочки выдерживали при 23 С/18 С (день/ночь) при 80%-ной относительной влажности. Через 1 неделю после посева растения ячменя инокулировали путем встряхивания растений, зараженных настоящей мучнистой росой, над опытными растениями. После 6-дневного периода инкубации оценивали признаки заболевания. Эффективность каждого тестируемого соединения рассматривали в качестве критерия системного действия. Каждое из соединений 14.024, 3.002, 3.048, 29.048, 3.027, 22.048, 21.048, 15.023, 15.027, 15.028 и 15.035 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-12. Действие против Fusarium culmorum на пшенице (фузариозная гниль пшеницы) (опыт в мешочках). Суспензию конидий F. culmorum (7105 конидий/мл) смешивали с композицией тестируемого соединения (0,002% действующего вещества). Смесь вносили в мешочек, в который предварительно поме- 26010264 щали фильтровальную бумагу. После такой обработки в верхнюю складку фильтровальной бумаги помещали семена пшеницы (сорта Orestis). Подготовленные таким образом мешочки выдерживали в течение 11 дней при температуре примерно 10-18 С и 100%-ной относительной влажности при продолжительности светового дня 14 ч. Оценивали степень поражения заболеванием по наличию коричневых повреждений на корнях. Каждое из соединений 14.024, 15.048, 20.048, 14.027, 24.048 и 3.035 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-13. Действие против Gaeumannomyces graminis на пшенице (офиоболез пшеницы) (опыт в мешочках). Определенное количество мицелия G. graminis смешивали с водой. Композицию тестируемого соединения (0,002% действующего вещества) добавляли в суспензию мицелия. Смесь вносили в мешочек,в который предварительно помещали фильтровальную бумагу. После такой обработки в верхнюю складку фильтровальной бумаги помещали семена пшеницы (сорта Orestis). Подготовленные таким образом мешочки выдерживали в течение 14 дней при 18 С/16 С (день/ночь) и 80%-ной относительной влажности при продолжительности светового дня 14 ч. Оценку опыта осуществляли по побурению корней. Каждое из соединений 15.048, 20.048, 21.048, 15.028 и 15.052 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-14. Действие против Puccinia recondita на пшенице (бурая ржавчина пшеницы) (опыты в мешочках). Композицию тестируемого соединения (0,002% действующего вещества) вносили в мешочек, в который предварительно помещали фильтровальную бумагу. После такой обработки в верхнюю складку фильтровальной бумаги помещали семена пшеницы (сорта Arina). Подготовленные таким образом мешочки выдерживали при 23 С/18 С (день/ночь) и 80%-ной относительной влажности. Через 1 неделю после посева растения пшеницы инокулировали путем опрыскивания тестируемых растений суспензией спор (1105 уредоспор/мл). После инкубации в течение 1 дня при 23 С и 95%-ной относительной влажности растения выдерживали в течение 9 дней при 20 С/18 С (день/ночь) и 80%-ной относительной влажности. Признаки заболевания оценивали через 10 дней после инокуляции. Эффективность каждого тестируемого соединения рассматривали в качестве критерия системного действия. Каждое из соединений 14.024, 3.002, 14.002, 15.048, 20.048, 3.027, 22.048, 15.023, 15.027, 15.028,3.035, 14.035 и 15.035 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-15. Действие против Rhizoctonia solani на растениях риса (ризоктониоз риса) (опыты в мешочках). Определенное количество мицелия R. solani смешивали с водой. Композицию тестируемого соединения (0,002% действующего вещества) добавляли в суспензию мицелия. Смесь вносили в мешочек, в который предварительно помещали фильтровальную бумагу. После такой обработки в верхнюю складку фильтровальной бумаги помещали семена риса (сорта Koshihikari). Подготовленные таким образом мешочки выдерживали в течение 10 дней при 23 С/21 С (день/ночь) и 100%-ной относительной влажности при продолжительности светового дня 14 ч. Оценивали степень поражения заболеванием по наличию коричневых повреждений на корнях. Каждое из соединений 3.048, 14.048, 29.048, 3.052, 29.052, 14.052, 15.048, 20.048, 3.027, 14.028,22.048, 21.048, 4.048, 15.023, 3.035, 14.035 и 15.035 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-16. Действие против Septoria nodorum на пшенице (септориозная пятнистость листьев пшеницы) (опыты в мешочках). Композицию тестируемого соединения (0,002% действующего вещества) вносили в мешочек, в который предварительно помещали фильтровальную бумагу. После такой обработки в верхнюю складку фильтровальной бумаги помещали семена пшеницы (сорта Arina). Подготовленные таким образом мешочки выдерживали при 23 С/18 С (день/ночь) и 80%-ной относительной влажности. Через 1 неделю после посева растения пшеницы инокулировали путем опрыскивания опытных растений суспензией спор(5105 конидий/мл). После инкубации в течение 1 дня при 23 С и 95%-ной относительной влажности растения выдерживали в течение 9 дней при 20/18 С (день/ночь) и 80%-ной относительной влажности. Признаки заболевания оценивали через 8 дней после инокуляции. Эффективность каждого тестируемого соединения рассматривали в качестве критерия системного действия. Каждое из соединений 3.048, 29.048, 15.048, 14.027, 15.023 и 15.027 проявило высокую активность в этом опыте (поражение заболеванием 50%). Пример В-17. Действие против Septoria tritici на пшенице (септориозная пятнистость листьев пшеницы). Двухнедельные растения пшеницы сорта Riband обрабатывали композицией тестируемого соединения (0,02% действующего вещества) в камере для опрыскивания. Через 1 день после обработки растения пшеницы инокулировали путем опрыскивания опытных растений суспензией спор (10105 конидий/мл). После инкубации в течение 1 дня при 23 С и 95%-ной относительной влажности растения выдерживали- 27010264 в теплице в течение 16 дней при 23 С и 60%-ной относительной влажности. Признаки заболевания оценивали через 18 дней после инокуляции. Каждое из соединений 14.202 или 14.210 проявило высокую активность в этом опыте (поражение заболеванием 20%). ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение формулы (I) в которой Het обозначает пирролил или пиразолил, которые замещены группами R8, R9 и R10;R2 и R3 в каждом случае независимо друг от друга обозначают водород, галоген, С 1-С 4 алкил, С 1 С 4 алкокси или С 1-С 4 галоалкокси;R4, R5, R6 и R7 в каждом случае независимо друг от друга обозначают водород, галоген, С 1-С 4 алкил,С 1-С 4 галоалкил, С 1-С 4 алкокси, С 1-С 4 галоалкокси, С 1-С 4 алкилтио, С 1-С 4 галоалкилтио, гидроксиметил, С 1 С 4 алкоксиметил, С(О)СН 3 или С(О)ОСН 3;R8, R9 и R10 в каждом случае независимо друг от друга обозначают водород, галоген, циано, нитро,С 1-С 4 алкил, С 1-С 4 галоалкил, С 1-С 4 алкокси(С 1-С 4)алкилен или С 1-С 4 галоалкокси(С 1-С 4)алкилен, при условии, что по меньшей мере одна из групп R8, R9 и R10 не обозначает водород;R12 и R13 в каждом случае независимо друг от друга обозначают водород, галоген, С 1-С 5 алкил, С 1 С 4 алкокси, СН 2 ОН, С 3-С 6 циклоалкил, СН 2 О-С(=О)СН 3, СН 2-С 3-С 6 циклоалкил или бензил; или R12 и R13 вместе с атомом углерода, к которому они присоединены, образуют группу С=О или 3-5-членное карбоциклическое кольцо; или R12 и R13 вместе образуют С 1-С 6 алкилиденовую группу или С 3-С 6 циклоалкилиденовую группу; иR14, R15, R16 и R17 в каждом случае независимо друг от друга обозначают водород или СН 3. 2. Соединение формулы (I) по п.1, где R8, R9 и R10 в каждом случае независимо друг от друга обозначают водород, хлор, фтор, метил, CF3, CHF2 или CH2F, при условии, что по меньшей мере одна из групп R8, R9 и R10 не обозначает водород; 3. Соединение формулы (I) по п.1, где m равно 0 и n равно 0. 4. Соединение формулы (I) по п.3, где R12 и R13 в каждом случае независимо друг от друга обозначают водород, С 1-С 4 алкил или С 1-С 4 алкокси. 5. Соединение формулы (I) по п.1, где R2 обозначает водород, галоген или С 1-С 4 алкил. 6. Соединение формулы (I) по п.1, где R3 обозначает водород или метил. 7. Соединение формулы (I) по п.1, где Het обозначает пиразолил. 8. 9. Соединение формулы (I) по п.1, где Het обозначает пирролил. 10. Композиция для борьбы с микроорганизмами и предупреждения их нападения и поражения ими растений, в которой действующее вещество представляет собой соединение формулы (I) по п.1 и которая содержит приемлемый носитель. 11. Способ борьбы с фитопатогенными микроорганизмами или предупреждения поражения ими культурных растений, который заключается в том, что соединения формулы (I) по п.1 наносят на листву или почву. 12. Способ борьбы с фитопатогенными микроорганизмами или предупреждения поражения ими культурных растений, который заключается в том, что соединения формулы (I) по п.1 наносят на затопленные рисовые поля.- 28010264 13. Способ борьбы с фитопатогенными микроорганизмами или предупреждения поражения ими культурных растений, который заключается в том, что соединения формулы (I) по п.1 наносят на семена.
МПК / Метки
МПК: C07D 213/78, A01N 43/32, C07D 493/08, C07D 231/14, C07D 277/56, C07D 207/34, C07D 487/08, C07D 263/34, C07D 495/08, C07D 327/06, A01N 43/36
Метки: производные, гетероциклокарбоксамидные
Код ссылки
<a href="https://eas.patents.su/30-10264-geterociklokarboksamidnye-proizvodnye.html" rel="bookmark" title="База патентов Евразийского Союза">Гетероциклокарбоксамидные производные</a>
Предыдущий патент: Способ химиопрофилактики рака предстательной железы
Следующий патент: Производные пиримидина для использования в качестве лигандов ваниллоидных рецепторов и их применение для терапии боли
Случайный патент: Коррозионностойкий и огнестойкий трубопровод