Сокристаллы госсипола и их применение
Формула / Реферат
1. Композиция, состоящая, по существу, из сокристаллов (-)-госсипола с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1.
2. Композиция по п.1, где указанное молярное соотношение составляет 1:1.
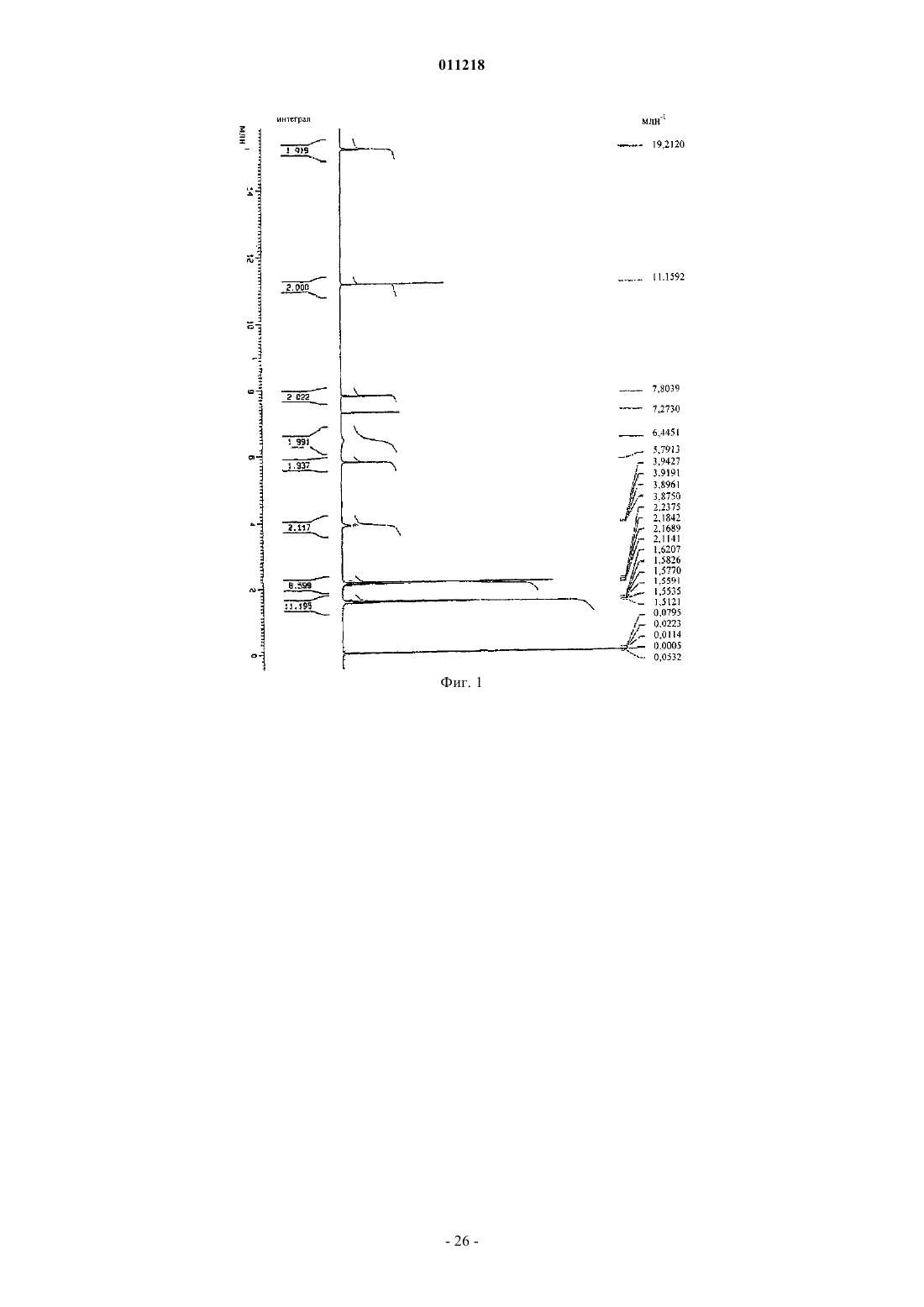
3. Композиция по п.1, которая характеризуется интеграцией спектра 1Н ЯМР при d 2,11 (s, 3H), который представляет собой один сигнал метила уксусной кислоты, и d 2,18 (s, 6H), который представляет собой два сигнала метила госсипола.
4. Способ получения композиции, состоящей, по существу, из сокристаллов (-)-госсипола с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1, при котором растворяют (-)-госсипол в ацетоне до образования раствора, фильтруют этот раствор, добавляют уксусную кислоту в этот раствор при перемешивании до тех пор, пока раствор не становится мутным, оставляют этот мутный раствор при комнатной температуре, затем при пониженной температуре от 0 до 15шС до образования сокристаллов, собирают эти сокристаллы, промывают их растворителем и высушивают.
5. Способ по п.4, где указанная пониженная температура составляет 4шС.
6. Фармацевтическая композиция, содержащая сокристаллы (-)-госсипола с уксусной кислотой и фармацевтически приемлемый носитель, где указанные сокристаллы (-)-госсипола с уксусной кислотой состоят, по существу, из сокристаллов (-)-госсипола с уксусной кислотой.
7. Фармацевтическая композиция, содержащая сокристаллы (-)-госсипола с уксусной кислотой и фармацевтически приемлемый носитель, где указанные сокристаллы (-)-госсипола с уксусной кислотой состоят, по существу, из (-)-госсипола и уксусной кислоты в молярном соотношении 1:1.
8. Способ изготовления фармацевтической композиции, при котором объединяют композицию, состоящую, по существу, из сокристаллов (-)-госсипола с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1, с фармацевтически приемлемым носителем.
9. Набор, содержащий сокристаллы по п.1 и инструкции по введению указанной композиции животному.
10. Набор по п.9, где указанная композиция находится в форме фармацевтической композиции, содержащей фармацевтически приемлемый носитель.
11. Набор по п.9, который дополнительно содержит химиотерапевтический агент.
12. Набор по п.9, где указанные инструкции представляют собой инструкции по введению указанной композиции животному, страдающему гиперпролиферативным заболеванием.
13. Набор по п.12, где указанное гиперпролиферативное заболевание представляет собой рак.
14. Набор по п.13, где указанный рак выбран из группы, состоящей из рака молочной железы, рака простаты, лимфомы, рака кожи, рака панкреатической железы, рака толстой кишки, меланомы, злокачественной меланомы, рака яичника, рака головного мозга, первичной карциномы головного мозга, рака в области головы и шеи, глиомы, глиобластомы, рака печени, рака мочевого пузыря, немелкоклеточного рака легкого, карциномы головы или шеи, карциномы молочной железы, карциномы яичника, карциномы легкого, мелкоклеточной карциномы легкого, опухоли Вильямса, цервикальной карциномы, карциномы яичка, карциномы мочевого пузыря, карциномы желудка, карциномы толстой кишки, карциномы простаты, карциномы мочеполовых органов, карциномы щитовидной железы, карциномы пищевода, миеломы, множественной миеломы, адренокарциномы, почечно-клеточного рака, карциномы эндометрия, карциномы коры надпочечников, злокачественной инсулиномы поджелудочной железы, злокачественной карциноидной опухоли, хориокарциномы, грибовидной гранулемы, злокачественной гиперкальцемии, цервикальной гиперплазии, лейкемии, острого лимфолейкоза, хронического лимфолейкоза, острого миелогенного лейкоза, хронического миелогенного лейкоза, хронического гранулоцитарного лейкоза, острого грануоцитарного лейкоза, лейкоза ворсистых клеток, нейробластомы, рабдомиосаркомы, саркомы Капоши, истинной полицитемии, идиопатического тромбоцитоза, болезни Ходжкина, неходжкинской лимфомы, саркомы мягких тканей, остеогенной саркомы, первичной макроглобулинемии и ретинобластомы.
Текст
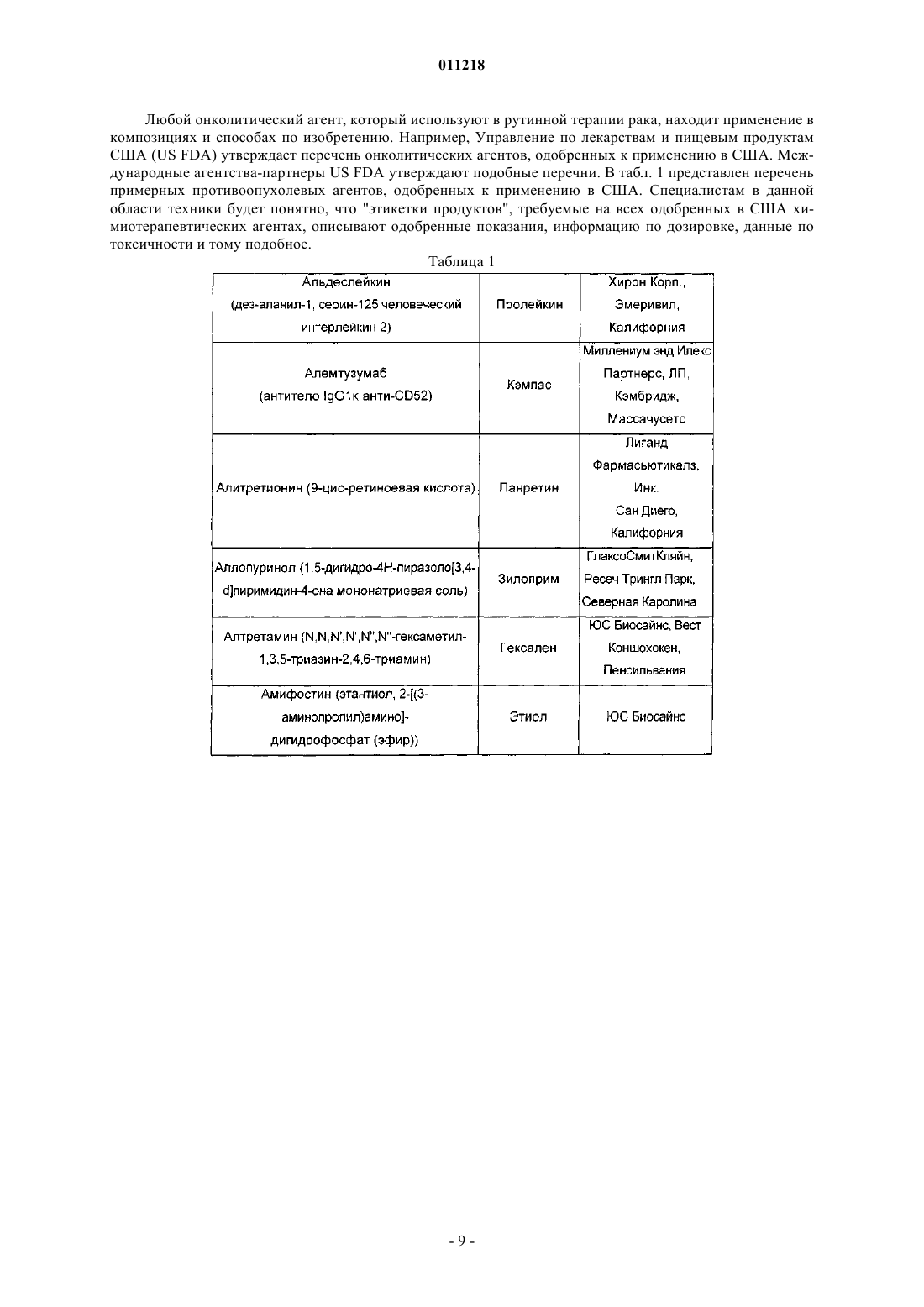
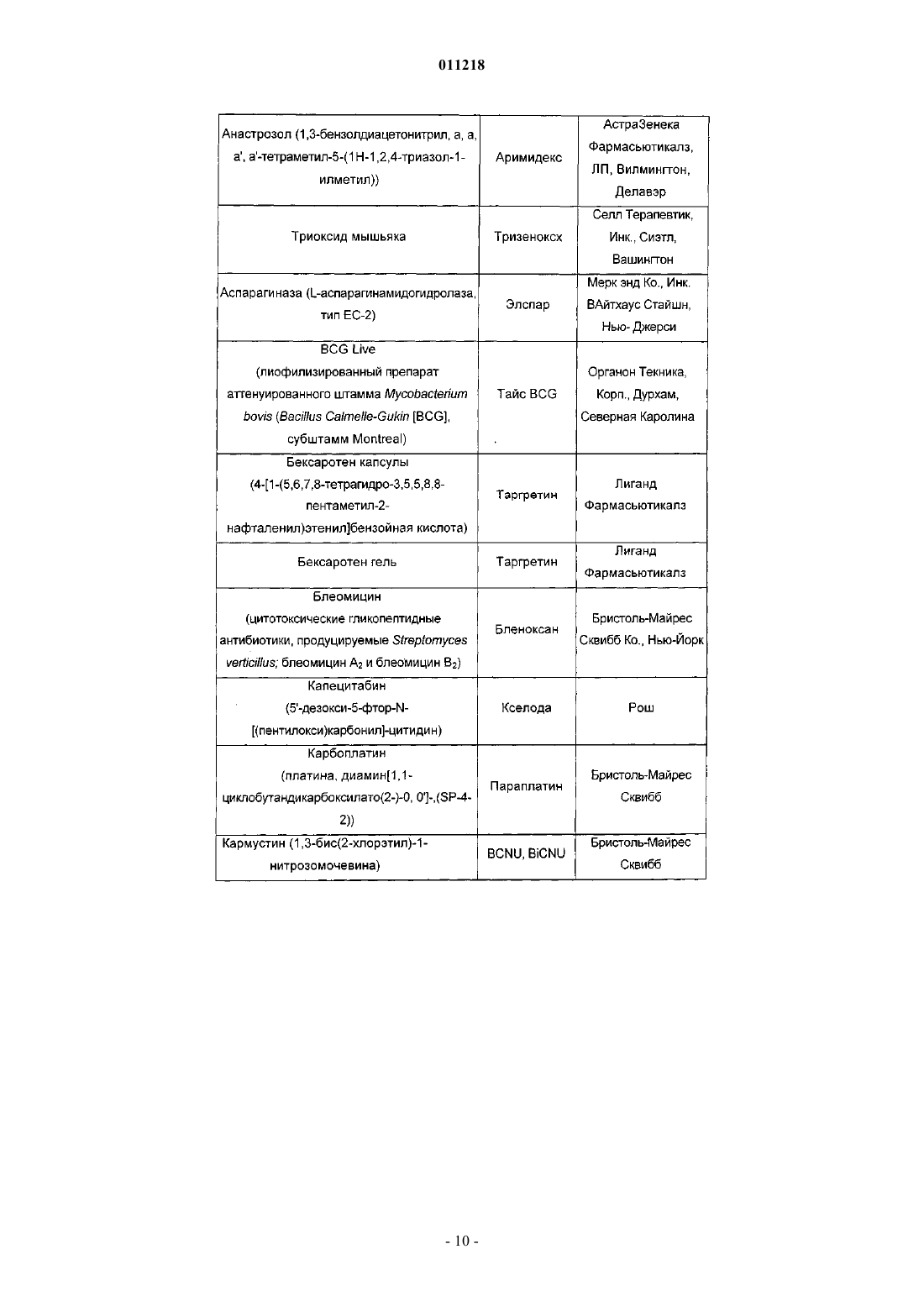
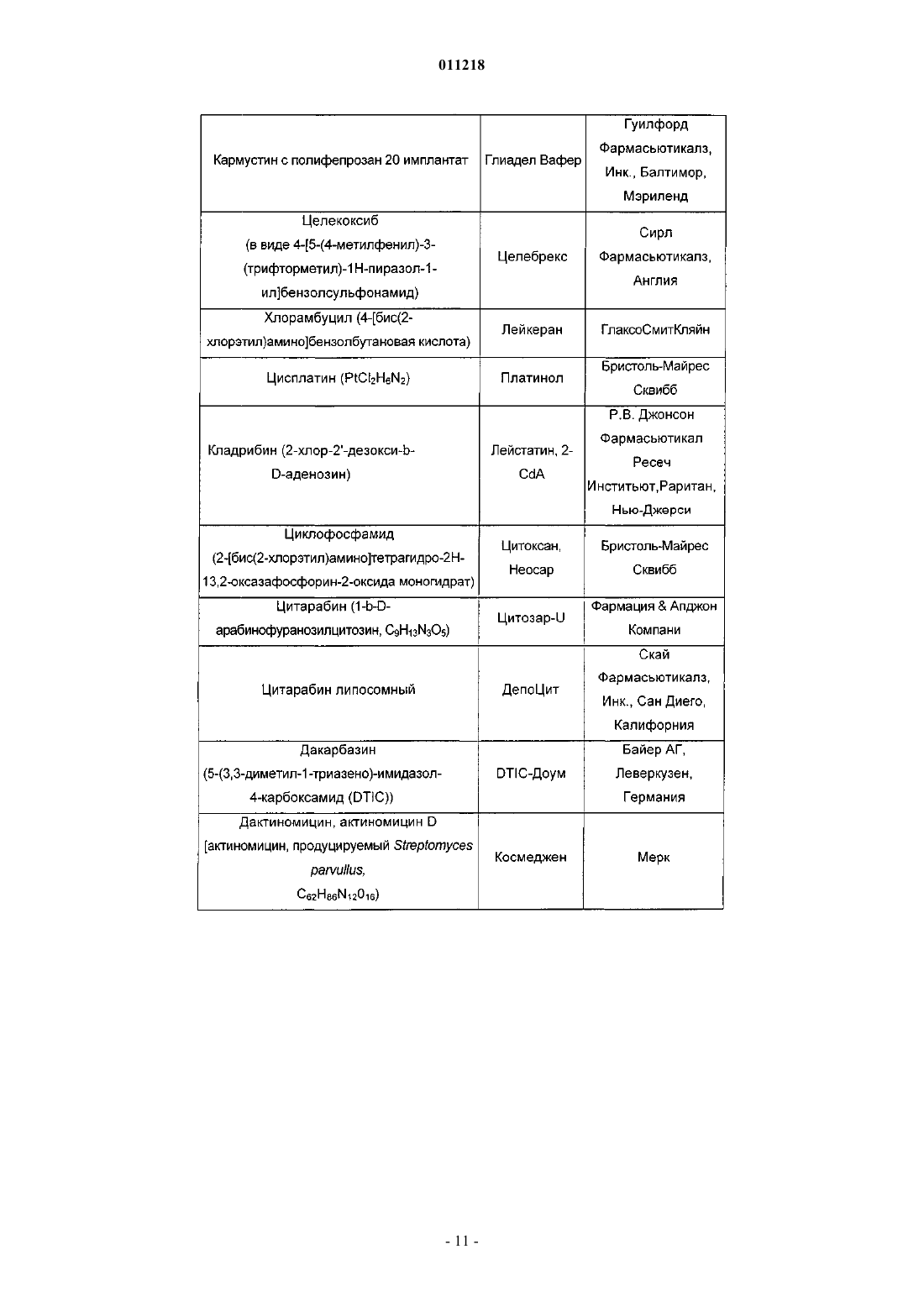
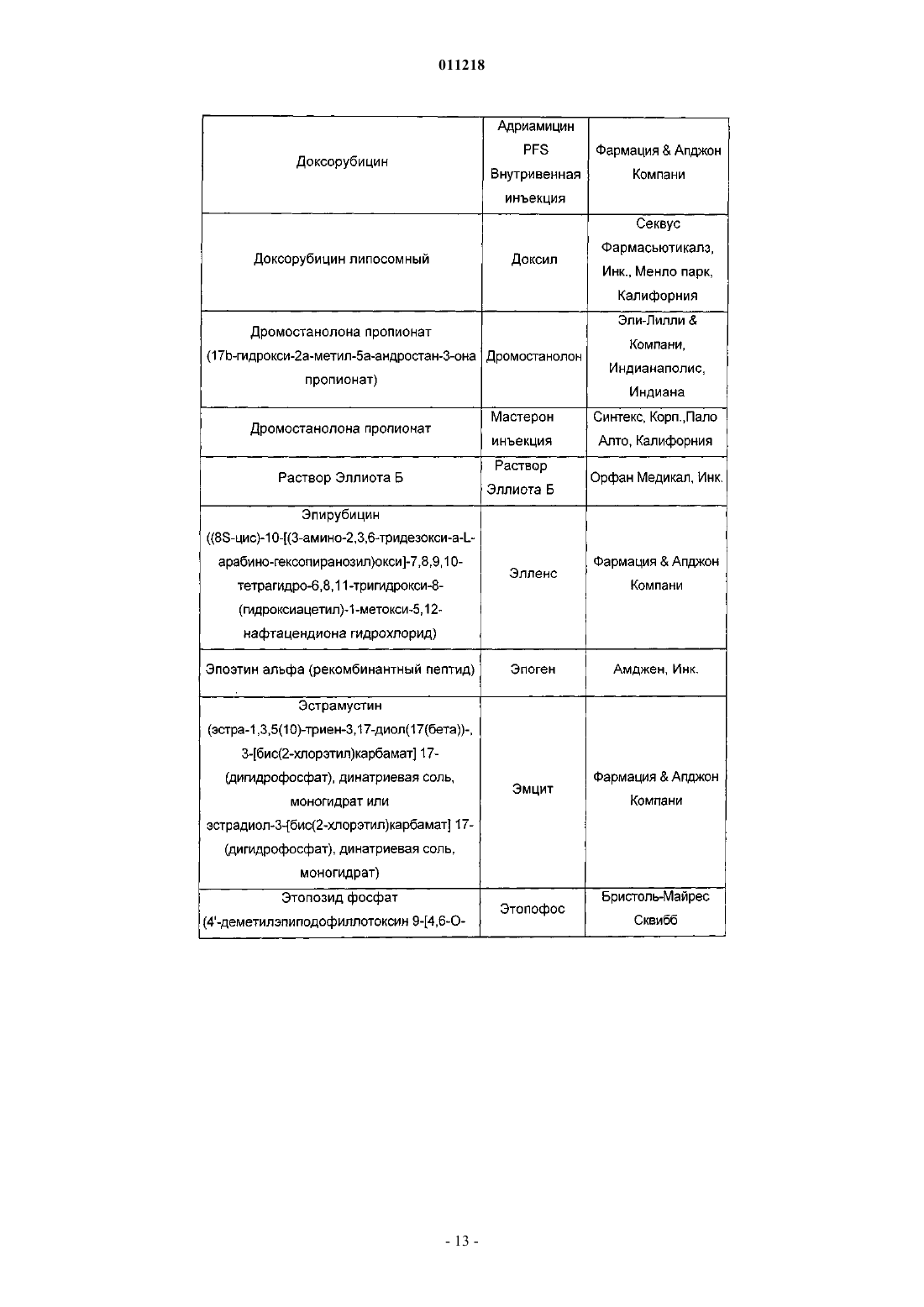
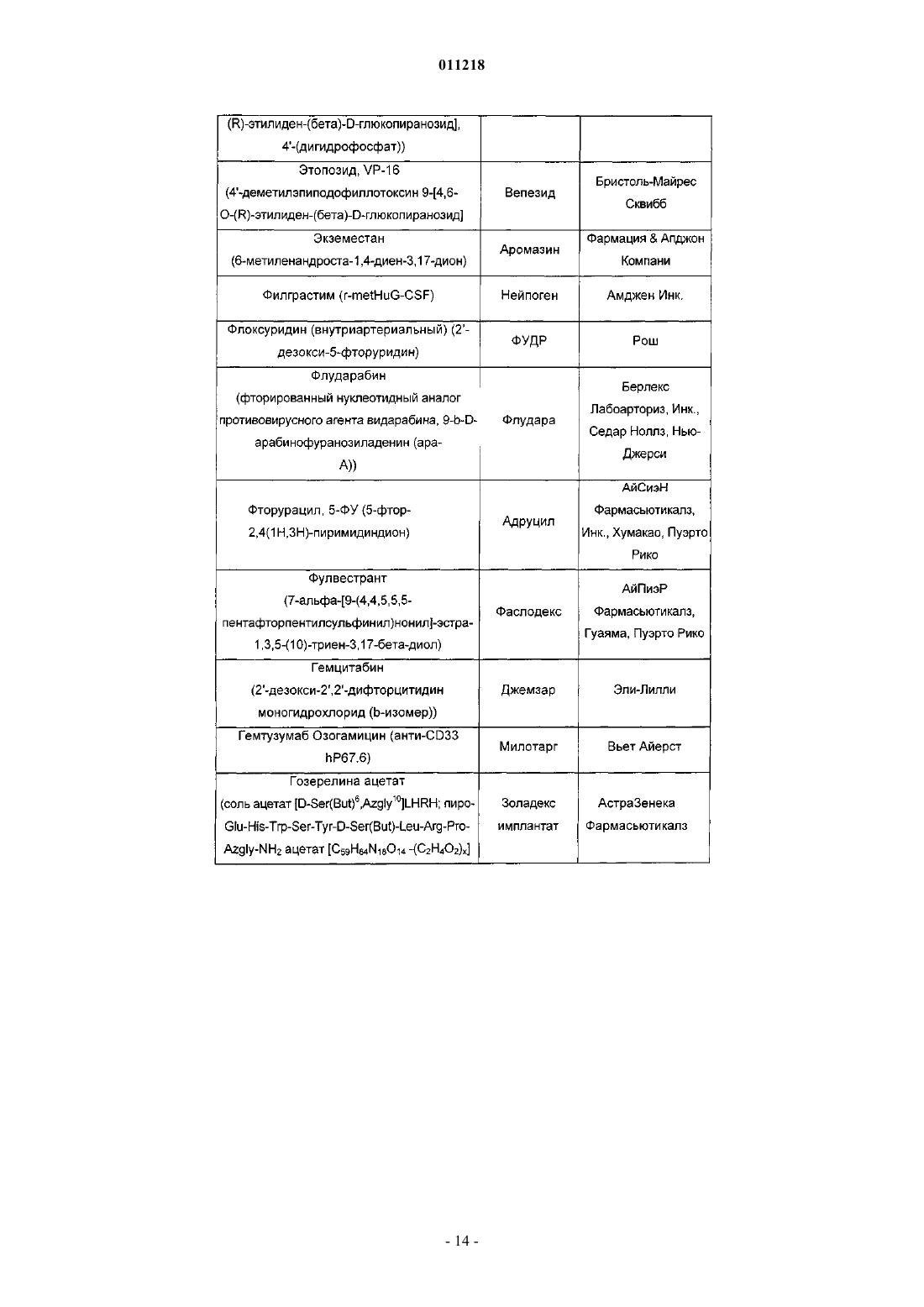
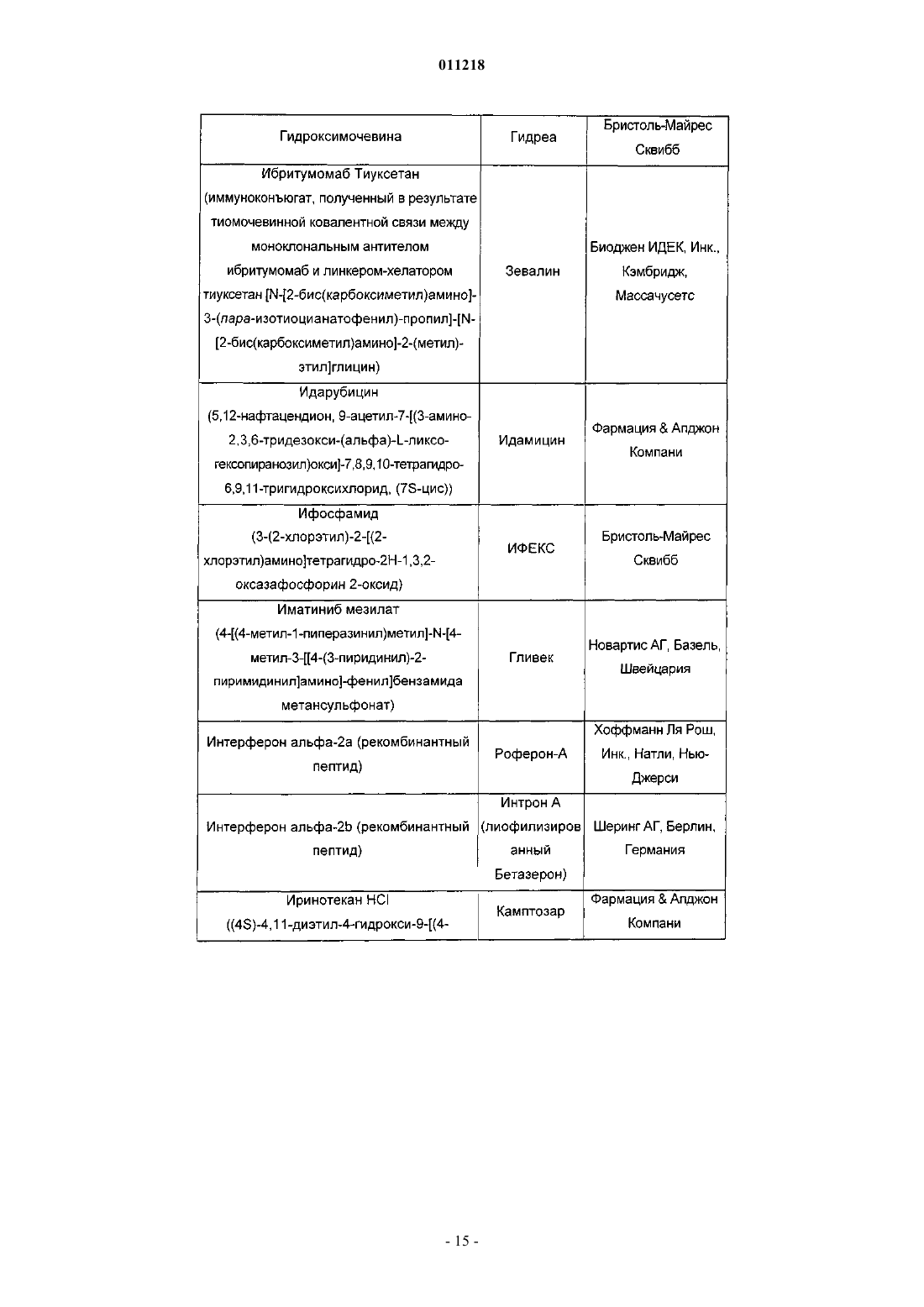
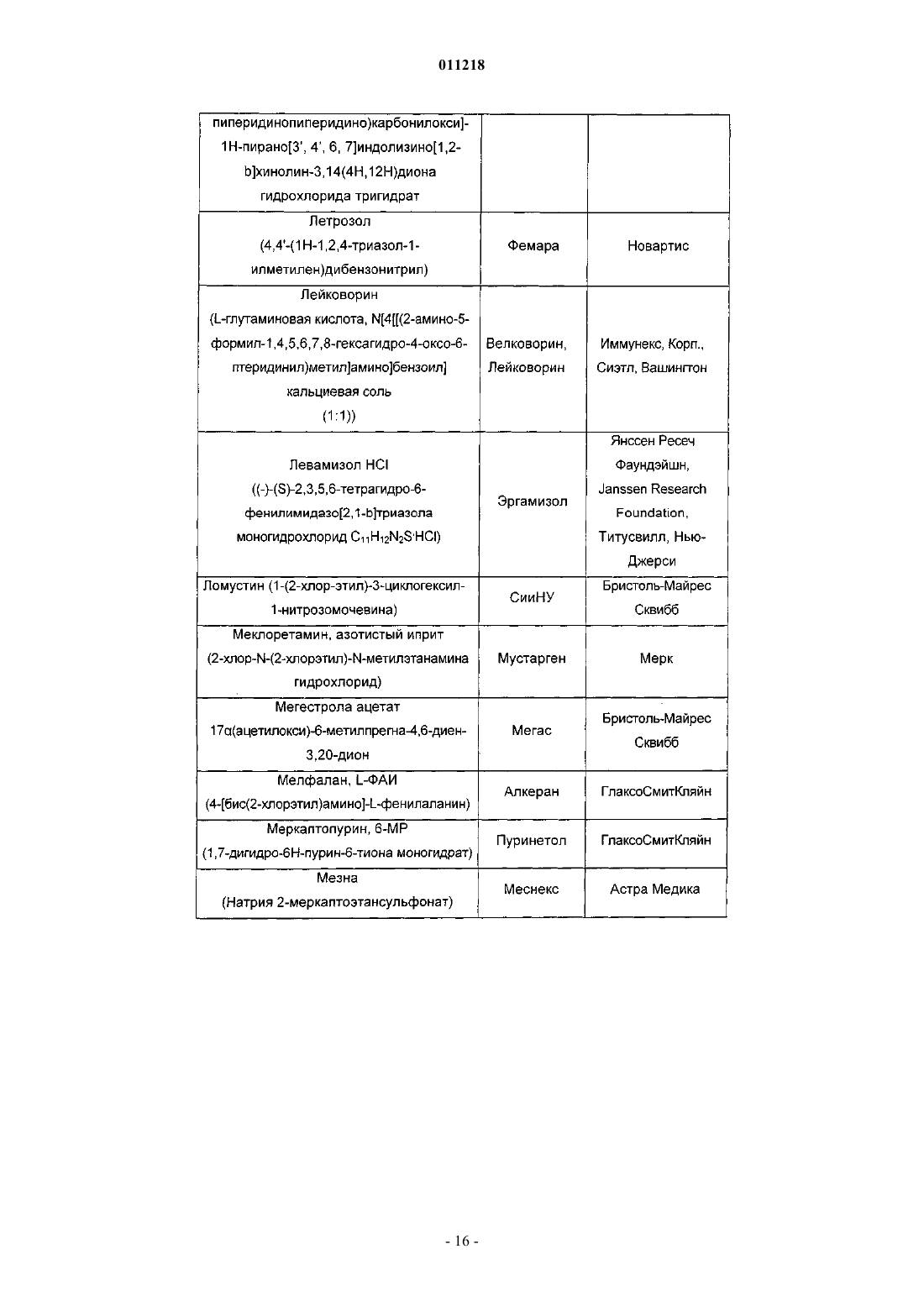
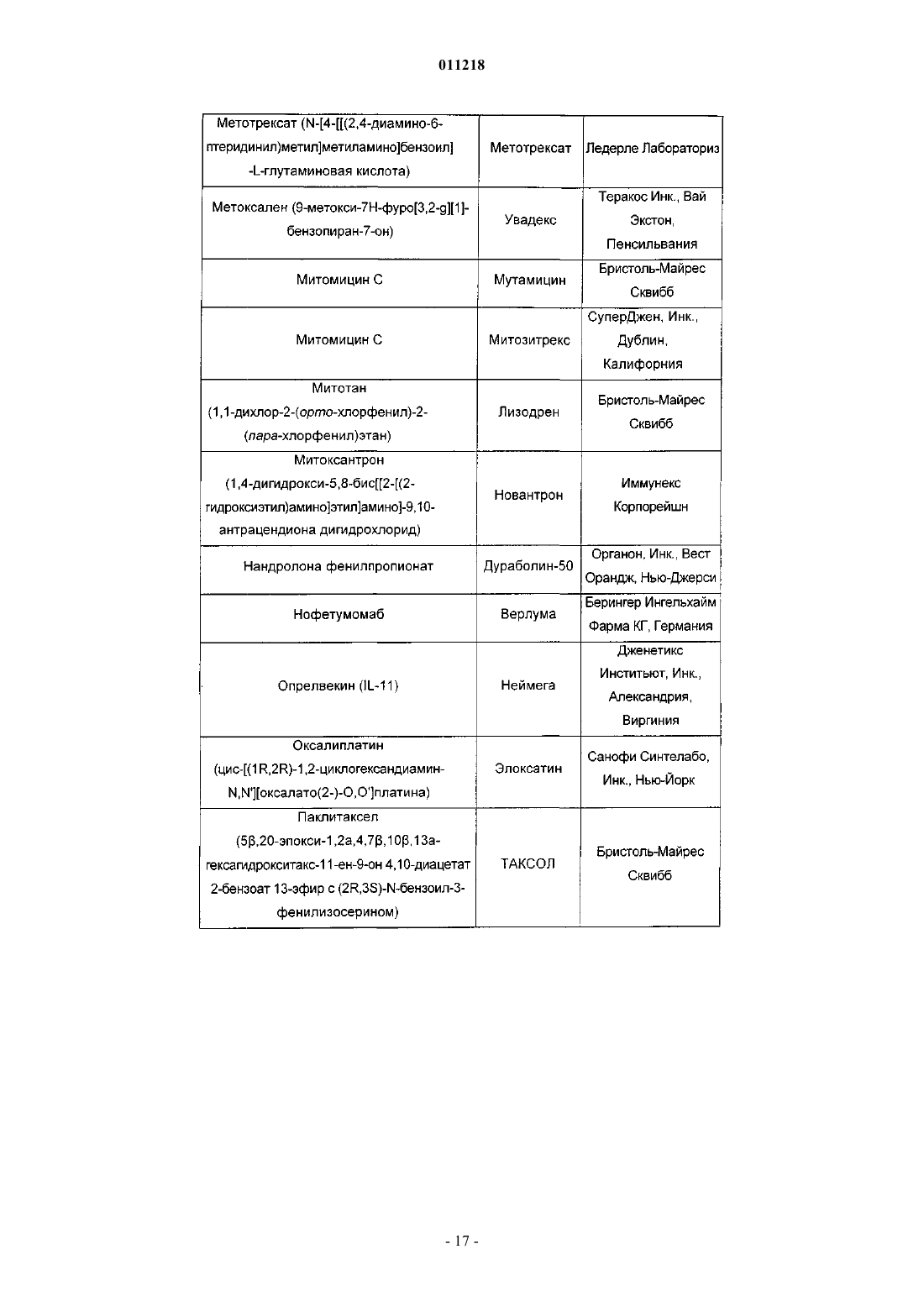
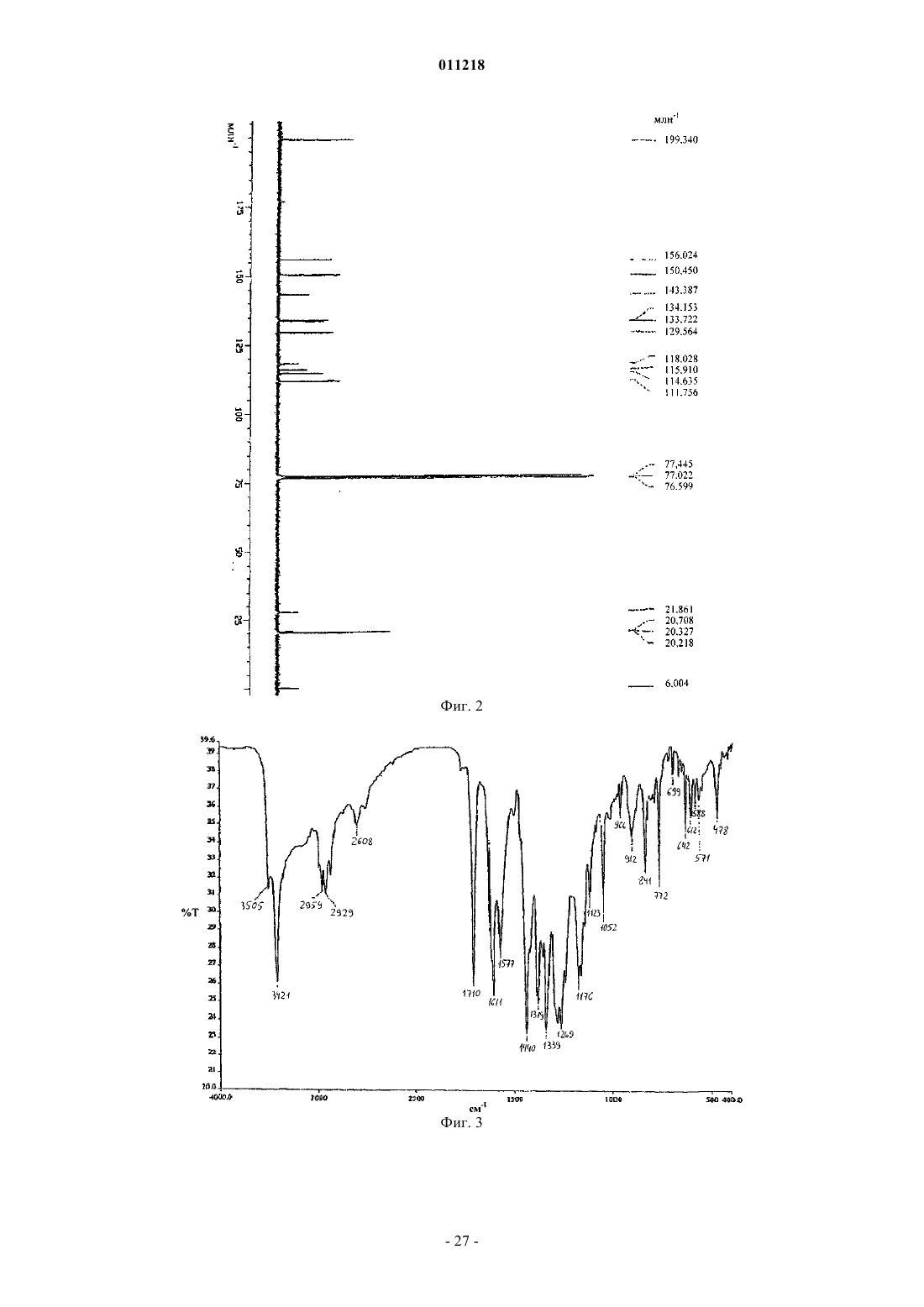
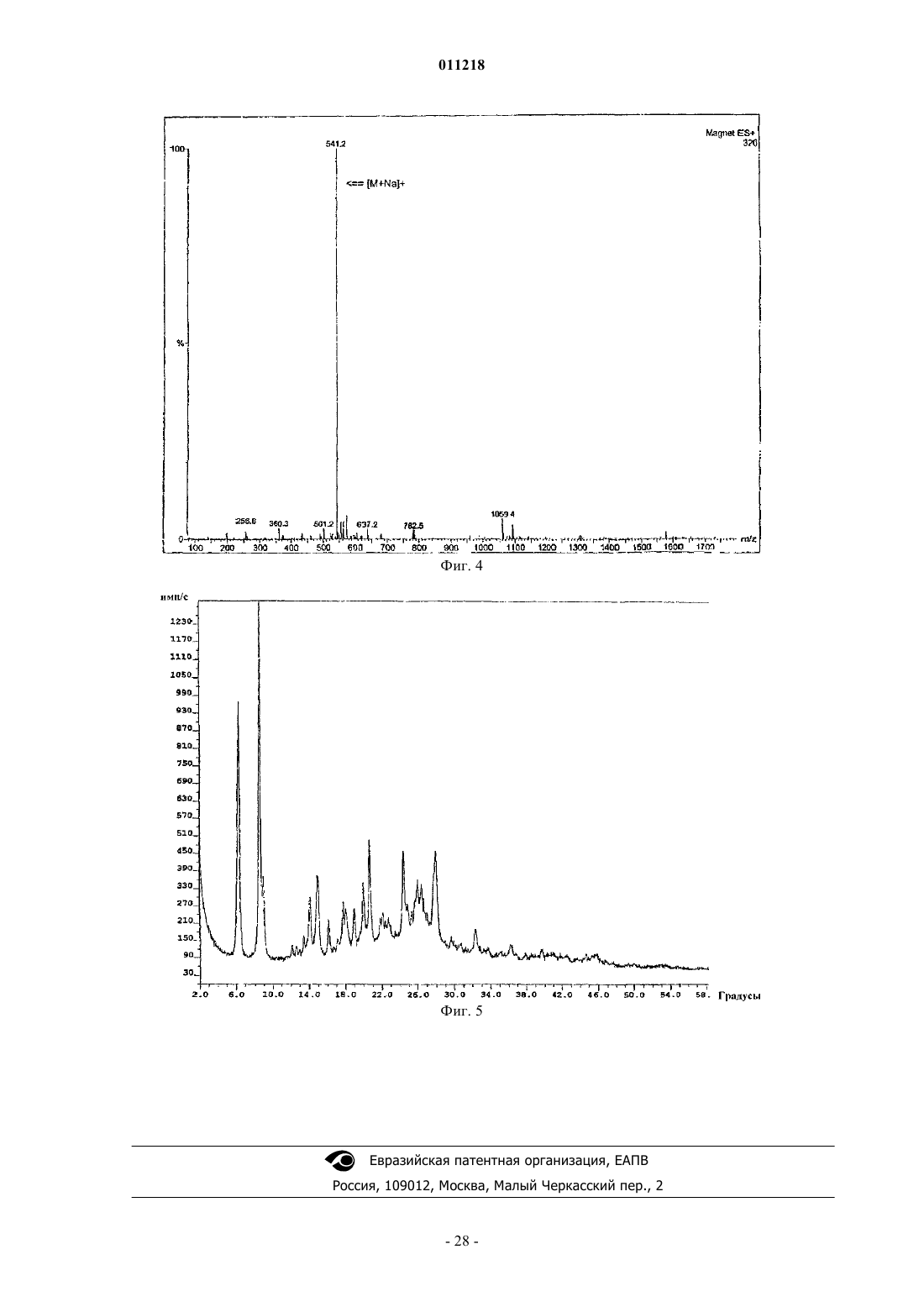
011218 Область изобретения Данное изобретение относится к области химии лекарств. В частности, изобретение относится к композициям, содержащим сокристаллы (-)-госсипола с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1, которые применимы в качестве ингибиторов белков семейства Bcl-2. Изобретение также относится к способу получения указанных композиций, фармацевтическим композициям, содержащим указанные сокристаллы (-)-госсипола с уксусной кислотой, способу получения этих фармацевтических композиций, и наборам, содержащим указанные сокристаллы. Уровень техники Агрессивный фенотип раковой клетки является результатом ряда генетических и эпигенетических изменений, приводящих к нарушению регуляции внутриклеточных путей передачи сигнала (Ponder, Nature 411: 336 (2001. Общей чертой для всех раковых клеток, однако, является их неспособность выполнять программу апоптоза и отсутствие соответствующего апоптоза вследствие дефектов в нормальном механизме апоптоза является отличительным признаком рака (Lowe et al., Carcinogenesis 21:485 (2000. Большинство современных методов терапии рака, включая химиотерапевтические агенты, облучение и иммунотерапию, действуют посредством косвенной индукции апоптоза в раковых клетках. Неспособность раковых клеток выполнять программу апоптоза вследствие дефектов в нормальном механизме апоптоза, таким образом, часто связано с повышением устойчивости к апоптозу, индуцированному химиотерапией, облучением и иммунотерапией. Первичная или приобретенная устойчивость рака различного происхождения у человека к современным методикам лечения вследствие дефектов апоптоза является основной проблемой в современной терапии рака (Lowe et al, Carcinogenesis 27: 485 (2000); Nicholson, Nature 407: 810 (2000. Соответственно, настоящие и будущие попытки в отношении разработки и развития новых специфичных молекулярных противораковых методов терапии с целью улучшения выживаемости и качества жизни раковых больных должны включать стратегии, которые специально направлены на устойчивость раковых клеток к апоптозу. В этом отношении направленность на ключевые негативные регуляторы,которые играют центральную роль в прямом ингибировании апоптоза в раковых клетках, представляет высокоперспективную терапевтическую стратегию для разработки новых противораковых лекарств. Идентифицированы два класса негативных регуляторов апоптоза. Первый класс регуляторов представляет собой ингибитор белков апоптоза (ИБА) (Deveraux et al., Genes Dev. 13: 239 (1999); Salvesen etal., Nat. Rev. Mol. Cell. Biol. 3: 401 (2002. Белки ИБА эффективно подавляют апоптоз, индуцированный широким рядом апоптотических стимулов, включая химиотерапевтические агенты, облучение и иммунотерапию, в раковых клетках. Второй класс центральных негативных регуляторов апоптоза представляет собой семейство белковBcl-2 (Adams et al., Science 281: 1322 (1998); Reed, Adv. Pharmacol. 41: 501 (1997); Reed et al., J. Cell. Biochem. 60: 23 (1996. Bcl-2 является основополагающим членом этого семейства и был впервые выделен как продукт онкогена. В настоящее время семейство Bcl-2 включает как антиапоптотические молекулы,такие как Bcl-2 и Bcl-XL, так и проапоптотические молекулы, такие как Вах, Bak, Bid и Bad. Сверхэкспрессия Bcl-2 и Bcl-XL происходит при многих типах рака человека (например, молочной железы, простаты, прямой и ободочной кишки, легкого и т.д.), включая лимфому не-Ходжкина, которая вызвана хромосомной транслокацией (114, 18), которая приводит к сверхэкспрессии Bcl-2. Это позволяет предположить, что многие типы раковых клеток зависят от повышенного уровня Bcl-2 и/или Bcl-XL, чтобы пережить другие клеточные перестройки, которые одновременно и определяют их как раковые или предраковые клетки, и вызывают их попытки осуществить программу апоптоза. Также признано, что повышенная экспрессия белков семейства Bcl-2 является основой для развития устойчивости к противораковым лекарствам и облучению, которые действуя различными путями, вызывают клеточную гибель в опухолевых клетках. Считают, что Bcl-2 и Bcl-XL играют роль в миграции и инвазии опухолевых клеток, а, следовательно, и в метастазах (Amberger et al., Cancer Res. 55: 149 (1998); Wick et al., FEBS Lett, 440: 419 (1998); Mohanam et al., Cancer Res. 53: 4143 (1993); Pedersen et al., Cancer Res., 53: 5158 (1993. Показано, что белки семейства Bcl-2 обеспечивают опухолевые клетки механизмом для выживания в новых и непермессивных условиях (например, метастатические сайты) и вносят вклад в органоспецифичный паттерн распространения метастазов рака (Rubio, Lab Invest. 81: 125 (2001); Fernandez et al., Cell Death Differ. 7: 350(2000. Считают, что антиапоптотические белки, такие как Bcl-2 и/или Bcl-XL также регулируют межклеточные взаимодействия, например, посредством регуляции интегринов клеточной поверхности (Reed,Nature 557: 773 (1997); Frisch et al., Curr. Opin. Cell Biol. 9: 701 (1997); Del Bufalo et al., FASEB J. 11: 941(1997. Проведен подробный обзор терапевтических стратегий, направленных на Bcl-2 и Bcl-XL при раке,для восстановления чувствительности раковой клетки и преодоления устойчивости раковых клеток к апоптозу (Adams et al., Science 257: 1322 (1998); Reed, Adv. Pharmacol. 41: 501 (1997); Reed ef al., J. Cell.Biochem. 60: 23 (1996. В настоящее время антисмысловая терапия Bcl-2 находится в нескольких клинических испытаниях фазы III для лечения больших и небольших опухолей.-1 011218 Госсипол представляет собой природное димерное бифенольное соединение, выделенное из масла хлопковых семян (Gossypium sp.). Испытания госсипола на человеке в качестве мужского контрацептивного средства продемонстрировало безопасность долгосрочного введения этого соединения (Wu, Drugs 35: 333 (1989. Недавно показано, что госсипол обладает некоторыми антипролиферативными эффектами (Flack et al, J. Clin. Endocrinol Metab. 76: 1019 (1993); Bushunow et al., J. Neuro-Oncol. 43: 79, (1999);Van Poznak et al., Breast Cancer Res. Treat. 66: 239 (2001. Недавно показано, что (-)-госсипол и его производные являются эффективными ингибиторами Bcl-2 и Bcl-XL и обладают сильной противораковой активностью (заявка на патент США 2003/0008924). Композиция, содержащая рацемический госсипол и уксусную кислоту, известна (Сигма Олдрич Корп., С. Льюис, Миссури). Результатом прежних попыток кристаллизации (-)-госсипола были кристаллы, которые не подходили для рентгеноструктурного анализа (Gdaniec et al., "Gossypol", in Comprehensive Supramolecular Chemistry (Atwood et al. eds.), Vol. 6, Pergamon), или сокристаллы (-)-госсипола и ацетона при использовании раствора рацемической смеси госсипола и уксусной кислоты в ацетоне (Dowd etal., J. Am. Oil Chem. Soc. 76: 1343(1999. Краткое описание изобретения Настоящее изобретение относится к композициям, содержащим сокристаллы (-)-госсипола (формула I) с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1 (сокристаллы (-)-госсипола). Эти композиции пригодны для ингибирования активности антиапоптотических белков семейства Bcl-2, индукции апоптоза в клетках и повышения чувствительности клеток к индукторам апоптоза. В целом принято, что неспособность раковых клеток или их поддерживающих клеток подвергаться апоптозу в ответ на генетические повреждения или воздействие индукторов апоптоза (таких как противораковые агенты и облучение) является главным фактором в возникновении и развитии рака. Индукцию апоптоза в раковых клетках или их поддерживающих клетках (например, неоваскулярных клетках в системе сосудов опухоли) сегодня считают универсальным механизмом действия практически всех эффективных противораковых терапевтических препаратов или лучевых методов терапии на рынке или на практике. Одной из причин неспособности клетки подвергаться апоптозу является повышенная экспрессия и накопление антиапоптотических белков семейства Bcl-2. В настоящем изобретении рассматривается, что воздействие на животных, страдающих раком, терапевтически эффективными количествами сокристаллов (-)-госсипола, которые ингибируют функцию(и) антиапоптотических белков семейства Bcl-2, полностью уничтожает раковые клетки или их поддерживающие клетки (те клетки, продолжительное выживание которых зависит от гиперактивности белков семейства Bcl-2,) и/или делать такие клетки как популяцию более чувствительными к активности противораковых терапевтических лекарств или лучевых методов терапии, индуцирующих клеточную гибель. В настоящем изобретении рассматривается, что сокристаллы (-)-госсипола будут удовлетворять сильную необходимость в лечении множественных типов рака либо при введении в качестве монотерапии для индукции апоптоза в раковых клетках, зависимых от функции антиапоптотических белков семействаBcl-2, либо при введении совместно с другими противораковыми терапевтическими лекарствами или лучевыми методами терапии, индуцирующими клеточную гибель, чтобы придать большей доле раковых клеток или поддерживающих клеток чувствительность к выполнению программы апоптоза по сравнению с соответствующей долей клеток у животного, которого лечат только противораковым препаратом или подвергают лучевой терапии. В некоторых воплощениях изобретения ожидается, что комбинированное лечение животных терапевтически эффективным количеством композиции по изобретению и курсом противоракового агента или облучения будет давать более значительный ответ у опухоли и клиническую пользу у таких животных по сравнению с теми, которых лечат только композицией или противораковыми лекарствами/облучением отдельно. Иными словами, поскольку композиции снижают апоптотический порог всех клеток, которые экспрессируют антиапоптотические белки семейства Bcl-2, доля клеток, которые успешно выполняют программу апоптоза в ответ на индуцирующую апоптоз активность противораковых лекарств/облучения, будет повышена. Альтернативно ожидается, что композиции по изобретению дают возможность введения более низкой, а, следовательно, менее токсичной и более переносимой, дозы противоракового агента и/или облучения для получения такого же ответа у опухоли/клинической пользы как и при общепринятой дозе только одного противоракового агента/облучения. Поскольку дозы всех одобренных противораковых лекарств и лучевых методов лечения известны, в настоящем изобретении рассматривают комбинированные терапии с различными комбинациями известных лекарств/терапий с ком-2 011218 позициями по изобретению. Также, поскольку композиции по изобретению действуют, по меньшей мере частично, посредством ингибирования антиапоптотических белков семейства Bcl-2, воздействие на раковые клетки и поддерживающие клетки терапевтически эффективными количествами композиций может быть связано по времени с совпадением с попытками клеток выполнить программу апоптоза в ответ на противораковый агент или облучение. Таким образом, в некоторых воплощениях введение композиций по изобретению в связи с определенным временным отношением обеспечит особенно эффективные терапевтические методики. Сокристаллы (-)-госсипола применимы для лечения, облегчения или предупреждения заболеваний,которые реагируют на индукцию апоптотической клеточной гибели, например, расстройств, характеризующихся нарушением регуляции апоптоза, включая гиперпролиферативные заболевания, такие как рак. В некоторых воплощениях сокристаллы (-)-госсипола можно применять для лечения, облегчения или предупреждения рака, который характеризуется устойчивостью к противораковым методам лечения (например, являющегося хеморезистентным, устойчивым к облучению, гормонам и т.п.). В дополнительных воплощениях сокристаллы (-)-госсипола можно применять для лечения, облегчения или предупреждения метастатического рака. В других воплощениях сокристаллы (-)-госсипола можно применять для лечения гиперпролиферативных заболеваний, характеризующихся сверхэкспрессией антиапоптотических белков семейства Bcl-2. В настоящем изобретении предложены фармацевтические композиции, содержащие сокристаллы (-)госсипола и фармацевтически приемлемый носитель. Кроме того, в изобретении предложены способы получения фармацевтической композиции, содержащей смесь сокристаллов (-)-госсипола в терапевтически эффективном количестве для индукции апоптоза в клетках или для сенсибилизации клеток к индукторам апоптоза с фармацевтически приемлемым носителем. Кроме того, в изобретении предложены наборы, содержащие сокристаллы (-)-госсипола и инструкции по введению этой композиции животному. Эти наборы могут, возможно, содержать другие терапевтические агенты, например, противораковые агенты. В изобретении также предложены способы получения сокристаллов (-)-госсипола. Например, сокристаллы могут быть получены способом, при котором растворяют (-)-госсипол в ацетоне до образования раствора, фильтруют этот раствор, добавляют уксусную кислоту в этот раствор при перемешивании до тех пор, пока раствор не становится мутным, оставляют мутный раствор при комнатной температуре,затем при пониженной температуре до образования сокристаллов, собирают эти сокристаллы, промывают их растворителем и высушивают. Краткое описание графических материалов На фиг. 1 показан спектр 1 Н ЯМР сокристалла (-)-госсипола и уксусной кислоты. На фиг. 2 показан спектр 13 С ЯМР сокристалла (-)-госсипола и уксусной кислоты. На фиг. 3 показан инфракрасный спектр сокристалла (-)-госсипола и уксусной кислоты. На фиг. 4 показан масс-спектр сокристалла (-)-госсипола и уксусной кислоты. На фиг. 5 показан порошковая дифрактограмма рентгеновских лучей сокристалла (-)-госсипола и уксусной кислоты. Подробное описание изобретения Настоящее изобретение относится к композициям, содержащим сокристаллы (-)-госсипола с уксусной кислотой (сокристаллы (-)-госсипола), которые применимы в качестве ингибиторов антиапоптотических белков семейства Bcl-2. Посредством ингибирования антиапоптотических белков семейства Bcl-2(-)-госсипол сенсибилизирует клетки для индукторов апоптоза и в некоторых случаях сам индуцирует апоптоз. Таким образом, изобретение относится к способам сенсибилизации клеток для индукции апоптоза и к способам индукции апоптоза в клетках, при которых вводят сокристаллы (-)-госсипола одни или в комбинации с индуктором апоптоза. Кроме того, изобретение относится к способам лечения, облегчения или предупреждения заболеваний у животного, которые реагируют на индукцию апоптоза и при которых животному вводят сокристаллы (-)-госсипола и индуктор апоптоза. Такие заболевания включают те, которые характеризуются нарушением регуляции апоптоза, и те, которые характеризуются сверхэкспрессией антиапоптотических белков семейства Bcl-2. Термины (-)-госсипол или соединение/композиция (-)-госсипола, как их используют здесь, относятся к оптически активной композиции госсипола, где активные молекулы, составляющие эту композицию, вращают плоскость поляризованного света против часовой стрелки (например, левовращающие молекулы), как измерено с помощью поляриметра. Предпочтительно соединение (-)-госсипола имеет энантиомерный избыток от 1 до 100%. В одном воплощении соединение (-)-госсипола имеет энантиомерный избыток по меньшей мере 10, 20, 30, 40, 50, 60, 70, 80, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100% (-)-госсипола. В одном примере соединения (-)-госсипола удельное вращение ([]D) этого соединения составляет от примерно -350 до примерно -390C, от примерно -375 до примерно -390C или от примерно -385 до примерно -390C. (см., например, Dowd, Chirality, 15: 486 (2003); Ciesielska et ai, Chem.(1983. Способы разделения рацемических соединений госсипола на очищенный (+)- или (-)-госсипол известны (см., например, Zhou et ai, Kexue Tongbao, 28: 1574 (1983) (где: метиловый эфир Lфенилаланина смешивали с альдегидными группами госсипола с образованием Шиффова основания с двумя диастереоизомерами, которые затем разделяли обычной флэш-хроматографией на колонке силикагеля. Фильтрат концентрировали и остаток очищали хроматографией на силикагеле, элюируя смесью гексанов и EtOAc в соотношении 3:1, с получением двух фракций. В результате кислотного гидролиза этих двух фракций в 5N HCl:тетрагидрофуран (1:5, комнатная температура, в течение ночи) восстанавливали индивидуальные энантиомеры госсипола, соответственно. Первая фракция с более высоким значением Rf содержала (-)-госсипол, а вторая фракция с более низким значением Rf содержала (+)-госсипол. Фракции сырого госсипола экстрагировали в эфир из остатка после удаления ТГФ из реакционной смеси. Затем фракции госсипола очищали хроматографией на силикагеле и элюировали смесью гексанов иEtOAc (отношение 3:1) с получением оптически чистого госсипола при выходе 30-40% за две стадии. Значения дисперсии оптического вращения для этих продуктов составляли D = -352C (с=0,65, CHCl3) для (-)-госсипола и D = +341C (c=0,53, CHCl3. Термин C1-8-карбоновая кислота, как его используют здесь, относится к содержащей прямую цепь или разветвленной, ароматической или неароматической, насыщенной или ненасыщенной, замещенной или незамещенной С 1-8-карбоновой кислоте, включая, но не ограничиваясь ими, муравьиную кислоту,уксусную кислоту, пропионовую кислоту, н-масляную кислоту, трет-масляную кислоту, н-пентановую кислоту, 2-пентановую кислоту, н-гексановую кислоту, 2-гексановую кислоту, н-гептановую кислоту, ноктановую кислоту, акриловую кислоту, янтарную кислоту, фумаровую кислоту, яблочную кислоту,винную кислоту, лимонную кислоту, молочную кислоту и бензойную кислоту. Термин С 1-8-сульфоновая кислота, как его используют здесь, относится к содержащей прямую цепь или разветвленной, ароматической или неароматической, насыщенной или ненасыщенной, замещенной или незамещенной С 1-8-сульфоновой кислоте, включая, но не ограничиваясь ими, метансульфоновую кислоту, этансульфоновую кислоту, н-пропансульфоновую кислоту, 2-пропансульфоновую кислоту, н-бутансульфоновую кислоту, н-пентансульфоновую кислоту, н-гексансульфоновую кислоту, нгептансульфоновую кислоту, н-октансульфоновую кислоту и бензолсульфоновую кислоту. Термин сокристалл (-)-госсипола, как его используют здесь, относится к композиции, содержащей сокристаллы (-)-госсипола и С 1-8-карбоновую кислоту или С 1-8-сульфоновую кислоту. Термин белки семейства Bcl-2, как его используют здесь, относится как к антиапоптотическим членам семейства Bcl-2, включая, но не ограничиваясь ими, Bcl-2, Bcl-XL, Mcl-1, A1/BFL-1, BOO-DIVA,Bcl-w, Bcl-6, Bcl-8 и Bcl-y, так и к проапоптотическим членам семейства Bcl-2, включая, но не ограничиваясь ими, Bak, Вах, Bad, tBid, Hrk, Bim, Bmf, а также к другим белкам, содержащим гомологичный Bcl-2 домен 3 (ВН 3), которые регулируются соединениями госсипола. Термин сверхэкспрессия антиапоптотических белков семейства Bcl-2, как его используют здесь,относится к повышенному уровню (например, к аберрантному уровню) мРНК, кодирующих антиапоптотический(е) белок (белки) семейства Bcl-2, и/или к повышенным уровням антиапоптотического(их) белка(ов) семейства Bcl-2 в клетках по сравнению с соответствующими непатологическими клетками, экспрессирующими базальные уровни мРНК, кодирующих антиапоптотические белки семейства Bcl-2, или имеющими базальные уровни антиапоптотических белков семейства Bcl-2. Способы определения уровней мРНК, кодирующих антиапоптотические белки семейства Bcl-2, или уровней антиапоптотических белков семейства Bcl-2 в клетке включают, но не ограничены ими, Вестерн-блоттинг с использованием антител к антиапоптотическим белкам семейства Bcl-2, способы иммуногистохимии и способы амплификации нуклеиновых кислот или непосредственного обнаружения РНК. Для определения того, что в клетках существует сверхэкспрессия антиапоптотических белков семейства Bcl-2, важен как абсолютный уровень антиапоптотических белков семейства Bcl-2 в клетках, так и относительный уровень антиапоптотических белков семейства Bcl-2 по отношению к другим проапоптотическим сигнальным молекулам(например, проапоптотических белков семейства Bcl-2) в таких клетках. Когда их баланс является не в пользу уровня антиапоптотических белков семейства Bcl-2, проапоптотические сигнальные молекулы вызывают выполнение клетками программы апоптоза и, следовательно, их гибель, поэтому выживание указанных клеток будут зависеть от антиапоптотических белков семейства Bcl-2. В таких клетках воздействие эффективного количества ингибитора антиапоптотических белков семейства Bcl-2 будет достаточным, чтобы вызвать выполнение клетками программы апоптоза и их гибель. Таким образом, термин сверхэкспрессия антиапоптотических белков семейства Bcl-2 также относится к клеткам, которые за счет относительных уровней проапоптотических сигналов и антиапоптотических сигналов подвергаются апоптозу в ответ на эффективные количества соединений, которые ингибируют функцию антиапоптотических белков семейства Bcl-2. Термины противораковый агент и противораковое лекарство, как их используют здесь, относятся к любому терапевтическому агенту (например, к химиотерапевтическим соединениям и/или молекулярным терапевтическим соединениям), лучевой терапии или хирургическим вмешательствам, применяемым при лечении гиперпролиферативных заболеваний, таких как рак (например, у млекопитающих).-4 011218 Термин терапевтически эффективное количество, как его используют здесь, относятся к количеству терапевтического агента, достаточному, чтобы привести в результате к облегчению одного или более симптома заболевания или к предупреждению прогрессирования болезни, либо вызвать регрессию заболевания. Например, в отношении лечения рака терапевтически эффективное количество предпочтительно относится к количеству терапевтического агента, которое снижает скорость опухолевого роста,уменьшает массу опухоли, снижает количество метастазов, увеличивает время до прогрессирования опухоли или увеличивает срок жизни по меньшей мере на 5%, предпочтительно по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 100%. Термины сенсибилизировать и сенсибилизация, как их используют здесь, относятся к тому,чтобы посредством введения первого агента (например, соединения формулы I) сделать животное или клетку этого животного более чувствительными или дающими более выраженный ответ к биологическим эффектам (например, стимуляции или задержке клеточной функции, включая, но не ограничиваясь ими, клеточный рост, пролиферацию, инвазию, ангиогенез или апоптоз) второго агента. Сенсибилизирующий эффект первого агента в отношении клетки-мишени можно измерить как разность в предназначенном биологическом эффекте (например, стимуляции или задержке клеточной функции, включая, но не ограничиваясь ими, клеточный рост, пролиферацию, инвазию, ангиогенез или апоптоз), наблюдаемом при введении второго агента с введением или без введения первого агента. Ответ сенсибилизированной клетки может быть повышен по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 100%, по меньшей мере на 150%, по меньшей мере на 200%, по меньшей мере на 300%, по меньшей мере на 350%, по меньшей мере на 400%, по меньшей мере на 450% или по меньшей мере на 500% по сравнению с ответом при отсутствии первого агента. Термин нарушение регуляции апоптоза, как его используют здесь, относятся к любому нарушению способности (например, предрасположенности) клетки к осуществлению клеточной гибели посредством апоптоза. Нарушение регуляции апоптоза связано с рядом состояний или вызвано ими, включая,например, аутоиммунные заболевания (например, системную красную волчанку, ревматоидный артрит,болезнь трансплантат против хозяина, тяжелую миастению или синдром Шегрена), хронические воспалительные состояния (например, псориаз, астму или болезнь Крона), гиперпролиферативные нарушения(например, опухоли, лимфомы В- и Т-лимфоцитов), вирусные инфекции (например, герпес, папиллому или ВИЧ) и другие состояния, такие как остеоартрит и атеросклероз. Следует отметить, что, когда нарушение регуляции вызвано вирусной инфекцией или связано с ней, эта вирусная инфекция может быть обнаруживаемой или необнаруживаемой в тот момент, когда происходит или наблюдается нарушение регуляции. То есть, нарушение регуляции, индуцированное вирусом, может происходить даже после исчезновения симптомов вирусной инфекции. Термин гиперпролиферативное заболевание, как его используют здесь, относится к любому состоянию, при котором локализованная популяция пролиферирующих клеток у животного не подчинена обычным ограничениям нормального роста. Примеры гиперпролиферативных нарушений включают опухоли, неоплазмы, лимфомы и тому подобное. Неоплазму считают доброкачественной, если она не инвазирует или метастазирует, и злокачественной, если она осуществляет хотя бы одно из двух. Метастатическая клетка означает, что эта клетка может осуществлять инвазию и разрушать соседние структуры организма. Гиперплазия представляет собой форму клеточной пролиферации, в которую вовлечено увеличение числа клеток в ткани или органе без значительного изменения в структуре или функции. Метаплазия представляет собой форму регулируемого клеточного роста, при которой один тип полностью дифференцированных клеток замещен другим типом дифференцированных клеток. Результатом патологического роста активированных лимфоидных клеток часто является аутоиммунное заболевание или хроническое воспалительное состояние. Термин аутоиммунное заболевание,как его используют здесь, относится к любому состоянию, при котором организм продуцирует антитела или иммунные клетки, которые распознают собственные молекулы, клетки или ткани организма. Не ограничивающие примеры аутоиммунных заболеваний включают аутоиммунную гемолитическую анемию,аутоиммунный гепатит, болезнь Бергера или IgA нефропатию, глютеновую болезнь, синдром хронической усталости, болезнь Крона, дерматомиозит, фибромиалгию, болезнь трансплантат против хозяина,болезнь Грейвса, тиреоидит Хасимото, идиопатическую тромбоцитопеническую пурпуру, плоский лишай, рассеянный склероз, тяжелую миастению, псориаз, ревматическую лихорадку, ревматический артрит, склеродерму, синдром Шегрена, системную красную волчанку, диабет типа I, неспецифический язвенный колит, витилиго и тому подобное. Термин неопластическое заболевание, как его используют здесь, относится к любому аномальному росту клеток, являющемуся либо доброкачественным (нераковым), либо злокачественным (рако-5 011218 вым). Термин антинеопластический агент, как его используют здесь, относится к любому соединению,которое задерживает пролиферацию, рост или распространение неоплазмы-мишени (например, злокачественной). Термины предупреждать, предупреждающий и предупреждение, как их используют здесь,относится к снижению количества патологических клеток (например, гиперпролиферативных или неопластических клеток) у животного. Предупреждение может быть полным, например, полное отсутствие патологических клеток у объекта. Предупреждение может быть также частичным, так что количество патологических клеток у объекта меньше, чем было бы их количество без настоящего изобретения. Термин синергичный, как его используют здесь, относится к эффекту, полученному, когда сокристаллы (-)-госсипола и второй агент вводят совместно (например, в одно и то же время или один после другого), который является более высоким, чем аддитивный эффект сокристаллов (-)-госсипола и второго агента, когда их вводят по отдельности. Синергичный эффект дает возможность для введения более низких доз сокристаллов (-)-госсипола и/или второго агента или обеспечивает большую эффективность при тех же дозах. Полученный синергичный эффект может быть по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 100%, по меньшей мере на 125%, по меньшей мере на 150%, по меньшей мере на 175%, по меньшей мере на 200%, по меньшей мере на 250%, по меньшей мере на 300%, по меньшей мере на 350%,по меньшей мере на 400% или по меньшей мере на 500% больше, чем аддитивный эффект сокристаллического соединения (-)-госсипола и второго агента, когда их вводят по отдельности. Например, в отношении лечения рака синергичный эффект может представлять собой снижение скорости опухолевого роста, уменьшение массы опухоли, снижение числа метастазов, увеличение времени до прогрессирования опухоли или увеличение срока жизни. Совместное введение сокристаллов (-)-госсипола и противоракового агента может дать возможность применения более низких доз сокристаллов (-)-госсипола и/или противоракового агента, так чтобы эффективно лечить рак, избегая при этом какой-либо существенной токсичности для объекта. Термин примерно, как его используют здесь, включает указанное число +/-10%. Так, примерно 0,5 означает от 0,45 до 0,55. Ингибиторы семейства антиапоптотических белков Bci-2 по изобретению представляют собой композиции, содержащие сокристаллы (-)-госсипола с уксусной кислотой (сокристаллы (-)-госсипола). Ожидают, что сокристаллы (-)-госсипола более стабильны, чем (-)-госсипол в отдельности. Специалистам в данной области техники будет понятна важность стабильности соединения при производстве,хранении, транспортировке и/или обращении с фармацевтическими композициями. Ожидают, что настоящие композиции более стабильны, чем описанные ранее композиции, содержащие (-)-госсипол. Любую С 1-8-карбоновую кислоту или C1-8-сульфоновую кислоту, которая способна стабилизировать (-)госсипол, можно использовать в изобретении. Молярное отношение (-)-госсипола к карбоновой кислоте или сульфоновой кислоте в сокристалле (-)-госсипола находится в интервале от примерно 10:1 до примерно 1:10, предпочтительно от примерно 2:1 до примерно 1:2, более предпочтительно примерно 1:1. В некоторых воплощениях молярное отношение (-)-госсипола к карбоновой кислоте или сульфоновой кислоте в сокристалле (-)-госсипола может составлять примерно 10:1, 9:1, 8:1, 7:1, 6:1, 5:1, 4:1, 3:1, 2:1,1,5:1, 1:1, 1:1,5, 1:2, 1:3, 1:4, 1:5, 1:6, 1:7, 1:8, 1:9 или 1:10. В одном воплощении изобретения С 1-8-карбоновая кислота представляет собой уксусную кислоту. В другом воплощении сокристалл (-)-госсипола содержит (-)-госсипол и уксусную кислоту в молярном отношении примерно 1:1. В предпочтительном воплощении сокристалл (-)-госсипола и уксусной кислоты (1:1) находится в форме желтых или бледно-желтых кристаллов игольчатой формы. В другом предпочтительном воплощении сокристалл характеризуется интеграцией спектра 1 Н ЯМР при 2,11 (s, 3H),который представляет собой один сигнал метила уксусной кислоты, и 2,18 (s, 6H), который представляет собой два сигнала метила госсипола. Композиции по данному изобретению могут быть получены, используя способы, известные специалистам в данной области техники, а также как описано в примерах. В одном воплощении сокристаллы получают путем растворения (-)-госсипола в ацетоне до образования раствора, фильтрования этого раствора, добавления уксусной кислоты в этот раствор при перемешивании до тех пор, пока раствор не становится мутным, выдерживания этого мутного раствора при комнатной температуре, затем при пониженной температуре до образования сокристаллов. В одном воплощении раствор смешивают путем постоянного перемешивания. Пониженная температура составляет менее чем примерно 20C, предпочтительно примерно 0-15C, более предпочтительно примерно 4C. Время для образования сокристаллов может находиться в интервале от 1 ч до 1 суток, предпочтительно это время составляет примерно 1-4 ч. Сокристаллы можно собирать любыми пригодными способами, включая фильтрование. Растворитель для промывки сокристаллов может представлять собой любой подходящий растворитель, например гексан, пентан, бензол, толуол или петролейный эфир. Промытые сокристаллы можно высушивать при ком-6 011218 натной температуре, предпочтительно в защищенном от света контейнере. Сокристаллы можно также высушивать в вакуумной сушилке, предпочтительно при повышенной температуре (например, примерно 30-60C, более предпочтительно примерно 40C) в течение примерно 6-72 ч, предпочтительно примерно 12-48 ч. Показано, что (-)-госсипол связывается с Bcl-2 и Bcl-XL по ВН 3-связывающей канавке и обладает значительной противораковой активностью (заявка на патент США 2003/0008924). Важный аспект настоящего изобретения состоит в том, что сокристалл (-)-госсипола связывается с антиапоптотическими белками Bcl-2 и ингибирует их таким же способом, что и госсипол. Однако ожидают, что сокристалл (-)госсипола более стабилен, чем (-)-госсипол. Кроме того, (-)-госсипол является более эффективным ингибитором, чем рацемический госсипол. Таким образом, композиции, содержащие сокристаллы (-)госсипола, можно применять для индукции апоптоза, а также усиливать индукцию апоптоза в ответ на сигналы индукции апоптоза. Рассматривают, что эти композиции сенсибилизируют клетки к индукторам апоптоза, включая клетки, которые являются устойчивыми к таким индукторам. Композиции по изобретению можно применять для индукции апоптоза при любом расстройстве, которое можно лечить, облегчать или предупреждать посредством индукции апоптоза. Таким образом, в настоящем изобретении предложены композиции и способы, направленные на животных, характеризующихся сверхэкспрессией антиапоптотических белков семейства Bcl-2. В некоторых воплощениях клетки (например, раковые клетки) проявляют повышенные уровни экспрессии одного или более антиапоптотического белка семейства Bcl-2 по сравнению с непатологическими образцами (например, нераковыми клетками). В других воплощениях клетки быстро проявляют повышенные уровни экспрессии антиапоптотических белков семейства Bcl-2 посредством выполнения программы апоптоза и гибели в ответ на введение эффективно ингибирующего количества сокристаллов (-)-госсипола, где указанный ответ осуществляется, по меньшей мере частично, благодаря зависимости выживания таких клеток от функции антиапоптотического белка семейства Bcl-2. В некоторых воплощениях композиции и способы по изобретению применяют для лечения пораженных заболеванием клеток, тканей, органов или патологических состояний и/или болезненных состояний у животного (например, у млекопитающего, включая, но не ограничиваясь ими, людей и ветеринарных животных). В этом отношении различные заболевания и патологии поддаются лечению или профилактике с применением настоящих способов и композиций. Не ограничивающий примерный перечень этих заболеваний и состояний включает, но не ограничен ими, различные виды рака, такие как рак молочной железы, рак простаты, лимфома, рак кожи, рак поджелудочной железы, рак толстой кишки, меланому, злокачественную меланому, рак яичника, рак головного мозга, первичную карциному головного мозга, рак в области головы и шеи, глиому, глиобластому, рак печени, рак мочевого пузыря, немелкоклеточный рак легкого, карциному головы или шеи, карциному молочной железы, карциному яичника, карциному легкого, мелкоклеточный рак легкого, опухоль Вильмса, карциному шейки матки, карциному яичка, карциному мочевого пузыря, карциному поджелудочной железы, карциному желудка, карциному толстой кишки, карциному простаты, карциному мочеполовых органов, карциному щитовидной железы,карциному пищевода, миелому, множественную миелому, адренокарциному, почечно-клеточный рак,карциному эндометрия, карциному коры надпочечников, злокачественную инсулиному поджелудочной железы, злокачественную карциноидную опухоль, хориокарциному, грибовидную гранулему, злокачественную гиперкальцемию, гиперплазию шейки матки, лейкоз, острый лимфолейкоз, хронический лимфолейкоз, острый миелогенный лейкоз, хронический миелогенный лейкоз, хронический гранулоцитарный лейкоз, лейкоз ворсистых клеток, нейробластому, рабдомиосаркому, саркому Капоши, истинную полицитемию, идиопатический тромбоцитоз, болезнь Ходжкина, лимфому не-Ходжкина, саркому мягких тканей, остеогенную саркому, первичную макроглобулинемию и ретинобластому и тому подобное; опосредованные Т- и В- клетками аутоиммунные заболевания, воспалительные заболевания, инфекции, гиперпролиферативные заболевания, СПИД, дегенеративные состояния, сосудистые заболевания и тому подобное. В некоторых воплощениях раковые клетки, подлежащие лечению, являются метастазирующими. В других воплощениях раковые клетки, подлежащие лечению, являются устойчивыми к противораковым агентам. В некоторых воплощениях настоящего изобретения предложены способы введения эффективного количества сокристаллов (-)-госсипола и по меньшей мере одного дополнительного терапевтического агента (включая, но не ограничиваясь ими, химиотерапевтические агенты, противоопухолевые агенты,противомикробные агенты, противовирусные агенты, противогрибковые агенты) и/или назначения терапевтической методики (например, хирургического вмешательства и/или лучевой терапии). В некоторых воплощениях комбинация сокристаллов (-)-госсипола и одного или более терапевтического агента будет обладать большим эффектом по сравнению с введением любого из соединений в отдельности. В других воплощениях ожидают, что комбинация сокристаллов (-)-госсипола и одного или более терапевтического агента приведет в результате к синергичному эффекту (то есть большему, чем аддитивный) по сравнению с введением любого из соединений в отдельности. Ряд пригодных противораковых агентов рассмотрен для применения в способах по изобретению. Действительно, в настоящем изобретении рассмотрено, но не ограничено ими, введение ряда противора-7 011218 ковых агентов, таких как: агенты, которые индуцируют апоптоз; полинуклеотиды (например, антисмысловые, рибозимы, малые интерферирующие РНК); полипептиды (например, ферменты и антитела); биологические миметики (например, миметики госсипола или ВН 3); агенты, которые связываются (например, олигомеризуют или образуют комплекс) с белком семейства Bcl-2, таким как Вах; алкалоиды; алкилирующие агенты; противоопухолевые антибиотики; антиметаболиты; гормоны; соединения платины; моноклональные или поликлональные антитела (например, антитела, конъюгированные с противораковыми лекарствами, токсинами, дефензинами), токсины; радионуклиды; модификаторы биологического ответа (например, интерфероны (например, IFN-) и интерлейкины (например, IL-2; агенты адаптивной иммунотерапии; гематопоэтические ростовые факторы; агенты, которые индуцируют дифференциацию опухолевых клеток (например, полностью транс-ретиноевая кислота); реагенты генотерапии(например, реагенты антисмысловой терапии и нуклеотиды); опухолевые вакцины; ингибиторы ангиогенеза; ингибиторы протеосом: модуляторы NF-KB; соединения, воздействующие на циклин-зависимые киназы (CDK); ингибиторы гистон-деацетилаз (HDAC) и тому подобное. Различные другие примеры химиотерапевтических соединений и противораковых терапий, пригодных для совместного введения с раскрытыми соединениями, известны в данной области техники. В предпочтительных воплощениях противораковые агенты включают агенты, которые индуцируют или стимулируют апоптоз. Агенты, которые индуцируют апоптоз, включают, но не ограничены ими, облучение (например, рентгеновские лучи, гамма-лучи, УФ); ингибиторы киназ (например, ингибитор киназы рецептора эпидермального ростового фактора (EGFR), ингибитор киназы рецептора фактора роста сосудов (VGFR), ингибитор киназы рецептора фактора роста фибробластов (FGFR), ингибитор киназы рецептора фактора роста тромбоцитарного происхождения (PDGFR) и ингибиторы киназ Bcr-Abl (такие как GLEEVEC; антисмысловые молекулы; антитела (например, Герцептин, Ритуксан, Зевалин,Бексар и Авастин); антиэстрогены (например, ралоксифен и тамоксифен); антиандрогены (например, флутамид, бикалутамид, финастерид, аминоглютетамид, кетоконазол и кортикостероиды); ингибиторы циклооксигеназы 2 (СОХ-2) (например, целекоксиб, мелоксикам, NS-398 и нестероидные противовоспалительные лекарства); противовоспалительные лекарства (например, бутазолидин, Декадрон,Делтазон, дексаметазон, дексаметазон интензол, Дексон, Гексадрол, гидроксихлорохин, Метикортен, Орадекзон, Оразон, оксифенбутазон, Периапред, фенилбутазон, Плаквенил, преднизолон, преднизон, Прелон и Тандеарил) и противораковые химиотерапевтические лекарства (например, иринотекан (Камптосар), СРТ-11, флударабин (Флудара), дакарбазин, дексаметазон, митоксантрон, Милотарг, вепезид VP-16, цисплатин, карбоплатин, оксалиплатин, 5-ФУ (флюороурацил), доксорубицин, гемцитабин, бортезомиб, гефитиниб, бевацизумаб, Таксотер или Таксол); молекулы клеточного сигналинга; церамиды и цитокины; стауроспорин и тому подобное. В других воплощениях в композициях и способах по изобретению предложены сокристаллы (-)госсипола и по меньшей мере один противогиперпролиферативный или противоопухолевый агент; например, выбранный из алкилирующих агентов, антиметаболитов и натуральных продуктов (например,лекарственных трав и/или других соединений растительного и/или животного происхождения). Алкилирующие агенты, пригодные для применения в композициях и способах по изобретению,включают, но не ограничены ими: 1) азотистые иприты (например, мехлоретамин, циклофосфамид,ифосфамид, мелфалан (L-сарколизин) и хлорамбуцил); 2) этиленимины и метилмеламины (например,гексаметилмеламин и тиотепа); 3) алкилсульфонаты (например, бусульфан); 4) нитрозомочевины (например, кармустин (BCNU); ломустин (CCNU); семустин (метил-CCNU) и стрептозоцин (стрептозотоцин и 5) триазены (например, дакарбазин (диметилтриазеноимидазолкарбоксамид. В некоторых воплощениях антиметаболиты, пригодные для применения в композициях и способах по изобретению, включают, но не ограничены ими: 1) аналоги фолиевой кислоты (например, метотрексат(6-меркаптопурин), тиогуанин (6-тиогуанин) и пентостатин (2'-дезоксикоформицин. В следующих воплощениях химиотерапевтические агенты, пригодные для применения в композициях и способах по изобретению, включают, но не ограничены ими: 1) алкалоиды винка (например,винбластин, винкристин); 2) эпиподофиллотоксины (например, этопозид и тенипозид); 3) антибиотики(например, дактиномицин (актиномицин D), даунорубицин (дауномицин; рубидомицин), доксорубицин,блеомицин, пликамицин (митрамицин) и митомицин (митомицин С; 4) ферменты (например, Lаспарагиназу); 5) модификаторы биологического ответа (например, интерферон-альфа); 6) координационные комплексы платины (например, цисплатин и карбоплатин); 7) антрацендионы (например, митоксантрон); 8) замещенные мочевины (например, гидроксимочевину); 9) производные метилгидразина (например, прокарбазин (N-метилгидразин; 10) адренокортикосупрессанты (например, митотан (o,p'-DDD) и аминоглютенимид); 11) адренокортикостероиды (например, преднизон); 12) прогестины (например,гидроксипрогестерона капроат, медроксипрогестерона ацетат и мегестрола ацетат); 13) эстрогены (например, диэтилстилбестрол и этинилэстрадиол); 14) антиэстрогены (например, тамоксифен); 15) андрогены (например, тестостерона пропионат и флуоксиместерон); 16) антиандрогены (например, флутамид) и 17) аналоги гормона, высвобождающего гонадотропин (например, лейпролид).-8 011218 Любой онколитический агент, который используют в рутинной терапии рака, находит применение в композициях и способах по изобретению. Например, Управление по лекарствам и пищевым продуктам США (US FDA) утверждает перечень онколитических агентов, одобренных к применению в США. Международные агентства-партнеры US FDA утверждают подобные перечни. В табл. 1 представлен перечень примерных противоопухолевых агентов, одобренных к применению в США. Специалистам в данной области техники будет понятно, что "этикетки продуктов", требуемые на всех одобренных в США химиотерапевтических агентах, описывают одобренные показания, информацию по дозировке, данные по токсичности и тому подобное. Таблица 1 Предпочтительные общепринятые противораковые агенты для применения при введении с настоящими соединениями включают, но не ограничены ими, адриамицин, 5-фторурацил, этопозид, камптоте- 20011218 цин, актиномицин D, митомицин С, цисплатин, доцетаксел, гемцитабин, карбоплатин, оксалиплатин,бортезомиб, гефитиниб и бевацизумаб. Эти агенты можно получать и применять отдельно, в комбинированных терапевтических композициях, в наборах или в комбинации с иммунотерапевтическими агентами и тому подобным. Для более подробного описания противораковых агентов и других терапевтических агентов специалистов в данной области техники отсылают к любым инструкциям, включая, но не ограничиваясь ими, Physician's Desk Reference и Goodman and Gilman, "Pharmaceutical Basis of Therapeutics", 9th edition,Eds. Hardman et al, 1996. В настоящем изобретении предложены способы введения сокристаллов (-)-госсипола с лучевой терапией. Изобретение не ограничено типами, количествами или системами доставки и введения, применяемыми для доставки терапевтической дозы облучения животному. Например, животное может получать фотонную радиотерапию, лучевую терапию пучком частиц, радиоизотопную терапию (например,радиоактивные конъюгаты с моноклональными антителами), другие типы лучевых терапий и их комбинации. В некоторых воплощениях облучение животного проводят, используя линейный ускоритель. В других воплощениях облучение проводят с использованием гамма-ножа. Источник излучения может быть наружным или внутренним для животного. Наружная лучевая терапия является наиболее распространенной и включает направление пучка излучения высокой энергии к сайту опухоли через кожу, используя, например, линейный ускоритель. Хотя пучок излучения локализован в сайте опухоли, почти невозможно избежать воздействия на нормальную здоровую ткань. Однако наружное излучение обычно хорошо переносится пациентами. Внутренняя лучевая терапия включает имплантацию источника излучения, такого как шарики, проволоки, гранулы, капсулы, частицы и тому подобное, внутрь организма около сайта опухоли или в него, включая использование систем доставки,которые специфично направлены на раковые клетки (например, использование частиц, присоединенных к лигандам, которые связываются с раковыми клетками). Такие имплантаты можно удалить после лечения или оставить в организме в неактивном состоянии. Типы внутренней лучевой терапии включают, но не ограничены ими, брахитерапию, интерстициальное облучение, внутриполостное облучение, радиоиммунотерапию и тому подобное. Животное может возможно получать радиосенсибилизаторы (например, метронидазол, мизонидазол, внутриартериальный БУДР, внутривенный иоддезоксиуридин (ИудР), нитроимидазол, 5 замещенные-4-нитроимидазолы, 2 Н-изоиндолдионы, (2-бромэтил)амино]метил]-1 Н-имидазол-1-этанол,производные нитроанилина, ДНК-аффинные избирательные гипоскические цитотоксины, галогенированный ДНК-лиганд, 1,2,4-бензотриазиноксиды, производные 2-нитроимидазола, фторсодержащие производные нитроазола, бензамид, никотинамид, акридин-интеркалятор, производное 5-тиотетразола, 3 нитро-1,2,4-триазол, производное 4,5-динитроимидазола, гидроксилированные тексафрины, цисплатин,митомицин, тирипазамин, нитрозомочевину, меркаптопурин, метотрексат, фторурацил, блеомицин, винкристин, карбоплатин, эпирубицин, доксорубицин, циклофосфамид, виндезин, этопозид, паклитаксел,тепло (гипертермию) и тому подобное), радиопротекторы (например, цистеамин, аминоалкилдигидрофосфоротиоаты, амифостин (WR 2721), интерлейкин IL-1, IL-6 и тому подобное). Радиосенсибилизаторы усиливают уничтожение опухолевых клеток. Радиопротекторы защищают здоровую ткань от повреждающих эффектов излучения. Любой тип облучения можно назначать пациенту до тех пор, пока доза облучения переносится пациентом без неприемлемых отрицательных побочных эффектов. Пригодные типы лучевой терапии включают, например, ионизирующую (электромагнитную) лучевую терапию (например, рентгеновские лучи или гамма-лучи) или лучевую терапию пучком частиц (например, излучение высокой энергии). Ионизирующее излучение определяют как излучение, содержащее частицы или фотоны, которые обладают достаточной энергией, чтобы производить ионизацию, например, добавление или потерю электронов(как описано, например, в US 5770581, включенном здесь путем ссылки в полном объеме). Эффекты облучения могут по меньшей мере частично контролироваться врачом. Доза облучения предпочтительно фракционирована с целью максимального воздействия на клетку-мишень и сниженной токсичности. Суммарная доза облучения, назначаемая животному, предпочтительно составляет от примерно 0,01 Грей (Гр) до примерно 100 Гр. Более предпочтительно от примерно 10 до примерно 65 Гр (например,примерно 15, 20, 25, 30, 35, 40, 45, 50, 55 или 60 Гр) вводят в течение курса лечения. Хотя в некоторых воплощениях полную дозу облучения можно назначать в течение курса в одни сутки, в идеале суммарную дозу разбивают на части и воздействуют в течение нескольких суток. Желательно лучевую терапию назначать в течение курса по меньшей мере примерно 3 суток, например, по меньшей мере 5, 7, 10, 14,17, 21, 25, 28, 32, 35, 38, 42, 46, 52 или 56 суток (примерно 1-8 недель). Соответственно, суточная доза облучения будет составлять примерно 1-5 Гр (например, примерно 1, 1,5, 1,8, 2, 2,5, 2,8, 3, 3,2, 3,5, 3,8, 4,4,2 или 4,5 Гр), предпочтительно 1-2 Гр (например, 1,5-2 Гр). Суточная доза облучения должна быть достаточна для индукции разрушения клеток-мишеней. Если его продолжают в течение периода времени,облучением предпочтительно не воздействовать каждые сутки, давая, таким образом, животному возможность отдыхать, а эффектам терапии проявляться. Например, облучение желательно воздействовать на 5 последовательных суток и не назначать на 2 суток для каждой недели лечения, давая, таким обра- 21011218 зом, возможность для отдыха 2 суток в неделю. Однако облучение можно назначать как 1 сутки/неделя, 2 суток/неделя, 3 суток/неделя, 4 суток/неделя, 5 суток/неделя, 6 суток/неделя или все 7 суток/неделя в зависимости от ответной реакции животного и каких-либо потенциальных побочных эффектов. Лучевую терапию можно начинать в любое время в терапевтический период. Предпочтительно лучевую терапию начинают на неделе 1 или неделе 2 и проводят в течение оставшейся продолжительности терапевтического периода. Например, облучение проводят на неделе 1-6 или на неделе 2-6 терапевтического периода, состоящего из 6 недель для лечения, например, большой опухоли. Альтернативно облучение проводят на неделе 1-5 или на неделе 2-5 терапевтического периода, состоящего из 5 недель. Эти примерные режимы назначения лучевой терапии не предназначены, однако, для ограничения настоящего изобретения. Противомикробные терапевтические агенты можно также применять в качестве терапевтических агентов в настоящем изобретении. Можно применять любой агент, который может убивать, ингибировать или иным путем ослаблять функционирование микроорганизмов, а также любой агент, рассматриваемый как обладающий такими активностями. Противомикробные агенты включают, но не ограничены ими, природные и синтетические антибиотики, антитела, ингибиторные белки (например, дефензины),антисмысловые нуклеиновые кислоты, агенты, разрушающие мембрану, и тому подобное, используемые отдельно или в комбинации. Действительно, можно применять любой тип антибиотика, включая, но не ограничиваясь ими, антибактериальные агенты, противовирусные агенты, противогрибковые агенты и тому подобное. В некоторых воплощениях настоящего изобретения сокристаллы (-)-госсипола и один или более терапевтический агент или противораковый агент вводят животному при одних или более из приведенных ниже условий: с различной периодичностью, с различной длительностью, при различных концентрациях,различными путями введения и т.д. В некоторых воплощениях сокристаллы (-)-госсипола вводят перед терапевтическим или противораковым агентом, например, за 0,5, 1, 2, 3, 4, 5, 10, 12 или 18 ч, 1, 2, 3, 4, 5 или 6 суток, 1, 2, 3 или 4 недели до введения терапевтического или противоракового агента. В некоторых воплощениях сокристаллы (-)-госсипола вводят после терапевтического или противоракового агента,например, через 0,5, 1, 2, 3, 4, 5, 10, 12 или 18 ч, 1, 2, 3, 4, 5 или 6 суток, 1, 2, 3 или 4 недели после введения противоракового агента. В некоторых воплощениях сокристаллы (-)-госсипола и терапевтический или противораковый агент вводят одновременно, но при различных режимах, например, сокристаллы (-)госсипола вводят ежесуточно, тогда как терапевтический или противораковый агент вводят раз в неделю,раз в две недели, раз в три недели или раз в четыре недели. В других воплощениях сокристаллы (-)госсипола вводят раз в неделю, тогда как терапевтический или противораковый агент вводят ежесуточно,раз в неделю, раз в две недели, раз в три недели или раз в четыре недели. Фармацевтические композиции могут быть получены путем объединения сокристаллов (-)госсипола в терапевтически эффективном количестве для индукции апоптоза в клетках или для сенсибилизации клеток к индукторам апоптоза с фармацевтически приемлемым носителем. Новые фармацевтические композиции по изобретению содержат интактные сокристаллы (-)-госсипола. В некоторых воплощениях фармацевтические композиции содержат сокристаллы (-)-госсипола в комбинации с жидкостью, в которой эти сокристаллы практически нерастворимы (например, с водой), для образования суспензии. Композиции в пределах объема данного изобретения включают все композиции, где композиции по изобретению содержатся в количестве, которое является эффективным для достижения поставленной цели. Хотя индивидуальные значения варьируют, определение оптимальных интервалов эффективных количеств каждого компонента находится в пределах компетенции специалистов в данной области техники. В основном композиции можно вводить млекопитающим, например, людям, перорально в дозе от 0,0025 до 50 мг или эквивалентное количество их фармацевтически приемлемой соли в сутки на 1 кг массы тела млекопитающего, подлежащего лечению заболеваний, реагирующих на индукцию апоптоза. Предпочтительно от примерно 0,01 до примерно 10 мг/кг вводят перорально для лечения, облегчения или предупреждения таких заболеваний. Для внутримышечной инъекции доза, как правило, составляет половину пероральной дозы. Например, подходящая внутримышечная доза будет составлять от примерно 0,0025 до примерно 25 мг/мг, и наиболее предпочтительно от примерно 0,01 до примерно 5 мг/мг. Стандартная пероральная доза может содержать от примерно 0,01 до примерно 200 мг, предпочтительно от примерно 0,1 до примерно 100 мг композиции. Стандартную дозу можно вводить один или более раз в сутки в виде одной или более таблетки или капсулы, каждая из которых содержит от примерно 0,1 до примерно 100 мг, для удобства от примерно 0,25 до 50 мг композиции. В местном препарате композиция может присутствовать в концентрации от примерно 0,01 до 100 мг на грамм носителя. В предпочтительном воплощении композиция присутствует в концентрации примерно 0,07-1,0 мг/мл, более предпочтительно примерно 0,1-0,5 мг/мл, наиболее предпочтительно примерно 0,4 мг/мл. Кроме введения сокристаллов (-)-госсипола в виде сырого химического вещества, композиции по изобретению можно вводить как часть фармацевтического препарата, содержащего подходящие фармацевтически приемлемые носители, содержащие эксципиенты и вспомогательные вещества, способст- 22011218 вующие получению из композиций препаратов, которые являются фармацевтически применимыми. Предпочтительно препараты, в частности, те препараты, которые можно вводить перорально или местным путем и которые можно применять для предпочтительного типа введения, такие как таблетки, драже, пастилки и капсулы с медленным высвобождением, полоскания для рта и промывания для рта, гели,жидкие суспензии, ополаскиватели для волос, гели для волос, шампуни, а также препараты, которые можно вводить ректально, такие как суппозитории, а также подходящие растворы для введения путем инъекции, местным путем или перорально, содержат примерно от 0,01 до 99%, предпочтительно примерно от 0,25 до 75%, активного(-ых) соединения(-й) вместе с эксципиентом. Фармацевтические композиции по изобретению можно вводить любому животному, которое может испытывать лечебные эффекты соединений по изобретению. Большинство среди таких животных составляют млекопитающие, например люди, хотя изобретение не следует ограничивать ими. Другие животные включают ветеринарных животных (коров, овец, свиней, лошадей, собак, кошек и тому подобных). Композиции и их фармацевтические композиции можно вводить любыми способами, которые позволяют достичь поставленной цели. Например, введение может быть парентеральным, подкожным,внутривенным, внутримышечным, внутрибрюшинным, чрескожным, трансбуккальным, внутриоболочечным, внутричерепным, интраназальным или местным путем. Альтернативное или сопутствующее введение можно осуществлять пероральным путем. Вводимая дозировка будет зависеть от возраста, состояния здоровья и массы реципиента, вида сопутствующего лечения, если оно есть, частоты введения и природы ожидаемого эффекта. Фармацевтические препараты по изобретению производят способом, который сам по себе является известным, например, с помощью общепринятых процессов смешивания, грануляции, изготовления драже, растворения или лиофилизации. Таким образом, фармацевтические препараты для перорального применения могут быть получены путем объединения активных соединений с твердыми эксципиентами,возможно измельчения полученной в результате смеси и обработки смеси гранул после добавления подходящих вспомогательных веществ, если желательно или необходимо, с получением таблеток или сердцевин драже. Пригодными эксципиентами являются, в частности, наполнители, такие как сахариды, например,лактоза или сахароза, манит или сорбит, препараты целлюлозы и/или фосфаты кальция, например, трикальция фосфат или кальция гидрофосфат, а также связующие агенты, такие как крахмальная паста с использованием, например, кукурузного крахмала, пшеничного крахмала, рисового крахмала, картофельного крахмала, желатин, трагакант, метилцеллюлоза, гидроксипропилметил целлюлоза, натрийкарбоксиметилцеллюлоза и/или поливинилпирролидон. Если требуется, можно добавлять разрыхляющие агенты, такие как вышеупомянутые крахмалы, а также карбоксиметилкрахмал, сетчатый поливинилпирролидон, агар-агар, либо альгиновая кислота или ее соль, такая как альгинат натрия. Вспомогательными агентами являются среди прочего агенты, регулирующие сыпучесть, и смазывающие агенты, например,силика, тальк, стеариновая кислота или ее соли, такие как стеарат магния или стеарат кальция и/или полиэтиленгликоль. Сердцевины драже снабжают подходящими покрытиями, которые, если требуется,являются устойчивыми к желудочным сокам. Для данной цели можно использовать концентрированные растворы сахаридов, которые необязательно могут содержать гуммиарабик, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, полирующие растворы и подходящие органические растворители или смеси растворителей. С целью производства покрытий, устойчивых к желудочным сокам,используют растворы подходящих препаратов целлюлозы, такие как фталат ацетилцеллюлозы или фталат гидроксипропилметилцеллюлозы. Красящие вещества или пигменты можно добавлять в таблетки или покрытия драже, например, для идентификации или в целях характеристики комбинаций доз активных соединений. Другие фармацевтические препараты, которые можно применять перорально, включают заполняемые капсулы, изготовленные из желатина, а также мягкие запаиваемые капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. Заполняемые капсулы могут содержать активные соединения в форме гранул, которые могут быть смешаны с наполнителями, такими как лактоза,связующие агенты, такие как крахмалы, и/или смазывающие агенты, такие как тальк или стеарат магния,и, возможно, стабилизаторы. В мягких капсулах активные соединения предпочтительно растворяют или суспендируют в подходящих жидкостях, таких как жирные масла или вазелиновое масло. Кроме того,можно добавлять стабилизаторы. Возможные фармацевтические препараты, которые можно применять ректально, включают, например, суппозитории, которые состоят из комбинации одного или более активного соединения с основой суппозитория. Пригодными основами суппозитория являются, например, натуральные или синтетические триглицериды или насыщенные углеводороды. Кроме того, также возможно использовать желатиновые ректальные капсулы, которые состоят из комбинации активных соединений с основой. Возможные материалы основы включают, например, жидкие триглицериды, полиэтиленгликоли или насыщенные углеводороды. Пригодные препараты для парентерального введения включают водные растворы активных соеди- 23011218 нений в растворимой в воде форме, например, растворимых в воде солей и щелочных растворов. Кроме того, можно вводить суспензии активных соединений в виде соответствующих масляных инъекционных суспензий. Подходящие липофильные растворители или среды включают жирные масла, например, кунжутное масло, или синтетические эфиры жирных кислот, например, этилолеат или триглицериды, либо полиэтиленгликоль-400. Водные инъекционные суспензии могут содержать вещества, которые повышают вязкость суспензии, включая, например, натрийкарбоксиметилцеллюлозу, сорбит и/или декстран. Суспензия необязательно может содержать стабилизаторы. Композиции по изобретению для местного применения готовят предпочтительно в виде масел, кремов, лосьонов, мазей и тому подобного путем выбора подходящих носителей. Подходящие носители включают растительные или минеральные масла, белый вазелин (белый мягкий парафин), жиры или масла с разветвленной цепью, животные жиры и высокомолекулярный спирт (выше, чем С 12). Предпочтительными носителями являются те, в которых активный ингредиент является растворимым. Можно также включать эмульгаторы, стабилизаторы, увлажнители и антиоксиданты, а также агенты, придающие цвет или запах, если желательно. Кроме того, в этих препаратах для местного применения можно использовать усилители проникновения через кожу. Примеры таких носителей можно найти в патентах США 3989816 и 4444762. Кремы предпочтительно готовят из смеси минерального масла, самоэмульгирующего пчелиного воска и воду, в которой замешивают активный ингредиент, растворенный в небольшом количестве масла, такого как миндальное масло. Типичным примером такого крема является крем, который включает примерно 40 частей воды, примерно 20 частей пчелиного воска, примерно 40 частей минерального масла и примерно 1 часть миндального масла. Мази можно готовить путем смешивания суспензии активного ингредиента в растительном масле,таком как миндальное масло, с теплым мягким парафином, и охлаждения смеси. Типичным примером такой мази является мазь, которая включает примерно 30 мас.% миндального масла и примерно 70 мас.% белого мягкого парафина. Лосьоны можно, как обычно, готовить путем получения суспензии активного ингредиента в подходящем высокомолекулярном спирте, таком как пропиленгликоль или полиэтиленгликоль. Приведенные ниже примеры способа и композиций по изобретению являются иллюстративными,но не ограничивающими. Другие подходящие модификации и адаптации ряда условий и параметров,обычно учитываемых в клинической терапии, и которые очевидны специалистам в данной области техники, находятся в пределах сущности и объема изобретения. Пример 1. Получение сокристалла (-)-госсипола и уксусной кислоты Все химические вещества и реагенты покупали у Олдрич Кемикал Ко. или Ланкастер Синтезиз Инк. и использовали без дополнительной очистки. (-)-Госсипол (1 г) растворяли в ацетоне (6 мл) и фильтровали. Уксусную кислоту добавляли в постоянно перемешиваемый фильтрат до тех пор, пока раствор не становился мутным. Смесь оставляли при комнатной температуре на 2 ч, а затем при 4C на 2 ч. Сокристаллы собирали фильтрованием, используя воронку Бюхнера, при пониженном давлении и промывали небольшим количеством гексана. Чистый (-)-госсипол с уксусной кислотой сначала высушивали в защищенном от света контейнере и дополнительно высушивали в вакуумной сушилке при 40C в течение 24 ч. Пример 2. Характеристика сокристалла (-)-госсипола и уксусной кислоты Сокристаллы (-)-госсипола и уксусной кислоты были желтыми или бледно-желтыми и имели игольчатую форму. Эти сокристаллы были легко растворимы в ацетоне и эфире, слабо растворимы в хлороформе и этаноле и очень плохо растворимы в керосине. Сокристаллы были нерастворимы в воде. Нескорректированная точка плавления сокристаллов была определена как 178-180C с использованием аппарата Mel-Temp. Спектры 1 Н и 13 С ядерного магнитного резонанса (ЯМР) сокристаллов (фиг. 1 и 2) записывали на приборе Bruker 300. Образцы растворяли в соответствующем дейтеризованном растворителе (CDCl3). Химические сдвиги протона приведены в виде миллионных долейотносительно тетраметилсилана(0,00 млн-1), который использовали в качестве внутреннего стандарта. Химические сдвиги для спектров 13 С ЯМР приведены в видеотносительно дейтеризованного хлороформа (CDCl3, 77,0 млн-1). 1 Н ЯМР (300 МГц, CDCl3)15,21 (s, 2H), 11,16 (s, 2H), 7,80 (s, 2H), 6,45 (s, 2H), 5,79 (s, 2H), 4,083,80 (m, 2 Н), 2,18 (s, 6 Н), 2,11 (s, 3 Н), 1,58 (d, J=6,8 Гц, 12 Н). I3C ЯМР (75 МГц, CDCl3)199,4, 176, 156,0,150,5, 143,4, 134,1, 133,7, 129,7, 118,1, 115,9, 114,6, 111,8, 27,9, 20,7, 20,3, 20,2. На основании спектра 1 Н ЯМР определили, что сокристалл представляет собой комплекс (-)госсипола с уксусной кислотой в молярном отношении 1:1. Инфракрасный спектр (фиг. 3) сокристаллов записывали на спектрометре Perkin-Elmer FT-IR. Инфракрасный спектр (KBr) 3421, 2959, 2929, 1710, 1611, 1577, 1440, 1379, 1339, 1269, 1176, 1052, 841, 772 см-1. Масс-спектр электрораспыления (фиг. 4) сокристаллов измеряли на масс-спектрометре с магнитным сектором Micromass AutoSpec Ultima. Масс-спектр m/z (масса/заряд) 541 (M+Na)+.- 24011218 Спектр порошковой дифракции рентгеновских лучей (фиг. 5) сокристаллов записывали на порошковом дифрактометре Scintag. На основании спектра определили, что сокристалл представляет собой комплекс (-)-госсипола с уксусной кислотой в молярном отношении 1:1. Теперь, имея полностью описанное изобретение, специалистам в данной области техники будет понятно, что аналогичное можно осуществить в пределах широкого и эквивалентного ряда условий, препаратов и других параметров без влияния на объем изобретения или любого его воплощения. Все патенты,патентные заявки и публикации, цитируемые здесь, полностью включены здесь путем ссылки в полном объеме. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Композиция, состоящая, по существу, из сокристаллов (-)-госсипола с уксусной кислотой, где (-)госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1. 2. Композиция по п.1, где указанное молярное соотношение составляет 1:1. 3. Композиция по п.1, которая характеризуется интеграцией спектра 1 Н ЯМР при 2,11 (s, 3H), который представляет собой один сигнал метила уксусной кислоты, и 2,18 (s, 6H), который представляет собой два сигнала метила госсипола. 4. Способ получения композиции, состоящей, по существу, из сокристаллов (-)-госсипола с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1,при котором растворяют (-)-госсипол в ацетоне до образования раствора, фильтруют этот раствор, добавляют уксусную кислоту в этот раствор при перемешивании до тех пор, пока раствор не становится мутным, оставляют этот мутный раствор при комнатной температуре, затем при пониженной температуре от 0 до 15 С до образования сокристаллов, собирают эти сокристаллы, промывают их растворителем и высушивают. 5. Способ по п.4, где указанная пониженная температура составляет 4 С. 6. Фармацевтическая композиция, содержащая сокристаллы (-)-госсипола с уксусной кислотой и фармацевтически приемлемый носитель, где указанные сокристаллы (-)-госсипола с уксусной кислотой состоят, по существу, из сокристаллов (-)-госсипола с уксусной кислотой. 7. Фармацевтическая композиция, содержащая сокристаллы (-)-госсипола с уксусной кислотой и фармацевтически приемлемый носитель, где указанные сокристаллы (-)-госсипола с уксусной кислотой состоят, по существу, из (-)-госсипола и уксусной кислоты в молярном соотношении 1:1. 8. Способ изготовления фармацевтической композиции, при котором объединяют композицию, состоящую, по существу, из сокристаллов (-)-госсипола с уксусной кислотой, где (-)-госсипол и уксусная кислота присутствуют в молярном соотношении примерно 1:1, с фармацевтически приемлемым носителем. 9. Набор, содержащий сокристаллы по п.1 и инструкции по введению указанной композиции животному. 10. Набор по п.9, где указанная композиция находится в форме фармацевтической композиции, содержащей фармацевтически приемлемый носитель. 11. Набор по п.9, который дополнительно содержит химиотерапевтический агент. 12. Набор по п.9, где указанные инструкции представляют собой инструкции по введению указанной композиции животному, страдающему гиперпролиферативным заболеванием. 13. Набор по п.12, где указанное гиперпролиферативное заболевание представляет собой рак. 14. Набор по п.13, где указанный рак выбран из группы, состоящей из рака молочной железы, рака простаты, лимфомы, рака кожи, рака панкреатической железы, рака толстой кишки, меланомы, злокачественной меланомы, рака яичника, рака головного мозга, первичной карциномы головного мозга, рака в области головы и шеи, глиомы, глиобластомы, рака печени, рака мочевого пузыря, немелкоклеточного рака легкого, карциномы головы или шеи, карциномы молочной железы, карциномы яичника, карциномы легкого, мелкоклеточной карциномы легкого, опухоли Вильямса, цервикальной карциномы, карциномы яичка, карциномы мочевого пузыря, карциномы желудка, карциномы толстой кишки, карциномы простаты, карциномы мочеполовых органов, карциномы щитовидной железы, карциномы пищевода,миеломы, множественной миеломы, адренокарциномы, почечно-клеточного рака, карциномы эндометрия, карциномы коры надпочечников, злокачественной инсулиномы поджелудочной железы, злокачественной карциноидной опухоли, хориокарциномы, грибовидной гранулемы, злокачественной гиперкальцемии, цервикальной гиперплазии, лейкемии, острого лимфолейкоза, хронического лимфолейкоза, острого миелогенного лейкоза, хронического миелогенного лейкоза, хронического гранулоцитарного лейкоза, острого грануоцитарного лейкоза, лейкоза ворсистых клеток, нейробластомы, рабдомиосаркомы, саркомы Капоши, истинной полицитемии, идиопатического тромбоцитоза, болезни Ходжкина, неходжкинской лимфомы, саркомы мягких тканей, остеогенной саркомы, первичной макроглобулинемии и ретинобластомы.
МПК / Метки
МПК: A61K 36/00, A61P 35/00, A61K 31/19
Метки: применение, госсипола, сокристаллы
Код ссылки
<a href="https://eas.patents.su/29-11218-sokristally-gossipola-i-ih-primenenie.html" rel="bookmark" title="База патентов Евразийского Союза">Сокристаллы госсипола и их применение</a>
Предыдущий патент: N-[(3s)пирролидин-3-ил]бензамидные производные в качестве ингибиторов обратного захвата моноаминов
Следующий патент: Способ и устройство для анализа флюидов в скважине с определением характеристик пластовых флюидов
Случайный патент: Способ кодирования координат перемещающегося на экране вычислительного устройства видеоизображения