Производные 5-циано-2-амино-1,3-тиазола в качестве антагонистов аденозинового а1 рецептора
Формула / Реферат
1. Соединение формулы (I)
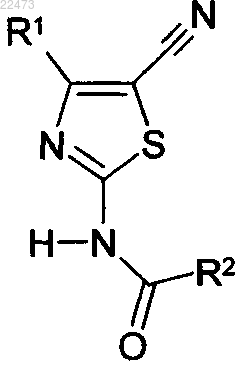
где R1 представляет собой C6-10 арил или C5-6 гетероарил, содержащий от 1 до 3 гетероатомов, выбранных из О и N, которые могут быть необязательно замещены одним или более заместителем, выбранным из группы, содержащей галоген, линейный или разветвленный C1-6 алкил, линейный или разветвленный галогенC1-6 алкил;
R2 представляет собой группу, выбранную из
a) линейного или разветвленного C1-6 алкила, необязательно замещенного одной или более карбоксильной группой (-СООН);
b) C3-8 циклоалкила, необязательно замещенного одной или более карбоксильной группой (-СООН),
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R1 представляет собой фенильную, пиридинильную или фурильную группу, необязательно замещенные одним или более заместителем, выбранным из группы, содержащей галоген, линейный или разветвленный C1-6 алкил и линейный или разветвленный галогенC1-6 алкил.
3. Соединение по п.1, где R2 представляет собой линейный или разветвленный C1-6 алкил, замещенный одной карбоксильной группой (-СООН).
4. Соединение по п.1, где R2 представляет собой C3-8 циклоалкил, замещенный одной карбоксильной группой (-СООН).
5. Соединение по п.1, которое является одним из следующих:
5-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексан-1,3-дикарбоновая кислота,
4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)-4-метилпентановая кислота,
4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)бутановая кислота,
(1R,3S)-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклопентанкарбоновая кислота,
3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклопентанкарбоновая кислота,
цис-2-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
транс-2-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
цис-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
транс-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
цис-4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
транс-4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)пентановая кислота,
(R)-4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)пентановая кислота,
(S)-4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)пентановая кислота,
3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)-3-метилбутановая кислота,
3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)бутановая кислота,
(R)-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)бутановая кислота,
(S)-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)бутановая кислота,
3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,
4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)бицикло[2.2.2]октан-1-карбоновая кислота,
4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)-3-метилбутановая кислота,
цис-3-[5-циано-4-(3-метилфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[4-(2-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[4-(2-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[4-(2-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
3-[4-(2-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]бутановая кислота,
цис-3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
транс-3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
цис-2-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-2-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(R)-4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(S)-4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]пентановая кислота,
3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(R)-3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(S)-3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]бутановая кислота,
3-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[4-(3-хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]бицикло[2.2.2]октан-1-карбоновая кислота,
4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
цис-3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
транс-3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
цис-2-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-2-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(R)-4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(S)-4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(R)-3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(S)-3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
3-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]бицикло[2.2.2]октан-1-карбоновая кислота,
4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
цис-3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
транс-3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
цис-2-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-2-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(R)-4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(S)-4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(R)-3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(S)-3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
3-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]бицикло[2.2.2]октан-1-карбоновая кислота,
4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
цис-3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
транс-3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклопентанкарбоновая кислота,
цис-2-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-2-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
транс-4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(R)-4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
(S)-4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]пентановая кислота,
3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]-3-метилбутановая кислота,
3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(R)-3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
(S)-3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]бутановая кислота,
3-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]бицикло[2.2.2]октан-1-карбоновая кислота,
4-[5-циано-4-(3,4-дифторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[5-циано-4-(3,4-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3,4-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[5-циано-4-(3,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
цис-3-[5-циано-4-(3-трифторметилфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(3-трифторметилфенил)-1,3-тиазол-2-илкарбамоил]циклогексан карбоновая кислота,
4-[5-циано-4-(3-трифторметилфенил)-1,3-тиазол-2-илкарбамоил]бицикло[2.2.2]октан-1-карбоновая кислота,
цис-3-[5-циано-4-(пиридин-4-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(пиридин-4-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(пиридин-4-ил)-1,3-тиазол-2-илкарбамоил]бицикло[2.2.2]октан-1-карбоновая кислота,
4-[5-циано-4-(пиридин-3-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[5-циано-4-(пиридин-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(пиридин-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(пиридин-2-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[5-циано-4-(пиридин-2-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(пиридин-2-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(фуран-2-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[5-циано-4-(фуран-2-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(фуран-2-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота,
цис-3-[5-циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,
4-[5-циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота.
6. Фармацевтическая композиция для применения в лечении патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, содержащая соединение по любому из пп.1-5 и фармацевтически приемлемый разбавитель или носитель.
7. Применение соединения формулы (1) по любому из пп.1-5 для приготовления лекарственного средства для лечения патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1.
8. Применение соединения формулы (1) по п.7, где патологическим состоянием или заболеванием является астма.
9. Способ лечения субъекта, страдающего патологическим состоянием или заболеванием, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, который включает введение указанному субъекту эффективного количества соединения по любому из пп.1-5.
10. Способ по п.9, где патологическим состоянием или заболеванием является астма.
11. Комбинация для применения в лечении патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, содержащая соединение по любому из пп.1-5 и соединение, выбранное из (а) ингибиторов ангиотензин-преобразовывающего энзима (АСЕ-ингибиторы), (b) антагонистов рецептора ангиотензина (ARB), (с) статинов, (d) β-блокаторов, (е) антагонистов кальция, (f) диуретиков, (g) антагонистов лейкотриенов, (h) кортикостероидов, (i) антагонистов альдостерона, (j) гистаминовых антагонистов, (k) антагонистов CRTh2, (l) ренин-ингибиторов, (m) антагонистов вазопрессина.
Текст
ПРОИЗВОДНЫЕ 5-ЦИАНО-2-АМИНО-1,3-ТИАЗОЛА В КАЧЕСТВЕ АНТАГОНИСТОВ АДЕНОЗИНОВОГО А 1 РЕЦЕПТОРА Настоящее изобретение относится к производным 5-циано-2-амино-1,3-тиазола формулы (I) Гонзалез Лио Лыхен, Цамачо Гомез Юан Алберто (ES) Теплова В.Е. (RU) которые являются антагонистами аденозинового А 1 рецептора, а также к фармацевтическим композициям, содержащим такие соединения, где R1 и R2 имеют значения, определенные в настоящем описании. Описываемые соединения также находят применение в качестве лекарственных средств, предназначенных для лечения патологических состояний или заболеваний,улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый A1 рецептор, например для лечения астмы. Область изобретения Настоящее изобретение относится к новым антагонистам аденозиновых рецепторов, в частности к антагонистам подтипа аденозинового рецептора A1, использованию указанных соединений в лечении заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновые рецепторы, в частности в лечении сердечно-сосудистых, ренальных (почечных) и респираторных заболеваний, интенсивность которых, как известно, может быть снижена при использовании антагонистов аденозиновых рецепторов A1, в частности таких нарушений, как застойная сердечная недостаточность, почечная недостаточность, гипертензионная интрадиалитическая гипотония, ишемия, суправентрикулярная аритмия, миокардиальная реперфузия, астма, COPD (хроническое обструктивное заболевание легких) и аллергические риниты, а также к композициям фармацевтических препаратов, включающих в себя названные соединения. Уровень техники Эффекты аденозина опосредованы по меньшей мере четырьмя специфическими рецепторами клеточной мембраны, которые в настоящее время идентифицированы и классифицированы как A1, A2A, A2B и A3 рецепторы, принадлежащие к группе рецепторов, связанных с G -белками. Рецепторы A1 и A3 понижают регуляцию клеточных уровней сАМР через их связывание с G-белками, которые ингибируют активность аденилатциклазы. Напротив, рецепторы A2A и A2B связываются с G-белками, что стимулирует активность аденилатциклазы и повышает внутриклеточные уровни сАМР. Через эти рецепторы аденозин регулирует широкий спектр физиологических функций. Так, в сердечно-сосудистой системе активация рецептора A1 защищает сердечную (кардиальную) ткань от последствий, возникающих при ишемии и гипоксии (Norton G.R. и др. Am. J. Physiol. 1999; 276(2 часть 2):Н 341-9; Auchampach J.A., Bolli R. Am. J. Physiol. 1999; 276(3 часть 2):H1113-6). Возможности антагонистов рецептора A1 в лечении застойной сердечной недостаточности задокументированы в литературе (Jacobson K., Gao Z., Nature Rev. Drag. Disc. 2006; 5, 247-264), а также подтверждены положительными клиническими результатами в фазе II клинических исследований соединений BG-9719 (Gottlieb S.S. и др., Circulation, 2002, 105, 1349-1353; Biogen idec, Website), BG-9928 (Greenberg B.H. и др., Circulation, 2003, 108, Abs 1602) и KW-3902 (Coletta А. и др., Eur. J. Heart Failure, 2006, 8,547-49; Novacardia, Website 2006). В почке аденозин производит бифазное действие, заключающееся в расширении сосудов при высоких концентрациях и сужении сосудов при низких концентрациях. Таким образом, аденозин играет определенную роль в патогенезе некоторых форм острой почечной недостаточности, при этом состояние может быть улучшено с помощью антагонистов рецептора A1 (Costello-Boerrigter L.C., и др Med ClinNorth Am. 2003 Mar; 87(2): 475-91; Gottlieb S.S., Drugs. 2001; 61(10): 1387-93). Недавно возможности антагонистов A1 в лечении интрадиалитической гипотонии были продемонстрированы в клинических испытаниях (Е. Imai; M. Fuji, и др. Kydney International, 2006, 69, 877-883). Более того, новый, сильнодействующий и избирательный антагонист FR194921 аденозинового рецептора A1 производит как когнитивноусиливающее, так и антифобическое седативное действие, предлагая терапевтические возможности таких соединений при деменции (слабоумии) и состояниях страха и тревожности (Maemoto T.; Tada M.,Pharmacol. Sci., 2004, 96, 42-52). Новейший отчет показал сильное проявление аденозинового рецептора A1, локализирующегося преимущественно в бронхиальном эпителии и гладкой бронхиальной мышце. Чувствительность астматиков к вдыхаемому аденозину в сочетании с усиленной экспрессией аденозинового рецептора A1, означает определенную роль этих рецепторов в патофизиологии астмы и других респираторных заболеваний(стр. С, Page С, Eur Respir J, 2007, 31(2):311-9). Некоторые производные 2-амино-1,3-тиазол известны как антагонисты аденозинового рецептора(Moro S., и др. Med. Res. Rev., 26, 131-159). В некоторых патентных заявках заявлены избирательные антагонисты рецепторов A2B и A3 (WO 9964418, WO 0242298, WO 05063743) и избирательный антагонист рецептора A2A (WO 06032273), основанные на производных 2-амино-1,3-тиазола. Один из докладов(Ijzerman Р., и др. J. Med. Chem. 2001, 44, 749-762) описывает избирательные антагонисты A1, основанные на этих структурах, но эффективность и избирательность, представленные в публикациях, были достаточно скромными, а результаты были получены от использования аденозиновых рецепторов крыс вместо человека. Краткое изложение сущности изобретения К удивлению было обнаружено, что эти новые производные от 5-циано-2-амино-1,3-тиазола являются эффективными и избирательными антагонистами аденозинового рецептора A1 и по этой причине могут быть использованы при лечении или для профилактики заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1. Далее было обнаружено, что введение цианогруппы в 5 положение тиазольного кольца играет существенную роль в активности заявленных в настоящем изобретении соединений в подавлении аденозинового рецептора A1, что может быть продемонстрировано на следующем примере. Дополнительными целями настоящего изобретения является создание способа изготовления указанных соединений; создание фармацевтических композиций, в состав которых входит эффективное количество указанных соединений; применение соединений в производстве лекарственных средств для лечения патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор, в частности аденозиновый рецептор A1; способы лечения патологических состояний и заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор, в частности аденозиновый рецептор A1, включающие в себя ведение нуждающемуся в лечении субъекту эффективного количества соединений по данному изобретению, а также комбинаций указанных соединений со следующими одним или более лекарственными препаратами: (а) ангиотензин, преобразовывающий энзим-ингибиторы (АСЕ-ингибиторы), (b) антагонисты рецептора ангиотензина (ARB), (с) статины, (d) -блокаторы, (е) антагонисты кальция, (f) диуретики, (g) антагонисты лейкотриена, (h) кортикостероиды, (i) антагонисты альдостерона, (j) гистаминовые антагонисты, (k) CRTh2 антагонисты, (l) ренин-ингибиторы, (m), антагонисты вазопрессина. Подробное описание изобретения Таким образом, настоящее изобретение направлено на 2-амино-5-циано-1,3-тиазол производные формулы (I) где R1 представляет собой C6-10 арил или C5-6 гетероарил, содержащий от 1 до 3 гетероатомов, выбранных из О и N, которые могут быть необязательно замещены одним или более заместителем, выбранным из группы, содержащей галоген, линейный или разветвленный C1-6 алкил, линейный или разветвленный галоген-C1-6 алкил;a) линейного или разветвленного C1-6 алкила, необязательно замещенного одной или более карбоксильной группой (-СООН),b) C3-8 циклоалкила, необязательно замещенного одной или более карбоксильной группой (-СООН). В соответствии с предпочтительным вариантом осуществления данного изобретения в соединениях формулы (I) R1 представляет собой фенильную, пиридинильную или фурильную группу, необязательно замещенные одним или более заместителем, выбранным из группы, содержащей галоген, линейный или разветвленный C1-6 алкил и линейный или разветвленный галоген-C1-6 алкил. При этом, R2 может представлять собой линейный или разветвленный C1-6 алкил, замещенный одной карбоксильной группой(-СООН) или C3-8 циклоалкил, замещенный одной карбоксильной группой (-СООН). Другими объектами настоящего изобретения являются: а) фармацевтические композиции, содержащие эффективное количество указанных соединений, смешанное с фармацевтически приемлемым разбавителем или носителем, b) применение указанных соединений для приготовления лекарственных средств для лечения болезней, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор, в частности аденозиновый рецептор A1, например астмы; с) способы лечения субъекта, страдающего патологическим состоянием или заболеванием, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, например астмы, которые включают в себя введение указанному субъекту эффективного количества соединения по данному изобретению; а также d) комбинации препаратов, включающих в себя указанные соединения и соедине-2 022473 ние, выбранное из (а) ингибиторов ангиотензинпреобразовывающего энзима (АСЕ - ингибиторы), (b) антагонистов рецептора ангиотензина (ARB), (с) статинов, (d) -блокаторов, (е) антагонистов кальция, (f) диуретиков, (g) антагонистов лейкотриенов, (h) кортикостероидов, (i) антагонистов альдостерона, (j) гистаминовых антагонистов, (k) антагонистов CRTh2, (l) ренин-ингибиторов, (m) антагонистов вазопрессина. Термин низший алкил в значении, используемом здесь, охватывает линейные или разветвленные радикалы необязательно замещенные, имеющие от 1 до 8, предпочтительно от 1 до 6 и еще более предпочтительно от 1 до 4 атомов углерода. Примеры включают в себя метил, этил, п-пропил, и-пропил, нбутил, втор-бутил и трет-бутил, н-пентил, 1-метилбутил, 2-метилбутил, изопентил, 1-этилпропил, 1,1 диметилпропил, 1,2-диметилпропил, п-гексил, 1-этилбутил, 2-этилбутил, 1,1-диметилбутил, 1,2 диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 2-метилпентил, 3-метилпентил и изогексил радикалы. Термин "низший алкокси" в значении, используемом здесь, охватывает необязательно замещенные линейные или разветвленные кислородсодержащие радикалы, каждый из которых имеет алкильные фрагменты (части) от 1 до 8, предпочтительно от 1 до 6 и еще более предпочтительно от 1 до 4 атомов углерода. Предпочтительные радикалы алкокси включают в себя метокси, этокси, н-пропокси ипропокси, н-бутокси, втор-бутокси, т-бутокси, трифторметокси, дифторметокси, гидроксиметокси, 2 гидроксиэтокси или 2-гидроксипропокси. Термин "арильная группа" в значении, используемом здесь, охватывает типично С 5-С 14 моноциклические или полициклические радикалы арила, такие как фенил или нафтил, антранил или фенантрил. Фенил является предпочтительным. Когда радикал арила несет 2 или более заместителя, заместители могут быть теми же или другими. Термин "гетероарильная группа" в значении, используемом здесь, охватывает типично 5-14 членную кольцевую структуру, включающую в себя по меньшей мере одно гетероароматическое кольцо и содержащую по меньшей мере один гетероатом, выбранный из О, S и N. Гетероарильный радикал может представлять собой единичное кольцо, или два, или более конденсированных (сочлененных) колец, в которых по меньшей мере одно кольцо содержит гетероатом. Примеры включают в себя пиридил, пиразинил, пиримидинил, пиридазинил, фурил, оксадиазолил, оксазолил, имидозалил, тиазолил, тиадиазолил,тиенил, пирролил, бензотиазолил, индолил, индазолил, пиринил, хинолил, изохинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, хинолизинил, циннолинил, триазолил, индолизинил, индолинил, изоиндолинил, изоиндолил, имидазолидинил, птеридинил и пиразолил радикалы. Предпочтительными радикалами являются тиенил и фурил, необязательно замещенные. Когда радикал гетероарила несет 2 или более заместителей, заместители могут быть теми же или другими. Термин "циклоалкил" в значении, используемом здесь, охватывает насыщенные, необязательно замещенные углеродно-кольцевые радикалы, и, если не указано иное, циклоалкильный радикал типично имеет от 3 до 7 атомов углерода. Примеры включают в себя циклопропил, циклобутил, циклопентил,циклогексил и циклогептил. Предпочтительными являются циклопропил, циклопентил или циклогексил. Когда циклоалкильный радикал несет 2 или более заместителей, заместители могут быть теми же или другими. В значении, используемом здесь, некоторые из атомов, радикалов, долей (компонентов), цепей или циклов, представленных в общих структурах данного изобретения, являются "необязательно замещенными". Это означает, что эти атомы, радикалы, доли, цепи или циклы могут быть либонезамещенными,либо замещенными в любой позиции одним или более заместителем, например 1, 2, 3 или 4 заместителем, в силу чего атомы водорода, привязанные к незамещаемым атомам, радикалам, долям, цепям или циклам заменяются химически приемлемыми атомами, радикалами, долями, цепями или циклами. Когда присутствуют два или более заместителей, каждый заместитель может быть тем же или другим. В значении, используемом здесь, термин "атом галогена" охватывает атомы хлора, фтора, брома или йода, типично - это атом фтора, хлора или брома, наиболее предпочтительно хлора и фтора. Термин"гало" в случае использования в качестве приставки имеет такое же значение. В значении, используемом здесь, термин "фармацевтически приемлемая соль" охватывает соли с фармацевтически приемлемыми кислотами или основаниями. Фармацевтически приемлемые кислоты включают в себя как неорганические кислоты, например хлористо-водородную, серную, фосфорную,дифосфорную, бромисто-водородную, йодисто-водородную и азотную кислоты, так и органические кислоты, например лимонную, фумаровую, малеиновую, яблочную, миндальную, аскорбиновую, щавелевую, янтарную, виннокаменную, бензойную, уксусную, метансульфоновую, этансульфоновую, бензосульфоновую или п-толуолсульфоновую кислоту. Фармацевтически приемлемые основания включают в себя щелочной металл (например, натрий или калий) и щелочно-земельный металл (например, кальций или магний), гидрооксидные и органические основания, например алкиламины, арилалкиламины, гетероциклические амины. Предпочтительными солями в соответствии с данным изобретением являются соли щелочных металлов, такие как соли натрия или калия. Специфические характерные соединения этого изобретения включают в себя Соединения настоящего изобретения могут быть приготовлены (составлены) при помощи одного из процессов, описанных ниже. Цианокетоны формулы (III), в которых R1 является арильной или гетероарильной группой с необязательным замещением, как было указано выше, могут быть получены при помощи реакции производного карбоновой кислоты формулы (II), где X - это хорошо замещаемая группа, как, например, галоген или О-алкил, с ацетонитриловой или цианоуксусной кислотой при наличии основания. Основанием, выбранным для этой реакции, может быть бутиллитий в апротик растворителе, таком как диэтилэфир или тетрагидрофуран (Turner J., и др. Synthesis. 1983, 308-9), или гидрид натрия, метоксид натрия или третбутоксид калия в растворителе, таком как толуол, диэтилэфир, тетрагидрофуран, диоксан, этанол или метанол, при температуре между 40 и 120C (Dorsch М., и др. J. Am. Chem. Soc. 1932, 54, 2960-63; TurnerJ., и др. J. Org. Chem 1989; 54, 4229-31). Цианокетоны формулы (III), в которых R1 является арильной или гетероарильной группой с необязательным замещением, как было указано выше, могут быть также получены с помощью реакции ароматических нитрилов формулы (VI) с ацетонитрилом при наличии сильного основания, такого как гидрид натрия, метоксид натрия, трет-бутоксид калия или лития вторично (триметилселил)амид, в растворителе,таком как тетрагидрофуран, диоксан или диэтилэфир (Polivka, Z., и др., Collect. Czech. Chem. Commun.,1984, 49, 621-36). В качестве альтернативы соединения формулы (III) могут быть получены при помощи двухступенчатой процедуры (схема 1), начиная с доступных для приобретения метилкетонов формулы (V), в которых R1 был выявлен ранее. На первой ступени соединения формулы (V) бромируются или иодинируются с использованием N-бромсукцинимида или N-йодсукцинимида, при стандартных условиях получения бром- или йодкетонов формулы (IV). Атом галогена этих галокетонов формулы (IV) может быть замещен цианогруппой с использованием цианоида натрия или калия, что дает желаемые цианокетоны формулы (III) (Reidlinger, С., и др., Monatsh. Chem., 1998, 129: 1207-12; Compton, V., и др., J. Chem. Soc. Perkin Trans. 1, 1992, 2029-32). С другой стороны, ацилирование соединений формулы (VII) уксусной кислотой или активированным производным при условиях Фридель-Крафтса (Friedel-Craft) создает альтернативный метод для синтезирования промежуточных цианокетонов формулы (III) (I.G. Farbenindustrie DE 544886). Производные 2-амино-5-циано-1,3-тиазол формулы (VIII), где R1 является арильной или гетероарильной группой, необязательно замещенной, как указано выше, могут быть получены при помощи реакции цианокетонов формулы (III) с йодом и тиомочевиной в растворителе, таком как пиридин или диметилформамид, при температуре между 80 и 120C (схема 2). Схема 2 Соединения формулы (VIII) могут быть ацилированы с использованием либо производного от хлорида карбоновой кислоты формулы (IX), или ангидрида карбоновой кислоты формулы (X), которые являются частными случаями соединений, заявленных настоящим изобретением. Схема 3 Фармакологическая активность Конкурентный анализ радиолигандного связывания подтипа аденозинового рецептора. Мембраны из рекомбинированных аденозиновых рецепторов человека были приобретены в корпорации Рецепторная биология, США (Receptor Biology, Inc.,USA). Конкурентные испытания были проведены путем культивирования (выращивания) мембран из рецепторов hA1, трансфектированных в СНО клетки, [3H]-DPCPX радиолиганд, буферный раствор (HEPES 20 мМ (pH 7,4), 10 мМ MgCl2, 100 мМ NaCl, 2 ед/мл аденозиндезаминазы), и в непомеченный лиганд, в общем объеме, равном 0,2 мл на 90 мин при 25C. Для определения неспецифической связи использовался R-PIA. Фильтрование проводилось через фильтры GF/52 Шлейшера-Шуэлла (SchleicherSchuell)(Brandel cell harvester). Несвязанные радиолиганды устраняются с помощью HEPES 30 мМ (3250 мкл),NaCl (100 мМ) и MgCl2 (10 мМ). Конкурентные испытания были проведены путем культивирования (выращивания) мембран из рецепторов hA2A трансфектированных в HEK293 клетки, [3 Н] ZM241385 в качестве радиолиганда, буферный раствор (50 мМ Tris-HCl (pH 7,4), 10 мМ MgCl2, 1 мМ ЕМА, 2 ед/мл аденозиндезаминазы), и непомеченный лиганд, в общем объеме, равном 0,2 мл на 90 мин при 25C. NECA использовался для определения неспецифической связи. Фильтрование осуществлялось через фильтры GF/52 Шлейшера-Шуэлла(SchleicherSchuell) (предварительно пропитанные 0,5% полиэтиленимином) в коллекторе клеток (харвестере) Брандела (Brandel cell harvester). Несвязанные (отделенные) радиолиганды были устранены с помощью 33 мл холодного как лед 50 мМ Tris-HCl (pH 7,4), 0,9% NaCl. Соединения настоящего изобретения не выявили никакого существенного подобия (родства) для аденозиновых рецепторов A3 и A2B. Ингибиторные константы (Ki) некоторых соединений, заявленных в данном изобретении для аденозиновых рецепторов A1 и A2A, показаны в табл. 1. Таблица 1 Как видно из табл. 1, соединения формулы (I) являются сильнодействующими ингибиторами подтипа аденозинового рецептора A1 и избирательно действующими против аденозинового рецептора A2A. Производные 2-амино-5-циано-1,3-тизол этого изобретения применимы для лечения или профилактики заболеваний, известных как болезни, которые поддаются лечению с помощью антагонистического воздействия на аденозиновый рецептор, в частности аденозиновый рецептор А 1. Такими заболеваниями являются, например, застойная сердечная недостаточность, гипертензия, ишемия, суправентрикулярная аритмия, острая почечная недостаточность, миокардиальная реперфузия, интрадиалитическая гипотония,деменция (слабоумие), состояния тревоги, а также респираторные заболевания, такие как астма и аллергические риниты. Соответственно, 2-амидо-5-циано-1,3-тиазол-производные данного изобретения, а также их фармацевтически приемлемые соли и фармацевтические композиции, включающие в себя такое соединение и/или их соли, могут применяться в способе лечения расстройств организма человека, что включает в себя назначение субъекту, нуждающемуся в таком лечении, эффективного количества 2-амидо-5-циано 1,3-тиазол-производного этого изобретения, либо его фармацевтически приемлемой соли. Данное изобретение предоставляет также фармацевтические композиции, включающие в себя в качестве активного ингредиента по меньшей мере 2-амино-5-циано-1,3-тиазол-производное формулы (I) или фармацевтически приемлемую соль этого вместе с фармацевтически приемлемым наполнителем,таким как носитель или разбавитель (растворитель). Активный ингредиент может составлять от 0,001 до 99 вес.%, предпочтительнее от 0,01 до 90 вес.% композиции, в зависимости от технологии приготовления лекарства, и от того, должен ли быть приготовлен используемый в дальнейшем разбавитель до применения. Предпочтительнее производить композиции в форме, удобной для орального, местного, назального,ректального, перкутанного или инъецируемого введения. Фармацевтически приемлемые наполнители, которые смешиваются с активным соединением или солями такого соединения, с тем, чтобы сформировать композицию согласно изобретения, общеизвестныper se (сами по себе), и фактические наполнители, используемые здесь, зависят, inter alia (между прочим),от намеченного метода введения композиций. Композиции этого изобретения адаптированы предпочтительно к инъецируемому или per os (пероральному) введению. В таком случае композиции для орального введения могут принимать форму таблеток, замедленных таблеток, подъязычных таблеток, капсул, аэрозолей для ингаляции, ингаляционных растворов, сухого порошка для ингаляций или жидких препаратов, таких как микстуры, эликсиры, сиропы или суспензии, при этом все они содержат соединение этого изобретения; такие препараты могут быть изготовлены методами, общеизвестными в этой области техники. Разбавители, которые могут быть использованы в изготовлении композиций, включают в себя жидкости и твердые разбавители, совместимые с активными ингредиентами, вместе с окрашивающими или ароматизирующими агентами, если таковые нужны. Таблетки или капсулы могут без труда содержать от 2 до 500 мг активного ингредиента или эквивалентное количество его солей. Жидкая композиция, адаптированная для орального применения, может иметь форму растворов или суспензий. Растворы могут представлять собой водные растворы, или растворимую соль, или другое производное активного соединения, например с сахарозой для приготовления сиропа. Суспензии могут включать в себя нерастворимые активные соединения этого изобретения или его фармакологически приемлемую соль в соединении с водой вместе с суспендирующим агентом или ароматизатором. Композиции для парентеральных инъекций могут быть приготовлены из растворимых солей, которые могут быть или не быть лиофилизированными и растворены в водной среде, свободной от пирогенов, или в другой жидкости, пригодной для парентеральных инъекций. Эффективные дозы обычно находятся в диапазоне 2-2000 мг активного ингредиента в день. Дневная доза может назначаться в количестве от одного или более приемов, предпочтительнее от 1 до 4 приемов в день. Настоящее изобретение далее иллюстрируется нижеследующими примерами. Примеры даны в качестве иллюстрации и никоим образом не ограничивают объем изобретения. Синтезирование композиций этого изобретения иллюстрируется следующими примерами (от 1 до 136), включая приготовление промежуточных продуктов, что никоим образом не ограничивает объем данного изобретения. Общая информация. Реагенты, исходный материал и растворители были приобретены у коммерческих поставщиков и использованы в полученном виде. Концентрация относится к испарению в условиях вакуума с использованием вращающегося выпаривателя Боша (Bchi). Продукты реакции при необходимости очищались при помощи кратковременной хроматографии на силикагеле (40-63 мкм) с индикацией системы растворителя. Спектроскопические данные регистрировались на спектрометре Varian Gemini 200, Varian Gemini 300, Varian Inova 400 и на спектрометре Brucker DPX-250. Точки плавления регистрировались на аппарате Bchi 535. HPLC-MS выполнялись на приборе Gilson, оборудованном поршневым насосом 321, Gilson, вакуумным дегаззером Gilson 864, манипулятором для жидкостей Gilson 215, впрыскивающим модулем Gilson 189, расщепителем (делителем) Gilson Valvemate 7000, а 1/1000, подпиточным насосом Gilson 307, диодным матричным детектором Gilson 170 и детектором Thermoquest FinniganaQa. Подготовительная полуочистка выполнялась с использованием симметричной колонки SymmetryC18 с вывернутой фазой (100, 5 мкм, 19100 мм, куплено у фирмы WATERS), формиата (formiate) вода/аммоний (0,1%, рН 3) и формиата ацетоннитрил/аммоний (0,1%, рН 3) в качестве подвижной фазы в газожидкостной хроматографии. Промежуточная форма 1. 2-Амино-4-фенил-1,3-тиазол-5-карбонитрил 5 г (34,0 ммоль) 3-оксо-3-(3-фторфенил)пропаннитрила было растворено в пиридине (30 мл) и последовательно добавлены тиомочевина (5 г, 68,0 ммоль) и йод (8,70 г, 34,40 ммоль). Раствор перемешивался (взбалтывался) при 100C в течение 12 ч. Затем смесь была охлаждена до комнатной температуры и вылита в ледяную воду (500 мл). Получившиеся в результате твердые частицы были отфильтрованы,промыты водой и рекристаллизированы из этанола, чтобы дать 70 г (91%) желтых твердых частиц NMR(300 МГц, DMSO-d6):= 7.52 (m, 3H), 7.93 (d, 2H), 8.26 (s, 2H). Следующие промежуточные формы были синтезированы с использованием процедуры, описанной для промежуточной формы 1, начиная с соответствующих кетонитрилов. Промежуточная форма 2. 2-Амино-4-(3-метилфенил)-1,3-тиазол-5-карбонитрил.NMR (300 МГц, DMSO-d6):= 2.57 (s, 3H), 6.88 (d, 1H), 7.65 (d, 1H), 8.17 (s, 2H). Синтез хлоридов карбоновой кислоты. Хлориды карбоновой кислоты, отсутствующие в продаже, были синтезированы из соответствующих карболовых кислот с использованием стандартных процедур (Burdett, K.A., Sfntesis, 1991, 441-42),как поясняется примером ниже. 1.3.5-Трихлорид циклогексанкарбоновой кислоты. 0,5 г (2,3 ммоль) 1,3,5-циклогексанкарбоновой кислоты было растворено в 1,2-дихлорэтане (5 мл). К этому раствору затем был добавлен бензилхлоридтриэтил аммония (0,001 г, 3 мкмоль) и тионилхлорид(0,562 мл, 7,7 ммоль). Суспензия перемешивалась (взбалтывалась) при 90C в течение 16 ч. Раствор был концентрирован и остаток использован в реакции ацилирования без последующей очистки. Синтез ангидридов карбоновой кислоты. 3-Окса-бицикло[3.3.1]нонан-2,4-дион (цис-1,3-циклогександикарбон ангидрид): 10 г (58,2 ммоль) 1,3-циклогександикарбоновой кислоты было суспензировано (взвешено) в уксусном ангидриде (40 мл) и нагревалось в течение 5 ч. Затем раствор был охлажден до комнатной температуры и растворители удалены в вакууме (in vacuo). Остатки были затем растворены в смеси гептана (20 мл) и толуена (20 мл) и раствор охлажден до 4C. Осадочное твердое вещество (твердые частицы) было затем собрано путем фильтрации и промыто пентаном, чтобы получить 5,9 г указанных соединений в виде белых иголочек. Примеры Производные от промежуточной формы 1. Пример 1. 5-(5-Циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексан-1,3-дикарбоновая кислота Промежуточная форма 1 (200 мг, 1,0 ммоль) была растворена в дихлорметане (10 мл) и триэтиламине (1 мл) и добавлением циклогексан 1,3,5-трикарбонилхлорида (0,2 мл, 1,5 ммоль). Раствор взбалтывался при комнатной температуре в течение 12 ч. Затем растворители были выпарены. Остатки были растворены в метаноле, добавлен раствор 4 М гидроксида натрия (1 мл), и смесь взбалтывалась при 60C в течение 12 ч. Раствор был вылит в ледяную воду (50 мл). Получившийся в результате раствор был промыт дихлорметаном (215 мл). Состояние воды было доведено до рН 3 с использованием 1 М холодного раствора соляной кислоты. Осадочное твердое вещество (твердые частицы) было затем собрано путем фильтрации, промыто холодной водой и высушено, чтобы получить 290 мг (68%) требуемого соединения в виде бледно-желтых твердых частиц.NMR (300 МГц, DMSO-d6):= 1.12 (m, 2 Н), 1.31 (m, 1 Н), 2.13 (m, 2H), 2.41 (m, 1H), 2.91 (m, 2H),3.16 (m, 1H), 7.56 (m, 3H), 8.02 (m, 2H), 12.01 (s, 2H), 13.06 (s, 1H). Следующие примеры были синтезированы с использованием процедуры, описанной для примера 1,где задействована соответствующая промежуточная форма, а также хлорид или ангидрид карбоновой кислоты в качестве исходного материала. Пример 2. 4-(5-Циано-4-фенил-1,3-тиазол-2-илкарбамоил)-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.78 (m, 1H), 1.88 (m, 2H), 1.97 (m, 2H), 2.24 (m, 1H), 2.80 (m, 1H),3.08 (m, 1H), 7.56 (m, 3H), 8.01 (m, 2H), 12.20 (s, 1H), 13.12 (s, 1H). Пример 6. цис-2-(5-Циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.38 (m, 3H), 1.63 (m, 1 Н), 1.76 (m, 2H), 1.92 (m, 1H), 2.07 (m, 1H),2.80 (m, 1H), 3.12 (m, 1H), 7.56 (m, 3H), 8.01 (m, 2H), 12.25 (s, 1H), 13.02 (s, 1H). Пример 8. цис-3-(5-Циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 0.96 (d, 3H), 2.17 (m, 1H), 2.24 (m, 1H), 2.32 (m, 1H), 2.37 (m, 1H),2.43 (m, 1H), 7.56 (m, 3H), 8.01 (m, 2H), 12.17 (s, 1H), 13.11 (s, 1H). Производные промежуточной формы 2 (R1 = 3-метилфенил). Пример 24. цис-3-[5-Циано-4-(3-метилфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.32 (m, 3H), 1.51 (m, 1 Н), 1.90 (m, 3H), 2.09 (m, 1H), 2.29 (m, 1H),2.39 (s, 3H), 2.63 (m, 1H), 7.38 (m, 1H), 7.48 (t, 1H), 7.85 (m, 2H), 12.2 (s, 1H), 13.1 (s, 1H). Производные промежуточной формы 3 (R1 = 2-хлорофенил). Пример 25. 4-[4-(2-Хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.(s, 1H). Пример 26. цис-3-[4-(2-Хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.79 (m, 2H), 2.08 (m, 4H), 2.87 (m, 1H), 3.14 (m, 1H), 7.63 (d, 2H),7.% (m, 1H), 7.99 (s, 1H), 12.20 (s, 1H), 13.09 (s, 1H). Пример 31. цис-2-[4-(3-Хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.39 (m, 3H), 1.65 (m, 1H), 1.77 (m, 2H), 1.94 (m, 1H), 2.10 (m, 1H),2.80 (m, 1H), 3.13 (m, 1H), 7.63 (d, 2H), 7.97 (m, 1H), 8.00 (s, 1H), 12.29 (s, 1H), 13.06 (s,1H). Пример 33. цис-3-[4-(3-Хлорфенил)-5-циано-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.47 (m, 6H), 1.81 (m, 6H), 7.63 (m, 2H), 7.97 (m, 2H), 12.16 (s, 1H),13.10 (s, 1H). Производные промежуточной формы 5 (R' = 2-фторфенил). Пример 47. 4-[5-Циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.37 (m, 3H), 1.63 (m, 1H), 1.77 (m, 2H), 1.92 (m, 1H), 2.09 (m, 1H),2.80 (m, 1H), 3.12 (m, 1H), 7.39 (dd, 1H), 7.45 (d, 1H), 7.61 (m, 1H), 7.72 (m, 1H), 12.22 (s, 1H), 13.04(s, 1H). Пример 54. цис-3-[5-Циано-4-(2-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилируюшего агента.NMR (300 МГц, DMSO-d6):= 1.46 (m, 6H), 1.84 (m, 6H), 7.39 (dd, 1H), 7.45 (d, 1H), 7.61 (m, 1H),7.72 (m, 1H), 12.05 (s, 1H), 13.08 (s, 1H). Производные промежуточной формы 6 (R1 = 3-фторфенил). Пример 68. 4-[5-Циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.79 (m, 2 Н), 2.08 (m, 4 Н), 2.88 (m, 1 Н), 3.14 (m, 1H), 7.40 (m, 1H),7.64 (q, 1H), 7.76 (m, 1H), 7.87 (m, 1H), 12.20 (s, 1H), 13.09 (s, 1H). Пример 73. цис-2-[5-циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилируюшего агента.NMR (300 МГц, DMSO-d6):= 1.39 (m, 3H), 1.66 (m, 1H), 1.77 (m, 2H), 1.92 (m, 1H), 2.10 (m, 1H),2.81 (m, 1H), 3.13 (m, 1H), 7.39 (m, 1H), 7.63 (q, 1H), 7.76 (m, 1H), 7.87 (m, 1H), 12.27 (s, 1H), 13.05 (s, 1H). Пример 75. цис-3-[5-Циано-4-(3-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.50 (m, 6H), 1.84 (m, 6H), 7.42 (m, 1H), 7.65 (q, 1H), 7.74 (dd, 1H),7.86 (d, 1H), 12.08 (s, 1H), 13.11 (s, 1H). Производные промежуточной формы 7 (R1 = 4-фторфенил). Пример 89. 4-[5-Циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.78 (m, 2H), 2.08 (m, 4H), 2.89 (m, 1H), 3.15 (m, 1H), 7.39 (t, 2H),8.03 (m, 2H), 12.21 (s, 1H), 13.10 (s, 1H). Пример 94. цис-2-[5-Циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.38 (m, 3H), 1.65 (m, 1H), 1.76 (m, 2H), 1.92 (m, 1H), 2.10 (m, 1H),2.80 (m, 1H), 3.13 (m, 1H), 7.39 (t, 2H), 8.03 (m, 2H), 12.27 (s, 1H), 13.05 (s, 1H). Пример 96. цис-3-[5-Циано-4-(4-фторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.50 (m, 6H), 1.83 (m, 6H), 7.40 (t, 2H), 8.06 (m, 2H), 12.07 (s, 1H),13.10 (s, 1H). Производные промежуточной формы 8 (R1 = 3,4-дифторфенил). Пример 110. 4-[5-Циано-4-(3,4-дифторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.(m, 1H), 12.16 (s, 1H), 12.90 (s, 1H). Пример 111. цис-3-[5-Циано-4-(3,4-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.(m, 1H), 7.96 (m, 1H), 12.16 (s, 1H), 13.11 (s, 1H). Производные промежуточной формы 9 (R1 = 3,5-дифторфенил). Пример 113. 4-[5-Циано-4-(3,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.26 (s, 6H), 1.94 (m, 2H), 2.15 (m, 2H), 7.50 (m, 1H), 7.64 (dd, 2H),12.16 (s, 1H), 12.89 (s, 1H). Пример 114. цис-3-[5-Циано-4-(3,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.(dd, 2H), 12.16 (s, 1H), 13.11 (s, 1H). Производные промежуточной формы 10 (R1 = 2,5-дифторфенил). Пример 116. 4-[5-Циано-4-(2,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.26 (s, 6H), 1.94 (m, 2H), 2.15 (m, 2H), 7.53 (m, 3H), 12.15 (s, 1 Н),12.88 (s, 1H). Пример 117. цис-3-[5- Циано-4-(2,5-дифторфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.50 (m, 4H), 1.96 (t, 4H), 2.23 (t, 1H), 2.56 (m, 1H), 7.53 (m, 3H),12.15 (s,1H), 13.10 (s,1H). Производные промежуточной формы 11 (R' = 3-(трифторметил)фенил). Пример 119. цис-3-[5-Циано-4-(3-трифторметилфенил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.(d, 1H), 12.08 (s, 1H), 13.12 (s, 1H). Производные промежуточной формы 12 (R' = пиридин-4-ил). Пример 122. цис-3-[5-Циано-4-(пиридин-4-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.46 (m, 6H), 1.85 (m, 6H), 7.46 (d, 2H), 8.60 (d, 2H), 12.08 (s, 1H),13.10 (s, 1H). Производные промежуточной формы 13 (R1 = пиридин-3-ил). Пример 125. 4-[5-Циано-4-(пиридин-3-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.(d, 1H), 9.16 (s, 1H), 12.16 (s, 1H), 12.85 (s, 1H). Пример 126. цис-3-[5-Циано-4-(пиридин-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.(d, 1H), 8.73 (d, 1H), 9.16 (s, 1H), 12.16 (s, 1H), 13.10 (s, 1H). Производные промежуточной формы 14 (R' = пиридин-2-ил). Пример 128. 4-[5-Циано-4-(пиридин-2-ил)-1,3-тиазол-2-илкарбамоил)-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.25 (s, 6H), 1.94 (m, 2H), 2.12 (m, 2H), 7.52 (m, 1H), 8.03 (m, 2H),8.74 (m, 1H), 12.13 (s, 1H), 12.84 (s, 1H). Пример 129. цис-3-[5-Циано-4-(пиридин-2-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.(m, 2H), 8.74 (m, 1H), 12.15 (s, 1H), 13.09 (s, 1H). Производные промежуточной формы 15 (R1 = фуран-2-ил). Пример 131. 4-[5-Циано-4-(фуран-2-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.NMR (300 МГц, DMSO-d6):= 1.22 (s, 6H), 1.92 (m, 2H), 2.10 (m, 2H), 6.76 (q, 1H), 7.08 (dd, 1H),7.99 (dd, 1H), 12.14 (s, 1H), 12.85 (s, 1H). Пример 132. цис-3-[5-Циано-4-(фуран-2-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента.NMR (300 МГц, DMSO-d6):= 1.47 (m, 4H), 1.97 (m, 4H), 2.24 (m, 1H), 2.58 (m, 1H), 6.76 (q, 1H),7.08 (dd, 1H), 7.99 (dd, 1H), 12.15 (s, 1H), 13.10 (s, 1H). Производные промежуточной формы 16 (R1 = 4-(метил)фуран-3-ил). Пример 134. 4-[5-Циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]-4-метилпентановая кислота.(s, 1H), 12.16 (s, 1H), 12.88 (s, 1H). Пример 135. цис-3-[5-Циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. Соединение было синтезировано с использованием ангидрида в качестве ацилирующего агента. где R1 представляет собой C6-10 арил или C5-6 гетероарил, содержащий от 1 до 3 гетероатомов, выбранных из О и N, которые могут быть необязательно замещены одним или более заместителем, выбранным из группы, содержащей галоген, линейный или разветвленный C1-6 алкил, линейный или разветвленный галогенС 1-6 алкил;a) линейного или разветвленного C1-6 алкила, необязательно замещенного одной или более карбоксильной группой (-СООН);b) C3-8 циклоалкила, необязательно замещенного одной или более карбоксильной группой (-СООН),или его фармацевтически приемлемая соль. 2. Соединение по п.1, где R1 представляет собой фенильную, пиридинильную или фурильную группу, необязательно замещенные одним или более заместителем, выбранным из группы, содержащей галоген, линейный или разветвленный C1-6 алкил и линейный или разветвленный галогенС 1-6 алкил. 3. Соединение по п.1, где R2 представляет собой линейный или разветвленный C1-6 алкил, замещенный одной карбоксильной группой (-СООН). 4. Соединение по п.1, где R2 представляет собой C3-8 циклоалкил, замещенный одной карбоксильной группой (-СООН). 5. Соединение по п.1, которое является одним из следующих: 5-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексан-1,3-дикарбоновая кислота,4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)-4-метилпентановая кислота,4-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)бутановая кислота,(1R,3S)-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклопентанкарбоновая кислота,3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклопентанкарбоновая кислота,цис-2-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,транс-2-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,цис-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,транс-3-(5-циано-4-фенил-1,3-тиазол-2-илкарбамоил)циклогексанкарбоновая кислота,- 21022473 цис-3-[5-циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота,4-[5-циано-4-(4-метилфуран-3-ил)-1,3-тиазол-2-илкарбамоил]циклогексанкарбоновая кислота. 6. Фармацевтическая композиция для применения в лечении патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, содержащая соединение по любому из пп.1-5 и фармацевтически приемлемый разбавитель или носитель. 7. Применение соединения формулы (1) по любому из пп.1-5 для приготовления лекарственного средства для лечения патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1. 8. Применение соединения формулы (1) по п.7, где патологическим состоянием или заболеванием является астма. 9. Способ лечения субъекта, страдающего патологическим состоянием или заболеванием, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, который включает введение указанному субъекту эффективного количества соединения по любому из пп.1-5. 10. Способ по п.9, где патологическим состоянием или заболеванием является астма. 11. Комбинация для применения в лечении патологических состояний или заболеваний, улучшаемых или облегчаемых с помощью антагонистического воздействия на аденозиновый рецептор A1, содержащая соединение по любому из пп.1-5 и соединение, выбранное из (а) ингибиторов ангиотензинпреобразовывающего энзима (АСЕ-ингибиторы), (b) антагонистов рецептора ангиотензина (ARB), (с) статинов, (d) -блокаторов, (е) антагонистов кальция, (f) диуретиков, (g) антагонистов лейкотриенов, (h) кортикостероидов, (i) антагонистов альдостерона, (j) гистаминовых антагонистов, (k) антагонистов
МПК / Метки
МПК: A61K 31/426, C07D 277/56, A61P 9/00, C07D 417/04
Метки: производные, рецептора, качестве, аденозинового, 5-циано-2-амино-1,3-тиазола, антагонистов
Код ссылки
<a href="https://eas.patents.su/25-22473-proizvodnye-5-ciano-2-amino-13-tiazola-v-kachestve-antagonistov-adenozinovogo-a1-receptora.html" rel="bookmark" title="База патентов Евразийского Союза">Производные 5-циано-2-амино-1,3-тиазола в качестве антагонистов аденозинового а1 рецептора</a>
Предыдущий патент: Соединения, активирующие теломеразу, и способы их применения
Следующий патент: Полупроводниковая полимерная композиция
Случайный патент: Система для бесконтактного распознавания линий руки и пальцев












