Оксимные о-эфирные соединения и фунгициды для применения в земледелии и садоводстве
Номер патента: 4574
Опубликовано: 24.06.2004
Авторы: Хамамура Хироси, Накагава Юуки, Сано Хироси, Сугиура Тадаси, Андо Такахиро, Митани Акира
Формула / Реферат
1. Оксимные O-эфирные соединения, представляемые общей формулой [I]
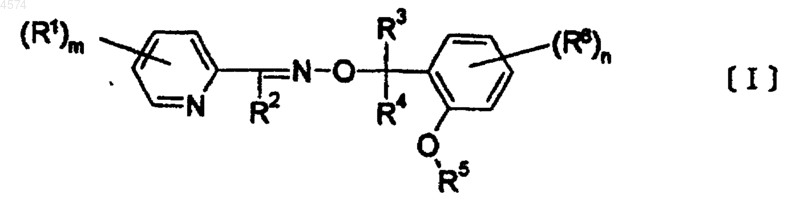
где R1 представляет C1-6алкил, C3-6циклоалкил, C1-6алкокси, C1-6алкилтио, амино, моно- или ди-(C1-6алкил)амино, C1-6ацилокси, C1-6алкокси-C1-6алкил, C1-6галогеналкил, гидрокси или атом галогена;
m представляет целое число от 1 до 4, и когда m равно 2 или более, каждый из R1 может быть одинаковым или разным;
R2 представляет атом водорода, C1-6алкил или C3-6циклоалкил;
R3 и R4 являются одинаковыми или разными, и каждый независимо представляет атом водорода или C1-6алкил;
R5 представляет атом водорода, C1-6алкил, C3-6циклоалкил, C1-6галогеналкил, C1-6алкокси-C1-6алкил, C1-6алкокси-C1-6алкокси-C1-6алкил, C7-10аралкил, C7-10аралкилоксиC1-6алкил, C1-6алкилкарбонил, C1-6алкилсульфонил или C1-6 галогеналкилсульфонил;
R6 представляет C1-6алкил, C3-6циклоалкил, C2-6алкенил, C2-6алкинил, C1-6алкокси, C1-6алкокси-C1-6алкокси, C1-6алкилкарбонилокси, C1-6алкокси-C1-6алкил, C1-6галогеналкил, циано, нитро, амино, моно- или ди-(C1-6алкил)амино, C1-6алкилкарбониламино, C1-6алкилтио, гидрокси или атом галогена и
n представляет целое число от 1 до 4, и когда n равно 2 или более, каждый из R6 может быть одинаковым или разным.
2. Оксимные эфирные соединения по п.1, представляемые общей формулой [I']
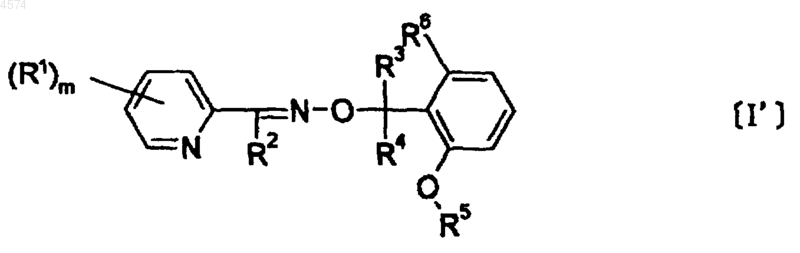
где R1, R2, R3, R4, R5, R6, m имеют значения, указанные выше.
3. Фунгицид для применения в земледелии и садоводстве, отличающийся тем, что содержит одно или более из оксимных эфирных соединений, представляемых общей формулой [I]
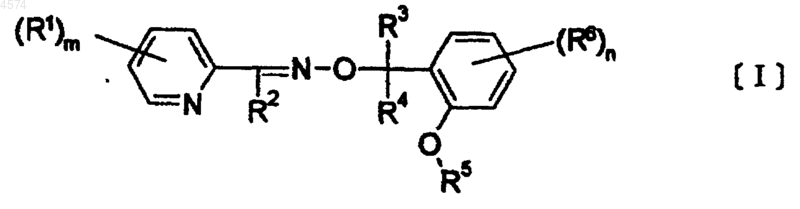
где R1, R2, R3, R4, R5, R6, n и m имеют значения, указанные выше, или их соли в качестве активного ингредиента.
4. Фунгицид по п.3, отличающийся тем, что активный ингредиент является соединением, представляемым общей формулой [I']
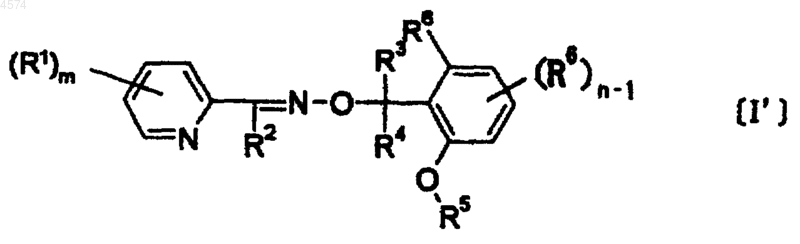
где R1, R2, R3, R4, R5, R6, n и m имеют значения, указанные выше.
Текст
1 Область изобретения Данное изобретение относится к новым оксимным О-эфирным соединениям и фунгицидам, содержащим указанное соединение в качестве активного вещества, для применения в земледелии и садоводстве. Предшествующий уровень техники В отношении сельскохозяйственных и садовых культур применялись различные химические средства защиты сельскохозяйственных растений для борьбы с болезнями растений. Однако из-за ухудшения активности химических средств защиты растений и появления устойчивых к этим химическим средствам штаммов патогенных для растений микроорганизмов,использование фунгицидов для защиты растений было ограничено. Кроме того, многие фунгициды обладают фитотоксичностью в отношении растений или являются токсичными для людей и животных. Следовательно, хотя существует множество фунгицидов, которые были разработаны и использовались для защиты растений, большинство из них неудовлетворительны с точки зрения указанных недостатков. В результате существует потребность получения фунгицидов для использования при защите растений, которые не имеют описанных выше недостатков и могут применяться безопасно. Например, оксимные О-эфирные соединения, подобные определенным в данном изобретении, описаны в ЕР 4754, ЕР 24888, WO 93/21157 как соединения, обладающие инсектицидной и акарицидной активностью. Кроме того, в Jpn. Pat. Appln. Publication(KOKAI)9-3047 раскрыто, что оксимные Оэфирные соединения, представляемые следующей химической формулой, пригодны в качестве фунгицидов. Описание изобретения Объектом данного изобретения является получение новых оксимных О-эфирных соединений, которые могут быть отличными фунгицидами для применения в земледелии и садоводстве, пригодными для производства в промышленном масштабе, обладающими стойкой биологической эффективностью и меньшей фитотоксичностью. Обнаружено, что фунгицидная активность указанных оксимных О-эфирных соединений,представляемых следующей общей формулой[I], может быть усилена, а фитотоксичность может быть снижена введением функциональной кислородной группы во 2 положение бензольного кольца указанного оксимного О-эфирного соединения и заместителя в произвольное положение, в частности в 6 положение бензольного кольца. 2 Поэтому данное изобретение направлено на оксимные О-эфирные соединения, представляемые следующей формулой [I] где R1 представляет C1-6 алкил, С 3-6 циклоалкил,C1-6 алкокси, C1-6 алкилтио, амино, моно- или ди(С 1-6 алкил)амино, C1-6 ацилокси, C1-6 алкоксиС 1-6 алкил, C1-6 галогеналкил, гидрокси или атом галогена;m представляет целое число от 1 до 4, и когда m равно 2 или более, каждый из R1 может быть одинаковым или разным;R3 и R4 являются одинаковыми или разными, и каждый независимо представляет атом водорода или C1-6 алкил;R6 представляет C1-6 алкил, С 3-6 циклоалкил,С 2-6 алкенил, С 2-6 алкинил, C1-6 алкокси, C1-6 алкокси-С 1-6 алкокси,C1-6 алкилкарбонилокси,C1-6 алкокси-C1-6 алкил, C1-6 галогеналкил, циано,нитро, амино, моно- или ди-(С 1-6 алкил)амино,C1-6 алкилкарбониламино, С 1-6 алкилтио, гидрокси или атом галогена; иn представляет собой целое число от 1 до 4, а когда n равно 2 или более, каждый из R6 может быть одинаковым или разным,и фунгицидам для применения в земледелии и садоводстве, содержащим оксимное О-эфирное соединение или его соль в качестве активного ингредиента. Более конкретно, в общей формуле [I]R1 представляет C1-6 алкил, такой как метил, этил, пропил, изопропил, бутил, вторбутил, изобутил, трет-бутил, пентил и его изомеры и гексил и его изомеры,необязательно замещенный С 3-6 циклоалкил, такой как циклопропил, циклопентил, 1 метилциклопентил, циклогексил и 1-метилциклогексил,C1-6 алкокси, такой как метокси, этокси,пропокси, изопропокси, бутокси, втор-бутокси,изобутокси и трет-бутокси,C1-6 алкилтио, такой как метилтио, этилтио,изопропилтио и бутилтио,амино,моно- или ди-(С 1-6 алкил)амино, этиламино,пропиламино, диметиламино, диэтиламино, дипропиламино, дибутиламино и этилизопропиламино,C1-6 ацилокси, такой как ацетокси и пропионилокси, пивалоилокси, 3C1-6 галогеналкил, такой как хлорметил,фторметил, бромметил, дихлорметил, дифторметил, дибромметил, трихлорметил, трифторметил, трибромметил, трихлорэтил, трифторэтил и пентафторэтил; гидрокси или атом галогена, такой как атом фтора, хлора, брома и йода;m представляет целое число от 1 до 4, и когда m равно 2 или более, каждый из R1 может быть одинаковым или разным;R2 представляет атом водорода,C1-6 алкил, такой как метил, этил, пропил,изопропил, бутил, втор-бутил, изобутил, третбутил, пентил и его изомеры, и гексил и его изомеры, или необязательно замещенный С 3-6 циклоалкил, такой как циклопропил, циклопентил, 1 метилциклопентил, циклогексил и 1-метилциклогексил;R3 и R4 могут быть одинаковыми или разными, и каждый независимо представляет атом водорода, илиR5 представляет атом водорода,C1-6 алкил, такой как метил, этил, пропил,изопропил, бутил, втор-бутил, изобутил, третбутил, пентил и его изомеры, и гексил и его изомеры, или необязательно замещенный С 3-6 циклоалкил, такой как циклопропил, циклопентил, 1 метилциклопентил, циклогексил и 1-метилциклогексил;C1-6 галогеналкил, такой как хлорметил,фторметил, бромметил, дихлорметил, дифторметил, дибромметил, трихлорметил, трифторметил, трибромметил, трихлорэтил, трифторэтил и пентафторэтил,C1-6 алкокси-С 1-6 алкил, такой как метоксиметил, метоксиэтил, этоксиметил, пропоксиметил и бутоксиметил,C1-6 алкокси-С 1-6 алкокси-С 1-6 алкил, такой как метоксиэтоксиметил и этоксиэтоксиметил,С 7-10 аралкил, такой как бензил и фенетил,С 7-10 аралкилокси, такой как бензилоксиметил и бензилоксиэтил,C1-6 алкилкарбонил, такой как ацетил, пропионил и пивалоил,C1-6 алкилсульфонил, такой как метансульфонил и этансульфонил, илиC1-6 галогеналкилсульфонил, такой как хлорметилсульфонил и трифторметилсульфонил; 4 бутил, изобутил, трет-бутил, пентил и его изомеры, и гексил и его изомеры,необязательно замещенный С 3-6 циклоалкил, такой как циклопропил, циклопентил, 1 метилциклопентил, циклогексил и 1-метилциклогексил; С 2-6 алкенил, такой как винил, пропенил и изопропенил,С 2-6 алкинил, такой как этинил и пропаргил,C1-6 алкокси, такой как метокси, этокси,пропокси, изопропокси, бутокси, втор-бутокси,изобутокси и трет-бутокси,C1-6 алкокси-С 1-6 алкокси, такой как метоксиметокси, метоксиэтокси, этоксиметокси, пропоксиметокси и бутоксиметокси,C1-6 алкилкарбонил, такой как ацетокси,пропионилокси и пивалоилокси,C1-6 алкокси-С 1-6 алкил, такой как метоксиметил, метоксиэтил, этоксиметил, пропоксиметил и бутоксиметил,C1-6 галогеналкил, такой как хлорметил,фторметил, бромметил, дихлорметил, дифторметил, дибромметил, трихлорметил, трифторметил, трибромметил, трихлорэтил, трифторэтил и пентафторэтил,циано, нитро, амино,моно- или ди-(С 1-6 алкил) амино, такой как метиламино, этиламино, пропиламино, диметиламино, диэтиламино, дипропиламино, дибутиламино и этилизопропиламино,C1-6 алкилкарбониламино, такой как ацетиламино и пивалоиламино,C1-6 алкилтио, такой как метилтио, этилтио и изопропилтио,гидроксил или атом галогена, такой как атом фтора, хлора, брома и йода; иn представляет целое число от 1 до 4, и когда n равно 2 или более, каждый из R6 может быть одинаковым и разным. Из соединений, определенных в данном изобретении, соединения, представляемые общей формулой [I'] где R1, R2, R3, R4, R5, R6, m и n определены выше, из которых бензольное кольцо является замещенным в 6 положении одной из групп, примеры которых представлены выше для R6, обладают превосходной активностью в качестве фунгицида для применения в земледелии и садоводстве. Каждое из соединений, определенных в данном изобретении, обладает отличной фунгицидной активностью против широкого ряда грибков, принадлежащих, например, к оомицетам, аскомицетам, деутеромицетам и базидиомицетам. В частности, соединения данного изобретения обладают необыкновенно высокой 5 фунгицидной активностью против болезни серой плесневой гнили, Botrytis cinerae, по сравнению с известными соединениями, описанными выше. Композиция, содержащая соединение данного изобретения в качестве активного ингредиента, может использоваться для борьбы с различными болезнями растений, поражающими сельскохозяйственные и садовые культуры,включая декоративные цветы, газонные и кормовые культуры, посредством обработки семян,нанесения на листву, почву, водную поверхность и т.д. Примеры болезней растений, с которыми можно бороться, применяя композицию, содержащую соединение данного изобретения, включают следующие. Сахарная свекла: Арахис: Церкоспорозная пятнистость листьев (Cercosporabeticola) Пятнистость листьев (Mycosphaerella arachidis) Поздняя пятнистость листьев (Mycosphaerella berkeleyi) Настоящая мучнистая роса(Sphaerotheca fuliginea) Черная микосфереллезная гниль (Mycosphaerella melonis) Белая гниль (Sclerotinia sclerotiorum) Серая гниль (Botrytis cinerea) Парша (Cladosporium cucumerinum) Серая гниль (Botrytis cinerea) Бурая пятнистость листьев(Sphaerotheca aphanis) Серая шейковая гниль (Botrytis allii) Серая гниль (Botrytis cinerea) Белая гниль (Sclerotinia sclerotiorum) Серая гниль (Botrytis cinerea) Настоящая мучнистая росаkaki) Угловатая пятнистость листьев (Cercospora kaki) Бурая гниль (Monilinia fructicola) Серая гниль (Botrytis cinerea) Настоящая мучнистая роса(Pseudocercosporella herpotrichoides) Сопториоз колосковой чешуи (Leptosohaeria nodorum) Настоящая мучнистая росаfujikuroi) Гельминтоспорийная пятнистость листьев (Cochliobolus(Cercospora kikuchii) Картофель и Ложная мучнистая роса томаты(Plasmopara viticola) Кроме того, нужно отметить, что в последние годы у различных патогенных для растений грибков развилась устойчивость к химическим средствам защиты растений, таким как бензимидазольные фунгициды и карбодиимидные фунгициды. Из этого следует, что существует проблема по борьбе с такой проблемной болезнью растений, так как ни один фунгицид не сдерживает эти болезни растений в достаточной степени. Поэтому крайне желателен эффективный фунгицид, который может бороться с такими грибками, являющимися резистентными,вызывающими эти проблемные болезни растений. Соединения данного изобретения эффективны в отношении этих устойчивых к вышеупомянутым фунгицидам штаммов грибков, а также и в отношении чувствительных штаммов. Соединения данного изобретения эффективны не только в отношении чувствительных грибков, но также и в отношении резистентных штаммов грибков, включая грибок серой гнили(Botrytis cinerea), грибка пятнистости листьев сахарной свеклы (Cercospora beticola), грибка парши яблонь (Venturia inaequalis) и грибка парши груш (Venturia nashicola), например, к тиофанатметилу, беномилу и карбендазиму. Кроме того, соединения, определенные в данном изобретении, эффективны также в отношении заболеваний серой гнили, вызываемыхBotrytis cinerea, который устойчив к дикарбоксиимидным фунгицидам, таким как винклозолин, просимидон и ипродион. Фунгицидное действие соединений данного изобретения в отношении резистентных штаммов грибка серой гнили эффективно так же, как и против чувствительных штаммов. Конкретно, примерами заболеваний растений, в отношении которых более предпочтительно использовать фунгицидную композицию(фунгицид для использования в земледелии и садоводстве), содержащую соединение данного изобретения, являются церспореллезная пятнистость листьев сахарной свеклы, настоящая мучнистая роса пшеницы, пирикуляриоз (риса) падди, парша яблонь, серая гниль фасоли, пятнистость листьев арахиса и т.д. Кроме того, соединения данного изобретения можно также использовать в качестве средства против заражения для профилактики об 004574 8 растания конструкций в воде, таких как днища кораблей и рыбацкие сети, от заражения водной среды обитания. Воплощения Соединения по данному изобретению получают способом, представленным следующим уравнением реакции 1) где R1, R2, R3, R4 и m определены выше, Ar представляет замещенную фенильную группу,представленную формулой где R5, R6 и n определены выше, и L представляет атом галогена, такой как атом хлора, брома и йода, или удаляемую группу, такую как метансульфонилокси или п-толуолсульфонилокси. В частности, в уравнении реакции (1),представленном выше, соединения, представленные общей формулой [I], можно получить по реакции соединения формулы [II] с соединением формулы [III], протекающей без растворителя или предпочтительно в растворителе при перемешивании в течение от 10 мин до 24 ч при температуре реакции от 0 до 150 С и в присутствии агента, снижающего кислотность. Примеры растворителя, который можно использовать в вышеуказанной реакции (1),включают кетон, такой как ацетон и 2-бутанон,простой эфир, такой как диэтиловый эфир и тетрагидрофуран, ароматический углеводород,такой как бензол и толуол, спирт, такой как метанол и этанол, ацетонитрил, N,N-диметилформамид, диметилсульфоксид и воду. Для реакции один или более из растворителей, названных выше, могут использоваться в сочетании. Примеры основания, которое можно использовать в вышеприведенной реакции (1),включают неорганическое основание, такое как гидроксид натрия, гидроксид калия, карбонат натрия и гидрид натрия, алкоголят щелочного металла, такой как метилат натрия и этилат натрия, и органическое основание, такое как пиридин, триэтиламин и ДБУ. Исходное вещество, представляемое формулой [II], для получения соединений по данному изобретению может быть получено по способу, описанному в Jap. Pat. Appln. KOKAI где R1, R2, R3, R4, Ar и m определены выше. В частности, по уравнению реакции (2),представленному выше, соединение, представ 9 ляемое общей формулой [I], получают по реакции соединения, представленного формулой[V], или его солью, протекающей при перемешивании без растворителя или предпочтительно в растворителе в течение от 10 мин до 24 ч при температуре реакции в интервале от 0 до 150 С. Примеры растворителя, который можно использовать при вышеприведенной реакции(2), включают спирт, такой как этанол и метанол, простой эфир, такой как диэтиловый эфир,тетрагидрофуран и диоксан, целлозольв, такой как метилцеллозольв и этилцеллозольв, ароматический углеводород, такой как бензол и толуол, уксусную кислоту, N,N-диметилформамид,диметилсульфоксид и воду. Для реакции (2) можно использовать один или более из растворителей, названных выше, в сочетании. Реакция(2) не требует присутствия катализатора, однако, реакция может быть иногда ускорена добавлением кислоты или основания. Примеры каталитической кислоты включают неорганическую кислоту, такую как серная кислота и соляная кислота, и органическую кислоту, такую как птолуолсульфоновая кислота. Примеры каталитического основания включают уксусную кислоту и т.п. После завершения реакций (1) и (2) целевые соединения могут быть получены в результате осуществления обычной послереакционной переработки продуктов реакции. Нужно отметить, что полученные целевые соединения могут быть далее химически модифицированы для получения их различных производных. Более конкретно, в качестве примеров указанной химической модификации можно привести превращение функциональной группы, представляемое превращением нитрогруппы в аминогруппу реакцией восстановления, снятия защиты функциональных групп, таких как метоксиметильная группа, известной в области органической химии в качестве защитной группы, превращение функциональных групп, таких как гидроксильная группа и аминогруппа, полученных снятием защиты посредством алкилирования и ацилирования, и превращения функциональных групп, представляемое реакцией Соногашира, известной в области органической химии как снятие защитной группы, такой как атомы галогена, с использованием нуклеофильного реагента. Указанные соли соединения формулы [I] могут быть получены путем осуществления реакции соединения формулы [I] и неорганической кислоты или органической кислоты в подходящем растворителе. Химические структуры соединений в соответствии с данным изобретением определены с помощью применения ЯМР, масс-спектра и т.д. Фунгицид Фунгицид в соответствии с данным изобретением содержит в качестве активного ин 004574 10 гредиента одно или более из соединений, определенных в данном изобретении. При практическом применении соединений данного изобретения эти соединения могут использоваться в форме чистого вещества без сочетания с ними другого компонента. А также соединение данного изобретения может быть изготовлено в обычной рецептуре, которая будет использоваться в целях получения химического препарата для защиты растений, например, смачиваемого порошка, гранул, порошка, эмульгируемого концентрата, растворимого в воде препарата,концентрата суспензии, жидкого препарата и т.д. Примеры добавок и носителей, которые можно использовать в рецептурах для применения соединения данного изобретения для защиты растений, являются следующими. Для препаратов твердого типа - фитогенные порошковые материалы, такие как соевый порошок(пудра) и мука, тонкие минеральные порошки,такие как диатомовая земля, апатит, гипс, тальк,бентонит, пирофиллит и глина, органические и неорганические соединения, такие как бензоат натрия, мочевина и глауберова соль. В том случае, когда соединения данного изобретения изготавливают в рецептурах жидкого типа, в качестве растворителя можно использовать фракции нефти, включая керосин,ксилол и сольвент-нафту, циклогексан, циклогексанон, диметилформамид, диметилсульфоксид, спирты, ацетон, трихлорэтилен, метилизобутилкетон, минеральные масла, растительные масла, воду и т.д. Кроме того, чтобы обеспечить однородность и стабильность приведенных в качестве примеров препаратов, при необходимости в каждую из рецептур можно добавлять поверхностно-активные вещества. Примеры поверхностно-активного вещества, которое может быть добавлено к указанным рецептурам, включают неионные поверхностно-активные вещества,такие как полиоксиэтилен с присоединением алкилфенилового эфира, полиоксиэтилен с присоединением эфира высшей жирной кислоты,полиоксиэтилен с присоединением эфира сорбитана и высшей жирной кислоты и полиоксиэтилен с присоединением тристирилфенилового эфира, сульфатный сложный эфир полиоксиэтилена с присоединением алкилфенилового эфира,алкилбензолсульфанат, сульфатный эфир высшего спирта, алкилнафталинсульфонат, поликарбонат, лигнинсульфонат, формальдегидный конденсат алкилнафталинсульфоната и сополимера изобутилена-малеинового ангидрида. В основном, содержание активного ингредиента в каждой из рецептур, приведенных выше, находится предпочтительно в интервале от 0,01 до 90 мас.%, а более предпочтительно от 0,05 до 85 мас.% от общей массы композиции 11 Каждый из изготовленных препаратов, таких как смачиваемый порошок, эмульгируемый концентрат и жидкий концентрат, разбавляют водой так, чтобы приготовить разбавленный раствор или суспензию с желаемой концентрацией, и наносят на культуры растений, например, путем распыления. Что касается таких препаратов, как гранулированные или порошковые препараты, то сам препарат наносят на намеченные культуры растений. Поэтому фунгицидные композиции по данному изобретению, изготовленные в виде препаратов соответствующих типов, описанных выше, наносят на культуры растений, семена, водную поверхность и почву или непосредственно, или в виде разбавленного водой раствора. Теперь будет дано объяснение в отношении дозы нанесения соответствующих препаратов. Доза нанесения может различаться в зависимости от различных условий, таких как климатические условия, тип препарата, время нанесения, метод нанесения, объект нанесения, болезнь, которую нужно подавить, намеченное растение и т.д. Однако доза нанесения в расчете на активный ингредиент на гектар обычно находится в интервале от 1 до 1000 г и предпочтительно от 10 до 100 г на гектар. Более конкретно, когда смачиваемый порошок, эмульгируемый концентрат, концентрат суспензии или жидкий препарат применяют с разбавлением водой, концентрация активного ингредиента при разбавлении будет находиться в интервале от 1 до 1000 ч./млн и предпочтительно от 10 до 250 ч./млн. С другой стороны, в случае гранулированных и порошковых препаратов их наносят непосредственно без приготовления разведения. Нет необходимости говорить о том, что соединение по данному изобретению само по себе обладает достаточной фунгицидной активностью, однако, оно может сочетаться при использовании с одним или более других химических средств защиты растений различных типов, например, с фунгицидами, инсектицидами,акарицидами и синергистами. В силу этого, будут приведены типичные примеры тех фунгицидов, инсектицидов, акарицидов, нематицидов и регуляторов роста растений, которые могут сочетаться при применении с фунгицидной композицией по данному изобретению. Фунгициды. Фунгициды на основе меди: основной хлорид меди, основной сульфат меди и т.д. Фунгициды на основе серы: тиурам, зинеб,манеб, манкозеб, зирам, пробинеб, поликарбамат и т.д. Фунгициды полигалогеналкилтио типа: каптан, фолпет, дихлорфлуанид и т.д. Хлорорганические фунгициды: хлорталонил, фталид и т.д.(ЕРВР), метилпаратион, метилоксадиметон,этион, салитион, цианофос, изоксатион, пиридафентион, фозалон, метидатион, сульпрофос,хлорфевинфос, тетрахлорвинфос, диметилвинфос, пропафос, изофенфос, этилтриметон, профенофос, пираклофос, монокротофос, азинфосметил, альдикарб, метомил, дитикарб, карбофуран, карбосульфан, бенфлакарб, флатиокарб,пропоксур, БФМС (ВРМС), МТМК (МТМС),МИФС (MIPC), карбарил, пиримикарб, ртифенкарб, феноксикарб и т.д. Пиретроидные инсектициды: перметрин,циперметрин, дельтаметрин, фенвалерат, фенпропатрин, пиретрин, аллетрин, тетраметрин,ресметрин, диметрин, пропатрин, фенотрин,протрин, флуваринат, сифлутрин, сигалотрин, 13 флуцитринат, этофенпрокс, циклопротрин, тралиметрин, силафлуофен, профенпрокс, акринатрин и т.д. Бензоилмочевина и другие инсектициды: дифлубензурон, хлорфлуазурон, гексафлумурон, трифлумурон, тетрабензурон, фулфеноксурон, флуциклоксурон, бупрофезин, пирипроксифен, метопрен, бензоэпин, диафентиурон,ацетамиприд, имидаклоприд, нитенпирам, фипронил, картап, тиоциклам, бенсультап, никотинсульфат, ротенон, метальдегид, машинное масло, микробные инсектициды, такие как БТ и инсектопатогенные вирусы и т.д. Нематициды: фенамифос, фостиазат и т.д. Акарициды: хлорбензилат, фенисобромолат, дикофол, амитраз, BPPS, бензомат, гекситиазокс, фенбутатин оксид, полинактин, хинометионат, CPCBS, тетрадифон, авермектин,милбемектин, клофентезин, сигексатин, пиридабен, фехпроксимат, тебуфенпирад, пиримидифен, фенотиокарб, диенохлор и т.д. Регуляторы роста растений: гиббереллин(например, гиббереллин A3, гиббереллин A5,гиббереллин А 7) с IAA, NAA и т.д. Наилучшие способы осуществления изобретения Теперь данное изобретение будет описано конкретно с обращением к примерам, описанным ниже. Пример 1. Получение 1-(4,6-диметил-2 пиридинил)этанон-O-[(2-фтор-6-метоксифенил) метил]оксима (соединение 1).(3,64 ммоль) 2-фтор-6 метоксибензилового спирта растворяли в 10 мл бензола и полученный раствор добавляли к 0,56 г (4,73 ммоль) тионилхлорида при комнатной температуре. Полученный раствор перемешивали в течение 1 ч при комнатной температуре до завершения реакции. Реакционный раствор затем концентрировали при пониженном давлении с получением неочищенного продукта 2 фтор-6-метоксибензилхлорида. С другой стороны, 0,46 г (2,80 ммоль) 1(4,6-диметил-2-пиридинил)этаноноксима растворяли в 10 мл N,N-диметилформамида, и к полученному раствору добавляли 0,13 г (3,36 ммоль) гидрида натрия (60%, в масле) при охлаждении раствора льдом. Затем полученный раствор перемешивали в течение 30 мин при той же температуре и туда последовательно добавляли все количество неочищенного 2-фтор-6 метоксибензилхлорида, полученного, как описано выше, при охлаждении раствора льдом. Полученную смесь далее перемешивали в течение 40 мин при комнатной температуре и реакционную смесь выливали в ледяную воду и затем экстрагировали диэтиловым эфиром. Полученный неводный слой промывали водой и за 004574 14 тем сушили безводным сульфатом магния. Осушенный неводный слой затем концентрировали при пониженном давлении с получением неочищенного продукта. Затем указанный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 7:3 по объему) с получением целевого соединения в количестве 0,55 г. Температура плавления: 87-89 С. Пример 2. Получение 1-(4,6-диметил-2 пиридинил)этанон-O-[(2,4-диметоксифенил) метил]оксима (соединение 13). 0,61 г (3,63 ммоль) 2,4-диметоксибензилового спирта растворяли в 9,2 мл толуола и к полученному раствору добавляли 0,3 мл пиридина. Полученный прозрачный раствор охлаждали до температуры ниже 0 С и затем каплями добавляли 1,8 мл толуольного раствора, содержащего 0,98 г (3,62 ммоль) трибромида фосфора, в течение 20 мин. Полученный раствор перемешивали в течение 35 мин, чтобы дать возможность соединениям прореагировать. Затем реакционный раствор выливали в ледяную воду и ледяную воду экстрагировали диэтиловым эфиром. Полученный неводный слой последовательно промывали водой, насыщенным водным раствором гидрокарбоната натрия и раствором хлорида натрия, все они заранее охлаждались, и затем сушили безводным сульфатом магния. Осушенный раствор затем подвергали перегонке при пониженном давлении приблизительно при 30 С с использованием роторного испарителя для отгонки диэтилового эфира, содержащегося в растворе, получая тем самым толуольный раствор 2,4-диметоксибензилхлорида. С другой стороны, 0,50 г (3,05 ммоль) 1(4,6-диметил-2-пиридинил)этаноноксима растворяли в 5 мл N,N-диметилформамида, и в полученный раствор добавляли 0,12 г (3,00 мл) гидрида натрия (60%, в масле) при охлаждении льдом. Полученный раствор перемешивали в течение 30 мин при температуре ниже 0 С и затем добавляли все количество толуольного раствора 2,4-диметоксибензилхлорида, приготовленного ранее, при охлаждении льдом. Полученный раствор перемешивали в течение 1,5 ч при охлаждении льдом и реакционный раствор затем выливали в ледяную воду и ледяную воду,содержащую реакционный раствор экстрагировали диэтиловым эфиром. Полученный неводный слой отделяли и промывали водой, а затем сушили безводным сульфатом магния. Осушенный слой концентрировали при пониженном давлении с получением неочищенного продукта. Затем указанный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 7:3 по объ 15 ему) с получением целевого соединения в количестве 0,62 г. 0,50 г (3,68 ммоль) 2,3-диметиланизола растворяли в 10 мл тетрахлорида углерода. В полученный раствор затем добавляли 0,72 г(4,04 ммоль) N-бромсукцинимида и полученный раствор облучали светом (инфракрасная лампа 375 Вт, производимая Toshiba) в течение 45 мин при температуре дефлегмации. Затем раствор охлаждали и его температуру поддерживали на уровне комнатной температуры, чтобы вызвать осаждение. Осажденный сукцинимид отфильтровывали и полученный фильтрат концентрировали при пониженном давлении с получением неочищенного продукта 2-метокси-6 метилбензилбромида. С другой стороны, 0,50 г (3,05 ммоль) 1(4,6-диметил-2-пиридинил)этаноноксима растворяли в 10 мл N,N-диметилформамида и к полученному раствору добавляли 0,12 г (3,00 ммоль) гидрида натрия (60%, в масле) при охлаждении льдом. Раствор затем перемешивали в течение 30 мин при температуре ниже 0 С и затем добавляли все количество неочищенного 2-метокси-6-метилбензилбромида,приготовленного ранее, при охлаждении льдом. Полученный раствор перемешивали в течение часа при комнатной температуре для завершения реакции и реакционный раствор выливали в ледяную воду и экстрагировали диэтиловым эфиром. Полученный неводный слой отделяли и отделенный слой промывали водой, а затем сушили безводным сульфатом магния. Осушенный неводный слой концентрировали при пониженном давлении с получением неочищенного продукта. Затем указанный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 7:3 по объему) и перекристаллизовывали с получением целевого соединения в количестве 0,30 г. Температура плавления: 71-72 С. Пример 4. Получение 4,6-диметил-2 пиридинкарбоксиальдегид-О-[(2,6-диметоксифенил)метил]оксима (соединение 196).(75,8 ммоль) 2-циано-4,6 диметилпиридина растворяли в 100 мл метиленхлорида и полученный раствор охлаждали и его 16 температуру поддерживали на уровне -78 С. Затем к раствору каплями в течение 20 мин добавляли 87,8 мл (83,3 ммоль) 0,95 М толуольного раствора гидродиизобутилалюминия при той же температуре. Полученный раствор перемешивали в течение 1,8 ч при той же температуре и дополнительно перемешивали в течение 1,3 ч после повышения температуры до комнатной температуры для завершения реакции. В реакционный раствор затем по каплям добавляли 3 н. соляную кислоту для того, чтобы прервать реакцию, и затем реакционный раствор нейтрализовали добавлением 10% водного раствора гидроксида натрия для последующей стадии экстрагирования хлороформом. Полученный хлороформный слой сушили безводным сульфатом магния и затем концентрировали при пониженном давлении с получением неочищенного продукта реакции. Полученный неочищенный продукт затем очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 9:1 по объему) с получением целевого соединения в количестве 0,34 г. 1 0,33 г (2,4 ммоль) 4,6-диметил-2 пиридинкарбоксиальдегида растворяли в 5 мл этанола и в полученный раствор добавляли 0,20 г (2,9 ммоль) гидрохлорида гидроксиламина. Затем смесь нагревали, чтобы повысить температуру до температуры дефлегмации и перемешивали в течение 35 мин. После перемешивания температуру снижали до комнатной температуры. Реакционный раствор, полученный в кислом состоянии, нейтрализовали 10% водным раствором гидроксида натрия. Раствор затем экстрагировали этилацетатом и полученный неводный слой отделяли, а затем сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением целевого соединения в количестве 0,32 г. 1 0,43 г (2,56 ммоль) 2,6-диметоксибензилового спирта растворяли в 5 мл бензола и к полученному раствору добавляли 0,40 г (3,36 ммоль) тионилхлорида при комнатной температуре. Смесь перемешивали в течение часа при комнатной температуре, чтобы облегчить реакцию указанных соединений. Реакционный раствор затем концентрировали при пониженном давлении с получением неочищенного 2,6 диметоксибензилхлорида. С другой стороны, 0,32 г (2,13 ммоль) 4,6 диметил-2-пиридинкарбоксиальдоксима добавляли к 5 мл N,N-диметилформамида для приготовления его суспензии. К суспензии добавляли 0,11 г (2,75 ммоль) гидрида натрия (60%, в масле) при охлаждении суспензии льдом. Смесь перемешивали в течение 25 мин при температуре ниже 0 С и затем к ней добавляли все количество неочищенного 2,6-диметоксибензилхлорида, приготовленного предварительно в условиях охлаждения льдом. Смесь перемешивали в течение 2 ч при комнатной температуре для облегчения взаимодействия соединений. Реакционную смесь затем выливали в ледяную воду и реакционную смесь в ледяной воде экстрагировали диэтиловым эфиром. Полученный неводный слой отделяли, промывали водой и сушили безводным сульфатом магния. Осушенный неводный слой затем концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 7:3 по объему) с получением целевого соединения в количестве 0,66 г. Температура плавления: 103-105 С. Пример 5. Получение 4-хлор-6-метил-2 пиридинкарбоксиальдегид-O-[(2,6-диметоксифенил)метил]оксима (соединение 219). том. Полученный неводный слой отделяли и промывали насыщенным раствором соли и затем сушили безводным сульфатом магния. Осушенный неводный слой затем концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт затем очищали колоночной хроматографией на силикагеле (элюент: бензол:этилацетат = 2:1 по объему) с получением целевого соединения в количестве 1,38 г. 4,0 (25,4 ммоль) 4-хлор-2,6-диметилпиридин-1-оксида растворяли в 12 мл уксусного ангидрида. Полученный раствор постепенно нагревали для повышения температуры до температуры дефлегмации и раствор затем перемешивали в течение ночи при той же температуре. Реакционный раствор затем концентрировали при пониженном давлении с получением неочищенного 4-хлор-6-метил-2-пиридинилметилового сложного эфира уксусной кислоты. Полученный неочищенный продукт растворяли в 14 мл метанола и к полученному раствору добавляли 7 мл воды и 0,9 г гидроксида калия. Полученную смесь затем перемешивали в течение 4 ч при комнатной температуре для осуществления взаимодействия. Реакционный раствор затем концентрировали при пониженном давлении с получением продукта реакции. Продукт реакции затем разбавляли водой и полученный раствор экстрагировали этилацета 1,08 г (6,9 ммоль) 4-хлор-6-метил-2 пиридинкарбоксиальдегида растворяли в 15 мл метанола. К полученному раствору добавляли 0,53 г (7,6 ммоль) гидрохлорида гидроксиламина и полученную смесь нагревали так, чтобы повысить температуру смеси до температуры дефлегмации. Смесь перемешивали в течение часа при той же температуре, чтобы облегчить взаимодействие соединений в смеси с последующим охлаждением реакционной смеси до комнатной температуры. Реакционный раствор,полученный в кислом состоянии, затем нейтрализовали водным раствором гидрокарбоната натрия. К нейтрализованному раствору затем добавляли этилацетат, проводили экстрагирование, и полученный неводный слой сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением целевого соединения. Общий выход целевого соединения из фильтрата и экстракта в целом, как найдено, составляет 1,13 г. 1,38 г (8,8 ммоль) 4-хлор-6-метил-2 пиридинилметанола растворяли в 20 мл бензола. К полученному раствору добавляли 3,3 г активированного диоксида марганца (производимого Aldrich) и смесь нагревали так, чтобы повысить температуру смеси до температуры дефлегмации. После того как температура смеси достигала температуры дефлегмации, смесь непрерывно перемешивали всю ночь для завершения реакции. Затем реакционную смесь охлаждали и температуру смеси поддерживали на уровне комнатной температуры. Затем нерастворимые вещества из смеси удаляли фильтрованием. Полученный фильтрат концентрировали при пониженном давлении с получением целевого соединения в количестве 1,08 г. 1 0,49 г (2,93 ммоль) 2,6-диметоксибензилового спирта растворяли в 6 мл бензола и в полученный раствор добавляли 0,41 г (3,32 ммоль) тионилхлорида при комнатной температуре. Полученный таким образом раствор затем перемешивали в течение 1,5 ч при комнатной температуре для завершения реакции. Реакционный раствор затем концентрировали при пониженном давлении с получением неочищенного продукта 2,6-диметоксибензилхлорида. С другой стороны, 0,50 г (2,93 ммоль) 4 хлор-6-метил-2-пиридинкарбоксиальдоксима добавляли в 5 мл N,N-диметилформамида с получением суспензии, туда добавляли 0,18 г (4,39 ммоль) гидрида натрия (60%, в масле) при охлаждении суспензии льдом. Затем смесь перемешивали в течение 30 мин при температуре ниже 0 С и добавляли все количество неочищенного 2,6-диметоксибензилхлорида, полученного ранее, при охлаждении смеси льдом. Полученную смесь затем перемешивали в течение 2 ч при комнатной температуре для завершения реакции и реакционную смесь затем выливали в ледяную воду. Ледяную воду, содержащую смесь, экстрагировали диэтиловым эфиром и полученный неводный слой промывали водой, сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением тем самым неочищенного продукта. Полученный неочищенный продукт затем очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 7:3 (по объему с получением целевого соединения в количестве 0,66 г. Температура плавления: 106-108 С. Пример 6. Получение 1-(4-хлор-6-метил-2 пиридинил)этанон-О-[(2,6-диметоксифенил) метилоксима (соединение 18). 32 г (223 ммоль) 4-хлор-2-метилпиридин 1-оксида растворяли в 250 мл метиленхлорида. К полученному раствору в течение 5 мин добавляли 24,6 г (248 ммоль) триметилсилиланилида при комнатной температуре. Смесь перемешивали в течение 10 мин и затем в течение 5 мин добавляли 23,5 г (219 ммоль) диметилкарбамо 004574 20 илхлорида при той же температуре. В это время внутренняя температура смеси повышалась до температуры ее дефлегмации за счет тепла, выделяющегося при реакции. При перемешивании смесь естественным образом охлаждалась до того момента, когда внутренняя температура смеси достигала комнатной температуры. После перемешивания смеси в течение 4 дней реакционный раствор охлаждали так, чтобы ее температура сохранялась на уровне 5 С, и затем добавляли 300 мл 10% водного раствора гидрокарбоната натрия. Органический слой отделяли и водный слой экстрагировали хлороформом. Полученный хлороформный слой объединяли с отделенным органическим слоем и объединенную смесь сушили безводным сульфатом магния и затем концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт затем очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 4:1 (по объему с получением целевого соединения в количестве 10 г. 1 10 г (66 ммоль) 4-хлор-2-циано-6-метилпиридина растворяли в 100 мл безводного диэтилового эфира. Полученный раствор охлаждали так, чтобы его температура сохранялась на уровне 5 С, и затем туда по каплям добавляли в течение 15 мин 262 мл (87 ммоль) 3 М раствора метилмагнийбромида (производимого Aldrich) в диэтиловом эфире при той же температуре. В это время внутренняя температура смеси повышается до 20 С за счет тепла, выделяющегося при реакции. Смесь перемешивали в течение 2,5 ч и затем охлаждали до 5 С и к ней добавляли водный раствор хлорида аммония, чтобы прекратить реакцию. Реакционную смесь экстрагировали диэтиловым эфиром и полученный неводный слой промывали водой, затем сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат= 4:1 (по объему с получением целевого соединения в количестве 3,8 г. 1 3,8 г (22,4 ммоль) 1-(4-хлор-6-метил-2 пиридинил)этанона растворяли в 40 мл метанола. Полученный раствор охлаждали до 5 С и туда добавляли 2,34 г (33,7 ммоль) гидрохлорида гидроксиламина и 6,49 г (33,7 ммоль) 28% метилата натрия. Полученную смесь выдерживали при комнатной температуре, затем непрерывно перемешивали всю ночь. Целевое соединение осаждали из смеси. Осадок затем отфильтровывали, промывали гексаном и сушили с получением целевого соединения в количестве 3,3 г. 1 1,86 г (11,1 ммоль) 2,6-диметоксибензилового спирта растворяли в 15 мл бензола и полученный раствор охлаждали до 5 С. К раствору затем добавляли 1,55 г (13,0 ммоль) тионилхлорида при той же температуре. Температуру смеси затем повышали до комнатной температуры, затем перемешивали в течение 70 мин для завершения реакции. Реакционный раствор концентрировали при пониженном давлении с получением неочищенного 2,6 диметоксибензилхлорида. С другой стороны, 1,66 (9,0 ммоль) 1-(4 хлор-6-метил-2-пиридинил)этаноноксима растворяли в 15 мл N,N-диметилформамида и к полученному раствору добавляли 0,18 г (4,39 ммоль) гидрида натрия (60%, в масле) при охлаждении раствора льдом. Смесь перемешивали в течение 15 мин при температуре ниже 0 С и добавляли все количество неочищенного 2,6 диметоксибензил хлорида, полученного ранее,при охлаждении смеси льдом. Полученную смесь перемешивали в течение 2,3 ч при комнатной температуре для завершения реакции. Реакционную смесь затем выливали в ледяную воду. В это время целевое соединение осаждалось в ледяной воде. Осадок отфильтровывали, промывали гексаном и сушили с получением целевого соединения в количестве 2,3 г. Температура плавления: 105-106 С. Пример 7. Получение 4,6-диметил-2 пиридинкарбоксилальдегид-О-[(2-метокси-6 нитрофенил)метил]оксима (соединение 217). 3,0 г (18 ммоль) 2-метил-3-нитроанизола растворяли в 500 мл тетрахлорида углерода. К полученному раствору добавляли 6,4 г (36 ммоль) N-бромсукцинимида и смесь облучали светом, излучаемым инфракрасной лампой 375 Вт (производимой Toshiba) в течение 3 ч при температуре дефлегмации. Затем смесь охлаждали до комнатной температуры. Сукцинимид,осажденный в смеси, отделяли фильтрованием и полученный фильтрат концентрировали при пониженном давлении с получением неочищенного 2-метокси-6-нитробензилбромида. С другой стороны, 2,7 г (18 ммоль) 4,6 диметил-2-пиридинкарбоксиальдоксима добавляли к 50 мл N,N-диметилформамида для приготовления суспензии и в суспензию добавляли 0,8 6 г (21,6 ммоль) гидрида натрия (60%, в масле) при комнатной температуре. Полученную смесь затем перемешивали в течение 30 мин при комнатной температуре, а затем туда добавляли все количество неочищенного 2-метокси-6 нитробензилбромида, полученного ранее, при охлаждении смеси льдом. Смесь затем перемешивали в течение 3 ч при комнатной температуре для завершения реакции. Реакционную смесь выливали в ледяную воду и добавленную ледяную воду экстрагировали диэтиловым эфиром. Полученный неводный слой промывали водой,затем сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: бензол:этилацетат = 20:1 (по объему с получением целевого соединения в количестве 3,1 г. Температура плавления: 122-123 С. Пример 8. Получение 4,6-диметил-2 пиридинкарбоксиальдегид-O-[(2-метокси-6 аминофенил)метил]оксима (соединение 222). 1,86 г (33,3 ммоль) электролизного порошка железа (производимого Wako Pure Chemical),20 мл воды и 1,2 г (20 ммоль) уксусной кислоты объединяли с получением суспензии. Суспензию нагревали до достижения 60 С и затем по каплям в течение 10 мин туда подавали ацетоновый раствор (10 мл), содержащий 4,6 диметил-2-пиридинкарбоксиальдегид-О-[(2 метокси-6-нитрофенил)метил]оксим в количестве 2,1 г (6,7 ммоль). Полученную смесь затем перемешивали в течение 2 ч при температуре дефлегмации для завершения реакции. Реакционную суспензию охлаждали до комнатной 23 температуры и затем разбавляли этилацетатом. Реакционную смесь фильтровали через целит для удаления нерастворимых веществ. Полученный фильтрат экстрагировали этилацетатом и полученный слой органического растворителя сушили безводным сульфатом магния. Осушенный слой затем концентрировали при пониженном давлении и потом очищали колоночной хроматографией на силикагеле (элюент: гексан:этилацетат = 7:3 (по объему с получением целевого соединения в количестве 1,8 г. Температура плавления: 115-117 С. Пример 9. Получение 4,6-диметил-2 пиридинкарбоксиальдегид-O-[(2-метокси-6 метиламинофенил)метил]оксима (соединение 223). 3,0 г (10,5 ммоль) 4,6-диметил-2-пиридинкарбоксиальдегид-O-[(2-метокси-6-аминофенил) метил]оксима растворяли в 100 мл ацетонитрила. К полученному раствору добавляли 1,0 г (7,2 ммоль) карбоната калия и 1,33 г (10,5 ммоль) диметилсульфата при комнатной температуре. Полученную смесь перемешивали в течение 3 ч при той же температуре для завершения реакции. Реакционный раствор затем концентрировали при пониженном давлении, к нему добавляли воду и потом экстрагировали этилацетатом. Полученный неводный слой сушили безводным сульфатом магния и затем концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: гексан: этилацетат = 7:3 (по объему с получением целевого соединения в количестве 0,5 г. Температура плавления: 115-117 С. Кроме того, из другой фракции, выделенной колоночной хроматографией, получали 0,3 г 4,6-диметил-2-пиридинкарбоксиальдегид-О-[(2 метокси-6-диметиламинофенил)метил]оксима 2,34 г (11,8 ммоль) 2-метоксиметокси-3 метоксибензилового спирта растворяли в 20 мл диэтилового эфира и к полученному раствору 24 добавляли 1,53 г (11,8 ммоль) N,N-диизопропилэтиламина. В полученный раствор по каплям в течение 15 мин добавляли 1,40 г (11,8 ммоль) тионилхлорида и диэтилового эфира (15 мл) при охлаждении раствора льдом. Температуру полученной смеси затем снова доводили до комнатной температуры и смесь перемешивали всю ночь. Нерастворимые вещества удаляли фильтрованием и фильтрат концентрировали под пониженным давлением с получением, неочищенного продукта 2-метоксиметокси-3-метоксибензилхлорида. С другой стороны, 1,94 г (11,8 ммоль) 1(4,6-диметил-2-пиридинил)этаноноксима растворяли в 20 мл N,N-диметилформамида и к полученному раствору добавляли 0,71 г (17,7 ммоль) гидрида натрия (60%, в масле) при охлаждении раствора льдом. Полученную смесь затем перемешивали в течение 30 мин при температуре ниже 0 С, а затем туда добавляли все количество неочищенного 2-метоксиметокси-3 метоксибензилхлорида, полученного ранее, при охлаждении смеси льдом. Смесь затем перемешивали в течение 3 ч при комнатной температуре для завершения реакции. Реакционную смесь выливали в ледяную воду и затем экстрагировали этилацетатом. Полученный неводный слой промывали водой, сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле(элюент: гексан:этилацетат = 4:1 (по объему с получением целевого соединения в количестве 1,77 г. 1 Н-ЯМР (CDCl3, ТМС,м.д.): 2,31 (с, 3 Н),2,36 (кв, 3 Н), 2,51 (с, 3 Н), 3,62 (с, 3 Н), 3,86 (3,3 Н), 5,16 (с, 2 Н), 5,40 (с, 2 Н), 6,86-7,13 (м, 4 Н),7,51 (д, 1 Н). 1,77 г (5,14 ммоль) 1-(4,6-диметил-2 пиридинил)этанон-О-[(2-метоксиметокси-3 метоксифенил)метил]оксима растворяли в 20 мл тетрагидрофурана и к полученному раствору добавляли 10 мл 1 н. соляной кислоты. Полученную смесь затем нагревали до достижения температуры дефлегмации и далее перемешивали в течение часа. Затем смесь охлаждали до комнатной температуры, нейтрализовали водным 1 н. раствором гидроксида натрия и экстрагировали диэтиловым эфиром. Полученный неводный слой промывали насыщенным раствором соли, сушили безводным сульфатом магния и затем концентрировали при пониженном давле 25 нии с получением целевого соединения в количестве 1,6 г. 0,2 г (0,67 ммоль) 1-(4,6-диметил-2-пиридинил)этанон-О-[(2-гидрокси-3-метоксифенил) метил]оксима растворяли в 5 мл метиленхлорида. К полученному раствору добавляли 0,11 г(1,34 ммоль) пиридина, 5 мг 4-(N,N-диметиламино)пиридина и 0,12 г (1,00 ммоль) пивалилового хлорангидрида. Полученную смесь нагревали до достижения температуры дефлегмации и перемешивали в течение 5 ч для завершения реакции. Реакционный раствор промывали последовательно водой и насыщенным раствором соли и полученный неводный слой сушили безводным сульфатом магния. Смесь затем концентрировали при пониженном давлении с получением неочищенного продукта. Неочищенный продукт затем очищали колоночной хроматографией на силикагеле (элюент: гексан: этилацетат = 9:1 (по объему с получением целевого соединения в количестве 0,2 г. 1 2,37 г (11,8 ммоль) 2-метил-3-броманизола растворяли в 100 мл тетрахлорида углерода. К полученному раствору добавляли 2,3 г (13,0 ммоль) N-бромсукцинимида и полученную смесь облучали светом, излучаемым инфракрасной лампой в 375 Вт (производимой Toshiba), в течение часа при температуре дефлегмации. Затем смесь охлаждали до комнатной температуры. Осадок, полученный в смеси, отфильтровывали и полученный фильтрат концентрировали при пониженном давлении с получением неочищенного продукта, состоящего из 2 метокси-6-бромбензилбромида. С другой стороны, 1,77 г (11,8 ммоль) 4,6 диметил-2-пиридинкарбоксиальдоксима добавляли к 20 мл N,N-диметилформамида для приготовления его суспензии и в суспензию добавляли 0,52 г (13,0 ммоль) гидрида натрия (60%, в масле) при комнатной температуре. Полученную смесь перемешивали в течение 30 мин при 26 комнатной температуре, а затем туда добавляли все количество неочищенного 2-метокси-6 бромбензилбромида, полученного ранее, при той же температуре. Полученную смесь далее перемешивали в течение 2 ч для завершения реакции и реакционный раствор выливали в ледяную воду. Смесь в ледяной воде экстрагировали диэтиловым эфиром и полученный неводный слой промывали водой, сушили безводным сульфатом магния и затем концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле (элюент: бензол:этилацетат= 20:1 (по объему с получением целевого соединения в количестве 3,67 г. Температура плавления: 68-70 С. Пример 13. Получение 4,6-диметил-2 пиридинкарбоксиальдегид-O-[(2-метокси-6 этинилфенил)метил]оксима (соединение 235). 1,00 г (2,86 ммоль) 4,6-диметил-2 пиридинкарбоксиальдегид-O-[(2-метокси-6 бромфенил)метил]оксима растворяли в 20 мл триэтиламина. К полученному раствору последовательно добавляли 0,56 г (5,72 ммоль) триметилсилилацетилена, 0,2 г (0,29 ммоль) хлорида бис-трифенилфосфинпалладия(II) и 0,1 г(0,57 ммоль) йодида меди(I). Полученную смесь нагревали до достижения температуры дефлегмации, перемешивали в течение 2 ч для завершения реакции. Реакционный раствор концентрировали при пониженном давлении с получением реакционного продукта. Путем пропускания реакционного продукта через короткую хроматографическую колонку получали неочищенный 4,6-диметил-2-пиридинкарбоксиальдегид-О-[(2-метокси-6-триметилсилилэтинилфенил)метил]оксим в количестве 0,81 г. Неочищенный продукт затем растворяли в 10 мл этанола и затем добавляли 0,31 г карбоната калия при комнатной температуре. Смесь затем перемешивали в течение часа при той же температуре для завершения реакции. Реакционную смесь концентрировали при пониженном давлении,добавляли воду и затем экстрагировали диэтиловым эфиром. Полученный неводный слой промывали водой, сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением неочищенного продукта. Полученный неочищенный продукт очищали колоночной хроматографией на силикагеле(элюент: бензол:этилацетат = 20:1 (по объему с получением целевого соединения в количестве 0,15 г. Температура плавления: 116-118 С. 1,1 г (6,74 ммоль) N-гидроксифталимида растворяли в 20 мл безводного тетрагидрофурана. К полученному раствору последовательно добавляли 2,65 г (10,1 ммоль) трифенилфосфина, 2,0 г (10,1 ммоль) 2,4,6-триметоксибензилового спирта и 10 мл тетрагидрофуранового раствора, содержащего 1,76 г (10,1 ммоль) диэтилазодикарбоксилата при комнатной температуре. Полученную смесь перемешивали в течение одного часа при комнатной температуре и затем добавляли воду для последующего экстрагирования этилацетатом. Полученный неводный слой сушили безводным сульфатом магния и затем концентрировали при пониженном давлении с получением осадка. Полученный осадок отфильтровывали и промывали диэтиловым эфиром с получением целевого соединения в количестве 1,5 г. 1,5 г (4,37 ммоль) N-(2,4,6-триметоксибензилокси)фталимида растворяли в 50 мл метанола. К полученному раствору добавляли 0,24 г (4,81 ммоль) гидразингидрата при комнатной температуре. Полученную смесь перемешивали в течение часа при той же температуре для завершения реакции. Затем смесь концентрировали при пониженном давлении и затем последовательно добавляли воду и этилацетат, чтобы осадить примеси. После того как осажденные примеси удаляли фильтрованием, смесь экстрагировали этилацетатом. Полученный неводный слой промывали водой, сушили безводным сульфатом магния и концентрировали при пониженном давлении с получением целевого соединения в количестве 0,85 г. 28 уксусной кислоты, к полученному раствору добавляли 10 мл раствора в уксусной кислоте, содержащего ацетат натрия в количестве 0,3 г(3,62 ммоль), при комнатной температуре. К смеси затем добавляли 0,85 г (4,02 ммоль) 2,4,6 триметоксибензилоксиамина при той же температуре и затем перемешивали в течение часа для завершения реакции. Реакционную смесь концентрировали при пониженном давлении, добавляли воду и затем экстрагировали этилацетатом. Полученный неводный слой промывали водным раствором гидрокарбоната натрия и затем сушили безводным сульфатом магния. Осушенный слой концентрировали при пониженном давлении с получением неочищенного продукта. Неочищенный продукт затем очищали колоночной хроматографией (элюент: гексан:этилацетат = 7:3 (по объему с получением целевого соединения в количестве 0,05 г. Температура плавления: 125-127 С. Типичные примеры соединений в соответствии с данным изобретением, а также соединения, описанные в примерах, представлены в табл. 1. Дополнительно, в табл. 1 соединения, отмеченныев колонке "физические константы",являются соединениями, для которых представлены показатели их ЯМР под табл. 1 соответственно. Аббревиатуры в табл. 1 обозначают следующее: Me: метил, Et: этил, Pr: пропил, Bu: бутил, Ph: фенил, n: нормальный, i: изо и t: третичный. Таблица 1-1(с, 1 Н) Фунгицид. Теперь примеры данного изобретения будут разъяснены. Однако нужно отметить, что данное изобретение не ограничивается описанием в примерах, и может быть модифицировано разными способами воплощений в объеме, охватываемым предметом данного изобретения. Отметим, что термин "часть" в примере препа 34 рата, описанном далее, обозначает "массовую часть". Пример 15. Рецептура смачиваемого порошка. Соединение данного изобретения 40 частей Диатомовая земля 53 части Сульфат высшего спирта 4 части Алкилнафталинсульфонат 3 части Приведенные выше компоненты смешивают и распыляют в тонкодисперсные частицы с получением, таким образом, препарата смачиваемого порошка для соединения данного изобретения с содержанием 40% в расчете на активный ингредиент. Пример 16. Рецептура эмульгируемого концентрата. Соединение данного изобретения 30 частей Ксилол 33 части Диметилформамид 30 частей Полиоксиэтиленалкилаллильный эфир 7 частей Приведенные выше компоненты смешивают и готовят раствор с получением тем самым препарата эмульгируемого концентрата для соединения данного изобретения с содержанием 30% в расчете на активный ингредиент. Пример 17. Сильнодействующий препарат. Соединение данного изобретения 10 частей Тальк 89 частей Полиоксиэтиленалкилаллильный эфир 1 часть Вышеназванные компоненты смешивают и распыляют в тонкодисперсные частицы с получением тем самым сильнодействующего препарата для соединения данного изобретения с содержанием 10% в расчете на активный ингредиент. Пример 18. Гранулированный препарат. Соединение данного изобретения 5 частей Глина 73 части Бентонит 20 частей Диоктилсульфосукцината натриевая соль 1 часть Фосфат натрия 1 часть Вышеназванные компоненты смешивают и тщательно размалывают, добавляют воду, затем перемешивают и гранулируют и затем сушат с получением, таким образом, гранулированного препарата для соединения данного изобретения с содержанием 5% в расчете на активный ингредиент. Пример 19. Рецептура концентрированной суспензии. Соединение данного изобретения 10 частей Лигнинсульфонат натрия 4 части Додецилбензолсульфонат натрия 1 часть Ксантановая камедь 0,2 части Вода 84,8 части Вышеназванные компоненты смешивают и тщательно размалывают влажным размолом до размера частиц менее 1 мкм с получением, таким образом, концентрата суспензии для соеди 35 нения данного изобретения с содержанием 10% в расчете на активный ингредиент. Промышленное применение данного изобретения Теперь дается объяснение того, каким образом соединения данного изобретения являются эффективными в качестве активного ингредиента фунгицида для борьбы с различными болезнями растений с обращением к примерам испытаний, описанным далее. В примерах испытаний эффективность при борьбе с болезнью определяют визуальной проверкой состояния зараженности испытуемых растений во время наблюдения, а именно, путем контроля поражения растений-хозяев и состояния развития вызывающего заболевание грибка, проявляющегося на листьях, стеблях и т.д. испытуемых растений, по сравнению с контрольными растениями в испытаниях, которые являются здоровыми. Пример испытания 1. Испытание по борьбе с паршой яблонь (профилактическое применение). Эмульгируемый концентрат, приготовленный из соединения данного изобретения, разбавляли так, чтобы приготовить раствор в концентрации 200 ч./млн, и разбавленным раствором опрыскивали молодые яблоневые деревья(разновидность: Kokko, на стадии 3-4 листа),выращиваемые в неглазированных горшках. Распыленный раствор естественным образом высыхал, затем испытуемые яблони заражали конидиями грибка яблоневой парши (Venturiainaequalis). Зараженные яблоневые деревья помещали в комнату с температурой, поддерживаемой на уровне 20 С, и высокой влажностью при освещении, повторяющемся через 12 часовые интервалы, и яблоневые деревья оставляли в комнате на две недели. После этого срока производили оценку эффективности борьбы с заболеванием путем проверки степени заражения грибком на листьях по сравнению с контрольными деревьями. В результате показано,что соединения, имеющие следующие номера,обладают превосходным рабочим показателем по борьбе с болезнью, выше 75%. Заметим, что номера соединений в следующем ниже соответствуют тем же номерам соединений в табл. 1. Соединения 1, 3, 6, 8, 12, 14, 15, 20, 24,25, 26, 37, 48, 49, 194, 200, 207, 210, 231, 244. Пример испытания 2. Испытания по борьбе с серой плесневой гнилью обыкновенной фасоли. Цветы фасоли обыкновенной (разновидность: Nagauzura), выращенной в плоском сосуде для культивирования рассады, срезали и срезанные цветы погружали в раствор, приготовленный путем разбавления эмульгируемого концентрата, изготовленного из соединения данного изобретения, до концентрации 50 ч./млн из расчета на активный ингредиент. После погружения цветы сушили при комнатной температуре. Затем на цветы распыляли раствор 36 спор грибка серой плесневой гнили фасолевых стручков (Botrytis cinerea). Опрысканные спорами грибка серой плесневой гнили цветы помещали на листья, которые отделяли от здоровых растений фасоли обыкновенной и эти листья помещали в комнату с температурой, поддерживаемой на уровне 20 С, и высокой влажностью, с освещением, повторяющимся через 12-часовые интервалы, и листья фасоли обыкновенной выдерживали в комнате в течение 7 дней. Затем степень заражения грибком на листьях проверяли в сравнении с контрольными здоровыми листьями для определения эффективности борьбы с болезнью. В результате показано, что соединения со следующими номерами обладают превосходным действием по борьбе с болезнью. Заметим, что номера соединений в следующем ниже соответствуют тем же номерам соединений в табл. 1. Соединения 1, 3, 6, 7, 11, 12, 13, 14, 15,18, 20, 21, 22, 23, 25, 26, 27, 29, 36, 48, 49, 192,194, 195, 196, 198, 201, 203, 204, 207, 208, 209,210, 213, 216, 219, 220, 222, 223, 224, 225, 227,228, 229, 231, 233, 234, 235, 236, 237, 239, 240,242. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Оксимные О-эфирные соединения,представляемые общей формулой [I] где R1 представляет C1-6 алкил, С 3-6 циклоалкил,C1-6 алкокси, C1-6 алкилтио, амино, моно- или ди(С 1-6 алкил)амино, C1-6 ацилокси, C1-6 алкокси-С 1-6 алкил, C1-6 галогеналкил, гидрокси или атом галогена;m представляет целое число от 1 до 4, и когда m равно 2 или более, каждый из R1 может быть одинаковым или разным;R3 и R4 являются одинаковыми или разными, и каждый независимо представляет атом водорода или C1-6 алкил;R6 представляет C1-6 алкил, С 3-6 циклоалкил,С 2-6 алкенил, С 2-6 алкинил, C1-6 алкокси, C1-6 алкокси-C1-6 алкокси,C1-6 алкилкарбонилокси,C1-6 алкокси-C1-6 алкил, C1-6 галогеналкил, циано,нитро, амино, моно- или ди-(С 1-6 алкил)амино,C1-6 алкилкарбониламино, C1-6 алкилтио, гидрокси или атом галогена иn представляет целое число от 1 до 4, и когда n равно 2 или более, каждый из R6 может быть одинаковым или разным. 2. Оксимные эфирные соединения по п.1,представляемые общей формулой [I'] где R1, R2, R3, R4, R5, R6, m имеют значения, указанные выше. 3. Фунгицид для применения в земледелии и садоводстве, отличающийся тем, что содержит одно или более из оксимных эфирных соединений, представляемых общей формулой [I] где R1, R2, R3, R4, R5, R6, n и m имеют значения,указанные выше, или их соли в качестве активного ингредиента. 4. Фунгицид по п.3, отличающийся тем,что активный ингредиент является соединением, представляемым общей формулой [I']
МПК / Метки
МПК: C07D 213/44, A01N 43/40
Метки: садоводстве, соединения, оксимные, фунгициды, о-эфирные, земледелии, применения
Код ссылки
<a href="https://eas.patents.su/20-4574-oksimnye-o-efirnye-soedineniya-i-fungicidy-dlya-primeneniya-v-zemledelii-i-sadovodstve.html" rel="bookmark" title="База патентов Евразийского Союза">Оксимные о-эфирные соединения и фунгициды для применения в земледелии и садоводстве</a>
Предыдущий патент: Способы лечения женщин в постклимактерическом состоянии с применением ультранизких доз эстрогена
Следующий патент: Гербицидные эмульгируемые концентрированные композиции на основе динитроанилиновых и оксиацетамидных гербицидов
Случайный патент: Синергическая пребиотическая композиция и ее применение












