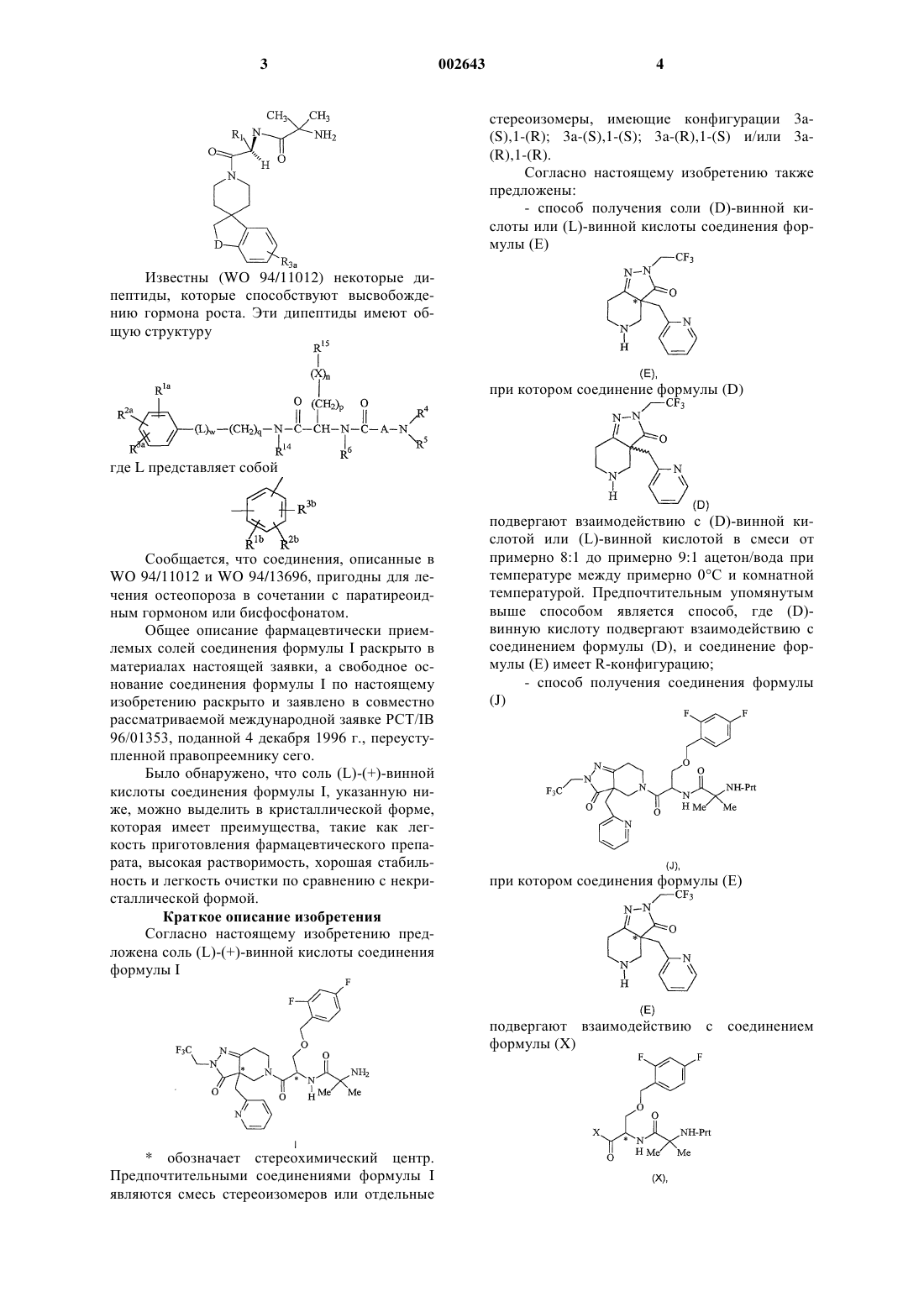
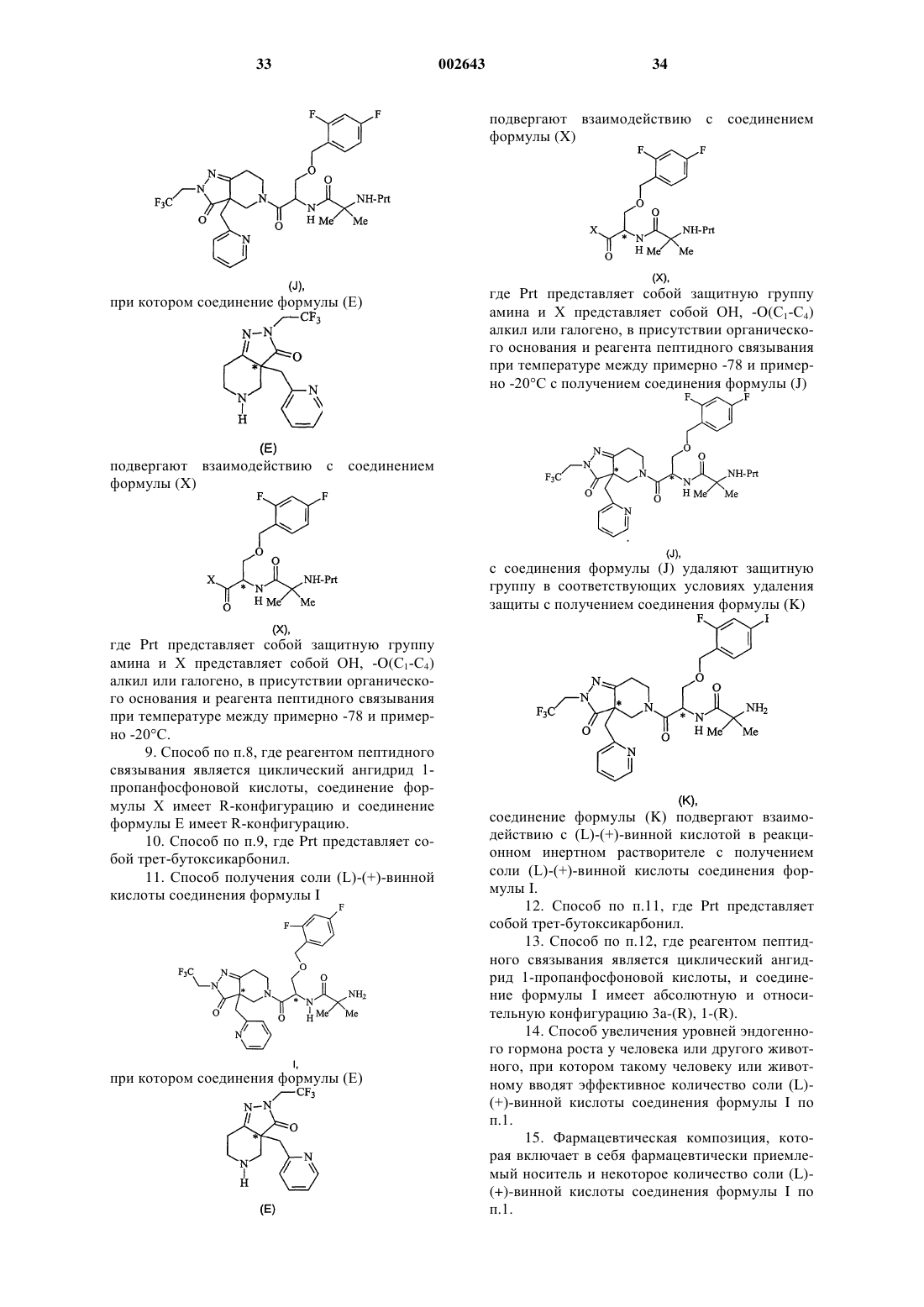
Тартрат замещенного дипептида как средство, стимулирующее секрецию гормона роста
Номер патента: 2643
Опубликовано: 29.08.2002
Авторы: Дасилва-Джардайн Пол Эндрю, Мерри Джерри Энтони, Карпайно Филип Алберт, Лефкер Брюс Аллен
Формула / Реферат
1. Соль (L)-(+)-винной кислоты соединения формулы I
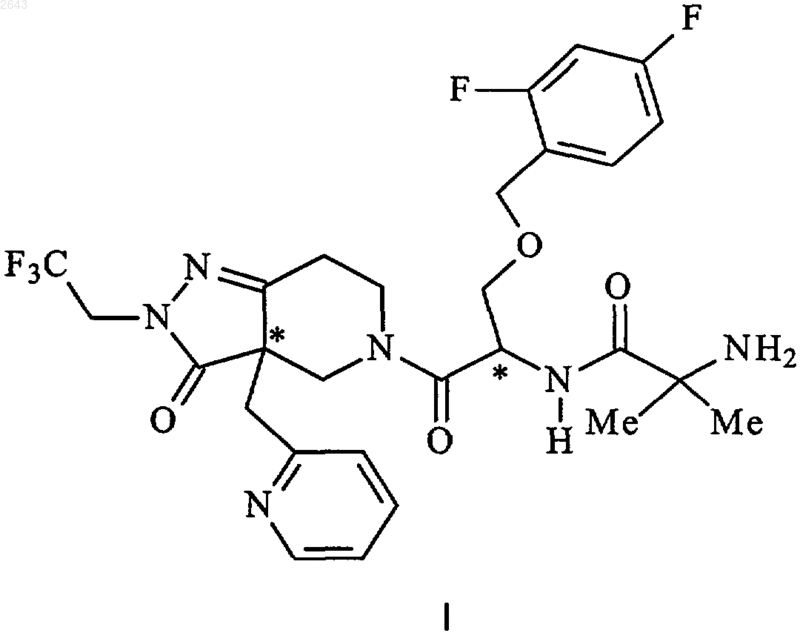
2. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-S, 1-R.
3. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-S, 1-S.
4. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-R, 1-S.
5. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-R, 1-R.
6. Способ получения соли (D)-винной кислоты или (L)-винной кислоты соединения формулы (Е)
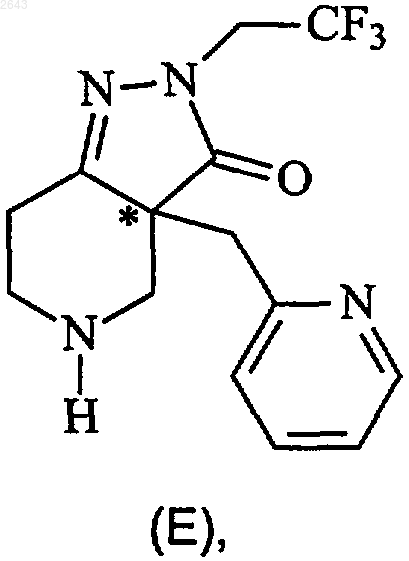
при котором соединение формулы (D)
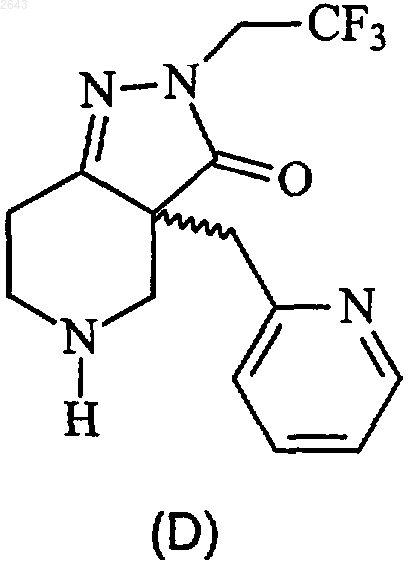
подвергают взаимодействию с (D)-винной кислотой или (L)-винной кислотой в смеси от примерно 8:1 до примерно 9:1 ацетон:вода при температуре между примерно 0шС и комнатной температурой.
7. Способ по п.6, где (D)-винную кислоту подвергают взаимодействию с соединением формулы (D) и соединение формулы (Е) имеет R-конфигурацию.
8. Способ получения соединения формулы (J)
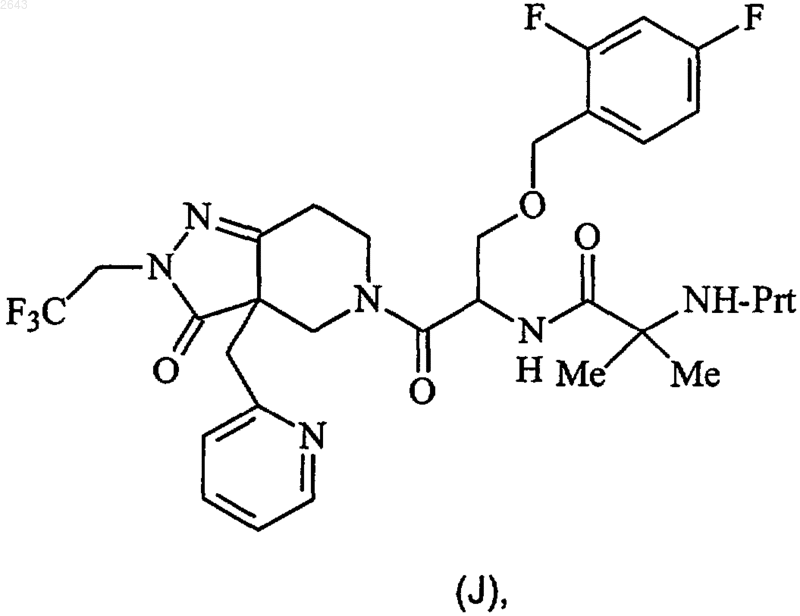
при котором соединение формулы (Е)

подвергают взаимодействию с соединением формулы (X)
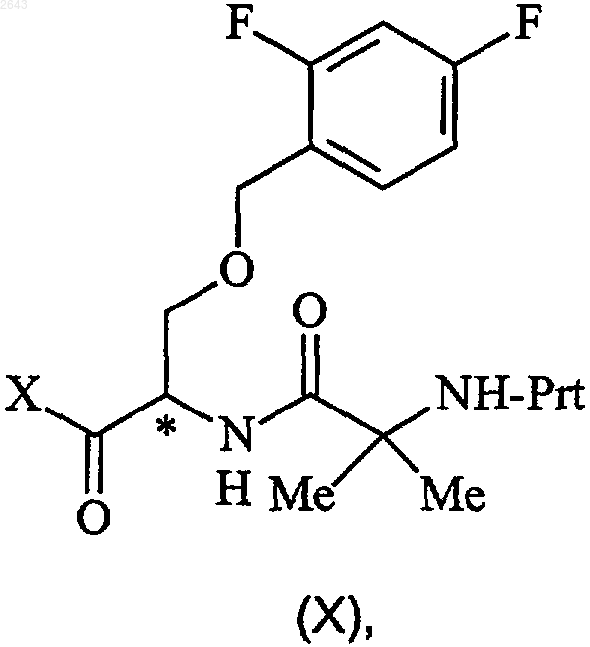
где Prt представляет собой защитную группу амина и Х представляет собой ОН, -O(С1-С4)алкил или галогено, в присутствии органического основания и реагента пептидного связывания при температуре между примерно -78 и примерно -20шС.
9. Способ по п.8, где реагентом пептидного связывания является циклический ангидрид 1-пропанфосфоновой кислоты, соединение формулы Х имеет R-конфигурацию и соединение формулы Е имеет R-конфигурацию.
10. Способ по п.9, где Prt представляет собой трет-бутоксикарбонил.
11. Способ получения соли (L)-(+)-винной кислоты соединения формулы I

при котором соединения формулы (Е)
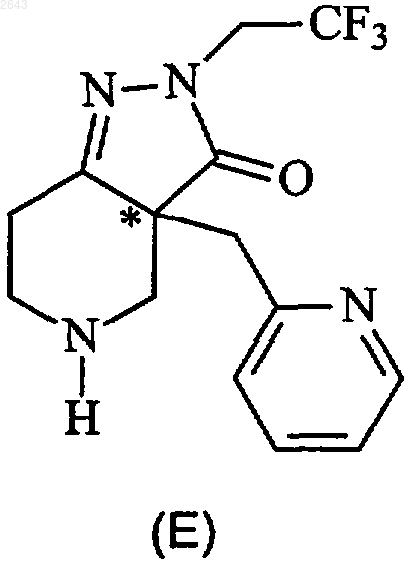
подвергают взаимодействию с соединением формулы (X)
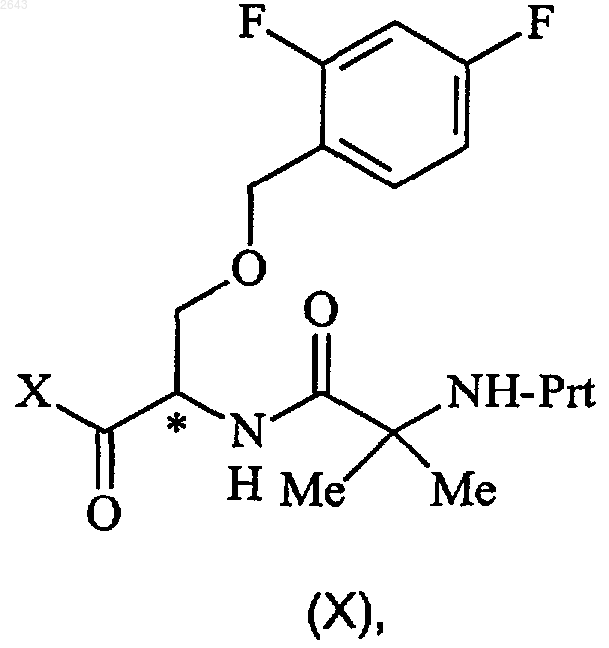
где Prt представляет собой защитную группу амина и Х представляет собой ОН, -O(С1-С4)алкил или галогено, в присутствии органического основания и реагента пептидного связывания при температуре между примерно -78 и примерно -20шС с получением соединения формулы (J)
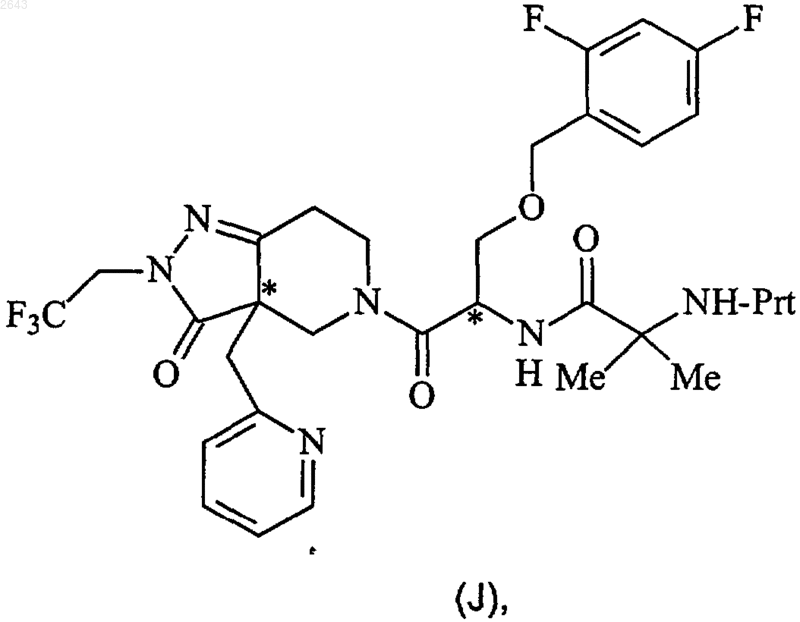
с соединения формулы (J) удаляют защитную группу в соответствующих условиях удаления защиты с получением соединения формулы (K)
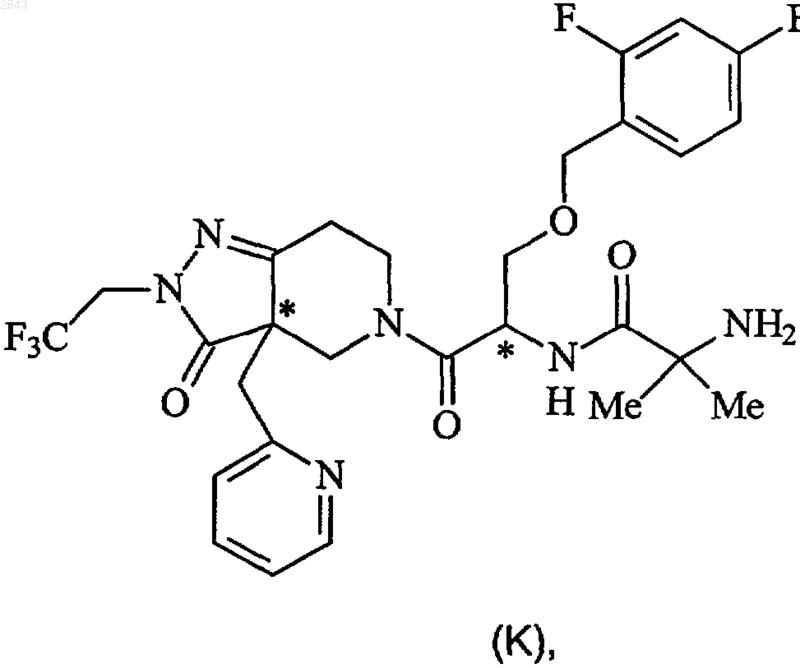
соединение формулы (K) подвергают взаимодействию с (L)-(+)-винной кислотой в реакционном инертном растворителе с получением соли (L)-(+)-винной кислоты соединения формулы I.
12. Способ по п.11, где Prt представляет собой трет-бутоксикарбонил.
13. Способ по п.12, где реагентом пептидного связывания является циклический ангидрид 1-пропанфосфоновой кислоты, и соединение формулы I имеет абсолютную и относительную конфигурацию 3a-(R), 1-(R).
14. Способ увеличения уровней эндогенного гормона роста у человека или другого животного, при котором такому человеку или животному вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1.
15. Фармацевтическая композиция, которая включает в себя фармацевтически приемлемый носитель и некоторое количество соли (L)-(+)-винной кислоты соединения формулы I по п.1.
16. Фармацевтическая композиция, пригодная для увеличения эндогенной выработки или высвобождения гормона роста у человека или другого животного, которая включает в себя фармацевтически приемлемый носитель, эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1 и средство, стимулирующее секрецию гормона роста, выбранное из группы, состоящей из рилизинг-пептида 6 гормона роста (GHRP-6), Hexarelin, рилизинг-пептида 1 гормона роста (GHRP-1), рилизинг-фактора гормона роста (GRF), инсулиноподобного фактора роста 1 (IGF-1), инсулиноподобного фактора роста 2 (IGF-2) и В-НТ920 или их аналога.
17. Способ лечения или предупреждения остеопороза, при котором человеку или другому животному, нуждающемуся в таком лечении или предупреждении, вводят количество соли (L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным при лечении или предупреждении остеопороза.
18. Способ лечения или предупреждения заболеваний или состояний, которые можно лечить или предупреждать посредством гормона роста, при котором человеку или другому животному, нуждающемуся в таком лечении или предупреждении, вводят количество соли (L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным для стимулирования высвобождения эндогенного гормона роста.
19. Способ по п.18, где заболеванием или состоянием является застойная сердечная недостаточность, ожирение или слабость, связанная со старением.
20. Способ по п.19, где заболеванием или состоянием является застойная сердечная недостаточность.
21. Способ по п.19, где заболеванием или состоянием является слабость, связанная со старением.
22. Способ ускорения восстановления кости после перелома, ослабления белкового катаболического ответа после тяжелой операции, уменьшения кахексии и потери белка вследствие хронического заболевания, ускорения заживления ран или ускорения выздоровления ожоговых пациентов или пациентов, подвергшихся тяжелой операции, при котором млекопитающему, нуждающемуся в таком лечении, вводят количество соли (L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным для стимулирования высвобождения эндогенного гормона роста.
23. Способ по п.22, где этот способ является способом ускорения выздоровления пациентов, подвергшихся тяжелой операции.
24. Способ по п.22, где этот способ является способом ускорения восстановления кости после перелома.
25. Способ увеличения мышечной силы, подвижности, поддержания толщины кожи, метаболического гомеостаза или ренального гомеостаза, при котором человеку или другому животному, нуждающемуся в таком лечении, вводят количество соли (L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным для стимулирования высвобождения эндогенного гормона роста.
26. Способ лечения или предупреждения остеопороза, при котором человеку или другому животному с остеопорозом вводят эффективные количества бисфосфонатного соединения и соли (L)-(+)-винной кислоты соединения формулы I по п.1.
27. Способ лечения остеопороза по п.26, где бисфосфонатным соединением является ибандронат.
28. Способ лечения остеопороза по п.26, где бисфосфонатным соединением является алендронат.
29. Способ увеличения уровней инсулиноподобного фактора роста 1 (IGF-1) у человека или другого животного с дефицитом IGF-1, при котором человеку или другому животному с дефицитом IGF-1 вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1.
30. Способ увеличения мышечной массы, при котором человеку или другому животному, нуждающемуся в таком лечении, вводят эффективное количество соли (1-)-(+)-винной кислоты соединения формулы I по п.1.
31. Способ стимулирования роста детей с дефицитом гормона роста, при котором ребенку с дефицитом гормона роста вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1.
32. Способ лечения инсулинрезистентности у млекопитающего, при котором указанному млекопитающему вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1.
33. Способ пю я.32, где состоянием, связанным с инсулинрезистентностью, является диабет типа I, диабет типа II, гипергликемия, нарушение толерантности к глюкозе или инсулинрезистентный синдром.
34. Способ по п.32, где состояние, связанное с инсулинрезистентностью, связано с ожирением или старостью.
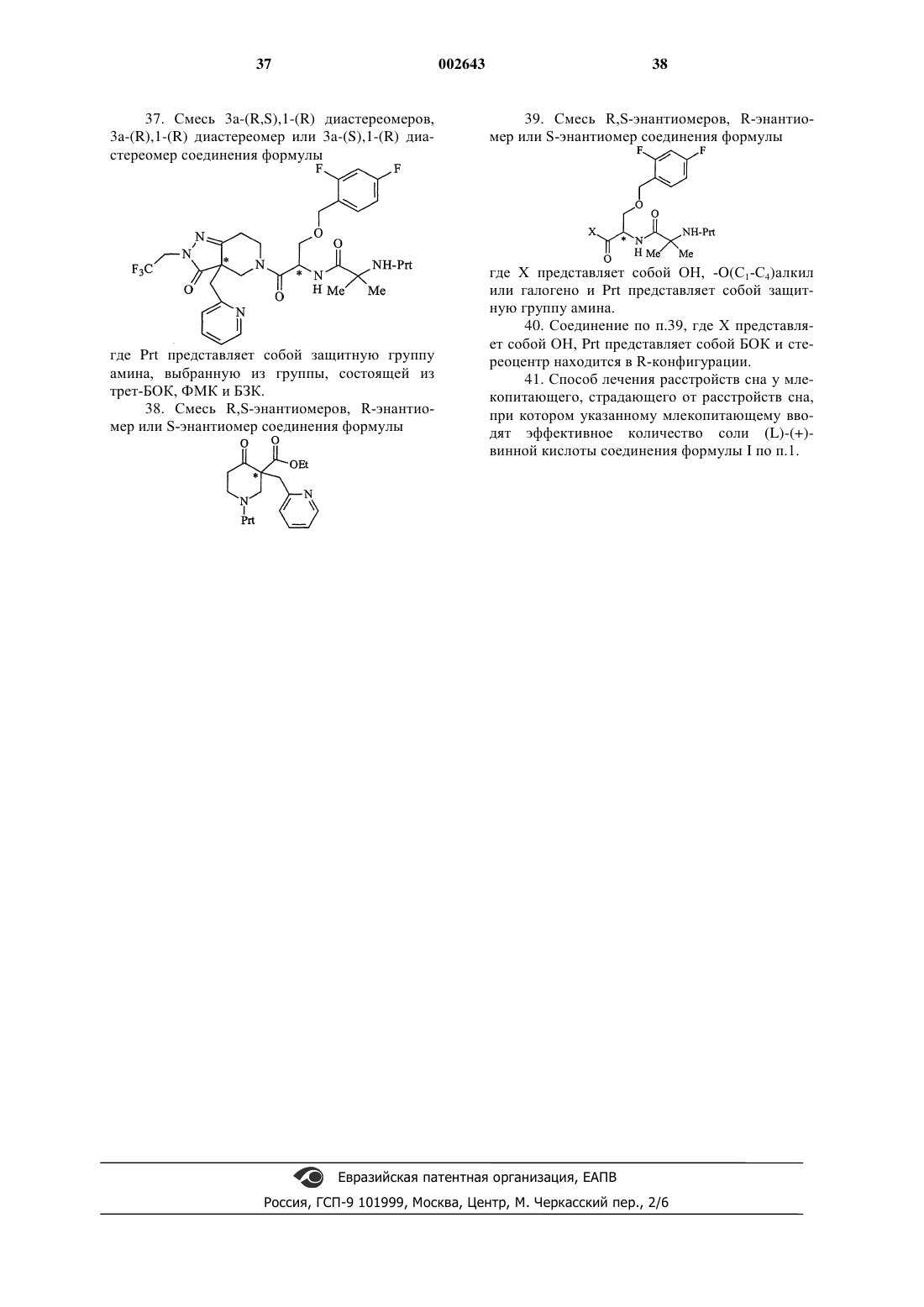
35. Смесь R,S-энантиомеров, R-энантиомер или S-энантиомер соединения формулы
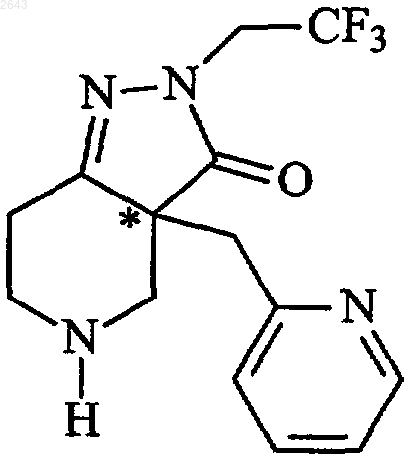
36. Соль (D)-винной кислоты или (L)-винной кислоты соединения по п.35.
37. Смесь 3a-(R.S),1-(R) диастереомеров, 3a-(R),1-(R) диастереомер или 3a-(S),1-(R) диастереомер соединения формулы
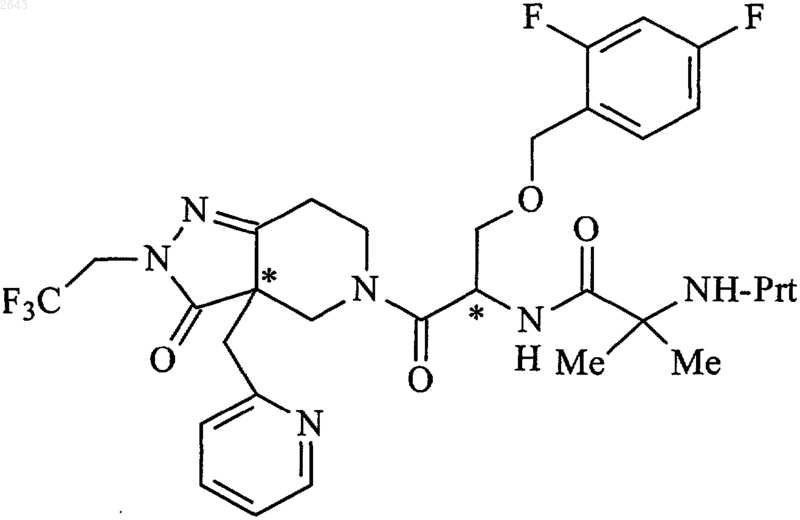
где Prt представляет собой защитную группу амина, выбранную из группы, состоящей из трет-БОК, ФМК и БЗК.
38. Смесь R,S-энантиомеров, R-энантиомер или S-энантиомер соединения формулы

39. Смесь R,S-энантиомеров, R-энантиомер или S-энантиомер соединения формулы
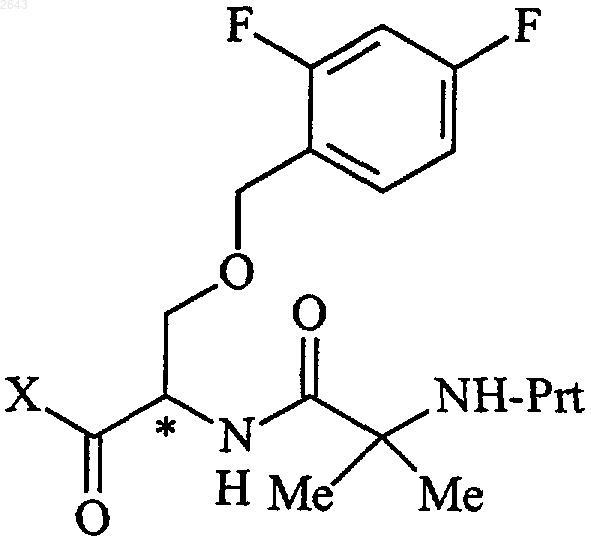
где X представляет собой ОН, -O(С1-С4)алкил или галогено и Prt представляет собой защитную группу амина.
40. Соединение по п.39, где Х представляет собой ОН, Prt представляет собой БОК и стереоцентр находится в R-конфигурации.
41. Способ лечения расстройств сна у млекопитающего, страдающего от расстройств сна, при котором указанному млекопитающему вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1.
Текст
1 Предпосылки изобретения Данное изобретение относится к соли(L)-(+)-винной кислоты 2-амино-N-1-(R)-(2,4 дифторбензилоксиметил)-2-оксо-2-[3-оксо-3 а(R)-пиридин-2-илметил-2-(2,2,2-трифторэтил)2,3,3 а,4,6,7-гексагидропиразоло[4,3-с]пиридин 5-ил]этил-2-метилпропионамида,которая представляет собой средство, стимулирующее секрецию гормона роста. Гормон роста (ГР), который секретируется из гипофиза, стимулирует рост всех тканей организма, которые являются способными к росту. Кроме того, известно, что гормон роста обладает следующими основными эффектами на процессы метаболизма человека: 1) повышенная скорость синтеза белков,по существу, во всех клетках организма; 2) пониженная скорость утилизации углеводов в клетках организма; и 3) повышенная мобилизация свободных жирных кислот и использование жирных кислот для энергии. Недостаток гормона роста приводит к множеству медицинских расстройств. У детей он является причиной карликовости. У взрослых последствия приобретенного дефицита гормона роста включают в себя основательное уменьшение нежировой массы тела и сопутствующее увеличение суммарной жировой ткани человека, особенно в области туловища. Уменьшенная скелетная и сердечная мышечная масса и мышечная сила приводят к значительному снижению способности выполнять физические упражнения. Плотность кости также понижается. Показано, что введение экзогенного гормона роста поворачивает многие метаболические изменения в обратном направлении. Дополнительные преимущества терапии включают в себя уменьшение холестерина липопротеина низкой плотности и улучшали психологическое здоровье. В случаях, когда требуются повышенные уровни гормона роста, проблему обычно решают, давая экзогенный гормон роста или вводя агент, который стимулирует выработку и/или высвобождение гормона роста. В любом случае пептидильная природа соединения делает необходимым введение этого соединения путем инъекции. Первоначально источником гормона роста была экстракция гипофиза трупов. Это приводило к получению дорогого продукта и сопровождалось риском, что болезнь, связанная с источником гипофиза, может быть передана реципиенту гормона роста (например, болезнь Якоба-Крейтцфельдта). Недавно стал доступным рекомбинантный гормон роста, который,хотя больше и не сопровождается никаким риском переноса болезни, все еще является очень дорогим продуктом, который следует вводить путем инъекции или в виде аэрозоля через нос. Причиной наибольшего дефицита ГР является нарушение высвобождения ГР, а не пер 002643 2 вичные нарушения гипофизарного синтеза ГР. Следовательно, альтернативной концепцией для нормализации сывороточных уровней ГР является концепция, в основе которой лежит стимулирование или ингибирование различных систем нейромедиаторов в головном мозге и гипоталамусе. В результате продолжается создание синтетических высвобождающих гормон роста агентов для стимулирования гипофизарной секреции ГР, и их создание может иметь некоторые преимущества перед дорогой и неудобной ГРзаместительной терапией. Действуя по физиологическим проводящим путям, наиболее желательные агенты могут стимулировать пульсирующую секрецию ГР, а чрезмерные уровни ГР,которые ассоциированы с нежелательными побочными эффектами экзогенного введения ГР,могут быть исключены в силу неповрежденных нервных узлов отрицательной обратной связи. Физиологические и фармакологические стимуляторы секреции ГР включают в себя аргинин,L-3,4-дигидроксифенилаланин(LДОФА), глюкагон, вазопрессин, а гипогликемия, вызванная инсулином, также как и деятельность, такая как сон и физкультура, косвенно вызывают высвобождение гормона роста из гипофиза, воздействуя некоторым образом на гипоталамус, возможно либо чтобы уменьшить секрецию соматостатина, либо чтобы увеличить секрецию известного средства, стимулирующего секрецию рилизинг-фактора гормона роста(GHRF), или неизвестного эндогенного рилизинг-гормона гормона роста, или всех их. Данное изобретение также относится к способу лечения инсулинрезистентных состояний, таких как инсулиннезависимый сахарный диабет (ИНСД) и пониженный гликемический контроль, связанный с ожирением или старостью, у млекопитающего, нуждающемуся в этом,при котором указанному млекопитающему вводят эффективное количество (L)-(+)-тартрата соединения формулы I, указанного ниже. Были разработаны другие соединения, которые стимулируют высвобождение эндогенного гормона роста, такие как аналогичные пептидильные соединения, родственные GHRF или пептидам (патент США 4411890). Эти пептиды,хотя и значительно меньше, чем гормоны роста,все же чувствительны к разным протеазам. Как у большинства пептидов, их потенциал в отношении пероральной биодоступности является низким. Известны (WO 94/13696) некоторые спиропиперидины и гомологи, которые способствуют высвобождению гормона роста. Предпочтительные соединения являются соединениями общей структуры, указанной ниже. 4 стереоизомеры, имеющие конфигурации 3a(S),1-(R); 3a-(S),1-(S); 3a-(R),1-(S) и/или 3a(R),1-(R). Согласно настоящему изобретению также предложены:- способ получения соли (D)-винной кислоты или (L)-винной кислоты соединения формулы (Е) Известны (WO 94/11012) некоторые дипептиды, которые способствуют высвобождению гормона роста. Эти дипептиды имеют общую структуру при котором соединение формулы (D)WO 94/11012 и WO 94/13696, пригодны для лечения остеопороза в сочетании с паратиреоидным гормоном или бисфосфонатом. Общее описание фармацевтически приемлемых солей соединения формулы I раскрыто в материалах настоящей заявки, а свободное основание соединения формулы I по настоящему изобретению раскрыто и заявлено в совместно рассматриваемой международной заявке РСТ/IВ 96/01353, поданной 4 декабря 1996 г., переуступленной правопреемнику сего. Было обнаружено, что соль (L)-(+)-винной кислоты соединения формулы I, указанную ниже, можно выделить в кристаллической форме,которая имеет преимущества, такие как легкость приготовления фармацевтического препарата, высокая растворимость, хорошая стабильность и легкость очистки по сравнению с некристаллической формой. Краткое описание изобретения Согласно настоящему изобретению предложена соль (L)-(+)-винной кислоты соединения формулы I подвергают взаимодействию с (D)-винной кислотой или (L)-винной кислотой в смеси от примерно 8:1 до примерно 9:1 ацетон/вода при температуре между примерно 0 С и комнатной температурой. Предпочтительным упомянутым выше способом является способ, где (D)винную кислоту подвергают взаимодействию с соединением формулы (D), и соединение формулы (Е) имеет R-конфигурацию;- способ получения соединения формулы при котором соединения формулы (Е) обозначает стереохимический центр. Предпочтительными соединениями формулы I являются смесь стереоизомеров или отдельные 5 где Prt представляет собой защитную группа амина, и Х представляет собой ОН, -O(С 1 С 4)алкил или галогено, в присутствии органического основания и реагента пептидного связывания при температуре между примерно -78 и примерно -20 С. Предпочтительным способом упомянутого непосредственно выше способа является способ, где реагентом пептидного связывания является циклический ангидрид 1 пропанфосфоновой кислоты, соединение формулы Х имеет R-конфигурацию, и соединение формулы Е имеет R-конфигурацию. Еще более предпочтительным является упомянутый непосредственно выше способ, где Prt представляет собой трет-бутоксикарбонил; и- способ получения соли (L)-(+)-винной кислоты соединения формулы I при котором соединения формулы (Е) где Prt представляет собой защитную группу амина, и Х представляет собой ОН, -O(С 1 С 4)алкил или галогено, в присутствии органического основания и реагента пептидного связывания при температуре между примерно -78 и примерно -20 С с получением соединения формулы (J) 6 с соединения формулы (J) удаляют защиту в соответствующих условиях удаления защиты с получением соединения формулы (К) соединение формулы (К) подвергают взаимодействию с (L)-(+)-винной кислотой в реакционном инертном растворителе с получением соли (L)-(+)-винной кислоты соединения формулы I. Предпочтительным упомянутым непосредственно выше способом является способ,где Prt представляет собой трет-бутоксикарбонил (БОК), еще более предпочтительным упомянутым непосредственно выше способом является способ, где реагентом пептидного связывания является циклический ангидрид 1 пропанфосфоновой кислоты, и соединение формулы I имеет абсолютную и относительную конфигурацию 3 а-(R),1-(R). В другом аспекте данного изобретения предложены где предпочтительной является соль (D)-винной кислоты или (L)-винной кислоты; где Prt представляет собой защитную группу амина, выбранную из группы, состоящей из трет-БОК,флуоренилметоксикарбонила где X представляет собой ОН, -O(С 1-С 4)алкил или галогено, и Prt представляет собой защитную группу амина; и предпочтительным является, если Х представляет собой ОН, Prt представляет собой БОК, а стереоцентр находится в Rконфигурации. В еще одном аспекте данного изобретения предложены (где соединение формулы (I) показано выше) способы увеличения уровней эндогенного гормона роста у человека или другого животного, при которых такому человеку или животному вводят эффективное количество соли (L)-(+)винной кислоты соединения формулы I; фармацевтические композиции, которые включают в себя фармацевтически приемлемый носитель и некоторое количество соли (L)-(+)винной кислоты соединения формулы I; фармацевтические композиции, пригодные для увеличения эндогенной выработки или высвобождения гормона роста у человека или другого животного, которые включают в себя фармацевтически приемлемый носитель, эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1 и средство, стимулирующее секрецию гормона роста, выбранное из группы, состоящей из рилизинг-пептида 6 гормона роста (GHRP-6), Hexarelin, рилизингпептида 1 гормона роста (GHRP-1), рилизингфактора гормона роста (GRF), инсулиноподобного фактора роста 1 (IGF-1), инсулиноподобного фактора роста 2 (IGF-2) и В-НТ 920 или их аналога; способы лечения или предупреждения остеопороза, при которых человеку или другому животному, нуждающемуся в таком лечении или предупреждении, вводят количество соли(L)-(+)-винной кислоты соединения формулы I,которое является эффективным при лечении или предупреждении остеопороза; способы лечения или предупреждения заболеваний или состояний, которые можно лечить или предупреждать посредством гормона роста, при которых человеку или другому животному, нуждающемуся в таком лечении или предупреждении, вводят количество соли (L)(+)-винной кислоты соединения формулы I, ко 002643 8 торое является эффективным для стимулирования высвобождения эндогенного гормона роста; предпочтительным является способ, где заболеванием или состоянием является застойная сердечная недостаточность, ожирение или слабость, связанная со старением; также предпочтительным является способ, где заболеванием или состоянием является застойная сердечная недостаточность; кроме того, предпочтительным является способ, где заболеванием или состоянием является слабость, связанная со старением; способы ускорения восстановления кости после перелома, ослабления белкового катаболического ответа после тяжелой операции,уменьшения кахексии и потери белка вследствие хронического заболевания, ускорения заживления ран или ускорения выздоровления ожоговых пациентов или пациентов, подвергшихся тяжелой операции, при которых млекопитающему, нуждающемуся в таком лечении,вводят количество соли (L)-(+)-винной кислоты соединения формулы I, которое является эффективным для стимулирования высвобождения эндогенного гормона роста; предпочтительным является способ ускорения выздоровления пациентов, подвергшихся тяжелой операции; также предпочтительным является способ ускорения восстановления кости после перелома; способы увеличения мышечной силы, подвижности, поддержания толщины кожи, метаболического гомеостаза или ренального гомеостаза, при которых человеку или другому животному, нуждающемуся в таком лечении, вводят количество соли (L)-(+)-винной кислоты соединения формулы I, которое является эффективным для стимулирования высвобождения эндогенного гормона роста; способы лечения или предупреждения остеопороза, при которых человеку или другому животному с остеопорозом, вводят эффективные количества бисфосфонатного соединения и соли (L)-(+)-винной кислоты соединения формулы I; предпочтительным способом лечения остеопороза является способ, где бисфосфонатным соединением является ибандронат; предпочтительным способом лечения остеопороза является способ, где бисфосфонатным соединением является алендронат; способы лечения или предупреждения остеопороза, при которых человеку или другому животному с остеопорозом вводят эффективные количества эстрогена или премарина и соли (L)-(+)-винной кислоты соединения формулы I и, возможно,прогестерона; способы лечения остеопороза, при которых человеку или другому животному с остеопорозом вводят эффективные количества кальцитонина и соли (L)-(+)-винной кислоты соединения формулы I; способы увеличения уровней IGF-1 у человека или другого животного с дефицитом IGF-1, 9 при которых человеку или другому животному с дефицитом IGF-1 вводят эффективное количество (L)-(+)-винной кислоты соли соединения формулы I; способы лечения остеопороза, при которых человеку или другому животному с остеопорозом вводят эффективные количества агониста или антагониста эстрогена и соли (L)-(+)винной кислоты соединения формулы I; предпочтительным является способ, где агонистом или антагонистом эстрогена является тамоксифен, дролоксифен, ралоксифен или идоксифен; также предпочтительным является способ, где агонистом или антагонистом эстрогена является цис-6-(4-фторфенил)-5-[4-(2-пиперидин-1 илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол;(-)-цис-6-фенил-5-[4-(2 пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол; цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол; цис-1-[6'-пирролидиноэтокси-3'пиридил]-2-фенил-6-гидрокси-1,2,3,4-тетрагидронафталин; 1-(4'-пирролидиноэтоксифенил)-2(4"-фторфенил)-6-гидрокси-1,2,3,4-тетрагидроизохинолин; цис-6-(4-гидроксифенил)-5-[4-(2 пиперидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол; или 1-(4'-пирролидинолэтоксифенил)-2-фенил-6-гидрокси-1,2,3,4-тетрагидроизохинолин; способы увеличения мышечной массы, при которых человеку или другому животному, которым требуется такое лечение, вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I; способы стимулирования роста детей с дефицитом гормона роста, при которых ребенку с дефицитом гормона роста вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I; способы лечения инсулинрезистентности у млекопитающего, при которых указанному млекопитающему вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I; предпочтительным является способ, где состоянием, связанным с инсулинрезистентностью, является диабет типа I, диабет типа II,гипергликемия, нарушение толерантности к глюкозе или инсулинрезистентный синдром; также предпочтительным является способ, где состояние, связанное с инсулинрезистентностью, связано с ожирением или старостью; способы увеличения уровней эндогенного гормона роста, при которых человеку или другому животному, нуждающемуся в этом, вводят эффективные количества функционального антагониста соматостатина и соли (L)-(+)-винной кислоты соединения формулы I; предпочтительным является способ, где функциональным антагонистом соматостатина является альфа-2 адренергический агонист; и способы лечения или предупреждения застойной сердечной недостаточности, ожирения 10 или слабости, связанной со старением, при которых человеку или другому животному, нуждающемуся в этом, вводят эффективные количества функционального антагониста соматостатина и соли (L)-(+)-винной кислоты соединения формулы I. Настоящее соединение формулы (I) стимулирует высвобождение гормона роста, является стабильным в разных физиологических условиях и его можно вводить парентерально, через нос или пероральным путем. Подробное описание изобретения Соль (L)-(+)-винной кислоты соединения формулы I может быть получена следующими ниже способами, которые включают в себя способы получения соединений, известные в химии. Некоторые способы получения соли (L)(+)-винной кислоты соединения формулы I предложены в качестве дополнительных признаков данного изобретения и представлены на схеме реакций, приведенной ниже. Соединение по настоящему изобретению имеет абсолютную и относительную конфигурацию, показанную ниже которую обозначают как 3a-(R),1-(R)-конфигурацию. Она может быть получена способом,описанным ниже. Высвобождающая гормон роста соль (L)(+)-винной кислоты соединения формулы I пригодна in vitro в качестве уникального средства для того, чтобы понять, как на гипофизарном уровне регулируется секреция гормона роста. Это включает в себя оценку влияния многих факторов, предполагаемых и известных, на секрецию гормона роста, таких как возраст, пол,питание, глюкоза, аминокислоты, жирные кислоты, а также состояния голодания и не голодания. Кроме того, соль (L)-(+)-винной кислоты соединения формулы I можно использовать для оценки того, как другие гормоны изменяют активность высвобождения гормона роста. Например, уже было установлено, что соматостатин ингибирует высвобождение гормона роста. Соль (L)-(+)-винной кислоты соединения формулы I можно вводить животным, в том числе человеку, для высвобождения гормона роста in vivo. Соль (L)-(+)-винной кислоты соединения формулы I пригодна для лечения симптомов, связанных с дефицитом ГР; для стимулирования роста или увеличения эффективности кормления животных, которых выращивают на мясо, для улучшения качества туши; для увели 11 чения надоев молока у молочного скота; для улучшения заживления костей или ран и для улучшения функции жизненно важных органов. Индуцируя секрецию эндогенного ГР, соль (L)(+)-винной кислоты соединения формулы I будет изменять состав тела и модифицировать другие ГР-зависимые метаболические процессы,иммунологические процессы и процессы, связанные с развитием организма. Например, соединения по настоящему изобретению можно давать цыплятам, индейкам, домашнему скоту(такому как овцы, свиньи, лошади, крупный рогатый скот и т.д.), животным-компаньонам(например, собакам) или можно использовать при разведении рыб для ускорения их роста и улучшения соотношения белок/жир. Кроме того, соль (L)-(+)-винной кислоты соединения формулы I можно вводить человеку in vivo в качестве диагностического средства для непосредственного определения способности гипофиза высвобождать гормон роста. Например,соль (L)-(+)-винной кислоты соединения формулы I можно вводить in vivo детям. Образцы сыворотки, взятые перед и после такого введения, могут быть проанализированы на гормон роста. Сравнение количеств гормона роста в каждом из таких образцов будет способом для непосредственного определения способности гипофиза пациента высвобождать гормон роста. Соответственно, настоящее изобретение охватывает в своем объеме фармацевтические композиции, содержащие в качестве активного ингредиента соль (L)-(+)-винной кислоты соединения формулы I в сочетании с фармацевтически приемлемым носителем. Возможно, что фармацевтические композиции, кроме того, могут содержать анаболический агент в дополнение к соли (L)-(+)-винной кислоты соединения формулы I или другое соединение, которое проявляет другую активность, например, антибиотический стимулятор роста или агент для лечения остеопороза, или другие фармацевтически активные материалы, причем такая комбинация повышает эффективность и минимизирует побочные эффекты. Агенты, стимулирующие рост, и анаболические агенты хорошо известны и включают в себя, но не ограничиваются ими, рилизинггормон тиреотропина (TRH), паратиреоидный гормон (РТН), диэтилстильбэстерол, эстрогены,-агонисты, теофиллин, анаболические стероиды, энкефалины, простагландины серии Е, соединения, раскрытые в патенте США 3239345,раскрытие которого приводится в настоящем описании посредством ссылки, например зеранол, соединения, раскрытые в патенте США 4036979, раскрытие которого приводится в настоящем описании посредством ссылки, например сульбенокс, и пептиды, раскрытые в патенте США 4411890, раскрытие которого приводится в настоящем описании посредством ссылки. 12 Соль (L)-(+)-винной кислоты соединения формулы I в комбинации с другими средствами,стимулирующими секрецию гормона роста, такими как рилизинг-петиды гормона ростаGHRP-6 и GHRP-1 (патент США 4411890, раскрытие которого приводится в настоящем описании посредством ссылки, и WO 89/07110 и(GHRH, также обозначаемый как GRF) и его аналоги, или в комбинации с гормоном роста и его аналогами, или соматомединами, в том числе IGF-1 и IGF-2, или адренергическими агонистами, такими как клонидин, ксилазин, детомидин и медетомидин (клонидин раскрыт в патенте США 3202660, раскрытие которого приводится в настоящем описании посредством ссылки, ксилазин раскрыт в патенте США 3235550,раскрытие которого приводится в настоящем описании посредством ссылки, а медетомидин раскрыт в патенте США 4544664, раскрытие которого приводится в настоящем описании посредством ссылки), или агонистами серотонина 5HTID, такими как сумитриптан, или агентами, которые ингибируют соматостатин или его высвобождение, такими как физостигмин и пиридостигмин, пригодна для увеличения эндогенных уровней ГР у млекопитающих. Комбинация соли (L)-(+)-винной кислоты соединения формулы I с GRF приводит к синергическим увеличениям эндогенного гормона роста. Как известно квалифицированным специалистам, известные и возможные применения гормона роста являются разнообразными и многочисленными ["Human Growth Hormone", Strobel and Thomas, Pharmacological Reviews, 46, pg. 1-34 (1994); Т. Rosen et al., Horm Res, 1995; 43:RM. Frieboes et al., Neuroendocrinology, (1995),61(5), pp. 584-589; и M. Llovera et al., Int. J. Cancer, (1995), 61(1), pp. 138-141]. Так, введение соли (L)-(+)-винной кислоты соединения формулы I с целью стимулировать высвобождение эндогенного гормона роста может иметь те же самые эффекты или применения, как и самого гормона роста. Эти разнообразные применения гормона роста можно суммировать следующим образом: стимулирование высвобождения гормона роста у пожилых людей; лечение взрослых людей с дефицитом гормона роста; предупреждение катаболических побочных эффектов глюкокортикоидов; лечение остеопороза; стимули 13 рование иммунной системы; ускорение заживления ран; ускорение восстановления кости после перелома; лечение задержки роста; лечение застойной сердечной недостаточности, как оно раскрыто в РСТ публикациях WO 95/28173 иWO 95/28174 (пример способа анализа эффективности средств, стимулирующих секрецию гормона роста, при лечении застойной сердечной недостаточности описан R. Yang et al. в Circulation, Vol. 92, No. 2, р. 262, 1995); лечение острой или хронической почечной недостаточности; лечение физиологически низкого роста, в том числе детей с дефицитом гормона роста; лечение низкого роста, связанного с хроническим заболеванием; лечение ожирения; лечение задержки роста, связанной с синдромом Прадера-Вилли и синдромом Трнера; ускорение выздоровления и сокращение срока госпитализации ожоговых пациентов или пациентов после тяжелой операции, такой как желудочнокишечная операция; лечение задержки внутриматочного роста, скелетной дисплазии, гиперкортицизма и синдрома Кушинга; восстановление гормона роста у пациентов в состоянии стресса; лечение остеохондродисплазий, синдрома Нунан, расстройств сна, болезни Альцгеймера, медленного заживления ран и социально-психологической депривации; лечение легочной дисфункции и дыхательной зависимости; ослабления белкового катаболического ответа после тяжелой операции; лечение синдромов мальабсорбции; уменьшение кахексии и потери белка вследствие хронического заболевания, такого как рак или СПИД; ускорение похудения и прироста белка у пациентов на полном парентеральном питании (ППП); лечение гиперинсулинемии, в том числе незидиобластоза; лечение адъювантом для индукции овуляции и для предупреждения и лечения язвы желудка и дуоденальной язвы; стимулирование тимусного развития и предупреждение ухудшения функции тимуса, связанного с возрастом; дополнительная терапия пациентов при постоянном гемодиализе; лечение пациентов с подавленной иммунной системой и усиление ответной реакции антител после вакцинации; увеличение мышечной силы, увеличение мышечной массы, подвижности, поддержание толщины кожи, метаболического гомеостаза, ренального гомеостаза у болезненных пожилых людей; стимулирование остеобластов, ремоделирования кости и роста хрящей; лечение неврологических заболеваний, таких как периферическая невропатия и невропатия, вызванная лекарственными средствами, синдром Гийена-Барре,боковой амиотрофический склероз, рассеянный склероз, цереброваскулярные случаи и демиелинизирующие болезни; стимулирование иммунной системы животных-компаньонов и лечение старческих расстройств у животныхкомпаньонов; активация роста домашнего скота; и стимулирование роста шерсти овец. 14 Квалифицированным специалистам известно, что в настоящее время существуют многочисленные соединения, которые в настоящее время используют, пытаясь лечить заболевания или терапевтические симптомы, перечисленные выше. Комбинации этих терапевтических агентов, некоторые из которых также упомянуты выше, со стимулятором роста, проявляют анаболические и желательные свойства этих многочисленных анаболических агентов. В этих комбинациях терапевтические агенты и соль(L)-(+)-винной кислоты соединения формулы I можно вводить независимо и последовательно или совместно в пределах доз от одной сотой до однократных уровней доз, которые являются эффективными, когда эти соединения и средства, стимулирующие секрецию, применяют отдельно. Комбинированную терапию для лечения резорбции кости, предупреждения остеопороза,ослабления скелетного разрушения, усиления заживления переломов костей, стимулирования образования кости и увеличения минеральной плотности кости можно осуществлять посредством комбинаций бис-фосфонатов и соли (L)-(+)винной кислоты соединения формулы I. Комбинированная терапия с использованием бисфосфонатов и средств, стимулирующих секрецию ГР, известна [РСТ публикация WO 95/11029]. Обзор по применению бисфосфонатов для этих целей был опубликован вHamdy, N.A.T., Role of Bisphosphonates in Metabolic Bone Diseases, Trends in Endocrinol. Metab.,1993, 4, pages 19-25. Бис-фосфонаты для этих целей включают в себя, но не ограничиваются ими, алендронат, тилудронат, диметил-APD,ризедронат, этидронат, YM-175, клодронат, памидронат и ВМ-210995 (ибандронат). В соответствии с их потенциалом действия, для достижения эффективного лечения остеопороза пациентам вводят суточные пероральные уровни доз бис-фосфоната между 0,1 мг и 5 г и суточные уровни доз соли (L)-(+)-винной кислоты соединения формулы I между 0,01 и 20 мг/кг веса тела. Соль (L)-(+)-винной кислоты соединения формулы I может быть объединена с агонистом/антагонистом эстрогена млекопитающего. Любой агонист/антагонист эстрогена можно использовать в качестве второго соединения по данному изобретению. Термин агонист/антагонист эстрогена относится к соединениям, которые связывают рецептор эстрогена, ингибируют обновление кости и предупреждают потерю кости. В частности, агонисты эстрогена в этом описании определены как химические соединения, которые способны связываться с сайтами рецептора эстрогена в ткани млекопитающего и имитировать действия эстрогена в одной или более чем одной ткани. Антагонисты эстрогена в этом описании определены как химические соединения, которые способны связываться с сайтами рецептора эстрогена в ткани мле 15 копитающего и блокировать воздействия эстрогена в одной или более чем одной ткани. Квалифицированные специалисты легко определяют такие активности по данным стандартных анализов, включая анализы связывания с рецептором эстрогена, стандартными костными гистоморфометрическими и денситометрическими способами (Eriksen E.F. et. al, Bone Histomorphometry, Raven Press, New York, 1994, pages 174; Grier S.J. et. al., The Use of Dual-Energy XRay Absorptiometry In Animals, Inv. Radiol.,1996, 31(1):50-62; Wahner H.W. and Fogelman I.,The Evaluaton of Osteoporosis: Dual-Energy XRay Absorptiometry in Clinical Practice., MartinDunitz Ltd., London 1994, pages 1-296). Многие из этих соединений описаны и упомянуты ниже,однако, квалифицированным специалистам могут быть известны другие агонисты/антагонисты эстрогена. Предпочтительным агонистом/антагонистом эстрогена является дролоксифен: (фенол, 3-[1-[4-[2-(диметиламино)этокси]фенил]-2-фенил-1-бутенил]-, (Е)-) и родственные соединения (патент США 504743, раскрытие которого приводится в настоящем описании посредством ссылки). Другим предпочтительным агонистом/ антагонистом эстрогена является тамоксифен:(этанамин, 2-[4-(1,2-дифенил-1-бутенил)фенокси]-N,N-диметил-, (Z)-2-, 2-гидрокси-1,2,3-пропантрикарбоксилат (1:1 и родственные соединения (патент США 4536516, раскрытие которого приводится в настоящем описании посредством ссылки). Другим родственным соединением является 4-гидрокситамоксифен (патент США 4623660, раскрытие которого приводится в настоящем описании посредством ссылки). Другим предпочтительным агонистом/ антагонистом эстрогена является ралоксифен:(метанон,[6-гидрокси-2-(4-гидроксифенил) бензо[b]тиен-3-ил][4-[2-(1-пиперидинил)этокси] фенил]-, гидрохлорид) и родственные соединения (патент США 4418068, раскрытие которого приводится в настоящем описании посредством ссылки). Другим предпочтительным агонистом/ антагонистом эстрогена является идоксифен: пирролидин, 1-[-[4-[1-(4-йодфенил)-2-фенил-1 бутенил]фенокси]этил] и родственные соединения (патент США 4839155, раскрытие которого приводится в настоящем описании посредством ссылки). Другие предпочтительные агонисты/ антагонисты эстрогена включают в себя соединения, описанные в надлежащим образом переуступленном патенте США 5552412, раскрытие которого приводится в настоящем описании посредством ссылки. Особенно предпочтительными соединениями, описанными в этом патенте, являются цис-6-(4-фторфенил)-5-[4-(2-пиперидин-1 илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2 ол;(-)-цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол; цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол; цис-1-[6'-пирролидиноэтокси-3'-пиридил]2-фенил-6-гидрокси-1,2,3,4-тетрагидронафталин; 1-(4'-пирролидиноэтоксифенил)-2-(4"фторфенил)-6-гидрокси-1,2,3,4-тетрагидроизохинолин; цис-6-(4-гидроксифенил)-5-[4-(2-пиперидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ол; и 1-(4'-пирролидинолэтоксифенил)-2-фенил 6-гидрокси-5,6,7,8-тетрагидроизохинолин. Описаны другие агонисты/антагонисты эстрогена (патент США 4133814, раскрытие которого приводится в настоящем описании посредством ссылки). Известны производные 2-фенил 3-ароилбензотиофена и 2-фенил-3-ароилбензотиофен-1-оксида (патент США 4133814). В следующих абзацах предлагаются предпочтительные пределы доз для различных антирезорбтивных агентов. Количество антирезорбтивного агента, которое следует применять, определяют по его активности как агента, ингибирующего потерю кости. Эту активность определяют по фармакокинетике индивидуального соединения и его минимальной и максимальной эффективной дозе для ингибирования потери кости с использованием протокола, такого как те, на которые ссылаются выше. В общем случае, эффективная доза для различных видов активности по данному изобретению, например для лечения остеопороза,для агонистов/антагонистов эстрогена (которые используют в комбинации с солью (L)-(+)винной кислоты соединения формулы I по данному изобретению) находится в пределах от 0,01 до 200 мг/кг/день, предпочтительно от 0,5 до 100 мг/кг/день. В частности, эффективная доза для дролоксифена находится в пределах от 0,1 до 40 мг/кг/день, предпочтительно от 0,1 до 5 мг/кг/день. В частности, эффективная доза для ралоксифена находится в пределах от 0,1 до 100 мг/кг/день, предпочтительно от 0,1 до 10 мг/кг/день. В частности, эффективная доза для тамоксифена находится в пределах от 0,1 до 100 мг/кг/день, предпочтительно от 0,1 до 5 мг/кг/день. В частности, эффективная доза для цис-6-(4-фторфенил)-5-[4-(2-пиперидин-1 илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2 ола; 17 цис-6-фенил-5-[4-(2-пирролидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2 ола; цис-1-[6'-пирролидиноэтокси-3'-пиридил]2-фенил-6-гидрокси-1,2,3,4-тетрагидронафталина; 1-(4'-пирролидиноэтоксифенил)-2-(4"фторфенил)-6-гидрокси-1,2,3,4-тетрагидроизохинолина; цис-6-(4-гидроксифенил)-5-[4-(2-пиперидин-1-илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2-ола; или 1-(4'-пирролидинолэтоксифенил)-2-фенил 6-гидрокси-5,6,7,8-тетрагидроизохинолина находится в пределах от 0,0001 до 100 мг/кг/день, предпочтительно от 0,001 до 10 мг/кг/день. В частности, эффективная доза для 4 гидрокситамоксифена находится в пределах от 0,0001 до 100 мг/кг/день, предпочтительно от 0,001 до 10 мг/кг/день. В общем случае, эффективная доза для различных видов активности по данному изобретению, например для лечения остеопороза,для агонистов/антагонистов эстрогена (которые используют в комбинации с солью (L)-(+)винной кислоты соединения формулы I по данному изобретению) находится в пределах от 0,01 до 200 мг/кг/день, предпочтительно от 0,5 до 100 мг/кг/день. В частности, эффективная доза для дролоксифена находится в пределах от 0,1 до 40 мг/кг/день, предпочтительно от 0,1 до 5 мг/кг/день. В частности, эффективная доза для ралоксифена находится в пределах от 0,1 до 100 мг/кг/день, предпочтительно от 0,1 до 10 мг/кг/день. В частности, эффективная доза для тамоксифена находится в пределах от 0,1 до 100 мг/кг/день, предпочтительно от 0,1 до 5 мг/кг/день. В частности, эффективная доза для цис-6-(4-фторфенил)-5-[4-(2-пиперидин-1 илэтокси)фенил]-5,6,7,8-тетрагидронафталин-2 ола; 18 1-(4'-пирролидинолэтоксифенил)-2-фенил 6-гидрокси-5,6,7,8-тетрагидроизохинолина находится в пределах от 0,0001 до 100 мг/кг/день, предпочтительно от 0,001 до 10 мг/кг/день. В частности, эффективная доза для 4 гидрокситамоксифена находится в пределах от 0,0001 до 100 мг/кг/день, предпочтительно от 0,001 до 10 мг/кг/день. Анализ на стимулирование высвобождения ГР из питуицитов крыс Соединения, которые обладают способностью стимулировать секрецию ГР из культивированных клеток гипофиза крысы, идентифицируют, используя следующую методику. Этот тест является также полезным для сравнения со стандартами для определения уровней доз. Клетки выделяют из гипофиза крыс-самцовWistar в возрасте 6 недель. После декапитации передние доли гипофиза помещают в холодный стерильный уравновешенный солевой раствор Хенка, не содержащий кальция или магния(HBSS). Ткани мелко измельчают, затем подвергают двум циклам ферментативного механического диспергирования, используя раствор бактериальной протеазы (ЕС 3.4.24.4, Sigma P6141, St. Louis, Missouri) в HBSS с концентрацией 10 ед./мл. Смесь ткань-фермент перемешивают во вращающейся колбе со скоростью 30 об./мин в атмосфере, содержащей 5% СО 2, примерно при 37 С в течение примерно 30 мин, с перетиранием вручную примерно через 15 мин,и в течение примерно 30 мин, используя 10-мл пипетку. Смесь центрифугируют при 200 х g в течение примерно 5 мин. К надосадочной жидкости для нейтрализации избытка протеазы добавляют лошадиную сыворотку (конечная концентрация 35%). Осадок ресуспендируют в свежем растворе протеазы (10 ед./мл), снова перемешивают в течение примерно 30 мин в предыдущих условиях и вручную перетирают в конечном счете через иглу 23-размера. Снова добавляют лошадиную сыворотку (конечная концентрация 35%), затем клетки из обоих гидролизатов объединяют, осаждают центрифугированием (200 х g в течение 15 мин), ресуспендируют в культуральной среде (модифицированная по способу Дульбеко среда Игла (D-MEM) с добавлением 4,5 г/л глюкозы, 10% лошадиной сыворотки, 2,5% сыворотки плода коровы, 1% заменимых аминокислот, 100 ед./мл нистатина и 50 мг/мл сульфата гентамицина, Gibco, GrandIsland, New York) и подсчитывают. Клетки засевают в количестве 6,0-6,5104 клеток на см 2 в 48-луночные чашки Costar (Cambridge, Massachusetts) и культивируют в течение 3-4 дней в культуральной среде. Непосредственно перед анализом на секрецию ГР лунки для культивирования два раза промывают средой высвобождения, затем уравновешивают в течение примерно 30 мин в среде высвобождения (D-МЕМ, забуференной 25 мМHEPES, рН 7,4 и содержащей 0,5% бычьего сывороточного альбумина при 37 С). Тестируемые соединения растворяют в ДМСО, затем разводят в предварительно нагретой среде высвобождения. Каждый анализ проводят четыре раза. Анализ инициируют добавлением 0,5 мл среды высвобождения (с носителем или испытуемым соединением) в каждую культуральную лунку. Культивирование проводят примерно при 37 С в течение примерно 15 мин, а затем завершают,удаляя среду высвобождения, которую центрифугируют при 2000 х g в течение примерно 15 мин для удаления клеточного материала. Концентрации гормона роста крысы в надосадочных жидкостях определяют по стандартному протоколу радиоиммунного анализа, описанному ниже. Измерение гормона роста крыс Концентрации гормона роста крысы определяют двойным радиоиммуноанализом антител с использованием эталонного препарата гормона роста собак (NIDDK-rGH-RP-2) и антисыворотки гормона роста крыс, выращенной в обезьяне (NIDDK-anti-rGH-S-5), полученной от Dr. A.Parlow (Harbor-UCLA Medical Center, Torrence,CA). Дополнительный гормон роста крысы (1,5 ед./мг, G2414, Scripps Labs, San Diego, CA) йодируют до удельной активности приблизительно 30 мкКи/мкг хлорамин Т-методом для использования в качестве индикатора. Иммунные комплексы получают, добавляя к IgG обезьяны(ICN/Cappel, Aurora, ОН) козью сыворотку и полиэтиленгликоль, MB 10000-20000 до конечной концентрации 4,3%; при этом извлечение выполняют центрифугированием. Этот образец имеет рабочий предел 0,08-2,5 мкг гормона роста крысы на пробирку вышеупомянутых минимально возможных уровней. Анализ на экзогенно-стимулированное высвобождение гормона роста у крысы после внутривенного введения тест-соединений Крыс-самок Sprague-Dawley в возрасте двадцать один день (Charles River laboratory,Wilmington, MA) оставляют акклиматизироваться к местным условиям вивария (24 С, цикл: 12 ч - свет, 12 ч - темнота) в течение приблизительно 1 недели до испытания соединения. Всем крысам оставляют доступ к воде и покупному пищевому рациону в виде пилюль (AgwayCountry Food, Syracuse, NY) ad libitum. Эксперименты проводят в соответствии с указаниями Национального института здоровья по содержанию и использованию лабораторных животныхAnimals). В день эксперимента тестируемые соединения растворяют в носителе, содержащем 1% этанола, 1 мМ уксусную кислоту и 0,1% бычьего сывороточного альбумина в солевом растворе. Каждый эксперимент проводят на трех крысах. Крыс взвешивают и анестезируют внутрибрюшинной инъекцией пентобарбитала натрия(Nembutol, 50 мг/кг веса тела). Через 14 мин после введения анестезирующего агента берут образец крови, отрезая кончик хвоста и оставляя кровь капать в микроцентрифужную пробирку(базовый образец крови, приблизительно 100 мкл). Через 15 мин после введения анестезирующего агента тестируемое соединение доставляют внутривенной инъекцией в хвостовую вену суммарным объемом 1 мл/кг веса тела. Дополнительные образцы крови берут из хвоста на 5, 10 и 15 минуты после введения соединения. Образцы крови держат во льду до отделения сыворотки центрифугированием (1430 х g в течение 10 мин при 10 С). Сыворотку хранят при-80 С до определения сывороточного гормона роста радиоиммунным анализом, описанным выше. Оценка экзогенно-стимулированного высвобождения гормона роста у собаки после перорального введения В день введения дозы тестируемое соединение взвешивают для соответствующей дозы и растворяют в воде. Дозы объемом 0,5-3 мл/кг доставляют 2-4 собакам в течение каждого режима дозирования через желудочный зонд. Образцы крови (5 мл) отбирают из яремной вены непосредственно перед дозированием и через 0,17, 0,33, 0,5, 0,75, 1, 2, 4, 6, 8 и 24 ч после введения с использованием 5 мл вакунтейнеров,содержащих литиевый гепарин. Приготовленную плазму хранят при -20 С до анализа. Измерение гормона роста собак Концентрации гормона роста собак определяют по стандартной методике радиоиммунного анализа с использованием гормона роста собак (антигена для йодирования и упомянутого препарата AFP-1983B) и антисыворотки гормона роста собак, выращенной в обезьяне (AFP21452578), полученной от Dr. A. Parlow (HarborUCLA Medical Center, Torrence, СА). Индикатор изготавливают хлорамин Т-йодированием гормона роста собаки до удельной активности 2040 мкКи/мкг. Иммунные комплексы получают добавляя к IgG обезьяны (ICN/Cappel, Aurora,ОН) козью сыворотку и полиэтиленгликоль,ММ 10000-20000, до конечной концентрации 4,3%; при этом извлечение выполняют центрифугированием. Этот образец имеет рабочий предел 0,08-2,5 мкг ГР собаки/пробирка. Оценка уровней гормона роста собак и инсулиноподобного фактора роста 1 у собак после постоянного перорального введения Собаки получают тестируемое соединение ежедневно в течение либо 7, либо 14 дней. В каждый из этих дней тестируемое соединение взвешивают для соответствующей дозы и растворяют в воде. Дозы объемом 0,5-3 мл/кг доставляют 5 собакам в течение каждого режима дозирования через желудочный зонд. Образцы крови отбирают в день 0, 3, 7, 10 и 14. Образцы крови (5 мл) отбирают из яремной вены непосредственно перед дозированием и через 0,17, 21 0,33, 0,5, 0,754, 1, 2, 3, 6, 8, 12 и 24 ч после введения на день 0, 7 и 14 с использованием 5 мл вакунтейнеров, содержащих литиевый гепарин. Кроме того, кровь отбирают перед дозированием и в 8 ч на день 3 и 10. Приготовленную плазму хранят при -20 С до анализа. Исследование крыс-самок Данное исследование предназначено для оценки эффекта постоянной обработки имитатором ГРВП на вес, состав тела и концентрации глюкозы, инсулина, лактата и липидов при неголодании в плазме у крыс-самок с дефицитом эстрогена и избытком эстрогена. Сильную чувствительность сывороточных уровней ГР к внутривенному введению высвобождающего ГР агента определяют в последний день дозирования. Вес тела контролируют еженедельно в продолжение всего периода обработки; дополнительно в конце обработки определяют состав тела и уровни глюкозы, инсулина, лактата, холестерина и триглицеридов в плазме. Девственные крысы-самки Sprague-Dawley получены из лаборатории Charles River Laboratories (Wilmington, MA). Их подвергают билатеральной овариэктомии (Ovx) или мнимой операции (Sham) в возрасте приблизительно 12 недель. Для мнимой операции яичники выделяют и обратно помещают в брюшную полость. После операции крыс размещают по отдельным клеткам размером 20 см 32 см 20 см в стандарных условиях вивария (примерно 24 С при следующем цикле: примерно 12 ч свет/12 ч темнота). Всем крысам оставляют свободный доступ к воде и покупному пищевому рациону в виде пилюль (Agway ProLab 3000, Agway Country Food, Inc., Syracuse, NY). Эксперимент проводят в соответствии с указаниями Национального института здоровья по содержанию и использованию лабораторных животных (NIHAnimals). Крыс Sham и Ovx через приблизительно 7 месяцев после операции взвешивают и произвольно распределяют по группам. Ежедневно крысам перорально вводят дозу 0,5 или 5 мг/кг высвобождающего гормон роста агента в 1 мл любого из двух носителей (1%-й раствор этанола в дистиллированной деионизированной воде) в течение 90 дней при помощи желудочного зонда. Крыс взвешивают еженедельно на протяжении всего исследования. Через 24 ч после последней пероральной дозы определяют сильную чувствительность сывороточного гормона роста (ГР) к тестируемому соединению по следующей методике. Крыс анестезируют пентобарбиталом натрия (50 мг/кг). Анестезированных крыс взвешивают и из хвостовой вены отбирают базовый образец крови (100 мкл). Затем внутривенно через хвостовую вену вводят тестируемый агент (высвобождающий гормон роста агент или носитель) в 1 мл. Через приблизительно 10 мин после инъекции из хвоста от 002643 22 бирают второй 100 мкл образец крови. Кровь оставляют свертываться примерно при 4 С, затем центрифугируют при 2000 х g в течение примерно 10 мин. Сыворотку хранят примерно при -70 С. Концентрации сывороточного гормона роста определяют радиоиммунным анализом, описанным ранее. Следуя этой методике все тело каждой анестезированной крысы подвергают сканированию с использованием двухэнергетической рентгеновской абсорбциометрии (DEXA, Hologic QDR 1000/W, Walthman МА). Конечные образцы крови отбирают кардиальной пункцией в гепаринизированные пробирки. Плазму отделяют центрифугированием и хранят замороженной так, как описано выше. Инсулин плазмы определяют радиоиммунным анализом с использованием набора Binax Corp. (Portland, Maine). Коэффициент отклонения результатов анализа составляет 10%. Уровни плазменных триглицеридов, полного холестерина, глюкозы и лактата измеряют с использованием Abbott VP и VP Super SystemAutoanalyzer (Abbott Laboratories, Irving, Texas),с использованием систем A-Gent тестреагентов триглицеридов, холестерина и глюкозы, и лактатного набора Sigma, соответственно. Инсулин, триглицериды, полный холестерин и лактат в плазме, которые понижают активность высвобождающего гормон роста пептида(ГРВП) или имитатора ГРВП, такого как соединение формулы I, определяют статистическим анализом (непарный т-тест) у контрольной группы, обработанной носителем. Соль (L)-(+)-винной кислоты соединения формулы I можно вводить пероральным, парентеральным (например, внутримышечной, внутрибрюшинной, внутривенной или подкожной инъекцией или имплантацией), назальным, вагинальным, ректальным, подъязычным или наружным путями введения, и фармацевтические препараты могут быть приготовлены в составе с фармацевтическими приемлемыми носителями для обеспечения лекарственных форм, соответствующих каждому пути введения. Твердые лекарственные формы для перорального введения включают в себя капсулы,таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах соль (L)-(+)винной кислоты соединения формулы I смешана, по меньшей мере, с одним инертным фармацевтически приемлемым носителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы также могут содержать, как это имеет место в обычной практике, дополнительные вещества, отличные от таких инертных разбавителей, например, связывающие агенты, такие как стеарат магния. В случае капсул, таблеток и пилюль лекарственные формы также могут содержать буферные агенты. Таблетки и пилюли, кроме того, могут быть приготовлены с энтеральными покрытиями. 23 Жидкие лекарственные формы для перорального введения включают в себя фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы, эликсиры, содержащие инертные разбавители, обычно применяемые на практике, например воду. Кроме таких инертных разбавителей, композиции также могут включать в себя адьюванты, такие как смачивающие агенты, эмульгаторы и суспендирующие агенты,и подсластители, корригенты и ароматизаторы. Препараты по данному изобретению для парентерального введения включают в себя стерильные водные или неводные растворы, суспензии или эмульсии. Примерами неводных растворителей или наполнителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и сложные органические эфиры для инъекций, такие как этиловый эфир олеиновой кислоты. Такие лекарственные формы также могут содержать адъюванты, такие как консерванты, эмульгаторы, смачивающие и диспергирующие агенты. Они могут быть простерилизованы, например, фильтрованием через фильтр, удерживающий бактерии, включением стерилизующих агентов в композиции, облучением композиций или нагреванием композиций. Их также можно изготавливать в форме стерильных твердых композиций, которые непосредственно перед применением можно растворять в стерильной воде или некоторых других стерильных средах для инъекции. Композициями для ректального или вагинального введения предпочтительно являются суппозитории, которые могут содержать, кроме активного вещества, эксципиенты, такие как масло какао или суппозиторный воск. Композиции для подъязычного введения или через нос также готовят с использованием стандартных хорошо известных эксципиентов. Дозировка соли (L)-(+)-винной кислоты соединения формулы I в композициях по данному изобретению может изменяться; однако,необходимо, чтобы ее количество было таким,чтобы получить подходящую лекарственную форму. Выбранная дозировка зависит от требуемого терапевтического эффекта, от пути введения и от продолжительности лечения. Обычно человеку или другим животным, например млекопитающим, ежедневно вводят уровни доз между 0,0001 и 100 мг/кг веса тела,чтобы получить эффективное высвобождение гормона роста. Предпочтительный диапазон дозировки составляет от 0,01 до 5,0 мг/кг веса тела ежедневно, которые можно вводить как однократную дозу или разделенную на многократные дозы. Следующая схема иллюстрирует синтез соли (L)-(+)-винной кислоты соединения формулы (I). Символобозначает стереохимический центр. На схеме Prt используют для обо 002643 24 значения любой подходящей защитной группы амина, которая будет известна квалифицированным специалистам. Ниже следует описание реакционных стадий, изображенных на упомянутой выше схеме. В этом описании защитная группа амина Prt показана предпочтительной защитной группой амина БОК. Стадия а. К раствору соединения А в реакционном инертном полярном апротонном растворителе, таком как ацетон, метилэтилкетон или предпочтительно ДМФ (диметилформамид), при температуре от примерно 0 С до комнатной температуры, предпочтительно 0 С, добавляют гидрохлорид пиколилхлорида, карбонат, такой как LiСО 3, СsCО 3 или предпочтительно карбонат калия, и йодид калия или йодид тетрабутиламмония. После перемешивания при температуре от примерно -20 до примерно 70 С,предпочтительно 0 С, в течение примерно от 2 до 16 ч, предпочтительно в течение примерно 2 ч, ледяную баню удаляют и добавляют 1,4 диазобицикло[2.2.2]октан (ДАБКО). Реакционную смесь перемешивают в течение примерно 15-30 мин и вливают в смесь воды и неполярного органического растворителя, такого как толуол, диэтиловый эфир или предпочтительно ИПЭ (изопропиловый эфир). Органический слой отделяют и обрабатывают стандартными способами, известными в химии, с получением соединения В. Стадия b. 70%-й водный растворCF3CH2NHNH2 используют в виде водного раствора в этаноле, воде или толуоле, предпочтительно 70%-й водный раствор CF3CH2NHNH2 экстрагируют толуолом. К раствору соединения В в органическом растворителе, таком как эта 25 нол или предпочтительно толуол, сначала добавляют толуольные экстракты, содержащие безводный 2,2,2-трифторэтилгидразин, а затем уксусную кислоту. Реакционную смесь нагревают примерно при 60-100C, предпочтительно 70 С, в течение примерно от 30 мин до 12 ч,предпочтительно 2 ч. Реакционную смесь охлаждают до комнатной температуры и нейтрализуют водным основанием, таким как NаНСО 3. Органический слой отделяют и обрабатывают стандартными способами, известными в химии,с получением соединения С. Стадия с. К раствору соединения С в инертном органическом растворителе, таком какEtOH, ИПЭ или предпочтительно CH2Cl2, добавляют кислоту, такую как HCl в ИПЭ или этаноле, трифторметансульфоновую кислоту или алкилсульфоновую кислоту, такую как метансульфоновую кислоту. Смесь перемешивают в течение примерно 1-2 ч, затем охлаждают до температуры примерно от 0 С до комнатной,предпочтительно 0 С, а потом к смеси добавляют аминное основание, такое как триэтиламин,или NH4OH. Смесь оставляют нагреваться до комнатной температуры, разбавляют дополнительным количеством органического растворителя и обрабатывают стандартными способами,известными в химии, с получением соединенияD. Стадия d. К соединению D в смеси ацетон/вода в соотношении от примерно 8:1 до примерно 9:1 примерно при комнатной температуре добавляют (D)- или (L)-винную кислоту,предпочтительно (D)-винную кислоту. Смесь перемешивают при комнатной температуре в течение от примерно 15 мин до ночи, предпочтительно в течение ночи, твердое вещество фильтруют, собирают и промывают холодным ацетоном с получением соединения формулы Е; соединение Е предпочтительно представляет собой (D)-тартрат единственного энантиомера. Стадия е. К раствору N-БОК-серина, предпочтительно N-БОК-(D)-серина (соединение F),в смеси ТГФ/ДМФ в соотношении от примерно 1:1 до примерно 2:1 примерно при 0 С добавляют н-BuLi или раствор трет-бутилата калия. Реакционную смесь перемешивают при примерно 0 С в течение примерно 10-30 мин, предпочтительно 20 мин, затем добавляют 2,4 дифторбензилбромид. После нагревания до комнатной температуры и перемешивания в течение примерно 6-24 ч реакционную смесь концентрируют в вакууме для удаления ТГФ и добавляют водный раствор кислоты, такой как 1 н. HCl, для установления рН смеси равным примерно 3. Затем реакционную смесь распределяют между водой и органическим растворителем, таким как CH2Cl2 или ИПЭ. Органический раствор обрабатывают стандартными способами, известными в химии, с получением соединения G, предпочтительно имеющего R 002643 26 конфигурацию по стереоцентру, также известного как (D)-энантиомер. Стадия f. К раствору соединения G в органическом растворителе, таком как ТГФ, CH2Cl2,ИПЭ или их смеси, предпочтительно в смеси СН 2 Сl2/ИПЭ в соотношении примерно 1:1, добавляют алкилсульфоновую кислоту, такую как метансульфоновую кислоту. Твердое вещество отфильтровывают и промывают смесью СН 2 Сl2/ИПЭ в соотношении 1:1, получая соединение Н, предпочтительно имеющее Rконфигурацию по стереоцентру, также известное как (D)-энантиомер. Стадия g. К раствору соединения Н в смеси ТГФ/вода в соотношении примерно 4:1 добавляют 2,5-диоксопирролидин-1-иловый эфир 2-трет-бутоксикарбониламино-2-метилпропионовой кислоты и алкиламин, такой как триэтиламин. Реакционную смесь перемешивают при комнатной температуре в течение примерно 124 ч и гасят водной кислотой, такой как 10%-й водный раствор лимонной кислоты. Смесь разделяют органическим растворителем, таким как этилацетат, органический слой отделяют и обрабатывают стандартными способами, известными в химии, с получением соединения X,предпочтительно имеющего R-конфигурацию по стереоцентру, также известного как (D)энантиомер. Соединения Х могут представлять собой кислоту, сложный алкиловый эфир или галогенангидрид (X представляет собой ОН,-O(С 1-С 4)алкил или галогено); кислота является предпочтительной. Стадия h.(а) Соединение Е, предпочтительно (D)тартрат единственного энантиомера, добавляют при температуре от примерно -35 до 0 С, предпочтительно примерно при -6 С, к этилацетату. Раствор охлаждают до температуры от примерно -30 до 50 С, затем добавляют алкиламин,такой как триэтиламин. Реакционную смесь перемешивают в течение примерно 30-90 мин при температуре между примерно -78 и примерно-20 С и фильтруют с получением раствора свободного основания соединения Е.(b) Когда Х в соединении Х представляет собой ОН, соединение X, предпочтительно имеющее R-конфигурацию по стереоцентру,добавляют при температуре от примерно -78 до-20 С, предпочтительно -35 С, к инертному органическому растворителю, такому как этилацетатный раствор, содержащий свободное основание соединения Е со стадии h(a), алкиламин,такой как триэтиламин и АПФК (циклический ангидрид 1-пропанфосфоновой кислоты) (50% в этилацетате). Реакционную смесь перемешивают в течение примерно 1-24 ч и обрабатывают стандартными способами, известными в химии,с получением соединения J, предпочтительно имеющего абсолютную и относительную 3a-(R),1-(R)-конфигурацию.-78 С к инертному органическому растворителю, такому как дихлорметановый раствор, содержащий свободное основание соединения Е и алкиламин, такой как триэтиламин. Реакционную смесь перемешивают в течение примерно 1-24 ч при примерно 0-30 С, а затем обрабатывают стандартными способами, известными в химии, с получением соединения J, предпочтительно имеющего абсолютную и относительную 3a-(R),1-(R)-конфигурацию. Когда Х в соединении Х представляет собой -O(С 1-C4)алкил, где метил является предпочтительным, соединение Х добавляют к раствору свободного или сопряженного основания Е (сопряженное основание соединения Е (-NM,где М = Li, Na, К, Мg или Al, предпочтительно алюминий) получают взаимодействием свободного аминного основания с соответствующим реагентом (т.е. М = Li, бутиллитий или диизопропиламид лития (ДИАЛ), М = Na, NaH илиNаN(SiМе 3)2, или М = К, КН или КN(SiМе 3)2,или М = Мg, любой реагент Гриньяра, предпочтительно диэтилмагнийбромид, или М = Al, любой триалкилалюминиевый реагент, предпочтительно триметилалюминий), предпочтительно алюминия, в инертном растворителе, таком как дихлорметан, и полученную реакционную смесь перемешивают в течение примерно 1-24 ч при температуре примерно 20 - 100 С и обрабатывают стандартными способами, известными в химии, с получением соединения J, предпочтительно имеющего абсолютную и относительную 3a-(R),1-(R)-конфигурацию. Стадия i. К соединению J в CH2Cl2, ИПЭ или ТГФ при температуре от примерно 0 С до комнатной температуры добавляют кислоту,такую как HCl в EtOH, метансульфоновую кислоту или трифторметансульфоновую кислоту вCH2Cl2. Смесь перемешивают в течение от примерно 40 мин до примерно 4 ч при комнатной температуре, затем добавляют насыщенный водный раствор основания, такого как NаНСО 3,до тех пор, пока раствор не станет нейтральным. Органический слой отделяют и обрабатывают стандартными способами, известными в химии,с получением соединения К, предпочтительно имеющего абсолютную и относительную 3a(R),1-(R)-конфигурацию. Стадия j. К раствору соединения К в спирте, предпочтительно метаноле, добавляют L-(+)винную кислоту. Реакционную смесь перемешивают в течение примерно 1-12 ч, фильтруют и концентрируют. Неочищенный остаток разбавляют органическим растворителем, таким как этилацетат, нагревают и оставляют медленно охлаждаться до комнатной температуры. Твердое вещество фильтруют и сушат с образованием соли (L)-(+)-винной кислоты соединения формулы I в виде белых кристаллов, которая 28 предпочтительно имеет абсолютную и относительную 3a-(R),1-(R)-конфигурацию. Следующие примеры предложены только с целью дальнейшей иллюстрации изобретения и не предназначены для ограничения раскрываемого изобретения. Для колоночной хроматографии использовали диоксид кремния. Температуры плавления определяли на приборе Buchi 510 и не корректировали. Протонные ЯМР спектры снимали наVarian XL-300, Bruker AC-300, Varian Unity 400 или Bruker AC-250 при 25 С. Химические сдвиги выражены в миллионных долях по нисходящей от триметилсилана. Пример 1. L-(+)-Тартрат 2-амино-N-1(2,4-дифторбензилоксиметил)-2-оксо-2-[3-оксо 3 а-пиридин-2-илметил-2-(2,2,2-трифторэтил)2,3,3 а,4,6,7-гексагидропиразоло[4,3-с]пиридин 5-ил]этил-2-метилпропионамида. А. 1-трет-Бутиловый 3-этиловый эфир 4 оксопиридин-2-илметилпиперидин-1,3-дикарбоновой кислоты. К раствору 1-трет-бутилового эфира 3 этилового эфира 4-оксопиперидин-1,3-дикарбоновой кислоты (10,34 г, 38,2 ммоль) в ДМФ(40 мл) примерно при 0 С добавляют гидрохлорид пиколилхлорида (5,7 г, 34,7 ммоль), карбонат калия (14,4 г, 104,1 ммоль) и йодид калия(5,76 г, 34,7 ммоль). После перемешивания примерно при 0 С в течение примерно 2 ч ледяную баню удаляют и добавляют ДАБКО (973 мг,8,68 ммоль). Реакционную смесь перемешивают в течение примерно 30 мин и вливают в смесь воды и ИПЭ. Органический слой отделяют и промывают насыщенным водным NаНСО 3 и насыщенным водным NaCl, сушат над Na2SO4 и концентрируют в вакууме. Неочищенный остаток кристаллизуют из смеси гексанов с образованием белого твердого вещества (8,19 г, выход 65%). 1B. трeт-Бутиловый эфир 3-оксо-3 апиридин-2-илметил-2-(2,2,2-трифторэтил)2,3,3 а,4,6,7-гексагидропиразоло[4.3-с]пиридин 5-карбоновой кислоты. 70%-й водный раствор СF3 СН 2NНNН 2 (325 мл, 1,986 моль) (полученный от Aldrich) экстрагируют толуолом (31200 мл). К раствору продукта, полученного на стадии А (600 г, 1,655 моль), в толуоле (900 мл) сначала добавляют объединенные толуольные экстракты, содержащие безводный 2,2,2-трифторэтилгидразин, а затем уксусную кислоту (121,4 г, 1,986 моль). Реакционную смесь нагревают примерно при 70 С в течение примерно 2 ч, затем добавляют другой толуольный экстракт 70%-го 2,2,2 трифторэтилгидразина (50 г). Реакционную смесь нагревают примерно при 80 С в течение 29 примерно 3,5 ч, охлаждают до комнатной температуры и разбавляют насыщенным воднымNaHCO3 (2 л). Толуольный слой отделяют и промывают насыщенным водным NaCl, сушат над Na2SO4 и концентрируют в вакууме с получением масла (754,8 г). Кристаллизация из смеси метанола и воды приводит к получению требуемого продукта в виде белого твердого вещества (609,5 г). 1(m, 1H), 4.19 (m, 1H), 4.46 (br s, 1H), 4.63 (br s,1H), 7.06 (m, 2H), 7.51 (m, 1H), 8.34 (m, 1H). С. 3 а-Пиридин-2-илметил-2-(2,2,2-трифторэтил)-2,3 а,4,5,6,7-гексагидропиразоло[4,3 с]пиридин-3-он. К раствору продукта со стадии В (10 г,24,2 ммоль) в СН 2 Сl2 (100 мл) примерно за 30 мин по каплям добавляют метансульфоновую кислоту (11,6 г, 121 ммоль). Реакционную смесь перемешивают в течение примерно 1 ч, затем охлаждают примерно до 0 С и через капельную воронку добавляют триэтиламин (18,6 мл, 133,1 ммоль). Смесь оставляют нагреваться до комнатной температуры примерно в течение 1 ч,разбавляют дополнительным количествомNaCl, сушат над Na2SO4, фильтруют и концентрируют в вакууме, получая продукт в виде белого твердого вещества (7,2 г). 1D. D-Тартрат 3 а-пиридин-2-илметил-2(2,2,2-трифторэтил)-2,3 а,4,5,6,7-гексагидропиразоло[4.3-с]пиридин-3-она. В сухую круглодонную колбу емкостью 5 л, снабженную механической мешалкой, которую предварительно продувают азотом, к соединению, полученному на стадии С (243 г, 0,78 моль), в смеси ацетон/вода (9:1, 2430 мл) при примерно 17 С добавляют D-(-)-винную кислоту (129 г, 0,86 моль). Смесь перемешивают при комнатной температуре в течение ночи, фильтруют и твердое вещество собирают и промывают холодным ацетоном и сушат под вакуумом. Получают продукт в виде желтого твердого вещества (284 г, выход 78,8%). Е. 2-трет-Бутоксикарбониламино-3-(2,4 дифторбензилокси)пропионовая кислота. К раствору N-БОК-(D)-серина (452 г,2,2026 моль) в смеси ТГФ (7 л) и ДМФ (3 л) примерно при 0 С добавляют раствор третбутилата калия (515,8 г, 4,5963 моль). Реакционную смесь перемешивают примерно при 0 С в течение примерно 30 мин, затем добавляют 2,4-дифторбензилбромид (456,5 г, 2,2051 моль). После нагревания до комнатной температуры реакционную смесь концентрируют в вакууме для удаления ТГФ. Реакционную смесь распределяют между 4,5 л H2 О и 4,5 л ИПЭ. Слои раз 002643 30 деляют и рН водного слоя доводят до 3 с использованием 1 н. NaOH. Водный слой два раза экстрагируют 4 л ИПЭ (каждый раз). Органический раствор сушат над Na2SO4 и концентрируют в вакууме с получением желтого воскообразного твердого вещества (518,0, выход 70,9%). 1 Н-ЯМР (CDCl3)1.44 (s, 9H), 3.73 (m, 1H), 3.94F. Соль метансульфоновой кислоты 2 амино-3-(2,4-дифторбензилокси)пропионовой кислоты. К раствору продукта со стадии Е (1,19 г,3,59 ммоль) в смеси CH2Cl2 и ИПЭ (1:1, 12 мл) шприцом примерно за 10 мин добавляют метансульфоновую кислоту (1,72 г, 17,95 ммоль). Сразу же из раствора выпадает в осадок твердое вещество. Примерно через 1 ч твердое вещество отфильтровывают и промывают смесью СН 2 О 2 и ИПЭ (1:1), получая 939 мг продукта (выход 80%).G. 2-(2-трет-Бутоксикарбониламино-2 метилпропиониламино)-3-(2,4-дифторбензилокси)пропионовая кислота. К раствору продукта со стадии F (520 мг,1,46 ммоль) в смеси ТГФ/вода (4:1, 10 мл) добавляют 2,5-диоксопирролидин-1-иловый эфир 2-трет-бутоксикарбониламино-2-метилпропионовой кислоты (438 мг, 1,46 ммоль) и триэтиламин (369 мг, 3,65 ммоль). Реакционную смесь перемешивают при комнатной температуре в течение примерно 1 ч и гасят 10%-м водным раствором лимонной кислоты (10 мл). Примерно через 15 мин добавляют этилацетат (50 мл) и органический слой отделяют и промывают насыщенным водным NaCl, сушат над Nа 2SO4 и концентрируют в вакууме с образованием пены(d, 1H), 3.92 (d, 1H), 4.52 (m, 3 Н), 6.92 (m, 1H),7.41 (m, 1H), 7.58 (d, 1H). Н. трет-Бутиловый эфир (1-1-(2,4-дифторбензилоксиметил)-2-оксо-2-[3-оксо-3 а-пиридин 2-илметил-2-(2,2,2-трифторэтил)-2,3,3 а,4,6,7 гексагидропиразоло[4,3-с]пиридин-5-ил]этилкарбамоил-1-метилэтил)карбаминовой кислоты. а). В сухую круглодонную колбу емкостью 12 л, снабженную механической мешалкой, которую предварительно продувают азотом, к этилацетату (5170 мл) примерно при -6 С добавляют соединение со стадии D (517 г, 1,12 моль). Раствор охлаждают примерно до -40 С,затем примерно за 45 мин добавляют триэтиламин (398 мл, 2,86 моль). Реакционную смесь перемешивают в течение примерно 90 мин при температуре между примерно -50 и примерно-40 С, фильтруют в 22 л круглодонную колбу,которую предварительно продувают азотом, и промывают этилацетатом (2068 мл, предварительно охлажденный примерно до -50 С) с по 31 лучением свободного основания в виде белого твердого вещества.b). Соединение, полученное на стадии G(425 г, 1,02 моль), примерно при -30 С добавляют к этилацетатному раствору, содержащему продукт со стадии Н(а), триэтиламин (654 мл,4,69 моль) и АПФК (50% в этилацетате, 916 мл,1,53 моль). Реакционную смесь перемешивают в течение примерно 1 ч, промывают водой и насыщенным водным NaCl, сушат над Na2SO4 и концентрируют в вакууме c образованием продукта в виде масла (636 г, выход: 87,8%).I. 2-Амино-N-1-(2,4-дифторбензилоксиметил)-2-оксо-2-[3-оксо-3 а-пиридин-2-илметил 2-(2,2,2-трифторэтил)-2,3,3 а,4,6,7-гексагидропиразоло[4.3-с]пиридин-5-ил]этил-2-метилпропионамид. К продукту со стадии Н (566 г, 0,796 моль) в СН 2 Сl2 (11,320 мл) в сухую 22 л круглодонную колбу, снабженную механической мешалкой,которую предварительно продувают азотом, по каплям примерно за 55 мин при примерно 15 С добавляют метансульфоновую кислоту (258,3 мл, 3,98 моль). Смесь перемешивают в течение примерно 40 мин примерно при 20 С, затем добавляют насыщенный водный NаНСО 3 (8,490 мл) до тех пор, пока рН не станет примерно равным 7,8. Органический слой отделяют, промывают водой и насыщенным водным NaCl,сушат над Na2SO4 и концентрируют в вакууме,получая маслянистый продукт (388,8 г, выход 80%).J. L-(+)-Tapтpaт 2-амино-N-1-(2,4-дифторбензилоксиметил)-2-оксо-2-[3-оксо-3 а-пиридин 2-илметил-2-(2,2,2-трифторэтил)-2,3,3 а,4,6,7 гексагидропиразоло[4,3-с]пиридин-5-ил]-этил 2-метилпропионамида. К раствору продукта со стадии I (370 г, 0,6 моль) в метаноле (4,070 мл) в круглодонную колбу емкостью 12 л, снабженную механической мешалкой, добавляют L-(+)-винную кислоту (90 г, 0,6 моль). Реакционную смесь перемешивают в течение примерно 90 мин примерно при 22 С, фильтруют и концентрируют. Неочищенный остаток разбавляют этилацетатом(4,560 мл), нагревают примерно до 70 С и оставляют медленно охлаждаться до комнатной температуры примерно в течение 17 ч. Твердое вещество фильтруют и сушат с образованием белых кристаллов, т.пл. 188-189 С (348,46 г,выход 76%). 1 Н ЯМР (МеОН, d4) : 8.28 (d, 1 Н), 7.59 (t,1H), 7.41-7.39 (m, 1H), 7.18-7.13 (m, 1H), 6.92 (t,1H), 5.2 (t, 1H), 4.56 (bs, 3 Н), 4.36 (s, 2 Н), 4.314.25 (m, 1H), 4.13-4.06 (m, 1H), 3.78 (d, 2H), 3.21 32 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соль (L)-(+)-винной кислоты соединения формулы I 2. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-S, 1-R. 3. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-S, 1-S. 4. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-R, 1-S. 5. Соль (L)-(+)-винной кислоты соединения формулы I по п.1, где стереохимической конфигурацией является 3a-R, 1-R. 6. Способ получения соли (D)-винной кислоты или (L)-винной кислоты соединения формулы (Е) при котором соединение формулы (D) подвергают взаимодействию с (D)-винной кислотой или (L)-винной кислотой в смеси от примерно 8:1 до примерно 9:1 ацетон:вода при температуре между примерно 0 С и комнатной температурой. 7. Способ по п.6, где (D)-винную кислоту подвергают взаимодействию с соединением формулы (D) и соединение формулы (Е) имеетR-конфигурацию. 8. Способ получения соединения формулы при котором соединение формулы (Е) где Prt представляет собой защитную группу амина и Х представляет собой ОН, -O(С 1-С 4) алкил или галогено, в присутствии органического основания и реагента пептидного связывания при температуре между примерно -78 и примерно -20 С с получением соединения формулы (J) с соединения формулы (J) удаляют защитную группу в соответствующих условиях удаления защиты с получением соединения формулы (K) где Prt представляет собой защитную группу амина и Х представляет собой ОН, -O(С 1-С 4) алкил или галогено, в присутствии органического основания и реагента пептидного связывания при температуре между примерно -78 и примерно -20 С. 9. Способ по п.8, где реагентом пептидного связывания является циклический ангидрид 1 пропанфосфоновой кислоты, соединение формулы Х имеет R-конфигурацию и соединение формулы Е имеет R-конфигурацию. 10. Способ по п.9, где Prt представляет собой трет-бутоксикарбонил. 11. Способ получения соли (L)-(+)-винной кислоты соединения формулы I при котором соединения формулы (Е) соединение формулы (K) подвергают взаимодействию с (L)-(+)-винной кислотой в реакционном инертном растворителе с получением соли (L)-(+)-винной кислоты соединения формулы I. 12. Способ по п.11, где Prt представляет собой трет-бутоксикарбонил. 13. Способ по п.12, где реагентом пептидного связывания является циклический ангидрид 1-пропанфосфоновой кислоты, и соединение формулы I имеет абсолютную и относительную конфигурацию 3a-(R), 1-(R). 14. Способ увеличения уровней эндогенного гормона роста у человека или другого животного, при котором такому человеку или животному вводят эффективное количество соли (L)(+)-винной кислоты соединения формулы I по п.1. 15. Фармацевтическая композиция, которая включает в себя фармацевтически приемлемый носитель и некоторое количество соли (L)(+)-винной кислоты соединения формулы I по п.1. 35 16. Фармацевтическая композиция, пригодная для увеличения эндогенной выработки или высвобождения гормона роста у человека или другого животного, которая включает в себя фармацевтически приемлемый носитель, эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1 и средство,стимулирующее секрецию гормона роста, выбранное из группы, состоящей из рилизингпептида 6 гормона роста (GHRP-6), Hexarelin,рилизинг-пептида 1 гормона роста (GHRP-1),рилизинг-фактора гормона роста (GRF), инсулиноподобного фактора роста 1 (IGF-1), инсулиноподобного фактора роста 2 (IGF-2) и ВНТ 920 или их аналога. 17. Способ лечения или предупреждения остеопороза, при котором человеку или другому животному, нуждающемуся в таком лечении или предупреждении, вводят количество соли(L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным при лечении или предупреждении остеопороза. 18. Способ лечения или предупреждения заболеваний или состояний, которые можно лечить или предупреждать посредством гормона роста, при котором человеку или другому животному, нуждающемуся в таком лечении или предупреждении, вводят количество соли (L)(+)-винной кислоты соединения формулы I по п.1, которое является эффективным для стимулирования высвобождения эндогенного гормона роста. 19. Способ по п.18, где заболеванием или состоянием является застойная сердечная недостаточность, ожирение или слабость, связанная со старением. 20. Способ по п.19, где заболеванием или состоянием является застойная сердечная недостаточность. 21. Способ по п.19, где заболеванием или состоянием является слабость, связанная со старением. 22. Способ ускорения восстановления кости после перелома, ослабления белкового катаболического ответа после тяжелой операции,уменьшения кахексии и потери белка вследствие хронического заболевания, ускорения заживления ран или ускорения выздоровления ожоговых пациентов или пациентов, подвергшихся тяжелой операции, при котором млекопитающему, нуждающемуся в таком лечении,вводят количество соли (L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным для стимулирования высвобождения эндогенного гормона роста. 23. Способ по п.22, где этот способ является способом ускорения выздоровления пациентов, подвергшихся тяжелой операции. 24. Способ по п.22, где этот способ является способом ускорения восстановления кости после перелома. 36 25. Способ увеличения мышечной силы,подвижности, поддержания толщины кожи, метаболического гомеостаза или ренального гомеостаза, при котором человеку или другому животному, нуждающемуся в таком лечении,вводят количество соли (L)-(+)-винной кислоты соединения формулы I по п.1, которое является эффективным для стимулирования высвобождения эндогенного гормона роста. 26. Способ лечения или предупреждения остеопороза, при котором человеку или другому животному с остеопорозом вводят эффективные количества бисфосфонатного соединения и соли(L)-(+)-винной кислоты соединения формулы I по п.1. 27. Способ лечения остеопороза по п.26,где бис-фосфонатным соединением является ибандронат. 28. Способ лечения остеопороза по п.26,где бис-фосфонатным соединением является алендронат. 29. Способ увеличения уровней инсулиноподобного фактора роста 1 (IGF-1) у человека или другого животного с дефицитом IGF-1, при котором человеку или другому животному с дефицитом IGF-1 вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1. 30. Способ увеличения мышечной массы,при котором человеку или другому животному,нуждающемуся в таком лечении, вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1. 31. Способ стимулирования роста детей с дефицитом гормона роста, при котором ребенку с дефицитом гормона роста вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1. 32. Способ лечения инсулинрезистентности у млекопитающего, при котором указанному млекопитающему вводят эффективное количество соли (L)-(+)-винной кислоты соединения формулы I по п.1. 33. Способ по п.32, где состоянием, связанным с инсулинрезистентностью, является диабет типа I, диабет типа II, гипергликемия,нарушение толерантности к глюкозе или инсулинрезистентный синдром. 34. Способ по п.32, где состояние, связанное с инсулинрезистентностью, связано с ожирением или старостью. 35. Смесь R,S-энантиомеров, R-энантиомер или S-энантиомер соединения формулы 36. Соль (D)-винной кислоты или (L)винной кислоты соединения по п.35. где Prt представляет собой защитную группу амина, выбранную из группы, состоящей из трет-БОК, ФМК и БЗК. 38. Смесь R,S-энантиомеров, R-энантиомер или S-энантиомер соединения формулы где X представляет собой ОН, -O(С 1-С 4)алкил или галогено и Prt представляет собой защитную группу амина. 40. Соединение по п.39, где Х представляет собой ОН, Prt представляет собой БОК и стереоцентр находится в R-конфигурации. 41. Способ лечения расстройств сна у млекопитающего, страдающего от расстройств сна,при котором указанному млекопитающему вводят эффективное количество соли (L)-(+)винной кислоты соединения формулы I по п.1.
МПК / Метки
МПК: C07K 5/023, A61K 38/06, C07D 401/06, A61P 5/06, C07D 471/04
Метки: роста, стимулирующее, дипептида, тартрат, замещенного, средство, гормона, секрецию
Код ссылки
<a href="https://eas.patents.su/20-2643-tartrat-zameshhennogo-dipeptida-kak-sredstvo-stimuliruyushhee-sekreciyu-gormona-rosta.html" rel="bookmark" title="База патентов Евразийского Союза">Тартрат замещенного дипептида как средство, стимулирующее секрецию гормона роста</a>
Предыдущий патент: Акарицидная композиция и способ борьбы с вредными клещами
Следующий патент: Производные 4-циано-4-деформилсордарицина
Случайный патент: Способ оздоровления организма "золотое сечение"