2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1н-бензимидазол, его применение и содержащая его композиция
Номер патента: 18369
Опубликовано: 30.07.2013
Авторы: Робичауд Альберт Дж., Юн Хидонг, Хайдар Саймон Н., Андрэ Патрик М.
Формула / Реферат
1. Соединение, представляющее собой 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1Н-бензимидазол или его фармацевтически приемлемую соль.
2. Применение 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1Н-бензимидазола или его фармацевтически приемлемой соли в качестве медикамента.
3. Применение по п.2 при модулировании функции 5-НТ6 рецептора у субъекта.
4. Применение по п.2 при лечении расстройства, связанного с 5-НТ6.
5. Применение по п.4, где расстройством, связанным с 5-НТ6, является заболевание или расстройство центральной нервной системы (ЦНС).
6. Композиция для лечения расстройств, связанных с 5-НТ6, содержащая соединение по п.1 и фармацевтически приемлемый носитель.
7. Применение соединения по п.1 для получения медикамента для лечения расстройства, связанного с 5-НТ6.
8. Применение по п.7, где расстройством, связанным с 5-НТ6, является заболевание или расстройство центральной нервной системы (ЦНС).
9. Применение по п.7 или 8, где расстройство, связанное с 5-НТ6, выбирают из следующих: психоз, тревога, депрессия, эпилепсия, синдром навязчивых состояний, мигрень, когнитивные расстройства, расстройства сна, расстройства питания, анорексия, ожирение, булимия, компульсивное переедание, приступы паники, расстройства, возникающие вследствие отказа от злоупотребления лекарственными средствами, нарушение когнитивных функций, связанное с шизофренией, расстройства желудочно-кишечного тракта, синдром раздраженного кишечника, расстройства памяти, болезнь Альцгеймера, болезнь Паркинсона, хорея Хантингтона, шизофрения, синдром дефицита внимания и гиперактивности, нейродегенеративные заболевания, которые характеризуются нарушением роста нейронов, и боль.
10. Применение по п.9, где расстройство, связанное с 5-НТ6, выбирают из следующих: депрессия, когнитивные расстройства, нарушение когнитивных функций, связанное с шизофренией, когнитивная дисфункция, связанная с болезнью Альцгеймера, и боль.
11. Применение по п.9, где расстройством, связанным с 5-НТ6, является болезнь Альцгеймера.
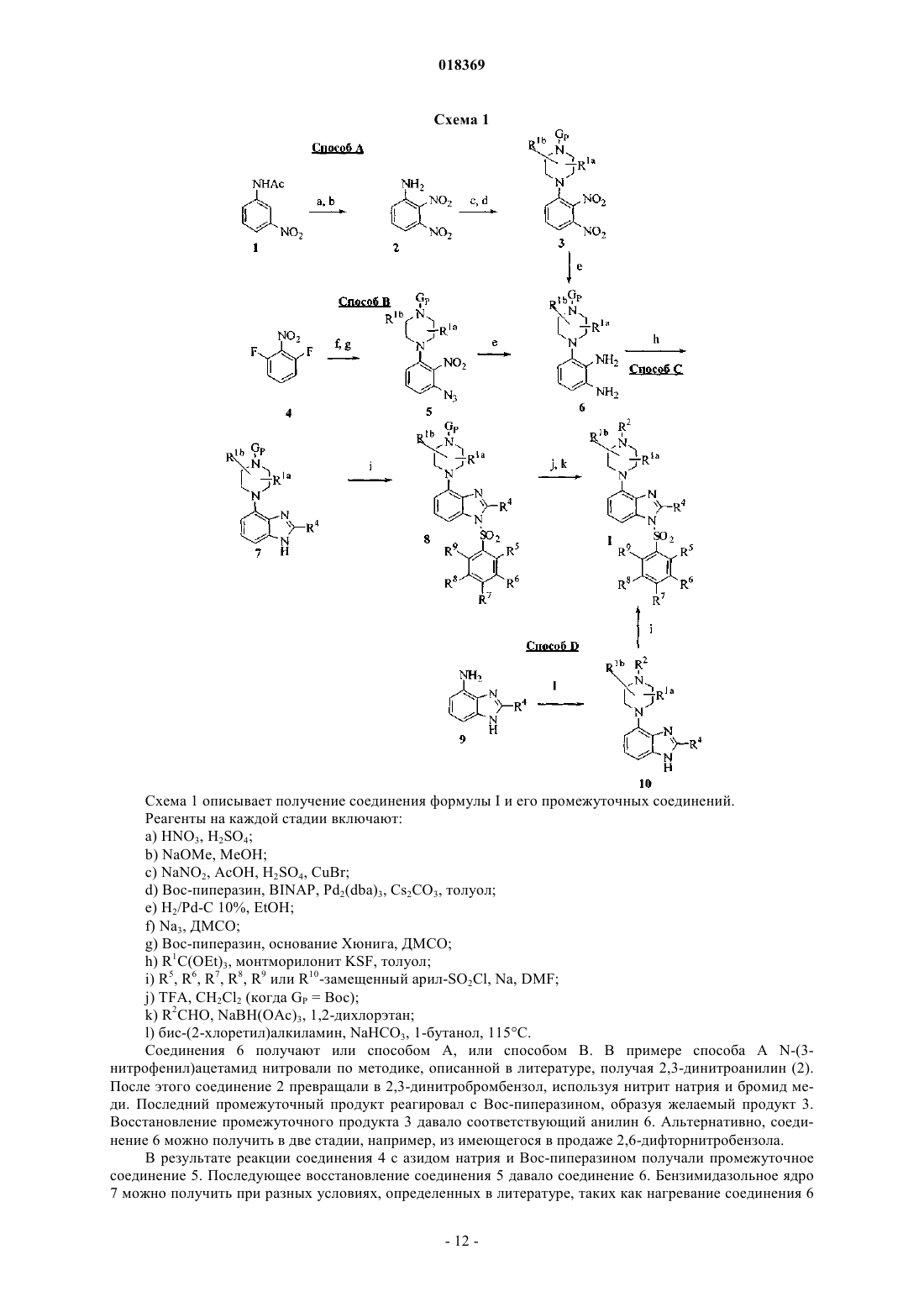
Текст
Изобретение касается 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Н-бензимидазола или его фармацевтически приемлемой соли, фармацевтической композиции и его применения в качестве медикамента и для модулирования активности 5-НТ 6. Область изобретения Данное изобретение касается 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Н-бензимидазола,фармацевтической композиции и его применения в качестве медикамента и для модулирования активности 5-НТ 6. Предпосылки изобретения Рецепторы серотонина (5-гидрокситриптамин) (5-НТ) играют решающую роль во многих физиологических и поведенческих функциях у людей и животных. Эти функции опосредствуются через разнообразные 5-НТ рецепторы, распространенные по всему телу. Сейчас известно приблизительно 15 разных клонированных подтипов рецепторов 5-НТ человека, многие из которых имеют четко определенную роль у человека. Недавно выявленным подтипом рецептора 5-НТ является рецептор 5-НТ 6, впервые клонированный из ткани крысы в 1993 году (Monsma, F.J.; Shen, Y.; Ward, R.P.; Hamblin, M.W. MolecularPharmacology 1993, 43, 320-327) и впоследствии из ткани человека (Kohen, R.; Metcalf, M.A.; Khan, N.;Druck, Т.; Huebner, K.; Sibley, D.R. Journal of Neurochemistry, 1996, 66, 47-56). Рецептор является рецептором, связанным с G-белком (GPCR), положительно связанным с аденилатциклазой (Ruat, M., Traiffort,E., Arrang, J.-M., Tardivel-Lacombe, L, Diaz, L, Leurs, R., and Schwartz, J.-C., Biochemical Biophysical Research Communications 1993, 193, 268-276). Рецептор практически полностью находится в центральной нервной системе (ЦНС) крыс и человека. Гибридизация in situ 5-HT6 рецептора мозга крыс, используя мРНК, указало на главную локализацию в участках 5-НТ проекции, включая полосатое тело, прилежащее ядро, обонятельный бугорок и гипокамп (Ward, R.P.; Hamblin, M.W.; Lachowicz, J.E.; Hoffman, В.J.;Sibley, D.R.; Dorsa, D.M. Neuroscience, 1995, 64, 1105-1111). Существует значительный потенциал терапевтического применения лигандов 5-НТ 6 у людей, базирующихся на непосредственном действии и данных доступных научных исследований. Эти исследования включают локализацию рецептора, сродство лигандов с известной in vivo активностью и разнообразные исследования на животных, осуществленные к настоящему времени. Одним из потенциальных способов применения модуляторов рецептора 5-НТ 6 является улучшение познавательной способности и памяти у людей, страдающих такими заболеваниями, как болезнь Альцгеймера. Высокие уровни рецептора, найденные в важных структурах переднего мозга, включая хвост/путамен, гипокамп, прилегающее ядро и кора, предусматривают роль рецептора в памяти и познании, поскольку, как известно, эти участки играют решающую роль в памяти (Gerard, С.; Martres, M.-P.;Lefevre, K.; Miquel, М.С.; Verge, D.; Lanfumey, R.; Doucet, E.; Hamon, M.; El Mestikawy, S. Brain Research,1997, 746, 207-219). Способность известных лигандов рецептора 5-НТ 6 улучшать холинэргическую передачу также поддерживает потенциальное когнитивное применение (Bentley, J.С.; Boursson, A.; Boess, F.G.; Kone, F.С.; Marsden, С.A.; Petit, N.; Sleight, A. J. British Journal of Pharmacology, 1999, 126(7), 15371542). В ходе исследований выяснили, что известный селективный антагонист 5-НТ 6 значительно повышает уровни глутамата и аспартата в лобной коре без повышения уровней норадреналина, допамина или 5-НТ. Известно, что такое селективное повышение уровней нейрохимикатов включено в память и когнитивные функции, что указывает на роль 5-НТ 6 лигандов в когнитивных функциях (Dawson, L.A.; Nguyen,H.Q.; Li, P. British Journal of Pharmacology, 2000, 130(1), 23-26). Исследование памяти и обучения у животных с использованием известного селективного антагониста 5-НТ 6 дало позитивные результаты(Rogers, D.С.; Hatcher, P.D.; Hagan, J.J. Society of Neuroscience, Abstracts, 2000, 26, 680). Потенциальным применением лигандов 5-НТ 6, в частности антагонистов, является лечение расстройств дефицита внимания (ADD) и расстройства внимания и гиперактивности (ADHD) у детей и взрослых (Ernst, M.; Zametkin, A.J.; Matochik, J.H.; Jons, P.A.; Cohen, R.M. Journal of Neuroscience, 1998,18(15), 5901-5907). Лиганды 5-НТ 6 также имеют потенциал относительно лечения шизофрении и депрессии. Например,клозапин (эффективное антипсихотическое лекарственное средство) имеет высокое сродство к рецепторам подтипа 5-НТ 6. Более того, несколько клинических антидепрессантов также имеют высокое сродство к рецептору и действуют как его антагонисты (Branchek, Т.A.; Blackburn, Т.P. Annual Reviews in Pharmacology and Toxicology, 2000, 40, 319-334). Нарушение когнитивной функции является ключевой характеристикой шизофрении и имеет много проявлений, включая фундаментальный дефект способности пациента манипулировать доступной информацией. Weinberger et. al. International clinical psychopharmacology, 1997, 12, 38-40. Шизофрения характеризуется значительным когнитивным расстройством, которое остается относительно стабильным,не считаясь с колебаниями других симптомов. Уровень дисфункции является значительным показателем при прогнозировании длительной нетрудоспособности. Хорошая когнитивная функция зависит от способности мозга определять приоритетные задачи и переключаться из параллельной к постепенной обработке данных при чрезмерной нагрузке. Это требует задействования исполнительной памяти. Нейровизуализация и функциональный анализ говорят о том, что такая когнитивная функция зависит от целостности предлобной активности. Появляется все больше доказательств относительно того, что антипсихотические лекарства с гидрокситриптамин-блокирующей активностью (в частности, 5-НТ 2 а) лучше влияют на когнитивную функцию у пациентов с шизофренией, чем лекарства с преимущественно допамин(D)2-блокирующей активностью (традиционные нейролептики). Соответственно улучшение или стабили-1 018369 зация когнитивной функции у пациентов с шизофренией вследствие введения антипсихотичных лекарств с гидрокситриптамин-блокирующей активностью приведет к улучшению результатов лечения. Нейрокогнитивный дефицит при шизофрении считается отдельной областью заболевания, т.е. относительно независимой от психотических симптомов, и более связан с функциональными последствиями. Нейрокогнитивный дефицит включает рабочую память, внимание/бдительность, вербальное обучение и память, визуальное обучение и память, мышление и решение проблем, скорость обработки и общественное признание (Green M.F., Nuechterlein K.H., Gold J.M., et al. "Approaching a consensus cognitivecriteria", Biol. Psychiatry 2004; 56:301-307). Кроме того, недавние исследования in vivo на крысах указывают на то, что модуляторы 5-НТ 6 могут быть полезными при лечении расстройств движения, включая эпилепсию (Stean, Т.; Routledge, С.; Upton,N. British Journal of Pharmacology, 1999, 127, Proc. Supplement 131P and Routledge, C.; Bromidge, S.M.;Moss, S.F.; Price, G.W.; Hirst, W.; Newman, H.; Riley, G.; Gager, Т.; Stean, Т.; Upton, N.; Clarke, S.E.; Brown,A.M. British Journal of Pharmacology 2000, 130(7), 1606-1612). Все вышеприведенные исследования указывают на то, что соединения, которые являются модуляторами 5-НТ 6 рецептора, т.е. лигандами, могут быть полезными при лечении следующих заболеваний,включая симптомы, связанные с болезнью Альцгеймера, такие как деменция, дефицит памяти, познания и обучение; расстройства личности, такие как шизофрения; расстройства поведения, например тревога,депрессия и синдром навязчивых состояний; лечение ADD и ADHD; расстройства движения или моторики, такие как болезнь Паркинсона и эпилепсия; заболевания, связанные с нейродегенерацией, такие как инсульт и травма головы; или абстиненция после завершения приема лекарственного средства,включая привычку к никотину, алкоголю и т.д. Учитывая то, что рецепторы 5-НТ 6 расположены практически полностью в мозге, модулирование рецепторов путем парентерального введение лекарственных средств требует, чтобы лекарство пересекло гематоэнцефалический барьер. Гематоэнцефалический барьер состоит из эндотелиальних клеток капилляров мозга с беспрерывными непроницаемыми синапсами, что практически делает невозможным попадание соединений в мозг в обход клеток (J. Bryan, Pharmaceutical Journal, 273 (2004) 475-476). Вместо этого, доступ к мозгу ограничен пассивной диффузией или активным транспортом через эндотелиальные клетки (GG, Pharmaceutical Basis of Therapeutics, 10th Ed at page 10). Соответственно, биодоступные парентерально введенные соединения, которые влияют на активность 5-НТ 6, должны иметь не только благоприятные профили растворимости для успешного попадания в кровяное русло, а еще им нужно пересечь гематоэнцефалический барьер, чтобы попасть к 5-НТ 6 рецепторам. Преимущественно, это изобретение касается соединений, способных модулировать активность рецептора 5-НТ 6 и которые являются биодоступными. Недавние клинические и доклинические исследования лигандов 5-НТ 6 описаны Rudy Schreiber, Andrew Sleight и Marie Woolley, "5-HT6 Receptors as Targets for the Treatment of Cognitive Deficits in Schizophrenia" в The Receptors Book The Serotonin Receptors, Humana Press, 2006, Pages 495-515, Edited by BryanDiscovery Today, 11 (7/8) April 2006, и Robin Emsley, "Drugs in development for the treatment of schizophrenia", Expert Opinion on Investigational Drugs, 18 (8): 1103-1118, August 2009. Девять лигандов 5-НТ 6 прошли клинические исследования на человеке. Lu-AE-58054 от Lundbeck исследовали при шизофренокогнитивном расстройстве Фаза II, SAM-531 от Wyeth исследовали при болезни Альцгеймера Фаза II, SYN-114 от Synosia Therapeutics исследовали при болезни Альцгеймера ФазаI, PRX-07034 от EPIX Pharmaceuticals Inc, исследовали при шизофрении, болезни Альцгеймера и ожирении Фаза Ib, SUVN-502 от Suven Life Sciences Ltd. исследовали при болезни Альцгеймера Фаза I, SB742457 от GlaxoSmithKline исследовали при когнитивной дисфункции, связанной с болезнью Альцгеймера Фаза II, LY-483518 от Lilly, которая выдала лицензию Saegis Pharmaceuticals (SGS-518), исследовали при нарушение когнитивных функций, связанных с шизофренией Фаза IIa, SAX-187 от Wyeth в настоящее время исследуют при тревоге Фаза I, и SB-271046 от GlaxoSmithKline исследовали при болезни Альцгеймера и шизофрении Фаза I, тем не менее были прерваны (возможно вследствие плохого проникновение через гематоэнцефалический барьер). 1-[(3-Фторфенил)сульфонил]-4-(1-пиперазинил)-1 Н-бензимидазол, 1-[(2-фторфенил)сульфонил]-4(1-пиперазинил)-1 Н-бензимидазол, 1-(3-хлорфенил)сульфонил]-4-(1-пиперазинил)-1 Н-бензимидазол, 1(1-нафталинилсульфонил)-4-(1-пиперазинил)-1 Н-бензимидазол и 1-[(2,5-дихлорфенил)сульфонил]-4-(1 пиперазинил)-1 Н-бензимидазол получали от ChemZoo, Inc. of Winston-Salem, North Carolina в 2008 г. через базу данных ChemSpider. Однако соединения никогда не предлагались к продаже. Не существует информации относительно их способности связываться с рецептором 5-НТ 6 или относительно их фармакологического действия или применения этих соединений. Не существует информации относительно их получения и способа их получения. Изобретение касается соединений, пригодных в качестве терапевтических агентов при лечении разнообразных состояний, связанных с активностью рецептора 5-НТ 6, включая психоз (например, шизофрению, тревогу или депрессию), расстройства движения (например, болезнь Паркинсона), тревогу, депрессию, зависимость от лекарственных средств, синдром навязчивых состояний, дефицит внимания или любое состояние, связанное с активностью рецептора 5-НТ 6. Эти и другие признаки этого изобретения будут более очевидными после детального описания приведенного ниже. Короткое описание изобретения Данное изобретение касается потенциальных антагонистов 5-НТ 6, представленных соединениями формулы I где значения переменных являются такими, как определено ниже. Детальное описание изобретения В одном из аспектов изобретение касается соединения формулы IR5, R6, R7, R8 и R9, каждый независимо, означают Н; или его фармацевтически приемлемой соли. В одном из вариантов осуществления R4 означает метил. Соединением формулы I является 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Н-бензимидазол или его фармацевтически приемлемая соль. В другом аспекте изобретение касается применения 2-метил-1-(фенилсульфонил)-4-пиперазин-1 ил-1 Н-бензимидазола или его фармацевтически приемлемой соли в качестве медикамента. В другом аспекте изобретение касается применения 2-метил-1-(фенилсульфонил)-4-пиперазин-1 ил-1 Н-бензимидазола или его фармацевтически приемлемой соли при модулировании функции 5-НТ 6 рецептора у субъекта. В другом аспекте изобретение касается применения 2-метил-1-(фенилсульфонил)-4-пиперазин-1 ил-1 Н-бензимидазола или его фармацевтически приемлемой соли при лечении расстройства, связанного с 5-НТ 6, где расстройством, связанным с 5-НТ 6, является заболевание или расстройство центральной нервной системы (ЦНС). В другом аспекте изобретение касается композиции для лечения расстройства, связанного с 5-НТ 6,содержащей 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Н-бензимидазол или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. В другом аспекте изобретение касается применения 2-метил-1-(фенилсульфонил)-4-пиперазин-1 ил-1 Н-бензимидазола или его фармацевтически приемлемой соли для получения медикамента для лечения расстройства, связанного с 5-НТ 6, где расстройством, связанным с 5-НТ 6, является заболевание или расстройство центральной нервной системы (ЦНС) и где расстройство, связанное с 5-НТ 6, выбирают из следующих: психоз, тревога, депрессия, эпилепсия, синдром навязчивых состояний, мигрень, когнитивные расстройства, расстройства сна, расстройства питания, анорексия, ожирение, булимия, компульсив-3 018369 ное переедание, приступы паники, расстройства, возникающие вследствие отказа от злоупотребления лекарственными средствами, нарушение когнитивных функций, связанное с шизофренией, расстройства желудочно-кишечного тракта, синдром раздраженного кишечника, расстройства памяти, болезнь Альцгеймера, болезнь Паркинсона, хорея Хантингтона, шизофрения, синдром дефицита внимания и гиперактивности, нейродегенеративные заболевания, которые характеризуются нарушением роста нейронов, и боль. В другом аспекте изобретения предпочтительное расстройство, связанное с 5-НТ 6, выбирают из следующих: депрессия, когнитивные расстройства, нарушение когнитивных функций, связанное с шизофренией, когнитивная дисфункция, связанная с болезнью Альцгеймера, и боль. В другом аспекте изобретения предпочтительным расстройством, связанным с 5-НТ 6, является болезнь Альцгеймера. В других аспектах изобретение касается способа синтеза соединения формулы I, который включает: а) взаимодействие соединения формулы IA где X означает R2 или защитную группу; с образованием соединения формулы IC где R1a, R1b и R2-R9 являются такими, как определено в формуле I; и если X означает R2, тогда образуется соединение формулы I; или если X означает защитную группу, способ дополнительно включает:b) снятие защиты с соединения формулы IC с образованием незащищенного соединения; где, если R2 означает Н, тогда получают соединение формулы I. В одном из вариантов осуществления взаимодействие соединения формулы IA с IB проводят в апротонном растворителе в присутствии основания. В одном из вариантов осуществления основанием является гидрид натрия (Na). В одном из вариантов осуществления защитная группа означает трет-бутоксикарбонил (Boc), бензил, ацетил, п-метоксибензил (РМВ) или бензилоксикарбонил (Cbz). В одном из вариантов осуществления стадия снятия защиты включает взаимодействие соединения формулы IC с трифторуксусной кислотой (TFA). В одном из вариантов осуществления GA означает гало, тозилат, мезилат, трифлат или оксо. В одном из вариантов осуществления GA означает оксо и стадия взаимодействия GA=R2 с незащищенным соединением включает восстановительное аминирование в присутствии боронового восстановительного агента. В другом аспекте изобретения способ также включает получение соединения формулы IB путем: а) взаимодействия соединения формулы ID где гало означает Cl, Br или I; и где получают соединение формулы IB. В одном из вариантов осуществления X означает защитную группу, и стадию взаимодействия соединения формулы ID с соединением формулы IE проводят в присутствии основания. В одном из вариантов осуществления основанием является бикарбонат натрия (NaHCO3), и стадию взаимодействия проводят приблизительно при 100 С. В другом аспекте изобретения способ также включает получение соединения формулы IB путем взаимодействия R4-C(OEt)3 с соединением формулы IF с образованием соединения формулы IB. В одном из вариантов осуществления стадию взаимодействия R4-C(OEt)3 с соединением формулыIF проводят в присутствии монтморилонита KSF и толуола. В другом аспекте изобретения способ также включает получение соединения формулы IF путем гидрирования соединения формулы IG где Y означает N3 или NO2. В одном из вариантов осуществления стадию гидрирования проводят в присутствии Н 2 и палладия на угле (H2/Pd-C). В другом аспекте изобретения Y означает NO2 и способ также включает получение соединения формулы IG путем: с образованием соединение формулы IG. В одном из вариантов осуществления стадию взаимодействия 2,3-динитроанилина с нитритом натрия (NaNO2) проводят в присутствии уксусной кислоты (АсОН) и бромида меди (CuBr). В одном из вариантов осуществления стадию взаимодействия проводят в присутствии 2,2'-бис(дифенилфосфино)-1,1'-бинафтила (BINAP), трис-(дибензилиденацетон)дипалладия (Pd2(dba)3), карбоната цезия (Cs2CO3) и толуола. В одном из вариантов осуществления 2,3-динитроанилин получают путем взаимодействия N-(3 нитрофенил)ацетамида с азотной кислотой (HNO3) и серной кислотой (H2SO4). В другом аспекте изобретения Y означает N3, и способ также включает получение соединения формулы IG путем:(a) взаимодействие азида натрия с 1,3-дифтор-2-нитробензолом с образованием 1-азидо-3-фтор-2 нитробензола; с образованием соединения формулы IG. В одном из вариантов осуществления стадию взаимодействия проводят в присутствии N,Nдиизопропилэтиламина (DIPEA). В одном из вариантов осуществления любую из вышеуказанных стадий проводят в протонном растворителе, апротонном растворителе, полярном растворителе, неполярном растворителе, протонном полярном растворителе, апротонном неполярном растворителе или апротонном полярном растворителе. В одном из вариантов осуществления любая из вышеуказанных стадий включает стадию очистки,которая включает, по меньшей мере, фильтрование, экстрагирование, хроматографию, растирание в порошок или перекристаллизацию. В другом варианте воплощения любая из вышеуказанных стадий включает аналитическую стадию,включающую жидкостную хроматографию (ЖХ), масс-спектроскопию (МС), жидкостную хроматографию/масс-спектроскопию (ЖХ/МС), газовую хроматографию (ГХ), газовую хроматографию/массспектроскопию (ГХ/МС), ядерный магнитный резонанс (ЯМР), тонкослойную хроматографию (ТСХ),определение точки плавления (ТП), оптическое вращение (ОВ) или элементный анализ. Представителями "фармацевтически приемлемых солей" являются, но не ограничиваются ими, например, водорастворимые и водонерастворимые соли, такие как ацетат, алюминий, амсонат (4,4 диаминостилбен-2,2-дисульфонат), бензатин (N,N'-дибензилетилендиамин), бензолсульфонат, бензоат,бикарбонат, висмут, бисульфат, битартрат, борат, бромид, бутират, кальций, кальция эдетат, камсилат(2-амино-2-(гидроксиметил)-1,3-пропандиол), валерат и цинк. Некоторые соединения данного изобретения содержат один или несколько хиральних центров и данное изобретение включает каждый отдельный энантиомер таких соединений, а также смеси энантиомеров. Когда соединения данного изобретения содержат несколько хиральных центров, изобретение включает каждую комбинацию, а также их смеси. Все хиральные, диастереомерные и рацемические формы структуры являются включенными, пока не указана конкретная стереохимия или изомерная форма. В этой области техники хорошо известно, как получить оптически активные формы, например, путем разделения рацемических форм или с помощью синтеза из оптически активных исходных материалов."Эффективное количество" по отношению к соединению данного изобретения означает количество,эффективное для ингибирования mTOR или PI3K у субъекта. Определения Следующие определения приводятся относительно соединений данного изобретения, пока не указано другое. Вообще, количество атомов углерода в определенной группе обозначается как "Сх-Су", где х и у является верхней и нижней границами соответственно. Например, группа, обозначенная как "C1-C6",содержит от 1 до 6 атомов углерода. Количество углерода, указанное в обозначении, касается углерода главной цепи и ответвлений, тем не менее не включает атомы углерода заместителей, таких как алкокси и т.д. Пока не указано другое, номенклатура четко не названных заместителей, начинается слева направо от терминальной части функциональной группы к соседней функциональной группе в направлении точки присоединения. Например, заместитель "арилалкилоксикарбонил" касается группы (C6-C14-арил)-(C1C6-алкил)-О-С(О)-. Понятно, что вышеприведенные определения не включают невозможные варианты замещения (например, метил замещен 5 атомами фтора, две гидроксильные группы на одном атоме углерода, гидроксильная группа на неароматической двойной связи). Такие невозможные замещения хорошо известны специалисту в этой области. В каждой из нижеследующих групп, когда подгруппы обозначаются с возможностью нескольких вариантов, каждый вариант выбирают независимо. Например, в ди(C1C6-алкил)амино-, например, (C1-C6-алкил)2N-, C1-C6-алкилы могут быть одинаковыми или разными."Активация" соединения касается взаимодействия соединения по реакционному центру с реагентом, с введением в этот центр активированной группы, где активированное соединение необязательно превращается в другое активированное соединение в одну или несколько стадий. Примеры активации включают галогенирование по углероду, после этого необязательно гидроборирование, где галоген превращается в необязательно замещенный боран; тозилирование, мезилирование или трифлатирование по кислороду; и нитрование по углероду, после этого необязательное восстановление нитрогруппы до аминогруппы и преобразование аминогруппы в диазогруппу."Активированная группа" является группой, которая при присоединении к центру, увеличивает реактивность при этом центре. Неограничивающими примерами активированной группы являются заместитель, присоединенный к электрофильному центру и способный к замещению нуклеофильным реагентом; заместитель, присоединенный к нуклеофильному центру и способный к замещению электрофильным реагентом; заместитель, способный к замещению радикалом; или заместитель, присоединенный к центру, где после присоединения или потери электрона, заместитель способен отделиться как анион или катион с образованием радикала по центру."Ацил-" касается группы с неразветвленной, разветвленной или циклической конфигурацией или их комбинации, присоединенной к основной структуре через карбонильную функциональную группу. Такие группы могут быть насыщенными или ненасыщенными, алифатическими или ароматическими, и карбоциклическими или гетероциклическими. При подсчете количества атомов углерода включают атом углерода карбонила. Примеры C1-C8-ацила включают НС(О)-, ацетил-, бензоил-, п-толуил, никотиноил-, пропионил-, изобутирил-, оксалил- и т.д. Нижний-ацил- касается ацильных групп, которые содержат от 1 до 4 атомов углерода. Ацил может быть незамещен или замещен одной или большим количеством следующих групп: галоген, H2N-, (C1-C6-алкил)амино-, ди(C1-C6-алкил)амино-, (C1-C6-алкил)С(О)N(C1-C3 алкил)-, (C1-C6-алкил)карбониламидо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкил)NHC(О)-, ди(C1-C6 алкил)NC(О)-, -CN, гидроксил, C1-C6-алкокси-, C1-C6-алкил-, НО 2 С-, (C1-C6-алкокси)карбонил-, C1-C8 ацил-, C6-C14-арил-, C1-C9-гетероарил- или C3-C8-циклоалкил-."Алкенил-" касается неразветвленной или разветвленной цепи ненасыщенного углеводорода, который содержит по меньшей мере одну двойную связь. Где возможны Е- и/или Z-изомеры, термин "алкенил" включает такие изомеры. Примеры C2-C6-алкенила включают, но не ограничиваются ими, этилен,пропилен, 1-бутилен, 2-бутилен, изобутилен, втор-бутилен, 1-пентен, 2-пентен, изопентен, пента-1,4 диен-1-ил, 1-гексен, 2-гексен, 3-гексен и изогексен. Алкенил может быть незамещен или замещен одной или большим количеством следующих групп: галоген, H2N-, (C1-C6-алкил)амино-, ди(C1-C6-алкил)амино-,(C1-C6-алкил)С(О)N(C1-C3-алкил)-, (C1-C6-алкил)карбониламидо-, HC(O)NH-, H2NC(O)-, (C1-C6 алкил)NHC(О)-, ди(C1-C6-алкил)NC(О)-, -CN, гидроксил, C1-C6-алкокси-, C1-C6-алкил-, НО 2 С-, (C1-C6 алкокси)карбонил-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил- и C3-C8-циклоалкил-."Алкокси-" касается группы R-O-, где R означает алкил, как указано ниже. Примеры C1-C6-алкоксивключают, но не ограничиваются ими, метокси, этокси, н-пропокси, 1-пропокси, н-бутокси и т-бутокси. Алкокси может быть незамещен или замещен одной или большим количеством следующих групп: галоген, гидроксил, C1-C6-алкокси-, H2N-, (C1-C6-алкил)амино-, ди(С 1-С 6 алкил)амино-, (C1-C6 алкил)С(О)N(C1-C3-алкил)-, (C1-C6-алкил)карбониламидо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкил)NHC(О)-,ди(C1-C6-алкил)NC(О)-, -CN, C1-C6-алкокси-, НО 2 С-, (C1-C6-алкокси)карбонил-, C1-C8-ацил-, C6-C14-арил-,C1-C9-гетероарил-, C3-C8-циклоалкил-, C1-C6-галоалкил-, C1-C6-аминоалкил-, (C1-C6-алкил)карбокси-, C1C6-карбониламидоалкил- или O2N-."Алкил-" касается углеводородной цепи с неразветвленной или разветвленной цепью, которая содержит определенное количество атомов углерода, например, C1-C10-алкил- может содержать от 1 до 10(включительно) атомов углерода. В отсутствии любого числового обозначения "алкил" является цепью(неразветвленной или разветвленной), которая содержит от 1 до 6 (включительно) атомов углерода. Примеры C1-C6-алкила включают, но не ограничиваются ими, метил, этил, пропил, бутил, пентил, гексил, изопропил, изобутил, втор-бутил, трет-бутил, изопентил, неопентил и изогексил. Алкил может быть незамещен или замещен одной или большим количеством следующих групп: галоген, H2N-, (C1-C6 алкил)амино-, ди(C1-C6-алкил)амино-, (C1-C6-алкил)С(О)N(C1-C3-алкил)-, (C1-C6-алкил)карбониламидо-,HC(O)NH-, H2NC(O)-, (C1-C6-алкил)NHC(О)-, ди(C1-C6-алкил)NC(О)-, -CN, гидроксил, C1-C6-алкокси-,C1-C6-алкил-, HO2C, (C1-C6-алкокси)карбонил-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил-, C3-C8 циклоалкил-, C1-C6-галоалкил-, C1-C6-аминоалкил-, (C1-C6-алкил)карбокси-, C1-C6-карбониламидоалкилили O2N-."Алкинил-" касается неразветвленного или разветвленного ненасыщенного углеводорода, который содержит по меньшей мере одну тройную связь. Примеры C2-C6-алкинила включают, но не ограничиваются ими, ацетилен, пропин, 1-бутин, 2-бутин, изобутин, втор-бутин, 1-пентин, 2-пентин, изопентин,пента-1,4-диин-1-ил, 1-гексин, 2-гексин, 3-гексин и изогексин. Алкинил может быть не замещен или замещен одной или большим количеством следующих групп: галоген, H2N-, (C1-C6-алкил)амино-, ди(C1C6-алкил)амино-, (C1-C6-алкил)С(О)N(C1-C3-алкил)-, (C1-C6-алкил)карбониламидо-, HC(O)NH-, H2NC(O)-,(C1-C6-алкил)NHC(О)-, ди(C1-C6-алкил)NC(О)-, -CN, гидроксил, C1-C6-алкокси-, C1-C6-алкил-, НО 2 С-,(C1-C6-алкокси)карбонил-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил- и C3-C8-циклоалкил-."Амино" касается группы H2N-. Арил- касается ароматического углеводорода. Примеры C6-C14-арила включают, но не ограничиваются ими, фенил, 1-нафтил, 2-нафтил, 3-бифен-1-ил, антрил, тетрагидронафтил, флуоренил, инданил,бифениленил и аценафтенил. Арил может быть моноциклическим или полициклическим, пока, по меньшей мере, одно кольцо является ароматическим и местом присоединения является атом углерода ароматического кольца. Арил может быть незамещен или замещен одной или большим количеством следующих групп: C1-C6-алкил-, галоген, галоалкил-, гидроксил, гидроксил(C1-C6-алкил)-, H2N-, аминоалкил-,ди(C1-C6-алкил)амино-,НО 2 С-,(C1-C6-алкокси)карбонил-,(C1-C6-алкил)карбокси-,ди(C1-C6 алкил)амидо-, H2NC(O)-, (C1-C6-алкил)амидо- или O2N-."(Арил)алкил-" касается алкила, как указано выше, где один или несколько атомов водорода алкила замещено арилом, как указано выше. (C6-C14-арил)алкил-заместителями являются: бензил, бензгидрил, 1 фенилэтил, 2-фенилэтил, 3-фенилпропил, 2-фенилпропил, 1-нафтилметил, 2-нафтилметил и т.д.(Арил)алкил- может быть незамещен или замещен одной или большим количеством следующих групп: галоген, H2N-, гидроксил, (C1-C6-алкил)амино-, ди(C1-C6-алкил)амино-, (C1-C6-алкил)С(О)N(C1-C3 алкил)-, (C1-C6-алкил)карбониламидо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкил)NHC(О)-, ди(C1-C6 алкил)NC(О)-, -CN, гидроксил, C1-C6-алкокси-, C1-C6-алкил-, НО 2 С-, (C1-C6-алкокси)карбонил-, C1-C8 ацил-, C6-C14-арил-, C1-C9-гетероарил-, C3-C8-циклоалкил-, C1-C6-галоалкил-, C1-C6-аминоалкил-, (C1-C6 алкил)карбокси-, C1-C6-карбониламидоалкил- или O2N-."Заболевание ЦНС" или "расстройство ЦНС" является заболеванием или расстройством, поражающим или начинающимся в центральной нервной системе, преимущественно болезнью, которая касается активности 5-НТ 6 или на которую влияет модулирование 5-НТ 6. Определенными заболеваниями или расстройствами ЦНС являются психоз, тревога, депрессия, эпилепсия, мигрень, когнитивные расстройства,расстройства сна, расстройства питания, анорексия, булимия, компульсивное переедание, приступы паники, расстройства возникающие вследствие отказа от злоупотребления лекарственными средствами,нарушение когнитивных функций, связанное с шизофренией, расстройства желудочно-кишечного тракта, синдром раздраженного кишечника, расстройства памяти, синдром навязчивых состояний, когнитивная дисфункция, связанная с болезнью Альцгеймера, ADD, ADHD, синдром беспокойных ног (СБН),болезнь Паркинсона, хорея Хантингтона, шизофрения, синдром дефицита внимания и гиперактивности,нейродегенеративные заболевания, которые характеризуются нарушением роста нейронов, и боль. Термин "заболевание ЦНС" или "расстройство ЦНС", использованные в данном документе, также включают симптомы другого заболевания, такой как когнитивные расстройства, связанные с шизофренией."Циклоалкил-" касается моноциклического насыщенного углеводородного кольца. Представителями C3-C8-циклоалкила- являются, но не ограничиваются ими, циклопропил, циклобутил, циклопентил,циклогексил, циклогептил и циклооктил. Циклоалкил- может быть незамещен или независимо замещен одной или большим количеством следующих групп: галоген, H2N-, (C1-C6-алкил)амино-, ди(C1-C6 алкил)амино-, (C1-C6-алкил)С(О)N(C1-C3-алкил)-, (C1-C6-алкил)карбониламидо-, HC(O)NH-, H2NC(O)-,(C1-C6-алкил)NHC(О)-, ди(C1-C6-алкил)NC(О)-, -CN, гидроксил, C1-C6-алкокси-, C1-C6-алкил-, НО 2 С-,(C1-C6-алкокси)карбонил-, C1-C8-ацил-, C6-C14-арил-, C1-C9-гетероарил- или C3-C8-циклоалкил-, C1-C6 галоалкил-, C1-C6-аминоалкил-, (C1-C6-алкил)карбокси-, C1-C6-карбониламидоалкил- или O2N-. Кроме этого, два любых атома водорода на одном и том же атоме углерода карбоциклического кольца могут быть замещены атомом кислорода с образованием оксо (=0) заместителя или два атома водорода могут быть замещены алкилендиоксигруппой, так что алкилендиоксигруппа вместе с атомом углерода, к которому она присоединена, образует 5-7-членный гетероцикл, который содержит два атома кислорода."Циклоалкенил-" касается неароматических карбоциклических колец с одним или несколькими С-С двойными связями внутри кольцевой системы. "Циклоалкенил" может иметь одно или несколько колец. Полициклические структуры могут быть мостиковыми или конденсированными кольцевыми структурами. Примеры C3-C10-циклоалкенила включают, но не ограничиваются ими, циклопропенил, циклобутенил, циклопентенил, циклогексенил, 4,4 а-окталин-3-ил и циклооктенил. Циклоалкенил может быть незамещен или независимо замещен одной или большим количеством следующих групп: галоген, H2N-, (C1C6-алкил)амино-,ди(C1-C6-алкил)амино-,(C1-C6-алкил)С(О)N(C1-C3-алкил)-,(C1-C6 алкил)карбониламидо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкил)NHC(O)-, ди(C1-C6-алкил)NC(O)-, -CN, гидроксил, C1-C6-алкокси-, C1-C6-алкил-, НО 2 С-, (C1-C6-алкокси)карбонил-, C1-C8-ацил-, C6-C14-арил-, C1-C9 гетероарил- или C3-C8-циклоалкил-, C1-C6-галоалкил-, C1-C6-аминоалкил-, (C1-C6-алкил)карбокси-, C1-C6 карбониламидоалкил- или O2N-. Кроме этого, два любых атома водорода на одном и том же атоме углерода циклоалкенильных колец могут быть замещены атомом кислорода с образованием оксо (=O) заместителя или два атома водорода могут быть замещены алкилендиоксигруппой, так что алкилендиоксигруппа вместе с атомом углерода, к которому она присоединена, образует 5-7-членный гетероцикл, который содержит два атома кислорода."Снятие защиты" касается удаления защитной группы, например, удаление бензила или ВОС группы, присоединенной к амину. Снятие защиты проводят нагреванием и/или добавлением реагентов, способных удалять защитные группы. В предпочтительных вариантах осуществления снятие защиты включает добавление кислоты, основания, восстановительного агента, окислителя, нагревание или любую их комбинацию. Один предпочтительный вариант удаления ВОС групп с аминогрупп включает прибавление к раствору HCl или TFA. Много реакций снятия защиты хорошо известны специалистам и описаны вProtective Groups in Organic Synthesis, Greene and Wuts, John WileySons, New York, NY, (3rd Edition,1999), содержимое которого включено в данный документ с помощью ссылки."Защитная группа" или "Gp" по отношению к аминогруппам, гидроксильным группам и сульфгидрильным группам касается таких форм этих групп, которые являются защищенными от нежелательных реакций защитными группами, известными специалистам, такими как те, что описаны в Protective Groupsin Organic Synthesis, Greene, T.W.; Wuts, P.G.M., John WileySons, New York, NY, (3rd Edition, 1999),содержимое которого включено в данный документ с помощью ссылки, эти группы вводят или удаляют согласно описанными здесь способам. Примеры защищенных гидроксильных групп включают, но не ограничиваются ими, силиловые эфиры, такие как эфиры, полученные путем взаимодействия гидроксильной группы с реагентом, таким как, но не ограничивающимся ими, т-бутилдиметилхлорсилан, триметилхлорсилан, триизопропилхлорсилан, триетилхлорсилан; замещенные метиловый и этиловый простые эфиры, такие как, но не ограничивающиеся ими, метоксиметиловый эфир, метилтиометиловый эфир, бензилоксиметиловый эфир, т-бутоксиметиловый эфир, 2-метоксиэтоксиметиловый эфир, тетрагидропираниловый эфир, 1-этоксиэтиловый эфир, алиловый эфир, бензиловый эфир; сложные эфиры,такие как, но не ограничивающиеся ими, бензоилформиат, формиат, ацетат, трихлорацетат и трифторацетат. Примеры защищенных аминогрупп включают, но не ограничиваются ими, амиды, такие как,формамид, ацетамид, трифторацетамид и бензамид; карбаматы; например Вос; имиды, такие как фталимид, Fmoc, Cbz, PMB, бензил и дитиосукцинимид; и другие. Примеры защищенных или кепированных сульфгидрильных групп включают, но не ограничиваются ими, тиоэфиры, такие как S-бензилтиоэфир и"Галоалкил-" касается алкила, как указано выше, где один или несколько атомов водород замещено-F, -Cl, -Br или -I. Каждое замещение выбирают независимо. Типичными примеры C1-C6-галоалкила включают, но не ограничиваются ими, -CH2F, -CCl3, -CF3, CH2CF3, -CH2Cl, -CH2CH2Br, -CH2CH2I,-CH2CH2CH2F,-CH2CH2CH2Cl,-CH2CH2CH2CH2Br,-CH2CH2CH2CH2I,-CH2CH2CH2CH2CH2Br,-CH2CH2CH2CH2CH2I, -CH2CH(Br)CH3, -СН 2 СН(Cl)СН 2 СН 3, -CH(F)CH2CH3 и -C(CH3)2(CH2Cl)."Модулирование активности рецептора 5-НТ 6" касается влияния (например, ингибирования или стимулирования) или процессов передачи сигналов, связанного с рецептором 5-НТ 6. В частности, ингибирование 5-НТ 6 увеличивает уровни ацетилхолина и глутамата в мозге, в то время как агонизм или стимулирование рецептора 5-НТ 6 приводит к увеличению клеточного цАМФ."Оксо" касается атома (=O). Как активирующая группа, "оксо" группы подвергаются восстановительному аминированию нуклеофильными аминогруппами с образованием алкиламино или аминоалкил заместителей. Предпочтительно стадию восстановительного аминирования проводят в присутствии борон-содержащего восстановительного агента."Стереоизомер" или "стереоизомеры" касается соединений, которые отличаются хиральностью или атомным присоединением по одному или нескольким стереоцентрам. Стереоизомеры включают энантиомеры, диастереомеры, а также цис-транс (E/Z) изомеры."Таутомер" касается переменных форм соединения, отличающихся положением протона, таких как энол-кето или имин-енамин таутомеры."Лечение" заболевания у субъекта касается ингибирования заболевания или задержки его развития; облегчения симптомов заболевания; или регресса заболевания. Соответственно "лечение болезни Альцгеймера", как указано в данном документе, включает облегчение симптомов болезни Альцгеймера, облегчение деменции, связанной с болезнью Альцгеймера, или лечение когнитивной дисфункции, связанной с болезнью Альцгеймера. Кроме этого, "лечение шизофрении" включает облегчение или стабилизацию когнитивной дисфункции и облегчение нарушения когнитивных функций, связанных с шизофренией. Термин "необязательно замещен", пока не указано другое, как указано в данном документе, означает, что по меньшей мере один атом водорода, необязательно замещенной группы, замещен галогеном,H2N-, (C1-C6-алкил)амино-, ди(C1-C6-алкил)амино-, (C1-C6-алкил)С(О)N(C1-C3-алкилом)-, (C1-C6 алкил)карбониламидо-, HC(O)NH-, H2NC(O)-, (C1-C6-алкил)NHC(О)-, ди(C1-C6-алкил)NC(О)-, -CN, гидроксилом, C1-C6-алкокси-, C1-C6-алкилом-, НО 2 С-, (С 1-С 6 алкокси)карбонилом-, С 1-С 8 ацилом-, С 6-С 14 арилом-, С 1-С 9-гетероарилом- или C3-C8-циклоалкилом-. Понятно, что во всех вышеприведенных замещенных группах, полимеры, которые попадают под определенные заместители с дополнительными за-9 018369 местителями, которые являются такими же самыми как и они (например, замещенный арил, который содержит замещенную арильную группу как заместитель, который замещен замещенным арилом, который также замещен замещенным арилом и т.д.) не являются предназначенными для включения в данный документ. В таких случаях, максимальное количество заместителей равняется трем. Например, серийные замещения замещенных арильных групп двумя другими замещенными арильными группами ограничивается замещенный арил-(замещенный арил)-замещенный арил. Соединения данного изобретения проявляют 5-НТ 6 модулирующую активность и поэтому могут использоваться для лечения пациентов, которые страдают от заболевания или расстройства центральной нервной системы (ЦНС), которое включает введение субъекту соединения, описанного в данном документе, в частности соединения формулы I. В другом варианте воплощения заболевание или расстройство (ЦНС) означает следующие: психоз,тревогу, депрессию, эпилепсию, синдром навязчивых состояний, мигрень, когнитивные расстройства,расстройства сна, расстройства питания, анорексию, булимию, компульсивное переедание, приступы паники, расстройства, возникающие вследствие отказа от злоупотребления лекарственными средствами,шизофрению, расстройства желудочно-кишечного тракта, синдром раздраженного кишечника, расстройства памяти, когнитивную дисфункцию, связанную с болезнью Альцгеймера, болезнь Паркинсона, хорею Хантингтона, шизофрению, синдром дефицита внимания и гиперактивности, нейродегенеративные заболевания, которые характеризуются нарушением роста нейронов, или боль. Другой вариант воплощения изобретения касается способа улучшения или стабилизации когнитивной функции у субъекта, который включает введение субъекту соединения, описанного в данном документе, в частности соединения формулы I или его или фармацевтически приемлемой соли. В другом варианте воплощения когнитивную функцию стабилизируют или улучшают у пациента,который страдает от шизофрении. Для терапевтического применения фармакологически активное соединение формулы I обычно вводятся в виде фармацевтических композиций, которые содержат, как необходимый активный ингредиент,по меньшей мере одно такое соединение вместе с твердым или жидким фармацевтически приемлемым носителем и, необязательно, с фармацевтически приемлемыми адъювантами и наполнителями с применением стандартных методик. Фармацевтические композиции данного изобретения включают пригодные лекарственные формы для перорального, парентерального (включая подкожное, внутримышечное, интрадермальное, внутривенное), бронхиального или назального введения. Таким образом, в случае использования твердого носителя, композицию можно формировать в таблетки, помещать в твердые желатиновые капсулы в форме порошка или гранулята или в форме саше, или лозенгов. Твердый носитель может содержать обычные наполнители, такие как связующие агенты, наполнители, лубриканты, которые используют при изготовлении таблеток, дезинтегранты, смачивающие агенты и т.д. В случае необходимости, таблетка может иметь пленочное покрытие, нанесенное обычным путем. В случае применения жидкого наполнителя лекарственная форма может находиться в форме сиропа, эмульсии, мягкой желатиновой капсулы, стерильного раствора для инъекции, водной или неводной жидкой суспензии или может быть сухим продуктом для восстановления водой или другим пригодным растворителем перед применением. Жидкие лекарственные формы могут содержать обычные добавки, такие как суспендирующие агенты, эмульгаторы,смачивающие агенты, неводные растворители (включая съедобные масла), консерванты, а также ароматизаторы и/или красители. Для парентерального введения растворитель по обыкновению содержит стерильную воду, по меньшей мере большую часть, хотя также можно использовать солевые растворы, растворы глюкозы и т.д. Также применяют инъецируемые суспензии, в этом случае используют обычные суспендирующие агенты. К парентеральным лекарственным формам также прибавляют обычные консерванты, буферирующие агенты и т.д. Особенно пригодным является введение соединения формулы I непосредственно в парентеральной форме. Фармацевтические композиции получают с помощью обычных технологий, соответствующих желаемой лекарственной форме, которая содержит соответствующее количество активного ингредиента, т.е. соединение формулы I согласно изобретению. См., например,Remington: The Science and Practice of Pharmacy, 20th Edition. Baltimore, MD: Lippincott WilliamsWilkins, 2000. Дозировка соединений формулы I для получения терапевтического эффекта будет зависеть не только от таких факторов, как возраст, масса и пол пациента и путь введения, а и от уровня активирующей активности калиевого канала и силы действия примененного соединения на определенное расстройство или заболевание. Считается, что лечение и доза определенного соединения может быть назначена в виде единичной дозированной формы и специалист в этой области подкорректирует единичную дозированную форму согласно нужному уровню активности. Решение относительно конкретной дозы и частоты введений в день принимается врачом, и может изменяться путем изменения дозы с подгонкой к определенным условиям этого изобретения с целью получения желаемого терапевтического действия. Пригодная доза соединения формулы I или его фармацевтической композиции для млекопитающего, включая человека, который страдает или вероятно страдает любым из состояний, описанным в данном документе, является количеством активного ингредиента от приблизительно 0,01 до 10 мг/кг массы тела. Для парентерального введения доза находится в диапазоне от 0,1 до 1 мг/кг массы тела при внутривенном введении. Для перорального введения доза находится в диапазоне от приблизительно 0,1 до 5 мг/кг массы тела. Активный ингредиент предпочтительно вводить в равных дозах 1-4 раза в день. Однако по обыкновению вводят небольшую дозу и ее постепенно увеличивают, доводя до оптимальной для пациента, которого лечат. Однако, разумеется, что количество фактически введенного соединения определяется врачом, учитывая соответствующие обстоятельства, включая состояние, подвергающееся лечению, выбор вводимого соединения, выбранный путь введения, возраст, массу и ответ пациента, а также тяжесть симптомов пациента. Количеством соединения данного изобретения или его фармацевтически приемлемой соли является количество, эффективное для модулирования активности рецептора 5-НТ 6 у субъекта. Кроме этого, для идентификации диапазона оптимальной дозы необязательно используют in vitro или in vivo анализы. Точное значение дозы также зависит от пути введения, состояния, тяжести состояния, а также от разнообразных физических факторов, связанных с пациентом, и определяется врачом. Эквивалентные дозы вводят через разные промежутки времени, включая, но не ограничиваясь следующими, приблизительно каждые 2 ч, приблизительно каждые 6 ч, приблизительно каждые 8 ч, приблизительно каждые 12 ч, приблизительно каждые 24 ч, приблизительно каждые 36 ч, приблизительно каждые 48 ч, приблизительно каждые 72 ч, приблизительно каждую неделю, приблизительно каждые две недели, приблизительно каждые три недели, приблизительно каждый месяц и приблизительно каждые два месяца. Количество и частота введений полного курса лечения определяется врачом. Количества эффективной дозы, описанные в данном документе, касаются общего введенного количества; т.е. в случае введения больше чем одного соединения данного изобретения или его фармацевтически приемлемой соли, количества эффективной дозы отвечают общему введенному количеству. В одном из вариантов осуществления соединение данного изобретения или его фармацевтически приемлемую соль вводят одновременно с другим терапевтическим агентом. В одном из вариантов осуществления вводят композицию, которая содержитэффективное количество соединения данного изобретения или его фармацевтически приемлемую соль и эффективное количество другого терапевтического агента в одной композиции. Эффективное количество другого терапевтического агента хорошо известно специалистам в области. Однако средний специалист в данной области может определить диапазон эффективного количества другого терапевтического агента. Соединение данного изобретения или его фармацевтически приемлемая соль и другой терапевтический агент могут взаимодействовать аддитивно, в одном из вариантов осуществления синергически. В одном из вариантов осуществления изобретения, когда животным вводят другой терапевтический агент, эффективное количество соединения данного изобретения или его фармацевтически приемлемой соли меньше, чем его эффективное количество в отсутствии другого терапевтического агента. В этом случае, без привязки к теории, считается, что соединение данного изобретения или его фармацевтически приемлемая соль и другой терапевтический агент взаимодействуют синергически. В другом аспекте изобретения используют наборы, которые включают одно или несколько соединений изобретения. Показательные наборы включают ингибитор 5-НТ 6 изобретения (например, соединение формулы I) и вкладыш или другую памятку, включая пути лечения заболеваний ЦНС путем введения эффективного количества соединения данного изобретения. Схема, показанная на схеме 1 ниже, и способы получения после схемы описывают синтез соединений данного изобретения. Определенные вариации описанных процедур, очевидные специалисту в данной области, являются включенными в рамки данного изобретения. Схема 1 описывает получение соединения формулы I и его промежуточных соединений. Реагенты на каждой стадии включают:l) бис-(2-хлоретил)алкиламин, NaHCO3, 1-бутанол, 115C. Соединения 6 получают или способом А, или способом В. В примере способа A N-(3 нитрофенил)ацетамид нитровали по методике, описанной в литературе, получая 2,3-динитроанилин (2). После этого соединение 2 превращали в 2,3-динитробромбензол, используя нитрит натрия и бромид меди. Последний промежуточный продукт реагировал с Вос-пиперазином, образуя желаемый продукт 3. Восстановление промежуточного продукта 3 давало соответствующий анилин 6. Альтернативно, соединение 6 можно получить в две стадии, например, из имеющегося в продаже 2,6-дифторнитробензола. В результате реакции соединения 4 с азидом натрия и Вос-пиперазином получали промежуточное соединение 5. Последующее восстановление соединения 5 давало соединение 6. Бензимидазольное ядро 7 можно получить при разных условиях, определенных в литературе, таких как нагревание соединения 6 в толуоле в присутствии монтморилонита KSF и триэтилортоформиата. Промежуточный сульфон 8 может быть получен реакцией соединения 7 с соответствующим замещенным арилсульфоном. Снятие защиты и последующее восстановительное аминирование соединения 8, используя приемлемый альдегид,давало желаемое соединение формулы I. Альтернативно, соединения формулы I можно получить из промежуточного соединения 10, которое, в свою очередь, получают взаимодействием промежуточного соединения 9 с бис-(2-хлорэтил)алкиламином. Специалист в данной области понимает, что схема 1 может быть адаптирована для получения другого соединения формулы I и фармацевтически приемлемых солей соединения формулы I согласно с данным изобретением. Примеры В данном документе использованы следующие аббревиатуры и они имеют следующие значения:ACN означает ацетонитрил; АсОН означает уксусную кислоту;Celite является флюс-кальцинированной диатомовой землей. Celite является зарегистрированной торговой маркой фирмы World Minerals Inc.;[3H]-LSD означает меченный тритием диэтиламид лизергиновой кислоты; основание Хюнига означает диизопропилэтиламин; ВЭЖХ означает высокоэффективную жидкостную хроматографию;MeCN означает ацетонитрил; МеОН означает метанол; МС означает масс-спектрометрию; ЯМР означает ядерный магнитный резонанс;PBS означает фосфатный солевой буфер (рН 7,4);THF означает тетрагидрофуран; ТСХ означает тонкослойную хроматографию; ТМС означает тетраметилсилан;PVT WGA SPA означает сцинтилляционный анализ сближения поливинилтолуиден агглютинин зародышей пшеницы. Способы синтеза. Каждый из следующих способов отвечает вышеприведенной схеме 1, где R1 означает Н, m равняется 0 и GP означает Boc. Соединения и/или промежуточные соединения охарактеризованы с помощью ЖХ масс-спектрометрии, осуществленной на ВЭЖХ Agilent и масс-спектрометре Hewlett-Packard с колонкойOnyx Monolithic C18 (1003,0 мм): система растворителя: 10-100% ацетонитрил в воде, скорость потока: 1,8 мл/мин, диапазон молекулярной массы 200-700. Спектры ядерного магнитного резонанса (ЯМР) соединений снимали на приборе Varian NMR с частотой 400 МГц (Palo Alto, CA). Спектральной точкой отсчета является или ТМС, или известный химический сдвиг растворителя. Некоторые образцы соединений анализировали при повышенных температурах (например, 75 С) для повышения растворимости образца. Нужно понимать, что органические соединения согласно изобретению могут проявлять таутомерию. Учитывая то, что химические структуры в этом описании могут представлять только одну из возможных таутомерных форм, разумеется, что изобретение включает любую таутомерную форму изображенной структуры. Способ А. Получение 2,3-динитроанилина (2). 2,3-Динитроанилин получают из N-(2,3-динитрофенил)ацетамида, который, в свою очередь, получают из коммерчески доступного 3-нитроацетамида, как описано на нижеследующей схеме: А. N-(2,3-динитрофенил)ацетамид. К перемешиваемой смеси концентрированной серной кислоты (216 мл) и 90% азотной (дымящей) кислоты (216 мл), охлажденной до -3 С, прибавляли порциями 3-нитроацетанилид (12,0 г) на протяжении 20 мин. Смесь перемешивали на протяжении 30 мин при -10 С. После этого реакционную смесь нагревали до комнатной температуре на протяжении 1 ч и выливали на измельченный лед (600 мл), получая желтое твердое вещество. Полученный осадок собирали отсасыванием. Полученное твердое вещество растворяли в кипящем этаноле (125 мл) и раствор оставляли стоять на протяжении 2 ч. Полученные светло-желтые иглы фильтровали, промывали этанолом и высушивали на воздухе, получая желаемый продукт (3,1 г, 21%). См. Arnold Т. Nielsen, Ronald L. Atkins, William P. Norris, Clifford L. Coon, MichaelE. Sitzmann J. Org. Chem.; 1980; 45(12): 2341-2347 (включен в данный документ как ссылка). Химическая формула: C8H7N3O5. Молекулярная масса: 225,16. МС (ЭС) m/z 226. В. 2,3-Динитроанилин. К раствору N-(2,3-динитрофенил)ацетамида (3,0 г) в метаноле (200 мл) прибавляли метоксид натрия(72 мг). Перемешанный раствор кипятили с обратным холодильником на протяжении 3 ч. К раствору прибавляли воду (300 мл), собирали желтый твердый осадок и высушивали, получая желаемый продукт(2,27 г, 93%). Химическая формула: C6H5N3O4. Молекулярная масса: 183,12. МС (ЭС) m/z 184. Получение трет-бутил 4-(2,3-динитрофенил)пиперазин-1-карбоксилата (3). Соединение 3 получали по нижеследующей схеме: 1-Бром-2,3-динитробензол. Раствор 2,3-динитроанилина (2,27 г, 12,4 ммоль) в 35 мл ледяной уксусной кислоты каплями прибавляли к перемешиваемому и охлажденному раствору нитрита натрия (0,95 г, 13,8 ммоль) в концентрированной серной кислоте (7 мл), в это время температуру реакции поддерживали на уровне 15-20 С. Полученный раствор диазония прибавляли на протяжении 5 мин к перемешиваемому раствору бромида меди (1,85 г, 12,9 ммоль) в смеси HBr (48%) (10 мл) и воды (10 мл), нагретой до 75-80 С. После прибавления смесь охлаждали до комнатной температуры и прибавляли к воде (500 мл). Светло-зеленый порошок фильтровали из раствора и высушивали в вакууме при комнатной температуре получая желаемый 1 бром-2,3-динитробензол (3,0 г, 99%). Этот продукт использовали в следующей реакции без дальнейшей очистки. См. Donald L. Vivian J. Org. Chem. 1956, 21, 1188. Соединение 3. Смесь 1-бром-2,3-динитробензола (1,0 г, 4,05 ммоль), N-Boc-пиперазина (0,90 г, 4,86 ммоль), карбоната цезия (1,58 г, 4,86 ммоль), BINAP (0,113 г, 0,182 ммоль) и трис-(дибензилиденацетон)дипалладия(0,111 г, 0,121 ммоль) в толуоле (12,0 мл) кипятили с обратным холодильником на протяжении 4 ч. Упаривали толуол и остаток растворяли в дихлорметане (100 мл), промывали водой, высушивали над сульфатом натрия и фильтровали. Дихлорметан упаривали и остаток хроматографировали на силикагеле, используя гексан/этилацетат (30-70% EtOAc), получая желаемый продукт 3 (0,37 г, 26%). МС (ЭС) m/z 353. См. Shashank Shekhar, Per Ryberg, John F. Hartwig, Jinu S. Mathew, Donna G. Blackmond, Eric R.Strieter, and Stephen L. Buchwald J. Am. Chem. Soc. 2006 128, 3584-3591 (включен в данный документ как ссылка). Получение трет-бутил 4-(2,3-диаминофенил)пиперазин-1-карбоксилата (6) из соединения (3) Способ А. трет-Бутил 4-(2,3-динитрофенил)пиперазин-1-карбоксилат (3) растворяли в этаноле (8,0 мл) и к нему прибавляли 10% Pd-C (30 мг). Гидрирование этой смеси завершали в аппарате Парра при 33 пси на протяжении ночи. Смесь фильтровали через CELITE и хроматографировали на колонке с силикагелем,используя дихлорметан и этилацетат (15-50% EtOAc), получая желаемый продукт в виде светлокоричневого аморфного твердого вещества (0,129 г, 79%). МС (ЭС) m/z 293 Получение трет-бутил 4-(3-азидо-2-нитрофенил)пиперазин-1-карбоксилата (5) Соединение 5 получают из соединения 4 по следующей схеме: К перемешиваемому раствору 2,6-дифторнитробензола (2,0 г, 12,6 ммоль) в ДМСО (6,0 мл) при комнатной температуре прибавляли азид натрия (0,82 г; 12,6 ммоль). Через 18 ч раствор выливали в 200 мл ледяной воды. Осадок, 1-азидо-3-фтор-2-нитробензол, собирали и высушивали в вакууме (2,26 г; 99%). 1 Н ЯМР (CDCl3, 400 МГц)7,00 (т, J=8,8 Гц, 1 Н); 7,07 (д, J=8,35 Гц, 1 Н); 7,47 (дт, J=8,35, 5,68 Гц,1 Н). МС (ЭС) m/z 182,1. Получение соединения 5. К раствору 1-азидо-3-фтор-2-нитробензола (0,35 г; 1,9 ммоль) в ДМСО (2,0 мл) прибавляли Воспиперазин (0,40 мл; 1,2 экв.) и N-Boc-пиперазин (1,2 экв.). Раствор нагревали при 60 С на протяжении 6 ч. После окончания реакции раствор выливали в воду (50 мл) и экстрагировали этилацетатом. Органический раствор высушивали над Na2SO4, фильтровали и упаривали при пониженном давлении. Остаток хроматографировали на кремнеземе, используя дихлорметан/метанол. Очищенный продукт 5 кристаллизовали из диэтилового эфира и гексана. МС (ЭС) m/z 348,2. Получение трет-бутил 4-(2,3-диаминофенил)пиперазин-1-карбоксилата (6) из соединения (5) (способ В).(0,37 г). Гидрирование этой смеси завершали в аппарате Парра 33 пси на протяжении 2 ч. Смесь фильтровали через Celite и хроматографировали на колонке с силикагелем, используя дихлорметан и этилацетат (15-50% EtOAc), получая желаемый продукт в виде светло-коричневого аморфного твердого вещества (1,97 г, 97%). МС (ЭС) m/z 293. К фенилендиамину (6) прибавляли триэтилортоформиат и толуол, после чего прибавляли 17 мг монтморилонита KSF. Смесь кипятили с обратным холодильником на протяжении ночи. Толуол упаривали и остаток хроматографировали на кремнеземе, используя обычный этилацетат и получая желаемый продукт (7). Общая методика получения трет-бутил 4-(2-алкил-1-арилсульфонил)-1 Н-бензо[d]имидазол-4 ил)пиперазина (8) из соединения 7 К смеси замещенного или незамещенного трет-бутил 4-(2-алкил-1 Н-бензо[d]имидазол-4 ил)пиперазина (7) в 5 мл DMF прибавляли гидрид натрия (2,0 экв.) при 0 С. Полученную суспензию перемешивали при комнатной температуре на протяжении 30 мин, после чего прибавляли замещенный или незамещенный арилсульфонилхлорид. Смесь перемешивали при комнатной температуре до завершения реакции, как показано с помощью ЖХ/МС. Раствор выливали в 100 мл Н 2 О и полученное твердое вещество отделяли от раствора фильтрованием с отсасыванием и высушивали в вакууме. Методика получение 2-алкил-4-(4-алкилпиперазин-1-ил)-1-(арилсульфонил)-1 Н-бензо[d]имидазола Соединение 8 растворяли в дихлорметане (CH2Cl2), после чего прибавляли в избыток TFA. Смесь перемешивали при комнатной температуре до завершения реакции, как показано с помощью ЖХ/МС. Растворитель удаляли в вакууме и суспендировали в дихлорметане, после чего прибавляли карбонат натрия калия. Реакционную смесь фильтровали через слой Celite и фильтрат упаривали в вакууме, получая желаемое свободное основание. Когда R2 не означает Н, к смеси свободного основания в дихлорэтане прибавляли альдегид (1,20 экв.), после чего прибавляли триацетоксиборгидрид натрия (1,6 экв.). Реакционную смесь перемешивали на протяжении ночи, растворитель упаривали и остаток очищали с помощью флэш-хроматографии, используя дихлорметан/метанол (5-20%). Методика получения 2-алкил-4-(4-алкилпиперазин-1-ил)-1-(арилсульфонил)-1 Н-бензо[d]имидазола(I) из соединения (10). Способ D. Соединение формулы I альтернативно получают из промежуточного соединения 10 по общей методике, описанной для получения соединения 8. Методика получения соединения (10). Смесь 4-аминобензимидазола, бис-(хлорэтил)алкиламина перемешивали в 25 мл 1-бутанола с бикарбонатом натрия (3,0 экв.). Смесь кипятили с обратным холодильником (115 С масляная баня) на протяжении ночи. Смесь охлаждали, фильтровали через слой Celite и фильтрат концентрировали в вакууме. Неочищенный остаток очищали на колонке с силикагелем, получая желаемый продукт. См. также методику синтеза, приведенную в WO 2006/009734; Villemin et al., Synthetic Communications, 1996,26(15), 2895-2899 и Marcos et al., Tetrahedron, 1991, 47(35), 7459-64 (включен в данный документ как ссылка). Каждый из следующих примеров соединений получали по вышеприведенной методике. Пример 1. 2-Метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Н-бензимидазол Это соединение получали, как описано выше. МС (ЭС) m/z 357,0. 1 Н ЯМР (400 МГц, ДМСО-d6)млн ч. 2,78 (с, 3 Н); 2,81-2,86 (м, 4 Н); 3,27-3,33 (м, 5 Н); 6,67 (д, J=8,1 Гц, 1 Н); 7,19 (т, J=8,2 Гц, 1 Н); 7,39 (д, J=8,1 Гц, 1 Н); 7,65 (т, J=7,9 Гц, 2 Н); 7,77 (т, J=7,4 Гц, 1 Н); 8,04 (д,J=7,6 Гц, 2 Н). Биологические исследования Сродство связывания 5-НТ 6.CHO-Dukx-A2 клетки, экспрессирующие 5-НТ 6 подтип рецептора серотонина (клон 50-7), выращенные сращенными группами по 10 клеток, разделяли и собирали в PBS буфере, который содержал 5 мМ EDTA, используя стандартные протоколы по сбору клеток, после чего центрифугировали при 2000 об/мин на протяжении 10 мин (супернатант сливали) или получали в виде влажного клеточного осадка от Applied Cell Sciences (Rockville, MD). Осадок осторожно ресуспендировали с соответствующим количеством PBS буфера (GIBCO 14040-133), который содержал MgCl2 и CaCl2, для получения конечной концентрации 40106 клеток/мл. Аликвоты клеточной суспензии прибавляли в пробирки для микроцентрифугирования, центрифугировали при 2000 об/мин на протяжении 10 мин, супернатант сливали и хранили как сухой осадок при -80 С. Уровень белка измеряли в 5 мкл лизата, смешанного с 200 мкл разбавленного реагента Bradford, используя в качестве стандарта гамма-глобулин плазмы быка. Эксперименты связывания проводили в общем объеме 200 мкл, используя 96-луночный микротитропланшет (Packard Optiplate). В день анализа клетки размораживали и ресуспендировали с достаточным количеством буфера (т.е. PBS, который содержит MgCl2 и CaCl2, (GIBCO 14040-133), дополненного дополнительным количеством MgCl2 для получения конечной концентрации 10 мМ), получая 40-80 мкг или 100-200 клеток/лунку. К каждой лунке микротитропланшета прибавляли 20 мкл 10 исследуемого соединения в воде, которая содержала 3,3% ДМСО, 3 нМ [3H]-LSD (GE, SA: 80 Ci/ммоль), клетки и буфер исследования объединяли, получая объем 150 мкл. Буфер исследования и 10 мкм холодного метиотепина замещали исследуемым соединением в отдельных лунках для определения "общего" и "неспецифического" связывания соответственно. Период инкубации инициировали путем прибавления 50 мкл 10 мг/мл гранул PVT WGA SPA (RPNQ0060, Amersham GE Healthcare), смешанных в буфере для исследования с конечной концентрацией 1 мг/лунку. Планшеты герметизировали и осторожно встряхивали при комнатной температуре, используя орбитальный шейкер (позиция 1,5) до достижения равновесия(2-6 ч). Радиоактивность (СРМ) измеряли с помощью Packard TopCount (1 мин измерения/лунку). Специфическое связывание описано, как общая связанная радиоактивность, которая меньше, чем количество связанное в присутствии 10 мкм метиотепина, и касается неспецифического связывания(NSB). Связывание в присутствии разных концентраций исследуемых соединений выражалось, как процент специфического связывания в отсутствии соединения:(Связанное-NSB)/(Общее-NSB)100=% Общее. Регрессивный анализ % связывания десяти концентрации представлен в GraphPad Prism, XL Fit или эквивалентном программном обеспечении. Значение IC50 рассчитывали, используя логистическую модель достраивания кривой с четырьмя параметрами и значения Ki, рассчитывали по приведенному ниже уравнению Ченга-Прусофа: где L означает использованную концентрацию радиоактивного лиганда в нМ;Kd означает константу диссоциации лиганда рецептора; Kd для [3H]-LSD в формате SPA связывания 3 нМ. Ссылаясь на нижеследующие примеры, синтезировали соединения данного изобретения, используя описанные в данном документе способы или другие известные в данной области способы. Соединения в таблице получали, как описано выше, и исследовали на связывание 5-НТ 6 согласно с приведенным выше биологическим исследованием. В этом описании приведены ссылки на разные публикации. Описания этих публикаций включены в данное описание с целью более полного описания предыдущего уровня техники, известного специалистам в данной области на дату создания описания изобретения и формулы изобретения. Хотя были проиллюстрированы и описаны определенные варианты воплощения данного изобретения, специалистам в данной области очевидно, что могут иметь место разнообразные изменения и модификации без отхода от сути и рамок изобретения. Поэтому формула изобретения охватывает все такие изменения и модификации, которые не выходят за рамки этого изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Соединение, представляющее собой 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Нбензимидазол или его фармацевтически приемлемую соль. 2. Применение 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1 Н-бензимидазола или его фармацевтически приемлемой соли в качестве медикамента. 3. Применение по п.2 при модулировании функции 5-НТ 6 рецептора у субъекта. 4. Применение по п.2 при лечении расстройства, связанного с 5-НТ 6. 5. Применение по п.4, где расстройством, связанным с 5-НТ 6, является заболевание или расстройство центральной нервной системы (ЦНС). 6. Композиция для лечения расстройств, связанных с 5-НТ 6, содержащая соединение по п.1 и фармацевтически приемлемый носитель. 7. Применение соединения по п.1 для получения медикамента для лечения расстройства, связанного с 5-НТ 6. 8. Применение по п.7, где расстройством, связанным с 5-НТ 6, является заболевание или расстройство центральной нервной системы (ЦНС). 9. Применение по п.7 или 8, где расстройство, связанное с 5-НТ 6, выбирают из следующих: психоз,тревога, депрессия, эпилепсия, синдром навязчивых состояний, мигрень, когнитивные расстройства, расстройства сна, расстройства питания, анорексия, ожирение, булимия, компульсивное переедание, приступы паники, расстройства, возникающие вследствие отказа от злоупотребления лекарственными средствами, нарушение когнитивных функций, связанное с шизофренией, расстройства желудочнокишечного тракта, синдром раздраженного кишечника, расстройства памяти, болезнь Альцгеймера, болезнь Паркинсона, хорея Хантингтона, шизофрения, синдром дефицита внимания и гиперактивности,нейродегенеративные заболевания, которые характеризуются нарушением роста нейронов, и боль. 10. Применение по п.9, где расстройство, связанное с 5-НТ 6, выбирают из следующих: депрессия,когнитивные расстройства, нарушение когнитивных функций, связанное с шизофренией, когнитивная дисфункция, связанная с болезнью Альцгеймера, и боль. 11. Применение по п.9, где расстройством, связанным с 5-НТ 6, является болезнь Альцгеймера.
МПК / Метки
МПК: A61K 31/496, C07D 487/08, C07D 235/22, A61P 25/00, C07D 403/04
Метки: композиция, 2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1н-бензимидазол, применение, содержащая
Код ссылки
<a href="https://eas.patents.su/19-18369-2-metil-1-fenilsulfonil-4-piperazin-1-il-1n-benzimidazol-ego-primenenie-i-soderzhashhaya-ego-kompoziciya.html" rel="bookmark" title="База патентов Евразийского Союза">2-метил-1-(фенилсульфонил)-4-пиперазин-1-ил-1н-бензимидазол, его применение и содержащая его композиция</a>
Предыдущий патент: Способ введения и удаления из ствола скважины фильтрационной корки
Следующий патент: Блочная система параллельно расположенных контейнеров для электролиза металлов
Случайный патент: Безопасный платеж и способ выставления счета с использованием номера мобильного телефона или абонентского лицевого счета