Нецеолитные нанокомпозитные материалы для твердых кислотных катализаторов
Формула / Реферат
1. Каталитическое соединение, представленное обобщенной формулой
R1/R4/R2-R3,
в которой R1 представляет металл, или металлический сплав, или биметаллическую систему;
R2 представляет любое металлическое легирующее вещество;
R3 представляет оксид металла или смеси любых оксидов металлов;
R4 выбирают из WOx, MoOx, SO42- или PO43-; и
x представляет целое или дробное число между 2 и 3, включительно.
2. Каталитическое соединение по п.1, в котором R1 представляет металл группы VIII.
3. Каталитическое соединение по п.1, в котором R1 представляет комбинацию металлов группы VIII.
4. Каталитическое соединение по п.2, в котором R1 выбирают из платины, палладия, иридия, родия или их комбинации.
5. Каталитическое соединение по п.1, в котором R1 выбирают из сплава или биметаллических систем Pt-Sn, Pt-Pd или Pt-Ge.
6. Каталитическое соединение по п.1, в котором R2 выбирают из группы Al3+, Ga3+, Ce4+, Sb5+, Sc3+, Mg2+, Co2+, Fe3+, Cr3+, Y3+, Si4+ и In3+.
7. Каталитическое соединение по п.6, в котором R2 представляет Al3+.
8. Каталитическое соединение по п.1, в котором R3 выбирают из оксида циркония, оксида титана, оксида олова, оксида железа или оксида церия.
9. Каталитическое соединение по п.8, в котором R3 представляет ZrO2.
10. Каталитическое соединение по п.1, в котором отношение металлического легирующего вещества к металлу в оксиде составляет меньше или равно примерно 0,20.
11. Каталитическое соединение по п.10, в котором отношение металлического легирующего вещества к металлу в оксиде составляет меньше или равно примерно 0,05.
12. Каталитическое соединение по п.10, в котором отношение металлического легирующего вещества к металлу в оксиде составляет примерно 0,05.
13. Каталитическое соединение по п.1, в котором R4 представляет WOx, где x представляет целое или дробное число между 2 и 3, включительно.
14. Каталитическое соединение по п.13, в котором х равен примерно 3.
15. Каталитическое соединение по п.13, в котором х равен примерно 2,9.
16. Способ изомеризации алканового или алкильного фрагмента, включающий реакционную стадию контактирования катализатора с алкилом, где указанный катализатор выбирают из соединений, представленных обобщенной формулой
R1/R4/R2-R3,
в которой R1 представляет металл, или металлический сплав, или биметаллическую систему;
R2 представляет любое металлическое легирующее вещество;
R3 представляет оксид металла или смеси любых оксидов металлов;
R4 выбирают из WOx, MoOx, SO42- или PO43-; и
x представляет целое или дробное число между 2 и 3, включительно.
17. Способ по п.16, в котором алкановой изомеризацией является изомеризация неразветвленного алкана.
18. Способ по п.17, в котором алкановой изомеризацией является изомеризация C4-C10-алкана.
19. Способ по п.18, в котором алкильной изомеризацией является изомеризация C6-C8-алкана.
20. Способ по п.16, в котором реакционная стадия имеет место при температуре ниже 210шC.
21. Способ по п.16, в котором реакционная стадия имеет место при температуре ниже 170шC.
22. Способ по п.16, в котором реакционная стадия имеет место при температуре ниже 150шC.
23. Способ по п.16, в котором выход реакции составляет более 70%.
24. Способ по п.23, в котором выход реакции составляет более 80%.
25. Способ по п.16, в котором алкановая изомеризация увеличивает октановое число алкана.
26. Каталитическое соединение, представленное формулой Pt/WO3/Al-ZrO2.
Текст
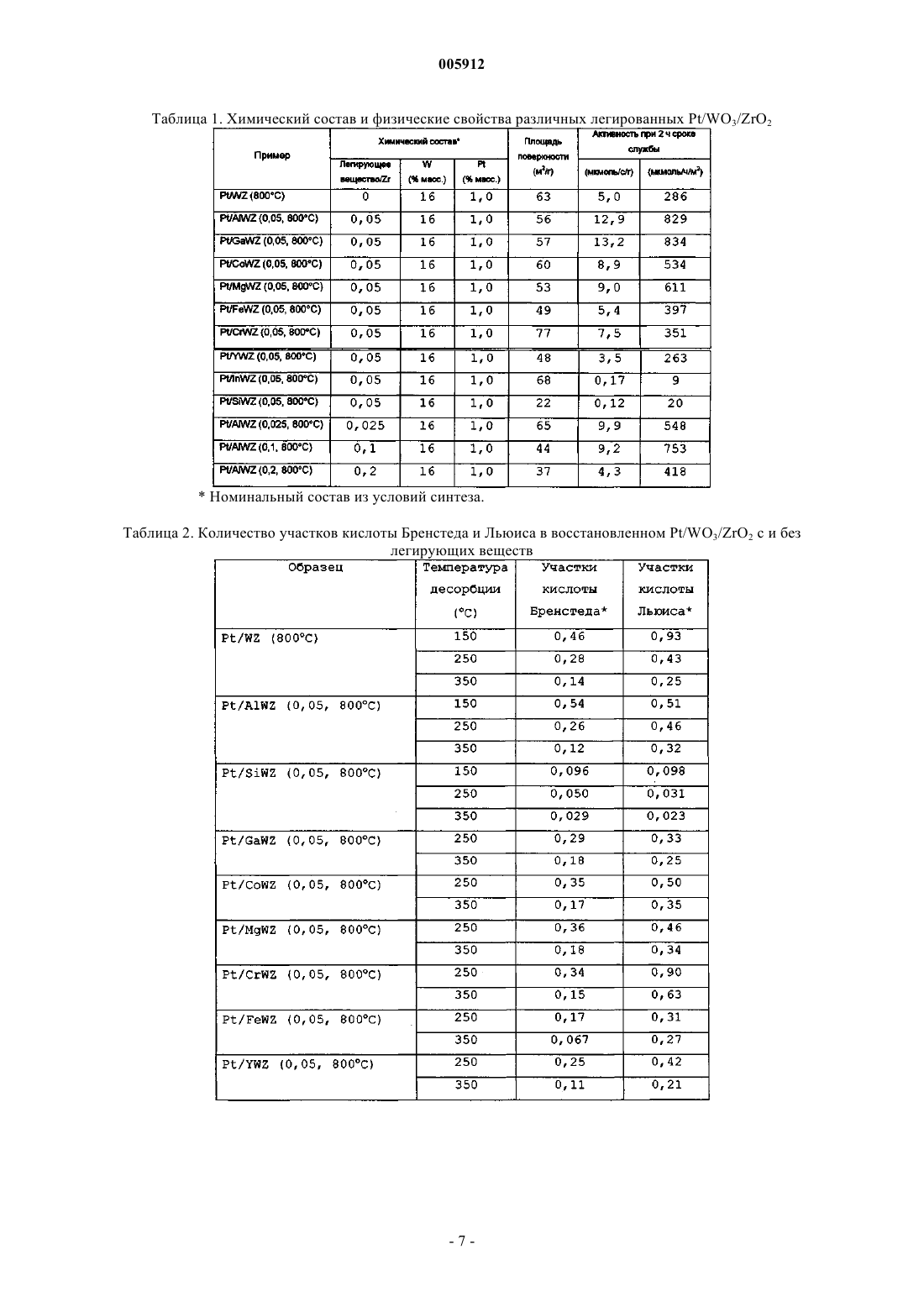
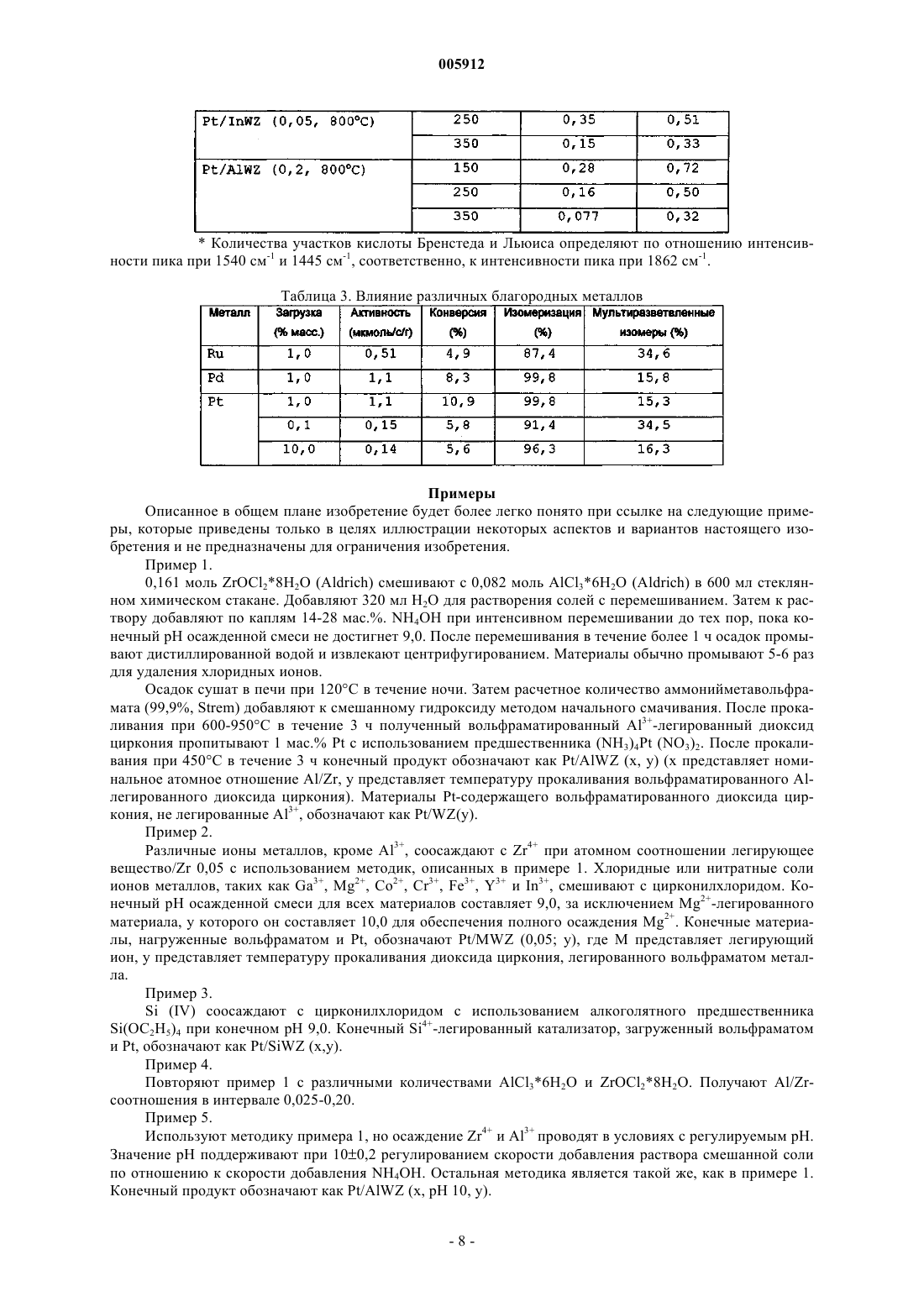
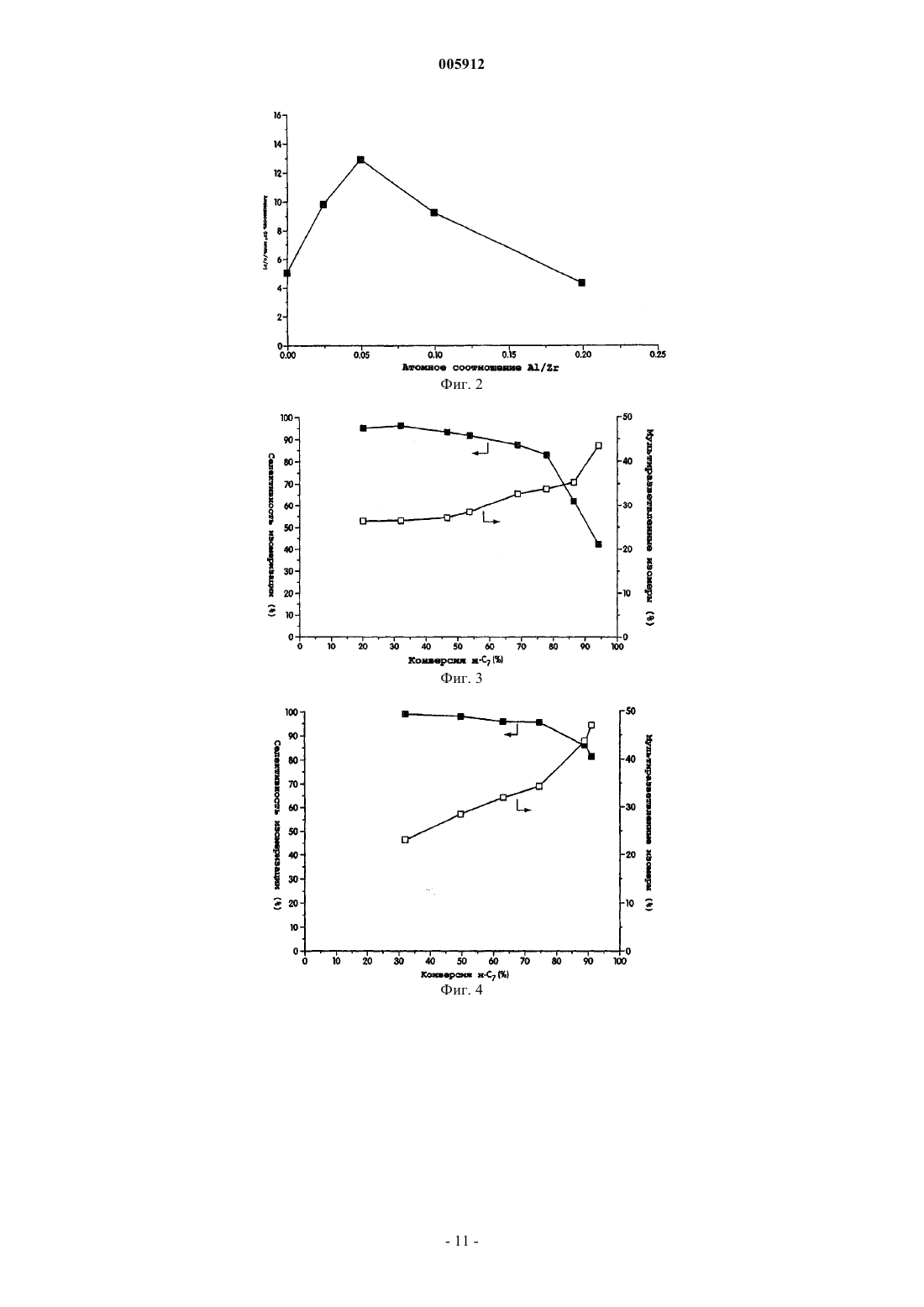
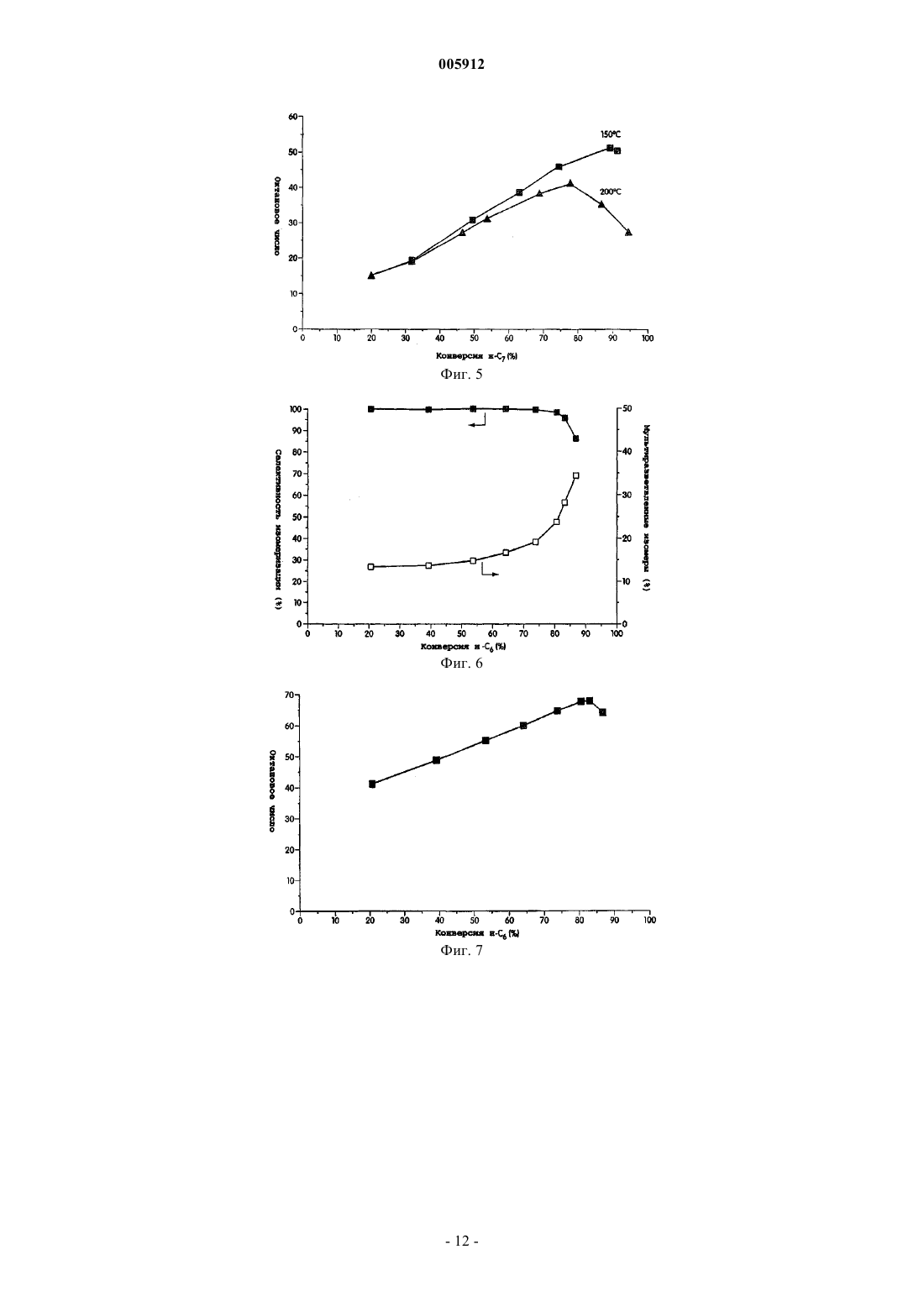
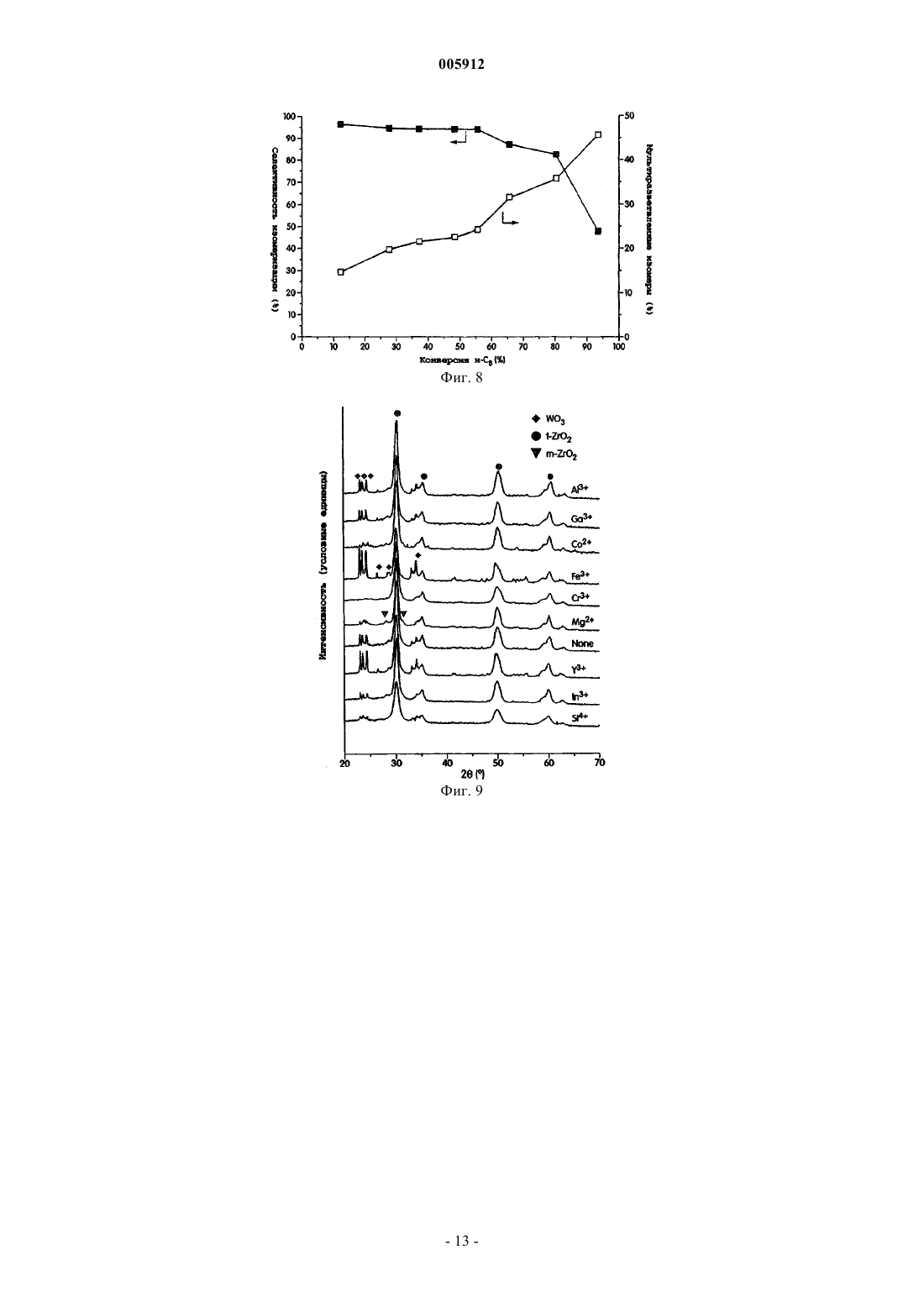
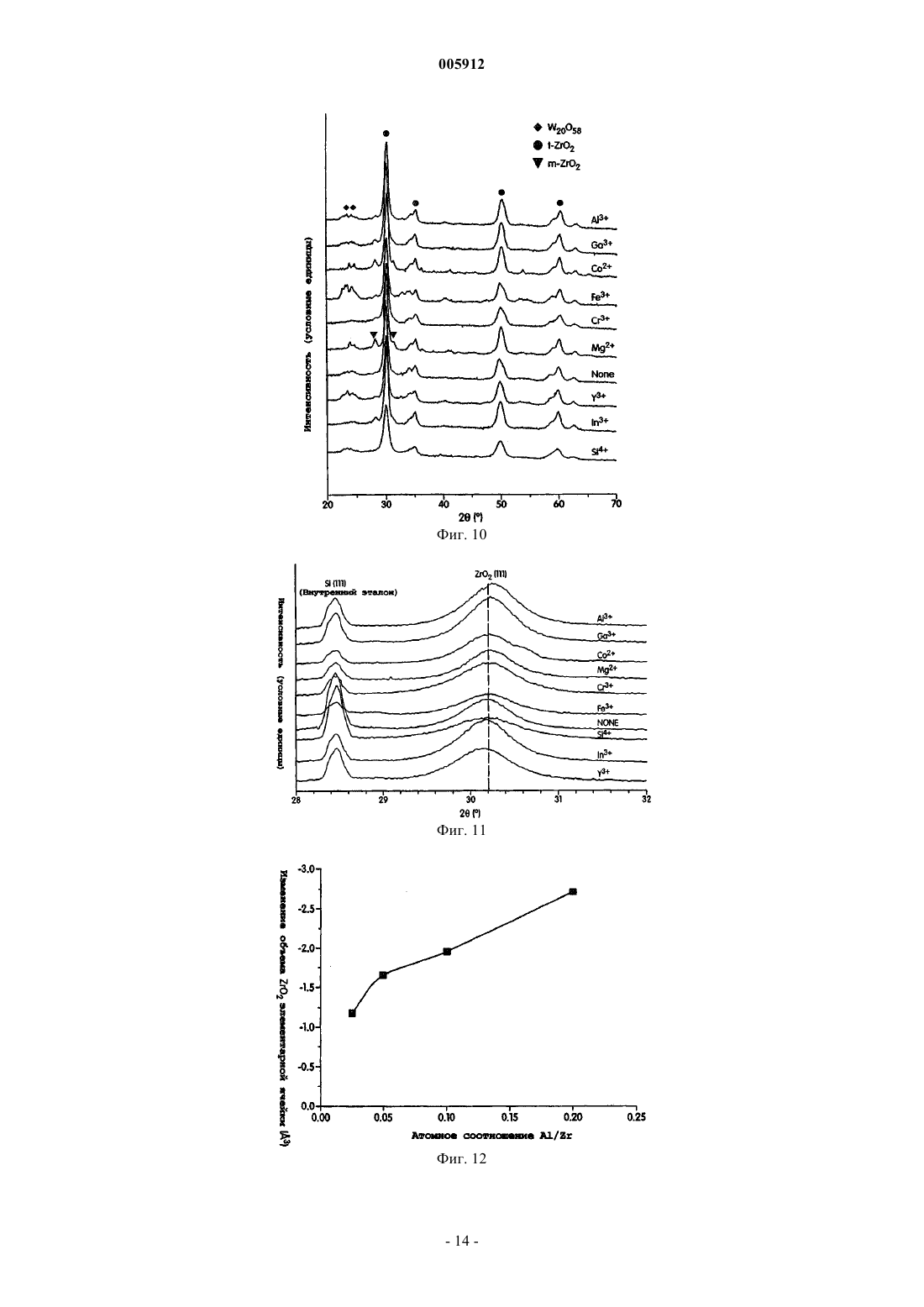
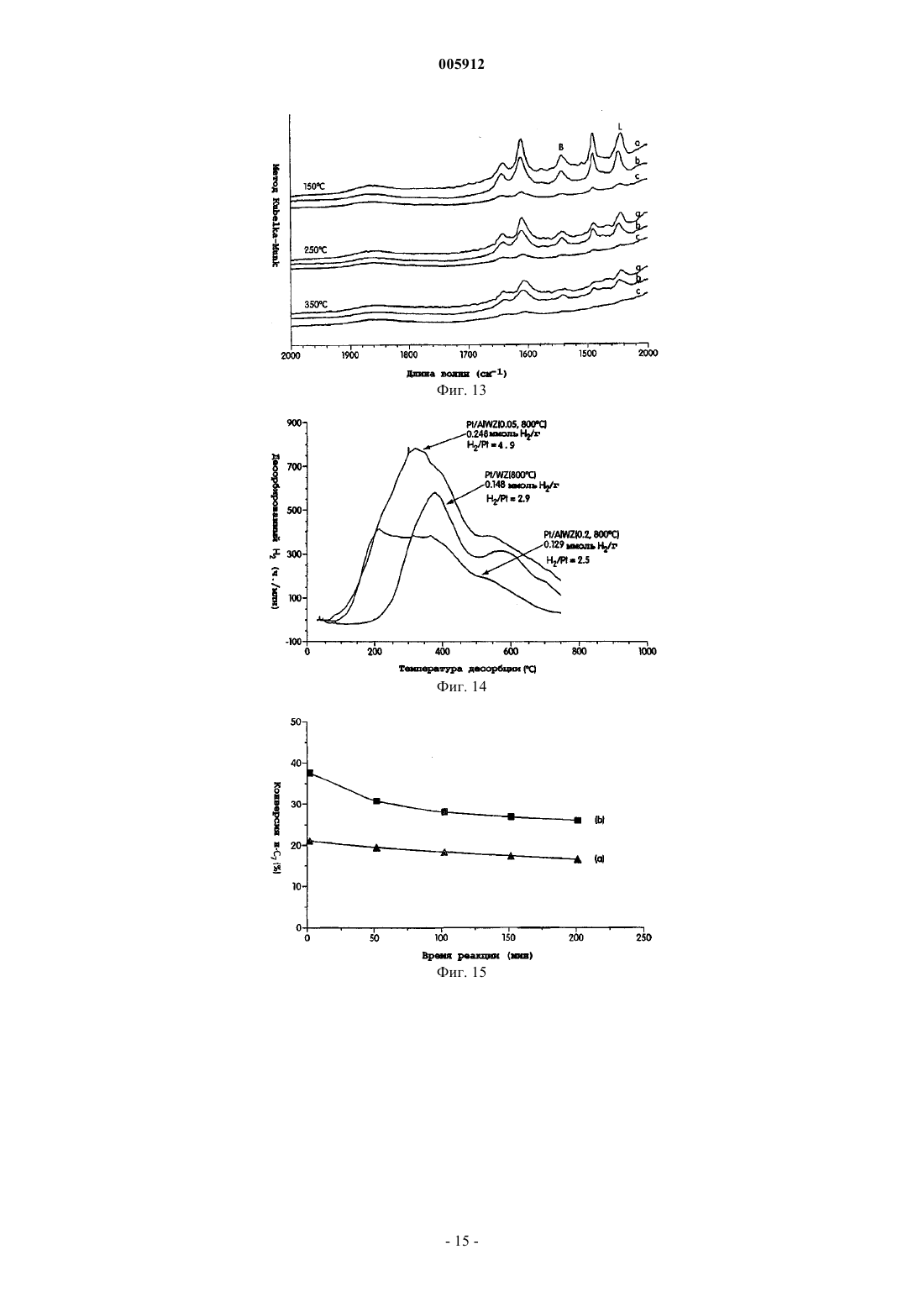
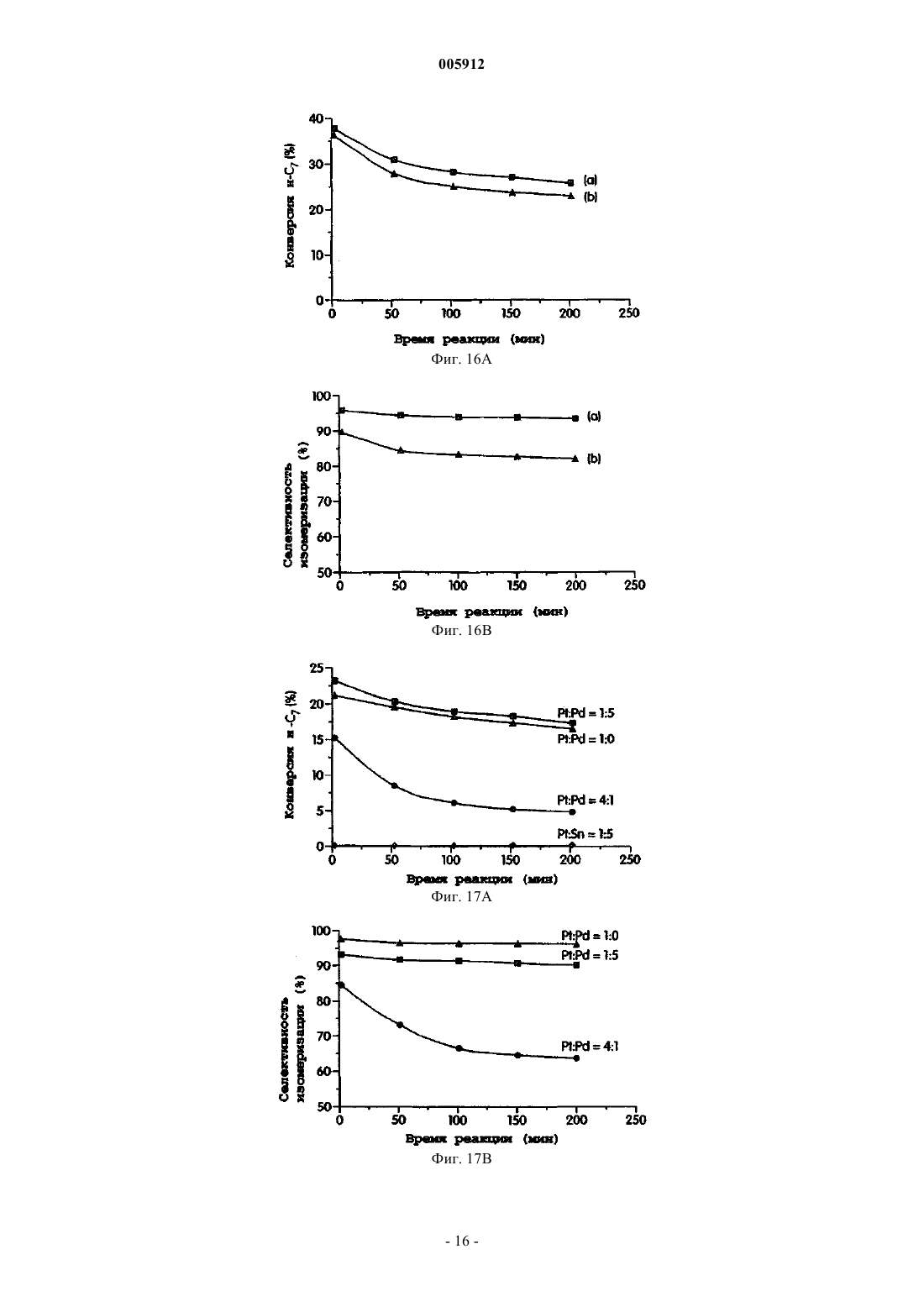
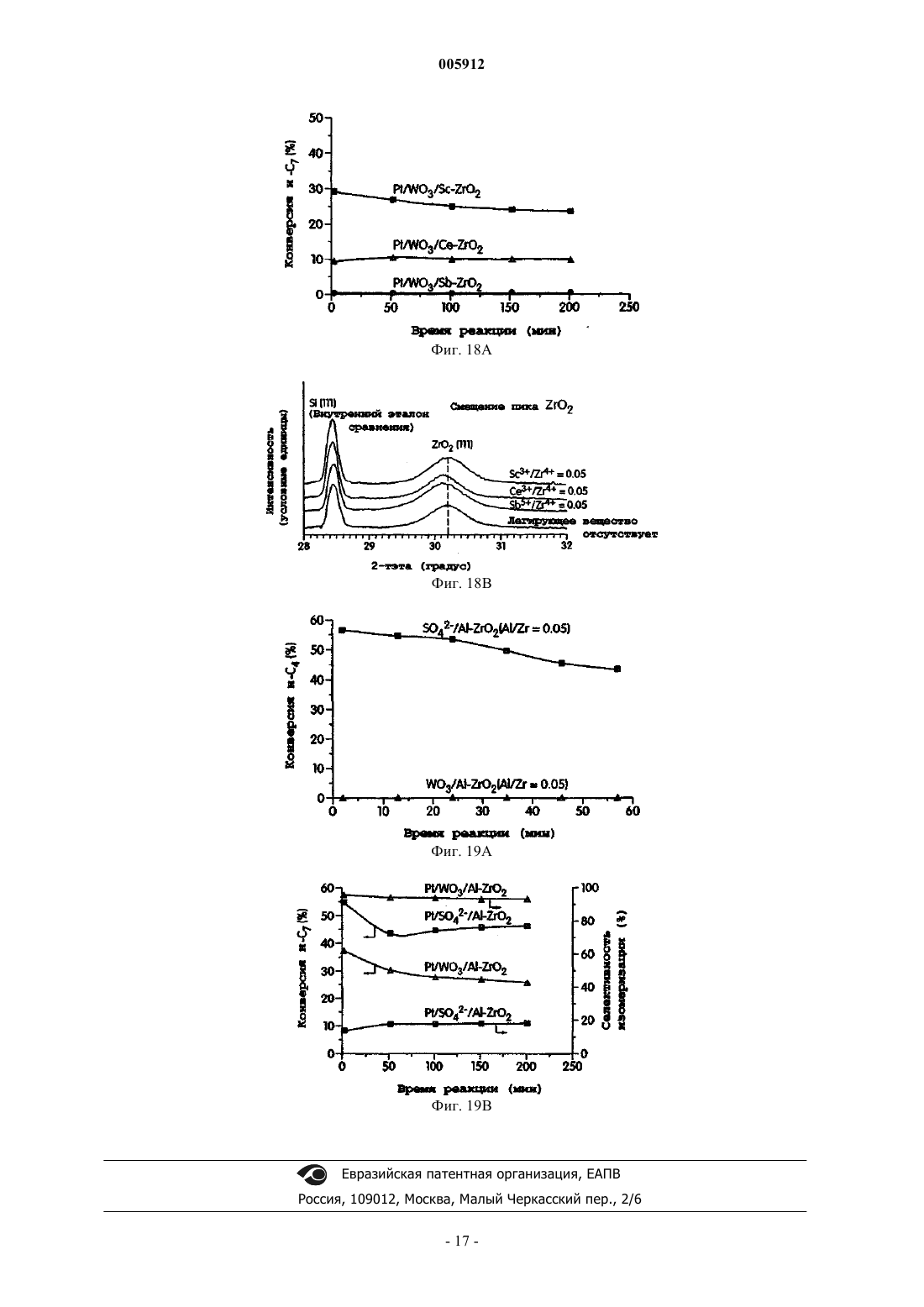
005912 Предпосылки создания изобретения Гетерогенные катализаторы играют определяющую роль во многих химических процессах. Вклад гетерогенно катализированных процессов в мировую экономику определен как 20% валового национального продукта, т.е. примерно 5 триллионов долларов в год. Главными промышленными применениями гетерогенных катализаторов являются нефтепереработка, химическое производство и защита окружающей среды. Нефтепереработка включает наибольший объем перерабатываемых материалов с мировым объемом нефтепереработки более 3,6 х 1012 кг/год. Кислотный катализ образует основу наиболее высоко используемых способов конверсии углеводородов в нефтяной промышленности и составляет активную область исследований сегодня. Хотя промышленные процессы, такие как изомеризация парафинов, алкилирование, каталитический крекинг и реформинг нефти, дают различные конечные продукты, они все зависят от материалов с кислотностью поверхности. Экологические проблемы в свете очищенных углеводородных продуктов обуславливают поиск улучшенных кислотных катализаторов. В производстве моторного топлива путем алкилирования изобутана алкенами в качестве катализатора используют H2SO4 или HF. Указанные жидкие минеральные кислоты являются агрессивными, опасными в обращении и трудными для удаления. Даже некоторые промышленные твердые кислотные катализаторы являются экологически вредными. Например, бифункциональный Pt-легированный хлорированный катализатор на основе оксида алюминия, используемый в процессе изомеризации н-бутана, требует введения хлорированных соединений для поддержания каталитической активности, поскольку он выщелачивает агрессивную НСl в процессе использования. Более значительными являются проблемы, относящиеся к дальнейшему использованию углеводородных продуктов, особенно, вредные выделения от сгорания бензинового моторного топлива. Ссылка может быть сделана на Clean Air Act Amendments of 1990, которые обязывают изменять рецептуру бензинового моторного топлива (40-50% всех нефтепродуктов США). В результате повысился спрос на отдельные компоненты смеси с увеличением нагрузки на существующие каталитические процессы. Были предприняты попытки решить указанные экологические проблемы с помощью алюмосиликатных цеолитов, но имеется больше вариантов для улучшения, связанных с разработкой новых твердых кислотных материалов. Алюмосиликатные цеолиты являются микропористыми кристаллическими материалами, состоящими из тетраэдров АlO4 и SiO4, расположенных вокруг высокоупорядоченных каналов и/или пустот. Цеолиты являются кислотными твердыми веществами, в которых кислотность поверхности образуется протонами, необходимыми для зарядного равновесия каркаса и расположенными вблизи Аl-катионов. Более часто называемые молекулярными ситами, указанные материалы имеют структурные свойства,требуемые для твердых кислотных катализаторов, такие как кислотность поверхности, высокая площадь поверхности и однородные размеры пор. Примеры цеолитов, используемых в качестве твердых кислот в нефтеочистке, включают Pt/морденит для С 5/С 6-изомеризации, ZSM-5 для ксилольной изомеризации и конверсии метанол-в-бензин, осерненный NiMo/фоязит для гидрокрекинга тяжелых нефтяных фракций иUSY для псевдоожиженного каталитического крекинга. Цеолиты также используют для других кислотно-катализируемых процессов. Главная трудность в использовании цеолитов в качестве кислотных катализаторов относится к их большой тенденции к дезактивации и к их ограниченной пригодности в реакциях, включающих большие молекулы. Цеолиты ограничены до определенных составов размерами пор и пористыми структурами, что ограничивает их применимость. Множество нецеолитных материалов с поверхностными кислотными свойствами было исследовано в качестве потенциальных твердых кислотных катализаторов. Суперкислотность является благоприятной для кислотно-катализированных реакций углеводородов, поскольку требуются низкие рабочие температуры. Кроме того, суперкислотные материалы показывают сильную кислотность и высокую активность для реакций углеводородов, которые являются трудными для катализа. Особенно интересными являются так называемые "суперкислоты", которые имеют силу кислоты больше, чем 100% H2SO4. Сульфатированный диоксид циркония и вольфраматированный диоксид циркония являются хорошо изученными примерами "суперкислотных" твердых веществ. Вольфраматированный оксид алюминия является другим примером сильнокислотного материала. Наиболее требующимся аспектом в изомеризации полудистиллятов является получение высокой селективности для изомеризации в сравнении с крекингом при высокой конверсии. Сульфатированный диоксид циркония является активным в превращении углеводородов даже при температурах ниже 100 С,но он благоприятствует реакциям крекинга. Авторами Iglesia et al. (1996) установлено, что при 200 С с примерно 50% конверсией н-гептана селективность изомеризации составляет 85% на Pt/WO3/ZrO2, но только 35% на Pt/SO42-/ZrO2. В настоящее время цеолиты и вольфраматированный диоксид циркония являются двумя наиболее изученными твердыми кислотами для изомеризации полудистиллятов благодаря селективности и стабильности указанных катализаторов. Преимущества использования нецеолитных материалов включают большую гибкость состава и поэтому больший контроль кислотности поверхности, более высокую термическую и гидротермическую стабильность и более низкую стоимость катализатора.-1 005912 Краткое описание изобретения В некоторых вариантах каталитические соединения изобретения представлены обобщенной формулойR1 представляет металл или металлический сплав, или биметаллическую систему;R2 представляет любое металлическое легирующее вещество;R3 представляет оксид металла или смеси любых оксидов металлов;R4 выбирают из WOx, MoOx, SO42- или РО 43-; и х представляет целое или дробное число между 2 и 3, включительно. В конкретном варианте R1 выбирают из благородного металла группы VIII или комбинации благородных металлов группы VIII. В другом варианте R1 выбирают из платины, палладия, иридия, родия или их комбинации. Еще в одном варианте R1 представляет Pt-Sn, Pt-Pd или Pt-Ga сплав или биметаллическую систему. В конкретном варианте R2 выбирают из группы Al3+, Ga3+, Се 4+, Sb5+, Sc3+, Mg2+, Co2+, Fe3+, Cr3+, Y3+,4+Si и In3+. В другом конкретном варианте R3 выбирают из группы: оксид циркония, оксид титана, оксид олова,оксид железа, оксид церия или их смеси. В другом конкретном варианте R4 выбирают из SO42-, WOx,MoOx, PO43-, W20O58, WO2,9 и анионов и их смесей. В конкретном варианте оксидом металла являетсяZrO2. В конкретном варианте х равен примерно 3. В одном варианте отношение металлического легирующего вещества к металлу в оксиде составляет менее чем или равно примерно 0,20. В другом варианте отношение металлического легирующего вещества к металлу в оксиде составляет менее чем или равно примерно 0,05. В еще одном варианте отношение металлического легирующего вещества к металлу в оксиде составляет примерно 0,05. В другом варианте каталитические соединения настоящего изобретения представлены Pt/WO3/AlZrO2. Другой аспект данного изобретения представляет способ изомеризации алканового или алкильного фрагмента, включающий стадию контактирования катализатора с алканом или алкилом, в котором указанный катализатор содержитR1 представляет металл или металлический сплав, или биметаллическую систему;R2 представляет любое металлическое легирующее вещество;R3 представляет оксид металла или смеси любых оксидов металлов;R4 выбирают из WOx, МоОх, SO42- или РО 43-; и х представляет целое или дробное число между 2 и 3, включительно. В предпочтительном варианте катализаторы используют для конверсии неразветвленных цепей или н-алкилов. В некоторых вариантах н-алкилом является низший алкан с неразветвленной цепью, или С 4 С 7-алкан. В некоторых других вариантах н-алкилом является н-гексан, н-октан или н-гептан. В конкретном варианте н-алкилом является н-гептан. В одном варианте температура реакции составляет ниже 210 С, ниже 170 С, ниже 150 С. В другом варианте конверсии изомеризации составляют выше 80%. В еще одном варианте каталитические соединения используют в способе получения изомеров фрагментов алкана или алкила с выходом более 70%,более 80% реакционного продукта. В другом варианте каталитические соединения используют для получения алканов в виде мультиразветвленных алканов с высоким октановым числом. Краткое описание чертежей На фиг. 1 показана активность Pt/WO3/M-ZrO2 с различными легирующими веществами (M/Zr=0,05; 800C) в изомеризации н-гептана; на фиг. 2 показано влияние уровня Аl3+-легирования на активность Pt/AlWZ (800C) в изомеризации н-гептана; на фиг. 3 - селективность изомеризации н-гептана по отношению к конверсии над Pt/AlWZ (0,05; 800 С) при 200 С в Н 2; на фиг. 4 - селективность изомеризации н-гептана по отношению к конверсии над Pt/AlWZ (0,05; 800 С) при 150 С в Н 2; на фиг. 5 - октановое число продуктов изомеризации н-гептана и непревращенного гептана надPt/AlWZ (0,05; 800 С) в Н 2; на фиг. 6 - селективность изомеризации н-гексана по отношению к конверсии над Pt/AlWZ (0,05; 800 С) при 200 С в Н 2; на фиг. 7 - октановое число продуктов изомеризации н-гексана и непревращенного гексана над-2 005912 на фиг. 8 показана селективность изомеризации н-октана по отношению к конверсии над Pt/AlWZ(0,05; 800 С) при 150 С в Н 2; на фиг. 9 - рентгенограммы WО 3/ZrO2 с легирующими веществами (M/Zr=0,05, 800C); на фиг. 10 - рентгенограммы Pt/WO3/ZrO2 с легирующими веществами (M/Zr=0,05, 800C) после восстановления при 350 С в Н 2; на фиг. 11 - рентгенограммы, показывающие сдвиг пика ZrO2(111) в образцах вольфраматированного диоксида циркония с различными легирующими веществами (M/Zr=0,05, 800 С); на фиг. 12 - изменение объема ZrO2 элементарной ячейки с уровнем Аl3+-легирования в Pt/AlWZ(800C); на фиг. 13 - DRIFT-спектры пиридина, адсорбированного над восстановленным при 350 С (a) Pt/WZ(800 С), (b) Pt/AlWZ (0,05; 800 С) и (с) Pt/SiWZ (0,05; 800 С), полученные после десорбции пиридина при определенных температурах; на фиг. 14 - температурно-программированная десорбция водорода над Pt/WZ (800C), Pt/AlWZ(0,05; 800 С) и Pt/AlWZ (0,2; 800 С); на фиг. 15 - конверсия н-гептана по отношению к времени реакции над (a) Pt/AlWZ (0,05; 800 С) и(объемная часовая скорость подачи сырья) = 110000 ч-1); на фиг. 16 представлены (i) конверсия н-гептана и (ii) селективность изомеризации по отношению к времени реакции над Pt/AlWZ (0,05; pH 10; 800C), полученного с (a) (NH3)4Pt (NO3)2 и (b) H2PtCl6 (реакционные условия: 38 мг катализатора, 200 С, 6% н-С 7 в Н 2, VHSV=110000 ч-1); на фиг. 17 а - конверсия н-гептана по отношению к времени реакции над AlWZ (0,05; 800 С) с (i) Pt,(ii) 4:1 Pt-Pd сплавом, (iii) 1:5 Pt-Pd сплавом и (iv) 1:5 Pt-Sn сплавом (реакционные условия: 38 мг катализатора, 200 С, 6% н-С 7 в Н 2, VHSV=110000 ч-1); на фиг. 17b - селективность изомеризации по отношению к времени реакции над AlWZ (0,05; 800 С) с (i) Pt, (ii) 4:1 Pt-Pd сплавом и (iii) 1:5 Pt-Pd сплавом (реакционные условия: 38 мг катализатора,200 С, 6% н-С 7 в Н 2, VHSV=110000 ч-1); на фиг. 18 - влияние легирующих оксидов, имеющих кристаллическую структуру, подобную ZrO2; на фиг. 19 а - конверсия н-бутана по отношению к времени реакции и влияние различных анионов на активность Pt/aнион/Al-ZrO2 (реакционные условия: 250 мг катализатора, 250 С, 2,47% н-С 4 в Н 2,VHSV=8000 ч-1); На фиг. 19b показана конверсия н-гептана по отношению к времени реакции и влияние различных анионов на активность и селективность Pt/анион/Al-ZrO2 (реакционные условия: 38 мг катализатора,200 С, 6% н-С 7 в Н 2, VHSV=110000 ч-1). Подробное описание изобретения А. Обзор Настоящее изобретение относится к каталитическому соединению анион-модифицированных оксидов металлов, легированных ионами металлов. Настоящее изобретение относится также к способу изомеризации н-алканового и алкильного фрагмента, содержащему каталитическое соединение по настоящему изобретению. В некоторых вариантах металлические легирующие вещества в каталитическом соединении значительно увеличивают активность вольфраматированных оксидов металлов с благородными металлами. Указанные материалы благородный металл/анион/легированный металлом оксид металла катализируют изомеризацию фрагментов н-алканов и алкилов с высокой селективностью. В некоторых аспектах настоящего изобретения каталитические материалы используют в реакции или способе изомеризационной конверсии. Такой способ имеет низкую температуру реакции и обеспечивает высокий выход изомеризационной конверсии.B. Определения Термин "алкил" относится к радикалу насыщенных алифатических групп, включая неразветвленные алкильные группы, разветвленные алкильные группы, циклоалкильные (алициклические) группы,алкилзамещенные циклоалкильные группы и циклоалкилзамещенные алкильные группы. В предпочтительных вариантах разветвленный и неразветвленный алкил имеет 30 или менее углеродных атомов в своей главной цепи (например, C1-С 30 для неразветвленной цепи, С 3-С 30 для разветвленной цепи) и, более предпочтительно 20 или менее. Аналогично, предпочтительные циклоалкилы имеют от 4 до 10 углеродных атомов в своей кольцевой структуре и более предпочтительно имеют 5, 6 или 7 углеродов в кольцевой структуре. Термины "алкенил" и "алкинил" относятся к ненасыщенным алифатическим группам, аналогичным по длине и возможному замещению алкилам, описанным выше, но которые содержат по крайней мере одну двойную или тройную связь углерод-углерод, соответственно. Если число углеродов не уточняется иначе, термин "низший алкил", как использовано здесь, означает алкильную группу, как определено выше, но имеющую от одного до десяти углеродов, более пред-3 005912 почтительно от одного до шести углеродных атомов в своей структуре основной цепи. Аналогично,"низший алкенил" и "низший алкинил" имеют подобные длины цепи.C. Соединения Соединениями изобретения являются каталитические соединения, представленные обобщенной формулой:R1/R4/R2-R3,в которой: R1 представляет металл или металлический сплав, или биметаллическую систему;R2 представляет любое металлическое легирующее вещество;R3 представляет оксид металла или смеси любых оксидов металлов;R4 представляет WOx, MoOx, SO42- или РО 43-; и х представляет число между 2 и 3, включительно. В конкретном варианте R1 выбирают из благородного металла группы VIII или комбинации благородных металлов группы VIII. В другом варианте R1 выбирают из платины, палладия, иридия, родия или их комбинации. Еще в одном варианте R1 представляет Pt-Sn, Pt-Pd или Pt-Ga сплав или биметаллическую систему. В конкретном варианте R2 выбирают из группы Al3+, Ga3+, Се 4+, Sb5+, Sc3+, Mg2+, Со 2+, Fe3+, Cr3+, Y3+,4+Si и In3+. В другом варианте R2 представляет Аl3+. В другом конкретном варианте оксидом металла является оксид циркония, оксид титана, оксид железа, оксид церия, оксид олова, SO42- и анионы и их смеси. В конкретном варианте оксидом металла является ZrO2. В другом варианте х равен примерно 3. В одном варианте отношение металлического легирующего вещества к металлу в оксиде составляет менее чем или равно примерно 0,20. В другом варианте отношение металлического легирующего вещества к металлу в оксиде составляет менее чем или равно примерно 0,05. В еще одном варианте отношение металлического легирующего вещества к металлу в оксиде составляет примерно 0,05. В другом варианте каталитические соединения настоящего изобретения представлены Pt/WO3/AlZrO2. В аспекте настоящего изобретения каталитические соединения используют для конверсии неразветвленных алкилов в разветвленные алкилы. В предпочтительном варианте катализаторы используют для конверсии неразветвленных алкилов или н-алкилов. Как показано на фиг. 1, легирование ZrO2 различными катионами резко изменяет активность Pt/WO3/ZrO2. Легирующие вещества, такие как Аl3+ иGa3+, увеличивают каталитическую активность в 2-3 раза. Этот промотирующий эффект не относится к кислотности/основности легирующего оксида или к восстановительному потенциалу легирующего катиона. Например, МgО и Y2O3 являются оба основными оксидами, но легирующее вещество Мg2+ увеличивает активность. Восстановительные потенциалы Аl3+, Сr3+ и Со 2+ сильно отличаются друг от друга; однако они все увеличивают активность вольфраматированного диоксида циркония с Pt. Здесь используется сокращенное обозначение каталитических соединений. Например, Pt/AlWZ(0,05; 800 С) обозначает катализатор платина/вольфраматированный диоксид циркония, легированный Аl3+, с отношением Al/Zr=0,05, и прокаленный при 800 С. В варианте отношение Al/Zr,05. Различные количества AL3+-иона вводят в диоксид циркония при получении Pt/AlWZ (800C). На фиг. 2 показано, что при низких уровнях легирующего вещества(Al/Zr0,05) активность Pt/AlWZ (800C) увеличивается с количеством легирующего вещества. Однако при высоких уровнях легирования активность Pt/AlWZ (800C) снижается с количеством легирующего вещества. Легирующие ионы Аl3+ и Ga3+ в диоксиде циркония промотируют активность Pt/WO3/ZrO2 в 23 раза. Здесь Pt/AlWZ (0,05; 800 С) выбран характерно для превращения ряда полудистиллятов, таких как н-гексан, н-гептан и н-октан. На фиг. 3-8 показаны селективности изомеризации по отношению к общей конверсии трех углеводородов. В варианте катализатор используют в реакции изомеризации с более 50% конверсией и более 60% селективностью. При 200 С 85% селективность изомеризации получают при 63% конверсии н-гептана над Pt/AlWZ (0,05; 800 С) (см. фиг. 3). Принимая во внимание, что скорость конверсии н-гептана надPt/AlWZ (0,05; 800 С) является очень высокой при 200 С (примерно 16 мкмоль н-С 7/с/г, первоначально),температура реакции снижается до 150 С. При 150 С нелегированный Pt/WZ (800C) является неактивным, но Pt/AlWZ (0,05; 800 С) является еще достаточно активным для превращения н-С 7 со скоростью 1,1 мкмоль/с/г со значительно улучшенной селективностью изомеризации. Селективность изомеризации является такой высокой, как 85% при 90% конверсии н-гептана (см. фиг. 4). Кроме общей селективности изомеризации представляет большой интерес процент мультиразветвленных изомеров в изомерных продуктах, поскольку октановые числа мультиразветвленных изомеров являются намного больше, чем у моноразветвленных изомеров. Как показано на фиг. 4, процент мультиразветвленных изомеров быстро увеличивается с процентом конверсии н-гептана. Соответственно, октановое число увеличивается с 0 до 50 и 40 посредством изомеризации н-гептана при 150 и 200 С, соответственно над Pt/AlWZ (0,05; 800 С)-4 005912 В варианте катализатор настоящего изобретения используют в реакции изомеризации алкановых или алкильных фрагментов для увеличения октанового числа. В другом варианте Pt/AlWZ (0,05; 800 С) увеличивает октановое число до более 50, более 60. Например, Pt/AlWZ (0,05; 800 С) может конвертировать н-гексан при высокой скорости 3,2 мкмоль/с/г при 200 С. При 85% конверсии сохраняется селективность изомеризации 90% (см. фиг. 6) . Процент мультиразветвленных изомеров в продуктах изомеризации может достигать 35% при 85% селективности изомеризации. В результате октановое число увеличивается с 32 до 66 посредством изомеризации н-гексана при 200 С (см. фиг. 7). Изомеризация н-октана над Pt/AlWZ (0,05; 800 С) может иметь место при 150 С при скорости 6,4 мкмоль/с/г. Селективность изомеризации также является превосходной (см. фиг. 8). При 80% конверсии получают 81% селективность изомеризации с 35% мультиразветвленных изомеров. Химический состав и физические свойства Pt/WO3/ZrO2 с различными легирующими веществами обобщены в табл. 1. Большая часть легирующих веществ снижает площадь поверхности Pt/WO3/ZrO2,только Cr3+, In3+ и низкий уровень Аl3+-легирования дают небольшое увеличение площади поверхности. Когда значения активности были переведены из единицы мкмоль/с/г в единицу мкмоль/ч/м 2, каталитическая активность Pt/MWZ (0,05; 800 С) еще довольно различается в зависимости от введенного легирующего вещества и снижается в порядке Ga3+Al3+Mg2+Co2+Fe3+Cr3+Y3+Si4+In3+. На фиг. 9 представлены рентгенограммы вольфраматированного диоксида циркония с легирующими веществами. Дифракционные пики легирующих оксидов не отмечены, что указывает на то, что легирующие вещества являются высоко диспергированными. ZrO2 присутствует, главным образом, в тетрагональной фазе с размерами кристаллитов 13-18 нм. В указанных образцах интенсивности дифракционных пиков WО 3 являются довольно различными. Более сильные пики WO3 найдены в рентгенограммах вольфраматированного диоксида циркония, легированного Аl3+, Ga3+, Fe3+ и Y3+. Катализаторы Pt/MWZ были исследованы с помощью рентгенографии после их восстановления при 350 С в Н 2 (см. фиг. 10). Было показано, что WO3 восстанавливается до W20O58 после предварительной обработки в Н 2. Диоксид циркония не изменяется в процессе, за исключением незначительного увеличения моноклинной фазы в некоторых легированных образцах. Поскольку отсутствует дифракционный пик легирующего оксида в рентгенограммах различных образцов, легирующие вещества должны быть высокодиспергированными. Так как большая часть легирующих веществ различается ионным радиусом от Zr4+, замещение Zr4+ легирующим веществом ведет к изменению в элементарной ячейке ZrO2. При использовании кремния в качестве внутреннего эталона сравнения в рентгенографических исследованиях исследуют положение пика диоксида циркония (111) для различных легированных образцов (см. фиг. 11). Для легирующих веществ с ионным радиусом меньшим, чем у Zr4+, пик диоксида циркония (111) сдвигается к более высоким углам, за исключениемSiWZ. Легирующие вещества с ионным радиусом, большим, чем у Zr4+, вызывают сдвиг пика диоксида циркония (111) к более низким углам. Указанные результаты предполагают, что все легирующие вещества, кроме Si4+, могут замещать Zr4+ в кристаллической структуре диоксида циркония. Для катализатораPt/SiWZ Si аналогично присутствует в виде силикагельного покрытия вместо структурного легирующего вещества для ZrO2; силикагель может иметь ослабленное взаимодействие между диоксидом циркония и оксидом вольфрама, что дает снижение каталитической активности. Для катализаторов Pt/AlWZ изомеризационная активность максимизируется при отношении Al/Zr 0,05 (см. фиг. 2). На фиг. 12 показано, что величина снижения объема элементарной ячейки диоксида циркония является меньше, когда отношение Al/Zr увеличивается свыше 0,05, что предполагает, что часть Аl3+ легирующих веществ не замещает Zr4+ при высоких нагрузках Аl3+. Взамен они могут образовывать поверхностное покрытие Al2O3, которое подвергает риску промотирующий эффект Аl3+ легирующих веществ в алкановой изомеризации. Кислотность Pt/WO3/ZrO2 с легирующими веществами и без них характеризуется пиридиновой адсорбцией DRIFT-спектроскопией. Катализатор предварительно обрабатывают в воздухе и затем восстанавливают в Н 2 в течение 1,5 ч. Восстановленный образец смешивают с 20 мас.%, силикагеля в качестве внутреннего эталона сравнения. После измельчения в дисперсный порошок с размером частиц менее 74 мкм образец загружают в DRIFT-ячейку. Образец предварительно обрабатывают в сухом Не при 450 С в течение 1 ч перед введением пиридина при комнатной температуре. После 30 мин адсорбции пиридина образец продувают током Не при 150, 250 и 350 С в течение 1 ч. DRIFT-спектр снимают незадолго до конца продувки при каждой температуре десорбции. DRIFT-спектры трех характерных образцов, Pt/WZ(800C), Pt/AlWZ (0,05; 800 С) и Pt/SiWZ (0,05; 800 С), представлены на фиг. 13. Пиковые интенсивности адсорбированного пиридина на каждом образце приводят к пиковой интенсивности Si-O-Si при 1862 см-1. Пики при 1540 см-1 и 1445 см-1 соответствуют участкам кислоты Бренстеда и Льюиса, соответственно. При каждой температуре десорбции наименее активный Pt/SiWZ (0,05; 800 С) имеет очень слабые пики при 1540 см-1 и 1445 см-1 по сравнению с Pt/WZ (800C) и Pt/AlWZ (0,05; 800 С). Количественное сравнение пиковых интенсивностей при 1540 см-1 и 1445 см-1 для различных легированных образцов представлено в табл. 2. Большая часть легирующих веществ, кроме Si4+ и Fe3+, не изменяет очень намного кислотность Pt/WO3/ZrO2. Si4+ легирующее вещество резко снижает количество кислотных участков, и-5 005912 имеются незначительные сильнокислотные участки в Pt/SiWZ (0,05; 800 С). Fe3+ легирующее вещество дает меньше и слабые участки кислоты Бренстеда. Для Pt/AlWZ более высокий уровень легированияAl/Zr=0,2 приводит к сниженной кислотности Бренстеда. Сильнокислотные участки являются важными и необходимыми для реакции изомеризации, но не единственным фактором в определении активности катализатора. Количество Н 2, адсорбированного над катализаторами, определяют температурно-программированной десорбцией водорода ( (Н 2-ТПД) (H2-TPD) ) над легированными и нелегированными катализаторами. Катализаторы предварительно обрабатывают в тех же условиях, как перед реакцией. После адсорбции Н 2 при 30 С в течение 2 ч образцы подвергают воздействию тока аргона для удаления слабоадсорбированного водорода. Затем исследование десорбции Н 2 инициируют нагреванием каталитического слоя при скорости 5 С/мин в токе аргона при атмосферном давлении, и выходящий газ анализируют с использованием детектора теплопроводности. Как показано на фиг. 14, десорбция Н 2 имеет место примерно на 150 С ниже на Pt/AlWZ по сравнению с Pt/WZ, и общее количество Н 2, десорбированного изPt/AlWZ (0,05; 800 С), примерно в 1,7 раз больше, чем из Pt/WZ (800C). Указанное различие в характеристиках десорбции Н 2 может объяснять различие в каталитической активности между образцом легированного и нелегированного Pt/WZ. Аномально высокое мольное отношение H2/Pt предполагает Н 2 перекрывающий эффект. Поскольку Pt-дисперсия над указанными образцами является подобной и не различается в Pt, наблюдается энергия связи путем рентгеноэлектронной спектроскопии (спектрометр SSX100 ESCA) , более низкая температура десорбции Н 2 и более высокое количество десорбции Н 2 надPt/AlWZ (0,05; 800 С) могут быть отнесены к структурным изменениям от включения Аl3+. В одном варианте металлическое легирующее вещество вводят при регулируемых значениях рН. В другом варианте металлическое легирующее вещество вводят при рН 10. Поскольку начальные значения рН осаждения для Zr4+ и различных легирующих веществ являются различными, осаждение Zr4+ и легирующих веществ может начинаться в различные моменты времени. Регулированием рН осаждения наноструктура и композиция (состав) катализатора могут быть оптимизированы. Для увеличения гомогенности легированного диоксида циркония, Zr4+ и катионы легирующего вещества осаждают при постоянном рН 10 (см. пример 5). При использовании регулируемого рН осаждения полученный катализатор(Pt/AlWZ (0,05; рН 10; 800 С) ) обуславливает значительно более высокую активность по сравнению сPt/AlWZ (0,05; 800 С) (см. фиг. 15). Предшественник, используемый для Pt, также влияет на активность и селективность получаемогоPt/AlWZ (0,05; рН 10; 800 С) (см. фиг. 16). При использовании (NH3)4Pt(NO3)2 в качестве Ptпредшественника вместо H2PtCl6 получают более активный и селективный катализатор Pt/AlWZ (0,05; рН 10; 800 С) для изомеризации н-гептана. В одном варианте благородный металл может различаться для оптимизации изомеризации н-алкилов; однако также можно использовать неблагородные металлы в катализаторах изомеризации. В табл. 3 показаны различные благородные металлы в соединении по настоящему изобретению. В другом варианте может быть использован сплав благородного металла (см. фиг. 17). В варианте может быть использован сплав 1:5 Pt-Pd с получением немного более высокой активности по сравнению с Pt для AlWZ (0,05; 800 С), но последний предусмотрен для более высокой селективности изомеризации. Другие сплавы, такие как Pt-Sn или Pt-Ge, могут быть использованы для снижения начальной дезактивации катализатора при сохранении высокой селективности изомеризации AlWZсистемы. В одном варианте легирующие металлы могут варьироваться для оптимизации каталитического поведения. На фиг. 18 показана изомеризация н-алканов с использованием различных легирующих оксидов с 38 мг катализатора, восстановленного при 350 С в Н 2 в течение 1,5 ч. Реакцию проводят при 200 С. В варианте металлический оксидный анион может варьироваться для оптимизации селективности изомеризации. В другом варианте металлическим оксидным анионом является SO42- или WO3 (см. фиг. 19). Нанокомпозитные катализаторы Pt/вольфраматированный диоксид циркония с легирующими веществами, такими как А 13+ и Ga3+, являются намного более активными и селективными, чем традиционныйPt/вольфраматированный диоксид циркония в изомеризации гексана, гептана и октана. Нанокомпозитная технология обеспечивает ультравысокую дисперсию компонентов, обеспечивающую эффективное замещение легирующих катионов в кристаллической решетке диоксида циркония. ПолучаемыйPt/легированный вольфраматированный диоксид циркония обеспечивает низкотемпературную конверсию полудистиллятов, более высокую адсорбцию Н 2 и низкую температуру десорбции Н 2. Такая система может быть также использована для эффективной изомеризации других углеводородов с незначительной дезактивацией катализатора во времени.-6 005912 Таблица 1. Химический состав и физические свойства различных легированных Pt/WO3/ZrO2 Номинальный состав из условий синтеза. Таблица 2. Количество участков кислоты Бренстеда и Льюиса в восстановленном Pt/WO3/ZrO2 с и без легирующих веществ Количества участков кислоты Бренстеда и Льюиса определяют по отношению интенсивности пика при 1540 см-1 и 1445 см-1, соответственно, к интенсивности пика при 1862 см-1. Таблица 3. Влияние различных благородных металлов Примеры Описанное в общем плане изобретение будет более легко понято при ссылке на следующие примеры, которые приведены только в целях иллюстрации некоторых аспектов и вариантов настоящего изобретения и не предназначены для ограничения изобретения. Пример 1. 0,161 моль ZrOCl28H2O (Aldrich) смешивают с 0,082 моль АlСl36 Н 2 О (Aldrich) в 600 мл стеклянном химическом стакане. Добавляют 320 мл Н 2O для растворения солей с перемешиванием. Затем к раствору добавляют по каплям 14-28 мас.%. NH4OH при интенсивном перемешивании до тех пор, пока конечный рН осажденной смеси не достигнет 9,0. После перемешивания в течение более 1 ч осадок промывают дистиллированной водой и извлекают центрифугированием. Материалы обычно промывают 5-6 раз для удаления хлоридных ионов. Осадок сушат в печи при 120 С в течение ночи. Затем расчетное количество аммонийметавольфрамата (99,9%, Strem) добавляют к смешанному гидроксиду методом начального смачивания. После прокаливания при 600-950 С в течение 3 ч полученный вольфраматированный Аl3+-легированный диоксид циркония пропитывают 1 мас.% Pt с использованием предшественника (NH3)4Pt (NО 3)2. После прокаливания при 450 С в течение 3 ч конечный продукт обозначают как Pt/AlWZ (х, у) (х представляет номинальное атомное отношение Al/Zr, у представляет температуру прокаливания вольфраматированного Аlлегированного диоксида циркония). Материалы Pt-содержащего вольфраматированного диоксида циркония, не легированные Аl3+, обозначают как Pt/WZ(y). Пример 2. Различные ионы металлов, кроме Аl3+, соосаждают с Zr4+ при атомном соотношении легирующее вещество/Zr 0,05 с использованием методик, описанных в примере 1. Хлоридные или нитратные соли ионов металлов, таких как Ga3+, Mg2+, Co2+, Cr3+, Fe3+, Y3+ и In3+, смешивают с цирконилхлоридом. Конечный рН осажденной смеси для всех материалов составляет 9,0, за исключением Мg2+-легированного материала, у которого он составляет 10,0 для обеспечения полного осаждения Мg2+. Конечные материалы, нагруженные вольфраматом и Pt, обозначают Pt/MWZ (0,05; у), где М представляет легирующий ион, у представляет температуру прокаливания диоксида циркония, легированного вольфраматом металла. Пример 3.Si(OC2H5)4 при конечном рН 9,0. Конечный Si4+-легированный катализатор, загруженный вольфраматом и Pt, обозначают как Pt/SiWZ (x,y). Пример 4. Повторяют пример 1 с различными количествами АlСl36 Н 2 О и ZrOCl28H2O. Получают Al/Zrсоотношения в интервале 0,025-0,20. Пример 5. Используют методику примера 1, но осаждение Zr4+ и Аl3+ проводят в условиях с регулируемым рН. Значение рН поддерживают при 100,2 регулированием скорости добавления раствора смешанной соли по отношению к скорости добавления NH4OH. Остальная методика является такой же, как в примере 1. Конечный продукт обозначают как Pt/AlWZ (x, рН 10, у).-8 005912 Пример 6. Кроме (NH3)4Pt (NO3)2, другой Pt предшественник, такой как H2PtCl6, используют в загрузке 1% масс. Pt поверх вольфраматированного легированного диоксида циркония. Помимо чистой Pt, вольфраматированный легированный диоксид циркония также загружают Pt-сплавами и другими благородными металлами. Пример 7. Структурное исследование Микроструктуру и поверхностные свойства наноструктурных твердокислотных материалов исследуют с использованием ряда экспериментальных методов. Рентгенографические данные анализа порошка были сняты на дифрактометре Siemens D5000, работавшем при 45 кВ и 40 мА, с использованием никельфильтрованного СuK-излучения с длиной волны 1,5406 . Размер кристаллитов определяют анализом пикового расширения с использованием метода Шеррера (Scherrer). Изотермы адсорбции азота получают при 77 K на газосорбционной и порометрической системе Micromeritics ASAP 2010. Образцы дегазируют при 150 С в вакууме до достижения конечного давления 1x10-3 Торр. Удельную поверхность БЭТ (по методу Брунауэра-Эммета-Теллера) определяют при относительном интервале давления 0,050,20. Пример 8. Кислотность катализатора Кислотность катализатора вольфраматированного легированного диоксида циркония анализируют инфракрасной (ИК) спектроскопией пиридиновой адсорбции. Образец восстанавливают при 350 С в течение 1,5 ч перед загрузкой в камеру диффузионного отражательного ИК-спектрометра с Фурьепреобразователем (DRIFT). Аморфную двуокись кремния физически смешивают с образцом в качестве внутреннего эталона сравнения (20 мас.% SiO2, всего). Образец предварительно обрабатывают в Не при 450 С в течение 1 ч перед адсорбцией пиридина при комнатной температуре. ИК спектры образца снимают после десорбции пиридина в токе Не (45 мл /мин) в течение 1 ч при 150 С, 250 С и 350 С на инфракрасном спектрометре Bio-Rad FTS-60 А. Площадь пика Si-0-Si при 1862 см-1 используют для сравнения. Количества кислоты Бренстеда и кислоты Льюиса в образце являются линейными по отношению к площадям пиков при 1540 см-1 и 1445 см-1, соответственно, так что указанные площади пиков могут быть использованы для сравнения количества кислотных участков в различных образцах. Пример 9. Каталитическая активность Изомеризацию н-гептана проводят в проточном реакторе с неподвижным слоем при давлении окружающей среды. Реакция имеет место при 150 или 200 С. Катализатор обеспечивается вместе с предварительно обработанной кварцевой тканью выше термопары. В реактор вводят н-гептан Н 2, идущим через н-гептановый сатуратор при 25 С, при мольном соотношении потока Н 2/н-гептан 16. Скорость потока Н 2 или количество загруженного катализатора регулируют с получением желаемой конверсии н-гептана. Для сравнения активности различных катализаторов конверсию н-гептана ограничивают до примерно 20% для исключения эффекта внутричастичного массопереноса. Катализатор предварительно обрабатывают в токе воздуха при 450 С в течение 1,5 ч перед контактированием с питающим газом. Реакционные продукты анализируют газовым хроматографом HP 6890, оборудованным пламенно-ионизационным детектором FID)(ПИД и 50-й деактивированной капиллярной колонной HP-PLOT/Al2O3 "KCl". Реакции изомеризации н-гексана и н-октана осуществляют в таких же условиях, как указано выше, кроме различного парциального давления. Н-гексановый сатуратор погружают в ловушку со льдом с получением мольного отношения потока Н 2/н-гексан 16, и н-октановый сатуратор устанавливают при 25 С с получением мольного соотношения потока Н 2/н-октан 53. Включение ссылок Все публикации и патенты, указанные здесь, включены в качестве ссылки во всей их полноте, как если бы каждая отдельная публикация или патент были бы специально и отдельно введены ссылкой. В случае конфликта настоящая заявка, включая любые определения здесь, будет использована для контроля. Эквиваленты Специалисты в данной области техники поймут или будут способны установить с использованием не более, чем рутинного экспериментирования, многие эквиваленты конкретным вариантам изобретения,описанным здесь. Такие эквиваленты охватываются следующей формулой изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Каталитическое соединение, представленное обобщенной формулойR1/R4/R2-R3,в которой R1 представляет металл или металлический сплав, или биметаллическую систему;R2 представляет любое металлическое легирующее вещество;R3 представляет оксид металла или смеси любых оксидов металлов;R4 выбирают из WOx, МоОх, SO42- или РО 43-; и х представляет целое или дробное число между 2 и 3, включительно. 2. Каталитическое соединение по п.1, в котором R1 представляет металл группы VIII. 3. Каталитическое соединение по п.1, в котором R1 представляет комбинацию металлов группы 4. Каталитическое соединение по п.2, в котором R1 выбирают из платины, палладия, иридия, родия или их комбинации. 5. Каталитическое соединение по п.1, в котором R1 выбирают из сплава или биметаллических систем Pt-Sn, Pt-Pd или Pt-Ge. 6. Каталитическое соединение по п.1, в котором R2 выбирают из группы Al3+, Ga3+, Ce4+, Sb5+, Sc3+,2+Mg , Co2+, Fe3+, Cr3+, Y3+, Si4+ и In3+. 7. Каталитическое соединение по п.6, в котором R2 представляет Аl3+. 8. Каталитическое соединение по п.1, в котором R3 выбирают из оксида циркония, оксида титана,оксида олова, оксида железа или оксида церия. 9. Каталитическое соединение по п.8, в котором R3 представляет ZrO2. 10. Каталитическое соединение по п.1, в котором отношение металлического легирующего вещества к металлу в оксиде составляет меньше или равно примерно 0,20. 11. Каталитическое соединение по п.10, в котором отношение металлического легирующего вещества к металлу в оксиде составляет меньше или равно примерно 0,05. 12. Каталитическое соединение по п.10, в котором отношение металлического легирующего вещества к металлу в оксиде составляет примерно 0,05. 13. Каталитическое соединение по п.1, в котором R4 представляет WOx, где х представляет целое или дробное число между 2 и 3, включительно. 14. Каталитическое соединение по п.13, в котором х равен примерно 3. 15. Каталитическое соединение по п.13, в котором х равен примерно 2,9. 16. Способ изомеризации алканового или алкильного фрагмента, включающий реакционную стадию контактирования катализатора с алкилом, где указанный катализатор выбирают из соединений,представленных обобщенной формулойR1/R4/R2-R3,в которой R1 представляет металл или металлический сплав или биметаллическую систему;R2 представляет любое металлическое легирующее вещество;R3 представляет оксид металла или смеси любых оксидов металлов;R4 выбирают из WOx, MoOx, SO42- или РО 43-; и х представляет целое или дробное число между 2 и 3, включительно. 17. Способ по п.16, в котором алкановой изомеризацией является изомеризация неразветвленного алкана. 18. Способ по п.17, в котором алкановой изомеризацией является изомеризация С 4-С 10-алкана. 19. Способ по п.18, в котором алкильной изомеризацией является изомеризация С 6-С 8-алкана. 20. Способ по п.16, в котором реакционная стадия имеет место при температуре ниже 210 С. 21. Способ по п.16, в котором реакционная стадия имеет место при температуре ниже 170 С. 22. Способ по п.16, в котором реакционная стадия имеет место при температуре ниже 150 С. 23. Способ по п.16, в котором выход реакции составляет более 70%. 24. Способ по п.23, в котором выход реакции составляет более 80%. 25. Способ по п.16, в котором алкановая изомеризация увеличивает октановое число алкана. 26. Каталитическое соединение, представленное формулой Pt/WO3/Al-ZrO2.
МПК / Метки
МПК: B01J 27/14
Метки: материалы, катализаторов, нанокомпозитные, нецеолитные, кислотных, твердых
Код ссылки
<a href="https://eas.patents.su/18-5912-neceolitnye-nanokompozitnye-materialy-dlya-tverdyh-kislotnyh-katalizatorov.html" rel="bookmark" title="База патентов Евразийского Союза">Нецеолитные нанокомпозитные материалы для твердых кислотных катализаторов</a>
Предыдущий патент: Легированные связующие порошки
Следующий патент: Фильтрующий элемент и способ его изготовления
Случайный патент: Способ игры в шахматы и устройство для его реализации