Терапевтическое лечение глазных заболеваний, связанных с фактором роста сосудистого эндотелия
Номер патента: 1752
Опубликовано: 27.08.2001
Авторы: Джироусек Майкл Р., Виньяти Луис, Кинг Джордж Л., Аиелло Ллойд П., Вэйс Дуглас Кирк
Формула / Реферат
1. Способ лечения глазных сосудистых расстройств, выбранных из группы, состоящей из дегенерации желтого пятна, отека желтого пятна, сосудистой ретинопатии, неоваскуляризации радужной оболочки, окклюзии вен сетчатки, гистоплазмоза и ишемической болезни сетчатки, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитора b изофермента протеинкиназы С следующей формулы
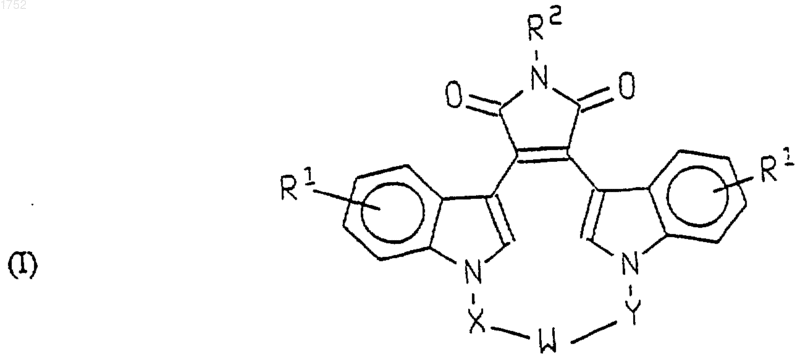
в которой W представляет -О-, -S-, -SO-, -SO2-, -СО-, С2-С6алкилен, замещенный алкилен, С2-С6алкенилен, -арил-, -арил(СН2)mО-, -гетероцикл-, -гетероцикл-(СН2)mО-, -сконденсированный бициклический-, -сконденсированный бициклический-(СН2)mО-, -NR3-, -NOR3-, -CONH- или -NHCO-,
Х и Y представляют независимо C1-C4алкилен, замещенный алкилен или X, Y и W скомбинированы вместе, образуя - (СН2)nАА-,
R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4алкокси, галогеналкил, нитро, NR4R5 или -NHCO(C1-C4 алкила),
R2 представляет водород, СН3СО-, NH2 или гидрокси,
R3 представляет водород, (CH2)mарил, C1-C4алкил, СОО(C1-C4алкил), -CONR4R5, -(C=NH)NH2, -SO(C1-C4алкил), -SO2(NR4R5) или -SO2(C1-C4алкил),
R4 и R5 представляют независимо водород, C1-C4алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,
АА представляет аминокислотный остаток,
m представляет независимо 0, 1, 2 или 3, а
n представляет независимо 2, 3, 4 или 5,
или его фармацевтически приемлемую соль, пролекарство или сложный эфир.
2. Способ по п.1, в котором ингибитор b изофермента протеинкиназы С представляет собой бис-индолилмалеимид или макроциклический бис-индолилмалеимид.
3. Способ по п.1, в котором ингибитор является изофермент-селективным и изофермент выбран из группы, состоящей из изоферментов бета-1 и бета-2.
4. Способ по п.3, в котором ингибитор протеинкиназы С представляет соединение, имеющее следующую формулу

в которой W представляет -О-, -S-, -SO-, -SO2-, -СО-, С2-С6алкилен, замещенный алкилен, С2-С6 алкенилен, -арил-, -арил(СН2)mО-, -гетероцикл-, -гетероцикл-(СН2)mО-, -сконденсированный бициклический-, -сконденсированный бициклический-(СН2)mО-, -NR3-, -NOR3-, -CONH- или -NHCO-,
Х и Y представляют независимо C1-C4 алкилен, замещенный алкилен, или X, Y и W скомбинированы вместе, образуя -(СН2)nАА,
R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкил, нитро, NR4R5 или -NHCO(C1-C4 алкила),
R2 представляет водород, СН3СО-, NH2 или гидрокси,
R3 представляет водород, (CH2)mарил, C1-C4алкил, СОО(C1-C4алкил), -CONR4R5, -(C=NH)NH2, -SO(C1-C4алкил), -SO2(NR4R5) или -SO2(C1-C4алкил),
R4 и R5 представляют независимо водород, C1-C4алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,
АА представляет аминокислотный остаток,
m представляет независимо 0, 1, 2 или 3, а
n представляет независимо 2, 3, 4 или 5,
или его фармацевтически приемлемую соль, пролекарство или сложный эфир.
5. Способ по п.4, в котором ингибитор протеинкиназы С имеет следующую формулу
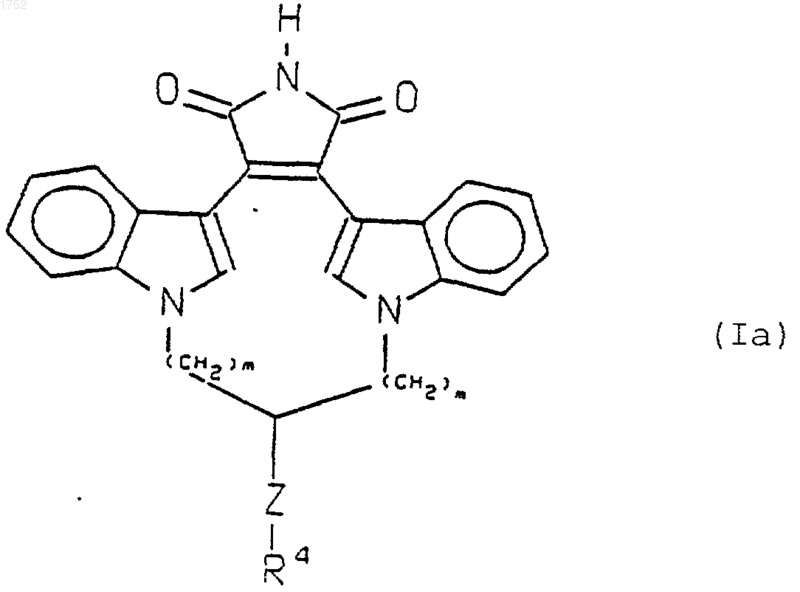
в которой Z представляет -(СН2)p- или -(СН2)p-O-(СН2)p,
R4 представляет гидрокси, -SH, C1-C4алкил, (СН2)mарил, -NH(арил), -N(СН3)(СF3), -NH(CF3) или NR5R6,
R5 представляет водород или C1-C4 алкил,
R6 представляет водород, C1-C4 алкил или бензил,
р представляет 0, 1 или 2, a
m представляет независимо 2 или 3,
или его фармацевтически приемлемую соль, пролекарство или сложный эфир.
6. Способ по п.4, в котором ингибитор протеинкиназы С представляет соединение следующей формулы
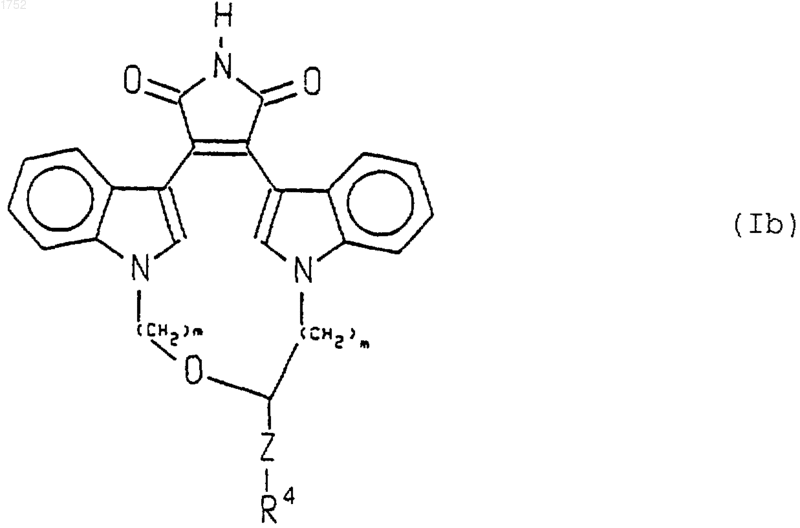
в которой Z представляет -(СН2)p-,
R4 представляет NR5R6, -NН(СF3) или -N(СН3)(СF3),
R5 и R6 представляют независимо Н или C1-C4 алкил,
р представляет 0, 1 или 2, a
m представляет независимо 2 или 3,
или его фармацевтически приемлемую соль, пролекарство или сложный эфир.
7. Способ по п.4, в котором ингибитор протеинкиназы С представляет (S)-3,4-[N,N'-1,1'-((2"-этокси)-3"'(O)-4'"-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-дион или его фармацевтически приемлемую кислотную соль.
8. Способ по п.1, в котором глазное сосудистое расстройство выбрано из группы, состоящей из дегенерации желтого пятна, отека желтого пятна, сосудистой ретинопатии, неоваскуляризации радужной оболочки, окклюзии вен сетчатки, гистоплазмоза и ишемической болезни сетчатки.
9. Способ по п.1, в котором глазное сосудистое расстройство выбрано из группы, состоящей из дегенерации желтого пятна, отека желтого пятна и окклюзии вен сетчатки.
10. Способ по п.8, в котором указанная сосудистая ретинопатия представляет собой ретинопатию недоношенности или преждевременного развития.
11. Способ ингибирования роста клеток эндотелия, стимулированного ФРСЭ, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитора b -изофермента протеинкиназы С общей формулы

в которой W представляет -О-, -S-, -SO-, -SO2-, -СО-, С2-С6алкилен, замещенный алкилен, С2-С6алкенилен, -арил-, -арил(СН2)mО-, -гетероцикл-, -гетероцикл-(СН2)mО-, -сконденсированный бициклический-, -сконденсированный бициклический-(СН2)mО-, -NR3-, -NOR3-, -CONH- или -NHCO-,
Х и Y представляют независимо C1-C4 алкилен, замещенный алкилен или X, Y и W скомбинированы вместе, образуя -(СН2)nАА,
R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкшы, нитро, NR4R5 или -NHCO(C1-C4алкила),
R2 представляет водород, СН3СО-, NH2 или гидрокси,
R3 представляет водород, (CH2)mарил, C1-C4алкил, -СОО(C1-C4алкил), -CONR4R5, -(C=NH)NH2, -SO(C1-C4алкил), -SO2(NR4R5) или -SO2(C1-C4алкил),
R4 и R5 представляют независимо водород, C1-C4 алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,
АА представляет аминокислотный остаток,
m представляет независимо 0, 1, 2 или 3, а
n представляет независимо 2, 3, 4 или 5,
или его фармацевтически приемлемую соль, пролекарство или сложный эфир.
12. Способ подавления связанной с отеком капиллярной проницаемости, стимулированной ФРСЭ, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитора b -изофермента протеинкиназы С общей формулы
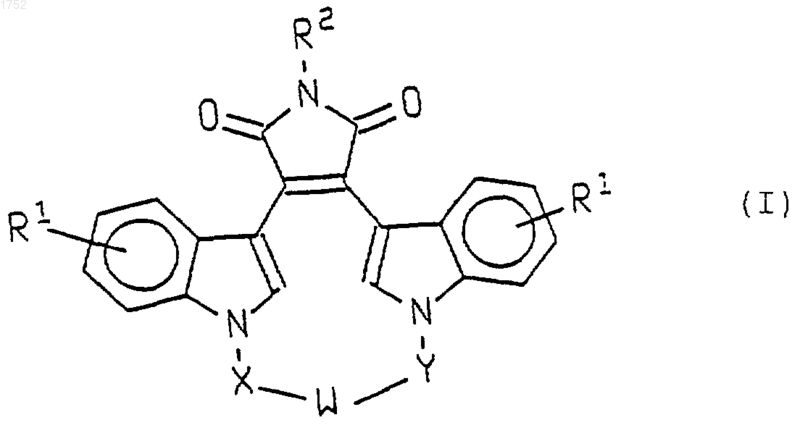
в которой W представляет -О-, -S-, -SO-, -SO2-, -СО-, С2-С6алкилен, замещенный алкилен, С2-С6алкенилен, -арил-, -арил(СН2)mО-, -гетероцикл-, -гетероцикл-(СН2)mО-, -сконденсированный бициклический-, -сконденсированный бициклический-(СН2)mО-, -NR3-, -NOR3-, -CONH- или -NHCO-,
Х и Y представляют независимо C1-C4 алкилен, замещенный алкилен или X, Y и W скомбинированы вместе, образуя -(СН2)nАА,
R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкил, нитро, NR4R5 или -NHCO(C1-C4 алкила),
R2 представляет водород, СН3СО-, NH2 или гидрокси,
R3 представляет водород, (СН2)m арил, C1-C4алкил, -СОО(C1-C4алкил), -CONR4R5, -(C=NH)NH2, -SO(C1-C4 алкил), -SO2(NR4R5) или -SO2( C1-C4 алкил),
R4 и R5 представляют независимо водород, C1-C4 алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,
АА представляет аминокислотный остаток,
m представляет независимо 0, 1, 2 или 3, а
n представляет независимо 2, 3, 4 или 5,
или его фармацевтически приемлемую соль, пролекарство или сложный эфир.
Текст
1 Предпосылки изобретения Область изобретения Настоящее изобретение в широком смысле направлено на способ ингибирования роста эндотелиальных клеток и капиллярной проницаемости, связанных с фактором роста сосудистого эндотелия (ФРСЭ), например, увеличенного клеточного роста и проницаемости, вызванных ФРСЭ, с использованием ингибитора изоферментапротеинкиназы С (ПКС). Эти состояния, вызванные ФРСЭ, тесно связаны с разнообразными глазными сосудистыми расстройствами. Настоящее изобретение направлено особенно на применение ингибитора изоферментапротеинкиназы С (ПКС) для лечения глазных сосудистых расстройств, включая дегенерацию желтого пятна, отек желтого пятна, сосудистую ретинопатию, окклюзию вен сетчатки, неоваскуляризацию радужной оболочки, гистоплазмоз и ишемические заболевания сетчатки. Описание предшествующего уровня техники ФСП/ФРСЭ представляет собой гликозилированный, многофункциональный цитокин. Избыточная экспрессия ФСП/ФРСЭ связана с разнообразными глазными сосудистыми расстройствами. ФСП/ФРСЭ вызывает пролиферацию эндотелиальных клеток, избыточную проницаемость посредством активации транспорта, опосредованного через пузырьково-вакуолярные органеллы, миграции и реорганизации актина с изменениями формы и индуляцией. Он изменяет экспрессию гена эндотелиальных клеток, вызывая повышенную выработку тканевого фактора и нескольких протеаз, включая интерстициальную коллагеназу и как урокиназоподобного активатора, так и активатора тканевого плазминогена. Большинство из этих самых генов индуцируются активацией ПКС, стимулированной форбол миристат ацетатом (ФМА). Считается, что фактор роста сосудистого эндотелия (ФРСЭ), наряду как с факторами роста фибробластов (ФРФ), так и с трансформирующим фактором роста (ТФР) играют главную роль в опосредовании активной внутриглазной неоваскуляризации у пациентов с ишемическими заболеваниями сетчатки (Aiello etSci., 35:3179-3188 (1994. Одним из глазных сосудистых расстройств, связанных с повышенной экспрессией ФРСЭ, является дегенерация желтого пятна. Связанная с возрастом дегенерация является ведущей причиной слепоты у пожилых людей. По данным оценки, дегенерация желтого пятна поражает более чем 16% людей в возрасте 85 лет и старше и 6% людей в возрасте между 65 и 74 годами. Более чем у 20% пациентов в возрасте старше 75 лет имеется дегенерация желтого 2 пятна. Болезнь чаще встречается у женщинMaculopathy: The Beaver Dam Study", Ophthalmology, 99(6):933-943, 1992). Дегенерацию желтого пятна можно разделить на сухой или влажный тип, причем сухой тип встречается в 10 раз чаще, но, в общем, по своим клиническим проявлениям протекает менее тяжело. Более тяжелая влажная или эксудативная дегенерация желтого пятна связана с патологическим ростом хориоидальных сосудов (хориоидальная неоваскуляризация) в подсетчаточный пигментный эпителий или подсетчаточное пространство и часто приводит к тяжелому ухудшению зрения. Дегенерация желтого пятна имеет первоначальное патологическое поражение, заключающееся в появлении друз, что представляет патологическое отложение ткани внутри слоя пигментного эпителия сетчатки (ПЭС) и, как считается, является вторичным по отношению к сосудистой недостаточности. Затем через оболочку Бруха, расположенную между ПЭС и хориокапиллярами, прорастают новые кровеносные сосуды, внедряясь в сетчатку. Это внедрение в сетчатку вызывает разрушение фоторецепторов и может привести к кровоизлиянию со снижением зрения. Одним из наиболее обычных видов лечения дегенерации желтого пятна является лазерная терапия. Лазерная терапия применяется для лечения зон неоваскуляризации, которые не распространяются на центральную область желтого пятна (центральная ямка). Однако после лазерной терапии часто происходит рецидив заболевания (MPS Group, Arch Ophthalmol., Vol. 109, pp. 1232-1241 (1991. Кроме того, лазерная терапия может привести к возникновению остаточных скотом и поэтому не является оптимальным способом лечения неоваскуляризации в центральной области желтого пятна. Лишь ограниченное число пациентов отвечают критериям показаний для данного способа лечения,главным образом ввиду недостаточно выявленной или скрытой природы обычно наблюдаемой хориоидальной неоваскуляризации (Freund etal., Amer. Jour. Ophthalmol., 115:786-791 (1993. В качестве терапевтического средства испытывался также интерферон на основе известной активности факторов роста, таких как фактор роста фибробластов, в отношении стимуляции патологического ангиогенеза. Однако стойкий эффект не наблюдался (Kirkpatrik et al., Br. J.Ophthalmol., 77:766-770 (1993); Chan et al., Ophthalmology, 101:289-300 (1994. Совсем недавно безуспешно завершились испытания по использованию трансформирующего фактора роста(ТФР) бета-2 для лечения дегенерации желтого пятна (Biotechnology Newswatch, January 1,1996). 3 С быстрым старением населения дегенерация желтого пятна становится существенной проблемой общественного здравоохранения. В настоящее время нет способов излечения этого заболевания, и единственным принятым способом лечения, дающим менее чем удовлетворительные результаты, является лазерное лечение,хотя FDA недавно одобрила талидомид для применения в клинических исследованиях на людях ("Researches Focus on Macular Degeneration: Common Eye Problems, Causes and Treatment Get New Attention" by Steven Sternberg,Washington Post Health, October 31, 1995). Сохраняется настоятельная потребность в способе эффективной медикаментозной терапии дегенерации желтого пятна. Отек желтого пятна связан со многими видами глазных сосудистых заболеваний, таких как пигментный ретинит, диабетическая ретинопатия, воспаление ресничного кружка, обструкция вен сетчатки, старческий гиалит, и с внутриглазными хирургическими вмешательствами (Henkind, Surv. Ophthalmol., 28:431-2Cunha-Vaz, Surv. Ophthalmol., 28: 485-92 (1984. Кистоидный отек желтого пятна является самым часто встречающимся осложнением после операций по поводу катаракты (Yanuzzi, Surv.Ophthalmol., 28: 540-53 (1984 и, возможно,самой частой причиной потери зрения у пациентов, подвергающихся экстракции хрусталика(1984. Кистоидный отек желтого пятна обычно самоограничивается, и даже в хронических случаях может произойти спонтанное улучшение(Yanuzzi, Surv. Ophthalmol., 28:540-53 (1984. Однако у небольшой части пациентов (от 1 до 15%) может развиться необратимое повреждение и постоянная утрата зрительной функции(1981. Отек желтого пятна является также причиной поздней потери зрения у пациентов с синдромом Vogt-Koyanagi-Harada (VKH) (Rutzen etal., J.Ret. and Vit. Dis., 15(6): 475-479 (1995. Отек желтого пятна тесно связан с микроаневризмами при диабетической ретинопатии, а у лиц, не страдающих диабетом - с серповидноклеточной анемией, окклюзией ответвляющихся вен, поражением сонных артерий или с тяжелой гипертонией (Klein, Med. Clin. N.Am., 72: 1415-1437 (1989. При микроаневризмах часто происходит утечка липопротеинового материала, что приводит к образованию твердых эксудатов. Эти эксудаты появляются в виде рассеянной, агрегированной или кольцеподобной конфигурации. Когда эксудаты и жидкость накапливаются в задней части сетчатки, может развиться отек желтого пятна, который может вызвать значительное затуманивание зрения и привести к потере остроты зрения. 4 Для лечения областей отечной сетчатки,примыкающих к микроаневризмам, применяется лазерная процедура, называемая очаговой фотокоагуляцией. Было показано, что очаговая фотокоагуляция снижает частоту ухудшения остроты зрения на 60% у пациентов с клинически выраженным отеком желтого пятна, но у пациентов с отеком желтого пятна от средней до умеренной степени не наблюдался благоприятный эффект фотокоагуляции (Raskin et al., Ann.Int. Med., 117(3): 226-233 (1992. Операции на стекловидном теле могут улучшить прогноз для зрения только в случаях диабетического отека желтого пятна, связанного с патологической поверхностью раздела между стекловидным телом и желтым пятном (Vaneffenterre et al., J.Francais D Ophthalmol., 16(11): 602-610 (1993. Проводилась оценка медикаментозных способов лечения отека желтого пятна, таких как оральное и местное применение индометацина (Miwa,Drag Intell. Clin. Farm., 20: 548-550 (1986, а также эритропоетина (Friedman et al., Amer. J.Kidney Dis., 26(1): 202-208 (1995, но существенный эффект не наблюдался. Существует потребность в способе эффективной медикаментозной терапии отека желтого пятна. Хотя известно, что ФРСЭ играет некоторую роль в патологии некоторых глазных сосудистых расстройств, остается необходимость определить, обеспечит ли благоприятный терапевтический эффект при лечении таких глазных сосудистых расстройств ингибирование функции, вызываемое ФРСЭ. Настоящее изобретение показывает, что с помощью ингибирования активности ФРСЭ можно снизить патологический потенциал множества из этих глазных сосудистых расстройств. Сущность изобретения Целью изобретения является предоставление способов лечения глазных сосудистых расстройств. Еще одной целью изобретения является предоставление способа ингибирования капиллярной проницаемости, связанной с отеком желтого пятна у млекопитающих. Еще одной целью изобретения является предоставление способа ингибирования неоваскуляризации, вызванной фактором роста сосудистого эндотелия (ФРСЭ). Эти и другие цели изобретения достигаются с помощью одного или более вариантов реализации, описанных ниже. Согласно одному воплощению изобретения предоставляется способ лечения глазных сосудистых расстройств, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. Согласно другому воплощению изобретения предоставляется способ печения дегенерации желтого пятна у млекопитающих, который 5 включает введение млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. Согласно еще одному варианту воплощения изобретения предоставляется способ ингибирования капиллярной проницаемости, связанной с отеком желтого пятна у млекопитающих,который включает введение млекопитающему терапевтически эффективного количества ингибитора изоферментапротеинкиназы С. Согласно еще одному воплощению изобретения предоставляется способ ингибирования фактора роста сосудистого эндотелия(ФРСЭ), который включает введение млекопитающему подавляющего ФРСЭ количества ингибитора изоферментапротеинкиназы С. Настоящее изобретение обеспечивает технику соединениями, которые дают профилактический и лечебный эффект при различных глазных сосудистых расстройствах. Краткое описание чертежей На фиг. 1 показано подавляющее действие ингибитора ПКС, (S)-3,4-[N,N'-1,1'-2"-этокси 3"'(О)-4"'-(N,N-диметиламино)-бутан)-бис-(3,3'индолил)]-1(Н)-пиррол-2,5-диона, на рост эндотелиальных клеток, стимулированный рекомбинантным ФРСЭ человека; на фиг. 2 дополнительно показано подавляющее действие ингибитора ПКС, (S)-3,4[N,N'-1,1'-2"-этокси-3'"(O)-4'"-(N,N-диметиламино)-бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона, на рост эндотелиальных клеток, стимулированный рекомбинантным ФРСЭ человека; на фиг. 3 показано воздействие ингибитора ПКС на активность эндогенного ФРСЭ, экспрессируемого после культивирования перицитов сетчатки в условиях гипоксии; на фиг. 4 дополнительно показано подавляющее влияние ингибитора ПКС на рост эндотелиальных клеток, стимулированный рекомбинантным ФРСЭ человека; на фиг. 5 А, 5 В показана динамика проницаемости сетчатки, вызванной ФРСЭ; на фиг. 6 показана реакция проницаемости сетчатки для флюоресцеина на ФРСЭ; на фиг. 7 показано действие ингибирования и стимуляции ПКС в стекловидном теле на проницаемость сетчатки; на фиг. 8 А, 8 В показано ингибирование проницаемости сетчатки в ответ на ФРСЭ с помощью орально вводимого ингибитора протеинкиназы С . Подробное описание изобретения Находкой согласно настоящему изобретению является то, что терапевтическое применение особого класса ингибиторов протеинкиназы С, а именно, ингибиторов изоферментапротеинкиназы С, и особенно, избирательных ингибиторов изоферментапротеинкиназы С, противодействует воздействиям ФРСЭ. В частно 001752 6 сти, открытием настоящего изобретения является то, что применение этого особого класса ингибиторов протеинкиназы С противодействует росту клеток эндотелия и капиллярной проницаемости, особенно, росту клеток эндотелия и капиллярной проницаемости, стимулированным фактором роста ФРСЭ. Следовательно, такие соединения могут применяться терапевтически для лечения заболеваний, связанных с ФРСЭ, в частности, множества глазных сосудистых расстройств. В способе данного изобретения предпочтительно используются те ингибиторы протеинкиназы С, которые эффективно ингибируют или подавляют изофермент . Одна подходящая группа соединений в общем описана в предшествующем уровне техники как бисиндолилмалеимиды или макроциклические бисиндолилмалеимиды. Бис-индолилмалеимиды,хорошо известные в предшествующем уровне техники, включают соединения, которые описаны в патентах США 5621098, 5552396, 5545636,5481003, 5491242 и 5057614, и все они приведены здесь для сведения. Макроциклические бисиндолилмалеимиды, в частности, представлены соединениями формулы I. Эти соединения и способы их получения были раскрыты в патенте США 5552396, который здесь - для сведения. Эти соединения вводятся в терапевтически эффективном количестве млекопитающему для ингибирования роста клеток эндотелия или капиллярной проницаемости, связанных с ФРСЭ,и для подавления воздействий ФРСЭ, связанных с глазными заболеваниями. Эти соединения можно также вводить пациентам, подверженным риску упомянутых выше патологических состояний в качестве профилактических средств. Один предпочтительный класс соединений для применения в способе изобретения представляет соединения формулыR1 радикалы представляют водород или до четырех необязательных заместителей, незави 7 симо выбранных из галогена, C1-C4 алкила, гидрокси, С 1-С 4 алкокси, галогеналкила, нитро,NR4R5 или -NHCO(C1-C4 алкил);R4 и R5 представляют независимо водород,C1-C4 алкил, фенил, бензил или комбинируются с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо; АА представляет аминокислотный остаток;n представляет независимо 2, 3, 4 или 5,или их фармацевтически приемлемые соли,пролекарства или сложные эфиры. Более предпочтительный класс соединений для применения в данном изобретении представлен формулой I, в которой фрагменты -XW-Y- содержат от 4 до 8 атомов, которые могут быть замещенными или незамещенными. Более предпочтительно, фрагменты -X-W-Y- содержат 6 атомов. Другие предпочтительные соединения для применения в способе данного изобретения являются соединениями формулы I, в которой R1 иR2 представляют независимо водород; и W представляет замещенный алкилен, -О-, S-,-CONH-, -NHCO- или -NR3. Особенно предпочтительными соединениями для применения в изобретении являются соединения формулы Iа в которой Z представляет -(CH2)p- или - (СН 2)pO-(CH2)p; R4 представляет гидрокси, -SH, C1C4 алкил, (СН 2)mарил, -NН(арил), -N(СН 3)(СF3),-NН(СF3) или NR5R6; R5 представляет водород или C1-С 4 алкил; R6 представляет водород, C1-C4 алкил или бензил; р представляет 0, 1 или 2; и m представляет независимо 2 или 3, или их фармацевтически приемлемые соли, пролекарства или сложные эфиры. Наиболее предпочтительными соединениями формулы Iа являются те, в которых Z представляет CH2; a R4 представляет-NH2, NН(СF3), или -N(СН 3)2, или их фармацевтически приемлемые соли, пролекарства или сложные эфиры. Другие предпочтительные соединения для применения в способе настоящего изобретения представляют соединения, в которых W в формуле I представляет -О-, Y представляет заме 001752 8 щенный алкилен, а Х представляет алкилен. Эти предпочтительные соединения представлены формулой Ib в которой Z представляет -(CH2)p-; R4 представляет NR5R6; -NН(СF3) или -N(СН 3)(СF3); R5 и R6 представляют независимо Н или C1-C4 алкил; р представляет 0, 1 или 2; a m представляет независимо 2 или 3, или их фармацевтически приемлемые соли, пролекарства или сложные эфиры. Наиболее предпочтительными соединениями формулы Ib являются соединения, в которых р представляет 1; а R5 и R6 представляют метил. Соединения формул I, Ia и Ib ввиду того,что они содержат основную часть или фрагмент,могут также существовать в виде фармацевтически приемлемых кислотно-аддитивных солей. Кислоты, обычно используемые для образования таких солей, включают неорганические кислоты, такие как хлористо-водородная, бромисто-водородная, иодисто-водородная, серная и фосфорная кислота, а также органические кислоты, такие как паратолуолсульфоновая, метансульфоновая, щавелевая, парабромфенилсульфоновая, карбоновая, янтарная, лимонная,бензойная, уксусная кислота и родственные неорганические и органические кислоты. Такие фармацевтически приемлемые соли, таким образом, включают сульфат, пиросульфат, бисульфат, сульфит, бисульфит, фосфат, моногидрофосфат, дигидрофосфат, метафосфат, пирофосфат, хлорид, бромид, иодид, ацетат, пропионат, деканоат, каприлат, акрилат, формат, изобутират, гептаноат, пропиолат, оксалат, малонат, сукцинат, суберинат, себацинат, фумарат,малеат, 2-бутин-1,4-диоат, 3-гексин-2,5-диоат,бензоат, хлорбензоат, гидроксибензоат, метоксибензоат, фталат, ксилолсульфонат, фенилацетат, фенилпропионат, фенилбутират, цитрат,лактат, гиппурат, -гидроксибутират, гликолят,малеат, тартрат, метансульфонат, пропансульфонат, нафталин-1-сульфонат, нафталин-2 сульфонат, манделат и аналогичные. Особенно применяются хлористо-водородная соль и мезилат. В дополнение к фармацевтически приемлемым солям могут также существовать другие соли. Они могут служить в качестве промежуточных продуктов при очистке соединений, при получении других солей или при идентификации и характеристике соединений или промежуточных продуктов. Фармацевтически приемлемые соли соединений формул I, Iа и Ib могут также сущест 9 вовать в виде различных сольватов, таких как с водой, метанолом, этанолом, диметилформамидом, этилацетатом и аналогичными. Могут также получаться смеси таких сольватов. Источником такого сольвата может быть растворитель кристаллизации, присущий растворителю получения или кристаллизации, или дополнительный к такому растворителю. Признано, что могут существовать различные стереоизомерные формы соединений формул I, Ia и Ib; например, W может содержать хиральный атом углерода в замещенной алкиленовой части. Соединения обычно получаются в виде рацематов и могут удобно использоваться в этом виде. Альтернативно, по желанию, с помощью обычных методик могут выделяться или синтезироваться индивидуальные энантиомеры. Такие рацематы и индивидуальные энантиомеры и их смеси образуют часть соединений, используемых в способах настоящего изобретения. Соединения, используемые в данном изобретении, также охватывают фармацевтически приемлемые пролекарства соединений формулI, Ia и Ib. Пролекарство представляет собой лекарство, которое подвергнуто химической модификации и может быть биологически неактивным в участке его действия, но которое может разрушаться или модифицироваться под влиянием одного или более ферментных или других процессов in vivo с образованием исходной родительской или биоактивной формы. Вероятно, это пролекарство может иметь фармакокинетический профиль, отличный от родительского, обеспечивая облегчение всасывания через эпителий слизистой оболочки, лучшее образование соли или лучшую растворимость и/или улучшенную системную устойчивость(например, увеличение периода полувыведения из плазмы). Обычно такие химические модификации включают следующие: 1) сложноэфирные или амидные производные, которые могут расщепляться эстеразами или липазами; 2) пептиды, которые могут распознаваться специфичными или неспецифичными протеазами; или 3) производные, которые накапливаются в участке действия посредством мембранной селекции пролекарственной формы или модифицированной пролекарственной формы; или любую комбинацию приведенных выше модификаций 1-3. Обычные способы отбора и получения подходящих производных пролекарств описаны, например, в работе Н. Bungaard, Design ofProdrugs, (1985). Синтез различных бис-индол-N-малеимидных производных описан в патенте США 5057614, выданном Davis et al., а синтез предпочтительных соединений, подходящих для использования в этом изобретении, описан в ранее указанном патенте США 5552396 и в описании 10 ЕР 0657411 А 1, выданного Faul et al., все из которых приведены здесь для сведения. Одним особенно предпочтительным ингибитором протеинкиназы- для использования в способе данного изобретения является соединение, описанное в примере 5g (хлористо-водородная соль (S)-3,4-[N,N'-1,1'-2"-этокси)-3"'(O)4'"-(N,N-диметиламино)-бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5-диона) упомянутого выше патента США 5552396. Это соединение является мощным ингибитором протеинкиназы С. Оно является селективным по отношению к протеинкиназе С, в сравнении с другими киназами и является высоко изоферментселективным, т.е. оно является селективным в отношении бета-1 и бета-2 изоферментов. Благоприятны также другие соли данного соединения, особенно мезилатные соли. Предпочтительная мезилатная соль может быть получена с помощью реакции соединения формулы II с метансульфоновой кислотой в не реакционноспособном органическом растворителе, предпочтительно смеси органического растворителя и воды, и наиболее предпочтительно водаацетон. Могут применяться и другие растворители, такие как метанол, ацетон, этилацетат и их смеси. Соотношение растворителя и воды не имеет принципиального значения и обычно определяется растворимостью реагентов. Предпочтительные соотношения растворителя и воды обычно составляют в интервале от 0,1:1 до 100:1 по объему. Предпочтительно, соотношение составляет от 1:1 до 20:1, и наиболее предпочтительно от 5:1 до 10:1. Оптимальное соотношение зависит от выбранного растворителя, и предпочтительным является ацетон при соотношении растворителя и воды 9:1. В реакции обычно участвуют эквимолярные количества двух реагентов, хотя могут применяться другие соотношения, особенно такие, при которых имеется избыток метансульфоновой кислоты. Скорость добавления метансульфоновой кислоты не имеет принципиального значения для реакции, и она может добавляться быстро (5 мин) или медленно в течение 6 ч или более. Реакция проводится при температурах в диапазоне от 0 С до температуры дефлегмации. Реакционная смесь перемешивается до тех пор, пока не завершится образование соли, что определяется по данным порош 11 ковой рентгенограммы и может занимать от 5 мин до 12 ч. Соли настоящего изобретения предпочтительно и легко получаются в кристаллической форме. Тригидратную форму соли можно легко превратить в моногидрат после сушки или воздействия относительной влажности от 20 до 60%. Соль является, по существу, кристаллической, имеющей определенную точку плавления,двойное лучепреломление и характер рентгеновской дифракции. Обычно кристаллы имеют менее чем 10% аморфного твердого вещества,предпочтительно менее чем 5% и наиболее предпочтительно менее чем 1% аморфного твердого вещества. Мезилатная соль выделяется с помощью фильтрования или других признанных в данной области техники приемов разделения непосредственно из реакционной смеси с выходом в диапазоне от 50 до 100%. При желании для дальнейшей очистки могут применяться перекристаллизация и другие приемы очистки, известные в данной области. Эндотелиальные клетки в тканевой культуре, стимулированные факторами роста, такими как ФРСЭ, проявляют более высокую скорость роста, чем скорость роста базальных клеток. Эксперименты, выполненные согласно настоящему изобретению, показали, что при введении in vitro в концентрации приблизительно от 0,1 до 100 нмоль, ингибитор протеин киназы С кислотная соль (S)-3,4-[N,N'-1,1'-2"-этокси)3"'(O)-4'"-(N,N-диметиламино)-бутан)-бис-(3,3'индолил)]-1(Н)-пиррол-2,5-диона значительно ингибирует рост не базальных клеток, стимулированных фактором роста (таким как ФРСЭ). Важно, другие исследования показали, что рост нормальных эндотелиальных клеток в тканевой культуре не ингибируется этим соединением, по данным отсутствия ингибирования роста эндотелиальных клеток без стимуляции ФРСЭ в нормоксических кондиционированных средах. В гипоксических кондиционированных средах скорость клеточного роста возрастает вследствие увеличения содержания эндогенного фактора роста, ФРСЭ, вырабатываемого гипоксическими клетками. И снова ингибитор протеинкиназы С, кислотная соль (S)-3,4-[N,N'-1,1'2"-этокси)-3"'(О)-4'"-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5 диона, нормализует клеточный рост, вызванный такими гипоксическими условиями. Эксперименты, предоставленные в настоящем изобретении, показывают, что факторы роста, такие как ФРСЭ, также воздействуют на капиллярную проницаемость. Исследования показали, что в экспериментальной модели ФРСЭ значительно увеличивает капиллярную проницаемость, вплоть до трехкратного уровня. Это зависимое от ФРСЭ увеличение капиллярной проницаемости также является дозозависимым. В соответствии с исследованиями на жи 001752 12 вотных in vivo, введение ингибитора протеинкиназы С в концентрации приблизительно 25 мг/кг/день перед провокационной пробой с введением ФРСЭ значительно ингибировало капиллярную проницаемость, вызванную ФРСЭ. Особенно предполагается применение концентраций от 1 нмоль до 5 ммоль и предпочтительно от 1 до 500 нмоль. Ингибирование может достигать 80% и обычно специфично для капиллярной проницаемости, вызванной фактором роста. Капиллярную проницаемость можно измерить с помощью ангиографии с флюоресцеином. В частности, при отеке желтого пятна ангиография с флюоресцеином является процедурой фотографирования сетчатки, включающей инъекцию флюоресцентного красителя в поток крови для выявления зон утечки в сетчатку. Хотя и не желая ограничиваться какимлибо техническим объяснением, заявитель (заявители) считают, что изменения перфузии сетчатки, возникающие вследствие сниженного кровотока, потеря капилляров сетчатки, агенез или облитерация периферической сосудистой системы или отделения хориоидального кровоснабжения от сетчатки - все это может в результате привести к относительной ишемии сетчатки. Эта ишемия стимулирует синтез и секрецию факторов роста, таких как ФРСЭ в перицитах сетчатки, эндотелиальных клетках, пигментном эпителии сетчатки, клетках глии и, возможно, в других типах клеток; и впоследствии ведет к неоваскуляризации сетчатки и повышенной капиллярной проницаемости. Эти состояния связаны со множеством глазных сосудистых расстройств. Ингибиторыизофермента ПКС согласно настоящему изобретению могут применяться для лечения болезненных состояний, связанных с ростом эндотелиальных клеток и капиллярной проницаемости, особенно множества глазных сосудистых расстройств. Глазные сосудистые расстройства, которые можно лечить с помощью соединений настоящего изобретения, включают, но не ограничиваются, дегенерацию желтого пятна, отек желтого пятна, сосудистую ретинопатию, окклюзию вен сетчатки, неоваскуляризацию радужной оболочки, гистоплазмоз и ишемические заболевания сетчатки. Дегенерация желтого пятна может быть возрастной. Отек желтого пятна может быть связан с диабетом или окклюзией центральной вены сетчатки. Используемая здесь фраза сосудистая ретинопатия не включает диабетическую ретинопатию, но включает сосудистую ретинопатию, связанную с серповидноклеточной анемией, недоношенностью(преждевременным развитием) младенцев и неоваскуляризацией угла или трабекулярной сети. Неоваскуляризация радужной оболочки может быть диабетической или не связанной с диабетом. 13 Специалист в данной области очевидно понимает, что терапевтически эффективное количество ингибиторов протеинкиназы С-, применяемых в соответствии с настоящим изобретением, представляет собой количество, достаточное для ингибирования роста эндотелиальных клеток или развития проницаемости капилляров путем ингибирования ФРСЭ, и что данное количество варьирует в зависимости от размера пораженной ткани, концентрации соединения в терапевтической готовой форме и массы тела пациента. Обычно количество ингибитораизофермента протеинкиназы С, вводимого в качестве терапевтического средства для лечения глазных сосудистых расстройств, определяется в каждом случае лечащим врачом. В качестве руководства при установлении соответствующей дозы будут рассматриваться степень неоваскуляризации, масса тела и возраст пациента. Обычно подходящей дозой является доза,которая дает концентрацию ингибитораизофермента протеинкиназы С в участке лечения, в диапазоне от 0,5 нмоль до 200 мкмоль, а более обычно от 0,5 до 200 нмоль. Ожидается, что в большинстве случаев должна быть достаточной концентрация в сыворотке от 0,5 до 100 нмоль. Для получения этих лечебных концентраций нуждающемуся в лечении пациенту, вероятно, будет вводиться приблизительно от 0,001 мг в день на 1 кг массы тела до 50,0 мг в день на 1 кг. Обычно потребуется не более чем приблизительно от 1,0 до 10,0 мг в день на 1 кг массы тела ингибитора протеинкиназы С-. Как отмечалось выше, указанные количества могут варьировать от случая к случаю. Соединения формулы I и предпочтительные соединения формулы Iа и Ib предпочтительно преобразуются в готовые формы или препараты перед введением. Подходящие фармацевтические готовые формы получают с помощью известных способов с использованием хорошо известных и легко доступных ингредиентов. При приготовлении композиций, подходящих для применения в способе настоящего изобретения, активный ингредиент обычно смешивается с носителем или разбавляется носителем, или помещается внутрь носителя, который может быть в форме капсулы, саше, бумаги или другого контейнера. Когда носитель служит в качестве разбавителя, он может быть твердым, полутвердым или жидким материалом,который действует в качестве носителя, наполнителя или среды для активного ингредиента. Так композиции могут быть в форме таблеток,пилюль, порошков, пастилок, саше, каше, эликсиров, суспензий, эмульсий, растворов, сиропов,аэрозоля (в виде твердого вещества или в жидкой среде), мягких и твердых желатиновых капсул, в форме свечей, стерильных растворов для инъекций и стерильных упакованных порошков 14 или для орального, или для местного применения. Некоторые примеры подходящих носителей, эксципиентов и разбавителей включают лактозу, декстрозу, сахарозный сорбит, маннит,крахмалы, камедь акации, фосфаты кальция,альгинат, трагакант, желатин, силикат кальция,микрокристаллическую целлюлозу, поливинилпирролидон, целлюлозу, водный сироп, метилцеллюлозу, метил и пропилгидроксибензоаты,тальк, стеарат магния и минеральное масло. Готовые формы могут дополнительно включать смазочные агенты, увлажняющие агенты,эмульгирующие и суспендирующие агенты,подслащивающие средства или агенты или ароматизирующие средства. Композиции изобретения могут составляться так, чтобы обеспечить быстрое, длительное или отсроченное высвобождение активного ингредиента после введения пациенту. Композиции предпочтительно составляются в форме единичной дозы, причем каждая доза содержит от приблизительно 0,05 мг до приблизительно 3 г, более обычно приблизительно 750 мг активного ингредиента. Однако следует понимать, что введенная терапевтическая доза определяется врачом с учетом соответствующих обстоятельств, включая тяжесть подлежащего лечению состояния, выбор подлежащего введению соединения и выбранный путь введения. Поэтому указанные выше диапазоны дозировки никоим образом не предназначены для ограничения объема притязаний изобретения. Термин "форма единичной дозы" относится к физически дискретным единицам,подходящим в качестве стандартных доз для людей и других млекопитающих, причем каждая единица содержит заданное количество активного материала, рассчитанное с целью вызвать желательный терапевтический эффект, в сочетании с подходящим фармацевтическим носителем. В дополнение к указанным выше готовым формам, большинство из которых может вводиться орально, соединения, применяемые в способе настоящего изобретения, могут также применяться местно. Формы для местного применения включают мази, кремы и гели. Мази обычно получают с использованием или 1) маслянистой основы, т.е. основы, состоящей из фиксированных масел или углеводородов, таких как белый вазелин, или минеральное масло, или 2) абсорбентной основы, т.е. основы, состоящей из безводного вещества или веществ, которые могут поглощать воду, например, безводный ланолин. Обычно после образования основы, маслянистой или абсорбентной, добавляется активный ингредиент (соединение) в количестве, обеспечивающем желаемую концентрацию. Кремы представляют собой масляно/водную эмульсию. Они состоят из масляной фазы (внутренней фазы), обычно включающей фиксированные масла, углеводороды и аналогичные, такие как воски, вазелин, минеральное масло и аналогичные, и водную фазу (непрерывная фаза), включающую воду и любые водорастворимые вещества, такие как соли. Эти две фазы стабилизируются с использованием эмульгирующего средства, например поверхностноактивного вещества, такого как натрийлаурилсульфат, гидрофильные коллоиды, такие как коллоидные глины акации, камедь и аналогичные. После составления эмульсии обычно добавляется активный ингредиент (соединение) в количестве, необходимом для достижения желательной концентрации. Гели включают основу, выбранную из маслянистой основы, воды или эмульсионносуспензионной основы. К основе добавляется желирующее средство, которое формирует в основе матрицу, увеличивая ее вязкость. Примерами желирующих агентов являются гидроксипропилцеллюлоза, полимеры акриловой кислоты и аналогичные. Обычно активный ингредиент (соединения) добавляется в готовую форму в желательной концентрации в момент,предшествующий добавлению желирующего агента. Количество соединения, включаемого в готовую форму для местного применения, не имеет принципиального значения; концентрация должна быть в диапазоне, достаточном для обеспечения возможности быстрого нанесения готового препарата на область пораженной ткани в количестве, которое доставит желаемое количество соединения в желаемый участок лечения. Обычное количество готовой формы для местного применения, которое предполагается нанести на пораженную ткань, зависит от размера пораженной ткани и концентрации соединения в форме. Обычно готовый препарат наносится на пораженную ткань в количестве, обеспечивающем приблизительно от 1 до 500 мкг соединения на 1 см 2 пораженной ткани. Предпочтительно нанесенное количество соединения находится в диапазоне приблизительно от 30 до 300 мкг/см 2, более предпочтительно приблизительно от 50 до 200 мкг/см 2 и наиболее предпочтительно приблизительно от 60 до 100 мкг/см 2. Следующие примеры готовых форм или препаратов являются только иллюстративными и никоим образом не предназначены для ограничения объема притязаний согласно изобретению. Готовая форма Твердые желатиновые капсулы изготовлены с использованием следующих ингредиентов: Активное средство Крахмал высушенный Стеарат магния Всего 16 Указанные ингредиенты смешивают и ими в количествах 460 мг заполняют твердые желатиновые капсулы. Готовая форма Таблетка изготавливается с использованием указанных ниже ингредиентов: Активное средство Целлюлоза микрокристаллическая Двуокись кремния мелкодисперсная Стеариновая кислота Всего Компоненты смешивают и прессуют для образования таблеток, масса каждой из которых составляет 665 мг. Готовая форма Таблетки, каждая из которых содержит 60 мг активного ингредиента, изготавливаются следующим образом: Активное средство Крахмал Микрокристаллическая целлюлоза Поливинилпирролидон (в виде 10% раствора в воде) Растворимый крахмал натрийкарбоксиметил Стеарат магния Тальк Всего Активный ингредиент, крахмал и целлюлозу пропускают через сито 45 меш США и тщательно смешивают. Раствор поливинилпирролидона смешивают с полученными в результате порошками, которые пропускают через сито 14 меш США. Полученные таким образом гранулы сушат при 50 С и пропускают через сито 18 меш США. Растворимый крахмал, стеарат магния и тальк, ранее пропущенные через сито 60 меш США, затем добавляют в гранулы, которые после смешивания прессуют с помощью таблетирующего устройства для получения таблеток, каждая из которых имеет массу 150 мг. Примеры Все эти примеры демонстрируют использование хлористо-водородной соли (S)-3,4[N,N'-1,1'-2"-этокси)-3'"(О)-4'"-(N,N-диметиламино)-бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона для ингибирования in vitro роста эндотелиальных клеток и ингибирования in vivo увеличенной капиллярной проницаемости, стимулированной ФРСЭ. Пример 1. В данном примере ингибирующий эффект указанного соединения в отношении роста клеток, стимулированного ФРСЭ, исследуют с использованием рекомбинантного человеческого ФРСЭ. 17 Бычьи эндотелиальные клетки сетчатки выделяют из свежих глаз телят с помощью гомогенизации и серии этапов фильтрации. Первичные культуры эндотелиальных клеток выращивают в покрытых фибронектином (NYBenDulbecco's Eagle's (DMEM) с 5,5 ммоль глюкозы,10% полученной из плазмы лошадиной сыворотки (Wheaton, Scientific), 50 мг гепарина на 1 л и 50 единиц фактора роста эндотелиальных клеток на 1 л (Boehringer Mannheim). После того, как клетки достигнут слияния, среду меняют,включая 5% сыворотки плода теленка (HyClonc). Среду меняют 1 раз в 3 дня. Гомогенность эндотелиальных клеток подтверждают с помощью антител против фактора VIII. Влияние указанного ингибитора ПКС на действие ФРСЭ in vitro оценивают с использованием высеянных с низкой плотностью на чашки культур микрососудистых эндотелиальных клеток бычьей сетчатки, которые претерпевают стимуляцию роста после добавления ФРСЭ. Эндотелиальные клетки бычьей сетчатки высевают с низкой плотностью (2500 клеток на 1 ячейку или лунку) на 24-луночные чашки (Costar), инкубированные в течение ночи в DMEM,содержащей 10% телячью сыворотку (GIBCO). Среду меняют на следующий день. Для исследования воздействия указанного ингибитора ПКС на рост эндотелиальных клеток, проводят одну серию экспериментов, в которой рост клеток в отсутствие какого-либо средства служит в качестве контроля, а затем исследуют воздействие добавления указанного ингибитора ПКС и в присутствии ВРСЭ (25 нг/мл; Genetech), и в отсутствие ФРСЭ. После инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% додецилсульфате натрия(НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюорометра(модель ТКО-100; Hoefer). Все определения выполняют, по меньшей мере, трижды и эксперименты повторяют минимум три раза. Результаты выражают в виде среднихстандартное отклонение по всем экспериментам. Анализ результатов in vitro выполняют с помощью непарного теста по Стьюденту. Величину Р, составляющую 0,050, считают статистически достоверной. На фиг. 1 показаны результаты, полученные с использованием рекомбинантного ФРСЭ. Как показано тремя самыми левыми столбиками на фигуре, добавление указанного ингибитора ПКС в культуру эндотелиальных клеток, по существу, не оказывало воздействия на исходную скорость роста (первый столбик). Скорость роста существенно возросла после добавления ФРСЭ (четвертый столбик). Эта скорость роста значительно уменьшается после добавления 0,5 нмоль указанного ингибитора ПКС (четыре самых правых столбика). 18 Пример 2. Этот пример аналогичен работе, представленной на фиг. 1, и дополнительно иллюстрирует ингибирующее влияние указанного ингибитора ПКС на рост клеток, стимулированный ФРСЭ, с использованием рекомбинантного человеческого ФРСЭ. Используя процедуры примера 1, выделяют и выращивают бычьи эндотелиальные клетки сетчатки; затем получают засеянные на чашки культуры с низкой плотностью. Опять же используя процедуру примера 1, проводят эксперименты, в которых исследуют влияние указанного ингибитора ПКС на рост эндотелиальных клеток и в присутствии ФРСЭ (25 нг/мл;Genetech), и в отсутствие ФРСЭ. После инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% додецилсульфате натрия (НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюорометра (модель ТКО-100; Hoefer). На фиг. 2 показаны результаты этой работы. Как показано столбиками над подписью-ФРСЭ, добавление указанного ингибитора ПКС в культуру эндотелиальных клеток при концентрации от 0,1 до 100 нмоль, по существу, не оказывало воздействия на исходную скорость роста клеток. Стимуляция эндотелиальных клеток рекомбинантным человеческим ФРСЭ (25 нг/мл) вызывала достоверное увеличение содержания клеточной ДНК через 4 дня, что указывает на увеличение скорости роста, в сравнении с нестимулированными клетками (сравните-ФРСЭ при 0 с +ФРСЭ при 0). Эта скорость роста значительно уменьшается после добавления указанного ингибитора ПКС (четыре самых правых столбика над надписью +ФРСЭ). В частности, стимулирующая способность ФРСЭ слегка снижалась в присутствии 0,1 нмоль ингибитора ПКС и, по существу, полностью устранялась одновременным добавлением ингибитора ПКС в концентрации 1 нмоль и выше. Пример 3. В этом примере исследуют воздействие указанного ингибитора ПКС на активность эндогенного ФРСЭ, экспрессируемую после культивации перицитов сетчатки в условиях гипоксии. Бычьи эндотелиальные клетки сетчатки и перициты сетчатки выделяют из свежих глаз телят с помощью гомогенизации и серии этапов фильтрации. Используя процедуры примера 1,эндотелиальные клетки выращивают и с низкой плотностью культивируют на чашках. Используя аналогичные методики, перициты бычьей сетчатки культивируют в DMEM/5,5 ммоль глюкозы с 20% сыворотки плода теленка. Гипоксическую кондиционированную среду для экспрессии эндогенного ФРСЭ и нормоксическую кондиционированную контрольную среду соответственно готовят, выполняя следующие процедуры. Слившиеся монослои пе 19 рицитов сетчатки подвергают воздействию в течение 24 ч 2% O2/5% СO2/93% N2 с использованием совершенного, контролируемого компьютером инкубатора CO2 Lab-Line Instruments с инфракрасной водяной рубашкой и контролем пониженного содержания кислорода (модель 480). Все клетки сохранялись при 37 С и при световой микроскопии в них не было никаких морфологических изменений, они исключали краситель трипан синий (98%) и в последующем их можно было нормально пересевать. Клетки, инкубированные в нормоксических условиях (95% воздуха/5% CO2) из той же партии и пересева используют в качестве контролей. Среду затем собирают и перед использованием фильтруют (Nalgene; 0,22 мкм). В этом примере проводят эксперименты, в которых исследуют воздействие указанного ингибитора ПКС на рост эндотелиальных клеток в присутствии или нормоксической кондиционированной среды, или гипоксической кондиционированной среды. Как и в предыдущих экспериментах, после инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% додецилсульфате натрия (НДС) и измеряют содержание ДНК с использованием красителя Hoechst 33258 и флюорометра (модель ТКО-100; Hoefer). В исследованиях, представленных на фиг. 3, указанный ингибитор ПКС используют в концентрации 10 нмоль. Как показано на фиг. 3,рост эндотелиальных клеток сетчатки стимулируется кондиционированной средой из перицитов сетчатки, культивированных в гипоксических условиях, которые, как известно, вызывают экспрессию ФРСЭ (сравните столбик 1 со столбиком 3 на фиг. 3). Эта стимуляция роста подавляется (нормализуется) в присутствии соли хлористо-водородной кислоты (S)-3,4-[N,N'1,1'-2"-этокси)-3'"(О)-4'"-(N,N-диметиламино)бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5 диона ингибитора ПКС (сравните столбик 3 со столбиком 4). Пример 4. Этот пример аналогичен работе, представленной на фиг. 1 и 2, и дополнительно иллюстрирует ингибирующее действие указанного ингибитора ПКС на рост клеток, стимулированный ФРСЭ, с использованием рекомбинантного человеческого ФРСЭ. Используя процедуру примера 1, выделяют и выращивают бычьи эндотелиальные клетки сетчатки; затем получают культуры, высеянные с низкой плотностью на чашки. Опять же, используя процедуру примера 1, проводят эксперименты, в которых исследуют влияние указанного ингибитора ПКС на рост эндотелиальных клеток и в присутствии (+ФРСЭ)(25 нг/мл; Genetech), и в отсутствие ФРСЭ (-ФРСЭ). Как указано выше, после инкубации при 37 С в течение 4 дней клетки лизируют в 0,1% додецилсульфате натрия (НДС), и измеряют содержание ДНК с 20 использованием красителя Hoechst 33258 и флюорометра (модель ТКО-100; Hoefer). На фиг. 4 показаны результаты этой работы. Как показано столбиками над подписью-ФРСЭ, добавление указанного ингибитора ПКС в культуру эндотелиальных клеток при концентрации 10 нмоль, по существу, не оказывало воздействия на исходную скорость роста клеток. Стимуляция эндотелиальных клеток рекомбинантным человеческим ФРСЭ (25 нг/мл) вызывала достоверное увеличение содержания клеточной ДНК, что указывает на увеличение скорости роста, в сравнении с нестимулированными клетками (сравните -ФРСЭ контроль с+ФРСЭ контролем). Эта скорость роста значительно уменьшается после добавления указанного ингибитора ПКС в концентрации 10 нмоль. Эти результаты показывают, что раскрытый класс ингибиторов ПКС и, в частности, (S)-3,4[N,N'-1,1'-2"-этокси)-3'"(О)-4'"-(N,N-диметиламино)-бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-дион предотвращает стимуляцию in vitro роста эндотелиальных клеток, как экзогенным,так и индуцированным гипоксией ФРСЭ. Поскольку экспрессия ФРСЭ была тесно связана с неоваскуляризацией, связанной с дегенерацией желтого пятна, эти результаты подтверждают пользу данных ингибиторов ПКС в качестве терапии для лечения дегенерации желтого пятна. Пример 5. Этот пример показывает динамику проницаемости сетчатки, индуцируемой ФРСЭ. В один глаз каждой крысы внутрь стекловидного тела производят инъекцию 2,0 нг ФРСЭ(определенная конечная концентрация 25 нг/мл). В противоположный глаз вводят аналогичный объем контрольного раствора. Через 10 мин через катетер в правую яремную вену производят инъекцию 30 микролитров флюоресцеина. Флюорофотометрию стекловидного тела выполняют в указанные отрезки времени после инъекции флюоресцеина. Как показано на фиг. 5 А, в глазах, обработанных ФРСЭ, наблюдается отчетливое увеличение проницаемости флюоресцеина в стекловидное тело. Это становится статистически достоверным в пределах 10 мин после ангиограмной инъекции флюоресцеина и сохраняется в течение, по меньшей мере, 30 мин. На фиг. 5 В показано, что эта стимуляция, выраженная в процентах от контроля, демонстрирует наличие дополнительной утечки флюоресцеина в глазах,обработанных ФРСЭ, с течением времени. Пример 6. Этот пример показывает дозозависимую реакцию проницаемости сетчатки на флюоресцеин в ответ на ФРСЭ. В один глаз каждого животного производят инъекцию контрольного раствора, тогда как в противоположный глаз производят инъекцию различных доз ФРСЭ. Через 10 мин производят 21 внутривенную инъекцию флюоресцеина и через 30 мин анализируют количество утечки в стекловидное тело. Как показано на фиг. 6, наблюдалось дозозависимое увеличение проницаемости сетчатки. Стимуляция была максимальной от 14 до 20 нг/мл, что, как известно, можно получить у людей. Пример 7. Этот пример показывает эффект ингибитора ПКС, хлористо-водородной соли (S)-3,4[N,N'-1,1'-2"-этокси)-3"'(О)-4'"-(N,N-диметиламино)-бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол 2,5-диона при введении в стекловидное тело и стимуляции ПКС проницаемости сетчатки. Как указано на фиг. 1, в глаза крыс производят инъекцию или 2,0 нг ФРСЭ на 1 глаз, 10 нмоля ПКСингибитора, или одного микрограмма PDBU (агониста ПКС). Инъекцию ПКСингибитора производят за 15 мин до добавления ФРСЭ. Через 10 мин после добавления ФРСЭ производят внутривенно введение флюоресцеина и через 30 мин оценивают содержание флюоресцеина в стекловидном теле. Как показано на фиг. 7, внутривенная инъекция ФРСЭ выявила ожидаемую стимуляцию проницаемости сетчатки. Инъекция ПКСингибитора в стекловидное тело за 15 мин до инъекции ФРСЭ устраняла большую часть реакции в виде увеличения проницаемости. Прямая стимуляция протеинкиназы С путем инъекцииPDBU показала увеличение проницаемости,очень похожее на ФРСЭ. Пример 8. Этот пример демонстрирует ингибирование проницаемости сетчатки в ответ на ФРСЭ под воздействием орального введения хлористо-водородной соли (S)-3,4-[N,N'-1,1'-2"этокси)-3"'(О)-4'"-(N,N-диметиламино)-бутан)бис-(3,3'-индолил)]-1(Н)-пиррол-2, 5-диона. Крыс кормят кормом, смешанным с ингибиторомпротеинкиназы С в дозах, указанных на фиг. 8 А и 8 В. После такого кормления в течение 1 недели, как обсуждалось ранее, определяют проницаемость сетчатки в ответ на внутривенную инъекцию 2,0 нг ФРСЭ. Оральное введение ингибитораПКС этого изобретения в течение одной недели снижало проницаемость сетчатки в ответ на ФРСЭ. Это было наиболее заметно при более высоких дозах. В предшествующем описании раскрыты принципы, предпочтительные варианты реализации и виды практического применения. Однако изобретение, защита которого предполагается в данном случае, не должно рассматриваться как ограниченное конкретными раскрытыми формами, поскольку они должны расцениваться как иллюстративные, а не ограничивающие. Специалисты в данной области могут вносить вариации и изменения, не отходя от существа изобретения. 22 ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ лечения глазных сосудистых расстройств, выбранных из группы, состоящей из дегенерации желтого пятна, отека желтого пятна, сосудистой ретинопатии, неоваскуляризации радужной оболочки, окклюзии вен сетчатки, гистоплазмоза и ишемической болезни сетчатки, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитораизофермента протеинкиназы С следующей формулы в которой W представляет -О-, -S-, -SO-, -SO2-,-СО-, С 2-С 6 алкилен, замещенный алкилен, С 2 С 6 алкенилен, -арил-, -арил(СН 2)mО-, -гетероцикл-, -гетероцикл-(СН 2)mО-, -сконденсированный бициклический-, -сконденсированный бициклический-(СН 2)mО-, -NR3-, -NOR3-, -CONHили -NHCO-,Х и Y представляют независимо C1C4 алкилен, замещенный алкилен или X, Y и W скомбинированы вместе, образуя -(СН 2)nАА-,R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкил, нитро,NR4R5 или -NHCO(C1-C4 алкила),R2 представляет водород, СН 3 СО-, NH2 или гидрокси,R3 представляет водород, (CH2)mарил, C1C4 алкил,СОО(C1-C4 алкил),-CONR4R5,-(C=NH)NH2, -SO(C1-C4 алкил), -SO2(NR4R5) или-SO2(C1-C4 алкил),R4 и R5 представляют независимо водород,C1-C4 алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,АА представляет аминокислотный остаток,m представляет независимо 0, 1, 2 или 3, аn представляет независимо 2, 3, 4 или 5,или его фармацевтически приемлемую соль,пролекарство или сложный эфир. 2. Способ по п.1, в котором ингибиторизофермента протеинкиназы С представляет собой бис-индолилмалеимид или макроциклический бис-индолилмалеимид. 3. Способ по п.1, в котором ингибитор является изофермент-селективным и изофермент выбран из группы, состоящей из изоферментов бета-1 и бета-2. 4. Способ по п.3, в котором ингибитор протеинкиназы С представляет соединение,имеющее следующую формулу 24 6. Способ по п.4, в котором ингибитор протеинкиназы С представляет соединение следующей формулы в которой W представляет -О-, -S-, -SO-, -SO2-,-CO-, С 2-С 6 алкилен, замещенный алкилен, С 2 С 6 алкенилен, -арил-, -арил(СН 2)mО-, -гетероцикл-,-гетероцикл-(СН 2)mО-,-сконденсированный бициклический-, -сконденсированный бициклический-(СН 2)mО-,-NR3-,-NOR3-,-CONH- или NHCO-,Х и Y представляют независимо C1C4 алкилен, замещенный алкилен, или X, Y и W скомбинированы вместе, образуя -(СН 2)nАА-,R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкил, нитро,NR4R5 или -NHCO(C1-C4 алкила),R2 представляет водород, СН 3 СО-, NH2 или гидрокси,R3 представляет водород, (СН 2)mарил, C1C4 алкил,-COO(C1-C4 алкил),-CONR4R5,-(C=NH)NH2, -SO(C1-C4 алкил), -SO2(NR4R5) или-SO2(C1-C4 алкил),R4 и R5 представляют независимо водород,C1-C4 алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,АА представляет аминокислотный остаток,m представляет независимо 0, 1, 2 или 3, аn представляет независимо 2, 3, 4 или 5,или его фармацевтически приемлемую соль,пролекарство или сложный эфир. 5. Способ по п.4, в котором ингибитор протеинкиназы С имеет следующую формулу в которой Z представляет -(СН 2)p- или -(СН 2)pO-(СН 2)p,R4 представляет гидрокси, -SH, C1C4 алкил, (СН 2)mарил, -NH(арил), -N(СН 3)(СF3),-NH(CF3) или NR5R6,R5 представляет водород или C1-C4 алкил,R6 представляет водород, C1-C4 алкил или бензил,р представляет 0, 1 или 2, am представляет независимо 2 или 3,или его фармацевтически приемлемую соль,пролекарство или сложный эфир.m представляет независимо 2 или 3,или его фармацевтически приемлемую соль,пролекарство или сложный эфир. 7. Способ по п.4, в котором ингибитор протеинкиназы С представляет (S)-3,4-[N,N'1,1'-2"-этокси)-3"'(O)-4'"-(N,N-диметиламино) бутан)-бис-(3,3'-индолил)]-1(Н)-пиррол-2,5 дион или его фармацевтически приемлемую кислотную соль. 8. Способ по п.1, в котором глазное сосудистое расстройство выбрано из группы, состоящей из дегенерации желтого пятна, отека желтого пятна, сосудистой ретинопатии, неоваскуляризации радужной оболочки, окклюзии вен сетчатки, гистоплазмоза и ишемической болезни сетчатки. 9. Способ по п.1, в котором глазное сосудистое расстройство выбрано из группы, состоящей из дегенерации желтого пятна, отека желтого пятна и окклюзии вен сетчатки. 10. Способ по п.8, в котором указанная сосудистая ретинопатия представляет собой ретинопатию недоношенности или преждевременного развития. 11. Способ ингибирования роста клеток эндотелия, стимулированного ФРСЭ, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитораизофермента протеинкиназы С общей формулы в которой W представляет О-, -S-, -SO-, -SO2-,-CO-, C2-С 6 алкилен, замещенный алкилен, C2C6 алкенилен, -арил-, -арил(СН 2)mО-, -гетероцикл-, -гетероцикл-(CH2)mO-, -сконденсированный бициклический-,-сконденсированный бициклический-(CH2)mO-,-NR3-,-NOR3-,-CONH- или NHCO-, 25 Х и Y представляют независимо C1C4 алкилен, замещенный алкилен или X, Y и W скомбинированы вместе, образуя -(СН 2)nАА-,R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкил, нитро,NR4R5 или -NHCO(C1-C4 алкила),R2 представляет водород, СН 3 СО-, NH2 или гидрокси,R3 представляет водород, (CH2)mарил, C1C4 алкил,-СОО(C1-C4 алкил),-CONR4R5,-(C=NH)NH2, -SO(C1-C4 алкил), -SO2(NR4R5) или-SO2(C1-C4 алкил),R4 и R5 представляют независимо водород,C1-C4 алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,АА представляет аминокислотный остаток,m представляет независимо 0, 1, 2 или 3, аn представляет независимо 2, 3, 4 или 5,или его фармацевтически приемлемую соль,пролекарство или сложный эфир. 12. Способ подавления связанной с отеком капиллярной проницаемости, стимулированной ФРСЭ, который включает введение нуждающемуся в таком лечении млекопитающему терапевтически эффективного количества ингибитораизофермента протеинкиназы С общей формулы 26 в которой W представляет -О-, -S-, -SO-, -SO2-,-CO-, С 2-С 6 алкилен, замещенный алкилен, С 2 С 6 алкенилен, -арил-, -арил(СН 2)mO-, -гетероцикл-, -гетероцикл-(СН 2)mО-, -сконденсированный бициклический-, -сконденсированный бициклический-(СН 2)mО-, -NR3-, -NOR3-, -CONHили -NHCO-,Х и Y представляют независимо C1C4 алкилен, замещенный алкилен или X, Y и W скомбинированы вместе, образуя -(СН 2)nАА-,R1 радикалы представляют водород или до четырех необязательных заместителей, независимо выбранных из галогена, C1-C4 алкила, гидрокси, C1-C4 алкокси, галогеналкил, нитро,NR4R5 или -NHCO(C1-C4 алкила),R2 представляет водород, СН 3 СО, NH2 или гидрокси,R3 представляет водород, (СН 2)m арил, C1C4 алкил,-СОО(C1-C4 алкил),-CONR4R5,-(C=NH)NH2, -SO(C1-C4 алкил), -SO2(NR4R5) или-SO2(C1-C4 алкил),R4 и R5 представляют независимо водород,C1-C4 алкил, фенил, бензил или скомбинированы с азотом, с которым они связаны, образуя насыщенное или ненасыщенное 5- или 6-членное кольцо,АА представляет аминокислотный остаток,m представляет независимо 0, 1, 2 или 3, аn представляет независимо 2, 3, 4 или 5,или его фармацевтически приемлемую соль,пролекарство или сложный эфир.
МПК / Метки
МПК: A61K 31/40, A61P 27/12
Метки: глазных, лечение, фактором, роста, связанных, терапевтическое, заболеваний, эндотелия, сосудистого
Код ссылки
<a href="https://eas.patents.su/16-1752-terapevticheskoe-lechenie-glaznyh-zabolevanijj-svyazannyh-s-faktorom-rosta-sosudistogo-endoteliya.html" rel="bookmark" title="База патентов Евразийского Союза">Терапевтическое лечение глазных заболеваний, связанных с фактором роста сосудистого эндотелия</a>
Предыдущий патент: 1,4-диарил-2,3-дифтор-2-бутены в качестве инсектицидов и акарицидов.
Следующий патент: Многослойная противопульная преграда
Случайный патент: Полисилоксаны для изготовления внутриглазной линзы и способы изготовления внутриглазной линзы












